KR20140132244A - 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 - Google Patents
헤테로환 화합물 및 이를 포함하는 유기 전자 소자 Download PDFInfo
- Publication number
- KR20140132244A KR20140132244A KR1020130051548A KR20130051548A KR20140132244A KR 20140132244 A KR20140132244 A KR 20140132244A KR 1020130051548 A KR1020130051548 A KR 1020130051548A KR 20130051548 A KR20130051548 A KR 20130051548A KR 20140132244 A KR20140132244 A KR 20140132244A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- substituted
- unsubstituted
- compound
- organic
- Prior art date
Links
- 0 *1c(cccc2)c2-c2c1cccc2 Chemical compound *1c(cccc2)c2-c2c1cccc2 0.000 description 2
- XRBYUNUGHQJRPO-UHFFFAOYSA-N C(C1)C2c(cccc3)c3-c3ccccc3C1C2 Chemical compound C(C1)C2c(cccc3)c3-c3ccccc3C1C2 XRBYUNUGHQJRPO-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Abstract
본 발명은 유기 전자 소자의 수명, 효율, 전기 화학적 안정성 및 열적 안정성을 크게 향상시킬 수 있는 신규 헤테로환 화합물 및 상기 헤테로환 화합물이 유기화합물 층에 함유되어 있는 유기 전자 소자를 제공한다.
Description
본 명세서는 새로운 헤테로환 화합물 및 이를 포함하는 유기 전자 소자에 관한 것이다.
유기 전자 소자란 정공 및/또는 전자를 이용한 전극과 유기물 사이에서의 전하 교류를 필요로 하는 소자를 의미한다. 유기 전자 소자는 동작 원리에 따라 하기와 같이 크게 두 가지로 나눌 수 있다. 첫째는 외부의 광원으로부터 소자로 유입된 광자에 의하여 유기물층에서 엑시톤(exiton)이 형성되고 이 엑시톤이 전자와 정공으로 분리되고, 이 전자와 정공이 각각 다른 전극으로 전달되어 전류원(전압원)으로 사용되는 형태의 전기소자이다. 둘째는 2개 이상의 전극에 전압 또는 전류를 가하여 전극과 계면을 이루는 유기물 반도체에 정공 및/또는 전자를 주입하고, 주입된 전자와 정공에 의하여 동작하는 형태의 전자소자이다.
유기 전자 소자의 예로는 유기 발광 소자, 유기 태양전지, 유기 트랜지스터 등이 있으며, 이들은 모두 소자의 구동을 위하여 정공의 주입 또는 수송 물질, 전자의 주입 또는 수송 물질, 또는 발광 물질을 필요로 한다. 이하에서는 주로 유기발광소자에 대하여 구체적으로 설명하지만, 상기 유기 전자 소자들에서는 정공의 주입 또는 수송 물질, 전자의 주입 또는 수송 물질, 또는 발광 물질이 유사한 원리로 작용한다.
일반적으로 유기 발광 현상이란 유기 물질을 이용하여 전기에너지를 빛에너지로 전환시켜주는 현상을 말한다. 유기 발광 현상을 이용하는 유기 발광 소자는 통상 양극과 음극 및 이 사이에 유기물층을 포함하는 구조를 가진다. 여기서 유기물층은 유기 발광 소자의 효율과 안정성을 높이기 위하여 각기 다른 물질로 구성된 다층의 구조로 이루어진 경우가 많으며, 예컨대 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등으로 이루어 질 수 있다. 이러한 유기 발광 소자의 구조에서 두 전극 사이에 전압을 걸어주게 되면 양극에서는 정공이, 음극에서는 전자가 유기물층에 주입되게 되고, 주입된 정공과 전자가 만났을 때 엑시톤(exciton)이 형성되며, 이 엑시톤이 다시 바닥상태로 떨어질 때 빛이 나게 된다.
상기와 같은 유기 발광 소자를 위한 새로운 재료의 개발이 계속 요구되고 있으며, 이와 같은 재료 개발의 필요성은 전술한 다른 유기 전자 소자에서도 마찬가지이다.
이에 본 발명자들은 상기와 같은 이유로 치환기에 따라 유기 전자 소자에서 요구되는 다양한 역할을 할 수 있는 화학 구조를 갖는 헤테로환 화합물 및 이를 포함하는 유기 전자 소자를 제공하는 것을 목적으로 한다.
본 명세서는 하기 화학식 1로 표시되는 헤테로환 화합물을 제공한다.
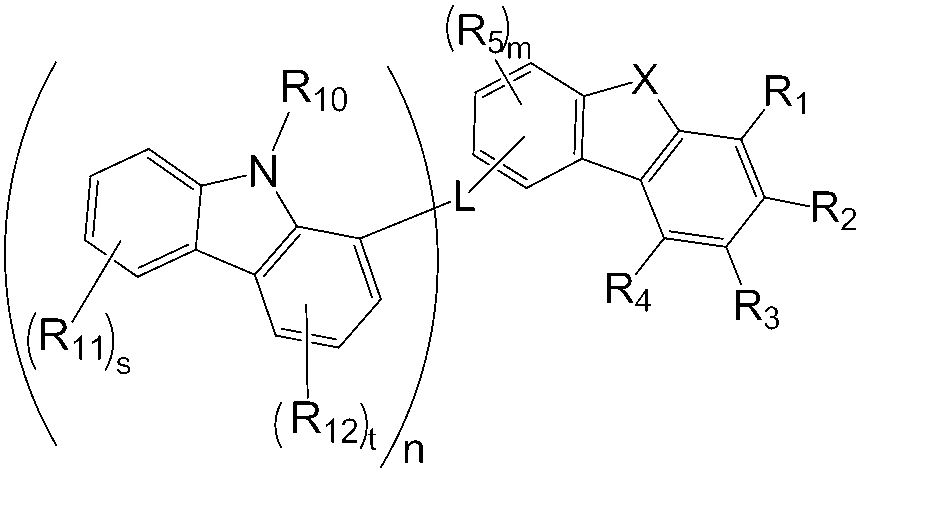
[화학식 1]
상기 화학식 1에 있어서,
X는 산소 또는 황이고,
R1, R2 및 R4는 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 시아노기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기이고,
R3는 시아노기이며,
R5는 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기이고,
m은 0 내지 3의 정수이며,
n은 1 내지 3의 정수이고,
Ar1은 치환 또는 비치환된 아릴기; 또는 치환 또는 비치환된 헤테로아릴기이며,
L은 직접연결이거나 -Ar2-Ar3-로 표시되며,
Ar2는 직접연결; 치환 또는 비치환된 아릴렌기; 또는 이종 원소로 O, N, S 를 갖는 치환 또는 비치환된 헤테로아릴렌기이고,
Ar3은 치환 또는 비치환된 아릴렌기; 또는 이종 원소로 O, N, S 를 갖는 치환 또는 비치환된 헤테로아릴렌기이다.
또한, 본 명세서는 제1 전극, 제2 전극, 및 상기 제1 전극과 제2 전극 사이에 배치된 1층 이상의 유기물층을 포함하는 유기 전자 소자로서, 상기 유기물층 중 1층 이상은 상기 화학식 1의 헤테로환 화합물을 포함하는 것인 유기 전자 소자를 제공한다.
본 명세서에 따른 새로운 헤테로환 화합물은 유기 발광 소자를 비롯한 유기 전자 소자의 유기물층의 재료로서 사용될 수 있고, 이를 사용함으로써 유기 발광 소자를 비롯한 유기 전자 소자에서 효율의 향상, 낮은 구동전압 및/또는 수명 특성의 향상이 가능하다.
본 명세서에 따른 새로운 헤테로환 화합물은 전자 주개(donor)와 받개(acceptor)를 한 분자 구조 안에 포함 함에도 불구하고, 큰 밴드 갭과 큰 삼중항 에너지를 갖는다. 또한, 합성적으로 기존에 알려진 다양한 전자 주개 혹은 받개 물질과 쉽게 결합 시켜 그 밴드 갭을 세밀하게 조정할 있는 장점이 있다. 이러한 성질은 발광 효율이 좋고 수명 특성이 양호한 OLED 소자를 제공할 수 있다.
도 1은 기판(1), 양극(2), 발광층(3), 음극(4)으로 이루어진 유기 발광 소자의 예를 도시한 것이다.
도 2는 기판 (1), 양극(2), 정공주입층(5), 정공수송층(6), 발광층(7), 전자수송층(8) 및 음극(4)으로 이루어진 유기 발광 소자의 예를 도시한 것이다.
도 2는 기판 (1), 양극(2), 정공주입층(5), 정공수송층(6), 발광층(7), 전자수송층(8) 및 음극(4)으로 이루어진 유기 발광 소자의 예를 도시한 것이다.
본 명세서는 상기 화학식 1로 표시되는 헤테로환 화합물을 제공한다.
상기 화학식 1에 있어서, R3는 시아노기인 경우, R1, R2 또는 R4이 시아노기인 경우보다, 합성적으로 더 수월하게 진행 할 수 있다.
또한, 전자 주개 (electron donor)인 X 위치의 원소와 전자 받개 (electron acceptor)인 시아노기가 파라 (para) 위치로 연결되어 강한 분자 내 전하이동 (intramolecular charge transfer)을 보일 것으로 예상되어, 유기 발광 소자 에서 상기 물질을 발광층 내 호스트로 사용하는 경우, 전자 또는 정공에 대한 안전성이 증가하여 유기 발광 소자의 수명이나 효율을 향상시킨다. 또한, HOMO 에너지 준위가 낮아져, 정공 차단 (hole blocking) 역할을 수행할 수 있다.
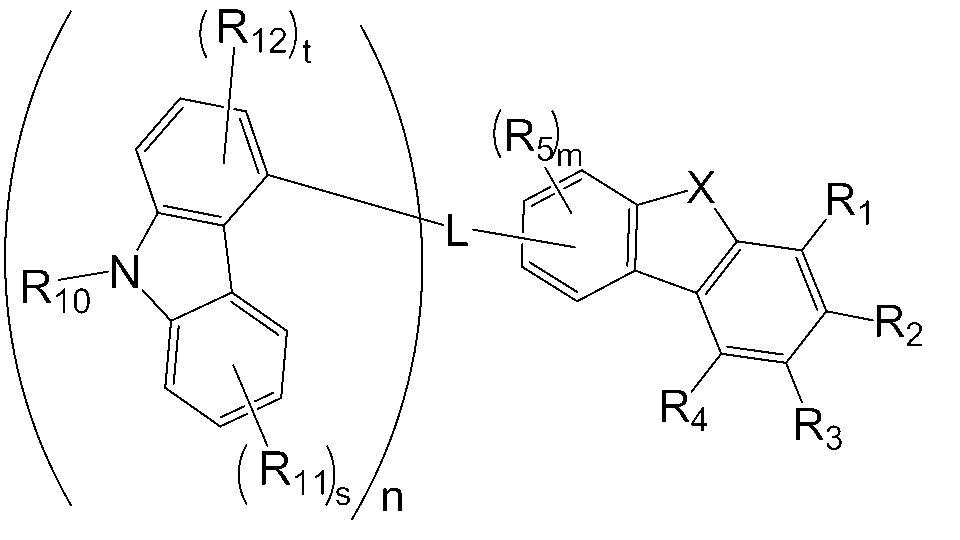
본 명세서의 일 실시상태에 따르면, 상기 화학식 1로 표시되는 헤테로환 화합물은 하기 화학식 1-1 또는 1-2 로 표시될 수 있다.
[화학식 1-1]
[화학식 1-2]
R1내지 R5, L, Ar1, Ar2, Ar3, m 및 n의 정의는 상기 화학식 1의 정의와 동일하다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar1은 치환 또는 비치환된 페닐기일 수 있다.
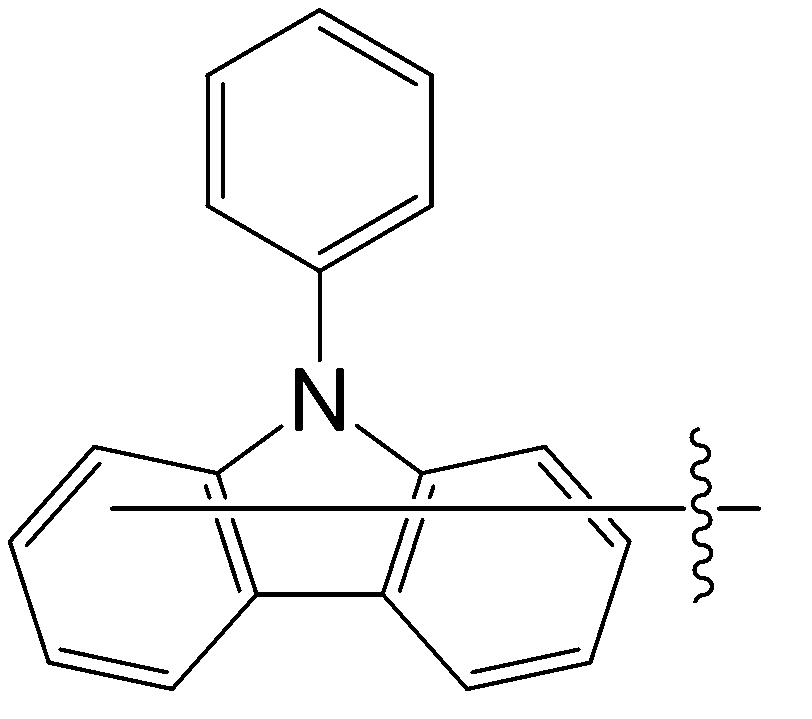
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar1은 치환 또는 비치환된 카바졸기일 수 있다.
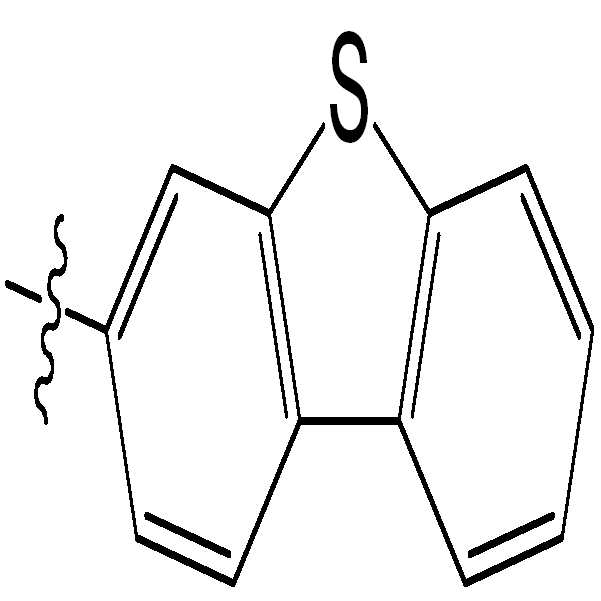
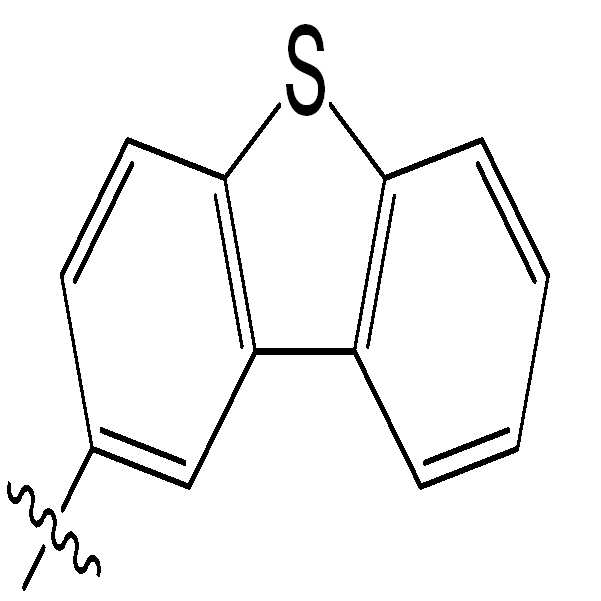
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar1은 치환 또는 비치환된 디벤조티오펜기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar1은 치환 또는 비치환된 디벤조퓨란기 일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar1은 치환 또는 비치환된 트리아진기일 수 있다.
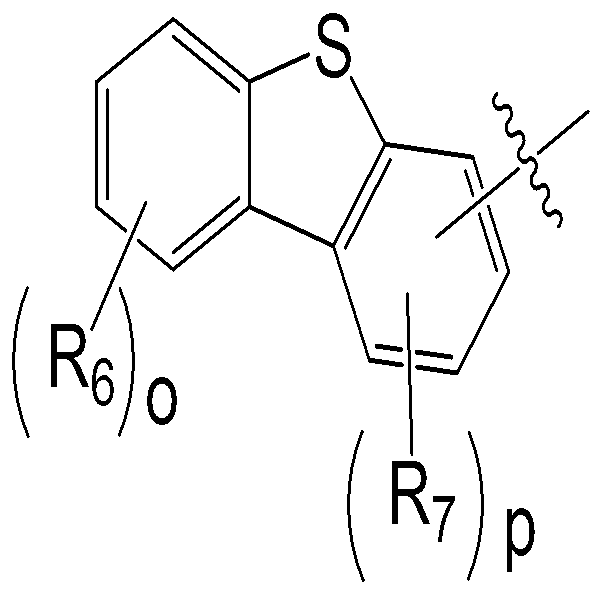
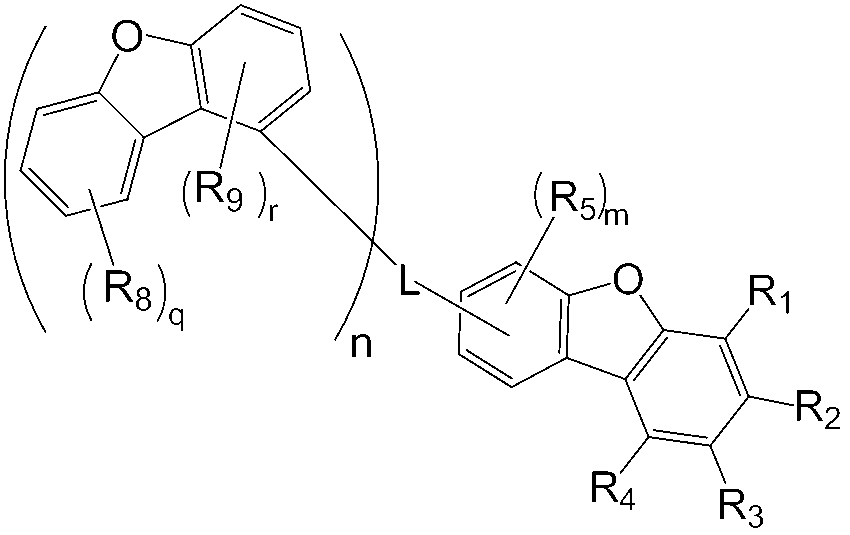
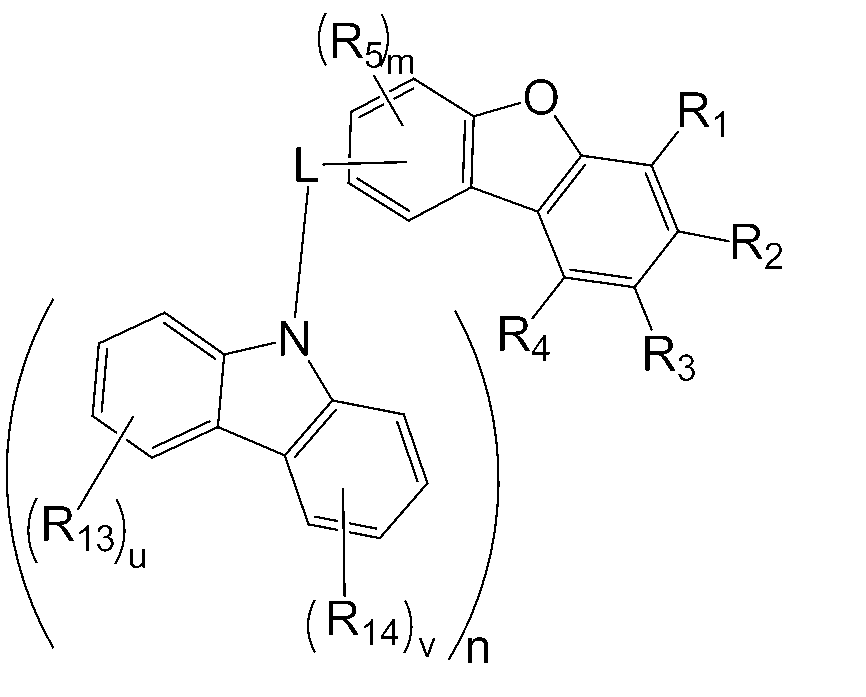
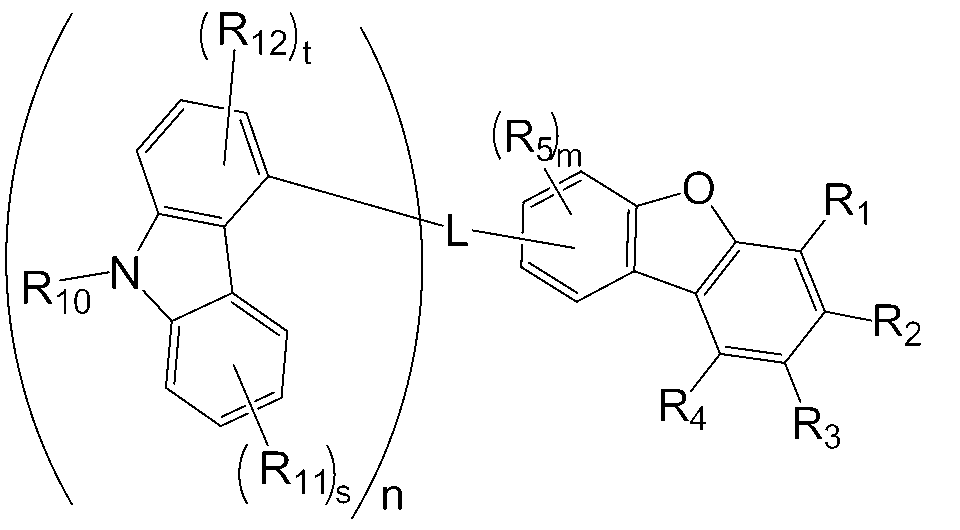
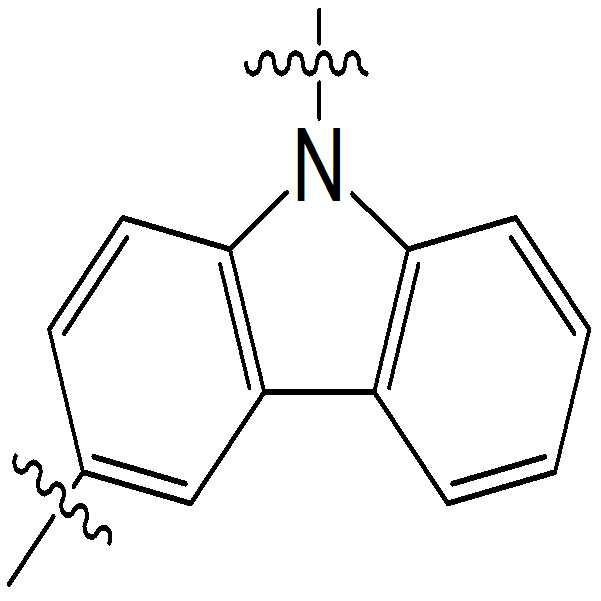
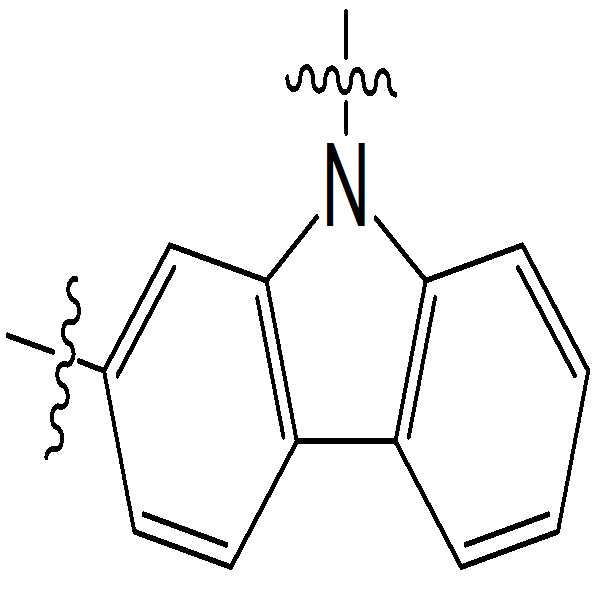
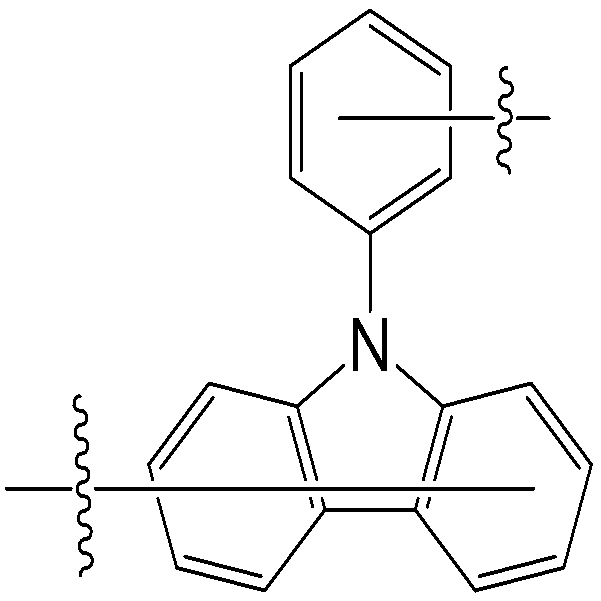
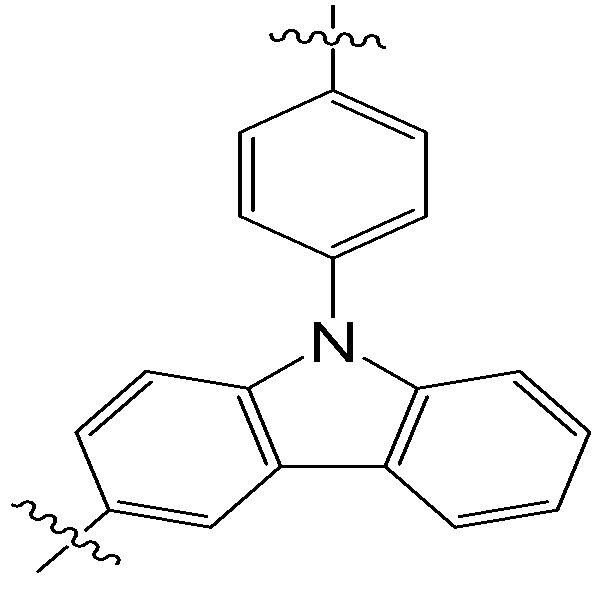
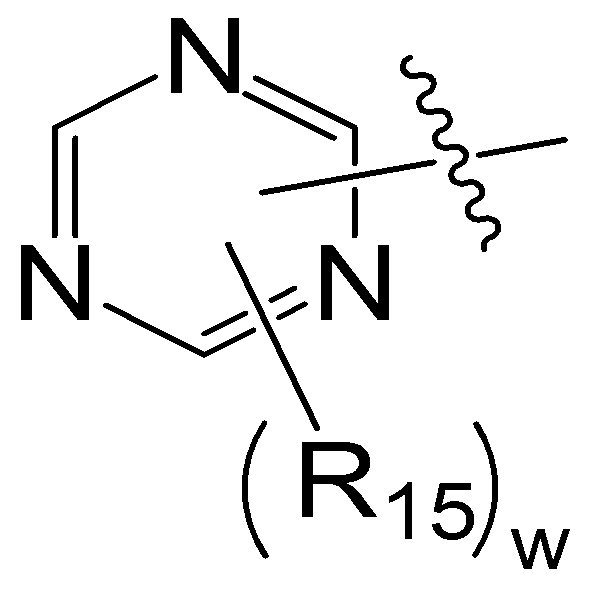
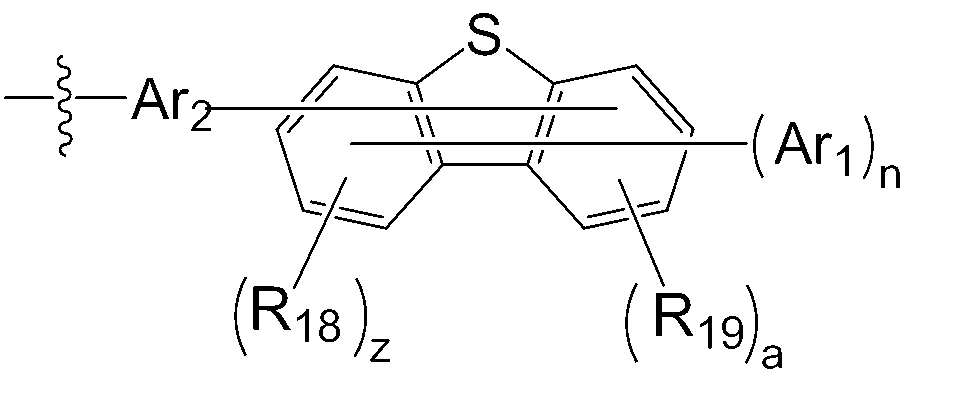
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar1은 화학식 2 내지 7중 어느 하나로 표시될 수 있다.
[화학식 2]
[화학식 3]
[화학식 4]
[화학식 5]
[화학식 6]
[화학식 7]
o, q, s, u 및 v는 각각 독립적으로 0 내지 4의 정수이고,
p, r 및 t는 각각 독립적으로 0 내지 3의 정수이며,
w는 0 내지 2의 정수이며,
x는 0 내지 5의 정수이고,
R6 내지 R16은 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기일 수 있다.
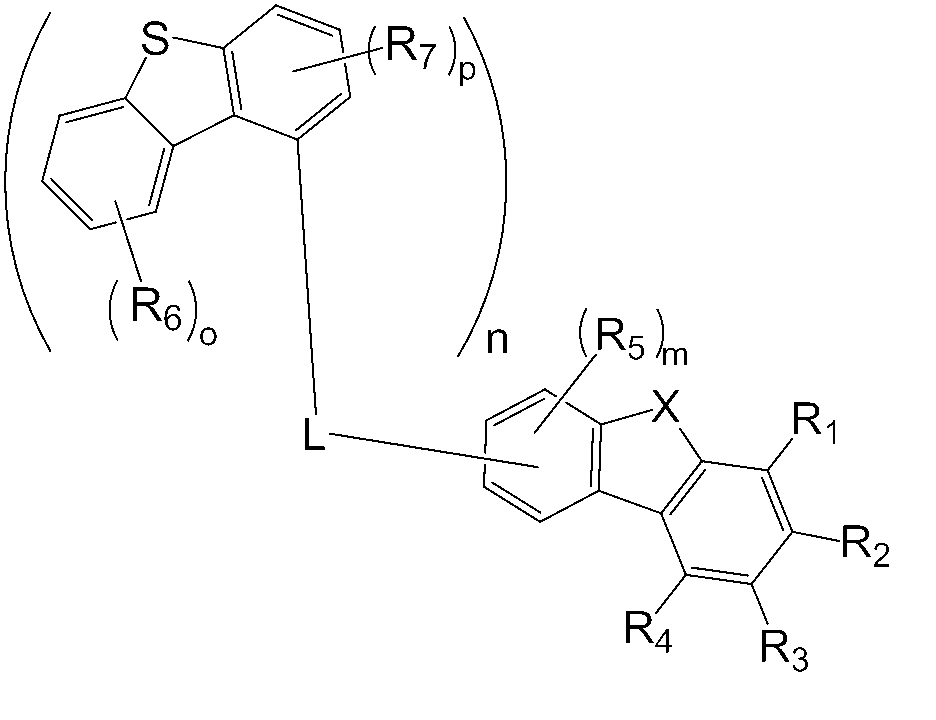
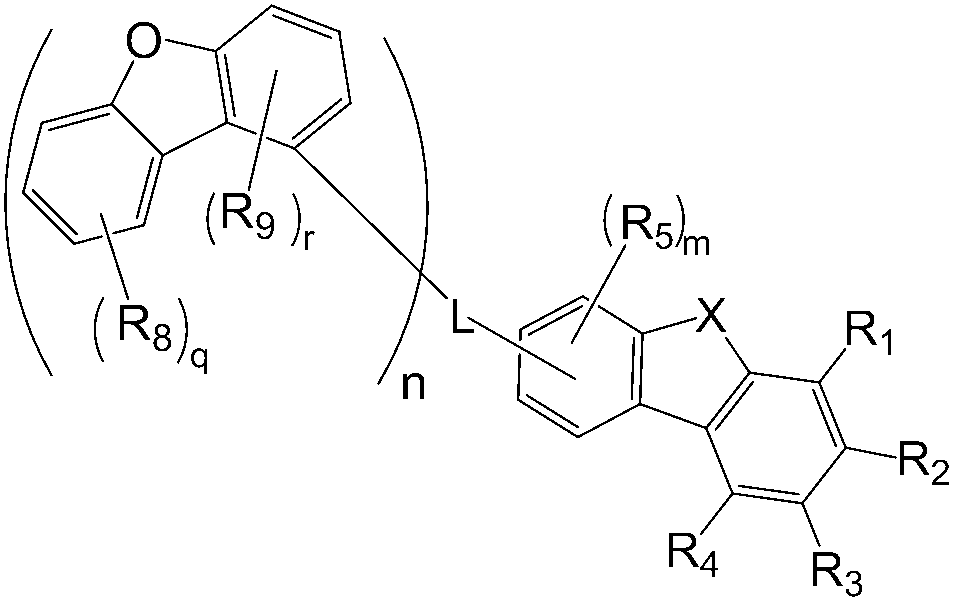
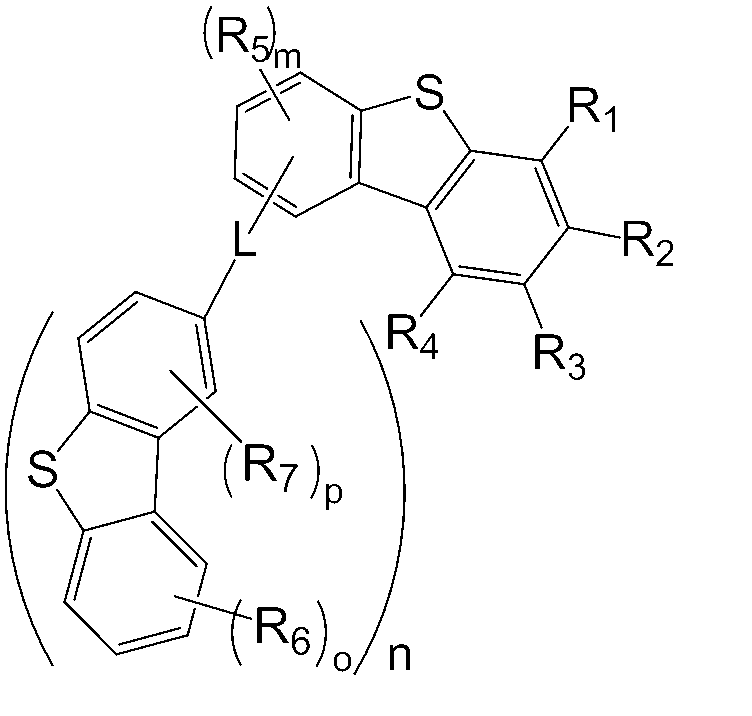
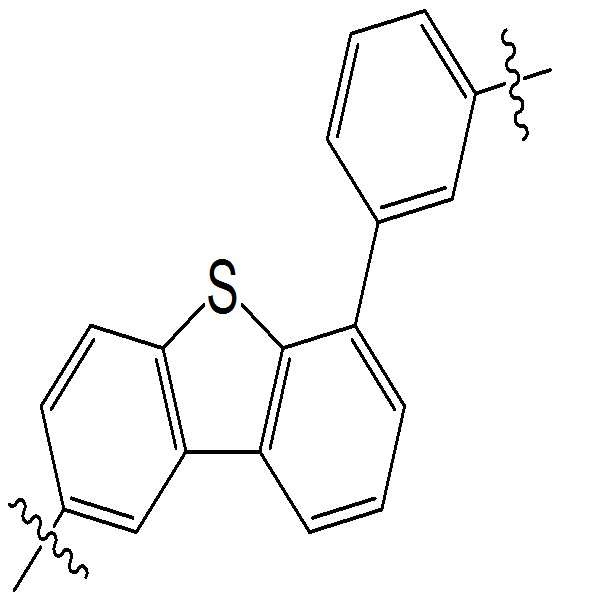
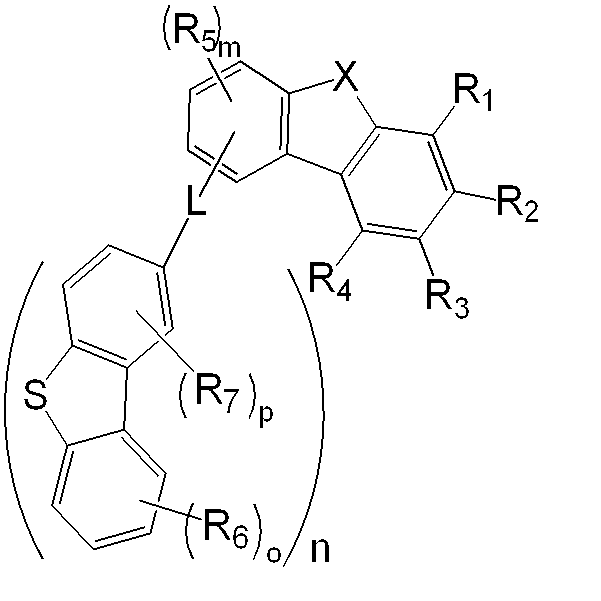
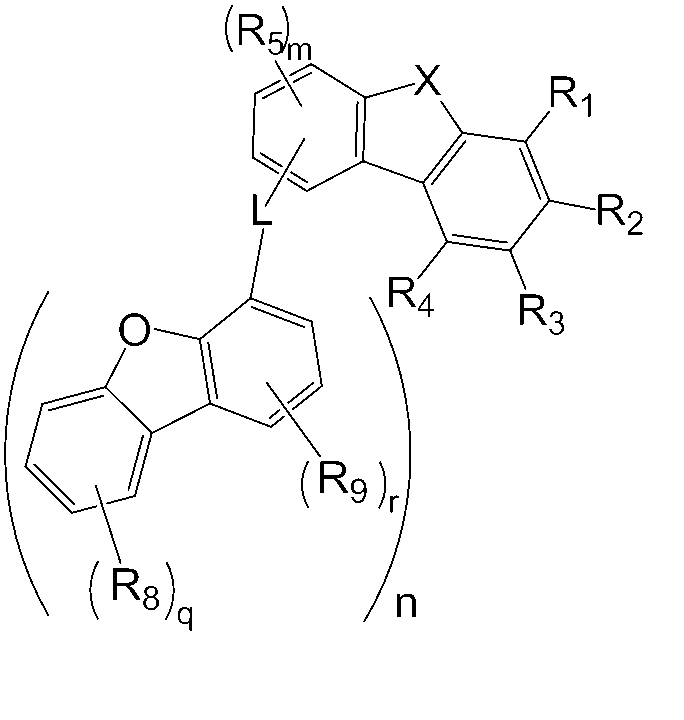
또한, 본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 L은 화학식 8 내지 12 중 어느 하나로 표시될 수 있다.
[화학식 8]
[화학식 9]
[화학식 10]
[화학식 11]
[화학식 12]
Ar1, Ar2 및 n은 상기 화학식 1에서 정의한 바와 동일하고
y는 0 내지 4의 정수이고,
z, a, b, c, d 및 e는 각각 0 내지 4의 정수이며,
y와 n의 합은 1 내지 5의 정수이고,
z와 a 및 7의 합은 1 내지 7의 정수이며,
b와 c 및 7의 합은 1 내지 7의 정수이고,
d와 e 및 7의 합은 1 내지 7의 정수이며,
R17 내지 R25 는 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 시아노기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기이다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1로 표시되는 헤테로환 화합물은 하기 화학식 1-0-1 내지 1-0-12 중 어느 하나로 표시될 수 있다.
[화학식 1-0-1]
[화학식 1-0-2]
[화학식 1-0-3]
[화학식 1-0-4]
[화학식 1-0-5]
[화학식 1-0-6]
[화학식 1-0-7]
[화학식 1-0-8]
[화학식 1-0-9]
[화학식 1-0-10]
[화학식 1-0-11]
[화학식 1-0-12]
상기 화학식 1-0-1 내지 1-0-12에 있어서,
X, R1 내지 R5, L, m 및 n은 상기 화학식 1에서 정의한 바와 동일하고,
o, q, s, u 및 v는 각각 독립적으로 0 내지 4의 정수이고,
p, r 및 t는 각각 독립적으로 0 내지 3의 정수이며,
w는 0 내지 2의 정수이고,
x는 0 내지 5의 정수이며,
R6 내지 R16 는 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로아릴기이다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1-1로 표시되는 헤테로환 화합물은 하기 화학식 1-1-1 내지 1-1-12 중 어느 하나로 표시될 수 있다.
[화학식 1-1-1]
[화학식 1-1-2]
[화학식 1-1-3]
[화학식 1-1-4]
[화학식 1-1-5]
[화학식 1-1-6]
[화학식 1-1-7]
[화학식 1-1-8]
[화학식 1-1-9]
[화학식 1-1-10]
[화학식 1-1-11]
[화학식 1-1-12]
상기 화학식 1-1-1 내지 1-1-12에 있어서,
R1 내지 R5, L, m 및 n은 상기 화학식 1에서 정의한 바와 동일하고,
o, q, s, u 및 v는 각각 독립적으로 0 내지 4의 정수이고,
p, r 및 t는 각각 독립적으로 0 내지 3의 정수이며,
w는 0 내지 2의 정수이고,
x는 0 내지 5의 정수이며,
R6 내지 R16 중 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로아릴기이다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1-2로 표시되는 헤테로환 화합물은 하기 화학식 1-2-1 내지 1-2-12 중 어느 하나로 표시될 수 있다.
[화학식 1-2-1]
[화학식 1-2-2]
[화학식 1-2-3]
[화학식 1-2-4]
[화학식 1-2-5]
[화학식 1-2-6]
[화학식 1-2-7]
[화학식 1-2-8]
[화학식 1-2-9]
[화학식 1-2-10]
[화학식 1-2-11]
[화학식 1-2-12]
상기 화학식 1-2-1 내지 1-2-12에 있어서,
R1 내지 R5, L, m 및 n은 상기 화학식 1에서 정의한 바와 동일하고,
o, q, s, u 및 v는 각각 독립적으로 0 내지 4의 정수이고,
p, r 및 t는 각각 독립적으로 0 내지 3의 정수이며,
w는 0 내지 2의 정수이고,
x는 0 내지 5의 정수이며,
R6 내지 R16 중 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로아릴기이다.
상기 치환기들의 예시들은 아래에서 설명하나, 이에 한정되는 것은 아니다.
본 명세서에 있어서, 상기 아릴기는 단환식 또는 다환식일 수 있고, 탄소수는 특별히 한정되지 않으나, 6 내지 60인 것이 바람직하다. 아릴기의 구체적인 예로는 페닐기, 비페닐기, 트라이페닐기, 터페닐기, 스틸벤기 등의 단환식 방향족 및 나프틸기, 비나프틸기, 안트라세닐기, 페난트레닐기, 파이레닐기, 페릴레닐기, 테트라세닐기, 크라이세닐기, 플루오레닐기, 아세나프타센닐기, 트리페닐렌기, 플루오란텐(fluoranthene)기 등의 다환식 방향족 등이 있으나, 이들에만 한정되는 것은 아니다.
본 명세서에 있어서, 상기 헤테로고리기는 이종원자로 O, N, S 또는 P를 포함하는 헤테로고리기로서, 탄소수는 특별히 한정되지 않으나, 탄소수 2 내지 60인 것이 바람직하다. 헤테로고리기의 예로는 티오펜기, 퓨란기, 피롤기, 이미다졸기, 티아졸기, 옥사졸기, 옥사디아졸기, 트리아졸기, 피리딜기, 비피리딜기, 트리아진기, 아크리딜기, 피리다진기, 퀴놀리닐기, 이소퀴놀린기, 인돌기, 카바졸기, 벤즈옥사졸기, 벤즈이미다졸기, 벤즈티아졸기, 벤즈카바졸기, 벤즈티오펜기, 디벤조티오펜기, 벤즈퓨란기, 디벤조티오펜기 및 디벤조퓨란기 등이 있으나, 이들에만 한정되는 것은 아니다.
본 명세서에 있어서, 상기 헤테로아릴기는 이종원자로 O, N, S 를 포함하는 헤테로아릴기로서, 탄소수는 특별히 한정되지 않으나, 탄소수 2 내지 60인 것이 바람직하다. 헤테로아릴기의 예로는 티에틸, 벤조[b]티에닐, 나프토[2,3-b]티에닐, 티안트레닐, 푸릴, 피라닐, 이소벤조푸라닐, 벤조옥사졸일, 크로메닐, 크산테닐, 페노크산티이닐, 2H-피롤릴, 피롤릴, 이미다졸일, 피라졸일, 피리딜, 피라지닐, 피리미디닐, 피리다지닐, 인돌리지닐, 이소인돌일, 3H-인돌일, 인돌일, 인다졸일, 푸리닐, 4H-퀴놀리지닐, 이소퀴놀일, 퀴놀리닐, 테트라히드로퀴놀리닐, 프탈아지닐, 나프티리디닐, 퀴나졸리닐, 신놀리닐, 프테리디닐, 4aH-카바졸일, 카바졸일, β-카볼리닐, 펜안트리디닐, 아크리디닐, 퍼이미디닐, 펜안트롤리닐, 페나지닐, 이소티아졸일, 페노티아지닐, 이소옥사졸일, 푸라자닐, 페녹사지닐기, 벤즈옥사졸기, 벤즈이미다졸기, 벤즈티아졸기, 벤즈카바졸기, 벤즈티오펜기, 디벤조티오펜기, 벤즈퓨란기, 디벤조티오펜기 및 디벤조퓨란기 등이 있으나, 이들에만 한정되는 것은 아니다.
본 명세서에 있어서, 상기 헤테로아릴렌기는 이종원자로 O, N, S 를 포함하는 헤테로아릴렌기로서, 탄소수는 특별히 한정되지 않으나, 탄소수 2 내지 60인 것이 바람직하다. 헤테로아릴렌기의 예로는 티에틸렌, 벤조[b]티에닐렌, 나프토[2,3-b]티에닐렌, 티안트레닐렌, 푸릴렌, 피라닐렌, 이소벤조푸라닐넬, 벤조옥사졸일렌, 크로메닐렌, 크산테닐렌, 페노크산티이닐렐, 2H-피롤릴렐, 피롤릴렌, 이미다졸일렌, 피라졸일렌, 피리딜렌, 피라지닐렌, 피리미디닐렌, 피리다지닐렌, 인돌리지닐렌, 이소인돌일렌, 3H-인돌일렌, 인돌일렌, 인다졸일렌, 푸리닐렌, 4H-퀴놀리지닐렌, 이소퀴놀일렌, 퀴놀리닐렌, 테트라히드로퀴놀리닐렌, 프탈아지닐렌, 나프티리디닐렌, 퀴나졸리닐렌, 신놀리닐렌, 프테리디닐렌, 4aH-카바졸일렌, 카바졸일렌, β-카볼리닐렌, 펜안트리디닐렌, 아크리디닐렌, 퍼이미디닐렌, 펜안트롤리닐렌, 페나지닐렌, 이소티아졸일렌, 페노티아지닐렌, 이소옥사졸일렌, 푸라자닐렌, 페녹사지닐기, 벤즈옥사졸기, 벤즈이미다졸기, 벤즈티아졸기, 벤즈카바졸기, 벤즈티오펜기, 디벤조티오펜기, 벤즈퓨란기, 디벤조티오펜기 및 디벤조퓨란기 등이 있으나, 이들에만 한정되는 것은 아니다.
본 명세서에 있어서, 상기 알킬기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나 1 내지 50인 것이 바람직하다. 구체적인 예로는 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, t-부틸기, 펜틸기, 헥실기 및 헵틸기 등이 있으나, 이들에 한정되지 않는다.
본 명세서에 있어서, 상기 알케닐기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나, 2 내지 50인 것이 바람직하다. 구체적인 예로는 스틸베닐기(stylbenyl), 스티레닐기(styrenyl)기 등의 아릴기가 치환된 알케닐기가 바람직하나 이들에 한정되지 않는다.
본 명세서에 있어서, 상기 알콕시기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나 1 내지 50인 것이 바람직하다.
화합물 중에 포함되어 있는 알킬기, 알케닐기 및 알콕시기의 길이는 화합물의 공액 길이에는 영향을 미치지 않고, 다만 부수적으로 화합물의 유기 전자 소자에의 적용 방법, 예컨대 진공 증착법 또는 용액 도포법의 적용에 영향을 미칠 뿐이므로 탄소수의 개수는 특별히 한정되지 않는다.
본 명세서에 있어서, 시클로알킬기는 특별히 한정되지 않으나, 탄소수 3 내지 60인 것이 바람직하며, 특히 시클로펜틸기, 시클로헥실기가 바람직하다.
본 명세서에 있어서, 할로겐기의 예로는 불소, 염소, 브롬 또는 요오드가 있다.
본 명세서에 있어서, 플루오레닐기는 열린 플루오레닐기의 구조를 포함하며, 여기서 열린 플루오레닐기는 2개의 고리 화합물이 1개의 원자를 통하여 연결된 구조에서 한쪽 고리 화합물이 연결이 끊어진 상태의 구조로서, 예로는 , 등이 있다.
본 명세서에 있어서, 아민기는 탄소수는 특별히 한정되지 않으나, 1 내지 50인 것이 바람직하다. 아민기의 구체적인 예로는 메틸아민기, 디메틸아민기, 에틸아민기, 디에틸아민기, 페닐아민기, 나프틸아민기, 비페닐아민기, 안트라세닐아민기, 9-메틸-안트라세닐아민기, 디페닐아민기, 페닐나프틸아민기, 디톨릴아민기, 페닐톨릴아민기, 트리페닐아민기 등이 있으나, 이들에만 한정되는 것은 아니다.
본 명세서에 있어서, 아릴아민기의 탄소수는 특별히 한정되지 않으나, 6 내지 50인 것이 바람직하다. 아릴아민기의 예로는 치환 또는 비치환된 단환식의 디아릴아민기, 치환 또는 비치환된 다환식의 디아릴아민기 또는 치환 또는 비치환된 단환식 및 다환식의 디아릴아민기를 의미한다.
본 명세서에 있어서, 아릴옥시기, 아릴티옥시기, 아릴술폭시기 및 아랄킬아민기의 탄소수는 특별히 한정되지 않으나, 6 내지 50인 것이 바람직하다. 아릴옥시기, 아릴티옥시기, 아릴술폭시기 및 아랄킬아민기 중의 아릴기는 전술한 아릴기의 예시와 같다.
본 명세서에 있어서, 알킬티옥시기, 알킬술폭시기, 알킬아민기 및 아랄킬아민기 중의 알킬기는 전술한 알킬기의 예시와 같다.
본 명세서에 있어서, 헤테로아릴아민기 중의 헤테로아릴기는 전술한 헤테로아릴기의 예시 중에서 선택될 수 있다.
본 명세서에 있어서, 아릴렌기, 알케닐렌기, 플루오레닐렌기, 및 헤테로아릴렌기는 각각 아릴기, 알케닐기, 플루오레닐기, 및 헤테로아릴기의 2가기이다. 이들은 각각 2가기인 것을 제외하고는, 전술한 아릴기, 알케닐기, 플루오레닐기, 헤테로아릴기의 설명이 적용될 수 있다.
또한, 본 명세서에서 "치환 또는 비치환" 이라는 용어는 중수소; 할로겐기; 알킬기; 알케닐기; 알콕시기; 시클로알킬기; 실릴기; 아릴알케닐기; 아릴기; 아릴옥시기; 알킬티옥시기; 알킬술폭시기; 아릴술폭시기; 붕소기; 알킬아민기; 아랄킬아민기; 아릴아민기; 헤테로아릴기; 카바졸기; 아릴아민기; 아릴기; 플루오레닐기; 니트릴기; 니트로기; 히드록시기; 시아노기 및 N, O, S 또는 P 원자 중 1개 이상을 포함하는 헤테로고리기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환되었거나 또는 어떠한 치환기도 갖지 않는 것을 의미한다.
본 명세서는 상기 화학식 1로 표시되는 새로운 헤테로환 화합물을 제공한다. 이와 같은 화합물은 구조적 특이성으로 인하여 유기 전자 소자에서 유기물층으로 사용될 수 있다.
본 명세서의 일 구현예에 따르면, 상기 화학식 1 중 R3 는 시아노기일 수 있다.
또 하나의 실시상태에 있어서, R3는 시아노기이고, R1, R2 및 R4는 수소일 수 있다.
또 하나의 실시상태에 있어서, 화학식 1 중 Ar2는 직접연결; 치환 또는 비치환된 페닐렌기; 또는 이종 원소로 O, N, S를 갖는 치환 또는 비치환된 헤테로아릴기일 수 있다.
또 하나의 실시상태에 있어서, 화학식 1 중 Ar3은 치환 또는 비치환된 페닐렌기; 또는 이종 원소로 O, N, S를 갖는 치환 또는 비치환된 헤테로아릴기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 L은 직접결합; 치환 또는 비치환된 페닐렌기; 치환 또는 비치환된 카바졸기; 치환 또는 비치환된 디벤조티오펜기; 치환 또는 비치환된 디벤조퓨란기; 또는 치환 또는 비치환된 트리아진기인 것일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 직접연결일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 탄소수 6 이상 탄소수 40 이하의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 탄소수 13 이상 탄소수 40 이하의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 1환 내지 8환 또는 이들이 결합된 고리들의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 3환 내지 8환 또는 이들이 결합된 고리들의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 N, O, S 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로아릴기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 탄소수 3 이상 탄소수 40 이하의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 탄소수 3 이상 탄소수 5 이하의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 탄소수 3의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 1환 내지 8환 또는 이들이 결합된 고리들의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 1환의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 치환 또는 비치환된 페닐렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 치환 또는 비치환된 디벤조티오펜기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 치환 또는 비치환된 디벤조퓨란기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar2는 치환 또는 비치환된 트리아진기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 탄소수 6 이상 탄소수 40 이하의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 탄소수 13 이상 탄소수 40 이하의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 1환 내지 8환 또는 이들이 결합된 고리들의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 3환 내지 8환 또는 이들이 결합된 고리들의 치환 또는 비치환된 아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 N, O, S 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로아릴기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 탄소수 3 이상 탄소수 40 이하의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 탄소수 3 이상 탄소수 5 이하의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 탄소수 3의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 1환 내지 8환 또는 이들이 결합된 고리들의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 1환의 치환 또는 비치환된 헤테로아릴렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 치환 또는 비치환된 페닐렌기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 치환 또는 비치환된 디벤조티오펜기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 치환 또는 비치환된 디벤조퓨란기일 수 있다.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1 중 Ar3은 치환 또는 비치환된 트리아진기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 직접연결이고, Ar3는 치환 또는 비치환된 페닐렌기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 직접연결이고, Ar3는 치환 또는 비치환된 디벤조티오펜기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 치환 또는 비치환된 아릴렌기 또는 치환 또는 비치환된 헤테로아릴렌기이고, Ar3는 치환 또는 비치환된 디벤조티오펜기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 페닐렌기이고, Ar3는 치환 또는 비치환된 디벤조티오펜기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 직접연결이고, Ar3는 치환 또는 비치환된 카바졸기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 치환 또는 비치환된 아릴렌기 또는 치환 또는 비치환된 헤테로아릴렌기이고, Ar3는 치환 또는 비치환된 카바졸기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 페닐렌기이고, Ar3는 치환 또는 비치환된 카바졸기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 직접연결이고, Ar3는 치환 또는 비치환된 트리아진기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 치환 또는 비치환된 아릴렌기 또는 치환 또는 비치환된 헤테로아릴렌기이고, Ar3는 치환 또는 비치환된 트리아진기일 수 있다.
또 하나의 실시상태에 있어서, Ar2는 페닐렌기이고, Ar3는 치환 또는 비치환된 트리아진기일 수 있다.
또 하나의 실시상태에 있어서, 화학식 1 중 Ar1은 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 아릴기; 또는 치환 또는 비치환된 헤테로아릴기일 수 있다.
또 하나의 실시상태에 있어서, Ar1은 치환 또는 비치환된 페닐기, 치환 또는 비치환된 카바졸기, 치환 또는 비치환된 카바졸기, 치환 또는 비치환된 디벤조퓨란기, 치환 또는 비치환된 디벤조퓨란기, 치환 또는 비치환된 디벤조티오펜기, 치환 또는 비치환된 트리아진기일 수 있다.
또 하나의 실시상태에 있어서, Ar1은 페닐기로 치환된 카바졸기일 수 있다.
또 하나의 실시상태에 있어서, Ar1은 페닐기로 치환된 디벤조퓨란기일 수 있다.
또 하나의 실시상태에 있어서, Ar1은 시아노기로 치환된 디벤조퓨란기일 수 있다.
또 하나의 실시상태에 있어서, Ar1은 시아노기로 치환된 디벤조티오펜기일 수 있다.
또 하나의 실시상태에 있어서, Ar1은 페닐기로 치환된 트리아진기일 수 있다.
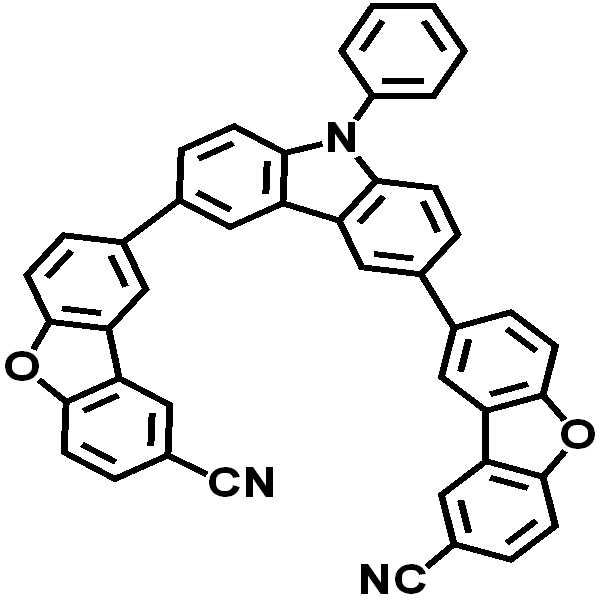
본 명세서에 따른 헤테로환 화합물의 구체예로는 하기 표 1의 화합물 1 내지 46이 있으나, 이들에만 한정되는 것은 아니다.
| 화합물 1 | 화합물 2 |
| 화합물 3 | 화합물 4 |
| 화합물 5 | |
| 화합물 6 | |
| 화합물 7 | 화합물 8 |
| 화합물 9 | 화합물 10 |
| 화합물 11 | 화합물 12 |
| 화합물 13 | 화합물 14 |
| 화합물 15 | 화합물 16 |
| 화합물 17 | 화합물 18 |
| 화합물 19 | 화합물 20 |
| 화합물 21 | 화합물 22 |
| 화합물 23 | 화합물 24 |
| 화합물 25 | 화합물 26 |
| 화합물 27 | 화합물 28 |
| 화합물 29 | 화합물 30 |
| 화합물 31 | |
| 화합물 32 | |
| 화합물 33 | |
| 화합물 34 | |
| 화합물 35 | |
| 화합물 36 | 화합물 37 |
| 화합물 38 | 화합물 39 |
| 화합물 40 | 화합물 41 |
| 화합물 42 | 화합물 43 |
| 화합물 44 | 화합물 45 |
| 화합물 46 | |
상기 화학식 1의 헤테로환 화합물은 후술하는 제조예를 기초로 제조될 수 있다.
본 발명은 또한 상기 화학식 1의 헤테로환 화합물을 이용하는 유기 전자 소자를 제공한다.
본 발명의 하나의 실시상태에 있어서, 유기 전자 소자는 제1 전극과 제2 전극 및 이 사이에 배치된 1층 이상의 유기물층을 포함하는 구조로 이루어질 수 있다.
상기 유기 전자 소자는 유기 발광 소자, 유기 태양 전지, 및 유기 트랜지스터로 이루어진 군에서 선택될 수 있다.
본 발명의 하나의 실시상태에 있어서, 상기 유기 전자 소자는 유기 발광 소자일 수 있다.
본 발명의 하나의 실시 상태에 있어서, 제1 전극, 제 2전극, 및 상기 제1 전극과 제2 전극 사이에 배치된 1층 이상의 유기물층을 포함하는 유기 발광 소자로서, 상기 유기물층 중 1층 이상은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함하는 것인 유기 발광 소자를 제공한다.
본 발명의 유기 발광 소자의 유기물층은 단층 구조로 이루어질 수도 있으나, 2층 이상의 유기물층이 적층된 다층 구조로 이루어질 수 있다. 예컨대, 본 발명의 유기 발광 소자는 유기물층으로서 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등을 포함하는 구조를 가질 수 있다. 그러나 유기 발광 소자의 구조는 이에 한정되지 않고 더 적은 수의 유기층을 포함할 수 있다.
따라서, 본 발명의 또 하나의 실시상태에 있어서, 상기 유기 발광 소자의 유기물층은 정공 주입층, 정공 수송층 및 정공 주입 및 정공수송을 동시에 하는 층 중 1층 이상을 포함할 수 있고, 상기 층들 중 1층 이상이 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 구체적으로, 상기 유기 발광 소자의 유기물층은 정공 주입층을 포함할 수 있고, 상기 정공 주입층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 또 하나의 예에 있어서, 상기 유기 발광 소자의 유기물층은 정공 수송층을 포함할 수 있고, 상기 정공 수송층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 또 하나의 예에 있어서, 상기 유기 발광 소자의 유기물층은 정공 수송층 및 정공 주입층을 포함할 수 있고, 상기 정공 수송층 및 정공 주입층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다.
또한, 상기 유기물층은 발광층을 포함할 수 있고, 상기 발광층이 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 하나의 예로서, 상기 화학식 1로 표시되는 헤테로환 화합물은 발광층의 호스트로서 포함될 수 있다. 또 하나의 예로서, 상기 화학식 1로 표시되는 헤테로환 화합물을 포함하는 유기물층은 상기 화학식 1로 표시되는 헤테로환 화합물을 호스트로서 포함하고, 다른 유기 화합물, 금속 또는 금속화합물을 도펀트로 포함할 수 있다.
상기 호스트로 포함되는 화학식 1로 표시되는 헤테로환 화합물에 있어서, 화학식 1의 L이 페닐렌기가 연결된 카바졸기 ()인 경우, 화학식 1의 L이 페닐렌기 (), 비페닐렌기 () 또는 페닐렌기가 연결된 디벤조티오펜기 ()인 경우보다 정공수송능력이 증가하여 발광특성을 향상시킬 수 있다.
상기 호스트로 포함되는 화학식 1로 표시되는 헤테로환 화합물에 있어서, 화학식 1의 L이 페닐렌기가 연결된 트리아진기인 경우 (), 화학식 1의 L이 페닐렌기 (), 비페닐렌기 () 또는 페닐렌기가 연결된 디벤조티오펜기 ()인 경우보다 전자주입능력이 향상되어 전압을 낮추고, 발광특성이 향상된다.
또한, 상기 유기물층은 전자 수송층, 전자 주입층 및 전자 수송 및 전자 주입을 동시에 하는 층 중 1층 이상을 포함할 수 있고, 상기 층들 중 1층 이상이 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 구체적으로, 상기 유기 발광 소자의 유기물층은 전자 주입층을 포함할 수 있고, 상기 전자 주입층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 또 하나의 예에 있어서, 상기 유기 발광 소자의 유기물층은 전자 수송층을 포함할 수 있고, 상기 전자 수송층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다. 또 하나의 예에 있어서, 상기 유기 발광 소자의 유기물층은 전자 수송층 및 전자 주입층을 포함할 수 있고, 상기 전자 수송층 및 전자 주입층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다.
상기 전자수송층에 포함되는 화학식 1로 표시되는 헤테로환 화합물에 있어서, 화학식 1의 L이 페닐렌기가 연결된 트리아진기인 경우 (), 화학식 1의 L이 페닐렌기 (), 비페닐렌기 () 또는 페닐렌기가 연결된 디벤조티오펜기 ()인 경우보다 전자주입능력이 향상되어 전압을 낮추고, 발광특성이 향상된다.
이와 같은 다층 구조의 유기물층에서 상기 화학식 1로 표시되는 헤테로환 화합물은 발광층, 정공 주입/정공 수송과 발광을 동시에 하는 층, 정공 수송과 발광을 동시에 하는 층, 또는 전자 수송과 발광을 동시에 하는 층 등에 포함될 수 있다.
또 하나의 실시 상태에 있어서, 상기 유기 발광 소자의 유기물층은 상기 화학식1로 표시되는 헤테로환 화합물을 포함하는 유기물층 이외에, 아릴아미노기, 카바졸기, 또는 벤즈카바졸기를 포함하는 화합물을 포함하는 정공 주입층 또는 정공 수송층을 포함할 수 있다.
본 발명의 하나의 실시상태에 있어서, 상기 유기 전자 소자는 유기 태양전지일 수 있다.
본 발명의 하나의 실시상태에 있어서, 제1 전극, 제 2전극, 및 상기 제1 전극과 제2 전극 사이에 배치된 광활성층을 포함하는 1층 이상의 유기물층을 포함하고, 상기 유기물층 중 1층 이상은 화학식 1로 표시되는 헤테로환 화합물을 포함하는 것인 유기 태양전지가 제공된다.
본 발명의 하나의 실시상태에 있어서, 상기 유기 태양 전지는 전하발생층을 포함할 수 있고, 상기 전하발생층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다.
또 하나의 실시상태에 있어서, 상기 광활성층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다.
또 하나의 실시상태에 있어서, 상기 유기 태양 전지는 광활성층과 전자주개(electron donor) 및 전자 받개(electron acceptor)를 포함할 수 있으며, 상기 광활성층과 전자주개 및 전자 받개는 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다.
본 발명의 실시상태에 있어서, 상기 유기 태양 전지가 외부 광원으로부터 광자를 받으면 전자 주개와 전자 받개 사이에서 전자와 정공이 발생한다. 발생된 정공은 전자 도너층을 통하여 양극으로 수송된다.
본 발명의 실시상태에 있어서, 상기 유기 태양 전지는 부가적인 유기물층을 더 포함할 수 있다. 상기 유기 태양 전지는 여러 기능을 동시에 갖는 유기물을 사용하여 유기물층의 수를 감소시킬 수 있다.
본 발명의 하나의 실시상태에 있어서, 상기 유기 전자 소자는 유기 트랜지스터일 수 있다.
본 발명의 하나의 실시상태에 있어서, 소스, 드레인, 게이트 및 1층 이상의 유기물층을 포함하는 유기 트랜지스터가 제공된다.
본 발명의 하나의 실시상태에 있어서, 상기 유기 트랜지스터는 전하발생층을 포함할 수 있고, 상기 전하발생층은 상기 화학식 1로 표시되는 헤테로환 화합물을 포함할 수 있다.
또 하나의 실시상태에 있어서, 상기 유기 트랜지스터는 절연층을 포함할 수 있고, 상기 절연층은 기판과 게이트 위에 위치할 수 있다.
상기 유기 전자 소자가 복수개의 유기물층을 포함하는 경우, 상기 유기물층은 동일한 물질 또는 다른 물질로 형성될 수 있다.
본 발명의 유기 전자 소자의 실시상태에 있어서, 도 1 및 도 2에 나타낸 것과 같은 구조를 가질 수 있으나, 이에만 한정되는 것은 아니다.
도 1은 기판(1), 양극(2), 발광층(3), 음극(4)이 순차적으로 적층된 유기 전자 소자의 구조가 예시되어 있다. 이와 같은 구조에 있어서, 상기 헤테로환 화합물은 상기 발광층(3)에 포함될 수 있다.
도 2는 기판 (1), 양극(2), 정공주입층(5), 정공수송층(6), 발광층(7), 전자수송층(8) 및 음극(4)이 순차적으로 적층된 유기 전자 소자의 구조가 예시되어 있다. 이와 같은 구조에 있어서 상기 헤테로환 화합물은 상기 정공주입층(5), 정공 수송층(6), 발광층(7) 및 전자 수송층(8) 중 1층 이상에 포함될 수 있다.
본 발명의 유기 전자 소자는 유기물층 중 1층 이상이 본 발명의 화합물, 즉 상기 화학식 1의 헤테로환 화합물을 포함하는 것을 제외하고는 당 기술분야에 알려져 있는 재료와 방법으로 제조될 수 있다.
예컨대, 본 발명의 유기 전자 소자는 기판 상에 제1 전극, 유기물층 및 제2 전극을 순차적으로 적층시킴으로써 제조할 수 있다. 이 때 스퍼터링법(sputtering)이나 전자빔 증발법(e-beam evaporation)과 같은 PVD(physical Vapor Deposition)방법을 이용하여, 기판 상에 금속 또는 전도성을 가지는 금속 산화물 또는 이들의 합금을 증착시켜 양극을 형성하고, 그 위에 정공 주입층, 정공 수송층, 발광층 및 전자 수송층을 포함하는 유기물층을 형성한 후, 그 위에 음극으로 사용할 수 있는 물질을 증착시킴으로써 제조될 수 있다. 이와 같은 방법 외에도, 기판 상에 음극 물질부터 유기물층, 양극 물질을 차례로 증착시켜 유기 전자 소자를 만들 수 있다.
또한, 상기 화학식 1의 헤테로환 화합물은 유기 전자 소자의 제조 시 진공 증착법 뿐만 아니라 용액 도포법에 의하여 유기물층으로 형성될 수 있다. 여기서, 용액 도포법이라 함은 스핀 코팅, 딥코팅, 닥터 블레이딩, 잉크젯프린팅, 스크린 프린팅, 스프레이법, 롤 코팅 등을 의미하지만, 이들만으로 한정되는 것은 아니다.
이와 같은 방법 외에도, 기판 상에 음극 물질로부터 유기물층, 양극 물질을 차례로 증착시켜 유기 전자 소자를 만들 수도 있다. 다만, 제조 방법이 이에 한정되는 것은 아니다.
상기 양극 물질로는 통상 유기물층으로 정공 주입이 원활할 수 있도록 일함수가 큰 물질이 바람직하다. 본 발명에서 사용될 수 있는 양극 물질의 구체적인 예로는 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연 산화물, 인듐 산화물, 인듐주석 산화물(ITO), 인듐아연 산화물(IZO)과 같은 금속 산화물; ZnO:Al 또는 SNO2 : Sb와 같은 금속과 산화물의 조합; 폴리(3-메틸티오펜), 폴리[3,4-(에틸렌-1,2-디옥시)티오펜](PEDOT), 폴리피롤 및 폴리아닐린과 같은 전도성 고분자 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 음극 물질로는 통상 유기물층으로 전자 주입이 용이하도록 일함수가 작은 물질인 것이 바람직하다. 음극 물질의 구체적인 예로는 마그네슘, 칼슘, 나트륨, 칼륨, 티타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석 및 납과 같은 금속 또는 이들의 합금; LiF/Al 또는 LiO2/Al과 같은 다층 구조 물질 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 정공 주입 물질로는 낮은 전압에서 양극으로부터 정공을 잘 주입 받을 수 있는 물질로서, 정공 주입 물질의 HOMO(highest occupied molecular orbital)가 양극 물질의 일함수와 주변 유기물층의 HOMO 사이인 것이 바람직하다. 정공 주입 물질의 구체적인 예로는 금속 포피린(porphyrin), 올리고티오펜, 아릴아민 계열의 유기물, 헥사니트릴헥사아자트리페닐렌 계열의 유기물, 퀴나크리돈(quinacridone)계열의 유기물, 페릴렌(perylene) 계열의 유기물, 안트라퀴논 및 폴리아닐린과 폴리티오펜 계열의 전도성 고분자 등이 있으나, 이들에만 한정 되는 것은 아니다.
상기 정공 수송 물질로는 양극이나 정공 주입층으로부터 정공을 수송받아 발광층으로 옮겨줄 수 있는 물질로 정공에 대한 이동성이 큰 물질이 적합하다. 구체적인 예로는 아릴아민 계열의 유기물, 전도성 고분자, 및 공액 부분과 비공액 부분이 함께 있는 블록 공중합체 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 발광 물질로는 정공 수송층과 전자 수송층으로부터 정공과 전자를 각각 수송받아 결합시킴으로써 가시광선 영역의 빛을 낼 수 있는 물질로서, 형광이나 인광에 대한 양자 효율이 좋은 물질이 바람직하다. 구체적인 예로는 8-히드록시-퀴놀린 알루미늄 착물(Alq3); 카르바졸 계열 화합물; 이량체화 스티릴(dimerized styryl) 화합물; BAlq; 10-히드록시벤조 퀴놀린-금속 화합물; 벤족사졸, 벤즈티아졸 및 벤즈이미다졸 계열의 화합물; 폴리(p-페닐렌비닐렌)(PPV) 계열의 고분자; 스피로(spiro) 화합물; 폴리플루오렌, 루브렌 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 전자 수송 물질로는 음극으로부터 전자를 잘 주입 받아 발광층으로 옮겨줄 수 있는 물질로서, 전자에 대한 이동성이 큰 물질이 적합하다. 구체적인 예로는 8-히드록시퀴놀린의 Al착물; Alq3를 포함한 착물; 유기 라디칼 화합물; 히드록시플라본-금속 착물 등이 있으나, 이들에만 한정되는 것은 아니다.
본 발명에 따른 유기 전자 소자는 사용되는 재료에 따라 전면 발광형, 후면 발광형 또는 양면 발광형일 수 있다.
실시예
이하 제조예 및 실험예를 통하여 본 발명을 보다 상세하게 설명하지만, 본 발명은 하기 제조예 및 실험예에 의하여 범위가 한정되지는 않는다.
제조예
반응예
1) 화합물 1의 합성
중간체 1-1의 합성
2-bromodibenzofuran 50 g (0.20 mol)을 DMF 380 mL에 녹인 후 CuCN 18.7 g (0.22 mol)을 첨가하여 환류 교반시킨다. 반응 종결 후 실온으로 냉각하여 2N HCl 수용액 600 mL를 천천히 투입하고 생겨나온 고체를 여과한다. 여과된 고체를 클로로포름에 녹인 후 물로 세척하여 분리 후 무수황산 마그네슘으로 수분을 제거하여 여과 후 감압 증류한다. 농축한 물질을 헥산으로 교반하고 여과하여 목적화합물인 중간체 1-1 26 g을 얻었다.
중간체 1-2의 합성
화합물 1-1 26 g (0.12 mol)을 클로로포름 240 mL에 녹인 후 아이스배스 (ice bath)로 냉각하여 브로민 19 mL (0.36 mol)를 천천히 첨가한다. 첨가 완료 후 혼합물을 실온에서 24 시간 교반한다. 반응 완료 후 생긴 고체를 여과하고, 여과된 고체를 클로로포름에 녹인 후 20 % 소듐티오설페이트 수용액과 소듐바이카보네이트 수용액으로 차례로 세척 후 유기층을 분리하여 무수황산마그네슘으로 수분을 제거하여 여과 후 감압 증류한다. 농축한 물질을 헥산으로 교반하고 여과하여 목적화합물인 중간체 1-2 15.1 g을 얻었다.
중간체 1-3의 합성
중간체 1-2 15 g (0.05 mol)을 1,4-다이옥산 180 mL에 녹인 후 bis(pinacolato)diboron 16 g (0.06 mol)을 투입한다. 혼합물을 교반하면서 포타슘아세테이트 15.6 g (0.16 mol)를 첨가하고 가온하여 환류시킨다. 환류 교반 상태에서 디벤질리덴아세톤팔라듐 900 mg (0.001 mol)과 트리시클로헥실포스핀 890 mg (0.003 mol)을 첨가하고 24 시간 환류 교반시킨다. 반응 종결 후 반응물을 실온으로 냉각하여 물로 세척 후 클로로포름으로 2회 추출한다. 모아진 유기층을 다시 한번 물로 세척 후 무수황산마그네슘으로 수분을 제거하고 여과하여 농축한다. 농축한 물질을 에틸아세테이트와 헥산의 혼합용액으로 가열 교반하고 여과하여 목적화합물인 중간체 1-3 15.7 g을 얻었다.
화합물 1의 합성
중간체 1-3 7.2 g (0.023 mol)과 9,9'(5-bromo-1,3-phenylene)bis(9H-carbazole) 11.0 g (0.023 mol)을 테트라하이드로퓨란 60 mL에 녹인 후 포타슘카보네이트 8.7 g (0.063 mol)을 녹인 수용액 15 mL를 첨가하여 가온한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 240 mg (0.0002 mol)을 투입한다. 혼합물을 6시간 동안 환류 교반시킨다. 반응 종결 후 실온으로 냉각하여 생긴 고체를 여과하고, 걸러진 고체를 클로로포름에 녹인 후 물로 세척한다. 모아진 유기층은 무수황산마그네슘으로 수분을 제거하고 여과하여 클로로포름과 헥산으로 재결정한다. 이를 통하여 목적화합물인 흰색 고체의 화합물 1 10.2 g을 얻었다. 합성된 화합물 1을 Mass Spectroscopy (이하, MS라 한다.)로 측정한 [M+H]+ 피크의 값은 600 m/z이다.
반응예
2) 화합물 2의 합성
중간체 2-1의 합성
상기 반응예 1의 중간체 1-1의 제조와 동일한 방법으로 2-브로모다이벤조티오펜 20 g (0.075 mol)을 출발물질로 하여 노란색 노체의 목적화합물인 중간체 2-1 12.7 g (0.06 mol)을 얻었다.
중간체 2-2의 합성
상기 반응예 1의 중간체 1-2의 제조와 동일한 방법으로 중간체 2-1 12 g (0.06 mol)을 출발물질로 하여 목적화합물인 미색 고체의 중간체 2-2 13 g (0.045 mol)을 얻었다.
중간체 2-3의 합성
상기 반응예 1의 중간체 1-3의 제조와 동일한 방법으로 중간체 2-2 13 g (0.045 mol)을 출발물질로 하여 목적화합물인 미색 고체의 중간체 2-3 13.4 g (0.045 mol)을 얻었다
화합물 2의 합성
상기 반응예 1의 중간체 1-3의 제조와 동일한 방법으로 중간체 2-3 7.5 g (0.022 mol)과 9,9'(5-bromo-1,3-phenylene)bis(9H-carbazole) 10.9 g (0.022 mol)을 반응하여 목적화합물인 흰색 고체의 화합물 2 10.3 g (0.0167 mol)을 얻었다. 합성된 화합물 2를 MS로 측정한 [M+H]+ 피크의 값은 616 m/z이다.
반응예
3) 화합물 3의 합성
상기 반응예 1에서 합성된 중간체 1-3 15 g (0.045mol)과 3,6-dibromo-9-phenyl-9H-carbazole 8.6 g (0.021mol)을 테트라하이드로퓨란 160 mL에 녹인 후 포타슘카보네이트 17.4 g (0.126mol)을 녹인 수용액 40 mL를 첨가하여 가온 한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 480 mg (0.0004 mol)을 투입한다. 혼합물을 6시간 동안 환류 교반 시킨다. 반응 종결 후 실온으로 냉각하고 생긴 고체를 여과하고, 걸러진 고체를 클로로포름에 다시 녹인 후 물로 세척한다. 모아진 유기층은 무수황산마그네슘으로 수분을 제거하고 여과하여 클로로포름과 헥산으로 재결정한다. 합성된 화합물 3을 MS로 측정한 [M+H]+ 피크의 값은 626 m/z이다.
반응예
4) 화합물 4의 합성
상기 반응예 2에서 합성된 중간체 2-3 8.4 g (0.025mol)과 3,6-dibromo-9-phenyl-9H-carbazole 5 g (0.012mol)을 테트라하이드로퓨란 40 mL에 녹인 후 포타슘카보네이트 10.3g(0.075mol)을 녹인 수용액 10 mL를 첨가하여 가온한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 290 mg (0.25 mmol)을 투입한다. 혼합물을 6 시간 동안 환류 교반 시킨다. 반응 종결 후 실온으로 냉각하여 생긴 고체를 여과하고, 걸러진 고체를 클로로포름에 녹인 후 물로 세척한다. 모아진 유기층은 무수황산마그네슘으로 수분을 제거하고 여과하여 클로로포름과 헥산으로 재결정한다. 이를 통하여 목적화합물인 흰색 고체의 화합물 4를 5.9 g를 얻었다. 합성된 제조된 화합물 4를 MS로 측정한 [M+H]+ 피크의 값은 658 m/z이다.
반응예
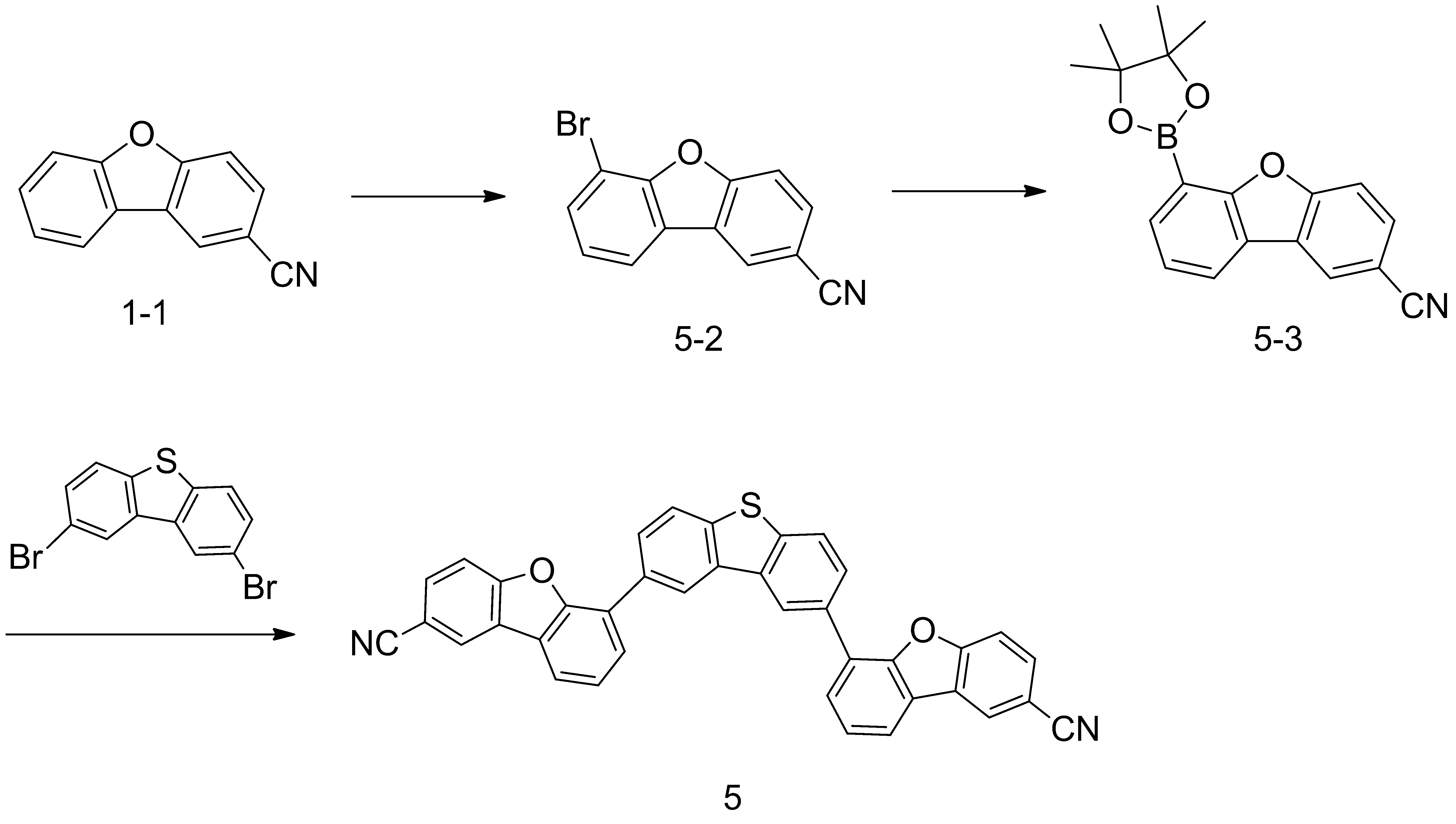
5) 화합물 5의 합성
중간체 5-2의 합성
화합물 1-1 20 g (0.10mol)을 무수테트라하이드로퓨란 200 mL에 첨가한 후 -78 ℃로 냉각한다. 혼합물을 교반 하면서 2.5 M 농도로 헥산에 혼합된 n-BuLi 60 mL를 천천히 투입한다. 혼합물을 1시간동안 같은 온도에서 교반한 후 1,2-dibromoethane 3.5 mL를 천천히 투입한다. 반응물을 서서히 실온으로 온도를 올리고, 3시간 정도 교반한다. 반응 종결 후 포화암모늄클로라이드 수용액을 첨가하고 에틸아세테이트로 추출한다. 유기층을 분리하여 물로 한번 더 세척하고 무수황산마그네슘으로 수분을 제거하여 여과 후 감압 증류한다. 농축한 물질을 헥산으로 교반하고 여과하여 목적화합물인 중간체 5-2 2 1g을 얻었다.
중간체 5-3의 합성
화합물 5-2 15 g (0.05mol)을 1,4-다이옥산 180 mL에 녹인 후 Bis(pinacolato)diboron 16 g (0.06mol)을 투입한다. 혼합물을 교반하면서 포타슘아세테이트 15.6 g (0.16 mol)를 첨가하고 가온 하여 환류 시킨다. 환류 교반 상태에서 디벤질리덴아세톤팔라듐 900 mg (0.001 mol)과 트리시클로헥실포스핀 890 mg (0.003 mol)을 첨가하고 24시간 환류 교반시킨다. 반응 종결 후 반응물을 실온으로 냉각하여 물로 세척 후 클로로포름으로 2회 추출한다. 모아진 유기층을 다시 한번 물로 세척 후 무수황산마그네슘으로 수분을 제거하고 여과하여 농축한다. 농축한 물질을 에틸아세테이트와 헥산의 혼합용액으로 가열 교반하고 여과하여 목적화합물인 중간체 5-3 15.7 g을 얻었다.
화합물 5의 합성
화합물 5-3 15 g (0.047 mol)과 2,8-dibromodibenzo[b,d]thiophene 8.0 g (0.023mol)을 테트라하이드로퓨란 64 mL에 녹인 후 포타슘카보네이트 19.4 g (0.14 mol)을 녹인 수용액 16 mL를 첨가하여 가온한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 540 mg (0.0004 mol)을 투입한다. 혼합물을 6 시간 동안 환류 교반시킨다. 반응 종결 후 실온으로 냉각하여 생긴 고체를 여과하고, 걸러진 고체를 클로로포름에 녹인 후 물로 세척한다. 모아진 유기층은 무수황산마그네슘으로 수분을 제거하고 여과하여 클로로포름과 에틸아세테이트로 재결정한다. 이를 통하여 목적화합물인 화합물 5를 흰색 고체 형태로 9.3 g을 얻었다. 합성된 화합물 5를 MS로 측정한 [M+H]+ 피크의 값은 567 m/z이다.
반응예
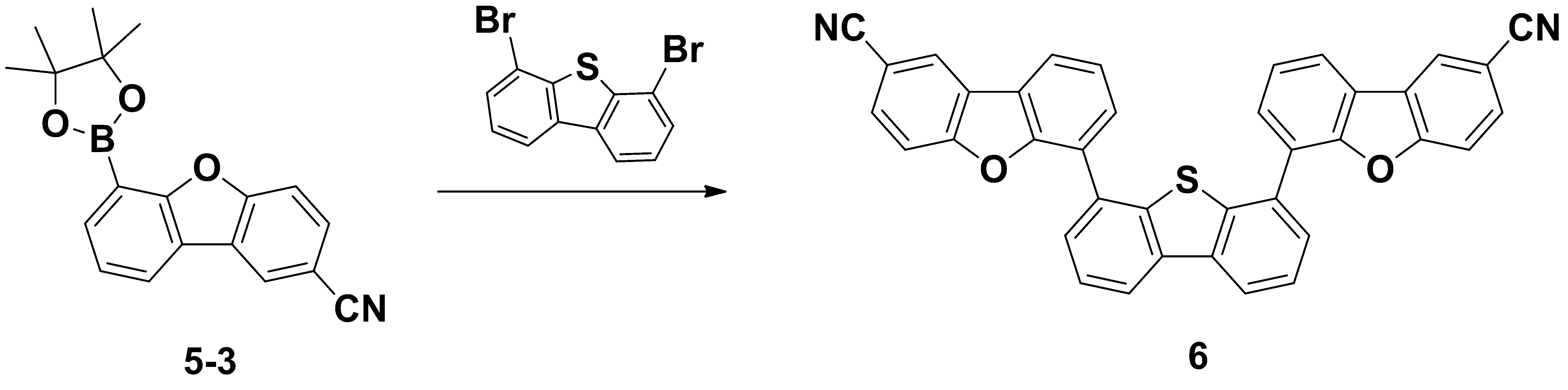
6) 화합물 6의 합성
화합물 5-3 10 g (0.031mol)과 4,6-dibromodibenzo[b,d]thiophene 5.3 g (0.015 mol)을 테트라하이드로퓨란 43 mL에 녹인 후 포타슘카보네이트 12.9 g (0.093 mol)을 녹인 수용액 10 mL를 첨가하여 가온 한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 360 mg (0.0002 mol)을 투입한다. 혼합물을 6 시간 동안 환류 교반시킨다. 반응 종결 후 실온으로 냉각하여 생긴 고체를 여과하고, 걸러진 고체를 클로로포름에 녹인 후 물로 세척한다. 모아진 유기층은 무수황산마그네슘으로 수분을 제거하고 여과하여 클로로포름과 에틸아세테이트로 재결정한다. 이를 통하여 목적화합물인 흰색 고체의 화합물 6을 6.5 g을 얻었다. 합성된 화합물 5를 MS로 측정한 [M+H]+ 피크의 값은 567 m/z이다.
반응예
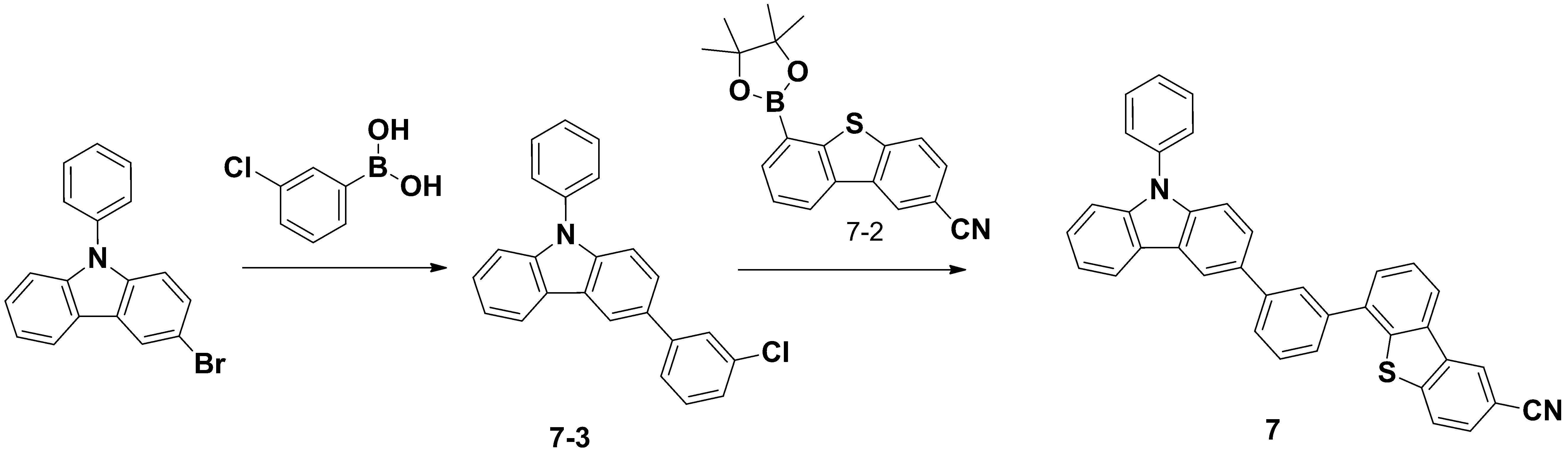
7) 화합물 7의 합성
중간체 7-1의 합성
상기 반응예 5의 중간체 5-2 합성과 동일한 방법으로 중간체 1-1 대신 중간체 2-1 20 g (0.10 mol)을 출발물질로 하여 목적화합물인 미색의 중간체 7-1을 19 g 얻었다.
중간체 7-2의 합성
상기 반응예 5의 중간체 5-3 합성과 동일한 방법으로 중간체 5-2 대신 중간체 7-1 15 g (0.052 mol)을 출발물질로 하여 목적화합물인 흰색의 중간체 7-2를 14.4 g 얻었다.
중간체 7-3의 합성
3-bromo-9-phenyl-9H-carbazole 10 g (0.03 mol)과 (3-chlorophenyl)boronic acid 5.3 g (0.034 mol)을 테트라하이드로퓨란 75 mL에 녹인 후 포타슘카보네이트 14.0 g(0.09 mol)을 녹인 수용액 25 mL를 첨가하여 가온 한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 340 mg (0.0003 mol)을 투입한다. 혼합물을 6 시간 동안 환류 교반 시킨다. 반응 종결 후 실온으로 냉각하여 유기층을 분리하여 물로 한번 더 세척하고 에틸아세테이트로 추출한다. 유기층을 분리하여 무수황산마그네슘으로 수분을 제거하고 여과하여 농축한다. 농축한 화합물에 소량의 클로로포름과 다량의 헥산을 첨가하여 30분간 교반한 후 여과한다. 이를 통하여 목적화합물인 흰색 고체의 중간체 7-3을 8.9 g을 얻었다.
화합물 7의 합성
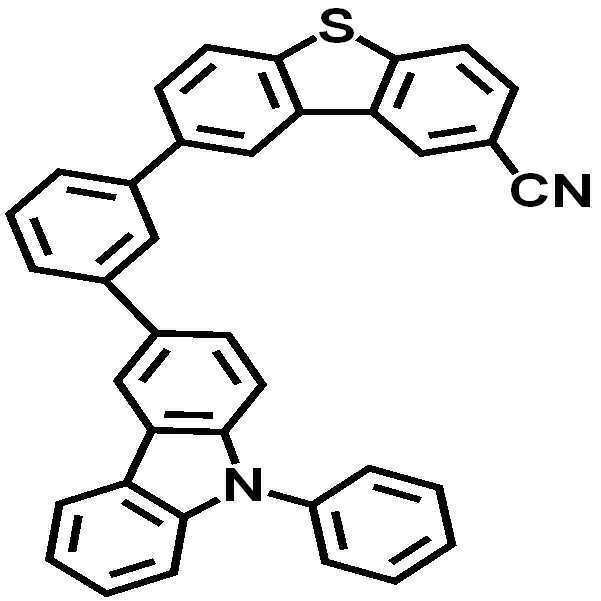
상기 반응예 1의 화합물 1의 합성과 동일한 방법으로 중간체 1-3 대신 중간체 7-2 8.3 g (0.025 mol)과 중간체 7-3 8 g (0.023 mol)을 출발물질로 하여 목적화합물인 흰색의 화합물 7을 8.5 g 얻었다. 합성된 화합물 7을 MS로 측정한 [M+H]+ 피크의 값은 527 m/z이다.
반응예
8) 화합물 8의 합성
상기 반응예 1의 화합물 1의 합성과 동일한 방법으로 중간체 1-3 대신 중간체 5-3 8 g (0.025 mol)과 중간체 7-3 8.0 g (0.023 mol)을 출발물질로 하여 목적화합물인 흰색의 화합물 8을 7.9 g 얻었다. 합성된 화합물 8을 MS로 측정한 [M+H]+ 피크의 값은 511 m/z이다.
반응예
9) 화합물 9의 합성
상기 반응예 1의 화합물 1의 합성과 동일한 방법으로 중간체 1-3 6.3 g (0.019 mol)과 중간체 7-3 6.1 g (0.017 mol)을 출발물질로 하여 7.7 g의 목적화합물인 화합물 9를 얻었다. 합성된 화합물 9를 MS로 측정한 [M+H]+ 피크의 값은 511 m/z이다.
반응예
10) 화합물 10의 합성
상기 반응예 1의 화합물 1의 합성과 동일한 방법으로 중간체 2-3 6.7g (0.020 mol)과 중간체 7-3 6.4 g (0.018 mol)을 출발물질로 하여 8.0 g의 목적화합물인 화합물 10을 얻었다. 합성된 화합물 10을 MS로 측정한 [M+H]+ 피크의 값은 527 m/z이다.
반응예
11) 화합물 11의 합성
중간체 11-1의 합성
4-bromodibenzothiophene 10 g (0.038 mol)과 (3-chlorophenyl)boronic acid 6.5 g (0.041 mol)을 테트라하이드로퓨란 100 mL 에 녹인 후 포타슘카보네이트 17.9 g (0.11 mol)을 녹인 수용액 25 mL를 첨가하여 가온한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 430 mg (0.0004 mol)을 투입한다. 혼합물을 6 시간 동안 환류 교반 시킨다. 반응 종결 후 실온으로 냉각하여 유기층을 분리하여 물로 한번 더 세척하고 에틸아세테이트로 추출한다. 유기층을 분리하여 무수황산마그네슘으로 수분을 제거하고 여과하여 농축한다. 농축한 화합물에 소량의 에틸아세테이트와 다량의 헥산을 첨가하여 30 분간 교반한 후 여과한다. 이를 통하여 목접화합물인 미색 고체의 중간체 11-1 10 g을 얻었다.
화합물 11의 합성
상기 반응예 1의 화합물 1의 합성과 동일한 방법으로 중간체 2-3 8.0 g (0.023 mol)과 중간체 11-1 6.4 g (0.021 mol)을 출발물질로 하여 9.8 g의 목적화합물인 화합물 11을 얻었다. 합성된 화합물 11을 MS로 측정한 [M+H]+ 피크의 값은 467 m/z이다.
반응예
12) 화합물 13의 합성
2-(3-bromophenyl)-4,6-diphenyl-1,3,5-triazine 8 g (0.020 mol)과 중간체 2-3 7.2 g (0.021 mol)을 출발물질로 하여 상기 반응예 1의 화합물 1의 합성과 동일한 방법으로 흰색의 목적화합물인 화합물 13 8.0 g을 얻었다. 합성된 화합물 13을 MS로 측정한 [M+H]+ 피크의 값은 516 m/z이다.
반응예
13) 화합물 17의 합성
중간체 17-1의 합성
(9-phenyl-9H-carbazol-3-yl)boronic acid 14 g (0.049mol), 3-bromo-9H-carbazole 10 g (0.041mol), 포타슘카보네이트 13.5g (0.098 mol)을 테트라하이드로퓨란 200 mL와 물 50 mL에 투입 후 가온한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 2.35 g (2.03 mmol)을 투입하여 6 시간 교반한다. 반응 종결 후 실온으로 냉각하여 유기층을 분리하고 감압 농축한다. 농축한 화합물을 클로로포름과 헥산으로 슬러리 여과하여 중간체 17-1 12 g을 얻었다.
중간체 17-2의 합성
중간체 17-1 14 g (0.034mol)과 1,3-Dibromobenzene 48.5 g (0.17 mol), CuI 3.3 g (0.017 mol), K2CO3 13.8 g (0.10 mol), EDA 2.3 mL (0.034 mol)을 자일렌 500mL에 투입 후 가온하여 12 시간 환류 교반하였다. 반응 종결 후 혼합물을 실온으로 냉각하여 물로 세척하고 에틸아세테이트로 추출한다. 유기층을 분리하여 무수황산마그네슘으로 수분을 제거하고 여과하여 감압농축한다. 농축된 화합물을 클로로포름과 헥산으로 슬러리화하여 중간체 17-2 15 g을 얻었다.
화합물 17의 합성
중간체 17-2 10 g (0.018 mol), 중간체 2-3 6.0 g (0.019 mol), 포타슘카보네이트 7.4 g (0.054 mol)을 테트라하이드로퓨란 80 mL와 물 20 mL에 투입 후 가온한다. 환류 상태에서 테트라키스(트리페닐포스핀)팔라듐(0) 200 mg (0.0002 mol)을 투입하여 6 시간 교반한다. 반응 종결 후 실온으로 냉각하여 유기층을 분리하고 감압 농축한다. 농축한 화합물을 클로로포름에 다시 녹인 후 물로 세척하여 분리하고 무수황산마그네슘으로 남은 수분을 제거하여 여과 후 재결정하여 목적화합물인 미색의 고체 화합물 17을 10 g 얻었다. 합성된 화합물 17을 MS로 측정한 [M+H]+ 피크의 값은 692 m/z이다.
반응예
14) 화합물 23의 합성
중간체 23-1의 합성
dibenzo[b,d]thiophen-2-ylboronic acid 10 g (0.043 mol), 3-bromo-9H-carbazole 10.8 g (0.043 mol)을 상기 반응예 13의 중간체 17-1의 합성과 동일한 방법으로 수행하여 중간체 23-1 12 g (출발물질 3-bromo-9H-carbazole에 대한 합성된 물질 중간체 23-1의 수득률 (몰비): 80 %)을 얻었다.
중간체 23-2의 합성
중간체 23-1 10 g (0.029mol)을 출발물질로 하여 상기 반응예 13의 중간체 17-2 합성과 동일한 방법으로 수행하여 중간체 23-2 10.8g (출발물질 중간체 23-1에 대한 합성된 물질 중간체 23-2의 수득률 (몰비): 75 %)을 얻었다.
화합물 23의 합성
중간체 23-2 10 g (0.020 mol)과 중간체 1-3 6.9 g (0.022 mol)을 상기 반응예 13의 화합물 17 합성과 동일한 방법으로 수행하여 화합물 23 9.7g (출발물질 중간체 23-2에 대한 합성된 물질 화합물 23의 수득률 (몰비): 78%)을 얻었다. 합성된 화합물 23을 MS로 측정한 [M+H]+ 피크의 값은 617 m/z이다.
반응예
15) 화합물 26의 합성
중간체 26-1의 합성
중간체 2-3 10 g (0.030 mol), 3-bromo-9H-carbazole 6.7 g (0.027 mol)을 출발물질로 하여 상기 반응예 13의 중간체 17-1의 합성과 동일한 방법으로 수행하여 중간체 26-1 9.3 g (3-bromo-9H-carbazole에 대한 합성된 물질 중간체 26-1의 수득률 (몰비): 83 %)을 얻었다.
화합물 26의 합성
중간체 26-1 8 g (0.021 mol), 2-(3-bromophenyl)-4,6-diphenyl-1,3,5-triazine 8.3 g (0.021 mol), 나트륨 터트-부톡사이드 4.0 g (0.042 mol)을 톨루엔에 첨가한 후 Pd(dba)2와 P(t-Bu)3를 투입하여 가온한다. 환류 상태에서 4시간 교반한 후 반응이 완결되면 실온으로 냉각하여 생성된 고체를 여과한다. 이를 다시 클로로포름에 녹인 후 물로 세척하여 분리 후 무수황산마그네슘으로 수분을 제거하여 여과한다. 이를 재결정하여 목적화합물인 화합물 26 10.8 g (출발물질 중간체 26-1에 대한 합성된 물질 화합물 26의 수득률 (몰비): 78 %)을 얻었다. 합성된 화합물 26을 MS로 측정한 [M+H]+ 피크의 값은 682 m/z이다.
반응예
16) 화합물 28의 합성
중간체 28-1의 제조
(9-phenyl-9H-carbazol-3-yl)boronic acid 10 g (0.035 mol), 3-bromo-9H-carbazole 8.6 g (0.035 mol)을 출발물질로 하여 상기 반응예 13의 중간체 17-1 합성과 동일한 방법을 수행하여 중간체 28-1을 12 g (출발물질 3-bromo-9H-carbazole 에 대한 합성된 물질 중간체 28-1의 수득률 (몰비): 84 %) 얻었다.
화합물 28의 합성
중간체 28-1 10 g (0.024 mol), 중간체 2-2 6.9 g (0.024 mol), 나트륨 터트-부톡사이드 4.5 g (0.048 mol)을 톨루엔에 첨가한 후 Pd(dba)2와 P(t-Bu)3를 투입하여 가온한다. 환류 상태에서 4시간 교반한 후 반응이 완결되면 실온으로 냉각하여 생성된 고체를 여과한다. 이를 다시 클로로포름에 녹인 후 물로 세척하여 분리 후 무수황산마그네슘으로 수분을 제거하여 여과한다. 이를 재결정하여 화합물 28 13.2 g (출발물질 28-1에 대한 합성된 물질 화합물 28의 수득률 (몰비): 89 %)을 얻었다. 합성된 화합물 28을 MS로 측정한 [M+H]+ 피크의 값은 616 m/z이다.
실험예
실험예 1
ITO (indium tin oxide)가 1500 Å의 두께로 박막 코팅된 유리 기판을 세제를 녹인 증류수에 넣고 초음파로 세척하였다. 이때, 세제로는 피셔 사(Fischer Co.) 제품을 사용하였으며, 증류수로는 밀리포어 사(Millipore Co.) 제품의 필터(Filter)로 2 차로 걸러진 증류수를 사용하였다. ITO를 30 분간 세척한 후 증류수로 2 회 반복하여 초음파 세척을 10 분간 진행하였다. 증류수 세척이 끝난 후, 이소프로필알콜, 아세톤 및 메탄올 중 하나의 종류 또는 둘 이상의 종류의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 수송시켰다. 또한, 산소 플라즈마를 이용하여 상기 기판을 5 분간 세정한 후 진공 증착기로 기판을 수송시켰다.
이렇게 준비된 ITO 투명 전극 위에 하기 화학식의 헥사니트릴 헥사아자트리페닐렌(hexanitrile hexaazatriphenylene; HAT)를 500 Å의 두께로 열 진공 증착하여 정공주입층을 형성하였다.
[HAT]
상기 정공주입층 위에 하기 구조의 NPB(N, N-Bis-(1-naphthalenyl)-N, N-bis-phenyl-(1, 1-biphenyl)-4, 4-diamine) 화합물을 400 Å의 두께로 열 진공 증착하여 정공수송층을 형성하였다.
[NPB]
이어서, 상기 정공수송층 위에 막 두께 300 Å으로 위에 상기 반응예 1에서 합성된 화합물 1을 Ir(ppy)3 도펀트와 10 % 농도 (화합물 1에 대한 Ir(ppy)3 도펀트의 중량비)로 진공증착하여 발광층을 형성하였다.
상기 발광층 위에 아래와 같은 전자 수송 물질을 200 Å의 두께로 진공 증착하여 전자주입 및 수송층을 형성하였다.
[전자 수송 물질]
상기 전자주입 및 수송층 위에 순차적으로 12 Å 두께로 리튬 플루라이드(LiF)와 2000 Å 두께로 알루미늄을 증착하여 음극을 형성하였다.
상기의 과정에서 유기물의 증착 속도는 0.4 ~ 0.7 Å/sec를 유지하였고, 음극의 리튬플루오라이드는 0.3 Å/sec, 알루미늄은 2 Å/sec의 증착 속도를 유지하였으며, 증착 시 진공도는 2 × 10-7 ~ 5 × 10-8 torr를 유지하였다.
실험예 2
상기 실험예 1에서 화합물 1 대신 화합물 4를 사용한 것 이외에는 동일하게 실험하였다.
실험예 3
상기 실험예 1에서 화합물 1 대신 화합물 10을 사용한 것 이외에는 동일하게 실험하였다.
실험예 4
상기 실험예 1에서 화합물 1 대신 화합물 12를 사용한 것 이외에는 동일하게 실험하였다.
실험예 5
상기 실험예 1에서 화합물 1 대신 화합물 13을 사용한 것 이외에는 동일하게 실험하였다.
비교예 1
상기 실험예 1에서 화합물 1 대신 상기의 H1을 사용한 것 이외에는 동일하게 실험하였다.
비교예 2
상기 실험예 1에서 화학식 1의 화합물 대신 상기의 H2를 사용한 것 이외에는 동일하게 실험하였다.
상기 실험예 1 내지 실험예 5에서 각각의 화합물을 발광층으로 사용하여 제작한 소자의 특성을 측정한 결과를 표 2에 나타내었다.
| 호스트 물질 | 도펀트 물질 | 도핑농도(%) | 구동전압 (V) (발광 휘도가 1,000 Cd/m2인 경우) |
발광효율 (Cd/A) |
|
| 비교예 | H1 | Ir(ppy)3 | 10 | 7.5 | 38 |
| 비교예 | H2 | Ir(ppy)3 | 10 | 7.9 | 34 |
| 실험예1 | 화합물1 | Ir(ppy)3 | 10 | 6..9 | 42. |
| 실험예2 | 화합물4 | Ir(ppy)3 | 10 | 6..2 | 53 |
| 실험예3 | 화합물10 | Ir(ppy)3 | 10 | 5.9 | 52 |
| 실험예4 | 화합물12 | Ir(ppy)3 | 10 | 6.0 | 55 |
| 실험예5 | 화합물13 | Ir(ppy)3 | 10 | 5.7 | 50 |
상기 표 2에서 확인 할 수 있듯이 실험예 1 내지 5는 녹색 발광층의 호스트로 이용될 수 있고, 비교예 1 내지 2 보다 저전압 특성과 향상된 효율을 나타내었다.
Claims (22)
- 하기 화학식 1로 표시되는 헤테로환 화합물:
[화학식 1]
상기 화학식 1에 있어서,
X는 산소 또는 황이고,
R1, R2 및 R4는 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 시아노기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기이고,
R3는 시아노기이며,
R5는 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기이고,
m은 0 내지 3의 정수이며,
n은 1 내지 3의 정수이고,
Ar1은 치환 또는 비치환된 아릴기; 또는 치환 또는 비치환된 헤테로아릴기이며,
L은 직접연결이거나 -Ar2-Ar3-로 표시되며,
Ar2는 직접연결; 치환 또는 비치환된 아릴렌기; 또는 이종 원소로 O, N, S 를 갖는 치환 또는 비치환된 헤테로아릴렌기이고,
Ar3은 치환 또는 비치환된 아릴렌기; 또는 이종 원소로 O, N, S 를 갖는 치환 또는 비치환된 헤테로아릴렌기이다. - 청구항 1에 있어서, 상기 Ar1은 치환 또는 비치환된 페닐기; 치환 또는 비치환된 카바졸기; 치환 또는 비치환된 디벤조티오펜기; 치환 또는 비치환된 디벤조퓨란기; 또는 치환 또는 비치환된 트리아진기인 것인 헤테로환 화합물.
- 청구항 1에 있어서, 상기 L은 치환 또는 비치환된 페닐렌기; 치환 또는 비치환된 카바졸기; 치환 또는 비치환된 디벤조티오펜기; 치환 또는 비치환된 디벤조퓨란기; 또는 치환 또는 비치환된 트리아진기인 것인 헤테로환 화합물.
- 청구항 2에 있어서, 상기 Ar1은 하기 화학식 2 내지 7 중 어느 하나로 표시되는 것인 헤테로환 화합물.
[화학식 2]
[화학식 3]
[화학식 4]
[화학식 5]
[화학식 6]
[화학식 7]
o, q, s, u 및 v는 각각 독립적으로 0 내지 4의 정수이고,
p, r 및 t는 각각 독립적으로 0 내지 3의 정수이며,
w는 0 내지 2의 정수이며,
x는 0 내지 5의 정수이고,
R6 내지 R16은 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기이다. - 청구항 3에 있어서, 상기 L은 하기의 화학식 8 내지 12 중 어느 하나로 표시되는 것인 헤테로환 화합물:
[화학식 8]
[화학식 9]
[화학식 10]
[화학식 11]
[화학식 12]
Ar1, Ar2 및 n은 상기 화학식 1에서 정의한 바와 동일하고
y는 0 내지 4의 정수이고,
z, a, b, c, d 및 e는 각각 0 내지 4의 정수이며,
y와 n의 합은 1 내지 5의 정수이고,
z와 a 및 7의 합은 1 내지 7의 정수이며,
b와 c 및 7의 합은 1 내지 7의 정수이고,
d와 e 및 7의 합은 1 내지 7의 정수이며,
R17 내지 R25 는 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 시아노기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로아릴기다. - 청구항 1에 있어서, 상기 화학식 1은 하기 화학식 1-0-1 내지 1-0-12 중 어느 하나로 표시되는 것인 헤테로환 화합물:
[화학식 1-0-1]
[화학식 1-0-2]
[화학식 1-0-3]
[화학식 1-0-4]
[화학식 1-0-5]
[화학식 1-0-6]
[화학식 1-0-7]
[화학식 1-0-8]
[화학식 1-0-9]
[화학식 1-0-10]
[화학식 1-0-11]
[화학식 1-0-12]
상기 화학식 1-0-1 내지 1-0-12에 있어서,
X, R1 내지 R5, L, m 및 n은 상기 화학식 1에서 정의한 바와 동일하고,
o, q, s, u 및 v는 각각 독립적으로 0 내지 4의 정수이고,
p, r 및 t는 각각 독립적으로 0 내지 3의 정수이며,
w는 0 내지 2의 정수이고,
x는 0 내지 5의 정수이며,
R6 내지 R16 는 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 시아노기; 할로겐기; 니트릴기; 니트로기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 플루오레닐기; 치환 또는 비치환된 카바졸기; 또는 N, O, S 및 P 원자 중 1개 이상을 포함하는 치환 또는 비치환된 헤테로고리기다. - 청구항 1에 있어서, 상기 R1, R2 및 R4는 수소인 것인 헤테로환 화합물.
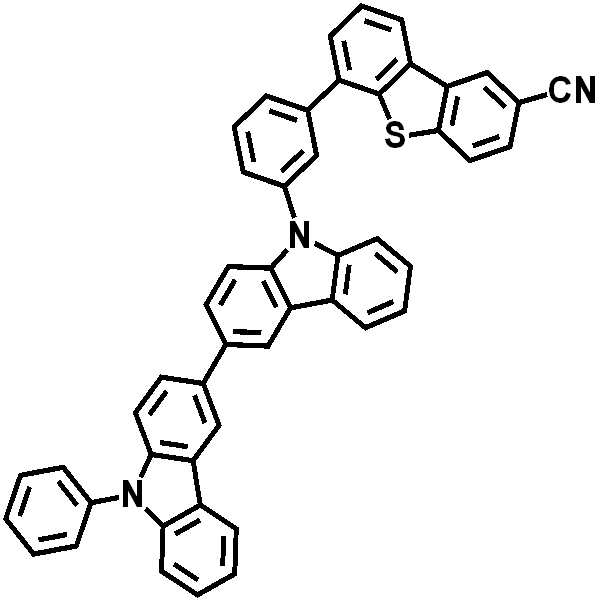
- 청구항 1에 있어서, 상기 화학식 1의 화합물은 하기의 화합물 1 내지 46 중 어느 하나인 것인 헤테로환 화합물:
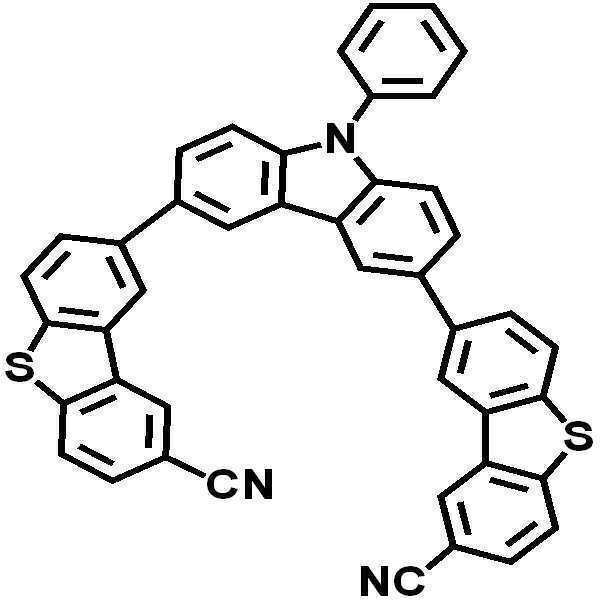
[화합물 1]
[화합물 2]
[화합물 3]
[화합물 4]
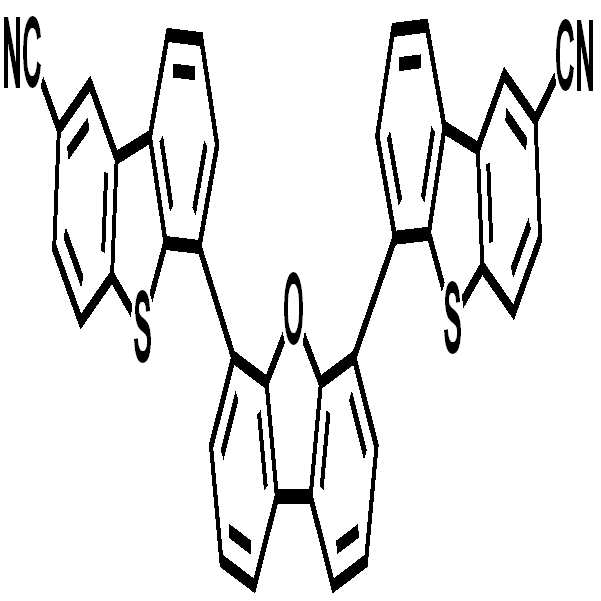
[화합물 5]
[화합물 6]
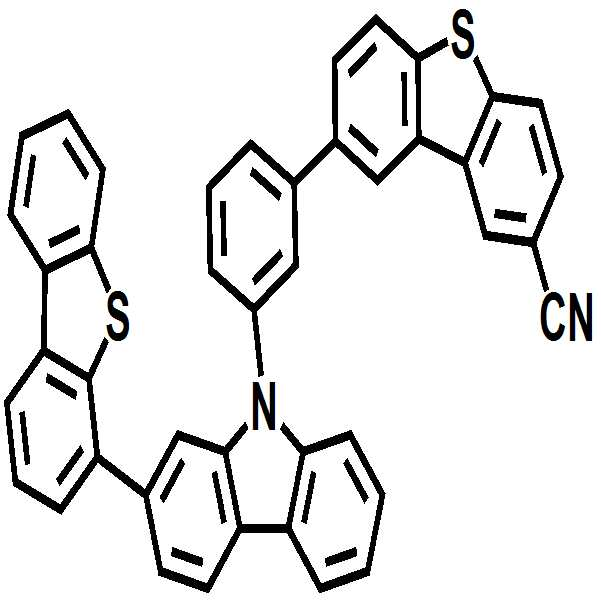
[화합물 7]
[화합물 8]
[화합물 9]
[화합물 10]
[화합물 11]
[화합물 12]
[화합물 13]
[화합물 14]
[화합물 15]
[화합물 16]
[화합물 17]
[화합물 18]
[화합물 19]
[화합물 20]
[화합물 21]
[화합물 22]
[화합물 23]
[화합물 24]
[화합물 25]
[화합물 26]
[화합물 27]
[화합물 28]
[화합물 29]
[화합물 30]
[화합물 31]
[화합물 32]
[화합물 33]
[화합물 34]
[화합물 35]
[화합물 36]
[화합물 37]
[화합물 38]
[화합물 39]
[화합물 40]
[화합물 41]
[화합물 42]
[화합물 43]
[화합물 44]
[화합물 45]
[화합물 46]
- 제1 전극, 제2 전극, 및 상기 제1 전극과 제2 전극 사이에 배치된 1층 이상의 유기물층을 포함하는 유기 전자 소자로서, 상기 유기물층 중 1 층 이상은 청구항 1 내지 8 중 어느 한 항에 따른 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 9에 있어서, 상기 유기 전자 소자는 유기 발광 소자, 유기 태양 전지 및 유기 트랜지스터로 이루어진 군에서 선택되는 것인 유기 전자 소자.
- 청구항 9에 있어서, 상기 유기 전자 소자는 제1 전극, 제2 전극, 및 상기 제1 전극과 제2 전극 사이에 배치된 1층 이상의 유기물층을 포함하는 유기 발광 소자로서, 상기 유기물층 중 1 층 이상은 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 11에 있어서, 상기 유기물층은 정공주입층 또는 정공수송층을 포함하고, 상기 정공주입층 또는 정공수송층이 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 11에 있어서, 상기 유기물층은 발광층을 포함하고, 상기 발광층이 상기 헤테로환 화합물을 발광층의 호스트로서 포함하는 것인 유기 전자 소자.
- 청구항 11에 있어서, 상기 유기물층은 전자수송층을 포함하고, 상기 전자수송층이 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 11에 있어서, 상기 유기물층은 상기 헤테로환 화합물을 포함하는 유기물층 이외에 아릴아미노기, 카바졸기 또는 벤즈카바졸기를 포함하는 화합물을 포함하는 정공주입층 또는 정공수송층을 포함하는 것인 유기 전자 소자.
- 청구항 11에 있어서, 상기 헤테로환 화합물을 포함하는 유기물층은 상기 헤테로환 화합물을 호스트로서 포함하고, 다른 유기화합물, 금속 또는 금속화합물을 도펀트로 포함하는 것인 유기 전자 소자.
- 청구항 9에 있어서, 상기 유기 전자 소자는 제1 전극, 제2 전극 및 상기 제1 전극과 제2 전극 사이에 배치된 광활성층을 포함하는 1층 이상의 유기물층을 포함하는 유기 태양 전지로서, 상기 유기물층 중 1층 이상은 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 17에 있어서, 상기 유기물층은 전하발생층을 포함하고, 상기 전하발생층은 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 17에 있어서, 상기 유기물층은 광활성층을 포함하고, 상기 광활성층은 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 17에 있어서, 상기 유기물층은 전자 주개 및 전자 받개를 포함할 수 있으며, 상기 전자 주개 및 전자 받개는 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 9에 있어서, 상기 유기 전자 소자는 소스, 드레인, 게이트 및 1층 이상의 유기물층을 포함하는 유기 트랜지스터로서, 상기 유기물층 중 1층 이상은 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
- 청구항 21에 있어서, 상기 유기물층은 전하 발생층을 포함할 수 있고, 상기 전하 발생층은 상기 헤테로환 화합물을 포함하는 것인 유기 전자 소자.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020130051548A KR101672074B1 (ko) | 2013-05-07 | 2013-05-07 | 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020130051548A KR101672074B1 (ko) | 2013-05-07 | 2013-05-07 | 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140132244A true KR20140132244A (ko) | 2014-11-17 |
| KR101672074B1 KR101672074B1 (ko) | 2016-11-02 |
Family
ID=52453323
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020130051548A KR101672074B1 (ko) | 2013-05-07 | 2013-05-07 | 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101672074B1 (ko) |
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3061759A1 (en) | 2015-02-24 | 2016-08-31 | Idemitsu Kosan Co., Ltd | Nitrile substituted dibenzofurans |
| KR20170022411A (ko) * | 2015-08-20 | 2017-03-02 | 삼성전자주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| WO2017078494A1 (ko) * | 2015-11-06 | 2017-05-11 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| KR20170097189A (ko) * | 2014-12-23 | 2017-08-25 | 메르크 파텐트 게엠베하 | 2 개의 디벤조푸란 또는 디벤조티오펜 치환기를 갖는 카르바졸 |
| KR20180031224A (ko) * | 2016-09-19 | 2018-03-28 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| US10217946B2 (en) | 2014-03-17 | 2019-02-26 | Idemitsu Kosan Co., Ltd. | Dibenzofurans and dibenzothiophenes |
| KR20190112243A (ko) * | 2018-03-23 | 2019-10-04 | 삼성디스플레이 주식회사 | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
| CN110551086A (zh) * | 2018-06-01 | 2019-12-10 | 乐金显示有限公司 | 有机化合物、以及包括该有机化合物的有机发光二极管和有机发光显示装置 |
| US10615348B2 (en) | 2015-11-16 | 2020-04-07 | Samsung Electronics Co., Ltd. | Organic light-emitting device |
| KR20200110230A (ko) * | 2019-03-15 | 2020-09-23 | 주식회사 엘지화학 | 유기 발광 소자 |
| US11228001B2 (en) | 2017-01-20 | 2022-01-18 | Lg Chem, Ltd. | Hetero-cyclic compound and organic light emitting device comprising the same |
| US11563183B2 (en) | 2017-06-21 | 2023-01-24 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US11588111B2 (en) | 2017-08-04 | 2023-02-21 | Samsung Display Co., Ltd. | Condensed-cyclic compound and organic light-emitting device including the same |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210009942A (ko) | 2019-07-18 | 2021-01-27 | 솔브레인 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20210033332A (ko) | 2019-09-18 | 2021-03-26 | 솔브레인 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090030202A1 (en) * | 2007-07-10 | 2009-01-29 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent element and organic electroluminescent element employing the same |
| JP2009267255A (ja) * | 2008-04-28 | 2009-11-12 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| US20120104370A1 (en) * | 2010-10-29 | 2012-05-03 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole Compound, Light-Emitting Element Material, Organic Semiconductor Material, Light-Emitting Element, Light-Emitting Device, Lighting Device, and Electronic Device |
| KR20120122812A (ko) * | 2011-04-29 | 2012-11-07 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
-
2013
- 2013-05-07 KR KR1020130051548A patent/KR101672074B1/ko active IP Right Grant
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090030202A1 (en) * | 2007-07-10 | 2009-01-29 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent element and organic electroluminescent element employing the same |
| JP2009267255A (ja) * | 2008-04-28 | 2009-11-12 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| US20120104370A1 (en) * | 2010-10-29 | 2012-05-03 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole Compound, Light-Emitting Element Material, Organic Semiconductor Material, Light-Emitting Element, Light-Emitting Device, Lighting Device, and Electronic Device |
| KR20120122812A (ko) * | 2011-04-29 | 2012-11-07 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
Cited By (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10217946B2 (en) | 2014-03-17 | 2019-02-26 | Idemitsu Kosan Co., Ltd. | Dibenzofurans and dibenzothiophenes |
| CN107108589B (zh) * | 2014-12-23 | 2021-01-01 | 默克专利有限公司 | 具有两个二苯并呋喃或二苯并噻吩取代基的咔唑 |
| KR20170097189A (ko) * | 2014-12-23 | 2017-08-25 | 메르크 파텐트 게엠베하 | 2 개의 디벤조푸란 또는 디벤조티오펜 치환기를 갖는 카르바졸 |
| CN107108589A (zh) * | 2014-12-23 | 2017-08-29 | 默克专利有限公司 | 具有两个二苯并呋喃或二苯并噻吩取代基的咔唑 |
| JP2018503622A (ja) * | 2014-12-23 | 2018-02-08 | メルク パテント ゲーエムベーハー | 2個のジベンゾフランまたはジベンゾチオフェン置換基を有するカルバゾール |
| US10600970B2 (en) | 2014-12-23 | 2020-03-24 | Merck Patent Gmbh | Carbazoles with two dibenzofuran or dibenzothiophene substituents |
| EP3061759A1 (en) | 2015-02-24 | 2016-08-31 | Idemitsu Kosan Co., Ltd | Nitrile substituted dibenzofurans |
| KR20170022411A (ko) * | 2015-08-20 | 2017-03-02 | 삼성전자주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| US10193082B2 (en) * | 2015-08-20 | 2019-01-29 | Samsung Electronics Co., Ltd. | Condensed-cyclic compound and organic light emitting device including the same |
| WO2017078494A1 (ko) * | 2015-11-06 | 2017-05-11 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| US10615348B2 (en) | 2015-11-16 | 2020-04-07 | Samsung Electronics Co., Ltd. | Organic light-emitting device |
| KR20180031224A (ko) * | 2016-09-19 | 2018-03-28 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| US11228001B2 (en) | 2017-01-20 | 2022-01-18 | Lg Chem, Ltd. | Hetero-cyclic compound and organic light emitting device comprising the same |
| US11563183B2 (en) | 2017-06-21 | 2023-01-24 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US11844273B2 (en) | 2017-06-21 | 2023-12-12 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US11588111B2 (en) | 2017-08-04 | 2023-02-21 | Samsung Display Co., Ltd. | Condensed-cyclic compound and organic light-emitting device including the same |
| KR20190112243A (ko) * | 2018-03-23 | 2019-10-04 | 삼성디스플레이 주식회사 | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
| KR20190137436A (ko) * | 2018-06-01 | 2019-12-11 | 엘지디스플레이 주식회사 | 유기 화합물과 이를 포함하는 유기발광다이오드 및 유기발광 표시장치 |
| CN110551086A (zh) * | 2018-06-01 | 2019-12-10 | 乐金显示有限公司 | 有机化合物、以及包括该有机化合物的有机发光二极管和有机发光显示装置 |
| CN110551086B (zh) * | 2018-06-01 | 2023-12-08 | 乐金显示有限公司 | 有机化合物、以及包括该有机化合物的有机发光二极管和有机发光显示装置 |
| KR20200110230A (ko) * | 2019-03-15 | 2020-09-23 | 주식회사 엘지화학 | 유기 발광 소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR101672074B1 (ko) | 2016-11-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101672074B1 (ko) | 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 | |
| KR101653920B1 (ko) | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 | |
| KR101380060B1 (ko) | 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 | |
| KR101412437B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| KR101350581B1 (ko) | 새로운 화합물 및 이를 이용한 유기 발광 소자 | |
| KR101503134B1 (ko) | 새로운 함질소 헤테로환 화합물 및 이를 이용한 유기 전자 소자 | |
| KR101408515B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| KR100864154B1 (ko) | 신규한 안트라센 유도체, 이의 제조방법 및 이를 이용한유기전자소자 | |
| KR101434018B1 (ko) | 새로운 화합물 및 이를 이용한 유기 발광 소자 | |
| KR20100079458A (ko) | 비스-카바졸 화합물 및 이를 이용한 유기전기소자, 그 단말 | |
| KR101408632B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| KR20130093195A (ko) | 오원자 헤테로 고리를 포함하는 유기전기소자용 화합물, 이를 포함하는 유기전기소자 및 그 전자 장치 | |
| KR20170096769A (ko) | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 | |
| EP3345891B1 (en) | Amine compound and organic light-emitting device comprising same | |
| KR101628438B1 (ko) | 함질소 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 | |
| KR20130100948A (ko) | 신규한 안트라센 유도체 및 이를 이용한 유기전자소자 | |
| KR101640637B1 (ko) | 신규한 화합물, 그 제조 방법 및 상기 화합물을 이용한 유기 전자 소자 | |
| KR101586531B1 (ko) | 신규한 화합물 및 이를 이용한 유기 발광 소자 | |
| KR20120083241A (ko) | 새로운 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 | |
| KR101380008B1 (ko) | 신규한 안트라센 유도체 및 이를 이용한 유기 전자 소자 | |
| KR101550523B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| KR101550485B1 (ko) | 새로운 화합물 및 이를 포함한 유기 발광 소자 | |
| JP6716854B2 (ja) | ヘテロ環化合物およびこれを含む有機発光素子 | |
| KR101944004B1 (ko) | 아민계 화합물 및 이를 포함하는 유기 발광 소자 | |
| KR101163044B1 (ko) | 안트라센 화합물 및 이를 이용한 유기전기소자, 그 단말 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E90F | Notification of reason for final refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20191016 Year of fee payment: 4 |