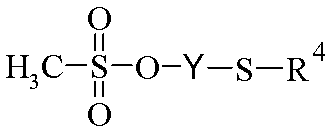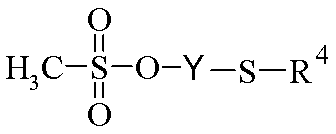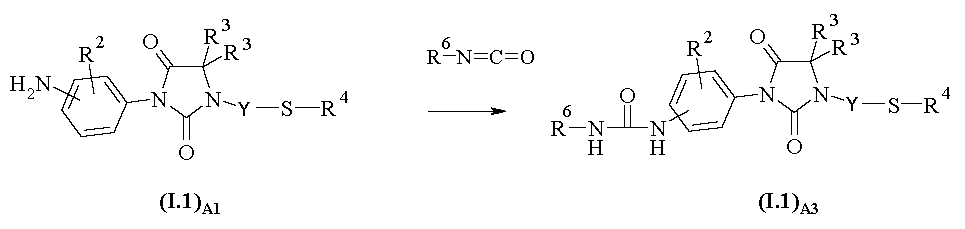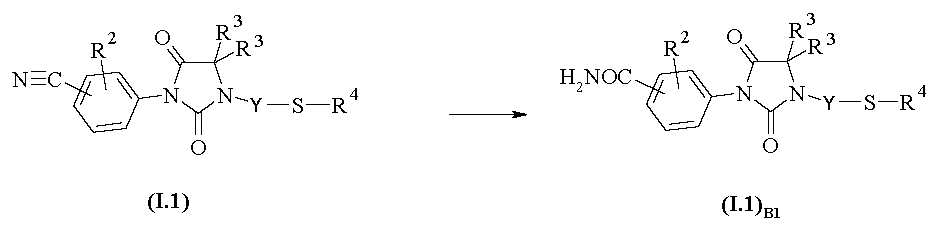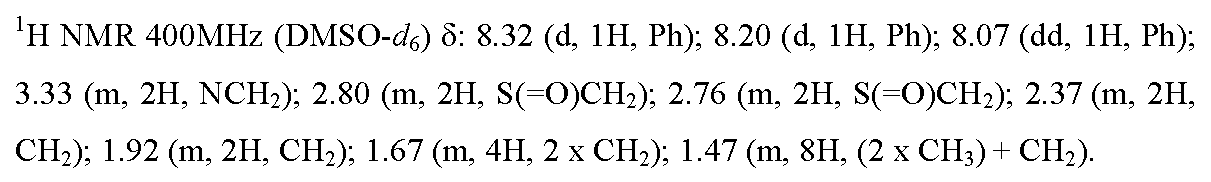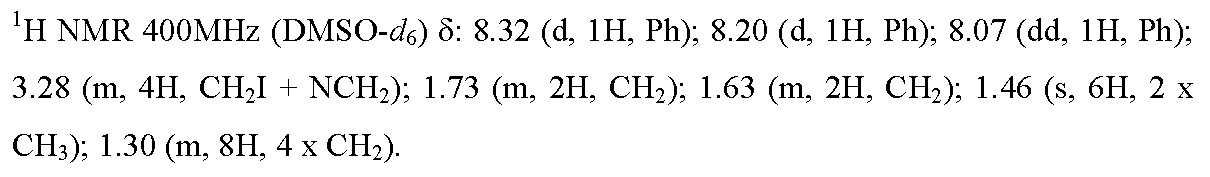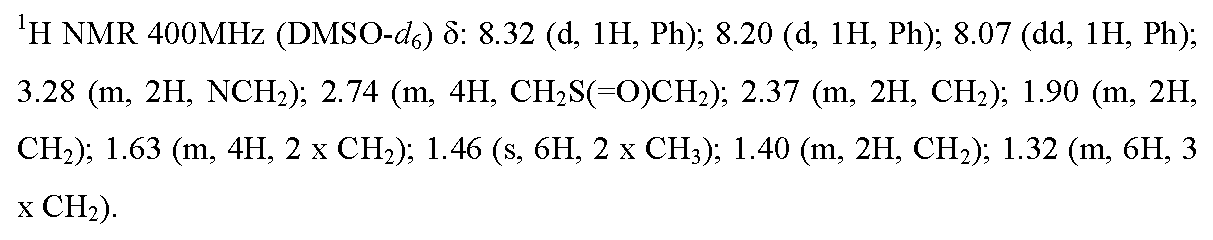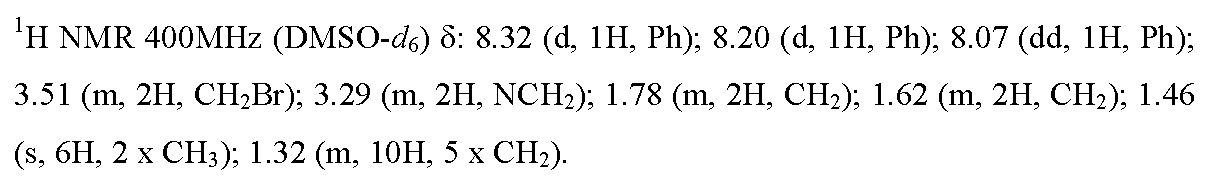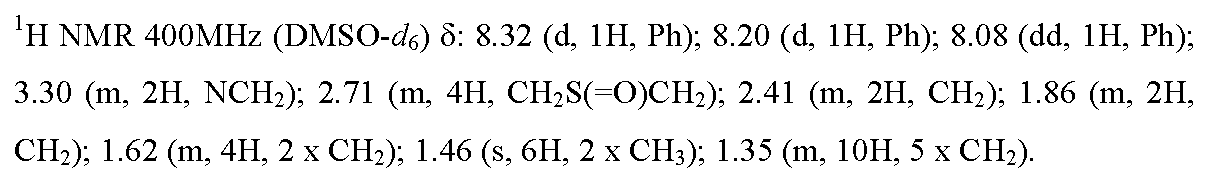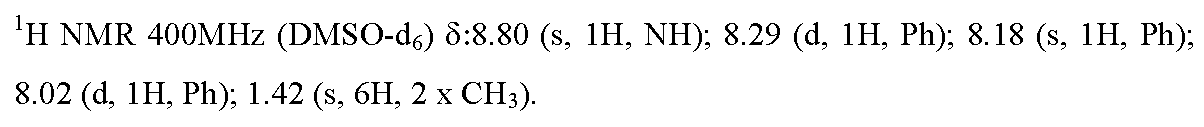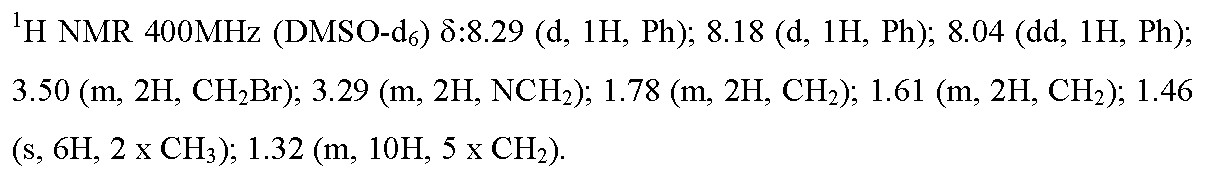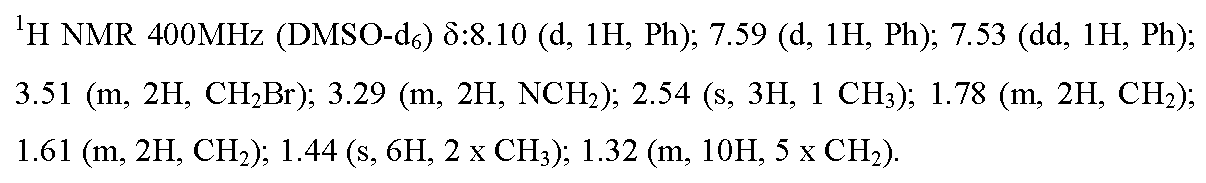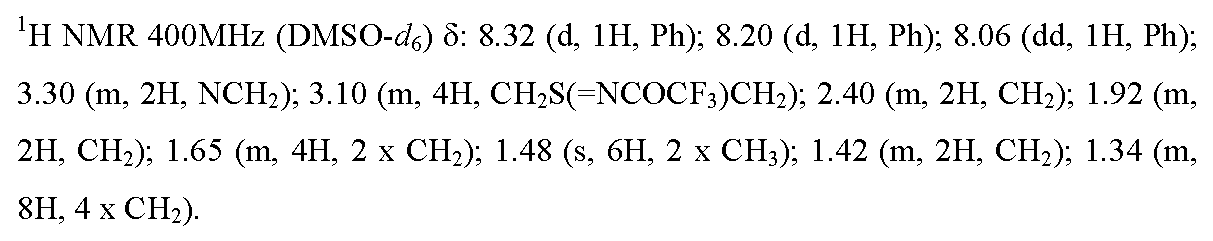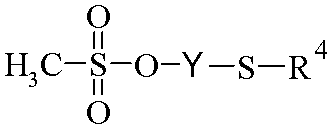발명의 개요
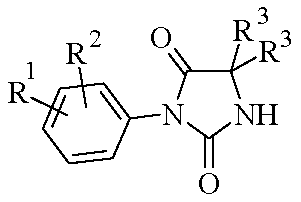
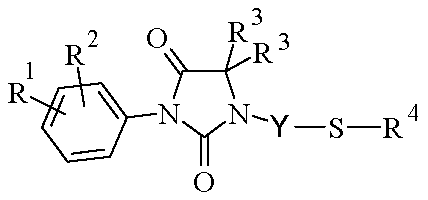
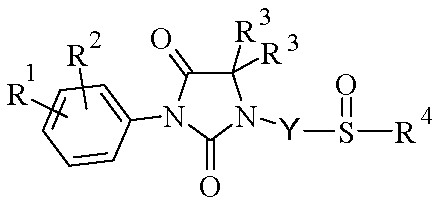
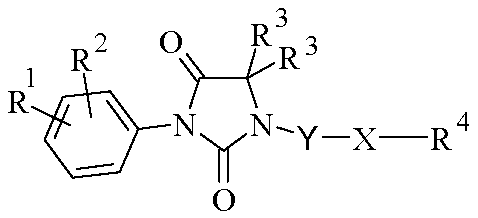
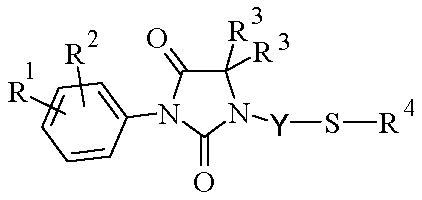
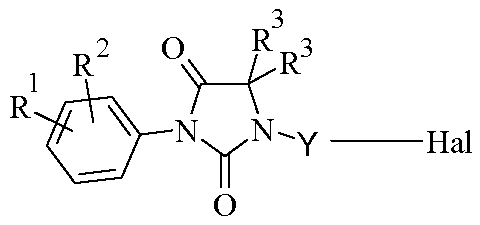
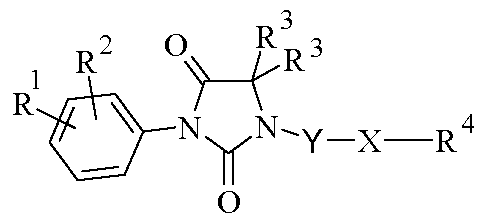
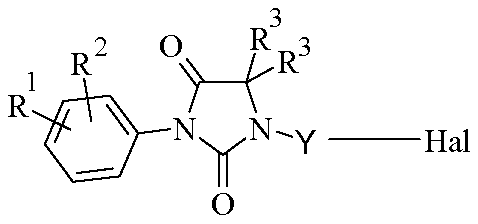
따라서, 본 발명의 대상은 라세미체 또는 거울상이성질체 형태 또는 이들 형태의 임의의 조합물인 하기 화학식 I의 화합물 또는 그의 제약상 허용되는 염이다.
<화학식 I>
상기 식에서,
R1 및 R2는 독립적으로 할로겐 원자, 또는 알킬, 할로알킬, 알콕시, 시아노, 니트로, 아미노, 알킬아미노, 디알킬아미노, -NR8-CO-R5, -NR8-SO2-R5, -NR8-CO-(CH2)n-NR6R7, -NR8-SO2-(CH2)n-NR6R7 또는 -CO-NH2 라디칼을 나타내고;
n은 0, 1, 2, 3, 4, 5 및 6으로부터 선택된 정수를 나타내고;
R5는 알킬, 아릴 또는 헤테로아릴 라디칼을 나타내고;
R6 및 R7은 독립적으로 수소 원자, 알킬 또는 알킬옥시카르보닐 라디칼을 나타내고;
R8은 수소 원자 또는 알킬 라디칼을 나타내고;
R3은 알킬 라디칼 또는 수소 원자를 나타내거나, 또는 2개의 R3 라디칼은 이들이 부착되어 있는 탄소 원자와 함께 3 내지 6개의 구성원을 포함하는 시클로알킬 라디칼을 형성하고;
R4는 2 내지 10개의 탄소 원자를 갖는 할로알킬 라디칼을 나타내고;
Y는 2 내지 14개의 탄소 원자를 갖는 선형 또는 분지형 알킬렌 쇄를 나타내고, 상기 쇄는 포화 또는 불포화일 수 있고, 1개 이상의 추가의 -O- 구성원을 함유할 수 있고;
X는 -S-, -SO-, -SO2-, -S=N(R9)- 또는 -S(O)=N(R9)-를 나타내고;
R9는 수소 원자 또는 할로알킬카르보닐 라디칼을 나타낸다.
바람직하게는, Y는 2 내지 14개의 탄소 원자를 갖는 포화 선형 알킬렌 쇄를 나타낸다.
바람직하게는, R1은 할로겐 원자, 또는 알킬, 알콕시, 시아노, 니트로, 아미노, 알킬아미노, 디알킬아미노, -NR8-CO-R5, -NR8-SO2-R5, -NR8-CO-(CH2)n-NR6R7, -NR8-SO2-(CH2)n-NR6R7, 또는 -CO-NH2 라디칼을 나타내고; R2는 할로겐 원자, 알킬 또는 할로알킬 라디칼을 나타낸다.
바람직하게는, R2는 수소 원자를 나타낸다.
바람직하게는, R8은 수소 원자를 나타낸다.
바람직하게는, R5는 알킬 라디칼을 나타낸다.
바람직하게는, R3은 알킬 라디칼을 나타낸다.
바람직하게는, R4는 4 내지 6개의 탄소 원자 및 3 내지 9개의 불소 원자를 포함하는 할로알킬 라디칼을 나타내고; Y는 5 내지 10개의 탄소 원자를 갖는 알킬렌 쇄를 나타낸다.
바람직하게는, n은 0, 1, 2, 3 및 4로부터 선택된 정수를 나타낸다. 바람직하게는, n은 0 또는 1이다. 바람직하게는, n은 0이다. 바람직하게는, n은 1이다. 대안적으로, n은 2이다. 대안적으로, n은 3이다.
바람직하게는, R1은 파라 위치에 있다.
바람직하게는, R2는 메타 위치에 있다.
바람직하게는, R1은 시아노, 니트로, 아미노, -NR8-CO-R5, -NR8-SO2-R5, -NR8-CO-(CH2)n-NR6R7, -NR8-SO2-(CH2)n-NR6R7, 또는 -CO-NH2 라디칼을 나타내고;
R2는 알킬 또는 할로알킬 라디칼을 나타내고;
R5는 알킬 라디칼을 나타내고;
R6 및 R7은 독립적으로 수소 원자, 알킬 또는 알킬옥시카르보닐 라디칼을 나타내고;
R3은 알킬 라디칼을 나타내거나, 또는 2개의 R3 라디칼은 이들이 부착되어 있는 탄소 원자와 함께 3 내지 6개의 구성원을 포함하는 시클로알킬 라디칼을 형성하고;
R4는 4 내지 6개의 탄소 원자 및 3 내지 9개의 불소 원자를 포함하는 할로알킬 라디칼을 나타내고;
n은 0 또는 1이고;
R9는 수소 원자 또는 -COCF3을 나타낸다.
바람직하게는, R1은 시아노, 니트로, 아미노, -NH-CO-R5, -CO-NH2, -NH-CO-NHR6, -NH-SO2-NHR6 라디칼을 나타내고;
R2는 알킬 또는 할로알킬 라디칼을 나타내고;
R5는 알킬 라디칼을 나타내고;
R6은 수소 원자, 알킬 또는 알킬옥시카르보닐 라디칼을 나타내고;
R3은 알킬 라디칼을 나타내고;
R4는 4 내지 6개의 탄소 원자 및 3 내지 9개의 불소 원자를 포함하는 할로알킬 라디칼을 나타내고;
n은 5 내지 11의 정수를 나타낸다.
바람직하게는, R1은 시아노, 니트로, -NR8-CO-R5, -NR8-SO2-R5, -NR8-CO-(CH2)nNR6R7, -NR8-SO2-(CH2)n-NR6R7 또는 -CO-NH2 라디칼을 나타내고; n은 0 또는 1이고; R5는 알킬 라디칼을 나타내고, R6 및 R7은 독립적으로 수소 원자 또는 알킬 라디칼을 나타내고, R2는 알킬 또는 할로알킬 라디칼을 나타낸다.
바람직하게는, R1은 시아노, 니트로, -NH-CO-R5, -CO-NH2, -NH-CO-NHR6, -NH-SO2-NHR6 라디칼을 나타내고; R5는 알킬 라디칼을 나타내고, R6은 수소 원자 또는 알킬 라디칼을 나타내고, R2는 알킬 또는 할로알킬 라디칼을 나타낸다.
바람직하게는, R1은 니트로 또는 -NR8-CO-R5 라디칼을 나타내고, 여기서 R5는 알킬 라디칼을 나타낸다.
바람직하게는, R1은 니트로 또는 -NH-CO-R5 라디칼을 나타내고, 여기서 R5는 알킬 라디칼을 나타낸다.
바람직하게는, 알킬 라디칼은 메틸 기를 나타내고/거나, 할로알킬 라디칼은 트리플루오로메틸 기 또는 분자식 C5H6F5, C5H4F7, C6H8F5, C6H6F7 또는 C6H4F9의 라디칼을 나타낸다.
바람직하게는, Y는 9 내지 10개의 탄소 원자를 갖는 알킬렌 쇄를 나타낸다.
우선적으로, 본 발명의 대상은 하기로부터 선택된 화학식 I의 화합물이다:
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술포닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)티오]펜틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]펜틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)티오]옥틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]옥틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)티오]데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{11-[(4,4,5,5,5-펜타플루오로펜틸)티오]운데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{11-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]운데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(3,3,4,4,5,5,6,6,6-노나플루오로헥실)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(3,3,4,4,5,5,6,6,6-노나플루오로헥실)술피닐]노닐}이미다졸리딘-2,4-디온
- 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤즈아미드
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤즈아미드
- 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 3-(4-아미노-3-메틸페닐)-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
- 3-(4-아미노-3-메틸페닐)-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 1-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]-3-(1-메틸프로필)우레아
- 1-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]-3-(1-메틸프로필)우레아
- tert-부틸 {[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파모일}카르바메이트
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술포닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
- 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 7-[4-니트로-3-(트리플루오로메틸)페닐]-5-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}-5,7-디아자스피로[3.4]옥탄-6,8-디온
- 5,5-디메틸-3-[4-니트로-2-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]에톡시}에톡시)에틸]이미다졸리딘-2,4-디온
- N-[4-{4,4-디메틸-2,5-디옥소-3-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-1-일}-2-(트리플루오로메틸)페닐]아세트아미드
- N-[4-{4,4-디메틸-2,5-디옥소-3-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]에톡시}에톡시)에틸]이미다졸리딘-1-일}-2-(트리플루오로메틸)페닐]아세트아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N-메틸아세트아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]메탄술폰아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드 히드로클로라이드
- N-[(1Z)-(9-{5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-2,4-디옥소이미다졸리딘-1-일}노닐)(4,4,5,5,5-펜타플루오로펜틸)-4-술파닐리덴]-2,2,2-트리플루오로아세트아미드
- N-[(9-{5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-2,4-디옥소이미다졸리딘-1-일}노닐)(옥시도)(4,4,5,5,5-펜타플루오로펜틸)-4-술파닐리덴]-2,2,2-트리플루오로아세트아미드
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[S-(4,4,5,5,5-펜타플루오로펜틸)술폰이미도일]노닐}이미다졸리딘-2,4-디온.
바람직하게는, 화학식 I의 화합물은 하기로부터 선택된다:
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술포닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)티오]펜틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]펜틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)티오]옥틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]옥틸}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)티오]데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{11-[(4,4,5,5,5-펜타플루오로펜틸)티오]운데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{11-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]운데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(3,3,4,4,5,5,6,6,6-노나플루오로헥실)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(3,3,4,4,5,5,6,6,6-노나플루오로헥실)술피닐]노닐}이미다졸리딘-2,4-디온
- 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤즈아미드
- 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤즈아미드
- 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 3-(4-아미노-3-메틸페닐)-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
- 3-(4-아미노-3-메틸페닐)-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 1-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]-3-(1-메틸프로필)우레아
- 1-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]-3-(1-메틸프로필)우레아
- tert-부틸 {[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파모일}카르바메이트
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술포닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
- 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온.
보다 더 바람직하게는, 본 발명의 대상은 하기로부터 선택된 화학식 I의 화합물이다:
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]데실}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)티오]노닐}이미다졸리딘-2,4-디온
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)술피닐]노닐}이미다졸리딘-2,4-디온
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드 히드로클로라이드.
바람직하게는, 화합물은 하기로부터 선택된다:
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온;
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]데실}이미다졸리딘-2,4-디온;
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)티오]노닐}이미다졸리딘-2,4-디온;
- 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)술피닐]노닐}이미다졸리딘-2,4-디온;
- N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드.
바람직하게는, 화합물은 N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드이다.
바람직하게는, 화합물은 N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드이다.
바람직하게는, 화합물은 N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드 히드로클로라이드이다.
본 발명의 대상은 또한
- 무수 극성 용매 중에서 25 내지 60℃의 온도에서 강염기의 존재 하에 하기 화학식 II의 히단토인 유도체를 하기 화학식 III의 메실레이트 유도체와 축합시킴으로써
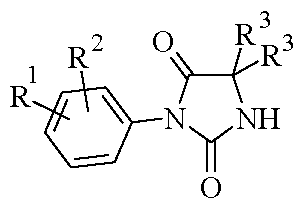
<화학식 II>
(상기 식에서, R1, R2 및 R3은 상기 정의된 바와 같음)
<화학식 III>
(상기 식에서, R4 및 Y는 상기 정의된 바와 같음), 또는
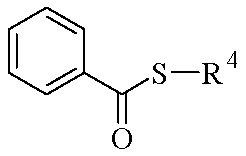
- 극성 양성자성 용매 중에서 하기 화학식 V의 티오벤조일 유도체를 알콜레이트로 처리한 후
<화학식 V>
(상기 식에서, R4는 상기 정의된 바와 같음),
- 극성 용매 중의 용액에서 하기 화학식 IV의 할로겐화 유도체를 첨가함으로써
<화학식 IV>
(상기 식에서, R1, R2, R3 및 Y는 상기 정의된 바와 같음),
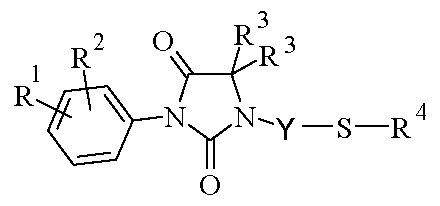
하기 화학식 I.1의 화합물 (X가 황 원자를 나타내는 화학식 I의 화합물)을 수득하는 것을 포함함을 특징으로 하는, 상기 정의된 바와 같은 화학식 I의 화합물의 제조 방법이다.
<화학식 I.1>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
바람직하게는, 상기 방법은 화학식 I.1의 화합물을 하기 화학식 I.2의 술폭시드 (X가 -SO- 라디칼을 나타내는 화학식 I의 화합물)로 산화시키는 단계를 추가로 포함한다.
<화학식 I.2>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
바람직하게는, 화학식 I의 화합물의 제조 방법은 화학식 I.2의 술폭시드 유도체를 하기 화학식 I.3의 술폰 (X가 -SO2- 기를 나타내는 화학식 I의 화합물)으로 산화시키는 단계를 추가로 포함한다.
<화학식 I.3>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
본 발명의 대상은 또한 중간체로서 하기 화합물 중 하나이다:
- 1-(5-요오도펜틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
- 1-(8-요오도옥틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
- 1-(9-브로모노닐)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
- 4-[3-(9-브로모노닐)-4,4-디메틸-2,5-디옥소이미다졸리딘-1-일]-2-(트리플루오로메틸)벤조니트릴
- 5,5-디메틸-3-(3-메틸-4-니트로페닐)이미다졸리딘-2,4-디온
- 1-(9-브로모노닐)-5,5-디메틸-3-(3-메틸-4-니트로페닐)이미다졸리딘-2,4-디온.
본 발명의 대상은 또한 의약으로서의 화학식 I의 화합물 중 하나이다.
본 발명의 대상은 또한 활성 성분으로서 상기 정의된 바와 같은 하나 이상의 화학식 I의 화합물을 제약상 허용되는 지지체와 함께 함유하는 제약 조성물이다.
본 발명의 대상은 또한 암의 치료를 위한 의약의 제조에서의 화학식 I의 화합물의 용도이다.
바람직하게는, 의약은 호르몬-의존성 암의 치료를 위해 의도된다.
바람직하게는, 의약은 안드로겐 수용체를 발현하는 암의 치료를 위해 의도된다
바람직하게는, 의약은 유방 또는 전립선의 암의 치료를 위해 의도된다.
발명의 실시양태의 상세한 설명
따라서, 본 발명의 대상은 라세미체 또는 거울상이성질체 형태 또는 이들 형태의 임의의 조합물인 하기 화학식 I의 화합물이다.
<화학식 I>
상기 식에서,
R1 및 R2는 독립적으로 할로겐 원자, 또는 알킬, 할로알킬, 알콕시, 시아노, 니트로, 아미노, 알킬아미노, 디알킬아미노, -NR8-CO-R5, -NR8-SO2-R5, -NR8-CO-(CH2)n-NR6R7, -NR8-SO2-(CH2)n-NR6R7 또는 -CO-NH2 라디칼을 나타낸다.
n은 0 내지 6에 포함된 정수를 나타낸다.
R5는 알킬, 아릴 또는 헤테로아릴 라디칼을 나타낸다. 바람직하게는, R5는 알킬 라디칼이다.
R6 및 R7은 독립적으로 수소 원자, 알킬 또는 알킬옥시카르보닐 라디칼을 나타낸다.
R8은 수소 원자 또는 알킬 라디칼을 나타낸다. 바람직하게는, R8은 수소 원자를 나타낸다.
R3은 알킬 라디칼 또는 수소 원자를 나타낸다. 대안적으로, 2개의 R3 라디칼은 이들이 부착되어 있는 탄소 원자와 함께 3 내지 6개의 구성원을 포함하는 시클로알킬 라디칼을 형성한다.
R4는 2 내지 10개의 탄소 원자를 갖는 할로알킬 라디칼을 나타낸다.
Y는 2 내지 14개의 탄소 원자를 갖는 알킬렌 쇄를 나타낸다. Y 쇄는 선형 또는 분지형일 수 있다. 이 쇄는 포화 또는 불포화일 수 있다. 이는 하나 이상의 추가의 -O- 구성원을 함유할 수 있다.
X는 -S-, -SO-, -SO2-, -S=N(R9)- 또는 -S(O)=N(R9)-를 나타낸다.
R9는 수소 원자 또는 할로알킬카르보닐 라디칼을 나타낸다.
화학식 I의 화합물은 제약상 허용되는 염 형태일 수 있다.
제약상 허용되는 염은 특히 무기 산의 부가염, 예컨대 히드로클로라이드, 히드로브로마이드, 술페이트, 포스페이트, 디포스페이트 및 니트레이트, 또는 유기 산의 부가염, 예컨대 아세테이트, 말레에이트, 푸마레이트, 타르트레이트, 숙시네이트, 시트레이트, 락테이트, 메탄술포네이트, 벤젠술포네이트, p-톨루엔술포네이트, 파모에이트 및 스테아레이트를 의미한다. 또한, 염기로부터 형성된 염, 예컨대 수산화나트륨 또는 수산화칼륨은, 사용될 수 있는 경우, 본 발명의 범위내에 포함된다. 제약상 허용되는 염의 다른 예에 대해서는 문헌 ["Salt selection for basic drugs", Int. J. Pharm. (1986), 33, 201-217]을 참고할 수 있다.
상기 언급된 정의에서, 할로겐 (또는 할로)의 표현은 플루오로, 클로로, 브로모 또는 요오도 라디칼, 바람직하게는 클로로, 플루오로 또는 브로모를 나타낸다. 더욱 우선적으로, 할로겐 (또는 할로)의 표현은 플루오로 라디칼을 나타낸다.
달리 명시되지 않는 한, 본 발명의 의미 내에서 용어 알킬은 1 내지 12개의 탄소 원자를 포함하는 선형 또는 분지형 알킬 라디칼, 예컨대 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸 및 tert-부틸, 펜틸 또는 아밀, 이소펜틸, 네오펜틸, 헥실 또는 이소헥실, 헵틸, 옥틸, 노닐, 데실, 운데실 또는 도데실 라디칼을 나타낸다. 우선적으로, 알킬 라디칼은 상기에 정의된 바와 같이 1 내지 6개의 탄소 원자를 갖는 알킬 라디칼을 나타내는 (C1-C6)알킬 라디칼, 또는 1 내지 4개의 탄소 원자를 갖는 알킬 라디칼을 나타내는 (C1-C4)알킬 라디칼, 예컨대 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸 및 tert-부틸 라디칼이다.
알콕시 (또는 알킬옥시), 알킬아미노, 디알킬아미노, 할로알킬 또는 알콕시카르보닐 (또는 알킬옥시카르보닐)의 표현에서 용어 알킬은 상기에 정의된 바와 같은 알킬 라디칼을 나타낸다.
보다 특히, 할로알킬은 수소 원자 중 1개 이상이 (및 임의로 모두가) 할로겐 원자 (할로)로 대체된 알킬 라디칼, 예컨대 및 우선적으로 트리플루오로메틸 또는 분자식 C5H6F5, C5H4F7, C6H8F5, C6H6F7 또는 C6H4F9의 라디칼을 의미한다.
할로알킬카르보닐의 표현에서 용어 할로알킬은 상기에 정의된 바와 같은 할로알킬 라디칼을 나타낸다.
달리 명시되지 않는 한, 시클로알킬은 3 내지 6개의 구성원을 포함하는 포화 시클릭 탄소 라디칼, 예컨대 시클로프로필, 시클로부틸, 시클로펜틸 또는 시클로헥실을 의미한다.
본 발명의 의미 내에서, 아릴 라디칼은 모노 또는 폴리시클릭 방향족 유형일 수 있다. 모노시클릭 아릴 라디칼은 페닐, 톨릴, 크실릴, 메시틸, 쿠메닐 라디칼 및 바람직하게는 페닐로부터 선택될 수 있다. 폴리시클릭 아릴 라디칼은 나프틸, 안트릴, 페난트릴, 플루오레닐 라디칼로부터 선택될 수 있다. 이들은 1개 이상의 동일하거나 상이한 라디칼, 예컨대 알킬, 할로알킬, 알콕시, 알콕시카르보닐, 알킬카르보닐옥시, 할로, 시아노, 니트로, 아릴, 아릴옥시, 아릴옥시카르보닐 또는 아릴카르보닐옥시에 의해 임의로 치환될 수 있다.
본 발명의 의미 내에서, 용어 헤테로아릴은 N, O 및 S로부터 선택된 1개 이상의 동일하거나 상이한 헤테로원자를 포함하는 불포화 방향족 고리, 예컨대 푸릴, 티에닐 이속사졸릴, 벤조티아디아졸릴, 피리디닐, 옥사졸릴, 피라졸릴, 피리미디닐 또는 퀴녹살릴을 지칭한다.
2 내지 14개의 탄소 원자를 갖는, 선형 또는 분지형, 포화 또는 불포화 알킬렌 쇄는 예를 들어 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸 및 tert-부틸, 펜틸 또는 아밀, 이소펜틸, 네오펜틸, 헥실 또는 이소헥실, 헵틸, 옥틸, 노닐, 데실, 운데실, 도데실, 에텐, 프로펜, 부텐, 펜텐, 헥센, 헵텐, 옥텐, 노넨, 데실렌, 운데실렌, 도데실렌 또는 부타-1,3-디엔 쇄를 의미한다.
제약상 허용되는 염은 특히 무기 산의 부가염, 예컨대 히드로클로라이드, 히드로브로마이드, 술페이트, 포스페이트, 디포스페이트 및 니트레이트, 또는 유기 산의 부가염, 예컨대 아세테이트, 말레에이트, 푸마레이트, 타르트레이트, 숙시네이트, 시트레이트, 락테이트, 메탄술포네이트, 벤젠술포네이트, p-톨루엔술포네이트, 파모에이트 및 스테아레이트를 의미한다. 또한 염기로부터 형성된 염, 예컨대 수산화나트륨 또는 수산화칼륨은, 사용될 수 있는 경우, 본 발명의 범위내에 포함된다. 제약상 허용되는 염의 다른 예에 대해서는 문헌 ["Salt selection for basic drugs", Int. J. Pharm. (1986), 33, 201-217]을 참고할 수 있다.
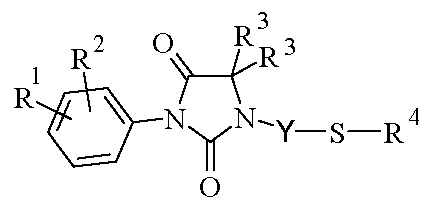
본 발명의 대상은 또한 상기에 정의된 바와 같은 화학식 I의 화합물의 제조 방법이다. 하기 화학식 I.1의 화합물 (X가 황 원자를 나타내는 화학식 I의 화합물)은 하기 화학식 II의 히단토인 유도체와 하기 화학식 III의 메실레이트 유도체의 축합에 의해 수득할 수 있다.
<화학식 I.1>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
<화학식 II>
(상기 식에서, R1, R2 및 R3은 상기 정의된 바와 같음)
<화학식 III>
(상기 식에서, R4 및 Y는 상기 정의된 바와 같음)
축합은 강염기의 존재 하에 수행된다. 축합은 25 내지 60℃의 온도에서 수행된다. 용매는 바람직하게는 무수 극성 용매이다.
화학식 I.1의 화합물은 또한
(i) 하기 화학식 V의 티오벤조일 유도체를 극성 양성자성 용매 중에서 알콜레이트로로 처리한 후, 극성 용매 중의 용액에서 하기 화학식 IV의 할로겐화 유도체를 첨가함으로써 수득될 수 있다.
<화학식 V>
(상기 식에서, R4는 상기 정의된 바와 같음)
<화학식 IV>
(상기 식에서, R1, R2, R3 및 Y는 상기 정의된 바와 같음)
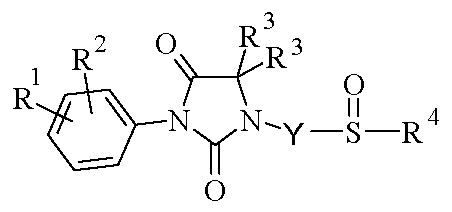
바람직하게는, 화학식 I.1의 화합물은 산화에 의해 하기 화학식 I.2의 술폭시드 (X가 -SO- 라디칼을 나타내는 화학식 I의 화합물)로 전환된다.
<화학식 I.2>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
바람직하게는, 화학식 I.2의 술폭시드 유도체는 산화에 의해 하기 화학식 I.3의 술폰 (X가 -SO2- 기를 나타내는 화학식 I의 화합물)로 전환될 수 있다.
<화학식 I.3>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
본 발명에 따른 화학식 I의 화합물은 하기 반응식 1에 나타낸 합성 경로에 따라 제조될 수 있다. 화학식 I의 화합물 (여기서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)은 중간체의 접근 용이성에 따라 두 가지 상이한 접근법으로 수득될 수 있다. 화학식 I.1의 화합물을 제조하기 위해, 화학식 II의 히단토인 유도체와 화학식 III의 메실레이트 유도체 (WO 2005077968에 기재된 실험 프로토콜에 따라 제조됨)의 축합은 염기, 예컨대 NaH의 존재 하에, 바람직하게는 무수 극성 용매, 예컨대 THF 또는 DMF 중에서 25 내지 60℃에서 5 내지 15 시간 동안 가열함으로써 수행된다. 대안적으로, 화학식 I.1의 화합물은 화학식 V의 티오벤조일 유도체 (WO 2005077968에 기재된 실험 프로토콜에 따라 제조됨)를 극성 양성자성 용매, 우선적으로 MeOH 중의 용액에서 30 분 내지 2 시간 동안 알콜레이트, 예컨대 tBuO-K+로 처리한 후, 극성 용매, 예컨대 MeOH 중의 용액에서 화학식 IV의 할로겐화 유도체를 첨가함으로써 제조될 수 있다. 반응은 일반적으로 약 20℃에서 10 내지 24 시간의 다양한 시간 동안 수행된다. 화학식 I.1의 화합물의 티오에테르 기를 화학식 I.2의 술폭시드로 산화시키는 것은 용매, 예컨대 THF 및 물의 혼합물 중에서 20℃의 온도에서 15 내지 30 분의 시간 동안 1 당량보다 적은 양의 옥손의 존재 하에 수행된다.
화학식 I.2의 술폭시드 유도체의 화학식 I.3의 술폰으로의 전환은 또한 용매, 예컨대 THF 및 물의 혼합물 중에서 옥손의 존재 하에 수행된다. 전체 전환을 수행하기 위해서는 일반적으로 3 당량의 산화제 및 3 내지 5 시간의 반응 시간이 필요하다.
<반응식 1>
화학식 I.2의 술파닐리덴 유도체 (여기서, R2, R3, R4, R9 및 Y는 상기 정의된 바와 같음)는 반응식 I-a에 따라 화학식 I.1의 티오 알킬 유도체로부터 제조된다. 반응은 문헌 [C. Bolm et al. in Organic Letters 2004, vol.6, No. 17, 1305-1307]에 기재된 것과 유사한 실험 조건 하에 수행된다. 반응은 산화제, 예컨대 산화마그네슘의 존재 하에, 20℃ 내지 30℃ (바람직하게는 25℃)의 온도에서, 불활성 용매, 예컨대 테트라히드로푸란 또는 염소화 용매 및 특히 디클로로메탄 중에서 수 시간 동안 아세트아미드 유도체 R9-NH2와 화학식 I.1의 티오 알킬 화합물의 반응에 의해 수행된다. 이어서, 화학식 I.2-a의 유도체를 20℃ 내지 30℃ (바람직하게는 25℃)의 온도에서, 무기 염기 및 특히 수산화칼륨의 존재 하에, 불활성 용매, 예컨대 테트라히드로푸란, 알콜화 용매 및 특히 메탄올 중에서 수 시간 동안 반응시켜, 화학식 I-2의 화합물을 수득한다.
<반응식 I-a>
화학식 I.3의 술폰이미드 유도체 (여기서, R2, R3, R4, R9 및 Y는 상기 정의된 바와 같음)는 반응식 I-b에 따라 화학식 I.2의 술폭시드 유도체로부터 제조된다. 반응은 문헌 [C. Bolm et al. in Organic Letters 2004, vol.6, No. 17, 1305-1307]에 기재된 것과 유사한 실험 조건 하에 수행된다. 반응은 산화제, 예컨대 산화마그네슘의 존재 하에, 20℃ 내지 30℃ (바람직하게는 25℃)의 온도에서, 불활성 용매, 예컨대 테트라히드로푸란 또는 염소화 용매 및 특히 디클로로메탄 중에서 수 시간 동안 아세트아미드 유도체 R9-NH2와 화학식 I.2의 술폭시드 화합물의 반응에 의해 수행된다. 이어서, 화학식 I.3-b의 유도체를 20℃ 내지 30℃ (바람직하게는 25℃)의 온도에서, 무기 염기 및 특히 탄산칼륨의 존재 하에, 불활성 용매, 예컨대 테트라히드로푸란 또는 알콜화 용매 및 특히 메탄올 중에서 수 시간 동안 반응시켜, 화학식 I.3의 화합물을 수득한다.
<반응식 I-b>
A)
R
1
이 임의로 치환된 아미노 기인 화학식 I.1의 화합물의 제조
:
A.1) 아닐린 유도체의 제조:
R1이 니트로 기이고, R2, R3 및 R4가 상기 정의된 바와 같은 특별한 경우, 화학식 I.1A1의 아닐린 유도체의 제조를 반응식 A1에 나타낸다. 화학식 I.1의 화합물의 니트로 기의 환원은 SnCl2, 2H2O를 이용하여 (문헌 [J. Heterocyclic Chem. 1987, 24, 927-930]; [Tetrahedron Letters 1984, 25 (8), 839-842]) 반응 혼합물을 환류 하에 용매, 예컨대 에틸 아세테이트 중에서 수 시간 동안 가열함으로써 수행한다.
<반응식 A1>
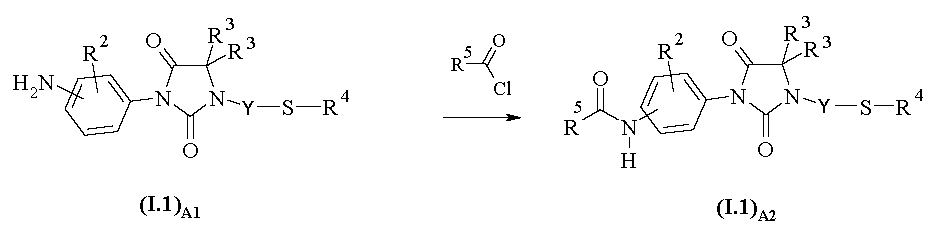
A.2) 아세트아미드 유도체의 제조:
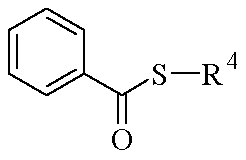
화학식 I.1A2의 아세트아미드 유도체 (여기서, R2, R3, R4 및 R5는 상기 정의된 바와 같음)는 반응식 A2에 따라 화학식 I.1A1의 아닐린 유도체로부터 한 단계로 제조가능하다. 아실화 반응은 과량의 화학식 R5-COCl의 산 클로라이드, 예를 들어 아세틸 클로라이드, 또는 (R5-CO)2O 유형의 무수물, 예컨대 아세트산 무수물을 이용하여 수행될 수 있다. 반응은 일반적으로 약 20℃에서 무수 용매, 예컨대 디클로로메탄 중에서 수 시간 동안 수행된다.
<반응식 A2>
반응식 A2a에서 화학식 I.1A2a의 중간체 (여기서, R2, R3, R4, R5, R8 및 Y는 상기 정의된 바와 같음)의 합성은 화학식 R8-Hal의 할로겐화 시약의 할로겐 원자를 염기, 예컨대 NaH의 존재 하에 극성 비양성자성 용매, 예컨대 DMF 또는 DMSO 중에서 생성된 화학식 I.1A2의 아세트아미드의 음이온으로 친핵성 치환시킴으로써 수행된다. 반응은 일반적으로 20 내지 30℃의 온도에서 1 내지 5 시간 동안 수행된다.
<반응식 A2a>
A.3) 우레아 유도체의 제조:
화학식 I.1A3의 우레아 유도체 (여기서, R2, R3, R4 및 R6은 상기 정의된 바와 같음)는 반응식 A3에 따라 화학식 I.1A1의 아닐린 유도체로부터 한 단계로 제조된다. 반응은 이소시아네이트 유도체 R6-N=C=O의 존재 하에 반응 혼합물을 일반적으로 불활성 용매, 예컨대 염소화 용매 및 특히 1,2-디클로로에탄 중에서 수 시간 동안 70 내지 120℃의 온도로 가열함으로써 수행된다.
<반응식 A3>
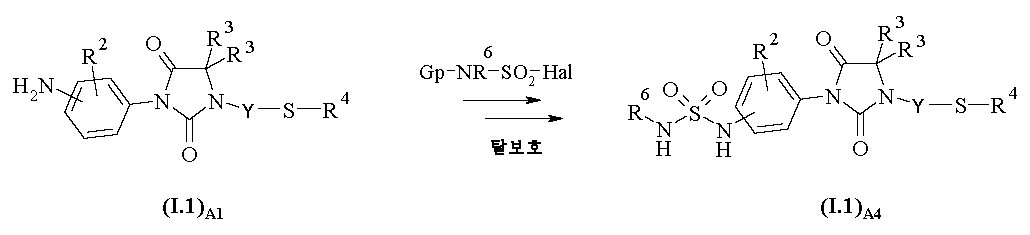
A.4) 술파미드 유도체의 제조:
화학식 I.1A3의 술파미드 유도체 (여기서, R2, R3, R4 및 R6은 상기 정의된 바와 같음)는 반응식 A4에 따라 화학식 I.1A1의 아닐린 유도체로부터 제조된다. 반응은 WO2007125197에 기재된 것과 유사한 실험 조건 하에 수행된다.
<반응식 A4>
A.5) 술폰아미드 유도체의 제조:
화학식 I.1A5의 술폰아미드 유도체 (여기서, R2, R3, R4, R5 및 Y는 상기 정의된 바와 같음)는 반응식 A5에 따라 화학식 I.1A1의 아닐린 유도체로부터 제조된다. 반응은 문헌 [G.H. Chu et al. in Bioorg. Med. Chem. Lett. 2007, 17, 1951-1955]에 기재된 것과 유사한 실험 조건 하에 수행된다. 반응은 20℃ 내지 30℃ (바람직하게는 25℃)의 온도에서, 불활성 용매, 예컨대 테트라히드로푸란, 염소화 용매 및 특히 1,2-디클로로에탄 중에서, 수 시간 동안 술포닐 클로라이드 유도체 R5-SO2-Cl과 화학식 I.1A1의 아닐린 화합물 (여기서, R2, R3, R4는 상기 정의된 바와 같음)의 반응에 의해 수행된다. 이어서, 화학식 I.1A5-1의 디술폰아미드 유도체를 20℃ 내지 30℃ (바람직하게는 25℃)의 온도에서, 무기 염기 및 특히 수산화리튬의 존재 하에, 불활성 용매, 예컨대 테트라히드로푸란, 알콜화 용매 및 특히 메탄올 중에서 수 시간 동안 반응시킨다.
<반응식 A5>
B)
R
1
이 카르복스아미드 기인 화학식 I.1의 화합물의 제조를 위한 합성
:
B.1) 카르복스아미드 유도체의 제조:
화학식 I.1B1의 카르복스아미드 유도체 (여기서, R2, R3 및 R4는 상기 정의된 바와 같음)는 반응식 B1에 따라 화학식 I.1의 니트릴 유도체로부터 한 단계로 제조된다. 가수분해 반응을 트리플루오로아세트산 및 황산의 혼합물 중에서 수행한 후, 수성 매질 중에서 처리한다 (문헌 [J. Org. Chem. 2005, 70 (5), 1926-1929]).
<반응식 B1>
C)
화학식 II의 중간체의 제조
:
화학식 II의 아릴히단토인 중간체 (여기서, R1, R2 및 R3은 상기 정의된 바와 같음)의 합성은 하기 반응식에 기재된 전략에 따라 수행될 수 있다:
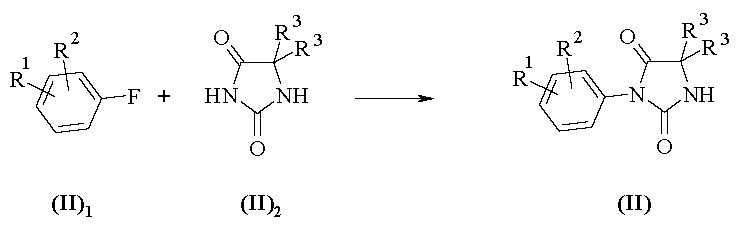
C.1) 축합에 의한 아릴히단토인의 제조:
반응식 B1에서 화학식 II의 아릴히단토인의 합성은 화학식 II1의 화합물의 방향족 고리에 보유된 불소 원자를 염기, 예컨대 K2CO3의 존재 하에 생성된 화학식 II2의 히단토인의 음이온으로 친핵성 치환시킴으로써 수행될 수 있다. 반응은 65 내지 140℃의 온도에서 극성 비양성자성 용매, 예컨대 DMF 또는 DMSO 중에서 수행된다. 상기 온도 및 반응 시간은 R1 및 R2의 성질에 의해 크게 좌우되는 불소 원자의 핵 배척 이탈기 특성의 함수이다. 상업적으로 입수되지 않는 화학식 II2의 히단토인은 문헌 (예를 들어 [J. Med. Chem. 1984, 27 (12), 1663-8])에 기재된 방법에 따라 제조될 수 있다. 상업적으로 입수되지 않는 화학식 II2의 히단토인은 문헌 (예를 들어 [J. Med. Chem. 1984, 27 (12), 1663-8])에 기재된 방법에 따라 제조될 수 있다.
<반응식 C1>
R1 및 R2가 반응식 C1에 기재된 방향족 친핵성 치환을 촉진시키기에는 불충분게 전자를 끄는 경우에는, 화학식 II의 화합물을 수득하기 위해서, 아세트산구리의 존재 하에 아릴 보론산과 화학식 II2의 히단토인의 커플링에 의한 접근법이 고려될 수 있다 (문헌 [Synlett 2006, 14, 2290-2]).
C.2) 아릴이소시아네이트로부터 히단토인 고리의 구성에 의한 아릴히단토인으 제조:
이 경우에는, 화학식 II의 히단토인의 형성은 문헌 [Bioorg. Med. Chem. Lett. 2004, 14, 5285]에 기재된 프로토콜에 따라 수행된다.
C.3) 아미노에스테르의 이소시아네이트로부터 히단토인 고리의 구성에 의한 아릴히단토인의 제조:
대안적으로, 화학식 II의 아릴히단토인은 문헌 [Eur. J. Med. Chem. 1984, 19 (3), 261]에 기재된 바와 같이 아미노에스테르의 이소시아네이트로부터 합성될 수 있다.
D)
화학식 IV의 중간체의 제조
:
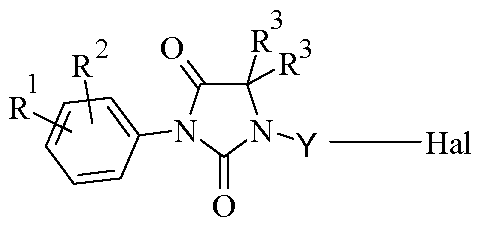
반응식 D1에서 화학식 IV의 중간체 (여기서, R1, R1, R3 및 Y는 상기 정의된 바와 같음)의 합성은 화학식 Hal-(CH2)n-Hal의 디할로겐화 시약의 할로겐 원자를 염기, 예컨대 NaH의 존재 하에 극성 비양성자성 용매, 예컨대 DMF 또는 DMSO 중에서 생성된 화학식 II의 히단토인의 음이온으로 친핵성 치환시킴으로써 수행된다. 반응은 일반적으로 20 내지 60℃의 온도에서 1 내지 15 시간 동안 수행된다.
<반응식 D1>
따라서, 본 발명의 대상은 또한
강염기의 존재 하에 25 내지 60℃의 온도에서 무수 극성 용매 중에서 하기 화학식 II의 히단토인 유도체를 하기 화학식 III의 메실레이트 유도체와 축합시킴으로써
<화학식 II>
(상기 식에서, R1, R2 및 R3은 상기 정의된 바와 같음)
<화학식 III>
(상기 식에서, R4 및 Y는 상기 정의된 바와 같음), 또는
하기 화학식 V의 티오벤조일 유도체를 극성 양성자성 용매 중에서 알콜레이트로 처리한 후, 극성 용매 중의 용액에서 하기 화학식 IV의 할로겐화 유도체를 첨가함으로써
<화학식 V>
(상기 식에서, R4는 상기 정의된 바와 같음)
<화학식 IV>
(상기 식에서, R1, R2, R3 및 Y는 상기 정의된 바와 같음)
하기 화학식 I.1의 화합물 (X가 황 원자를 나타내는 화학식 I의 화합물)을 수득하고
<화학식 I.1>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음),
화학식 I.1의 화합물의 티오에테르 기를 하기 화학식 I.2의 술폭시드 (X가 -SO- 라디칼을 나타내는 화학식 I의 화합물)로 산화시키고
<화학식 I.2>
(상기 식에서, R1, R2, R3, R4 및 Y가 상기 정의된 바와 같음),
화학식 I.2의 술폭시드 유도체를 하기 화학식 I.3의 술폰 (X가 -SO2- 기를 나타내는 화학식 I의 화합물)으로 산화시키는 것을 포함하는, 상기 정의된 바와 같은 화학식 I의 화합물의 제조 방법이다.
<화학식 I.3>
(상기 식에서, R1, R2, R3, R4 및 Y는 상기 정의된 바와 같음)
우선적으로, 상기 언급된 산화는 옥손(Oxone?)의 존재 하에 수행된다.
화학식 I의 화합물의 염화는 당업자에게 공지된 방법에 의해 수행될 수 있다. 예를 들어, 염화는 염기 또는 산, 예를 들어 수산화나트륨, 수산화칼륨, 또는 염산의 첨가에 의해 수행될 수 있다.
변형예에 따르면, 본 발명의 대상은 중간체로서 하기 화합물 중 하나이다:
- 1-(5-요오도펜틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
1-(8-요오도옥틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
- 1-(9-브로모노닐)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
- 4-(4,4-디메틸-2,5-디옥소이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
- 4-[3-(9-브로모노닐)-4,4-디메틸-2,5-디옥소이미다졸리딘-1-일]-2-(트리플루오로메틸)벤조니트릴
- 5,5-디메틸-3-(3-메틸-4-니트로페닐)이미다졸리딘-2,4-디온
- 1-(9-브로모노닐)-5,5-디메틸-3-(3-메틸-4-니트로페닐)이미다졸리딘-2,4-디온.
본 발명에 따른 화학식 I의 화합물은 유용한 약리학적 특성을 갖는다. 실제로, 본 발명의 화학식 I의 화합물이 항종양 (항암) 활성, 보다 특히 안드로겐 수용체를 발현하는 세포, 예컨대 LnCAP 유형 전립선 세포의 세포 증식에 대한 억제 활성을 갖는다는 것이 이미 발견되었다. 따라서, 본 발명의 화합물은 상이한 치료 적용에 사용될 수 있다. 이들은 유리하게는 암, 특히 호르몬-의존성 암, 안드로겐 수용체를 발현하는 암 및 보다 특히 유방암 및 전립선암의 치료에 사용된다. 본 발명의 화합물의 약리학적 특성의 설명은 이후 실험 부분에서 확인될 것이다.
따라서, 본원의 대상은 또한 의약으로서 상기 정의된 바와 같은 화학식 I의 화합물이다.
또한, 본원의 대상은 증식성 질환, 우선적으로 암, 매우 우선적으로 호르몬-의존성 암 또는 안드로겐 수용체를 발현하는 암, 또는 전립선암 및 유방암 및 매우 우선적으로 전립선암의 치료를 위한 의약으로서 상기 정의된 바와 같은 화학식 I의 화합물이다.
본원의 대상은 또한 활성 성분으로서 상기 정의된 바와 같은 하나 이상의 화학식 I의 화합물을 제약상 허용되는 지지체와 함께 함유하는 제약 조성물이다.
본원의 대상은 또한 항종양 의약의 제조에서의 본 발명에 따른 화학식 I의 화합물의 용도이다.
본원의 대상은 또한 세포 증식의 억제를 위한 의약의 제조에서의 본 발명에 따른 화학식 I의 화합물의 용도이다.
본원의 대상은 또한 증식성 질환, 우선적으로 암, 매우 우선적으로 호르몬-의존성 암 또는 안드로겐 수용체를 발현하는 암, 또는 전립선암 및 유방암 및 매우 우선적으로 전립선암의 치료를 위한 의약의 제조에서의 본 발명에 따른 화학식 I의 화합물의 용도이다.
제약 조성물은 고체 형태, 예를 들어 분말, 과립, 정제, 젤라틴 캡슐일 수 있다. 적절한 고체 지지체는 예를 들어 인산칼슘, 스테아르산마그네슘, 활석, 당, 락토스, 덱스트린, 전분, 젤라틴, 셀룰로스, 메틸 셀룰로스, 나트륨 카르복시메틸 셀룰로스, 폴리비닐피롤리딘 및 왁스일 수 있다.
본 발명의 화합물을 함유하는 제약 조성물은 또한 액체 형태, 예를 들어 용액, 에멀젼, 현탁액 또는 시럽으로 제시될 수 있다. 적절한 액체 지지체는 예를 들어 물, 유기 용매, 예컨대 글리세롤 또는 글리콜, 뿐만 아니라 제약상 허용되는 오일 또는 지방에 첨가된 물 중에서 다양한 비율의 이들의 혼합물일 수 있다. 멸균 액체 조성물은 근육내, 복강내 또는 피하 주사에 사용될 수 있고, 멸균 조성물은 또한 정맥내 경로에 의해 투여될 수 있다.
본문에 사용된 모든 전문 학술 용어는 당업자에게 공지된 의미를 갖는다. 더욱이, 모든 특허 (또는 특허 출원) 뿐만 아니라 다른 문헌 참고은 본원에 참고로 포함된다.
<실시예>
실험 부분
가변기 R1, R2, R3, X, n 및 R4의 정의에 따라, 본 발명에 따른 화합물은 상기 기재된 상이한 방법에 따라 제조될 수 있다.
실시예는 상기 절차를 설명하기 위해 제시되며, 어떠한 경우에도 본 발명의 범위를 제한하는 것으로 고려되어서는 안된다.
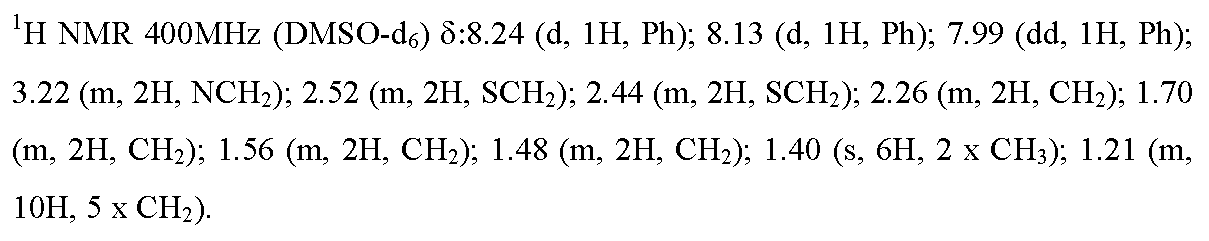
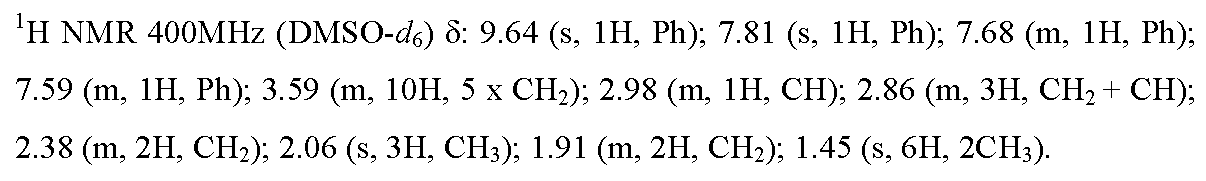
실시예 1 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온
NaH (60%에서) (44 mg, 1.1 mmol)를 아르곤 하에 무수 DMF (8 ml) 중 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-이미다졸리딘-2,4-디온 (317 mg, 1 mmol)의 용액에 첨가하였다. 기체 방출에 의해 반응 매질의 색이 오렌지색으로 변하였다. 23℃에서 1 시간 동안 교반을 유지한 후, 9-[(4,4,5,5,5-펜타플루오로펜틸)-티오]노닐 메탄술포네이트 (WO 2005077968에 기재된 실험 프로토콜에 따라 제조됨) (332 mg, 0.8 mmol)를 첨가하였다. 15 시간 동안 반응시킨 후, 반응 매질을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: CH2Cl2/AcOEt: 1/1 -> 0/1). 목적 화합물을 72% (364 mg)의 수율로 연황색 오일의 형태로 수득하였다.
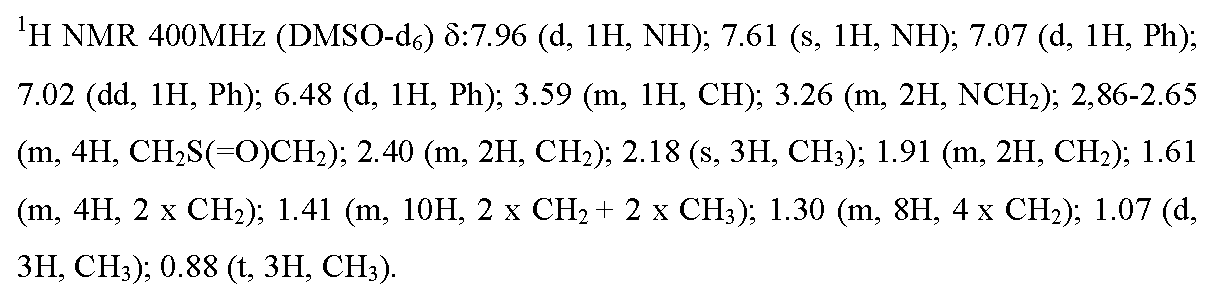
실시예 2 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
옥손? (211 mg, 0.34 mmol) 및 물 (10 ml)을 THF (75 ml) 중 실시예 1에 기재된 화합물 (364 mg, 0.57 mmol)의 용액에 첨가하였다. 반응 혼합물을 20 분 동안 (출발 생성물의 완전한 전환에 필요한 시간) 교반한 다음, 물 (100 ml)에 부었다. 상기 화합물을 AcOEt (2 x 75 ml)로 추출하고, 유기상을 합하고, 소금물로 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: CH2Cl2/AcOEt: 1/1 -> 1/4). 목적 화합물을 86% (321 mg)의 수율로 무색 오일의 형태로 수득하였다.
실시예 3 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술포닐]노닐}이미다졸리딘-2,4-디온
옥손? (566 mg, 0.93 mmol)을 THF (6 ml) 중 실시예 2의 화합물 (200 mg, 0.31 mmol)의 용액에 첨가하였다. 반응 혼합물을 물 (3 ml)로 마무리하고, 23℃에서 3 시간 30 분 동안 (출발 생성물의 전체 전환에 필요한 시간) 교반하였다. 이어서, 혼합물을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 경사분리한 후, 유기상을 합하고, 소금물 (20 ml)로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축에 의해 건조시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 1/1 -> 3/7). 목적 화합물을 89% (185 mg)의 수율로 무색 오일의 형태로 수득하였다.
실시예 4 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)티오]펜틸}이미다졸리딘-2,4-디온
4.1) 1-(5-요오도펜틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
NaH (60%까지) (65 mg, 1.6 mmol)를 아르곤 하에 무수 DMF (20 ml) 중 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-이미다졸리딘-2,4-디온 (500 mg, 1.6 mmol)의 용액에 첨가하였다. 기체 방출에 의해 반응 매질의 색이 오렌지색으로 변하였다. 23℃에서 1 시간 동안 교반을 유지한 후, 희석하지 않고, 1,5-디요오도펜탄 (350 ㎕, 2.4 mmol)을 첨가하였다. 15 시간 동안 반응시킨 후, 반응 매질을 NH4Cl의 포화 수용액 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 7/3 -> 6/4). 목적 화합물을 47% (380 mg)의 수율로 무색 오일의 형태로 수득하였다.
4.2) 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)티오]펜틸}이미다졸리딘-2,4-디온
tBuO-K+ (124 mg, 1.11 mmol)를 아르곤 하에 MeOH (10 ml) 중 S-(4,4,5,5,5-펜타플루오로펜틸) 벤젠-카르보티오에이트 (WO 2005077968에 기재된 실험 프로토콜에 따라 제조됨) (221 mg, 0.74 mmol)의 용액에 첨가하고, 23℃에서 30 분 동안 교반을 유지하였다. 이어서, MeOH (10 ml) 중 중간체 4.1 (380 mg, 0.74 mmol)의 용액을 한번에 첨가하였다. 24 시간 동안 교반한 후, 반응 혼합물을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 경사분리한 후, 유기상을 합하고, 물 (20 ml) 및 소금물 (20 ml)로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축에 의해 건조시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 7/3 -> 6/4). 목적 화합물을 75% (320 mg)의 수율로 무색 오일의 형태로 수득하였다.
실시예 5 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{5-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]펜틸}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 4의 화합물로 교체하였다. 136 mg의 백색 고체를 수득하였다 (73%). 융점: 95-96℃.
실시예 6 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)티오]옥틸}이미다졸리딘-2,4-디온
6.1) 1-(8-요오도옥틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 중간체 4.1의 합성에 대해 기재된 것과 동일하지만, 1,5-디요오도펜탄을 1,8-디요오도옥탄으로 교체하였다. 목적 화합물을 44% (229 mg)의 수율로 연황색 오일의 형태로 수득하였다.
6.2) 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)티오]옥틸}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 4의 화합물의 합성에 대해 기재된 것과 동일하지만, 중간체 4.1을 중간체 6.1로 교체하였다. 연황색 오일을 78%의 수율로 수득하였다.
실시예 7 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{8-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]옥틸}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 6으로 교체하였다. 61 mg의 연황색 오일을 수득하였다 (64%).
실시예 8 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)티오]데실}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 1의 화합물의 합성에 대해 기재된 것과 동일하지만, 9-[(4,4,5,5,5-펜타플루오로펜틸)-티오]노닐 메탄술포네이트를 10-[(4,4,5,5,5-펜타플루오로펜틸)티오]데실 메탄술포네이트 (WO 2005077968에 기재된 것과 유사한 실험 프로토콜에 따라 제조됨)로 교체하였다. 목적 화합물을 13% (125 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 9 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{10-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]데실}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 8의 화합물로 교체하였다. 목적 화합물을 74% (71 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 10 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{11-[(4,4,5,5,5-펜타플루오로펜틸)티오]운데실}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 1의 화합물의 합성에 대해 기재된 것과 동일하지만, 9-[(4,4,5,5,5-펜타플루오로펜틸)-티오]노닐 메탄술포네이트를 10-[(4,4,5,5,5-펜타플루오로펜틸)티오]운데실 메탄술포네이트 (WO 2005077968에 기재된 것과 유사한 실험 프로토콜에 따라 제조됨)로 교체하였다. 목적 화합물을 43% (328 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 11 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{11-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]운데실}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 10으로 교체하였다. 목적 화합물을 72% (240 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 12 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)티오]노닐}이미다졸리딘-2,4-디온
12.1) 1-(9-브로모노닐)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 중간체 4.1의 합성에 대해 기재된 것과 동일하지만, 1,5-디요오도펜탄을 1,9-디브로모노난으로 교체하였다. 목적 화합물을 45% (1.24 g)의 수율로 연황색 오일의 형태로 수득하였다.
12.2) 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)티오]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 4의 합성에 대해 기재된 것과 동일하지만, 중간체 4.1을 중간체 12.1로 교체하고, 중간체 S-(4,4,5,5,5-펜타플루오로펜틸) 벤젠-카르보티오에이트를 S-(4,4,4-트리플루오로부틸) 벤젠카르보티오에이트 (WO 2005077968에 따라 제조됨)로 교체하였다. 목적 화합물을 83% (231 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 13 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,4-트리플루오로부틸)술피닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 12의 화합물로 교체하였다. 연황색 오일을 73% (140 mg)의 수율로 수득하였다.
실시예 14 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(3,3,4,4,5,5,6,6,6-노나플루오로헥실)티오]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 4의 합성에 대해 기재된 것과 동일하지만, 중간체 4.1을 중간체 12.1로 교체하고, 중간체 S-(4,4,5,5,5-펜타플루오로펜틸) 벤젠-카르보티오에이트를 S-(3,3,4,4,5,5,6,6,6-노나플루오로헥실) 벤젠카르보티오에이트 (WO 2005077968에 따라 제조됨)로 교체하였다. 목적 화합물을 78% (212 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 15 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(3,3,4,4,5,5,6,6,6-노나플루오로헥실)술피닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 14의 화합물로 교체하였다. 연황색 오일을 85% (145 mg)의 수율로 수득하였다.
실시예 16 : 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온
SnCl2, 2H2O (3.84 g, 17 mmol)를 AcOEt (30 ml)에 용해된 실시예 1의 화합물 (1.08 g, 1.7 mmol)에 첨가하였다. 반응 혼합물을 환류 하에 출발 화합물이 사라질 때까지 (5 시간 30 분) 가열한 다음, 빙조를 이용하여 냉각시켰다. AcOEt (30 ml)로 희석한 후, 혼합물을 NaHCO3의 1M 수용액 (120 ml)에 부었다. 혼합물을 수 시간 동안 교반하였고, 이 동안 백색 침전물이 형성되었다. 이 침전물을 셀라이트 상에서 여과에 의해 제거하였다. 여과물을 경사분리하고, 유기 용액을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축에 의해 건조시켰다. 목적 화합물을 84% (868 mg)의 수율로 황색 오일의 형태로 수득하였다.
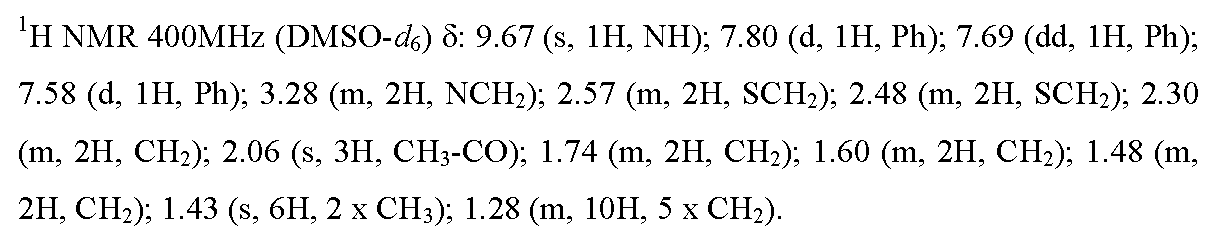
실시예 17 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
아세틸 클로라이드 (1 ml, 37 eq)를 23℃에서 무수 CH2Cl2 (2 ml) 중 실시예 16 (230 mg, 0.38 mmol)의 용액에 적가하였다. 반응 혼합물을 1 시간 동안 교반하고, 진공 하에 농축에 의해 건조시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 1/1 -> 3/7). 순수한 분획을 수집하고 농축시킨 후, 목적 화합물을 무색 오일의 형태로 수득하였고, 이를 91% (225 mg)의 수율로 천천히 결정화시켰다. 융점: 84-86℃.
실시예 18 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 17의 화합물로 교체하였다. 무색 오일을 61% (98 mg)의 수율로 수득하였다.
실시예 19 : 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
19.1) 4-(4,4-디메틸-2,5-디옥소이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
DMF (45 ml) 중 4-플루오로-2-(트리플루오로메틸)벤조니트릴 (5.67 mg, 30 mmol), 5,5-디메틸-히단토인 (7.68 g, 60 mmol), K2CO3 (8.28 g, 60 mmol)의 혼합물을 3개의 튜브에 동일한 분량으로 분배하여 마이크로파 오븐에 넣었다. 자기 교반 하에, 각각의 튜브를 140℃에서 20 분 동안 조사하였다. 이어서, 반응 물질들을 합하고, 물 (200 ml)에 붓고, AcOEt (2 x 75 ml)로 추출하였다. 유기상을 합하고, 소금물로 세척하고, Na2SO4 상에서 건조시키고, 여과하였다. 여과물을 감압하에 농축시키고, 잔류물을 Et2O (25 ml)로부터 결정화시켰다. EtOH (75 ml)로부터 재결정화시킨 후, 분말을 여과하고, 진공하에 건조시켰다. 목적 화합물을 46% (4.1 g)의 수율로 백색 고체의 형태로 수득하였다. 융점: 212-213℃.
19.2) 4-[3-(9-브로모노닐)-4,4-디메틸-2,5-디옥소이미다졸리딘-1-일]-2-(트리플루오로메틸)벤조니트릴
이용된 실험 프로토콜은 중간체 12.1의 합성에 대해 기재된 것과 동일하지만, 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온을 중간체 19.1로 교체하였다. 목적 화합물을 80%의 수율로 황색 오일의 형태로 수득하였다.
19.3) 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
이용된 실험 프로토콜은 중간체 4.2의 합성에 대해 기재된 것과 동일하지만, 중간체 4.1을 중간체 19.2로 교체하였다. 목적 화합물을 89%의 수율로 황색 오일의 형태로 수득하였다.
실시예 20 : 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤조니트릴
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 19의 화합물로 교체하였다. 무색 오일을 78%의 수율로 수득하였다.
실시예 21 : 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤즈아미드
실시예 19의 화합물 (359 mg, 0.58 mmol)을 트리플루오로아세트산 (4 ml) 및 황산 (1 ml)과 혼합하였다. 60℃에서 15 시간 동안 교반한 후, 반응 매질을 물-얼음 혼합물에 붓고, AcOEt (2 x 50 ml)로 추출하였다. 유기상을 합하고, 물, NaHCO3의 포화 수용액 및 소금물로 연속 세척하였다. 이어서, 유기 용액을 Na2SO4 상에서 건조시키고, 여과하고, 용매를 감압 하에 증발시켰다. 증발 잔류물을 실리카 칼럼 상의 크로마토그래피에 의해 정제하였다 (용리액: 헵탄/AcOEt: 9/1 -> 4/6). 목적 화합물을 70%의 수율로 황색 오일의 형태로 수득하였다.
실시예 22 : 4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)벤즈아미드
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 21의 화합물로 교체하였다. 무색 오일을 50%의 수율로 수득하였다.
실시예 23 : 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
23.1) 5,5-디메틸-3-(3-메틸-4-니트로페닐)이미다졸리딘-2,4-디온
DMF (15 ml) 중 5-플루오로-2-니트로톨루엔 (1.55 g, 10 mmol), 5,5-디메틸히단토인 (1.28 g, 10 mmol), K2CO3 (1.38 g, 10 mmol)의 혼합물을 바이알에 도입하여 마이크로파 오븐에 넣고, 자기 교반 하에 100℃에서 70 분 동안 조사하였다. 이어서, 반응 혼합물을 물 (200 ml)에 붓고, AcOEt (2 x 75 ml)로 추출하였다. 유기상을 합하고, 소금물로 세척하고, Na2SO4 상에서 건조시키고, 여과하였다. 여과물을 감압하에 농축시키고, 잔류물을 실리카 칼럼 상의 크로마토그래피에 의해 정제하였다 (용리액: 헵탄/AcOEt: 7/3). 목적 화합물을 25% (666 mg)의 수율로 백색 고체의 형태로 수득하였다. 융점: 177-178℃.
23.2) 1-(9-브로모노닐)-5,5-디메틸-3-(3-메틸-4-니트로페닐)이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 중간체 12.1의 합성에 대해 기재된 것과 동일하지만, 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온을 중간체 23.1로 교체하였다. 목적 화합물을 74%의 수율로 황색 오일의 형태로 수득하였다.
23.3) 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 중간체 4.2의 합성에 대해 기재된 것과 동일하지만, 중간체 4.1을 중간체 23.2로 교체하였다. 목적 화합물을 90%의 수율로 황색 오일의 형태로 수득하였다.
실시예 24 : 5,5-디메틸-3-(3-메틸-4-니트로페닐)-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 23의 화합물로 교체하였다. 무색 오일을 50%의 수율로 수득하였다.
실시예 25 : 3-(4-아미노-3-메틸페닐)-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
실험 프로토콜은 실시예 16의 화합물에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 23의 화합물로 교체하였다. 목적 화합물을 93%의 수율로 갈색 오일의 형태로 수득하였다.
실시예 26 : 3-(4-아미노-3-메틸페닐)-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 25의 화합물로 교체하였다. 무색 오일을 56%의 수율로 수득하였다.
실시예 27 : 1-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]-3-(1-메틸프로필)우레아
실시예 25의 화합물 (395 mg, 0.72 mmol)을 아르곤 분위기하에 무수 1,2-디클로로에탄 (10 ml)에 용해시킨 후, 23℃에서 sec-부틸이소시아네이트 (0.35 ml, 3 mmol)를 적가하였다. 이어서, 혼합물을 환류 하에 24 시간 동안 가열하였다. 이어서, 반응 매질을 냉수에 붓고, CH2Cl2로 추출하였다. 경사분리한 후, 유기상을 물 및 소금물로 세척하였다. 이어서, 유기 용액을 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축에 의해 건조시키고, 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 1/0 -> 4/6). 목적 화합물을 36%의 수율로 무색 오일의 형태로 수득하였다.
실시예 28 : 1-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]-3-(1-메틸프로필)우레아
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 25의 화합물로 교체하였다. 무색 오일을 63%의 수율로 수득하였다.
실시예 29 : tert-부틸 {[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파모일}카르바메이트
무수 CH2Cl2 (30 ml) 중 실시예 25의 화합물 (612 mg, 1.1 mmol) 및 Et3N (0.19 ml, 1.33 mmol)의 용액을 0℃에서 교반하였다. 이어서, 0℃로 냉각된 무수 CH2Cl2 (10 ml) 중 클로로술포닐 이소시아네이트 (0.11 ml, 1.22 mmol)의 용액을 t-BuOH (0.12 ml, 1.22 mmol)로 마무리한 후, 실시예 25의 화합물의 용액을 신속히 첨가하였다. 혼합물을 0℃에서 30 분 동안 교반한 후, 23℃에서 1 시간 반 동안 교반하였다. 이어서, 반응 매질을 물 (2 x 100 ml), NaHCO3의 포화 수용액 (50 ml) 및 소금물 (50 ml)로 연속 세척하였다. 유기 용액을 Na2SO4 상에서 건조시키고, 여과하고, 농축에 의해 건조시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 1/0 -> 6/4). 목적 화합물을 85%의 수율로 백색 고체의 형태로 수득하였다. 융점 122-124℃.
실시예 30 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
에틸 에테르 중 HCl의 용액 (2N, 3 ml)을 0℃로 냉각된 CH2Cl2/AcOEt 혼합물 (5 ml/3 ml) 중 실시예 29 (250 mg, 0.36 mmol)의 용액에 1-ml 분량으로 3회 첨가하고, 혼합물을 23℃에서 60 시간 동안 교반하였다. 휘발성 물질을 진공하에 증발시키고, 잔류물을 CH2Cl2 (50 ml) 및 NaHCO3 (50 ml) 혼합물에 녹였다. 교반하고 경사분리한 후, 유기상을 물 (50 ml)에 이어 소금물로 세척하였다. Na2SO4 상에서 건조시키고, 여과하고, 농축에 의해 건조시킨 후, 잔류물을 실리카 칼럼 상에서 정제하였다 (헵탄/AcOEt: 10/0 -> 1/1). 목적 생성물을 76%의 수율로 백색 고체의 형태로 수득하였다. 융점: 102-104℃.
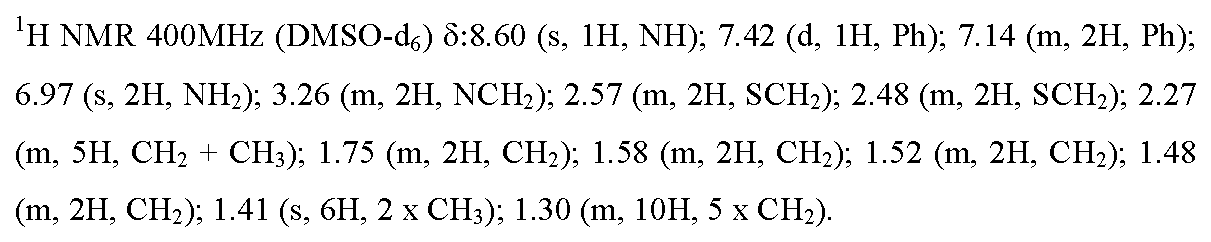
실시예 31 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 화합물을 실시예 30의 화합물로 교체하였다. 백색 고체를 62%의 수율로 수득하였다.
실시예 32 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술포닐]노닐}이미다졸리딘-1-일)-2-메틸페닐]술파미드
이용된 실험 프로토콜은 실시예 3의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 2의 화합물을 실시예 31의 화합물로 교체하였다. 무색 오일을 수득하였다.
실시예 33 : 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 3의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 2의 화합물을 실시예 16의 화합물로 교체하였다.
실시예 34 : 7-[4-니트로-3-(트리플루오로메틸)페닐]-5-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}-5,7-디아자스피로[3.4]옥탄-6,8-디온
34.1) 5,7-디아자스피로[3.4]옥탄-6,8-디온
시안화나트륨 (1.47 g, 30 mmol)에 이어, 탄산암모늄 (7.5 g, 78 mmol)을 아르곤 하에 23℃에서 에탄올-물 용매 혼합물 (16 ml)에 용해된 시클로부타논 (1.49 ml, 20 mmol)의 용액에 첨가하였다. 반응 혼합물을 6 시간 동안 70℃에서 가열하였다. 반응 매질을 냉각시킨 후, 물 (15 ml)을 부은 다음, 진한 염산 용액 (13 ml)을 주의해서 첨가하였다. 23℃에서 10 시간 동안 교반한 후, 반응 혼합물의 에탄올 및 일부 물 함량을 회전식 증발기에 의해 증발시켰다. 침전물을 프릿 상에서 여과시킨 다음, 물로 세척하였다. 목적 화합물을 39% (1.1 g)의 수율로 베이지색 분말의 형태로 수득하였다.
융점: 223-225℃
34.2) 7-[4-니트로-3-(트리플루오로메틸)페닐]-5,7-디아자스피로[3.4]옥탄-6,8-디온
탄산칼륨 (1.09 g, 7.85 mmol) 및 화합물 5-플루오로-2-니트로-3-(트리플루오로메틸)페닐]-이미다졸리딘-2,4-디온 (500 mg, 1.6 mmol)을 아르곤 하에 DMF (6 ml) 중 5,7-디아자스피로[3.4]옥탄-6,8-디온 (상기에서 제조됨) (221 mg, 0.74 mmol)의 용액에 첨가하였다. 반응 혼합물을 65℃에서 2 시간 동안 가열한 다음, 23℃에서 12 시간 동안 교반을 유지하였다. 반응 매질을 NH4Cl의 포화 수용액 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 7/3 -> 3/7). 이소펜탄으로 세척한 다음, 여과한 후, 목적 화합물을 50% (645 mg)의 수율로 연황색 분말의 형태로 수득하였다.
34.3) 7-[4-니트로-3-(트리플루오로메틸)페닐]-5-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}-5,7-디아자스피로[3.4]옥탄-6,8-디온
NaH (60%까지) (44 mg, 1.1 mmol)를 아르곤 하에 무수 DMF (9 ml) 중 7-[4-니트로-3-(트리플루오로메틸)페닐]-5,7-디아자스피로[3.4]옥탄-6,8-디온 (329 mg, 1 mmol)의 용액에 첨가하였다. 기체 방출에 의해 반응 매질의 색이 오렌지색으로 변하였다. 23℃에서 1 시간 동안 교반을 유지한 후, 9-[(4,4,5,5,5-펜타플루오로펜틸)-티오]노닐 메탄술포네이트 (WO 2005077968에 기재된 실험 프로토콜에 따라 제조됨) (332 mg, 0.8 mmol)를 첨가하였다. 15 시간 동안 반응시킨 후, 반응 매질을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 RP18 실리카 칼럼 상에서 정제하였다 (용리액: ACN/H2O: 8/2 -> 100). 목적 화합물을 33% (214 mg)의 수율로 무색 오일의 형태로 수득하였다.
34.4) 7-[4-니트로-3-(트리플루오로메틸)페닐]-5-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}-5,7-디아자스피로[3.4]옥탄-6,8-디온
하기 기재된 화합물 34.4는 실시예 2에 기재된 것과 유사한 방법에 따라 합성하였지만, 실시예 1의 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온을 중간체 34.3으로 교체하였다. 목적 화합물을 79% (170 mg)의 수율로 연황색 오일의 형태로 수득하였다.
실시예 35 : 5,5-디메틸-3-[4-니트로-2-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
35.1) 5,5-디메틸-3-[4-니트로-2-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 19.1의 화합물의 합성에 대해 기재된 것과 동일하지만, 4-플루오로-2-(트리플루오로메틸)벤조니트릴을 1-플루오로-4-니트로-2-(트리플루오로메틸)벤젠으로 교체하였다. 목적 화합물을 77%의 수율로 백색 분말의 형태로 수득하였다.
융점: 201-203℃
35.2) 5,5-디메틸-3-[4-니트로-2-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 1의 합성에 대해 기재된 것과 동일하지만, 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온을 중간체 35.1로 교체하였다. 목적 화합물을 50%의 수율로 무색 오일의 형태로 수득하였다.
35.3) 5,5-디메틸-3-[4-니트로-2-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 2의 화합물의 합성에 대해 기재된 것과 동일하지만, 실시예 1의 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온을 중간체 35.2로 교체하였다. 목적 화합물을 85%의 수율로 무색 오일의 형태로 수득하였다.
실시예 36 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-2,4-디온
36.1) 1-{2-[2-(2-요오도에톡시)에톡시]에틸}-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 중간체 4.1의 합성에 대해 기재된 것과 동일하지만, 1,5-디요오도펜탄을 1,2비스-(2-요오도에톡시)에탄으로 교체하였다. 목적 화합물을59% (666 mg)의 수율로 연황색 오일의 형태로 수득하였다.
36.2) 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-2,4-디온
이용된 실험 프로토콜은 실시예 4의 합성에 대해 기재된 것과 동일하지만, 1-(5-요오도펜틸)-5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]이미다졸리딘-2,4-디온을 중간체 36.1로 교체하였다. 목적 화합물을 73%의 수율로 무색 오일의 형태로 수득하였다.
실시예 37 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]에톡시}에톡시)에틸]이미다졸리딘-2,4-디온
하기 기재된 화합물 37은 출발 시약으로서 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온 대신에 화합물 36을 사용하여 실시예 2에 기재된 것과 유사한 방법에 따라 합성하였다. 목적 화합물을 88%의 수율로 연황색 오일의 형태로 수득하였다.
실시예 38 : N-[4-{4,4-디메틸-2,5-디옥소-3-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-1-일}-2-(트리플루오로메틸)페닐]아세트아미드
38.1) 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-2,4-디온
하기 기재된 화합물 38은 출발 시약으로서 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온 대신에 화합물 36을 사용하여 실시예 16에 기재된 것과 유사한 방법에 따라 합성하였다. 목적 화합물을 88%의 수율로 연황색 오일의 형태로 수득하였다.
38.2) N-[4-{4,4-디메틸-2,5-디옥소-3-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]에톡시}에톡시)에틸]이미다졸리딘-1-일}-2-(트리플루오로메틸)페닐]아세트아미드
하기 기재된 화합물 38은 출발 시약으로서 3-[4-아미노-3-(트리플루오로메틸)페닐]-5,5-디메틸-1-{9-[(4,4,5,5,5-펜타플루오로펜틸)티오]노닐}이미다졸리딘-2,4-디온 대신에 화합물 38.1을 사용하여 실시예 17에 기재된 것과 유사한 방법에 따라 합성하였다. 목적 화합물을 88%의 수율로 연황색 오일의 형태로 수득하였다.
실시예 39 : N-[4-{4,4-디메틸-2,5-디옥소-3-[2-(2-{2-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]에톡시}에톡시)에틸]이미다졸리딘-1-일}-2-(트리플루오로메틸)페닐]아세트아미드
하기 기재된 화합물 39는 출발 시약으로서 실시예 1의 화합물 대신에 실시예 38의 화합물을 사용하여 실시예 2에 기재된 것과 유사한 방법에 따라 합성하였다. 목적 화합물을 75%의 수율로 연황색 오일의 형태로 수득하였다.
실시예 40 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N-메틸아세트아미드
NaH (60%까지) (6 mg, 0.16 mmol)를 아르곤 하에 무수 DMF (2 ml) 중 N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]-노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]아세트아미드 (100 mg, 0.15 mmol) (실시예 18에 따라 제조됨)의 용액에 첨가하였다. 기체 방출에 의해 반응 매질의 색이 변하였다. 23℃에서 1 시간 동안 교반을 유지한 후, 메틸 요오다이드 (10 ㎕, 0.16 mmol)를 첨가하였다. 1 시간 동안 반응시킨 후, 상기 기재된 바와 같이 동일한 양의 수소화나트륨 및 메틸 요오다이드를 첨가한 다음, 반응 혼합물을 다시 23℃에서 3 시간 동안 교반하였다. 반응 매질을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: CH2Cl2/MeOH: 95/5 -> 90/10). 목적 화합물을 72% (72 mg)의 수율로 무색 오일의 형태로 수득하였다.
실시예 41 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]메탄술폰아미드
41.1) N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N-(메틸술포닐)메탄술폰아미드
술포닐 클로라이드 (193 ㎕, 10 eq)를 23℃에서 무수 CH2Cl2 (5 ml) 중 실시예 16 (151 mg, 0.25 mmol)의 용액에 적가하였다. 23℃에서 15 시간 동안 교반을 유지한 다음, 술포닐 클로라이드 (0.58 ml, 30 eq) 및 디이소프로필에틸아민 (1.75 ml, 40 eq)을 첨가하였다. 23℃에서 3 시간 동안 교반을 유지한 다음, 반응 혼합물을 진공 하에 농축에 의해 건조시켰다. 증발 잔류물을 테트라히드로푸란/메탄올/물 1/1/1 (3 ml)의 용매 혼합물로 희석하고, 수산화리튬 (25 mg, 1 mmol)을 첨가하였다. 23℃에서 15 시간 동안 교반을 유지한 다음, 테트라히드로푸란/메탄올/물 2/2/2 (6 ml)의 용매 혼합물 중 수산화리튬 (50 mg, 2 mmol)을 첨가하였다. 23℃에서 2 시간 후, 반응 매질을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 7/3 -> 5/5). 순수한 분획을 수집하고 농축시킨 후, 목적 화합물을 무색 오일의 형태로 수득하였고, 이를 47% (81 mg)의 수율로 천천히 결정화시켰다.
41.2) N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]메탄술폰아미드
하기 기재된 화합물 41은 출발 시약으로서 실시예 1의 화합물 대신에 실시예 41.1의 화합물을 사용하여 실시예 2에 기재된 것과 유사한 방법에 따라 합성하였다. 목적 화합물을 71%의 수율로 연황색 오일의 형태로 수득하였다.
실시예 42 : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술파닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드
하기 기재된 화합물 41은 출발 시약으로서 아세틸 클로라이드 대신에 히드로클로라이드 형태의 디메틸 아미노 아세틸 클로라이드를 사용하여 실시예 17에 기재된 것과 유사한 방법에 따라 합성하였다 . 목적 화합물을 83%의 수율로 연황색 오일의 형태로 수득하였다.
실시예 43a : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드
하기 기재된 화합물 43a는 출발 시약으로서 실시예 1의 화합물 대신에 실시예 42의 화합물을 사용하여 실시예 2에 기재된 것과 유사한 방법에 따라 합성하였다. 목적 화합물을 65%의 수율로 연황색 오일의 형태로 수득하였다.
실시예 43b : N-[4-(4,4-디메틸-2,5-디옥소-3-{9-[(4,4,5,5,5-펜타플루오로펜틸)술피닐]노닐}이미다졸리딘-1-일)-2-(트리플루오로메틸)페닐]-N2,N2-디메틸글리신아미드 히드로클로라이드
2N 에테르 중 염산의 용액 (904 ㎕, 2 eq)을 23℃에서 무수 에테르 (35 ml) 중 실시예 43a (639 mg, 0.904 mmol)의 용액에 적가하였다. 23℃에서 15 시간 동안 교반을 유지한 다음, 에테르 (2 x 20 ml)로 2회에 이어 이소펜탄 (2 x 20 ml)으로 2회 녹인 반응 혼합물을 진공 하에 농축에 의해 건조시켰다. 증발 잔류물을 55℃에서 진공하에 건조시켰다. 목적 화합물을 93% (624 mg)의 수율로 베이지색 분말의 형태로 수득하였다.
실시예 44 : N-[(1Z)-(9-{5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-2,4-디옥소이미다졸리딘-1-일}노닐)(4,4,5,5,5-펜타플루오로펜틸)-λ4-술파닐리덴]-2,2,2-트리플루오로아세트아미드
2,2,2-트리플루오로아세트아미드 (106 mg, 0.94 mmol), 산화마그네슘 (76 mg, 4 eq), 이량체 형태의 로듐 아세테이트 (5.2 mg, 0.025 eq) 및 요오도벤젠 디아세테이트 (228 mg, 1.5 eq)를 23℃에서 무수 CH2Cl2 (5 ml) 중 실시예 1 (300 mg, 0.48 mmol)의 용액에 첨가하였다. 23℃에서 6 시간 동안 교반을 유지한 다음, 반응 혼합물을 진공 하에 여과하였다. 여과물을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 5/5 -> 3/7). 순수한 분획을 수집하고 농축시킨 후, 목적 화합물을 34% (77 mg)의 수율로 무색 오일의 형태로 수득하였다.
실시예 45 : N-[(9-{5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-2,4-디옥소이미다졸리딘-1-일}노닐)(옥시도)(4,4,5,5,5-펜타플루오로펜틸)-λ4-술파닐리덴]-2,2,2-트리플루오로아세트아미드
2,2,2-트리플루오로아세트아미드 (38 mg, 0.33 mmol), 산화마그네슘 (27 mg, 4 eq), 이량체 형태의 로듐 아세테이트 (1.8 mg, 0.025 eq) 및 요오도벤젠 디아세테이트 (81 mg, 1.5 eq)를 23℃에서 무수 CH2Cl2 (5 ml) 중 실시예 2 (109 mg, 0.17 mmol)의 용액에 첨가하였다. 23℃에서 6 시간 동안 교반을 유지한 다음, 반응 혼합물을 진공 하에 여과하였다. 여과물을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 유기상을 합하고, 물 (25 ml) 및 소금물 (25 ml)로 연속 세척하였다. Na2SO4 상에서 건조시킨 후, 유기 용액을 여과하고, 진공하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액: 헵탄/AcOEt: 5/5 -> 2/8). 순수한 분획을 수집하고 농축시킨 후, 목적 화합물을 88% (114 mg)의 수율로 무색 오일의 형태로 수득하였다.
실시예 46 : 5,5-디메틸-3-[4-니트로-3-(트리플루오로메틸)페닐]-1-{9-[S-(4,4,5,5,5-펜타플루오로펜틸)술폰이미도일]노닐}이미다졸리딘-2,4-디온
탄산칼륨 (35 mg, 0.25 mmol)을 23℃에서 무수 MeOH (0.5 ml) 중 실시예 45 (38 mg, 0.05 mmol)의 용액에 첨가하였다. 23℃에서 15 시간 동안 교반을 유지한 다음, 반응 혼합물을 진공 하에 여과하였다. 여과물을 물 (25 ml)에 붓고, AcOEt (2 x 25 ml)로 추출하였다. 여과물을 진공 하에 농축시켰다. 증발 잔류물을 실리카 칼럼 상에서 정제하였다 (용리액 2 x 10 ml의 AcOEt/CH2Cl2: 5/5에 이어, 10 ml의 AcOEt/헵탄 7.5/2.5). 순수한 분획을 수집하고 농축시킨 후, 목적 화합물을 67% (22 mg)의 수율로 무색 오일의 형태로 수득하였다.
본 발명에 따른 화합물의 약리학적 연구
항증식 활성의 측정:
1. 완전 배지에서 LNCaP에 대한 항증식 활성
본 발명의 화합물의 항증식 활성을 하기 실험 절차를 적용하여 완전 배지에서 LNCaP에 대해 측정하였다:
LNCaP 세포 유형 (ATCC, 1740)은 안드로겐 수용체를 발현하는 전립선 암종으로부터 유래되며, 상기 세포주는 호르몬-의존성이다.
LNCaP 세포주의 유지는 완전 배양 배지에서 수행하였다: RPMI, 10%의 소 태아 혈청, 2 mM 글루타민, 100 U/ml 페니실린, 0.1 mg/ml의 스트렙토마이신 및 0.01M HEPES, 1 mM 나트륨 피루베이트, 40%의 D-글루코스.
ㆍ 플레이트 시딩:
LNCaP 세포주를 폴리-D-리신 (바이오코트(Biocoat), 코스타(Costar))으로 코팅된 96-웰 플레이트 중의 90 ㎕의 완전 배지에 20,000 세포/웰로 시딩하였다.
ㆍ 세포의 처리: 시딩 24 시간 후, 세포를 배양 배지에 희석된 10 ㎕/웰의 화합물로 처리하였다. 화합물의 용량 효과의 실험은 1 nM 내지 100 μM의 규모로 수행하였다. 이용된 농도는 1 nM/10/30/100/300/1000/3000/10,000/100,000 nM이었다. 테스토스테론 (시그마(SIGMA) T1500)은 참고로 사용되어 동일한 농도에서 시험하였다. 세포를 37℃, 5% CO2에서 144 시간 동안 인큐베이션하였다.
ㆍ 판독: 제6일에, 10 ㎕의 "WST-1 세포 증식" 시약 (로슈(Roche) 참고번호 1644807)을 각 웰에 첨가하였다. 37℃, 5% CO2에서 2 시간 동안 인큐베이션한 후, 450 nm에서의 흡광도를 분광광도측정법 (엔비젼(Envision), 퍼킨 엘머(Perkin Elmer))에 의해 측정하였다.
ㆍ 결과: 실험은 2벌식으로 수행하였고, 최상의 화합물을 2회 시험하였다. 증식하는 세포를 50% 억제하는 농도 값 (IC50)을 계산하였다.
하기 실시예의 화합물은 배양물 중 LNCaP 세포에 대해 2000 nM 미만의 IC50을 갖는다: 1, 2, 3, 4, 5, 7, 9, 11, 12, 13, 15, 17, 18, 20, 22, 24, 28, 30, 31, 32, 34, 35, 36, 37, 38, 40, 41, 42, 43, 44, 45 및 46.
이들 중에서, 하기 실시예의 화합물은 배양물 중 LNCaP 세포에 대해 1000 nM 미만의 IC50을 갖는다: 2, 3, 9, 12, 13, 15, 17, 18, 20, 22, 24, 32, 34, 35, 36, 38, 41, 43, 44, 45 및 46.
하기 실시예의 화합물은 배양물 중 LNCaP 세포에 대해 500 nM 미만의 IC50을 갖는다: 2, 9, 12, 13, 18, 35, 36, 38, 43, 44 및 45.
2. 스테로이드 비함유 배지에서 LNCaP에 대한 항증식 활성:
본 발명의 화합물의 항증식 활성을 스테로이드 비함유 배지에서 LNCaP에 대해 측정하였다.
LNCaP 세포주의 유지는 RPMI, 10%의 소 태아 혈청, 2 mM의 글루타민, 100 U/mL의 페니실린, 0.1 mg/ml의 스트렙토마이신 및 0.01M HEPES, 1 mM 나트륨 피루베이트, 40%의 D-글루코스 중에서 통상적인 조건 하에 수행하였다.
스테로이드 비함유 조건 하에서의 연구의 경우, 시딩하기 24 시간 전에 세포의 배양 배지를 제거하였다. 세포를 PBS로 세척한 다음, 페놀 레드 비함유 RPMI 배지, 스테로이드 비함유 10% 소 태아 혈청 (탄소로 처리), 2 mM의 글루타민, 100 U/ml의 페니실린, 0.1 mg/ml의 스트렙토마이신 및 0.01M HEPES, 1 mM의 나트륨 피루베이트, 40%의 D-글루코스의 존재 하에 인큐베이션하였다.
ㆍ 플레이트 시딩:
LNCaP 세포주를 폴리-D-리신 (바이오코트, 코스타)으로 코팅된 96-웰 플레이트 중의 스테로이드 비함유 10% 소 태아 혈청을 갖는 90 ㎕의 RPMI 배지에 20,000 세포/웰로 시딩하였다.
ㆍ 세포의 처리: 시딩 24 시간 후, 세포를 배양 배지에 희석된 10 ㎕/웰의 화합물로 처리하였다. 화합물의 용량 효과를 보여주는 실험은 1 nM 내지 100 μM의 규모로 수행하였다. 이용된 농도는 1 nM/10/30/100/300/1000/3000/10,000/100,000 nM이었다. 테스토스테론 (시그마 T1500)은 참고로 사용되어 동일한 농도에서 시험하였다. 세포를 37℃, 5% CO2에서 144 시간 동안 인큐베이션하였다.
ㆍ 판독: 제6일에, 10 ㎕의 세포 증식 시약 WST-1 (로슈 참고번호 1644807)을 각 웰에 첨가하였다. 37℃, 5% CO2에서 2 내지 4 시간 동안 인큐베이션한 후, 450 nm에서의 흡광도를 분광광도측정법 (엔비젼, 퍼킨 엘머)에 의해 측정하였다.
ㆍ 결과: 실험은 2벌식으로 수행하였고, 최상의 화합물을 2회 시험하였다. 증식하는 세포를 50% 억제하는 농도 값 (IC50)을 계산하였다.
실시예 1 내지 46의 생성물은 스테로이드 비함유 배지에서 LNCaP에 대해 효능제 효과를 나타내지 않는다.
도 1은 스테로이드 비함유 배지에서 배양된 LNCaP의 세포 증식에 대한 실시예 18 및 43a의 화합물의 효과를 도시한다.
화합물 18 및 43a는 놀랍게도 효능제 효과 없이 LNCaP 세포에 대해 항증식 활성을 보여준다. 정반대로, 닐루타미드는 저농도에서의 효능제 활성 이후 고농도에서의 억제 활성을 갖는 2상 프로파일을 갖는다.
3. 완전 배지에서 DU-145에 대한 항증식 활성:
본 발명의 화합물의 항증식 활성을 완전 배지에서 DU-145에 대해 측정하였다.
DU-145 세포주의 유지는 DMEM, 10%의 소 태아 혈청, 2 mM의 글루타민, 100 U/ml의 페니실린, 0.1 mg/ml의 스트렙토마이신 중에서 수행하였다.
ㆍ 플레이트 시딩:
DU145 세포주를 96-웰 플레이트 (TPP) 중의 90 ㎕의 DMEM 완전 배지에 400 또는 800 세포/웰로 시딩하였다.
ㆍ 세포의 처리: 시딩 24 시간 후, 세포를 배양 배지에 희석된 10 ㎕/웰의 화합물로 처리하였다. 화합물의 용량 효과를 보여주는 실험은 1 nM 내지 100 μM의 규모로 수행하였다. 이용된 농도는 1 nM/10/30/100/300/1000/3000/10,000/100,000 nM이었다. 세포를 37℃, 5% CO2에서 144 시간 동안 인큐베이션하였다.
ㆍ 판독: 제6일에, 10 ㎕의 세포 증식 시약 WST-1 (로슈 참고번호 1644807)을 각 웰에 첨가하였다. 37℃, 5% CO2에서 2 내지 4 시간 동안 인큐베이션한 후, 450 nm에서의 흡광도를 분광광도측정법 (엔비젼, 퍼킨 엘머)에 의해 측정하였다.
ㆍ 결과: 실험은 2벌식으로 수행하였고, 최상의 화합물을 2회 시험하였다. 세포 증식을 50% 억제하는 농도 값 (IC50)을 계산하였다.
ㆍ 하기 실시예의 화합물은 배양물 중의 DU145 세포에 대해 10,000 nM 초과의 IC50을 갖는다: 1, 2, 3, 4, 5, 7, 8, 9, 11, 14, 15, 16, 17, 18, 20, 22, 24, 26, 28, 30, 31, 32, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44 및 45.
4. 안드로겐 수용체의 소멸의 측정
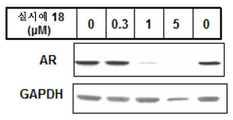
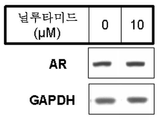
화합물이 안드로겐 수용체의 단백질 발현의 수준을 감소시킨다는 것을 보여줄 것이다.
LNCaP 세포주의 세포를 RPMI, 10%의 소 태아 혈청, 2 mM의 글루타민, 100 U/mL의 페니실린, 0.1 mg/mL의 스트렙토마이신 및 0.01M HEPES, 1 mM의 나트륨 피루베이트, 40%의 D-글루코스 중에서 10 cm의 페트리 디쉬 당 250만개 세포의 비율로 시딩하였다. 4 일 후, 세포를 시험할 화합물로 처리하였다. 처리 72 시간 후, 세포를 용해 완충제 (50 mM 트리스 pH 7.4, 150 mM NaCl, 1 mM EDTA, 20 mM NaF, 100 mM Na2VO3, 0.5%의 NP40, 1%의 트리톤 X-100, 1 mM EGTA, 페파블록(Pefabloc), 프로테아제 억제제 칵테일 11836170001 로슈다이아그노스틱스(RocheDiagnostics), 포스파타제 억제제 칵테일 세트 II 칼바이오켐(Calbiochem)) 중에 용해시켰다. 이어서, 세포를 스크랩하고, 용해물을 4℃에서 15 분 동안 13,000 rpm에서의 원심분리를 위해 퀴아슈레더(QIAshredder) 튜브 (카탈로그 번호 79656 퀴아젠(Qiagen))로 옮겼다. DNA 필라멘트를 완전히 제거하기 위해, 상청액을 5 분 동안 13,000 rpm에서의 제2 원심분리를 위해 퀴아슈레더로 옮겼다. -80℃에서 동결시킨 후, 단백질 농도를 측정하고 (바이오-라드(Bio-Rad) DC 단백질 검정 키트), 웰당 10 내지 20 ㎍으로 조정하였다. 1% 베타-메르캅토에탄올 및 50 mM DTT가 첨가된 로딩 완충제 (샘플 로딩 완충제 3X 참고번호 7722 셀 시그널링 테크놀로지(Cell signaling technology))를 샘플에 첨가한 다음, 90℃에서 10 분 동안 가열하였다. 샘플을 NuPAGE 4-12% 비스-트리스 겔 (카탈로그 번호 NP0322BOX, 인비트로젠(Invitrogen)) 상에서 20 ㎕의 부피 하에 침착시켰다. 이동을 MOPS 완충제 (인비트로젠) 중에서 실시하고, 180V에서 1 시간 동안 수행하였다. 단백질을 반건조 조건 하에 전달 완충제 (NP0006-1, 인비트로젠)의 존재 하에 15V에서 45 분에 걸쳐 니트로셀룰로스 막 (하이본드(Hybond) ECL RPN78D, 지이 헬쓰케어(GE Healthcare))으로 옮겼다. 이어서, 막을 TBS 0.1% 트윈 20 중 5%로 차단 완충제 (비-지방 건조 우유, 카탈로그 170-6404, 바이오라드) 중에서 1 시간 동안 차단시켰다. 이어서, 이를 차단 완충제 중에서 1/2000로 희석된 안드로겐 수용체 (AR441, sc-7305, 산타 크루즈(Santa Cruz))에 대해 지정된 일차 항체의 존재 하에서 뿐만 아니라, 차단 완충제 중에서 1/20,000로 희석된 GAPDH (카탈로그 MAB374, 밀리포어(Millipore))에 대해 지정된 일차 항체의 존재 하에서 4℃에서 밤새 인큐베이션하였다 (단백질 로드의 모니터링). 이어서, 막을 세척 완충제 (TBS, 0.1% 트윈 20) 중에서 3회 세척하였다. 이어서, 막을 차단 완충제 중에서 1/5000로 희석된 HRP (염소 항-마우스 IgG-HRP, sc 2031, 산타 크루즈)와 커플링된 이차 항-이뮤노글로불린 마우스 항체의 존재 하에 인큐베이션하였다.
이어서, 막을 세척 완충제 중에서 3회 세척하였다. 단백질을 사진용 필름 (바이오맥스(Biomax) 광, 시그마)의 이용에 의해 또는 화학발광 획득 시스템 (지:박스(G:Box), 신젠(Syngene))에 의해 검출되는 전자화학발광 (웨스턴 블롯팅 검출 시스템 ECL+, 아머샴(Amersham))에 의해 밝혔다. 도 2 및 3은 수용체의 발현에 대해 화합물 18 및 43a의 효과를 나타낸다. 도 4는 안드로겐 수용체의 발현에 대한 닐루타미드의 효과의 부재를 나타낸다.