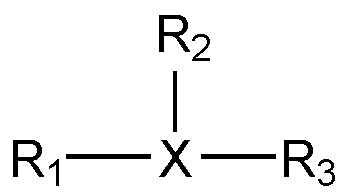KR101247442B1 - 분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법 - Google Patents
분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법 Download PDFInfo
- Publication number
- KR101247442B1 KR101247442B1 KR1020090123256A KR20090123256A KR101247442B1 KR 101247442 B1 KR101247442 B1 KR 101247442B1 KR 1020090123256 A KR1020090123256 A KR 1020090123256A KR 20090123256 A KR20090123256 A KR 20090123256A KR 101247442 B1 KR101247442 B1 KR 101247442B1
- Authority
- KR
- South Korea
- Prior art keywords
- polylactic acid
- branched polylactic
- oligomer
- lactic acid
- polycaprolactone copolymer
- Prior art date
Links
- 0 CC(*)**(*)(***)N*** Chemical compound CC(*)**(*)(***)N*** 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/02—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds
- C08G63/06—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds derived from hydroxycarboxylic acids
- C08G63/08—Lactones or lactides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/78—Preparation processes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2650/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G2650/28—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule characterised by the polymer type
- C08G2650/30—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule characterised by the polymer type branched
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L2201/00—Properties
- C08L2201/06—Biodegradable
Abstract
분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법이 제공된다.
상기 분지상 폴리락트산-폴리카프로락톤 공중합체는 분지상 폴리락트산과 카프로락톤 올리고머의 반응 생성물이다. 상기 분지상 폴리락트산은 락트산 올리고머와 분지제의 반응 생성물일 수 있다. 상기 분지제는 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 3개 이상 포함할 수 있다.
상기 제조 방법은 락트산 올리고머에 분지제를 첨가하여 축합중합 반응시켜 분지상 폴리락트산을 형성하는 단계, 및 상기 분지상 폴리락트산에 카프로락톤 올리고머를 첨가하여 축합중합 반응시키는 단계를 포함한다.
락트산, 락트산 올리고머, 카프로락톤 올리고머, 축합중합, 분지제
Description
본 발명은 폴리락트산-폴리카프로락톤 공중합체에 관한 것으로, 더욱 상세하게는 분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법에 관한 것이다.
지구온난화의 주요 원인인 이산화탄소의 배출을 감소시키고, 한정된 자원과 고가의 석유 원료를 대체하기 위한 환경 친화적 바이오매스(biomass)에 관한 연구가 활발하게 진행되고 있다. 예를 들어, 옥수수 전분을 발효하여 얻을 수 있는 폴리락트산계 수지는 저렴한 가격, 공급용이성 등의 이유로 범용수지 대체를 위한 친환경소재의 주원료로서 주목 받고 있으며 동식물 또는 인체에 무해하여 의료용 재료로서 수술용 봉합사나 약물의 서방성 중합체로도 많이 이용되고 있다.
그러나, 폴리락트산은 유사계열의 폴리에스테르계 생분해성 고분자들에 비해 우수한 인장강도를 갖는 반면, 충격 강도가 취약한 단점이 있다.
상기와 같은 문제점을 해결하기 위하여, 본 발명은 충격 강도가 향상된 분지상 폴리락트산-폴리카프로락톤 공중합체를 제공한다.
본 발명은 상기 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법을 제공한다.
본 발명에 따른 분지상 폴리락트산-폴리카프로락톤 공중합체는 분지상 폴리락트산과 카프로락톤 올리고머의 반응 생성물이다.
상기 분지상 폴리락트산은 락트산 올리고머와 분지제의 반응 생성물일 수 있다.
상기 분지제는 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 3개 이상 포함할 수 있다.
상기 분지제의 함량은 상기 락트산 올리고머 100중량부에 대하여 0.01 내지 2중량부일 수 있다.
상기 락트산 올리고머의 분자량은 3,000 내지 50,000일 수 있다.
상기 분지상 폴리락트산의 분자량은 10,000 내지 250,000일 수 있다.
상기 카프로락톤 올리고머의 분자량은 200 내지 10,000일 수 있다. 상기 카프로락톤 올리고머의 함량은 상기 락트산 올리고머 100중량부에 대하여 1 내지 20중량부일 수 있다.
상기 분지상 폴리락트산-폴리카프로락톤 공중합체의 분자량은 20,000 내지 300,000일 수 있다.
본 발명에 따른 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법은 락트산 올리고머에 분지제를 첨가하여 축합중합 반응시켜 분지상 폴리락트산을 형성하는 단계; 및 상기 분지상 폴리락트산에 카프로락톤 올리고머를 첨가하여 축합중합 반응시키는 단계를 포함한다.
상기 락트산 올리고머는 100 내지 180℃의 불활성 기체 분위기 하에서 락트산을 탈수 반응시킴으로써 형성될 수 있고, 3,000 내지 50,000의 분자량을 가질 수 있다.
상기 탈수 반응 및 상기 축합중합 반응에서 사용되는 촉매는, 산화아연, 산화안티몬, 염화안티몬, 산화납, 산화칼슘, 산화알루미늄, 산화철, 염화칼슘, 초산아연, 파라톨루엔 슬폰산, 염화제1주석, 황산제1주석, 산화제1주석, 산화제2주석, 옥탄산제1주석, 테트라페닐주석, 주석분말 및 사염화티탄 중 적어도 어느 하나를 포함할 수 있다.
상기 촉매의 함량은 상기 락트산 또는 상기 락트산 올리고머 100중량부에 대하여 0.0005 내지 5중량부일 수 있다.
상기 분지제는 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 3개 이상 포함할 수 있다. 상기 분지제는 상기 락트산 올리고머 100중량부에 대하여 0.01 내지 2중량부로 첨가될 수 있다.
상기 분지상 폴리락트산의 분자량은 10,000 내지 250,000일 수 있다.
상기 카프로락톤 올리고머의 분자량은 200 내지 10,000일 수 있다.
상기 분지상 폴리락트산-폴리카프로락톤 공중합체의 분자량은 20,000 내지 300,000일 수 있다.
본 발명에 따르면, 상기 분지상 폴리락트산-폴리카프로락톤 공중합체는 향상된 유연성으로 인해 향상된 충격 강도를 가질 수 있고, 저비용으로 짧은 시간에 높은 분자량을 가질 수 있도록 제조될 수 있다.
또, 상기 분지상 폴리락트산-폴리카프로락톤 공중합체는 주쇄에 가지가 도입되어 연신 과정에서 용융 강도가 향상될 수 있다. 이에 의해, 상기 분지상 폴리락트산-폴리카프로락톤 공중합체는 종래의 선형 폴리락트산계 수지보다 향상된 가공성을 가질 수 있어, 섬유 방사나 필름, 블로우 성형, 발포 가공 등 다양한 가공에 이용될 수 있다.
또, 상기 분지상 폴리락트산-폴리카프로락톤 공중합체는 다양한 형태의 친환경 소재에 적용될 수 있다.
이하, 실시예들을 통하여 본 발명을 보다 상세하게 설명한다. 본 발명의 목적, 특징, 장점은 이하의 실시예들을 통해 쉽게 이해될 것이다. 본 발명은 여기서 설명되는 실시예들에 한정되지 않고, 다른 형태로 구체화될 수도 있다. 여기서 소개되는 실시예들은 개시된 내용이 철저하고 완전해질 수 있도록 그리고 본 발명이 속하는 기술 분야에서 통상의 지식을 가진 자에게 본 발명의 사상이 충분히 전달될 수 있도록 하기 위해 제공되는 것이다. 따라서, 이하의 실시예들에 의하여 본 발명이 제한되어서는 안 된다.
본 명세서에서 사용된 용어인 "반응 생성물"은 둘 이상의 반응물이 반응하여 형성되는 생성물을 의미한다.
또, 본 명세서에서 기재된 화학식에서 사용된 영문자 "A", "B", 및 "R"은 숫자로 표시되는 하첨자를 갖지만, 상기 "A", "B", 및 "R"은 이 같은 하첨자에 의해 한정되어서는 안된다. 예를 들어, 분지제의 작용기를 대표하여 표현하기 위해 사용된 "R"들은 서로 독립적이며, 상기 "R"들이 서로 다른 숫자의 하첨자를 갖는다고 하여도, 이 "R"들은 같은 작용기를 나타낼 수도 있고, 다른 작용기를 나타낼 수도 있다.
본 발명에 따른 분지상 폴리락트산-폴리카프로락톤 공중합체는 분지상 폴리락트산과 카프로락톤 올리고머의 반응 생성물이다. 상기 분지상 폴리락트산은 락트산 올리고머와 분지제의 반응 생성물일 수 있다.
상기 락트산 올리고머는 락트산을 탈수 반응시킴으로써 형성될 수 있다. 상기 락트산은 한 분자 내에 히드록시기와 카르복실기를 모두 가지고 있다. 상기 락트산은 이성질체로 존재할 수 있고, L 락트산, D 락트산, 또는 L 락트산과 D 락트산의 혼합물일 수 있다.
상기 탈수 반응은 상기 락트산에 촉매를 첨가함으로써 진행될 수 있다. 상기 촉매는 산화아연, 산화안티몬, 염화안티몬, 산화납, 산화칼슘, 산화알루미늄, 산화철, 염화칼슘, 초산아연, 파라톨루엔 슬폰산, 염화제1주석, 황산제1주석, 산화제1주석, 산화제2주석, 옥탄산제1주석, 테트라페닐주석, 주석분말 및 사염화티탄 중 적어도 어느 하나를 포함할 수 있다. 상기 촉매는 상기 락트산 100중량부에 대하여 0.0005 내지 5중량부, 바람직하게는 0.003 내지 1중량부로 첨가될 수 있다. 촉매 함량이 0.0005중량부 미만이면 반응 속도가 매우 느려 락트산 올리고머가 제대로 형성되기 어렵고, 촉매 함량이 5중량부 초과이면 반응 속도는 빨라지나 반응 후 잔존하는 촉매에 의해 물성이 떨어질 수 있고, 색상이 저하될 수 있다.
상기 탈수 반응은 100 내지 180℃의 질소와 같은 불활성 기체 분위기 하에서 진행될 수 있다. 바람직하게는 상기 탈수 반응은 130 내지 150℃에서 진행될 수 있다. 반응 온도가 100℃ 미만이면 수분이 효과적으로 제거되지 않을 수 있고, 반응 온도가 180℃ 초과이면 해중합이 일어나고 열분해가 촉진되어 물성 저하 및 색상 변화가 일어날 수 있다.
상기 탈수 반응에서 락트산 분자의 히드록시기와 카르복실기는 각각 다른 분자의 카르복실기 또는 히드록시기와 에스테르화 반응을 하여 결합한다. 상기 탈수 반응에 의해 하기 화학식 1을 갖는 락트산 올리고머가 형성될 수 있다.
[화학식 1]
상기 화학식 1에서, n은 40 내지 700의 정수를 나타낼 수 있다.
상기 락트산 올리고머는 그 일단에 히드록시기를 가질 수 있고, 그 타단에 카르복실기를 가질 수 있다.
상기 락트산 올리고머의 분자량은 3,000 내지 50,000, 바람직하게는 5,000 내지 30,000일 수 있다. 상기 락트산 올리고머의 분자량이 3,000 미만이면 분지화되는 과정에서 분자량 분포(Mw/Mn)가 커지고 고온에서 열분해가 촉진되어 고분자량을 얻기 힘들고, 50,000 초과이면 분지화되는 과정에서 겔화가 일어나 반응이 진행되지 못할 우려가 있다.
상기 탈수 반응이 완료된 후, 형성된 락트산 올리고머가 정제될 수 있다. 먼저, 상기 락트산 올리고머를 클로로포름 또는 메틸렌클로라이드 등의 양용매에 충분히 용해한 후 메탄올 등의 빈용매에 침지시켜, 상기 탈수 반응 후 잔존하는 락트산과 수분이 제거될 수 있다. 상기 잔존하는 락트산은 락트산 올리고머 100중량부에 대하여 0.5중량부, 바람직하게는 0.3중량부를 초과하지 않도록 제거될 수 있다. 상기 잔존하는 락트산 함량이 0.5중량부 초과이면 이후 공정에서 락트산 올리고머의 중합반응 속도가 매우 느려질 수 있고, 해중합이 일어나고 열분해가 촉진되어 고분자량의 폴리락트산을 얻기 힘들 수 있다.
상기 락트산 올리고머에 분지제를 첨가하여 축합중합 반응시켜, 분지상 폴리락트산이 형성될 수 있다.
상기 분지제는 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 3개 이상 포함할 수 있다. 상기 분지제는 세 개 이상의 작용 기를 갖는 다가의 지방족 또는 환상 알코올 및 다가의 지방족 또는 환상 카르복실산 중 적어도 어느 하나를 포함할 수 있다. 상기 분지제는 하기 화학식 2a 및 2b 중 적어도 어느 하나를 가질 수 있다.
[화학식 2a]
[화학식 2b]
상기 화학식 2a 및 2b에서, X는 탄소수 1 내지 20의 알킬렌, 탄소수 6 내지 20의 아릴렌, 탄소수 3 내지 20의 시클로알킬렌 또는 탄소수 8 내지 20의 아릴알킬렌을 나타낼 수 있고, R1 내지 R4는 각각 독립적으로, 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 나타낼 수 있다.
상기 분지제는 예를 들어, 1,2,2-에탄트리카르복실산, 1,3,5-펜타트리카르복실산, 트리메틸올프로판, 글리세롤, 1,1,4,4-테트라키스(히드록시메틸)사이클로헥산, 펜타에리트리톨 및 디펜타에리트리톨 중 적어도 어느 하나를 포함할 수 있다.
상기 분지제는 상기 락트산 올리고머 100중량부에 대하여 0.01 내지 2중량부, 바람직하게는 0.1 내지 0.5중량부로 첨가될 수 있다. 분지제 함량이 0.01중량 부 미만이면 분지제의 효과가 미비할 수 있고, 2중량부 초과이면 과도한 분지제의 효과로 겔화(gelation)가 발생하여 가공이 어려울 수 있다.
상기 축합중합 반응은 상기 락트산 올리고머와 상기 분지제를 포함하는 혼합물에 촉매를 첨가함으로써 진행될 수 있다. 상기 혼합물은 필요에 따라 다양한 종류의 산화방지제와 열안정제를 더 포함할 수 있다. 상기 촉매는 산화아연, 산화안티몬, 염화안티몬, 산화납, 산화칼슘, 산화알루미늄, 산화철, 염화칼슘, 초산아연, 파라톨루엔 슬폰산, 염화제1주석, 황산제1주석, 산화제1주석, 산화제2주석, 옥탄산제1주석, 테트라페닐주석, 주석분말 및 사염화티탄 중 적어도 어느 하나를 포함할 수 있다. 상기 촉매는 상기 락트산 올리고머 100중량부에 대하여 0.0005 내지 5중량부, 바람직하게는 0.003 내지 1중량부로 첨가될 수 있다. 촉매 함량이 0.0005중량부 미만이면 반응 속도가 매우 느려 고분자량의 폴리락트산을 얻기 힘들 수 있고, 촉매 함량이 5중량부 초과이면 반응 속도는 빨라지나 반응 후 잔존하는 촉매에 의해 물성이 떨어질 수 있고, 색상이 저하될 수 있다.
상기 축합중합 반응은 150 내지 220℃, 바람직하게는 170 내지 200℃에서 진행될 수 있다. 반응 온도가 150℃ 미만이면 반응 속도가 느려져 축합중합 시간이 길어질 수 있고, 반응 온도가 220℃ 초과이면 열분해가 촉진될 수 있다. 또 상기 축합중합 반응은 0.5torr 이하, 바람직하게는 0.1torr 이하의 고진공 조건에서 진행될 수 있다. 반응 압력이 0.5torr 초과이면 반응시간이 길어지고 고분자량의 폴리락트산이 형성되기 어렵다. 단, 상기 축합중합 반응에서, 반응 온도, 반응 압력, 및 촉매의 종류는 첨가되는 분지제의 종류를 고려하여 적절하게 선택될 수 있다.
상기 축합중합 반응에 의해 형성된 분지상 폴리락트산은 하기 화학식 3a 및 3b 중 적어도 어느 하나를 가질 수 있다.
[화학식 3a]
[화학식 3b]
상기 화학식 3a 및 3b에서, X는 탄소수 1 내지 20의 알킬렌, 탄소수 6 내지 20의 아릴렌, 탄소수 3 내지 20의 시클로알킬렌 또는 탄소수 8 내지 20의 아릴알킬렌을 나타낼 수 있다. R1* 내지 R4*는 각각 독립적으로, 상기 화학식 2a 및 2b의 분지제의 작용기 R1 내지 R4가 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응한 후의 구조를 나타낼 수 있다. 상기 R1* 내지 R4*는 예를 들어, 상기 작용기 R1 내지 R4에서 -OH 또는 -H가 제거된 구조를 나타낼 수 있다. 즉, 상기 분지제의 작용기 R1 내지 R4와 상기 락트산 올리고머의 히드록시기 또는 카르복실기가 상기 축합중합 반응에 의해 A1-R1* 내지 A4-R4* 결합을 형성할 수 있다. 상기 R1* 내지 R4*에 대한 상기 A1 내지 A4의 결합 방향은 상기 분지제의 작용기 R1 내지 R4의 종류에 따라 결정될 수 있다. 상기 분지제의 작용기가 히드록시기와 반응할 수 있는 경우와 카르복실기와 반응할 수 있는 경우에 있어서, 상기 A1 내지 A4의 결합 방향은 서로 반대 방향일 수 있다.
상기 화학식 3a 및 3b에서, A1 내지 A4는 각각 독립적으로, 하기 화학식 4를 나타낼 수 있다.
[화학식 4]
상기 화학식 4에서, m은 100 내지 2,000의 정수를 나타낼 수 있다.
상기 분지상 폴리락트산의 분자량은 10,000 내지 250,000, 바람직하게는 30,000 내지 200,000일 수 있다. 상기 분지상 폴리락트산의 분자량이 10,000 미만이면 제품을 성형했을 때 물성이 떨어질 수 있고, 250,000 초과이면 겔이 형성될 가능성이 높아 더 이상의 반응이 어려운 문제점이 있다.
상기 분지상 폴리락트산에 카프로락톤 올리고머를 첨가하여 축합중합 반응 시켜, 분지상 폴리락트산-폴리카프로락톤 공중합체가 형성될 수 있다.
상기 카프로락톤 올리고머의 첨가량은 분지상 폴리락트산 100중량부에 대하여 1 내지 20중량부, 바람직하게는 1 내지 10중량부일 수 있다. 상기 카프로락톤 올리고머의 참가량이 1중량부 미만이면, 충격강도 향상 효과가 적고, 20중량부 초과이면, 수지의 내열성이 저하될 수 있는 문제가 있다.
상기 카프로락톤 올리고머의 분자량은 200 내지 10,000일 수 있고, 바람직하게는 500 내지 2,000일 수 있다. 상기 카프로락톤 올리고머의 분자량이 200 미만이면, 축합중합 시간이 길어지고, 고분자량을 얻기가 어렵고, 분자량이 10,000 초과이면, 분지상 폴리락트산과의 반응성이 저하될 수 있다.
상기 분지상 폴리락트산-폴리카프로락톤 공중합체를 형성하기 위한 축합중합 반응에서도 전술한 분지상 폴리락트산을 형성하기 위한 축합중합 반응에 사용되는 다양한 종류의 산화방지제와 열안정제가 추가적으로 사용될 수 있다.
상기 축합중합 반응은 150 내지 200℃, 바람직하게는 170 내지 190℃에서 진행될 수 있다. 반응 온도가 150℃ 미만이면 반응 속도가 느려져 축합중합 시간이 길어질 수 있고, 반응 온도가 200℃ 초과이면 열분해가 촉진될 수 있다. 또 상기 축합중합 반응은 0.5torr 이하, 바람직하게는 0.1torr 이하의 고진공 조건에서 진행될 수 있다. 반응 압력이 0.5torr 초과이면 반응시간이 길어지고 고분자량의 공중합체를 얻기가 어렵다.
상기 분지상 폴리락트산-폴리카프로락톤 공중합체는 하기 화학식 5a 및 5b 중 적어도 어느 하나를 가질 수 있다.
[화학식 5a]
[화학식 5b]
상기 화학식 5a 및 5b에서, X는 탄소수 1 내지 20의 알킬렌, 탄소수 6 내지 20의 아릴렌, 탄소수 3 내지 20의 시클로알킬렌 또는 탄소수 8 내지 20의 아릴알킬렌을 나타낼 수 있다. R1* 내지 R4*는 각각 독립적으로, 상기 화학식 2a 및 2b의 분지제의 작용기 R1 내지 R4가 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응한 후의 구조를 나타낼 수 있다. A1 내지 A4는 각각 독립적으로, 상기 화학식 4를 나타낼 수 있다.
상기 화학식 5a 및 5b에서, B1 내지 B4는 각각 독립적으로, 하기 화학식 6을 나타낼 수 있다.
[화학식 6]
상기 화학식 6에서, p는 2 내지 500의 정수를 나타낼 수 있으며, 바람직하게는 5 내지 200의 정수일 수 있다.
상기 분지상 폴리락트산-폴리카프로락톤 공중합체의 분자량은 20,000 내지 300,000, 바람직하게는 50,000 내지 200,000일 수 있다. 상기 분지상 폴리락트산-폴리카프로락톤 공중합체의 분자량이 20,000 미만이면 제품을 성형했을 때 물성이 떨어질 수 있고, 300,000 초과이면 겔이 형성될 가능성이 높아 가공시 더 많은 에너지가 소비되는 문제점이 있다.
<실시예>
실시예1
5ℓ 3구 축합반응기에 락트산 1.5kg과 촉매 3g을 넣고 질소 가스 분위기 하에서 150℃로 승온시켜 탈수 반응을 진행시켰다. 더 이상 물이 증류되지 않는 3시간 후에 탈수 반응을 종결시켜 락트산 올리고머를 얻었다. 상기 락트산 올리고머900g, 분지제1 0.9g(락트산 올리고머 100중량부에 대하여 0.1 중량부), 촉매 1.5g 및 산화방지제 0.1g을 반응기에 넣어 교반하면서 180℃로 승온시켰다. 1시간에 걸 쳐 압력을 점차적으로 0.1 torr까지 낮추어 감압 상태에서 12시간 동안 축합 반응을 진행하였다. 그 후 감압을 해제하고 카프로락톤 올리고머(Solvay, Mn=1250) 45g(락트산 올리고머 100중량부에 대하여 5중량부)을 넣은 후 다시 30분에 걸쳐 압력을 0.1torr까지 낮추어 감압 상태에서 축합 반응을 진행하였다. 점도가 급격히 상승하는 지점에서 축합 반응을 종결시켜 분지상 폴리락트산-폴리카프로락톤 공중합체 수지를 얻었다.
실시예2
분지제1의 함량을 1.8g(락트산 올리고머 100중량부에 대하여 0.2중량부)으로 하는 것을 제외하고는 실시예1과 동일한 방법으로 분지상 폴리락트산-폴리카프로락톤 공중합체 수지를 얻었다.
실시예3
분지제1의 함량을 4.5g(락트산 올리고머 100중량부에 대하여 0.5중량부)으로 하는 것을 제외하고는 실시예1과 동일한 방법으로 분지상 폴리락트산-폴리카프로락톤 공중합체 수지를 얻었다.
실시예4
분지제1 대신에 분지제2 1.8g(락트산 올리고머 100중량부에 대하여 0.2중량부)을 첨가하는 것을 제외하고는 실시예1과 동일한 방법으로 분지상 폴리락트산-폴 리카프로락톤 수지를 얻었다.
비교예1
카프로락톤 올리고머를 투입하지 않고 실시예2와 동일한 방법으로 중합을 실시하였고, 점도가 급상승하는 지점에서 중합반응을 종료시켜 분지상 폴리락트산 수지를 얻었다.
비교예2
분지제를 첨가하지 않고 실시예1과 동일한 방법으로 중합을 실시하여 직쇄구조의 폴리락트산-폴리카프로락톤 수지를 얻었다.
하기 표 1에 상기 실시예1 내지 4와 비교예1 및 2에 사용된 락트산 올리고머, 카프로락톤 올리고머, 분지제1 및 2, 촉매, 및 산화방지제의 양을 정리하여 기재하였다.
| 구분 |
구성 성분(g) | ||||||
| 락트산 올리고머 | 카프로락톤 올리고머 | 분지제1 | 분지제2 | 촉매 | 산화방지제 | ||
| 탈수반응 | 축합중합반응 | ||||||
| 실시예1 | 900 | 45 | 0.9 | 0 | 3 | 1.5 | 0.1 |
| 실시예2 | 900 | 45 | 1.8 | 0 | 3 | 1.5 | 0.1 |
| 실시예3 | 900 | 45 | 4.5 | 0 | 3 | 1.5 | 0.1 |
| 실시예4 | 900 | 45 | 0 | 1.8 | 3 | 1.5 | 0.1 |
| 비교예1 | 900 | 0 | 1.8 | 0 | 3 | 1.5 | 0.1 |
| 비교예2 | 900 | 45 | 0 | 0 | 3 | 1.5 | 0.1 |
* 카프로락톤 올리고머: Solvay
* 분지제1(1,3,5-PENTANETRICARBOXYLIC ACID): Aldrich
* 분지제2(PENTAERYTHRITOL): Aldrich
* 촉매(ANTIMONY(Ⅲ) OXIDE): Fluka
* 산화방지제(Irganox 1010): Ciba
상기 실시예1 내지 4와 비교예1 및 2에 따라 제조된 분지상 폴리락트산-폴리카프로락톤 공중합체의 물성을 다음의 방법으로 측정하여 그 결과를 하기 표 2에 기재하였다.
(1) 수평균 분자량(Mn): GPC(Gel Permeation Chromatograph, 겔 투과 크로마토그래프) (Waters 2690, PL)를 사용하여 온도를 40℃ 조건으로 하고 유량(flow rate)을 1㎖/min로 하여 수평균 분자량(Mn)을 측정하였다. (Standard: Polystyrene)
(2) 유리전이온도(Tg): 시차주사열량계(DSC Q100, TA Instrument)를 사용하여 승온 속도를 10℃/min로 하여 20℃에서 200℃까지 승온시켰으며, 20℃까지 급냉한 후, 다시 200 ℃까지 승온시켜 측정하였다.
(3) 충격강도: ASTM D256 방법으로 노치 컷(notch cut)된 시편을 준비하고, 충격시험기(CEAST, IT-98)를 사용하여 충격강도를 측정하였다.
| 구분 | 수평균 분자량 | 유리전이온도(℃) | 충격 강도(kgf/㎠) |
| 실시예1 | 54,000 | 52 | 8 |
| 실시예2 | 59,000 | 48 | 12 |
| 실시예3 | 72,000 | 42 | 15 |
| 실시예4 | 57,000 | 49 | 9 |
| 비교예1 | 58,000 | 57 | 3 |
| 비교예2 | 12,000 | 35 | 2 |
상기 표 2에 나타난 바와 같이, 분지제가 첨가되지 않은 비교예2의 경우에는 축합반응 중 점도의 급상승을 관찰할 수 없었으며 높은 분자량을 얻는 것이 어려운 반면, 분지제 함량이 증가함에 따라 높은 분자량과 낮은 유리전이온도를 갖는 폴리락트산-폴리카프로락톤 공중합체를 얻을 수 있음을 알 수 있다. 또, 충격 강도가 향상되는 결과로부터 낮은 유리전이온도에서 분자쇄의 유연성이 증가하는 것을 알 수 있다.
실시예2 및 4와 비교예 1의 결과로부터, 유연한 구조를 갖는 폴리카프로락톤을 폴리락트산의 축합중합에 도입함으로써 유사 수준의 분자량임에도 불구하고 충격 강도가 현저히 향상됨을 알 수 있다.
실시예2 및 4의 결과에서는, 분지제 1을 사용하면 분지제 2를 사용하는 것보다 그 효과가 우수한 것으로 나타났다.
이제까지 본 발명에 대한 구체적인 실시예들을 살펴보았다. 본 발명이 속하는 기술 분야에서 통상의 지식을 가진 자는 본 발명이 본 발명의 본질적인 특성에서 벗어나지 않는 범위에서 변형된 형태로 구현될 수 있음을 이해할 수 있을 것이다. 그러므로 개시된 실시예들은 한정적인 관점이 아니라 설명적인 관점에서 고려되어야 한다. 본 발명의 범위는 전술한 설명이 아니라 특허청구범위에 나타나 있으며, 그와 동등한 범위 내에 있는 모든 차이점은 본 발명에 포함된 것으로 해석되어야 할 것이다.
Claims (19)
- 분지상 폴리락트산과 카프로락톤 올리고머의 반응 생성물인 분지상 폴리락트산-폴리카프로락톤 공중합체로,상기 분지상 폴리락트산은 락트산 올리고머와 분지제의 반응 생성물인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 분지제는 1,3,5-펜타트리카르복실산인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 분지제는 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 3개 이상 포함하는 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 분지제의 함량은 상기 락트산 올리고머 100중량부에 대하여 0.01 내지 2중량부인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 락트산 올리고머의 분자량은 3,000 내지 50,000인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 분지상 폴리락트산의 분자량은 10,000 내지 250,000인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 카프로락톤 올리고머의 분자량은 200 내지 10,000인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항에 있어서,상기 카프로락톤 올리고머의 함량은 상기 락트산 올리고머 100중량부에 대하여 1 내지 20중량부인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 제 1 항 내지 제 9 항 중 어느 한 항에 있어서,20,000 내지 300,000의 분자량을 갖는 분지상 폴리락트산-폴리카프로락톤 공중합체.
- 락트산 올리고머에 분지제를 첨가하여 축합중합 반응시켜 분지상 폴리락트산 을 형성하는 단계; 및상기 분지상 폴리락트산에 카프로락톤 올리고머를 첨가하여 축합중합 반응시키는 단계를 포함하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 락트산 올리고머는 100 내지 180℃의 불활성 기체 분위기 하에서 락트산을 탈수 반응시킴으로써 형성되고, 3,000 내지 50,000의 분자량을 갖는 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 11 항에 있어서,상기 탈수 반응 및 상기 축합중합 반응에서 사용되는 촉매는, 산화아연, 산화안티몬, 염화안티몬, 산화납, 산화칼슘, 산화알루미늄, 산화철, 염화칼슘, 초산아연, 파라톨루엔 슬폰산, 염화제1주석, 황산제1주석, 산화제1주석, 산화제2주석, 옥탄산제1주석, 테트라페닐주석, 주석분말 및 사염화티탄으로 이루어진 군으로부터 선택되는 하나 이상을 포함하는 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 12 항에 있어서,상기 촉매의 함량은 상기 락트산 또는 상기 락트산 올리고머 100중량부에 대하여 0.0005 내지 5중량부인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락 톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 분지제는 상기 락트산 올리고머의 히드록시기 또는 카르복실기와 반응할 수 있는 작용기를 3개 이상 포함하는 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 분지제는 상기 락트산 올리고머 100중량부에 대하여 0.01 내지 2중량부로 첨가되는 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 분지상 폴리락트산의 분자량은 10,000 내지 250,000인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 카프로락톤 올리고머의 분자량은 200 내지 10,000인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 분지상 폴리락트산-폴리카프로락톤 공중합체의 분자량은 20,000 내지 300,000인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
- 제 10 항에 있어서,상기 분지제는 1,3,5-펜타트리카르복실산인 것을 특징으로 하는 분지상 폴리락트산-폴리카프로락톤 공중합체의 제조 방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020090123256A KR101247442B1 (ko) | 2009-12-11 | 2009-12-11 | 분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020090123256A KR101247442B1 (ko) | 2009-12-11 | 2009-12-11 | 분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20110066553A KR20110066553A (ko) | 2011-06-17 |
| KR101247442B1 true KR101247442B1 (ko) | 2013-03-25 |
Family
ID=44399366
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020090123256A KR101247442B1 (ko) | 2009-12-11 | 2009-12-11 | 분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101247442B1 (ko) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5578662A (en) * | 1994-07-22 | 1996-11-26 | United States Surgical Corporation | Bioabsorbable branched polymers containing units derived from dioxanone and medical/surgical devices manufactured therefrom |
| KR970002523B1 (en) * | 1993-04-24 | 1997-03-05 | Korea Inst Sci & Tech | Biodegradable polylactic acid having improved properties and method for manufacturing the same |
-
2009
- 2009-12-11 KR KR1020090123256A patent/KR101247442B1/ko active IP Right Grant
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR970002523B1 (en) * | 1993-04-24 | 1997-03-05 | Korea Inst Sci & Tech | Biodegradable polylactic acid having improved properties and method for manufacturing the same |
| US5578662A (en) * | 1994-07-22 | 1996-11-26 | United States Surgical Corporation | Bioabsorbable branched polymers containing units derived from dioxanone and medical/surgical devices manufactured therefrom |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20110066553A (ko) | 2011-06-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6713595B2 (en) | Copolyester resin composition and a process of preparation thereof | |
| US7256250B2 (en) | Biodegradable coating | |
| Jahandideh et al. | Star-shaped lactic acid based systems and their thermosetting resins; synthesis, characterization, potential opportunities and drawbacks | |
| JPH08504850A (ja) | ゴム変性されたポリラクチドおよび/またはグリコリド組成物 | |
| US8071690B2 (en) | Lactic acid based compositions with enhanced properties | |
| CN111087580A (zh) | 聚乙醇酸的制备方法 | |
| JP5223347B2 (ja) | 樹脂組成物及びその製造方法、並びに共重合体 | |
| Liu et al. | Characterization, biodegradability and blood compatibility of poly [(R)‐3‐hydroxybutyrate] based poly (ester‐urethane) s | |
| CN101815741B (zh) | 制备丙交酯与1:4-3:6双脱水己糖醇的共聚物的方法 | |
| CN110684179A (zh) | 一种高分子量聚乳酸的制备方法 | |
| KR20150017797A (ko) | 친환경적 코폴리에스테르 수지 및 그 제조방법 | |
| Reyhanoglu et al. | Synthesis of polyglycolic acid copolymers from cationic copolymerization of C1 feedstocks and long chain epoxides | |
| US9102782B2 (en) | Transparent copolyester, preparing method thereof and articles made from the same | |
| KR101247442B1 (ko) | 분지상 폴리락트산-폴리카프로락톤 공중합체 및 그 제조 방법 | |
| JP3666525B2 (ja) | 脂肪族ポリエステルカーボネート及びその製造方法 | |
| JP4390273B2 (ja) | 生分解性樹脂組成物 | |
| KR100817905B1 (ko) | 생체적합성이 우수한 생분해성 지방족 폴리에스테르 수지 조성물 및 그 제조방법 | |
| KR20150056684A (ko) | 폴리에테르 에스테르 엘라스토머 및 제조 방법 | |
| KR102350740B1 (ko) | 아세틸화 락타이드 올리고머계 가소제 및 이의 제조방법, 및 아세틸화 락타이드 올리고머계 가소제를 포함하는 pla 수지 조성물 | |
| KR101395357B1 (ko) | 폴리락트산-폴리실록산 공중합체 및 그 제조 방법 | |
| KR100656986B1 (ko) | 전단 담화와 강인성이 향상된 신규한 폴리락티드/클레이나노 복합체의 제조방법 | |
| CN116120532B (zh) | 一种聚丁二酸丁二醇酯的制备方法及聚丁二酸丁二醇酯 | |
| KR100683941B1 (ko) | 전단 담화와 강인성이 향상된 신규한 폴리락티드/클레이나노 복합체의 제조방법 | |
| CN113004499B (zh) | 生物可降解的聚酯弹性体及其制备方法和应用 | |
| JP4696306B2 (ja) | 生分解性ポリエステル及びその製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| N231 | Notification of change of applicant | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20151204 Year of fee payment: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20161202 Year of fee payment: 5 |
|
| FPAY | Annual fee payment |
Payment date: 20171213 Year of fee payment: 6 |
|
| FPAY | Annual fee payment |
Payment date: 20181205 Year of fee payment: 7 |
|
| FPAY | Annual fee payment |
Payment date: 20191216 Year of fee payment: 8 |