JP7686802B2 - 抗-tm4sf4ヒト化抗体及びこの用途 - Google Patents
抗-tm4sf4ヒト化抗体及びこの用途 Download PDFInfo
- Publication number
- JP7686802B2 JP7686802B2 JP2023578042A JP2023578042A JP7686802B2 JP 7686802 B2 JP7686802 B2 JP 7686802B2 JP 2023578042 A JP2023578042 A JP 2023578042A JP 2023578042 A JP2023578042 A JP 2023578042A JP 7686802 B2 JP7686802 B2 JP 7686802B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- amino acid
- cancer
- acid sequence
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/5758—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumours, cancers or neoplasias, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides or metabolites
- G01N33/5759—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumours, cancers or neoplasias, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides or metabolites involving compounds localised on the membrane of tumour or cancer cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70596—Molecules with a "CD"-designation not provided for elsewhere in G01N2333/705
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Biochemistry (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Microbiology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Animal Behavior & Ethology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Biotechnology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Oncology (AREA)
Description
Member 4)に高い親和度で特異的結合することができ、ヒトにおいて低い免疫原性を示すヒト化抗体及びこれを含む癌の予防又は治療用組成物に関する。
合親和度が減少する可能性が発生する。よって、人体においてHAMAの発生を誘導しないとともに、抗原に対する高い特異性と親和度を示すヒト化抗体を開発することには依然として困難を伴うことが実情である。
る癌細胞、癌幹細胞を標的として有用に用いることができる。特に、本発明のヒト化抗体は、マウス由来の抗体と類似するか、キメラ抗体に比べて結合親和度が顕著に高いという特徴があるので優れた効果を奏する。
本発明の一側面は、TM4SF4に特異的に結合して人体で低い免疫原性を示すヒト化抗体又はこの抗原結合断片を提供する。
明の抗体は、単一クローン抗体又はこの抗原結合断片であってよい。前記単一クローン抗体は、実質的に同一の抗体集団から得た単一分子組成の抗体分子を称し、このような単一クローン抗体は、特定のエピトープに対して単一結合特異性及び親和度を示す。前記全長抗体は、2個の全長軽鎖及び2個の全長重鎖を有する構造であり、それぞれの軽鎖は重鎖とジスルフィド結合で連結されてよい。前記抗体は、重鎖(heavy chain、HC)及び軽鎖(light chain、LC)ポリペプチドを含み、前記重鎖及び軽鎖は、可変領域及び不変領域を含むことができる。
を介して重鎖可変領域と軽鎖可変領域が共有結合で連結されるか、又はC-末端で直ぐ連結されているので、二重鎖Fvのようにダイマーのような構造をなすことができる。前記抗原結合断片は、タンパク質加水分解酵素を用いるか(例えば、全体抗体をパパインで制限切断すればFabを得ることができ、ペプシンで切断すればF(ab’)2断片を得ることができる)、又は遺伝子組換え技術を介して製作することができるが、これに制限されるものではない。
本発明のまた他の側面は、前記ヒト化抗体又はこの抗原結合断片を発現して製造するために用いられ得る、ポリヌクレオチド、発現ベクター、宿主細胞及び生産方法を提供する。
するヌクレオチドだけでなく、糖又は塩基部位が変形された類似体(analogue)も含まれてよい。
のアミノ酸配列を暗号化するものであってよく、前記配列番号51の塩基配列は、前記配列番号23のアミノ酸配列を暗号化するものであってよく、前記配列番号52の塩基配列は、前記配列番号24のアミノ酸配列を暗号化するものであってよく、前記配列番号53の塩基配列は、前記配列番号25のアミノ酸配列を暗号化するものであってよく、前記配列番号54の塩基配列は、前記配列番号26のアミノ酸配列を暗号化するものであってよく、前記配列番号55の塩基配列は、前記配列番号27のアミノ酸配列を暗号化するものであってよく、前記配列番号56の塩基配列は、前記配列番号28のアミノ酸配列を暗号化するものであってよい。
Bacteriol、(1984)158:1018-1024)、そしてファージλの左向プロモーター(pLλプロモーター、Herskowitz,I and Hage
n,D,Ann Rev Genet,(1980)14:399-445)が調節部位として用いられてよい。宿主細胞としてバチルス菌が用いられる場合、バチルスチューリンゲンシスの毒素タンパク質遺伝子のプロモーター(Appl Environ Microbiol(1998)64:3932-3938;Mol Gen Genet(1
996)250:734-741)又はバチルス菌で発現可能な如何なるプロモーターであっても調節部位に用いられてよい。前記発現ベクターは、当業界でたびたび用いられるプラスミド(例えば、pCL、pSC101、pGV1106、pACYC177、ColE1、pKT230、pME290、pBR322、pUC8/9、pUC6、pBD9、pHC79、pIJ61、pLAFR1、pHV14、pGEXシリーズ、pETシリーズ及びpUC19など)、ファージ(例えば、λgt4・λB、λ-Charon、λΔz1及びM13など)又はウイルス(例えば、SV40など)を操作して製作されてよい。
on)又は標的形質転換(targetedTransformation)を介して宿主細胞に導入され得る。同時形質転換は、軽鎖及び重鎖をコーディングするそれぞれのベクターDNAを同時に宿主細胞に導入した後、軽鎖と重鎖を全て発現する細胞を選別する方法である。標的形質転換は、軽鎖(又は重鎖)を含むベクターに形質転換された細胞を選別し、選別された細胞を重鎖(又は軽鎖)を含むベクターに再び形質転換して軽鎖及び重鎖の全部を発現する細胞を最終的に選別する方法である。
Bacillus thuringiensis)のようなバチルス属菌株、ストレプトマイセス(Streptomyces)、シュードモナス(Pseudomonas)、例えば、シュードモナスプチダ(Pseudomonas putida)、プロテウスミラビリス(Proteus mirabilis)、又はスタフィロコッカス(Staphylococcus)、例えば、スタフィロコッカスカルノーサス(Staphylococcus carnosus)のような原核宿主細胞であってよいが、これに制限されるものではない。
species)のような真菌、ピキアパストリス(Pichia pastoris)、サッカロマイセスセレビシエ(Saccharomyces cerevisiae)、シゾサッカロミケス(Schizosaccharomyces)及びニューロスポラクラッサ(Neurospora crassa)のような酵母、その他の下等真核細胞、昆虫-由来細胞のような高等真核生物の細胞、そして植物又は哺乳動物から由来した細胞を用いることができる。前記宿主細胞は、COS7細胞(monkey kidney cells)、NSO細胞、SP2/0、チャイニーズハムスター卵巣(CHO:Chinese hamster ovary)細胞、W138、ベビーハムスターの腎臓(BHK:baby hamster kidney)細胞、MDCK、骨髄腫細胞株、HuT 78細胞又は293細胞であってよいが、これに制限されない。
窒素源を含んでよく、これらの窒素源は単独で又は組み合わせて用いられてよい。
本発明のまた他の側面は、前記ヒト化抗体又はこの抗原結合断片のTM4SF4検出の用途を提供する。具体的に、本発明では、TM4SF4検出用組成物、TM4SF4検出用キット及びTM4SF4を検出する方法を提供する。
TM4SF4検出用組成物、これを含むキット又は前記ヒト化抗体、この抗原結合断片を用いたTM4SF4抗原の定量方法は、抗原-抗体複合体の形成を確認して行われてよく、前記抗原-抗体複合体の形成の確認は、酵素免疫分析法(ELISA)、ウエスタンブロッティング(Western Blotting)、免疫蛍光(Immunofluorescence)、免疫組織化学染色(Immunohistochemistry staining)、フローサイトメトリー(Flow cytometry)、免疫疫
細胞化学法(Immunocytochemistry)、放射免疫分析法(RIA)、免疫沈澱分析法(Immunoprecipitation Assay)、免疫拡散分析法(Immunodiffusion assay)、補体固定分析法(Complement Fixation Assay)、タンパク質チップ(Protein Chip)などによりなされてよいが、これに制限されるものではない。前記酵素免疫分析法(ELISA)には、固体支持体に付着された抗原を認知する標識された抗体を用いる直接的ELISA、固体支持体に付着された抗原を認知する抗体の複合体で捕獲抗体を認知する標識された2次抗体を用いる間接的ELISA、固体支持体に付着された抗体と抗原の複合体で抗原を認知する標識されたまた他の抗体を用いる直接的サンドイッチELISA、固体支持体に付着された抗体と抗原の複合体で抗原を認知するまた他の抗体と反応させた後、この抗体を認知する標識された2次抗体を用いる間接的サンドイッチELISAなどの多様なELISA方法を含む。
本発明のまた他の側面は、前記ヒト化抗体又はこの抗原結合断片を含む癌の予防又は治療用薬学的組成物、癌幹細胞の成長抑制用組成物及び放射線抗癌治療補助用組成物を提供する。
甲状腺癌であり、より具体的には、肺癌、乳癌、肝癌、腎臓癌、胃癌、すい臓癌、脳癌であってよいが、これに制限されない。本発明における癌は、特にTM4SF4の過剰発現、増幅、突然変異又は活性化による癌であってよいが、これに制限されない。すなわち、本発明のヒト化抗体又はこの結合断片を含む組成物は、TM4SF4の異常発現又は突然変異と関わりなく全ての癌腫に対して増殖抑制効果を有するので、本発明の医薬用途がTM4SF4の発現様態又は突然変異の有無により制限されない。
、自己調節機能に異常があって細胞分裂活性化で細胞数が増加するようになり、自ら悪性腫瘍細胞に分化する。このような癌幹細胞の特徴により、抗癌治療を介して一般の癌細胞は除去されるが癌幹細胞は生き残り、生き残った一部の癌幹細胞により癌の再発及び転移がなされると知られている。
的に、前記癌関連細胞は、癌細胞又は癌幹細胞であってよく、具体的に癌幹細胞であってよい。
TM4SF4に特異的に結合するヒト化抗体の設計及び発現ベクターの製造
TM4SF4タンパク質に対し高い親和度を有して特異的に結合することができるヒト化抗体を製造した。このために、TM4SF4と特異的な結合を形成するための抗体部位のうち可変領域のCDR(complementarity determining regions)のアミノ酸配列を、ヒト抗体の不変領域のアミノ酸配列と可変領域のFR(framework regions)のアミノ酸配列を用いて、TM4SF4に対する特異的結合性を有しながらも、人体に投与されたときに低い免疫原性(immunogenicity)を示し得る新規のヒト化抗体を製造した。
発明のヒト化抗体を製造した。先ず、前記CDR配列中で重鎖可変領域のCDR配列(配列番号10、配列番号11及び配列番号14)の前方に信号ペプチド配列を追加して得たCDR配列のアミノ酸配列に基づき、逆翻訳(reverse translate)プログラム(https://www.bioinformatics.org/sms2/rev_trans.html)を用いて、これを暗号化する塩基配列に変換した。その後、組換えPCRを用いて、前記FR配列(配列番号1、配列番号2、配列番号4及び配列番号5)と連結して本発明のヒト化抗体の重鎖可変領域を暗号化する遺伝子を合成した。約450bpの長さの遺伝子を3個の区間に分け、図1に示したように、ECL-2B7-S-H-5’及びECL-2B7-S-H-3’プライマーを用いてT1(164bp)を、ECL-2B7-HC-1-5’及びECL-2B7-HC-1-3’プライマーを用いてT2(167bp)を、そして、ECL-2B7-HC-2-5’及びECL-2B7-HC-2-3’プライマーを用いてT3(157bp)に該当する部位の重鎖可変領域遺伝子の切片を合成した。その後、T1及びT2切片を組換えPCRを介して連結して310bp大きさの切片に合成し、T1とT2が連結された切片を再びT3切片とCh57-H.C-5’及びECL-2B7-WH-3’プライマーを用いて連結することにより、EcoRIとApaI制限酵素切断部位を両末端に有した約450bpの本発明のヒト化抗体の重鎖可変領域(Hz2B7-1.0)遺伝子を合成した。前記重鎖可変領域は、FR-H1、CDR-H1、FR-H2、CDR-H2、FR-H3、CDR-H3、FR-H4の順に配列されるように製作し、これをアガロースゲルで確認した(図2)。この過程に用いられた前記プライマー配列は、下記表1に示した。そして、本発明のヒト化抗体の軽鎖可変領域(Hz2B7-0.1)の遺伝子は、遺伝子合成業者(Bionics、韓国)に依頼し、FR-L1(配列番号6)、CDR-L1(配列番号15)、FR-L2(配列番号7)、CDR-L2(配列番号18)、FR-L3(配列番号8)、CDR-L3(配列番号19)、FR-L4(配列番号9)の順に配列されるようにして約450bpの長さの軽鎖可変領域(Hz2B7-0.1)遺伝子を合成し、これをアガロースゲルで確認した(図3)。そして、T4連結酵素(T4 ligase、NEB、米国)を用いて前記重鎖可変領域遺伝子をpdCMV-dhfrベクターのEcoRI-ApaIの位置に、前記軽鎖可変領域遺伝子をHindIII-BsiWIの位置にT4連結酵素を用いてクローニングし(図8)、本発明のヒト化抗体(Hz2B7-1.1)を暗号化するベクターpdCMV-dhfrC-Hz2B7-1.1を製造した。
前記実施例1を介して設計した本発明のヒト化抗体のアミノ酸配列のうち一部の配列を変形させた変異体抗体を製造するために、先ず、前記ヒト化抗体と標的であるTM4SF4のエピトープの間の相互作用を確認した。一般に、抗原-抗体の結合力は、ドッキングシミュレーション(docking simulation)を介して定性的に予測することができるが、前記実施例1のヒト化抗体は、X-線構造が知られていないため、ホモロジー(Homology)モデリングを介してその構造を予測し、それに基づいて前記
抗体とエピトープの間の結合力を確認した。このために、MODELLERプログラムの8.2バージョンを用いて、前記実施例1のヒト化抗体とアミノ酸配列との類似度が高いマウスのキメリック抗体X836をBLASTを用いてホモロジーモデリングのテンプレートとして用いた。前記X836抗体の235個のアミノ酸のうち、実施例1のヒト化抗体と176個のアミノ酸が一致してアミノ酸配列の類似性が75%程度と示され、これに基づいて前記実施例1のヒト化抗体の3次元構造を予測することができた(図4)。
る55番のトリプトファン(Trp,W)は、エピトープのアスパラギン酸と隣接した位置にあるので、水素結合をより強く形成することができるアミノ酸で置換する場合、結合力が増加するものと予測された。したがって、軽鎖可変領域のCDR1に該当する31番、重鎖可変領域のCDR2に該当する55番の位置は、エピトープと親和度を増加させることができる重要な位置である(図4、図5)。また、軽鎖可変領域のCDR3に該当する100番のトレオニン(Thr,T)、重鎖可変領域のCDR2に該当する54番のトリプトファン、重鎖可変領域のCDR2に該当する56番のアスパラギンなどの3つのアミノ酸もエピトープと比較的に近くの距離に位置しているので、これらを化学的性質が異なるアミノ酸で置換すると、エピトープとの新たな水素結合又はファンデルワールス結合が誘導されて抗体の効能を増大させることができるものと予想される。したがって、軽鎖可変領域のCDR3に該当する100番、重鎖可変領域のCDR2に該当する54番、56番の位置も、エピトープと親和度を増加させることができるまた他の重要な位置である(図4、図5)。
前記実施例2-1のドッキングシミュレーション分析を介し、前記実施例1のヒト化抗体重鎖可変領域の46番のアラニン(Ala、A)をバリン(Val,V)で置換することにより、前記実施例1のヒト化抗体配列のうちFR-H2を配列番号3のアミノ酸配列として重鎖可変領域Hz2B7-2.0(HC A46V)を設計した(図5)。
dCMV-dhfr-Hz2B7-0.3を製造した。
前記実施例1及び2のヒト化抗体は、抗体の重鎖/軽鎖可変領域のうちCDR配列は、マウス抗体のCDR配列を用い、抗体の不変領域と可変領域のうちFR配列は、ヒト抗体の配列を用いて製造したものである。よって、本発明のヒト化抗体と比較するために、重鎖/軽鎖可変領域全体はマウス抗体から由来し、不変領域はヒト抗体から由来するキメラ抗体(chimeric antibody)を製造した。すなわち、前記キメラ抗体は、ヒト抗体との類似度の側面から、マウス抗体とヒト化抗体の中間に該当する抗体であるとみることができる。
GAA TGG A)プライマーとECL-2B7-S-H-3’(CTT CAC CTC GGA GTG GAC ACC TGT AGT TA-3`)プライマーを用いてPCRを行った(図7のA)。また、重鎖可変領域を増幅するために、重鎖可変領域のDNAを鋳型として2B7-S-H-5’(5`-GTC CAC TCC GAG GTG AAG CTG GAG GAG TC)プライマーとECL-2B7-HC-Chi-3’(TTG GGC CCT TGG TGG AGG CTG CAG AGA CAG TGA CCA G-3`)プライマーを用いてPCRを行った(図7のA)。その後、前記重鎖の信号配列と重鎖可変領域遺伝子を連結するために、5’-signal-EcoR1プライマーとECL-2B7-HC-Chi-3’プライマーを用いて組換えPCRを行った。これを介して重鎖可変領域と重鎖信号配列が連結された遺伝子を得、1%のアガロースゲルに展開させて確認し、DNA分離キット(FavorPreP GELTM PCR Purification Kit、Farvorgen、台湾)を用いて約450bpに該当するDNAを分離した(図7のA)。前記信号配列が連結された重鎖可変領域遺伝子をEcoRI及びApaIで処理した後、前記FavorPrep GELTM PCR Purification Kitを用いて分離した(図7のB)。このように得られた重鎖可変領域遺伝子を、ヒト抗体の重鎖不変領域(IgG1)遺伝子が含まれているpdCMV-dhfrベクターのEcoRI及びApaIの位置にT4 DNA連結酵素(T4 DNA ligase、NEB、米国)を用いてクローニングした(図8)。軽鎖遺伝子の場合にも同様に、信号配列を合成するためにpdCMV-dhfr-ch57ベクターを鋳型として、ch57-LC-whole 5’(5`-CTG CAA AGC TTC GGC ACG AGC A)プライマーとECL-2B7-S-L-3’(CAC AAT ATC TCC TTC AAC ACC AGA CAA CC-3`)プライマーを用いてPCRを行い、軽鎖可変領域遺伝子の増幅のためにECL-2B7-S-L-5’(5`-GTT GAA GGA GAT ATT GTG ATG ACC CAG TCT)プライマーとECL-2B7-LC-chi-3’(CCA CCG TAC GTT TGA TTT CCA GCT T-3`)プライマーを用いてPCRを行った(図7のA)。前記信号配列と軽鎖可変領域の連結のために、ch57-LC-whole 5’プライマーとECL-2B7-LC-chi-3’プライマーを用いて組換えPCRを行った後、1%のアガロースゲルに展開させて確認し、重鎖可変領域遺伝子と同一の方法で分離した(図7のA)。前記軽鎖可変領域遺伝子をHindIII及びBsiwIで処理して分離した後、ヒト抗体の軽鎖不変領域(Ck)遺伝子を含んで先に製作した重鎖遺伝子が挿入されたpdCMV-dhfr-chi2B7-HCベクターのHindIII及びBisWIの位置にクローニングすることにより(図7のC)、前記キメラ抗体を発現させることができるベクターを製造した(pdCMV-dhfr-chi2B7、図8)。前記ベクターを大腸菌DH5αにRbCl2方法で形質転換した後、約450bpの大きさを有した大腸菌を選抜した。この大腸菌を50μg/mlのアンピシリンが含有された5mlのLB培地で一晩中培養した後、プラスミドDNA分離のためのキット(DNA-spinTM Plasmid DNA purification kit、INTRON、韓国)を用いてプラスミドDNAを分離して塩基配列を確認した(Bionics、韓国)。その結果、前記形質転換体から分離されたcDNAの塩基配列は、前記ECL-2B7抗体の可変領域遺伝子と同一であり、ヒト抗体の重鎖及び軽鎖不変領域遺伝子と正しく連結されていることを確認した。
ヒト化抗体及びキメラ抗体の発現及び精製
前記実施例1、2を介して製造した本発明のヒト化抗体のベクターと、前記比較例のキメラ抗体ベクターから抗体タンパク質を発現させて精製した。
の培養皿を用いて1×107のHEK293T細胞(ヒト胚芽腎細胞株)を20mlのDMEM培地(Biowest、フランス)で培養した。培養された細胞に50μgの前記pdCMV-dhfr-chi2B7発現ベクターと75μlのポリエチレンイミン(polyethyleneimine、1mg/ml)を混ぜた後、トランスフェクション最適化培地500μlと混ぜて均一に細胞培養培地の上にふりかけた。翌日、上澄液を収集し、新しい培地を満たして細胞株から発現されて出たキメラ抗体を収集し、その上澄液をビーズ(Protein G agarose beads、Amicogen、韓国)がパッキングされているカラムに入れ、抗体が前記ビーズと結合することができるようにした。その後、PBS(pH8.0)でビーズを洗浄し、0.1Mのグリシン(pH2.8)10mlと1MのTris-HCl(pH9.0)を用いて抗体をビーズから溶出することでChi2B7キメラ抗体を精製し、SDS-PAGEとクマシブルー(Coomassie blue)染色法を介してこれを確認した(図9のA)。また、前記精製したキメラ抗体がヒト抗体の不変領域を有したものなのか否かを、ヤギの抗体(goat-α-hIgG-gamma chain-HRP、Invitrogen、米国、そして、goat-α-hIgG-kappa chain-HRP、Bethyl、米国)を2次抗体として用いてウェスタンブロッティングを介して検出した結果、前記キメラ抗体は、ヒト抗体の不変領域を含む抗体であることを確認することができた(図9のB)。
ELISAによるヒト化抗体のTM4SF4抗原結合能の比較
本発明のヒト化抗体、そしてキメラ抗体を用いて、間接ELISA(indirect
ELISA)を介しTM4SF4に対する結合能を確認した。
具体的に、前記ヒト化抗体は、前記実施例1、2を介して設計した重鎖可変領域変異種の4種と軽鎖可変領域変異種の3種を組み合わせて、Hz2B7-1.1、Hz2B7-1
.2、Hz2B7-1.3、Hz2B7-2.1、Hz2B7-3.1、Hz2B7-3.2、Hz2B7-3.3、Hz2B7-4.1、Hz2B7-4.2及びHz2B7-4.3の10種の形態に製造した。このために、96-ウェルプレートの各ウェルの底にコーティング緩衝溶液(100mM carbonate/bicarbonate coating buffer、pH9.6)で溶解させたTM4SF4-BSA(1μg/ml)又はBSA溶液(1μg/ml)100μlを加えて4℃で16時間以上吸着させた。その後、コーティングされた抗原を洗浄緩衝溶液(wash buffer、0.05% PBS-T、Tween-20)で3回洗浄し、各ウェルの底に抗原が吸着されていない部分にブロック緩衝溶液(blocking buffer、5% skim milk in wash buffer)200μlを加えて4℃で16時間以上反応させた後、再び洗浄緩衝溶液で3回洗浄した。その後、前記実験例1を介して精製させた前記10種の組み合わせのヒト化抗体とキメラ抗体をブロック緩衝溶液を用いて多様な濃度も希釈して準備した後、濃度別に各ウェルに100μlずつ入れて室温で2時間反応させた。再び3回洗浄した後、これを検出するための1mg/mlの抗体(α-human
IgG-Kappa chain-HRP、Bethyl、米国)をブロック緩衝溶液を用いて10,000倍に希釈し、各ウェルに100μlを加えて室温で1時間反応させた。反応が終わった後、洗浄緩衝溶液で3回洗浄し、基質溶液(OPD solution、30%のH2O2 4μl、100μlのOPD stock(40mg/ml)、phosphate citrate bufferで10mlに合わせる)を各ウェルに100μlずつ加えて室温で反応させた後、2.5MのH2SO4 50μlを加えて反応を終結させた。最後に、固体状に結合された酵素の活性を測定するために、ELISAリーダーを用いて490nmで吸光度を測定した(図10)。
SPR分析による抗-TM4SF4ヒト化単一クローン抗体敏感度の比較
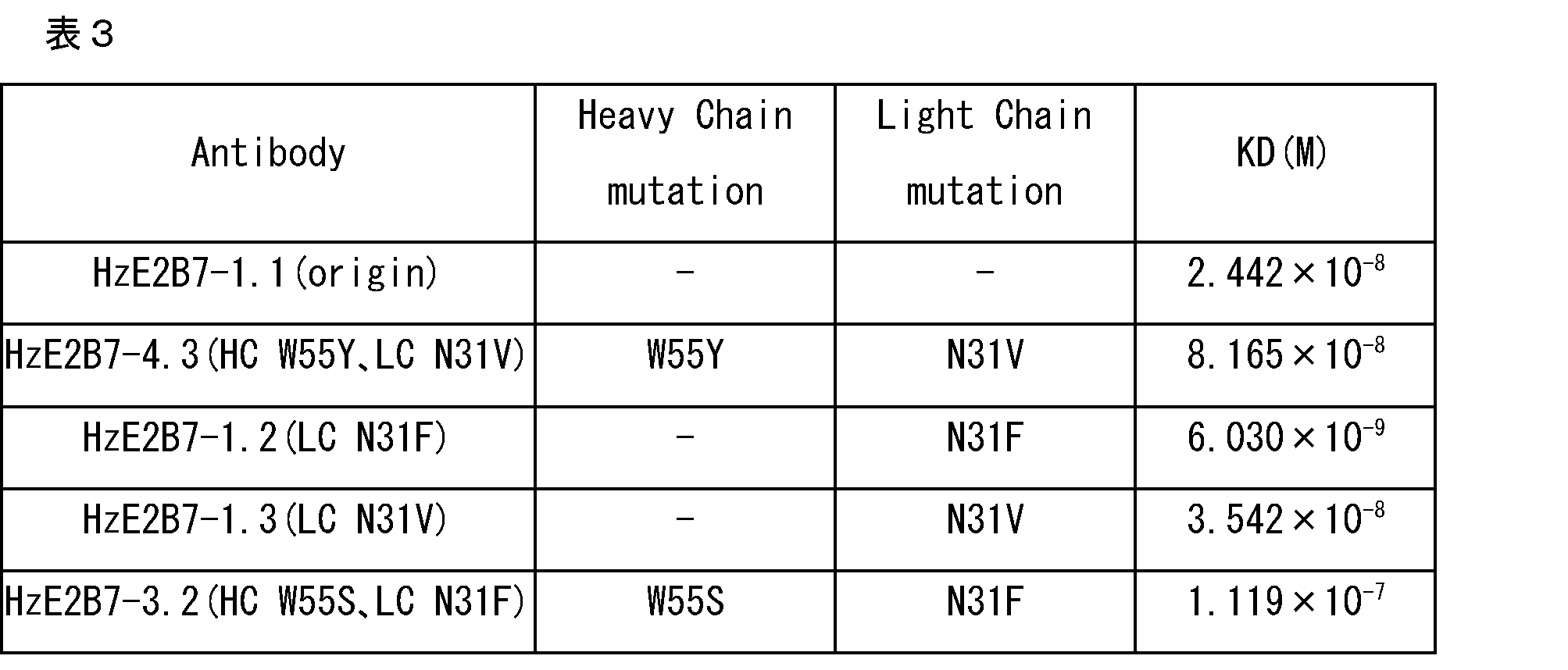
構築された抗-TM4SF4ヒト化単一クローン抗体のヒトTM4SF4-ペプチド(hTM4SF4 aa 126-140)抗原に対する結合能を比較するために表面プラズモン共鳴(Surface plasmon resonance、SPR)分析を行った。
な価値がより高い抗体であることが分かる。
FACSによるヒト化抗体の癌細胞結合能の比較
前記実験例2を介し、本発明のヒト化抗体がTM4SF4に対して高い親和度を有し特異的に結合することを確認したので、前記TM4SF4を過剰発現する特徴がある癌細胞に本発明のヒト化抗体を処理して結合可否を確認した。
IgG-FITC(2μg/ml)抗体を入れた。そして、ヒトアイソタイプIgG、キメラ抗体及びヒト化抗体が入っているグループにはFITC蛍光が結合されており、ヒトIgGに対して特異的なα-Human IgG-FITC(2μg/ml、Invitrogen)抗体を入れ、30分間4℃で反応させた。反応後、PBAで洗浄し、500μlのPBAで浮遊させた後、フローサイトメーター(FACS Calibur、BD、米国)を用いて前記抗体が抗原に対して特異性を有するのかを確認した。
本発明のヒト化抗体を高い生産性で生産することができる細胞株の製造
本発明のヒト化抗体を生産することができる細胞株を製造するために、CHO細胞(Chinese ovary hamster cells)の中でジヒドロ葉酸還元酵素(dihydrofolate reductase)を暗号化する遺伝子が欠損されているDG44細胞株を用いた。前記DG44細胞は、IMDM培地(Welgene、韓国)にH.T.(hypoxanthine-thymidine、sigma、Germany)及びDialyed FBS(Gibco、USA)を添加して培養し、トリプシン-EDTA(welgene、韓国)で細胞株を離した後、6ウェルプレートに1×106cells/wellだけ分株した。ここに、本発明のヒト化抗体の中でHz2B7-1.1及びHz2B7-1.2(LC N31F)を暗号化する発現ベクターを形
質転換(transfection)するために、15ugのPvuI制限酵素(Enzynomics、韓国)をそれぞれ処理して線形化させたpdCMV-dhfr-hz2B7-1.1及びpdCMV-dhfr-hz2B7-1.2をTOM培地(transfection optimized medium)によく混ぜて準備し、15μlのリポフェクタミン(lipofectamine)2000(Invitrogen、USA)をTOM培地で反応させた後、前記ベクターが含有された培地と混合して20分間反応させた。そして、反応された溶液を前記DG44細胞に滴下して形質転換を行った。
に増幅したHz2B7-1.2-4A12-0.08クローンの場合、#9クローンは約14.2μg/106cell/24hr、#20クローンは7.9μg/106cell/24hrの抗体生産量を示し、遺伝子が増幅されていないクローンと比べてそれぞれ約5.7倍、3.1倍増加した抗体生産量を示したので、最大5.7倍に抗体生産性が増加したことが分かる(図15)。
Claims (21)
- 配列番号1のアミノ酸配列を含むFR-H1、配列番号10のアミノ酸配列を含むCDR-H1、配列番号2又は配列番号3のアミノ酸配列を含むFR-H2、配列番号11、配列番号12及び配列番号13より構成される群から選択されるいずれか1つのアミノ酸配列を含むCDR-H2、配列番号4のアミノ酸配列を含むFR-H3、配列番号14のアミノ酸配列を含むCDR-H3及び配列番号5のアミノ酸配列を含むFR-H4を含む重鎖可変領域;及び
配列番号6のアミノ酸配列を含むFR-L1、配列番号15、配列番号16及び配列番号17より構成される群から選択されるいずれか1つのアミノ酸配列を含むCDR-L1、配列番号7のアミノ酸配列を含むFR-L2、配列番号18のアミノ酸配列を含むCDR-L2、配列番号8のアミノ酸配列を含むFR-L3、配列番号19のアミノ酸配列を含むCDR-L3及び配列番号9のアミノ酸配列を含むFR-L4を含む軽鎖可変領域;
を含み、
TM4SF4(TransMembrane 4 Superfamily Member 4)に特異的に結合する、ヒト化抗体又はこの抗原結合断片。 - 配列番号1のアミノ酸配列よりなるFR-H1、配列番号10のアミノ酸配列よりなるCDR-H1、配列番号2又は配列番号3のアミノ酸配列よりなるFR-H2、配列番号11、配列番号12及び配列番号13より構成される群から選択されるいずれか1つのアミノ酸配列よりなるCDR-H2、配列番号4のアミノ酸配列よりなるFR-H3、配列番号14のアミノ酸配列よりなるCDR-H3及び配列番号5のアミノ酸配列よりなるFR-H4を含む重鎖可変領域;及び
配列番号6のアミノ酸配列よりなるFR-L1、配列番号15、配列番号16及び配列番号17より構成される群から選択されるいずれか1つのアミノ酸配列よりなるCDR-L1、配列番号7のアミノ酸配列よりなるFR-L2、配列番号18のアミノ酸配列よりなるCDR-L2、配列番号8のアミノ酸配列よりなるFR-L3、配列番号19のアミノ酸配列よりなるCDR-L3及び配列番号9のアミノ酸配列よりなるFR-L4を含む
軽鎖可変領域;
を含む、請求項1に記載のヒト化抗体又はこの抗原結合断片。 - 前記重鎖可変領域は、配列番号10のアミノ酸配列を含むCDR-H1、配列番号11のアミノ酸配列を含むCDR-H2及び配列番号14のアミノ酸配列を含むCDR-H3を含み、
前記軽鎖可変領域は、配列番号16のアミノ酸配列を含むCDR-L1、配列番号18のアミノ酸配列を含むCDR-L2及び配列番号19のアミノ酸配列を含むCDR-L3を含むものである、請求項1に記載のヒト化抗体又はこの抗原結合断片。 - 前記重鎖可変領域は、配列番号20、配列番号21、配列番号22及び配列番号23よりなる群から選択されるいずれか1つのアミノ酸配列を含むものであり、
前記軽鎖可変領域は、配列番号24、配列番号25及び配列番号26よりなる群から選択されるいずれか1つのアミノ酸配列を含むものである、請求項1に記載のヒト化抗体又はこの抗原結合断片。 - 前記重鎖可変領域は、配列番号20、配列番号21、配列番号22及び配列番号23よりなる群から選択されるいずれか1つのアミノ酸配列よりなるものであり、
前記軽鎖可変領域は、配列番号24、配列番号25及び配列番号26よりなる群から選択されるいずれか1つのアミノ酸配列よりなるものである、請求項1に記載のヒト化抗体又はこの抗原結合断片。 - 前記ヒト化抗体は、配列番号27のアミノ酸配列を含む重鎖不変領域及び配列番号28のアミノ酸配列を含む軽鎖不変領域より構成される群から選択される少なくとも1つを含むものである、請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片。
- 前記抗原結合断片は、Fab、F(ab’)、F(ab’)2及びFvよりなる群から選択されるいずれか1つのものである、請求項1から5のいずれか1項に記載の抗体又はこの抗原結合断片。
- 前記抗体又はこの抗原結合断片は、平衡解離定数(KD)が2.4×10-8M以下のものである、請求項1から5のいずれか1項に記載の抗体又はこの抗原結合断片。
- 請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片を暗号化する塩基配列を含む、ポリヌクレオチド。
- 請求項9に記載のポリヌクレオチドを含む、発現ベクター。
- 請求項10に記載の発現ベクターを含む、宿主細胞。
- 請求項11に記載の宿主細胞を培養する段階を含む、TM4SF4(TransMembrane 4 Superfamily Member 4)に特異的に結合する、ヒト化抗体又はこの抗原結合断片を生産する方法。
- 請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片を含む、TM4SF4検出用組成物。
- 請求項13に記載のTM4SF4検出用組成物を含む、TM4SF4検出用キット。
- 請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片を、TM4SF4が含まれているものと予想される検出対象試料と接触させる段階を含む、TM4SF4を検出する方法。
- 請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片を含む、癌の予防又は治療用薬学的組成物。
- 前記癌の予防又は治療は、癌治療途中の癌化学耐性、癌治療後の癌化学耐性、癌再発及び癌転移よりなる群から選択される少なくとも1つを予防するか治療するものである、請求項16に記載の癌の予防又は治療用薬学的組成物。
- 前記癌は、肺癌、胃癌、卵巣癌、子宮頸部癌、乳癌、すい臓癌、大腸癌、結腸癌、食道癌、皮膚癌、甲状腺癌、腎臓癌、肝癌、頭頸部癌、膀胱癌、前立腺癌、血液癌、多発性骨髓腫、急性骨髓性白血病、悪性リンパ腫、胸腺癌、骨肉腫、繊維質腫瘍及び脳癌よりなる群から選択される少なくとも1つのものである、請求項16に記載の癌の予防又は治療用薬学的組成物。
- 請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片を含む、癌幹細胞成長抑制用組成物。
- 請求項1から5のいずれか1項に記載のヒト化抗体又はこの抗原結合断片を含む、放射線抗癌治療補助用組成物。
- 前記ヒト化抗体又はこの抗原結合断片は、癌幹細胞を含む癌細胞の放射線に対する敏感度を増進させるものである、請求項20に記載の放射線抗癌治療補助用組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2021-0079629 | 2021-06-18 | ||
| KR20210079629 | 2021-06-18 | ||
| PCT/KR2022/008570 WO2022265439A1 (ko) | 2021-06-18 | 2022-06-16 | 항-tm4sf4 인간화 항체 및 이의 용도 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2024526134A JP2024526134A (ja) | 2024-07-17 |
| JP7686802B2 true JP7686802B2 (ja) | 2025-06-02 |
Family
ID=84526696
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023578042A Active JP7686802B2 (ja) | 2021-06-18 | 2022-06-16 | 抗-tm4sf4ヒト化抗体及びこの用途 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20240288436A1 (ja) |
| EP (1) | EP4357363A4 (ja) |
| JP (1) | JP7686802B2 (ja) |
| KR (1) | KR20220169424A (ja) |
| CN (1) | CN117597363A (ja) |
| AU (1) | AU2022293217A1 (ja) |
| CA (1) | CA3221714A1 (ja) |
| MX (1) | MX2023015501A (ja) |
| WO (1) | WO2022265439A1 (ja) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007537197A (ja) | 2004-05-11 | 2007-12-20 | ガニュメート・ファーマシューティカルズ・アクチェンゲゼルシャフト | 腫瘍の診断と治療を目的とした表面会合抗原の同定 |
| JP2008283945A (ja) | 2007-05-21 | 2008-11-27 | Toru Tani | 肝癌検出用マーカー |
| JP2009530422A (ja) | 2006-03-21 | 2009-08-27 | ウェイバー,デヴィッド,ティー. | 抗体のヒト化方法及びそれによって得られるヒト化抗体 |
| US20110177098A1 (en) | 2008-07-15 | 2011-07-21 | Lori Sussel | Tm4sf4 and modulators thereof and methods for their use |
| JP2014528944A (ja) | 2011-09-26 | 2014-10-30 | コリア アトミック エナジー リサーチ インスティテュート | 非小細胞肺癌におけるtm4sf4の発現または活性を調節することによって癌細胞の放射線耐性ならびに増殖、転移および浸潤を低減させる方法 |
| WO2021112640A1 (ko) | 2019-12-06 | 2021-06-10 | 한국원자력연구원 | 항-tm4sf4 항체 및 이의 용도 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10647756B2 (en) * | 2015-05-18 | 2020-05-12 | Pfizer Inc. | Humanized antibodies |
-
2022
- 2022-06-16 JP JP2023578042A patent/JP7686802B2/ja active Active
- 2022-06-16 CN CN202280042376.1A patent/CN117597363A/zh active Pending
- 2022-06-16 WO PCT/KR2022/008570 patent/WO2022265439A1/ko not_active Ceased
- 2022-06-16 CA CA3221714A patent/CA3221714A1/en active Pending
- 2022-06-16 MX MX2023015501A patent/MX2023015501A/es unknown
- 2022-06-16 EP EP22825362.1A patent/EP4357363A4/en active Pending
- 2022-06-16 KR KR1020220073674A patent/KR20220169424A/ko not_active Ceased
- 2022-06-16 US US18/571,623 patent/US20240288436A1/en active Pending
- 2022-06-16 AU AU2022293217A patent/AU2022293217A1/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007537197A (ja) | 2004-05-11 | 2007-12-20 | ガニュメート・ファーマシューティカルズ・アクチェンゲゼルシャフト | 腫瘍の診断と治療を目的とした表面会合抗原の同定 |
| JP2009530422A (ja) | 2006-03-21 | 2009-08-27 | ウェイバー,デヴィッド,ティー. | 抗体のヒト化方法及びそれによって得られるヒト化抗体 |
| JP2008283945A (ja) | 2007-05-21 | 2008-11-27 | Toru Tani | 肝癌検出用マーカー |
| US20110177098A1 (en) | 2008-07-15 | 2011-07-21 | Lori Sussel | Tm4sf4 and modulators thereof and methods for their use |
| JP2014528944A (ja) | 2011-09-26 | 2014-10-30 | コリア アトミック エナジー リサーチ インスティテュート | 非小細胞肺癌におけるtm4sf4の発現または活性を調節することによって癌細胞の放射線耐性ならびに増殖、転移および浸潤を低減させる方法 |
| WO2021112640A1 (ko) | 2019-12-06 | 2021-06-10 | 한국원자력연구원 | 항-tm4sf4 항체 및 이의 용도 |
Non-Patent Citations (2)
| Title |
|---|
| Drug Delivery System,2013年,No.28-5,pp.412-423 |
| 日本結晶学会誌,1995年,Vol.37,pp.134-136 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4357363A4 (en) | 2024-12-18 |
| MX2023015501A (es) | 2024-01-22 |
| EP4357363A1 (en) | 2024-04-24 |
| US20240288436A1 (en) | 2024-08-29 |
| AU2022293217A1 (en) | 2023-12-14 |
| JP2024526134A (ja) | 2024-07-17 |
| CN117597363A (zh) | 2024-02-23 |
| CA3221714A1 (en) | 2022-12-22 |
| KR20220169424A (ko) | 2022-12-27 |
| WO2022265439A1 (ko) | 2022-12-22 |
| AU2022293217A9 (en) | 2024-01-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7386796B2 (ja) | 抗-her2抗体又はその抗原結合フラグメント、及びこれを含むキメラ抗原受容体 | |
| TW201542594A (zh) | 雙特異性her2抗體 | |
| JP2018504113A (ja) | 共通軽鎖を有する二重特異性抗体又は抗体混合物 | |
| KR20230113348A (ko) | 항 SIRPα 항체 및 이의 용도 | |
| CN110770254A (zh) | 新的抗c-MET抗体及其用途 | |
| US20240294622A1 (en) | Novel anti-gremlin1 antibodies | |
| US20220153863A1 (en) | Prame binding molecules and uses thereof | |
| CN111051513A (zh) | 抗cd147抗体 | |
| EP4071171B1 (en) | Anti-tm4sf4 antibody and use thereof | |
| JP7686802B2 (ja) | 抗-tm4sf4ヒト化抗体及びこの用途 | |
| US20250297013A1 (en) | Hla-g-specific antibody and use thereof | |
| US20240383988A1 (en) | Antibodies against egfr and their uses | |
| JP2025512671A (ja) | Her3結合タンパク質及びその使用 | |
| EP4635985A1 (en) | Anti-tm4sf4 humanized antibodies and use thereof | |
| US20250043012A1 (en) | Antibodies against egfr and their uses | |
| CN120058950A (zh) | 抗adam9的抗体及其用途 | |
| WO2024131849A1 (zh) | Cd38单克隆抗体及其应用 | |
| HK40016575A (en) | A novel anti-c-met antibody and use thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231218 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20250107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250407 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250422 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250521 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7686802 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |