JP7525762B2 - Il6rに結合する抗体及びその使用 - Google Patents
Il6rに結合する抗体及びその使用 Download PDFInfo
- Publication number
- JP7525762B2 JP7525762B2 JP2022569148A JP2022569148A JP7525762B2 JP 7525762 B2 JP7525762 B2 JP 7525762B2 JP 2022569148 A JP2022569148 A JP 2022569148A JP 2022569148 A JP2022569148 A JP 2022569148A JP 7525762 B2 JP7525762 B2 JP 7525762B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- amino acid
- antibody
- acid residues
- nos
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
- C07K14/7155—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons for interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Cell Biology (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本出願は、2020年5月18日に出願された米国仮特許出願第63/026,274号に対する優先権を主張するものである。
(a)表1中で上に列挙されるアミノ酸配列を含み得る重鎖可変領域;及び
(b)表1中で上に列挙されるアミノ酸配列を含み得る軽鎖可変領域、又は別の抗IL6R抗体のVLを含み得、ここで、抗体は、ヒトIL6Rに特異的に結合する。
(a)表1中で上に列挙される重鎖可変領域のCDR1、CDR2、及びCDR3領域;及び
(b)表1中で上に列挙される軽鎖可変領域のCDR1、CDR2、及びCDR3領域又は別の抗IL6R抗体のCDRを含み得、ここで、抗体は、ヒトIL6Rに特異的に結合する。
別の実施形態において、本開示の抗体は、1つ以上の保存的修飾だけ、本開示の抗IL6R抗体のものと異なるCDR1、CDR2及びCDR3配列の重鎖及び/又は軽鎖可変領域配列を含み得る。特定の保存的配列修飾が、抗原結合を除去せずに作製され得ることが、当該技術分野において理解される。例えば、Brummell et al.,(1993)Biochem 32:1180-8;de Wildt et al.,(1997)Prot.Eng.10:835-41;Komissarov et al.,(1997)J.Biol.Chem.272:26864-26870;Hall et al.,(1992)J.Immunol.149:1605-12;Kelley and O'Connell(1993)Biochem.32:6862-35;Adib-Conquy et al.,(1998)Int.Immunol.10:341-6及びBeers et al.,(2000)Clin.Can.Res.6:2835-43を参照されたい。
(a)重鎖可変領域CDR1配列は、上記の表1に列挙される配列、及び/又はその保存的修飾を含み得;及び/又は
(b)重鎖可変領域CDR2配列は、上記の表1に列挙される配列、及び/又はその保存的修飾を含み得;及び/又は
(c)重鎖可変領域CDR3配列は、上記の表1に列挙される配列、及び/又はその保存的修飾を含み得;及び/又は
(d)軽鎖可変領域CDR1、及び/又はCDR2、及び/又はCDR3配列は、上記の表1に列挙される配列;及び/又はその保存的修飾を含み得;
(e)抗体は、ヒトIL6Rに特異的に結合する。
[実施例]
[免疫化]
マウスを、E Harlow,D.Lane,Antibody:A Laboratory Manual,Cold Spring Harbor Laboratory Press,Cold Spring Harbor,N.Y.,1998に記載されている方法にしたがって免疫化した。組換えヒトIL6Rα-hisタンパク質(Acro biosystems、Cat#ILR-H4223)を、免疫原として使用し、社内調製ヒトIL6R-Fcタンパク質(配列番号43に記載されるアミノ酸配列)を、抗血清力価を決定するため、及び抗原特異的抗体を分泌するハイブリドーマをスクリーニングするために使用した。免疫化投与量は、一次免疫のために50μgのヒトIL6Rα-his/マウス/注射、及び追加免疫のために25μgのヒトIL6Rα-his/マウス/注射を含んでいた。免疫応答を増加させるために、完全フロイントアジュバント及び不完全フロイントアジュバント(Sigma,St.Louis,Mo.,USA)を、一次及び追加免疫のためにそれぞれ使用した。簡潔には、所望の量のアジュバントを、加圧滅菌された1.5mLの微小遠心分離管に移した。抗原を、0.25~1.0mg/mlの範囲の濃度を有するPBS又は生理食塩水中で調製した。次に、計算された量の抗原を、アジュバントとともに微小遠心分離管に加え、溶液を、2分間にわたって穏やかにボルテックスすることによって混合して、油中水型エマルジョンを生成した。次に、アジュバント-抗原混合物を、動物に注射するための適切なシリンジに吸い込ませた。合計で50又は25μgの抗原を、100~200μlの体積で注射した。各動物を免疫化し、次に、抗血清力価に応じて2~3回追加接種した。良好な力価を有する動物に、融合前に腹腔内注射によって最終追加接種を与えた。
マウス骨髄腫細胞株(SP2/0-Ag14、ATCC#CRL-1581)の細胞を培養して、融合直前に対数期段階に到達させた。免疫化マウスに由来する脾臓細胞を、E Harlow,D.Lane,Antibody:A Laboratory Manual,Cold Spring Harbor Laboratory Press,Cold Spring Harbor,N.Y.,1998に記載される方法にしたがって、滅菌的に調製し、骨髄腫細胞と融合させた。続いて、融合された「ハイブリッド細胞」を、DMEM/20% v/vのFCS/HAT培地中の96ウェル細胞プレート中に分配した。生存しているハイブリドーマコロニーが、融合の7~10日後に顕微鏡で観察された。2週間後、各ウェルからの上清を、(配列番号43として社内で調製された)ヒトIL6R-Fcタンパク質を用いて間接ELISA及び捕捉ELISAに供した。次に、ヒトIL6R-Fcに結合された抗体を分泌する陽性ハイブリドーマを選択し、24ウェルプレートに移した。これらのハイブリドーマを、IL6R-IL6結合をブロックするための活性についてさらに試験した。ヒトIL6Rに対する高特異性及び高いIL6-IL6Rブロッキング活性を示した抗体を産生するハイブリドーマクローンを、細胞株のクローン性を確実にするため、限界希釈によってサブクローニングし、次に、モノクローナル抗体を精製した。簡潔に述べると、プロテインAセファロースカラム(bestchrom(Shanghai)Biosciences製、Cat#AA0273)を、5~10カラム体積中でPBS緩衝液を用いて洗浄した。細胞上清を、カラムに通過させ、次に、タンパク質の吸光度がベースラインに達するまで、カラムを、PBS緩衝液を用いて洗浄した。カラムを、溶出緩衝液(0.1Mのグリシン-HCl、pH2.7)で溶離し、直ちに中和緩衝液(1MのTris-HCl、pH9.0)を含む1.5ml管に収集した。免疫グロブリンを含有する画分を、プールし、4℃で一晩、PBS中で透析した。続いて、精製されたモノクローナル抗体のインビトロ機能活性を、以下のように特性決定した。
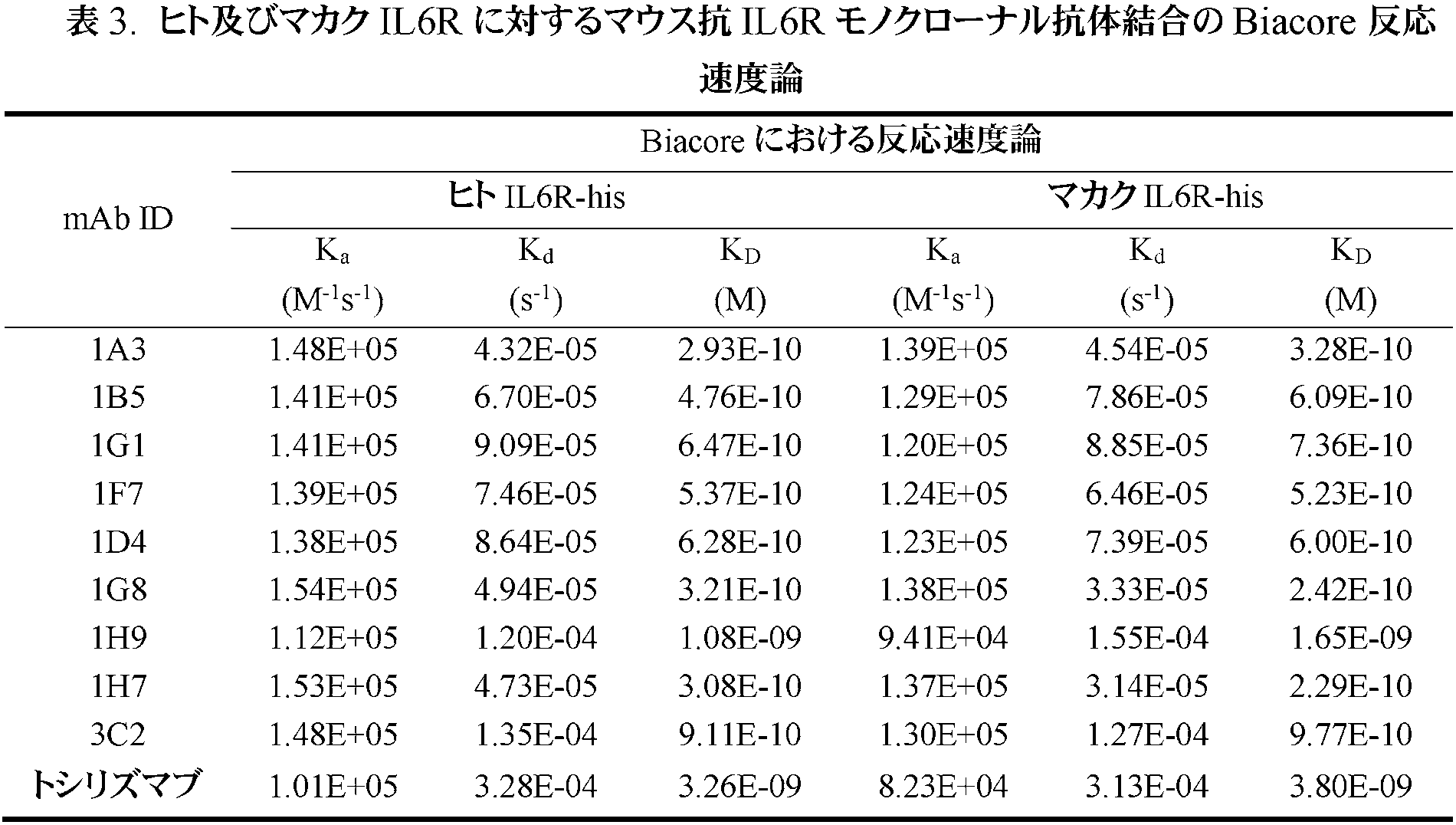
実施例1で生成された、精製抗IL6Rマウスモノクローナル抗体(mAb)を、Biacore T200システム(GE healthcare,Pittsburgh,PA,USA)によって、結合親和性及び結合速度について特性決定した。
マウス抗IL6R抗体を、それらの結合活性について、捕捉ELISA、間接ELISA及びフローサイトメトリー(FACS)によって試験した。
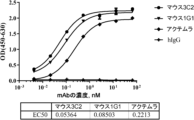
捕捉ELISAの場合、96ウェルマイクロプレートを、100μl/ウェルのPBS中の2μg/mlのAffiniPureヤギ抗マウスIgGのF(ab')2フラグメント特異的(Jackson ImmunoResearch Laboratories,Inc.、Cat#115-005-072)で被覆し、37℃で2時間インキュベートした。プレートを、洗浄緩衝液(PBS+0.05% v/vのTween(登録商標)-20、PBST)で1回洗浄し、次に、4℃で一晩にわたって、200μl/ウェルのブロッキングバッファー(PBST中5% w/vの無脂肪乳)でブロックした。プレートを4回洗浄し、100μl/ウェルの本開示の連続希釈されたマウス抗IL6R抗体、ベンチマーク及び陰性対照hIgG(静脈注射用のヒト免疫グロブリン(pH4)、Hualan Biological Engineering Inc.)、10000ng/mlから出発してPBST中2.5% w/vの無脂肪乳中の5倍希釈のそれぞれとともに、37℃で40分間にわたってインキュベートし、次に、再度4回洗浄した。捕捉抗IL6R抗体を含有するプレートを、ビオチン標識ヒトIL6R-Fcタンパク質(社内で調製、配列番号43、PBST中2.5% w/vの無脂肪乳中39.5ng/ml、100μl/ウェル)とともに、37℃で40分間にわたってインキュベートし、4回洗浄し、ストレプトアビジンコンジュゲートHRP(PBST中1:10000希釈、Jackson ImmunoResearch Laboratories,Inc.、Cat#016-030-084、100μl/ウェル)とともに、37℃で40分間にわたってインキュベートした。最後の洗浄の後、プレートを、100μl/ウェルのELISA基質TMB(InnoReagents、Cat#TMB-S-002)とともにインキュベートした。反応を、50μl/ウェルの1MのH2SO4で、室温で3~10分間で停止させ、各ウェルの吸光度を、TMBについて450nm及び基準波長として630nmの二波長モードを用いて、マイクロプレートリーダーで読み取った。次に、OD(450~630)値を、抗体濃度に対してプロットした。データを、Graphpad Prismソフトウェアを用いて分析し、EC50値を報告した。
抗IL6R抗体を、マカクIL6Rとのそれらの交差反応性について試験した。簡潔に述べると、96ウェルマイクロプレートを、37℃で2時間にわたって、炭酸塩/炭酸水素塩緩衝液(pH9.6)中の100μl/ウェルの2μg/mlのマカクIL6R-hisタンパク質(社内で調製、配列番号45に記載されるアミノ酸配列)で被覆した。ELISAプレートを、洗浄緩衝液(PBS+0.05% v/vのTween-20、PBST)で1回洗浄し、次に、37℃で2時間にわたって、200μl/ウェルのブロッキングバッファー(PBST中5% w/vの無脂肪乳)でブロックした。プレートを4回洗浄し、100μl/ウェルの、本開示の連続希釈された抗IL6R抗体又は対照(66.67nMから出発して、2.5% w/vの無脂肪乳でPBST中5倍連続希釈)とともにインキュベートし、37℃で40分間インキュベートした。ELISAプレートを、再度4回洗浄し、37℃で40分間にわたって、100μl/ウェルのペルオキシダーゼAffiniPureヤギ抗マウスIgGのFcγフラグメント特異的(PBST緩衝液中1:5000希釈、Jackson ImmunoResearch Laboratories,Inc.、Cat#115-035-071)とともにインキュベートした。最後の洗浄の後、プレートを、100μl/ウェルのTMB(InnoReagents)とともにインキュベートした。反応を、50μl/ウェルの1MのH2SO4で、室温で3~10分後に停止させ、各ウェルの吸光度を、TMBについて450nm及び基準波長として630nmの二波長モードを用いて、マイクロプレートリーダーで読み取った。次に、OD(450~630)値を、抗体濃度に対してプロットした。データを、Graphpad Prismソフトウェアを用いて分析し、EC50値を報告した。
細胞表面上に発現されたIL6Rに対するマウス抗IL6R抗体の結合活性を、フローサイトメトリー(FACS)によって試験した。簡潔に述べると、ヒト骨髄腫細胞U266(ATCC(登録商標)TIB-196(商標))を、細胞培養フラスコから収集し、2回洗浄し、2% v/vのウシ胎仔血清(FACS緩衝液)を含有するリン酸緩衝生理食塩水(PBS)中で再懸濁させた。96ウェルプレート中のウェル当たり2×105個のU266細胞を、氷上で40分間にわたって、様々な濃度で(FACS緩衝液中、3倍連続希釈で40nMから出発する)、100μlの抗IL6R抗体又は対照とともにインキュベートした。細胞を、FACS緩衝液で2回洗浄し、100μL/ウェルのR-フィコエリトリンAffiniPure F(ab')2フラグメントヤギ抗マウスIgG(H+L)(FACS緩衝液中1:1000希釈、Jackson ImmunoResearch Laboratories,Inc.、Cat#115-116-146)を加えた。暗所で、4℃で40分間にわたるインキュベーションの後、細胞を3回洗浄し、FACS緩衝液中で再懸濁させた。蛍光を、Becton Dickinson FACS Canto II-HTS機器を用いて測定した。データを、Graphpad Prismソフトウェアを用いて分析し、EC50値を報告した。
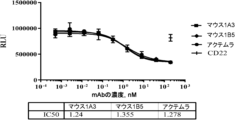
[4.1 リガンドブロッキングELISA]
IL6-IL6R結合をブロックする本開示の抗IL6R抗体の能力を、競合ELISAアッセイにおいて測定した。簡潔に述べると、ヒトIL6タンパク質(Sino biological Inc.、Cat#10395-HNAE)を、37℃で2時間にわたって、炭酸塩/重炭酸塩緩衝液(pH9.6)中2μg/mL、96ウェルマイクロプレート上、100μl/ウェルで被覆した。ELISAプレートを、洗浄緩衝液(PBS+0.05% v/vのTween-20、PBST)で1回洗浄し、次に、4℃で一晩にわたって、200μl/ウェルのブロッキングバッファー(PBST中5% w/vの無脂肪乳)でブロックした。
ヒトIL6Rタンパク質へのベンチマーク(トシリズマブ)結合をブロックする本開示の抗IL6R抗体の能力を、競合ELISAアッセイで測定した。簡潔に述べると、ベンチマークを、PBS中2μg/mLで、96ウェルマイクロプレート上で、100μl/ウェルで被覆し、37℃で2時間にわたってインキュベートした。ELISAプレートを、洗浄緩衝液(PBS+0.05% v/vのTween-20、PBST)で1回洗浄し、次に、4℃で一晩にわたって、200μl/ウェルのブロッキングバッファー(PBST中5% w/vの無脂肪乳)でブロックした。
本開示の全ての抗IL6R抗体を、IL6誘導性のTF-1細胞増殖に対する阻害効果について、さらに試験した。
抗IL6RマウスmAbの重鎖及び軽鎖可変領域をシーケンシングし、配列番号を表1に要約した。
マウス抗IL6R抗体1H7を、ヒト化し、さらに特性決定した。抗体のヒト化を、以下に詳細に記載される十分に確立されたCDRグラフト方法を用いて行った。
ヒト化抗体を含有する細胞上清を、振とうフラスコ中で6日後に収集し、修正を伴う上述されたプロトコルにしたがって、直接的にBIAcore試験に供した。具体的には、ヤギ抗ヒトIgG(GE healthcare、Cat#BR100839、Human Antibody Capture Kit)を、ヤギ抗マウスIgGの代わりに、CM5チップに共有結合し、CM5チップを、プロテインGチップの代わりに、トシリズマブに使用した。キメラ抗体及びトシリズマブを、10μg/mlの濃度で、HBS-EP+中で調製し、ヒト化抗体を含む細胞上清を10倍に希釈した。Ka、Kd及びKD値を決定し、以下の表5に要約した。
Claims (15)
- インターロイキン6受容体サブユニットα(IL6R)に結合することができる、単離モノクローナル抗体又はその抗原結合部分であって、
i)VH CDR1領域、VH CDR2領域及びVH CDR3領域を含む、重鎖可変領域と、
ii)VL CDR1領域、VL CDR2領域及びVL CDR3領域を含む軽鎖可変領域を含み、
前記VH CDR1領域、前記VH CDR2領域及び前記VH CDR3領域、前記VL CDR1領域、前記VL CDR2領域及び前記VL CDR3領域が、(1)配列番号1、4、11、15、18及び22のそれぞれ、(2)配列番号2、5、12、16、19及び22のそれぞれ、(3)配列番号2、6、13、15、20及び22のそれぞれ、(4)配列番号3、7、11、16、20及び22のそれぞれ、(5)配列番号2、8、13、16、20及び22のそれぞれ、(6)配列番号2、9、13、15、20及び22のそれぞれ、若しくは(7)配列番号2、10、14、17、21及び23のそれぞれに記載のアミノ酸配列を含む、
単離モノクローナル抗体又はその抗原結合部分。 - 前記重鎖可変領域が、配列番号24、25、26、27、28、29、30、31、32又は33に対する少なくとも90%同一性を有するアミノ酸配列を含み、
配列番号25の48番目、74番目、及び79番目のアミノ酸残基は、それぞれIle(I)、Lys(K)、及びAla(A)、それぞれMet(M)、Thr(T)、及びVal(V)、又はそれぞれIle(I)、Thr(T)、及びVal(V)であり、
配列番号27の67番目、70番目、及び72番目のアミノ酸残基は、それぞれLys(K)、Leu(L)、及びArg(R)、それぞれLys(K)、Met(M)、及びVal(V)、又はそれぞれArg(R)、Leu(L)、及びVal(V)であり、
配列番号32の73番目及び83番目のアミノ酸残基は、それぞれAsn(N)及びLeu(L)、又はそれぞれGlu(E)及びPhe(F)である、
請求項1に記載の単離モノクローナル抗体又はその抗原結合部分。 - 前記軽鎖可変領域が、配列番号34、35、36、37、38、39又は40に対する少なくとも90%同一性を有するアミノ酸配列を含み、
配列番号35の72番目及び79番目のアミノ酸残基は、それぞれTyr(Y)及びMet(M)、又はそれぞれPhe(F)及びLeu(L)であり、
配列番号39の50番目、62番目及び82番目のアミノ酸残基は、それぞれTyr(Y)、His(H)及びGlu(E)、又はそれぞれSer(S),Arg(R),Gly(G)である、
請求項1または2に記載の単離モノクローナル抗体又はその抗原結合部分。 - 前記重鎖可変領域及び前記軽鎖可変領域が、
(1)配列番号24及び34のそれぞれ、
(2)配列番号25の48番目、74番目及び79番目のアミノ酸残基がそれぞれIle(I)、Lys(K)、及びAla(A)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれTyr(Y)及びMet(M)である、配列番号25及び35のそれぞれ、
(3)配列番号26及び36のそれぞれ、
(4)配列番号27の67番目、70番目及び72番目のアミノ酸残基がそれぞれLys(K)、Leu(L)及びArg(R)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれTyr(Y)及びMet(M)である、配列番号27及び35のそれぞれ、
(5)配列番号27の67番目、70番目及び72番目のアミノ酸残基がそれぞれLys(K)、Met(M)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれTyr(Y)及びMet(M)である、配列番号27及び35のそれぞれ、
(6)配列番号25の48番目、74番目及び79番目のアミノ酸残基がそれぞれMet(M)、Thr(T)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれTyr(Y)及びMet(M)である、配列番号25及び35のそれぞれ、
(7)配列番号27の67番目、70番目及び72番目のアミノ酸残基がそれぞれArg(R)、Leu(L)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれTyr(Y)及びMet(M)である、配列番号27及び35のそれぞれ、
(8)配列番号25の48番目、74番目及び79番目のアミノ酸残基がそれぞれIle(I)、Thr(T)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれTyr(Y)及びMet(M)である、配列番号25及び35のそれぞれ、
(9)配列番号25の48番目、74番目及び79番目のアミノ酸残基がそれぞれIle(I)、Lys(K)及びAla(A)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれPhe(F)及びLeu(L)である、配列番号25及び35のそれぞれ、
(10)配列番号27の67番目、70番目及び72番目のアミノ酸残基がそれぞれLys(K)、Leu(L)及びArg(R)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれPhe(F)及びLeu(L)である、配列番号27及び35のそれぞれ、
(11)配列番号27の67番目、70番目及び72番目のアミノ酸残基がそれぞれLys(K)、Met(M)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれPhe(F)及びLeu(L)である、配列番号27及び35のそれぞれ、
(12)配列番号25の48番目、74番目及び79番目のアミノ酸残基がそれぞれMet(M)、Thr(T)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれPhe(F)及びLeu(L)である、配列番号25及び35のそれぞれ、
(13)配列番号27の67番目、70番目及び72番目のアミノ酸残基がそれぞれArg(R)、Leu(L)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれPhe(F)及びLeu(L)である、配列番号27及び35のそれぞれ、
(14)配列番号25の48番目、74番目及び79番目のアミノ酸残基がそれぞれIle(I)、Thr(T)及びVal(V)であり、配列番号35の72番目及び79番目のアミノ酸残基がそれぞれPhe(F)及びLeu(L)である、配列番号25及び35のそれぞれ、
(15)配列番号28及び37のそれぞれ、
(16)配列番号29及び38のそれぞれ、
(17)配列番号39の50番目、62番目及び82番目のアミノ酸残基がそれぞれTyr(Y)、His(H)及びGlu(E)である、配列番号30及び39のそれぞれ、
(18)配列番号39の50番目、62番目及び82番目のアミノ酸残基がそれぞれSer(S)、Arg(R)及びGly(G)である、配列番号31及び39のそれぞれ、
(19)配列番号32の73番目及び83番目のアミノ酸残基がそれぞれAsn(N)及びLeu(L)である、配列番号32及び38のそれぞれ、
(20)配列番号32の73番目及び83番目のアミノ酸残基がそれぞれ、Glu(E)及びPhe(F)である、配列番号32及び38のそれぞれ、又は
(21)配列番号33及び40のそれぞれ
に対する少なくとも90%同一性を有するアミノ酸配列を含む、請求項1から3のいずれか一項に記載の単離モノクローナル抗体又はその抗原結合部分。 - IgG1、IgG2又はIgG4アイソタイプである、請求項1から4のいずれか一項に記載の単離モノクローナル抗体又はその抗原結合部分。
- 前記重鎖可変領域に連結された、配列番号41の前記アミノ酸配列を有する重鎖定常領域、及び前記軽鎖可変領域に連結された、配列番号42の前記アミノ酸配列を有する軽鎖定常領域を含む、請求項1から4のいずれか一項に記載の単離モノクローナル抗体又はその抗原結合部分。
- マウス、キメラ又はヒト化抗体である、請求項1から6のいずれか一項に記載の単離モノクローナル抗体又はその抗原結合部分。
- 請求項1から7のいずれか一項に記載の単離モノクローナル抗体又はその抗原結合部分をコードするヌクレオチド。
- 請求項8に記載のヌクレオチドを含む発現ベクター。
- 請求項9に記載の発現ベクターを含む宿主細胞。
- 請求項1から7のいずれか一項に記載の単離モノクローナル抗体又はその抗原結合部分、請求項8に記載のヌクレオチド、請求項9に記載の発現ベクター、又は請求項10に記載の宿主細胞、及び薬学的に許容される担体を含む医薬組成物。
- 過剰なIL6/IL6Rシグナル伝達に関連する炎症性疾患を治療するための、請求項11に記載の医薬組成物。
- 前記炎症性疾患が、関節リウマチ、全身型及び多関節型若年性特発性関節炎、巨細胞性動脈炎、高安動脈炎、キャッスルマン病、サイトカイン放出症候群、シュニッツラー症候群、又は視神経脊髄炎である、請求項12に記載の医薬組成物。
- 過剰なIL6/IL6Rシグナル伝達に関連する癌を治療するための請求項11に記載の医薬組成物。
- 前記癌が、非小細胞肺癌、又はびまん性大細胞型B細胞リンパ腫である、請求項14に記載の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063026274P | 2020-05-18 | 2020-05-18 | |
| US63/026,274 | 2020-05-18 | ||
| PCT/CN2021/094107 WO2021233246A1 (en) | 2020-05-18 | 2021-05-17 | Antibodies binding il6r and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023526294A JP2023526294A (ja) | 2023-06-21 |
| JP7525762B2 true JP7525762B2 (ja) | 2024-07-31 |
Family
ID=78708123
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022569148A Active JP7525762B2 (ja) | 2020-05-18 | 2021-05-17 | Il6rに結合する抗体及びその使用 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20230167182A1 (ja) |
| EP (1) | EP4153626A4 (ja) |
| JP (1) | JP7525762B2 (ja) |
| KR (1) | KR102934248B1 (ja) |
| CN (1) | CN115667297B (ja) |
| WO (1) | WO2021233246A1 (ja) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016530495A (ja) | 2013-07-04 | 2016-09-29 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 血清サンプル中の抗薬物抗体を検出するための干渉抑制イムノアッセイ |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100249937B1 (ko) * | 1991-04-25 | 2000-04-01 | 나가야마 오사무 | 인간 인터루킨-6 수용체에 대한 재구성 인간 항체 |
| DK2374818T3 (da) * | 2006-06-02 | 2013-01-21 | Regeneron Pharma | Højaffinitetsantistoffer mod human IL-6-receptor |
| WO2008020079A1 (en) * | 2006-08-18 | 2008-02-21 | Ablynx N.V. | Amino acid sequences directed against il-6r and polypeptides comprising the same for the treatment of deseases and disorders associated with il-6-mediated signalling |
| MX2011000071A (es) * | 2008-07-02 | 2011-05-03 | Emergent Product Dev Seattle | Inmunoterapeuticos de interleucina-6 (il6). |
| RU2013144392A (ru) * | 2011-03-03 | 2015-04-10 | Апексиджен, Инк. | Антитела к рецептору il-6 и способы применения |
| US9017678B1 (en) * | 2014-07-15 | 2015-04-28 | Kymab Limited | Method of treating rheumatoid arthritis using antibody to IL6R |
| RU2656160C2 (ru) * | 2016-08-17 | 2018-05-31 | Закрытое Акционерное Общество "Биокад" | Антитело или его антигенсвязывающий фрагмент, способный связываться с рецептором интерлейкина-6 человека |
| TW201915023A (zh) | 2017-09-13 | 2019-04-16 | 大陸商江蘇恆瑞醫藥股份有限公司 | Il-6r抗體、其抗原結合片段及醫藥用途 |
| CN110483640B (zh) * | 2019-07-16 | 2020-05-01 | 北京汇智和源生物技术有限公司 | 白介素-6r的人源化单克隆抗体、其编码基因及应用 |
| CN110903393B (zh) * | 2019-12-17 | 2021-08-13 | 源道隆(苏州)医学科技有限公司 | 可结合IL6Rα的多肽及其应用 |
-
2021
- 2021-05-17 EP EP21808161.0A patent/EP4153626A4/en active Pending
- 2021-05-17 US US17/997,583 patent/US20230167182A1/en active Pending
- 2021-05-17 KR KR1020227043558A patent/KR102934248B1/ko active Active
- 2021-05-17 WO PCT/CN2021/094107 patent/WO2021233246A1/en not_active Ceased
- 2021-05-17 JP JP2022569148A patent/JP7525762B2/ja active Active
- 2021-05-17 CN CN202180035889.5A patent/CN115667297B/zh active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016530495A (ja) | 2013-07-04 | 2016-09-29 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 血清サンプル中の抗薬物抗体を検出するための干渉抑制イムノアッセイ |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023526294A (ja) | 2023-06-21 |
| CN115667297A (zh) | 2023-01-31 |
| CN115667297B (zh) | 2026-02-03 |
| KR20230009502A (ko) | 2023-01-17 |
| WO2021233246A1 (en) | 2021-11-25 |
| EP4153626A4 (en) | 2024-09-11 |
| EP4153626A1 (en) | 2023-03-29 |
| KR102934248B1 (ko) | 2026-03-04 |
| US20230167182A1 (en) | 2023-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7456075B2 (ja) | 抗体結合bcma及びその使用 | |
| JP7331298B2 (ja) | 抗体結合tslp及びその使用 | |
| JP7711079B2 (ja) | Il4rに結合する抗体とその使用 | |
| JP7827951B2 (ja) | 抗体結合Siglec15及びその使用 | |
| JP7730100B2 (ja) | Cd40に結合する抗体及びその使用 | |
| WO2023202672A1 (en) | Antibodies targeting sirp-alpha and uses thereof | |
| JP7525762B2 (ja) | Il6rに結合する抗体及びその使用 | |
| WO2021136323A1 (en) | Antibodies binding bcma and uses thereof | |
| JP7494413B2 (ja) | C5に結合する抗体及びその用途 | |
| WO2025045192A1 (en) | Antibodies binding btn3a1 and uses thereof | |
| WO2021115465A1 (en) | Antibodies binding rankl and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221116 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221116 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20231003 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231208 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240206 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240418 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240611 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240612 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7525762 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |