JP7267253B2 - Pivkaに対する新規結合剤およびアッセイ - Google Patents
Pivkaに対する新規結合剤およびアッセイ Download PDFInfo
- Publication number
- JP7267253B2 JP7267253B2 JP2020501157A JP2020501157A JP7267253B2 JP 7267253 B2 JP7267253 B2 JP 7267253B2 JP 2020501157 A JP2020501157 A JP 2020501157A JP 2020501157 A JP2020501157 A JP 2020501157A JP 7267253 B2 JP7267253 B2 JP 7267253B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- pivka
- amino acid
- specific binding
- binding agent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/36—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against blood coagulation factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
- C07K16/3076—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells against structure-related tumour-associated moieties
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57438—Specifically defined cancers of liver, pancreas or kidney
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/86—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving blood coagulating time or factors, or their receptors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/745—Assays involving non-enzymic blood coagulation factors
Description
プレプロトロンビン(配列番号5)は、細胞内で合成され、最初の43個のN末端アミノ酸(シグナルペプチドおよびプロペプチド配列→配列番号6)の切断、およびプロトロンビンポリペプチドの6、7、12、14、16、19、20、25、26および31位のグルタミン酸残基のγ-カルボキシル化によって(「成熟」)プロトロンビンにプロセスされる。循環において経時的に、プロトロンビンも種々の分解産物に分解される。低カルボキシル化の検出に関して特に興味深いのは、少なくともいわゆるGLAドメイン(配列番号7)を含むプロトロンビン切断(分解)産物である。主に関連するプロトロンビン切断産物は、それぞれいわゆるF1/F2-断片(配列番号8)およびいわゆるF1-断片(配列番号9)である。
一実施形態では、特異的結合剤は、アプタマーとしても公知の特異的結合核酸である。
一実施形態では、本明細書で開示される特異的結合剤は、モノクローナル抗体である。
抗体の全体構造は、当技術分野において周知であり、ジスルフィド結合によって繋がれた2本の重鎖および2本の軽鎖から構成される。重鎖および軽鎖は、それぞれ1つの定常ドメインおよび1つの可変ドメインからなる。抗原への結合特異性は、抗体を形成する軽鎖および重鎖の可変ドメインによってもたらされる。より具体的には、それらの特異性を決定し、特異的リガンドと接触する抗体の部分は、相補性決定領域(CDR)と称される。CDRは、分子の最も可変性の部分であり、これらの分子の多様性に寄与する。各可変ドメインには3つのCDR領域、CDR1、CDR2およびCDR3があり、4つのフレームワーク領域(FW)に埋め込まれる。本明細書において使用される場合、CDR-HC(またはCDR(HC))は可変重鎖のCDR領域を示し、CDR-LC(またはCDR(LC))は可変軽鎖のCDR領域に関する。同様に、FW-HC(またはFW(HC))は可変重鎖のフレームワーク領域を示し、FW-LC(またはFW(LC))は可変軽鎖のフレームワーク領域に関する。
(i)軽鎖可変ドメイン中の配列番号10のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号12のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号13のアミノ酸配列を含むCDR1、配列番号14のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;
(ii)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号19のアミノ酸配列を含むCDR2および配列番号20のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号21のアミノ酸配列を含むCDR1、配列番号22のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;
(iii)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号20のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号21のアミノ酸配列を含むCDR1、配列番号25のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;または
(iv)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号28のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号29のアミノ酸配列を含むCDR1、配列番号25のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3。
(i)軽鎖可変ドメイン中の配列番号10のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号12のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号13のアミノ酸配列を含むCDR1、配列番号14のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;
(ii)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号19のアミノ酸配列を含むCDR2および配列番号20のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号21のアミノ酸配列を含むCDR1、配列番号22のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;
(iii)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2およびに配列番号20のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号21のアミノ酸配列を含むCDR1、配列番号25のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;または
(iv)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号28のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号29のアミノ酸配列を含むCDR1、配列番号25のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3。
重鎖および軽鎖の両方の軽鎖可変領域/ドメイン/配列は、抗体の特異性を決定するCDRおよび「CDRを適切な位置に保つ」さらなる一般的フレームワーク領域をそれぞれ含む。
FW(LC)1-CDR(LC)1-FW(LC)2-CDR(LC)2-FW(LC)3-CDR(LC)3-FW(LC)4(式I)
に表されるフレームワーク領域(FW)およびCDRからなる。
FW(HC)1-CDR(HC)1-FW(HC)2-CDR(HC)2-FW(HC)3-CDR(HC)3-FW(HC)4(式II)
に表されるFWおよびCDRからなる。
さらに本開示は、配列番号1の合成ペプチドに結合し、配列番号2の合成ペプチドと比較して配列番号1のペプチドに対して少なくとも10倍の結合優先性を有し、配列番号1のペプチドと比較して配列番号3の合成ペプチドに少なくとも同様に結合することを特徴とする、PIVKA-IIに特異的に結合する抗体に関し、ここで前記抗体は、
(i)配列番号10のCDR1、配列番号11のCDR2および配列番号12のCDR3を含む配列番号16の軽鎖可変配列ならびに配列番号13のCDR1、配列番号14のCDR2および配列番号15のCDR3を含む配列番号17の重鎖可変配列;
(ii)配列番号18のCDR1、配列番号19のCDR2および配列番号20のCDR3を含む配列番号23の軽鎖可変配列ならびに配列番号21のCDR1、配列番号22のCDR2および配列番号15のCDR3を含む配列番号24の重鎖可変配列;
(iii)配列番号18のCDR1、配列番号11のCDR2および配列番号20のCDR3を含む配列番号26の軽鎖可変配列ならびに配列番号21のCDR1、配列番号25のCDR2および配列番号15のCDR3を含む配列番号27の重鎖可変配列;または
(iv)配列番号18のCDR1、配列番号11のCDR2および配列番号28のCDR3を含む配列番号30の軽鎖可変配列ならびに配列番号29のCDR1、配列番号25のCDR2および配列番号15のCDR3を含む配列番号31の重鎖可変配列
を含むことをさらに特徴とし、
ここで、それぞれのFWは、上の所与の可変鎖配列に含有されるとおりであるか、または上の可変鎖配列を介して開示されるFW配列と少なくとも85%同一であるその変種であり、ここでそれぞれのCDRは、上に示されるとおりであるか、または最大1個のアミノ酸置換において異なっている。
フレームワーク領域に関して、ある特定の程度の変動も本明細書において想定される、すなわち個々のFWは、具体的に述べられるアミノ酸配列またはそれに少なくとも85%同一のアミノ酸配列を含み得る、またはそれからなり得る。さらなる一実施形態では、同一性は、少なくとも90%である。またさらなる実施形態では、同一性は少なくとも95%である。
本発明により使用される場合、用語「欠失」は、具体的に述べられるアミノ酸配列から1つまたは複数のアミノ酸を失うことを指す。
(i)配列番号10のCDR1、配列番号11のCDR2および配列番号12のCDR3を含む配列番号16の軽鎖可変配列ならびに配列番号13のCDR1、配列番号14のCDR2および配列番号15のCDR3を含む配列番号17の重鎖可変配列;
(ii)配列番号18のCDR1、配列番号19のCDR2および配列番号20のCDR3を含む配列番号23の軽鎖可変配列ならびに配列番号21のCDR1、配列番号22のCDR2および配列番号15のCDR3を含む配列番号24の重鎖可変配列;
(iii)配列番号18のCDR1、配列番号11のCDR2および配列番号20のCDR3を含む配列番号26の軽鎖可変配列ならびに配列番号21のCDR1、配列番号25のCDR2および配列番号15のCDR3を含む配列番号27の重鎖可変配列;または
(iv)配列番号18のCDR1、配列番号11のCDR2および配列番号28のCDR3を含む配列番号30の軽鎖可変配列ならびに配列番号29のCDR1、配列番号25のCDR2および配列番号15のCDR3を含む配列番号31の重鎖可変配列。
(i)配列番号16のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる軽鎖可変ドメイン、および配列番号17のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる重鎖可変ドメイン;
(ii)配列番号23のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる軽鎖可変ドメイン、および配列番号24のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる重鎖可変ドメイン;
(iii)配列番号26のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる軽鎖可変ドメイン、および配列番号27のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる重鎖可変ドメイン;または
(iv)配列番号30のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる軽鎖可変ドメイン、および配列番号31のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列からなる重鎖可変ドメイン
を含む。
一実施形態では、PIVKA-IIに特異的に結合する抗体は、配列番号1の合成ペプチドに結合し、配列番号2の合成ペプチドと比較して配列番号1のペプチドに対して少なくとも10倍の結合優先性を有し、配列番号1のペプチドと比較して配列番号3の合成ペプチドに少なくとも同様に結合し、
(i)軽鎖可変ドメインとして配列番号16のアミノ酸配列および重鎖可変ドメインとして配列番号17のアミノ酸配列(すなわち、添付の実施例において7A10と呼ばれるモノクローナル抗体の可変鎖領域に対応する)を含む;
(ii)軽鎖可変ドメインとして配列番号23のアミノ酸配列および重鎖可変ドメインとして配列番号24のアミノ酸配列(すなわち、添付の実施例において4E8と呼ばれるモノクローナル抗体の可変鎖領域に対応する)を含む;
(iii)軽鎖可変ドメインとして配列番号26のアミノ酸配列および重鎖可変ドメインとして配列番号27のアミノ酸配列(すなわち、添付の実施例において9A6と呼ばれるモノクローナル抗体の可変鎖領域に対応する)を含む;または
(iv)軽鎖可変ドメインとして配列番号30のアミノ酸配列および重鎖可変ドメインとして配列番号31のアミノ酸配列(すなわち、添付の実施例において13H7と呼ばれる可変鎖領域に対応する)を含むことを特徴とする。
本発明の核酸分子は、例えば標準的化学合成方法および/もしくは組換え法によって合成され得る、または例えば化学合成と組換え法を組み合わせることによって半合成的に産生され得る。コード配列の転写制御エレメントへの、および/または他のアミノ酸コード配列へのライゲーションは、制限消化、ライゲーションおよび分子クローニングなどの確立された方法を使用して実行され得る。
(i)配列番号10のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号11のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号12のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む軽鎖可変領域;
(ii)配列番号18のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号19のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号20のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む軽鎖可変領域;
(iii)配列番号18のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号11のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号20のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む軽鎖可変領域;
(iv)配列番号18のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号11のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号28のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む軽鎖可変領域;
(v)配列番号16のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列;
(vi)配列番号23のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列;
(vii)配列番号26のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列;または
(viii)配列番号30のアミノ酸配列からなる軽鎖可変ドメインと少なくとも85%同一であるアミノ酸配列
をコードする。
(i)配列番号13のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号14のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号15のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む重鎖可変領域;
(ii)配列番号21のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号22のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号15のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む重鎖可変領域;
(iii)配列番号21のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号25のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号15のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む重鎖可変領域;
(iv)配列番号29のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR1、配列番号25のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR2、および配列番号15のアミノ酸配列または最大1個のアミノ酸置換において異なっているその変種を含むCDR3を含む重鎖可変領域;
(v)配列番号17のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列;
(vi)配列番号24のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列;
(vii)配列番号27のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列;または
(viii)配列番号31のアミノ酸配列からなる重鎖可変ドメインと少なくとも85%同一であるアミノ酸配列
をコードする。
好適な複製開始点の追加的例として、例えば全長ColE1、切断型ColEI、SV40ウイルス性およびM13複製開始点が挙げられる一方で、好適なプロモーターの追加的例として、限定されることなく、サイトメガロウイルス(CMV)プロモーター、SV40プロモーター、RSVプロモーター(ラウス肉腫(Rous sarcome)ウイルス)、lacZプロモーター、テトラサイクリンプロモーター/オペレーター(tetp/o)、ニワトリβ-アクチンプロモーター、CAG-プロモーター(ニワトリβ-アクチンプロモーターとサイトメガロウイルス最初期エンハンサーとの組合せ)、gai10プロモーター、ヒト伸長因子1α-プロモーター、AOX1プロモーター、GAL1プロモーターCaM-キナーゼプロモーター、lac、trpもしくはtacプロモーター、T7もしくはT5プロモーター、lacUV5プロモーター、Autographa californica多核多角体ウイルス(multiple nuclear polyhedrosis virus)(AcMNPV)多角体プロモーターまたは哺乳動物および他の動物細胞におけるグロビンイントロンが挙げられる。エンハンサーの一例は、例えばSV40エンハンサーである。転写終結を確実にする制御エレメントについての非限定的な追加的例として、SV40-ポリA部位、tk-ポリA部位、rho-非依存性lppターミネーターまたはAcMNPV多角体ポリアデニル化シグナルが挙げられる。選択可能マーカーのさらなる非限定的例として、メトトレキサートへの耐性を付与するdhfr(Reiss、Plant Physiol.(Life Sci.Adv.)13(1994)、143~149)、アミノグリコシド ネオマイシン、カナマイシンおよびパロマイシン(paromycin)に対する耐性を付与するnpt (Herrera-Estrella、EMBO J.2(1983)、987~995)ならびに、ハイグロマイシンへの耐性を付与するhygro(Marsh、Gene 32(1984)、481~485)が挙げられる。追加的な選択可能遺伝子は、記載されており、すなわちtrpB、細胞がトリプトファンの代わりにインドールを利用できるようにする;hisD、細胞がヒスチジンの代わりにヒスチノール(histinol)を利用できるようにする(Hartman、Proc.Natl.Acad.Sci.USA 85(1988)、8047);マンノース-6-リン酸イソメラーゼ、細胞がマンノースを利用できるようにする(WO94/20627)、およびODC(オルニチンデカルボキシラーゼ)、オルニチンデカルボキシラーゼ阻害剤、2-(ジフルオロメチル)-DL-オルニチン、DFMOに対する耐性を付与する(McConlogue、1987、In:Current Communications in Molecular Biology、Cold Spring Harbor Laboratory ed.)またはAspergillus terreus由来のデアミナーゼ、ブラストサイジンSに対する耐性を付与する(Tamura、Biosci.Biotechnol.Biochem.59(1995)、2336~2338)。
本発明のベクター、具体的にはベクターの種類または制御配列に関して、本明細書において上で提供されるすべての定義および具体的に例示される実施形態を準用する。この第2の種類のベクターは、少なくとも2つの核酸分子、すなわち1つは軽鎖可変ドメインをコードし1つは重鎖可変ドメインをコードする2つの核酸分子を含むベクターに関する。上の組合せから明らかであるとおり、軽鎖可変ドメインと重鎖可変ドメインとは、本発明の機能性抗PIVKA-II抗体の発現が可能であるようにベクターにおいて組み合わされる。この第2の種類のベクターは、本明細書において「本発明の組合せベクター」とも称される。
(i)本発明の組合せベクター;または
(ii)本発明の第1の核酸分子、すなわち本発明による軽鎖可変領域をコードする核酸分子を含む本発明の個別のベクターおよび本発明の第2の核酸分子、すなわち本発明の重鎖可変領域をコードする核酸分子を含む本発明の個別のベクターであって、これら2つのベクターが上に定義される合致する軽鎖および重鎖可変領域をコードする核酸分子を含む、ベクター
を含む宿主細胞または非ヒト宿主にさらに関する。
さらに、本発明は、配列番号1の合成ペプチドに結合し、配列番号2の合成ペプチドと比較して配列番号1のペプチドに対して少なくとも10倍の結合優先性を有し、配列番号1のペプチドと比較して配列番号3の合成ペプチドに少なくとも同様に結合することを特徴とする、PIVKA-IIに特異的に結合する抗体であって、本発明の方法によって得ることができるまたは得られる、抗体に関する。
(i)本発明の抗体、
(ii)本発明の核酸分子、
(iii)本発明のベクター、
(iv)本発明の宿主細胞、および/または
(v)本発明の方法によって産生された抗体
の少なくとも1つを含む組成物にさらに関する。
一実施形態では本開示は、a)試料を、配列番号1の合成ペプチドに結合し、配列番号2の合成ペプチドと比較して配列番号1のペプチドに対して少なくとも10倍の結合優先性を有し、配列番号1のペプチドと比較して配列番号3の合成ペプチドに少なくとも同様に結合することを特徴とする、PIVKA-IIに結合する特異的結合剤と;特異的結合剤-PIVKA-II複合体の形成のために十分な時間および条件下で接触させるステップ;およびb)特異的結合剤-PIVKA-II複合体の存在を検出するステップであって、特異的結合剤-PIVKA-II複合体の存在が試料中のPIVKA-IIの存在を示す、ステップを含む試料中のPIVKA-IIを検出する方法に関する。
用語「試料」または「目的の試料」または「検査試料」は、本明細書において互換的に用いられる。試料は、in vitro試料であり、in vitroで分析され、身体に戻されない。試料の例として、これだけに限らないが血液、血清、血漿、滑膜液、尿、唾液およびリンパ液などの液体試料または、組織抽出物、軟骨、骨、滑膜および結合組織などの固形試料が挙げられる。一実施形態では試料は、血液、血清、血漿、滑膜液および尿から選択される。一実施形態では試料は、血液、血清および血漿から選択される。一実施形態では試料は、血清または血漿である。
(a)蛍光色素
蛍光色素は、例えば、Briggsら、”Synthesis of Functionalized Fluorescent Dyes and Their Coupling to Amines and Amino Acids,” J.Chem.Soc.、Perkin-Trans.1(1997)1051~1058)によって記載されている。
発光色素または標識は、化学発光および電気化学発光色素にさらに細分類され得る。
化学発光(chemiluminogenic)標識のさまざまなクラスとして、ルミノール、アクリジニウム化合物、セレンテラジンおよび類似物、ジオキセタン、ペルオキシオキサリック酸(peroxyoxalic acid)およびそれらの誘導体に基づく系が挙げられる。免疫診断手順のために主にアクリジニウムに基づく標識が使用される(詳細な概説は、Dodeigne C.ら、Talanta 51(2000)415~439に示されている)。
モノクローナル抗PIVKA-II抗体の生成における使用のためのペプチド免疫原の合成
1.1免疫原においておよびスクリーニング試薬において使用されるペプチドのための一般的合成方法
ペプチドを例えばProtein Technologies,Incからのマルチプルペプチド合成機でフルオレニルメチルオキシカルボニル(Fmoc)固相ペプチド合成によって合成した。この合成では、合成の各ステップにおいて各アミノ酸誘導体の4当量を使用した。アミノ酸誘導体を1当量の1-ヒドロキシ-7-アザベンゾトリアゾールを含有するジメチルホルムアミドに溶解した。ペプチドをTentagel(登録商標)レジン(Rapp Polymere GmbH、Tubingen)上で合成した。カップリング反応を、レジン負荷量と比較して4当量のHATU(1-[Bis(ジメチルアミノ)メチレン]-1H-1,2,3-トリアゾロ[4,5-b]ピリジニウム3-オキシドヘキサフルオロホスフェート)および8当量のN,N-ジイソプロピルエチルアミンを含む、反応媒体としてのジメチルホルムアミド中で5分間実行した。Fmoc基をジメチルホルムアミド中の20%ピペリジンを使用して各合成ステップ後8分間以内に切断した。合成レジンからのペプチドの遊離および酸不安定性保護基の切断を3時間以内に室温で、トリフルオロ酢酸、トリイソプロピルシランおよび水(38:1:1)を含有するカクテルを用いて達成した。次に反応溶液を、ペプチドを沈殿させるための冷却ジイソプロピルエーテルと混合した。沈殿物をろ過し、冷却ジイソプロピルエーテルを用いて再度洗浄し、少量の酢酸水溶液に溶解し、凍結乾燥させた。得られた粗物質を0.1%トリフルオロ酢酸を含有するアセトニトリル/水の勾配を使用して調製用RP-HPLCによって精製した。精製された物質の同一性をイオンスプレー質量分析によって調べた。
プレプロトロンビン(配列番号5)のアミノ酸51から73を含み、但し、53位のリシンがアルギニンによって置換され、βAla-Ahx-βAla-βAlaのN末端伸長がある、ペプチドβAla-Ahx-βAla-βAla-VRRGNLERECVEETCSYEEAFEA-NH2(配列番号32)を合成した。
ESI-MSexp:[M+3H]3+=1015.6Da
このペプチドのジスルフィド酸化を以下のとおり実施した。CLEAR-OX(商標)レジン(130mg、26μmol)をジクロロメタン(DCM)中で30分間膨潤させ、次にジメチルホルムアミド(DMF)、メタノールおよびアセトニトリルを用いて連続的に洗浄した。還元ペプチド(16mg、8.5μmol)を脱気したアンモニウムアセテート緩衝液(0.1M;pH7.8)とアセトニトリルとの混合物(1:1、2.5mL)に溶解し、レジンに加え、穏やかに4時間撹拌した。レジンを50%アセトニトリル水溶液を用いて洗浄し、ろ液を凍結乾燥した。
次のステップは、ジエチルスクアレート(スクアレート=3-エトキシ-3-シクロブテン-1,2-ジオン)のN末端コンジュゲーションであった。エタノールおよび水(1:1)中のペプチド(9mg、3μmol)の溶液に3,4-ジエトキシ-3-シクロブテン-1,2-ジオン(1.2当量)を加えた。溶液を炭酸ナトリウムの添加によってpH8.0に保ち、一晩撹拌し、次に乾燥のために蒸発させた。
次に、ペプチド-KLHコンジュゲートを合成した。ホウ酸緩衝液(10mL、0.1M、pH9.0)中KLH(35mg)の溶液にスクアラミド含有ペプチド(9mg、3μmol)を加えた。反応物を一晩、室温でインキュベートし、リン酸緩衝液(0.1M、pH7.0)に対して透析し、35.3mgペプチド-KLHコンジュゲートを得た。
プレプロトロンビン(配列番号5)のアミノ酸55から70およびβAla-Ahx-βAla-βAlaのN末端伸長を含んで、ペプチドβAla-Ahx-βAla-βAla-NLERECVEETCSYEEA-NH2(配列番号33)を合成した。
ESI-MSexp:[M+2H]2+=1115.5Da
このペプチドのジスルフィド酸化を以下のとおり実施した。CLEAR-OX(商標)レジン(230mg、46μmol)をDCM中で30分間膨潤させ、次にDMF、メタノールおよびアセトニトリルを用いて連続的に洗浄した。還元ペプチド(34mg、15.3μmol)を脱気したアンモニウムアセテート緩衝液(0.1M;pH7.8)とアセトニトリルとの混合物(1:1、5mL)に溶解し、レジンに加え、穏やかに4時間撹拌した。レジンを50%アセトニトリル水溶液を用いて洗浄し、ろ液を凍結乾燥した。
ESI-MSexp:[M+2H]2+=1114.5Da
次のステップは、ジエチルスクアレートのN末端コンジュゲーションであった。エタノールおよび水(1:1)中のペプチド(34mg、15.3μmol)の溶液に3,4-ジエトキシ-3-シクロブテン-1,2-ジオン(1.5当量)を加えた。溶液を炭酸ナトリウムの添加によってpH8.0に保ち、一晩撹拌し、次に乾燥のために蒸発させた。
ESI-MSexp:[M+2H]2+=1176.6Da
次にペプチド-KLHコンジュゲートを合成した。ホウ酸緩衝液(15mL、0.1M、pH9.0)中KLH(50mg)の溶液にスクアラミド含有ペプチド(27.2mg、12.2μmol)を加えた。反応物を一晩、室温でインキュベートし、リン酸緩衝液(0.1M、pH7.0)に対して透析し、49.5mgペプチド-KLHコンジュゲートを得た。
モノクローナル抗PIVKA-II抗体の生成
2.1 PIVKA-IIに対する抗体の生成のためのウサギの免疫処置
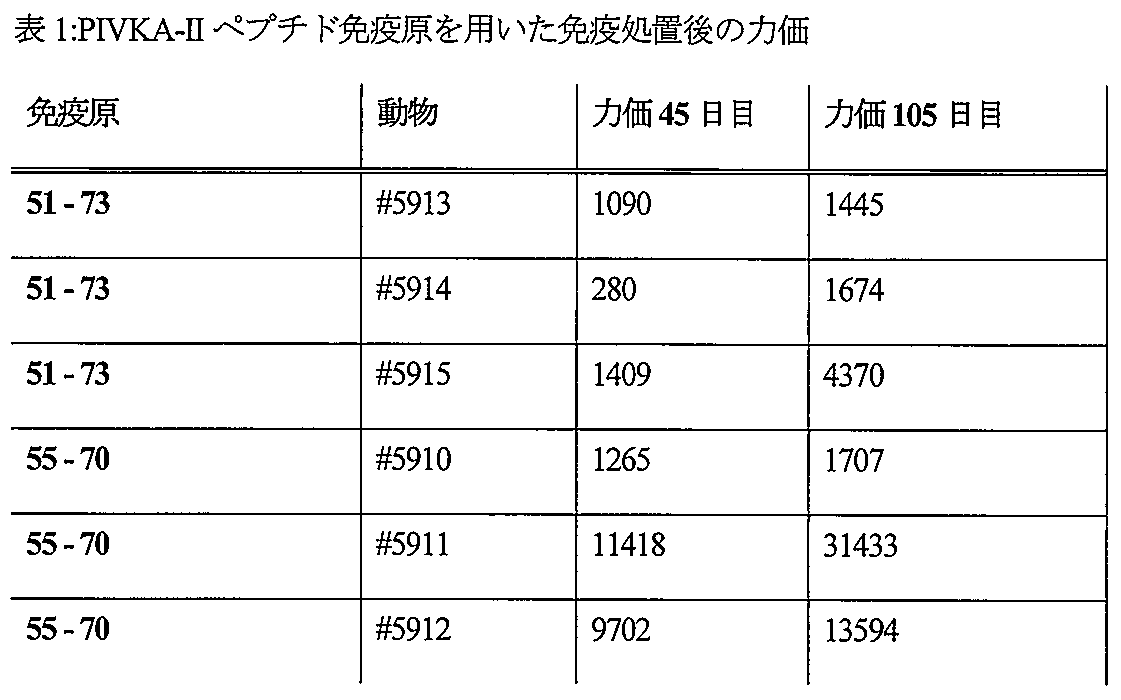
本明細書において本発明者らは、PIVKA-IIのN末端領域内のさまざまなエピトープに結合する能力を有する抗体の開発を記載する。かかる抗体の生成のために、12~16週齢NZWウサギをPIVKA-IIのN末端領域にわたる種々のペプチドを用いて免疫処置した。ペプチドの免疫原性を増強するために、実施例1に記載のとおり、それらを担体タンパク質としてのKLHにカップルした。免疫処置のために、プレプロトロンビンのそれぞれAA51~73および55~70を網羅するペプチドを選択した。すべてのウサギを反復免疫処置に供した。1ヵ月目は、動物を毎週免疫処置した。2ヵ月目からは、動物を1ヵ月に1回免疫処置した。1回目の免疫処置のために500μgKLH-カップルペプチドを1mL 140mM NaClに溶解し、1mlフロイント完全アジュバント(CFA)に乳化した。続くすべての免疫処置についてはCFAをフロイント不完全アジュバント(IFA)によって置き換えた。動物の力価を免疫処置の開始後45日目および105日目にそれぞれ評価した。
免疫処置した動物の力価を決定するために、血清滴定を配列番号1のC末端ビオチン化ペプチド(=NLERECVEETCSYEEA-E(ビオチン-PEG)-NH2、ジスルフィドとしてC/Cを含む)を使用して実施した。ペプチドを例えばProtein Technologies, Incからのマルチプルペプチド合成機でフルオレニルメチルオキシカルボニル(Fmoc)固相ペプチド合成によって合成した。このために各アミノ酸誘導体の4当量を使用した。アミノ酸誘導体を1当量の1-ヒドロキシ-7-アザベンゾトリアゾールを含有するジメチルホルムアミドに溶解した。ペプチドをTentagel Rレジン上で合成した。カップリング反応を、レジン負荷量と比較して4当量のHATUおよび8当量のN,N-ジイソプロピルエチルアミンを含む、反応媒体としてのジメチルホルムアミド中で5分間実行した。Fmoc基をジメチルホルムアミド中の20%ピペリジンを使用して各合成ステップ後8分間以内に切断した。合成レジンからのペプチドの遊離および酸不安定性保護基の切断を3時間以内に室温で、トリフルオロ酢酸、トリイソプロピルシランおよび水(38:1:1)を含有するカクテルを用いて達成した。次に反応溶液を、ペプチドを沈殿させるための冷却ジイソプロピルエーテルと混合した。沈殿をろ過し、冷却ジイソプロピルエーテルを用いて再度洗浄し、少量の酢酸水溶液に溶解し、凍結乾燥させた。得られた粗物質を0.1%トリフルオロ酢酸を含有するアセトニトリル/水の勾配を使用して調製用RP-HPLCによって精製した。精製された物質の同一性をイオンスプレー質量分析によって調べた。
略号:DMF=ジメチルホルムアミド;DCM=ジクロロメタン;E(ビオチン-PEG)=Nδ-(N-ビオチニル-3-(2-(2-(3-アミノプロピルオキシ)-エトキシ)-エトキシプロピル)-L-グルタミン;-NH2=C末端カルボキサミド;
ESI-MScalc:M+=2459.7Da;ESI-MSexp:[M+2H]2+=1231.0Da
ジスルフィド酸化
CLEAR-OX(商標)レジン(80mg、16μmol)をDCM中で30分間膨潤させ、次にDMF、メタノールおよびアセトニトリルを用いて連続的に洗浄した。還元ペプチド(10.4mg、4.2μmol)を脱気したアンモニウムアセテート緩衝液(0.1M;pH7.8)とアセトニトリルとの混合物(1:1、1.5mL)に溶解し、レジンに加え、穏やかに2時間撹拌した。レジンを水を用いて洗浄し、ろ液を凍結乾燥した。
上のビオチン化スクリーニングペプチドを96ウエルストレプトアビジンコートマイクロタイタープレートの表面に固定した。固定化のために、ビオチン化ペプチド(100μl)をマイクロタイタープレートのウエルで30分間、100ng/mlの濃度でインキュベートした。各ウサギの少量の血清(動物あたり2~3ml)を免疫処置キャンペーンの開始後45日目および105日目にそれぞれ回収した。各ウサギからの血清を1%BSAを含むPBSに希釈し、希釈物をプレートに加えた。血清を1:300、1:900、1:2700、1:8100、1:24300、1:72900、1:218700および1:656100の希釈でそれぞれ検査した。ELISA検査のために種々の希釈での100μlの血清を、各ペプチドを用いて上に記載のとおりコートした96ウエルプレートのウエルに加えた。血清を30分間、室温でインキュベートした。結合抗体をHRP-標識F(ab‘)2ヤギ抗ウサギFcγ(Dianova)および基質としてのABTS(Roche)を用いて検出した。分析した動物の力価は希釈曲線の50%シグナル減少に設定した。
PIVKA-IIに結合する抗体の開発では、Seeberら、(2014)、PLoS One.2014 Feb4;9(2)に記載されるB細胞クローニングを使用した。抗原反応性B細胞の濃縮のために、免疫原に相同性の配列を有するビオチン化スクリーニングペプチドそれぞれをストレプトアビジンコート磁気ビーズ(Miltenyi)に固定した。ビーズのコーティングのために、ペプチドを250ng/mlの濃度で使用した。その後、免疫処置した動物の末梢血液単核細胞(PBMC)プールを調製し、ペプチドコートビーズと共に1時間インキュベートした。抗原反応性B細胞の濃縮のために、MACSカラム(Miltenyi)を使用した。B細胞選別およびインキュベーションをSeeberら、(2014)、PLoS One.2014 Feb4;9(2)に記載のとおり行った。いわゆるHit-ELISAのために、スクリーニングペプチドそれぞれをストレプトアビジンコート96ウエルプレート(Greiner Bio-One)の表面に固定化した。ビオチン化ペプチドをプレート表面に100ng/mlの濃度で固定化した。それにより100μlのペプチド溶液をプレート上で30分間、室温でインキュベートした。洗浄後、バックグラウンドシグナルを低減するためにプレートを、100μlの5%BSAを用いて30分間、室温でブロックした。プレートを再度洗浄し、30μlのウサギB細胞培養物を96ウエルプレートに移し、1時間、室温でインキュベートした。スクリーニングペプチドに結合した抗体の検出のために、HRP-標識F(ab‘)2ヤギ抗ウサギFcγ(Dianova)およびABTS(Roche)を基質として加えた。それらそれぞれのスクリーニングペプチドに結合したクローンを続く分子クローニングのためにSeeberら、(2014)、PLoS One.2014 Feb 4;9(2)に記載のとおり選択した。
ヒトプロトロンビンは、Haemochrom Diagnostica (Essen、Germany)から得た。プロトロンビンのγ-カルボキシグルタミン酸残基を、Bajaj,S.P.ら、(1982)、JBC 1982、Vol.257、No.7、3726~3731の方法に従って熱で脱炭酸させた。ビオチン化プロトロンビンおよびビオチン化脱炭酸(decarboylated)プロトロンビンを以下のとおり生成した:プロトロンビン変種を100mM KPO4/100mM KCl、pH8.0に対して透析し、続いてpHをpH8.4に調整し、それぞれのプロトロンビン変種をビオチン-DDS(ビオチノイル-アミノ-3,6-ジオキサオクタノイル-アミノカルボニル-ヘプタン酸-N-ヒドロキシサクシニミドエステル(EP0632810 B1))を化学量論1:2.75(mol PT/mol ビオチン-NHS-エステル)で使用してビオチン化した。反応完了後、ビオチン化プロトロンビン変種をSuperdex200HR 10/30カラム(GE Healthcare Life Sciences)でのサイズ排除クロマトグラフィーによって精製した。
最初に、培養物上清中の(試料量20μL)ウサギ-IgGの濃度を標準ウサギIgGサンドイッチECL-イムノアッセイを使用して決定した。このアッセイでは、いずれもアッセイ緩衝液(アッセイ緩衝液は、40mM NaPO4、150mM NaCl、5mM EDTA、0.1%(w/v)ポリドカノール、2.0%(w/v)ウシ血漿アルブミンを含み、pH7.5を有する)中の、1μg/mLビオチン化IgGヒツジ抗ウサギFcγ(75μL)および1μg/mLルテニル化ヒツジ抗ウサギFcγ(70μl)をストレプトアビジンコート磁気ビーズ(=Elecsys(登録商標)ビーズ)(35μL;0.7mg/mL)と混合し、形成されたサンドイッチをElecsys 2010(Roche Diagnostics、Germany)自動化イムノアナライザーで測定する。ここで使用されるストレプトアビジンコート磁気ビーズ(Elecsys(登録商標)ビーズ)は、Roche(Roche Diagnostics GmbH、Germany)によって販売されるElecsys(登録商標)試薬容器に含まれるストレプトアビジンコート磁気ビーズと同じである。
抗体結合へのカルボキシル化の影響
PIVKA-IIにおける規定のグルタミン酸残基のガンマカルボキシル化の影響に関する、選択されたクローンのエピトープ-特異度の詳細な分析のために一連のビオチン化ペプチドを使用した(表2):
50μLのルテニル化(ruthenylated)抗PIVKA-II抗体(アッセイ緩衝液中300ng/mL。実施例2.4を参照されたい)を第1のステップでビオチン化ペプチド(アッセイ緩衝液中2.5ng/mL)50μLおよびアッセイ緩衝液70μLと反応させ、37℃、9分間インキュベートした。ストレプトアビジンコート常磁性Elecsys(登録商標)ビーズ(0.7mg/mL;実施例2.4を参照されたい)30μLの添加および第2のインキュベーションステップ(37℃、9分間)後、反応混合物を、微小粒子が測定電極の表面に磁気的に捕捉される測定セルに吸引した。未結合物質をProCellシステム緩衝液(Roche Diagnostics GmbH、Germany)を用いて除去する。次いで電極への電圧の印加は、光電子増倍管によって測定される光の電気化学発光に基づく発光を誘導する。
PIVKA-IIの測定のためのサンドイッチアッセイ
4.1 抗体の多量産生および精製
HEK-細胞の1L トランスフェクション培養上清のpHを2M酢酸を用いてpH4.75に調整し、溶液を20分間、室温で撹拌した。濁った溶液を≧20000xg、>20分間の遠心分離によって透明化した。続いて溶液のpHを2M K3PO4の添加によってpH7.5に再調整した。ウサギIgGをMabSelect SuRe Protein A mediaを使用する親和性クロマトグラフィーによって精製した:10mL MabSelect SuRe(商標)Protein Aカラム(GE Healthcare Life Sciences)をPBS(25mM KPO4、150mM KCl、pH7.5)を用いて平衡化し、次に、透明培養上清をカラムに流速5~20CV/時でポンプで注入し、PBSを用いる第1の洗浄、130mM KPO4/15mM クエン酸Na pH6.5を用いる第2の洗浄および0,14M KPO4、15mMクエン酸、0,1M硫酸アンモニウム、pH5.0を使用する最終溶出が続いた。IgG含有画分をプールし、プールのpHをpH7.5~8.0に2M K3PO4を使用して再調整した。最後に溶液を50mM KPO4、150mM KCl、pH7.5に対して透析した。
IgG(100mM KPO4/150mM KCl pH8.4中4.5mg/mL)の溶液1mLに、ビオチン-DDS(ビオチノイル-アミノ-3,6-ジオキサオクタニル-アミノカルボニル-ヘプタン酸-N-ヒドロキシサクシニミドエステル(EP 0632810 B1);DMSO中1.4mg/ml)の50μL溶液を加えた(すなわち、IgG 1molあたり3molビオチン-NHS-エステルの化学量論)。30分間、室温で撹拌した後、10mMリシンの添加によって誘導体化を停止した。pHを飽和KH2PO4を用いてpH7.5に調整し、溶液を50mM KPO4/150mM KCl pH7.4に対して透析した。凝集物の除去のために、適切な画分をSuperdex 200 HR 10/30カラム(GE Healthcare Life Sciences)上でのサイズ排除クロマトグラフィーから回収した。
IgG(100mM KPO4/150mM KCl pH8.4中4.5mg/mL)の溶液1mLに、ルテネート(3-)、ビス(2,2’-ビピリジン-κN1,κN1’)[N-[4-(4’-メチル[2,2’-ビピリジン]-4-イル-κN1,κN1’)-1-オキソブチル]-β-アラニル-L-α-グルタミル-L-α-グルタミル-N6-[8-[(2,5-ジオキソ-1-ピロリジニル)オキシ]-1,8-ジオキソオクチル]-L-リジネート(3-)]-、(OC-6-33)-(9CI)(BPRu-UEEK-DSS;CAS406218-59-5;DMSO中4.3mg/ml)の溶液50μLを加えた(すなわち1molのIgGあたり4.0molルテニウム-NHS-エステルの化学量論)。30分間、室温で撹拌した後、10mMリシンの添加によって誘導体化を停止した。pHを飽和KH2PO4を用いてpH7.0に調整し、反応混合物を50mM K-PO4/0.15M KCl/2%ショ糖、pH7.0に対して透析した。凝集物の除去のために、適切な画分をSuperdex 200 HR 10/30カラム(GE Healthcare Life Sciences)上でのサイズ排除クロマトグラフィーから回収した。
PIVKA-IIのN末端への抗体の生成
PIVKA-IIのN末端へのモノクローナル抗体も生成した。簡潔にはペプチドANTFLEEVRKGNLERE-βAla-Ahx-βAla-Cys-NH2(配列番号34)を、プレプロトロンビンのアミノ酸44から59(配列番号5)および-βAla-Ahx-βAla-Cys-NH2からなるN末端リンカーを含んで、合成した。このリンカーは、アミノ酸誘導体βAla=ベーターアラニンおよびAhx=6-アミノヘキサン酸をそれぞれ含んだ。
ESI-MSexp:[M+2H]2+=1131.8Da
リン酸緩衝液(45mL、20mM、pH7.2)中のキーホールリンペットヘモシアニン(KLH)(150mg)の溶液に3-(マレイミド)プロピオン酸N-ヒドロキシサクシニミドエステル(55mg、1.5mLジメチルスルホキシド(DMSO)中に溶解207μmol)を加えた。反応混合物を5時間、室温でインキュベートし、次にリン酸緩衝液(0.1M、pH7.05)に対して透析した。N末端システインを含むペプチド(配列番号34)(6.8mg、3μmol)をDMSOに溶解し、0.1M EDTAを含有するマレイミド活性化KLH(36.7mg)の溶液に加えた。溶液を5時間、室温で撹拌し、次にリン酸緩衝液(0.1M、pH7.05)に対して透析し、28mg KLH-ペプチドコンジュゲートを得た。
実施例6
Elecsysサンドイッチアッセイの一般的記載
免疫学的サンドイッチアッセイの検査原理を図1に示す。アッセイのために必要な総インキュベーション時間は、18分間である。
新たに開発されたPIVKA-II Elecsys(登録商標)アッセイの測定範囲は、0~5000ng/mlである。
肝細胞癌(HCC)の早期検出におけるPIVKA-II Elecsysアッセイの応用
7.1 分析試料
PIVKA-IIレベルを前向き多施設試料回収で患者および対照から回収した血清において検討した。
患者:
・ 肝細胞癌(HCC)(n=309)、次を含む
・ BCLC(バルセロナ臨床肝臓がん)ステージ0(n=10)、BCLC A(n=116)、BCLC B(n=77)、BCLC C(n=82)、BCLC D:(n=12);ステージ分類を有さない患者(n=12)
・ 他の患者CCC(=胆管細胞癌)およびHCC/CCC混合(n=21)、
対照:
対照対象から、慢性B型肝炎感染(HBV)患者(n=226)、慢性C型肝炎感染(HCV)患者(n=52)、肝硬変+HBV(n=173)、肝硬変+HCV(n=136)、肝硬変混合(n=88)、その他(n=67)を含んで合計742試料を得た。対照対象の別の群は、疑わしいがさらには明らかにされなかった症例(n=12)を含む。
試料は、以下の施設で回収された:(1)タイ:Songklanagarind Hospital Hat Yai;Srinagarind Hospital Khon Kaen; Siriraj Hospital Bangkok;Maharaj Nakorn Hospital Chiang Mai;(2)中国:Prince of Wales Hospital、Hong Kong;(3)ドイツ:NCT Heidelberg;(4)スペイン:Hospital Vall d‘Hebron Barcelona
7.1に記載の血清試料(n=1084)をPIVKA-II ElecsysアッセイおよびWAKO DCPアッセイ(WAKO Chemicals GmbH、Fuggerstr.12、D-41 468 Neuss、Germany)によって分析した。
Roche PIVKA-IIおよびWAKO DCPアッセイに関する臨床感度を90%特異度で算出した。並行して、Roche PIVKA-IIおよびWAKO DCPアッセイに関する臨床特異度を90%感度で算出した。独立した評価をすべてのステージのHCC(n=309)対すべての対照について、および初期ステージHCC(BCLC 0およびA、n=126)対すべての対照について実施した。加えて、曲線下面積(AUC)を両アッセイおよび評価方法について算出した。
Elecsys PIVKA-IIアッセイは、すべてのHCCおよび初期ステージHCC群の両方についてそれぞれ対照に対して算出されたAUCのわずかな増加も示す。高感度領域(60~95%)における受信者動作曲線(ROC)の詳細な分析は、WAKO DCPに対するElecsys PIVKA-IIの優れた特異度をすべてのHCCステージ(図3)および初期HCCステージ(図4)それぞれについて確認している。
既存のPIVKA-IIアッセイにおける擬陽性率が、いまだ著しいことから(Leeら、Korean J.Clin.Pathol.1997;17(3):395~404、Taketaら、Acta Med.Okayama 2002;56(6):317~320)ならびに初期ステージのHCCの検出における感度および特異度が後期HCCについてほど良好でない(Limら、Scand.J.Gastroenterol.2016;51(3):344~53)ことので、PIVKA-II検出方法の改善は、臨床的判断において重要性が高い。本明細書において開示のとおり、PIVKA-IIのγ-カルボキシル化アミノ酸19および20付近にそれぞれ独自の結合特性を有する抗体の使用は、この新たに開発されたPIVKA-IIアッセイの特異度の改善を、特に高感度領域においてもたらす。すべてのHCC患者の検出およびさらにHCCの初期ステージ(BCLC 0~A)の検出の両方についてもこれはあてはまる。
Claims (14)
- 配列番号1の合成ペプチドに結合し、配列番号2の合成ペプチドと比較して配列番号1のペプチドに対して少なくとも10倍の結合優先性を有し、配列番号1のペプチドと比較して配列番号3の合成ペプチドに少なくとも同様に結合することを特徴とする、PIVKA-IIに結合する特異的結合剤であって、
前記特異的結合剤がモノクローナル抗体である、前記特異的結合剤。 - 配列番号1の合成ペプチドに結合し、配列番号2の合成ペプチドと比較して配列番号1のペプチドに対して少なくとも15倍の結合優先性を有し、配列番号1のペプチドと比較して配列番号3の合成ペプチドに少なくとも同様に結合することを特徴とする、PIVKA-IIに結合する特異的結合剤であって、
前記特異的結合剤がモノクローナル抗体である、前記特異的結合剤。 - 配列番号4のペプチドと比較して配列番号1のペプチドに結合優先性を有することをさらに特徴とする、請求項1または2に記載の特異的結合剤。
- CDRが、以下のアミノ酸配列を含む:
(i)軽鎖可変ドメイン中の配列番号10のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号12のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号13のアミノ酸配列を含むCDR1、配列番号14のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;
(ii)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号19のアミノ酸配列を含むCDR2および配列番号20のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号21のアミノ酸配列を含むCDR1、配列番号22のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;
(iii)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号20のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号21のアミノ酸配列を含むCDR1、配列番号25のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3;または
(iv)軽鎖可変ドメイン中の配列番号18のアミノ酸配列を含むCDR1、配列番号11のアミノ酸配列を含むCDR2および配列番号28のアミノ酸配列を含むCDR3、ならびに重鎖可変ドメイン中の配列番号29のアミノ酸配列を含むCDR1、配列番号25のアミノ酸配列を含むCDR2および配列番号15のアミノ酸配列を含むCDR3
ことをさらに特徴とするモノクローナル抗体である、請求項1~3のいずれか一項に記載の特異的結合剤。 - a)試料を請求項1から4のいずれかに記載のPIVKA-IIへの特異的結合剤と、特異的結合剤-PIVKA-II複合体の形成のために十分な時間および条件下で接触させるステップ;および
b)特異的結合剤-PIVKA-II複合体の存在を検出するステップであって、特異的結合剤-PIVKA-II複合体の存在が試料中のPIVKA-IIの存在を示す、ステップ
を含む、試料中のPIVKA-IIを検出する方法。 - a)試料を請求項1から4のいずれかに記載のPIVKA-IIへの第1の特異的結合剤およびPIVKA-IIへの第2の特異的結合剤と、第1の特異的結合剤-PIVKA-II-第2の特異的結合剤複合体を形成するために十分な時間および条件下で接触させるステップであって、第2の特異的結合剤が検出可能に標識化されている、ステップ;および
b)(a)において形成された複合体を測定することにより、試料中のPIVKA-IIを検出するステップ
を含む、試料中のPIVKA-IIを検出する方法。 - a)試料を請求項1から4のいずれかに記載のPIVKA-IIへの第1の特異的結合剤と、第1の特異的結合剤-PIVKA-II複合体の形成のために十分な時間および条件下で接触させるステップ;
b)PIVKA-IIへの第2の特異的結合剤を第1の特異的結合剤-PIVKA-II複合体に、第1の特異的結合剤-PIVKA-II-第2の特異的結合剤複合体を形成するために十分な時間および条件下で加えておくステップであって、第2の特異的結合剤が検出可能に標識化されている、ステップ;および
c)(b)において形成された複合体を測定することにより、試料中のPIVKA-IIを検出するステップ
を含む、試料中のPIVKA-IIを検出する方法。 - 第2の特異的結合剤がポリクローナルまたはモノクローナル抗体である、請求項6または7に記載の方法。
- 第2の特異的結合剤が結合するPIVKA-II上のエピトープがF1/F2内に含まれる、請求項6から8のいずれかに記載の方法。
- 第2の特異的結合剤が結合するPIVKA-II上のエピトープがF1内に含まれる、請求項6から9のいずれかに記載の方法。
- 第2の特異的結合剤が結合するPIVKA-II上のエピトープがPIVKA-IIのGla-ドメイン内に含まれる、請求項6から10のいずれかに記載の方法。
- a)患者から得られた試料を請求項1から4のいずれかに記載のPIVKA-IIへの第1の特異的結合剤およびPIVKA-IIへの第2の特異的結合剤と、第1の特異的結合剤-PIVKA-II-第2の特異的結合剤複合体を形成するために十分な時間および条件下で接触させるステップであって、第2の特異的結合剤が検出可能に標識化されている、ステップ;
b)(a)において形成された複合体を測定することにより、試料中に存在するPIVKA-IIの量を測定するステップであって、参照レベルより多いPIVKA-IIの量が患者におけるHCCの存在を示す、ステップ
を含む、HCCを有することが疑われる患者においてHCCを診断するための指標を提供する方法。 - PIVKA-IIのインビトロ測定における、請求項1から4のいずれかに記載の特異的結合剤の使用。
- 請求項1から4のいずれかに記載の特異的結合剤を含有する容器を含む、試料中のPIVKA-IIを検出するおよび/またはその量を定量するためのキット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17181242 | 2017-07-13 | ||
| EP17181242.3 | 2017-07-13 | ||
| PCT/EP2018/068871 WO2019012019A1 (en) | 2017-07-13 | 2018-07-12 | NEW BINDING AGENT AND DOSAGE FOR PIVKA |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020526542A JP2020526542A (ja) | 2020-08-31 |
| JP7267253B2 true JP7267253B2 (ja) | 2023-05-01 |
Family
ID=59337570
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020501157A Active JP7267253B2 (ja) | 2017-07-13 | 2018-07-12 | Pivkaに対する新規結合剤およびアッセイ |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US11466098B2 (ja) |
| EP (1) | EP3652214A1 (ja) |
| JP (1) | JP7267253B2 (ja) |
| KR (1) | KR20200027522A (ja) |
| CN (1) | CN111133008A (ja) |
| BR (1) | BR112020000386A2 (ja) |
| WO (1) | WO2019012019A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113817063B (zh) * | 2021-10-19 | 2022-05-10 | 厦门英博迈生物科技有限公司 | 抗人异常凝血酶原抗体及其应用 |
| CN116041525B (zh) * | 2022-11-25 | 2023-06-23 | 山东纳睿博恩生物医药科技有限公司 | Dcp特异性抗体及其应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013541936A (ja) | 2010-07-26 | 2013-11-21 | アボット・ラボラトリーズ | Pivka−iiに関する抗体およびその使用 |
| US20140024050A1 (en) | 2009-03-10 | 2014-01-23 | Abbott Laboratories | Antibodies which detect pivkaii and methods of use thereof |
| JP2014035278A (ja) | 2012-08-09 | 2014-02-24 | Fujirebio Inc | Pivka−ii測定方法、測定試薬及び測定キット |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5316757A (en) | 1984-10-18 | 1994-05-31 | Board Of Regents, The University Of Texas System | Synthesis of polyazamacrocycles with more than one type of side-chain chelating groups |
| US5342606A (en) | 1984-10-18 | 1994-08-30 | Board Of Regents, The University Of Texas System | Polyazamacrocyclic compounds for complexation of metal ions |
| US5223409A (en) | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| US5877397A (en) | 1990-08-29 | 1999-03-02 | Genpharm International Inc. | Transgenic non-human animals capable of producing heterologous antibodies of various isotypes |
| US5582981A (en) | 1991-08-14 | 1996-12-10 | Gilead Sciences, Inc. | Method for identifying an oligonucleotide aptamer specific for a target |
| GB9304200D0 (en) | 1993-03-02 | 1993-04-21 | Sandoz Ltd | Improvements in or relating to organic compounds |
| US5885793A (en) | 1991-12-02 | 1999-03-23 | Medical Research Council | Production of anti-self antibodies from antibody segment repertoires and displayed on phage |
| US5480990A (en) | 1991-12-10 | 1996-01-02 | The Dow Chemical Company | Bicyclopolyazamacrocyclocarboxylic acid complexes for use as contrast agents |
| US5428139A (en) | 1991-12-10 | 1995-06-27 | The Dow Chemical Company | Bicyclopolyazamacrocyclophosphonic acid complexes for use as radiopharmaceuticals |
| US5739294A (en) | 1991-12-10 | 1998-04-14 | The Dow Chemical Company | Bicyclopol yazamacrocyclophosphonic acid complexes for use as contrast agents |
| DE4302241A1 (de) | 1993-01-27 | 1994-07-28 | Boehringer Mannheim Gmbh | Neues Biotinylierungsreagenz |
| US5385893A (en) | 1993-05-06 | 1995-01-31 | The Dow Chemical Company | Tricyclopolyazamacrocyclophosphonic acids, complexes and derivatives thereof, for use as contrast agents |
| US5462725A (en) | 1993-05-06 | 1995-10-31 | The Dow Chemical Company | 2-pyridylmethylenepolyazamacrocyclophosphonic acids, complexes and derivatives thereof, for use as contrast agents |
| US5834456A (en) | 1996-02-23 | 1998-11-10 | The Dow Chemical Company | Polyazamacrocyclofluoromonoalkylphosphonic acids, and their complexes, for use as contrast agents |
| US20100111856A1 (en) | 2004-09-23 | 2010-05-06 | Herman Gill | Zirconium-radiolabeled, cysteine engineered antibody conjugates |
| US20110111856A1 (en) | 2008-06-04 | 2011-05-12 | Andrew William White | Slot machine group tournament management and scoring system |
| JP5856956B2 (ja) | 2010-06-29 | 2016-02-10 | エーディア株式会社 | 血液検査方法 |
| CA2822899A1 (en) | 2011-02-09 | 2012-08-16 | F. Hoffmann-La Roche Ag | New iridium-based complexes for ecl |
-
2018
- 2018-07-12 JP JP2020501157A patent/JP7267253B2/ja active Active
- 2018-07-12 KR KR1020207003104A patent/KR20200027522A/ko not_active Application Discontinuation
- 2018-07-12 CN CN201880059264.0A patent/CN111133008A/zh active Pending
- 2018-07-12 EP EP18737627.2A patent/EP3652214A1/en active Pending
- 2018-07-12 BR BR112020000386-7A patent/BR112020000386A2/pt unknown
- 2018-07-12 WO PCT/EP2018/068871 patent/WO2019012019A1/en unknown
-
2020
- 2020-01-13 US US16/740,778 patent/US11466098B2/en active Active
-
2022
- 2022-08-24 US US17/821,937 patent/US20230055005A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140024050A1 (en) | 2009-03-10 | 2014-01-23 | Abbott Laboratories | Antibodies which detect pivkaii and methods of use thereof |
| JP2013541936A (ja) | 2010-07-26 | 2013-11-21 | アボット・ラボラトリーズ | Pivka−iiに関する抗体およびその使用 |
| JP2014035278A (ja) | 2012-08-09 | 2014-02-24 | Fujirebio Inc | Pivka−ii測定方法、測定試薬及び測定キット |
Non-Patent Citations (1)
| Title |
|---|
| KINUKAWA, H., et al.,"Epitope characterization of an anti-PIVKA-II antibody and evaluation of a fully automated chemiluminescent immunoassay for PIVKA-II.",CLIN. BIOCHEM.,2015年,Vol.48,pp.1120-1125,DOI: 10.1016/j.clinbiochem.2015.08.017,EPUB 2015/08/19 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11466098B2 (en) | 2022-10-11 |
| US20230055005A1 (en) | 2023-02-23 |
| KR20200027522A (ko) | 2020-03-12 |
| CN111133008A (zh) | 2020-05-08 |
| US20200140569A1 (en) | 2020-05-07 |
| BR112020000386A2 (pt) | 2020-07-21 |
| EP3652214A1 (en) | 2020-05-20 |
| WO2019012019A1 (en) | 2019-01-17 |
| JP2020526542A (ja) | 2020-08-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20230055005A1 (en) | New binding agent and assay for pivka | |
| US10809263B2 (en) | Antigenic composition for detecting auto-antibody with specific response to exosomal protein EIF3A, and method for diagnosing liver cancer using antigenic composition | |
| JP2023065484A (ja) | 新規タウ種 | |
| US8642347B2 (en) | Urinary CA125 peptides as biomarkers of ovarian cancer | |
| KR101138460B1 (ko) | 항-fasn 자가면역 항체를 포함하는 간암 진단 마커 및 이의 항원을 포함하는 간암 진단용 조성물 | |
| US20090298196A1 (en) | Quantitative measurement method for recombinant protein | |
| JP6088501B2 (ja) | プレプロバソプレッシンまたはそのフラグメントへの結合物を得る方法 | |
| JP2023126845A (ja) | 新規抗トロポニンt抗体 | |
| CN111936522A (zh) | 新型抗胸苷激酶抗体 | |
| KR20120095301A (ko) | 항-사이토케라틴 8/18 복합체 자가면역항체를 포함하는 암 진단 마커 및 이의 항원을 포함하는 암 진단용 조성물 | |
| US20210009993A1 (en) | Method for affinity maturation of antibodies | |
| EP4010366A1 (en) | Novel anti-troponint antibodies | |
| US20230331865A1 (en) | Antibodies for use in immunohistochemistry (ihc) protocols to diagnose cancer | |
| JP6729917B2 (ja) | EphA2 N末端フラグメント抗体 | |
| CA3203749A1 (en) | Anti-human cd10 antibodies for use in immunohistochemistry (ihc) protocols to diagnose cancer | |
| CN115925924A (zh) | 用于检测tsp-1特异性肽段的抗体及其用途 | |
| EP3817761A1 (en) | Novel thyroid peroxidase autoantibody immunoassay |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210524 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220323 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220405 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220704 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221004 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221207 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230331 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230419 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7267253 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |