JP7201800B2 - Flt3およびaxlの阻害剤としての3,9-ジアザスピロ[5,5]ウンデカン系化合物 - Google Patents
Flt3およびaxlの阻害剤としての3,9-ジアザスピロ[5,5]ウンデカン系化合物 Download PDFInfo
- Publication number
- JP7201800B2 JP7201800B2 JP2021517760A JP2021517760A JP7201800B2 JP 7201800 B2 JP7201800 B2 JP 7201800B2 JP 2021517760 A JP2021517760 A JP 2021517760A JP 2021517760 A JP2021517760 A JP 2021517760A JP 7201800 B2 JP7201800 B2 JP 7201800B2
- Authority
- JP
- Japan
- Prior art keywords
- compound
- acid
- compounds
- flt3
- mmol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Description
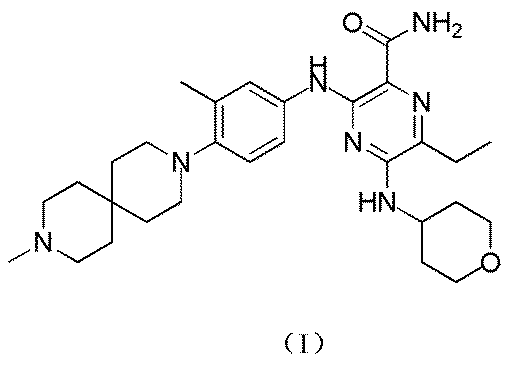
本発明は、新規のFLT3/AXL二重阻害剤を提供する。従来技術と比較して、本発明は、インビトロで予想外に高い酵素活性、細胞活性を有し、特に、FLT3変異の酵素活性試験において顕著な利点を有する。また、本発明の薬物動態特性は、従来技術よりも優れている。MV4-11のインビボ実験において、本発明は、低用量でも良好な腫瘍阻害活性を示す。薬物離脱リバウンド実験(drug withdrawal-rebound assay)では、本発明の化合物が強力な持続性腫瘍抑制能力を有することが証明された。Molm-13のインビボ実験において、本発明は、予想外に優れた腫瘍阻害効果を示し、これは、従来技術よりも明らかに優れている。
特に明記しない限り、本明細書で使用される以下の用語は、以下の意味を有することを意図している。特定の用語は、特定の定義がない場合に、不定または不明瞭と見なされるべきではないが、通常の意味で理解されるべきである。本明細書に商品名が記載される場合、その対応する商品またはその活性成分を指す。
実験材料:
FLT3 Kinase Enzyme System(キナーゼシステム)はPromega社から購入した。Envisionマルチラベルアナライザー(PerkinElmer)。
キット中の緩衝液稀を使用して、酵素、基質、ATP(アデノシン三リン酸)および阻害剤を希釈した。
試験する化合物をピペットで8番目の濃度まで5倍希釈し、すなわち5μmol/Lから0.065nmol/Lまで希釈し、ジメチルスルホキシドの最終濃度が5%であった。実験は2回行った。各濃度勾配の阻害剤1μl、FLT3酵素(15ng)2μL、および基質とATPとの混合物(50μmol/LのATP、0.1μg/μLのMBP)2μLをマイクロプレートに添加した。この時、化合物の最終濃度勾配は1μmol/Lから0.013nmol/Lであった。反応系を30℃で120分間反応させた。反応完了後、5μLのADP-Glo試薬を各ウェルに加え、さらに30℃で40分間反応させた。反応完了後、10μLのキナーゼ検出試薬を各ウェルに添加し、30℃で30分間反応させた。その後、PerkinElmerEnvisionマルチラベルアナライザーによって0.5秒の積分時間で化学発光を読み取った。
元のデータを阻害率に換算し、4パラメータカーブフィッティングによってIC50値を得た。FLT3酵素に対する本発明の化合物の阻害活性を表1に示す。
実験材料:
AXL Kinase Enzyme System(キナーゼシステム)はPromega社から購入した。Envisionマルチラベルアナライザー(PerkinElmer)。
キット中の緩衝液稀を使用して、酵素、基質、ATPおよび阻害剤を希釈した。
試験する化合物をピペットで8番目の濃度まで5倍希釈し、すなわち5μmol/Lから0.065nmol/Lまで希釈し、ジメチルスルホキシドの最終濃度が5%であった。実験は2回行った。各濃度勾配の阻害剤1μl、AXL酵素(6ng)2μL、および基質とATPとの混合物(50μmol/LのATP、0.2μg/μLのAxltide)2μLをマイクロプレートに添加した。この時、化合物の最終濃度勾配は1μmol/Lから0.013nmol/Lであった。反応系を30℃で60分間反応させた。反応完了後、5μLのADP-Glo試薬を各ウェルに加え、さらに30℃で40分間反応させた。反応完了後、10μLのキナーゼ検出試薬を各ウェルに添加し、30℃で30分間反応させた。その後、PerkinElmerEnvisionマルチラベルアナライザーによって0.5秒の積分時間で化学発光を読み取った。
元のデータを阻害率に換算し、4パラメータカーブフィッティングによってIC50値を得た。AXL酵素に対する本発明の化合物の阻害活性を表2に示す。
実験方法:
KINOMEscan(商標)技術を使用して実験を行った。実験化合物は100%DMSOに保存された。実験は、3倍希釈および11ポイントフィッティングによって実施された。Kdの測定に使用されたすべての化合物を超音波によって分散した後、直接希釈して実験を行った。反応は、いずれも384ウェルのポリプロピレンプレートで実施した。それぞれの最終容量は0.02mlであった。プレートを室温で1時間振とうしながらインキュベートして処理した。最終的にqPCR法によって溶離液中のキナーゼ濃度を測定し、フィッティングによってKdを得た。
実験材料:
IMDM培地、ウシ胎児血清、ペニシリン/ストレプトマイシン抗生物質はPromega(Madison,WI)社から購入した。MV-4-11細胞株は中国科学院細胞バンクから購入した。Envisionマルチラベルアナライザー(PerkinElmer)。
MV-4-11細胞を白色の96ウェルプレートに播種し、各ウェルに、10000個のMV-4-11細胞を含む80μLの細胞懸濁液を含む。二酸化炭素インキュベーターで細胞プレートを一晩培養した。
試験する化合物をピペットで8番目の濃度まで5倍希釈し、すなわち2mmol/Lから26nmol/Lまで希釈した。実験は2回行った。中間プレートに78μLの培地を加え、次に、対応する位置に応じて、勾配希釈した化合物を1ウェルあたり2μLで中間プレートに移し、均一に混合した後、1ウェルあたり20μLで細胞プレートに移した。二酸化炭素インキュベーターで細胞プレートを3日間培養した。
Promega CellTiter-Glo試薬を1ウェルあたり25μLで細胞プレートに添加し、室温で10分間インキュベートして、発光シグナルを安定化させた。読み取りには、PerkinElmer Envisionマルチラベルアナライザーを使用した。
元のデータを阻害率に換算し、4パラメータカーブフィッティングによってIC50値を得た。MV-4-11細胞の増殖に対する本発明の化合物の阻害活性を表4に示す。
実験の目的:
本実験の目的は、静脈内注射および強制経口投与による単回投与後の化合物の薬物動態学的挙動を評価し、強制経口投与後のバイオアベイラビリティを調査することである。
7~10週齢のCD-1雄マウスを選択した。静脈内投与および経口投与の用量は、それぞれ1mg/kgおよび2.5mg/kgであった。マウスは、投与前に少なくとも12時間絶食させ、投与4時間後に摂食を再開した。実験期間中、マウスは水を自由に摂取できた。
実験当日、静脈内投与群の動物に、5mL/kgの投与量で尾静脈への単回注射によって、対応する化合物を投与し;経口群に、10mL/kgの投与量で単回強制経口投与によって、対応する化合物を投与した。投与前に動物の体重を測定し、体重に基づいて投与量を計算した。サンプルを採取する時間は、0.083(注射群)、0.25、0.5、1、2、4、8、24時間であった。各時点で伏在静脈から約30μLの全血を採取し、血漿を調製して、高速液体クロマトグラフィー-タンデム質量分析(LC-MS/MS)による濃度測定に供した。最後の時点でPKサンプルを採取した後、すべての動物をCO2麻酔で安楽死処置させた。薬物動態ソフトウェアWinNonlin(商標)バージョン6.3(Pharsight,Mountain View,CA)の非コンパートメントモデルを利用して血漿中濃度を処理し、線形対数台形法によって薬物動態パラメーターを算出した。
マウスにおいて、本発明の化合物は、インビボクリアランス率が適切で、経口AUC、バイオアベイラビリティが良好で、優れた薬物動態特性を有する。本発明の化合物は、化合物Aと比較して、予想外に改善されたPK特性を有する。
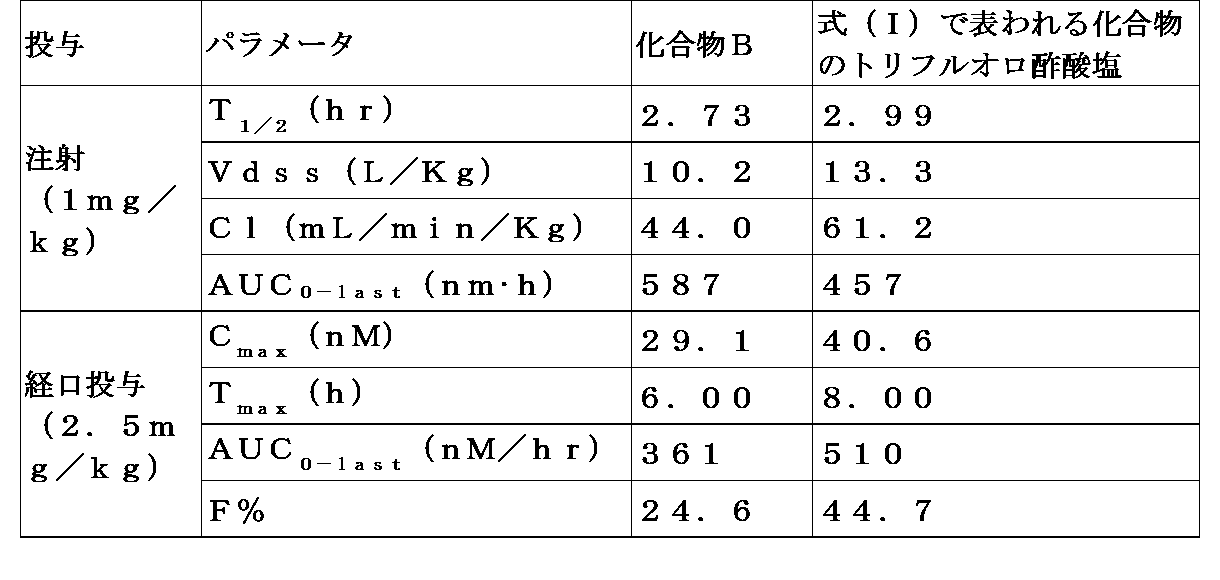
表5 インビボでの薬物動態特性評価の結果
実験の目的:
本実験では、ヒト二表現型(biphenotypic)B骨髄単球性白血病細胞MV4-11の皮下異種移植腫瘍のヌードマウスモデルを使用して、化合物の抗腫瘍効果を評価した。
10%ウシ胎児血清、100U/mLペニシリンおよび100μg/mLストレプトマイシンを添加したRPMI1640培地、37℃、5%CO2細胞インキュベーター内という条件下、ヒト二表現型B骨髄単球性白血病細胞MV4-11をインビトロで懸濁培養した。定期的な継代を週に2回行い、対数増殖期の細胞を回収し、カウントして接種に使用した。
各マウスの右頚背部に、10×106個のMV4-11細胞を皮下接種した。接種量は0.2mLで、細胞懸濁液はPBSとマトリゲル(体積比1:1)を混合したものであった。細胞接種後13日目に、インビボでの有効性実験を行った。腫瘍の平均体積は181mm3に達した。無作為にマウスを6匹ずつ群分けして、投与を開始した。
ノギスで腫瘍の直径を週に2回測定した。腫瘍の体積の計算式は、V=0.5a×b2であり、ここで、aおよびbはそれぞれ腫瘍の長径および短径を表す。
投与14日後、投与を停止し、腫瘍のリバウンドを観察した。
本発明の化合物は、ヒト二表現型B骨髄単球性白血病細胞MV4-11の異種移植腫瘍の増殖に対して有意な抑制効果を有する。本発明の化合物は、低用量(5mg/kg)でも、化合物Aの高用量(20mg/kg)と同等の腫瘍抑制効果を示す。薬物離脱リバウンド実験において、本発明の化合物は、化合物Bに比べて、同じ用量(5mg/kg)でより顕著な持続性腫瘍抑制効果を有する。
実験の目的:
本実験の目的は、静脈内注射および強制経口投与による単回投与後の化合物の薬物動態学的挙動を評価し、強制経口投与後のバイオアベイラビリティを調査することである。
7~10週齢のSD雄ラットを選択した。静脈内投与および経口投与の用量は、それぞれ1mg/kgおよび2.5mg/kgであった。ラットは、投与前に少なくとも12時間絶食させ、投与4時間後に摂食を再開した。実験期間中、ラットは水を自由に摂取できた。
実験当日、静脈内投与群の動物に、5mL/kgの投与量で尾静脈への単回注射によって、対応する化合物を投与し;経口群に、10mL/kgの投与量で単回強制経口投与によって、対応する化合物を投与した。投与前に動物の体重を測定し、体重に基づいて投与量を計算した。サンプルを採取する時間は、0.083(注射群)、0.25、0.5、1、2、4、8、24時間であった。各時点で頸静脈から約200μLの全血を採取し、血漿を調製して、高速液体クロマトグラフィー-タンデム質量分析(LC-MS/MS)による濃度測定に供した。最後の時点でPKサンプルを採取した後、すべての動物をCO2麻酔で安楽死処置させた。薬物動態ソフトウェアWinNonlin(商標)バージョン6.3(Pharsight,Mountain View,CA)の非コンパートメントモデルを利用して血漿中濃度を処理し、線形対数台形法によって薬物動態パラメーターを算出した。
ラットにおいて、本発明の化合物は、インビボ経口AUC、バイオアベイラビリティが優れ、良好な薬物動態特性を有する。本発明の化合物は、化合物Bと比較して、予想外に改善されたPK特性を有する。
実験の目的:
本実験の目的は、ヒト急性骨髄腫MOLM-13細胞株の皮下異種移植のNOD/SCID雌マウスモデルにおける化合物の薬力学効果を評価することである。
10%ウシ胎児血清を含むRPMI1640培地で、MOLM-13細胞を培養した。対数増殖期のMOLM-13細胞を回収し、ヌードマウスの皮下腫瘍接種に適した濃度になるまでPBSで再懸濁させた。
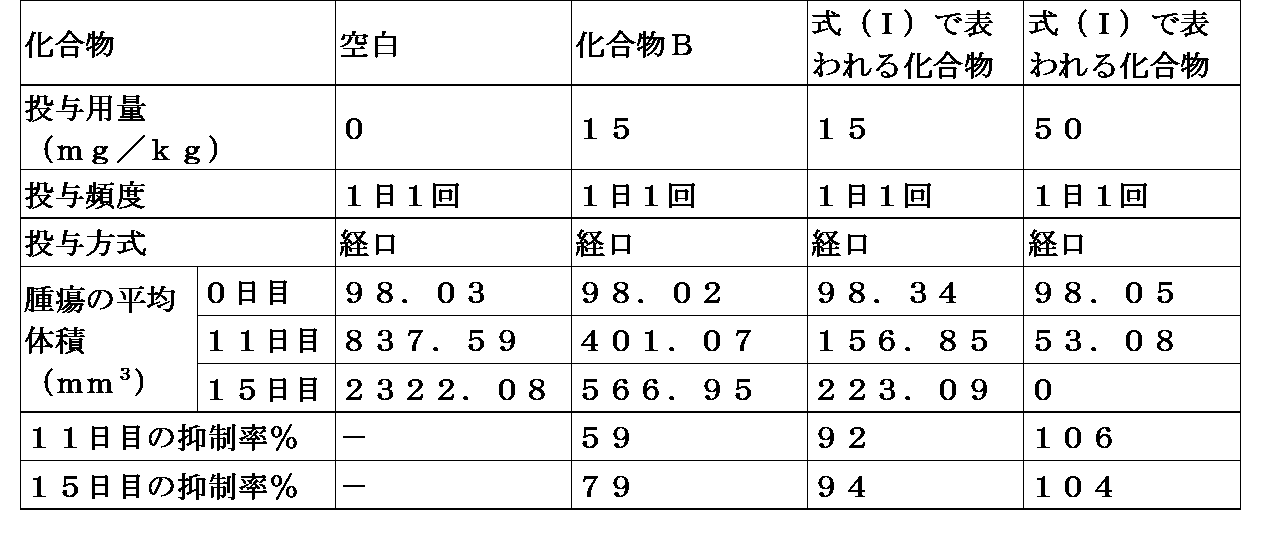
実験マウスの右頚背部に、0.1mlのPBS(0.1ml/匹)に再懸濁した5×106個のMOLM-13細胞を皮下接種した。腫瘍の成長を定期的に観察した。腫瘍が平均体積98mm3に成長した際、無作為にマウスを群分けして、腫瘍のサイズおよびマウスの体重に応じて投与した。
投与開始後、マウスの体重および腫瘍のサイズを週に3回測定した。腫瘍の体積の計算式は、腫瘍体積(mm3)=1/2×(a×b2)(ここで、aは長径、bは短径を表す)である。
本発明の化合物は、ヒト由来のMolm-13異種移植腫瘍の増殖に対して有意な抑制効果を有する。本発明の化合物は、化合物Bに比べて、同等の用量(15mg/kg)でより優れた腫瘍抑制効果を示す。用量が50mg/kgである場合、腫瘍の体積はゼロに減少した。
Claims (4)
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201811157842 | 2018-09-30 | ||
| CN201811157842.2 | 2018-09-30 | ||
| CN201910193150 | 2019-03-14 | ||
| CN201910193150.1 | 2019-03-14 | ||
| PCT/CN2019/108522 WO2020063856A1 (zh) | 2018-09-30 | 2019-09-27 | 作为flt3和axl抑制剂的3,9-二氮杂螺[5,5]十一烷类化合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022503943A JP2022503943A (ja) | 2022-01-12 |
| JP7201800B2 true JP7201800B2 (ja) | 2023-01-10 |
Family
ID=69949738
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021517760A Active JP7201800B2 (ja) | 2018-09-30 | 2019-09-27 | Flt3およびaxlの阻害剤としての3,9-ジアザスピロ[5,5]ウンデカン系化合物 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US11691974B2 (ja) |
| EP (1) | EP3858819A4 (ja) |
| JP (1) | JP7201800B2 (ja) |
| CN (1) | CN112839930B (ja) |
| WO (1) | WO2020063856A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021197344A1 (zh) * | 2020-03-30 | 2021-10-07 | 南京明德新药研发有限公司 | 二氮杂螺吡喃化合物的晶型 |
| CN111423387B (zh) * | 2020-05-11 | 2022-03-08 | 苏州康纯医药科技有限公司 | 一种Gilteritinib关键中间体的制备方法 |
| US11945785B2 (en) | 2021-12-30 | 2024-04-02 | Biomea Fusion, Inc. | Pyrazine compounds as inhibitors of FLT3 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010128659A1 (ja) | 2009-05-08 | 2010-11-11 | アステラス製薬株式会社 | ジアミノへテロ環カルボキサミド化合物 |
| WO2012053606A1 (ja) | 2010-10-22 | 2012-04-26 | アステラス製薬株式会社 | アリールアミノヘテロ環カルボキサミド化合物 |
| WO2013108754A1 (ja) | 2012-01-17 | 2013-07-25 | アステラス製薬株式会社 | ピラジンカルボキサミド化合物 |
| JP2016515537A (ja) | 2013-03-15 | 2016-05-30 | ダナ ファーバー キャンサー インスティテュート,インコーポレイテッド | ピリミド−ジアゼピノン化合物および障害の治療方法 |
| CN109384774A (zh) | 2017-08-11 | 2019-02-26 | 中国科学院上海药物研究所 | 一类多取代的吡嗪/三嗪酰胺类化合物及其制备方法和应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106083821B (zh) * | 2016-06-22 | 2019-01-11 | 上海皓元生物医药科技有限公司 | 一种3,5-二取代-吡嗪-2-甲酰胺化合物的合成方法 |
-
2019
- 2019-09-27 CN CN201980064621.7A patent/CN112839930B/zh active Active
- 2019-09-27 JP JP2021517760A patent/JP7201800B2/ja active Active
- 2019-09-27 WO PCT/CN2019/108522 patent/WO2020063856A1/zh active Application Filing
- 2019-09-27 US US17/281,479 patent/US11691974B2/en active Active
- 2019-09-27 EP EP19865038.4A patent/EP3858819A4/en not_active Withdrawn
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010128659A1 (ja) | 2009-05-08 | 2010-11-11 | アステラス製薬株式会社 | ジアミノへテロ環カルボキサミド化合物 |
| WO2012053606A1 (ja) | 2010-10-22 | 2012-04-26 | アステラス製薬株式会社 | アリールアミノヘテロ環カルボキサミド化合物 |
| WO2013108754A1 (ja) | 2012-01-17 | 2013-07-25 | アステラス製薬株式会社 | ピラジンカルボキサミド化合物 |
| JP2016515537A (ja) | 2013-03-15 | 2016-05-30 | ダナ ファーバー キャンサー インスティテュート,インコーポレイテッド | ピリミド−ジアゼピノン化合物および障害の治療方法 |
| CN109384774A (zh) | 2017-08-11 | 2019-02-26 | 中国科学院上海药物研究所 | 一类多取代的吡嗪/三嗪酰胺类化合物及其制备方法和应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3858819A4 (en) | 2022-05-18 |
| CN112839930A (zh) | 2021-05-25 |
| WO2020063856A1 (zh) | 2020-04-02 |
| US11691974B2 (en) | 2023-07-04 |
| CN112839930B (zh) | 2022-03-15 |
| EP3858819A1 (en) | 2021-08-04 |
| US20210395252A1 (en) | 2021-12-23 |
| JP2022503943A (ja) | 2022-01-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2021037018A1 (zh) | 二氢或四氢喹唑啉类化合物及其中间体、制备方法和应用 | |
| US9890168B2 (en) | 2,4-disubstituted 7H-pyrrolo[2,3-d]pyrimidine derivative, preparation method and medicinal use thereof | |
| CN112552295A (zh) | Kras突变蛋白抑制剂 | |
| EP3059227B1 (en) | Salt of nitrogen-containing heterocyclic compound or crystal thereof, pharmaceutical composition, and flt3 inhibitor | |
| JP7201800B2 (ja) | Flt3およびaxlの阻害剤としての3,9-ジアザスピロ[5,5]ウンデカン系化合物 | |
| CN112341457A (zh) | Kras突变蛋白抑制剂 | |
| US20200031805A1 (en) | Aryl hydrocarbon receptor (ahr) modulator compounds | |
| CA2813607C (en) | Substituted pyridazine carboxamide compounds | |
| KR102480074B1 (ko) | 설폰아마이드 화합물 및 이의 용도 | |
| CN112745335B (zh) | 一种三并杂环化合物及其用途 | |
| WO2017092413A1 (zh) | 一种二氨基嘧啶化合物及包含该化合物的组合物 | |
| WO2017003862A1 (en) | Lysyl oxidase-like 2 inhibitors and uses thereof | |
| EP3891152A1 (en) | Tyrosine kinase inhibitors, compositions and methods there of | |
| JP2023036991A (ja) | Ehmt2阻害剤としてのアミン置換複素環化合物、その塩、及びそれらの合成方法 | |
| US20220017520A1 (en) | Macrocyclic compound as cdk inhibitor, preparation method therefor, and use thereof in medicine | |
| WO2019057103A1 (zh) | Jak激酶抑制剂及其制备方法和在医药领域的应用 | |
| CN111362946A (zh) | 一种药物化合物及其组合物和应用 | |
| WO2023143147A1 (zh) | 一种哒嗪并吡啶酮类化合物、其药物组合物及应用 | |
| TWI804016B (zh) | 一種噻吩並嘧啶類化合物、包含其藥物組合物及其應用 | |
| CN109111439A (zh) | 一种酰胺类化合物及包含该化合物的组合物及其用途 | |
| CN108137614B (zh) | 一种稠合嘧啶化合物及包含该化合物的组合物及其用途 | |
| JP2020518563A (ja) | 抗ガン幹細胞性薬物 | |
| CN111138459B (zh) | Fgfr4抑制剂的光学异构体及其应用 | |
| WO2021088845A1 (zh) | 咪唑烷酮类化合物及其制备方法与应用 | |
| WO2021088839A1 (zh) | 咪唑烷酮类化合物及其制备方法与应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210528 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210528 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220526 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220607 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220907 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20221206 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20221222 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7201800 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |