JP7122002B2 - 疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 - Google Patents
疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 Download PDFInfo
- Publication number
- JP7122002B2 JP7122002B2 JP2019503129A JP2019503129A JP7122002B2 JP 7122002 B2 JP7122002 B2 JP 7122002B2 JP 2019503129 A JP2019503129 A JP 2019503129A JP 2019503129 A JP2019503129 A JP 2019503129A JP 7122002 B2 JP7122002 B2 JP 7122002B2
- Authority
- JP
- Japan
- Prior art keywords
- positive
- cells
- eae
- human animal
- disease
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/027—New or modified breeds of vertebrates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5082—Supracellular entities, e.g. tissue, organisms
- G01N33/5088—Supracellular entities, e.g. tissue, organisms of vertebrates
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2207/00—Modified animals
- A01K2207/35—Animals modified by environmental factors, e.g. temperature, O2
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/105—Murine
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0306—Animal model for genetic diseases
- A01K2267/0318—Animal model for neurodegenerative disease, e.g. non- Alzheimer's
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
- A01K2267/0356—Animal model for processes and diseases of the central nervous system, e.g. stress, learning, schizophrenia, pain, epilepsy
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
- A01K2267/0368—Animal model for inflammation
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
- A01K2267/0375—Animal model for cardiovascular diseases
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Molecular Biology (AREA)
- Pharmacology & Pharmacy (AREA)
- Environmental Sciences (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Cell Biology (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Husbandry (AREA)
- Biodiversity & Conservation Biology (AREA)
- Microbiology (AREA)
- Toxicology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Cardiology (AREA)
- Neurology (AREA)
- Epidemiology (AREA)
- Neurosurgery (AREA)
- Biophysics (AREA)
Description
(2)脳内血管が第三脳室と視床と歯状回との境界領域の血管である、(1)に記載の製造方法。
(3)疾患モデル非ヒト動物が進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を有する動物である、(1)又は(2)に記載の製造方法。
(4)ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程が、ストレス負荷後の非ヒト動物に中枢神経組織由来抗原反応性のCD4陽性T細胞を移入する工程である、(1)~(3)のいずれか一項に記載の製造方法。
(5)第三脳室と視床と歯状回との境界領域の血管に炎症があり、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を有する、疾患モデル非ヒト動物。
(6)(i)ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程、
(ii)工程(i)の開始前から終了後のいずれかの時点で非ヒト動物に被験物質を投与する工程、並びに
(iii)被験物質を投与した非ヒト動物において、脳内血管の炎症、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状の発症、進行又は発生を観察し、被験物質を投与しない非ヒト動物のそれと比較する工程
を含む、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための薬剤のスクリーニング方法。
(7)(a)第三脳室と視床と歯状回との境界領域の血管における炎症の有無を検出する工程、並びに
(b)炎症が検出された場合に進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を罹患又は発症するリスクが高いと判定する工程
を含む、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を罹患又は発症するリスクを判定する方法。
(8)CCケモカインリガンド5(CCL5)に対する抗体を有効成分とする、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬。
(9)GABA受容体アゴニストを有効成分とする、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬。
(10)ATP受容体アンタゴニストを有効成分とする、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬。
(11)プロトンポンプ阻害剤を有効成分とする、進行性多発性硬化症、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬。
(12)lymphocyte antigen 6 family member G5C(LY6G6C)に対する抗体を有効成分とする、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬。
(13)α2Cアドレナリン受容体に対する抗体を有効成分とする、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬。
(14)疾患又は症状が、ストレス負荷に起因する疾患又は症状である、(8)から(13)のいずれか一項に記載の医薬。
本発明の第一の態様は、ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程を含む、脳内血管に炎症を有する疾患モデル非ヒト動物の製造方法に関する。
本発明のさらなる態様は、(i)ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程、
(ii)工程(i)の開始前から終了後のいずれかの時点で非ヒト動物に被験物質を投与する工程、並びに
(iii)被験物質を投与した非ヒト動物において、脳内血管の炎症、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状の発症、進行又は発生を観察し、被験物質を投与しない非ヒト動物のそれと比較する工程
を含む、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための薬剤のスクリーニング方法に関する。
本発明のさらなる別の態様は、(a)第三脳室と視床と歯状回との境界領域の血管における炎症の有無を検出する工程、並びに
(b)炎症が検出された場合に進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患に罹患する又は症状を発症するリスクが高いと判定する工程
を含む、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患に罹患する又は症状を発症するリスクを判定する方法に関する。
本発明はまた、CCL5に対する抗体、GABA受容体アゴニスト、ATP受容体アンタゴニスト、プロトンポンプ阻害剤、LY6G6Cに対する抗体又はα2Cアドレナリン受容体に対する抗体を有効成分とする、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための医薬を別の態様として提供する。
C57BL/6マウスは日本SLCから、C57BL/6-PLマウスはTaconicから購入し、CX3CR1CreER ROSA26-TdTomatoマウスはフライブルク大学Marco Prinz教授から分与を受け、SPF条件下で飼育した。全ての動物実験は、北海道大学実験動物委員会の承認の下で行った。
FITCコンジュゲート抗CD19抗体(eBioscience)、抗CD11b抗体(eBioscience)、抗CD44抗体(eBioscience)、抗CD4抗体(eBioscience)、PEコンジュゲート抗CD44抗体(eBioscience)、抗TCR抗体(eBioscience)、PE-Cy7コンジュゲート抗CD90.2抗体(eBioscience)、APCコンジュゲート抗CD4抗体(BioLegend)、抗I-A/I-E抗体(BioLegend)、ビオチンコンジュゲート抗CD11b抗体(eBioscience)、抗CD19抗体(eBioscience)、抗NK1.1抗体(eBioscience)、抗CD11c抗体(eBioscience)及び抗TCR抗体(eBioscience)。
FITCコンジュゲート抗I-A/I-E抗体(BioLegend)、抗ドーパミントランスポーター抗体(Abcam)、抗ノルアドレナリントランスポーター抗体(Abcam)、抗リン酸化CREB抗体(Cell Signaling)、抗チロシンヒドロキシラーゼ抗体(Abcam)、抗リン酸化c-Fos(Ser32)(Cell Signaling)、対照ウサギIgG(DA1E)(Cell Signaling)、ビオチンコンジュゲート抗CD4抗体(BioLegend)、抗CD11b抗体(eBioscience)、抗I-A/I-E抗体(BioLegend)、抗ファセオルス・ブルガリス(Phaseolus・vulgaris)アグルチニン抗体(VECTOR)、抗CD31抗体(Abcam)、抗活性化caspase3抗体(Cell Signaling)、抗CHT1抗体(北海道大学医学系研究科解剖学講座解剖発生学分野作出)、Alexa Fluor 546ロバ抗ヤギIgG抗体(H+L)、Alexa Fluor 488ヤギ抗ウサギIgG抗体(H+L)、Alexa Fluor 546ヤギ抗ウサギIgG抗体(H+L)、Alexa Fluor 647ヤギ抗ウサギIgG抗体(H+L)、Alexa Fluor 647ヤギ抗ニワトリIgG抗体(Invitrogen)及びストレプトアビジンAlexa Fluor 546コンジュゲート(Invitrogen)。
抗マウスIL-17抗体及び抗CCL5抗体(いずれもR&D Systems)、抗IFN-γ抗体(Ueda et al.(2006) Int.Immunol. 18,1397-1404に従って精製)。
実施例に含まれる全ての実験は少なくとも3回行い、代表的データを結果として示した。各グラフは平均値±標準誤差を示す。また、2群間の差の統計解析にはStudentのt検定(両側)を、3群以上の差の統計解析には分散分析をそれぞれ用いた。p値0.05未満を統計的に有意とし、グラフ中で*p<0.05、**p<0.01、***p<0.001で表した。
(1)睡眠障害誘導による疾患モデルマウス
(i)ストレス負荷
PAWWストレスの負荷及びこれによる睡眠障害の誘導は、既法の通りに実施した(Miyazaki,K. et al.,PloS one,2013,8,e55452)。6~8週齢のC57BL/6マウスを、回転輪を備えたプラスチックケージ内で個別に順化飼育した。その後、ケージ内の木製床敷を深さ1.5cmの水に置き換え、回転輪上で継続的に運動させるPAWWストレスを2日間マウスに負荷することで睡眠障害を誘導した。
EAE病原性CD4陽性T細胞の調製及び移入は、既報の通りに実施した(Arima,Y. et al.,Cell,2012,148,447-457;Arima,Y. et al.,eLife,2015,4,e08733;Ogura,H. et al.,Immunity,2008,29,628-636)。簡潔には、C57BL/6マウスの尾基部にMOG(35-55)ペプチド(Sigma-Aldrich)を完全フロイントアジュバント(Sigma-Aldrich)と共に皮下注射し、さらに百日咳毒素(Sigma-Aldrich)をMOGペプチド投与後0、2及び7日目に静脈内注射した。MOGペプチド投与から9日後、マウス脾臓からリンパ球を回収し、抗CD4マイクロビーズ(Miltenyi Biotec)を用いてソートすることでCD4陽性T細胞に富む細胞集団を得た。この細胞集団(4×106個)を、MOGペプチドをパルスした放射線照射脾臓細胞(1×107個)と共に、rIL-23(10ng/ml;R&D Systems)の存在下で2日間、共培養した。培養液から細胞を回収し、抗CD4マイクロビーズを用いてCD4陽性T細胞を濃縮することでEAE病原性CD4陽性T細胞を調製した。
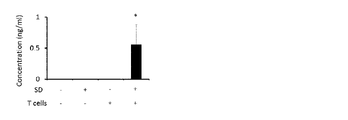
上記(i)のストレス負荷を開始してから2日後、上記(ii)で調製したEAE病原性CD4陽性T細胞(1.5×107個)を静脈内注射によりマウスに移入することで疾患モデルマウスを作製した。また、ストレスを負荷せずにEAE病原性CD4陽性T細胞移入を行ったマウス、ストレス負荷後にEAE病原性CD4陽性T細胞移入を行わないマウス、いずれの処置も行わないマウスを対照として用意した。
睡眠障害誘導に代えて湿潤床敷によりストレス負荷を与えること以外は上記(1)と同様の方法で、疾患モデルマウスを作製した。木製床敷を入れた飼育ケージ内に350mL/ケージの水を入れて床敷を湿らせ、このケージ内で6~8週齢のC57BL/6マウスを2日間飼育することで湿潤床敷ストレスを負荷した。湿潤床敷は毎日交換した。
それぞれの群あたり3~5匹のマウスを用いて、以下の試験を行った。
(1)EAE
実施例1で作製したマウスについて、EAEの病態を臨床スコアにより評価した。臨床スコアは既報の通りに測定した(Arima,Y. et al.,Cell,2012,148,447-457;Arima,Y. et al.,eLife,2015,4,e08733;Ogura,H. et al.,Immunity,2008,29,628-636)。臨床スコアは数字が大きくなるほど脳脊髄炎の症状が深刻であることを表し、0は異常症状が観察されない正常状態に、5は死亡に相当する。
実施例1(1)で作製したマウスについて、EAE病原性CD4陽性T細胞移入から10日後に胃腸炎の病態を評価した。各マウスから採取した便を生理食塩水(便1gあたり20mL)に懸濁し、遠心分離(8000rpm、5分間)により回収した上清を生理食塩水で10倍希釈し、Hemastix(SIEMENS)により潜血便試験を行った。潜血便スコアはHemastixの容器に記載されているスコアリング法に従って算出した。
実施例1(1)で作製したマウスについて、心筋障害の病態を評価した。EAE病原性CD4陽性T細胞移入の9日後に血液を採取し、ELISA kit(Life diagnotics)を用いて血中トロポニンI濃度を、及びELISA kit(Lifespan BioSciences)を用いて血中クレアチンキナーゼMB濃度を測定した。ストレス状態下でEAE病原性CD4陽性T細胞の移入を受けたマウスは、血中トロポニンI濃度(図7)及び血中クレアチンキナーゼMB濃度(図8)のいずれも上昇しており、心臓における細胞死を特徴とする心筋障害の病態を有することが示唆された。この群のマウスの心電を測定したところ、心不全の兆候が検出された(データを図示せず)。
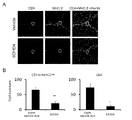
実施例1(1)で作製したマウスについて、MHCクラスII陽性細胞及びCD4陽性T細胞の集積を調べた。EAE病原性CD4陽性T細胞移入から10日後のマウスから摘出した第5腰髄及び脳をSCEM(SECTION-LAB)中に包埋し、マイクロトーム装置CM3050(Leica Microsystems)を用いて10μm厚の切片とした。切片はCryofilmタイプIIIC(16UF)(SECTION-LAB)を用いて回収し、ヘマトキシリン/エオジン染色、又は抗MHCクラスII抗体若しくは抗CD4抗体を用いて免疫組織化学的に染色し、BZ-9000顕微鏡(KEYENCE)で解析した。解析はBZ-IIアナライザー(KEYENCE)のHS ALLソフトウェアにより実施した。
(1)CCL5
実施例1(1)で作製した睡眠障害誘導後にEAE病原性CD4陽性T細胞移入を行ったマウスに、抗CCL5抗体又は対照のラットIgG抗体(いずれも100μg/マウス)をEAE病原性CD4陽性T細胞移入後毎日腹腔内注射し、EAE病態を実施例2(1)と同様に評価した。また、EAE病原性CD4陽性T細胞移入から10日後のマウスを用いて、特定血管における細胞の集積を実施例2(4)と同様に調べた。
マウスHPRTプライマー:
5’-AGCCCCAAAATGGTTAAGGTTG-3’(配列番号1)及び
5’-CAAGGGCATATCCAACAACAAAC-3’(配列番号2)
マウスHPRTプローブ:
5’-ATCCAACAAAGTCTGGCCTGTATCCAACAC-3’(配列番号3)
マウスCCL5プライマー:
5’-CTCCCTGCTGCTTTGCCTAC-3’(配列番号4)及び
5’-CGGTTCCTTCGAGTGACAAACA-3’(配列番号5)
マウスCCL5プローブ:5’-TGCCTCGTGCCCACGTCAAGGAGTATT-3’(配列番号6)
であった。リアルタイムPCR条件は、50℃ 2分間、95℃ 3分間の後、95℃ 3秒間、60℃ 30秒間を40サイクルであった。
実施例1(1)で作製した睡眠障害誘導後にEAE病原性CD4陽性T細胞移入を行ったマウスに、抗IFN-γ抗体、抗IL17A抗体又は対照のラットIgG抗体(いずれも100μg/マウス)をEAE病原性CD4陽性T細胞移入後毎日腹腔内注射し、EAE病態を実施例2(1)と同様に評価した。また、EAE病原性CD4陽性T細胞移入から10日後のマウスを用いて、特定血管における細胞の集積を実施例2(4)と同様に調べた。
(1)PVNの交感神経と特定血管との連絡
C57BL/6マウスに対して、実施例3(2)と同様の方法で、ドーパミン/ノルアドレナリン作動性ニューロンを変性させる神経毒である6-ヒドロキシドーパミン(6-OHDA)塩酸塩(2mg/ml)又は溶媒の0.02%アスコルビン酸それぞれ0.2μlをEAE病原性CD4陽性T細胞移入の四日前(ストレス負荷の二日前)に特定血管にマイクロインジェクションした。その後、実施例1(1)と同様に、睡眠障害誘導及びEAE病原性CD4陽性T細胞移入を行った。
実施例1(1)で作製した睡眠障害誘導後にEAE病原性CD4陽性T細胞移入を行ったマウスに対して、EAE病原性CD4陽性T細胞移入から5日後に、順行性トレーサーであるPHA-L(25mg/ml)又は溶媒の生理食塩水を特定血管にマイクロインジェクションした。PHA-LはPVNよりもDMHにおいて多く観察された(図27)。また、FITC-CTBをDMH(座標AP -1.46mm;ML 0.37mm;DV 5mm)にマイクロインジェクションしたところ、特定血管においてFITCの蛍光が観察された(図28)。
睡眠障害を誘導したC57BL/6マウスの特定血管に、EAE病原性CD4陽性T細胞+MOG樹状細胞又はIFN-γ+IL-17Aを実施例3(2)と同様にマイクロインジェクションした。マイクロインジェクションから2日後のPVN及びDMHにおいて、リン酸化cfosの増加、すなわち神経の活性化が観察された(図30)。
上記(2)において特定血管にマイクロインジェクションされた順行性トレーサーPHA-LはDMXに到達していた(結果を図示せず)。また、実施例3(2)と同様に、睡眠障害を誘導したマウスの特定血管にEAE病原性CD4陽性T細胞+MOG樹状細胞をマイクロインジェクションしたところ、DMX及び求心性迷走神経の主要な核であるNTSにおけるリン酸化cfosの増加、すなわち神経の活性化が観察された(図36)。
睡眠障害誘導を行って2日後のC57BL/6マウスから、約100個の脳の凍結切片(15μm厚)を調製し、PAXgene(QIAGEN)で15分間固定し、次いで100% EtOHで10分間固定した。切片中の第三脳室領域血管周辺の組織をレーザーマイクロダイセクションデバイスDM6000B(Leica Microsystems)により回収し、全RNAをRNeasyマイクロキット(QIAGEN)により抽出し、かずさDNA研究所に委託してRNAシークエンスを行い、全遺伝子を対象とした発現解析を実施した。
C57BL/6マウスに睡眠障害誘導後、EAE病原性CD4陽性T細胞を移入した。5日後に当該マウスの頭部を麻酔下で定位装置に固定し、頭蓋骨上の毛をそり、皮膚を70%エタノールで拭いた。30ゲージの針を特定血管(座標AP -1.06mm;ML 1mm;DV 2.25mm)に向けて下げ入れ、液量0.5μlの抗Ly6G6C抗体(clone;NIMP-R14) 0.1mg/ml(NOVUS BIOLOGICALS)、抗alpha 2c Adrenergic Receptor抗体 1mg/ml(GeneTex)、又はそれぞれのコントロール抗体(ラットIgG(Sigma)若しくはウサギIgG(Sigma))を90秒かけて、マイクロインジェクションにより投与した。その後、経時的にマウスの病態観察を行った。
配列番号2 マウスHPRTリバースプライマー
配列番号3 マウスHPRTプローブ
配列番号4 マウスCCL5フォワードプライマー
配列番号5 マウスCCL5リバースプライマー
配列番号6 マウスCCL5プローブ
Claims (5)
- ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程を含む、脳内血管に炎症を有する疾患モデル非ヒト動物の製造方法であって、前記工程が、ストレス状態にある非ヒト動物に中枢神経組織由来抗原反応性のCD4陽性T細胞を移入する工程、又はストレス状態にある非ヒト動物に中枢神経組織由来抗原を投与して中枢神経組織由来抗原反応性のCD4陽性T細胞を誘導する工程である、前記製造方法。
- 脳内血管が第三脳室と視床と歯状回との境界領域の血管である、請求項1に記載の製造方法。
- 疾患モデル非ヒト動物が進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を有する動物である、請求項1又は2に記載の製造方法。
- (i)ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程、
(ii)工程(i)の開始前から終了後のいずれかの時点で非ヒト動物に被験物質を投与する工程、並びに
(iii)被験物質を投与した非ヒト動物において、脳内血管の炎症、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状の発症、進行又は発生を観察し、被験物質を投与しない非ヒト動物のそれと比較する工程
を含む、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状を予防及び/又は治療するための薬剤のスクリーニング方法であって、
工程(i)が、ストレス状態にある非ヒト動物に中枢神経組織由来抗原反応性のCD4陽性T細胞を移入する工程、又はストレス状態にある非ヒト動物に中枢神経組織由来抗原を投与して中枢神経組織由来抗原反応性のCD4陽性T細胞を誘導する工程である、前記スクリーニング方法。 - (i)ストレス状態にある非ヒト動物の体内に中枢神経組織由来抗原反応性のCD4陽性T細胞を存在させる工程、
(ii)工程(i)の開始前から終了後のいずれかの時点で非ヒト動物に被験物質を投与する工程、並びに
(iii)被験物質を投与した非ヒト動物において、脳内血管の炎症、進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状の発症、進行又は発生を観察し、被験物質を投与しない非ヒト動物のそれと比較する工程
を含む、被験物質の進行性多発性硬化症、胃腸炎、心筋障害及び突然死よりなる群から選択される少なくとも1の疾患又は症状に対する予防的及び/又は治療的効果を評価する方法であって、
工程(i)が、ストレス状態にある非ヒト動物に中枢神経組織由来抗原反応性のCD4陽性T細胞を移入する工程、又はストレス状態にある非ヒト動物に中枢神経組織由来抗原を投与して中枢神経組織由来抗原反応性のCD4陽性T細胞を誘導する工程である、前記評価方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017038115 | 2017-03-01 | ||
| JP2017038115 | 2017-03-01 | ||
| PCT/JP2018/007901 WO2018159787A1 (ja) | 2017-03-01 | 2018-03-01 | 疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2018159787A1 JPWO2018159787A1 (ja) | 2019-12-26 |
| JP7122002B2 true JP7122002B2 (ja) | 2022-08-19 |
Family
ID=63370490
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019503129A Active JP7122002B2 (ja) | 2017-03-01 | 2018-03-01 | 疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US11733232B2 (ja) |
| JP (1) | JP7122002B2 (ja) |
| WO (1) | WO2018159787A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7122002B2 (ja) | 2017-03-01 | 2022-08-19 | 国立大学法人北海道大学 | 疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 |
| US20210405011A1 (en) * | 2018-09-01 | 2021-12-30 | National University Corporation Hokkaido University | Pharmaceutical for preventing and/or treating stress load-related disease |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011500645A (ja) | 2007-10-17 | 2011-01-06 | ティクセル | 多発性硬化症の治療のための組成物 |
| JP2015142578A (ja) | 2006-08-11 | 2015-08-06 | ライフ・サイエンシーズ・リサーチ・パートナーズ・フェレニゲング・ゾンデル・ウィンストーメルクLife Sciences Research Partners Vzw | 免疫原性ペプチドおよび免疫障害におけるその使用 |
| WO2016141262A1 (en) | 2015-03-04 | 2016-09-09 | The Rockefeller University | Anti-inflammatory polypeptides |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001519154A (ja) | 1998-10-05 | 2001-10-23 | 財団法人相模中央化学研究所 | 膜貫通ドメインを有するヒトタンパク質及びそれをコードするdna |
| US20040121004A1 (en) | 2002-12-20 | 2004-06-24 | Rajneesh Taneja | Dosage forms containing a PPI, NSAID, and buffer |
| JP4913751B2 (ja) | 2004-12-21 | 2012-04-11 | メルク セローノ ソシエテ アノニム | 新規cc−ケモカインアンタゴニスト |
| CA2590446A1 (en) | 2004-12-21 | 2006-06-29 | Laboratoires Serono S.A. | Cc-chemokine antagonists |
| US20070203216A1 (en) | 2006-02-14 | 2007-08-30 | Bjarke Ebert | Method of treating inflammatory diseases |
| US8338109B2 (en) | 2006-11-02 | 2012-12-25 | Mayo Foundation For Medical Education And Research | Predicting cancer outcome |
| ES2553412T3 (es) | 2007-10-31 | 2015-12-09 | Merck Sharp & Dohme Corp. | Antagonistas del receptor P2X3 para el tratamiento del dolor |
| HRP20150162T1 (hr) | 2009-08-28 | 2015-05-08 | Regeneron Pharmaceuticals, Inc. | Antikin antitijela koja se vežu na višestruke cc kemokine |
| GB201117313D0 (en) | 2011-10-07 | 2011-11-16 | Gt Biolog Ltd | Bacterium for use in medicine |
| JP2014071016A (ja) | 2012-09-28 | 2014-04-21 | Mitsubishi Chemical Medience Corp | 神経系の変性疾患の検出方法 |
| UA119032C2 (uk) | 2012-10-02 | 2019-04-25 | Женеро Са | Фармацевтична композиція для лікування блокади ремієлінізації при захворюваннях, які пов'язані з експресією білка оболонки herv-w |
| WO2015057939A1 (en) | 2013-10-18 | 2015-04-23 | Biogen Idec Ma Inc. | Anti-s1p4 antibodies and uses thereof |
| WO2016131944A1 (en) | 2015-02-20 | 2016-08-25 | INSERM (Institut National de la Santé et de la Recherche Médicale) | New method for treating cardiovascular diseases |
| JP7058417B2 (ja) | 2016-08-18 | 2022-04-22 | 国立大学法人神戸大学 | ジストログリカン糖鎖修飾異常に伴う疾患の治療剤及び関連酵素測定法 |
| CN106544430A (zh) | 2016-11-04 | 2017-03-29 | 叶伟亮 | 一种检测前列腺癌的分子标记物及其应用 |
| JP7122002B2 (ja) | 2017-03-01 | 2022-08-19 | 国立大学法人北海道大学 | 疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 |
-
2018
- 2018-03-01 JP JP2019503129A patent/JP7122002B2/ja active Active
- 2018-03-01 US US16/490,145 patent/US11733232B2/en active Active
- 2018-03-01 WO PCT/JP2018/007901 patent/WO2018159787A1/ja not_active Ceased
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015142578A (ja) | 2006-08-11 | 2015-08-06 | ライフ・サイエンシーズ・リサーチ・パートナーズ・フェレニゲング・ゾンデル・ウィンストーメルクLife Sciences Research Partners Vzw | 免疫原性ペプチドおよび免疫障害におけるその使用 |
| JP2011500645A (ja) | 2007-10-17 | 2011-01-06 | ティクセル | 多発性硬化症の治療のための組成物 |
| WO2016141262A1 (en) | 2015-03-04 | 2016-09-09 | The Rockefeller University | Anti-inflammatory polypeptides |
Non-Patent Citations (1)
| Title |
|---|
| eLife (2015) Vol.4, e08733, pp.1-23 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2018159787A1 (ja) | 2018-09-07 |
| US20200049696A1 (en) | 2020-02-13 |
| US11733232B2 (en) | 2023-08-22 |
| JPWO2018159787A1 (ja) | 2019-12-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Martin et al. | New role of P2X7 receptor in an Alzheimer’s disease mouse model | |
| Wang et al. | P2X7R/NLRP3 signaling pathway-mediated pyroptosis and neuroinflammation contributed to cognitive impairment in a mouse model of migraine | |
| KR102248804B1 (ko) | Cns의 질환 및 손상을 치료하기 위한 전신적 조절 t 세포 수준 또는 활성의 감소 | |
| Semple et al. | Interleukin-1 receptor in seizure susceptibility after traumatic injury to the pediatric brain | |
| Provencio et al. | Neutrophil depletion after subarachnoid hemorrhage improves memory via NMDA receptors | |
| Singh et al. | Allopregnanolone restores hippocampal-dependent learning and memory and neural progenitor survival in aging 3xTgAD and nonTg mice | |
| Cruz-Orengo et al. | Enhanced sphingosine-1-phosphate receptor 2 expression underlies female CNS autoimmunity susceptibility | |
| Kim et al. | Astrocyte CCL2 sustains immune cell infiltration in chronic experimental autoimmune encephalomyelitis | |
| Geppetti et al. | Antidromic vasodilatation and the migraine mechanism | |
| Dong et al. | Sitagliptin protects the cognition function of the Alzheimer’s disease mice through activating glucagon-like peptide-1 and BDNF-TrkB signalings | |
| Ineichen et al. | Nogo-A antibodies enhance axonal repair and remyelination in neuro-inflammatory and demyelinating pathology | |
| Marcon et al. | Exacerbation of DSS‐induced colitis in mice lacking kinin B 1 receptors through compensatory up‐regulation of kinin B 2 receptors: the role of tight junctions and intestinal homeostasis | |
| Liu et al. | Distinctive roles for α7*-and α9*-nicotinic acetylcholine receptors in inflammatory and autoimmune responses in the murine experimental autoimmune encephalomyelitis model of multiple sclerosis | |
| Zelena | Vasopressin in health and disease with a focus on affective disorders | |
| Vu et al. | Inhibition of vasoactive intestinal polypeptide (VIP) induces resistance to dextran sodium sulfate (DSS)-induced colitis in mice | |
| JP7122002B2 (ja) | 疾患モデル非ヒト動物の製造方法、疾患モデル非ヒト動物、該動物を用いた薬剤のスクリーニング方法及び疾患リスク判定方法 | |
| EP3096781B1 (en) | Agents for use in the treatment of retinal inflammation | |
| JP7779739B2 (ja) | 認知障害を処置するためのパルス状gnrh投与 | |
| Fritze et al. | TNFα causes thrombin-dependent vagal neuron apoptosis in inflammatory bowel disease | |
| WO2019146805A1 (ja) | 前頭側頭葉変性症治療剤、前頭側頭葉変性症治療剤のスクリーニング方法、及び前頭側頭葉変性症の治療方法 | |
| JP7317377B2 (ja) | ストレス負荷が関与する疾患を予防及び/又は治療するための医薬 | |
| Sipos | Neuropathological examinations in the mouse brain-investigation of a new pharmaceutical target in the cuprizone model and comparative histological analyses of primary cilia in the physiological central nervous system | |
| Kennedy | The role of Toll-like receptors in Parkinson's disease | |
| Liu et al. | Distinctive Roles For α7*-And α9*-Nicotinic Acetylcholine Receptors In Inflammatory And Autoimmune Responses In The Murine Experimental Autoimmune Encephalomyelitis Model Of Multiple Sclerosis | |
| Grandi et al. | Long-term peripheral infusion of nociceptin/orphanin FQ promotes hyperplasia, activation and migration of mucosal mast cells in the rat gastric fundus |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220325 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220715 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220801 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7122002 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |