JP7053479B2 - IL7受容体細胞外ドメインα鎖に対する非拮抗性抗体及び癌治療におけるそれらの使用 - Google Patents
IL7受容体細胞外ドメインα鎖に対する非拮抗性抗体及び癌治療におけるそれらの使用 Download PDFInfo
- Publication number
- JP7053479B2 JP7053479B2 JP2018545380A JP2018545380A JP7053479B2 JP 7053479 B2 JP7053479 B2 JP 7053479B2 JP 2018545380 A JP2018545380 A JP 2018545380A JP 2018545380 A JP2018545380 A JP 2018545380A JP 7053479 B2 JP7053479 B2 JP 7053479B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- residue
- antigen
- seq
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/53—Hinge
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/54—F(ab')2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/624—Disulfide-stabilized antibody (dsFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/03—Fusion polypeptide containing a localisation/targetting motif containing a transmembrane segment
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
IL-7のIL-7Rへの結合は、Janusキナーゼ(JAK)-1及び-3、シグナル伝達兼転写活性化因子5(STAT5)、及びホスファチジルイノシトール3-キナーゼ(PI3-k)を含む、いくつかのシグナル伝達経路の活性化を誘発する。STAT1及びSTAT3経路が活性化されることが報告されているが、それらは主要な経路ではないように思われる。STAT5経路の活性化は、抗アポトーシスタンパク質Bcl-2の誘導及びアポトーシス促進性タンパク質Baxのミトコンドリアへの侵入の防止に必要とされ、従って、胸腺で発生するT細胞前駆細胞の生存に必要とされる。PI3-k経路の活性化は、アポトーシス促進性タンパク質Badのリン酸化及び細胞質保持をもたらす。
-Effi3-VH3又はVH3又はEffi3-VHvar3又はVHvar3と称される、重鎖可変ドメイン(表6の配列番号:2の配列、又はシグナルペプチドを含む配列番号:8の配列)であって、VH3-CDR1、VH3-CDR2、VH3-CDR3と称されるCDRを含むもの、又はEffi3-VH3、Effi3-VHvar3もしくはVHvar3の接頭辞を持つ同等の呼称;並びに
-Effi3-VH3VL3と称される変異体に関して、Effi3-VL3又はVH3又はEffi3-VLvar3又はVLvar3と称される軽鎖可変ドメイン(表6の配列番号:4の配列、又はシグナルペプチドを含む配列番号:10の配列)であって、VL3-CDR1、VL3-CDR2、VL3-CDR3と称されるCDRを含むもの、又はEffi3-VL3、Effi3-VLvar3もしくはVLvar3の接頭辞を持つ同等の呼称;あるいは
-Effi3-VH3VL4と称される変異体に関して、Effi3-VL4又はVH3又はEffi3-VLvar4又はVLvar4と称される軽鎖可変ドメイン(表6の配列番号:6の配列、又はシグナルペプチドを含む配列番号:12の配列)であって、VL4-CDR1、VL4-CDR2、VL4-CDR3と称されるCDRを含むもの、又はEffi3-VL4、Effi3-VLvar4もしくはVLvar4の接頭辞を持つ同等の呼称:のいずれか。
-特に表6の配列番号:2の配列として本明細書において開示されたVH3重鎖のCDRを伴う、各々、表6の配列番号:14、16及び18の配列を有するVH3-CDR1、VH3-CDR2及びVH3-CDR3を伴う、重鎖;並びに
-各々、配列番号:4及び6の配列として本明細書において開示されたVL3軽鎖もしくはVL4軽鎖のCDRを伴う、特に各々、配列番号:20、22及び24の配列を有するVL3-CDR1、VL3-CDR2及びVL3-CDR3を伴うか、又は各々、配列番号:26、22及び24の配列を有するVL4-CDR1、VL3-CDR2及びVL3-CDR3を伴う、軽鎖。
別の実施態様において、本抗体又は抗原結合性断片は、追加的に、VH-CDR3(重鎖のCDR3)において位置V101及び/又はV102に置換を有さないか、あるいはV101又はV102置換を有さない。
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、及び/又は
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基G、位置82に残基R、位置85に残基A、位置90に残基T。
-VH3の配列、すなわち配列番号:2の配列を伴う、重鎖;並びに
-VL3の配列(配列番号:4の配列)又はVL4の配列(配列番号:6の配列)を伴う、軽鎖。
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基Gもしくは残基E、特に残基E、位置82に残基R、位置85に残基A、位置90に残基T。
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基Gもしくは残基E、特に残基E、位置82に残基R、位置85に残基A、位置90に残基T。
ヒト化抗体又はその抗原結合性断片が位置28にS残基を含む(VL3-CDR1におけるように、VL-CDR1において)特定の実施態様において、該抗体又は断片は、位置73にE残基を含む(VLフレームワーク残基において)。
-疎水性相互作用により一緒に会合された、VL鎖及びVH鎖からなるFv断片;
-VH:VLヘテロ二量体が、ジスルフィド結合によって安定化されている、dsFv断片;
-VL鎖及びVH鎖が、可動性ペプチドリンカーにより互いに接続され、その結果1本鎖タンパク質を形成している、scFv断片;
-ジスルフィド結合を介して一緒に結合された、全L鎖、及びH鎖のVH-CH1断片を含む単量体断片である、Fab断片;
-Fab’断片;
-2個のFab’断片、及び追加的に抗体のヒンジ領域の一部を含む、F(ab')2断片。
重鎖に関して、IgG1m-E333A定常ドメイン(表6の配列番号:28の配列)又はIgG4m-S228P(配列番号:30の配列)又はIgG2b(配列番号:32の配列)のドメイン;
軽鎖に関して、CLκ定常ドメイン(配列番号:34の配列)又はCLλ(配列番号:36の配列)のドメイン。
-VH3及びVL3又はVL4のCDR配列を有する、変異体であって、ここで該配列に対する置換は、フレームワーク残基に限定され、特にここで20%未満(又は25残基未満)、好ましくは10%未満(又は12残基未満)、より好ましくは5%未満(又は6残基未満)及び更により好ましくは3、2もしくは1フレームワーク残基(複数可)が、該配列に対して置換されているもの;
-VH3及びVL3又はVL4のCDRに対して、それらのCDRの各々において、わずか2及び好ましくはわずか1つの置換(複数可)を有する、変異体であって、好ましくはここで、少なくとも3、より好ましくは少なくとも4及び更により好ましくは5のCDRが、修飾されず(修飾されたCDRは、各々2以下の置換及び好ましくはただ1つの置換を有する);そのような変異体は、先の好ましい制限により、任意に追加的に、フレームワーク残基中に置換を有するもの;
-VH-CDR3にV101T及び/又はV102T置換(複数可)を、並びに先の好ましい制限により、CDR及び/又はフレームワーク残基に任意に追加の置換を有する変異体;
-V101T又はV102T置換を有する変異体、並びに特にV101及びV102置換を有さない変異体:
ここで好ましい変異体は、VL-CDR1の位置28にS残基(すなわち、配列番号:20の配列を持つVL3のVL-CDR1を有する)、並びにVLフレームワーク配列の位置73にE残基(配列番号:4の配列を持つVL3を有するように)、又はVL-CDR1の位置28にD残基(すなわち、配列番号:26の配列を持つVL4のVL-CDR1を有する)並びにVLフレームワーク配列の位置73にG残基(配列番号:6の配列を持つVL4におけるように)のいずれかを有する。
-該抗体又は抗原結合性断片の抗原結合能を保持し、且つ抗原結合性抗体模倣物である、キメラタンパク質、特に人工タンパク質;又は
-該分子へ、認識、結合、アンカリング、シグナル伝達の機能を集合的に提供する、複数の機能性ドメインを有する複合分子、特に、組換え分子に、特に融合タンパク質に関連して、(i)本明細書において定義した該抗体又は抗原結合性断片のscFv断片に由来するか又はそのようなscFv断片である、エクトドメイン、(ii)細胞膜へのアンカリングのための、膜貫通ドメイン、並びに(iii)少なくとも1つの細胞内シグナル伝達ドメインを含む、エンドドメイン:を含む、キメラ抗原受容体(CAR):である。
-CD3ζ細胞質ドメインにより提供されるような、T細胞活性化の開始;
-T細胞媒介性細胞傷害性;
-T細胞活性化シグナルの増幅、又は4-1BB、CD28もしくはICOSもしくはOX40などの受容体から誘導された同時刺激エレメントにより提供されるような、該シグナルの同時刺激:
を集合的に可能にする。
a. 抗体又はその抗原結合性断片、特にscFv断片をコードしているポリヌクレオチドを提供する工程;
b. 工程a)の該ポリヌクレオチドをそのC-末端で、膜貫通ドメイン、及び細胞、特にT細胞、より特定するとヒトT細胞へ、刺激シグナル(複数可)を提供するのに適した少なくとも1つの、特に2つの細胞内シグナル伝達ドメイン(複数可)を、N-からC-末端へコードしているポリヌクレオチドにより組換える工程;
c. 工程b)において得られた組換え分子を、細胞において、特にT細胞において、より特定するとヒトT細胞において、発現させる工程;
d. 任意にその特性のために生成されたキメラ抗原受容体を、ヒトCD127を発現している細胞と接触させた後、これを選択する工程:
にも関する。
a. 抗体、抗原結合性断片又はそのような抗体の模倣物の、CD127の細胞外ドメインへ、特に配列番号:55の配列を持つエピトープを含むか又はこれからなるポリペプチドへ結合する能力を(例えば、「サイトフルオロメトリーによるIL7R結合アッセイ」及び「ELISAにより評価された抗-h-CD127 MabのrCD127認識」と題する「実施例」セクションにおいて説明された方法に従い)試験する工程;
b. IL-7シグナル伝達経路に対する、抗体、抗原結合性断片又はそのような抗体の模倣物の作用を(例えば、「ホスホStat5活性アッセイ」と題する「実施例」セクションにおいて説明された方法に従い)試験する工程;
c. TSLPシグナル伝達経路に対する、抗体、抗原結合性断片又はそのような抗体の模倣物の作用を(例えば、「TARC分泌アッセイ」と題する「実施例」セクションにおいて説明された方法に従い)試験する工程;
d. 抗体、抗原結合性断片又はそのような抗体の模倣物の細胞傷害活性、特にADCC活性を(例えば、「抗体依存性細胞傷害」と題する「実施例」セクションにおいて説明された方法に従い)試験する工程。
-これは、CD127のアンタゴニストではなく、IL7-Rを発現している細胞におけるSTAT5のIL-7が誘導したリン酸化を阻害しない;並びに/又は
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を阻害しない;並びに/又は
-これは、CD127のアゴニストではない;並びに/又は
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を増大しない;並びに/又は
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激された分泌を増大しない。
-本明細書に定義された、抗体又はその抗原結合性断片、キメラ分子、細胞、もしくはポリヌクレオチド、
-化学療法薬、放射線治療薬、手術用薬剤、免疫治療薬、プロバイオティックス及び抗生物質の群から選択された、少なくとも1種の更なる治療薬:
を含む、組み合わせ治療手段であって、
ここで該活性成分が、個別治療、同時治療又は併用治療のために、特に組合せ使用又は逐次使用のために、製剤化される、組み合わせ治療手段に関する。
-特に本発明の抗-CD127抗体又はその抗原結合性断片又はその抗原結合性抗体模倣物により、対象の腫瘍試料中のCD127の発現レベルを決定すること、並びに
-このCD127の発現レベルを、無反応対象集団におけるCD127の発現レベルの代表値と比較すること:を含み、
ここで対象の腫瘍試料中のより高いCD127の発現レベルは、該治療に反応する対象の指標である。
本方法に従う発現レベルの決定は、試料の細胞上のCD127分子を定量することを包含してよい。
(図面の簡単な説明)
(ヒト化)
MD707-3クローンは、先に説明したインシリコ法における脱免疫化及びリサーフェシングにより、ヒト化した。
Effi3クローンのVH領域及びVL領域を、RACE PCR技術を用いてシークエンシングした。簡潔に述べると、全RNAを抽出し、逆転写し、得られたcDNAを、dATP及びターミナルトランスフェラーゼ酵素を用いて、分子の3’末端でポリアデニル化させた。1回目の35サイクルのPCR反応は、オリゴdTアンカープライマー及びHerculease酵素(Stratagene社)を用いて行った。2回目の35サイクルのPCRは、ネステッドPCRアンカープライマーを用いて行った。その後、得られたPCR産物を大腸菌(E. Coli)内でTAクローニングし、アンピシリンで選択した後、得られたコロニーを制限酵素プロファイリングによってスクリーニングし、挿入されたcDNAをシークエンシングした。
pFuseCHIg-hG1e4発現プラスミド(Invivogen社)は、ヒトIgG1のCH1+ヒンジ+CH2+CH3定常ドメインを含み、これは、ADCC及びCDC細胞傷害作用を改善するように修飾された。開始するために、ヒト化MD707変異体のWT、VH3及びVH4(最もヒト化された抗体)の配列のみを、Genscriptにより合成し、EcoRV 5’及び3’末端(extremities)並びにATGの前に追加のKozak配列(GCCACC)を持つクローニングベクター(pUC57)内に挿入し、本発明者らに送付し(凍結乾燥された4μg)、かつ20μl H2O中に再懸濁させた。各プラスミドを、EcoRV制限酵素により消化し、挿入断片VH(400bp)を抽出した。
pFuseCLIg-hk発現プラスミド(Invivogen社)は、ヒトIgG1のCLκ定常ドメインを含んだ。開始するために、ヒト化MD707変異体VLwt、VL3及びVL4の配列のみを、Genscriptにより合成し、BsiWI 5’及び3’末端並びにATGの前に追加のKozak配列(GCCACC)を持つクローニングベクター(pUC57)内に挿入し、本発明者らに送付し(凍結乾燥された4μg)、かつ20μl H2O中に再懸濁させた。各プラスミドを、BsiWI制限酵素により消化し、挿入断片VL(400bp)を抽出した。精製した挿入断片を、BsiWI中で開環され且つ脱リン酸化された発現プラスミドであるpFuseCLIg-hk発現プラスミドにライゲーションさせた。ヒト定常ドメインの前に右方向にVL断片が挿入された陽性クローンを、トランスフェクション工程のために、Midiprep-エンドトキシンフリー(Macherey-Nagel社)により、増幅及び精製した。
トランスフェクションの前日:COSを、完全培地(DMEM SVF10%(Hyclone社)+PS 1%+Glu 1%)の入ったP12プレート中に、100000個細胞/ウェルで播種し、37℃、5%CO2でインキュベーションした。
同時-トランスフェクションの各上清中の、分泌されたMD707-3(VH+VL)の濃度を、ヒトIvIgG標準に応じて、サンドイッチELISAアッセイ(抗-hFc抗体/抗-hκ抗体)により測定した。各同時-トランスフェクションにおけるMD707-3のCD127への結合を、活性ELISAアッセイ(CD127Fc組換えタンパク質/抗-hκ抗体)により決定し、精製したキメラMD707-3標準の活性と比較した。プラスミドVH又はVLのみを伴う陰性対照は、抗-CD127活性を有さなかった。
・VHvar3+VLvar3、配列番号:2の配列及び配列番号:4の配列(又は、シグナル配列を伴う、配列番号:8及び10の配列)。この抗体は、本明細書においてVH3VL3と称される。
・VHvar3+VLvar4、配列番号:2の配列及び配列番号:6の配列(又は、シグナル配列を伴う、配列番号:8及び12の配列)。この抗体は、本明細書においてVH3VL4と称される。
ヒトPBMCへの抗-IL7Rの結合を測定するために、抗体を、ヒトPBMCと一緒に、4℃で30分間インキュベーションし、洗浄し、その後、APC-標識した抗-CD3(クローンHIT3a、BD Bioscience社、照会番号555342)に加え、Effi7抗体とは交差反応しないPE-標識した抗-CD127(クローンhIL7R-M21、BD Bioscience社、照会番号557938)により4℃で30分間染色した。試料を分析し、BD LSRIIサイトフルオロメーター上でCD3+細胞をゲートした。
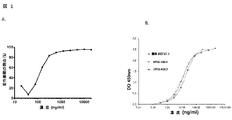
抗hCD127抗体の結合活性を、ELISA(酵素結合免疫吸着アッセイ)により評価した。ELISAアッセイのために、組換えhCD127(Sino Biologicals社、北京、中国:照会番号10975-H08H)を、プラスチック上に1μg/mlで固定し、精製した抗体を添加し、結合を測定した。インキュベーション及び洗浄後、ペルオキシダーゼ-標識マウス抗-ラットκ鎖(AbdSerotec社)を添加し、従来法により顕示させた。
ヒト化Effi3抗体(クローンVH3VL4)を、4℃、37℃、-80℃又は室温で、28日間インキュベーションした。結合活性を、ELISAアッセイにより試験し、組換えhCD127(Sino Biologicals社、北京、中国;照会番号10975-H08H)を、プラスチック上に1μg/mlで固定し、上清の希釈物を添加して、結合を測定した。インキュベーション及び洗浄の後、マウス抗ヒト軽鎖(κ特異的)+ペルオキシダーゼ標識ロバ抗マウス抗体を添加し、従来法により顕示させた。増加する投与量のMabを添加し、結合を測定した。インキュベーション及び洗浄後、ペルオキシダーゼ-標識マウス抗-ラットκ鎖(AbdSerotec社)を添加し、従来法により顕示させた。
図1Bの結果は、精製したEffi3は、長期間、及び様々な温度で貯蔵した後、安定していることを示している。
健常志願者由来のフィコール勾配により収集したヒト末梢血単核細胞(PBMC)を、異なる濃度の関心対象の抗体を含む血清-非含有培地において、室温で15分間インキュベーションし、その後0.1又は5ng/mlの組換えヒトIL-7(rhIL-7;AbD Serotec社、照合番号PHP046)と共に、37℃で15分間インキュベーションした。rhIL-7で未処理のPBMCを、バックグラウンドシグナルとして分析し、他方抗体を含まないIL-7処理細胞を、陰性対照として設定した。その後PBMCを、急速冷却し、FACS緩衝液で洗浄し、反応を停止した。次に細胞を、冷Cytofix/Cytoperm溶液(BD Bioscience社、照合番号554722)と共に15分間インキュベーションし、Perm/Wash緩衝液(Bd Bioscience社)により2回洗浄し、抗-ヒトCD3 FITC抗体(Bd Bioscience社、照合番号557694)により氷上で30分間染色した。その後PBMCを、Perm/Wash緩衝液により2回洗浄し、BD Perm緩衝液III(Bd Bioscience社、照合番号558050)中で30分間透過性上昇させた。次に細胞を、FACS緩衝液(及び/又は1%BSA及び0.1%アジドを含むPBS)中で2回洗浄し、抗-ヒトpSTAT5 Alexa 647抗体(BD Bioscience社、照合番号612599)と共に、室温で30分間インキュベーションした。試料を、BD CANTO II FACS装置上で分析した。図3Aに示したように、MD707-3抗体から誘導されたEffi3抗体(変異体VH3VL4)は、親抗体MD707-3と比べ、STAT5リン酸化の阻害活性を有さなかった。
骨髄樹状細胞(DC)を、健常志願者の血液から、CD1c(BDCA-1)+樹状細胞単離キット(Miltenyi Biotec社、ベルギッシュ・グラートバッハ、独国)により単離した(Etablissement Francais du Sang、ナント、仏国)。骨髄樹状細胞を、10%牛胎仔血清、1%ピルビン酸、1%Hepes、1%L-グルタミン及び1%ペニシリン-ストレプトマイシンを含有するRPMIにおいて培養した。細胞を、平底-96-ウェルプレート中、TSLP(15ng/ml)、LPS(1μg/ml)の存在下又は培養培地のみで、5.104個細胞/ウェルで播種し、異なるヒトCD127抗体(MD707-3、Effi3-VH3VL4)又は抗-TSLP抗体を異なる濃度で添加した。24時間培養した時点で、上清を収集し、ELISAアッセイ(R&D sytems社、ミネアポリス、米国)により、TARC産生について分析した。
抗-ヒトCD127 MabのADCCであるADCCとは、標的細胞上に発現するエピトープに対する抗体の結合、並びにその後の、主にグランザイム/パーフォリン系機構による標的細胞の死滅をもたらす、Fc受容体を発現するエフェクター免疫細胞(本質的にNK細胞及び活性化リンパ球)のFc依存性動員を指す。
Peptide Technologies PepStar(商標)ペプチドマイクロアレイは、ガラス表面に化学選択的かつ共有結合的に固定されている、抗原又は他の給源に由来する精製合成ペプチドを含む。立体障害によって生じる偽陰性を回避するために、最適化された親水性リンカー部分がガラス表面と抗原由来ペプチド配列の間に挿入されている。技術的な理由で、全てのペプチドがC-末端グリシンを含む。試料のプロファイリング実験を52種のペプチドからなるペプチドライブラリーに対して行った。ペプチドの完全なリストを下に示す:
(構成1)
抗体又はその抗原結合性断片であって、以下のCDR:
-そのアミノ酸配列が、配列番号:14のEffi3-VH3-CDR1である、VH-CDR1;
-そのアミノ酸配列が、配列番号:16のEffi3-VH3-CDR2である、VH-CDR2;
-そのアミノ酸配列が、配列番号:18のEffi3-VH3-CDR3配列である、VH-CDR3;
-そのアミノ酸配列が、配列番号:22のEffi3-VL3-CDR2である、VL-CDR2;
-そのアミノ酸配列が、配列番号:24のEffi3-VL3-CDR3である、VL-CDR3;並びに、
-そのアミノ酸配列が、配列番号:20のEffi3-VL3-CDR1であるか、又はそのアミノ酸配列が、配列番号:26のEffi3-VL4-CDR1である、VL-CDR1:を含み、
ここで、この抗体又はその抗原結合性断片が、ヒトCD127の細胞外ドメインへ特異的に結合し、且つCD127のアンタゴニストではない、前記抗体又はその抗原結合性断片。
(構成2)
下記の特徴の一つ以上:
-該抗体又は断片は、IL7-Rを発現している細胞におけるSTAT5のヒトIL-7誘導したリン酸化を阻害しないこと;
-該抗体又は断片は、TSLP-Rを発現している細胞におけるTARCのヒトTSLP-刺激した分泌を阻害しないこと;
-該抗体又は断片は、ヒトCD127のアゴニストではないこと;
-該抗体又は断片は、IL7-Rを発現している細胞におけるSTAT5のヒトIL-7誘導したリン酸化を増大しないこと;
-該抗体又は断片は、TSLP-Rを発現している細胞におけるTARCのヒトTSLP-刺激した分泌を増大しないこと:を有する、構成1記載の抗体又は断片。
(構成3)
前記抗体又はその抗原結合性断片が、重鎖及び軽鎖を含み、ここで:
-重鎖は、配列番号:14のVH-CDR1、配列番号:16のVH-CDR2、配列番号:18のVH-CDR3を含み;並びに
-軽鎖は、配列番号:20又は26のVL-CDR1、配列番号:22のVL-CDR2、配列番号:24のVL-CDR3を含む、構成1又は2記載の抗体又はその抗原結合性断片。
(構成4)
前記重鎖及び/又は軽鎖が、それらのフレームワーク内に、1又は複数の下記のアミノ酸残基を、並びに特に下記のアミノ酸残基の全て:
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、及び/又は
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基Gもしくは残基E、好ましくは残基E、位置82に残基R、位置85に残基A、位置90に残基T:
を、Kabat付番体系に関して同定された位置に含む、構成3記載の抗体又はその抗原結合性断片。
(構成5)
構成3又は4記載の抗体又はその抗原結合性断片であって、それが:
(i)前記軽鎖が、配列番号:26のVL4-CDR1を含み、且つ位置73に残基Gであるアミノ酸残基を有する、重鎖及び軽鎖、又は
(ii)好ましくは、前記軽鎖が、配列番号:20のVL3-CDR1を含み、且つ位置73に残基Eであるアミノ酸残基を有する、重鎖及び軽鎖:を含む、抗体又はその抗原結合性断片。
(構成6)
前記重鎖及び/又は軽鎖が、それらのフレームワーク内に、下記のアミノ酸残基の全て:
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、及び/又は
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基E、位置82に残基R、位置85に残基A、位置90に残基T:
を含む、構成4記載の抗体又はその抗原結合性断片。
(構成7)
構成1~4のいずれか一項記載の抗体又はその抗原結合性断片であって、それが:
-そのアミノ酸配列が配列番号:2の配列であるEffi3-VH3の配列を含むか又はこれからなる重鎖;並びに
-そのアミノ酸配列が配列番号:4の配列であるEffi3-VL3の配列、又はそのアミノ酸配列が配列番号:6の配列であるEffi3-VL4の配列を含むか又はこれからなる軽鎖:
を含むか又はこれらからなる、抗体又はその抗原結合性断片。
(構成8)
CD127-陽性細胞、特にヒトCD127-陽性細胞に対し、細胞傷害活性、特にADCC活性を有する、構成1~7のいずれか一項記載の抗体又はその抗原結合性断片。
(構成9)
下記の断片の一つ:
-疎水性相互作用により一緒に会合された、VL鎖及びVH鎖からなるFv断片;
-VH:VLヘテロ二量体が、ジスルフィド結合によって安定化されている、dsFv断片;
-VL鎖及びVH鎖が、可動性ペプチドリンカーにより互いに接続され、その結果一本鎖タンパク質を形成している、scFv断片;
-ジスルフィド結合を介して一緒に結合された、全L鎖、及びH鎖のVH-CH1断片を含む単量体断片である、Fab断片;
-Fab’断片;
-2個のFab’断片、及び追加的に抗体のヒンジ領域の一部を含む、F(ab')2断片:
である、構成1~8のいずれか一項記載の抗体の抗原結合性断片。
(構成10)
配列番号:55の配列を持つエピトープからなるか又はこれを含むポリペプチドを認識し、且つ任意に該ポリペプチドに対して生じる、構成1~9のいずれか一項記載の抗体又はその抗原結合性断片。
(構成11)
前記抗体が、以下を含むか又はこれらからなるヒト化モノクローナル抗体:
-そのアミノ酸配列が配列番号:28の配列であるIgG1m-E333Aの定常領域を含む重鎖、特にそのアミノ酸配列が配列番号:42の配列であるEffi3-VH3-IgG1m-E333Aの重鎖;並びに
-そのアミノ酸配列が配列番号:34の配列であるCLκ定常領域を含む軽鎖、特にそのアミノ酸配列が配列番号:50の配列であるEffi3-VL3-CLκ、又はそのアミノ酸配列が配列番号:48の配列であるEffi3-VL4-CLκの軽鎖:
である、構成1~10のいずれか一項記載の抗体。
(構成12)
前記抗体が、以下を含むか又はこれらからなるヒト化モノクローナル抗体:
-そのアミノ酸配列が配列番号:30の配列であるIgG4m-S228Pの定常領域、又はそのアミノ酸配列が配列番号:32の配列であるIgG2bの定常領域を含む重鎖;並びに
-そのアミノ酸配列が配列番号:34の配列であるCLκ定常領域、又はそのアミノ酸配列が配列番号:36の配列であるCLλ定常配列を含む、軽鎖:
である、構成1~11のいずれか一項記載の抗体。
(構成13)
構成1~8のいずれか一項記載の抗体の断片であり、且つ以下の一つ:
-そのアミノ酸配列が配列番号:14の配列であるEffi3-VH3-CDR1のVH-CDR1;
-そのアミノ酸配列が配列番号:16の配列であるEffi3-VH3-CDR2のVH-CDR2;
-そのアミノ酸配列が配列番号:18の配列であるEffi3-VH3-CDR3のVH-CDR3;
-そのアミノ酸配列が配列番号:22の配列であるEffi3-VL3-CDR2のVL-CDR2;
-そのアミノ酸配列が配列番号:24の配列であるEffi3-VL3-CDR3のVL-CDR3;
-そのアミノ酸配列が配列番号:20の配列であるEffi3-VL3-CDR1又はそのアミノ酸配列が配列番号:26の配列であるEffi3-VL4-CDR1のVL-CDR1;
-そのアミノ酸配列が配列番号:2の配列であるEffi3-VH3の配列を含む重鎖;
-そのアミノ酸配列が配列番号:4の配列であるEffi3-VL3の配列を含む軽鎖;又は
-そのアミノ酸配列が配列番号:6の配列であるEffi3-VL4の配列;
にある、ポリペプチド。
(構成14)
構成1~13のいずれか一項記載の抗体又はその断片を含むキメラ分子であって、それが:
-該抗体又は抗原結合性断片の抗原-結合能を保持し、且つ抗原-結合性抗体模倣物である、キメラタンパク質、特に人工タンパク質;又は
-該分子へ、認識、結合、アンカリング、シグナル伝達の機能を集合的に提供する、複数の機能性ドメインを有する複合分子、特に、1以上の組換え分子(複数可)に、特に1以上の融合タンパク質(複数可)に関連して、(i)構成1~15のいずれか一項記載の該抗体又は抗原結合性断片のscFv断片由来であるか又はそのようなscFv断片である、エクトドメイン、(ii)細胞膜へのアンカリングのための、膜貫通ドメイン、並びに(iii)少なくとも1つの細胞内シグナル伝達ドメインを含む、エンドドメイン:を含む、キメラ抗原受容体(CAR):
である、キメラ分子。
(構成15)
下記の特徴の少なくとも一つ:
-CD3ζ細胞質ドメインにより提供されるような、T細胞活性化の開始;
-T細胞媒介性細胞傷害性;
-T細胞活性化シグナルの増幅、又は4-1BB、CD28もしくはICOSもしくはOX40などの受容体から誘導された同時刺激エレメントにより提供されるような、該シグナルの同時刺激:
を集合的に可能にする、少なくとも2、有利には少なくとも3のシグナル伝達ドメインを含む、構成14記載のキメラ抗原受容体。
(構成16)
構成1~13のいずれか一項記載のポリペプチドをコードしている、ポリヌクレオチド、特に単離されたポリヌクレオチド、特に構成1~13のいずれか一項記載のポリペプチドをコードしているポリヌクレオチドを挿入断片として含むベクターである、前記ポリヌクレオチド。
(構成17)
配列番号:13、15、17、19、21及び23の配列、又は配列番号:13、15、17、25、21及び23の配列を含む、特に配列番号:1及び3の配列又は配列番号:1及び5の配列を含む、特に配列番号:41及び47の配列又は配列番号:41及び49の配列を含む、構成16記載のポリヌクレオチド。
(構成18)
構成1~13のいずれか一項記載の抗体又は抗原結合性断片、もしくは構成14又は15記載のキメラ分子、もしくは構成16又は17記載のポリヌクレオチドを含む、細胞、特にT細胞。
(構成19)
キメラ抗原受容体(CAR)の方法又は調製であって、それが:
a. 構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、特にscFv断片をコードしているポリヌクレオチドを提供する工程;
b. 工程a)の該ポリヌクレオチドをそのC-末端で、膜貫通ドメイン、及び細胞、特にT細胞、より特定するとヒトT細胞へ、刺激シグナル(複数可)を提供するのに適した少なくとも1つの、特に2つの細胞内シグナル伝達ドメイン(複数可)を、N-からC-末端へコードしているポリヌクレオチドにより組換える工程;
c. 工程b)において得られた組換え分子を、細胞において、特にT細胞において、より特定するとヒトT細胞において、発現させる工程;
d. 任意に、生成されたキメラ抗原受容体を、ヒトCD127を発現している細胞と接触させた後、これをその特性について選択する工程:
を含む、前記方法。
(構成20)
活性成分として、構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、構成14又は15記載のキメラ分子、構成18記載の細胞、もしくは構成16又は17記載のポリヌクレオチドを含有する、医薬組成物。
(構成21)
活性成分として:
-構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、構成14又は15記載のキメラ分子、構成18記載の細胞、もしくは構成16又は17記載のポリヌクレオチド、並びに
-化学療法薬、放射線治療薬、手術用薬剤、免疫治療薬、プロバイオティックス及び抗生物質の群から選択された、少なくとも1種の更なる治療薬:
を含む、組み合わせ治療手段、特に組み合わせ製品であって、
ここで該活性成分が、個別治療、同時治療又は併用治療のために、特に組合せ使用又は逐次使用のために、製剤化される、組み合わせ治療手段。
(構成22)
前記製品を必要とするヒト患者への投与に適しており、且つ活性成分として:(i)構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、構成14又は15記載のキメラ分子、構成18記載の細胞、あるいは、構成16又は17記載のポリヌクレオチド、並びに、(ii)追加の免疫治療薬、特に構成14又は15記載のCAR分子、又は細胞受容体もしくはCD19、CD20、CD52又はHer2などの抗原を標的化するCAR分子を生じるT細胞などの、T細胞に関与する免疫治療薬:を含有する、構成21記載の組み合わせ製品。
(構成23)
医薬品として使用するための、構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、構成14又は15記載のキメラ分子、構成18記載の細胞、もしくは構成16又は17記載のポリヌクレオチド。
(構成24)
癌、特にCD127+細胞に関連した癌、より特定するとCD127陽性細胞の増殖及び/又はCD127陽性細胞の浸潤に関連した癌の治療における使用のための、構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、構成14又は15記載のキメラ分子、構成16又は17記載のポリヌクレオチド、もしくは構成18記載の細胞もしくは構成23記載の医薬品。
(構成25)
乳癌、腎臓癌、膀胱癌、肺癌、膵臓癌の群から選択された癌の治療における構成24記載の使用のための、又はセザリーリンパ腫などのT細胞皮膚リンパ腫の治療のための、又はIL7-R/TSLP経路の獲得型変異を有する急性リンパ芽球様白血病及び中皮腫の治療のための、構成1~13のいずれか一項記載の抗体又はその抗原結合性断片、構成14又は15記載のキメラ分子、構成16又は17記載のポリヌクレオチド、もしくは構成18記載の細胞。
(構成26)
配列番号:55の配列を持つエピトープからなるポリペプチド。
(構成27)
構成23記載のポリペプチドに対し、非-ヒト動物、特に非-ヒト哺乳動物を免疫化し、並びに特に該免疫化した非-ヒト動物から得られる血清を収集し、該ポリペプチドに対する抗体を得ることを含む、構成1~13のいずれか一項記載の抗体の製造方法。
(構成28)
CD127の細胞外ドメインに特異的に結合し、且つ下記の特徴の少なくとも一つ:
-これは、CD127のアンタゴニストではなく、且つIL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を阻害しない、並びに/又は
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を阻害しない、並びに/又は
-これは、CD127のアゴニストではない、並びに/又は
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を増大しない、並びに/又は
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を増大しない:
を示す抗体、そのような抗体の抗原結合性断片又は模倣物を選択する工程を更に含む、構成27記載の方法。
(構成29)
前記抗体又はその抗原結合性断片又は模倣物が、下記の特徴:
-これは、CD127の細胞外ドメインに特異的に結合する、並びに
-これは、CD127のアンタゴニストではない、並びに
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を阻害しない、並びに
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を阻害しない、並びに
-これは、CD127のアゴニストではない、並びに
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を増大しない、並びに
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を増大しない:
を有する、構成28記載の方法。
(構成30)
本発明の抗-CD127抗体又はその抗原結合性断片又はその抗原結合性模倣物が、先に対象から得られた試料中のCD127+細胞の検出のために及び任意にCD127の発現の定量のために使用される、インビトロ又はエクスビボ診断方法、特に個別化医療における、より特定するとコンパニオン診断における使用に適した診断方法。
(構成31)
診断試験における使用、特に個別化医療における又はコンパニオン診断試験における使用に適した医薬品の製造における、構成1~15のいずれか一項記載の本発明の抗-CD127抗体又はその抗原結合性断片又はその抗原結合性模倣物の使用。
(構成32)
治療に対する対象の反応、特に癌と診断された対象の反応を予測するバイオマーカーとしてCD127の存在を決定することを含む、先に対象から得られた試料中のCD127+細胞の存在を決定する、インビトロ又はエクスビボ方法であって、該方法が:
-特に本発明の抗-CD127抗体又はその抗原結合性断片又はその抗原-結合性抗体模倣物を使用し、対象の腫瘍試料中のCD127の発現レベルを決定すること、並びに
-このCD127の発現レベルを、無反応対象集団におけるCD127の発現レベルの代表値と比較すること:を含み、
ここで対象の腫瘍試料中のより高いCD127の発現レベルは、該治療に反応する対象の指標である、方法。
Claims (41)
- 抗体又はその抗原結合性断片であって、以下のCDR:
-そのアミノ酸配列が、配列番号:14のEffi3-VH3-CDR1である、VH-CDR1;
-そのアミノ酸配列が、配列番号:16のEffi3-VH3-CDR2である、VH-CDR2;
-そのアミノ酸配列が、配列番号:18のEffi3-VH3-CDR3配列である、VH-CDR3;
-そのアミノ酸配列が、配列番号:22のEffi3-VL3-CDR2である、VL-CDR2;
-そのアミノ酸配列が、配列番号:24のEffi3-VL3-CDR3である、VL-CDR3;並びに、
-そのアミノ酸配列が、配列番号:20のEffi3-VL3-CDR1であるか、又はそのアミノ酸配列が、配列番号:26のEffi3-VL4-CDR1である、VL-CDR1:を含み、
ここで、この抗体又はその抗原結合性断片が、ヒトCD127の細胞外ドメインへ特異的に結合し、且つCD127のアンタゴニストではない、前記抗体又はその抗原結合性断片。 - 下記の特徴の一つ以上:
-該抗体又は断片は、IL7-Rを発現している細胞におけるSTAT5のヒトIL-7誘導したリン酸化を阻害しないこと;
-該抗体又は断片は、TSLP-Rを発現している細胞におけるTARCのヒトTSLP-刺激した分泌を阻害しないこと;
-該抗体又は断片は、ヒトCD127のアゴニストではないこと;
-該抗体又は断片は、IL7-Rを発現している細胞におけるSTAT5のヒトIL-7誘導したリン酸化を増大しないこと;
-該抗体又は断片は、TSLP-Rを発現している細胞におけるTARCのヒトTSLP-刺激した分泌を増大しないこと:を有する、請求項1記載の抗体又は断片。 - 前記抗体又はその抗原結合性断片が、重鎖及び軽鎖を含み、ここで:
-該重鎖は、配列番号:14のVH-CDR1、配列番号:16のVH-CDR2、配列番号:18のVH-CDR3を含み;並びに
-該軽鎖は、配列番号:20又は26のVL-CDR1、配列番号:22のVL-CDR2、配列番号:24のVL-CDR3を含む、請求項1又は2記載の抗体又はその抗原結合性断片。 - 前記重鎖及び/又は軽鎖が、それらのフレームワーク内に、1又は複数の下記のアミノ酸残基を、又は下記のアミノ酸残基の全てを:
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、及び/又は
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基Gもしくは残基E、位置82に残基R、位置85に残基A、位置90に残基T:
Kabat付番体系に関して同定された位置に含む、請求項3記載の抗体又はその抗原結合性断片。 - 請求項3又は4記載の抗体又はその抗原結合性断片であって、それが:
(i)前記軽鎖が、配列番号:26のVL4-CDR1を含み、且つKabat付番体系に関して同定された位置73に残基Gであるアミノ酸残基を有する、前記重鎖及び軽鎖、又は
(ii)前記軽鎖が、配列番号:20のVL3-CDR1を含み、且つKabat付番体系に関して同定された位置73に残基Eであるアミノ酸残基を有する、前記重鎖及び軽鎖:を含む、前記抗体又はその抗原結合性断片。 - 前記重鎖及び/又は軽鎖が、それらのフレームワーク内に、下記のアミノ酸残基の全て:
-VH配列において:位置3に残基Q、位置15に残基G、位置16に残基G、位置21に残基T、位置80に残基T、位置87に残基S、位置91に残基E、位置95に残基T、位置118に残基L、及び/又は
-VL配列において:位置7に残基S、位置9に残基S、位置11に残基L、位置12に残基P、位置18に残基P、位置47に残基Q、位置50に残基K、位置68に残基S、位置73に残基E、位置82に残基R、位置85に残基A、位置90に残基T:
を含む、請求項4記載の抗体又はその抗原結合性断片。 - 請求項1~4のいずれか一項記載の抗体又はその抗原結合性断片であって、それが:
-そのアミノ酸配列が配列番号:2の配列であるEffi3-VH3の配列を含むか又はこれからなる重鎖;並びに
-そのアミノ酸配列が配列番号:4の配列であるEffi3-VL3の配列、又はそのアミノ酸配列が配列番号:6の配列であるEffi3-VL4の配列を含むか又はこれからなる軽鎖:
を含むか又はこれらからなる、前記抗体又はその抗原結合性断片。 - CD127-陽性細胞に対し、細胞傷害活性を有する、請求項1~7のいずれか一項記載の抗体又はその抗原結合性断片。
- ADCC活性を有する請求項8記載の抗体又はその抗原結合性断片。
- ヒトCD127-陽性細胞に対し細胞傷害活性及び/又はADCC活性を有する、請求項8又は9記載の抗体又はその抗原結合性断片。
- 前記抗体又はその抗原結合性断片のCD127への結合後にFc受容体を発現しているエフェクター免疫細胞を動員し、該動員がFc-依存性である、請求項8~10のいずれか一項記載の抗体又はその抗原結合性断片。
- 下記の断片の一つ:
-疎水性相互作用により一緒に会合された、VL鎖及びVH鎖からなるFv断片;
-VH:VLヘテロ二量体が、ジスルフィド結合によって安定化されている、dsFv断片;
-VL鎖及びVH鎖が、可動性ペプチドリンカーにより互いに接続され、その結果一本鎖タンパク質を形成している、scFv断片;
-ジスルフィド結合を介して一緒に結合された、全L鎖、及びH鎖のVH-CH1断片を含む単量体断片である、Fab断片;
-Fab’断片;
-2個のFab’断片、及び追加的に抗体のヒンジ領域の一部を含む、F(ab')2断片:
である、請求項1~11のいずれか一項記載の抗体の抗原結合性断片。 - 配列番号:55の配列を持つエピトープからなるか又はこれを含むポリペプチドを認識し、且つ任意に該ポリペプチドに対して生じる、請求項1~12のいずれか一項記載の抗体又はその抗原結合性断片。
- 前記抗体が、以下を含むか又はこれらからなるヒト化モノクローナル抗体:
-そのアミノ酸配列が配列番号:28の配列であるIgG1m-E333Aの定常領域を含む重鎖;及び
-そのアミノ酸配列が配列番号:34の配列であるCLκ定常領域を含む軽鎖;
である、請求項1~13のいずれか一項記載の抗体又はその抗原結合性断片。 - 前記重鎖が、そのアミノ酸配列が配列番号:42の配列であるEffi3-VH3-IgG1m-E333Aの配列を有する、請求項14記載の抗体。
- 前記軽鎖が、そのアミノ酸配列が配列番号:50の配列であるEffi3-VL3-CLκ、又はそのアミノ酸配列が配列番号:48の配列であるEffi3-VL4-CLκの配列を有する、請求項14又は15記載の抗体。
- 前記抗体が、以下を含むか又はこれらからなるヒト化モノクローナル抗体:
-そのアミノ酸配列が配列番号:30の配列であるIgG4m-S228Pの定常領域、又はそのアミノ酸配列が配列番号:32の配列であるIgG2bの定常領域を含む重鎖;並びに
-そのアミノ酸配列が配列番号:34の配列であるCLκ定常領域、又はそのアミノ酸配列が配列番号:36の配列であるCLλ定常配列を含む軽鎖;
である、請求項1~16のいずれか一項記載の抗体又はその抗原結合性断片。 - 請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片を含むキメラ分子であって、それが、
該分子へ、認識、結合、アンカリング、シグナル伝達の機能を集合的に提供する、複数の機能性ドメインを有する複合分子である、前記キメラ分子。 - 前記複合分子が、(i)請求項1~17のいずれか一項記載の抗体又は抗原結合性断片のscFv断片由来である、エクトドメイン、(ii)細胞膜へのアンカリングのための、膜貫通ドメイン、及び(iii)少なくとも1つの細胞内シグナル伝達ドメインを含む、エンドドメインを含む、キメラ抗原受容体(CAR)であり、
(i)、(ii)及び(iii)が、1以上の関係づけられた組換え分子(複数可)、又は、1以上の融合タンパク質(複数可)である、請求項18記載の抗体又はその抗原結合性断片を含むキメラ分子。 - 下記の特徴の少なくとも一つ:
-T細胞活性化の開始;
-T細胞媒介性細胞傷害性;
-T細胞活性化シグナルの増幅、又は該シグナルの同時刺激、を集合的に可能にする、少なくとも2、又は少なくとも3のシグナル伝達ドメインを含む、請求項19記載のキメラ抗原受容体。 - 請求項1~17のいずれか一項記載の抗体又は抗原結合性断片をコードしている、ポリヌクレオチド、又はその単離されたポリヌクレオチド。
- 配列番号:13、15、17、19、21及び23の配列、又は配列番号:13、15、17、25、21及び23の配列を含む、請求項21記載のポリヌクレオチド。
- 配列番号:1及び3の配列又は配列番号:1及び5の配列を含む、請求項22記載のポリヌクレオチド。
- 配列番号:41及び47の配列又は配列番号:41及び49の配列を含む、請求項22又は23記載のポリヌクレオチド。
- 請求項1~17のいずれか一項記載の抗体又は抗原結合性断片、請求項18又は19記載のキメラ分子、請求項20記載のキメラ抗原受容体、又は請求項21~24いずれか一項記載のポリヌクレオチドを含む、細胞。
- T細胞である、請求項25記載の細胞。
- キメラ抗原受容体(CAR)の調製の方法であって、それが:
a. 請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片をコードしているポリヌクレオチドを提供する工程;
b. 工程a)の該ポリヌクレオチドをそのC-末端で、膜貫通ドメイン、及び細胞又はT細胞、又はヒトT細胞へ、刺激シグナル(複数可)を提供するのに適した少なくとも1つの又は2つの細胞内シグナル伝達ドメイン(複数可)を、N-からC-末端へコードしているポリヌクレオチドにより組換える工程;及び
c. 工程b)において得られた組換え分子を、該細胞において発現させる工程を含む、前記方法。 - 前記生成されたキメラ抗原受容体を、ヒトCD127を発現している細胞と接触させた後、これをその特性について選択する工程をさらに含む、請求項27記載の方法。
- 活性成分として、請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片、請求項18又は19記載のキメラ分子、請求項20記載のキメラ抗原受容体、請求項25又は26記載の細胞、あるいは請求項21~24いずれか一項記載のポリヌクレオチドを含有する、医薬組成物。
- 活性成分として:
-請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片、請求項18~19記載のキメラ分子、請求項20記載のキメラ抗原受容体、請求項25又は26記載の細胞、あるいは請求項21~24いずれか一項記載のポリヌクレオチド、並びに
-化学療法薬、放射線治療薬、手術用薬剤、免疫治療薬、プロバイオティックス及び抗生物質の群から選択された、少なくとも1種の更なる治療薬:
を含む、治療組み合わせ製品であって、
ここで該活性成分が、個別治療、同時治療又は併用治療のために製剤化される、前記治療組み合わせ製品。 - 組合せ使用又は逐次使用のための、請求項30記載の治療組み合わせ製品。
- それを必要とするヒト患者への投与に適しており、且つ活性成分として:(i)請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片、請求項18又は19記載のキメラ分子、請求項20記載のキメラ抗原受容体、請求項25又は26記載の細胞、あるいは、請求項21~24いずれか一項記載のポリヌクレオチド、並びに、(ii)追加の免疫治療薬、T細胞に関与する免疫治療薬、CAR分子を保持するT細胞、あるいは、細胞受容体又は抗原を標的化するCAR分子を含有する、請求項31記載の治療組み合わせ製品。
- 癌、CD127+細胞に関連した癌、CD127陽性細胞の増殖及び/又はCD127陽性細胞の浸潤に関連した癌の治療における使用のための、請求項29記載の医薬組成物、あるいは請求項30又は31記載の治療組み合わせ製品。
- 乳癌、腎臓癌、膀胱癌、肺癌、膵臓癌の群から選択された癌の治療における使用のための、又はT細胞皮膚リンパ腫、セザリーリンパ腫の治療のための、又はIL7-R/TSLP経路の獲得型変異を有する急性リンパ芽球様白血病及び中皮腫の治療のための、請求項33記載の医薬組成物。
- 配列番号:55の配列を持つエピトープからなるポリペプチドに対し、非-ヒト動物、又は非-ヒト哺乳動物を免疫化することを含み、
CD127の細胞外ドメインに特異的に結合し、且つ下記の特徴の少なくとも一つ:
-これは、CD127のアンタゴニストではなく、且つIL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を阻害しない、並びに/又は
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を阻害しない、並びに/又は
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を増大しない、並びに/又は
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を増大しない:
を示す抗体を選択する工程を含む、請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片の製造方法。 - 前記免疫化した非-ヒト動物から得られる血清を収集し、前記ポリペプチドに対する抗体を得る工程をさらに含む、請求項35記載の抗体の製造方法。
- 前記抗体が、下記の特徴:
-これは、CD127の細胞外ドメインに特異的に結合する、並びに
-これは、CD127のアンタゴニストではない、並びに
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を阻害しない、並びに
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を阻害しない、並びに
-これは、CD127のアゴニストではない、並びに
-これは、IL7-Rを発現している細胞におけるSTAT5のIL-7誘導したリン酸化を増大しない、並びに
-これは、TSLP-Rを発現している細胞におけるTARCのTSLP-刺激した分泌を増大しない:
を有する、請求項35又は36記載の方法。 - 請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片、請求項18又は19記載のキメラ分子、又は請求項20記載のキメラ抗原受容体が、先に対象から得られた試料中のCD127+細胞の検出及び/又は定量化のために使用される、インビトロ又はエクスビボ診断のためにデータを取得する方法。
- 診断試験における使用、又は個別化医療における又はコンパニオン診断試験における使用に適した医薬品の製造における、請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片、あるいは請求項18又は19記載のキメラ分子、あるいは請求項20記載のキメラ抗原受容体の使用。
- 治療に対する対象の反応を予測するバイオマーカーとしてCD127の存在を決定することを含む、先に対象から得られた試料中のCD127+細胞の存在を決定する、インビトロ又はエクスビボ方法であって
-請求項1~17のいずれか一項記載の抗体又はその抗原結合性断片、あるいは請求項18又は19記載のキメラ分子、あるいは請求項20記載のキメラ抗原受容体を使用し、対象の腫瘍試料中のCD127の発現レベルを決定すること、並びに
-このCD127の発現レベルを、無反応対象集団におけるCD127の発現レベルの代表値と比較すること:を含み、
ここで該対象の腫瘍試料中のより高いCD127の発現レベルは、該治療に反応する対象の指標である、前記方法。 - 治療を受ける対象が癌に対する診断を受ける、請求項40記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662301271P | 2016-02-29 | 2016-02-29 | |
| US62/301,271 | 2016-02-29 | ||
| PCT/IB2017/000293 WO2017149394A1 (en) | 2016-02-29 | 2017-02-28 | Non-antagonistic antibodies directed against the alpha chain of the il7 receptor extracellular domain and use thereof in cancer treatment |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019515648A JP2019515648A (ja) | 2019-06-13 |
| JP2019515648A5 JP2019515648A5 (ja) | 2020-04-16 |
| JP7053479B2 true JP7053479B2 (ja) | 2022-04-12 |
Family
ID=58530580
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018545380A Active JP7053479B2 (ja) | 2016-02-29 | 2017-02-28 | IL7受容体細胞外ドメインα鎖に対する非拮抗性抗体及び癌治療におけるそれらの使用 |
Country Status (23)
| Country | Link |
|---|---|
| US (1) | US11230602B2 (ja) |
| EP (1) | EP3423496B1 (ja) |
| JP (1) | JP7053479B2 (ja) |
| KR (1) | KR20180118746A (ja) |
| CN (1) | CN109195987B (ja) |
| AU (1) | AU2017225495B2 (ja) |
| BR (1) | BR112018067479A2 (ja) |
| CA (1) | CA3014313A1 (ja) |
| CY (1) | CY1122072T1 (ja) |
| DK (1) | DK3423496T3 (ja) |
| ES (1) | ES2737307T3 (ja) |
| HR (1) | HRP20191445T1 (ja) |
| HU (1) | HUE045183T2 (ja) |
| IL (1) | IL261330B2 (ja) |
| LT (1) | LT3423496T (ja) |
| MA (1) | MA43767B1 (ja) |
| MD (1) | MD3423496T2 (ja) |
| ME (1) | ME03446B (ja) |
| PL (1) | PL3423496T3 (ja) |
| PT (1) | PT3423496T (ja) |
| RS (1) | RS59223B1 (ja) |
| SI (1) | SI3423496T1 (ja) |
| WO (1) | WO2017149394A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2955196A1 (en) | 2014-06-10 | 2015-12-16 | Effimune | Antibodies directed against CD127 |
| EP3676292A1 (en) * | 2017-08-29 | 2020-07-08 | OSE Immunotherapeutics | Method and preparation for sorting out t effector cells using anti-cd127 antibodies for applications in cell therapy |
| JP7530638B2 (ja) * | 2018-05-10 | 2024-08-08 | ニューラクル サイエンス カンパニー リミテッド | 配列類似性19、メンバーa5抗体を有する抗ファミリー及びその使用方法 |
| JP2022539753A (ja) * | 2019-06-28 | 2022-09-13 | ザ ユニバーシテイ オブ メルボルン | ガンマデルタt細胞を阻害する、または活性化させる方法 |
| CN110894237B (zh) * | 2019-12-05 | 2021-08-03 | 山东省分析测试中心 | 抗cd127的抗体、分泌该抗体的细胞株及其制备方法和应用 |
| WO2021222227A1 (en) * | 2020-04-27 | 2021-11-04 | Memorial Sloan-Kettering Cancer Center | Chimeric antigen receptors targeting cd127 and use thereof |
| AU2021275055A1 (en) * | 2020-05-18 | 2023-02-02 | Mouhannad Jumaa | Composition for the treatment of Philadelphia chromosome-positive acute lymphoblastic leukemia |
| CN113501878B (zh) * | 2021-02-03 | 2022-12-02 | 北京智仁美博生物科技有限公司 | 针对人tslp的多种抗体及其用途 |
| US20220389104A1 (en) * | 2021-05-28 | 2022-12-08 | Ose Immunotherapeutics | Method for Treating CD127-Positive Cancers by Administering an Anti-CD127 Agent |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010017468A1 (en) | 2008-08-08 | 2010-02-11 | Glaxo Wellcome Manufacturing Pte Ltd | Treatment of autoimmune and inflammatory disease |
| WO2011094259A2 (en) | 2010-01-28 | 2011-08-04 | Glaxo Group Limited | Cd127 binding proteins |
| WO2013056984A1 (en) | 2011-10-19 | 2013-04-25 | Effimune | Antibodies directed against the alpha chain of il7 receptor - their use for the preparation of drug candidates |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19742706B4 (de) | 1997-09-26 | 2013-07-25 | Pieris Proteolab Ag | Lipocalinmuteine |
| AU2007266450A1 (en) | 2006-05-31 | 2007-12-06 | The Regents Of The University Of California | CD127 expression inversely correlates with FoxP3 and suppressive function of CD4+ Tregs |
| EP1930342B1 (en) | 2006-12-04 | 2012-01-25 | Institut Pasteur | OB-fold used as scaffold for engineering new specific binders |
| GB0724051D0 (en) | 2007-12-08 | 2008-01-16 | Medical Res Council | Mutant proteins and methods for producing them |
| WO2010085643A1 (en) | 2009-01-22 | 2010-07-29 | University Of Miami | Targeting il-7 signaling as a therapy for multiple sclerosis and other il-7 signaling dependent disorders |
| SA114360064B1 (ar) * | 2010-02-24 | 2016-01-05 | رينات نيوروساينس كوربوريشن | طرق وأجسام مضادة معارضة ضد مستقبل il-7 |
| US20150297310A1 (en) | 2014-04-17 | 2015-10-22 | Georgia Regents Research Institute, Inc. | Methods for selecting a treatment for cancer |
| EP2955196A1 (en) * | 2014-06-10 | 2015-12-16 | Effimune | Antibodies directed against CD127 |
-
2017
- 2017-02-28 JP JP2018545380A patent/JP7053479B2/ja active Active
- 2017-02-28 IL IL261330A patent/IL261330B2/en unknown
- 2017-02-28 CA CA3014313A patent/CA3014313A1/en active Pending
- 2017-02-28 DK DK17716593.3T patent/DK3423496T3/da active
- 2017-02-28 LT LTEP17716593.3T patent/LT3423496T/lt unknown
- 2017-02-28 MD MDE20190066T patent/MD3423496T2/ro not_active IP Right Cessation
- 2017-02-28 CN CN201780014099.2A patent/CN109195987B/zh active Active
- 2017-02-28 HU HUE17716593A patent/HUE045183T2/hu unknown
- 2017-02-28 RS RSP20190987 patent/RS59223B1/sr unknown
- 2017-02-28 ES ES17716593T patent/ES2737307T3/es active Active
- 2017-02-28 MA MA43767A patent/MA43767B1/fr unknown
- 2017-02-28 KR KR1020187028377A patent/KR20180118746A/ko not_active Application Discontinuation
- 2017-02-28 PL PL17716593T patent/PL3423496T3/pl unknown
- 2017-02-28 ME MEP-2019-215A patent/ME03446B/me unknown
- 2017-02-28 WO PCT/IB2017/000293 patent/WO2017149394A1/en active Application Filing
- 2017-02-28 US US16/080,572 patent/US11230602B2/en active Active
- 2017-02-28 AU AU2017225495A patent/AU2017225495B2/en active Active
- 2017-02-28 SI SI201730078T patent/SI3423496T1/sl unknown
- 2017-02-28 BR BR112018067479A patent/BR112018067479A2/pt unknown
- 2017-02-28 EP EP17716593.3A patent/EP3423496B1/en active Active
- 2017-02-28 PT PT17716593T patent/PT3423496T/pt unknown
-
2019
- 2019-08-09 HR HRP20191445 patent/HRP20191445T1/hr unknown
- 2019-08-23 CY CY20191100905T patent/CY1122072T1/el unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010017468A1 (en) | 2008-08-08 | 2010-02-11 | Glaxo Wellcome Manufacturing Pte Ltd | Treatment of autoimmune and inflammatory disease |
| WO2011094259A2 (en) | 2010-01-28 | 2011-08-04 | Glaxo Group Limited | Cd127 binding proteins |
| WO2013056984A1 (en) | 2011-10-19 | 2013-04-25 | Effimune | Antibodies directed against the alpha chain of il7 receptor - their use for the preparation of drug candidates |
Non-Patent Citations (1)
| Title |
|---|
| CHUNG B. et al.,Blood,110(8)(2007),p.2803-2810 |
Also Published As
| Publication number | Publication date |
|---|---|
| LT3423496T (lt) | 2019-09-25 |
| ME03446B (me) | 2020-01-20 |
| ES2737307T3 (es) | 2020-01-13 |
| AU2017225495A1 (en) | 2018-08-23 |
| HRP20191445T1 (hr) | 2019-11-15 |
| WO2017149394A1 (en) | 2017-09-08 |
| JP2019515648A (ja) | 2019-06-13 |
| RS59223B1 (sr) | 2019-10-31 |
| EP3423496A1 (en) | 2019-01-09 |
| PL3423496T3 (pl) | 2020-01-31 |
| CY1122072T1 (el) | 2020-11-25 |
| CA3014313A1 (en) | 2017-09-08 |
| CN109195987B (zh) | 2022-05-27 |
| KR20180118746A (ko) | 2018-10-31 |
| BR112018067479A2 (pt) | 2019-01-15 |
| AU2017225495B2 (en) | 2024-05-09 |
| MD3423496T2 (ro) | 2020-01-31 |
| IL261330B2 (en) | 2023-03-01 |
| CN109195987A (zh) | 2019-01-11 |
| IL261330A (en) | 2018-10-31 |
| MA43767B1 (fr) | 2019-08-30 |
| DK3423496T3 (da) | 2019-08-19 |
| IL261330B (en) | 2022-11-01 |
| US20200308288A1 (en) | 2020-10-01 |
| MA43767A (fr) | 2019-01-09 |
| US11230602B2 (en) | 2022-01-25 |
| PT3423496T (pt) | 2019-09-05 |
| SI3423496T1 (sl) | 2019-10-30 |
| EP3423496B1 (en) | 2019-07-03 |
| HUE045183T2 (hu) | 2019-12-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7053479B2 (ja) | IL7受容体細胞外ドメインα鎖に対する非拮抗性抗体及び癌治療におけるそれらの使用 | |
| CN110366560B (zh) | 抗b7-h4抗体、其抗原结合片段及其医药用途 | |
| KR20200105849A (ko) | 항-tigit 항체 및 치료제 및 진단제로서 이의 용도 | |
| JP7324565B2 (ja) | Cd127に対する抗体 | |
| US11555077B2 (en) | 4-1BB antibody and preparation method and use thereof | |
| US11525005B2 (en) | Anti-CD40 antibody, antigen binding fragment thereof and medical use thereof | |
| WO2018161872A1 (zh) | 抗b7-h3抗体、其抗原结合片段及其医药用途 | |
| KR20200061320A (ko) | 세포독성 t-림프구-관련 단백질 4 (ctla-4)에 대한 신규의 단일클론 항체 | |
| CN112969714B (zh) | 抗cd40抗体、其抗原结合片段及其医药用途 | |
| WO2021228218A1 (zh) | 抗cd25抗体、其抗原结合片段及其医药用途 | |
| JP2020532279A (ja) | 抗gitr抗体、その抗原結合性断片、およびその医薬用途 | |
| CN114008077A (zh) | 抗体和使用方法 | |
| RU2792748C2 (ru) | Антитело к b7-h4, его антигенсвязывающий фрагмент и его фармацевтическое применение | |
| RU2779649C1 (ru) | Антитело, связывающее человеческий il-4r, его антигенсвязывающий фрагмент и его медицинское применение | |
| RU2779128C2 (ru) | Антитело к cd40, его антигенсвязывающий фрагмент и его медицинское применение |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181129 |
|
| A529 | Written submission of copy of amendment under article 34 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A529 Effective date: 20181026 |
|
| A59 | Written plea |
Free format text: JAPANESE INTERMEDIATE CODE: A59 Effective date: 20190116 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20190116 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200227 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210330 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210629 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211124 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220222 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220308 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220331 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7053479 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |