JP6916768B2 - 内視鏡システム - Google Patents
内視鏡システム Download PDFInfo
- Publication number
- JP6916768B2 JP6916768B2 JP2018165806A JP2018165806A JP6916768B2 JP 6916768 B2 JP6916768 B2 JP 6916768B2 JP 2018165806 A JP2018165806 A JP 2018165806A JP 2018165806 A JP2018165806 A JP 2018165806A JP 6916768 B2 JP6916768 B2 JP 6916768B2
- Authority
- JP
- Japan
- Prior art keywords
- light
- amount
- light source
- image
- unit
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000005286 illumination Methods 0.000 claims description 129
- 238000004364 calculation method Methods 0.000 claims description 91
- 238000005259 measurement Methods 0.000 claims description 29
- 238000000034 method Methods 0.000 description 48
- 239000004065 semiconductor Substances 0.000 description 30
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 29
- 229910052760 oxygen Inorganic materials 0.000 description 29
- 239000001301 oxygen Substances 0.000 description 29
- 238000012545 processing Methods 0.000 description 29
- 230000035945 sensitivity Effects 0.000 description 28
- 230000003595 spectral effect Effects 0.000 description 27
- 230000008569 process Effects 0.000 description 26
- 238000012937 correction Methods 0.000 description 22
- 238000006243 chemical reaction Methods 0.000 description 19
- 210000004204 blood vessel Anatomy 0.000 description 18
- 238000000295 emission spectrum Methods 0.000 description 18
- 238000003384 imaging method Methods 0.000 description 18
- 102000001554 Hemoglobins Human genes 0.000 description 12
- 108010054147 Hemoglobins Proteins 0.000 description 12
- 230000008859 change Effects 0.000 description 12
- 230000004044 response Effects 0.000 description 12
- 238000010586 diagram Methods 0.000 description 10
- 230000003287 optical effect Effects 0.000 description 10
- 230000008033 biological extinction Effects 0.000 description 9
- 230000000295 complement effect Effects 0.000 description 7
- 238000005070 sampling Methods 0.000 description 7
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 6
- 238000004891 communication Methods 0.000 description 6
- 230000001965 increasing effect Effects 0.000 description 6
- 238000003780 insertion Methods 0.000 description 6
- 230000037431 insertion Effects 0.000 description 6
- 239000008280 blood Substances 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 238000009825 accumulation Methods 0.000 description 4
- 239000003086 colorant Substances 0.000 description 4
- 230000005284 excitation Effects 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- 230000007547 defect Effects 0.000 description 3
- 229910044991 metal oxide Inorganic materials 0.000 description 3
- 150000004706 metal oxides Chemical class 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 2
- UQMRAFJOBWOFNS-UHFFFAOYSA-N butyl 2-(2,4-dichlorophenoxy)acetate Chemical compound CCCCOC(=O)COC1=CC=C(Cl)C=C1Cl UQMRAFJOBWOFNS-UHFFFAOYSA-N 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 239000008400 supply water Substances 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 229910052724 xenon Inorganic materials 0.000 description 2
- FHNFHKCVQCLJFQ-UHFFFAOYSA-N xenon atom Chemical compound [Xe] FHNFHKCVQCLJFQ-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000009434 installation Methods 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 230000001360 synchronised effect Effects 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/00002—Operational features of endoscopes
- A61B1/00004—Operational features of endoscopes characterised by electronic signal processing
- A61B1/00009—Operational features of endoscopes characterised by electronic signal processing of image signals during a use of endoscope
- A61B1/000094—Operational features of endoscopes characterised by electronic signal processing of image signals during a use of endoscope extracting biological structures
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/00002—Operational features of endoscopes
- A61B1/00004—Operational features of endoscopes characterised by electronic signal processing
- A61B1/00006—Operational features of endoscopes characterised by electronic signal processing of control signals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/04—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor combined with photographic or television appliances
- A61B1/044—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor combined with photographic or television appliances for absorption imaging
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/06—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor with illuminating arrangements
- A61B1/0638—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor with illuminating arrangements providing two or more wavelengths
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/06—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor with illuminating arrangements
- A61B1/0655—Control therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/06—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor with illuminating arrangements
- A61B1/0661—Endoscope light sources
- A61B1/0669—Endoscope light sources at proximal end of an endoscope
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/06—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor with illuminating arrangements
- A61B1/0661—Endoscope light sources
- A61B1/0676—Endoscope light sources at distal tip of an endoscope
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/1455—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using optical sensors, e.g. spectral photometrical oximeters
- A61B5/1459—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using optical sensors, e.g. spectral photometrical oximeters invasive, e.g. introduced into the body by a catheter
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B23/00—Telescopes, e.g. binoculars; Periscopes; Instruments for viewing the inside of hollow bodies; Viewfinders; Optical aiming or sighting devices
- G02B23/24—Instruments or systems for viewing the inside of hollow bodies, e.g. fibrescopes
- G02B23/2407—Optical details
- G02B23/2461—Illumination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/06—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor with illuminating arrangements
- A61B1/0661—Endoscope light sources
- A61B1/0684—Endoscope light sources using light emitting diodes [LED]
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Surgery (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Optics & Photonics (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pathology (AREA)
- Public Health (AREA)
- Biophysics (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Medical Informatics (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Radiology & Medical Imaging (AREA)
- Signal Processing (AREA)
- Astronomy & Astrophysics (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Endoscopes (AREA)
- Instruments For Viewing The Inside Of Hollow Bodies (AREA)
Description
従来、内視鏡用光源装置には、照明光として白色光を発するキセノンランプ、およびハロゲンランプ等のランプ光源が使用されていたが、最近では、ランプ光源に代えて、特定の色の光を発するレーザダイオード(LD: Laser Diode)または発光ダイオード(LED: Light Emitting Diode)等の半導体光源が用いられつつある。省エネルギー化、長寿命化、および狭帯域光観察機能の搭載のためにも、上述の半導体光源を利用することは有効である。
マルチフレーム観察モードを実施できる内視鏡システムとして、例えば、特許文献1の内視鏡システムがある。
特許文献1の内視鏡システムでは、照明光を発生する光源部と、画素に電荷を蓄積し得る最大期間である蓄積期間と画素から信号を読み出す読出期間とからなる撮像フレームの単位で照明光を用いて観察対象を撮像するイメージセンサーと、撮像フレーム毎に照明光の波長帯域または分光スペクトルを変更する光源制御部と、照明光の波長帯域または分光スペクトルが異なる複数の撮像フレームにおいて取得する複数の撮像画像を用いて1つの観察画像を生成する画像処理部と、観察画像の生成に使用する複数の撮像画像を得る複数の撮像フレームの蓄積期間および読出期間の合計時間を一定に保ち、かつ、一定の合計時間において各々の撮像フレームの蓄積期間または読出期間の長さを延長または短縮する撮像制御部とを備えている。
特許文献2には、通常光観察から特殊光観察に切り替えられた直後の所定時間、紫色レーザ光の発光量はオーバーシュートすることが記載されている。紫色レーザ光の発光量のオーバーシュートを低減するために、紫色レーザ光源が完全に消灯とならないように制御することが記載されている。
酸素飽和度イメージングは、照明波長を切り替えて複数の画像を取得し、組織酸素飽和度に関連した1枚の画像を生成している。いわゆる、マルチフレーム画像処理を実施している。通常の内視鏡照明は観察中に連続点灯しているのに対して、酸素飽和度イメージングでは、撮像フレームに同期して各照明光を短時間で完全に消灯し、点灯する必要がある。
1つの画像を得るために消灯から点灯に転ずるときに、半導体光源のオーバーシュートまたは応答遅れが生じる。上述のオーバーシュートまたは応答遅れによって、1フレーム目の発光量と2フレーム目の発光量の比率関係が所定の範囲から外れると、2つの画像信号の比も変わってしまうため、正しく酸素飽和度を算出できない。特に、酸素飽和度等の定量指標を画像化する観察機能では、照明光を短時間で完全に消灯し、点灯しており、オーバーシュートおよび応答遅れが及ぼす誤差影響は、従来の白色光観察および画像強調観察よりも大きく、高精度な制御が求められるが、十分に対策が取られていない。
なお、半導体光源はスイッチングレギュレータ回路で制御することが多く、スイッチング周波数をアップすると負荷応答が良くなるが、電力効率が悪くなり高い熱が発生するため、高出力化が難しい。
複数の光源にそれぞれ設けられており、複数の光源の光の一部を受光し、複数の光源の発光量の情報を得る光検出器と、複数の光源のうち、少なくとも1つの光源から射出される光により構成される第1の照明光と第2の照明光とを少なくとも用いて、各照明光毎に観察対象の画像を取得する画像取得部と、画像取得部で取得された複数の画像における相互間の画像信号比を一定にする制御部とを有する、内視鏡システムを提供するものである。
第1の照明光と、第2の照明光とは、異なる光源から出射されていることが好ましい。
第1の照明光と、第2の照明光とは、同一の光源から出射されていることが好ましい。
光源を点灯してから、定められた誤差算出期間における光検出器で得られた積算光量を得る計測部と、計測部で得られた積算光量と、目標光量との差を得る誤差算出部とを有し、制御部は、誤差算出部で得られた差に応じて、誤差算出期間以降の光源の消灯タイミングを変更することにより、定められた露光期間内の積分光量を一定にすることが好ましい。
光源を点灯してから、定められた誤差算出期間における光検出器で得られた積算光量を得る計測部と、計測部で得られた積算光量と、目標光量との差を得る誤差算出部とを有し、制御部は、第1の照明光における誤差算出部で得られた差に応じて、第2の照明光の消灯タイミングを変更することにより、複数の画像間における、定められた露光期間内での積分光量の比率を一定にすることが好ましい。
光検出器は、フォトダイオードであることが好ましい。
なお、以下に説明する図は、本発明を説明するための例示的なものであり、以下に示す図に本発明が限定されるものではない。
なお、以下において数値範囲を示す「〜」とは両側に記載された数値を含む。例えば、εが数値α〜数値βとは、εの範囲は数値αと数値βを含む範囲であり、数学記号で示せばα≦ε≦βである。
「平行」等は、特に記載がなければ、該当する技術分野で一般的に許容される誤差範囲を含む。また、「同一」とは、該当する技術分野で一般的に許容される誤差範囲を含む。
一般的には、青色の波長は約445nmから約485nm程度であり、例えば、青色と緑色との中間の色は例えば青緑と称して青色とは区別する場合がある。しかし、内視鏡システム10においては、少なくとも光源部の各光源が出射する光について色の種類(色の名称)を過剰に細分化する必要がない。このため、約440nm以上約490nm未満の波長を有する光の色を青色という。また、約490nm以上約600nm未満の波長を有する光の色を緑色といい、かつ約600nm以上約680nm未満の波長を有する光の色を赤色という。そして、上述の青色の波長の下限である「約440nm」未満の波長を有する可視光、例えば、約380nm以上約440nm未満の可視光の色を紫色といい、紫色よりも短波長であるがイメージセンサー48が感度を有する光の色を表す場合に紫外という。また、上述の赤色の波長の上限である「約680nm」以上の波長を有し、かつイメージセンサー48が感度を有する光の色を表す場合に赤外という。また、「広帯域」とは、波長範囲が複数の色の波長範囲に及ぶことをいう。白色とは少なくとも上述の青色または紫色に属する光と、緑色に属する光と、赤色に属する色の光と、を含む光の色をいう。
図1は本発明の実施形態の内視鏡システムの一例を概念的に示す斜視図であり、図2は本発明の実施形態の内視鏡システムの一例を概念的に示すブロック図である。
図1に示すように、内視鏡システム10は、観察対象である生体内(被検体内)の観察部位を撮像する内視鏡スコープ(以下、単に内視鏡ともいう)12と、撮像により得られた画像信号に基づいて観察部位の表示画像を生成するプロセッサ装置16と、観察部位を照射する照明光を内視鏡12に供給する内視鏡用光源装置(以下、単に光源装置という)14と、表示画像を表示するモニタ18とを備えている。プロセッサ装置16には、キーボードおよびマウス等の操作入力部であるコンソール19が接続されている。
マルチフレーム観察モードにおいては、複数の撮像フレームにおいて得られる複数の撮像画像を用いて1つの観察画像を生成する。後述の血管強調観察モードがシングルフレーム観察モードに該当する。
また、内視鏡システム10は、観察部位を観察するための通常観察モードと、観察部位の粘膜内部に存在する血管を強調して観察するための血管強調観察モードとが実行可能である。また、観察対象の酸素飽和度を算出し、算出した酸素飽和度を表す観察画像(以下、酸素飽和度画像という)を生成し、表示する酸素飽和度観察モードを有する。
血管強調観察モードは、血管情報として血管のパターンを可視化して、腫瘍の良悪鑑別等の診断を行うためのモードである。この血管強調観察モードでは、血中ヘモグロビンに対する吸光度が高い特定の波長帯域の光の成分を多く含む照明光を観察部位に照射する。
通常観察モードでは、観察部位の全体の観察に適した通常観察画像が表示画像として生成される。血管強調観察モードでは、血管のパターンの観察に適した血管強調観察画像が表示画像として生成される。
ユニバーサルコード17には、挿入部12aから延設される通信ケーブルまたはライトガイド41(図2参照)が挿通されており、プロセッサ装置16および光源装置14側の一端には、コネクタが取り付けられている。コネクタは、通信用コネクタと光源用コネクタからなる複合タイプのコネクタである。通信用コネクタと光源用コネクタはそれぞれ、プロセッサ装置16および光源装置14に着脱自在に接続される。通信用コネクタには通信ケーブルの一端が配設されている。光源用コネクタにはライトガイド41の入射端が配設されている。
この場合、光源部20には、後述するように光検出器91、92、93(図5参照)が設けられており、光検出器91、92、93(図5参照)が検出した各光源の光量の情報が光源制御部22に入力されて、各光源の光量の情報が得られる。各光源の光量の情報と、イメージセンサー48の輝度値とに基づいて光源部20の光源の発光量を自動的に正確に制御する。
なお、ズームレンズ47は、ズーム操作部13aの操作をすることで移動する。その結果、イメージセンサー48を用いて撮影する観察対象を拡大または縮小して観察する。
イメージセンサー48は、例えば、1フレームの取得期間内で、画素に信号電荷を蓄積する蓄積動作と、蓄積した信号電荷を読み出す読み出し動作を行う。光源装置14は、イメージセンサー48の蓄積動作のタイミングに合わせて照明光を生成し、ライトガイド41に入射させる。
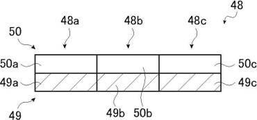
イメージセンサー48では、第1の素子部48aは、光電変換機能を有する第1画素49aと、第1色成分に対する分光感度を有する第1フィルター50aとを有する。イメージセンサー48に入射された光に応じて第1の素子部48aでは第1色成分の第1の信号値が得られる。
第2の素子部48bは、光電変換機能を有する第2画素49bと、第2色成分に対する分光感度を有する第2フィルター50bとを有する。イメージセンサー48に入射された光に応じて第2の素子部48bでは第2色成分の第2の信号値が得られる。
第3の素子部48cは、光電変換機能を有する第3画素49cと、第3色成分に対する分光感度を有する第3フィルター50cとを有する。第3色成分は、第1色成分および第2色成分以外の色のことである。イメージセンサー48に入射された光に応じて第3の素子部48cでは第3色成分の第3の信号値が得られる。
第1画素49a、第2画素49bおよび第3画素49cの各画素のうち、Rカラーフィルタを有する画素がR画素であり、Gカラーフィルタを有する画素がG画素であり、かつ、Bカラーフィルタを有する画素がB画素である。イメージセンサー48のセンサー信号として、R画素からR信号が得られ、G画素からG信号が得られ、およびB画素からB信号が得られる。R信号、G信号およびB信号が画像信号としてDSP56に入力される。
このように、イメージセンサー48は、例えば、R画素、G画素、およびB画素の3色の画素を有するので、照明光に白色光を使用して観察対象を撮影すると、R画素で観察対象を撮影して得るR画像、G画素で観察対象を撮影して得るG画像、およびB画素で観察対象を撮影して得るB画像が同時に得られる。
複数の画像における相互間の画像信号比を一定にするとは、複数の画像において、それぞれの画像同士のR画素の値、G画素の値、およびB画素の値の比率が同じであることである。上述の比率が同じであれば、各画像の画像データに基づき定量化、数値化できる。例えば、酸素飽和度、血液量等を求める際に精度を高くできる。
また、上述の比率が同じであれば、画像の明るさが違っても色味等変わらず、観察画像としては同じである。このため、通常観察モードにおいても、優れた画質が得られる。
なお、例えば、上述のR信号の信号値が第2の信号値に相当し、G信号の信号値が第1の信号値に相当し、B信号の信号値が第3の信号値に相当する。
画像取得部54は、イメージセンサー48の各画素から画像信号を得て、イメージセンサー48を用いて観察対象を撮影して得る複数色の撮影画像を取得する。具体的には、画像取得部54は、撮影フレーム毎に、B画像、G画像、およびR画像の組を取得する。また、画像取得部54は、DSP56と、ノイズ低減部58と、変換部59とを有し、これらを用いて、取得した撮影画像に各種処理を施す。イメージセンサー48の各画素から、センサー信号として得られた、例えば、R信号、G信号およびB信号が補正量算出部60および制御部69に出力される。
オフセット処理は、欠陥補正処理を施した画像から暗電流成分を低減し、正確な零レベルを設定する処理である。
ゲイン補正処理は、オフセット処理をした画像にゲインを乗じることにより各画像の信号レベルを整える処理である。
リニアマトリクス処理は、オフセット処理をした画像の色再現性を高める処理であり、ガンマ変換処理は、リニアマトリクス処理後の画像の明るさまたは彩度を整える処理である。
デモザイク処理(等方化処理または同時化処理とも言う)は、欠落した画素の画素値を補間する処理であり、ガンマ変換処理後の画像に対して施す。欠落した画素とは、カラーフィルタの配列のため、イメージセンサー48において他の色の画素を配置しているために、画素値がない画素である。例えば、B画像はB画素において観察対象を撮影して得る画像なので、イメージセンサー48のG画素およびR画素に対応する位置の画素には画素値がない。デモザイク処理は、B画像を補間して、イメージセンサー48のG画素およびR画素の位置にある画素の画素値を生成する。
YC変換処理は、デモザイク処理後の画像を、輝度チャンネルYと色差チャンネルCbおよび色差チャンネルCrに変換する処理である。
変換部59は、ノイズ低減処理後の輝度チャンネルY、色差チャンネルCbおよび色差チャンネルCrを再びBGRの各色の画像に再変換する。
補正量算出部60は、内視鏡画像の色味を維持するための補正するものであり、後述の補正係数を算出したり、補正係数を記憶したりする。
制御部69は、イメージセンサー48の動作を制御する撮像制御部70を備える。
なお、内視鏡システム10が複数の観察モードを有する場合、制御部69は、モード切替スイッチ13bからの操作入力を受けることにより、光源制御部22を介して照明光を切り替える。これにより、観察モードが切り替わる。光源制御部22は制御部69に含まれる。
撮像制御部70は、シングルフレーム観察モードの場合、蓄積期間と読出期間を一定の時間毎に、例えば、1/60秒毎に交互に繰り返すようにイメージセンサー48を制御する。したがって、シングルフレーム観察モードにおいては、撮像フレームの長さは一定である。
撮像制御部70は、イメージセンサー48の電子シャッター(図示せず)のシャッタ速度を調整するものである。例えば、マルチフレーム観察モードの場合、電子シャッターのシャッタ速度を変更する。
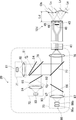
図5に示す光源装置14の光源部20は、異なる波長の光を射出する複数の光源を有するものであり、例えば、互いに異なる波長の光を射出する4つの光源を有する。
光源部20は、第1の光源71と、第2の光源72と、第3の光源73と、第4の光源74とを有する。第1の光源71、第2の光源72、第3の光源73および第4の光源74は各々独立に、光量および消灯タイミング等を制御可能である。また、光源部20には、第1の光源71、第2の光源72、第3の光源73および第4の光源74の各光源の発光素子を冷却する、ヒートシンク等の冷却部材を備える。
光源装置14では、光源部20から出射された光はライトガイド41を通過して照明光Lsとして対象物Obに照射される。対象物Obに照射された照明光Lsの反射光Lrが対物レンズ46を介してイメージセンサー48に入射される。
第1の光源71と合波部材76との間にビームスプリッタ94が設けられている。ビームスプリッタ94により第1の光源71が出射した第1の光の一部を所定割合で反射する。ビームスプリッタ94が反射した反射した光は、光検出器91で受光される。光源制御部22は、光検出器91が検出した光量を用いて第1の光源71の第1の光の発光量を自動的に正確に制御する機能を有する。
第2の光源72と合波部材76との間にビームスプリッタ95が設けられている。ビームスプリッタ95により第2の光源72が出射した第2の光の一部を所定割合で反射する。ビームスプリッタ95が反射した反射した光は、光検出器92で受光される。光源制御部22は、光検出器92が検出した光量を用いて第2の光源72の第2の光の発光量を自動的に正確に制御する機能を有する。
第3の光源73と合波部材79との間にビームスプリッタ96が設けられている。ビームスプリッタ96により第3の光源73が出射した第3の光の一部を所定割合で反射する。ビームスプリッタ96が反射した反射した光は、光検出器93で受光される。光源制御部22は、光検出器93が検出した光量を用いて第3の光源73の第3の光の発光量を自動的に正確に制御する機能を有する。
第4の光源74と合波部材79との間にビームスプリッタ98が設けられている。ビームスプリッタ98により第4の光源74が出射した第4の光の一部を所定割合で反射する。ビームスプリッタ98が反射した反射した光は、光検出器97で受光される。光源制御部22は、光検出器97が検出した光量を用いて第4の光源74の第4の光の発光量を自動的に正確に制御する機能を有する。
光検出器91、92、93、97は、各光源の発光量の情報を得るものであり、例えば、光電効果を利用した光電子増倍管、光照射による電気抵抗変化を利用したCdS、PbS等の光電導素子、または半導体のpn接合を利用した光起電力型のフォトダイオード等である。
発光素子86は、例えば、互いに波長の異なる2つの色成分を含む光を第3の光として出射するものである。発光素子86は、例えば、励起光を発光する発光素子86aと、発光素子86aが発光した励起光が入射することによって、互いに波長の異なる2つの色成分を含む光を発光する蛍光体86bとを有する。
第3の光源73において、第3の光源73は、例えば、第1色成分が緑、第2色成分が赤の、互いに波長の異なる2つの色成分を含む緑色成分からなる光(以下、緑色光という)を出射するものである。緑色光のことを、緑色を示す光ともいう。
例えば、発光素子86aが発光する励起光は、約445nmにピークを有する青色光であり、蛍光体86bが発光する光が緑色成分の他に赤色成分を含む広帯域な緑色光である。赤色成分からなる光のことを、赤色光といい、赤色光のことを、赤色を示す光ともいう。
なお、発光素子86は、例えば、第1色成分が緑、第2色成分が赤の、互いに波長の異なる2つの色成分を含む緑色光を出射するものでもよい。この場合も、発光素子86は、例えば、LED(発光ダイオード)またはLD等の半導体素子である。
また、主波長の異なる2以上の光源において、主波長が異なるとは、各光源が出射する光のピーク波長、ピーク波長がなければ中心波長が同一波長ではないことをいう。ピーク波長または中心波長の同一の範囲は、内視鏡システム10の仕様等に応じて適宜決定されるものである。
なお、特定光は、用途が限定されているため、狭帯域であることが好ましい。狭帯域とは、内視鏡システム10において概ね単波長であるとみなせる程度に狭い波長帯域を言う。例えば、中心波長に対して数10nm幅の波長帯域が狭帯域である。
また、各種の観察画像の取得にも狭帯域の特定光が用いられる。例えば、特定の深さにある組織または構造を選択的に強調した観察画像(以下、特定深さ強調画像という)、粘膜下の特に深い位置にある太い血管(以下、深層血管という)を強調する観察画像(以下、深層血管強調画像という)である。これ以外に、観察画像としていわゆる狭帯域観察画像がある。狭帯域観察画像とは、青色および緑色の狭帯域光を用いて観察対象を撮像し、得られた撮像画像を用いて、血管等を強調した観察画像である。
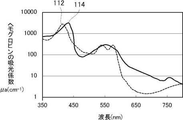
また、酸素飽和度の測定には狭帯域光が用いられる。狭帯域光は、酸化ヘモグロビンの吸光係数と還元ヘモグロビンの吸光係数との差が大きい波長を中心波長に有する光である。後述の図15に示すが、例えば、約470nmの波長において、酸化ヘモグロビンの吸光係数と還元ヘモグロビンの吸光係数の差が大きくなる。酸素飽和度の測定には、中心波長が約470nmの狭帯域光を用いることができる。
第3の光源73が、第1色成分が緑、第2色成分が赤の緑色光を出射し、第1の光源71が青色光を出射する場合、通常観察モード時には、第3の光源73が出射した緑色光と赤色光を含む光と、第1の光源71が出射した青色光とを合波して、広帯域の白色光を生成する。一方、血管強調観察モード時には、白色光に、血中ヘモグロビンに対する吸光度が高い紫色光を混合した混合光を生成する。なお、光源制御部22は、血管強調観察モード時では青色光より紫色光のほうが支配的となるように、青色光の光量の割合を下げる。
なお、上述の第1の光源71、第2の光源72、第3の光源73および第4の光源74は、いずれも上述の構成に限定されるものではなく、半導体光源と、半導体光源が発光する光を励起光として他の色の光を発光する蛍光体等を組み合わせて用いてもよい。キセノンランプ等のランプ光源も使用してもよい。また、半導体光源、半導体光源と蛍光体、およびランプ光源と、波長帯域または分光スペクトルを調節する光学フィルタとを組み合わせた構成の光源でもよい。例えば、白色LEDに光学フィルタを組み合わせた構成の光源でもよい。
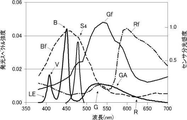
ここで、図6は本発明の実施形態の内視鏡システムの光源部の発光スペクトルおよびイメージセンサーの分光感度の一例を示すグラフである。
なお、図6に示す発光スペクトルLEにおいて、符号Vは紫色光を示し、符号Bは青色光を示し、符号Gは緑色光を示し、符号Rは赤色光を示す。符号GAは、緑色光と赤色光とを含む色を示す。符号S4は、第4の光源が出射する波長約470nmの光を示す。また、図6に示す発光スペクトルLEにおいて、実線で示すものは相対的に光量が低いものであり、破線で示すものは相対的に光量が高いものである。
波長470nm〜700nmの光は、第3の光源73により出射された緑色光によるものであり、色成分として緑と赤とを含む。
また、第1の光源71は、第1の素子部48aの分光感度のピーク波長と第2の素子部48bの分光感度のピーク波長との間に発光ピークがある発光ダイオードを有する構成でもよい。この場合、第1の素子部48aが分光感度Gfであり、第2の素子部48bが分光感度Rfであれば、波長550〜600nmに発光ピークがある発光ダイオードが用いられる。第1の素子部48aが分光感度Bfであり、第2の素子部48bが分光感度Gfであれば、波長450〜550nmに発光ピークがある発光ダイオードが用いられる。
なお、光源としては、上述の構成以外に第1の光源71が赤色光を射出する光源、第2の光源72が緑色光を射出する光源、第3の光源73が青色光を射出する光源であってもよい。
そして、第1の信号値と第2の信号値とを、DSP56から補正量算出部60に出力する。補正量算出部60にて、第1の信号値と第2の信号値との信号比を求め、第1の信号値および第2の信号値のうち、少なくとも1つの信号値を変えることによって、信号比を予め定められた設定値に設定する。
また、光量に応じて、第1の信号値、第2の信号値および第3の信号値のうち、少なくとも1つの信号値を変えることによって、信号比を予め定められた設定値に設定するようにしてもよい。この場合、光量に応じて変える第1の信号値、第2の信号値または第3の信号値を決定し、かつ変える値を補正係数として求め、補正係数を補正量算出部60に記憶させる。
この場合、補正量算出部60において、基準値となる第1の信号値、第2の信号値または第3の信号値を決定し、光量に応じて変える第1の信号値、第2の信号値または第3の信号値を決定し、かつ変える値を補正係数として求め、補正係数を補正量算出部60に記憶させる。
なお、上述では1つの信号値を基準値としたが、これに限定されるものではない。基準値を設定することなく、光量に応じて、第1の信号値、第2の信号値および第3の信号値のうち、少なくとも1つの信号値を変えることによって、信号比を予め定められた設定値に設定してもよい。
各光検出器91、92、93、97は、ビームスプリッタ94、95、96、98により反射された光を受光して、図7に示すように、受光した各光の光量に応じた光量測定信号を出力し、これを光源制御部22に出力する。光源制御部22は、光量測定信号と目標とする光量(以下、単に目標光量という)とを比較し、この比較結果に基づいて、光量が目標光量値となるように、第1の光源71、第2の光源72、第3の光源73および第4の光源74に与える駆動信号を光源駆動部21において調整させるフィードバック制御を実施している。図7に示すフィードバック制御のことを、APC(Auto Power Control)という。なお、光源制御部22は、目標光量が記憶されているか、または制御部69から目標光量値が入力される。
上述のように第1の光源71、第2の光源72、第3の光源73および第4の光源74の各光量を光検出器91、92、93、97で常に監視し、光量の測定結果に基づき与える駆動信号を調整することにより、常に目標光量値に合うように光量を制御することができる。光量の測定精度は戻り光が抑制されているため高い。このため、目標とする発光スペクトルの照明光をより高い精度で安定して得ることができる。なお、光源部20の構成は上述の図5に示す構成に限定されるものではない。
計測部23は、光源を点灯してから、定められた誤差算出期間における光検出器で得られた積算光量を得るものである。誤差算出期間は、例えば、光源が光を発光している総時間を示す露光期間に対して設定される。誤差算出期間は、例えば、露光期間の半分であり、光源を点灯してから時間がカウントされる。
誤差算出部24は、計測部で得られた積算光量と、目標光量との差を得るものである。このため、誤差算出部24は、目標光量が予め記憶されているか、光源制御部22に記憶された目標光量値が入力される。
なお、計測部23と誤差算出部24とを、それぞれ1つ設ける構成としたが、光検出器91、92、93、97毎に設ける構成でもよい。この場合、光検出器の数に応じた計測部と誤差算出部とが設けられる。
次に、内視鏡システム10の制御方法について説明する。
内視鏡システム10では、例えば、第4の光源74が、第1色成分が緑、第2色成分が赤の緑色光を出射し、第1の光源71が青色光を出射する場合、通常観察モード時には、第4の光源74が出射した緑色光と赤色光を含む光と、第1の光源71が出射した青色光とを合波して、広帯域の白色光を生成する。この白色光がライトガイド41に入射され、ライトガイド41から照明光Ls(図5参照)として白色光が対象物Obに照射される。
また、マルチフレーム観察モード時においては、光源制御部22は、上述の各光源の制御の結果、観察画像の生成に使用する複数の撮像画像を得る各々の撮像フレーム毎に照明光の波長帯域または分光スペクトルを変更する。なお、点灯とは、イメージセンサー48において観察対象を撮像できる程度、すなわち、観察画像において観察対象の像を視認できる程度の光量で発光することをいう。点灯のことをオンともいう。
消灯とは、完全に発光を停止することの他、イメージセンサー48において観察対象を撮像し得ない程度の光量に減光することを含む。消灯のことをオフともいう。
マルチフレーム点灯制御の場合、照明光Lsを完全にオンオフする必要があり、必ず照明光Lsの消灯状態が生じる。消灯状態から点灯状態にする際に、オーバーシュート、または発光の時間遅れが生じやすい。
また、光源部20は、被写体距離に応じた広いダイナミックレンジでの光量制御が必要であり、光領域によってオーバーシュート具合も異なり、制御条件または光源駆動部21を構成する駆動回路特性を最適化させることが難しい。
上述のように内視鏡システム10の光源部20は、上述のように各光源に対して、図7に示すようにAPCと呼ばれるフィードバック制御機能を設けている。しかしながら、APCでは、例えば、1つの画像を得るための1フレームのような短時期間に発生するオーバーシュートおよび発光遅れに対して対応できない。そこで、本発明では、以下のように制御することにより、光源による照明光を完全に消灯し、点灯させて、各照明光毎に観察対象の画像を取得しても、複数の画像における相互間の画像信号比を一定にすることができる。
制御方法では、各光源の光量をモニターする光検出器は、例えば、PD(フォトダイオード)で構成されている。フォトダイオードで発生した、光量に応じた電流は電圧変換され、さらにADC(Analog-to-Digital Converter)で、例えば、16ビットのデジタル値に変換される。
目標光量も16ビットの信号値で入力する。16ビット同士の目標光量とPD受光値を比較し、誤差がなくなるようにフィードバック制御される。例えば、露光期間を10msとし、光量モニターおよびAPCをサンプリング周期100μsで連続的に実施する。
図8〜図13は本発明の実施形態の内視鏡システムの制御方法を説明するためのグラフである。
光源制御部22は、誤差算出部24で得られた差に応じて、誤差算出期間以降の目標光量を変更することにより、定められた露光期間内の積分光量を一定にする。この場合、目標光量は、誤差算出部24で得られた差に基づき、光源制御部22で算出される。上述の光源を点灯してから、定められた誤差算出期間が、例えば、露光期間の半分であれば、露光期間の半分における、光検出器での積算光量を用いて目標光量を調整する。目標光量の調整は、目標光量を高くすることと、目標光量を低くすることの両方を含む。
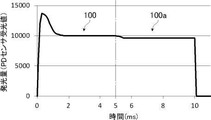
具体的には、例えば、目標光量10000で発光を開始した場合、点灯直後は光源の発光特性をAPCでは対応できず、図8に示す光量波形100のように、光量が目標光量よりも大きくなる過大発光、いわゆる、オーバーシュートが生じる。その後、APCにより目標光量に収束する。
ここで、誤差算出期間を点灯開始から5.0msまでとして、サンプリング周期100μs毎の光量積算値を算出する。誤差算出期間における光量積算値は、例えば、520300である。ここで、誤差算出期間における目標光量積算値が500000であると、実際に発光された光量積算値と、目標光量積算値とでは4.1%の差が生じる。
このため、誤差算出期間を過ぎた後、領域100aにおける目標光量を、10000から、例えば、9594に変更することにより、露光期間内の積分光量を目標値に合わせることができる。
ここで、誤差算出期間を点灯開始から5.0msまでとして、サンプリング周期100μs毎の光量積算値を算出する。誤差算出期間における光量積算値は、例えば、479800である。ここで、誤差算出期間における目標光量積算値が500000であると、実際に発光された光量積算値と、目標光量積算値とでは−4.1%の差が生じる。
このため、誤差算出期間を過ぎた後、領域102aにおける目標光量を、10000から、例えば、10404に変更することにより、露光期間内の積分光量を目標値に合わせることができる。
また、光源制御部22は、誤差算出部24で得られた差に応じて、誤差算出期間以降の光源の消灯タイミングを変更することにより、定められた露光期間内の積分光量を一定にすることもできる。この場合、消灯タイミングは、誤差算出部24で得られた差に基づき、光源制御部22で算出される。上述の光源を点灯してから、定められた誤差算出期間が、例えば、露光期間の半分であれば、露光期間の半分における、光検出器での積算光量を用いて消灯タイミングを変更する。すなわち、いつ消灯するかを決定する。消灯タイミングの変更は、早く消灯することと、遅く消灯することの両方を含む。
具体的には、例えば、目標光量10000で発光を開始して、図10に示す光量波形104のように、オーバーシュートが生じた場合、誤差算出期間を点灯開始から5.0msまでとして、サンプリング周期100μs毎の光量積算値を算出する。誤差算出期間における光量積算値は、例えば、520300である。上述のように、誤差算出期間における目標光量積算値が500000であると、実際に発光された光量積算値と、目標光量積算値とでは4.1%の差が生じる。この差を補完するために、例えば、消灯タイミングを0.2ms早めることにより、露光期間内の積分光量を目標値に合わせることができる。なお、図10において時間tは設定された露光時間を示し、時間tcは補正された露光時間を示す。この場合、露光時間は0.2ms短い。
なお、露光時間を利用した場合、発光中、目標光量を変える必要がなく、目標光量のフィードバック制御が不要である。
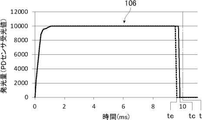
また、光源制御部22は、誤差算出部24で得られた差に応じて、定められた露光期間を変更することにより、露光期間内の積分光量を一定にすることもできる。この場合、露光期間の変更は、誤差算出部24で得られた差に基づき、光源制御部22で算出される。上述の光源を点灯してから、定められた誤差算出期間が、例えば、露光期間の半分であれば、露光期間の半分における、光検出器での積算光量を用いて露光期間を変更する。露光期間は、例えば、電子シャッターのシャッタ速度で調整される。このため、光源制御部22から撮像制御部70に電子シャッターのシャッタ速度を設定する信号が出力されて、撮像制御部70により、電子シャッターのシャッタ速度が調整される。
具体的には、図12に示すようにオーバーシュートが発生している光量波形108に対して、例えば、誤差算出期間を点灯開始から5.0msまでとして、サンプリング周期100μs毎の光量積算値を算出する。誤差算出期間における実際に発光された光量積算値と、目標光量積算値との差を求める。この差を補完するために、電子シャッターの時間を調整する。この場合、差が4.1%であれば、この差を補完するために、例えば、電子シャッターを0.2ms早めて閉じる。すなわち、電子シャッターのシャッター速度を早くする。これにより、露光期間内の積分光量を目標値に合わせることができる。なお、図12において時間tは設定された露光時間を示し、時間tsは補正された電子シャッターを閉じる時間を示す。この場合、補正された電子シャッターを閉じる時間は0.2ms早い。
なお、電子シャッターを用いた場合、発光中、目標光量を変える必要がなく、目標光量のフィードバック制御が不要である。
例えば、図14に示すように、オーバーシュートした第1の光量波形110aの第1の照明光により得られる第1の画像の画像信号比と、第2の光量波形110bの第2の照明光により得られる第2の画像の画像信号比とを一定にすることができる。
また、図14に示すように、発光遅れがある第1の光量波形110cの第1の照明光により得られる第1の画像の画像信号比と、第2の光量波形110dの第2の照明光により得られる第2の画像の画像信号比とを一定にすることができる。このようにして、酸素飽和度算出等の定量化および数値化の精度を高くできる。
なお、図14は本発明の実施形態の内視鏡システムの光源部による照明光の発光状態の一例を示すグラフである。
なお、上述のように光源に、高出力光源を採用した場合、一般的に駆動回路の高出力化と高速応答性とを両立することは難しく、光源の応答遅れを引き起こす原因となり得る。しかしながら、本発明の制御方法によれば、光源の応答遅れがあっても、複数の画像における相互間の画像信号比を一定にすることができる。
酸素飽和度画像は、第1の画像と、第2の画像の2つの画像を用いて画像処理部61にて作成される。第1の画像は、B1画像により構成される。第1の画像は、第1の照明光として、第4の光源74から出射された中心波長が約470nmの光により得られた画像である。
第2の画像は、R2画像、G2画像およびB2画像により構成される。第2の画像は、第2の照明光として、第1の光源71から出射された青色光、および第3の光源73から出射された緑と赤の色成分を含む緑色光により得られた画像である。
酸素飽和度画像は、B1画像、B2画像、G2画像、およびR2画像を用いて画像処理部61で作成される。
例えば、G2画像に対するB1画像の比(以下、信号比B1/G2という)と、R2画像に対するG2画像の比(以下、信号比R2/G2)と、をそれぞれ画素毎に算出する。信号比B1/G2は、主に観察対象の酸素飽和度の値と血液量によって変化し、信号比R2/G2は、主に観察対象の血液量に応じて変化する。
次に、例えば、観察対象の酸素飽和度を色で表す酸素飽和度画像を生成する。
具体的には、B2画像、G2画像、およびR2画像を用いてカラーの観察画像を生成する。その後、生成した観察画像の各画素を、酸素飽和度の値に応じて着色することによって酸素飽和度画像を生成する。生成した酸素飽和度画像を表示制御部66に入力することにより、モニタ18に表示する。
図16は本発明の実施形態の内視鏡システムの光源部の第2の例を示す模式図であり、図17は本発明の実施形態の内視鏡システムの光源部の第3の例を示す模式図である。
図16および図17に示す光源部20において、図5に示す光源部20と同一構成物には同一符号を付して、その詳細な説明は省略する。
図16および図17に示す光源部20は、いずれも3つの光源を有するものである。
図16に示す光源は、図5に示す光源部20に比して、第4の光源74がない構成である点が異なり、それ以外の構成は、図5に示す光源部20と同じ構成である。
また、図17に示すように、第3の光源73は、発光素子86が発光素子86aと蛍光体86bとの組み合わせではない構成でもよい。この場合、発光素子86は、例えば、LED(発光ダイオード)またはLD等の半導体素子である。
例えば、第1の光源71は、青色光を出射するものであり、第2の光源72は、例えば、紫色光を出射するものである。第3の光源73は、第1色成分が緑、第2色成分が赤の、互いに波長の異なる2つの色成分を含む緑色光を出射するものである。図16および図17に示す光源部20でも、図6に示す発光スペクトルLEが得られる。
図16および図17に示す光源部20でも、例えば、内視鏡の先端部12dと対象物Obとの距離Ldが変わっても、内視鏡画像の明るさが一定になるように照明光Lsの光量を制御する。
また、図16および図17に示す光源部20を有する内視鏡システムにおいても、上述の内視鏡システムの制御方法による制御を実施できる。
図18に示す発光スペクトルLEでは、赤色光R、緑色光G、青色光B、および紫色光Vを含む。例えば、赤色光Rは、波長帯域が615nm〜635nmであり、中心波長が620±10nmである。緑色光Gは、例えば、波長帯域が500nm〜600nmであり、中心波長が520±10nmである。青色光Bは、例えば、波長帯域が440nm〜470nmであり、中心波長が455±10nmである。そして、紫色光Vは、例えば、波長帯域が395nm〜415nmであり、中心波長が405±10nmである。このように、白色光が得られ、特定光がない発光スペクトルLEでもよい。
12 内視鏡
12a 挿入部
12b 操作部
12c 湾曲部
12d 先端部
12e アングルノブ
13a ズーム操作部
13b モード切替スイッチ
14 光源装置
16 プロセッサ装置
17 ユニバーサルコード
18 モニタ
19 コンソール
20 光源部
21 光源駆動部
22 光源制御部
23 計測部
24 誤差算出部
30a 照明光学系
30b 撮影光学系
41 ライトガイド
45 照明レンズ
46 対物レンズ
47 ズームレンズ
48 イメージセンサー
48a 第1の素子部
48b 第2の素子部
48c 第3の素子部
49 画素部
49a 第1画素
49b 第2画素
49c 第3画素
50 フィルター部
50B Bカラーフィルタ
50G Gカラーフィルタ
50R Rカラーフィルタ
50a 第1フィルター
50b 第2フィルター
50c 第3フィルター
54 画像取得部
58 ノイズ低減部
59 変換部
60 補正量算出部
61 画像処理部
66 表示制御部
69 制御部
70 撮像制御部
71 第1の光源
72 第2の光源
73 第3の光源
74 第4の光源
76、77、79 合波部材
78、82、84 レンズ
81、83、86、86a、88 発光素子
86b 蛍光体
87、89 レンズ
91、92、93、97 光検出器
94、95、96、98 ビームスプリッタ
98 ビームスプリッタ
100、102、104、106、108、109 光量波形
100a、102a 領域
112、114 吸光係数
B 青色光
Bf、Gf、Rf 分光感度
G 緑色光
LE 発光スペクトル
Ld 距離
Lr 反射光
Ls 照明光
Ob 対象物
R 赤色光
S4 波長約470nmの光
t 時間(露光時間)
tc 時間(補正された露光時間)
te 時間(標準状態での発光時間)
ts 時間(補正された電子シャッターを閉じる時間)
V 紫色光
Claims (5)
- 異なる波長の光を射出する複数の光源と、
前記複数の光源にそれぞれ設けられており、前記複数の光源の光の一部を受光し、前記複数の光源の発光量の情報を得る光検出器と、
前記複数の光源のうち、少なくとも1つの光源から射出される光により構成される第1の照明光と第2の照明光とを少なくとも用い、前記光源による照明光を完全に消灯し、点灯させて、各照明光毎に観察対象の画像を取得し、複数の撮像画像を用いて1つの観察画像を生成する画像取得部と、
前記画像取得部で取得された複数の画像における相互間の積分光量の比率を一定にする制御部とを有し、
前記複数の光源は、レーザダイオードまたは発光ダイオードを有し、
前記制御部は、前記光源の発光量が目標光量になるように、前記光検出器の受光量に応じて、前記光源の発光量を変更する光量制御部を有し、
さらに、前記光源を点灯してから、定められた誤差算出期間における前記光検出器で得られた積算光量を得る計測部と、
前記計測部で得られた前記積算光量と、定められた前記誤差算出期間における目標光量積算値との差を得る誤差算出部とを有し、
前記制御部は、前記誤差算出部で得られた前記差に応じて、前記誤差算出期間以降の前記目標光量を変更することにより、定められた露光期間内の積分光量の比率を一定にする、内視鏡システム。 - 異なる波長の光を射出する複数の光源と、
前記複数の光源にそれぞれ設けられており、前記複数の光源の光の一部を受光し、前記複数の光源の発光量の情報を得る光検出器と、
前記複数の光源のうち、少なくとも1つの光源から射出される光により構成される第1の照明光と第2の照明光とを少なくとも用い、前記光源による照明光を完全に消灯し、点灯させて、各照明光毎に観察対象の画像を取得し、複数の撮像画像を用いて1つの観察画像を生成する画像取得部と、
前記画像取得部で取得された複数の画像における相互間の積分光量の比率を一定にする制御部とを有し、
前記複数の光源は、レーザダイオードまたは発光ダイオードを有し、
前記制御部は、前記光源の発光量が目標光量になるように、前記光検出器の受光量に応じて、前記光源の消灯タイミングを変更する光量制御部を有し、
前記光源を点灯してから、定められた誤差算出期間における前記光検出器で得られた積算光量を得る計測部と、
前記計測部で得られた前記積算光量と、定められた前記誤差算出期間における目標光量の積算値である目標光量積算値との差を得る誤差算出部とを有し、
前記光量制御部は、前記誤差算出部で得られた前記差に応じて、前記誤差算出期間以降の前記光源の前記消灯タイミングを変更することにより、定められた露光期間内の積分光量の比率を一定にする、内視鏡システム。 - 異なる波長の光を射出する複数の光源と、
前記複数の光源にそれぞれ設けられており、前記複数の光源の光の一部を受光し、前記複数の光源の発光量の情報を得る光検出器と、
前記複数の光源のうち、少なくとも1つの光源から射出される光により構成される第1の照明光と第2の照明光とを少なくとも用い、前記光源による照明光を完全に消灯し、点灯させて、各照明光毎に観察対象の画像を取得し、複数の撮像画像を用いて1つの観察画像を生成する画像取得部と、
前記画像取得部で取得された複数の画像における相互間の積分光量の比率を一定にする制御部とを有し、
前記複数の光源は、レーザダイオードまたは発光ダイオードを有し、
前記制御部は、前記光源の発光量が目標光量になるように、前記光検出器の受光量に応じて、定められた露光期間を変更する光量制御部を有し、
前記光源を点灯してから、定められた誤差算出期間における前記光検出器で得られた積算光量を得る計測部と、
前記計測部で得られた前記積算光量と、定められた誤差算出期間における目標光量の積算値である目標光量積算値との差を得る誤差算出部とを有し、
前記光量制御部は、前記誤差算出部で得られた前記差に応じて、定められた前記露光期間を変更することにより、前記露光期間内の積分光量の比率を一定にする、内視鏡システム。 - 前記第1の照明光と、前記第2の照明光とは、異なる光源から出射されている、請求項1〜3のいずれか1項に記載の内視鏡システム。
- 前記光検出器は、フォトダイオードである、請求項1〜4のいずれか1項に記載の内視鏡システム。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018165806A JP6916768B2 (ja) | 2018-09-05 | 2018-09-05 | 内視鏡システム |
| EP19184709.4A EP3620099A1 (en) | 2018-09-05 | 2019-07-05 | Endoscope system |
| US16/509,504 US11419488B2 (en) | 2018-09-05 | 2019-07-12 | Endoscope system |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018165806A JP6916768B2 (ja) | 2018-09-05 | 2018-09-05 | 内視鏡システム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020036780A JP2020036780A (ja) | 2020-03-12 |
| JP6916768B2 true JP6916768B2 (ja) | 2021-08-11 |
Family
ID=67184894
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018165806A Active JP6916768B2 (ja) | 2018-09-05 | 2018-09-05 | 内視鏡システム |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US11419488B2 (ja) |
| EP (1) | EP3620099A1 (ja) |
| JP (1) | JP6916768B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11576554B2 (en) * | 2019-12-20 | 2023-02-14 | Verily Life Sciences Llc | Method for adjusting an exposure of an endoscope |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011200410A (ja) * | 2010-03-25 | 2011-10-13 | Fujifilm Corp | キャリブレーション手段を備えた内視鏡システムおよびそのキャリブレーション方法 |
| JP5616303B2 (ja) * | 2010-08-24 | 2014-10-29 | 富士フイルム株式会社 | 電子内視鏡システム及び電子内視鏡システムの作動方法 |
| JP2012110485A (ja) | 2010-11-24 | 2012-06-14 | Fujifilm Corp | 光源装置および内視鏡装置 |
| JP5331904B2 (ja) | 2011-04-15 | 2013-10-30 | 富士フイルム株式会社 | 内視鏡システム及び内視鏡システムの作動方法 |
| JP6136062B2 (ja) * | 2012-12-25 | 2017-05-31 | 株式会社リコー | 光源駆動装置、光源駆動方法及び画像形成装置 |
| WO2015005277A1 (ja) * | 2013-07-11 | 2015-01-15 | オリンパスメディカルシステムズ株式会社 | 光源装置 |
| WO2015016172A1 (ja) * | 2013-08-01 | 2015-02-05 | オリンパスメディカルシステムズ株式会社 | 内視鏡システム、内視鏡システムの作動方法 |
| CN105873495B (zh) * | 2014-04-17 | 2018-09-14 | 奥林巴斯株式会社 | 光源装置 |
| EP3231352A4 (en) * | 2014-12-09 | 2018-08-08 | Sony Corporation | Illumination device, method for controlling illumination device, and image-acquiring system |
| US9977232B2 (en) * | 2015-01-29 | 2018-05-22 | Fujifilm Corporation | Light source device for endoscope, endoscope system, and method for operating light source device for endoscope |
| JPWO2017115552A1 (ja) * | 2015-12-28 | 2018-10-18 | ソニー株式会社 | 光源装置及び撮像システム |
| JP2018000228A (ja) * | 2016-06-27 | 2018-01-11 | ソニー株式会社 | 照明装置、照明装置の制御方法、および撮像システム |
| CN109310270B (zh) * | 2016-07-05 | 2021-03-19 | 奥林巴斯株式会社 | 具有多个窄带光源的照明装置 |
| JP6654117B2 (ja) | 2016-08-31 | 2020-02-26 | 富士フイルム株式会社 | 内視鏡システム及び内視鏡システムの作動方法 |
| WO2018216276A1 (ja) * | 2017-05-22 | 2018-11-29 | ソニー株式会社 | 観察システム、および光源制御装置 |
| EP3656283B1 (en) * | 2017-07-20 | 2022-11-23 | Sony Group Corporation | Light source system, control device, and control method |
| JP6791821B2 (ja) * | 2017-08-31 | 2020-11-25 | 富士フイルム株式会社 | 内視鏡システム |
| CN111989027A (zh) * | 2018-04-24 | 2020-11-24 | 奥林巴斯株式会社 | 内窥镜系统 |
-
2018
- 2018-09-05 JP JP2018165806A patent/JP6916768B2/ja active Active
-
2019
- 2019-07-05 EP EP19184709.4A patent/EP3620099A1/en active Pending
- 2019-07-12 US US16/509,504 patent/US11419488B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20200069163A1 (en) | 2020-03-05 |
| JP2020036780A (ja) | 2020-03-12 |
| US11419488B2 (en) | 2022-08-23 |
| EP3620099A1 (en) | 2020-03-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6791821B2 (ja) | 内視鏡システム | |
| JP5303012B2 (ja) | 内視鏡システム、内視鏡システムのプロセッサ装置及び内視鏡システムの作動方法 | |
| US9629555B2 (en) | Endoscope system, endoscope system processor device, operation method for endoscope system, and operation method for endoscope system processor device | |
| US9895054B2 (en) | Endoscope system, light source device, operation method for endoscope system, and operation method for light source device | |
| US10321816B2 (en) | Light source device and endoscope system | |
| US20170251932A1 (en) | Processor device for endoscope, operation method thereof, and non-transitory computer readable medium | |
| US11044416B2 (en) | Endoscope system, processor device, and endoscope system operation method | |
| US11039739B2 (en) | Endoscope system | |
| JP6654117B2 (ja) | 内視鏡システム及び内視鏡システムの作動方法 | |
| JP5921984B2 (ja) | 電子内視鏡装置及び照明装置 | |
| WO2019163470A1 (ja) | 内視鏡システム及びその作動方法 | |
| JP2019136555A (ja) | 内視鏡光源装置、内視鏡システム、及び内視鏡光源装置の作動方法 | |
| JP6916768B2 (ja) | 内視鏡システム | |
| JP2020014718A (ja) | 内視鏡用光源装置および内視鏡システム | |
| JP6905038B2 (ja) | 光源装置及び内視鏡システム | |
| JP7159261B2 (ja) | 内視鏡システム | |
| US20240268650A1 (en) | Endoscope system and method of operating the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200728 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210413 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210610 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210706 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210716 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6916768 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |