JP6860652B2 - 医薬組成物 - Google Patents
医薬組成物 Download PDFInfo
- Publication number
- JP6860652B2 JP6860652B2 JP2019508989A JP2019508989A JP6860652B2 JP 6860652 B2 JP6860652 B2 JP 6860652B2 JP 2019508989 A JP2019508989 A JP 2019508989A JP 2019508989 A JP2019508989 A JP 2019508989A JP 6860652 B2 JP6860652 B2 JP 6860652B2
- Authority
- JP
- Japan
- Prior art keywords
- administration
- obinutuzumab
- hour
- cycle
- pharmaceutical composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2887—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against CD20
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/183—Amino acids, e.g. glycine, EDTA or aspartame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Saccharide Compounds (AREA)
- Steroid Compounds (AREA)
Description
第III相GADOLIN試験におけるオビヌツズマブ維持を続けて行うベンダムスチン+オビヌツズマブは、低悪性度B細胞非ホジキンリンパ腫(NHL)を有するリツキシマブ抵抗性患者における有効性をベンダムスチン単剤療法以上に改善した(非特許文献6)。
より短時間の注入(本明細書では「SDI」と略記する)の主な潜在的な欠点は、サイトカイン放出により媒介されるインフュージョン関連リアクション(IRRs)のリスクが増大する可能性にある。しかしながら関節リウマチ又はB細胞NHLを有する患者における試験は、リツキシマブの注入時間を少なくとも4時間から1.5−2時間に短縮することが可能であることを示しており、このことからリツキシマブの注入速度を高めることの推奨と、同様にオビヌツズマブを投与されている患者におけるSDIの調査に至っている。
[1]オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物であって、前記医薬組成物は、1回の投与あたりオビヌツズマブとして1000 mgが点滴静注され、2回以上のサイクルで投与され、且つ、以下の(a)及び(b)の投与速度に従い投与される医薬組成物。
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200 mg/時以上、好ましくは300 mg/時以上、より好ましくは400 mg/時以上である。
(b)2回目以降のサイクルの投与におけるオビヌツズマブの最大投与速度が、700 mg/時以上、好ましくは800 mg/時以上、より好ましくは900 mg/時以上で投与される。
[2]前記2回目以降のサイクルの1回の投与時間が、180分以内、好ましくは150分以内、より好ましくは120分以内、最も好ましくは90分以内である、[1]に記載の医薬組成物。
[3]前記初回サイクルにおいては3回、前記2回目以降のサイクルにおいては1回投与される、[1]又は[2]に記載の医薬組成物。
[4]前記初回サイクルの初回の投与では50 mg/時でオビヌツズマブの投与が開始され、前記初回サイクルの2回目以降の投与では100 mg/時でオビヌツズマブの投与が開始される、[3]に記載の医薬組成物。
[5]前記2回目以降のサイクルの投与速度が、オビヌツズマブ700 mg/時以上、好ましくはオビヌツズマブ800 mg/時以上、より好ましくはオビヌツズマブ900 mg/時まで上げられる、[1]〜[4]のいずれか一項に記載の医薬組成物。
[6](b)において、以下の条件(c)から(e)の少なくとも1つに従い投与される、[1]〜[5]のいずれか一項に記載の医薬組成物:
(c)前回までの3回の投与で、グレード(Grade)3以上のインフュージョンリアクション(infusion reaction)が発現しておらず、投与前の末梢血リンパ球数が5000/μL未満である場合は、投与が100mg/時で30分間行われる。その間にインフュージョンリアクションが認められない場合は、速度は900mg/時まで上げることができる。患者の状態により、速度は、例えばサイクル1での投与速度に、適宜減速され得る。
(d)グレード1/2のインフュージョンリアクションが発現した場合、投与中断前の半分の速度で投与を再開する。30分間インフュージョンリアクションが認めらなかった場合は、速度は、900mg/時まで上げることができる。
(e)グレード3のインフュージョンリアクションが発現した場合、投与は200mg/時以下として再開する。30分間インフュージョンリアクションが認められなかった場合は、速度は30分毎に50mg/時ずつ上げ、最大400mg/時まで上げることができる。
[7]前記初回サイクルは 1、8、15 日目に、前記2回目以降のサイクルは 1日目に投与される、[1]〜[6]のいずれか一項に記載の医薬組成物。
[8]3週間を1サイクルとする、[1]〜[7]のいずれか一項に記載の医薬組成物。
[9]一以上の他の抗悪性腫瘍剤と組合せて用いられ、前記医薬組成物が前記一以上の他の抗悪性腫瘍剤の投薬サイクルに合せて投与され、前記投薬サイクルが4週間を1サイクルとする、[1]〜[7]のいずれか一項に記載の医薬組成物。
[10]前記他の抗悪性腫瘍剤が、CHOP、CVP、ベンダムスチン、フルダラビン、レナリドミド、抗PD−1抗体、及び抗PD−L1抗体から選択される一以上である、[9]に記載の医薬組成物。
[11]前記2回以上のサイクル後、オビヌツズマブを含有する単剤により2カ月毎に2年間維持療法が行われる、[1]〜[10]のいずれか一項に記載の医薬組成物。
[12]前記オビヌツズマブの濃度が、10〜40 mg/mL、好ましくは20〜30 mg/mL、より好ましくは25 mg/mLである、[1]〜[11]のいずれか一項に記載の医薬組成物。
[13]さらに添加物として、トレハロース水和物、L-ヒスチジン、L-ヒスチジン塩酸塩水和物、又はポリオキシエチレン(160)ポリオキシプロピレン(30)グリコールを含有する、[1]〜[12]のいずれか一項に記載の医薬組成物。
[14]オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物の製造におけるオビヌツズマブの使用であって、前記医薬組成物は、1回の投与あたりオビヌツズマブとして1000 mgが点滴静注され、2回以上のサイクルにおいて以下の(a)及び(b)の投与速度に従い投与される使用。
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200 mg/時以上、好ましくは300 mg/時以上、より好ましくは400 mg/時以上である。
(b)2回目以降のサイクルの投与におけるオビヌツズマブの最大投与速度が、700 mg/時以上、好ましくは800 mg/時以上、より好ましくは900 mg/時以上で投与される。
[15]オビヌツズマブを含有する医薬組成物により、CD20陽性のB細胞リンパ腫を治療するための方法であり、前記組成物は、1回の投与あたりオビヌツズマブとして1000 mgが点滴静注され、2回以上のサイクルにおいて以下の(a)及び(b)の投与速度に従い投与される方法。
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200 mg/時以上、好ましくは300 mg/時以上、より好ましくは400 mg/時以上である。
(b)2回目以降のサイクルの投与におけるオビヌツズマブの最大投与速度が、700 mg/時以上、好ましくは800 mg/時以上、より好ましくは900 mg/時以上で投与される。
I.オビヌツズマブの用量と投与についての概要
本出願で、オビヌツズマブは、糖鎖改変型の遺伝子組換えヒト化抗CD20モノクローナル抗体であり、タイプII抗CD20抗体の特性を示し、449個のアミノ酸残基からなるH鎖2本及び219個のアミノ酸残基からなるL鎖2本で構成される糖タンパク質であり、分子量が約148,000〜150,000である。具体的には、本書におけるオビヌツズマブは、医薬品一般的名称(JAN)において「オビヌツズマブ(遺伝子組換え)(Obinutuzumab(Genetical Recombination))」で特定されるもののほか、そのバイオシミラー製品やバイオベター製品をも包含する。
以下、オビヌツズマブを含有する医薬組成物を「本剤」と称する。
・一実施形態として、本剤の「効能・効果」は以下が例示される。
・本剤の対象疾患としては、CD20陽性のB細胞性リンパ腫が挙げられる。すなわち、本剤は、オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物である。CD20陽性のB細胞性リンパ腫としては、たとえば、濾胞性リンパ腫、低悪性度リンパ腫、中悪性度リンパ腫、及び高悪性度リンパ腫が挙げられる。CD20陽性のB細胞性リンパ腫は、CD20陽性のB細胞性濾胞性リンパ腫が好ましい。
・一実施形態として、本剤の「用法・用量」は以下が例示される。なお、以下に例示される投与速度を含む用法用量に関する許容性は、GATS試験により示された。
・通常、成人には、オビヌツズマブとして1回1000 mgを点滴静注する。
・導入療法は、3週間を1サイクルとし、初回サイクルは1、8、15日目に、2-8サイクルは1日目に投与する。併用する抗悪性腫瘍剤が4週間隔投与の場合には、4週間を1サイクルとし、初回サイクルは1、8、15日目に、2-6サイクルは1日目に投与する。
・24週間の導入療法後、本剤単独にて2カ月毎に2年間維持療法を行う。
・本剤は以下の投与速度で投与される。なお、Gradeの判定基準は、NCI-CTCAE ver. 4.03に従う。
50 mg/時の速度で点滴静注を開始し、患者の状態を十分観察しながら、30分毎に50 mg/時ずつ上げて、最大400 mg/時まで上げることができる。
前回の投与でGrade2以上のinfusion reactionが発現しなかった場合は、100 mg/時で投与を開始し、infusion reactionが認められない場合は、30分毎に100 mg/時ずつ最大400 mg/時まで上げることができる。
前回までの3回の投与で、Grade3以上のinfusion reactionが発現しておらず、投与前の末梢血中リンパ球数が5000/μL 未満である場合は、100 mg/時で30分投与し、infusion reactionが認められない場合は、900 mg/時まで上げることができる。なお、患者の状態により、サイクル1での投与速度に戻す等、適宜減速すること。
・Infusion reactionが発現したときは以下のとおり対応する。
投与を中断するか投与速度を下げる。
投与を中断して適切な処置を行う。
投与を中断した場合は、infusion reactionが回復/軽快後、後述のとおり、投与速度を変更し再開する。
本剤の投与を直ちに中止し、適切な処置を行う。
本剤を再投与しない。
・Infusion reaction発現後、投与を中断し、再開する時の投与速度は以下のとおり対応する。
投与中断前の半分の速度で投与を再開する。30分間infusion reactionが認められなかった場合は、30分毎に50 mg/時ずつ上げ、最大400 mg/時まで上げることができる。
投与中断前の半分の速度で投与を再開する。30分間infusion reaction が認められなかった場合は、900 mg/時まで上げることができる。
200 mg/時以下として再開する。30分間infusion reaction が認められなかった場合は、30分毎に50 mg/時ずつ上げ、最大400 mg/時まで上げることができる。
本発明において、医薬組成物は、オビヌツズマブを含有する。一実施形態において、医薬組成物は、薬学的有効量のオビヌツズマブを含有する。オビヌツズマブは、II型抗CD20抗体の特徴を示し且つ449アミノ酸残基の2本の重鎖と219アミノ酸残基の2本の軽鎖とを含む糖タンパク質である、糖鎖改変、遺伝子組換え且つヒト化抗CD20モノクローナル抗体であり、約148,000−150,000の分子量を有する。具体的には、本出願におけるオビヌツズマブは、日本医薬品一般的名称(JAN)における「オビヌツズマブ(遺伝子組換え)」だけでなく、重鎖のアミノ酸配列が配列番号1で示され且つ軽鎖のアミノ酸配列が配列番号2で示されるバイオシミラー、及びそれらのアミノ酸配列に由来するそのバイオベター製品を含む。
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200 mg/時以上、好ましくは300 mg/時以上、より好ましくは400 mg/時以上である。
(b)2回目以降のサイクルの投与におけるオビヌツズマブの最大投与速度が、700 mg/時以上、好ましくは800 mg/時以上、より好ましくは900 mg/時以上で投与される。
オビヌツズマブは、WO2005/044859で示される既知の方法に従って、通常の技術者により製造され得る。医薬組成物は、通常の技術により、オビヌツズマブを他の原料と混合することによっても製造される。
本発明は、オビヌツズマブを含有する医薬組成物により、CD20陽性B細胞リンパ腫を治療するための方法をも提供する。本方法では、医薬組成物は、1回の投与あたりオビヌツズマブとして1000 mgが点滴静注され、2回以上のサイクルにおいて以下の(a)及び(b)の投与速度に従い投与される。
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200 mg/時以上、好ましくは300 mg/時以上、より好ましくは400 mg/時以上である。
(b)2回目以降のサイクルの投与におけるオビヌツズマブの最大投与速度が、700 mg/時以上、好ましくは800 mg/時以上、より好ましくは900 mg/時以上で投与される。
題目:日本人非ホジキンリンパ腫患者における、オビヌツズマブ(GA101)SDIの安全性及び忍容性
試験デザインと治療
試験のエンドポイント
統計及び分析の方法
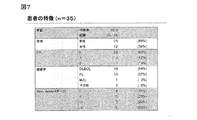
患者集団
インフュージョン関連リアクション
他の安全性及び忍容性エンドポイント
薬物動態
サイトカイン
有効性
Claims (14)
- オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物であって、前記医薬組成物は、1回の投与あたりオビヌツズマブとして1000mgが点滴静注され、2回以上のサイクルにおいて、以下の(a)及び(b):
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200mg/時以上、好ましくは300mg/時以上、より好ましくは400mg/時以上、
(b)2回目以降のサイクルの投与における開始投与速度が、オビヌツズマブ100mg/時、最大投与速度が、オビヌツズマブ800mg/時以上、
の投与速度に従い投与される医薬組成物。 - 前記2回目以降のサイクルの1回の投与時間が、180分以内、好ましくは150分以内、より好ましくは120分以内、最も好ましくは90分以内である、請求項1に記載の医薬組成物。
- 前記初回サイクルにおいては3回、前記2回目以降のサイクルにおいては1回投与される、請求項1又は2に記載の医薬組成物。
- 前記初回サイクルの初回の投与では50mg/時でオビヌツズマブの投与が開始され、前記初回サイクルの2回目以降の投与では100mg/時でオビヌツズマブの投与が開始される、請求項3に記載の医薬組成物。
- 前記2回目以降のサイクルの投与速度が、オビヌツズマブ900mg/時まで上げられる、請求項1〜4のいずれか一項に記載の医薬組成物。
- オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物であって、前記医薬組成物は、1回の投与あたりオビヌツズマブとして1000mgが点滴静注され、2回以上のサイクルにおいて、以下の(a)及び(b)の投与速度に従い投与される医薬組成物:
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200mg/時以上である、
(b)2回目以降のサイクルの投与におけるオビヌツズマブの最大投与速度が、以下の条件(c)から(e)の少なくとも1つに従い投与される:
(c)初回サイクルの投与で、グレード3以上のインフュージョンリアクションが発現しておらず、投与前の末梢血リンパ球数が5000/μL未満である場合は、投与が100mg/時で30分間行われ、その間にインフュージョンリアクションが認められない場合は、速度は900mg/時まで上げられる、
(d)2回目以降のサイクルの投与で、グレード1/2のインフュージョンリアクションが発現し、投与が中断された場合、投与中断前の半分の速度で投与を再開し、30分間インフュージョンリアクションが認めらなかった場合は、速度は、900mg/時まで上げられる、
(e)2回目以降のサイクルの投与で、グレード3のインフュージョンリアクションが発現し、投与が中断された場合、投与は200mg/時以下として再開し、30分間インフュージョンリアクションが認められなかった場合は、速度は30分毎に50mg/時ずつ上げ、最大400mg/時まで上げられる。 - 前記初回サイクルは1、8、15日目に、前記2回目以降のサイクルは1日目に投与される、請求項1〜6のいずれか一項に記載の医薬組成物。
- 3週間を1サイクルとする、請求項1〜7のいずれか一項に記載の医薬組成物。
- 一以上の他の抗悪性腫瘍剤と組合せて用いられ、前記医薬組成物が前記一以上の他の抗悪性腫瘍剤の投薬サイクルに合せて投与され、前記投薬サイクルが4週間を1サイクルとする、請求項1〜7のいずれか一項に記載の医薬組成物。
- 前記他の抗悪性腫瘍剤が、CHOP、CVP、ベンダムスチン、フルダラビン、レナリドミド、抗PD−1抗体、及び抗PD−L1抗体から選択される一以上である、請求項9に記載の医薬組成物。
- 前記2回以上のサイクル後、オビヌツズマブを含有する単剤により2カ月毎に2年間維持療法が行われる、請求項1〜10のいずれか一項に記載の医薬組成物。
- 前記オビヌツズマブの濃度が、10〜40mg/mL、好ましくは20〜30mg/mL、より好ましくは25mg/mLである、請求項1〜11のいずれか一項に記載の医薬組成物。
- さらに添加物として、トレハロース水和物、L−ヒスチジン、L−ヒスチジン塩酸塩水和物、又はポリオキシエチレン(160)ポリオキシプロピレン(30)グリコールを含有する、請求項1〜12のいずれか一項に記載の医薬組成物。
- オビヌツズマブを含有するCD20陽性のB細胞性リンパ腫治療用医薬組成物の製造におけるオビヌツズマブの使用であって、前記医薬組成物は、1回の投与あたりオビヌツズマブとして1000mgが点滴静注され、2回以上のサイクルにおいて以下の(a)及び(b):
(a)初回サイクルの投与におけるオビヌツズマブの最大投与速度が、200mg/時以上、好ましくは300mg/時以上、より好ましくは400mg/時以上、
(b)2回目以降のサイクルの投与における開始投与速度が、オビヌツズマブ100mg/時、最大投与速度が、オビヌツズマブ800mg/時以上、
の投与速度に従い投与される使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021052571A JP7370357B2 (ja) | 2017-10-19 | 2021-03-26 | 医薬組成物 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762574297P | 2017-10-19 | 2017-10-19 | |
| US62/574,297 | 2017-10-19 | ||
| PCT/JP2018/038924 WO2019017499A2 (en) | 2017-10-19 | 2018-10-19 | PHARMACEUTICAL COMPOSITION |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021052571A Division JP7370357B2 (ja) | 2017-10-19 | 2021-03-26 | 医薬組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019528282A JP2019528282A (ja) | 2019-10-10 |
| JP6860652B2 true JP6860652B2 (ja) | 2021-04-21 |
Family
ID=64362606
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019508989A Active JP6860652B2 (ja) | 2017-10-19 | 2018-10-19 | 医薬組成物 |
| JP2021052571A Active JP7370357B2 (ja) | 2017-10-19 | 2021-03-26 | 医薬組成物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021052571A Active JP7370357B2 (ja) | 2017-10-19 | 2021-03-26 | 医薬組成物 |
Country Status (14)
| Country | Link |
|---|---|
| US (2) | US12129304B2 (ja) |
| EP (2) | EP3697818B1 (ja) |
| JP (2) | JP6860652B2 (ja) |
| KR (3) | KR102906969B1 (ja) |
| CN (2) | CN111212854A (ja) |
| AU (2) | AU2018303836B2 (ja) |
| BR (1) | BR112020007731A2 (ja) |
| CA (1) | CA3079374A1 (ja) |
| ES (1) | ES3005784T3 (ja) |
| IL (2) | IL321935A (ja) |
| MX (2) | MX419643B (ja) |
| PL (1) | PL3697818T3 (ja) |
| TW (2) | TWI805630B (ja) |
| WO (1) | WO2019017499A2 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3697818B1 (en) * | 2017-10-19 | 2024-11-27 | F. Hoffmann-La Roche AG | Treatment of cd20-positive b-cell lymphoma with obinutuzumab |
| US20240050562A1 (en) * | 2019-10-04 | 2024-02-15 | Chugai Seiyaku Kabushiki Kaisha | Inhibitor of cell proliferation in obinutuzumab resistant cd20-positive cancer, and medicinal composition, medicine, production, method for inhibiting cell proliferation, therapeutic method, type ii anti-cd20 antibody, compounds, combination of same, enhancer and inducer, each relating thereto |
| EP4404430A4 (en) | 2021-09-17 | 2025-10-29 | Canon Kk | POWER TRANSMISSION DEVICE AND POWER RECEPTION DEVICE |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2672640T3 (es) | 2003-11-05 | 2018-06-15 | Roche Glycart Ag | Moléculas de unión a antígeno con afinidad de unión a receptores Fc y función efectora incrementadas |
| DK2234600T3 (da) | 2007-12-21 | 2014-09-08 | Hoffmann La Roche | Antistofformulering |
| SI3179992T1 (sl) * | 2014-08-11 | 2022-09-30 | Acerta Pharma B.V. | Terapevtske kombinacije zaviralca BTK, zaviralca PD-1 in/ali zaviralca PD-L1 |
| US11149091B2 (en) * | 2015-12-09 | 2021-10-19 | Cedars-Sinai Medical Center | Methods for treating nephrotic syndrome |
| CN108395482B (zh) | 2017-02-08 | 2021-02-05 | 西比曼生物科技(香港)有限公司 | 一种靶向cd20抗原嵌合抗原受体的构建及其工程化t细胞的活性鉴定 |
| JP6881583B2 (ja) | 2017-07-21 | 2021-06-02 | 横浜ゴム株式会社 | 空気入りタイヤ |
| EP3697818B1 (en) * | 2017-10-19 | 2024-11-27 | F. Hoffmann-La Roche AG | Treatment of cd20-positive b-cell lymphoma with obinutuzumab |
-
2018
- 2018-10-19 EP EP18804720.3A patent/EP3697818B1/en active Active
- 2018-10-19 KR KR1020247035575A patent/KR102906969B1/ko active Active
- 2018-10-19 CN CN201880067120.XA patent/CN111212854A/zh not_active Withdrawn
- 2018-10-19 CA CA3079374A patent/CA3079374A1/en active Pending
- 2018-10-19 JP JP2019508989A patent/JP6860652B2/ja active Active
- 2018-10-19 TW TW107137033A patent/TWI805630B/zh active
- 2018-10-19 KR KR1020207014191A patent/KR102766089B1/ko active Active
- 2018-10-19 IL IL321935A patent/IL321935A/en unknown
- 2018-10-19 EP EP24213649.7A patent/EP4520347A3/en active Pending
- 2018-10-19 ES ES18804720T patent/ES3005784T3/es active Active
- 2018-10-19 AU AU2018303836A patent/AU2018303836B2/en active Active
- 2018-10-19 US US16/756,057 patent/US12129304B2/en active Active
- 2018-10-19 KR KR1020257043253A patent/KR20260011191A/ko active Pending
- 2018-10-19 CN CN202511095071.9A patent/CN120983618A/zh active Pending
- 2018-10-19 TW TW112120572A patent/TWI828593B/zh active
- 2018-10-19 BR BR112020007731-3A patent/BR112020007731A2/pt unknown
- 2018-10-19 PL PL18804720.3T patent/PL3697818T3/pl unknown
- 2018-10-19 WO PCT/JP2018/038924 patent/WO2019017499A2/en not_active Ceased
- 2018-10-19 IL IL273909A patent/IL273909B2/en unknown
- 2018-10-19 MX MX2020003418A patent/MX419643B/es unknown
-
2020
- 2020-07-13 MX MX2024009217A patent/MX2024009217A/es unknown
-
2021
- 2021-03-26 JP JP2021052571A patent/JP7370357B2/ja active Active
-
2024
- 2024-09-23 US US18/893,101 patent/US20250026847A1/en active Pending
-
2025
- 2025-07-15 AU AU2025205481A patent/AU2025205481A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| IL273937B2 (en) | Antibodies, activatable antibodies, bispecific antibodies, and bispecific activatable antibodies and methods of use thereof | |
| US20250026847A1 (en) | Treatment of cd20-positive b-cell lymphoma with obinutuzumab | |
| US20230014026A1 (en) | Anti-Tumor Combination Therapy comprising Anti-CD19 Antibody and Polypeptides Blocking the SIRPalpha-CD47 Innate Immune Checkpoint | |
| JP2025522729A (ja) | ガレクチン-9を阻害する抗体を用いた悪性血液疾患の処置 | |
| JP2023052642A (ja) | 抗cd52抗体を用いて多発性硬化症を処置するための経路およびスケジュール | |
| HK40031517A (en) | Treatment of cd20-positive b-cell lymphoma with obituzumab | |
| BR122025025322A2 (pt) | Composição farmacêutica para o tratamento de linfoma de células b e uso do obinutuzumabe | |
| WO2025215124A2 (en) | Combination treatment of glofitamab and chemotherapy | |
| CN118871129A (zh) | 抗tim-3抗体与去甲基化药物的药物组合 | |
| JP2022546686A (ja) | 形質細胞に対する抑制剤または細胞傷害剤を使用する慢性疲労症候群の処置のための方法 | |
| CN118324910A (zh) | Ccr8抗体的应用 | |
| HK1172823A (en) | Cd40 antibody formulation and methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190215 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191210 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200309 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20200309 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20200311 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200609 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200904 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201202 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210224 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210326 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6860652 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |