JP6624126B2 - 含フッ素オレフィンの製造方法 - Google Patents
含フッ素オレフィンの製造方法 Download PDFInfo
- Publication number
- JP6624126B2 JP6624126B2 JP2017047353A JP2017047353A JP6624126B2 JP 6624126 B2 JP6624126 B2 JP 6624126B2 JP 2017047353 A JP2017047353 A JP 2017047353A JP 2017047353 A JP2017047353 A JP 2017047353A JP 6624126 B2 JP6624126 B2 JP 6624126B2
- Authority
- JP
- Japan
- Prior art keywords
- reaction
- hfc
- fraction
- reactor
- producing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Description
ラフルオロプロペン(以下、本明細書において「HFO−1234yf」と略記する)は、地球温暖化係数の低い冷媒化合物として有望視されている。
CF3CF=CF2+ H2 → CF3CFHCF2H (HFC-236ea) (1)
CF3CFHCF2H → CF3CF=CFH (HFO-1225ye(E/Z)) + HF (2)
CF3CF=CFH + H2 → CF3CFHCFH2(HFC-245eb) (3)
CF3CFHCFH2 → CF3CF=CH2(HFO-1234yf) + HF (4)
また、下記反応式(5)のようにHFO−1243zfをフッ素化してHFC−245e
bを得た後、上記の反応式(4)の反応を行い、HFO−1234yfを得る反応工程も知
られている。
CF3CH=CFH + F2 → CF3CFHCFH2(HFC-245eb) (5)
CF3CFHCFH2 → CF3CF=CH2(HFO-1234yf) + HF (4)
上記のように、いずれの反応工程にあってもHFC−245ebの脱フッ化水素反応により、HFO−1234yfが製造される。このような脱フッ化水素反応については従来から種々検討されており(例えば、特許文献2〜4等を参照)、触媒の種類、反応温度あるいは接触時間等を適宜調節して、効率よくHFO−1234yf等の含フッ素オレフィンを製造する方法が提案されている。
−1234ze)が多く副生しやすいという問題があり、さらに、反応に使用する触媒寿命が低下するという課題もあった。触媒寿命の低下する問題に関しては、酸素を同伴させることによって解消させることも考えられるが、この場合、原料や目的物の燃焼が促進されるので、収率が低下するという問題があった。
項1.
触媒の存在下、ハイドロフルオロカーボンの脱フッ化水素が行われる第1反応工程を経て含フッ素オレフィンを製造する方法において、
前記ハイドロフルオロカーボンは、一般式(1)RfCFYCHZ2(一般式(1)中、Rfは
炭素数1〜3の直鎖状又は分岐状のパーフルオロアルキル基、Y及びZはそれぞれ独立にH又はFであるが、ZがすべてHである場合、YはFである)で表される化合物であり、
前記触媒は、化学式CrOm(1.5<m<3)で表される酸化クロムを含む、含フッ素オレフィンの製造方法。
項2.
前記触媒は、化学式CrOm(ここで、2.0≦m<3)で表される酸化クロムである、上記項1に記載の含フッ素オレフィンの製造方法。
項3.
前記触媒は、化学式CrOm(ここで、2.05≦m≦2.3)で表される酸化クロムである、上記項1に記載の含フッ素オレフィンの製造方法。
項4.
一般式(1)において、RfがCF3である、上記項1〜3のいずれか1項に記載の含フッ
素オレフィンの製造方法。
項5.
前記ハイドロフルオロカーボンがHFC−236ea、HFC−245eb及びHFC−245cbの群から選ばれる少なくとも1種を含む、上記項4に記載の含フッ素オレフィンの製造方法。
項6.
前記ハイドロフルオロカーボンがHFC−245ebである、上記項5に記載の含フッ素オレフィンの製造方法。
項7.
前記ハイドロフルオロカーボンがHFC−245ebであり、
前記第1反応工程の後、該第1反応工程が行われる反応器から排出する全生成物の流量S(mol/min)に対して、前記全生成物に含まれるE体及びZ体のHFO−1234zeの流量とHFC−245faの流量との合計S1(mol/min)の割合が20%以下である、上記項1〜6のいずれか1項に記載の含フッ素オレフィンの製造方法。
項8.
前記流量S(mol/min)に対して、前記合計S1(mol/min)が10%以下である、上記項7に記載の含フッ素オレフィンの製造方法。
項9.
前記流量S(mol/min)に対して、前記合計S1(mol/min)が5%以下である、上記項7に記載の含フッ素オレフィンの製造方法。
項10.
前記第1反応工程の脱フッ化水素が50〜400℃で行われる、上記項1〜9のいずれ
か1項に記載の含フッ素オレフィンの製造方法。
項11.
前記第1反応工程の脱フッ化水素が100〜400℃で行われる、上記項1〜9のいずれか1項に記載の含フッ素オレフィンの製造方法。
項12.
前記第1反応工程の脱フッ化水素が230〜400℃で行われる、上記項1〜9のいずれか1項に記載の含フッ素オレフィンの製造方法。
項13.
前記第1反応工程の後、該第1反応工程が行われる反応器からの流出物の一部又は全部を少なくとも第1留分と第2留分とに分離する分離工程を行い、
前記第1留分は、HFC−245eb濃度が前記分離工程の前よりも増大しており、前記第2留分は、HFC−245eb濃度が前記分離工程の前よりも低下しており、
前記分離工程の後、前記第1留分の少なくとも一部の脱フッ化水素を行う、上記項5〜12のいずれか1項に記載の含フッ素オレフィンの製造方法。
項14.
前記第1反応工程の後、該第1反応工程が行われる反応器からの流出物の一部又は全部を少なくとも第3留分と第4留分とに分離する分離工程を行い、
前記第3留分は、HFC−245cb濃度が前記分離工程の前よりも増大しており、前記第4留分は、HFC−245cb濃度が前記分離工程の前よりも低下しており、
前記分離工程の後、前記第3留分の少なくとも一部の脱フッ化水素を行う、上記項5〜12のいずれか1項に記載の含フッ素オレフィンの製造方法。
項15.
前記第1留分の少なくとも一部は、前記第1反応工程にリサイクルされて脱フッ化水素が行われる上記項13に記載の含フッ素オレフィンの製造方法。
項16.
前記第3留分の少なくとも一部は、前記第1反応工程にリサイクルされて脱フッ化水素が行われる上記項14に記載の含フッ素オレフィンの製造方法。
項17.
前記ハイドロフルオロカーボンは、酸素ガスを同伴させて前記第1反応工程に供する、上記項1〜16のいずれか1項に記載の含フッ素オレフィンの製造方法。
項18.
酸素ガスの流量(mol/min)が、前記ハイドロフルオロカーボンの流量(mol/min)に対して0.1%以上10%以下である、上記項17に記載の方法。
項19.
前記酸化クロムは、第5族金属をさらに含む、上記項1〜18のいずれか1項に記載の含フッ素オレフィンの製造方法。
項20.
前記酸化クロムに含まれる第5族金属の原子数の割合は、前記酸化クロムに含まれる全金属原子数に対して0.1%以上50%以下である、上記項19に記載の含フッ素オレフィンの製造方法。
ここで、一般式(1)中、Rfは炭素数1〜3の直鎖状又は分岐状のパーフルオロアルキル基であり、Y及びZはそれぞれ独立にH又はFであるが、ZがすべてHである場合、YはFである。
原料のハイドロフルオロカーボンの転化率も向上させることができる。なお、クロムの価数は、公知の方法によって測定することができる。
ことがより好ましく、0.5%以上3%以下であることが特に好ましい。
の中でも特に好ましくは300℃である。また、第1反応工程における脱フッ化水素の反応温度の下限は、生産性の面から転化率が許容できないほど低下するのを防止しやすいという観点から、常圧下の場合であれば、好ましくは50℃、より好ましくは100℃、さらに好ましくは200℃、特に好ましくは230℃、その中でも特に好ましくは270℃である。
に同じである)で表される。
類にもよるが、例えば、ハイドロフルオロカーボンとしてHFC−245eb又はHFC−245cbを使用すれば、得られる含フッ素オレフィンは、1,1,1,2−テトラフルオロプロペン(HFO−1234yf)となる。また、ハイドロフルオロカーボンとしてHFC−236eaを使用すれば、得られる含フッ素オレフィンは、1,2,3,3,3−ペンタフルオロプロペン(HFO−1225ye)となる。同様に、ハイドロフルオロカーボンとして1,1,2,2,3−ペンタフルオロプロパン(HFC−245ca)を使用すれば、得られる含フッ素オレフィンは1,1,2,3−ペンタフルオロプロペン(HFO−1234ye)となる。
の第1反応工程内で行うようにしてもよい。すなわち、第1反応工程で得られた上記流出物を分離工程で第3留分と第4留分とに分離した後、得られた上記第3留分を再度、第1反応工程にリサイクルしてもよい。この場合、より効率的にHFO−1234yfを製造することができ、原料の転化率及び目的物の選択率をさらに高めることができる。
ハイドロフルオロカーボンとしてHFC−245ebを使用して第1反応工程の脱フッ化水素反応を実施した。触媒は、化学式CrO2.09で表される酸化クロムを用いた。また、触媒を反応に使用する前処理として、触媒を収容した反応器に窒素で希釈した無水フッ化水素を流通させ、反応器の温度を200℃〜350℃に加熱させてフッ素化処理を行った。
ハイドロフルオロカーボンとしてHFC−245ebを使用して第1反応工程の脱フッ化水素反応を実施した。触媒は、フッ素化したアルミナ触媒を用いた。
ハイドロフルオロカーボンとしてHFC−245ebを使用して第1反応工程の脱フッ化水素反応を実施した。触媒は、オキシフッ化クロム触媒を用いた。
器を加熱した。反応器が所定の温度(本比較例では420℃)に達した後、HFC−245ebを反応器に導入し、窒素の供給を停止させた。酸素ガスは反応器入口のHFC−245ebに対して5モル%となるよう適宜、反応器入口から導入した。反応の運転条件は、圧力を0.0MPaG、反応温度を420℃、W/F0を164g・sec・ml−1とした。
反応温度を200℃とした以外は比較例1と同様の方法で第1反応工程の脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表1に示している。
ハイドロフルオロカーボンとしてHFC−245ebを使用して第1反応工程の脱フッ化水素反応を実施した。触媒は、活性炭に4.6重量%の塩化鉄(III)を担持させた触
媒を用いた。
4yfは、2,3,3,3−テトラフルオロプロペン、245cbは、1,1,1,2,2−ペンタフルオロプロパン、1234zeは1,3,3,3−ペンタフルオロプロペン、245faは、1,1,1,3,3−ペンタフルオロプロパンを示す。表2〜4においても同様である。
ハイドロフルオロカーボンとしてHFC−245ebを使用して第1反応工程の脱フッ化水素反応を実施した。触媒は、化学式CrO2.09で表される酸化クロムを用いた。また、触媒を反応に使用する前処理として、触媒を収容した反応器に窒素で希釈した無水フッ化水素を流通させ、反応器の温度を200℃〜380℃に加熱させてフッ素化処理を行った。
反応温度を245℃に変更したこと以外は実施例2−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表2に示している。
反応温度を275℃に変更したこと以外は実施例2−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて
分析した。結果は後掲の表2に示している。
反応温度を320℃に変更したこと以外は実施例2−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表2に示している。
反応温度を345℃に変更したこと以外は実施例2−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表2に示している。
反応温度を380℃に変更したこと以外は実施例2−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表2に示している。
ハイドロフルオロカーボンとしてHFC−245ebを使用して第1反応工程の脱フッ化水素反応を実施した。触媒は、化学式CrO2.09で表される酸化クロムを用いた。また、触媒を反応に使用する前処理として、触媒を収容した反応器に窒素で希釈した無水フッ化水素を流通させ、反応器の温度を最高380℃に加熱させてフッ素化処理を行った。
反応温度を250℃に変更したこと以外は実施例3−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表3に示している。
反応温度を280℃に変更したこと以外は実施例3−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表3に示している。
反応温度を300℃に変更したこと以外は実施例3−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表3に示している。
反応温度を320℃に変更したこと以外は実施例3−1と同様に脱フッ化水素反応を実施した。反応器出口から抜き出された流出物の成分組成を、ガスクロマトグラフを用いて分析した。結果は後掲の表3に示している。
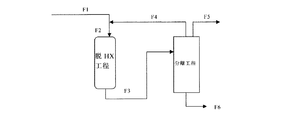
図1に示すフロー図に従って、実施例3−4における脱フッ化水素反応の後、反応器出口から抜き出された流出物の分離工程を行い、回収されたHFC−245ebのリサイクルを行った。具体的には、実施例3−4における脱フッ化水素反応の反応器出口から抜き出された流出物F3を分離工程の装置へ供給し、分離処理を行った。この分離工程により、HFC−245eb濃度が前記分離工程の前よりも増大した第1留分及びHFC−245eb濃度が前記分離工程の前よりも低下した第2留分を得た。第1留分F4は、脱フッ化水素反応にリサイクルさせ、第1留分中のHFC−245ebの脱フッ化水素反応を行った。また、目的のHFO−1234yf(F5)は、精留又は抽出蒸留等の分離工程に供することにより分離回収させた。
Claims (11)
- 触媒の存在下、ハイドロフルオロカーボンの脱フッ化水素が行われる第1反応工程によって含フッ素オレフィンを製造する方法において、
前記ハイドロフルオロカーボンは、HFC−245ebであり、
前記触媒は、化学式CrOm(1.5<m<3)で表される酸化クロムを含み、
前記脱フッ化水素の反応温度は、200℃以上、300℃以下であり、
前記第1反応工程の後、該第1反応工程が行われる反応器から排出する全生成物の流量S(mol/min)に対して、前記全生成物に含まれるE体及びZ体のHFO−1234zeの流量とHFC−245faの流量との合計S1(mol/min)の割合が5%以下である、含フッ素オレフィンの製造方法。 - 前記触媒は、化学式CrOm(2≦m<3)で表される酸化クロムである、請求項1に記載の含フッ素オレフィンの製造方法。
- 前記触媒は、化学式CrOm(2.05≦m≦2.3)で表される酸化クロムである、上記請求項1に記載の含フッ素オレフィンの製造方法。
- 前記第1反応工程の後、該第1反応工程が行われる反応器からの流出物の一部又は全部を少なくとも第1留分と第2留分とに分離する分離工程を行い、
前記第1留分は、HFC−245eb濃度が前記分離工程の前よりも増大しており、前記第2留分は、HFC−245eb濃度が前記分離工程の前よりも低下しており、
前記分離工程の後、前記第1留分の少なくとも一部の脱フッ化水素を行う、請求項1〜3のいずれか1項に記載の含フッ素オレフィンの製造方法。 - 前記第1反応工程の後、該第1反応工程が行われる反応器からの流出物の一部又は全部を少なくとも第3留分と第4留分とに分離する分離工程を行い、
前記第3留分は、HFC−245cb濃度が前記分離工程の前よりも増大しており、前記第4留分は、HFC−245cb濃度が前記分離工程の前よりも低下しており、
前記分離工程の後、前記第3留分の少なくとも一部の脱フッ化水素を行う、請求項1〜3のいずれか1項に記載の含フッ素オレフィンの製造方法。 - 前記第1留分の少なくとも一部は、前記第1反応工程にリサイクルされて脱フッ化水素が行われる請求項4に記載の含フッ素オレフィンの製造方法。
- 前記第3留分の少なくとも一部は、前記第1反応工程にリサイクルされて脱フッ化水素が行われる請求項5に記載の含フッ素オレフィンの製造方法。
- 前記ハイドロフルオロカーボンは、酸素ガスを同伴させて前記第1反応工程に供する、請求項1〜7のいずれか1項に記載の含フッ素オレフィンの製造方法。
- 酸素ガスの流量(mol/min)が、前記ハイドロフルオロカーボンの流量(mol/min)に対して0.1%以上10%以下である、請求項8に記載の方法。
- 前記酸化クロムは、第5族金属をさらに含む、請求項1〜9のいずれか1項に記載の含フッ素オレフィンの製造方法。
- 前記酸化クロムに含まれる第5族金属の原子数の割合は、前記酸化クロムに含まれる全金属原子数に対して0.1%以上50%以下である、請求項10に記載の含フッ素オレフィンの製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017047353A JP6624126B2 (ja) | 2017-03-13 | 2017-03-13 | 含フッ素オレフィンの製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017047353A JP6624126B2 (ja) | 2017-03-13 | 2017-03-13 | 含フッ素オレフィンの製造方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015110774A Division JP6328589B2 (ja) | 2015-05-29 | 2015-05-29 | 含フッ素オレフィンの製造方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017132784A JP2017132784A (ja) | 2017-08-03 |
| JP2017132784A5 JP2017132784A5 (ja) | 2018-05-31 |
| JP6624126B2 true JP6624126B2 (ja) | 2019-12-25 |
Family
ID=59503228
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017047353A Active JP6624126B2 (ja) | 2017-03-13 | 2017-03-13 | 含フッ素オレフィンの製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6624126B2 (ja) |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7560602B2 (en) * | 2005-11-03 | 2009-07-14 | Honeywell International Inc. | Process for manufacture of fluorinated olefins |
| KR102116848B1 (ko) * | 2008-05-07 | 2020-06-01 | 더 케무어스 컴퍼니 에프씨, 엘엘씨 | 1,1,1,2,3-펜타플루오로프로판 또는 2,3,3,3-테트라플루오로프로펜을 포함하는 조성물 |
| EP2326612B1 (en) * | 2008-08-22 | 2014-08-20 | Daikin Industries, Ltd. | Process for preparing 2,3,3,3-tetrafluoropropene |
| US8050246B2 (en) * | 2009-03-03 | 2011-11-01 | Adc Telecommunications, Inc. | Range extension for time division duplex systems |
| HUE034982T2 (en) * | 2009-06-03 | 2018-05-02 | Chemours Co Fc Llc | Process for the preparation of 2,3,3,3-tetrafluoropropene |
| ES2567178T5 (es) * | 2010-02-12 | 2023-04-28 | Daikin Ind Ltd | Procedimiento para producir un alqueno que contiene flúor |
-
2017
- 2017-03-13 JP JP2017047353A patent/JP6624126B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017132784A (ja) | 2017-08-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9388099B2 (en) | Process for producing 2,3,3,3-tetrafluoropropene | |
| US9862661B2 (en) | Process for the preparation of 2, 3, 3, 3-tetrafluoropropene | |
| US9284240B2 (en) | Process for the manufacture of 2-chloro-3,3,3-trifluoropropene by gas phase fluorination of pentachloropropane | |
| JP2015509096A (ja) | 含フッ素オレフィンの製造方法 | |
| EP3978462A1 (en) | Method for producing fluorine-containing compounds | |
| JP6176262B2 (ja) | 含フッ素オレフィンの製造方法 | |
| JP6328589B2 (ja) | 含フッ素オレフィンの製造方法 | |
| JP6583360B2 (ja) | 2,3,3,3−テトラフルオロプロペンの製造方法 | |
| EP2990396B1 (en) | Method for producing fluorine-containing olefin | |
| EP2534120B2 (en) | Process for producing fluorine-containing alkene | |
| JP6233535B2 (ja) | テトラフルオロプロペンの製造方法 | |
| JP6624126B2 (ja) | 含フッ素オレフィンの製造方法 | |
| JP6623561B2 (ja) | 含フッ素オレフィンの製造方法 | |
| Rao et al. | Processes for producing pentafluoropropenes and certain azeotropes comprising HF and certain halopropenes of the formula C 3 HClF 4 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180326 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180413 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190507 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190708 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20191029 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20191111 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6624126 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |