JP6288936B2 - 癌診断装置 - Google Patents
癌診断装置 Download PDFInfo
- Publication number
- JP6288936B2 JP6288936B2 JP2013089515A JP2013089515A JP6288936B2 JP 6288936 B2 JP6288936 B2 JP 6288936B2 JP 2013089515 A JP2013089515 A JP 2013089515A JP 2013089515 A JP2013089515 A JP 2013089515A JP 6288936 B2 JP6288936 B2 JP 6288936B2
- Authority
- JP
- Japan
- Prior art keywords
- raman scattering
- visible light
- image
- light
- diagnostic apparatus
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 206010028980 Neoplasm Diseases 0.000 title claims description 27
- 201000011510 cancer Diseases 0.000 title claims description 27
- 238000001069 Raman spectroscopy Methods 0.000 claims description 95
- 238000005259 measurement Methods 0.000 claims description 55
- 238000003384 imaging method Methods 0.000 claims description 51
- 238000001514 detection method Methods 0.000 claims description 31
- 238000005286 illumination Methods 0.000 claims description 16
- 239000003086 colorant Substances 0.000 claims description 4
- 238000003745 diagnosis Methods 0.000 claims description 4
- 238000000034 method Methods 0.000 description 36
- 230000008569 process Effects 0.000 description 35
- 230000003287 optical effect Effects 0.000 description 18
- 238000012545 processing Methods 0.000 description 12
- 238000010586 diagram Methods 0.000 description 10
- 239000013307 optical fiber Substances 0.000 description 8
- 230000008859 change Effects 0.000 description 7
- 210000002784 stomach Anatomy 0.000 description 6
- 230000006870 function Effects 0.000 description 5
- 230000007423 decrease Effects 0.000 description 4
- 230000005284 excitation Effects 0.000 description 4
- 238000003780 insertion Methods 0.000 description 4
- 230000037431 insertion Effects 0.000 description 4
- 238000005452 bending Methods 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- 238000001237 Raman spectrum Methods 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- 238000003841 Raman measurement Methods 0.000 description 1
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 239000011669 selenium Substances 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
Images
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pathology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Physics & Mathematics (AREA)
- Endoscopes (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Surgery (AREA)
- General Health & Medical Sciences (AREA)
- Optics & Photonics (AREA)
- Biomedical Technology (AREA)
- Biophysics (AREA)
- General Physics & Mathematics (AREA)
- Radiology & Medical Imaging (AREA)
- Biochemistry (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Heart & Thoracic Surgery (AREA)
- Medical Informatics (AREA)
- Molecular Biology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Analytical Chemistry (AREA)
- Chemical & Material Sciences (AREA)
Description
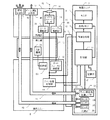
IR12、IRref21 ラマン散乱検出フィルタ
34 CIGSイメージセンサ
IR12 測定用赤外フィルタ
IRref21 参照用赤外フィルタ
24、26、28 可視光域の照明光源
30 ラマン散乱用光源
16 記憶部
4 表示部
64 ラマン散乱の検知部分を特定する重畳表示
32 撮像レンズ
Claims (11)
- 撮像レンズを有し、可視光画像の撮像およびラマン散乱の測定が可能であるとともに、前記可視光画像の表示において前記ラマン散乱の検知部分を特定する重畳表示を行い、前記重畳表示は、前記撮像レンズの状態に応じて行われ、かつ、可視光域のフィルタおよびラマン散乱検出フィルタを設けたCIGSイメージセンサを有し、前記撮像レンズにより結像される像を前記CIGSイメージセンサで受けることによって前記可視光画像の撮像および前記ラマン散乱の測定を行う癌診断装置であって、前記ラマン散乱検出フィルタは、ラマン散乱光を選択的に透過させる測定用赤外フィルタおよびラマン散乱光がない近接域の赤外光を選択的に透過させる参照用赤外フィルタを含むことを特徴とする癌診断装置。
- 可視光域の照明光源およびラマン散乱用光源を有し、前記CIGSイメージセンサは前記可視光域の照明光源および前記ラマン散乱用光源に基づきそれぞれ前記可視光画像の撮像と前記ラマン散乱の検出を行うことを特徴とする請求項1記載の癌診断装置。
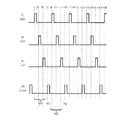
- 前記可視光域の照明光源の光および前記ラマン散乱用光源の光は時分割で対象に照射されることを特徴とする請求項2記載の癌診断装置。
- 前記可視光域の照明光源は時分割で点灯される複数色の光源を含み、前記可視光域のフィルタはこれら複数色の光源の光をいずれも透過させることを特徴とする請求項2または3記載の癌診断装置。
- 前記可視光域のフィルタは複数色を選択的に透過させることを特徴とする請求項2または3記載の癌診断装置。
- 前記ラマン散乱検出フィルタを設けた前記CIGSイメージセンサの出力によるラマン散乱強度の測定値を以後の正常組織のラマン散乱強度判断のための基準値として記憶する記憶部を有することを特徴とする請求項1から5のいずれかに記載の癌診断装置。
- 前記記憶部は、前記ラマン散乱検出フィルタを設けた前記CIGSイメージセンサによるラマン散乱強度の複数の測定値の平均値を前記基準値として記憶することを特徴とする請求項6記載の癌診断装置。
- 前記CIGSイメージセンサによる前記可視光画像の撮像と前記ラマン散乱の検出は時分割で行われるとともに、前記可視光画像の表示部を有し、前記表示部における前記可視光画像の表示は、前記ラマン散乱の検出時も継続されることを特徴とする請求項1から7のいずれかに記載の癌診断装置。
- 前記重畳表示を行うための表示データを作成し、前記撮像レンズの調節位置に基づいて前記重畳表示を行うための前記表示データを自動的に更新することを特徴とする請求項1から8のいずれかに記載の癌診断装置。
- 前記表示データは、前記撮像レンズのフォーカス調節に応じて更新されることを特徴とする請求項9記載の癌診断装置。
- 前記表示データは、前記撮像レンズのズーミングに応じて更新されることを特徴とする請求項9または10記載の癌診断装置。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013089515A JP6288936B2 (ja) | 2013-04-22 | 2013-04-22 | 癌診断装置 |
| PCT/JP2014/061186 WO2014175223A1 (ja) | 2013-04-22 | 2014-04-21 | 癌診断装置、診断システム、診断装置 |
| US14/785,902 US10184894B2 (en) | 2013-04-22 | 2014-08-21 | Cancer diagnostic device, diagnostic system, and diagnostic device |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013089515A JP6288936B2 (ja) | 2013-04-22 | 2013-04-22 | 癌診断装置 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2014212801A JP2014212801A (ja) | 2014-11-17 |
| JP2014212801A5 JP2014212801A5 (ja) | 2016-04-21 |
| JP6288936B2 true JP6288936B2 (ja) | 2018-03-07 |
Family
ID=51939168
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013089515A Expired - Fee Related JP6288936B2 (ja) | 2013-04-22 | 2013-04-22 | 癌診断装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6288936B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5988907B2 (ja) * | 2013-03-27 | 2016-09-07 | オリンパス株式会社 | 内視鏡システム |
| JPWO2016098171A1 (ja) | 2014-12-15 | 2017-09-28 | オリンパス株式会社 | 撮像装置およびカプセル型内視鏡 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05289001A (ja) * | 1992-04-10 | 1993-11-05 | Asahi Optical Co Ltd | 内視鏡用撮像装置 |
| JP3288504B2 (ja) * | 1993-10-19 | 2002-06-04 | 富士写真光機株式会社 | レーザー光照射装置を用いる電子内視鏡装置 |
| US6205354B1 (en) * | 1999-06-18 | 2001-03-20 | University Of Utah | Method and apparatus for noninvasive measurement of carotenoids and related chemical substances in biological tissue |
| US20060239673A1 (en) * | 2003-03-13 | 2006-10-26 | Roke Manor Research Limited | Camera illumination system |
| JP2006300611A (ja) * | 2005-04-18 | 2006-11-02 | Hamamatsu Photonics Kk | 試料分析装置及びそれを用いた試料分析方法 |
| WO2010024397A1 (ja) * | 2008-08-28 | 2010-03-04 | 独立行政法人理化学研究所 | ラマン散乱測定装置 |
| US8901541B2 (en) * | 2009-04-07 | 2014-12-02 | Rohm Co., Ltd. | Photoelectric conversion device and image pick-up device |
| JP5948076B2 (ja) * | 2011-08-23 | 2016-07-06 | オリンパス株式会社 | フォーカス制御装置、内視鏡装置及びフォーカス制御方法 |
-
2013
- 2013-04-22 JP JP2013089515A patent/JP6288936B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2014212801A (ja) | 2014-11-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10184894B2 (en) | Cancer diagnostic device, diagnostic system, and diagnostic device | |
| US8553075B2 (en) | Endoscope apparatus and control method therefor | |
| JP4846042B2 (ja) | 眼科撮像装置、眼科システム及びプログラム | |
| JP4643481B2 (ja) | 画像処理装置 | |
| US20110237895A1 (en) | Image capturing method and apparatus | |
| US20200163538A1 (en) | Image acquisition system, control apparatus, and image acquisition method | |
| WO2019087557A1 (ja) | 内視鏡システム | |
| WO2015012096A1 (ja) | 医療用観察装置 | |
| WO2020170669A1 (ja) | 光源装置、医療用観察システム、調整装置、照明方法、調整方法およびプログラム | |
| US20210294084A1 (en) | Medical image processing device, medical observation system, and image processing method | |
| WO2014199984A1 (ja) | 手術用顕微鏡システム | |
| JP2011005002A (ja) | 内視鏡装置 | |
| US11684238B2 (en) | Control device and medical observation system | |
| JP6288936B2 (ja) | 癌診断装置 | |
| WO2014156604A1 (ja) | 内視鏡システム及びその作動方法並びにプロセッサ装置 | |
| JP6116188B2 (ja) | 眼底撮像装置 | |
| JP2010259530A (ja) | 眼科撮影装置 | |
| JP6255662B2 (ja) | 眼底撮影装置 | |
| JP6560485B2 (ja) | 診断システム | |
| JP6113033B2 (ja) | 内視鏡装置 | |
| JP6120686B2 (ja) | 角膜内皮細胞撮影装置 | |
| JP2006340855A (ja) | 画像処理装置 | |
| JP5701357B2 (ja) | 眼科撮像装置及び眼科撮像方法 | |
| JPWO2013001994A1 (ja) | 分光画像取得装置及び分光画像取得方法 | |
| US11648080B2 (en) | Medical observation control device and medical observation system that correct brightness differences between images acquired at different timings |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160308 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20160308 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160311 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170321 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170502 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20171024 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171218 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20180109 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20180206 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6288936 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |