JP6133210B2 - 不整脈のリスクを判定する方法 - Google Patents
不整脈のリスクを判定する方法 Download PDFInfo
- Publication number
- JP6133210B2 JP6133210B2 JP2013535391A JP2013535391A JP6133210B2 JP 6133210 B2 JP6133210 B2 JP 6133210B2 JP 2013535391 A JP2013535391 A JP 2013535391A JP 2013535391 A JP2013535391 A JP 2013535391A JP 6133210 B2 JP6133210 B2 JP 6133210B2
- Authority
- JP
- Japan
- Prior art keywords
- arrhythmia
- drug
- cardiomyocytes
- pps
- channel
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
- G01N33/5061—Muscle cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6887—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids from muscle, cartilage or connective tissue
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
- G01N27/04—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance by investigating resistance
- G01N27/12—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance by investigating resistance of a solid body in dependence upon absorption of a fluid; of a solid body in dependence upon reaction with a fluid, for detecting components in the fluid
- G01N27/128—Microapparatus
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/32—Cardiovascular disorders
- G01N2800/326—Arrhythmias, e.g. ventricular fibrillation, tachycardia, atrioventricular block, torsade de pointes
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Hematology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- General Health & Medical Sciences (AREA)
- Biotechnology (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Wood Science & Technology (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- Electrochemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Toxicology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Engineering & Computer Science (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Investigating Or Analyzing Materials By The Use Of Electric Means (AREA)
- Cardiology (AREA)
- Rheumatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
生命を脅かす多形の心室性不整頻脈である薬物誘導性トルサード・ド・ポワント(Torsades de Pointes)(TdP)は、多数の薬物の使用の中止または厳しい制限をもたらしている(Journal of Pharmacological and Toxicological Methods 52: 46-59, 2005(非特許文献1))。TdPの典型的な原因は、延長したQT間隔を結果として生じる、カリウムチャンネルであるhERG(KCNH2によりコードされるヒトether-a-go-go関連遺伝子)の内向き整流の阻害である。現在、hERGを過剰発現する非心臓細胞株を用いて、hERG阻害についての薬物候補をスクリーニングすることが、標準的なアプローチである。しかしながら、hERGチャンネルを阻害する化合物のすべてが、QT延長を結果として生じるまたはTdPを誘導するわけではないため、hERGスクリーニングは次善である(Cardiovascular Research 58: 32-45, 2003(非特許文献2))。さらに、不整脈は、インビトロhERG阻害を呈さない、または前臨床動物モデルにおいてQT延長を引き起こさない薬物により、ヒトにおいて誘導され得る。例えば、強力なhERG阻害剤であるベラパミルは、患者においてQT延長またはTdPを引き起こさず、安全にかつ有効に使用される。この不一致にもかかわらず、主として洗練された代案が一般的に欠如しているため、ヒトTdPの可能性に代えて、hERG阻害およびQT間隔延長に対する化合物の効果を調査することに、薬物の発見における大規模な時間および努力が費やされている。
a)心筋細胞を用意する段階;
b)該心筋細胞を薬物と接触させる段階;
c)細胞収縮または電場電位のいずれかをモニタリングすることにより、拍動率の不規則性を検出する段階。
d)IBRを計算する段階。
e)結果としてPPSを生じる、Cmaxに対するIB20の比を計算する段階、または結果としてPPSを生じる、Cmaxに対するIB20の比を計算する段階。
[本発明1001]
以下の段階を含む、薬物誘導性不整脈のリスクを判定する方法:
a)心筋細胞を用意する段階;
b)該心筋細胞を薬物と接触させる段階;
c)細胞収縮または電場電位のいずれかをモニタリングすることにより、拍動率の不規則性を検出する段階。
[本発明1002]
心筋細胞が、イヌ、サル、ラット、ウサギ、またはヒト起源のものである、本発明1001の方法。
[本発明1003]
心筋細胞が、ヒト起源のものである、本発明1001または1002の方法。
[本発明1004]
心筋細胞が、幹細胞源から産生される、本発明1001〜1003のいずれかの方法。
[本発明1005]
幹細胞源が、胚性幹細胞源である、本発明1001〜1004のいずれかの方法。
[本発明1006]
心筋細胞が、多能性幹細胞源から産生される、本発明1001〜1005のいずれかの方法。
[本発明1007]
幹細胞源が、人工多能性幹細胞源である、本発明1006の方法。
[本発明1008]
不整脈の発生率が、細胞電場電位における変化をモニタリングすることにより検出される、本発明1001〜1007のいずれかの方法。
[本発明1009]
細胞収縮が、インピーダンスを測定することによりモニタリングされる、本発明1001〜1008のいずれかの方法。
[本発明1010]
細胞収縮が、収縮中の心筋細胞の動きを同定可能なデータ捕捉率頻度でインピーダンスを測定することによりモニタリングされる、本発明1009の方法。
[本発明1011]
インピーダンスが、約12.9ミリ秒毎のサンプリングレートで測定される、本発明1009または1010の方法。
[本発明1012]
不整脈の検出が、拍動率リズムの増加、減少、または不規則性をモニタリングすることを含む、本発明1001〜1011のいずれかの方法。
[本発明1013]
拍動率リズムの不規則性が、トルサード・ド・ポワント(Torsades de Pointes)を示す、本発明1012の方法。
[本発明1014]
拍動率リズムの不規則性が、QTの延長を示す、本発明1012の方法。
[本発明1015]
拍動率リズムの不規則性が、心臓イオンチャンネルの破壊のためである、本発明1012の方法。
[本発明1016]
心臓イオンチャンネルが、カリウムチャンネルである、本発明1015の方法。
[本発明1017]
カリウムチャンネルが、hERGチャンネルである、本発明1016の方法。
[本発明1018]
心臓イオンチャンネルが、カルシウムチャンネルである、本発明1015の方法。
[本発明1019]
心臓イオンチャンネルが、ナトリウムチャンネルである、本発明1015の方法。
[本発明1020]
以下の段階をさらに含む、本発明1001〜1019のいずれかの方法:
d)IBRを計算する段階。
[本発明1021]
0.2に等しいまたはそれ未満のIBRが、不整脈の低リスクを表すために使用される、本発明1020の方法。
[本発明1022]
以下の段階をさらに含む、本発明1020または1021の方法:
e)結果としてPPSを生じる、C max に対するIB 20 の比を計算する段階、または結果としてPPSを生じる、C max に対するIB 20 の比を計算する段階。
[本発明1023]
以下の段階をさらに含む、本発明1020または1021の方法:
e)結果としてPPSを生じる、IB 20 に対するC max の比を計算する段階。
[本発明1024]
100に等しいまたはそれ未満のPPSが、不整脈の低リスクを表すために使用される、本発明1020または1021の方法。
[本発明1025]
以下の段階をさらに含む、本発明1020〜1024のいずれかの方法:
f)段階e)の結果を、公知の不整脈誘導薬物の結果と比較する段階。
[本発明1026]
ハイスループットフォーマットで実施される、本発明1001〜1025のいずれかの方法。
[本発明1027]
薬物開発状況において分子をスクリーニングするために実施される、本発明1001〜1027のいずれかの方法。
本出願は、以下の段階を含む、薬物誘導性不整脈のリスクを判定する方法を提供する:
a)心筋細胞を用意する段階;
b)該心筋細胞を薬物と接触させる段階;
c)細胞収縮または電場電位のいずれかをモニタリングすることにより、拍動率の不規則性を検出する段階。
d)IB20を計算する段階。
e)結果としてPPSを生じる、Cmaxに対するIB20の比を計算する段階、または結果としてPPSを生じる、Cmaxに対するIB20の比を計算する段階。
e)結果としてPPSを生じる、IB20に対するCmaxの比を計算する段階。
f)段階e)の結果を、公知の不整脈誘導薬物の結果と比較する段階。
本明細書において使用される「一つの(a)」または「一つの(an)」実体という句は、一つまたは複数のその実体を指し;例えば、一つの化合物とは、一つもしくは複数の化合物、または少なくとも一つの化合物を指す。そのように、「一つの」、「一つまたは複数の」、および「少なくとも一つの」という用語は、本明細書において互換的に使用され得る。
化学物質
インビトロの試薬は、Sigma Chemical Co.(St Louis MO)から購入した。
細胞培養
Cellular Dynamics International(CDI)のhiPSC由来心筋細胞(iCell)を、プレーティング培地(CDI)において融解し、単一細胞として、0.1%ゼラチン(Sigma)でコーティングした6ウェル組織培養プレート(Corning)上に、ウェル当たり2.2〜2.7×106細胞の密度でプレーティングした。xCELLigence(登録商標)96ウェルcardio e-plate(ACEA/Roche Applied Sciences)または微小電極アレイ(MEA, Multichannel Systems)上に再プレーティングする前に、細胞を3〜5日間、37℃、7%CO2で培養した。細胞への温度ショックを最小化するために37℃に余熱した維持培地(CDI)を用いて、プレーティング後2日毎に、培地を交換した。
新たなRTCA cardioシステムは、より長い時間枠にわたって細胞実験のモニタリングを可能にし、かつ、並行して細胞の収縮(拍動)を測定する。各測定時点で、細胞インデックスならびに基となる収縮の頻度および振幅が測定される。
xCELLigence(登録商標)RTCA Cardioステーションは、7%CO2に設定されたインキュベーター中に設置される。インキュベーターは、顧客の現場で利用可能である。以下のコンポーネントが試験される。
6ウェルプレートにおいて培養したiCellを、dPBS(GIBCO)中で2回洗浄し、その後、37℃、7%CO2でインキュベーションしながら0.5%トリプシン-EDTA(GIBCO)で剥離させることによって採取した。トリプシンを維持培地で失活させ、細胞を集めて69gで5分間遠心分離し、目標密度を生じるように維持培地中に再懸濁した。cardio e-plateの再播種のために、80%の播種効率と見積もってウェル当たり5×104の目標密度で、細胞をプレーティングした。cardio e-plateは、0.1%ゼラチンで3時間、37℃でコーティングした。細胞を再播種する直前に、cardio e-plateについてのバックグラウンドインピーダンスの測定を、37℃に平衡化されているが細胞を含まない最終容積の培地で行った。実験を開始する前に、細胞を、xCELLigence(登録商標)RTCA cardioシステムによりその最大サンプリングレート(77 Hz)で、1時間毎に20秒の掃引持続時間によりモニタリングした。
化合物ストックを、DMSOまたはdH2Oにおいて最高試験濃度の1000倍で調製した。xCELLigence(登録商標)実験のために、化合物ストックを、維持培地において別々の96ウェル組織培養プレート(Corning)中で目標濃度の2倍に、連続的に希釈した。細胞曝露の前に、希釈プレートをインキュベーションし、37℃に平衡化した。存在する培地容積の半分をcardio e-plateから除去し、それぞれ2倍高い化合物濃度の等容積と置換して、それぞれのウェルにおいて最終目標濃度を生じた。すべての化合物を、複数のcardio e-plate上でn≧3として試験した。xCELLigence(登録商標)は、77 Hzでの周期的な20秒の掃引持続時間について拍動の変化をモニタリングした。
データを最初に、xCELLigence(登録商標)およびMEAシステムの内蔵解析モジュールにより解析し、最初の結果を次に、さらなる半自動解析のために社内で開発されたMicrosoft Excelテンプレートにエクスポートした。xCELLigence(登録商標)およびMEA記録の両方において、大きく減少した振幅を伴い、かつ予想される規則的な収縮/拍動の前に早発に起きるものとして、不整収縮/拍動を定義した。本発明者らは、「予測催不整脈スコア」(PPS)を計算するために、最初に「不規則拍動比」(IBR)を決定した。IBRは、1分間での拍動の総数に対する不整拍動数の比として定義された。各選択された時点での各濃度についてのIBR値を、3〜5枚のe-plateから平均化した。0.2以上のIBR値を生じた薬物の最低濃度を測定し、「IB20」と呼んだ。最後に、治療的最大血漿中濃度(Cmax)をIB20で割り、PPSを得た。PPS>100が、薬物誘導性不整脈について懸念すべきレベルである。
プロトコール:
1. iCellを、プレーティング培地において6ウェルプレート上に付着させる。
2. 最初の培地交換を、付着の48時間後に行い、細胞をiCell維持培地で満たす。
3. 細胞を分離し、フィブロネクチンでコーティングしたe-plate上に50K細胞/ウェルでプレーティングする。細胞を、1測定/時間の測定率で3日間までモニタリングする。その後、細胞を洗浄し、再び、1測定/時間の測定率で2〜3日間モニタリングする。
4. 播種の24時間後またはそれより後に、安定な拍動がすべてのウェルで達して初めて、化合物を三連でウェルに適用する。
5. インピーダンス測定を、実験全体を通して30秒の測定間隔で、細胞播種の完了時に開始する。化合物添加後の測定率は、処置後最初の1時間は60測定/時間であり、処置後2時間および3時間は12測定/時間であり、その後24時間は2測定/時間である。処置後24〜72時間のモニタリングについては、測定率は1/時間である。
6. 化合物適用後、収縮および生存率を、72時間までモニタリングする。選択された例において、化合物をより長い期間にわたって研究してもよい。
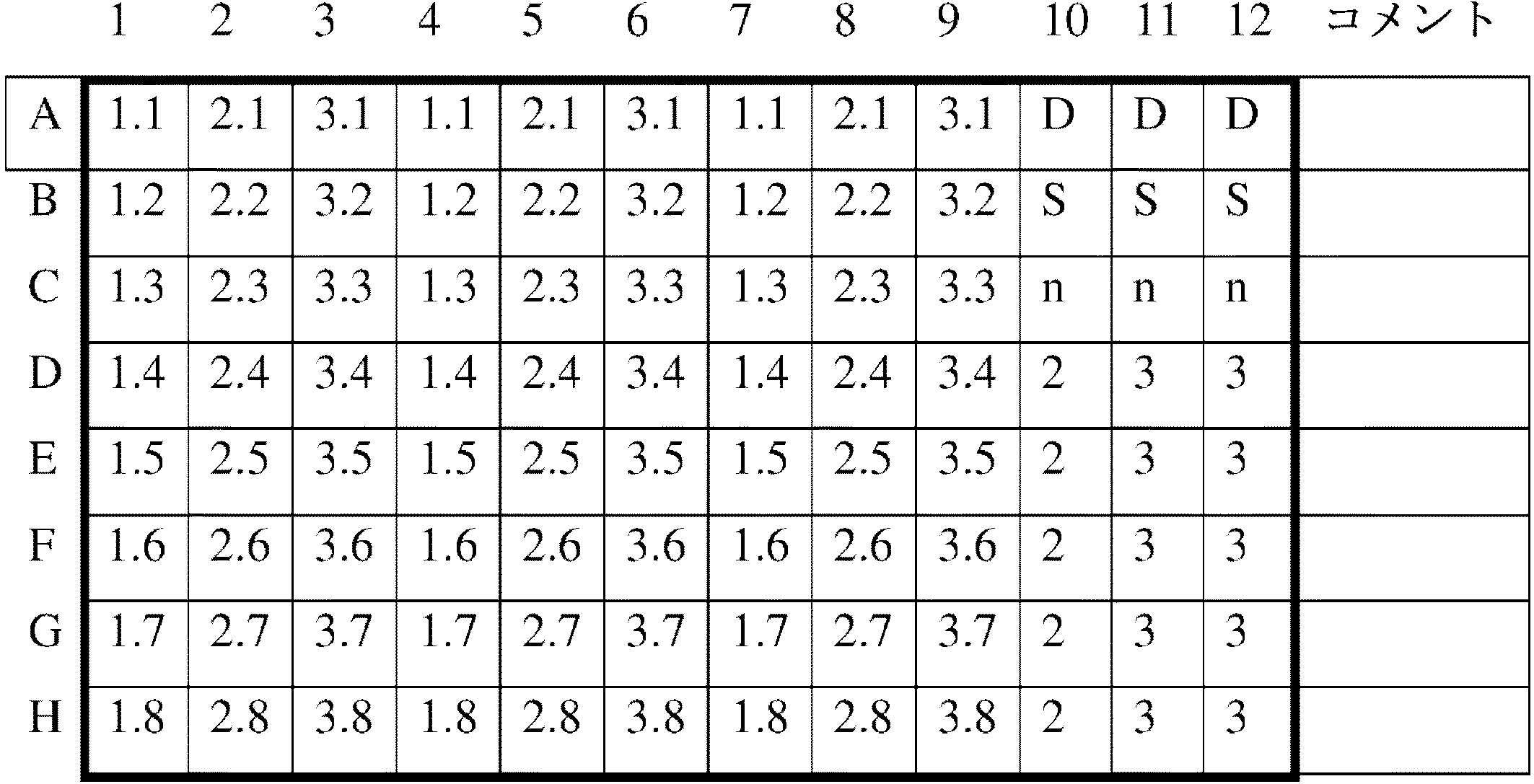
ゼラチン上のiCell心筋細胞
1.1:濃度1における化合物1
2.1:濃度2における化合物2
x.y:濃度yにおける化合物x
D:DMSO
S:溶媒
N:陰性対照
RTCA Cardio実験に使用した化合物を、微小電極アレイ(MEA)でスクリーニングし、細胞傷害性について基準としてATPを用いてスクリーニングした。
Claims (22)
- 薬物開発状況において分子をスクリーニングするために実施される、以下の段階を含む、薬物誘導性不整脈のリスクを判定するインビトロ方法:
a)心筋細胞を薬物と接触させる段階;
b)細胞収縮または電場電位のいずれかをモニタリングすることにより、拍動率の不規則性を検出する段階;
c)不規則拍動比(IBR)を計算する段階であって、0.2に等しいまたはそれ未満のIBRが、不整脈の低リスクを表すために使用される段階;および、
d)結果として予測催不整脈スコア(PPS)を生じる、薬物の臨床的有効最大血漿中濃度(C max )に対する20%を上回る不整拍動を結果として生じる薬物の最低濃度(IB 20 )の比を計算する段階、または結果としてPPSを生じる、IB 20 に対するC max の比を計算する段階。 - 心筋細胞が、イヌ、サル、ラット、ウサギ、またはヒト起源のものである、請求項1記載の方法。
- 心筋細胞が、ヒト起源のものである、請求項1または2記載の方法。
- 心筋細胞が、幹細胞源から産生される、請求項1〜3のいずれか一項記載の方法。
- 心筋細胞が、多能性幹細胞源から産生される、請求項1〜4のいずれか一項記載の方法。
- 幹細胞源が、人工多能性幹細胞源である、請求項5記載の方法。
- 不整脈の発生率が、細胞電場電位における変化をモニタリングすることにより検出される、請求項1〜6のいずれか一項記載の方法。
- 拍動率の不規則性が、細胞収縮をモニタリングすることにより測定される、請求項1〜7のいずれか一項記載の方法。
- 細胞収縮が、収縮中の心筋細胞の動きを同定可能なデータ捕捉率頻度でインピーダンスを測定することによりモニタリングされる、請求項8記載の方法。
- インピーダンスが、約12.9ミリ秒毎のサンプリングレートで測定される、請求項8または9記載の方法。
- 不整脈の検出が、拍動率リズムの増加、減少、または不規則性をモニタリングすることを含む、請求項1〜10のいずれか一項記載の方法。
- 拍動率リズムの不規則性が、トルサード・ド・ポワント(Torsades de Pointes)を示す、請求項11記載の方法。
- 拍動率リズムの不規則性が、QTの延長を示す、請求項11記載の方法。
- 拍動率リズムの不規則性が、心臓イオンチャンネルの破壊のためである、請求項11記載の方法。
- 心臓イオンチャンネルが、カリウムチャンネルである、請求項14記載の方法。
- カリウムチャンネルが、hERGチャンネルである、請求項15記載の方法。
- 心臓イオンチャンネルが、カルシウムチャンネルである、請求項14記載の方法。
- 心臓イオンチャンネルが、ナトリウムチャンネルである、請求項14記載の方法。
- 以下の段階をさらに含む、請求項1〜18のいずれか一項記載の方法:
e)結果としてPPSを生じる、IB20に対するCmaxの比を計算する段階。 - 100に等しいまたはそれ未満のPPSが、不整脈の低リスクを表すために使用される、請求項1〜19のいずれか一項記載の方法。
- 以下の段階をさらに含む、請求項19〜20のいずれか一項記載の方法:
f)段階e)の結果を、公知の不整脈誘導薬物の結果と比較する段階。 - ハイスループットフォーマットで実施される、請求項1〜21のいずれか一項記載の方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US40793110P | 2010-10-29 | 2010-10-29 | |
| US61/407,931 | 2010-10-29 | ||
| US41536810P | 2010-11-19 | 2010-11-19 | |
| US61/415,368 | 2010-11-19 | ||
| PCT/EP2011/068579 WO2012055828A1 (en) | 2010-10-29 | 2011-10-25 | Method of determining risk of arrythmia |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013543726A JP2013543726A (ja) | 2013-12-09 |
| JP6133210B2 true JP6133210B2 (ja) | 2017-05-24 |
Family
ID=45001708
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013535391A Expired - Fee Related JP6133210B2 (ja) | 2010-10-29 | 2011-10-25 | 不整脈のリスクを判定する方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US20120107861A1 (ja) |
| EP (1) | EP2633322B1 (ja) |
| JP (1) | JP6133210B2 (ja) |
| KR (2) | KR101774182B1 (ja) |
| CN (1) | CN103221826B (ja) |
| BR (1) | BR112013009888A2 (ja) |
| CA (1) | CA2815108A1 (ja) |
| MX (1) | MX2013004351A (ja) |
| RU (1) | RU2583941C2 (ja) |
| WO (1) | WO2012055828A1 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2954322B1 (en) * | 2013-02-08 | 2018-07-18 | Johannes Backs | In vitro method for cardiovascular risk stratification |
| KR101617683B1 (ko) * | 2015-01-09 | 2016-05-03 | 연세대학교 산학협력단 | 부정맥 치료제 효과 평가 시스템 및 방법 |
| US9983198B2 (en) | 2015-03-19 | 2018-05-29 | Axion Biosystems, Inc. | Systems and methods for assessing data collected from an electrically active cell culture |
| JP6940920B2 (ja) * | 2017-02-04 | 2021-09-29 | アナバイオス コーポレーション | 医薬誘発性の変力作用および不整脈誘発のリスクを予測するためのシステムおよび方法 |
| US20200240980A1 (en) * | 2017-10-12 | 2020-07-30 | The Research Foundation For The State University Of New York | Method for delayed rectifier current enhancement, characterization, and analysis in human induced pluripotent stem cells |
| JP7341478B2 (ja) * | 2017-12-26 | 2023-09-11 | 株式会社マイオリッジ | 心筋細胞の薬剤応答性試験方法 |
| EP3979997A1 (en) * | 2019-06-06 | 2022-04-13 | Novo Nordisk A/S | Application of antiarrhythmic agents to stem cell derived cardiomyocytes and uses thereof |
| WO2022004963A1 (ko) * | 2020-07-02 | 2022-01-06 | 주식회사 티앤알바이오팹 | 인간 전분화능줄기세포 유래 심근세포를 이용한 SARS-CoV-2 바이러스 대상 후보 약물의 부정맥 위험성 평가용 조성물 및 이를 이용한 부정맥 위험성 평가 방법 |
| KR102590512B1 (ko) * | 2021-04-19 | 2023-10-16 | 건국대학교 글로컬산학협력단 | 인간 유도만능줄기세포 유래 심근세포 및 다중전극 분석을 이용한 이중-심장독성평가 방법 |
| KR102629870B1 (ko) * | 2021-05-14 | 2024-01-29 | (주) 넥셀 | 인간 줄기세포 유래 심근세포를 이용한 약물의 심장 안전성 평가 방법 |
| WO2022255532A1 (ko) * | 2021-06-01 | 2022-12-08 | 주식회사 티앤알바이오팹 | 인간 전분화능줄기세포 유래 심근세포를 이용한 약물의 부정맥 위험성 평가 방법 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1301414A1 (ru) * | 1985-09-27 | 1987-04-07 | Научно-Исследовательский Институт По Биологическим Испытаниям Химических Соединений | Способ определени индивидуальной чувствительности к кардиотропному препарату |
| US7611852B2 (en) * | 2002-07-26 | 2009-11-03 | Wisconsin Alumni Research Foundation | Functional cardiomyocytes from human embryonic stem cells |
| US20050009006A1 (en) * | 2003-05-09 | 2005-01-13 | Ofer Binah | High throughput monitoring chamber for testing drug effects on repolarization and conduction |
| US8318488B1 (en) * | 2004-05-11 | 2012-11-27 | Axiogenesis Ag | Assay for drug discovery based on in vitro differentiated cells |
| US7813792B2 (en) * | 2006-04-17 | 2010-10-12 | General Electric Company | Method and apparatus for analyzing and editing ECG morphology and time series |
| EP2213721B1 (en) * | 2007-09-18 | 2016-03-02 | Reprocell, Inc. | Cell measuring vessel, extracellular potential measuring method, and chemical testing method |
| JP2009244197A (ja) * | 2008-03-31 | 2009-10-22 | Hioki Ee Corp | 薬剤感受性試験方法及び装置 |
| WO2009137440A1 (en) * | 2008-05-05 | 2009-11-12 | Acea Biosciences, Inc. | Label-free monitoring of excitation-contraction coupling and excitable cells using impedance based systems with millisecond time resolution |
-
2011
- 2011-10-25 EP EP11773470.7A patent/EP2633322B1/en not_active Not-in-force
- 2011-10-25 CA CA2815108A patent/CA2815108A1/en not_active Abandoned
- 2011-10-25 RU RU2013123513/15A patent/RU2583941C2/ru not_active IP Right Cessation
- 2011-10-25 BR BR112013009888-0A patent/BR112013009888A2/pt not_active IP Right Cessation
- 2011-10-25 KR KR1020167003467A patent/KR101774182B1/ko not_active Expired - Fee Related
- 2011-10-25 CN CN201180051232.4A patent/CN103221826B/zh not_active Expired - Fee Related
- 2011-10-25 KR KR1020137010889A patent/KR20130079566A/ko not_active Ceased
- 2011-10-25 WO PCT/EP2011/068579 patent/WO2012055828A1/en not_active Ceased
- 2011-10-25 MX MX2013004351A patent/MX2013004351A/es unknown
- 2011-10-25 JP JP2013535391A patent/JP6133210B2/ja not_active Expired - Fee Related
- 2011-10-27 US US13/282,634 patent/US20120107861A1/en not_active Abandoned
-
2017
- 2017-05-10 US US15/591,525 patent/US20170241987A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN103221826A (zh) | 2013-07-24 |
| KR101774182B1 (ko) | 2017-09-01 |
| CA2815108A1 (en) | 2012-05-03 |
| JP2013543726A (ja) | 2013-12-09 |
| EP2633322A1 (en) | 2013-09-04 |
| MX2013004351A (es) | 2013-06-07 |
| RU2013123513A (ru) | 2014-12-10 |
| KR20130079566A (ko) | 2013-07-10 |
| WO2012055828A1 (en) | 2012-05-03 |
| US20120107861A1 (en) | 2012-05-03 |
| CN103221826B (zh) | 2016-02-03 |
| HK1187678A1 (zh) | 2014-04-11 |
| EP2633322B1 (en) | 2018-02-14 |
| RU2583941C2 (ru) | 2016-05-10 |
| KR20160022393A (ko) | 2016-02-29 |
| US20170241987A1 (en) | 2017-08-24 |
| BR112013009888A2 (pt) | 2021-07-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6133210B2 (ja) | 不整脈のリスクを判定する方法 | |
| Abassi et al. | Dynamic monitoring of beating periodicity of stem cell‐derived cardiomyocytes as a predictive tool for preclinical safety assessment | |
| Sala et al. | Integrating cardiomyocytes from human pluripotent stem cells in safety pharmacology: has the time come? | |
| Kitaguchi et al. | CSAHi study: evaluation of multi-electrode array in combination with human iPS cell-derived cardiomyocytes to predict drug-induced QT prolongation and arrhythmia—effects of 7 reference compounds at 10 facilities | |
| Hu et al. | High-performance beating pattern function of human induced pluripotent stem cell-derived cardiomyocyte-based biosensors for hERG inhibition recognition | |
| Braam et al. | Repolarization reserve determines drug responses in human pluripotent stem cell derived cardiomyocytes | |
| Zhang et al. | Multi-parametric assessment of cardiomyocyte excitation-contraction coupling using impedance and field potential recording: A tool for cardiac safety assessment | |
| Kitaguchi et al. | CSAHi study: detection of drug-induced ion channel/receptor responses, QT prolongation, and arrhythmia using multi-electrode arrays in combination with human induced pluripotent stem cell-derived cardiomyocytes | |
| Ciammola et al. | Low anaerobic threshold and increased skeletal muscle lactate production in subjects with Huntington's disease | |
| Zhao et al. | Drug testing in human‐induced pluripotent stem cell–derived cardiomyocytes from a patient with short QT syndrome type 1 | |
| Asai et al. | Combination of functional cardiomyocytes derived from human stem cells and a highly-efficient microelectrode array system: an ideal hybrid model assay for drug development | |
| Zhao et al. | Cardiotoxicity evaluation using human embryonic stem cells and induced pluripotent stem cell-derived cardiomyocytes | |
| Obergrussberger et al. | Safety pharmacology studies using EFP and impedance | |
| Cai et al. | Homocysteine inhibits potassium channels in human atrial myocytes. | |
| Haws et al. | Developmental regulation of mechanosensitive calcium channels in skeletal muscle from normal and mdx mice | |
| SG192305A1 (en) | Induced pluripotent stem cell (ipsc)-derived cardiomyocyte-like cells and uses thereof in screening for agents | |
| CN109983342B (zh) | 用于模拟疾病和评估其治疗副作用的系统和方法 | |
| Zhang et al. | Enhancing the functional maturity of hiPSC-derived cardiomyocytes to assess inotropic compounds | |
| Šarić et al. | Induced pluripotent stem cells as cardiac arrhythmic in vitro models and the impact for drug discovery | |
| Li et al. | Induced pluripotent stem cells in congenital long QT syndrome: Research progress and clinical applications | |
| Goineau et al. | Proarrhythmic risk assessment using conventional and new in vitro assays | |
| HK1187678B (en) | Method of determining risk of arrythmia | |
| Vos | Literature‐based evaluation of four ‘hard endpoint’models for assessing drug‐induced torsades de pointes liability | |
| Xian et al. | Kinase inhibitor-induced cardiotoxicity assessed in vitro with human pluripotent stem cell derived cardiomyocytes | |
| Zheng et al. | Personalized In Vitro Models Reveal Functional Impact of a KCNH2 Mutation and Enable Drug Screening in LQT2 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141001 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141222 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150331 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150421 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150826 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151221 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160125 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20160129 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20160311 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161219 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170419 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6133210 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |