JP5488564B2 - ウミホタルルシフェリン発光基質及びその製造法 - Google Patents
ウミホタルルシフェリン発光基質及びその製造法 Download PDFInfo
- Publication number
- JP5488564B2 JP5488564B2 JP2011234649A JP2011234649A JP5488564B2 JP 5488564 B2 JP5488564 B2 JP 5488564B2 JP 2011234649 A JP2011234649 A JP 2011234649A JP 2011234649 A JP2011234649 A JP 2011234649A JP 5488564 B2 JP5488564 B2 JP 5488564B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- cypridina
- compound
- luciferin
- luciferase
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- HZAXKUQPEHFHHP-JRTLGTJJSA-N CC[C@H](C)C1=NC2=C(CCCNC(N)=N)NC(c3c[nH]c4c3cccc4)=CN2C1O Chemical compound CC[C@H](C)C1=NC2=C(CCCNC(N)=N)NC(c3c[nH]c4c3cccc4)=CN2C1O HZAXKUQPEHFHHP-JRTLGTJJSA-N 0.000 description 1
- 0 C[C@@]([C@@](C)N=C(C(CCCNC(N)=N)=NC)N)C1c2ccccc2*1 Chemical compound C[C@@]([C@@](C)N=C(C(CCCNC(N)=N)=NC)N)C1c2ccccc2*1 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/67—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton
- C07C45/68—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/04—Saturated compounds containing keto groups bound to acyclic carbon atoms
- C07C49/175—Saturated compounds containing keto groups bound to acyclic carbon atoms containing ether groups, groups, groups, or groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/04—Saturated compounds containing keto groups bound to acyclic carbon atoms
- C07C49/185—Saturated compounds containing keto groups bound to acyclic carbon atoms containing —CHO groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/20—Unsaturated compounds containing keto groups bound to acyclic carbon atoms
- C07C49/255—Unsaturated compounds containing keto groups bound to acyclic carbon atoms containing ether groups, groups, groups, or groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
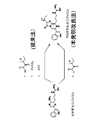
<スキーム1>
本製造法はArndt-Eistert反応を鍵反応とする三工程である。まず、(+)−2−メチル酪酸(1A)の1モルに対し、1モル程度から過剰量の塩化チオニルを使用し、室温で1〜24時間反応させることで酸クロライドが得られる。次に、得られた酸クロライドを2当量のトリメチルシリルジアゾメタンまたはジアゾメタンを使用し、0〜4℃で1〜4時間を反応させると、ジアゾケトン化合物が得られる。得られたジアゾケトン化合物は1当量程度の酸化剤(特にtert-butyl hypochlorite)を使用し、当量又は過剰のアルコールまたはグリコールの存在下に0〜4℃で1〜2時間反応させることで、新規の光学活性な化合物(2)を得ることができる。また、R1とR2はベンジルオキシ基である場合、触媒量の酸化白金の存在下に、加水素分解で一般式(2)の化合物(アルデヒド体)を得ることができる。
<スキーム2>
反応は、一般式(3)の化合物1モルに対して、一般式(2)の化合物を1〜4モル程度使用し、酸の存在下または非存在下に65〜100℃程度の温度で1〜2時間反応させることで有利に進行する。
<スキーム3>
スキーム3で示している一般式(5)または一般式(3)の化合物の製造法について説明する。
<スキーム4>
一般式(5)の化合物1モルに対して、一般式(6)の化合物を1〜4モル程度使用し、酸の存在下または非存在下に65〜100℃の温度で1〜2時間反応させることで一般式(7)の化合物が得られる。
<スキーム5>
一般式(3)の化合物1モルに対して、一般式(6)の化合物を1〜4モル程度使用し、酸の存在下または非存在下に65〜100℃の温度で1〜2時間反応させることで一般式(8)の化合物が得られる。
化合物(13)(0.4g, 1 mmol)および1-(phenylsulfonyl)3-indoleboronic acid (0.73 g, 2 mmol)のジオキサン50 ml-飽和Na2CO3(24ml)溶液にPd(PPh3)4(30 mg)を加えた。混合物を1時間80℃で加熱した。冷却後、反応混合物を酢酸エチルで希釈し、食塩水で洗浄、硫酸ナトリウムで乾燥させた。ろ過後、濃縮して粗抽出物が得られた。粗抽出物はクロマトグラフィーにて精製されて所望の生成物を得た。所望の生成物を8ml Methanol-Dioxane溶液で溶かし、5N 水酸化ナトリウム(2ml)を加えた。室温で一晩攪拌した。後処理した後、混合物をクロマトグラフィーにて精製し、化合物(14)(170mg, 46%)が得られた。1H NMR (500 MHz, CDCl3) 1.45 (9H, s), 4.04 (2H, br), 4.55 (2H, br), 4.80 (1H, br), 6.61 (1H, d, J=15 Hz), 6.94 (1H, br), 7.21−7.27(2H, m), 7.41 (1H, d, J =7 Hz), 7.66 (1H, d, J =2.5 Hz) 8.41(1H, br), 8.35(1H, s).
1H NMR (500 MHz, CD3OD) 3.85 (2H, d, J =7 Hz), 6.98-7.17(4H, m), 7.41 (1H, d, J =7 Hz), 7.77 (1H, s), 8.28 (1H, d, J =7 Hz), 8.34(1H, s).
化合物(10)は実施例4で示した化合物(16)の製造法と同じ方法で製造された。
化合物(10)の物性:1H NMR (500 MHz, CDCl3) 2.03 (2H, d, J=7 Hz), 2.80 (2H, d, J=7 Hz), 3.28 (2H, d, J=7 Hz), 7.08-7.16 (2H, m), 7.41(1H, d, J =7Hz) 7.90(1H, s), 8.30 (1H, s).
化合物(30)の合成:ナスフラスコの中に化合物(10)(10 mg)、水(0.1 ml)、29 (0.020 ml)、エタノール(0.1 ml)、49% HBr (0.01 ml) 1時間100℃で加熱した。反応液を室温に戻したのち、減圧濃縮した。残渣をエタノールで溶かし、LH-20カラムにて精製し、化合物(30)(6 mg, 42%)が得られた。1H NMR (500 MHz, CD3OD) 2.24 (2H, quintet, J=7 Hz), 3.25 (2H, t, J=7 Hz), 3.39 (2H, t, J=7 Hz), 4.27 (2H, s), 7.10 (2H, dd, J=7 Hz), 7.24 (1H, t, J=7 Hz), 7.30-7.45 (5H, m), 7.93(1H, dd, J=7 Hz), 7.96 (1H, s), 8.27 (1H, s).
0.1ml の50mM Tris-HCl緩衝液(pH7.5)の中に、ウミホタルルシフェラ−ゼ(終濃度100 ng/ml)とウミホタルルシフェリンまたはオレフィン基を有する新規ウミホタルルシフェリンアナログ(化合物(17))を混合し、30秒間積算した発光スペクトルを計測した結果、化合物(17)の発光最大波長は天然ルシフェリンに比べて、約15 nmほど長波長側へシフトした。
0.1ml の50mM Tris-HCl緩衝液(pH7.5)の中に、ウミホタルルシフェラ−ゼ(終濃度100 ng/ml)と新規ウミホタルルシフェリンアナログ(化合物(30),(32),(34),(36),(37))を混合し、発光スペクトルを計測した(図2)。
0.3M アスコルビン酸ナトリウムを含むまたは含まない0.1 ml の100mM Tris-HCl緩衝液(pH7.5)または0.1 ml の100mM Tris-HCl緩衝液(pH7.5)・0.3M NaClの中に、ウミホタルルシフェリン(終濃度1μM)を混合し、10秒間の発光値(バックグランド)を測定したのちに、ウミホタルルシフェラ−ゼ(終濃度5 ng/ml)を加え、10秒間のルシフェラーゼによる発光値を測定した。
結果を表1に示す。
0.3M アスコルビン酸ナトリウムと0.02M 亜硫酸ナトリウムを含む100mM Tris-HCl緩衝液(pH7.5)の中に、ウミホタルルシフェリン(終濃度1μM)とウミホタルルシフェラ−ゼ(終濃度5 ng/ml)を混合し、10秒間のルシフェラーゼによる発光値を測定した。さらに、室温で放置したルシフェリンの24時間後の生物発光活性を測定した。結果を表3に示す。
酸化防止剤が無い条件、0.3M アスコルビン酸ナトリウム、0.3M アスコルビン酸ナトリウムと0.02M Na2SO3を含む100mM Tris-HCl緩衝液/1% BSA(pH7.5)の中に、ウミホタルルシフェリン(終濃度1μM)を混合し、10秒間の発光値(バックグランド)を測定したのちに、ウミホタルルシフェラ−ゼ(終濃度5 ng/ml)を加え、10秒間のルシフェラーゼによる発光値を測定した。結果を表4に示す。
1.発光最大波長が390〜620nmであって、発光波長が測定条件に依存しない光を発光する2つのウミホタルルシフェラーゼ及びウミホタルルシフェラーゼ・蛍光タンパク質融合体遺伝子による2つの遺伝子転写活性を、細胞外に分泌されたタンパク質で計測するシステム。
2.ウミホタルルシフェラーゼ・ウミホタルルシフェリンアナログ反応により発光最大波長が390-520nmとなる発光反応。ウミホタルルシフェリンアナログ36なら最大発光波長およそ390nm(図3A)
3.ウミホタルルシフェラーゼ・蛍光タンパク質融合体・ウミホタルルシフェリンアナログ反応により発光最大波長が500-620nmとなる発光反応。例えば、ウミホタルルシフェラーゼ・GFPならおよそ510nm(図3A)
4.2,3の組み合わせは最大発光波長が100nm以上離れていることが望ましいが、30nmなら色分割可能であり、その組み合わせでデュアルレポーターアッセイを行う。
5.ウミホタルルシフェラーゼ遺伝子上流にプロモ−ターAを、ウミホタルルシフェラーゼ・蛍光タンパク質融合体上流にプロモ−ターBを挿入(図3B)、2つの遺伝子構築体を細胞内にトランスフェクション、トランスフェクション後、一定時間培養後、回収した培養液か、或いは培養プレートに直接、ウミホタルルシフェリンアナログを加え、色フィルターで分離、2つの発光量を測定、プロモーターA、Bの活性量を測定する(細胞破砕する必要がないことから、生きた細胞のまま、遺伝子転写活性を測定できる)(図3C)。プロモーターAのみが活性化している場合、最大発光波長390nmの発光のみ観察されるが、プロモーターBの活性化と共に510nm付近にピークが観察され、これが増大する。発光スペクトルはフィルターによって簡単に分離可能である。
Claims (5)
- ウミホタルルシフェリンとアスコルビン酸またはその塩及び亜硫酸塩を含む、ウミホタルルシフェラーゼとウミホタルルシフェリンを用いた生物発光系に使用するためのウミホタルルシフェリン安定化組成物。
- ウミホタルルシフェリンをアスコルビン酸またはその塩及び亜硫酸塩の存在下に保存することを特徴とする、ウミホタルルシフェラーゼとウミホタルルシフェリンを用いた生物発光系に使用されるウミホタルルシフェリンの保存方法。
- ウミホタル生物発光系に使用するためのキットであって、ウミホタルルシフェリンと、アスコルビン酸またはその塩及び亜硫酸塩を含むキットであって、ウミホタル生物発光系はウミホタルルシフェラーゼとウミホタルルシフェリンを用いた生物発光系である、キット。
- アスコルビン酸またはその塩、エリソルビン酸またはその塩及び亜硫酸塩のウミホタル生物発光系のバックグラウンドを低減するための使用であって、ウミホタル生物発光系はウミホタルルシフェラーゼとウミホタルルシフェリンを用いた生物発光系である、使用。
- ウミホタルルシフェラーゼとウミホタルルシフェリンの生物発光測定系においてアススコルビン酸またはその塩及び亜硫酸塩の存在下に生物発光を測定することを特徴とする、ウミホタル系生物発光の測定方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011234649A JP5488564B2 (ja) | 2005-09-26 | 2011-10-26 | ウミホタルルシフェリン発光基質及びその製造法 |
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005277020 | 2005-09-26 | ||
| JP2005277020 | 2005-09-26 | ||
| JP2006024176 | 2006-02-01 | ||
| JP2006024176 | 2006-02-01 | ||
| JP2006073818 | 2006-03-17 | ||
| JP2006073818 | 2006-03-17 | ||
| JP2006130203 | 2006-05-09 | ||
| JP2006130203 | 2006-05-09 | ||
| JP2011234649A JP5488564B2 (ja) | 2005-09-26 | 2011-10-26 | ウミホタルルシフェリン発光基質及びその製造法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007536587A Division JP4915955B2 (ja) | 2005-09-26 | 2006-09-25 | ウミホタルルシフェリン発光基質及びその製造法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012095649A JP2012095649A (ja) | 2012-05-24 |
| JP5488564B2 true JP5488564B2 (ja) | 2014-05-14 |
Family
ID=37888994
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007536587A Active JP4915955B2 (ja) | 2005-09-26 | 2006-09-25 | ウミホタルルシフェリン発光基質及びその製造法 |
| JP2011234649A Active JP5488564B2 (ja) | 2005-09-26 | 2011-10-26 | ウミホタルルシフェリン発光基質及びその製造法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007536587A Active JP4915955B2 (ja) | 2005-09-26 | 2006-09-25 | ウミホタルルシフェリン発光基質及びその製造法 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US7989621B2 (ja) |
| EP (2) | EP2940020B1 (ja) |
| JP (2) | JP4915955B2 (ja) |
| CN (2) | CN102532143B (ja) |
| WO (1) | WO2007034952A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5224100B2 (ja) * | 2008-03-05 | 2013-07-03 | 独立行政法人産業技術総合研究所 | 変異型ルシフェラーゼ |
| JP7448993B2 (ja) * | 2019-09-26 | 2024-03-13 | ウィタヤシリメティ インスティチュート オブ サイエンス アンド テクノロジー | ルシフェリン誘導体及びその合成方法 |
| JP7194404B1 (ja) * | 2021-03-19 | 2022-12-22 | 関東電化工業株式会社 | D-ルシフェリン及びd-ルシフェリン誘導体、並びにこれら化合物の前駆体、並びにこれらの製造方法 |
| WO2024014536A1 (ja) * | 2022-07-15 | 2024-01-18 | 国立研究開発法人産業技術総合研究所 | Sars関連コロナウイルスの検出試薬 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE145004T1 (de) | 1988-08-09 | 1996-11-15 | Toray Industries | Verfahren zur herstellung von luciferase durch rekombinante expression eines luciferase- kodierenden gens |
| JP2834187B2 (ja) | 1989-06-29 | 1998-12-09 | 財団法人大阪バイオサイエンス研究所 | ルシフェラーゼをコードするdna化合物およびそれを含有する発現ベクター |
| JPH0560697A (ja) | 1991-08-30 | 1993-03-12 | Nippon Oil & Fats Co Ltd | スーパーオキシドアニオンの定量方法及びスーパーオキシドアニオン消去物質の定量方法 |
| JP3314397B2 (ja) | 1992-01-28 | 2002-08-12 | 日本油脂株式会社 | ウミホタルルシフェリン誘導体 |
| DE69313611T2 (de) | 1992-07-02 | 1998-01-08 | Erkki Soini | Biospezifisches multiparameter-analyseverfahren |
| JPH09201397A (ja) | 1996-01-26 | 1997-08-05 | Kyowa Medex Co Ltd | 液状診断薬の保存方法 |
| US5876995A (en) | 1996-02-06 | 1999-03-02 | Bryan; Bruce | Bioluminescent novelty items |
| EP0955497A4 (en) * | 1996-12-20 | 2000-05-03 | Kikkoman Corp | LUMINESCENT TOOL, ITS AUXILIARY ELEMENTS AND METHOD FOR THE PRESERVATION OF BIOLUMINESCENTS, COMPOSITION USED IN THE TOOL AND AUXILIARY ELEMENT |
| JP4484429B2 (ja) | 2002-12-06 | 2010-06-16 | アトー株式会社 | 高分泌型ウミボタル類縁発光酵素のタンパク質 |
| EP1580196B1 (en) | 2002-12-12 | 2010-08-04 | Japan Science And Technology Agency | Monitor protein for measuring processing of protein |
| JP2005169768A (ja) | 2003-12-10 | 2005-06-30 | Seiko Epson Corp | 印刷装置及び印刷装置における画像データの書込み方法 |
| US7718389B2 (en) * | 2006-07-24 | 2010-05-18 | National Institute Of Advanced Industrial Science And Technology | Stabilizing composition and stabilizing method of coelenterazine solution for high-throughput measurement of luciferase activity |
-
2006
- 2006-09-25 JP JP2007536587A patent/JP4915955B2/ja active Active
- 2006-09-25 CN CN201110444084.4A patent/CN102532143B/zh not_active Expired - Fee Related
- 2006-09-25 EP EP15000899.3A patent/EP2940020B1/en not_active Not-in-force
- 2006-09-25 US US11/992,660 patent/US7989621B2/en active Active
- 2006-09-25 CN CN2006800354103A patent/CN101273041B/zh not_active Expired - Fee Related
- 2006-09-25 EP EP06810525.3A patent/EP1930332B1/en not_active Not-in-force
- 2006-09-25 WO PCT/JP2006/319000 patent/WO2007034952A1/ja not_active Ceased
-
2011
- 2011-06-09 US US13/067,565 patent/US8343729B2/en not_active Expired - Fee Related
- 2011-10-26 JP JP2011234649A patent/JP5488564B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US8343729B2 (en) | 2013-01-01 |
| US20110287459A1 (en) | 2011-11-24 |
| EP1930332A1 (en) | 2008-06-11 |
| EP2940020A1 (en) | 2015-11-04 |
| JP4915955B2 (ja) | 2012-04-11 |
| WO2007034952A1 (ja) | 2007-03-29 |
| EP1930332A4 (en) | 2010-03-31 |
| JPWO2007034952A1 (ja) | 2009-04-02 |
| JP2012095649A (ja) | 2012-05-24 |
| US7989621B2 (en) | 2011-08-02 |
| CN101273041A (zh) | 2008-09-24 |
| US20090136974A1 (en) | 2009-05-28 |
| CN102532143B (zh) | 2015-06-24 |
| EP1930332B1 (en) | 2015-06-03 |
| CN102532143A (zh) | 2012-07-04 |
| EP2940020B1 (en) | 2018-04-25 |
| CN101273041B (zh) | 2012-02-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2454261B1 (en) | Imidazo[1,2-alpha]pyrazin-3(7h)-one derivatives bearing a new electron-rich structure | |
| JP5582505B2 (ja) | セレンテラジン類縁体及びその製造方法 | |
| Shimomura et al. | Mechanism of the luminescent oxidation of Cypridina luciferin | |
| JP5488564B2 (ja) | ウミホタルルシフェリン発光基質及びその製造法 | |
| US8962854B2 (en) | Luminescent substrate for luciferase | |
| US8709821B2 (en) | Luminescent substrate for liciferase | |
| JP5550035B2 (ja) | 波長が制御されたルシフェラーゼの発光基質および製造方法 | |
| JP2010215795A5 (ja) | ||
| Toya et al. | Synthesis and Chemiluminescence Properties of 6-(4-Methoxyphenyl)-2-methylimidazo (1, 2-a) pyrazin-3 (7H)-one and 2-Methyl-6-(2-naphthyl) imidazo (1, 2-a) pyrazin-3 (7H)-one. | |
| Dunn et al. | The synthesis of fluorine-containing pterins | |
| JP2014218456A (ja) | 新規ハロゲン化水素塩 | |
| US7897787B2 (en) | Maleimide derivative | |
| JP2013184909A (ja) | ルシフェラーゼの発光基質 | |
| Isobe et al. | 19F-Dehydrocoelenterazine as probe to investigate the active site of symplectin | |
| Teranishi et al. | No electron-donating substituent effect on the singlet excited state formation from the 5-(5-aryl-2-pyrazinylamino)-1, 2, 4-trioxanes in dimethyl sulfoxide triggered by potassium t-butoxide. | |
| US20250368636A1 (en) | Novel heterocyclic compound, salt thereof, and luminescent substrate composition | |
| Zheng et al. | Synthesis, Chemi-and Bioluminescence Properties, and Photolysis of a Coelenterazine Analogue Having a Photoreactive Azido Group. | |
| US20250171450A1 (en) | Novel coelenterazine derivatives | |
| JP7713216B2 (ja) | 新規複素環式化合物及びその塩、並びに、発光基質組成物 | |
| Tsuge et al. | INTRAMOLECULAR OXIDATIVE COUPLING OF BROMINATED 2, 4′-DIHYDROXYDIARYLMETHANES. A BIOGENETIC SYNTHESIS OF THELEPIN AND ITS ANALOGS | |
| JP2023022662A (ja) | 化合物、アミノ酸酸化酵素の酵素活性測定用試薬、及びアミノ酸酸化酵素の酵素活性測定方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130716 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130904 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20130904 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140210 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5488564 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |