JP5289963B2 - 抗addlモノクローナル抗体およびその使用 - Google Patents
抗addlモノクローナル抗体およびその使用 Download PDFInfo
- Publication number
- JP5289963B2 JP5289963B2 JP2008536730A JP2008536730A JP5289963B2 JP 5289963 B2 JP5289963 B2 JP 5289963B2 JP 2008536730 A JP2008536730 A JP 2008536730A JP 2008536730 A JP2008536730 A JP 2008536730A JP 5289963 B2 JP5289963 B2 JP 5289963B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- antibodies
- amino acid
- seq
- binding
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/567—Framework region [FR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/71—Decreased effector function due to an Fc-modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Neurosurgery (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Pharmacology & Pharmacy (AREA)
- Neurology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
本出願は、2005年10月21日出願のPCT出願番号PCT/US2005/0038125の一部継続出願である。
アルツハイマー病は、進行性および変性認知症である(Terryら(1991)、Ann. Neurol. 30:572-580;Coyle (1987)、Encyclopedia of Neuroscience, Adelman(編)、Birkhaeuser, Boston-Basel-Stuttgart, 29〜31頁中)。初期段階において、アルツハイマー病は、報告されたところではアミロイドベータ(Aβ)から由来する神経毒のために、新たな記憶の形成の深刻な不能として出現する(Selkoe (2002)、Science 298:789-791)。Aβは、存在量がアルツハイマー病に関連する変異や危険因子により増加する、両親媒性ペプチドである。Aβから形成される原繊維は、アミロイドプラークの核を構成し、これは、アルツハイマー病の脳の特徴である。インビトロで産生された類似する原繊維は、培養した脳ニューロンに対して致命的である。これらの所見により、記憶喪失が、原繊維状Aβにより生じたニューロン死の結果であることが、示される。
本発明は、1種または2種以上のAβ由来拡散性リガンドの多次元立体構造を区別して認識することができる、単離された抗体またはその断片である。特に、本発明の抗体は、Arg−Xaa1−Leu−Xaa2−Xaa3−Xaa4−Xaa5−Xaa6−Asp−Ala−Met−Asp−Tyr(配列番号9)の相補性決定領域(CDR)を有し、ここでXaa1はGlnまたはAlaであり;Xaa2はSerまたはGlyであり;Xaa3はPro、Ala、Lys、ArgまたはThrであり;Xaa4はLysまたはArgであり;Xaa5はGly、SerまたはLysであり;Xaa6はVal、Thr、IleまたはArgである。特別な態様において、本発明の抗体は、薬学的に許容し得る担体との混合物においてである。他の態様において、本発明の抗体は、キットにおいてである。さらに他の態様は、配列番号108および配列番号112に定める重鎖可変領域および軽鎖可変領域の配列を有する抗体を包含する。配列番号138および配列番号140に定める重鎖および軽鎖配列を有する抗体を、また、提供する。
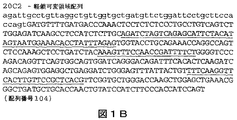
図1は、マウス抗ADDL抗体20C2の重鎖可変領域(図1A)および軽鎖可変領域(図1B)の核酸配列を示す。小文字は、抗体リーダー配列を示し、大文字は、抗体可変領域配列を示す。相補性決定領域(CDR)をコードするヌクレオチドに、下線を付す。
図9は、一次海馬ニューロンに結合するbADDLのHu20C2A3阻害を示す。
図10は、Hu20C2A3の蛍光熱溶融分析を示す。
Aβ由来拡散性リガンド(即ちADDL)の多次元立体構造を差別化的に認識するモノクローナル抗体が、ここで生成された。本発明の抗体は、マウスモノクローナル抗体20C2に由来する。マウス20C2は、当該分野において、以下の特徴を示すものと知られている。マウス20C2は、培養海馬細胞に結合した合成ADDLと内因性ADDLとの両方に結合するIgG1抗体である。さらに、この抗体は、培養した細胞に結合する内因性ADDLと合成ADDLとの両方を遮断し、ビオチン化ADDL(bADDL)のニューロンへの結合を弱め、タウリン酸化を防止し得る。20C2のコアの直線状エピトープは、Glu−Phe−Arg−His−Asp−Ser(配列番号1)であり、これは、Aβ1−42のアミノ酸残基3〜8に相当し、Aβの残基17〜42内からの要素に依存する立体構造的エピトープを有するが、これは、構築された場合のみである。
ADDL調製。F12培地(Biosource, Camarillo, CA)中のADDLを、確立された方法(Lambertら(2001)、上記)により、Aβ1−42から調製した。要するに、Aβ1−42ペプチド(American Peptide Co., Sunnyvale, CAまたはCalifornia Peptide Research, Inc., Napa, CA)を、秤量し、HFIP(1,1,1,3,3,3−ヘキサフルオロ−2−プロパノール)の十分な量を保持することができるガラスバイアル中に配置して、10mg/mLのペプチド濃度を達成した。HFIPを、乾燥ペプチドに加え、バイアルを覆い、温和に回転させて混合し、ペプチド/HFIP溶液を、室温で少なくとも1時間貯蔵した。ペプチド溶液のアリコート(それぞれ50または100μL、0.5または1.0mg)を、一連の1.5mLの円錐形遠心管中に分配した。この管を、SPEEDVAC(登録商標)中に一晩配置して、HFIPを除去した。乾燥ペプチドフィルムを含有する管を覆い、乾燥剤を有する密閉した容器中で−70℃で貯蔵した。
20C2マウス抗体の可変ドメインをコードするcDNAを、クローン化し、ポリメラーゼ連鎖反応法(PCR)に従って、マウス定常領域の5’末端に、およびV領域の上流のマウスリーダー配列にハイブリダイズする特別に設計されたプライマーを用いて配列決定した。これにより、得られたマウス可変領域配列が、完全であり、正確であることが確実になった。要するに、mRNAを、マウスハイブリドーマ細胞系から、QIAGEN(登録商標)OLIGOTEX(登録商標)Direct mRNA Mini Kitを用いて抽出し、その後一本鎖cDNA合成キットを用いてcDNAに変換した。次に、cDNAを、PCR反応における鋳型として用いて、抗体可変領域配列を得た。
マウスハイブリドーマ細胞系20C2から得られたマウス抗体重鎖可変ドメインおよび軽鎖可変ドメイン核酸を、CDR移植方法を用いてヒト化した。当業者は、マウス抗体配列のヒト化は、この血清半減期およびFcエフェクター機能を改善し、これにより抗グロブリン応答を低減することにより、抗体の治療的効力を最大化することができることを、理解する。
親和性成熟を、Hu20C2抗体において実行した。ヒト化Hu20C2バージョンAおよびB可変重鎖のみ、軽鎖のみ、または重鎖バージョンAおよび軽鎖を一緒にコードする核酸分子を、Fabファージ提示ベクターpFab4中でクローン化した。核酸配列分析により、pFab4における配列および配向が確認された。pFab4中の注釈付きのHu20C2 Fab配列を、図4A〜4Cに示し、本明細書中で重鎖バージョンAについて配列番号116で、重鎖バージョンBについて配列番号117で、また軽鎖について配列番号118で定める。pFab4ベクターにおける重鎖バージョンAおよび軽鎖の一緒についてのヌクレオチド配列を、図4D〜4Eに示す。これらの構築を、当該分野において確立されたファージ提示Fabライブラリー法を用いて、Hu20C2成熟プログラムで用いた。
b20C2LC3−2対高分子量10%bADDL。
c20C2LC3−1+20C2LC3−2対高分子量10%bADDL。
*コロニーの合計数あたりのヒット。
IgG2m4抗体誘導体を製造して、Fcレセプター会合、C1q結合、不要な細胞毒性または免疫複合体生成を低減し、同時に典型的なヒト抗体の長い半減期および薬物動態特性を共に維持した。IgG2m4の基本的な抗体様式は、IgG2のものであり、これは、実験的モデルにおいて優れた半減期を有すると示されている(Zuckierら(1994)、Cancer Suppl. 73:794-799)。IgG4配列の選択的な導入により、IgG2の構造を改変して、C1q結合を解消し、一方典型的な低レベルのFcγR結合を維持した(CanfieldおよびMorrison (1991)、J. Exp. Med. 173:1483-1491)。これは、IgG2およびIgG4の配列が同一である交差点を用いることにより達成され、これにより、すべての人工的な突然変異配列よりもむしろ、天然のFc配列を含む抗体が得られた。最小のエフェクター関連活性を示すこのIgG2m4抗体を用いることの利点は、Wilcockら((2006) J. Neurosci. 26:5340-6)により開示されている脱グリコシル抗体に相当する。
aHougsら(2001)、Immunogenetics 52(3-4):242-8。
bWO 97/11971。
cMedgyesiら(2004)、Eur. J. Immunol. 34:1127-1135。
dTaoら(1991)、J. Exp. Med. 173:1025-1028。
eArmourら(1999)、Eur. J. Immunol. 29:2613。
fXuら(1994)、J. Biol. Chem. 269:3469-3474。
gCanfieldおよびMorrison (1991)、J. Exp. Med. 173:1483。
親和性成熟を行って、親和性を改善し、ADDLへの優先的な結合を改善した。ヒト化された抗体のADDL結合親和性を評価するために、BIACORE(登録商標)および滴定ELISAを、本明細書中に開示したように行った。要するに、ストレプトアビジンを塗布した96ウェルマイクロタイタープレート(Sigma, St. Louis, MO)に、10%ビオチン化ADDL抗原(1μM)を塗布した。500ng/mLで開始した、精製した抗体の一連の2倍希釈を、ADDL捕獲プレートに加え、プレートを、2時間25℃でインキュベートした。プレート洗浄機(Bio-Tek, Winooski, VA)を用いてPBS溶液で5回洗浄した後に、ポリクローナルヤギ抗ヒトカッパ軽鎖抗体(Biomeda, Foster City, CA)を、3%脱脂乳ブロッカーでの1/2000の希釈において加え、室温で1時間インキュベートした。次に、ウサギ抗ヤギIgG(H+L)HRP結合(Bethyl Laboratories, Inc., Montgomery, TX)検出抗体を、遮断溶液での1/2000の希釈において加え、室温で1時間インキュベートした。PBSで洗浄した後、HRP基質、3,3’,5’,5−テトラメチルベンジジン(使用可能な状態のTMB;Sigma, St. Louis, MO)を加え、反応を、10分後に0.5NのH2SO4で停止した。450nmの波長における吸光度を、プレートリーダー(モデルVICTOR V; Perkin Elmer, Boston, MA)において読み取り、データを、EXCEL(登録商標)ワークシートを用いて加工した。プレート間のアッセイ変動は、20%以内であると推定された。
ヒト化抗ADDL抗体をさらに、一次海馬ニューロンへのADDL結合を遮断するこれらの能力について、本明細書中に開示した方法を用いて評価した。Hu20C2A3抗体または対照としてのPBSを、種々のモル比でbADDLと混合し、低速ローテータ上で1時間37℃でインキュベートした。プレインキュベーションの後、抗体/bADDL調製物を、一次ニューロン培養物に加え、さらに1時間37℃でインキュベートした。インキュベーション期間の終了時に、bADDL/抗体混合物を除去し、プレートを、培地で6回洗浄した。次に、細胞を、4%パラホルムアルデヒド中で10分間室温で固定し、溶液を除去し、新鮮な固定液を加え、細胞を、さらに10分間固定した。
Hu20C2A3のタンパク質安定性の評価を、SEC−HPLC、蛍光熱溶融分析および粒径分析を用いて評価した。蛍光熱溶融分析により、FcおよびFabのアンフォールディング転移が、それぞれ約70℃および80℃において発生することが示され、これは、許容できる固有のタンパク質安定性と整合する(図10)。
従来技術により、モノクローナル抗Aβ抗体の全身への注射は、Aβの血漿レベルを急速に増大し得、一方脳Aβの測定可能な低下には、慢性投与が必要であることが、示されている。測定可能なAβでの種における受動的な免疫化の結果、脳と末梢分画との間のAβの平衡における変化による血漿Aβの上昇がもたらされることが、示唆されている。この「末梢のシンク」により、最終的に、脳Aβの低下がもたらされる。しかし、認知の改善は、脳Aβにおける顕著な変化の前の急激な抗体の投与に続いて動物において観察され、これは、脳Aβの変化が、これらの変化を既知の手法を用いて測定することができる時点の前に、ある形態で起こり得ることを示す。あるいはまた、血漿Aβの上昇が、抗体の投与の後の末梢Aβの安定化により説明され得る。
Claims (11)
- 1種または2種以上のAβ由来拡散性リガンドをAβ単量体と区別して認識することができる、単離された抗体またはその断片であって、軽鎖可変領域が、
Arg−Ser−Ser−Gln−Ser−Ile−Leu−His−Serのアミノ酸配列と、
Asn−Gly−Asn−Thr−Tyr−Leu−Gluのアミノ酸配列と、
Xaa1−Gln−Xaa2−Thr−Arg−Val−Pro−Leu−Thr(ここで、Xaa1はPheまたはLeuであり、Xaa2はAlaまたはThrである)、配列番号39、52、58、61、63、64、65、67、76、79、86、90および94からなる群から選択されるアミノ酸配列とを含み、
重鎖可変領域が、
Thr−Ser−Gly−Met−Gly−Val−Glyのアミノ酸配列と、
His−Ile−Trp−Trp−Asp−Asp−Asp−Lys−Ser−Tyr−Asn−Pro−Ser−Leu−Lys−Serのアミノ酸配列と、
配列番号3、8、99、142および150からなる群から選択されるアミノ酸配列とを含む、
前記単離された抗体またはその断片。 - 抗体の重鎖可変領域および軽鎖可変領域がそれぞれ、配列番号108および配列番号112で定めるアミノ酸配列を含む、請求項1に記載の単離された抗体。
- 抗体の重鎖および軽鎖がそれぞれ、配列番号138および配列番号140で定めるアミノ酸配列を含む、請求項1に記載の単離された抗体。
- 請求項1〜3のいずれか一項に記載の単離された抗体またはこの断片を、薬学的に許容し得る担体との混合物において含む、医薬組成物。
- Aβ由来拡散性リガンドのニューロンへの結合を防止するための、請求項4に記載の医薬組成物。
- Aβ由来拡散性リガンドの構築を阻害するための、請求項4に記載の医薬組成物。
- タウタンパク質のSer202/Thr205におけるリン酸化を遮断するための、請求項4に記載の医薬組成物。
- アルツハイマー病を予防的に、または治療的に処置するための、請求項4に記載の医薬組成物。
- Aβ由来拡散性リガンドのニューロンへの結合を防止する治療剤を同定するための方法であって、薬剤の存在下でニューロンをAβ由来拡散性リガンドと接触させ、請求項1〜3のいずれか一項に記載の抗体を用いて、前記薬剤の存在下でのAβ由来拡散性リガンドの前記ニューロンへの結合を決定することを含む、前記方法。
- 試料中のAβ由来拡散性リガンドを検出するための方法であって、試料を請求項1〜3のいずれか一項に記載の抗体と接触させて、Aβ由来拡散性リガンドを検出するようにすることを含む、前記方法。
- Aβ由来拡散性リガンドを検出するためのキットであって、請求項1〜3のいずれか一項に記載の単離された抗体またはその断片を含む、前記キット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| USPCT/US2005/38125 | 2005-10-21 | ||
| US2005381125 | 2005-10-21 | ||
| PCT/US2006/040508 WO2007050359A2 (en) | 2005-10-21 | 2006-10-17 | Anti-addl monoclonal antibody and use thereof |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| JP2009519895A JP2009519895A (ja) | 2009-05-21 |
| JP2009519895A6 JP2009519895A6 (ja) | 2009-12-24 |
| JP2009519895A5 JP2009519895A5 (ja) | 2012-04-05 |
| JP5289963B2 true JP5289963B2 (ja) | 2013-09-11 |
Family
ID=39671607
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008536730A Active JP5289963B2 (ja) | 2005-10-21 | 2006-10-17 | 抗addlモノクローナル抗体およびその使用 |
Country Status (8)
| Country | Link |
|---|---|
| EP (1) | EP1940466B1 (ja) |
| JP (1) | JP5289963B2 (ja) |
| CN (1) | CN101291692A (ja) |
| AU (1) | AU2006306553B9 (ja) |
| CA (1) | CA2626783A1 (ja) |
| NO (1) | NO20082288L (ja) |
| RU (1) | RU2008120027A (ja) |
| WO (1) | WO2007050359A2 (ja) |
Families Citing this family (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2001268005A1 (en) | 2000-07-07 | 2002-01-21 | Lars Lannfelt | Prevention and treatment of alzheimer's disease |
| DE10303974A1 (de) | 2003-01-31 | 2004-08-05 | Abbott Gmbh & Co. Kg | Amyloid-β(1-42)-Oligomere, Verfahren zu deren Herstellung und deren Verwendung |
| SE0401601D0 (sv) | 2004-06-21 | 2004-06-21 | Bioarctic Neuroscience Ab | Protofibril specific antibodies and uses thereof |
| KR20180058863A (ko) | 2005-11-30 | 2018-06-01 | 애브비 인코포레이티드 | 아밀로이드 베타 단백질에 대한 모노클로날 항체 및 이의 용도 |
| PT1954718E (pt) | 2005-11-30 | 2014-12-16 | Abbvie Inc | Anticorpos anti-globulómeros aβ, suas porções de ligação ao antigénio, correspondentes hibridomas, ácidos nucleicos, vectores, células hospedeiras, métodos de produção dos ditos anticorpos, composições compreendendo os ditos anticorpos, usos dos ditos anticorpos e métodos para uso dos ditos anticorpos |
| PL2004688T5 (pl) | 2006-03-23 | 2014-09-30 | Bioarctic Neuroscience Ab | Ulepszone przeciwciała wobec protofibryli oraz ich zastosowania |
| US8455626B2 (en) | 2006-11-30 | 2013-06-04 | Abbott Laboratories | Aβ conformer selective anti-aβ globulomer monoclonal antibodies |
| US20100311767A1 (en) | 2007-02-27 | 2010-12-09 | Abbott Gmbh & Co. Kg | Method for the treatment of amyloidoses |
| US7931899B2 (en) | 2007-05-14 | 2011-04-26 | Medtronic, Inc | Humanized anti-amyloid beta antibodies |
| US8323654B2 (en) | 2007-05-14 | 2012-12-04 | Medtronic, Inc. | Anti-amyloid beta antibodies conjugated to sialic acid-containing molecules |
| US8613923B2 (en) | 2007-06-12 | 2013-12-24 | Ac Immune S.A. | Monoclonal antibody |
| NZ599497A (en) * | 2007-06-12 | 2013-11-29 | Ac Immune Sa | Humanized antibodies to amyloid beta |
| US8048420B2 (en) | 2007-06-12 | 2011-11-01 | Ac Immune S.A. | Monoclonal antibody |
| EP2586795B1 (en) | 2007-10-05 | 2018-05-16 | Genentech, Inc. | Use of anti-amyloid beta antibody in ocular diseases |
| WO2009070648A2 (en) * | 2007-11-27 | 2009-06-04 | Medtronic, Inc. | Humanized anti-amyloid beta antibodies |
| CA2707309A1 (en) | 2007-12-18 | 2009-06-25 | Acumen Pharmaceuticals, Inc. | Novel addl receptor polypeptides, polynucleotides and host cells for recombinant production |
| AU2009282234A1 (en) * | 2008-08-14 | 2010-02-18 | Merck Sharp & Dohme Corp. | Methods for purifying antibodies using protein a affinity chromatography |
| DK2510359T3 (en) | 2009-12-11 | 2015-12-07 | Araclón Biotech S L | METHODS AND REAGENTS FOR IMPROVED DETECTION OF AMYLOID-BETA PEPTIDES |
| MX336196B (es) | 2010-04-15 | 2016-01-11 | Abbvie Inc | Proteinas de union a amiloide beta. |
| US9320793B2 (en) | 2010-07-14 | 2016-04-26 | Acumen Pharmaceuticals, Inc. | Method for treating a disease associated with soluble, oligomeric species of amyloid beta 1-42 |
| BR112013000796B1 (pt) | 2010-07-14 | 2021-08-31 | Merck Sharp & Dohme Corp | Anticorpo isolado ou um fragmento de ligação ao antígeno, composição farmacêutica, métodos para inibir a montagem de ligantes difusíveis derivados de ß-amiloide, para inibir a fosforilação de proteína tau em ser202/thr205, para identificar um suposto agente terapêutico, para detectar ligantes difusíveis derivados de ß-amiloide e para diagnosticar uma doença associada aos ligantes difusíveis derivados de ß-amiloide, e, kit para detectar ligantes difusíveis derivados de ß-amiloide |
| US9176151B2 (en) | 2010-07-14 | 2015-11-03 | Acumen Pharmaceuticals, Inc. | Antibodies, kit and method for detecting amyloid beta oligomers |
| MY164579A (en) | 2010-07-30 | 2018-01-15 | Ac Immune Sa | Safe and functional humanized antibodies |
| EP3533803B1 (en) | 2010-08-14 | 2021-10-27 | AbbVie Inc. | Anti-amyloid-beta antibodies |
| EP2511296A1 (en) | 2011-04-12 | 2012-10-17 | Araclón Biotech, S. L. | Antibody, kit and method for determination of amyloid peptides |
| US20140302532A1 (en) | 2011-04-12 | 2014-10-09 | Quanterix Corporation | Methods of determining a treatment protocol for and/or a prognosis of a patient's recovery from a brain injury |
| US20130052670A1 (en) * | 2011-07-13 | 2013-02-28 | Merck | Method for detection of amyloid beta oligomers in a fluid sample and uses thereof |
| JP6231263B2 (ja) * | 2012-07-17 | 2017-11-15 | 株式会社島津製作所 | アフィニティ支持体及びそれを用いた物質の捕捉方法 |
| SMT202100263T1 (it) | 2014-07-10 | 2021-07-12 | Eisai R&D Man Co Ltd | Anticorpi leganti protofibrille a-beta migliorati |
| US10093731B2 (en) | 2017-02-24 | 2018-10-09 | Kindred Biosciences, Inc. | Anti-IL31 antibodies for veterinary use |
| US12352719B2 (en) | 2019-09-20 | 2025-07-08 | KYCERA AVX Components Corporation | Somatic cell-based electrical biosensor |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994017197A1 (fr) * | 1993-01-25 | 1994-08-04 | Takeda Chemical Industries, Ltd. | ANTICORPS DIRIGE CONTRE LE β-AMYLOIDE OU UN DERIVE DE CE DERNIER ET SON UTILISATION |
| US5786180A (en) * | 1995-02-14 | 1998-07-28 | Bayer Corporation | Monoclonal antibody 369.2B specific for β A4 peptide |
| US20030068316A1 (en) * | 1997-02-05 | 2003-04-10 | Klein William L. | Anti-ADDL antibodies and uses thereof |
| CN1177616C (zh) * | 1997-04-09 | 2004-12-01 | 曼德塞特生物制药公司 | 特异于β-淀粉状蛋白末端的重组抗体,编码它们的DNA及其使用方法 |
| CA2501091A1 (en) * | 2002-10-01 | 2004-04-15 | Northwestern University | Amyloid beta-derived diffusible ligands (addls), addl-surrogates, addl-binding molecules, and uses thereof |
| TWI306458B (en) * | 2003-05-30 | 2009-02-21 | Elan Pharma Int Ltd | Humanized antibodies that recognize beta amyloid peptide |
| NZ554725A (en) * | 2004-10-25 | 2009-10-30 | Merck & Co Inc | Anti-ADDL antibodies and uses thereof |
-
2006
- 2006-10-17 JP JP2008536730A patent/JP5289963B2/ja active Active
- 2006-10-17 RU RU2008120027/13A patent/RU2008120027A/ru not_active Application Discontinuation
- 2006-10-17 EP EP06836346A patent/EP1940466B1/en active Active
- 2006-10-17 AU AU2006306553A patent/AU2006306553B9/en not_active Expired - Fee Related
- 2006-10-17 CN CNA2006800392637A patent/CN101291692A/zh active Pending
- 2006-10-17 CA CA002626783A patent/CA2626783A1/en not_active Abandoned
- 2006-10-17 WO PCT/US2006/040508 patent/WO2007050359A2/en not_active Ceased
-
2008
- 2008-05-19 NO NO20082288A patent/NO20082288L/no not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| AU2006306553B2 (en) | 2011-08-25 |
| WO2007050359A8 (en) | 2008-05-08 |
| AU2006306553A1 (en) | 2007-05-03 |
| RU2008120027A (ru) | 2009-11-27 |
| CN101291692A (zh) | 2008-10-22 |
| EP1940466A4 (en) | 2010-04-07 |
| EP1940466B1 (en) | 2012-11-28 |
| WO2007050359A3 (en) | 2007-06-21 |
| EP1940466A2 (en) | 2008-07-09 |
| NO20082288L (no) | 2008-05-19 |
| AU2006306553B9 (en) | 2011-09-29 |
| CA2626783A1 (en) | 2007-05-03 |
| WO2007050359A2 (en) | 2007-05-03 |
| JP2009519895A (ja) | 2009-05-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5289963B2 (ja) | 抗addlモノクローナル抗体およびその使用 | |
| US8105593B2 (en) | Anti-ADDL monoclonal antibody and use thereof | |
| JP5634975B2 (ja) | 抗addl抗体およびこの使用 | |
| JP2009519895A6 (ja) | 抗addlモノクローナル抗体およびその使用 | |
| US9309309B2 (en) | Anti-ADDL monoclonal antibody and uses thereof | |
| JP6731727B2 (ja) | アミロイドベータ1−42の可溶性オリゴマー種に関連する疾患を治療するための方法 | |
| CA2590337A1 (en) | Humanized amyloid beta antibodies for use in improving cognition | |
| CN101137394A (zh) | 抗addl抗体及其应用 | |
| US8420093B2 (en) | Anti-ADDL monoclonal antibody and use thereof | |
| MX2007004909A (en) | Anti-addl antibodies and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091015 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091015 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120207 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120313 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120613 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120620 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120713 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121030 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130130 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20130223 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130507 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130605 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5289963 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |