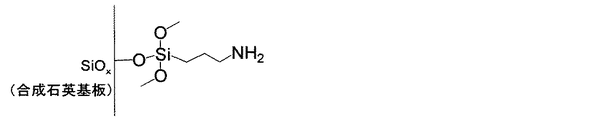JP4849552B2 - 蛍光誘導体物質の固体基板表面への固定化方法 - Google Patents
蛍光誘導体物質の固体基板表面への固定化方法 Download PDFInfo
- Publication number
- JP4849552B2 JP4849552B2 JP2007006366A JP2007006366A JP4849552B2 JP 4849552 B2 JP4849552 B2 JP 4849552B2 JP 2007006366 A JP2007006366 A JP 2007006366A JP 2007006366 A JP2007006366 A JP 2007006366A JP 4849552 B2 JP4849552 B2 JP 4849552B2
- Authority
- JP
- Japan
- Prior art keywords
- substance
- chemically bonded
- solid substrate
- fluorescent
- chemically
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 CC(C*1(CIIC)C2C1)*2=C Chemical compound CC(C*1(CIIC)C2C1)*2=C 0.000 description 1
- WGQKYBSKWIADBV-UHFFFAOYSA-N NCc1ccccc1 Chemical compound NCc1ccccc1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 description 1
- DLRBIDBYCGAORF-UHFFFAOYSA-N O=C(CCCCCN(C(CC1)=O)C1=O)ON(C(CC1)=O)C1=O Chemical compound O=C(CCCCCN(C(CC1)=O)C1=O)ON(C(CC1)=O)C1=O DLRBIDBYCGAORF-UHFFFAOYSA-N 0.000 description 1
- OMWQUXGVXQELIX-UHFFFAOYSA-N S=C=Nc(cc1)ccc1N=C=S Chemical compound S=C=Nc(cc1)ccc1N=C=S OMWQUXGVXQELIX-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
Description
しかしながら、従来のこれらの方法は、蛍光誘導体化物質と検体中の特定物質との反応を行った後、液体クロマトグラフィーや電気泳動を用いるため、検出に時間が掛かるばかりでなく、一度に測定できる数に限りがあるという課題がある。
しかしながら、これらの方法では、特定物質を検出するには、別途、検体を蛍光物質で標識する等の工程を必要とするものであり、センサーを用いて直ちに検出することはできないという問題がある。
"Fluorescentproducts of the reaction for the determination of catecholamines with1,2-diphenylethylenediamine", H. Nohta et al., Anal. Chem. 1992, 267, 137-139. "Aromaticglycinonitriles and methylamines as pre-column fluorescence derivatizationreagents for catecholamines", H. Nohta et al., Anal. Chim. Acta 1997, 344,233-240. "Simultaneousdetermination of urinary catecholamines and 5-hidroxyindoleamines byhigh-performance liquid chromatography with fluorescence detection", M.Yamaguchi et al., Analyst 1998, 123, 307-311.
(1)検体中の特定物質と縮合反応して検出波長の蛍光を有する物質を形成する蛍光誘導体化物質を、固体基板表面と接続分子との化学結合を介して接続分子との化学結合(但し、疎水的相互作用による結合を除く)により、固定化することを特徴とする蛍光体誘導体化物質の固体基板表面への固定化方法。
(2)前記接続分子は、固体基板表面と化学結合が可能であり且つ前記蛍光誘導体化物質と化学結合ができる、あるいは前記固体基板表面と化学結合が可能であり且つ他の接続分子と化学結合ができる、あるいは他の接続分子と化学結合が可能であり且つ前記蛍光誘導体化物質と化学結合ができる、あるいは、他の接続分子と化学結合が可能であり且つ別の接続分子と化学結合ができることを特徴とする上記(1)の固定化方法。
(3)前記特定物質は、カテコールアミン類、又はヒドロキシインドール類であって、酸化剤あるいは酸素の存在下で前記蛍光誘導体化物質と化学結合することを特徴とする上記(1)又は(2)の固定化方法。
(4)前記蛍光誘導体化物質は、ベンジルアミン誘導体、フェニルグリシノニトリル誘導体、又はジフェニルエチレンジアミン誘導体のいずれかであり、酸化剤あるいは酸素の存在下で前記特定物質と化学結合して蛍光体を形成することを特徴とする上記(1)〜(3)のいずれかの固定化方法。
(5)前記固体基板は、ガラス又はプラスチック又は金属又は金属酸化物又は珪素を主成分として形成されていることを特徴とする上記(1)〜(4)のいずれかに記載の固定化方法。
(6)前記特定物質が固体基板表面上に固定化された前記蛍光誘導体化物質と化学結合する前は検出波長において蛍光性を示さず、化学結合後に蛍光性を示すことを特徴とする上記(1)〜(5)のいずれかに記載の固定化方法。
基板の形状は、とくに限定されるものではないが、カード状又はディスク状に形成されているのが好ましい。
固体基板を形成するための材料は、蛍光検出型ケミカルバイオセンサの支持体として機能することができれば、とくに限定されるものではなく、例えば、ガラス、石英、セラミックス、プラスチックス、金属、金属酸化物又は珪素を主成分とするものなどによって形成することができる。プラスチックスとしては、ポリカーボネート樹脂、オレフィン樹脂、アクリル樹脂、エポキシ樹脂、ポリスチレン樹脂、ポリエチレン樹脂、ポリプロピレン樹脂、シリコン樹脂、フッ素系樹脂、ABS樹脂、ウレタン樹脂、フェノール樹脂、ポリメチルメタクリレート樹脂、ポリイソブチルメタクリレート樹脂、ポリイミド樹脂などが挙げられる。
本発明において用いられる接続分子は、(I)固体基板表面と化学結合が可能であり且つ前記蛍光誘導体化物質と化学結合ができるもの、あるいは(II)前記固体基板表面と化学結合が可能であり且つ他の接続分子と化学結合ができるもの、あるいは(III)他の接続分子と化学結合が可能であり且つ前記蛍光誘導体化物質と化学結合ができるもの、あるいは、(IV)他の接続分子と化学結合が可能であり且つ別の接続分子と化学結合ができるもの、から選ばれる。
以下に、これらの例を記載する。
「ジ(N−スクシンイミジル)カーボネート(DSC)」
「4−メルカプト安息香酸」
「3−アミノプロピルトリエトキシシラン(APS)」
「N−スクシンイミジル−4−マレイミドブチラート」
「1,4−フェニレンヂイソチオシアネート(PDIC)」
「上記(化6)で示される4−メルカプト安息香酸」
一方の末端(メルカプト基)が他の接続分子のマレイミド基と化学結合し、他方の末端(カルボキシル基)が蛍光誘導体化物質のベンジルアミン誘導体であるXDAのアミノ基と化学結合する。
「テレフタル酸」
「1,4−ジアミノブタン」
「上記(化12)で示されるテレフタル酸」又は「上記(化13)で示されるアジピン酸」
「上記(化11)で示されるPDIC」
本発明の方法により得られた、蛍光誘導体化物質を固定化した固体基板上に、検体液を流し、該検体中の特定物質と前記蛍光誘導体化物質との縮合反応により検出波長の蛍光を有する物質を形成させ、その蛍光を検出することにより、検体中の特定物質の有無を検出することができる。
前記検体液は、検出すべき特定物質を充分に溶解しうる溶媒を用いて溶液とするとともに、緩衝液を用いてpHが8前後となるようにして調製される。こうして調製された検体液を前記固体基板上に流した後、しばらく静置して該検体中の特定物質と前記蛍光誘導体化物質との縮合反応を充分に行わせ、その後蒸留水でセンサー表面をリンスし、乾燥させる。
例えば、蛍光誘導体化物質としてベンジルアミン誘導体としてp−キシレリンジアミン(pXDA)を用いてエピネフェリンを検出する場合には、励起光として375nmの光を照射し、470nm付近にピークを有する蛍光の有無を検出する。
また、前記蛍光の検出は、透過光、反射光、迷光などの影響がもっとも少ないことから、該入射光に対して直角方向から行われることが好ましい。
さらに、本発明の方法により蛍光誘導体化物質がその表面に固定化された固体基板を用いた場合、検体中の前記特定物質と前記蛍光誘導体化物質との縮合反応により形成される物質の蛍光スペクトルから、検体中に存在する特定物質の種類を特定することができる。
(実施例1)
以下のようにして、合成石英基板表面に、蛍光誘導体化物質を固定化した。図1ないし図3は、その手順を模式的に示すものである。
水、エタノール等で洗浄した合成石英基板を真空乾燥後、オゾン照射処理をすることによって、表面を親水化し、次に、接続分子である3−アミノプロピルトリエトキシシラン(APS)(前記(化7))10mMを含むエタノール溶液中に、上記合成石英基板を50℃で15時間浸漬した。その後基板を取り出して、エタノールで基板表面をリンスし、乾燥後、100℃1時間放置することによってAPSを合成石英基板表面に化学結合させた。(図1)。
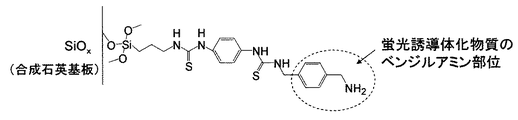
さらに蛍光誘導体化物質ベンジルアミン誘導体であるp−キシリレンジアミン(XDA)(前記(化3))50mMを含む、50mMほう酸バッファー溶液(pH8.5)中に室温で2時間浸漬し、蛍光誘導体化物質ベンジルアミンの部位が末端に出るように化学結合させた(図3)。
この結果から、エピネフェリンは図5に模式的に示すように固体基板表面上に化学的に固定化されたベンジルアミン部位によって蛍光誘導体化されたものと推測できる。
以下のようにして、合成石英基板表面に、蛍光誘導体化物質を固定化した。図6及び図7は、その手順を模式的に示すものである。
水、エタノール等で洗浄した合成石英基板を真空乾燥後、オゾン照射処理をすることによって、表面を親水化し、次に、接続分子であるジ(N−スクシンイミジル)カーボネート(DSC)(前記(化5)参照)5mMを含むアセトン溶液15mlを調製し、ここに1.25mlのトリエチルアミンを含むピリジン溶液15mlを混合した。この混合溶液中に親水化した合成石英基板を室温で15時間浸漬することによってDSCを合成石英基板表面に化学結合させた(図6)。
次に、エタノールで基板表面をリンスし乾燥後、蛍光誘導体化物質ベンジルアミン誘導体であるXDA1mMを含む、1/15Mリン酸緩衝液(pH7.4)を30ml調製し、この中に室温で2時間浸漬し、ベンジルアミン部位が末端に出るように化学結合させた(図7)。
以下のようにして、合成石英基板表面に、蛍光誘導体化物質を固定化した。図1及び図8は、その手順を模式的に示すものである。
水、エタノール等で洗浄した合成石英基板を真空乾燥後、オゾン照射処理をすることによって、表面を親水化し、次に、接続分子である3−アミノプロピルトリエトキシシラン(APS)10mMを含むエタノール溶液中に、合成石英基板を50℃で15時間浸漬した。取り出して、エタノールで基板表面をリンスし乾燥後、100℃1時間放置することによってAPSを合成石英基板表面に化学結合させた(図1)。
次に、4−アミノメチル安息香酸(前記(化4))500μMを含むリン酸緩衝液(pH7.4)10mlと500μMの1−エチルー3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC)を含むリン酸緩衝液(pH7.4)10mlを混合した溶液を調製し、APSが表面に結合した基板を室温で1時間浸漬することによって末端にベンジルアミン部位を化学的に固定化させた(図8)。
Claims (6)
- 検体中の特定物質と縮合反応して検出波長の蛍光を有する物質を形成する蛍光誘導体化物質を、固体基板表面と接続分子との化学結合を介して接続分子との化学結合(但し、疎水的相互作用による結合を除く)により、固定化することを特徴とする蛍光体誘導体化物質の固体基板表面への固定化方法。
- 前記接続分子は、固体基板表面と化学結合が可能であり且つ前記蛍光誘導体化物質と化学結合ができる、あるいは前記固体基板表面と化学結合が可能であり且つ他の接続分子と化学結合ができる、あるいは他の接続分子と化学結合が可能であり且つ前記蛍光誘導体化物質と化学結合ができる、あるいは、他の接続分子と化学結合が可能であり且つ別の接続分子と化学結合ができることを特徴とする請求項1に記載の固定化方法。
- 前記特定物質は、カテコールアミン類、又はヒドロキシインドール類であって、酸化剤あるいは酸素の存在下で前記蛍光誘導体化物質と化学結合することを特徴とする請求項1又は2に記載の固定化方法。
- 前記蛍光誘導体化物質は、ベンジルアミン誘導体、フェニルグリシノニトリル誘導体、又はジフェニルエチレンジアミン誘導体のいずれかであり、酸化剤あるいは酸素の存在下で前記特定物質と化学結合して蛍光体を形成することを特徴とする請求項1〜3のいずれかに記載の固定化方法。
- 前記固体基板は、ガラス又はプラスチック又は金属又は金属酸化物又は珪素を主成分として形成されていることを特徴とする請求項1〜4のいずれかに記載の固定化方法。
- 前記特定物質が固体基板表面上に固定化された前記蛍光誘導体化物質と化学結合する前は検出波長において蛍光性を示さず、化学結合後に蛍光性を示すことを特徴とする請求項1〜5のいずれかに記載の固定化方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007006366A JP4849552B2 (ja) | 2007-01-15 | 2007-01-15 | 蛍光誘導体物質の固体基板表面への固定化方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007006366A JP4849552B2 (ja) | 2007-01-15 | 2007-01-15 | 蛍光誘導体物質の固体基板表面への固定化方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008170399A JP2008170399A (ja) | 2008-07-24 |
| JP4849552B2 true JP4849552B2 (ja) | 2012-01-11 |
Family
ID=39698619
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007006366A Expired - Fee Related JP4849552B2 (ja) | 2007-01-15 | 2007-01-15 | 蛍光誘導体物質の固体基板表面への固定化方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4849552B2 (ja) |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01265158A (ja) * | 1988-04-18 | 1989-10-23 | Hitachi Ltd | カテコールアミン類の分析方法及び装置 |
| JP3216203B2 (ja) * | 1992-02-07 | 2001-10-09 | 東ソー株式会社 | カテコールアミンの測定試薬及びそれを用いるカテコールアミンの定量方法 |
| JPH06258311A (ja) * | 1993-03-09 | 1994-09-16 | Hitachi Ltd | 1,2−ジフェニルエチレンジアミンとカテコールアミン類との反応媒体 |
| JP3069292B2 (ja) * | 1996-06-13 | 2000-07-24 | 株式会社分子バイオホトニクス研究所 | カテコール化合物及びバニリル化合物の蛍光検出用固相化試薬および検出方法 |
-
2007
- 2007-01-15 JP JP2007006366A patent/JP4849552B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2008170399A (ja) | 2008-07-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Fu et al. | Recent advances in biosensors for nucleic acid and exosome detection | |
| JP4676983B2 (ja) | テラヘルツ放射を用いて生体分子結合を検出するための方法及び系 | |
| JP5295149B2 (ja) | 生体物質分析方法並びにそれに用いられる生体物質分析セル、チップおよび装置 | |
| TWI668429B (zh) | 含有石墨烯之生物感測晶片以及應用該生物感測晶片之檢測裝置 | |
| Drozd et al. | Recent advancements in receptor layer engineering for applications in SPR-based immunodiagnostics | |
| KR20090083685A (ko) | 표면증강 라만분광을 이용한 시료 내 특정물질의 분석방법및 분석장치 | |
| Gupta et al. | Epitope imprinting of iron binding protein of Neisseria meningitidis bacteria through multiple monomers imprinting approach | |
| JP2023175818A (ja) | 弾性表面波センサー用の生物活性コーティング | |
| Liu et al. | A Sensitive Microchip‐Based Immunosensor for Electrochemical Detection of Low‐Level Biomarker S100B | |
| Zhang et al. | “Click” chemistry‐based surface modification of poly (dimethylsiloxane) for protein separation in a microfluidic chip | |
| JP2013253972A (ja) | 関心ある標的の検出のためのセンサー | |
| Qiu et al. | Aptamer-based detection of melamine in milk using an evanescent wave fiber sensor | |
| Trumpie et al. | Lateral flow assays | |
| CN102037358B (zh) | 用标准计算机光学驱动器评估基于盘的生物测定的结果的方法 | |
| Dou et al. | Voltammetric immunoassay for the detection of protein biomarkers | |
| Mastichiadis et al. | Capillary-based immunoassays, immunosensors and DNA sensors–steps towards integration and multi-analysis | |
| JP4972295B2 (ja) | 免疫分析方法及びバイオチップ | |
| JP4849552B2 (ja) | 蛍光誘導体物質の固体基板表面への固定化方法 | |
| Mustafaoglu et al. | Site‐specific fab fragment biotinylation at the conserved nucleotide binding site for enhanced ebola detection | |
| CN105137064B (zh) | 一种小分子有机物修饰生物传感元件的方法 | |
| Guliy et al. | Biosensors for virus detection | |
| Chen et al. | Osmotic processor for enabling sensitive and rapid biomarker detection via lateral flow assays | |
| JP2006030155A (ja) | 分光法を用いたプレートアッセイ | |
| Kim et al. | Sensitive “capillary elisa” via vapor-phase surface modification | |
| JP5004076B2 (ja) | 蛍光検出型ケミカルバイオセンサー及びそれを用いた検体中の特定物質の検出方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090227 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20101217 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101221 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110221 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110712 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110912 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20111011 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20111013 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141028 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141028 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |