JP4820192B2 - 急性冠症候群でのadamts13の測定と利用 - Google Patents
急性冠症候群でのadamts13の測定と利用 Download PDFInfo
- Publication number
- JP4820192B2 JP4820192B2 JP2006075498A JP2006075498A JP4820192B2 JP 4820192 B2 JP4820192 B2 JP 4820192B2 JP 2006075498 A JP2006075498 A JP 2006075498A JP 2006075498 A JP2006075498 A JP 2006075498A JP 4820192 B2 JP4820192 B2 JP 4820192B2
- Authority
- JP
- Japan
- Prior art keywords
- adamts13
- amount
- vwf
- patients
- myocardial infarction
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Description
[1] 急性冠症候群(ACS)患者から採取した被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定することを含む、急性冠症候群患者の病態を検出する方法。
[2] VWFとADAMTS13量または活性の比率を測定する[1]の急性冠症候群患者の病態を検出する方法。
[3] 病態の検出が、急性冠症候群の重篤度の判定または予後の予測である[1]または[2]に記載の急性冠症候群患者の病態を検出する方法。
[4] 病態の検出が、急性冠症候群患者にMACEが起こるリスクの評価である[1]〜[3]のいずれかの急性冠症候群患者の病態を検出する方法。
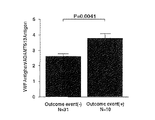
[5] ADAMTS13量または活性に対するVWFの比率が有意に高い場合またはあらかじめ定めたカットオフ値よりも高い場合に、急性冠症候群患者にMACEが起こるリスクが高いと評価し得る[1]〜[4]のいずれかの急性冠症候群患者の病態を検出する方法。
[6] 急性冠症候群(ACS)患者から経時的に被検試料を採取し、各被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定し、経時的な変化をモニターすることを含む[1]〜[5]のいずれかの急性冠症候群患者の病態を検出する方法。
[7] 急性冠症候群発症または診断後20〜30時間後に採取した被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定することを含む[1]〜[6]のいずれかの急性冠症候群患者の病態を検出する方法。
[8] 急性冠症候群(ACS)患者から採取した被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定することを含む急性冠症候群患者にフォンヴィレブランド因子分解酵素の補充を施す必要性を判定する方法。
[9] VWFとADAMTS13量または活性の比率を測定する[8]の急性冠症候群患者にフォンヴィレブランド因子分解酵素の補充を施す必要性を判定する方法。
[10] ADAMTS13量または活性に対するVWFの比率が有意に高い場合またはあらかじめ定めたカットオフ値よりも高い場合に、急性冠症候群患者にフォンヴィレブランド因子分解酵素の補充を施す必要性が高いと評価し得る、[8]または[9]の急性冠症候群患者にフォンヴィレブランド因子分解酵素の補充を施す必要性を判定する方法。
[11] 急性冠症候群(ACS)患者から経時的に被検試料を採取し、各被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定し、経時的な変化をモニターすることを含む[8]〜[10]のいずれかの急性冠症候群患者にフォンヴィレブランド因子分解酵素の補充を施す必要性を判定する方法。
[12] 急性冠症候群発症または診断後20〜30時間後に採取した被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定することを含む[8]〜[11]のいずれかの急性冠症候群患者にフォンヴィレブランド因子分解酵素の補充を施す必要性を判定する方法。
[13] 急性冠症候群(ACS)患者から経時的に被検試料を採取し、各被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定し、経時的な変化をモニターすることを含む、急性冠症候群患者の処置の経過をモニターする方法。
[14] VWF検出用試薬およびADAMTS13検出用試薬を含む急性冠症候群患者の病態検出用キット。
[15] VWF検出用試薬がVWF量測定用試薬でありADAMTS13検出用試薬がADAMTS13量またはADAMTS13活性測定用試薬である[14]の急性冠症候群患者の病態検出用キット。
[16] 病態の検出が、急性冠症候群の重篤度の判定または予後の予測である[14]または[15]の急性冠症候群患者の急性冠症候群患者の病態検出用キット。
[17] 病態の検出が、急性冠症候群患者にMACEが起こるリスクの評価である[14]〜[16]のいずれかの急性冠症候群患者の病態検出用キット。
[18] VWFおよびADAMTS13からなる急性冠症候群病態検出用マーカー。
[19] VWFおよびADAMTS13の急性冠症候群病態検出用マーカーとしての使用。
さらに、本発明は以下の通りである。
[20] 急性冠症候群患者において、フォンヴィレブランド因子分解酵素(以下ADAMTS13と称することがある)の量あるいは活性及びフォンヴィレブランド因子(以下VWFと称することがある)の量を分析することを特徴とする、前記急性冠症候群(以下ACSと称することがある)患者における病態の検出方法。
[21] 病態の検出が、重篤度の検出または重篤度の予測ならびにフォンヴィレブランド因子分解酵素の補充の指標となる、[20]の方法。
[22] 患者から得られた複数の試験サンプルをフォンヴィレブランド因子切断酵素量ならびにフォンヴィレブランド因子量について分析および比較することを含み、ここで、前記試験サンプルが同一の患者から異なる時間に得られたものである、患者の処置の経過をモニターする方法。
[23] 患者から得られたサンプル中のフォンヴィレブランド因子切断酵素量ならびにフォンヴィレブランド因子量が前記急性冠状動脈症候群の不利な結果(以下MACEと称することがある)に対する疾病素質と関係するかどうかを決定することにより、前記患者の予後ならびにフォンヴィレブランド因子切断酵素量を調節することによる治療方法と関連づけること、を含む、急性冠状動脈症候群と診断された患者の予後を決定する方法ならびにADAMTS13の補充療法による治療法。
[24] [23]の予後判定を急性冠症候群発症後ないし診断後24時間後において行う方法ならびにADAMTS13の補充療法による治療法。
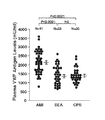
AMI患者41名及びSEA患者33名、CPS患者30名より、3.8%クエン酸加血漿を採取した。解析には表1に示すように喫煙歴(Smokers)以外は患者背景の揃った被験者群を用いた。
患者血漿の採取はAMI発症時、24時間、72時間、1週間後および慢性期と経時的に実施例1と同様クエン酸により採血を行い、VWF量、ADAMTS13量およびADAMTS13酵素活性の測定を実施例1と同様の方法で行った。
Claims (9)
- 急性心筋梗塞(AMI)患者から採取した被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定することを含む、急性心筋梗塞患者にMACEが起こるリスクを検出する方法。
- ADAMTS13量または活性に対するVWFの比率が有意に高い場合またはあらかじめ定めたカットオフ値よりも高い場合に、急性心筋梗塞患者にMACEが起こるリスクが高いと評価し得る請求項1記載の急性心筋梗塞患者の病態を検出する方法。
- 急性心筋梗塞(AMI)患者から経時的に被検試料を採取し、各被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定し、経時的な変化をモニターすることを含む請求項1または2に記載の急性心筋梗塞患者の病態を検出する方法。
- 急性心筋梗塞発症または診断後20〜30時間後に採取した被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定することを含む請求項1〜3のいずれか1項に記載の急性心筋梗塞患者の病態を検出する方法。
- 急性心筋梗塞(AMI)患者から経時的に被検試料を採取し、各被検試料中のフォンヴィレブランド因子分解酵素(ADAMTS13)の量もしくは活性ならびにフォンヴィレブランド因子(VWF)の量を測定し、経時的な変化をモニターすることを含む、急性心筋梗塞患者にMACEが起こるリスクをモニターする方法。
- VWF検出用試薬およびADAMTS13検出用試薬を含む急性心筋梗塞患者にMACEが起こるリスクを検出するためのキット。
- VWF検出用試薬がVWF量測定用試薬でありADAMTS13検出用試薬がADAMTS13量またはADAMTS13活性測定用試薬である請求項6記載のキット。
- VWFおよびADAMTS13からなる急性心筋梗塞患者におけるMACEが起こるリスクを検出するためのマーカー。
- VWFおよびADAMTS13の急性心筋梗塞患者におけるMACEが起こるリスクを検出するためのマーカーとしての使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006075498A JP4820192B2 (ja) | 2006-03-17 | 2006-03-17 | 急性冠症候群でのadamts13の測定と利用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006075498A JP4820192B2 (ja) | 2006-03-17 | 2006-03-17 | 急性冠症候群でのadamts13の測定と利用 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2007248395A JP2007248395A (ja) | 2007-09-27 |
| JP2007248395A5 JP2007248395A5 (ja) | 2009-04-23 |
| JP4820192B2 true JP4820192B2 (ja) | 2011-11-24 |
Family
ID=38592839
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006075498A Active JP4820192B2 (ja) | 2006-03-17 | 2006-03-17 | 急性冠症候群でのadamts13の測定と利用 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4820192B2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10858689B2 (en) | 2016-10-11 | 2020-12-08 | Laboratory Corporation Of America Holdings | Methods and systems for determining ADAMTS13 enzyme activity |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HUE039881T2 (hu) | 2002-05-09 | 2019-02-28 | Brigham & Womens Hospital Inc | 1L1RL-1, mint egy kardiovaszkuláris betegség-marker |
| EP2241888B1 (en) | 2006-04-24 | 2011-10-05 | Critical Care Diagnostics, Inc. | Predicting mortality and detecting severe disease |
| JP5377289B2 (ja) | 2006-05-01 | 2013-12-25 | クリティカル ケア ダイアグノスティクス インコーポレイテッド | 心血管疾患の診断方法 |
| EP2374878B1 (en) | 2007-06-22 | 2015-08-19 | The Chemo-Sero-Therapeutic Research Institute | Novel adamts-13 mutant |
| PT2827152T (pt) * | 2008-04-18 | 2016-09-13 | Critical Care Diagnostics Inc | Previsão do risco de eventos cardíacos adversos maiores |
| PL2358895T3 (pl) * | 2008-12-05 | 2019-03-29 | Baxalta GmbH | Sposoby pomiaru zależnego od ADAMTS13 cięcia in vivo czynnika von Willebranda i ich zastosowanie |
| US8501420B2 (en) * | 2009-08-31 | 2013-08-06 | Abbott Laboratories | Biomarkers for prediction of major adverse cardiac events and uses thereof |
| CN104737170A (zh) | 2012-08-21 | 2015-06-24 | 重症监护诊断股份有限公司 | 多标记风险分层 |
| CN106066401B (zh) * | 2014-03-07 | 2018-11-23 | 重庆早柒天生物科技股份有限公司 | 生物标志物vwf和adamts13及其在肝硬化诊断试剂中的用途 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2344606A1 (en) * | 1998-10-23 | 2000-05-04 | Huabing Yuan | Conformation-specific anti-von willebrand factor antibodies |
| JP4666942B2 (ja) * | 2003-04-25 | 2011-04-06 | 学校法人慶應義塾 | フォンビルブラント因子切断酵素遺伝子解析による血栓性疾患関連の遺伝子変異検出方法 |
| AU2004258113B2 (en) * | 2003-07-07 | 2009-11-05 | University Of North Carolina At Chapel Hill | Method and system for detection of von Willebrand factor (vWF) multimers |
| JP4398188B2 (ja) * | 2003-07-09 | 2010-01-13 | 積水メディカル株式会社 | 急性冠症候群およびその病態の検査方法 |
| KR20060123348A (ko) * | 2003-12-22 | 2006-12-01 | 가부시키가이샤 미쓰비시 가가쿠 야토론 | 본 윌브랜드 인자 분해효소의 측정에 의한 혈전병의검출방법 |
-
2006
- 2006-03-17 JP JP2006075498A patent/JP4820192B2/ja active Active
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10858689B2 (en) | 2016-10-11 | 2020-12-08 | Laboratory Corporation Of America Holdings | Methods and systems for determining ADAMTS13 enzyme activity |
| US11959124B2 (en) | 2016-10-11 | 2024-04-16 | Laboratory Corporation Of America Holdings | Methods and systems for determining ADAMTS13 enzyme activity |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2007248395A (ja) | 2007-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4820192B2 (ja) | 急性冠症候群でのadamts13の測定と利用 | |
| Twerenbold et al. | High-sensitive troponin T measurements: what do we gain and what are the challenges? | |
| Eggers et al. | Persistent cardiac troponin I elevation in stabilized patients after an episode of acute coronary syndrome predicts long-term mortality | |
| Panteghini et al. | Use of biochemical markers in acute coronary syndromes. IFCC Scientific Division, Committee on Standardization of Markers of Cardiac Damage | |
| Kavsak et al. | The impact of the ESC/ACC redefinition of myocardial infarction and new sensitive troponin assays on the frequency of acute myocardial infarction | |
| Panteghini et al. | Proposals from IFCC Committee on Standardization of Markers of Cardiac Damage (C-SMCD): recommendations on use of biochemical markers of cardiac damage in acute coronary syndromes | |
| Qin et al. | Release patterns of pregnancy associated plasma protein A (PAPP-A) in patients with acute coronary syndromes | |
| Pengo et al. | Survey of lupus anticoagulant diagnosis by central evaluation of positive plasma samples | |
| Eggers et al. | Clinical implications of the change of cardiac troponin I levels in patients with acute chest pain—an evaluation with respect to the Universal Definition of Myocardial Infarction | |
| Sayre et al. | Measurement of cardiac troponin T is an effective method for predicting complications among emergency department patients with chest pain | |
| Scirica et al. | Troponins in acute coronary syndromes | |
| WO2008017928A2 (en) | Method for the prediction of vascular events and the diagnosis of acute coronary syndrome | |
| Miyamoto et al. | Increased serum levels and expression of S100A8/A9 complex in infiltrated neutrophils in atherosclerotic plaque of unstable angina | |
| EP1990421B1 (en) | Method of detecting condition in patient with disturbance of consciousness | |
| Luxembourg et al. | Cardiovascular risk factors in idiopathic compared to riskassociated venous thromboembolism: a focus on fibrinogen, factor VIII, and high-sensitivity C-reactive protein (hs-CRP) | |
| Sylvén et al. | Excellent reliability of nurse-based bedside diagnosis of acute myocardial infarction by rapid dry-strip creatine kinase MB, myoglobin, and troponin T | |
| Adam et al. | Efficacy of hematological and coagulation parameters in the diagnosis and prognosis of patients with acute coronary syndrome | |
| Wang et al. | Red cell distribution width is increased in chronic thromboembolic pulmonary hypertension | |
| Hamm | Risk stratifying acute coronary syndromes: gradient of risk and benefit | |
| Gil et al. | Plasma fibrinogen and troponin I in acute coronary syndrome and stable angina | |
| Hamm | Acute coronary syndromes: the diagnostic role of troponins | |
| Casals et al. | Impact of ultrasensitive cardiac troponin I dynamic changes in the new universal definition of myocardial infarction | |
| Wu | Use of cardiac markers as assessed by outcomes analysis | |
| KR20190088181A (ko) | 뇌졸중 진단 또는 예후예측용 바이오마커 및 이의 용도 | |
| Frey et al. | Coagulation factor XIII activity predicts left ventricular remodelling after acute myocardial infarction |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090311 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090311 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110210 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110222 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110420 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110823 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110902 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140909 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4820192 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313532 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |