JP4746046B2 - 末梢神経と神経組織の向上された成長のための方法およデバイス - Google Patents
末梢神経と神経組織の向上された成長のための方法およデバイス Download PDFInfo
- Publication number
- JP4746046B2 JP4746046B2 JP2007530763A JP2007530763A JP4746046B2 JP 4746046 B2 JP4746046 B2 JP 4746046B2 JP 2007530763 A JP2007530763 A JP 2007530763A JP 2007530763 A JP2007530763 A JP 2007530763A JP 4746046 B2 JP4746046 B2 JP 4746046B2
- Authority
- JP
- Japan
- Prior art keywords
- silk
- lumen
- tubular body
- fibers
- nerve
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 34
- 210000000578 peripheral nerve Anatomy 0.000 title claims description 20
- 230000001537 neural effect Effects 0.000 title description 4
- 230000008929 regeneration Effects 0.000 claims abstract description 22
- 238000011069 regeneration method Methods 0.000 claims abstract description 22
- 210000002569 neuron Anatomy 0.000 claims abstract description 19
- 238000004519 manufacturing process Methods 0.000 claims abstract description 3
- 239000000835 fiber Substances 0.000 claims description 92
- 210000004116 schwann cell Anatomy 0.000 claims description 43
- 210000000278 spinal cord Anatomy 0.000 claims description 39
- 239000002131 composite material Substances 0.000 claims description 38
- 239000011159 matrix material Substances 0.000 claims description 38
- 210000004027 cell Anatomy 0.000 claims description 33
- 108090000623 proteins and genes Proteins 0.000 claims description 27
- 102000004169 proteins and genes Human genes 0.000 claims description 26
- 235000018102 proteins Nutrition 0.000 claims description 25
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 claims description 14
- 229920002674 hyaluronan Polymers 0.000 claims description 14
- 229960003160 hyaluronic acid Drugs 0.000 claims description 14
- 108010022355 Fibroins Proteins 0.000 claims description 13
- 108010085895 Laminin Proteins 0.000 claims description 13
- 102000007547 Laminin Human genes 0.000 claims description 13
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 claims description 9
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 claims description 9
- 210000002744 extracellular matrix Anatomy 0.000 claims description 9
- 238000004132 cross linking Methods 0.000 claims description 8
- 239000000126 substance Substances 0.000 claims description 8
- 241000255789 Bombyx mori Species 0.000 claims description 6
- 108010039918 Polylysine Proteins 0.000 claims description 6
- 239000000017 hydrogel Substances 0.000 claims description 6
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 claims description 6
- 229920000656 polylysine Polymers 0.000 claims description 6
- 108010067306 Fibronectins Proteins 0.000 claims description 5
- 102000016359 Fibronectins Human genes 0.000 claims description 5
- 229920000249 biocompatible polymer Polymers 0.000 claims description 5
- 235000010443 alginic acid Nutrition 0.000 claims description 4
- 229920000615 alginic acid Polymers 0.000 claims description 4
- 239000005018 casein Substances 0.000 claims description 4
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 claims description 4
- 235000021240 caseins Nutrition 0.000 claims description 4
- 239000003102 growth factor Substances 0.000 claims description 4
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 claims description 3
- 229940072056 alginate Drugs 0.000 claims description 3
- 239000003242 anti bacterial agent Substances 0.000 claims description 3
- 229940088710 antibiotic agent Drugs 0.000 claims description 3
- 239000002775 capsule Substances 0.000 claims description 3
- 239000003018 immunosuppressive agent Substances 0.000 claims description 3
- 150000003431 steroids Chemical class 0.000 claims description 3
- 102000004127 Cytokines Human genes 0.000 claims description 2
- 108090000695 Cytokines Proteins 0.000 claims description 2
- 108010028203 spidroin 2 Proteins 0.000 claims description 2
- 230000000975 bioactive effect Effects 0.000 claims 2
- 229940124589 immunosuppressive drug Drugs 0.000 claims 1
- 210000005036 nerve Anatomy 0.000 abstract description 50
- 238000002513 implantation Methods 0.000 abstract description 4
- 210000003050 axon Anatomy 0.000 description 34
- 210000003594 spinal ganglia Anatomy 0.000 description 29
- 239000000243 solution Substances 0.000 description 21
- 108010025020 Nerve Growth Factor Proteins 0.000 description 17
- 102100025038 Ubiquitin carboxyl-terminal hydrolase isozyme L1 Human genes 0.000 description 16
- 101710186825 Ubiquitin carboxyl-terminal hydrolase isozyme L1 Proteins 0.000 description 16
- 239000007943 implant Substances 0.000 description 16
- 210000001519 tissue Anatomy 0.000 description 16
- 101000979249 Homo sapiens Neuromodulin Proteins 0.000 description 15
- 102100023206 Neuromodulin Human genes 0.000 description 15
- 239000003550 marker Substances 0.000 description 15
- 208000027418 Wounds and injury Diseases 0.000 description 14
- 238000002372 labelling Methods 0.000 description 14
- 102000015336 Nerve Growth Factor Human genes 0.000 description 13
- 208000014674 injury Diseases 0.000 description 13
- 229940053128 nerve growth factor Drugs 0.000 description 13
- 230000003376 axonal effect Effects 0.000 description 12
- 230000006378 damage Effects 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- 238000002054 transplantation Methods 0.000 description 11
- 230000008595 infiltration Effects 0.000 description 10
- 238000001764 infiltration Methods 0.000 description 10
- 210000002540 macrophage Anatomy 0.000 description 10
- 230000008439 repair process Effects 0.000 description 10
- 210000004940 nucleus Anatomy 0.000 description 9
- 102000008186 Collagen Human genes 0.000 description 8
- 108010035532 Collagen Proteins 0.000 description 8
- 229920001436 collagen Polymers 0.000 description 8
- 210000002241 neurite Anatomy 0.000 description 8
- 239000002510 pyrogen Substances 0.000 description 8
- 210000003497 sciatic nerve Anatomy 0.000 description 8
- 239000001993 wax Substances 0.000 description 8
- 238000012856 packing Methods 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 102100036220 PC4 and SFRS1-interacting protein Human genes 0.000 description 6
- 229930040373 Paraformaldehyde Natural products 0.000 description 6
- 241000700159 Rattus Species 0.000 description 6
- 239000002771 cell marker Substances 0.000 description 6
- 210000003169 central nervous system Anatomy 0.000 description 6
- 229920002866 paraformaldehyde Polymers 0.000 description 6
- 210000001428 peripheral nervous system Anatomy 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 102000053171 Glial Fibrillary Acidic Human genes 0.000 description 5
- 101710193519 Glial fibrillary acidic protein Proteins 0.000 description 5
- 108090000704 Tubulin Proteins 0.000 description 5
- 102000004243 Tubulin Human genes 0.000 description 5
- 239000012867 bioactive agent Substances 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 210000004556 brain Anatomy 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 5
- 239000011248 coating agent Substances 0.000 description 5
- 238000000576 coating method Methods 0.000 description 5
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 5
- 239000000499 gel Substances 0.000 description 5
- 210000005046 glial fibrillary acidic protein Anatomy 0.000 description 5
- 239000002953 phosphate buffered saline Substances 0.000 description 5
- 230000001737 promoting effect Effects 0.000 description 5
- 238000011084 recovery Methods 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 210000004885 white matter Anatomy 0.000 description 5
- OBYNJKLOYWCXEP-UHFFFAOYSA-N 2-[3-(dimethylamino)-6-dimethylazaniumylidenexanthen-9-yl]-4-isothiocyanatobenzoate Chemical compound C=12C=CC(=[N+](C)C)C=C2OC2=CC(N(C)C)=CC=C2C=1C1=CC(N=C=S)=CC=C1C([O-])=O OBYNJKLOYWCXEP-UHFFFAOYSA-N 0.000 description 4
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 description 4
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 description 4
- 108010080379 Fibrin Tissue Adhesive Proteins 0.000 description 4
- 108010010803 Gelatin Proteins 0.000 description 4
- 102000007072 Nerve Growth Factors Human genes 0.000 description 4
- 102000004230 Neurotrophin 3 Human genes 0.000 description 4
- 108090000742 Neurotrophin 3 Proteins 0.000 description 4
- 102000035195 Peptidases Human genes 0.000 description 4
- 108091005804 Peptidases Proteins 0.000 description 4
- 206010040030 Sensory loss Diseases 0.000 description 4
- 238000013459 approach Methods 0.000 description 4
- 229940077737 brain-derived neurotrophic factor Drugs 0.000 description 4
- 239000008273 gelatin Substances 0.000 description 4
- 229920000159 gelatin Polymers 0.000 description 4
- 235000019322 gelatine Nutrition 0.000 description 4
- 235000011852 gelatine desserts Nutrition 0.000 description 4
- 230000028709 inflammatory response Effects 0.000 description 4
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 4
- 230000005012 migration Effects 0.000 description 4
- 238000013508 migration Methods 0.000 description 4
- 210000003205 muscle Anatomy 0.000 description 4
- 210000004498 neuroglial cell Anatomy 0.000 description 4
- 229940032018 neurotrophin 3 Drugs 0.000 description 4
- 230000002093 peripheral effect Effects 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- HLWRUJAIJJEZDL-UHFFFAOYSA-M sodium;2-[2-[bis(carboxymethyl)amino]ethyl-(carboxymethyl)amino]acetate Chemical compound [Na+].OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC([O-])=O HLWRUJAIJJEZDL-UHFFFAOYSA-M 0.000 description 4
- 238000001356 surgical procedure Methods 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- 102000004889 Interleukin-6 Human genes 0.000 description 3
- 108090001005 Interleukin-6 Proteins 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 208000028389 Nerve injury Diseases 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 206010033799 Paralysis Diseases 0.000 description 3
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 3
- 230000028600 axonogenesis Effects 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 229940098773 bovine serum albumin Drugs 0.000 description 3
- 239000006059 cover glass Substances 0.000 description 3
- 238000000502 dialysis Methods 0.000 description 3
- 238000007598 dipping method Methods 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 3
- 238000003364 immunohistochemistry Methods 0.000 description 3
- 230000001338 necrotic effect Effects 0.000 description 3
- 230000008764 nerve damage Effects 0.000 description 3
- 230000005015 neuronal process Effects 0.000 description 3
- 238000010899 nucleation Methods 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 108010073385 Fibrin Proteins 0.000 description 2
- 102000009123 Fibrin Human genes 0.000 description 2
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 2
- 206010016654 Fibrosis Diseases 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 108060003393 Granulin Proteins 0.000 description 2
- 238000010867 Hoechst staining Methods 0.000 description 2
- 208000005890 Neuroma Diseases 0.000 description 2
- QGMRQYFBGABWDR-UHFFFAOYSA-M Pentobarbital sodium Chemical compound [Na+].CCCC(C)C1(CC)C(=O)NC(=O)[N-]C1=O QGMRQYFBGABWDR-UHFFFAOYSA-M 0.000 description 2
- 208000010886 Peripheral nerve injury Diseases 0.000 description 2
- 229920000954 Polyglycolide Polymers 0.000 description 2
- 206010036790 Productive cough Diseases 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 108010071390 Serum Albumin Proteins 0.000 description 2
- 102000007562 Serum Albumin Human genes 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 108090000787 Subtilisin Proteins 0.000 description 2
- 238000010640 amide synthesis reaction Methods 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 210000001130 astrocyte Anatomy 0.000 description 2
- 230000003140 astrocytic effect Effects 0.000 description 2
- 229920001222 biopolymer Polymers 0.000 description 2
- 239000002981 blocking agent Substances 0.000 description 2
- 230000021164 cell adhesion Effects 0.000 description 2
- 239000000356 contaminant Substances 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- OILAIQUEIWYQPH-UHFFFAOYSA-N cyclohexane-1,2-dione Chemical compound O=C1CCCCC1=O OILAIQUEIWYQPH-UHFFFAOYSA-N 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 229950003499 fibrin Drugs 0.000 description 2
- 230000004761 fibrosis Effects 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000002518 glial effect Effects 0.000 description 2
- LEQAOMBKQFMDFZ-UHFFFAOYSA-N glyoxal Chemical compound O=CC=O LEQAOMBKQFMDFZ-UHFFFAOYSA-N 0.000 description 2
- 229960003444 immunosuppressant agent Drugs 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000010354 integration Effects 0.000 description 2
- 238000009940 knitting Methods 0.000 description 2
- 230000033001 locomotion Effects 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 238000002406 microsurgery Methods 0.000 description 2
- 230000017074 necrotic cell death Effects 0.000 description 2
- 210000003757 neuroblast Anatomy 0.000 description 2
- 230000007514 neuronal growth Effects 0.000 description 2
- 238000004806 packaging method and process Methods 0.000 description 2
- -1 parchment Proteins 0.000 description 2
- 229920000729 poly(L-lysine) polymer Polymers 0.000 description 2
- 239000004633 polyglycolic acid Substances 0.000 description 2
- 239000012460 protein solution Substances 0.000 description 2
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 2
- 230000029058 respiratory gaseous exchange Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 238000001878 scanning electron micrograph Methods 0.000 description 2
- 231100000241 scar Toxicity 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 208000020431 spinal cord injury Diseases 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 210000003802 sputum Anatomy 0.000 description 2
- 208000024794 sputum Diseases 0.000 description 2
- 239000010935 stainless steel Substances 0.000 description 2
- 229910001220 stainless steel Inorganic materials 0.000 description 2
- 230000001954 sterilising effect Effects 0.000 description 2
- 238000004659 sterilization and disinfection Methods 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 230000019635 sulfation Effects 0.000 description 2
- 238000005670 sulfation reaction Methods 0.000 description 2
- 229920002994 synthetic fiber Polymers 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 229910001428 transition metal ion Inorganic materials 0.000 description 2
- 230000008733 trauma Effects 0.000 description 2
- 238000004804 winding Methods 0.000 description 2
- XBBVURRQGJPTHH-UHFFFAOYSA-N 2-hydroxyacetic acid;2-hydroxypropanoic acid Chemical compound OCC(O)=O.CC(O)C(O)=O XBBVURRQGJPTHH-UHFFFAOYSA-N 0.000 description 1
- 241000239290 Araneae Species 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 108091016585 CD44 antigen Proteins 0.000 description 1
- 108010076119 Caseins Proteins 0.000 description 1
- 102000011413 Chondroitinases and Chondroitin Lyases Human genes 0.000 description 1
- 108010023736 Chondroitinases and Chondroitin Lyases Proteins 0.000 description 1
- 102000012422 Collagen Type I Human genes 0.000 description 1
- 108010022452 Collagen Type I Proteins 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- AZKVWQKMDGGDSV-BCMRRPTOSA-N Genipin Chemical compound COC(=O)C1=CO[C@@H](O)[C@@H]2C(CO)=CC[C@H]12 AZKVWQKMDGGDSV-BCMRRPTOSA-N 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 102000008055 Heparan Sulfate Proteoglycans Human genes 0.000 description 1
- 229920002971 Heparan sulfate Polymers 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 238000012404 In vitro experiment Methods 0.000 description 1
- 206010021639 Incontinence Diseases 0.000 description 1
- 235000008708 Morus alba Nutrition 0.000 description 1
- 240000000249 Morus alba Species 0.000 description 1
- 102000006386 Myelin Proteins Human genes 0.000 description 1
- 108010083674 Myelin Proteins Proteins 0.000 description 1
- 239000012580 N-2 Supplement Substances 0.000 description 1
- 102100037369 Nidogen-1 Human genes 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 241000700157 Rattus norvegicus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 1
- 108010013296 Sericins Proteins 0.000 description 1
- 206010040844 Skin exfoliation Diseases 0.000 description 1
- 208000029033 Spinal Cord disease Diseases 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 108090000054 Syndecan-2 Proteins 0.000 description 1
- 108090000190 Thrombin Proteins 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 229920006243 acrylic copolymer Polymers 0.000 description 1
- 238000007605 air drying Methods 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 230000003872 anastomosis Effects 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 230000037007 arousal Effects 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 239000007640 basal medium Substances 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 210000005056 cell body Anatomy 0.000 description 1
- 230000012292 cell migration Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 239000002415 cerumenolytic agent Substances 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 238000000942 confocal micrograph Methods 0.000 description 1
- 238000004624 confocal microscopy Methods 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 230000009615 deamination Effects 0.000 description 1
- 238000006481 deamination reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000002224 dissection Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 210000001951 dura mater Anatomy 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000004299 exfoliation Methods 0.000 description 1
- 210000003195 fascia Anatomy 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 230000003176 fibrotic effect Effects 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 210000003811 finger Anatomy 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- AZKVWQKMDGGDSV-UHFFFAOYSA-N genipin Natural products COC(=O)C1=COC(O)C2C(CO)=CCC12 AZKVWQKMDGGDSV-UHFFFAOYSA-N 0.000 description 1
- 210000004907 gland Anatomy 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229940015043 glyoxal Drugs 0.000 description 1
- BCQZXOMGPXTTIC-UHFFFAOYSA-N halothane Chemical compound FC(F)(F)C(Cl)Br BCQZXOMGPXTTIC-UHFFFAOYSA-N 0.000 description 1
- 229960003132 halothane Drugs 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 201000001881 impotence Diseases 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000011850 initial investigation Methods 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 210000000876 intercostal muscle Anatomy 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 150000002540 isothiocyanates Chemical class 0.000 description 1
- 238000002684 laminectomy Methods 0.000 description 1
- 238000003754 machining Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 108010012064 mouse beta3 tubulin Proteins 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 210000005012 myelin Anatomy 0.000 description 1
- 230000023105 myelination Effects 0.000 description 1
- 210000003061 neural cell Anatomy 0.000 description 1
- 210000001178 neural stem cell Anatomy 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 108010008217 nidogen Proteins 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 210000003105 phrenic nerve Anatomy 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920000747 poly(lactic acid) Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- HJORMJIFDVBMOB-UHFFFAOYSA-N rolipram Chemical compound COC1=CC=C(C2CC(=O)NC2)C=C1OC1CCCC1 HJORMJIFDVBMOB-UHFFFAOYSA-N 0.000 description 1
- 229950005741 rolipram Drugs 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 230000036573 scar formation Effects 0.000 description 1
- 230000037390 scarring Effects 0.000 description 1
- 238000009991 scouring Methods 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000001953 sensory effect Effects 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 229920000260 silastic Polymers 0.000 description 1
- 229920002379 silicone rubber Polymers 0.000 description 1
- 239000004945 silicone rubber Substances 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 210000005070 sphincter Anatomy 0.000 description 1
- 238000007447 staining method Methods 0.000 description 1
- 239000010902 straw Substances 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 210000001590 sural nerve Anatomy 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 210000003448 thoracic nerve Anatomy 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 210000003813 thumb Anatomy 0.000 description 1
- 230000000451 tissue damage Effects 0.000 description 1
- 231100000827 tissue damage Toxicity 0.000 description 1
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 1
- 230000002485 urinary effect Effects 0.000 description 1
- 210000001835 viscera Anatomy 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/043—Proteins; Polypeptides; Degradation products thereof
- A61L31/047—Other specific proteins or polypeptides not covered by A61L31/044 - A61L31/046
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/22—Polypeptides or derivatives thereof, e.g. degradation products
- A61L27/227—Other specific proteins or polypeptides not covered by A61L27/222, A61L27/225 or A61L27/24
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/40—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
- A61L27/44—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix
- A61L27/48—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix with macromolecular fillers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/12—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
- A61L31/125—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix
- A61L31/129—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix containing macromolecular fillers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/32—Materials or treatment for tissue regeneration for nerve reconstruction
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T29/00—Metal working
- Y10T29/49—Method of mechanical manufacture
- Y10T29/49826—Assembling or joining
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Dermatology (AREA)
- Engineering & Computer Science (AREA)
- Composite Materials (AREA)
- Materials Engineering (AREA)
- Surgery (AREA)
- Medicinal Chemistry (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Heart & Thoracic Surgery (AREA)
- Vascular Medicine (AREA)
- Materials For Medical Uses (AREA)
- Prostheses (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Description
管状のボディの内腔の長軸に沿って本質的に平行に置かれた、複数の絹の要素、を含む医療デバイスを提供する。
内腔内の絹の要素は、約lμから約l00μmの距離で、互いに好ましくは離れて置かれる。
本発明のデバイスは、10,000μm2当たり約1から約30まで、好ましくは10,000μm2当たり約1から約10、または10,000μm2当たり約5から約10の範囲の、絹の要素の充填密度を有することができる。
管状のボディの壁は、約250μmから約750μm、好適には約300μmから約600μmの厚さを有することができ、300μmから350μmの値が好ましい。
本発明のいくつかの好ましい実施態様では、デバイスは長さ2.0mmであり、直径は0.5mmである。
絹の要素は、典型的には細片絹または巻きとられた絹かよじられた絹の形をしている。絹の要素は便利なように調整されることができ、デバイスの壁に対して本質的に長さ方向に配向される。
ヒドロゲル(例えばポリリシンまたはカゼインとともに、またはこれらを含まないアルギン酸またはヒアルロン酸)のような、再吸収可能な生体適合性のポリマーを含む内腔マトリックス中に、絹の要素がセットされることは特に好ましい。他の成分、たとえば、細胞外マトリックス(ECM)、たとえば、フィブロネクチンおよび/またはラミニンが存在することができる。これらの物質は導管中の内腔マトリックスに加えられるか、または内腔マトリックス中の絹のフィラメント上にコーティングされることができる。
その上に管状のボディが形成される型台の調製;
型台の上に繊維を置くこと;
繊維にマトリックスを適用して複合物ボディを形成すること;および
型台を除去すること。
チューブの内腔内の絹の要素間に、内腔マトリックス成分を導入することも好ましい。
絹の要素は、例えばエチレンジアミン4酢酸ナトリウム塩(EDTA)のようなキレート試薬の溶液で洗浄して、有毒な場合がある遷移金属イオンのような、可能性のある汚染物質を除去することができる。他のキレート試薬も使用することができる。好ましくは、絹からセリシンを除いて精練される。これは絹をプロテアーゼ、例えばサブチリシンを使用して処理することにより達成することができる。しかし、他の穏やかな蛋白質分解酵素も使用されてもよい。その後、酵素は、処理の後に洗浄することができる。
本発明は、末梢神経および中枢神経の白質の再生に関して、先行技術の試みに伴う損失の多くを除去するか本質的に減じることができる移植可能なデバイスに関する。
より詳細には、本発明のデバイスは生体適合性の再吸収可能な物質から構成され、神経軸索、シュワン細胞およびグリア細胞を成長させるために結合部位を提供するその能力が調整されることができる。
移植のために、適切な直径のデバイスが、治療される神経または白質路の直径に応じて選択されている。デバイスは適切な長さに鋭いブレードまたは他の道具で切断される。1つの実施態様では、デバイスは、1つ以上の縫合糸によって適所に保持される。別の実施態様では、デバイスは、フィブリン糊で適所に保持することができる。デバイスは乾燥した状態で、移植されることができ、または使用の前に適切な生理的塩類溶液で5分から5時間の間ソーキングすることができる。
本発明は、以下において実施例および図を参照しつつさらに記述されるが、これらは例としてのみ提供され、本発明を何ら制限するものではない。多くの図が言及される:
図1は、シュワン細胞核のヘキスト染色をした後根神経節(DRG)外植片を示す。多くのシュワン細胞が外植片から移動しており、絹の繊維に接着したことを示す。
図2は、さらにヘキスト染色をしたDRG外植片を示す。多くのシュワン細胞が外植片から移動しており、絹の繊維に接着したことを示す。さらに、GAP−43の免疫反応性の神経突起(矢印)は、個々の絹の繊維に沿って伸び、ある場合には個々の繊維に橋を架ける。
図3は、ヘキストラベルされた坐骨神経外植片を示し、GAP−43の免疫反応性のシュワン細胞が外植片から移動しており、絹の繊維に接着したことを示す。
図4は、ヘキストラベルされたシュワン細胞核およびGAP−43の免疫反応性の神経突起を含む成体DRG培養物を示す。ラミニンでコーティングされている絹の個々の絹の繊維に接着することが示される。
図5は、ヘキストラベルされたシュワン細胞核およびGAP−43の免疫反応性の神経突起を含む成体DRG培養物を示す。ラミニンでコーティングされていない絹の個々の絹の繊維に接着することが示される。
図6は、神経膠の特定のマーカーS100を使用した細胞のラベル付けを示し、多くのS100の免疫反応性のシュワン細胞が絹の繊維と関連性を有することを示す。
図8は、絹繊維および脊髄(白色の繊維、図8、左)を示す。星状細胞マーカーGFAPでラベルを付けると、一般に、絹の繊維が完全な脊髄(図8、右)のすぐ近くにあり、ホスト脊髄と移植物の間にほとんど壊死の組織がないことを示した。
図9は、脊髄内へ移植された絹の繊維の束の内のマクロファージ浸潤と、周囲の組織を示す。
図10は、絹の繊維の配向と平行に配向した絹移植物内への、PGP 9.5軸索のマーカーでラベルを付けた軸索(矢印)の成長を示す。
図11は、個々の絹の繊維の間にも沿って成長する、PGP 9.5軸索のマーカーでラベルを付けた軸索の共焦点顕微鏡検査写真を示す。左の写真は矢印でマークされた軸索を示し、右の写真は矢印でマークされた絹の繊維を示す。
図12は、軸索のマーカーPGP 9.5およびシュワン細胞マーカーp75による二重のラベリングを示す。左の写真は軸索を示し、右の写真はシュワン細胞を示す。
図14は、脊髄へ移植された導管の構造を示し、細長い小さな絹の破片(矢)が外被膜の各壁に見られ、長さ方向に配向したストランド(矢じり)として内側のコアが現れる。
図15は、絹の導管中へのマクロファージ浸潤が、結合されていない絹の繊維で見られたそれに、外観と程度において類似することを示す(図9を参照)。さらに、移植後8週において、マクロファージは、個々の絹の繊維の回りにクラスターとなるのを見ることができることがある。
図16は、絹の繊維間に成長するPGP 9.5で染色された軸索を示す。
図17は、軸索のマーカーPGP 9.5およびシュワン細胞マーカーp75により二重ラベリングされ、マットに成長したシュワン細胞と軸索の間で密接な対応を示すことを示す。左の写真は軸索を示し、右の写真はシュワン細胞を示す。
図18は、本発明の1つの実施態様による神経導管の走査型電子顕微鏡写真を示す。
神経再生導管の調製は、次の工程のうちのいくつかまたはすべてを要求する:
型台の調製;
型台に繊維を置くこと;
水性のタンパク質の溶液を適用し、複合チューブを形成すること;
型台からの取り出し;
ワックス除去;
複合材料の架橋;
チューブ内へ配向された絹のフィラメントを差し込むこと;
チューブの内腔内のフィラメント間へのマトリックス成分の追加;
フィブロネクチンおよび/またはラミニンのような細胞外マトリックス成分の導入;
神経成長因子の導入、発熱物質の除去および殺菌;
1つまたは複数の神経成長因子の追加;および
乾燥および所定の長さへのデバイスの切断。
型台は以下のように調製される。型台を調製する最も簡単な方法は、適切な直径のステンレス鋼管材料またはロッドを使用することである。これらは使用の前に清浄にされ、研摩される。適用されたマトリックス材が乾燥された後、チューブは、容易に型台から滑らせて排出させることができる。小さな直径の型台については、比較的堅い直線のワイヤーが、パラフィンワックスの薄い層または周囲温度よりも高い比較的低い温度で溶融する他の物質の薄い層で最初にコーティングされる。コーティングはワイヤーを溶融したワックスに垂直に浸漬することにより達成することができる。型台上のワックスコーティングの外側の直径は、その上に形成されるチューブの内側(管腔)の直径を画定する。30mmまでのより大きな直径の型台は、適切な直径のワックスのロッドをキャスティングまたは機械加工することにより、または適切な直径のシリンダをワックスでコーティングすることにより調製することができる。それらのまわりに形成された絹のチューブの内腔の内部から除去することができる型台を調製する他の方法が存在し、それらはこの分野での当業者に容易に利用可能である。
3つのタイプの絹のフィラメントが、神経再生導管の外側壁を形成するチューブの壁を強化する繊維として好適に使用される:絹の細片(繭廃棄物からコーミングして取り出し、カージングして精練されたフィラメント);一度に1つの繭から巻きとられた絹から調製された、精練された単一の繭糸;一度に7−13の繭から巻きとられた絹から調製された、20−37デニールの7−13の精練された繭糸。Antheraea pernyiiからのタッサーシルクが使用されたが、任意の蚕または非蚕絹、または天然、組み換え、再生された絹のタンパク質から押し出された絹のフィラメントも代わりに使用することができる。
様々なタンパク質が絹複合材料のマトリックスを供給するために使用することができる。6.3Mの臭化リチウム水溶液中に市販のフィブロイン粉末を溶解したことにより調製された、新鮮に調製した再生された蚕フィブロインの濃度10−40%w/vの溶液で好結果が得られた。臭化リチウムは4℃で蒸留水に対する完全な透析によって除去される。透析物は蒸発または逆透析によって透析チューブ内に濃縮される。得られた再生フィブロイン溶液は、型台上にある間に絹糸上へペイントされ、孔のないチューブを生産する。フィブロイン溶液は、乾燥される。得られる再生された絹/Antheraea絹の複合チューブは、型台から取り除くことができる。複合チューブは、再生フィブロイン溶液をスプレーすること、または型台を同じ溶液に浸漬することによっても形成できる。蚕または非蚕から直接得られた濃縮フィブロイン溶液は、再生されたフィブロインの代わりに使用することができる。複数のタンパク質も再生されたフィブロインの代わりに使用することができる。これらとしてはフィブロイン糊、ゼラチンの希薄溶液または血清アルブミンを包含する。他の水溶性のタンパク質、ヒアルロン酸または他の生体適合性のポリマーを代わりに使用することができる場合がある。型台に絹を使用する代わりに、編んだ絹のチューブをマトリックス・タンパク質または他の高分子溶液で、スプレーまたは浸漬することによりコーティングすることができる。
ステンレス鋼型台が使用される場合、絹の複合チューブは、型台からそれを滑らせることにより容易に除去することができる。狭い複合チューブについては、これは小さな鉗子で達成することができる。ワックスがコーティングされた型台が使用される場合には、ワックスまたは型台への他の低い融点のコーティングを穏やかに溶融することにより、絹の複合チューブはこれから取り除かれる。あるいは、直径を小さくすることができる型台が使用されることができ、たとえば、中央の芯を除去し、その後それを囲む絹の複合チューブを滑らせて排出することができる。
ワックスが使用された場合、絹の複合チューブ上のこのトレース量を、ベンゼン、キシレンまたは他のワックス溶剤に浸漬することにより除去できる。
下記手順は絹の複合チューブのマトリックスタンパク質を架橋するために使用することができる。過剰の乾燥したパラホルムアルデヒドが、封ができる包装容器の底に置かれ、0.2mlの蒸留水が、0.5リットルの容器中の2グラムのパラホルムアルデヒドに加えられる。パラホルムアルデヒドは濾紙によってカバーされる。また、絹複合チューブはこの上に置かれる。包装容器を密封した後に、それは800℃に1時間熱される。冷却後、絹のチューブが容器から取り出され、温かい湯で徹底的に洗われる。
絹の細片のフィラメントは、乾燥した絹の複合チューブへ以下のように導入される。最初に適当なサイズの針または千枚通しを絹の細片に通す。より大きな直径の絹複合チューブにはサックニードルが役立つ。その後、典型的には、フィラメントはかなり粘着性のヒアルロン酸溶液でペイントされる。糸を通した針または千枚通しは絹の複合チューブを通して押され、チューブを配向した絹のフィラメントで満たす。この条件では、過剰のヒアルロン酸はチューブの切断端からしみ出る。ヒアルロン酸の代わりに他の再吸収可能なゲル剤を使用することができることがある。1つの実施態様では、ヒアルロン酸または他の再吸収可能なゲル剤の使用は省略される。必要な場合には、糸を通した針が、チューブの内腔内において適切な充填密度が達成されるまで、繰り返し絹の複合チューブを通して押される。経験で、これは目視で判断することができる。あるいは、チューブの中への絹のフィラメントの充填密度の正確な測定は、以下のようにして行うことができる:測定された長さの絹の複合チューブの重量を測定し、絹フィラメントを導入し、チューブの端でそれらを切断した後に再度秤量される。チューブの内腔内に所望の重量のフィラメントが存在するまで、フィラメントを追加、または除去することができる。2倍の接眼鏡を取り付けた双眼実体顕微鏡が、チューブの1mm平方の断面当たりのフィラメントの数を測定するために使用される。実験的な移植の前に、走査電子顕微鏡が、10,000μm2当たり10から1本のフィラメントの充填密度であり、フィラメント間の平均間隔がおよそ30から100μmであることは最良である。
絹のフィラメント間の内腔マトリックス成分は、ヒドロゲルの形成により、フィラメント間の適当な離隔を維持しつつ、デバイス調製および挿入に続くすべての工程において、フィラメントを所定の位置に保持するために使用される。さらに、それらはデバイス内への神経成長を高める。様々な生体高分子が、フィラメント間の内腔マトリックスを提供するために使用することができる。これらのヒドロゲルとしては、ポリリシンを含むかまたは含まないヒアルロン酸、ポリリシンを含むかまたは含まないアルギン酸塩、カゼイン、フィブリン糊、血清アルブミン、およびゼラチンが含まれる。必要に応じて、これらの高分子の水溶液は加熱して調製される。他の溶剤を水の代わりに使用することができる。それらの内腔内に配向された絹のフィラメントを含んでいる絹の複合チューブは、これらのポリマーの1つ以上を含んでいる溶液に浸される。真空は浸潤を支援するために適用することができる。フィブリン糊の場合には、フィブリン糊の形成を始めるために、配向された絹のフィラメントを含んでいる絹の複合チューブが、最初にフィブリン溶液で、その後トロンビン溶液で浸透される。
発熱物質の除去は、神経成長因子を加える前に行なわれるのが最もよい。それは、最終濃度0.1%v/vのトゥイーン20(登録商標)を含んでいるジメチルスルホキシドの1%v/vの水溶液で洗うことにより最もよく実行される。2から5回の洗浄が、この溶液で通常実行される。発熱物質除去の後、デバイスは無菌の発熱物質を含まない生理的食塩水液中で洗浄することができる。発熱物質除去に使用された溶液に接触するすべてのガラスまたはプラスチック用具または他の実験装置は、発熱物質を除去するために少なくとも2時間2400℃で焼成されるべきである。
神経成長因子のような一連の生物活性物質は、デバイスへ導入することができる。これらには、デバイスが末梢神経の回復を高めるために使用されることになっている場合には、これらは末梢神経NGFを包含し、デバイスが脳または脊髄の中で使用されることになっている場合には、中枢神経neurotrophin−3(NT3)または脳由来神経栄養因子(BDNF)を包含する。神経成長因子は、フィラメント間の内腔マトリックス成分を形成する際に最もよく加えられる。その内腔内に配向した絹のフィラメントを含んでいる絹の複合チューブにそれらが加えられる前に、それらは内腔マトリックス溶液と混合することができる。
デバイスは最初にブロットされ、乾燥される前に過剰溶液を除去する。複数の乾燥方法を使用することができ、空気乾燥または凍結乾燥を使用することができる。最適には、導管の適当な長さは、乾いたデバイスから切断される。これらは直接移植するか、または移植の前に、無菌で発熱物質を含まない09% w/vの生理的食塩水中で水分が補給される。
脊柱の離断または部分的な離断の処理については、厚さ2から10mmのデバイスのディスクが、絹のフィラメントを含んでいる2−20mmの直径の絹の複合チューブの長さ方向から切断される。これらは、損傷している場所で脊髄に横に挿入される。剥離損傷の場合には、導管は脊髄を引き剥がされた根に結び付けるように挿入することができる。末梢神経の再生を促進するための導管は、1−15mmの直径の細いチューブから調製される。直径は治療される神経のサイズおよび位置に応じて変化する。デバイスは、所定の位置に軽く縫合されるべきである。
最初のインヴィトロでの実験は、培養組織中のAntherea pernyii絹繊維が、末梢神経系(PNS)ニューロン(後根神経節細胞)による神経突起の成長をサポートし、およびさらにPNS支持細胞(シュワン細胞)の接着およびマイグレーションをサポートすることを実証する。実験は、ラット新生児(P3)の後根神経節(DRG)、および坐骨神経体外培養物、および分離された成体ラットDRG細胞を使用して実行された。
成体のラットまたは新生児ラット(P3)は、CO2の高濃度の吸入によって犠牲にされた。DRGニューロンは、英国動物(科学的方法)行為に従う手順(Huangら、Neuroreport 16:89−93(2005))を使用して培養された。後根神経節は取り出され、清浄にされ、化学的に分離され(0.125%のコラゲナーゼ、2時間;シグマ、英国)、ボッテンシュタイン アンド サトーの無血清培地(BSF−2;ハムのF−12基礎培地中に0.3%のウシ血清アルブミン(BSA)、1%のN−2サプリメントおよびl00単位の ml−1ペニシリン/100μg ml−1ストレプトマイシンを含む;全ての試薬は米国ライフ・テクノロジーズ(アメリカ製)の中で機械的に分離された。その後、細胞懸濁物は、600回転/分で5分間遠心分離され、再度懸濁された後、15%のBSAクッションによって900回転/分で10分間遠心分離された。ペレットにされた細胞は、BSF−2中に再度懸濁され、次に、ガラス・カバーガラス上に900−1000のニューロン/カバーガラスの密度で、絹の繊維が配置されたカバーガラス上にシーデイングされた。培養が、95%の空気および5%のCO2の湿った大気中で、37℃で7日間、BSF−2中の100ナノグラム/mlの神経成長因子(NGF)で維持された。カバーガラスは、ポリ−L−リジン(l00μg/ml)およびラットテール・コラーゲンで最初にコーティングし、ついで絹の繊維をコラーゲンに付着させて調製された。ある場合には、絹繊維が接着されたカバーガラスが、l0μg/mlのラミニンでコーティングされた後、DRG細胞でシーデイングされた。さらに、いくつかの実験では、DRGと坐骨神経の外植片が分離されたDRG細胞の代わりに使用された。そのような場合、新生児ラット(P3)はCO2の高濃度の吸入によって犠牲にされた。また、腰神経後根神経節と坐骨神経のセグメントが削除され、ラミニンがコーティングされた絹の繊維が接着された、ポリ−L−リジンおよびコラーゲンでコーティングされたカバーガラスに付着された。そして7−10日の間、NGFを含むBSF−2において培養された。
新生児のDRGおよび坐骨神経外植片
DRG外植片(図1、2)では、ヘキスト色付けは、多くのシュワン細胞が外植片から外へ移動し、絹の繊維に付着したことを示した。さらに、GAP−43の免疫反応性の神経突起は、個々の絹の繊維に沿って伸び、およびある場合には個々の繊維間に橋を架けることを、はっきりと見ることができる。
坐骨神経外植片(図3)では、ヘキストでラベルが付けられた多くのGAP−43の免疫反応性のシュワン細胞が、外植片から外へ移動しており、絹の繊維に付着した。繊維がシュワン細胞の付着のための非常に優れた基体を提供することが確認された。
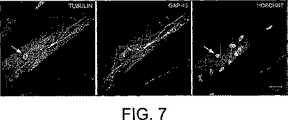
成体のDRG培養物(図4)中で、多くのヘキストでラベルが付けられたシュワン細胞核およびGAP―43の免疫反応性の神経突起が、個々の絹の繊維に付着することが観察された。繊維が成体PNSニューロンの成長を支持し、グリア細胞を支持することが確認された。外延的成長は、絹がラミニンでコーティングされた培養物(図4)およびラミニンのない培養物(図5)の両方で見られた。絹がそれ自身ニューロンの成長に良好な基体であり、付加的な細胞外マトリックスコーティングを必要としないことが確認された。
成体のラット脊髄中への絹の繊維の移植
最初のインヴィボの実験は、脊髄へ移植する絹の繊維の影響を検討するために行われた。特に興味のあることは、(絹の繊維に対する)軸索の成長の程度および配向、および周囲の完全な神経組織に対する移植の影響(すなわち壊死および炎症反応の程度)であった。
脊髄へ移植された絹についての最初のインヴィボの実験は、結合されていない(すなわち、導管内に含まれていない)絹の繊維の束について行われた。動物の治療および手順は、英国ホームオフィスによって承認されたガイドラインとプロトコルに従って実行された。若い成体雄ウィスターラットは、ハロタン(4%の誘導、2%のメンテナンス)で麻酔をかけられた。切り込みが、脊柱の上の皮膚および筋肉につけられた。また、椎弓切除はT7とT9のレベル間で行なわれた。硬膜が開かれ、中線から横方向にほぼ0.5mm、脊髄の表面から腹部方向にlmm伸びた、長さおよそ2mmの脊髄の一部分を、虹彩はさみを使用して除去した。その後、一束の絹の繊維が、脊髄の長さ方向の軸と平行に絹の繊維を向けて、損傷キャビティーに入れられた。その後、損傷サイトはゲルフォームでカバーされ、上の筋肉および皮膚を縫合した。動物は移植後、1〜8週間生存した。適切な生存時間の後、動物は、ペントバルビタールナトリウム塩(Sagatal、RMB、60mg/kg)で深く麻酔をかけられ、0.01Mリン酸緩衝食塩水(PBS)の50ml、ついで0.01Mリン酸塩緩衝液中4%のパラホルムアルデヒド、pH 7.4が上行大動脈を通して潅流された。脊髄は解剖され、4%のパラホルムアルデヒド中に1−4時間浸けられ、PBS中の15%の蔗糖の中で一晩、凍結防止された。長さ方向の断面の厚さが10−12mmの移植部位が採取された。
免疫組織化学用の一般的手順は以下の通りだった:第一の抗体中の48時間の培養、リン酸緩衝食塩水中での10分の洗浄2回、イソチオシアン酸テトラメチルローダミン(TRITC)またはイソチオシアン酸フルオレセイン(FITC)(両方ともJackson Immunoresearch Laboratories社から入手)に結合した第二の抗体中での2時間の培養。3回の10分の洗浄に続いて、スライドは2.5%の1,4−ジアザビシクロ―(2.2.2)―オクタンを含むPBSグリセリン(1:3)の中でカバーグラスをかけられるか、または上に記載された方法と同じ方法で第2抗体への免疫組織化学のために処理された。
絹の導管内の絹の繊維の移植(第1の反復)
脊髄中の絹に基づいた導管の使用についての最初の調査により、コア内にきっちりと充填された絹の繊維を有する絹の導管からできている導管を検討した(図13)。
方法:
移植方法は、上記の(2)に記載された方法と同一だった。ただし、脊髄の中に作られた損傷キャビティーがわずかに広く、必要とされた移植物の直径(およそ1mm)が異なるものとされた。
結果:
結果は、これらの移植物が脊髄と一体化せず、組織取り出しの間に脊髄から離れたことを示した。これは、おそらく、導管内の繊維の充填密度が大きすぎ、移植物内へ内因性の要素の浸透を許容することができず、それによりホスト脊髄とのいかなる種類の一体化も不可能となったためであろう。しかしながら、損傷キャビティーが本質的にすべての動物中の移植物と同じサイズで、移植物部位のまわりの脊髄が壊死を示さず、これらの移植物がホスト脊髄によってよく許容されたことを示したことに注目することは重要である。
ヒアルロン酸を含む絹の導管内への絹の繊維の移植
絹の導管の一体化が見られなかったこと(上記参照)は、導管のコア内の絹の繊維に対して、繊維が生体分解性の媒体中で懸濁可能であり、軸索および他の内因性の要素の浸潤のためのスペースを許容するだけでなく、軸索の成長を妨げないことを繊維に要求するだろうということを示唆した。したがって、ヒアルロン酸中に懸濁された絹の繊維を有する絹の外側鞘から成る導管がコア内に移植された。
移植と染色法は、上記の実施例3に記載された方法と同一だった。ただし、脊髄の中に作られた損傷キャビティーがわずかに広く、必要とされた移植物の直径(およそ1mm)が異なるものとされた。
結果:
導管の構造は明瞭に見ることができる(図14)。外側の鞘の各壁は小さな絹の細長い小片(矢印)として現れ、および内側のコアは長さ方向に配向したストランドとして現れる(矢じり)。結合されていない絹では(セクション2を参照)、GFAPラベリングは、絹移植物は、星状細胞の瘢痕と移植物との間に壊死組織がほとんどまたは全くなく、ホスト脊髄で良好に一体化されたことを示した。
Claims (22)
- 内腔および長軸を有している管状のボディ、および
管状のボディの内腔の長軸に実質的に平行に、該管状のボディの内腔内に置かれた複数の絹の要素を含み、
該管状のボディは再吸収可能な絹タンパク質を含み、該絹の要素はRGDトリプレットの少なくとも8個の繰り返しを含んでいる主要な絹のタンパク質を有する、
神経細胞の再生のための医療用デバイス。 - 再吸収可能な絹タンパク質は、蚕または非蚕から得られた再溶解された絹タンパク質、または蚕または非蚕から得られた天然絹糸フィブロインである、請求項1記載のデバイス。
- 該ボディは、絹タンパク質マトリックス中に配置された繊維を含む複合構造を有し、該マトリックスは架橋によって安定させられている、請求項1または2記載のデバイス。
- ボディを形成する繊維はヘリカルに置かれるか編まれている、請求項3記載のデバイス。
- ボディを形成する繊維は絹の繊維である、請求項3または4記載のデバイス。
- 絹の要素または繊維は、蚕絹、非蚕絹、クモ・ドラグライン絹、または組み換え絹タンパク質もしくはタンパク質類似化合物から紡がれたフィラメントを含む、請求項1から5のいずれか1項記載のデバイス。
- 再吸収可能な生体適合性のポリマーを含む内腔マトリックス中に、複数の絹の要素がセットされる、請求項1から6のいずれか1項記載のデバイス。
- 再吸収可能な生体適合性のポリマーはヒドロゲルを含む、請求項7記載のデバイス。
- ヒドロゲルはポリリシンまたはカゼインを含むかまたは含まない、ヒアルロン酸またはアルギン酸塩である、請求項8記載のデバイス。
- 内腔または絹の要素はさらに細胞外マトリックスを含む、請求項1から9のいずれか1項記載のデバイス。
- 細胞外マトリックスはフィブロネクチンおよび/またはラミニンを含む、請求項10記載のデバイス。
- デバイスはさらに1つ以上の生物活性物質を含む、請求項1から11のいずれか1項記載のデバイス。
- 生物活性物質は、生長因子、サイトカイン、抗生物質、免疫抑制薬、ステロイド、非ステロイド抗炎症剤(NSAID)から成る群から選ばれる、請求項12記載のデバイス。
- デバイスはさらに細胞集団を含む、請求項1から13のいずれか1項記載のデバイス。
- 細胞はシュワン細胞または嗅覚被膜細胞(OEC)である、請求項14記載のデバイス。
- 管状のボディを形成し、管状のボディの内腔の長軸に本質的に平行に配置されるように該管状のボディの内腔内へ絹の要素を導入することを含み、
該管状のボディは再吸収可能な絹タンパク質を含み、該絹の要素はRGDトリプレットの少なくとも8個の繰り返しを含んでいる主要な絹のタンパク質を有する、
神経細胞の再生のための医療用デバイスを製造する方法。 - 管状のボディの形成は、以下の工程を含む、請求項16記載の方法:
− 管状のボディが形成される型台を調製すること;
− 型台上に繊維を置くこと;
− 繊維にマトリックスを適用し、複合ボディを形成すること;および
− 型台を除去すること。 - さらにマトリックスの架橋を含む、請求項17記載の方法。
- チューブの内腔内の絹の要素間に内腔マトリックス成分を導入することを更に含む、請求項16、17または18記載の方法。
- 神経細胞の再生での使用のための、請求項1から14のいずれか1項記載の医療用デバイス。
- 脊髄中の神経細胞の再生での使用のための、請求項1から14のいずれか1項記載の医療用デバイス。
- 末梢神経中の神経細胞の再生での使用のための、請求項1から14のいずれか1項記載の医療用デバイス。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0420411.1 | 2004-09-14 | ||
| GB0420411A GB2417904A (en) | 2004-09-14 | 2004-09-14 | Tubular prosthesis for nerve regeneration |
| GB0422019.0 | 2004-10-05 | ||
| GB0422019A GB0422019D0 (en) | 2004-10-05 | 2004-10-05 | Medical device |
| PCT/GB2005/003456 WO2006030182A2 (en) | 2004-09-14 | 2005-09-08 | Methods and apparatus for enhanced growth of peripheral nerves and nervous tissue |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2008513051A JP2008513051A (ja) | 2008-05-01 |
| JP2008513051A5 JP2008513051A5 (ja) | 2008-11-13 |
| JP4746046B2 true JP4746046B2 (ja) | 2011-08-10 |
Family
ID=35733979
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007530763A Active JP4746046B2 (ja) | 2004-09-14 | 2005-09-08 | 末梢神経と神経組織の向上された成長のための方法およデバイス |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8106014B2 (ja) |
| EP (1) | EP1789103B1 (ja) |
| JP (1) | JP4746046B2 (ja) |
| AT (1) | ATE428453T1 (ja) |
| CA (1) | CA2580349C (ja) |
| DE (1) | DE602005013979D1 (ja) |
| WO (1) | WO2006030182A2 (ja) |
Families Citing this family (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0405045D0 (en) | 2004-03-05 | 2004-04-07 | Spinox Ltd | Composite materials |
| DE102005042455A1 (de) * | 2005-09-06 | 2007-04-12 | Medizinische Hochschule Hannover | Nervenimplantat |
| CN100382772C (zh) * | 2005-09-28 | 2008-04-23 | 南通大学 | 含蚕丝丝素的医用神经移植物的制备方法 |
| EP2097117B1 (en) * | 2006-12-11 | 2013-05-22 | Medizinische Hochschule Hannover | Implant of cross-linked spider silk threads |
| WO2009023615A1 (en) * | 2007-08-10 | 2009-02-19 | Trustees Of Tufts College | Tubular silk compositions and methods of use thereof |
| FR2941610A1 (fr) * | 2009-02-03 | 2010-08-06 | Xavier Renard | Dispositif pour relier au moins deux portions d'un nerf sectionne |
| KR101151358B1 (ko) * | 2010-03-17 | 2012-06-08 | 동국대학교 산학협력단 | 실크 및 콜라겐을 포함하는 복합 지지체 및 그 제조방법 |
| US8758374B2 (en) | 2010-09-15 | 2014-06-24 | University Of Utah Research Foundation | Method for connecting nerves via a side-to-side epineurial window using artificial conduits |
| GB201113856D0 (en) | 2011-08-11 | 2011-09-28 | Oxford Biomaterials Ltd | Medical device |
| WO2013066619A1 (en) | 2011-10-17 | 2013-05-10 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| US10842494B2 (en) | 2011-10-17 | 2020-11-24 | University Of Utah Research Foundation | Methods and devices for connecting nerves |
| CN102732525B (zh) * | 2012-06-29 | 2014-02-26 | 苏州大学 | 一种用于克隆含精氨酸-甘氨酸-天门冬氨酸的多肽的dna分子及克隆方法 |
| AU2013329076A1 (en) * | 2012-10-11 | 2015-04-23 | Tufts University | Silk reservoirs for sustained delivery of anti-cancer agents |
| US20140170162A1 (en) * | 2012-12-18 | 2014-06-19 | The Regents Of The University Of California | Preservation of the neuromuscular junction (nmj) after traumatic nerve injury |
| JP2014155622A (ja) * | 2013-02-15 | 2014-08-28 | Terumo Corp | 管状体 |
| ES2701226T3 (es) * | 2013-02-19 | 2019-02-21 | Univ Texas | Gradientes químicos |
| US10363041B2 (en) * | 2013-06-24 | 2019-07-30 | The Trustees Of The Stevens Institute Of Technology | Implantable nerve guidance conduits having polymer fiber guidance channel |
| US20150044259A1 (en) * | 2013-08-08 | 2015-02-12 | Mauris N. DeSilva | Scaffold for enhanced neural tissue regeneration |
| US20150047532A1 (en) * | 2013-08-13 | 2015-02-19 | Utah State University | Synthetic spider silk protein compositions and methods |
| AU2015346044A1 (en) * | 2014-11-15 | 2017-07-13 | Tissuegen, Inc. | Device for induction of cellular activity and modification |
| CA2995233C (en) | 2015-07-20 | 2024-01-02 | Tufts University | Biodegradable silk ear tubes |
| US10420939B2 (en) | 2016-03-31 | 2019-09-24 | The Cleveland Clinic Foundation | Nerve stimulation to promote neuroregeneration |
| EP3490624B1 (en) * | 2016-08-01 | 2022-02-09 | Association for the Advancement of Tissue Engineering and Cell based Technologies & Therapies (A4TEC) - Associação | Nerve guidance conduits, methods of production and uses thereof |
| CN109513041B (zh) * | 2018-12-29 | 2023-10-03 | 南通纺织丝绸产业技术研究院 | 一种镁丝蚕丝复合编织结构神经导管及其制备方法 |
| EP4178635A1 (en) | 2020-07-08 | 2023-05-17 | Newrotex Limited | Bridging peripheral nerve gaps with conduits for enhanced nerve regeneration |
| EP3991762A1 (en) * | 2020-11-02 | 2022-05-04 | Medizinische Hochschule Hannover | Implant for nerve regeneration |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998022155A1 (fr) * | 1996-11-20 | 1998-05-28 | Tapic International Co., Ltd. | Canal rachidien artificiel |
| JP2002369878A (ja) * | 2001-04-13 | 2002-12-24 | Yasuhiko Tabata | 組織の体内再生用材料 |
| JP2004173772A (ja) * | 2002-11-25 | 2004-06-24 | National Institute Of Agrobiological Sciences | 医療用基材としての繭糸構造物及びその製造法 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5019087A (en) * | 1986-10-06 | 1991-05-28 | American Biomaterials Corporation | Nerve regeneration conduit |
| US4963146A (en) * | 1989-04-20 | 1990-10-16 | Colla-Tec Incorporated | Multi-layered, semi-permeable conduit for nerve regeneration |
| US5026381A (en) * | 1989-04-20 | 1991-06-25 | Colla-Tec, Incorporated | Multi-layered, semi-permeable conduit for nerve regeneration comprised of type 1 collagen, its method of manufacture and a method of nerve regeneration using said conduit |
| US5656605A (en) * | 1994-01-26 | 1997-08-12 | Institute Of Molecular Biology, Inc. | Device to promote drug-induced nerve regeneration |
| US5834029A (en) * | 1994-07-20 | 1998-11-10 | Cytotherapeutics, Inc. | Nerve guidance channel containing bioartificial three-dimensional hydrogel extracellular matrix derivatized with cell adhesive peptide fragment |
| CA2334688A1 (en) * | 1998-06-10 | 1999-12-16 | Yasuhiko Shimizu | Artificial tube for nerve |
| US6676675B2 (en) * | 2000-04-19 | 2004-01-13 | Iowa State University Research Foundation, Inc. | Patterned substrates and methods for nerve regeneration |
| US6716225B2 (en) * | 2001-08-02 | 2004-04-06 | Collagen Matrix, Inc. | Implant devices for nerve repair |
| US6902932B2 (en) * | 2001-11-16 | 2005-06-07 | Tissue Regeneration, Inc. | Helically organized silk fibroin fiber bundles for matrices in tissue engineering |
| TWI264301B (en) * | 2002-03-11 | 2006-10-21 | Ind Tech Res Inst | Multi-channel bioresorbable nerve regeneration conduit and preparation method for the same |
| CA2525994C (en) * | 2002-06-24 | 2012-10-16 | Tufts University | Silk biomaterials and methods of use thereof |
-
2005
- 2005-09-08 WO PCT/GB2005/003456 patent/WO2006030182A2/en active Application Filing
- 2005-09-08 EP EP05778571A patent/EP1789103B1/en active Active
- 2005-09-08 US US11/575,268 patent/US8106014B2/en active Active
- 2005-09-08 DE DE602005013979T patent/DE602005013979D1/de active Active
- 2005-09-08 CA CA2580349A patent/CA2580349C/en active Active
- 2005-09-08 AT AT05778571T patent/ATE428453T1/de not_active IP Right Cessation
- 2005-09-08 JP JP2007530763A patent/JP4746046B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998022155A1 (fr) * | 1996-11-20 | 1998-05-28 | Tapic International Co., Ltd. | Canal rachidien artificiel |
| JP2002369878A (ja) * | 2001-04-13 | 2002-12-24 | Yasuhiko Tabata | 組織の体内再生用材料 |
| JP2004173772A (ja) * | 2002-11-25 | 2004-06-24 | National Institute Of Agrobiological Sciences | 医療用基材としての繭糸構造物及びその製造法 |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE428453T1 (de) | 2009-05-15 |
| DE602005013979D1 (de) | 2009-05-28 |
| EP1789103B1 (en) | 2009-04-15 |
| JP2008513051A (ja) | 2008-05-01 |
| US8106014B2 (en) | 2012-01-31 |
| CA2580349C (en) | 2014-06-17 |
| WO2006030182A2 (en) | 2006-03-23 |
| US20090099580A1 (en) | 2009-04-16 |
| EP1789103A2 (en) | 2007-05-30 |
| WO2006030182A3 (en) | 2006-05-04 |
| CA2580349A1 (en) | 2006-03-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4746046B2 (ja) | 末梢神経と神経組織の向上された成長のための方法およデバイス | |
| Fornasari et al. | Natural-based biomaterials for peripheral nerve injury repair | |
| Bozkurt et al. | The role of microstructured and interconnected pore channels in a collagen-based nerve guide on axonal regeneration in peripheral nerves | |
| Chiono et al. | Trends in the design of nerve guidance channels in peripheral nerve tissue engineering | |
| US8652215B2 (en) | Nanofilament scaffold for tissue regeneration | |
| EP0772466B1 (en) | Compositions and methods for a bioartificial extracellular matrix | |
| Chiono et al. | Artificial scaffolds for peripheral nerve reconstruction | |
| Koh et al. | In vivo study of novel nanofibrous intra-luminal guidance channels to promote nerve regeneration | |
| CA1328710C (en) | Composite nerve guidance channels | |
| CN101072593B (zh) | 促进外周神经和神经组织生长的方法及装置 | |
| Donzelli et al. | Role of extracellular matrix components in facial nerve regeneration: an experimental study | |
| US20230310002A1 (en) | Bridging peripheral nerve gaps with conduits for enhanced nerve regeneration | |
| Mey et al. | Electrospun fibers as substrates for peripheral nerve regeneration | |
| Cirillo et al. | 3D conduits for peripheral nerve regeneration | |
| Guarino et al. | Bioinspired scaffolds for bone and neural tissue and interface engineering | |
| Riva et al. | Beyond the limiting gap length: peripheral nerve regeneration through implantable nerve guidance conduits | |
| CN2469906Y (zh) | 周围神经修复用组织工程诱导支架 | |
| Cirillo et al. | 16.1 Pathophysiology of nerve degeneration and regeneration | |
| Eleftheriadou et al. | Collagen Biomaterials for Nerve Tissue Engineering | |
| Blekhman et al. | Polymers and composites for peripheral nerve repair | |
| Kriebel | Construction and biological testing of artificial implants for peripheral nerve repair | |
| Chen et al. | Gelatin-Tricalcium phosphate membrane modified with ngf and cultured schwann cells for peripheral nerve repair: A tissue engineering approach | |
| Mallapragada et al. | Polymeric biomaterials for nerve regeneration | |
| Yannas | Regeneration of a Peripheral Nerve |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080815 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080815 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100215 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100315 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100614 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100621 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100709 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100817 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101215 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110209 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20110228 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110426 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110512 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140520 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4746046 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |