JP4246265B2 - 大便失禁を治療するための医薬組成物 - Google Patents
大便失禁を治療するための医薬組成物 Download PDFInfo
- Publication number
- JP4246265B2 JP4246265B2 JP52855098A JP52855098A JP4246265B2 JP 4246265 B2 JP4246265 B2 JP 4246265B2 JP 52855098 A JP52855098 A JP 52855098A JP 52855098 A JP52855098 A JP 52855098A JP 4246265 B2 JP4246265 B2 JP 4246265B2
- Authority
- JP
- Japan
- Prior art keywords
- phenylephrine
- anal
- patients
- incontinence
- treatment
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 208000034347 Faecal incontinence Diseases 0.000 title claims abstract description 18
- 239000008194 pharmaceutical composition Substances 0.000 title claims 2
- 229960001802 phenylephrine Drugs 0.000 claims description 58
- SONNWYBIRXJNDC-VIFPVBQESA-N phenylephrine Chemical compound CNC[C@H](O)C1=CC=CC(O)=C1 SONNWYBIRXJNDC-VIFPVBQESA-N 0.000 claims description 58
- 238000011282 treatment Methods 0.000 claims description 25
- 150000003839 salts Chemical class 0.000 claims description 14
- 239000003814 drug Substances 0.000 claims description 13
- 230000000699 topical effect Effects 0.000 claims description 9
- 230000000694 effects Effects 0.000 claims description 6
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 claims description 5
- 229960002748 norepinephrine Drugs 0.000 claims description 5
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 claims description 5
- WJAJPNHVVFWKKL-UHFFFAOYSA-N Methoxamine Chemical compound COC1=CC=C(OC)C(C(O)C(C)N)=C1 WJAJPNHVVFWKKL-UHFFFAOYSA-N 0.000 claims description 4
- 239000000695 adrenergic alpha-agonist Substances 0.000 claims description 4
- 229960005192 methoxamine Drugs 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 3
- 238000004519 manufacturing process Methods 0.000 claims description 2
- 239000000464 adrenergic agent Substances 0.000 claims 1
- 239000003937 drug carrier Substances 0.000 claims 1
- 210000000664 rectum Anatomy 0.000 claims 1
- 230000000284 resting effect Effects 0.000 abstract description 30
- 210000000436 anus Anatomy 0.000 abstract description 25
- 210000005072 internal anal sphincter Anatomy 0.000 abstract description 5
- 230000008901 benefit Effects 0.000 abstract description 4
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 abstract description 4
- 210000003205 muscle Anatomy 0.000 abstract description 4
- 238000002271 resection Methods 0.000 abstract description 4
- 229960005181 morphine Drugs 0.000 abstract description 2
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 abstract 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 abstract 2
- PXGPLTODNUVGFL-BRIYLRKRSA-N (E,Z)-(1R,2R,3R,5S)-7-(3,5-Dihydroxy-2-((3S)-(3-hydroxy-1-octenyl))cyclopentyl)-5-heptenoic acid Chemical compound CCCCC[C@H](O)C=C[C@H]1[C@H](O)C[C@H](O)[C@@H]1CC=CCCCC(O)=O PXGPLTODNUVGFL-BRIYLRKRSA-N 0.000 abstract 1
- 229940123921 Nitric oxide synthase inhibitor Drugs 0.000 abstract 1
- 208000003251 Pruritus Diseases 0.000 abstract 1
- 239000002876 beta blocker Substances 0.000 abstract 1
- 229940097320 beta blocking agent Drugs 0.000 abstract 1
- 229960003638 dopamine Drugs 0.000 abstract 1
- 239000000236 nitric oxide synthase inhibitor Substances 0.000 abstract 1
- PXGPLTODNUVGFL-UHFFFAOYSA-N prostaglandin F2alpha Natural products CCCCCC(O)C=CC1C(O)CC(O)C1CC=CCCCC(O)=O PXGPLTODNUVGFL-UHFFFAOYSA-N 0.000 abstract 1
- 210000005070 sphincter Anatomy 0.000 description 30
- 206010021639 Incontinence Diseases 0.000 description 29
- 239000000203 mixture Substances 0.000 description 20
- 229940068196 placebo Drugs 0.000 description 13
- 239000000902 placebo Substances 0.000 description 13
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 12
- 208000024891 symptom Diseases 0.000 description 10
- 210000002255 anal canal Anatomy 0.000 description 9
- 239000006071 cream Substances 0.000 description 9
- 239000004480 active ingredient Substances 0.000 description 8
- 229940079593 drug Drugs 0.000 description 7
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 229920002125 Sokalan® Polymers 0.000 description 6
- 230000003872 anastomosis Effects 0.000 description 6
- 239000000499 gel Substances 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 230000006378 damage Effects 0.000 description 5
- 239000002674 ointment Substances 0.000 description 5
- 238000001356 surgical procedure Methods 0.000 description 5
- 241000282414 Homo sapiens Species 0.000 description 4
- 230000002159 abnormal effect Effects 0.000 description 4
- 230000017531 blood circulation Effects 0.000 description 4
- 239000012188 paraffin wax Substances 0.000 description 4
- 239000003755 preservative agent Substances 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 230000005856 abnormality Effects 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 210000003503 anal sac Anatomy 0.000 description 3
- 229960001631 carbomer Drugs 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000003995 emulsifying agent Substances 0.000 description 3
- 230000003511 endothelial effect Effects 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 230000002335 preservative effect Effects 0.000 description 3
- 238000002604 ultrasonography Methods 0.000 description 3
- 206010068172 Anal pruritus Diseases 0.000 description 2
- 206010009866 Cold sweat Diseases 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 239000000048 adrenergic agonist Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 210000005071 external anal sphincter Anatomy 0.000 description 2
- 230000002550 fecal effect Effects 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 238000000034 method Methods 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 230000035515 penetration Effects 0.000 description 2
- 229960003733 phenylephrine hydrochloride Drugs 0.000 description 2
- OCYSGIYOVXAGKQ-FVGYRXGTSA-N phenylephrine hydrochloride Chemical compound [H+].[Cl-].CNC[C@H](O)C1=CC=CC(O)=C1 OCYSGIYOVXAGKQ-FVGYRXGTSA-N 0.000 description 2
- 229940074583 phenylephrine ophthalmic solution Drugs 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000002203 pretreatment Methods 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 229940100611 topical cream Drugs 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- DKSZLDSPXIWGFO-BLOJGBSASA-N (4r,4ar,7s,7ar,12bs)-9-methoxy-3-methyl-2,4,4a,7,7a,13-hexahydro-1h-4,12-methanobenzofuro[3,2-e]isoquinoline-7-ol;phosphoric acid;hydrate Chemical compound O.OP(O)(O)=O.OP(O)(O)=O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC DKSZLDSPXIWGFO-BLOJGBSASA-N 0.000 description 1
- IQXJCCZJOIKIAD-UHFFFAOYSA-N 1-(2-methoxyethoxy)hexadecane Chemical compound CCCCCCCCCCCCCCCCOCCOC IQXJCCZJOIKIAD-UHFFFAOYSA-N 0.000 description 1
- AXTGDCSMTYGJND-UHFFFAOYSA-N 1-dodecylazepan-2-one Chemical compound CCCCCCCCCCCCN1CCCCCC1=O AXTGDCSMTYGJND-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 1
- 208000004998 Abdominal Pain Diseases 0.000 description 1
- 208000019901 Anxiety disease Diseases 0.000 description 1
- LRMCSRVUZMPTGZ-UHFFFAOYSA-N CC=1C(=C(C(=O)O)C=CC1)O.C(C(C)O)O Chemical compound CC=1C(=C(C(=O)O)C=CC1)O.C(C(C)O)O LRMCSRVUZMPTGZ-UHFFFAOYSA-N 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 206010010774 Constipation Diseases 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 235000009161 Espostoa lanata Nutrition 0.000 description 1
- 240000001624 Espostoa lanata Species 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010029216 Nervousness Diseases 0.000 description 1
- 206010033557 Palpitations Diseases 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 206010036772 Proctalgia Diseases 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 206010039203 Road traffic accident Diseases 0.000 description 1
- 206010040880 Skin irritation Diseases 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 230000003187 abdominal effect Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000000533 adrenergic alpha-1 receptor agonist Substances 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 238000002266 amputation Methods 0.000 description 1
- 229940035674 anesthetics Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000036506 anxiety Effects 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 230000003416 augmentation Effects 0.000 description 1
- 230000002567 autonomic effect Effects 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 238000009530 blood pressure measurement Methods 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 210000001217 buttock Anatomy 0.000 description 1
- CNYFJCCVJNARLE-UHFFFAOYSA-L calcium;2-sulfanylacetic acid;2-sulfidoacetate Chemical compound [Ca+2].[O-]C(=O)CS.[O-]C(=O)CS CNYFJCCVJNARLE-UHFFFAOYSA-L 0.000 description 1
- 229940031663 carbomer-974p Drugs 0.000 description 1
- 229950009789 cetomacrogol 1000 Drugs 0.000 description 1
- 230000035606 childbirth Effects 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 229960004415 codeine phosphate Drugs 0.000 description 1
- 238000012321 colectomy Methods 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 238000001246 colloidal dispersion Methods 0.000 description 1
- 230000000112 colonic effect Effects 0.000 description 1
- 230000009989 contractile response Effects 0.000 description 1
- 238000011443 conventional therapy Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 239000000850 decongestant Substances 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- NIJJYAXOARWZEE-UHFFFAOYSA-N di-n-propyl-acetic acid Natural products CCCC(C(O)=O)CCC NIJJYAXOARWZEE-UHFFFAOYSA-N 0.000 description 1
- 208000010643 digestive system disease Diseases 0.000 description 1
- 230000000916 dilatatory effect Effects 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000004945 emulsification Methods 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- -1 for example Chemical class 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000003193 general anesthetic agent Substances 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 238000009775 high-speed stirring Methods 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 206010022000 influenza Diseases 0.000 description 1
- 230000030214 innervation Effects 0.000 description 1
- 230000008991 intestinal motility Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 229940045996 isethionic acid Drugs 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000008141 laxative Substances 0.000 description 1
- 229940125722 laxative agent Drugs 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- RDOIQAHITMMDAJ-UHFFFAOYSA-N loperamide Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(C(=O)N(C)C)CCN(CC1)CCC1(O)C1=CC=C(Cl)C=C1 RDOIQAHITMMDAJ-UHFFFAOYSA-N 0.000 description 1
- 229960001571 loperamide Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- 230000002911 mydriatic effect Effects 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 229940054534 ophthalmic solution Drugs 0.000 description 1
- 239000002997 ophthalmic solution Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- KHPXUQMNIQBQEV-UHFFFAOYSA-N oxaloacetic acid Chemical compound OC(=O)CC(=O)C(O)=O KHPXUQMNIQBQEV-UHFFFAOYSA-N 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 210000003903 pelvic floor Anatomy 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 230000002980 postoperative effect Effects 0.000 description 1
- VJZLQIPZNBPASX-OJJGEMKLSA-L prednisolone sodium phosphate Chemical compound [Na+].[Na+].O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)COP([O-])([O-])=O)[C@@H]4[C@@H]3CCC2=C1 VJZLQIPZNBPASX-OJJGEMKLSA-L 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 150000004040 pyrrolidinones Chemical class 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000007467 rectal resection Methods 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000036556 skin irritation Effects 0.000 description 1
- 231100000475 skin irritation Toxicity 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 229940084026 sodium valproate Drugs 0.000 description 1
- AEQFSUDEHCCHBT-UHFFFAOYSA-M sodium valproate Chemical compound [Na+].CCCC(C([O-])=O)CCC AEQFSUDEHCCHBT-UHFFFAOYSA-M 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000012549 training Methods 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/557—Eicosanoids, e.g. leukotrienes or prostaglandins
- A61K31/5575—Eicosanoids, e.g. leukotrienes or prostaglandins having a cyclopentane, e.g. prostaglandin E2, prostaglandin F2-alpha
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/223—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin of alpha-aminoacids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/4045—Indole-alkylamines; Amides thereof, e.g. serotonin, melatonin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/485—Morphinan derivatives, e.g. morphine, codeine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/557—Eicosanoids, e.g. leukotrienes or prostaglandins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
Landscapes
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Emergency Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Physical Education & Sports Medicine (AREA)
- Neurology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Dermatology (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Cephalosporin Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Plant Substances (AREA)
Description
【0001】
本発明は、特に大腸切除や吻合術を受けた患者における大便失禁を治療するかまたは軽減させることに係る。
【背景技術】
【0002】
肛門または大便失禁とは、大便またはガスを自由意志で肛門を通過させることが出来ないことをいうのであって、大便汚損としてまたは稀なエピソード症状であるがガス若しくは水様便としての何れかの形状で生起する。何れにしても極めて悲惨で、つらい症状であり、自己課外した社会的孤立や絶望に到る可能性がある。
【0003】
大便失禁に対する従来の治療法としては、大便の軟度を改善するための薬物治療、例えば腸の運動性を低減させるためのモルヒネ、ロペルアミドやリン酸コデイン、また大便を柔らかくして便秘を軽減する緩下剤などがある。バイオフィードバック訓練は、もう一つの治療法であって、肛門管の安静時圧力や圧出圧力を改善し、また肛門管機能の持つ対称性を教えるための種々の筋肉増強運動を含むものである。しかしながら、最も普通の治療形態は、外科的修復術であり、例えば肛門の他の部位からの筋肉移植からなる新括約筋形成術、即ち結腸造瘻術が挙げられる(Gastroenterology in Practice、Summer 1995、p18-21; Dig Dis 1990;8:179-188;およびThe New England Journal of Medicine、April 1992、p1002-1004)。肛門漏出の中程度の症例においては、患者は、綿ボールを詰めて肛門に栓をするよう試みることが多い。
【0004】
Gut、1991、32、p.345-346において、特発性大便失禁の患者のうちの三分の二は、内部括約筋機能が異常であるため生じた肛門安静時圧力が低下している旨の報告がなされている。多くの失禁患者においては、肛門内部の括約筋が異常な程に薄くなっており、また他方では肛門外部の括約筋の損傷が認められている。
【0005】
肛門内部の括約筋のノルアドレナリンに対するインビトロでの収縮応答が、失禁においては低下していることもまた報告されている(Br. J. Surg. 1992、vo1. 79、August、p829-832; Digestive Diseases and Sciences、vpl.38、no.11、Nov.1993、p.1961-1969)。肛門内部の括約筋の神経支配と制御および健常な肛門の安静時圧力を増加または低下させる医薬についてさらに詳細な検討が、教科書であるColoproctology and the PelvicFloor(Butterwaorths)、second edition、1992、第3章、p37-53;Autonomic Control of Internal Anal Sphincter;およびJournal of Clinical Investigation 1990、86: 424-429においてなされている。
【0006】
Surgery 1990; 107: p311-315において、バルプロ酸ナトリウムが、直腸肛門吻合術後のマイナーな失禁症の治療に有用であることが報告されている。
【発明の開示】
【発明が解決しようとする課題】
【0007】
ところで驚くべきことに、大便失禁が、α−アドレナリン作動薬で局所的に治療することによって解消することが出来ることが見出されたのである。
【0008】
このことは、これまでは肛門括約筋が一旦正常に機能し始めると、患者は大手術を必要とすることになると見なされてきたことに鑑みてまさに驚くべきことである。
【0009】
かくして、肛門漏出は、患者は大手術を受けることなく低減されるか解消されるのである。
【課題を解決するための手段】
【0010】
従って本発明の第一の曲面において、大便失禁の治療または予防のために局所適用する医薬を製造するための、フェニレフリン、ノルアドレナリン、メトキサミンおよびその薬理学的に受容可能な塩から選択されるα−アドレナリン作動薬の使用が提供される。
【発明の効果】
【0011】
本発明の薬剤は、肛門内部の括約筋の安静時圧力を増加させることによって少なくとも部分的に失禁を治療するように思われる。
【発明を実施するための最良の形態】
【0012】
適当なα1−アドレナリン作動薬の例は、ノルアドレナリン、メトキサミンであるが、特に好ましいのは、フェニレフリンである。
【0013】
かかる医薬品は、単一の有効薬剤または上記した有効薬剤のうちの如何なる組合せを含有していてもよい。
【0014】
フェニレフリン(α1アドレナリン作動剤の一つであるが)は、眼科においては散瞳薬として使用され、また例えば風邪やインフルエンザ治療薬においてうっ血除去薬として使用されている。
【0015】
しかしながら、本発明者らの知る限りにおいては、これらの有効薬剤を大便失禁を治療するために局所使用する示唆は、これまでに一切なされたことはなかった。
【0016】
本明細書において使用する”大便失禁”には、あらゆる種類の肛門漏出が含まれ、マイナー漏出、即ち”汚れ”、から中程度の漏出を経て大便失禁のメジャーな事例に到るまでの全てを含み、また神経性、活動性、切迫性や受動性失禁が含まれる。
【0017】
さらに具体的には、本発明から最も便宜を受けるであろう失禁患者のタイプは、特発性失禁患者や肛門内部または肛門外部の括約筋の何れかの弱さが少なくとも原因の一部である失禁患者、特に最大肛門圧力が正常であるかまたは低く、肛門内部の括約筋が構造的に無傷である患者、例えば括約筋が異常に薄い患者である。しかしながら、例えば括約筋の切断などのマイナーな構造的損傷を持った患者もやはり、本発明から恩恵を受けるであろう。肛門内部の括約筋が損傷されているかまたは異常である失禁患者だけでなくまた外部括約筋が損傷されているかまたは異常である患者も、治療を受けることが可能である、その理由は、本発明によって誘発された肛門内部の安静圧力の増加が、外部括約筋の不充分な機能を補償するからである。
【0018】
本発明から特に便益を受ける患者の別の種類は、メジャーな大腸切除や肛門吻合術を受けたことのある術後患者である。例えば、直腸肛門吻合術(修復的直腸結腸切除術)、肛門結腸(結腸肛門嚢を伴うかまたは伴わない)吻合術、前下部切除術および回腸直腸吻合術を伴う直腸切除術を受けた患者である。
【0019】
括約筋への損傷は、例えば出産時、外科手術または街路交通事故に際して蒙る外傷によって生じ可能性がある。更には、原発性の肛門内部の変性退化によって惹起される失禁も、本発明によって軽減緩和することが可能であるものと信じられる。
【0020】
肛門漏出はまた、肛門掻痒症を引き起こすことになり、かかる漏出を低減させるかまたは無くすことによって、肛門掻痒症も軽減されるかまたは予防防止されることになる。
【0021】
更には、肛門の安静時圧力が上昇した結果、患者はもはや、肛門括約筋が拡張したという不快感を持つことはなくなるのである。
【0022】
上記有効成分の生理学的に受容可能な塩も、本発明の範囲に含まれる。適した塩としては、有機および無機の酸、例えば塩酸、臭化水素酸、硫酸、クエン酸、酒石酸、リン酸、乳酸、ピルビン酸、酢酸、三フッ化酢酸、コハク酸、シュウ酸、フマール酸、マレイン酸、オキザロ酢酸、メタンスルホン酸、エタンスルホン酸、p−トルエンスルホン酸、ベンゼンスルホン酸およびイセチオン酸などと形成される塩が挙げられる。
【0023】
塩なる用語によって、本発明者らはまた、錯塩または擬酸との塩をも含むものと意図するのであるが、ここにおいてかかる有効成分(例えばフェニレフリンなど)は、例えば有機または無機の酸の誘導体と関連づけられる。
【0024】
生体内において有効成分(例えばフェニレフリンなど)に転換されるプロドラッグおよび他の生物前駆体も、本発明の範囲に含まれる。
【0025】
フェニレフリンの特に好ましい塩は、塩酸塩である。
【0026】
大便失禁は、大便失禁患者の肛門管の内部および/またはその内部に本医薬品を局所適用または局所外用することによって治療処置する。少なくとも一種の生理学的に受容可能なキャリアーが有効成分とともに存在し、含まれるであろう。
【0027】
かかる組成物は、軟膏、クリーム、分散液、ローション、粉体、溶液、ペースト、ゲル、スプレー、フォーム又はオイルなどに製剤してもよい。
【0028】
かかる組成物は、乳化剤、防腐剤、緩衝剤や抗酸化剤を含んでなっていてもよい。好ましくは、かかる組成物はまたステロイド類や局所的に作用する麻酔剤を含んでいてもよい。
【0029】
かかる組成物の投薬量は、大便失禁の重危度または治療する患者の年齢、体重や症状に依存して異なる。
【0030】
例えばフェニレフリンなど有効成分の百分率は、好ましくは少なくとも組成物の5%w/w、より好ましくは少くとも10%w/wであり、有利にはほぼ50%w/wである。フェニレフリンなどの有効成分の投与量は、好ましくは組成物0.5ml当り少なくとも40mg、より好ましくは組成物0.5ml当り少なくとも50mgであり、例えばほぼ250mg/0.5mlまでである。事実、初期の検討の結果から、投与量が高ければ、肛門括約筋の感受性が正常以下であるのでそれだけ好便であることが判っている。局所組成物(例えばチューブ)中に含まれる有効成分の全量は、適当には40ないし5000mgであり、例えば40mgないし1000mg、または40ないし500mgである。かかる局所組成物は、大便失禁からの回復が実現されるまで一日当り1回ないし6回であり、例えば一日当り3回である。
【0031】
かかる局所組成物は、皮膚浸透剤、特に例えばジメチルスルホキシド(DMSO)などのスルホキシド類を25%ないし50%w/wまでの量を含んでなっていてもよい。アミド類(DMA、DMF)、ピロリドン類、有機溶媒、ラウロカプロム(AZONE)およびチオグリコール酸カルシウムが、好ましい代替浸透剤である。かかる組成物はまた、選択的にはポリアクリル酸誘導体、より具体的にはカルボマーを含有していてもよい。このものは、薬剤の浸透を促進する皮膚湿潤剤としてまた乳化剤として機能する。カルボマーは、DMSOの乳化を促進し、かくして皮膚刺激を緩和しかつ皮膚湿潤を高める。プロピレングリコールも、皮膚を軟化させ、熱力学的ポテンシャルを高めかつDMSOの、従って医薬の皮膚浸透を促進させるために当該組成物中に存在させてもよい。かかる組成物の最終pHは、有利にはpH3.5ないし4.5である。
【実施例1】
(本発明外の組成物)
【0032】
プロトコール
市販の10%フェニレフリン塩酸塩(Minims)点眼液の製剤品を左側臥位の被験者の肛門に投与した。投与量は、フェニレフリン溶液の容量およびフェニレフリンのミリグラム数の双方として表してある。フェニレフリンの点眼液を肛門内に投与使用するに先立って、黄色軟質パラフィンを用いて作製したフェニレフリン軟膏製剤を肛門周囲に塗布したが、投与量としてほぼ500mgの10%軟膏(フェニレフリンとして50mg)を塗布するまでは効果が全くないことが判明した。このことは恐らくは、経皮吸収が行われなかったことを表すものであり、その後はフェニレフリン点眼液だけを肛門内部に滴注した。
【0033】
水を満たしたマイクロバルーンシステムをプラスチックスの硬質カテーテルとトランスジューサーとに接続し、次いでペンチャート記録形に接続したものを使用して、マノメトリー(肛門の最大安静時圧力を測定するための)を実施した。肛門の最大安静時圧力は、ステーションプルスルー技法(Station pull through technique)を用いて決定した。カテーテルを臀部にテープ留めして、肛門圧力が安定するまで、連続して圧力の読み取りを行った。医薬品を投与した後は、連続して圧力の読み取りを15ないし31分間行った。心拍数と血圧とをモニターし、被験者に対して頭痛、不安、動悸および腹痛または肛門痛の有無を質問した。
【0034】
単一ボランティアにおける用量作用の研究
10%フェニレフリン溶液を0.9%の生理食塩水で逐次希釈し、標準投与量として0.5mlを単一の健常なボランティアに投与した。1%で始めて、フェニレフリンの濃度を上げたものを、肛門の安静時圧力が上昇するまで異なる日に投与した。この単一のボランティアだけで作用時間を判定するために、マノメトリーを13時間で反復繰り返した。
【0035】
0.5mlの0.1%(0.5mg)、0.5%(2.5mg)、1%(5mg)または5%(25mg)のフェニレフリンを投与しても、最大安静時圧力は有意に上昇しなかった。0.5mlの10%フェニレフリン(50mg)を肛門管に滴注した場合、安静時圧力は120から210cmH2O(12−21KPa)まで上昇した。このような肛門の安静時圧力の上昇は、25分間の連続記録から明かであったが、13時間後には治療・処置前の数値に戻った。
【実施例2】
(本発明外の組成物)
【0036】
健常なボランティア群
10人の健常なボランティア(5人の男性)に対して実施例1に記載した10%フェニレフリン(50mg)を0.5ml肛門内投与した。平均年齢は26才(22−37才の範囲)であった。これらのボランティアの誰も、これまでに肛門失禁の症状を呈したことはなく肛門外科手術を受けたこともなかった。また女性は未経産であり、従って肛門の内部および外部括約筋に異常はないものと想定された。フェニレフリン投与前の平均安静時圧力は、110cmH2O(11KPa)(範囲45−125cmH2O;4.5−12.5KPa)であった。
【0037】
0.5mlの10%フェニレフリン(50mg)を投与した後、最高安静時圧力は180cmH2O(17.5KPa)(範囲は120−210cmH2O;12−20.5KPa)(p<0.05、Wilcoxon sign rank test)にまで有意に上昇した(第1図)。このように上昇した圧力は、記録時間の間、平均23分間(範囲は14−31分)維持された。
【実施例3】
【0038】
ベースゲルの組成は下記のようであった:
カルメルロースナトリウム 6g、ポリエチレングリコール 30ml、メチルヒドロキシ安息香酸塩 150mg、プロピルヒドロキシ安息香酸塩 15mg、所定量に必要な蒸留水(pH4)。
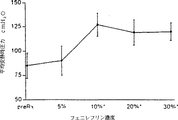
種々の量のフェニレフリンを5%、10%、29%および30%(w/w)となるよう添加し、至適用量決定研究を行うための種々の組成物を製造した(図2)。
【実施例4】
【0039】
本発明のベースクリームは、以下の組成のものであった:
ジメチルスルホキシド 250g
カルボマー974P 5g
白色軟質パラフィン 15g
セトマクロゴール乳化性軟膏* 11g
プロピレングリコール 23g
メチルヒドドロキシ安息香酸塩(防腐溶液) 所定量
このものに、10%w/wのフェニレフリン塩酸塩を添加した。
注記 *:組成は、白色軟質パラフィン50g、液体パラフィン20g、セトマクロゴール乳化性ワックス30g(セトステリルアルコール24gおよびセトマクロゴール1000が6g)であった。
【0040】
ベースクリームは、先ずクリームの水性成分と非水性成分とを別々に混合して作成した。プロピレングリコールの秤量重量と防腐溶液の一部をビーカーに入れ、カルボマー粉体の秤量重量をインペラー型混合装置を使用しながら添加して、カルボマーのコロイド状分散液を作成した。次いで、DMSOを秤量重量だけ添加し、半透明状のゲルが形成されるまで室温で高速攪拌を継続した。
【0041】
その間、それぞれ秤量した重量の白色軟質パラフィンとセタマクロゴール乳化性軟膏を別のビーカーに入れ、融点にまで加熱し、緩やかに攪拌して均質一様なベースを得た。
【0042】
医薬を次いで防腐溶液の残部に添加し、このものをゲルに加え、激しく攪拌しつつ均質ベース(上記)を添加してクリームを作成した。カルボマーは、中和剤および一次乳化剤(オイルと水性相との)としての二つの機能を果たし、均質一様なクリームベースを形成するものであった。
【実施例5】
【0043】
年齢が21才ないし53才(平均35才)である12人の健常なボランティアを四つの事例の検討に供した。肛門括約筋の安静時圧力と肛門管内皮血流(レーザ−ドップラーフローメータを使用)を、実施例3において作成した、濃度を高めた種々のフェニレフリンゲル(Slaco Pharma(UK)Ltd.から販売)を肛門に局所外用する前後において測定した。単回投与した後は終日目盛りを読み取り、効果の持続性を決定した。
【0044】
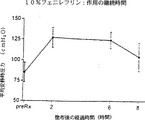
図2から明らかなように、肛門括約筋の平均安静時圧力(MRP)は処置前の肛門括約筋圧力と比較して、5%フェニレフリン塗布後においては若干(6%)上昇し(p<0.04)また10%フェニレフリンを用いた場合臨床的に有意な33%の上昇が認められた(85±12対127±12cmH2O、処置前対処置後、MRP。p<0.0001)−図3を参照。その後、フェニレフリンの濃度を上げても加成性の応答は一切認められなかった。10%フェニレフリンを単回投与適用した場合の効果時間は、平均7時間(範囲6ないし8時間)であった。肛門管内皮血流については、観察可能な変化は一切記録されなかった。その後10%フェニレフリンゲルを局所塗布したところ、健常なボランティアの肛門括約筋の安静時圧力が有意に上昇した。
【実施例6】
(本発明外の組成物)
【0045】
患者群
10人の患者(3人の男性)に対しても実施例1に記載した10%フェニレフリン0.5ml(50mg)を肛門内投与した。平均年齢は45才(27−76才の範囲)であった。患者は全て、これまでに切迫肛門失禁を伴うかまたは伴わない受動性失禁の症状を呈していた。患者は、受動性大便失禁を基準として選択したが、受動性大便失禁は、肛門内部括約筋に関連性を有するものと知られている。かかる治療が、構造的分断の患者または単なる肛門内部括約筋の薄化を伴う患者において有効であるか否かを決定するために、それぞれのタイプの患者を5人ずつ集めた。
【0046】
フェニレフリン治療前の平均安静時圧力は、25cmH2O(2.5KPa)(範囲は20−100cmH2O;2−10KPa)であった。肛門管内皮の超音波検査の結果、全ての患者において肛門内部括約筋の異常が認められた。患者の半数は、構造的分断があり、一方他の5人の患者は、正常であったが異常に薄いものであった(1mm以下)。7人の患者は、肛門外部括約筋にも若干の構造的損傷を受けていたが、3人の患者は、その周囲に損傷はなかった。
【0047】
0.5mlの10%フェニレフリン(50mg)を肛門内に注入した場合、平均最高安静時圧力は、55cmH2O(5.5KPa)(範囲は20−80cmH2O;2−8KPa)(p=0.39、Wilcoxon sign rank test)(図5を参照)にまで上昇した。7人の患者は、肛門圧力が上昇したが、2人は下降し、1人の患者は変化が認められなかった。肛門括約筋が断片化していて、構造的には損傷がないものの薄化した患者においては、安静時圧力が上昇した、治療前の安静時圧力は、フェニレフリンへの応答・作用を予見できなかった。
【0048】
失禁患者の圧力上昇は、それほど一貫性があるわけではなくまた健常ボランティアにおける程顕著ではないが、それでもなお驚くべきであり、失禁を治療することにおいて治療上貴重である。大便失禁患者の安静時肛門圧力の上昇が低いことは、かかる症状について凝れまでに知られている病理学を勘案すれば説明することができる。受動性大便失禁患者は、肛門内部括約筋の線維化とコラーゲン置換が増大している。従って、肛門の安静時圧力のフェニレフリンによる絶対的上昇は、対照被験者と比較して応答患者においてはそれほど顕著ではないものの、受動性大便失禁の非外科手術滴治療における大きな進歩である。患者の中にはフェニレフリンに応答しない者もいたが、これは、肛門括約筋が構造的に異常であるかまたは感受性が変化したことに因るのであろう。このような患者は、恐らくは安静時肛門圧力を増大させるには投与量を増やす必要があるであろう。
【実施例7】
【0049】
無作為抽出プラセボ対照交差臨床実験を実施して、特発性受動大便失禁を治療するために10%フェニレフリン局所クリーム(実施例3および4において作成した)を使用することを評価した。
【0050】
30人の患者がこの治験を完了した。患者は全て治験前に、肛門内部超音波検査および肛門直腸病理学(最大安静時肛門圧力を測定するため)ならびにレーザードップラーフローメトリによって診察評価した。後者二つの方法による測定を、有効成分(フェニレフリン10%)についての3週間の治験の後で繰り返し、プラセボの”失禁スコアー”を、それぞれの治療の前後で算出する。
【0051】
研究の対象となった30人の患者のうち、3人(10%)は、フェニレフリン処置後に治療前のベースラインとプラセボと比較して症状が有意に客観的に改善した。3人とも年齢が55ないし64才(平均59才)である女性であり、治療前では肛門括約筋の安静時圧力は低い/正常であり、超音波検査では肛門括約筋は構造的に正常であった。肛門直腸マノメトリを行ったところ、10%フェニレフリン投与後においても平均安静時圧力は有意に変化がなかった(62から58cmH2O,フェニレフリン投与の前後で)。同様に、プラセボ投与後においても圧力は有意の変化が一切認められなかった。失禁スコアーは、平均14から平均10にまで改善した。フェニレフリンまたはプラセボ投与後でも、肛門管内皮血流にも有意の変化は一切認められなかった。
【0052】
要約すれば、特発性大便失禁の患者の3/30は、10%フェニレフリンクリームを局所塗布した後では症状を客観的に改善し、失禁スコアーの改善も認められた。
【実施例8】
【0053】
無作為抽出プラセボ対照交差臨床実験を実施して、回腸肛門嚢患者の大便失禁を治療するために10%フェニレフリン局所クリーム(実施例2aおよび3において作成した)を使用することを評価した。
【0054】
12人の患者がこの治験に参加登録し、そのうち10人が治験を完了した。10人の患者は、主として夜間失禁の障害を持ち、2人は昼間および夜間失禁を抱えていた。
【0055】
治験を完了した10人のうち、7人が女性でありまた3人が男性であり、年齢範囲は(34−67才)であった。全ての患者について肛門直腸マノメトリを行いまたレーザー・ドップラー・フローメトリを実施した。また失禁スコアを算定した。これらの測定は全て、二種類の治験クリーム(フェニレフリンおよびプラセボ)による治療を行った後でも繰り返した。
【0056】
6/10(60%)の患者は、プラセボと比較してフェニレフリン10%で症状の有意な改善を示した。このことは、フェニレフリン治療においてこれらの患者は、平均肛門括約筋安静時圧力が上昇したこととよく相関していたが、プラセボ治療後ではそうではなかった(ベースラインと比較してフェニレフリン投与後は29%の上昇したが、プラセボでは8%の上昇であった。p<0.005)。失禁スコアは、フェニレフリン投与後では平均45%の改善が見られたが、プラセボ投与後では3%の改善であった。肛門管内皮血流の相違は認められなかった。患者の報告した症状の平均客観的改善度は、フェニレフリン投与後では83%であり、またプラセボ投与後では14%であった(p<0.01)。
【0057】
一人の患者では、肛門括約筋の圧力が測定可能な上昇を示さなかったが、プラセボ投与後と比較してフェニレフリン投与後では失禁スコアは47%改善し、自覚症状は75%良くなった。3/10の患者は改善しなかった。
【0058】
要約すれば、開口肛門嚢患者の7/10は、10%フェニレフリンクリームを局所塗布した場合失禁症状が改善されたが、その内6人は客観的な改善、即ち肛門括約筋の圧力測定が可能となった。
【図面の簡単な説明】
【0059】
本発明を次に、添付した図面を参照して例として以下に記述説明するが、添付図面において:
図1は、10%フェニレフリン(50mg)の0.5mlを健康なボランティアの肛門内部に塗布した場合の肛門の最高安静時圧力のグラフを表す;
図2は、健康なボランティアにおけるフェニレフリンの投与量依存グラフを表す(preRx=治療前;MRP+/−1SD);
図3は、10%フェニレフリン(50mg)の0.5mlを塗布する前後における健康なボランティアでの肛門の最高圧力のグラフを表す;
図4は、10%フェニレフリンの作用の継続時間のグラフを表す;
図5は、10%フェニレフリン(50mg)の0.5mlを受動的大便失禁患者10人の肛門内部に塗布した場合の肛門の最高安静時圧力のグラフを表す。
Claims (6)
- 大便失禁の治療または予防のために局所適用する医薬を製造するための、フェニレフリン、ノルアドレナリン、メトキサミンおよびその薬理学的に受容可能な塩から選択されるα−アドレナリン作動薬の使用。
- 該α−アドレナリン作動薬が、フェニレフリンとその薬理学的に受容可能な塩から選択されるものである請求項1記載の使用。
- 薬理学的に受容可能な担体と共に、フェニレフリン又はその薬理学的に受容可能な塩が少なくとも5%w/w含有されている、大便失禁の治療のために直腸へ局所塗布適用する、局所作用する医薬組成物。
- 該フェニレフリン又はその薬理学的に受容可能な塩が、少なくとも10%w/w含有されている請求項3記載の組成物。
- 大便失禁の治療または予防のために局所適用するための、フェニレフリン、ノルアドレナリン、メトキサミンおよびその薬理学的に受容可能な塩から選択されるα−アドレナリン作動薬を含有する医薬。
- 該α−アドレナリン作動薬が、フェニレフリンとその薬理学的に受容可能な塩から選択されるものである請求項5記載の医薬。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB9626750.5 | 1996-12-23 | ||
| GBGB9626739.8A GB9626739D0 (en) | 1996-12-23 | 1996-12-23 | Pharmaceutical composition for treating anal incontinence |
| GB9626739.8 | 1996-12-23 | ||
| GBGB9626750.5A GB9626750D0 (en) | 1996-12-23 | 1996-12-23 | Pharmaceutical composition for treating anal incontinence |
| GB9703309.6 | 1997-02-18 | ||
| GBGB9703309.6A GB9703309D0 (en) | 1997-02-18 | 1997-02-18 | Pharmacuetical composition for treating anal incontinence |
| PCT/GB1997/003525 WO1998027971A1 (en) | 1996-12-23 | 1997-12-23 | Pharmaceutical composition for treating fecal incontinence and anal itch |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2001507020A JP2001507020A (ja) | 2001-05-29 |
| JP4246265B2 true JP4246265B2 (ja) | 2009-04-02 |
Family
ID=27268647
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP52855098A Expired - Fee Related JP4246265B2 (ja) | 1996-12-23 | 1997-12-23 | 大便失禁を治療するための医薬組成物 |
Country Status (11)
| Country | Link |
|---|---|
| US (3) | US6635678B1 (ja) |
| EP (1) | EP0946155B2 (ja) |
| JP (1) | JP4246265B2 (ja) |
| AT (1) | ATE320796T1 (ja) |
| AU (1) | AU728889C (ja) |
| CA (1) | CA2275663C (ja) |
| DE (1) | DE69735552T3 (ja) |
| DK (1) | DK0946155T4 (ja) |
| ES (1) | ES2259806T5 (ja) |
| PT (1) | PT946155E (ja) |
| WO (1) | WO1998027971A1 (ja) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6156780A (en) * | 1996-10-17 | 2000-12-05 | Milkhaus Laboratory, Inc. | Treatment of fecal incontinence |
| AU728889C (en) * | 1996-12-23 | 2001-08-02 | S.L.A. Pharma Ag | Pharmaceutical composition for treating fecal incontinence and anal itch |
| KR20010093828A (ko) * | 1998-12-14 | 2001-10-29 | 셀러지 파마세우티칼스, 인크 | 항문직장 질환 치료용 조성물 및 치료 방법 |
| US6627632B2 (en) | 1998-12-14 | 2003-09-30 | Cellegy Pharmaceuticals, Inc. | Compositions and methods for the treatment of anorectal disorders |
| GB0030580D0 (en) * | 2000-12-15 | 2001-01-31 | Medicare Man Consultancy Ltd | Composition and method |
| GB0130763D0 (en) * | 2001-12-21 | 2002-02-06 | Norgine Res Ltd | Treatment methods |
| CN1610552A (zh) * | 2002-02-22 | 2005-04-27 | 大正制药株式会社 | 止痒剂 |
| US20040266880A1 (en) * | 2002-02-22 | 2004-12-30 | Fumie Sato | Antipruritics |
| US7737182B2 (en) * | 2002-08-09 | 2010-06-15 | Taisho Pharmaceutical Co., Ltd. | Pharmaceuticals for xerosis |
| AU2003254850B2 (en) * | 2002-08-09 | 2008-05-15 | Fumie Sato | Antipruritic agent |
| AU2003301900A1 (en) * | 2002-11-13 | 2004-06-03 | Fumie Sato | Antipruritic drug |
| US8648213B2 (en) * | 2004-10-06 | 2014-02-11 | Allergan, Inc. | Prostamides for the treatment of glaucoma and related diseases |
| AU2012202731B2 (en) * | 2005-06-17 | 2014-06-19 | Wisconsin Alumni Research Foundation | Topical vasoconstrictor preparations and methods for protecting cells during cancer chemotherapy and radiotherapy |
| AU2016202290B2 (en) * | 2005-06-17 | 2017-10-05 | Wisconsin Alumni Research Foundation | Topical vasoconstrictor preparations and methods for protecting cells during cancer chemotherapy and radiotherapy |
| EP1890732B1 (en) | 2005-06-17 | 2018-03-28 | Wisconsin Alumni Research Foundation | Topical vasoconstrictor preparations and methods for protecting cells during cancer chemotherapy and radiotherapy |
| AU2014202738B2 (en) * | 2005-06-17 | 2016-05-12 | Wisconsin Alumni Research Foundation | Topical vasoconstrictor preparations and methods for protecting cells during cancer chemotherapy and radiotherapy |
| US7553273B2 (en) | 2006-05-01 | 2009-06-30 | Duodyn Technology, Llc | Apparatus and method for managing incontinence |
| US7828715B2 (en) | 2006-06-29 | 2010-11-09 | Ams Research Corporation | Method of treating anal incontinence |
| WO2008085825A1 (en) * | 2007-01-03 | 2008-07-17 | Ams Research Corporation | Methods for installing sling to treat fecal incontinence, and related devices |
| PE20091084A1 (es) * | 2007-12-07 | 2009-07-23 | Schering Plough Healthcare | Formulaciones farmaceuticas de fenilefrina y composiciones para absorcion transmucosal |
| US20090156891A1 (en) * | 2007-12-12 | 2009-06-18 | Ams Research Corporation | Prolapse and Perineal Repair Concepts |
| US8993630B2 (en) | 2008-11-10 | 2015-03-31 | Bayer Intellectual Property Gmbh | Substituted sulphonamido phenoxybenzamides |
| JP2013508320A (ja) | 2009-10-21 | 2013-03-07 | バイエル・ファルマ・アクチェンゲゼルシャフト | 置換されたハロフェノキシベンズアミド誘導体 |
| US20120269803A1 (en) | 2009-10-21 | 2012-10-25 | Bayer Intellectual Property Gmbh | Substituted benzosulphonamides |
| CA2777304A1 (en) | 2009-10-21 | 2011-04-28 | Marion Hitchcock | Substituted benzosulphonamides |
| WO2012055953A1 (en) | 2010-10-29 | 2012-05-03 | Bayer Pharma Aktiengesellschaft | Substituted phenoxypyridines |
| ES2630102T3 (es) * | 2011-04-26 | 2017-08-18 | Rdd Pharma Ltd. | Oximetazolina para el tratamiento de trastornos ano-rectales |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1593261A (en) * | 1976-07-23 | 1981-07-15 | Inveresk Res Int | Controlled release suppository |
| DK339289D0 (da) | 1989-07-07 | 1989-07-07 | Dak Lab As | Farmaceutisk praeparat |
| DK469989D0 (da) * | 1989-09-22 | 1989-09-22 | Bukh Meditec | Farmaceutisk praeparat |
| NL9102142A (nl) | 1991-12-20 | 1993-07-16 | Dagra Pharma Bv | Zetpillen met vertraagde afgifte en werkwijze voor de bereiding daarvan. |
| FR2697162B1 (fr) † | 1992-10-23 | 1995-01-13 | Lafon Labor | Utilisation du modafinil pour la fabrication d'un médicament pour le traitement de l'incontinence urinaire et des troubles sphinctériens urétro vésicaux. |
| EP0692975A4 (en) * | 1993-04-08 | 2000-11-29 | Univ Queensland | ADMINISTRATION OF A VASO ACTIVE AND A THERAPEUTIC ACTIVE |
| GB9422571D0 (en) | 1994-11-09 | 1995-01-04 | Whitehall Lab Ltd | Haemorrihoidal compositions and method of use |
| US5595753A (en) * | 1995-04-14 | 1997-01-21 | President And Fellows Of Harvard College | Topical formulations and methods for treating hemorrhoidal pain and sphincter and smooth muscle spasm in the gastrointestinal tract |
| AU728889C (en) * | 1996-12-23 | 2001-08-02 | S.L.A. Pharma Ag | Pharmaceutical composition for treating fecal incontinence and anal itch |
-
1997
- 1997-12-23 AU AU53315/98A patent/AU728889C/en not_active Ceased
- 1997-12-23 ES ES97950311T patent/ES2259806T5/es not_active Expired - Lifetime
- 1997-12-23 PT PT97950311T patent/PT946155E/pt unknown
- 1997-12-23 WO PCT/GB1997/003525 patent/WO1998027971A1/en active IP Right Grant
- 1997-12-23 AT AT97950311T patent/ATE320796T1/de active
- 1997-12-23 EP EP97950311A patent/EP0946155B2/en not_active Expired - Lifetime
- 1997-12-23 JP JP52855098A patent/JP4246265B2/ja not_active Expired - Fee Related
- 1997-12-23 DE DE69735552T patent/DE69735552T3/de not_active Expired - Lifetime
- 1997-12-23 DK DK97950311T patent/DK0946155T4/da active
- 1997-12-23 US US09/331,163 patent/US6635678B1/en not_active Expired - Fee Related
- 1997-12-23 CA CA002275663A patent/CA2275663C/en not_active Expired - Fee Related
-
2003
- 2003-03-18 US US10/389,773 patent/US7928146B2/en not_active Expired - Fee Related
-
2007
- 2007-10-31 US US11/932,939 patent/US7781444B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| ATE320796T1 (de) | 2006-04-15 |
| JP2001507020A (ja) | 2001-05-29 |
| AU728889B2 (en) | 2001-01-18 |
| AU728889C (en) | 2001-08-02 |
| DE69735552T3 (de) | 2009-08-13 |
| AU5331598A (en) | 1998-07-17 |
| ES2259806T3 (es) | 2006-10-16 |
| WO1998027971A1 (en) | 1998-07-02 |
| ES2259806T5 (es) | 2009-05-01 |
| EP0946155A1 (en) | 1999-10-06 |
| DK0946155T3 (da) | 2006-07-31 |
| CA2275663A1 (en) | 1998-07-02 |
| EP0946155B2 (en) | 2009-01-21 |
| US7781444B2 (en) | 2010-08-24 |
| US7928146B2 (en) | 2011-04-19 |
| EP0946155B1 (en) | 2006-03-22 |
| CA2275663C (en) | 2008-03-18 |
| US20030216420A1 (en) | 2003-11-20 |
| PT946155E (pt) | 2006-07-31 |
| US6635678B1 (en) | 2003-10-21 |
| DK0946155T4 (da) | 2009-05-11 |
| DE69735552D1 (de) | 2006-05-11 |
| DE69735552T2 (de) | 2007-02-01 |
| US20080058363A1 (en) | 2008-03-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4246265B2 (ja) | 大便失禁を治療するための医薬組成物 | |
| US20230255940A1 (en) | Oxymetazoline for the treatment of ano-rectal disorders | |
| CN104023707B (zh) | 用于治疗肛门直肠疾患的羟甲唑啉 | |
| WO2022178144A1 (en) | Remittive effects of tapinarof in the treatment of plaque psoriasis, atopic dermatitis, or radiation dermatitis | |
| KR20090107551A (ko) | 분변실금의 치료 | |
| WO2013150354A1 (en) | Local composition to treat stress urinary incontinence in a female subject | |
| WO2013070236A1 (en) | Methods and compositions for treating hemorrhoids while providing local anesthetic and anti-inflammatory effects |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040218 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070313 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20070329 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20070521 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070905 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080902 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081030 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20081216 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090108 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120116 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130116 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140116 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |