JP4076587B2 - 希釈された単核細胞を収集するシステムおよび方法 - Google Patents
希釈された単核細胞を収集するシステムおよび方法 Download PDFInfo
- Publication number
- JP4076587B2 JP4076587B2 JP50717199A JP50717199A JP4076587B2 JP 4076587 B2 JP4076587 B2 JP 4076587B2 JP 50717199 A JP50717199 A JP 50717199A JP 50717199 A JP50717199 A JP 50717199A JP 4076587 B2 JP4076587 B2 JP 4076587B2
- Authority
- JP
- Japan
- Prior art keywords
- chamber
- container
- interface
- mnc
- tube
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D21/00—Separation of suspended solid particles from liquids by sedimentation
- B01D21/30—Control equipment
- B01D21/302—Active control mechanisms with external energy, e.g. with solenoid valve
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3601—Extra-corporeal circuits in which the blood fluid passes more than once through the treatment unit
- A61M1/3603—Extra-corporeal circuits in which the blood fluid passes more than once through the treatment unit in the same direction
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3622—Extra-corporeal blood circuits with a cassette forming partially or totally the blood circuit
- A61M1/36222—Details related to the interface between cassette and machine
- A61M1/362227—Details related to the interface between cassette and machine the interface providing means for actuating on functional elements of the cassette, e.g. plungers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3622—Extra-corporeal blood circuits with a cassette forming partially or totally the blood circuit
- A61M1/36225—Extra-corporeal blood circuits with a cassette forming partially or totally the blood circuit with blood pumping means or components thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3622—Extra-corporeal blood circuits with a cassette forming partially or totally the blood circuit
- A61M1/36226—Constructional details of cassettes, e.g. specific details on material or shape
- A61M1/362261—Constructional details of cassettes, e.g. specific details on material or shape at least one cassette surface or portion thereof being flexible, e.g. the cassette having a rigid base portion with preformed channels and being covered with a foil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3622—Extra-corporeal blood circuits with a cassette forming partially or totally the blood circuit
- A61M1/36226—Constructional details of cassettes, e.g. specific details on material or shape
- A61M1/362265—Details of valves
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3622—Extra-corporeal blood circuits with a cassette forming partially or totally the blood circuit
- A61M1/36226—Constructional details of cassettes, e.g. specific details on material or shape
- A61M1/362266—Means for adding solutions or substances to the blood
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3693—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits using separation based on different densities of components, e.g. centrifuging
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3693—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits using separation based on different densities of components, e.g. centrifuging
- A61M1/3696—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits using separation based on different densities of components, e.g. centrifuging with means for adding or withdrawing liquid substances during the centrifugation, e.g. continuous centrifugation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/38—Removing constituents from donor blood and storing or returning remainder to body, e.g. for transfusion
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D21/00—Separation of suspended solid particles from liquids by sedimentation
- B01D21/26—Separation of sediment aided by centrifugal force or centripetal force
- B01D21/262—Separation of sediment aided by centrifugal force or centripetal force by using a centrifuge
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B04—CENTRIFUGAL APPARATUS OR MACHINES FOR CARRYING-OUT PHYSICAL OR CHEMICAL PROCESSES
- B04B—CENTRIFUGES
- B04B5/00—Other centrifuges
- B04B5/04—Radial chamber apparatus for separating predominantly liquid mixtures, e.g. butyrometers
- B04B5/0442—Radial chamber apparatus for separating predominantly liquid mixtures, e.g. butyrometers with means for adding or withdrawing liquid substances during the centrifugation, e.g. continuous centrifugation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2221/00—Applications of separation devices
- B01D2221/10—Separation devices for use in medical, pharmaceutical or laboratory applications, e.g. separating amalgam from dental treatment residues
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B04—CENTRIFUGAL APPARATUS OR MACHINES FOR CARRYING-OUT PHYSICAL OR CHEMICAL PROCESSES
- B04B—CENTRIFUGES
- B04B5/00—Other centrifuges
- B04B5/04—Radial chamber apparatus for separating predominantly liquid mixtures, e.g. butyrometers
- B04B5/0442—Radial chamber apparatus for separating predominantly liquid mixtures, e.g. butyrometers with means for adding or withdrawing liquid substances during the centrifugation, e.g. continuous centrifugation
- B04B2005/045—Radial chamber apparatus for separating predominantly liquid mixtures, e.g. butyrometers with means for adding or withdrawing liquid substances during the centrifugation, e.g. continuous centrifugation having annular separation channels
Description
本発明は、遠心処理システムおよび装置に関する。
発明の背景
今日の血液収集組織は日常的に、遠心分離により、全血を、赤血球、血小板および血漿などの、様々な治療成分に分離している。
従来の血液処理システムおよび方法は、1回の使用に関連する耐久性のある遠心分離機器、典型的にはプラスチックからなる滅菌処理チャンバを使用する。遠心分離機器は、これらのチャンバを回転させながらチャンバに全血を導入して、遠心力場(centrifugal field)を作り出す。
全血は、回転しているチャンバ内で、遠心力場の影響下で、より高密度の赤血球と、血小板の豊富な血漿とに分離する。白血球からなる中間層は、赤血球と、血小板の豊富な血漿との間の界面を形成する。単核細胞(MNC、mononuclearcell)は、この界面中に存在する。
発明の要旨
本発明は、全血から単核細胞を分離するシステムおよび方法を提供する。このシステムおよび方法は、チャンバを回転させ、このチャンバにおいて、全血が、濃縮(packed)赤血球と、血漿成分と、濃縮赤血球と血漿成分との間の界面とに遠心分離される。界面は、血小板と、単核細胞とを保持する。このシステムおよび方法は、界面制御ユニットを含む。界面制御ユニットは、3つの状態で動作する。第1の状態では、血小板および単核細胞の両方をチャンバ内に保持し、第1の容器に通じる経路で、チャンバから血小板の乏しい血漿を除去することを可能にし、血小板の乏しい血漿は、第1の容器で収集されて希釈液体として使用される。第2の状態では、単核細胞をチャンバ内に保持しながら、別の経路で、チャンバから血小板の豊富な血漿を除去することを可能にする。この別の経路は、血小板の乏しい収集容器を迂回し、それにより、この容器の血小板の乏しい特性を維持する。第3の状態は、第2の容器に通じる経路で、チャンバから単核細胞を除去することを可能にし、第2の容器に、単核細胞が収集される。このシステムおよび方法は、血小板の乏しい血漿を、第1の容器から第2の容器に送り、第2の容器で、除去された単核細胞を希釈する。処理中に血小板の豊富な血漿を分離する能力により、純粋な濃度の単核細胞が提供される。血小板の乏しい血漿を希釈液として選択的に提供する追加能力により、単核細胞生成物が、希釈後に純粋なままであることが保証される。
好適な実施形態では、界面制御ユニットは、検知エレメントを含み、この検知エレメントは、チャンバ内の界面の場所を光学的に特定して検知出力を提供し、界面制御を助ける。
本発明のその他の特徴および利点は、以下の明細書、図面、および添付の請求の範囲を検討すれば、明らかになる。
【図面の簡単な説明】
図1は、本発明の特徴を実施する分離チャンバを有する血液遠心分離機の側断面図である。
図2は、図1に示される遠心分離機に関連するスプールエレメントを示し、使用のために、関連する処理容器がスプールエレメントの周りに巻き付けられていた状態である。
図3Aは、図1に示される遠心分離機の斜視図であり、ボウルおよびスプールエレメントがそのアクセス位置まで旋回された状態である。
図3Bは、ボウルおよびスプールエレメントの斜視図であり、図2に示される処理容器をスプールエレメントの周りに固定することを可能にするために、ボウルおよびスプールエレメントが互いに分離された状態である。
図4は、図2に示される処理容器の平面図である。
図5は、処理容器に関連する流体回路であって、遠心分離機のポンプステーションに関連して取り付けられるカセットを含む流体回路の斜視図である。
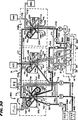
図6は、図5に示される流体回路の概略図である。
図7は、図6に示される流体回路の部分を形成するカセットの裏面の斜視図である。
図8は、図7に示されるカセットの正面の斜視図である。
図9は、図7に示されるカセット内に形成される流れチャネルおよびバルブステーションの概略図である。
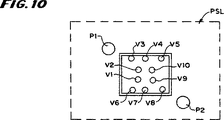
図10は、図7に示されるタイプのカセットを受け入れるために意図されたポンプステーションの概略図である。
図11は、図10に示されるポンプステーションに取り付けられた、図9に示されるカセットの概略図である。
図12は、図6に示される流体回路の部分を形成するカセットおよびポンプステーションの斜視図である。
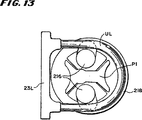
図13は、図6に示される流体回路の部分を形成する蠕動ポンプの上面図であり、ポンプロータが退縮位置にある状態である。
図14は、図6に示される流体回路の部分を形成する蠕動ポンプの上面図であり、ポンプロータが、ポンプチューブを係合する伸長位置にある状態である。
図15は、図1に示される遠心分離機の分離チャンバの概略上面図であり、高G壁および低G壁の動径方向の輪郭を示すようにレイアウトされている。
図16Aおよび図16Bは、分離チャンバ内の血小板の豊富な血漿の収集ゾーンの部分を幾分か概略的に示し、高G壁表面が、赤血球と血小板の豊富な血漿との間の界面を含み且つこの界面の位置を制御するためのテーパ状ウェッジを形成する。
図17は、処理チャンバの内部の幾分か概略的な図であり、全血が処理チャンバに入り赤血球と血小板の豊富な血漿とに分離され、且つ、血小板の豊富な血漿が処理チャンバに収集される領域で、低G壁から高G壁の方を見た図である。
図18は、図17に示される血液分離チャンバ内にMNCを閉じ込めて「とどまらせる(park)」、確立された動的な流れ状態を示す概略図である。
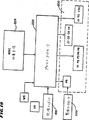
図19は、所定のMNC収集手順を行うように図6に示される流体回路を構成するプロセスコントローラの概略図である。
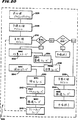
図20は、図19に示されるコントローラが支配するMNC収集手順の様々なサイクルおよびフェーズを示すフローチャートである。
図21は、図20に示される手順の予備処理サイクル中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図22は、図20に示される手順のMNC蓄積フェーズ中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図23は、図20に示される手順のPRBC収集フェーズ中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図24Aは、図20に示される手順のMNC除去フェーズの開始時の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図24Bは、図20に示される手順のMNC除去フェーズ中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図24Cは、図20に示される手順のMNC除去フェーズの終了時の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図25は、図20に示される手順のPRPフラッシュフェーズ中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図26は、図20に示される手順のMNC懸濁フェーズ中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図27は、図20に示される手順のクリーンアップフェーズ中の、図6に示される回路内での血液成分および流体の運搬を示す概略図である。
図28は、図6に示される回路に関連して使用され、採取のためのMNC領域を検知および定量化するための光センサの概略図である。
図29は、MNCの収集および採取に適した流体回路の別の実施形態を示す。
図30は、図20に示される手順のPRBC収集フェーズ中の、図29に示される回路内での血液成分および流体の運搬を示す概略図である。
図31は、図20に示される手順のMNC除去フェーズ中の、図29に示される回路内での血液成分および流体の運搬を示す概略図である。
本発明は、本発明の精神または本質的な特徴から逸脱することなく、幾つかの形で実施され得る。本発明の範囲は、添付の請求の範囲の前に示される具体的な説明ではなく、添付の請求の範囲において規定される。従って、請求の範囲の等価物の意味および範囲内にある実施形態はすべて、請求の範囲に含まれることが意図される。
好適な実施形態の説明
I.遠心分離機
図1は、全血から単核細胞(MNC)を採取するのに適した血液処理チャンバ12を有する血液遠心分離機10を示す。チャンバ12の境界は、回転するスプールエレメント18とボウルエレメント20との間の環状間隙16内に保持される可撓性のある処理容器14により形成される。示された好適な実施形態では、処理容器14は、細長いチューブの形を取り(図2参照)、使用前にスプールエレメント18の周りに巻き付けられる。
遠心分離機10のさらなる詳細は、「Enhanced Yield Platelet Systems and Methods」と題された米国特許第5,370,802号に示される。本明細書において、上記特許を参考として援用する。
ボウルおよびスプールエレメント18および20は、ヨーク22を中心に、図3Aおよび図3Bが示すような直立位置と、図1が示すような懸架位置との間で旋回される。
直立状態であるとき、ボウルおよびスプールエレメント18および20は、ユーザによるアクセスのために与えられる。機構は、図3Bが示すようにスプールおよびボウルエレメント18および20が開かれることを可能にし、そのため、オペレータは、図2が示すように容器14をスプールエレメント20の周りに巻き付けることができる。スプールエレメント20上のピン150は、容器14上の切り抜き部を係合し、容器14をスプールエレメント20上に固定する。
スプールおよびボウルエレメント18および20は、閉じられると、図1に示される懸架位置に旋回され得る。動作において、遠心分離機10は、懸架されたボウルおよびスプールエレメント18および20を、軸28を中心に回転させ、処理チャンバ12内に遠心力場を作り出す。
今説明したスプールエレメント18および20の相対移動を引き起こすための機構のさらなる詳細は、「Centrifuge With Separable Bowl and Spool Elements Providing Access to the Separation Chamber」と題された米国特許第5,360,542号に開示されている。本明細書において、上記特許を参考として援用する。
遠心力場の動径方向の境界(図1参照)は、ボウルエレメント18の内壁24と、スプールエレメント20の外壁26とにより形成される。ボウル内壁24は、高G壁を規定する。スプール外壁26は、低G壁を規定する。
II.処理容器
示された実施形態(図4参照)では、第1の周囲シール42が、容器14の外縁部を形成する。第2の内部シール44は、回転軸28にほぼ平行に延び、容器14を2つの区画38および40に分割する。
使用中、全血は、区画38で遠心分離される。使用中、区画40は、生理食塩水などの液体を保持し、区画38との平衡を保つ。図4に示される実施形態では、区画38は、約1〜約1.2の容積測定比だけ、区画40よりも大きい。
3つのポート46、48および50は、処理区画38に連通し、全血およびその成分を運ぶ。2つの追加ポート52および54は、バラスト区画40に連通し、平衡を保つ流体を運ぶ。
III.流体処理回路
流体回路200(図4)は、容器14に連結される。図5は、流体回路200の全体的なレイアウトを、可撓性のあるチューブ、液体ソースおよび収集容器、インラインポンプ、ならびにクランプのアレイに関して示す。これらはすべて、以下に詳細に説明される。図6は、流体回路200の詳細を概略図の形で示す。
示された実施形態では、左、中央および右カセット23L、23Mおよび23Rは、流体回路200のバルブおよびポンプ機能の多くを集中させる。左、中央および右カセット23L、23Mおよび23Rは、それぞれPSL、PSMおよびPSRとして示される、遠心分離機10の左、中央および右ポンプステーションと対になる(mate)。
A.カセット
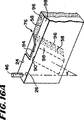
各カセット23L、23Mおよび23Rは、同じように構成されるため、1つのカセット23Lの説明は、すべてのカセットに当てはまる。図7および図8は、カセット23Lの構造の詳細を示す。
カセット23Lは、成形されたプラスチックボディ202を含む。液体流れチャネル208は、ボディ202の前側204に一体に成形される。剛性パネル214が、ボディの前側204を覆い且つ封止する。
バルブステーション210は、カセットボディ202の裏側206に成形される。可撓性のあるダイアフラム212が、ボディ202の裏側206を覆い且つ封止する。
図9は、各カセットの流れチャネル208およびバルブステーション210の代表的なアレイを概略的に示す。示されるように、チャネルC1〜C6は、交差して星形アレイを形成し、中央ハブHから放射状に広がる。チャネルC7はチャネルC5に交差し、チャネルC8はチャネルC6に交差し、チャネルC9はチャネルC3に交差し、そして、チャネル10はチャネルC2に交差する。言うまでもなく、その他のチャネルパターンを用いてもよい。
この構成では、バルブステーションVS1、VS2、VS9およびVS10は、ハブHの共通交点のすぐ隣で、チャネルC2、C3、C5およびC6にそれぞれ配置される。バルブステーションVS3、VS4、VS5、VS6、VS7およびVS8は、チャネルC8、C1、C2、C5、C4およびC3の外先端に配置される。
各カセット23Lは、カセット23Lの外側でチャネルC7とチャネルC6との間に延びる可撓性のある上側チューブループULと、カセットの外側でチャネルC3とチャネルC10との間に延びる下側チューブループLLとを有する。使用中、チューブループULおよびLLは、関連するポンプステーションのポンプの蠕動ポンプロータを係合する。
B.ポンピングステーション
ポンプステーションPSL、PSMおよびPSRは、カセット23L、23Mおよび23Rと同様に、同一に構成されるため、1つのステーションPSLの説明が、すべてのステーションに当てはまる。図12は、左ポンプステーションPSLの構造の詳細を示す。図10は、左ポンプステーションPSLをより概略的な形で示す。
ステーションPSLは、2つの蠕動ポンプを含むため、回路200には、P1〜P6として示される合計6つのポンプがある。(図6参照)。ステーションPSLはまた、10個のバルブアクチュエータのアレイ(図10に示す)を含むため、回路200には、VA1〜VA30として示される合計30個のバルブアクチュエータがある(図6参照)。
使用中(図11参照)、カセット23LのチューブループULおよびLLは、左ポンプステーションPSLのポンプP1およびP2を係合する。同様の態様で(図6が示すように)、中央カセット23MのチューブループULおよびLLは、ポンプP3およびP4を係合する。右カセット23LのチューブループULおよびLLは、ポンプP5およびP6を係合する。
図11が示すように、カセット23LのバルブステーションVS1〜VS10は、左ポンプステーションPSLのバルブアクチュエータV1〜V10と整列する。図6が示すように、中央および右カセット23Mおよび23Rのバルブステーションも同様に、それぞれ中央および右ポンプステーションPSMおよびPSRのバルブアクチュエータと整列する。
以下の表1は、図6に示されるポンプステーションバルブアクチュエータV1〜V30と、カセットバルブアクチュエータVS1〜VS10との動作上の関連をまとめている。
カセット23L、23Mおよび23Rは、カセットの裏側206を下にして、それぞれのポンプステーションPSL、PSM、PSRに取り付けられ、そのため、ダイアフラム212は、バルブアクチュエータに面し且つバルブアクチュエータを係合する。バルブアクチュエータVnは、バルブ閉鎖位置に向かって付勢されるソレノイド作動式ラム215である(図12参照)。バルブアクチュエータVnは、表1に示された態様でカセットバルブステーションVSnと整列するようなパターンで配置される。所定のラム215が付勢されると、関連するカセットバルブステーションが開き、液体の通過を可能にする。ラム215が付勢されていないとき、ラム215は、ダイアフラム215を、関連するバルブステーション内に変位し、関連するバルブステーションを通る液体の通過を阻止する。
示された実施形態では、図12が示すように、各ポンプステーションPSL、PSMおよびPSRのポンプP1〜P6は、回転する蠕動ポンプロータ216を含む。ロータ216は、それぞれのチューブループを係合していない退縮状態(図13に示される)と、ロータ216がそれぞれのチューブループをポンプレース218に抗して係合する動作状態(図14に示される)との間で動かされ得る。
それにより、ポンプP1およびP6は、以下の3つの状態で動作し得る。
(i)ポンプオン状態:(図14が示すように)この状態の間、ポンプロータ216は回転し、動作位置にあり、ポンプチューブをポンプレース218に抗して係合する。従って、回転するポンプロータ216は、蠕動的に流体をチューブループを通して運ぶ。
(ii)開ポンプオフ状態:(図13が示すように)この状態の間、ポンプロータ216は回転せず、退縮位置にあり、ポンプチューブループを係合しない。従って、この開ポンプオフ状態は、ポンプロータの回転がない場合に、ポンプチューブループを通る流体の流れを可能にする。
(iii)閉ポンプオフ状態:この状態の間、ポンプロータ216は回転せず、ポンプロータは動作状態にある。それにより、静止したポンプロータ216がポンプチューブループを係合し、クランプとしての役割を果たして、ポンプチューブループを通る流体の流れを遮断する。
言うまでもなく、退縮しない蠕動ポンプロータを用いて、ポンプロータの上流および下流にクランプおよびチューブ経路を適切に配置することにより、ポンプ状態の等価な組み合わせを達成してもよい。
カセット23L、23M、23R、蠕動ポンプP1〜P6、およびバルブアクチュエータV1〜V30の構造についてのさらなる詳細は、本発明に不可欠なものではない。これらの詳細は、「Peristaltic Pump Tube Cassette with Angle Port Tube Connectors」と題された米国特許第5,427,509号に記載されている。本明細書において、上記特許を参考として援用する。
C.流体流れチューブ
流体回路200は、図6でT1〜T20として示される、ある長さの可撓性のあるプラスチックチューブをさらに含む。可撓性のあるチューブT1〜T20は、カセット23L、23Mおよび23Rを、処理容器14、外部ソースおよび収集バッグまたは容器、ならびに供血者/患者に連結する。
MNCの収集および採取に関するチューブT1〜T20の流体流れ機能については、後で説明する。図6に示されるようなチューブT1〜T20の取り付けを、構造上の観点から、以下にまとめる。
チューブT1は、供血者/患者から(図示しない従来の静脈切開針を介して)外部クランプC2を通って左カセット23LのチャネルC4に延びる。
チューブT2は、チューブT1から、外部クランプC4を通って中央カセット23MのチャネルC5に延びる。
チューブT3は、空気検出チャンバD1から左カセット23LのチャネルC9に延びる。
チューブT4は、滴下(drip)チャンバD1から処理容器14のポート48に延びる。
チューブT5は、処理容器14のポート50から中央カセット23MのチャネルC4に延びる。
チューブT6は、中央カセット23MのチャネルC9から延び、チャンバD1の下流にあるチューブT4に結合する。
チューブT7は、右カセット23RのチャネルC8から左カセット23LのチャネルC8に延びる。
チューブT8は、中央カセット23MのチャネルC1から延び、チューブT7に結合する。
チューブT9は、左カセット23LのチャネルC5から、空気検出チャンバD2および外部クランプC3を通って(図示しない従来の静脈切開針を介して)供血者/患者に延びる。
チューブT10は、処理容器14のポート46から、インライン光センサOSを通って右カセット23RのチャネルC4に延びる。
チューブT11は、右カセット23RのチャネルC9からチャンバD1に延びる。
チューブT12は、右カセット23RのチャネルC2から、PPPとして示される、血小板の乏しい血漿を受けるように意図された容器に延びる。重量スケール(weight scale)(図示せず)は、流体容積の変化を得る目的で、容器PPPの重量を検知する。
チューブT13は、右カセット23RのチャネルC1から、MNCとして示される、単核細胞を受けるように意図された容器に延びる。
チューブT14は、中央カセット23MのチャネルC2から、PRBCとして示される、濃縮赤血球を受けるように意図された容器に延びる。重量スケールWSは、流体容積の変化を得る目的で、容器PRBCの重量を検知する。
チューブT15は、ACDとして示された抗凝血剤の容器から、中央カセット23MのチャネルC8に延びる。重量スケール(図示せず)は、流体容積の変化を得る目的で、容器ACDの重量を検知する。
チューブT16およびT17は、PRIMEとして示された、生理食塩水などのプライミング液体(priming liquid)の容器から延び、すべてのカセット23L、23Mおよび23Rを迂回し、外部クランプC1を通って、チューブT9(空気検出チャンバD2とクランプC3との間)およびチューブT1(クランプC3の上流)にそれぞれ交差する。重量スケール(図示せず)は、流体容積の変化を得る目的で、容器PRIMEの重量を検知する。
チューブT18は、処理容器14のポート52から、右カセット23RのチャネルC5に延びる。
チューブT19は、処理容器14のポート54から延び、チューブT18に交差する。
チューブT20は、左カセット23LのチャネルC2から、WASTEとして示される、廃棄プライミング液体を受けるように意図された容器に延びる。重量スケール(図示せず)は、流体容積の変化を得る目的で、容器WASTEの重量を検知する。
チューブの部分は、臍部(umbilicus)30において合わせられる(図1参照)。臍部30は、遠心力場内にある処理容器14の内部と、遠心力場外にある回路200のその他の静止構成要素との間の流体流連通を提供する。非回転(ゼロオメガ)ホルダ32は、臍部30の上部を、懸架されたスプールおよびボウルエレメント18および20の上で、非回転位置に保持する。ヨーク22上のホルダ34は、臍部30の中央部を、懸架されたスプールおよびボウルエレメント18および20の周りで第1の(1オメガ)速度で回転させる。別のホルダ36は、臍部30の下端部を、1オメガ速度の2倍の第2の速度(2オメガ速度)で回転させる。懸架されたスプールおよびボウルエレメント18および20もまた、この速度で回転する。このような臍部30の公知の相対回転は、臍部30をねじれない状態に保ち、このようにして、回転するシールの必要性を回避する。
IV.血液処理チャンバでの分離(概要)
容器14および流体回路200を用いてMNCを収集する手順の詳細を説明する前に、主に図4および図15〜図17を参照して、処理区画38での全血分離の流体力学について、まず大まかに説明する。
まず図4を参照して、抗凝血処理された全血(WB)が、供血者/患者から引き込まれ、ポート48を通して処理区画内に運ばれる。血液処理区画38は、内部シール60および66を含む。内部シール60および66は、WB流入領域74に通じるWB入口通路72を形成する。
WBが、回転軸28を中心に、区画38内の円周流路に従うため、容器14の側壁は、スプールエレメント18の外(低G)壁26およびボウルエレメント20の内(高G)壁24の輪郭と一致するように広がる。
図17が示すように、WBは、血液処理区画38内の遠心力場において、高G壁24に向かって移動する濃縮赤血球(参照番号96で示されるPRBC)と、PRBC96の移動により、低G壁26に向かって動かされる血小板の豊富な血漿(参照番号98で示されるPRP)とに分離する。界面と呼ばれる中間層(参照番号58で示される)が、PRBC96とPRP98との間に形成される。
再び図4を参照して、内部シール60はまた、血液処理区画38内にPRP収集領域76を作り出す。図17がさらに示すように、PRP収集領域76は、WB流入領域74に隣接する。PRBC96が遠心力に応答して高G壁24に向かって移動する速度は、血液処理区画38内の他のどの場所よりも、WB流入領域74で最も速い。WB流入領域74には、低G壁26に向かって移動する比較的より多くの血漿容積もある。その結果、WB流入領域74において、低G壁26に向かう比較的大きい動径方向の血漿速度が起こる。このような低G壁26に向かう大きい動径方向速度により、PRBC96から、すぐ近くのPRP収集領域76に多数の血小板が溶出される。
図4が示すように、内部シール66はまた、PRBC収集通路78を規定するドッグレッグ70を形成する。強化バリア115(図15参照)は、高G壁24に沿ったPRBC質量内に延び、強化バリア115と、それに面する等動径方向の高G壁24との間に、制限された通路114を作り出す。制限された通路114は、高G壁24に沿って存在するPRBC96が、バリア115を越えてPRBC収集領域50内に移動して、PRBC収集通路78によりPRBCポート50に運ばれることを可能にする。それと同時に、強化バリア115は、強化バリア115を越えるPRP98の通過を阻止する。
図15、図16Aおよび図16Bが示すように、高G壁24はまた、低G壁26に向かって突出し、PRP収集領域76にテーパ状のランプ84を形成する。ランプ84は、低G壁26に沿って、狭窄通路90を形成し、PRP98の層は、この通路90に沿って延びる。ランプ84は、界面58およびPRBC96を、PRP収集ポート46に近づけないようにしながら、PRP98がPRP収集ポート46に到達することを可能にする。
示された好適な実施形態(図16A参照)では、ランプ84は、PRPポート46の軸に対して45°未満(好ましくは、約30°)の平行でない角度αの向きで配置される。角度αは、界面およびPRBCが、狭窄通路90を通ってあふれ出るのを調停する(mediates)。
図16Aおよび図16Bが示すように、ランプ84はまた、関連する界面コントローラ220(図19参照)により容器14の側壁を通して見るために、界面26を見せる。界面コントローラ220は、それぞれのポート48、50および46を通るWB、PRBCおよびPRPの相対流量を制御する。このようにして、コントローラ220は、界面58を、(図16Aが示すように)狭窄通路90に近い位置か、または、(図16Bが示すように)狭窄通路90から間隔があけられた位置のいずれかの、ランプ上の所定の位置に維持することができる。
狭窄通路90に対する界面58のランプ84上での位置を制御することにより、コントローラ220はまた、ポート46を通して収集される血漿の血小板含有量を制御することができる。血漿中の血小板濃度は、界面58に近接するに従って増加する。(図16Bに示すように)界面58をランプ84上の比較的低い位置に維持することにより、血小板の豊富な領域は、ポート46から離され、ポート46により運ばれる血漿は、比較的低い血小板含有量を有する。(図16Aが示すように)界面58を、ポート46により近い、ランプ84上の高い位置に維持することにより、ポート46により運ばれる血漿には、血小板が豊富である。
上記の代わりに、または上記と組み合わせて、コントローラは、WBが血液処理区画38に導入されるレート、または、PRBCが血液処理区画134から運ばれるレート、またはその両方を変えることにより、界面58の位置を制御し得る。
界面コントローラの好適な実施形態のさらなる詳細は、米国特許第5,316,667号に記載されている。本明細書において、上記特許を参考として援用する。
図15が示すように、動径方向に対向した表面88および104は、WB流入領域74の高G壁24に沿って、流れ制限領域108を形成する。図17にも示すように、領域108は、WB流入領域74においてWBの流れを制限して、その通過を低減し、それにより、WBを、低G壁26に沿って血液処理区画38内により均一に潅流させる。このWBの均一な潅流は、PRP収集領域76に隣接して起こり、且つ、界面58の好適な制御された位置がある平面とほぼ同じ平面で起こる。一旦ゾーンダム104の狭窄領域108を越えると、PRBC96は、遠心力に応答して、急速に高G壁24に向かって移動する。
狭窄領域108は、WBを、ほぼ界面58の好適な制御された高さで、流入領域74内に運ぶ。界面58の制御された高さよりも下または上の高さで流入領域74に運ばれたWBは、すぐに界面の高さを探す。そしてWBは、界面の高さを探すときに界面の高さの周りで振動し、界面58に沿って不必要な二次的な流れおよび乱れ(perturbations)を引き起こす。領域108は、WBをほぼ界面レベルで流入領域74内に運ぶことにより、界面58に沿った二次的な流れおよび乱れの発生を低減する。
図15が示すように、低G壁26は、回転軸28から外側に高G壁24に向かってWBの流れ方向にテーパ状になっており、それに面する高G壁24は、一定の半径を保持している。テーパは、(図15が示すように)連続していてもよく、階段状になっていてもよい。高G壁24および低G壁26に沿ったこれらの輪郭は、PRP収集領域76の方向の遠心力場に対してほぼ横方向の動的な円周方向の血漿流れ状態を作り出す。図18に概略的に示されるように、この方向(矢印214)に起こる円周方向の血漿流れ状態は、界面58をPRP収集領域76の方に絶えず引き戻す。PRP収集領域76では、既に説明したより高い動径方向の血漿流れ状態が存在し、さらに多くの血小板を界面58から取り除く。それと同時に、逆流パターンは、界面58のその他のより重い成分(リンパ球、単球、および顆粒球)を循環させて、PRPストリームから離れたPRBC質量に戻す役割を果たす。
この動的な円周方向の血漿流れ状態内で、MNC(図18などに示される)は最初に、高G壁24に沿って落ち着くが、最終的には、高ヘマトクリットPRBC収集領域50付近の界面58の表面に浮かぶ。テーパ状になった低G壁は、図18に矢印214で示される血漿逆流パターンを作り出す。この逆流パターン214は、MNCを低ヘマトクリットPRP収集領域76の方に引き戻す。MNCは再び、低ヘマトクリットPRP収集領域76付近で、高G壁24に向かって落ち着く。
MNCは、図18に216で示されるこの経路で循環するが、WBは、PRBCとPRPとに分離される。MNCはこのように収集され、そして、PRBC収集領域50およびPRP収集領域76の両方から離れた、区画38内のこの閉じ込められた経路216に「とどまらされる」。
処理区画38で起こる分離の力学のさらなる詳細は、米国特許第5,573,678号に見られる。本明細書において、上記特許を参考として援用する。
V.単核細胞処理手順
遠心分離機10は、プロセスコントローラ222(図19参照)を含む。プロセスコントローラ222は、流体回路200の動作を命令し、容器14を用いた所定のMNC収集および採取手順224を実行する。
図20が示すように、手順224は、流体回路200にプライミングする(primes)前処理プライミングサイクル226を含む。手順224は次に、予備処理サイクル228を含む。予備処理サイクル228では、供血者/患者から得られた全血からPPPを処理し、手順224の遅くに、採取されたMNCの懸濁培地として使用する。手順224は次に、少なくとも1回の主処理サイクル230を含む。主処理サイクル230は、収集ステージ232を含み、その後に採取ステージ234を含む。
収集ステージ232は、収集フェーズ236および238の連続を含み、これらの収集フェーズの間、上記の態様で全血が処理され、第1の区画38に単核細胞を蓄積する。
採取ステージは同様に、採取フェーズ240、242、244および246の連続を含み、これらの採取フェーズの間、単核細胞の蓄積は、第1の区画38から、回路200に連結された収集容器MNCに移される。予備処理サイクル228の間に収集された懸濁培地は、MNCに付加される。
通常、主処理サイクル230は、所定の手順224の間に1回よりも多く行われる。所定の手順224で行われる処理サイクル230の回数は、収集したいMNCの総容積に依存する。
例えば、代表的な手順224では、主処理サイクル230は、続けて5回繰り返される。各主処理サイクル230の間、1サイクルあたり約3mlのMNC容積を得るために、約1500〜約3000mlの全血が処理され得る。5回の処理サイクル230の終わりで、約15mlのMNC容積が収集され得、このMNC容積が、約200mlの最終希釈PPPに懸濁される。
A.前処理プライミング/バラストシーケンス
供血者/患者を(チューブT1およびT9を介して)流体回路200につなぐ前に、コントローラ222は、プライミングサイクル228を行う。プライミングサイクル228の間、コントローラ222は、遠心分離機10に、軸28を中心にスプールおよびボウルエレメント18および20を回転させるよう命令するとともに、ポンプP1〜P6に、流体回路15および容器14の全体にわたって、生理食塩水などの滅菌プライミング液体を容器PRIMEから運び、抗凝血剤を容器ACDから運ぶよう命令する。プライミング液体は、回路15および容器14から空気を追い出す。
第2の区画40は、単一のチューブT18により扱われるため、事実上、単一のアクセスポートを有する。プライミングを達成するために、区画40は、プライミング液体との流れ連通から分離され、ポンプP5は、区画40から空気を引き込むように動作し、それにより、区画40に負圧(真空)状態を作り出す。区画40から空気を除去すると、次いで、プライミング液体の流れに連通が開かれ、プライミング液体が、真空により区画40に引き込まれる。ポンプP5はまた、区画40内への液体の運搬を助け、且つ、区画40に正圧状態を作り出すように動作する。コントローラ222は、プライミング液体を第2の区画40に保持して、血液処理中に第1の区画38との平衡を保つ。
言うまでもなく、この真空プライミング手順が、単一のアクセスポートまたはその等価物により扱われる実質的にいかなる容器のプライミングにも適用可能であることが認識されるはずである。
B.予備処理サイクル
容器MNCで採取されるMNCは、好ましくは、MNC供血者/患者から得られる血小板の乏しい血漿(PPP)培地に懸濁される。予備処理サイクル228の間、コントローラ222は、流体回路222を、供血者/患者から予め確立されたPPP容積を収集して容器PPPに保持するように構成する。この容積は後に、処理中にMNCの懸濁媒体として使用されるとともに、処理後にMNCに付加されて、所望の最終希釈容積を達成する。
一旦供血者/患者を瀉血すると、コントローラ222は、ポンプステーションPSL、PSMおよびPSRを、予備処理サイクル228を開始するように構成する。このサイクル228の間、上記のように、全血は、区画38で、濃縮赤血球(PRBC)と、血小板の豊富な血漿(PRP)とに遠心分離される。PRBCは、供血者/患者に戻され、単核細胞は、区画38に蓄積する。
MNCが区画38に蓄積すると、分離された血漿成分の部分が取り除かれ、収集されて、MNC懸濁培地として使用される。このサイクル228の間、コントローラ222は、(図16Bに示されるように)界面58をランプ84上の比較的低い位置に維持する。その結果、区画38から運ばれ、容器PPPに保存される血漿には、血小板が比較的乏しいため、この血漿を、PPPとして特徴付けることができる。区画38から運ばれたPPPの残りは、このサイクル228の間に、供血者/患者に戻される。
予備処理サイクル228中の流体回路200の構成を、図21に示し、さらに以下の表2にまとめる。
予備サイクル228の間、ポンプP2は、全血(WB)を供血者/患者からチューブT1を介して左カセット23Lに引き込み、チューブT3に引き込んで、チャンバD1を通り、そしてチューブT4を通して血液処理区画38に引き込む。ポンプP3は、抗凝血剤ACDを、チューブT15を通して中央カセット23Mに引き込み、そしてチューブT2に引き込んで、全血と混合する。
抗凝血処理された全血は、ポート48を通って区画38に運ばれる。上記のように、全血は、PRPと、PRBCと、界面(MNCを含む)とに分離される。
ポート50は、PRBC96を、血液処理区画38からチューブT5を通して中央カセット23Mに運ぶ。PRBCは、チューブT8を通ってチューブT7に入り、左カセット23LおよびチューブT9を介して供血者/患者に戻る。
ポート46は、血液処理区画38からPPPを運ぶ。PPPは、チューブT10をたどって、右カセット23Rに入る。ポンプP5は、PPPの部分をチューブT7に運び、PRBCとともに供血者/患者に戻す。界面コントローラ220は、(図16Bに示されるように)界面をランプ84上の低い位置に維持するようにポンプP5の流量を設定し、それにより、このサイクル中に区画38から運ばれる血小板の濃度を最小にする。ポンプP6は、MNC懸濁および最終希釈のための所定の容積が収集されるまで、PPPの部分を、チューブT12を通して容器PPPに運ぶ。この容積は、VOLSUSとして示される。
C.主処理サイクル
1.単核細胞(MNC)収集ステージ
(i)MNC蓄積フェーズ
コントローラ222は次に、主処理サイクル230のMNC収集ステージ232に切り替わる。まず、コントローラ222は、MNC蓄積フェーズ236用に流体回路200を構成する。
フェーズ236のために、コントローラ222は、PPPの収集を停止するよう、ポンプステーションPSRの構成を変える。コントローラ222はまた、界面コントローラ220に、ポンプP5の流量を維持して(図16Aに示されるように)界面をランプ84上のより高い位置に維持するよう命令し、それにより、PRPの分離を可能にする。
構成を変えたため、ポンプP6はまた、以下により詳細に説明されるように、PRPの部分を血液処理チャンバ38に再循環して血小板分離効率を高める。
MNC収集ステージ232のMNC蓄積フェーズ236の構成を、図22に示し、さらに以下の表3にまとめる。
1.PRPの再循環による高血小板分離効率の促進
通常、血小板は、MNC手順中は収集されない。その代わりに、血小板を供血者/患者に戻すことが望ましいと考えられる。分離された血小板の平均血小板容積MPV(フェムトリットルflまたは立方ミクロンで表される)が高いことは、高い血小板分離効率を示すため、望ましい。MPVは、従来の技術により、PRPサンプルから測定され得る。より大きい血小板(即ち、約20フェムトリットルよりも大きい)は、最も界面58に捕らえられやすく、供血者/患者に戻されるPRPに入らない。その結果、供血者/患者に戻されるPRP中のより大きい血小板の数(population)が低減され、従って、MPVもより低くなる。
上記のような、界面58からより大きい血小板を持ち上げるのに十分な動径方向の血漿流れ状態の確立は、血液処理区画38に入るWBの流入ヘマトクリットHiに大きく依存する。この理由のため、ポンプ6は、チューブT10を流れるPRPの部分を再循環させて、WB入口ポート48に戻す。再循環するPRPは右カセット23Rを通り、入口ポート48に連結されるチューブT4に結合するチューブT11に流入する。再循環するPRPは、血液処理区画38に入るWBと混ざり、それにより、流入ヘマトクリットHiを低下させる。
コントローラは、所望の流入ヘマトクリットHiを達成するように、ポンプP6のPRP再循環流量QRecircを設定する。好適な実現では、Hiは、約40%以下であり、最も好適には、約32%である。これらの値は、高MPVを達成する。
流入ヘマトクリットHiは、従来、チューブT4のインラインセンサ(図示せず)により測定され得る。本願と同時係属中の米国特許出願シリアル番号第08/471,883号に開示されるように、流入ヘマトクリットHiはまた、検知された流れ状態に基づいて、経験的に判定され得る。本明細書において、上記出願を参考として援用する。
2.PRBCの再循環による高MNC濃度および純度の促進
図18に概略的に示されるように、区画38内の血漿の逆流(矢印214)は、界面58を、PRP収集領域76の方に引き戻す。このPRP収集領域76で、増強された動径方向の血漿流れ状態が、界面58から血小板を取り除いて、供血者/患者に戻す。逆流パターン214はまた、リンパ球、単球、および顆粒球などの、界面58のその他のより重い成分を循環させ、再びPRBC質量内に循環させる。
一方、PRBC収集領域80のヘマトクリットが比較的高いため、MNCは、領域80付近で、界面58の表面に浮かぶ。そこで、MNCは、血漿逆流214により、低ヘマトクリットPRP収集領域76の方に引き寄せられる。この領域76のヘマトクリットがより低いため、MNCは、再び高G壁24の方に移動する。図18の矢印216は、MNCが区画38に蓄積するときのMNCの所望の循環流を示す。
PRBC収集領域50において所望のPRBC流出ヘマトクリットHoを維持することが重要である。PRBCの流出ヘマトクリットHoが、所定の低しきい値(例えば、約60%)を下回ると、MNCの大多数は、図18の矢印216で示されるように、細胞質量として循環しない。低Hoに曝露されると、MNCのすべてまたは幾つかは、界面58の方に浮かばない。その代わりに、MNCは、高G壁に沿って集まったままとなり、PRBCとともに、区画38から運び出される。結果として得られるMNC収率は、不十分である。
一方、Hoが所定の高しきい値(例えば、85%)を上回ると、より重い顆粒球がより多く界面58に浮かぶ。その結果、より少ない顆粒球が、界面58から運び去られ、PRBCとともに供血者/患者に戻される。その代わりに、より多くの顆粒球が、界面58を占有し、MNCに混入する。
この理由のため、MNC収集ステージ232の間、プロセスコントローラ222は、ポンプP4に、チューブT5を流れるPRBCの部分を再循環してWB入口ポート48に戻すよう命令する。図21および図22が示すように、再循環するPRBCは中央カセット23Mを通り、入口ポート48に連結されたチューブT4に結合するチューブT6に流れる。再循環するPRBCは、血液処理区画38に入るWBと混ざる。
概して、流出ヘマトクリットHoの大きさは、ポンプP4(PRBC)およびポンプP2(WB)により左右されるPRBC再循環流量Qrの関数として逆に変わる。ポンプP2により設定されたWB流量が与えられると、流出ヘマトクリットHoは、Qrを低下させることにより増加され得、逆に、流出ヘマトクリットHoは、Qrを増加させることにより低減され得る。QrとHoとの間の厳密な関係は、区画38内での流体の遠心加速度(区画38内の遠心力の大きさにより左右される)と、区画38の面積と、区画38への流入流量全血(Qb)(ポンプP2により左右される)および区画38からの流出流量PRP(Qp)(界面制御ポンプP5により左右される)とを考慮に入れる。
この関係を表し、それによりQrを所望のHoに基づいて定量化する方法には様々なものがある。示された実施形態では、コントローラ222は、Qb、QpおよびQrを周期的にサンプリングする。区画38内で活性(active)である遠心力ファクタをさらに考慮して、コントローラは、以下のように、目標のHoに基づいて、ポンプP4の新しいPRBC再循環ポンプレートQr(NEW)を得る。
(i)サンプル時間n=0で開始する。
(ii)現在のQrを以下のように計算する。
ここで、
Hoは、目標の流出ヘマトクリット値であり、小数で表される(例えば、75%の場合、0.75)。
aは、遠心力により左右される流体の加速度であり、以下のように計算される。
ここで、
Ωは、区画38の回転レートであり、ラジアン/秒で表される。
rは、回転の半径である。
gは、単位重力であり、981cm/sec2に等しい。
Aは、区画38の面積である。
kは、ヘマトクリット定数であり、mは、分離性能定数である。kおよびmは、経験データおよび/または理論モデリングに基づいて得られる。好適な実施形態では、以下の理論モデルが使用される。
であり、
βは、剪断に敏感な項であり、以下のように規定される。
ここで、
経験データに基づいて、b=6.0s-nであり、n=0.75であり、剪断レートは、以下のように規定される。
ここで、(u)は、流体速度であり、(y)は、空間寸法である。
そして、
Srは、経験的に得られる赤血球沈降ファクタであり、このファクタは、実験データに基づいて、95×10-9sに設定され得る。
このモデルは、Brown、「The Physics of Continuous Flow Centrifugal Cell Separation」、Artificial Organs;13(1):4-20、Raven Press, Ltd.、New York(1989)(「Brown Article」)の式(19)に基づくものである。本明細書において、上記文献を参考として援用する。このモデルのプロットは、Brown Articleの図9に出てくる。
上記モデルは、予想される実際的な血液処理状態動作範囲にわたって単純な線形回帰を用いて線形化される。代数代入(algebraic substitutions)は、以下の式に基づいて行われる。
ここで、Qoは、出口チューブT5を流れるPRBCの流量であり、以下のように表され得る。
この線形化により、(m)の値が傾きを構成し、(k)の値がy切片を構成する単純化された曲線が得られる。
この単純化された曲線において、傾き(m)は、以下のように表される。
ここで、
β/Srは、経験データに基づいて、1.57/μsの一定値として表され得る。
従って、単純化された曲線において、mは、531.13の値を有する。mの値については、約500と約600との間の範囲が、概して、遠心力による連続流れ全血分離手順に適用可能であると考えられる。
単純化された曲線の場合、(k)のy切片値は、0.9489に等しい。kの値については、約0.85と約1.0との間の範囲が、概して、遠心力による連続流れ全血分離手順に適用可能であると考えられる。
(iii)平均Qrを計算する。
Qrは、選択された間隔で測定され、これらの瞬間測定値が、処理期間にわたって以下のように平均される。
(iv)新しいQrを以下のように計算する。
ここで、
Fは、Qrの制御を可能にする(F=1の場合)か、または、Qrの制御を不能にする(F=0の場合)か、または、システムの変動に基づいてQrのスケーリングを可能にする(Fが0と1との間の分数として表される場合)、任意の制御ファクタである。Fは、定数を含んでいてもよく、あるいは、処理時間の関数として変動してもよく、例えば、所定手順の開始時に第1の値で始まり、手順が進むに従って第2またはそれ以上の値に変わってもよい。
(v)Qrを所定の範囲内(例えば、0ml/minと20ml/minとの間)に維持する。
MNC収集ステージ232(図22)の間、コントローラ222は、高純度MNCの高収率の蓄積に最適な区画38の処理状態を達成するように、多数のポンプ流量を同時に設定し且つ維持する。コントローラは、WB流入流量Qb(ポンプP2を介して)と、PRP流出流量Qp(ポンプP5を介して)と、PRP再循環流量QRecirc(ポンプP6を介して)と、PRBC再循環流量Qr(ポンプP4を介して)とを設定し且つ維持する。典型的には供血者/患者の快適さと、許容可能な処理時間の達成とに合わせて設定されるWB流入流量Qbが与えられると、コントローラ222は、
(i)ポンプP5に、ランプ84上の所望の界面位置を保持するように設定されたQpを維持するよう命令し、それにより、血漿中の所望の血小板濃度(PPPまたはPRP)を達成し、
(ii)ポンプP6に、所望の流入ヘマトクリットHi(約32%と約34%との間)を保持するように設定されたQRecircを維持するよう命令し、それにより、高い血小板分離効率を達成し、そして、
(iii)ポンプP4に、所望の流出ヘマトクリットHo(約75%と約85%との間)を保持するように設定されたQrを維持するよう命令し、それにより、顆粒球の混入を防ぐとともに、MNC収率を最大にする。
(ii)第2のフェーズ(PRBC収集)
コントローラ222は、予め確立された全血容積(例えば、1500ml〜3000ml)が処理されると、MNC蓄積フェーズ236を終了する。あるいは、MNC蓄積フェーズは、目標のMNC容積が収集されたときに終了されてもよい。
次いで、コントローラ22は、MNC収集ステージ232のPRBC収集フェーズ238に入る。このフェーズ238では、(V14を閉じることにより)PRBCを供血者/患者に戻すのを停止し、(バルブV18を閉じ、ポンプP4を閉ポンプオフ状態にすることにより)PRBCの再循環を停止し、そしてその代わりに(V15を開くことにより)PRBCを容器PRBCに運ぶよう、ポンプステーションPSMの構成が変えられる。
この新しい構成を、図23に示し、さらに以下の表4にまとめる。
このフェーズ238では、ラインT5中のPRBCは、中央カセット23Mを通ってラインT14に運ばれ、そして容器PRBCに運ばれる。コントローラ222は、容器PRBCに所望の容積のPRBC(例えば、35ml〜50ml)が集まるまで、このフェーズ238で動作する。以下により詳細に説明されるように、このPRBC容積は後に、MNC採取ステージ234のMNC除去フェーズ240で使用される。
コントローラ222は、容器PRBCが所望の容積のPRBCを保持していることを(重量スケールWSを用いて、重量測定により)検知すると、PRBC収集フェーズ238を終了する。
このようにして、主処理サイクル230のMNC収集ステージ232を終了する。
2.単核細胞採取ステージ
(i)第1のフェーズ(MNC除去)
コントローラ222は、主処理サイクル230のMNC採取ステージ234に入る。このステージ234の第1のフェーズ240では、全血が引き込まれ、そして血液処理区画38を通らずに再循環されて供血者/患者に戻される。区画38を回転させ続けながら、前のPRBC収集フェーズ238で容器PRBCに収集されたPRBCがWB入口チューブT4を通して処理区画38に戻される。MNC収集ステージ232中に区画38に蓄積されたMNCは、PRPとともに、チューブT10を通って区画38から運び出される。
MNC採取ステージ234のMNC除去フェーズ240中の流体回路15の構成を図24Aに示し、さらに以下の表5にまとめる。
図24Aが示すように、PRBCがポンプP4により容器PRBCからチューブT14およびT6を通してチューブT4に運ばれ、WB入口ポート48を通して区画38に導入されている間、コントローラ222は、PRBC出口チューブT5を閉じる。コントローラ222は、TCYCSTARTでサイクル時間カウンタを開始する。
容器PRBCからWB入口ポート48を通って入るPRBCの流入は、PRP収集領域76のヘマトクリットを増加する。それに応答して、区画38に蓄積されたMNCの集中領域(図18に示されるような)は、界面58の表面に浮かぶ。入ってくるPRBC容積は、PRPを、PRP出口ポート46を通して追い出す。界面58、および界面58とともにMNC集中領域(図24AでMNC領域として示される)もまた、PRP出口ポート46を通して区画38から追い出される。MNC領域は、PRPチューブT10に沿って、光センサOSの方に移動する。
図28が示すように、チューブT10内では、MNC集中領域の前に、PRP領域112がある。この領域112のPRPは、(図24Aが示すように)右カセット23RおよびチューブT12を通して容器PPPに運ばれる。チューブT10内ではまた、MNC集中領域の後に、PRBC領域114が続く。
PRP領域112とMNC集中領域との間に、第1の遷移領域116がある。第1の遷移領域116は、着実に減少する濃度の血小板(図28に正方形模様で示される)と、着実に増加する数のMNC(図28にテクスチャ模様で示される)とからなる。
MNC集中領域とPRBC領域114との間に、第2の遷移領域118がある。第2の遷移領域118は、着実に減少する濃度のMNC(図28にテクスチャ模様で示される)と、着実に増加する数のPRBC(図28に波模様で示される)とからなる。
光センサOSで見ると、MNC領域の前にある領域112および116と、MNC領域の後に続く領域118および114とは、遷移光学密度を示し、これらの密度で、MNC領域が識別され得る。光センサOSは、PRP出口ポート46と右カセット23Rとの間で、チューブT10により運ばれる液体の光学密度の変化を検知する。図28が示すように、光学密度は、MNC領域が光センサOSを通り過ぎて進むに従って、光透過性が高い(即ち、PRP領域112である)ことを示す低い値から、光吸収性が高い(即ち、PRBC領域114である)ことを示す高い値に変わる。
図28に図示される示された実施形態では、光センサOSは、例えばBaxter Healthcare CorporationのFenwal Divisionにより市販されているAutopheresis-C▲R▼などで使用される従来のヘモグロビン検出器である。センサOSは、チューブT10を通して光を出射する赤発光ダイオード102を含む。言うまでもなく、緑または赤外のようなその他の波長を使用してもよい。センサOSはまた、チューブT10の反対側に、PINダイオード検出器106を含む。
コントローラ222は、処理エレメント100を含む。処理エレメント100は、発光装置102および検出器106から受け取った電圧信号を分析して、チューブT10内の液体の光透過を計算する。この光透過を、OPTTRANSと呼ぶ。
OPTTRANSを計算するために、処理エレメント100により様々なアルゴリズムが使用され得る。
例えば、OPTTRANSは、赤発光ダイオード102がオンであり、液体がチューブT10を通って流れているときのダイオード検出器106の出力(RED)に等しい値であり得る。
OPTTRANSを得るために、背景光学「雑音」は、以下のようにREDからフィルタリングされ得る。
ここで、COR(RED SPILL)は、以下のように計算される。
ここで、
REDは、赤発光ダイオード102がオンであり、液体がチューブT10を通って流れているときのダイオード検出器106の出力であり、
REDBKGRDは、赤発光ダイオード102がオフであり、液体がチューブT10を通って流れているときのダイオード検出器106の出力である。
そして、CORREFは、以下のように計算される。
ここで、
REFは、赤発光ダイオード102がオンであるときのダイオードの出力であり、
REFBKGRDは、赤発光ダイオード102がオフであるときのダイオードの出力である。
処理エレメント100は、供血者/患者のPRPがチューブT10を通って運ばれているとき、前のMNC収集ステージ232中のセンサOSからのデータを得ることにより、センサOSを、供血者/患者のPRPの光学密度に正規化する。このデータは、チューブおよび供血者/患者のPRPについてのベースライン光透過値(OPTTRANSBASE)を確立する。例えば、OPTTRANSBASEは、上記のように、フィルタリングされた検出機構またはフィルタリングされていない検出機構のいずれかを用いて、収集ステージ232中の選択された時間に測定され得、例えば、ステージ232の半ばで測定され得る。あるいは、フィルタリングされた検出機構またはフィルタリングされていない検出機構のいずれかを用いて、MNC収集ステージ232中に、光透過値の組が計算される。この値の組は、収集ステージ全体にわたって平均され、OPTTRANSBASEが得られる。
その後のMNC除去フェーズ240の間、処理エレメント100は、MNC除去フェーズ240中のチューブT10およびチューブT10を流れる液体についての1つ以上の光透過値(OPTTRANSHARVEST)を検知し続ける。OPTTRANSHARVESTは、MNC除去フェーズ240の選択された時間(例えば、フェーズ240の半ば)に検知された単一の読み出しを含んでいてもよく、MNC除去フェーズ240の間に得られた多数の読み出しの平均を含んでいてもよい。
処理エレメント100は、OPTTRANSBASEを0.0として確立し、光学飽和値を1.0として確立し、そして、正規化された0.0〜1.0の値の範囲にOPTTRANSHARVESTの値を比例して当てはめることにより、正規化された値DENSITYを得る。
図28が示すように、処理エレメント100は、2つの所定しきい値THRESH(1)およびTHRESH(2)を保持する。THRESH(1)の値は、DENSITYの選択された公称値(例えば、0.0〜1.0の正規化されたスケールでは0.45)に対応する。この公称値は、第1の遷移領域116のMNC濃度が予め選択された処理目標を満たすときに起こると経験的に判定されている値である。THRESH(2)の値は、DENSITYの別の選択された公称値(例えば、0.0〜1.0の正規化されたスケールでは0.85)に対応する。この公称値は、第2の遷移領域118のPRBC濃度が予め選択された処理目標を上回るときに起こると経験的に判定されている値である。
光センサOSと、右カセット23RのバルブステーションV24との間のチューブT10の液体容積は、第1のオフセット容積VOLOFF(1)としてコントローラ222に入力される既知の値を構成する。コントローラ222は、VOLOFF(1)と、ポンプP4のポンプレート(QP4)とに基づいて、以下のように第1の制御時間値Time1を計算する。
示された好適な実施形態では、オペレータは、合計MNC採取容積VOLMNCを増加するために、公称の追加容積を表す第2のオフセット容積VOLOFF(2)(図28に図示)を特定して、コントローラ222に入力し得る。VOLOFF(2)の量は、システムおよび処理の変動と、供血者/患者の間でのMNC純度の変動とを考慮に入れたものである。コントローラ222は、VOLOFF(2)と、ポンプP4のポンプレート(QP4)とに基づいて、以下のように第2の制御時間値Time2を計算する。
ポンプP4の動作によりPRBCがWB入口ポート48を通して運ばれると、界面58およびMNC領域は、PRPチューブT10内を、光センサOSに向かって進む。MNC領域の前にあるPRPは、光センサODを越え、チューブT12を通って容器PPPに入る。
MNC領域が光センサOSに到達すると、センサOSは、DENSITY=THRESH(1)を検知する。この事象が起こると、コントローラ222は、第1の時間カウンタTC1を開始する。光センサOSがDENSITY=THRESH(2)を検知すると、コントローラ222は、第2の時間カウンタTC2を開始する。検知MNC容積は、所定のQP4についてのTC1とTC2との間の間隔に基づいて得られ得る。
時間が進むと、コントローラ222は、TC1の大きさを第1の制御時間T1と比較するとともに、TC2を第2の制御時間T2と比較する。TC1=T1のとき、図24Bが示すように、対象のMNC領域の前縁が、バルブステーションV24に到達している。コントローラ222は、バルブステーションV24に開くよう命令し、バルブステーションV25に閉じるよう命令する。コントローラ222は、サイクル時間カウンタに、この事象をTCYCSWITCHとして記す。対象のMNC領域は、容器MNCに通じるチューブT13に運ばれる。TC2=T2のとき、図24Cが示すように、第2のオフセット容積VOLOFF(2)もまた、チューブT13に運ばれる。それにより、所定のサイクルについて選択された合計MNC採取容積(VOLMNC)が、チューブT13に存在する。TC2=T2になると、コントローラ222は、ポンプP4に、停止するよう命令する。従って、チューブT13内でVOLMNCがそれ以上前進しなくなる。
コントローラ222は、前のMNC除去フェーズ中に容器PPPに運ばれたPRPの容積を得る。このPRP容積(VOLPRPとして示される)は、以下のように得られる。
好適な実施形態では、ポンプP4がTCYCSTART後に特定のPRBC流体容積よりも多くの容積(例えば、60mlよりも多くの容積)を運ぶと、コントローラ222は、TC1およびTC2に関係なくMNC除去フェーズを終了する。このタイムアウト環境は、例えば、光センサOSがTHRESH(1)を検出しない場合などに起こり得る。この容積測定によるタイムアウト環境では、VOLPRP=60−VOLOFF(1)である。
容積測定タイムアウトの代わりに、または容積測定タイムアウトと組み合わせて、コントローラ222は、容器PRBCの重量スケールWSが所定値未満の重量(例えば、4グラム未満、または、4ml未満の流体容積と等価な重量)を検知すると、TC1およびTC2に関係なくMNC除去フェーズを終了してもよい。
(ii)第2のフェーズ(PRPフラッシュ)
一旦MNC領域が図24Cに示されるような位置になると、コントローラ222は、MNC採取ステージ234のPRPフラッシュフェーズ242に入る。このフェーズ242の間、コントローラ222は、VOLPRPを容器PPPおよびチューブT12から出して血液処理区画38に入れるよう回路200を構成する。
PRPフラッシュフェーズ242の間の流体回路200の構成を、図25に示し、さらに表6にまとめる。
PRPフラッシュステージ242の間、コントローラ222は、区画38を回転させ続けながら、全血再循環を停止し、VOLPRPをポンプによりチューブT11を通して処理区画38に送るようポンプステーションPSL、PSMおよびPSRを構成する。VOLPRPは、ポンプP6により、チューブT12を通って右カセット23Rに運ばれ、次いでチューブT11に運ばれ、チューブT4およびポート48を通って処理区画38に入る。PRBCは、処理区画38からポート50およびチューブT5を通って中央カセット23Mに運ばれ、次いでチューブT8およびT7に運ばれて、左カセット23Lに入る。PRBCは、チューブT9に運ばれ、供血者/患者に戻る。このフェーズ242の間、流体回路15において、その他の流体は運ばれない。
VOLPRPを戻すことにより、容器PPP内の液体の容積を、上述の予備処理サイクル228の間に収集されたVOLSUSに回復する。また、VOLPRPを戻すことにより、MNCの懸濁のために予定された容器PPP内のVOLSUS中の低い血小板数(population)が保たれる。また、VOLPRPを戻すことにより、TC1=T1の前に第1の遷移領域116に存在する残留MNCが処理区画38に戻され(従って、VOLMNCの部分は戻されず)、その後の主処理サイクル230においてさらに収集される。
(iii)第3のフェーズ(MNC懸濁)
VOLPRPを区画38に戻して、コントローラ222は、MNC採取ステージ234のMNC懸濁フェーズ244に入る。このフェーズ244の間、容器PPP内のVOLSUSの部分は、VOLMNCとともに容器MNCに運ばれる。
MNC懸濁フェーズ244中の流体回路200の構成を図26に示し、さらに以下の表7にまとめる。
MNC懸濁フェーズ244では、コントローラは、C3を閉じて、PRBCを供血者/患者に戻すのを停止する。VOLSUSの所定のアリコート(例えば、5ml〜10ml)が、ポンプP6によりチューブT12を通して右カセット23Rに運ばれ、次いでチューブT13に運ばれる。図26が示すように、VOLSUSのアリコートは、チューブT13を通るVOLMNCをさらに容器MNCに前進させる。
(iii)第4のフェーズ(クリーンアップ)
このとき、コントローラ222は、MNC採取ステージ234の最後のクリーンアップフェーズ246に入る。このフェーズ246の間、コントローラ222は、チューブT10にあるPRBCを所定区画38に戻す。
クリーンアップフェーズ246中の流体回路200の構成を図27に示し、さらに以下の表7にまとめる。
クリーンアップフェーズ246は、TC2=T2の後に第2の遷移領域118(図28参照)にあるいかなる残留MNCも処理区画38に戻し(従って、VOLSENの部分は戻さず)、その後の処理サイクルにおいてさらに収集される。
クリーンアップフェーズ246では、コントローラ222は、左および中央カセット23Lおよび23Mのすべてのバルブステーションを閉じ、そして、PRBCをチューブT10から循環させてチューブT11およびT4を通して処理区画38に戻すよう右ポンプステーションPSRを構成する。この期間中、供血者/患者からはいかなる成分も引き込まれておらず、または、供血者/患者にはいかなる成分も戻されていない。
クリーンアップフェーズ246の終わりで、コントローラ222は、新しい主処理サイクル230を開始する。コントローラ222は、手順全体で目標にされた所望のMNC容積に達するまで、主処理サイクル230の連続を繰り返す。
最後の主処理サイクル230の終わりで、オペレータは、手順中に収集されたMNCをさらに希釈するために、追加のVOLSUSを求め得る。この環境では、コントローラ222は、上記のような予備処理サイクル228を実行して容器PPPに追加のVOLSUSを収集するように流体回路200を構成するよう命令され得る。次いで、コントローラ222は、MNC懸濁フェーズ244を実行して追加のVOLSUSを容器MNCに運び、VOLMNCの所望の希釈を達成するように流体回路200を構成する。
IV.別の単核細胞処理手順
図29は、MNCの収集および採取に適した流体回路300の別の実施形態を示す。回路300は、ほとんどの点で、図6に示される回路200と同じであり、共通の構成要素には、同じ参照番号が付されている。
回路300は、容器14の第2の区画310が区画38と同一であり、それにより、第2の区画310自体が、区画38と同じ特徴を有する第2の血液処理区画を含むという点で、回路200とは異なる。区画310は、図4で区画38について示されたような内部シールを含み、PRPおよびPRBCのための同じ血液収集領域を作り出すため、これらの血液収集領域の詳細は、図29には示されていない。区画310は、全血を区画310に運ぶためのポート304と、区画310からPRPを運ぶためのポート306と、区画310からPRBCを運ぶためのポート302とを含む。区画310はまた、図16Aおよび図16Bに示され、区画38に関して以前に説明されたようなテーパ状のランプ84を含む。
流体回路300はまた、チューブT14、T18およびT19が含まれないという点でも、流体回路200とは異なる。さらに、容器PRBCが含まれない。その代わりに、流体回路300は、以下のような幾つかの新しいチューブ経路およびクランプを含む。
チューブ経路T21は、区画310のPRP出口ポート306から、新しいクランプC5を通って、チューブ経路T10に結合する。
チューブ経路T22は、区画310のWB入口ポート306から、新しい空気検出器D3および新しいクランプC6を通って、チューブ経路T3に結合する。
チューブ経路T33は、区画310のPRBC出口ポート302から、新しいクランプC8を通って、チューブT4に結合する。
新しいクランプC7は、空気検出器D1の上流のチューブT3にも設けられる。
新しいクランプC9は、光センサOSと新しいチューブT21の結合部との間のチューブT10にも設けられる。
回路300を用いて、コントローラ222は、回路200について以前に説明された上記のプライミングサイクル226、予備処理サイクル228、および主処理サイクル230を進み、MNC蓄積フェーズ236まで進む。回路300を使用する場合、PRBC収集フェーズ238は、その後に区画38からMNCを除去するために使用されるPRBCが、第2の区画310で処理および収集されるという点で異なる。
具体的には、図30に示されるように、PRBC収集フェーズ238の間、コントローラ222は、供血者/患者からの全血の容積を第2の区画310に運ぶ。全血容積は、ポンプP2により、チューブT1を通ってチューブT3内に引き込まれ、次いで、開いたクランプC6を通って、区画310につながるチューブT22に引き込まれる。採取のためにMNCが蓄積されている区画38への全血の運搬を遮るために、クランプC7が閉じられる。区画38からのPRPの運搬を遮るために、クランプC9も閉じられ、それにより、区画38においてMNCの蓄積が乱されない状態に保つ。
区画310において、全血容積は、区画38でPRBCおよびPRPが分離された態様と同じ態様で、PRBCとPRPとに分離される。PRPは、ポンプP5の動作により、区画310からチューブT23と開いたクランプC5とを通って運ばれ、供血者/患者に戻される。区画310にPRBCを保持するために、クランプC8は閉じられる。
コントローラ222はまた、回路300を用いて異なるMNC除去フェーズ240を行う。図31に示されるように、MNC除去フェーズ240の間、コントローラ222は、引き込まれた全血の部分を再循環して供血者/患者に戻し、全血の別の部分を、図30に関して以前に説明された経路と同じ経路をたどって区画310に送る。コントローラ222は、クランプC8およびC9を開き、クランプC5を閉じる。区画310に入る全血は、PRBCを、PRBC出口ポート302を通してチューブT23に追い出す。区画310からのPRBCは、区画38のWB入口ポート48に入る。上記のように、区画38の外側から入ってくるPRBCの流れは、区画38内のPRBCのヘマトクリットを増加し、蓄積されたMNCを界面58に浮かばせる。上記のように、区画38の外側から入ってくるPRBCは、図31に示されるMNC領域とともに、PRPを、PRPポート46を通して追い出す。このMNC領域は、回路200について説明された態様と同じ態様で、光センサOSにより検出され、そしてその後の処理242、244および246で採取される。
本発明の様々な特徴は、以下の請求の範囲に示される。
Claims (8)
- 全血から単核細胞を分離するシステムであって、
回転軸を中心に回転するチャンバであって、該チャンバは、入口領域を含み、全血は、該入口領域に入って、濃縮赤血球と、血漿成分と、該濃縮赤血球と該血漿成分との間で血小板および単核細胞を保持する界面とに分離される、チャンバと、
第1の収集容器と、
第2の収集容器と、
ポンプと、
該入口領域に該全血を運びながら、該チャンバから該濃縮赤血球および該血漿成分を除去するように動作可能なコントローラと、を含み、該コントローラは、(i)該血小板および該単核細胞を、該チャンバ内に、該第1の容器に通じ該第2の容器には通じていない経路で、該チャンバから血小板の乏しい血漿を除去することを可能にするために保持する該チャンバ内の第1の位置に該界面を位置決めするようにポンプの流速を設定する第1の状態と、(ii)該単核細胞を、該チャンバ内に、該第1および第2の容器を迂回する経路で、該チャンバから血小板の豊富な血漿を除去することを可能にしながら保持する、該第1の状態より比較的より高い位置に該界面を位置決めするように該ポンプの流速を設定する第2の状態と、(iii)該第2の容器に通じ該第1の容器には通じていない経路で、該チャンバから該単核細胞を除去することを可能にする、該第2の状態におけるより該チャンバー内の比較的より高い位置で該界面を位置決めするように該ポンプの流速を設定する第3の状態とで動作する界面制御ユニットを含み、
該コントローラはさらに、該血小板の乏しい血漿を該第1の容器から該第2の容器に送り、該第2の容器で、該除去された単核細胞を希釈するように該ポンプを動作する、システム。 - 前記界面制御ユニットが、前記チャンバ内の前記界面の場所を特定して検知出力を提供する検知エレメントを含む、請求項1に記載のシステム。
- 前記検知エレメントが、前記チャンバ内の前記界面の場所を光学的に特定する、請求項2に記載のシステム。
- 希釈された単核細胞を収集する方法であって、
チャンバを回転軸を中心に回転させる工程と、
全血を該チャンバの入口領域に運び、濃縮赤血球と、血漿成分と、該濃縮赤血球と該血漿成分との間で血小板および単核細胞を保持する界面とに分離する工程と、
該界面を、該チャンバ内で第1の位置に、該血小板および該単核細胞を該チャンバ内に保持して、第1の容器に通じ第2の容器には通じていない経路で、該チャンバから血小板の乏しい血漿を除去することを可能にするために維持するように該チャンバ中への、そして/または該チャンバからの流速を設定する工程と、
該界面を、該チャンバ内で該第1の位置より比較的より高い第2の位置に、該単核細胞を該チャンバ内に保持しながら、該第1および第2の容器を迂回する経路で、該チャンバから血小板の豊富な血漿を除去することを可能にするために維持するように該チャンバ中への、そして/または該チャンバからの流速を設定する工程と、
該界面を、該チャンバ内で該第2の位置より比較的より高い第3の位置に、該第2の容器に通じ該第1の容器には通じていない経路で、該チャンバから該単核細胞を除去することを可能にするために維持するように該チャンバ中への、そして/または該チャンバからの流速を設定する工程と、
該血小板の乏しい血漿を該第1の容器から該第2の容器に送り、該第2の容器で、該除去された単核細胞を希釈する工程と、を包含する、方法。 - 前記界面を前記第1、第2および第3の状態に維持する前記工程の少なくとも1つが、前記チャンバ内の該界面の場所を検知する工程を包含する、請求項4に記載の方法。
- 前記検知工程が、前記チャンバ内の前記界面の場所を光学的に特定する工程を包含する、請求項5に記載の方法。
- 前記コントローラがさらに、前記第2の状態において、前記血小板の豊富な血漿の少なくとも一部を前記チャンバの前記入口領域への再循環を可能にするように動作する、請求項1に記載のシステム。
- 前記チャンバから除去した前記血小板の豊富な血漿の少なくとも一部を、該チャンバの入口領域へと再循環させる工程を包含する、請求項4に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/886,732 US6027657A (en) | 1997-07-01 | 1997-07-01 | Systems and methods for collecting diluted mononuclear cells |
| US08/886,732 | 1997-07-01 | ||
| PCT/US1998/012166 WO1999001197A1 (en) | 1997-07-01 | 1998-06-22 | Systems and methods for collecting diluted mononuclear cells |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2002509534A JP2002509534A (ja) | 2002-03-26 |
| JP2002509534A5 JP2002509534A5 (ja) | 2005-12-22 |
| JP4076587B2 true JP4076587B2 (ja) | 2008-04-16 |
Family
ID=25389648
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP50717199A Expired - Fee Related JP4076587B2 (ja) | 1997-07-01 | 1998-06-22 | 希釈された単核細胞を収集するシステムおよび方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US6027657A (ja) |
| EP (2) | EP1024872B1 (ja) |
| JP (1) | JP4076587B2 (ja) |
| CN (1) | CN1261815A (ja) |
| BR (1) | BR9810661A (ja) |
| CA (1) | CA2294395A1 (ja) |
| WO (1) | WO1999001197A1 (ja) |
Families Citing this family (83)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5958250A (en) * | 1995-06-07 | 1999-09-28 | Baxter International Inc. | Blood processing systems and methods which optically derive the volume of platelets contained in a plasma constituent |
| US6312607B1 (en) | 1995-06-07 | 2001-11-06 | Baxter International Inc. | Blood processing systems and methods which optically monitor incremental platelet volumes in a plasma constituent |
| US20020077241A1 (en) * | 1999-09-03 | 2002-06-20 | Baxter International Inc. | Blood processing systems and methods with quick attachment of a blood separation chamber to a centrifuge rotor |
| US6315707B1 (en) | 1999-09-03 | 2001-11-13 | Baxter International Inc. | Systems and methods for seperating blood in a rotating field |
| US6524231B1 (en) * | 1999-09-03 | 2003-02-25 | Baxter International Inc. | Blood separation chamber with constricted interior channel and recessed passage |
| US7011761B2 (en) * | 1999-09-03 | 2006-03-14 | Baxter International Inc. | Red blood cell processing systems and methods which control red blood cell hematocrit |
| US6294094B1 (en) | 1999-09-03 | 2001-09-25 | Baxter International Inc. | Systems and methods for sensing red blood cell hematocrit |
| US6348156B1 (en) | 1999-09-03 | 2002-02-19 | Baxter International Inc. | Blood processing systems and methods with sensors to detect contamination due to presence of cellular components or dilution due to presence of plasma |
| US6860846B2 (en) * | 1999-09-03 | 2005-03-01 | Baxter International Inc. | Blood processing systems and methods with umbilicus-driven blood processing chambers |
| US6322488B1 (en) * | 1999-09-03 | 2001-11-27 | Baxter International Inc. | Blood separation chamber with preformed blood flow passages and centralized connection to external tubing |
| US6284142B1 (en) | 1999-09-03 | 2001-09-04 | Baxter International Inc. | Sensing systems and methods for differentiating between different cellular blood species during extracorporeal blood separation or processing |
| US7430478B2 (en) | 2000-03-01 | 2008-09-30 | Caridian Bct, Inc. | Blood processing information system with blood loss equivalency tracking |
| CA2370758A1 (en) * | 2000-03-01 | 2001-09-07 | Gambro, Inc. | Extracorporeal blood processing information management system |
| US6890291B2 (en) * | 2001-06-25 | 2005-05-10 | Mission Medical, Inc. | Integrated automatic blood collection and processing unit |
| US6878105B2 (en) * | 2001-08-16 | 2005-04-12 | Baxter International Inc. | Red blood cell processing systems and methods with deliberate under spill of red blood cells |
| US7479123B2 (en) * | 2002-03-04 | 2009-01-20 | Therakos, Inc. | Method for collecting a desired blood component and performing a photopheresis treatment |
| US7186230B2 (en) * | 2002-03-04 | 2007-03-06 | Therakos, Inc | Method and apparatus for the continuous separation of biological fluids into components |
| US7211037B2 (en) * | 2002-03-04 | 2007-05-01 | Therakos, Inc. | Apparatus for the continuous separation of biological fluids into components and method of using same |
| WO2003089926A2 (en) * | 2002-04-19 | 2003-10-30 | Mission Medical, Inc. | Integrated automatic blood processing unit |
| US6849039B2 (en) * | 2002-10-24 | 2005-02-01 | Baxter International Inc. | Blood processing systems and methods for collecting plasma free or essentially free of cellular blood components |
| US7297272B2 (en) * | 2002-10-24 | 2007-11-20 | Fenwal, Inc. | Separation apparatus and method |
| US20050049539A1 (en) * | 2003-09-03 | 2005-03-03 | O'hara Gerald P. | Control system for driving fluids through an extracorporeal blood circuit |
| US7708710B2 (en) * | 2003-12-23 | 2010-05-04 | Fenwal, Inc. | Method and apparatus for collecting and processing blood |
| US7476209B2 (en) * | 2004-12-21 | 2009-01-13 | Therakos, Inc. | Method and apparatus for collecting a blood component and performing a photopheresis treatment |
| US8075468B2 (en) * | 2008-02-27 | 2011-12-13 | Fenwal, Inc. | Systems and methods for mid-processing calculation of blood composition |
| US8685258B2 (en) * | 2008-02-27 | 2014-04-01 | Fenwal, Inc. | Systems and methods for conveying multiple blood components to a recipient |
| US8394006B2 (en) | 2010-11-19 | 2013-03-12 | Kensey Nash Corporation | Centrifuge |
| US8556794B2 (en) | 2010-11-19 | 2013-10-15 | Kensey Nash Corporation | Centrifuge |
| US8469871B2 (en) | 2010-11-19 | 2013-06-25 | Kensey Nash Corporation | Centrifuge |
| US8870733B2 (en) | 2010-11-19 | 2014-10-28 | Kensey Nash Corporation | Centrifuge |
| US8317672B2 (en) | 2010-11-19 | 2012-11-27 | Kensey Nash Corporation | Centrifuge method and apparatus |
| US9744498B2 (en) | 2011-03-11 | 2017-08-29 | Fenwal, Inc. | Disposable fluid circuits and methods for cell washing with on-line dilution of cell feed |
| WO2013043433A2 (en) | 2011-09-22 | 2013-03-28 | Fenwal, Inc. | Disposable fluid circuits and methods for cell washing |
| US9402866B2 (en) | 2011-04-07 | 2016-08-02 | Fenwal, Inc. | Automated methods and systems for providing platelet concentrates with reduced residual plasma volumes and storage media for such platelet concentrates |
| US9089479B2 (en) | 2011-05-03 | 2015-07-28 | Fenwal, Inc. | Medium, solutions and methods for the washing, culturing and storage of white blood cells |
| US9347540B2 (en) * | 2011-09-22 | 2016-05-24 | Fenwal, Inc. | Flexible shaft drive system for centrifuge with pivoting arms |
| WO2013043316A1 (en) * | 2011-09-22 | 2013-03-28 | Fenwal, Inc. | Drive system for centrifuge |
| US9399093B2 (en) | 2012-01-27 | 2016-07-26 | Fenwal, Inc. | Systems and methods for performing online extracorporeal photopheresis |
| US20130252227A1 (en) | 2012-03-20 | 2013-09-26 | Fenwal, Inc. | Apparatus and Method for Providing Cryopreserved ECP-Treated Mononuclear Cells |
| US20190224494A1 (en) * | 2012-03-20 | 2019-07-25 | Fenwal, Inc. | Apparatus and method for batch photoactivation of mononuclear cells with cryopreservation |
| US11571504B2 (en) | 2019-03-21 | 2023-02-07 | Fenwal, Inc. | Apparatus and method for batch photoactivation of mononuclear cells |
| US9393359B2 (en) * | 2012-04-10 | 2016-07-19 | Fenwal, Inc. | Systems and methods for achieving target post-procedure fraction of cells remaining, hematocrit, and blood volume during a therapeutic red blood cell exchange procedure with optional isovolemic hemodilution |
| US9733805B2 (en) | 2012-06-26 | 2017-08-15 | Terumo Bct, Inc. | Generating procedures for entering data prior to separating a liquid into components |
| CN104383726B (zh) * | 2012-07-30 | 2016-05-25 | 第五空间健康管理江苏有限公司 | 富血小板血浆的提取方法和提取的富血小板血浆 |
| US10172995B2 (en) | 2013-02-06 | 2019-01-08 | Fenwal, Inc. | System and method for determining irradiation exposure time with irradiation sensors during extracorporeal photopheresis |
| US9974899B2 (en) | 2013-02-06 | 2018-05-22 | Fenwal, Inc. | Method for delivering desired light dose to cells in a light attenuating medium |
| US10213544B2 (en) | 2013-06-13 | 2019-02-26 | Fenwal, Inc. | Methods for treating a suspension of mononuclear cells to facilitate extracorporeal photopheresis |
| KR102502975B1 (ko) | 2014-01-31 | 2023-02-23 | 디에스엠 아이피 어셋츠 비.브이. | 지방 조직 원심 분리기 및 그 사용 방법 |
| US9597444B2 (en) | 2014-05-12 | 2017-03-21 | Fenwal, Inc. | Systems and methods for determining replacement fluid and plasma flow rates for red blood cell exchange procedures |
| US20160114095A1 (en) | 2014-10-27 | 2016-04-28 | Fenwal, Inc. | Methods and systems for collecting mononuclear cells |
| US9833557B2 (en) | 2014-12-19 | 2017-12-05 | Fenwal, Inc. | Systems and methods for determining free plasma hemoglobin |
| JP6632359B2 (ja) | 2015-01-05 | 2020-01-22 | フェンウォール、インコーポレイテッド | 体外フォトフェレーシスにおいて照射受光部を用いて最小ヘマトクリットを検出するためのシステムと方法 |
| EP3053616A1 (en) | 2015-02-06 | 2016-08-10 | Fenwal, Inc. | System and method for determining irradiation exposure time with irradiation sensors during extracorporeal photopheresis |
| US9816073B2 (en) | 2015-07-27 | 2017-11-14 | Fenwal, Inc. | Systems and methods for detecting fluid leaks using a non-contact sensor |
| US20170028121A1 (en) | 2015-07-31 | 2017-02-02 | Fenwal, Inc. | Irradiation device for biological fluids |
| US10434240B2 (en) * | 2015-08-17 | 2019-10-08 | Fenwal, Inc. | Methods and systems for processing and washing a photopheresis mononuclear cell product |
| US11383015B2 (en) | 2016-01-11 | 2022-07-12 | Fenwal, Inc. | System and method for plasma purification prior to mononuclear cell collection |
| US11793720B2 (en) * | 2016-01-29 | 2023-10-24 | Terumo Kabushiki Kaisha | Medical bag hanger and blood collection device package |
| US10363355B2 (en) | 2016-09-21 | 2019-07-30 | Fenwal, Inc. | System and method for platelet removal during mononuclear cell collection |
| US20180078694A1 (en) * | 2016-09-21 | 2018-03-22 | Fenwal, Inc. | Disposable Fluid Circuits for Extracorporeal Photopheresis with Integrated Source of Photoactive Agent |
| US11364331B2 (en) * | 2016-09-21 | 2022-06-21 | Fenwal, Inc. | Methods and systems for maintaining patient fluid balance during an extracorporeal therapeutic cell treatment |
| EP3354300B1 (en) | 2017-01-30 | 2020-08-05 | Fenwal, Inc. | Systems for collecting mononuclear cells having a suitable hematocrit for extracorporeal photopheresis |
| EP3372259B1 (en) * | 2017-03-07 | 2022-11-23 | Fenwal, Inc. | System and methods for separating blood under conditions of reduced plasma clarity |
| CN107189975B (zh) * | 2017-05-26 | 2020-12-25 | 奥凯(苏州)生物技术有限公司 | 一种封闭式细胞扩增系统的细胞收集方法 |
| EP3422354A1 (en) | 2017-06-29 | 2019-01-02 | Fenwal, Inc. | System and method for authenticating medical device disposable components |
| EP3461510B1 (en) | 2017-10-02 | 2022-04-27 | Fenwal, Inc. | Systems and methods for returning treated mononuclear cells to a blooo source |
| EP4112093A1 (en) | 2017-10-02 | 2023-01-04 | Fenwal, Inc. | Systems and methods for monitoring and controlling fluid balance during a biological fluid procedure |
| US11679193B2 (en) | 2017-12-20 | 2023-06-20 | Fenwal, Inc. | System and method of collecting and infusing an apoptotic white blood cell component and a transplant component |
| WO2019140491A1 (en) * | 2018-01-22 | 2019-07-25 | Scinogy Products Pty Ltd | System, method and controller for recovery of concentrated particles suspended in fluid |
| US11318239B2 (en) | 2018-03-01 | 2022-05-03 | Fenwal, Inc. | Systems and methods for performing online extracorporeal photopheresis |
| US11904081B2 (en) * | 2018-05-11 | 2024-02-20 | Lupagen, Inc. | Systems and methods for closed loop, real-time modifications of patient cells |
| US10886022B2 (en) | 2018-05-18 | 2021-01-05 | Fenwal, Inc. | System and method for authenticating disposable components in extracorporeal photopheresis |
| US11678825B2 (en) * | 2018-10-04 | 2023-06-20 | Fenwal, Inc. | Methods and systems for collecting samples in a photopheresis procedure |
| US20200188685A1 (en) | 2018-12-13 | 2020-06-18 | Fenwal Inc. | Systems and Methods for Treating a Biological Fluid with Light in the Event of a Bulb Outage |
| EP3679968A3 (en) | 2019-01-10 | 2020-10-07 | Fenwal, Inc. | Systems and methods for verifying that a biological product is ready for treatment |
| US11311823B2 (en) | 2019-03-05 | 2022-04-26 | Fenwal, Inc. | Collection of mononuclear cells and peripheral blood stem cells |
| US11883543B2 (en) | 2019-04-16 | 2024-01-30 | Fenwal, Inc. | Systems and methods for photoactivation of a biological fluid |
| US11517919B2 (en) | 2019-06-06 | 2022-12-06 | Fenwal, Inc. | Systems and methods for harvesting MNCs as part of a plasma collection procedure |
| EP3868477A1 (en) * | 2020-02-18 | 2021-08-25 | Alfa Laval Corporate AB | Centrifugal separator for separating a liquid mixture |
| US20220347368A1 (en) | 2021-04-13 | 2022-11-03 | Fenwal, Inc. | Systems and methods for performing extracorporeal photopheresis |
| US20230044027A1 (en) * | 2021-08-06 | 2023-02-09 | Fenwal, Inc. | Systems and methods for separation of platelets from blood and return of mononuclear cells |
| US20230043534A1 (en) | 2021-08-06 | 2023-02-09 | Fenwal, Inc. | Systems and Methods for Converting an Apheresis Fluid Processing Circuit to Single or Double Needle Mode |
| EP4309694A1 (en) | 2022-07-22 | 2024-01-24 | Fenwal, Inc. | Blood processing and treatment systems and methods with procedure estimator |
Family Cites Families (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3145713A (en) * | 1963-09-12 | 1964-08-25 | Protein Foundation Inc | Method and apparatus for processing blood |
| US3655123A (en) * | 1966-08-08 | 1972-04-11 | Us Health Education & Welfare | Continuous flow blood separator |
| US3519201A (en) * | 1968-05-07 | 1970-07-07 | Us Health Education & Welfare | Seal means for blood separator and the like |
| BE794220A (fr) * | 1972-01-28 | 1973-05-16 | Ibm | Reservoir destine notamment au traitement du sang |
| US4934995A (en) * | 1977-08-12 | 1990-06-19 | Baxter International Inc. | Blood component centrifuge having collapsible inner liner |
| US4113173A (en) * | 1975-03-27 | 1978-09-12 | Baxter Travenol Laboratories, Inc. | Centrifugal liquid processing apparatus |
| US3957197A (en) * | 1975-04-25 | 1976-05-18 | The United States Of America As Represented By The United States Energy Research And Development Administration | Centrifuge apparatus |
| US4010894A (en) * | 1975-11-21 | 1977-03-08 | International Business Machines Corporation | Centrifuge fluid container |
| US4007871A (en) * | 1975-11-13 | 1977-02-15 | International Business Machines Corporation | Centrifuge fluid container |
| US4425112A (en) * | 1976-02-25 | 1984-01-10 | The United States Of America As Represented By The Department Of Health And Human Services | Flow-through centrifuge |
| US4636193A (en) * | 1976-05-14 | 1987-01-13 | Baxter Travenol Laboratories, Inc. | Disposable centrifugal blood processing system |
| US4430072A (en) * | 1977-06-03 | 1984-02-07 | International Business Machines Corporation | Centrifuge assembly |
| US4094461A (en) * | 1977-06-27 | 1978-06-13 | International Business Machines Corporation | Centrifuge collecting chamber |
| US4419089A (en) * | 1977-07-19 | 1983-12-06 | The United States Of America As Represented By The Department Of Health And Human Services | Blood cell separator |
| US5006103A (en) * | 1977-08-12 | 1991-04-09 | Baxter International Inc. | Disposable container for a centrifuge |
| US4114802A (en) * | 1977-08-29 | 1978-09-19 | Baxter Travenol Laboratories, Inc. | Centrifugal apparatus with biaxial connector |
| US4191182A (en) * | 1977-09-23 | 1980-03-04 | Hemotherapy Inc. | Method and apparatus for continuous plasmaphersis |
| US4387848A (en) * | 1977-10-03 | 1983-06-14 | International Business Machines Corporation | Centrifuge assembly |
| US4164318A (en) * | 1977-10-12 | 1979-08-14 | Baxter Travenol Laboratories, Inc. | Centrifugal processing apparatus with reduced-load tubing |
| US4146172A (en) * | 1977-10-18 | 1979-03-27 | Baxter Travenol Laboratories, Inc. | Centrifugal liquid processing system |
| US4386730A (en) * | 1978-07-21 | 1983-06-07 | International Business Machines Corporation | Centrifuge assembly |
| SE412528B (sv) * | 1978-07-25 | 1980-03-10 | Separex Sa | Centrifugrotor och kollaberbar separationsbehallare |
| US4283004A (en) * | 1979-08-15 | 1981-08-11 | Baxter Travenol Laboratories, Inc. | Vibration attenuation support assembly for a centrifugal liquid processing apparatus |
| US4464167A (en) * | 1981-09-03 | 1984-08-07 | Haemonetics Corporation | Pheresis apparatus |
| US4447221A (en) * | 1982-06-15 | 1984-05-08 | International Business Machines Corporation | Continuous flow centrifuge assembly |
| SE8302215D0 (sv) * | 1983-04-20 | 1983-04-20 | Alfa Laval Marine Power Eng | Centrifugalseparator |
| US4605503A (en) * | 1983-05-26 | 1986-08-12 | Baxter Travenol Laboratories, Inc. | Single needle blood fractionation system having adjustable recirculation through filter |
| FR2548541B1 (fr) * | 1983-07-07 | 1986-09-12 | Rhone Poulenc Sa | Procede de plasmapherese et appareillage utilisable notamment pour ce procede |
| FR2548907B1 (fr) * | 1983-07-13 | 1985-11-08 | Rhone Poulenc Sa | Procede de plasmapherese et appareillage utilisable notamment pour ce procede |
| US4530691A (en) * | 1983-12-13 | 1985-07-23 | Baxter Travenol Laboratories, Inc. | Centrifuge with movable mandrel |
| DE3410286C2 (de) * | 1984-03-21 | 1986-01-23 | Fresenius AG, 6380 Bad Homburg | Verfahren zur Trennung von Blut sowie Vorrichtung zur Durchführung des Verfahrens |
| US4776964A (en) * | 1984-08-24 | 1988-10-11 | William F. McLaughlin | Closed hemapheresis system and method |
| JPS61245855A (ja) * | 1985-04-22 | 1986-11-01 | Green Cross Corp:The | 連続式血液分離装置 |
| US4647279A (en) * | 1985-10-18 | 1987-03-03 | Cobe Laboratories, Inc. | Centrifugal separator |
| US4724317A (en) * | 1985-12-05 | 1988-02-09 | Baxter Travenol Laboratories, Inc. | Optical data collection apparatus and method used with moving members |
| US4670002A (en) * | 1985-12-09 | 1987-06-02 | Hitachi Koki Company, Ltd. | Centrifugal elutriator rotor |
| US4708712A (en) * | 1986-03-28 | 1987-11-24 | Cobe Laboratories, Inc. | Continuous-loop centrifugal separator |
| US5076911A (en) * | 1987-01-30 | 1991-12-31 | Baxter International Inc. | Centrifugation chamber having an interface detection surface |
| US5370802A (en) * | 1987-01-30 | 1994-12-06 | Baxter International Inc. | Enhanced yield platelet collection systems and methods |
| US4834890A (en) * | 1987-01-30 | 1989-05-30 | Baxter International Inc. | Centrifugation pheresis system |
| US5104526A (en) * | 1987-01-30 | 1992-04-14 | Baxter International Inc. | Centrifugation system having an interface detection system |
| US4806252A (en) * | 1987-01-30 | 1989-02-21 | Baxter International Inc. | Plasma collection set and method |
| US5573678A (en) * | 1987-01-30 | 1996-11-12 | Baxter International Inc. | Blood processing systems and methods for collecting mono nuclear cells |
| US4936820A (en) * | 1988-10-07 | 1990-06-26 | Baxter International Inc. | High volume centrifugal fluid processing system and method for cultured cell suspensions and the like |
| US5078671A (en) * | 1988-10-07 | 1992-01-07 | Baxter International Inc. | Centrifugal fluid processing system and method |
| US5316667A (en) * | 1989-05-26 | 1994-05-31 | Baxter International Inc. | Time based interface detection systems for blood processing apparatus |
| CA2103911C (en) * | 1991-12-23 | 1999-08-24 | Warren P. Williamson, Iv | Centrifuge with separable bowl and spool elements providing access to the separation chamber |
| US5437624A (en) * | 1993-08-23 | 1995-08-01 | Cobe Laboratories, Inc. | Single needle recirculation system for harvesting blood components |
| SE9302369D0 (sv) * | 1993-07-08 | 1993-07-08 | Omega Medicinteknik Ab | Paassystem avsett foer centrifugalseparationsamt an vaendning av detta paassystem |
| US5704888A (en) * | 1995-04-14 | 1998-01-06 | Cobe Laboratories, Inc. | Intermittent collection of mononuclear cells in a centrifuge apparatus |
| US5704889A (en) * | 1995-04-14 | 1998-01-06 | Cobe Laboratories, Inc. | Spillover collection of sparse components such as mononuclear cells in a centrifuge apparatus |
-
1997
- 1997-07-01 US US08/886,732 patent/US6027657A/en not_active Expired - Lifetime
-
1998
- 1998-06-22 WO PCT/US1998/012166 patent/WO1999001197A1/en active Application Filing
- 1998-06-22 EP EP98930151A patent/EP1024872B1/en not_active Expired - Lifetime
- 1998-06-22 CN CN98806734A patent/CN1261815A/zh active Pending
- 1998-06-22 CA CA002294395A patent/CA2294395A1/en not_active Abandoned
- 1998-06-22 EP EP04076782A patent/EP1468713A3/en not_active Ceased
- 1998-06-22 BR BR9810661-9A patent/BR9810661A/pt not_active IP Right Cessation
- 1998-06-22 JP JP50717199A patent/JP4076587B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CA2294395A1 (en) | 1999-01-14 |
| CN1261815A (zh) | 2000-08-02 |
| BR9810661A (pt) | 2000-10-03 |
| EP1024872B1 (en) | 2011-08-10 |
| EP1024872A1 (en) | 2000-08-09 |
| EP1024872A4 (en) | 2001-03-14 |
| US6027657A (en) | 2000-02-22 |
| WO1999001197A1 (en) | 1999-01-14 |
| EP1468713A3 (en) | 2004-10-27 |
| JP2002509534A (ja) | 2002-03-26 |
| EP1468713A2 (en) | 2004-10-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4076587B2 (ja) | 希釈された単核細胞を収集するシステムおよび方法 | |
| JP4076588B2 (ja) | 濃縮赤血球の再循環により単核細胞を採取するシステムおよび方法 | |
| US6027441A (en) | Systems and methods providing a liquid-primed, single flow access chamber | |
| US5961842A (en) | Systems and methods for collecting mononuclear cells employing control of packed red blood cell hematocrit | |
| US7857744B2 (en) | Blood processing apparatus with flared cell capture chamber and method | |
| AU702151B2 (en) | Particle separation apparatus and method | |
| JP2002291872A (ja) | 血液成分採取装置 | |
| JP2001198212A (ja) | 中間密度成分血液製品を増大した収量で得るための方法 | |
| JP3817079B2 (ja) | 血液成分採取装置 | |
| WO1994008687A1 (en) | Enhanced yield platelet collection systems and methods | |
| JP2002159569A (ja) | 血小板採取装置 | |
| US20080035585A1 (en) | Method and Apparatus for Recirculating Elutriation Fluids | |
| JP2002272836A (ja) | 血液成分採取装置 | |
| MXPA99011979A (en) | Systems and methods for collecting diluted mononuclear cells | |
| WO1994008689A1 (en) | Blood processing systems with improved data transfer between stationary and rotating elements | |
| MXPA99011977A (en) | Systems and methods for harvesting mononuclear cells by recirculation of packed red blood cells | |
| MXPA99001874A (en) | Systems and methods for collecting mononuclear cells employing control of packed red blood cell hematocrit | |
| MXPA99011985A (en) | Blood processing chamber counter-balanced with blood-free liquid |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050617 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050617 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20060912 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20061127 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070508 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070725 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080108 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080130 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110208 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120208 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130208 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140208 Year of fee payment: 6 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |