JP3710141B2 - ホルモン依存性腫瘍の検査方法 - Google Patents
ホルモン依存性腫瘍の検査方法 Download PDFInfo
- Publication number
- JP3710141B2 JP3710141B2 JP51552095A JP51552095A JP3710141B2 JP 3710141 B2 JP3710141 B2 JP 3710141B2 JP 51552095 A JP51552095 A JP 51552095A JP 51552095 A JP51552095 A JP 51552095A JP 3710141 B2 JP3710141 B2 JP 3710141B2
- Authority
- JP
- Japan
- Prior art keywords
- hormone
- tumor
- culture medium
- dependent
- growth
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- G01N33/57557—
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/25—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving enzymes not classifiable in groups C12Q1/26 - C12Q1/66
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/74—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving hormones or other non-cytokine intercellular protein regulatory factors such as growth factors, including receptors to hormones and growth factors
- G01N33/743—Steroid hormones
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Zoology (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Biotechnology (AREA)
- Wood Science & Technology (AREA)
- Hematology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Biomedical Technology (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Medicinal Chemistry (AREA)
- Endocrinology (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Paper (AREA)
- Reinforced Plastic Materials (AREA)
- Steroid Compounds (AREA)
Description
技術分野
本発明はホルモン依存性腫瘍の検査方法に関する。さらに詳しくは腫瘍組織のホルモン依存的増殖とホルモン合成酵素の存在を同時に判定する方法に関する。本発明により腫瘍の診断と治療指針を得ることができる。
背景技術
ホルモン依存性腫瘍と呼ばれる一群の腫瘍がある。これはおもにホルモンの標的臓器に発生し、ホルモンの存在下に発育、増殖が促進される腫瘍、即ちホルモン依存的増殖を呈する腫瘍をさす。たとえば乳癌(エストロジェン依存)、前立腺癌(アンドロジェン依存)、甲状腺癌(甲状腺刺激ホルモン依存)等を例示できる。これらのホルモン依存性腫瘍に対してはホルモン内分泌療法が広く適用されている。
ある種の乳癌は女性ホルモンエストロジェンによって癌が悪化することが知られており、このため、古くはエストロジェンの主産生臓器である卵巣の摘出がホルモン内分泌療法として行われてきた。現在では、エストロジェンと競合してエストロジェンレセプターに結合するタモキシフェンなどの抗エストロジェン剤投与による治療方法が広く適用されている。
乳癌の治療にあたって、抗エストロジェン剤の適応の可否を判断する根拠として、手術またはバイオプシーにより採取した組織のホモジェネートを調製し、このホモジェネート中のエストロジェンレセプターの存在を検査する方法が採用されている。これは上述したように、抗エストロジェン剤がエストロジェンと競合してエストロジェンレセプターに結合することによって薬効を示すからである。エストロジェンレセプターの存在が確認された場合には、抗エストロジェン剤が処方される。実際、抗エストロジェン剤の治療成績とエストロジェンレセプターの存在の間には相関関係があることが臨床的にも確認されている。しかしながら、エストロジェンレセプターを検査する方法は繁雑であり、しかもたとえエストロジェンレセプターの存在自体が確認されてもそれが生理的に機能していなければ、エストロジェン依存的な増殖は呈さない。実際エストロジェンレセプターの存在が確認された腫瘍の全てがエストロジェン依存的増殖を呈するわけではない。
一方、近年の研究によれば、一部のホルモン依存性疾患やホルモン依存性腫瘍は、その疾患の悪化や腫瘍の増殖に関与するホルモンを疾患の組織自体で産生する能力を有していることが明らかになってきている。例えば、乳癌のある種のタイプでは、その腫瘍組織中にアンドロジェンからエストロジェンを合成する酵素系(アロマターゼ)が存在し、この酵素によって、腫瘍組織内でエストロジェンが高濃度に合成されることが確認されている(内海俊明,日外会誌,第90回,920−927,1989)。
このような、組織中でホルモンが合成される疾患の場合には、そのホルモン合成を抑制することが治療の手段として試みられている。上述した乳癌の治療では、局所的なエストロジェン産生を抑制するために、エストロジェン合成酵素であるアロマターゼを阻害する目的で、この酵素の阻害剤が使用される例がある。
組織中のホルモン合成酵素の存在の有無を確認する方法としては、手術やバイオプシーで得られた組織を採取し、このホモジュネートの酵素活性を直接測定する。アロマターゼ活性の測定は、上述した内海らの報告に詳細な測定方法が開示されている。
アロマターゼ活性の存在が確認され、さらにエストロジェン依存的増殖の存在が確認された腫瘍組織であれば、アロマターゼ阻害剤による治療が可能である。しかしこのような腫瘍組織の検査は殆ど行われていないのが実状である。これは、目的とする腫瘍組織の採取が困難であるか、あるいは採取しても極微量であり、酵素活性を測定することが困難なためである。このため、組織を採取しても、微量分析が可能なエストロジェンレセプターの検査のみを行い、この結果のみでアロマターゼ阻害剤の投与を判断することとなる。しかしながらこの検査方法ではアロマターゼ活性の存在の有無が判らず、且つ上述したようにエストロジェンレセプターの存在が確認された腫瘍の全てがエストロジェン依存的増殖を呈するとは限らないため、誤った判断を下す場合が発生する。このような問題は、エストロジェン以外のホルモン依存性疾患や腫瘍についてもいえる。
一方、ホルモン標的臓器に発生する腫瘍は、一般にそのホルモン合成酵素の有無とホルモン依存的増殖の有無により、次の表1のように分類することができる。
本発明者等は、ホルモン合成酵素の存在の有無とホルモン依存的増殖の有無を同時にかつ容易に判定する方法について鋭意研究し、本発明に到達した。
発明の開示
本発明の目的は、ホルモン依存性疾患、とくにホルモン依存性腫瘍であって、腫瘍組織中でホルモン合成を行う腫瘍のホルモン合成系酵素の存在の有無と、ホルモン依存的増殖を同時に検査する簡便な方法を提供することにある。
本発明の他の目的は、ホルモン合成酵素が存在しかつホルモン依存的増殖が行われるタイプ(上記の表1のタイプ1)の腫瘍と他のタイプの腫瘍とを容易に鑑別する方法を提供することにある。
本発明は、腫瘍組織を(a)培養基、(b)ホルモン合成酵素の基質を含む培養基、および(c)ホルモン合成酵素の基質とホルモン合成酵素の阻害剤を含む培養基でそれぞれ培養し、各培養基での腫瘍細胞の成長を測定し、(i)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成基質の存在下の成長率および(ii)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成酵素の基質とホルモン合成酵素阻害剤の存在下での成長率を求めることにより、腫瘍組織のホルモン依存的増殖とホルモン合成酵素の存在を同時に判定することを特徴とするホルモン依存性腫瘍の検査方法に関する。
本発明によれば、上記表1に示したタイプ1および2のホルモン依存的増殖を示す腫瘍やタイプ3および4のホルモン非依存的増殖を示す腫瘍のうち、1のタイプの腫瘍を他のタイプの腫瘍と、容易に鑑別することが可能となる。
本発明の検査方法は次のような手順で検査を行う。
(1)ヒト腫瘍組織の摘出、またはバイオプシーなどの生検により検査試料を調製する。
(2)この試料を(a)培養基、(b)ホルモン合成酵素の基質を含む培養基、および(c)ホルモン合成酵素の基質とホルモン合成酵素の阻害剤を含む培養基でそれぞれ培養する。
(3)各培養基での検査試料(腫瘍組織)の増殖を測定する。
(4)増殖を確認して判定を行う。
この確認は、(i)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成基質の存在下の成長率および(ii)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成酵素の基質とホルモン合成酵素阻害剤の存在下での成長率とを求め、腫瘍組織のホルモン依存増殖とホルモン合成酵素の存在を同時に判定することにより行なう。
本発明の検査方法を、代表的なホルモン依存性腫瘍であるエストロジェン依存性腫瘍を例として説明する。
エストロジェン依存性腫瘍として代表的なものに乳癌を例示することができる。このエストロジェンはアンドロジェンからアロマターゼにより変換されるが従来はこのエストロジェンのレセプターを検査するのみであった。
入手した腫瘍組織、例えば、手術やバイオプシーにより採取した組織を無菌的に細切し、この組織を培養する。培養に用いる培養基は細胞培養に用いるものであればどのようなものであっても使用可能であるが、ソフトアガーを用いた培養基やコラーゲンマトリックスを用いた培養基が例示でき、また培地としては細胞培養に用いられる、イーグルの培地、RPMI培地などを例示できる。組織培養の方法やこれに用いる方法は、公知の方法であればどのような方法であってもさしつかえない。培養方法の詳細については中井準之助他編集の組織培養(朝倉書店刊、1976年)などの公知文献に詳細に説明されている。
この培養基に、エストロジェン合成酵素であるアロマターゼの基質であるテストステロンを添加したもの、およびアロマターゼの基質であるテストステロンとアロマターゼの阻害剤を添加したものを調製する。アロマターゼの基質であるテストステロンは1−1000nM濃度になるように調整するが、通常は1−100nMが好ましい。またアロマターゼ阻害剤は、酵素活性のみを選択的に阻害し、細胞毒性を示さないような化合物であればどのような化合物であっても使用できるが、4−ヒドロキシ−4−アンドロステン−3,17−ジオン(一般名 フォルメスタン、チバガイギー製)や特開昭63−192794号に開示されている14α−ヒドロキシ−4−アンドロステン−3,6,17−トリオン(略称 NKS01 雪印乳業製)が例示できる。
本発明においては14α−ヒドロキシ−4−アンドロステン−3,6,17−トリオン(以下NKS01と略記する)を用いて説明する。このアロマターゼ阻害剤は阻害活性に応じてその培養基中の濃度を変えることができるが、通常 NKS01を用いた場合は0.01〜100μM濃度になるように調製する。この培地に上述の組織切片を移植し、常法によって培養を行う。培養期間は通常1〜14日間とする。細胞増殖の判定は、ラベル化したチミジンの取り込み量で測定を行う。一般的には、トリチウムチミジンの取り込み量で測定する方法が簡便に実施できる。
トリチウムチミジンの取り込み量で測定する場合は、培養終了の3〜4日前に、各培地中にトリチウムチミジンを添加し、培養終了後、組織片を取り出しこの組織片中に取り込まれたトリチウムチミジン量を液体シンチレーションカウンターで計測し成長量とする。この際、この組織片中の核酸含量を測定し、取り込まれたチミジン量を核酸含量で除することにより、培養基毎のバラツキを少なくすることができる。
培養基のみの成長量に対する、基質を添加した培養基での成長量、あるいは阻害剤添加した培養基での成長量を求め、成長率を計算する。成長率は下記の計算式により求める。
成長率(%)=〔(各培養基中の組織3H−チミジン取り込み量/各培養基組織DNA濃度)/(培養基中のみで培養した組織3H−チミジン取り込み量/培養基のみで培養した組織のDNA濃度)〕×100
乳癌の患者の腫瘍組織で、ホルモン依存性と考えられる場合上記の方法で検査を行うことにより、癌患者の患部組織を従来と異なる観点から分類することが可能となる。例えば、手術により摘出された乳癌組織サンプルが、エストロジェン依存的増殖とエストロジェン合成酵素であるアロマターゼを共に有していれば、アロマターゼの基質であるテストステロンを添加した培養基で培養した場合には、テストステロンはエストロジェンに変換され、このエストロジェンによって増殖することとなる。またこの増殖はアロマターゼ阻害剤により抑制される。上述の表1に示したタイプ1のホルモン依存性の腫瘍であると判断される。
また手術により摘出された乳癌組織サンプルが、エストロジェン依存的増殖とエストロジェン合成酵素であるアロマターゼの一方または両方を欠如していればテストステロン存在下で成長率が促進されることはない。
本発明の実施により、ホルモン依存性腫瘍の、ホルモン合成酵素の存在とホルモン依存的増殖の有無を同時に且つ容易に判定することが可能となる。またこの判定結果は腫瘍のあらたな分類や、治療指針の選定などに利用することが可能である。
上記のタイプ1の腫瘍であれば、アロマターゼ阻害剤による治療が可能であると推測することができ、このような治療方針を立てることができる。
発明を実施するための最良の形態
以下に実施例および参考例を示しさらに本発明を詳細に説明する。本発明は本実施例に限定されるものではない。
実施例1
乳癌と診断された患者21例を対象として本発明方法により検査を行った。
乳癌の手術時に、腫瘍の中心部より採取した組織片(10mm角)を速やかに100U/mlのペニシリンとストレプトマイシンを含有するハンクス液(ギブコ製)中で、無菌的に壊死組織を除去した後、手術用メスで0.5〜1mm角程度の大きさに細片化した。この組織細片を4〜5個、24ウエルマイクロプレート内のコラーゲンマトリックス上に静置した。コラーゲンマトリックスは、あらかじめ、スポンジ状コラーゲンゲルマトリックス(スポンゴスタン製)を無菌的に1cm3大に細切し、24ウエルマイクロプレートの各ウエルに入れ、10%ウシ胎児血清(FCS)、100U/mlのペニシリン、100U/mlのストレプトマイシンを含むフェノールレッド不含のイーグル改変ミニマムエッセンシャル培地(ギブコ製)を培養基としてコラーゲンマトリックスの表面に到達するまで、ウエル中に注入しておいた。
この24ウエルマイクロプレートを二酸化炭素5%を含む空気中に置き、37℃で7日間培養を行った。培養基は1日おきに、全量交換したが、これに用いる培養基に添加するFCSは予めチャコールデキストラン処理を行って、ステロイド成分を除いたものを使用した。
培養組織の検査培養基としては、次の3群で行った。
(1)対照群(培地のみ)
(2)10nMテストステロン添加群(基質添加群)
(3)10nMテストステロン、1μM NKS01添加群(基質、酵素阻害剤添加群)
培養7日後、0.67μCiのトリチウムチミジンを含有する培養基に交換し、さらに3日間の培養を行った。培養終了後、各ウエルのコラーゲンスポンジ上に培養した組織片をウエルごとに、一つのチューブに移し、0.1mg/mlのコラゲナーゼを含むハンクス液1mlを加え、37℃で8時間インキュベートした。ついでピペッティング操作により、細胞塊を分散させ、3000rpmで10分間遠心を行った。沈殿に1%ドデシル硫酸ナトリウムおよび200μg/mlプロテナーゼを含む100mMトリス緩衝液(pH7.5)1mlを加え、50℃で3時間インキュベートした。
この溶液に1mlのフェノール/クロロフォルム/イソアミルアルコール(25:24:1)を加え、数分間混和した。その後、3000rpmで10分間遠心処理を行った後、上層の水層を分取した。ここに100μlの3M酢酸ナトリウム、2、5mlの冷エチルアルコールを添加し、析出してきたDNAをガラス棒に巻き取った。DNAはガラス棒に巻きつけたまま、70%、80%、90%濃度のエチルアルコール水溶液に順次浸した後、風乾させた。次いで100mMトリス緩衝液(pH7.5)1mlに溶解させ、DNA溶液を調製した。
このDNA溶液の濃度を260nmの波長の吸光度を測定し、さらに液体シンチレーションカウンターを用いて100μl当たりのトリチウムチミジン含量を測定した。測定はDNA1μg当たりのカウント数(dpm/μgDNA)で測定した。細胞の成長をDNAあたりのトリチウムチミジン含量で測定する方法は、広く普及しており、例えば福岡らの方法(福岡正晃他、ACTA OBST GYNAEC JPN,Vol.43,No.12,1667-1973)に従って行うことができる。本実施例においてもこの方法に準じて測定した。結果は表2に示した。
本発明検査方法により検査を行ったところ21例中6例が、エストロジェン依存的増殖とアロマターゼの両方を腫瘍組織中に有することが確認できた。この症例の乳癌はホルモン依存性であって、腫瘍組織内でホルモンが合成されて増殖している可能性が高いことが推測された。
実施例2
エストロジェンレセプターの存在がすでに確認されている、すなわち従来の検査に従えば「内分泌的治療(アロマターゼ阻害剤投与)が可」と判断されるヒト由来腫瘍細胞株4株(表3)を対象として、本発明方法により改めてアロマターゼ阻害剤適応可否の検査を行った。
各々の腫瘍細胞株を固形腫瘍にするべく7週齢メスヌードマウスの腋窩皮下に1×105/0.1ml/mouseとなるように移植し、大きさが直径1cm程度になった時点でヌードマウスよりこの移植腫瘍を摘出した。これらの腫瘍を前述の本発明方法によって検査をした結果を表4に示した。
次に、これらの腫瘍株細胞を再度7週齢メスヌードマウスの腋窩皮下に1×105/0.1ml/mouseとなるように移植し、腫瘍塊の大きさが直径約3mmとなった時点で10匹程度を1群として、アロマターゼ阻害剤を投与しない対照群と実験終了時まで毎日アロマターゼ阻害剤を投与するアロマターゼ阻害剤投与群とに分けた。なお、アロマターゼ阻害剤としては4-ヒドロキシ-4-アンドロステン-3、17-ジオン(一般名フォルメスタン、チバガイギー製)や4-(5、6、7、8-テトラヒドロイミダゾ−〔1、5a〕−ピリジン-5-イル)ベンゾニトリルモノヒドロクロリド(一般名ファドラゾール、チバガイギー製)、特開昭63−192794号に開示されている14α-ヒドロキシ-4-アンドロステン-3、6、17-トリオン(略称NKS01 雪印乳業製)をそれぞれ使用した。
投与期間は、各腫瘍のヌードマウス上での増殖速度により異なり、BG-1、R-27、ISHIKAWAでは28日間、MCF-7では42日間とした。最終投与日翌日に腫瘍の長径および短径をノギス等で測定し、以下の計算式によって推定腫瘍体積を算出し、その結果を表5に示した。
推定腫瘍体積=(長径)×(短径)2×0.5
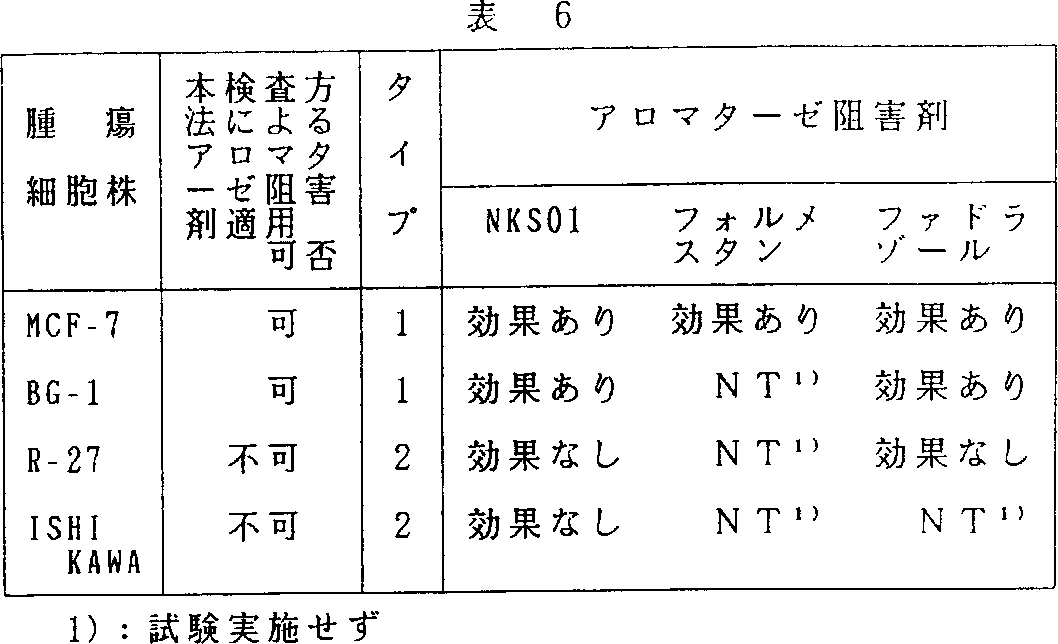
効果の判定は、対照群とアロマターゼ阻害剤投与群との間で、腫瘍の大きさに統計学的に有意な差が認められた際に、「抗腫瘍効果あり」と判断した。統計手法には幾つかの種類が知られているが、今回は対照群とアロマターゼ阻害剤投与群との間でT検定を行い有意水準5%以下を効果の判断基準とした。今回使用した4種類の腫瘍細胞株に対するそれぞれのアロマターゼ阻害剤の抗腫瘍効果判定結果を併せて表5に示した。
この様に、本発明方法によりアロマターゼ阻害剤による治療が有効であると判断した判定結果と実際抗腫瘍試験でのアロマターゼ阻害剤の有効性は一致していた(表6)。以上の実施例より明らかなように本発明方法をエストロジェン依存性腫瘍の患者に適用することによって同患者へのアロマターゼ阻害剤適応の可否をより正確に判断できる。
本発明はホルモン依存性腫瘍の検査方法に関する。さらに詳しくは腫瘍組織のホルモン依存的増殖とホルモン合成酵素の存在を同時に判定する方法に関する。本発明により腫瘍の診断と治療指針を得ることができる。
背景技術
ホルモン依存性腫瘍と呼ばれる一群の腫瘍がある。これはおもにホルモンの標的臓器に発生し、ホルモンの存在下に発育、増殖が促進される腫瘍、即ちホルモン依存的増殖を呈する腫瘍をさす。たとえば乳癌(エストロジェン依存)、前立腺癌(アンドロジェン依存)、甲状腺癌(甲状腺刺激ホルモン依存)等を例示できる。これらのホルモン依存性腫瘍に対してはホルモン内分泌療法が広く適用されている。
ある種の乳癌は女性ホルモンエストロジェンによって癌が悪化することが知られており、このため、古くはエストロジェンの主産生臓器である卵巣の摘出がホルモン内分泌療法として行われてきた。現在では、エストロジェンと競合してエストロジェンレセプターに結合するタモキシフェンなどの抗エストロジェン剤投与による治療方法が広く適用されている。
乳癌の治療にあたって、抗エストロジェン剤の適応の可否を判断する根拠として、手術またはバイオプシーにより採取した組織のホモジェネートを調製し、このホモジェネート中のエストロジェンレセプターの存在を検査する方法が採用されている。これは上述したように、抗エストロジェン剤がエストロジェンと競合してエストロジェンレセプターに結合することによって薬効を示すからである。エストロジェンレセプターの存在が確認された場合には、抗エストロジェン剤が処方される。実際、抗エストロジェン剤の治療成績とエストロジェンレセプターの存在の間には相関関係があることが臨床的にも確認されている。しかしながら、エストロジェンレセプターを検査する方法は繁雑であり、しかもたとえエストロジェンレセプターの存在自体が確認されてもそれが生理的に機能していなければ、エストロジェン依存的な増殖は呈さない。実際エストロジェンレセプターの存在が確認された腫瘍の全てがエストロジェン依存的増殖を呈するわけではない。
一方、近年の研究によれば、一部のホルモン依存性疾患やホルモン依存性腫瘍は、その疾患の悪化や腫瘍の増殖に関与するホルモンを疾患の組織自体で産生する能力を有していることが明らかになってきている。例えば、乳癌のある種のタイプでは、その腫瘍組織中にアンドロジェンからエストロジェンを合成する酵素系(アロマターゼ)が存在し、この酵素によって、腫瘍組織内でエストロジェンが高濃度に合成されることが確認されている(内海俊明,日外会誌,第90回,920−927,1989)。
このような、組織中でホルモンが合成される疾患の場合には、そのホルモン合成を抑制することが治療の手段として試みられている。上述した乳癌の治療では、局所的なエストロジェン産生を抑制するために、エストロジェン合成酵素であるアロマターゼを阻害する目的で、この酵素の阻害剤が使用される例がある。
組織中のホルモン合成酵素の存在の有無を確認する方法としては、手術やバイオプシーで得られた組織を採取し、このホモジュネートの酵素活性を直接測定する。アロマターゼ活性の測定は、上述した内海らの報告に詳細な測定方法が開示されている。
アロマターゼ活性の存在が確認され、さらにエストロジェン依存的増殖の存在が確認された腫瘍組織であれば、アロマターゼ阻害剤による治療が可能である。しかしこのような腫瘍組織の検査は殆ど行われていないのが実状である。これは、目的とする腫瘍組織の採取が困難であるか、あるいは採取しても極微量であり、酵素活性を測定することが困難なためである。このため、組織を採取しても、微量分析が可能なエストロジェンレセプターの検査のみを行い、この結果のみでアロマターゼ阻害剤の投与を判断することとなる。しかしながらこの検査方法ではアロマターゼ活性の存在の有無が判らず、且つ上述したようにエストロジェンレセプターの存在が確認された腫瘍の全てがエストロジェン依存的増殖を呈するとは限らないため、誤った判断を下す場合が発生する。このような問題は、エストロジェン以外のホルモン依存性疾患や腫瘍についてもいえる。
一方、ホルモン標的臓器に発生する腫瘍は、一般にそのホルモン合成酵素の有無とホルモン依存的増殖の有無により、次の表1のように分類することができる。
本発明者等は、ホルモン合成酵素の存在の有無とホルモン依存的増殖の有無を同時にかつ容易に判定する方法について鋭意研究し、本発明に到達した。
発明の開示
本発明の目的は、ホルモン依存性疾患、とくにホルモン依存性腫瘍であって、腫瘍組織中でホルモン合成を行う腫瘍のホルモン合成系酵素の存在の有無と、ホルモン依存的増殖を同時に検査する簡便な方法を提供することにある。
本発明の他の目的は、ホルモン合成酵素が存在しかつホルモン依存的増殖が行われるタイプ(上記の表1のタイプ1)の腫瘍と他のタイプの腫瘍とを容易に鑑別する方法を提供することにある。
本発明は、腫瘍組織を(a)培養基、(b)ホルモン合成酵素の基質を含む培養基、および(c)ホルモン合成酵素の基質とホルモン合成酵素の阻害剤を含む培養基でそれぞれ培養し、各培養基での腫瘍細胞の成長を測定し、(i)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成基質の存在下の成長率および(ii)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成酵素の基質とホルモン合成酵素阻害剤の存在下での成長率を求めることにより、腫瘍組織のホルモン依存的増殖とホルモン合成酵素の存在を同時に判定することを特徴とするホルモン依存性腫瘍の検査方法に関する。
本発明によれば、上記表1に示したタイプ1および2のホルモン依存的増殖を示す腫瘍やタイプ3および4のホルモン非依存的増殖を示す腫瘍のうち、1のタイプの腫瘍を他のタイプの腫瘍と、容易に鑑別することが可能となる。
本発明の検査方法は次のような手順で検査を行う。
(1)ヒト腫瘍組織の摘出、またはバイオプシーなどの生検により検査試料を調製する。
(2)この試料を(a)培養基、(b)ホルモン合成酵素の基質を含む培養基、および(c)ホルモン合成酵素の基質とホルモン合成酵素の阻害剤を含む培養基でそれぞれ培養する。
(3)各培養基での検査試料(腫瘍組織)の増殖を測定する。
(4)増殖を確認して判定を行う。
この確認は、(i)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成基質の存在下の成長率および(ii)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成酵素の基質とホルモン合成酵素阻害剤の存在下での成長率とを求め、腫瘍組織のホルモン依存増殖とホルモン合成酵素の存在を同時に判定することにより行なう。
本発明の検査方法を、代表的なホルモン依存性腫瘍であるエストロジェン依存性腫瘍を例として説明する。
エストロジェン依存性腫瘍として代表的なものに乳癌を例示することができる。このエストロジェンはアンドロジェンからアロマターゼにより変換されるが従来はこのエストロジェンのレセプターを検査するのみであった。
入手した腫瘍組織、例えば、手術やバイオプシーにより採取した組織を無菌的に細切し、この組織を培養する。培養に用いる培養基は細胞培養に用いるものであればどのようなものであっても使用可能であるが、ソフトアガーを用いた培養基やコラーゲンマトリックスを用いた培養基が例示でき、また培地としては細胞培養に用いられる、イーグルの培地、RPMI培地などを例示できる。組織培養の方法やこれに用いる方法は、公知の方法であればどのような方法であってもさしつかえない。培養方法の詳細については中井準之助他編集の組織培養(朝倉書店刊、1976年)などの公知文献に詳細に説明されている。
この培養基に、エストロジェン合成酵素であるアロマターゼの基質であるテストステロンを添加したもの、およびアロマターゼの基質であるテストステロンとアロマターゼの阻害剤を添加したものを調製する。アロマターゼの基質であるテストステロンは1−1000nM濃度になるように調整するが、通常は1−100nMが好ましい。またアロマターゼ阻害剤は、酵素活性のみを選択的に阻害し、細胞毒性を示さないような化合物であればどのような化合物であっても使用できるが、4−ヒドロキシ−4−アンドロステン−3,17−ジオン(一般名 フォルメスタン、チバガイギー製)や特開昭63−192794号に開示されている14α−ヒドロキシ−4−アンドロステン−3,6,17−トリオン(略称 NKS01 雪印乳業製)が例示できる。
本発明においては14α−ヒドロキシ−4−アンドロステン−3,6,17−トリオン(以下NKS01と略記する)を用いて説明する。このアロマターゼ阻害剤は阻害活性に応じてその培養基中の濃度を変えることができるが、通常 NKS01を用いた場合は0.01〜100μM濃度になるように調製する。この培地に上述の組織切片を移植し、常法によって培養を行う。培養期間は通常1〜14日間とする。細胞増殖の判定は、ラベル化したチミジンの取り込み量で測定を行う。一般的には、トリチウムチミジンの取り込み量で測定する方法が簡便に実施できる。
トリチウムチミジンの取り込み量で測定する場合は、培養終了の3〜4日前に、各培地中にトリチウムチミジンを添加し、培養終了後、組織片を取り出しこの組織片中に取り込まれたトリチウムチミジン量を液体シンチレーションカウンターで計測し成長量とする。この際、この組織片中の核酸含量を測定し、取り込まれたチミジン量を核酸含量で除することにより、培養基毎のバラツキを少なくすることができる。
培養基のみの成長量に対する、基質を添加した培養基での成長量、あるいは阻害剤添加した培養基での成長量を求め、成長率を計算する。成長率は下記の計算式により求める。
成長率(%)=〔(各培養基中の組織3H−チミジン取り込み量/各培養基組織DNA濃度)/(培養基中のみで培養した組織3H−チミジン取り込み量/培養基のみで培養した組織のDNA濃度)〕×100
乳癌の患者の腫瘍組織で、ホルモン依存性と考えられる場合上記の方法で検査を行うことにより、癌患者の患部組織を従来と異なる観点から分類することが可能となる。例えば、手術により摘出された乳癌組織サンプルが、エストロジェン依存的増殖とエストロジェン合成酵素であるアロマターゼを共に有していれば、アロマターゼの基質であるテストステロンを添加した培養基で培養した場合には、テストステロンはエストロジェンに変換され、このエストロジェンによって増殖することとなる。またこの増殖はアロマターゼ阻害剤により抑制される。上述の表1に示したタイプ1のホルモン依存性の腫瘍であると判断される。
また手術により摘出された乳癌組織サンプルが、エストロジェン依存的増殖とエストロジェン合成酵素であるアロマターゼの一方または両方を欠如していればテストステロン存在下で成長率が促進されることはない。
本発明の実施により、ホルモン依存性腫瘍の、ホルモン合成酵素の存在とホルモン依存的増殖の有無を同時に且つ容易に判定することが可能となる。またこの判定結果は腫瘍のあらたな分類や、治療指針の選定などに利用することが可能である。
上記のタイプ1の腫瘍であれば、アロマターゼ阻害剤による治療が可能であると推測することができ、このような治療方針を立てることができる。
発明を実施するための最良の形態
以下に実施例および参考例を示しさらに本発明を詳細に説明する。本発明は本実施例に限定されるものではない。
実施例1
乳癌と診断された患者21例を対象として本発明方法により検査を行った。
乳癌の手術時に、腫瘍の中心部より採取した組織片(10mm角)を速やかに100U/mlのペニシリンとストレプトマイシンを含有するハンクス液(ギブコ製)中で、無菌的に壊死組織を除去した後、手術用メスで0.5〜1mm角程度の大きさに細片化した。この組織細片を4〜5個、24ウエルマイクロプレート内のコラーゲンマトリックス上に静置した。コラーゲンマトリックスは、あらかじめ、スポンジ状コラーゲンゲルマトリックス(スポンゴスタン製)を無菌的に1cm3大に細切し、24ウエルマイクロプレートの各ウエルに入れ、10%ウシ胎児血清(FCS)、100U/mlのペニシリン、100U/mlのストレプトマイシンを含むフェノールレッド不含のイーグル改変ミニマムエッセンシャル培地(ギブコ製)を培養基としてコラーゲンマトリックスの表面に到達するまで、ウエル中に注入しておいた。
この24ウエルマイクロプレートを二酸化炭素5%を含む空気中に置き、37℃で7日間培養を行った。培養基は1日おきに、全量交換したが、これに用いる培養基に添加するFCSは予めチャコールデキストラン処理を行って、ステロイド成分を除いたものを使用した。
培養組織の検査培養基としては、次の3群で行った。
(1)対照群(培地のみ)
(2)10nMテストステロン添加群(基質添加群)
(3)10nMテストステロン、1μM NKS01添加群(基質、酵素阻害剤添加群)
培養7日後、0.67μCiのトリチウムチミジンを含有する培養基に交換し、さらに3日間の培養を行った。培養終了後、各ウエルのコラーゲンスポンジ上に培養した組織片をウエルごとに、一つのチューブに移し、0.1mg/mlのコラゲナーゼを含むハンクス液1mlを加え、37℃で8時間インキュベートした。ついでピペッティング操作により、細胞塊を分散させ、3000rpmで10分間遠心を行った。沈殿に1%ドデシル硫酸ナトリウムおよび200μg/mlプロテナーゼを含む100mMトリス緩衝液(pH7.5)1mlを加え、50℃で3時間インキュベートした。
この溶液に1mlのフェノール/クロロフォルム/イソアミルアルコール(25:24:1)を加え、数分間混和した。その後、3000rpmで10分間遠心処理を行った後、上層の水層を分取した。ここに100μlの3M酢酸ナトリウム、2、5mlの冷エチルアルコールを添加し、析出してきたDNAをガラス棒に巻き取った。DNAはガラス棒に巻きつけたまま、70%、80%、90%濃度のエチルアルコール水溶液に順次浸した後、風乾させた。次いで100mMトリス緩衝液(pH7.5)1mlに溶解させ、DNA溶液を調製した。
このDNA溶液の濃度を260nmの波長の吸光度を測定し、さらに液体シンチレーションカウンターを用いて100μl当たりのトリチウムチミジン含量を測定した。測定はDNA1μg当たりのカウント数(dpm/μgDNA)で測定した。細胞の成長をDNAあたりのトリチウムチミジン含量で測定する方法は、広く普及しており、例えば福岡らの方法(福岡正晃他、ACTA OBST GYNAEC JPN,Vol.43,No.12,1667-1973)に従って行うことができる。本実施例においてもこの方法に準じて測定した。結果は表2に示した。
本発明検査方法により検査を行ったところ21例中6例が、エストロジェン依存的増殖とアロマターゼの両方を腫瘍組織中に有することが確認できた。この症例の乳癌はホルモン依存性であって、腫瘍組織内でホルモンが合成されて増殖している可能性が高いことが推測された。
実施例2
エストロジェンレセプターの存在がすでに確認されている、すなわち従来の検査に従えば「内分泌的治療(アロマターゼ阻害剤投与)が可」と判断されるヒト由来腫瘍細胞株4株(表3)を対象として、本発明方法により改めてアロマターゼ阻害剤適応可否の検査を行った。
各々の腫瘍細胞株を固形腫瘍にするべく7週齢メスヌードマウスの腋窩皮下に1×105/0.1ml/mouseとなるように移植し、大きさが直径1cm程度になった時点でヌードマウスよりこの移植腫瘍を摘出した。これらの腫瘍を前述の本発明方法によって検査をした結果を表4に示した。
次に、これらの腫瘍株細胞を再度7週齢メスヌードマウスの腋窩皮下に1×105/0.1ml/mouseとなるように移植し、腫瘍塊の大きさが直径約3mmとなった時点で10匹程度を1群として、アロマターゼ阻害剤を投与しない対照群と実験終了時まで毎日アロマターゼ阻害剤を投与するアロマターゼ阻害剤投与群とに分けた。なお、アロマターゼ阻害剤としては4-ヒドロキシ-4-アンドロステン-3、17-ジオン(一般名フォルメスタン、チバガイギー製)や4-(5、6、7、8-テトラヒドロイミダゾ−〔1、5a〕−ピリジン-5-イル)ベンゾニトリルモノヒドロクロリド(一般名ファドラゾール、チバガイギー製)、特開昭63−192794号に開示されている14α-ヒドロキシ-4-アンドロステン-3、6、17-トリオン(略称NKS01 雪印乳業製)をそれぞれ使用した。
投与期間は、各腫瘍のヌードマウス上での増殖速度により異なり、BG-1、R-27、ISHIKAWAでは28日間、MCF-7では42日間とした。最終投与日翌日に腫瘍の長径および短径をノギス等で測定し、以下の計算式によって推定腫瘍体積を算出し、その結果を表5に示した。
推定腫瘍体積=(長径)×(短径)2×0.5
効果の判定は、対照群とアロマターゼ阻害剤投与群との間で、腫瘍の大きさに統計学的に有意な差が認められた際に、「抗腫瘍効果あり」と判断した。統計手法には幾つかの種類が知られているが、今回は対照群とアロマターゼ阻害剤投与群との間でT検定を行い有意水準5%以下を効果の判断基準とした。今回使用した4種類の腫瘍細胞株に対するそれぞれのアロマターゼ阻害剤の抗腫瘍効果判定結果を併せて表5に示した。
この様に、本発明方法によりアロマターゼ阻害剤による治療が有効であると判断した判定結果と実際抗腫瘍試験でのアロマターゼ阻害剤の有効性は一致していた(表6)。以上の実施例より明らかなように本発明方法をエストロジェン依存性腫瘍の患者に適用することによって同患者へのアロマターゼ阻害剤適応の可否をより正確に判断できる。
Claims (7)
- 腫瘍組織を(a)培養基、(b)ホルモン合成酵素の基質を含む培養基、および(c)ホルモン合成酵素の基質とホルモン合成酵素の阻害剤を含む培養基でそれぞれ培養し、各培養基での腫瘍細胞の成長を測定し、(i)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成基質の存在下の成長率および(ii)培養基のみで培養した場合の腫瘍細胞の成長に対する、ホルモン合成酵素の基質とホルモン合成酵素阻害剤の存在下での成長率を求めることにより、腫瘍組織のホルモン依存的増殖とホルモン合成酵素の存在を同時に判定することを特徴とするホルモン依存性腫瘍の検査方法。
- 腫瘍組織がヒト腫瘍組織をヌードマウス中に移植し、増殖させたものである請求項1記載の方法。
- ホルモンがエストロジェンである、請求の範囲第1又は2項記載の方法。
- ホルモン合成酵素の基質がテストステロンであり、ホルモン合成酵素がアロマターゼである、請求の範囲第1項または第3項記載の方法。
- テストステロンの濃度を1−1000nMに調整する、請求の範囲第4項記載の方法。
- ホルモン合成阻害剤が、14α−ヒドロキシ−4−アンドロステン−3,6−17トリオン、4−ヒドロキシ−4−アンドロステン3、17−ジオン、4−(5,6,7,8−テトラヒドロイミダゾ−〔1,5α〕ピリジン−5−イル)ベンゾニトリルモノヒドロクロリドから選択される1又はそれ以上の合成阻害剤である、請求の範囲第1〜5項のいずれかに記載の方法。
- 請求項1〜6記載の方法によりホルモン依存性腫瘍の検査を行い、アロマターゼ阻害剤の適応腫瘍を判定し、治療指針を得る方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP5-339608 | 1993-12-03 | ||
| JP33960893 | 1993-12-03 | ||
| PCT/JP1994/000779 WO1995015398A1 (en) | 1993-12-03 | 1994-05-13 | Method of examining hormone-dependent tumor |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO1995015398A1 JPWO1995015398A1 (ja) | 1996-03-26 |
| JP3710141B2 true JP3710141B2 (ja) | 2005-10-26 |
Family
ID=18329101
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP51552095A Expired - Fee Related JP3710141B2 (ja) | 1993-12-03 | 1994-05-13 | ホルモン依存性腫瘍の検査方法 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US5914227A (ja) |
| EP (1) | EP0683237B1 (ja) |
| JP (1) | JP3710141B2 (ja) |
| AT (1) | ATE214103T1 (ja) |
| AU (1) | AU681660B2 (ja) |
| CA (1) | CA2155182C (ja) |
| DE (1) | DE69430052T2 (ja) |
| DK (1) | DK0683237T3 (ja) |
| ES (1) | ES2176243T3 (ja) |
| FI (2) | FI941359A0 (ja) |
| HU (2) | HU9400876D0 (ja) |
| NZ (1) | NZ265711A (ja) |
| WO (1) | WO1995015398A1 (ja) |
| ZA (1) | ZA943783B (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030013694A1 (en) * | 2001-05-25 | 2003-01-16 | Jens Hoffmann | Use and compositions of antiprogestins for treatment of prostate diseases |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8615092D0 (en) * | 1986-06-20 | 1986-07-23 | Erba Farmitalia | Androst-4-ene-317-diones |
| JPH0267296A (ja) * | 1988-09-01 | 1990-03-07 | Bunichi Takegawa | ステロイド化合物 |
-
1994
- 1994-03-24 FI FI941359A patent/FI941359A0/fi unknown
- 1994-03-28 HU HU9400876A patent/HU9400876D0/hu unknown
- 1994-05-13 JP JP51552095A patent/JP3710141B2/ja not_active Expired - Fee Related
- 1994-05-13 EP EP94914618A patent/EP0683237B1/en not_active Expired - Lifetime
- 1994-05-13 ES ES94914618T patent/ES2176243T3/es not_active Expired - Lifetime
- 1994-05-13 DK DK94914618T patent/DK0683237T3/da active
- 1994-05-13 AT AT94914618T patent/ATE214103T1/de not_active IP Right Cessation
- 1994-05-13 DE DE69430052T patent/DE69430052T2/de not_active Expired - Lifetime
- 1994-05-13 NZ NZ265711A patent/NZ265711A/en unknown
- 1994-05-13 WO PCT/JP1994/000779 patent/WO1995015398A1/ja not_active Ceased
- 1994-05-13 AU AU66909/94A patent/AU681660B2/en not_active Ceased
- 1994-05-13 CA CA002155182A patent/CA2155182C/en not_active Expired - Fee Related
- 1994-05-13 HU HU9502267A patent/HU219328B/hu not_active IP Right Cessation
- 1994-05-30 ZA ZA943783A patent/ZA943783B/xx unknown
-
1995
- 1995-08-01 FI FI953656A patent/FI111271B/fi not_active IP Right Cessation
-
1997
- 1997-07-14 US US08/892,291 patent/US5914227A/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| HUT73345A (en) | 1996-07-29 |
| WO1995015398A1 (en) | 1995-06-08 |
| ATE214103T1 (de) | 2002-03-15 |
| AU6690994A (en) | 1995-06-19 |
| FI953656L (fi) | 1995-08-15 |
| FI953656A0 (fi) | 1995-08-01 |
| FI111271B (fi) | 2003-06-30 |
| EP0683237B1 (en) | 2002-03-06 |
| DK0683237T3 (da) | 2002-07-01 |
| ES2176243T3 (es) | 2002-12-01 |
| HU9400876D0 (en) | 1994-07-28 |
| AU681660B2 (en) | 1997-09-04 |
| ZA943783B (en) | 1995-02-09 |
| EP0683237A4 (en) | 1998-07-29 |
| US5914227A (en) | 1999-06-22 |
| DE69430052D1 (de) | 2002-04-11 |
| FI941359A0 (fi) | 1994-03-24 |
| CA2155182C (en) | 2004-02-24 |
| EP0683237A1 (en) | 1995-11-22 |
| CA2155182A1 (en) | 1995-06-08 |
| DE69430052T2 (de) | 2002-11-14 |
| HU9502267D0 (en) | 1995-10-30 |
| HU219328B (en) | 2001-03-28 |
| NZ265711A (en) | 1997-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Yue et al. | In situ aromatization enhances breast tumor estradiol levels and cellular proliferation | |
| Anderson et al. | Estrogen responsiveness and control of normal human breast proliferation | |
| Burchardt et al. | Transdifferentiation of prostate cancer cells to a neuroendocrine cell phenotype in vitro and in vivo | |
| Boyd et al. | The origins of breast cancer associated with mammographic density: a testable biological hypothesis | |
| Pertschuk et al. | Histochemical analyses of steroid hormone receptors in breast and prostatic carcinoma. | |
| Hornung et al. | Regulated on activation, normal T-cell-expressed and-secreted mRNA expression in normal endometrium and endometriotic implants: assessment of autocrine/paracrine regulation by in situ hybridization | |
| Zhai et al. | Analysis of clinical factors and PDGFR-β in predicting prognosis of patients with clival chordoma | |
| Koivisto et al. | Increased cell proliferation activity and decreased cell death are associated with the emergence of hormone‐refractory recurrent prostate cancer | |
| Kiplesund et al. | Light microscopic morphometric analysis of castration effects in the different lobes of the rat prostate | |
| Pati et al. | Hormone-induced chromosomal instability in p53-null mammary epithelium | |
| Fish et al. | Competing causes of death for primary breast cancer | |
| Liehr et al. | Inhibition of estrogen-induced renal carcinogenesis in male Syrian hamsters by tamoxifen without decrease in DNA adduct levels | |
| JP3710141B2 (ja) | ホルモン依存性腫瘍の検査方法 | |
| Ozdemir et al. | Can core biopsy be used instead of surgical biopsy in the diagnosis and prognostic factor analysis of breast carcinoma? | |
| Coates et al. | Differential contextual responses of normal human breast epithelium to ionizing radiation in a mouse xenograft model | |
| Van Weerden et al. | Ki‐67 expression and BrdUrd incorporation as markers of proliferative activity in human prostate tumour models | |
| Chen et al. | Neoplastic odontogenic epithelial cells express bone sialoprotein | |
| Beckman Jr et al. | Autoradiographic localization of estrogen and androgen target cells in human and rat prostate carcinoma | |
| JPWO1995015398A1 (ja) | ホルモン依存性腫瘍の検査方法 | |
| JP2000513208A (ja) | Ivfの成果についての予測アッセイ | |
| Satyaswaroop | Development of a preclinical model for hormonal therapy of human endometrial carcinomas | |
| Kuliczkowski et al. | Upregulation of p21 RAS levels in HL-60 cells during differentiation induction with DMSO, all-trans-retinoic acid and TPA | |
| Blance et al. | Normal breast tissue implanted into athymic nude mice identifies biomarkers of the effects of human pregnancy levels of estrogen | |
| Taniguchi et al. | Histochemical detection of intranuclear DNA fragmentation and its relation to the expression of bcl‐2 oncoprotein in human prostatic cancer | |
| Agarwala et al. | Soft Tissue Sarcomas |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20050412 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20050726 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20050809 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |