JP2025519090A - 多結晶構造体を含む分光分析用基板及びその製造方法 - Google Patents
多結晶構造体を含む分光分析用基板及びその製造方法 Download PDFInfo
- Publication number
- JP2025519090A JP2025519090A JP2024569022A JP2024569022A JP2025519090A JP 2025519090 A JP2025519090 A JP 2025519090A JP 2024569022 A JP2024569022 A JP 2024569022A JP 2024569022 A JP2024569022 A JP 2024569022A JP 2025519090 A JP2025519090 A JP 2025519090A
- Authority
- JP
- Japan
- Prior art keywords
- substrate
- spectroscopic
- spectroscopic analysis
- reducing agent
- manufacturing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01J—MEASUREMENT OF INTENSITY, VELOCITY, SPECTRAL CONTENT, POLARISATION, PHASE OR PULSE CHARACTERISTICS OF INFRARED, VISIBLE OR ULTRAVIOLET LIGHT; COLORIMETRY; RADIATION PYROMETRY
- G01J3/00—Spectrometry; Spectrophotometry; Monochromators; Measuring colours
- G01J3/28—Investigating the spectrum
- G01J3/44—Raman spectrometry; Scattering spectrometry ; Fluorescence spectrometry
- G01J3/4412—Scattering spectrometry
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/65—Raman scattering
- G01N21/658—Raman scattering enhancement Raman, e.g. surface plasmons
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y15/00—Nanotechnology for interacting, sensing or actuating, e.g. quantum dots as markers in protein assays or molecular motors
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y20/00—Nanooptics, e.g. quantum optics or photonic crystals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y40/00—Manufacture or treatment of nanostructures
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/02—Mechanical
- G01N2201/022—Casings
- G01N2201/0221—Portable; cableless; compact; hand-held
Landscapes
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Nanotechnology (AREA)
- Materials Engineering (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Crystallography & Structural Chemistry (AREA)
- Composite Materials (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Manufacture Of Metal Powder And Suspensions Thereof (AREA)
- Powder Metallurgy (AREA)
- Analysing Materials By The Use Of Radiation (AREA)
Abstract
本発明は、多結晶構造体を含む分光分析用基板及びこれの製造方法に関することである。より詳細には、本発明は、多結晶構造体を含む信号の強度及び信号均一度が改善された多結晶構造体を含むユニバーサル素材基盤の分光分析用基板及び様々な素材の表面に単純な工程で形状が制御された多結晶構造体を含む分光分析用基板を製造する方法に関することである。【選択図】図1
Description
本発明は、多結晶構造体を含む分光分析用基板及びこれの製造方法に関することである。より詳細には、本発明は、信号の強度及び信号均一度が改善された多結晶構造体を含むユニバーサル素材基盤の分光分析用基板及び様々な素材の表面に単純な工程で形状が制御された多結晶構造体を含む分光分析用基板を製造する方法に関することである。
ラマン散乱(Raman scattering)は、入射される光のエネルギーが変わる非弾性散乱で、光を特定の分子体に加えると、分子体固有の振動遷移によって照射された光と波長が若干異なる光が発生する現象を指す。
実際、ほぼすべての有機分子らは固有のラマンシフト(Raman shift)を持っており、ラマン散乱を用いたラマン分光法によれば、分子の誘導偏極率変化がある非極性分子の場合でも信号を得ることができる。また、ラマン分光法は水分子による干渉の影響を受けないため、タンパク質、遺伝子などの生体分子(biomolecules)の検出にさらに適している。
ラマン放出スペクトルの波長はサンプル内の光吸収分子の化学組成及び構造の特性を示すので、このようなラマンシグナルを分析すると分析対象物質を直接的に分析することができる。
本願の背景技術として、大韓民国特許第10-1867670号には、連続的な化学的な反応法を用いた紙ベース表面増強ラマン散乱基材の製造方法が記載されている。しかしながら、前記特許では、1~100nmの直径を有する金属ナノパーティクルを製造し、第1金属前駆体溶液及び第2金属前駆体溶液及び第1還元剤溶液及び第2還元剤溶液を用いて、工程が複雑であるだけではなく、これによって、前駆体吸着段階、前駆体洗浄段階、還元剤溶液への担持段階、及び還元剤溶液洗浄段階等の工程を数回繰り返して遂行することなどで、工程制御が容易ではない問題点がある。
本発明の目的は、貴金属含有ナノパーティクルがベース部材上に直接に成長されたものであり、分光分析用として利用する時、感度及び信号均一性に優れた分光分析用基板を提供することである。
本発明の他の目的は、柔軟性に優れ、様々な3次元表面への適用が容易な分光分析用基板を提供することである。
本発明のもう一つの目的は、ベース部材の素材に関係なく形成される貴金属ナノ結晶粒子の形状を容易に調整することができ、多結晶粒子を容易に形成することができることで、表面増強ラマン分光(Surface Enhanced Raman Spectroscopy, SERS)信号の感度及び信号均一度を高められる分光分析用基板製造用組成物を提供することである。
本発明のもう一つの目的は、がんなどの現場診断が可能なラマン分光装置を提供することである。
本発明のもう一つの目的は、ベース部材の素材に関係なく、簡単な工程によって、SERS信号の感度及び信号均一度が高い分光分析用基板を効率的に製造できる分光分析用基板の製造方法を提供することである。
本発明の目的は、以上で言及した目的らに制限されず、言及されないもう一つの目的らは、詳細な説明の記載から明確に理解されることができる。
一側面によれば、ベース部材;及び前記ベース部材上に形成された複数個のナノ粒子の群集から構成され、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を含み、溶液工程で形成される、分光分析用基板が提供される。
一実施例によれば、前記ベース部材は、紙、ポリマー、ウェルプレート、ウェハ、及びタンパク質のうち、1種以上から構成され得る。
一実施例によれば、前記ナノ粒子間は枝(branch)構造で連結され、前記多結晶構造体は平均粒径が1μm~100μmであり得る。
一実施例によれば、本願の分光分析用基板は、電気化学的活性表面積(Electrochemically Active Surface Area, EASA)が0.1cm2~10.0cm2であり得る。
一実施例によれば、前記ナノ粒子はAu、Ag、及びPtのうち、1種以上から構成され得る。
一実施例によれば、前記分光分析用基板は、500nm以上の波長を使用するラマン分光システム又は1064nmの波長を使用するnear-IR FTラマン分光システムに適用可能であり得る。
一実施例によれば、前記分光分析用基板は、3次元スワブスティック、ウェアラブル基板、又はプラズモニックウェルプレートで構成され得る。
他の側面によれば、貴金属前駆体及び還元剤を含み、貴金属前駆体に対する還元剤の比率が1:0.5~1:15である、分光分析用基板製造用組成物が提供される。
一実施例によれば、本願の分光分析用基板製造用組成物は、前記貴金属前駆体に対する還元剤の比率が増加するほど、分光分析用基板に形成される多結晶構造体の大きさが減少し、多結晶構造体の密度が増加することができる。
一実施例によれば、前記貴金属前駆体は、HAuCl4及びNaAuCl4のうち、1種以上であり得る。
一実施例によれば、前記還元剤は、ヒドロキシルアミン(hydroxylamine)、アスコルビン酸(ascorbic acid)、FeSO4、及びヒドロキシキノン(hydroxyquinone)のうち、1種以上であり得る。
さらに他の側面によれば、光源;本願に記載された分光分析用基板;及びラマン分光を検出する検出器を含む、ラマン分光装置が提供される。
一実施例によれば、本願のラマン分光装置は第1端部が開放された筒形であり、第1端部は前記ラマン分光装置に締結される締結部を備え、第2端部は光源からの光を誘導する貫通孔が形成された結合部を備えるアダプタ;及びヘッド部及び前記ヘッド部から延長された一字形のボディー部で構成されるスプーン形であって、前記ヘッド部は、前記アダプタの第2端部の結合部が着座される半球形着座部及び前記ボディー部の中心に長手方向に前記半球形の着座部まで延長されて、一字形分光分析用ストリップ基板が着座される着座溝が測定部材をさらに含むことができる。
一実施例によれば、前記着座溝はT字形に形成され、前記分光分析用ストリップ基板の末端が前記半球形の着座部から外れないようにすることを特徴とすることができる。
一実施例によれば、前記検出器の標的物質は、小便、唾、汗及び涙内の細胞、代謝物質、タンパク質、核酸、DNA、RNA、酵素、有機分子、ウイルス、細胞外小胞(extracellular vesicles)、微小小胞(Microvesicles)、エキソソーム(Exosomes)、及び脂肪から1種以上、選択され得る。
一実施例によれば、前記ラマン分光装置はがんの現場診断が可能であり得る。
さらに他の側面によれば、本願に記載された分光分析用基板の製造方法であって、a)ベース部材を準備するベース部材の準備段階;及びb)前記ベース部材を貴金属前駆体及び還元剤溶液を含む分光分析用基板製造用組成物に担持し、前記ベース部材上に複数個のナノ粒子の群集から構成され、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を形成する段階;を含み、前記段階b)において、貴金属前駆体溶液に対する還元剤の比率を1:0.5~1:15とし、前記多結晶構造体の形状を調整する形状調整段階を含む、分光分析用基板の製造方法が提供される。
一実施例によれば、本願の分光分析用基板の製造方法の前記段階a)において、前記ベース部材表面を、多結晶構造体を形成する段階の以前に、表面改質する表面改質段階;をさらに含むことができる。
一実施例によれば、本願の分光分析用基板の製造方法において、前記表面改質段階は、塩基1~3%及び酸1~3%から選択される1種以上を含み、溶媒(solvent)としてC1-5のアルコール又は水を含む表面改質組成物で前記ベース部材表面を処理することを含むことができる。
一実施例によれば、本願の分光分析用基板は、貴金属含有ナノパーティクルが直接に成長されて枝(branch)構造に連結され、マイクロパーティクル大きさの多結晶構造体を含むことができ、分光分析用に利用時、感度及び信号均一性に優れる。
一実施例によれば、本願の分光分析用基板のベース部材は様々な素材で構成され、柔軟性に優れ、様々な3次元表面への適用が容易であり得る。
一実施例によれば、本願の分光分析用基板製造用組成物は、貴金属前駆体及び還元剤の比率を調節し、ベース部材の素材に関係なく形成される貴金属ナノ結晶粒子の形状を容易に調節することができ、多結晶粒子を容易に形成することができ、SERS信号の感度及び信号均一性を高めることができる。
一実施例によれば、本願のラマン分光装置は、現場で非-標識分析物質の種類を確認して定量分析ができる。
一実施例によれば、本願のラマン分光装置は、少量の小便などの生体試料を用いてがんなどの現場診断が可能である。
一実施例によれば、本願の分光分析用基板の製造方法は、ベース部材の素材に関係なく、1回の溶液工程という単純な工程で貴金属含有多結晶構造体をベース部材に直接に成長させ、SERS信号の強度及び信号均一度が高い分光分析用基板を効率的に製造することができる。
一実施例によれば、本願の分光分析用基板の製造方法は、表面改質を通じて高いパーティクル密度及び向上された信号均一度を有する分光分析用基板を効率的に製造することができる。
一実施例によれば、本願の分光分析用基板の製造方法は、表面改質を通じて高いパーティクル密度及び向上された信号均一度を有する分光分析用基板を効率的に製造することができる。
本開示の目的、特定なメリットら及び新規な特徴らは、添付された図面らに連関される以下の詳細な説明と実施例らからさらに明らかになるであろう。
これに先立ち、本明細書及び請求の範囲で使用された用語又は単語は、通常的かつ辞書的な意味で解釈されるべきではなく、発明者がその自分の発明を最善の方法で説明するために用語の概念を適切に定義することができるという原則に基づいて、本開示の技術的思想に符合される意味と概念で解釈されなければならない。
本明細書において、層、部分、又は基板のような構成要素が他の構成要素「上」、「連結されて」、又は「結合されて」いるものと記載されている場合、これは直接的に他の構成要素「上」、「連結されて」、又は「結合されて」いるかもしれないし、また、両方の構成要素の間に1つ以上の他の構成要素を介在している可能性がある。対照的に、構成要素が他の構成要素「直接的に上」、「直接的に連結されて」、又は「直接的に結合されて」あることと記載されている場合、両方の構成要素の間には他の構成要素が介在されている可能性がない。
本明細書で使用した用語は、単に特定な実施例を説明するために使用されたものであり、本開示を限定しようとする意図ではない。単数の表現は、文脈上明らかに異なる意味を持たない限り、複数の表現を含む。
本明細書において、「含む」又は「有する」などの用語は、明細書上に記載された特徴、数字、段階、動作、構成要素、部品、又はこれらを組み合わせしたものが存在することを指定しようとするものであり、1つ又はそれ以上の他の特徴など、数字、段階、動作、構成要素、部品、又はこれらを組み合わせたものなどの存在又は付加の可能性を予め排除しないことで理解されるべきである。
本明細書において、ある部分がある構成要素を「含む」と言う場合、これは、特別に反対される記載がない限り、他の構成要素を除外することではなく、他の構成要素をさらに含むことができることを意味する。なお、明細書の全体において、「上に」とは、対象部分の上又は下に位置することを意味することであり、必ず重力方向を基準として上側に位置することを意味することではない。
本開示は、様々な変換を加えることができ、様々な実施例らを有することができるので、特定の実施例らを図面に例示し、詳細な説明に詳細に説明しようとする。しかし、これは本開示を特定な実施形態に対して、限定しようとすることをではなく、本開示の思想及び技術範囲に含まれるすべての変換、均等物から代替物を含むことで理解されるべきである。本開示を説明することにおいて、関連される公知技術に対しての具体的な説明が本開示の要旨を不明瞭にすると判断される場合、その詳細な説明は省略する。
以下、本開示の実施例を添付図面を参照して詳細に説明することにし、添付図面を参照して説明するにあたって、同一するか又は対応する構成要素は同一な図面番号を付与し、これに対する重複される説明は省略することにする。
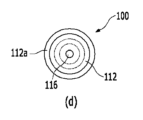
図1(a)は、本発明の一実施例によるセルロースアセテート(cellulose acetate)をベース部材として製造された紙ベースの分光分析用基板を示したものである。図1(b)~図1(e)は、図1(a)の分光分析用基板のSEM写真(図1(b))、多結晶検証結果(図1(c))、粒子形成メカニズム(図1(d))、及び粒子分布グラフ(図1(e))を示す。図2は、本発明の実施例らによるナノセルロース(Nano Cellulose、NC)、混合セルロースエステル(Mixed Cellulose Ester, MCE)、クロマトグラフィー紙、及び印刷用紙をベース部材として成長された粒子の形状を示したSEM写真である。
図3(a)~図3(c)は、本発明の実施例らによる分光分析用基板製造用組成物に含まれる還元剤の比率によって、電気化学的な表面積を測定した結果を示す図面である。
本願の分光分析用基板はベース部材;及び前記ベース部材上に形成された複数個のナノ粒子の群集から構成され、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を含み、溶液工程で形成される基板である。
図1(a)~図1(e)及び図2を参照すると、セルロースアセテート(図1(a)~図1(e)参照)及びそれ以外の様々なベース部材上に形成された複数個のナノ粒子が群集で形成された多結晶体を確認することができる(図2参照)。図1(d)を参照すると、これに限定されないが、貴金属のうち、Au前駆体がナノ粒子を形成して群集をなることが示されており、特に、これらは溶液工程を用いて、ベース部材上に直接成長する。具体的に群集されたナノ粒子は、結合(coalescence)によって、小さなサイズの多角形構造粒子(grain)を形成し、その後、方向性付着成長(oriented attachment)によって粒子は徐々に大きく成長する。従って、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を形成する。これに限定するものではないが、多結晶構造体である、貴金属コーラル(coral)形態のパーティクルは平均的にマイクロサイズで成長することができる(図1(e)参照)。前記のように複数個のグレインバウンダリを有する多結晶構造体は、複数個のグレインバウンダリで散乱が増加され、分光分析用基板として利用時、信号強度及び信号均一度を画期的に改善することができる。
本願に適用可能なベース部材は特に制限がなく、様々な素材が活用可能である。これに限定されないが、前記ベース部材は、紙、ポリマー、ウェルプレート、ウェハ、及びタンパク質のうち、1種以上から構成され得る。これに限定するものではないが、前記紙は、セルロースアセテート、ナノセルロース(Nano Cellulose、NC)、混合セルロースエステル(Mixed Cellulose Ester、MCE)、クロマトグラフィー紙及び一般的に使用する印刷用紙と同じ紙であり得る。また、分析分光用基板は、多孔質ポリマー、プラズモニックウェルプレート、ウェハ及びシルク、コラーゲン、キチン、エラスチン、ケラチンなどの1種以上のタンパク質で構成されたタンパク質フィルムであり得る。図2を参照すると、ナノセルロース(Nano Cellulose、NC)(図2(a))、混合セルロースエステル(Mixed Cellulose Ester、MCE)(図2(b))、クロマトグラフィー紙(図2(c))、及び一般的に使用する印刷用紙(図2(d))基盤のベース部材上に成長された類似な構造の多結晶構造体の形態を確認することができる。これに限定されないが、ベース部材は、適用される分野によって、多孔質及び/又は柔軟性が備えたベース部材が適合でき、紙、ポリマー、又はタンパク質フィルムが適合できる。さらに、プラズモニックウェルプレートは、複数の試料を同時に検出する時に適合できる。
これに限定されないが、前記ナノ粒子間は枝(branch)構造に連結され、前記多結晶構造体は平均粒径が1μm~100μmであり得る。本願の分光分析用基板は、溶液工程によって、多結晶構造体に成長し、枝(branch)構造に連結され、平均粒径が1μm~100μmであり得る。これに限定されないが、前記多結晶構造体の平均粒径が、前記範囲で信号強度及び信号均一度の向上に適合できる。
これに限定されないが、本願の分光分析用基板は、電気化学的活性表面積(Electrochemically Active Surface Area、EASA)が0.1cm2~10.0cm2であり得る。本願の分光分析用基板は、溶液工程によって、多結晶構造体に成長し、表面積が増加することができる。さらに、図3(a)~図3(c)を参照すると、本願による分光分析用基板製造用組成物に含まれた金属イオン前駆体に対する還元剤の比率が増加することによって、電気化学的表面積(EASA、cm2)が増加したことを確認することができる。一方、金属イオン前駆体に対する還元剤比率が1:0.5未満では貴金属多結晶構造体の密度が低くて、電流が通じないかもしれない。
これに限定されないが、前記ナノ粒子は、Au、Ag、及びPtのうち、1種以上で構成されることができ、Auが信号強度及び信号均一性の向上面で最も適合できる。
これに限定されないが、本願の分光分析用基板は、500nm以上の波長を使用するラマン分光システム又は1064nmの波長を使用するnear-IR FT ラマン分光システムに適用可能であり得る。
図6(b)を参照すると、本願による分光分析用基板を用いると、500nm以上の波長の広い吸光領域を示すので、現在商用されている様々な波長を利用するラマン分光システムを利用できることを確認することができる。これに限定するものではないが、633nm又は785nmでより適合できる。
図4(a)~図4(d)は、本発明の実施例らによる様々な形態の分光分析用基板を示した写真である。
これに限定されないが、前記分光分析用基板は、3次元スワップスティック、ウェアラブル基板、又はプラズモニックウェルプレートで構成され得る。本願の光分析用基板は様々なベース部材を含むことができ、柔軟性がある素材から製造されることができ、様々な形態を有することができる。図4を参照すると、平面形状の基板以外に、3次元多孔質材料を用いた3Dスワップスティック、ウェアラブル基板形態、ウェルプレート形態、タンパク質フィルム形態など様々な形態として適用が可能である。
前記3次元スワップスティック形態の分光分析用基板は試料採取が容易にでき、ウェアラブル基板はパッチ又はレンズ形態で構成されて比較的長時間試料採取が可能であり、目を通して試料採取が可能であり得る。また、プラズモニックウェルプレートの場合、多量の試料を同時に分析することができ、分析時間を短縮することができる。
本願の他の側面によれば、本願の分光分析用基板製造用組成物は貴金属前駆体及び還元剤を含む。
図5(a)~図5(c)は、本発明の一実施例による分光分析用基板に適用された還元剤がヒドロキシルアミン(hydroxylamine)(金属前駆体に対する還元剤の比率が1:2)である場合、メチレンブルー(methylene blue, MB)を濃度別に塗布し、633nm及び785nmでSERS信号の強度を示したグラフである。図5(d)及び図5(e)は本発明の一実施例による分光分析用基板の信号均一度を示したグラフであり、図5(f)は本発明の一実施例による分光分析用基板の柔軟性(flexibility)を示した写真である。
図5(a)~図5(f)を参照すると、セルロースアセテートをベース部材として製造された本願の分光分析用基板を用いて、メチレンブルー(methylene blue, MB)の濃度別にSERS信号の強度を測定した後、メチレンブルーの濃度によって、633nm及び785nmでそれぞれSERS信号強度を検証した。本願の分光分析用基板を用いる場合、信号の均一度が高くて、一定であることが確認することができる。また、本願の分光分析用基板の場合、小さくて、柔軟性を有しているから、携帯が簡便で、様々な表面に適用が可能である。
これに限定するものではないが、貴金属前駆体に対する還元剤の比率が1:0.5未満であれば、様々な波長のラマン分光システムを利用できず、1:15を超えると、フィルム化して、信号強度及び信号均一性に優れる分光分析用基板を得ることが難しいかもしれない。
従って、本願の分光分析用基板製造用組成物において、貴金属前駆体に対する還元剤の比率が1:0.5~1:15である場合が、信号強度及び信号均一性に優れた分光分析用基板を製造することに適合でき、1:0.5~1:12であり得、1:0.5~1:10であり得、1:1~1:10であり得、1:1~1:9であり得、1:1~1:8であり得、1:1~1:7であり得、1:1~1:6であり得、1:1~1:5であり得、1:1~1:4であり得、1:1~1:3であり得る。また、還元剤の種類によってその範囲が多少異なり得る。
これに限定されないが、本願の分光分析用基板製造用組成物は、前記貴金属前駆体に対する還元剤の比率が増加するほど、分光分析用基板に形成される多結晶構造体の大きさが減少し、多結晶構造体の密度が増加することができる。
図6(a)は、本発明の一実施例による分光分析用基板製造用組成物内、金属前駆体と還元剤比率による粒子形状の変化を示したSEM写真である。図6(b)は、本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体と還元剤比率による波長別、分析分光用基板の吸光表面プラズモン共鳴(surface plasmon resonance, SPR)変化を示したものである。図6(c)は、本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体と還元剤比率による波長別、分析分光用基板のSERS信号強度変化を示すグラフである。
図6を参照すると、金属前駆体に対する低い還元剤の比率では多結晶構造体の大きさが大きくて、枝構造の連結が少ないが、金属前駆体に対する還元剤の比率が増加するほど多結晶構造体の大きさが小さくて、より多くの枝構造で連結されていることを確認することができる。一方、分光分析用基板製造用組成物内、金属前駆体に対する還元剤の最適比率範囲によって、多結晶構造体の密度が増加して、透過度は減少し、吸光度が増加するため、感度がより高いラマン分光装置を製造することができる。
図7(a)及び図7(b)は、ベース部材を本発明による分光分析用基板製造用組成物に担持した後、反応時間による粒子の形状変化を示したSEM写真(図7(a))及びこれによる吸光SPR変化を示したグラフ(図7(b))である。
また、図7を参照すると、本願による分光分析用基板製造用組成物に基板を担持した時間による粒子の形状が示されている。特に、担持時間が増加するほど、吸光度が高くなることが確認することができる。
これに限定されないが、前記貴金属前駆体は、HAuCl4、AuCl、AuCl2、AuCl3、Na2Au2Cl8及びNaAuCl2からなる群から選択され得るが、HAuCl4及びNaAuCl4のうち、1種以上がより適合できる。
これに限定されないが、前記還元剤は、ヒドロキシルアミン(hydroxylamine)、アスコルビン酸(ascorbic acid)、FeSO4、及びヒドロキシキノン(hydroxyquinone)のうち、1種以上であり得る。
これに限定されないが、前記還元剤は、ヒドロキシルアミン(hydroxylamine)、アスコルビン酸(ascorbic acid)、FeSO4、及びヒドロキシキノン(hydroxyquinone)のうち、1種以上であり得る。
図8(a)~図12には、ヒドロキシルアミン(Hydroxylamine)、アスコルビン酸(Ascorbic acid)、FeSO4、及びヒドロキシキノン(Hydroxykinone)還元剤を用いた場合、SERS信号強度の比較を通じて示した貴金属前駆体に対する還元剤の最適な比率が示されている。
図8(a)は、本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とヒドロキシルアミン(hydroxylamine)還元剤比率による分光分析用基板の色相変化を示した写真であり、図8(b)は図8(a)の分光分析用基板の吸光SPR変化を示したグラフであり、図8(c)は図8(a)の分光分析用基板の633nmで測定したSERS信号強度変化を示すグラフであり、図8(d)は図8(a)の分光分析用基板の785nmで測定したSERS信号強度変化を示すグラフであり、図8(e)は本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とヒドロキシルラミン(hydroxylamine)還元剤比率による分光分析用基板の粒子形状を示したSEM写真である。
図8を参照すると、ヒドロキシルアミン(hydroxylamine)還元剤の場合、1:1比率から粒子の密度が増加し始め、貴金属前駆体に対する還元剤の比率が増加するほどSERS強度は増加した。SERS信号が最も強いと観察される1:2の比率を最適化比率に設定することができ、1:1以上1:5未満を最適化比率範囲に設定することができる。
図9(a)は、本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とアスコルビン酸(ascorbic acid)還元剤比率による分光分析用基板の色相変化を示した写真であり、図9(b)は図9(a)の分光分析用基板の吸光SPR変化を示したグラフであり、図9(c)は図9(a)の分光分析用基板の633nmで測定したSERS信号強度変化を示すグラフであり、図9(d)は図9(a)の分光分析用基板の785nmで測定したSERS信号強度変化を示すグラフであり、図9(e)は本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とアスコルビン酸(ascorbic acid)還元剤比率による分光分析用基板の粒子形状を示したSEM写真である。
図9を参照すると、アスコルビン酸(ascorbic acid)還元剤の場合、785nmで、貴金属前駆体に対する還元剤の比率が増加するほどSERS信号の強度が増加した。SERS信号が最も強いと観察される1:10の比率を最適化比率に設定することができ、1:0.5~1:15を最適化比率範囲に設定することができる。但し、633nmである場合、SERS信号が最も強いと観察される1:1の比率を最適化比率に設定することができ、1:0.5~1:15を最適化比率範囲に設定することができる。
図10(a)は、本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とFeSO4還元剤比率による分光分析用基板の色相変化を示した写真であり、図10(b)は図10(a)の分光分析用基板の吸光SPR変化を示したグラフであり、図10(c)は、図10(a)の分光分析用基板の633nmで測定したSERS信号強度変化を示すグラフであり、図10(d)は図10(a)の分光分析用基板の785nmで測定したSERS信号強度変化を示すグラフであり、図10(e)は本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とFeSO4還元剤比率による分光分析用基板の粒子形状を示したSEM写真である。
図10を参照すると、FeSO4還元剤の場合、貴金属前駆体に対する還元剤の比率が増加するほどSERS強度が増加した。SERS信号が最も強いと観察される1:5の比率を最適化比率に設定することができ、1:1超過1:15以下を最適化比率範囲に設定することができる。
図11(a)は、本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とヒドロキシキノン(hydroxyquinone)還元剤比率による分光分析用基板の色相変化を示した写真であり、図11(b)は図11(a)の分光分析用基板の吸光SPR変化を示したグラフであり、図11(c)は図11(a)の分光分析用基板の633nmで測定したSERS信号強度変化を示すグラフであり、図11(d)は図11(a)の分光分析用基板の785nmで測定したSERS信号強度変化を示すグラフであり、図11(e)は本発明の一実施例による分光分析用基板製造用組成物内、金属イオン前駆体とヒドロキシキノン(hydroxyquinone)還元剤比率による分光分析用基板の粒子形状を示したSEM写真である。
図11を参照すると、ヒドロキシキノン(hydroxyquinone)還元剤の場合、SERS信号が最も強いと観察される1:2の比率を最適化比率に設定することができ、1:0.5~1:15未満を最適化比率範囲に設定することができる。
図12(a)及び図12(b)は、本発明の実施例らによる金属イオン前駆体とそれぞれの還元剤が最適比率で含まれた分光分析用基板製造用組成物で製造された分光分析用基板の633nm(図12(a))及び785nm(図12(b))波長でのSERS強度を比較して示したものである。
図12を参照すると、還元剤別、最適な比率を導出したし、すべての還元剤に対する最適化条件を633nm及び785nm波長で確認した。
本願の他の側面によれば、光源;本願に記載された分光分析用基板;及びラマン分光を検出する検出器を含む、ラマン分光装置が提供される。
図13(a)~図13(d)は、本発明の一実施例による携帯用ラマン分光装置(図13(a))を用いてがんを現場診断する方法を概略的に示したものである。
図13(a)~図13(d)を参照すると、一例として、がん細胞の代謝物質が含まれた尿排泄物を本願による分析分光用基板(センサー)及び携帯用ラマン分光装置を用いて、ラマンスペクトルを導出し、多変量分析(multivariate analysis)を用いて、現場分析(On-site analysis)を通じて、前立腺がん及び膵臓がんを診断するラマン分光装置及び分析方法について概略的に示されている。
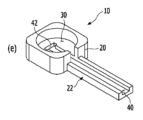
図14は、本発明の一実施例によるラマン分光装置を示した図面である。図15(a)は本発明の一実施例によるラマン分光装置用アダプタの斜視写真であり、図15(b)は図15(a)のアダプタの正面図であり、図15(c)は図15(a)のアダプタの平面図であり、図15(d)は図15(a)のアダプタの底面図であり、図15(e)は図15(a)のアダプタの斜視図である。
図16(a)は本発明の一実施例によるラマン分光装置用分析部材の平面写真であり、図16(b)は図16(a)の分析部材の平面図であり、図16(c)は図16(a)の分析部材のA方向の正面図であり、図16(d)は図16(a)の分析部材のB方向の側面図であり、図16(e)は図(a)の分析部材の斜視図である。
図14~図16を参照すると、本願のラマン分光装置200は、前記ラマン分光装置200に締結されるアダプタ100及び前記アダプタ100及び分光分析用ストリップ基板が着座されて分析される分析部材10をさらに含むことができる。
図14~図16を参照すると、前記アダプタ100は、第1端部が開放され、中空112を有する筒形ボディー部110を備え、第1端部が前記ラマン分光装置200に締結される締結部112aを備える。前記締結部112aは、筒形ボディー部110の内側に形成されたねじ山であり得る。また、前記アダプタ100の第2端部は、光源からの光を誘導する貫通孔116が形成された結合部114を備える。前記結合部114は、前記分析部材10と安定的に結合することができる形状で構成され得る。
図15及び図16を参照すると、前記分析部材10は、ヘッド部20及び前記ヘッド部20から延長される一字形ボディー部22から構成されるスプーン形で構成される。前記ヘッド部20は、前記アダプタ100の第2端部の結合部114が着座される半球形着座部30及び前記ボディー部22の中心に長手方向に前記半球形着座部30まで延長され、一字形分光分析用ストリップ基板が着座される着座溝40が備える。
これに限定されないが、前記着座溝40は、T字形に形成されるように前記着座部30に延長された末端部42を備え、前記分光分析用ストリップ基板の末端が前記半球形着座部30をずらさないようにして分析正確度を高めることができることを特徴とすることができる。
図17は本発明の一実施例によるラマン分光装置にアダプタ及び分析部材を結合して分析を進める方法を概略的に示した写真である。
図17を参照すると、まず、ラマン分光装置にアダプタをねじ結合させる(図17(a)及び図17(b))。次に、ラマン分光装置に締結されたアダプタを分析部材に結合させる(図17(c))。前記分析部材の安着溝に分光分析用ストリップ基板を押し込んだ後、分析を進める。
これに限定されないが、前記検出器の標的物質は、小便、唾、汗及び涙内の細胞、代謝物質、タンパク質、核酸、 DNA、RNA、酵素、有機分子、ウイルス、細胞外小胞、微小小胞(microvesicles)、エキソソーム(exosomes)、及び脂肪から1種以上、選択され得る。
これに限定されないが、前記標的物質は液体試料で、従来では分光分析用基板の場合、吸湿性が低くて、液体試料は測定時の感度が非常に低かった。しかし、本願による分光分析用基板は吸湿性があって、液体試料でも現場で迅速に診断が可能である。
これに限定されないが、前記ラマン分光装置はがんの現場診断が可能であり得る。これに限定するものではないが、前記記載された標的物質の代謝物質分析を通じて、がん診断に必要な情報を提供することができ、非侵襲的な検査によって、がんを早期診断することができ、極めて高いレベルの感度を持って、多重分析が可能であり得る。
前記がんは、肺がん、気管支がん、結腸直腸がん、前立腺がん、乳がん、胃がん、卵巣がん、膀胱がん、脳がん、甲状腺がん、食道がん、子宮がん、肝がん、腎臓がん、胆道がん、及び膵臓がんからなる群から選択された1種以上であり得、これに限定するものではないが、前立腺がん又は膵臓がんがより適合できる。
図18は本発明の一実施例による分析分光用基板を含むラマン分光装置(図18(a))を用いて測定された前立腺がんと膵臓がんのラマンスペクトル(図18(b)及び図18(c))及びこれを基づいていた前立腺がんと膵臓がんの多変量分析データ(図18(d)及び図18(e))を示したものである。
他の側面によれば、本発明によるラマン分光装置を用いたがん診断方法は、公知された多変量分析方法によってすることができる。前記全体スペクトルに対する多変量分析方法は公知された分析方法、例えば一般的に利用される部分最小二乗判別分析法(Partial Least Squares-Discriminant Analysis、PLS-DA)、判別分析法(General Discriminant Analysis;GDA)、主成分分析法(Principal Component Analysis、PCA)、パラレルファクター分析法(Parallel Factor Analysis; PARAFAC)、ニューラルネットワーク分析法(Neural Network Analysis、NNA)及び/又はサポートベクターマシン技法(Support Vector Machine; SVM)などによって分析することができるが、これに限定するものではない。
これに限定されないが、一実施例によるがん診断方法は下記の段階を含むことができる。得られたスペクトルについてバックグラウンド(background)信号を除去する段階;全体スペクトルに対して部分最小二乗判別分析法(PLS-DA)を遂行して潜在変数(latent variable)を得る段階、前記変数を基づいて入力された2つのグループを区別する段階、これに対して信頼度を確認する段階を含むことができる。
前記のように本発明によれば、現場でがんを正確かつ迅速に診断することができ、特に前立腺がん及び膵臓がんは90%以上の診断正確度を示された。
さらに他の側面によれば、分光分析用基板の製造方法は、本願に記載された分光分析用基板の製造方法であって、a)ベース部材準備段階;及びb)前記ベース部材を分光分析用基板製造用組成物に担持して多結晶構造体を形成する段階;を含む。前記において、分光分析用基板に対しての説明と重複される部分に対しては、詳細な説明を省略する。
段階a)は、ベース部材を準備する段階であり、上述したように、本願では様々なベース部材を利用することができる。これに限定されないが、紙、ポリマー、ウェルプレート、ウェハ、及びタンパク質のうち、1種以上から構成されるベース部材を準備することができる。
段階b)は、ベース部材を分光分析用基板製造用組成物に担持して多結晶構造体を形成する段階である。前記分光分析用基板製造用組成物は貴金属前駆体及び還元剤溶液を含み、溶液工程で前記ベース部材上に直接複数個のナノ粒子の群集から構成され、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を形成することができる。
前記段階b)において、貴金属前駆体溶液に対する還元剤の比率を1:0.5~1:15とし、前記多結晶構造体の形状を調整する形状調整段階を含むことができる。還元剤の種類による最適な還元剤の比率で調整して、分光分析用基板に形成される多結晶構造体の形状を容易に調整することができる。また、前記ベース部材を分光分析用基板製造用組成物に担持する時間を調整して、分光分析用基板に形成される多結晶構造体の形状を容易に調整することができる。本願の分光分析用基板の製造方法は、1回の担持という単一工程によって、信号強度及び信号均一性を同時に改善することができる。
これに限定されないが、本願の分光分析用基板の製造方法の前記段階a)において、前記ベース部材表面を、多結晶構造体を形成する段階の以前に表面改質する表面改質段階;をさらに含むことができる。前記表面改質段階はこれに限定するものではないが、化学的な表面処理を通じて、粒子形成を調節することかもしれないし、表面改質後の粒子形成時、粒子の密度を増加させることができる。
これに限定されないが、本願の分光分析用基板の製造方法において、前記表面改質段階は、塩基1~3%及び酸1~3%から選択される1種以上を含み、溶媒(solvent)として、C1-5のアルコール又は水を含む表面改質組成物で前記ベース部材表面を処理することを含むことができる。これに限定されないが、前記塩基及び酸は1%を使用し、溶媒はエタノールを使用することが信号強度及び信号均一性改善の観点に適合できる。
図19(a)及び図19(b)には、本発明の一実施例による表面改質組成物を用いて、表面改質した結果が示している。すなわち、図19(a)は本発明の一実施例による表面改質組成物を用いて表面改質した結果粒子の密度が増加した結果を示したSEM写真であり、図19(b)はこれによって、信号均一度が向上された結果を示したグラフである。従って、本発明の一実施例による表面改質組成物を用いて粒子の密度が増加したことを確認することができ、前記増加された粒子の密度によって信号均一度が向上したことを確認することができる。
実施例
1.分光分析用基板の製造
紙、多孔質ポリマーから構成される3次元スワップスティック、ウェアラブルパッチ、及びフィルム形態のベース部材を準備した。貴金属前駆体溶液に対する還元剤溶液の比率を5:1、2:1、1:1~1:15とし、混合して分光分析用基板製造用組成物を製造した。但し、当該組成物が準備され、1分以内にベース部材を担持しなければならない。但し、ウェルプレートの場合、組成物をウェルプレート各ウェルの内部に担持する方法で準備される。準備されたベース部材を前記混合された分光分析用基板製造用組成物に30秒~24hにかけて担持して、前記ベース部材上に複数個のナノ粒子の群集から形成された多結晶構造体を形成した。前記基板製造用組成物は貴金属前駆体溶液としてHAuCl4を用い、還元剤としてはヒドロキシルアミン(hydroxylamine)、アスコルビン酸(ascorbic acid)、FeSO4、及びヒドロキシキノン(hydroxyquinone)を用いた。多結晶構造体形成が完了された以降には、水又はエタノールを用いて2回以上洗浄し、残っている前駆体と還元剤を除去した。その後、1時間以上常温で乾燥して前記分光分析用基板製造を完了した。
1.分光分析用基板の製造
紙、多孔質ポリマーから構成される3次元スワップスティック、ウェアラブルパッチ、及びフィルム形態のベース部材を準備した。貴金属前駆体溶液に対する還元剤溶液の比率を5:1、2:1、1:1~1:15とし、混合して分光分析用基板製造用組成物を製造した。但し、当該組成物が準備され、1分以内にベース部材を担持しなければならない。但し、ウェルプレートの場合、組成物をウェルプレート各ウェルの内部に担持する方法で準備される。準備されたベース部材を前記混合された分光分析用基板製造用組成物に30秒~24hにかけて担持して、前記ベース部材上に複数個のナノ粒子の群集から形成された多結晶構造体を形成した。前記基板製造用組成物は貴金属前駆体溶液としてHAuCl4を用い、還元剤としてはヒドロキシルアミン(hydroxylamine)、アスコルビン酸(ascorbic acid)、FeSO4、及びヒドロキシキノン(hydroxyquinone)を用いた。多結晶構造体形成が完了された以降には、水又はエタノールを用いて2回以上洗浄し、残っている前駆体と還元剤を除去した。その後、1時間以上常温で乾燥して前記分光分析用基板製造を完了した。
結果
紙、多孔質スポンジから構成される3次元スワップスティック、パッチ及びフィルム形態などベース部材のどのような組成及び形態にかかわらず、分光分析用基板製造用組成物に含まれる貴金属前駆体溶液に対する還元剤溶液の比率が増加するほど製造される分光分析用基板上に群集される多結晶構造体の大きさが減少し、多結晶構造体の密度が増加した。
紙、多孔質スポンジから構成される3次元スワップスティック、パッチ及びフィルム形態などベース部材のどのような組成及び形態にかかわらず、分光分析用基板製造用組成物に含まれる貴金属前駆体溶液に対する還元剤溶液の比率が増加するほど製造される分光分析用基板上に群集される多結晶構造体の大きさが減少し、多結晶構造体の密度が増加した。
これによって透過度が減少し、吸光度が増加した。また、多結晶構造体は、平均粒径が1μm~100μmの間で多数の分布を成り、還元剤の種類によって、SERS感度及びSERSの信号の強さを考慮して、貴金属前駆体に対する最適な還元剤の比率範囲を導出した。
下記表1には、還元剤の種類による貴金属前駆体に対する最適な還元剤の比率範囲が示している。
以上で、本発明内容の特定な部分を詳細に記述したことで、当業界の通常の知識を有する者にとって、このような具体的な技術は単に好ましい実施様態であるだけであり、これによって、本発明の範囲が制限されることではないことは明らかであろう。従って、本発明の実質的な範囲は、添付された請求項らとそれらの等価物によって定義されると言えるだろう。
Claims (19)
- ベース部材;及び
前記ベース部材上に形成された複数個のナノ粒子の群集から構成され、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を含み、溶液工程で形成される、分光分析用基板。 - 前記ベース部材は、紙、ポリマー、ウェルプレート、ウェハ、及びタンパク質のうち、1種以上から構成される、請求項1に記載の分光分析用基板。
- 前記ナノ粒子間は枝(branch)構造で連結され、前記多結晶構造体は平均粒径が1μm~100μmである、請求項1に記載の分光分析用基板。
- 電気化学的活性表面積(Electrochemically Active Surface Area, EASA)は0.1cm2~10.0cm2である、請求項1に記載の分光分析用基板。
- 前記ナノ粒子はAu、Ag、及びPtのうち、1種以上から構成される、請求項1に記載の分光分析用基板。
- 前記分光分析用基板は、500nm以上の波長を使用するラマン分光システム又は1064nmの波長を使用するnear-IR FTラマン分光システムに適用可能な、請求項1に記載の分光分析用基板。
- 前記分光分析用基板は、3次元スワブスティック、ウェアラブル基板、又はプラズモニックウェルプレートで構成される、請求項1に記載の分光分析用基板。
- 貴金属前駆体及び還元剤を含み、
貴金属前駆体に対する還元剤の比率が1:0.5~1:15である、分光分析用基板製造用組成物。 - 前記貴金属前駆体に対する還元剤の比率が増加するほど、分光分析用基板に形成される多結晶構造体の大きさが減少し、多結晶構造体の密度が増加する、請求項8に記載の分光分析用基板製造用組成物。
- 前記貴金属前駆体は、HAuCl4及びNaAuCl4のうち、1種以上である、請求項8に記載の分光分析用基板製造用組成物。
- 前記還元剤は、ヒドロキシルアミン(hydroxylamine)、アスコルビン酸(ascorbic acid)、FeSO4、及びヒドロキシキノン(hydroxyquinone)のうち、1種以上である、請求項8に記載の分光分析用基板製造用組成物。
- 光源;
請求項1に記載の分光分析用基板;及び
ラマン分光を検出する検出器を含む、ラマン分光装置。 - 第1端部が開放された筒形であり、第1端部は前記ラマン分光装置に締結される締結部を備え、第2端部は光源からの光を誘導する貫通孔が形成された結合部を備えるアダプタ;及び
ヘッド部及び前記ヘッド部から延長された一字形のボディー部で構成されるスプーン形であって、前記ヘッド部は、前記アダプタの第2端部の結合部が着座される半球形着座部及び前記ボディー部の中心に長手方向に前記半球形の着座部まで延長されて、一字形分光分析用ストリップ基板が着座される着座溝が備えられる測定部材をさらに含む、請求項12に記載のラマン分光装置。 - 前記着座溝はT字形に形成され、前記分光分析用ストリップ基板の末端が前記半球形の着座部から外れないようにすることを特徴とする、請求項13に記載のラマン分光装置。
- 前記検出器の標的物質は、小便、唾、汗及び涙内の細胞、代謝物質、タンパク質、核酸、DNA、RNA、酵素、有機分子、ウイルス、細胞外小胞(extracellular vesicles)、微小小胞(microvesicles)、エキソソーム(exosomes)、及び脂肪から1種以上、選択される、請求項12に記載のラマン分光装置。
- 前記ラマン分光装置はがんの現場診断が可能である、請求項12に記載のラマン分光装置。
- 請求項1に記載の分光分析用基板の製造方法であって、
a)ベース部材を準備するベース部材の準備段階;及び
b)前記ベース部材を貴金属前駆体及び還元剤溶液を含む分光分析用基板製造用組成物に担持し、前記ベース部材上に複数個のナノ粒子の群集から構成され、複数個のグレインバウンダリ(grain boundary)を有する多結晶構造体を形成する段階;を含み、
前記段階b)において、貴金属前駆体溶液に対する還元剤の比率を1:0.5~1:15とし、前記多結晶構造体の形状を調整する形状調整段階を含む、分光分析用基板の製造方法。 - 前記段階a)において、前記ベース部材表面を、多結晶構造体を形成する段階の以前に、表面改質する表面改質段階;をさらに含む、請求項17に記載の分光分析用基板の製造方法。
- 前記表面改質段階は、塩基1~3%及び酸1~3%から選択される1種以上を含み、溶媒(solvent)としてC1-5のアルコール又は水を含む表面改質組成物で前記ベース部材表面を処理することを含む、請求項18に記載の分光分析用基板の製造方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020220066874A KR102837577B1 (ko) | 2022-05-31 | 2022-05-31 | 다결정 구조체를 포함하는 분광분석용 기판 및 이의 제조방법 |
| KR10-2022-0066874 | 2022-05-31 | ||
| PCT/KR2022/020335 WO2023234506A1 (ko) | 2022-05-31 | 2022-12-14 | 다결정 구조체를 포함하는 분광분석용 기판 및 이의 제조방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2025519090A true JP2025519090A (ja) | 2025-06-24 |
Family
ID=89025117
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024569022A Pending JP2025519090A (ja) | 2022-05-31 | 2022-12-14 | 多結晶構造体を含む分光分析用基板及びその製造方法 |
Country Status (8)
| Country | Link |
|---|---|
| EP (1) | EP4534980A1 (ja) |
| JP (1) | JP2025519090A (ja) |
| KR (1) | KR102837577B1 (ja) |
| CN (1) | CN119301437A (ja) |
| AU (1) | AU2022461179A1 (ja) |
| CA (1) | CA3252675A1 (ja) |
| MX (1) | MX2024014784A (ja) |
| WO (1) | WO2023234506A1 (ja) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017524829A (ja) * | 2014-06-20 | 2017-08-31 | ローディア オペレーションズ | 安定剤を含まない金属ナノ粒子合成およびそれから合成される金属ナノ粒子の使用 |
| JP2017181308A (ja) * | 2016-03-30 | 2017-10-05 | キッコーマン株式会社 | 金属ナノ構造体アレイ及び電場増強デバイス |
| JP2019090612A (ja) * | 2016-04-05 | 2019-06-13 | 株式会社ニコン | がん検査方法 |
| JP2021528555A (ja) * | 2018-05-25 | 2021-10-21 | カーボンエックス・アイピー・5・ビー.ブイ.Carbonx Ip 5 B.V. | カーボンナノファイバー含有カーボンネットワークの使用 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20140064872A (ko) * | 2011-08-15 | 2014-05-28 | 퍼듀 리서치 파운데이션 | 흑연 페탈 나노시트 구조의 용도, 및 제조 방법 및 장치 |
| MX384536B (es) * | 2013-02-18 | 2025-03-14 | Labrador Diagnostics Llc | Sistemas y metodos para multiples analisis. |
| KR101484773B1 (ko) * | 2013-06-25 | 2015-01-21 | 가천대학교 산학협력단 | 금 나노입자 복합체 및 그의 제조방법 |
| KR101553467B1 (ko) * | 2014-02-14 | 2015-09-15 | 서울대학교산학협력단 | 시드 성장법을 이용하는 나노입자의 제조 방법 |
| KR101734303B1 (ko) * | 2015-05-22 | 2017-05-12 | 한국기계연구원 | 표면증강라만산란 활성입자 및 그 제조 방법 |
| KR101690877B1 (ko) * | 2015-06-02 | 2016-12-29 | 경희대학교 산학협력단 | 종이 기반 표면증강라만산란 플랫폼의 제조방법 |
| KR101867670B1 (ko) | 2015-07-06 | 2018-06-15 | 경희대학교 산학협력단 | 연속적인 화학적 반응법을 이용한 종이 기반 표면증강라만산란 기재의 제조방법 |
| KR101733664B1 (ko) * | 2016-01-14 | 2017-05-25 | 한국화학연구원 | 저중합체 유전층을 이용한 표면증강라만분석용 기판의 제조방법 |
| KR102046436B1 (ko) * | 2018-04-26 | 2019-11-19 | 한국기계연구원 | 미끄럼 절연막을 포함하는 기판 및 이의 제조방법 |
| KR102257770B1 (ko) * | 2019-08-06 | 2021-05-31 | 한국재료연구원 | 종이기반 분광분석용 기판 및 이의 제조방법 |
-
2022
- 2022-05-31 KR KR1020220066874A patent/KR102837577B1/ko active Active
- 2022-12-14 CN CN202280096555.3A patent/CN119301437A/zh active Pending
- 2022-12-14 CA CA3252675A patent/CA3252675A1/en active Pending
- 2022-12-14 WO PCT/KR2022/020335 patent/WO2023234506A1/ko not_active Ceased
- 2022-12-14 EP EP22945044.0A patent/EP4534980A1/en active Pending
- 2022-12-14 AU AU2022461179A patent/AU2022461179A1/en active Pending
- 2022-12-14 JP JP2024569022A patent/JP2025519090A/ja active Pending
-
2024
- 2024-11-28 MX MX2024014784A patent/MX2024014784A/es unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017524829A (ja) * | 2014-06-20 | 2017-08-31 | ローディア オペレーションズ | 安定剤を含まない金属ナノ粒子合成およびそれから合成される金属ナノ粒子の使用 |
| JP2017181308A (ja) * | 2016-03-30 | 2017-10-05 | キッコーマン株式会社 | 金属ナノ構造体アレイ及び電場増強デバイス |
| JP2019090612A (ja) * | 2016-04-05 | 2019-06-13 | 株式会社ニコン | がん検査方法 |
| JP2021528555A (ja) * | 2018-05-25 | 2021-10-21 | カーボンエックス・アイピー・5・ビー.ブイ.Carbonx Ip 5 B.V. | カーボンナノファイバー含有カーボンネットワークの使用 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20230166644A (ko) | 2023-12-07 |
| KR102837577B1 (ko) | 2025-07-24 |
| WO2023234506A1 (ko) | 2023-12-07 |
| MX2024014784A (es) | 2025-01-09 |
| CN119301437A (zh) | 2025-01-10 |
| CA3252675A1 (en) | 2025-07-07 |
| AU2022461179A1 (en) | 2024-12-05 |
| EP4534980A1 (en) | 2025-04-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Lin et al. | Lab-on-capillary platform for on-site quantitative SERS analysis of surface contaminants based on Au@ 4-MBA@ Ag core–shell nanorods | |
| Adamo et al. | Fast and straightforward in-situ synthesis of gold nanoparticles on a thread-based microfluidic device for application in surface-enhanced Raman scattering detection | |
| Zhou et al. | Amphiphilic functionalized acupuncture needle as SERS sensor for in situ multiphase detection | |
| Wallace et al. | From single cells to complex tissues in applications of surface-enhanced Raman scattering | |
| Rajapandiyan et al. | Sensitive cylindrical SERS substrate array for rapid microanalysis of nucleobases | |
| Wu et al. | 3D hierarchic interfacial assembly of Au nanocage@ Au along with IS-AgMNPs for simultaneous, ultrasensitive, reliable, and quantitative SERS detection of colorectal cancer related miRNAs | |
| CN111770837B (zh) | 用于感知尿代谢物和毒素的超疏水性平台 | |
| Ma et al. | Precision improvement in dark-field microscopy imaging by using gold nanoparticles as an internal reference: a combined theoretical and experimental study | |
| EP3350117B1 (en) | End-cap suitable for optical fiber devices and nanoplasmonic sensors | |
| Na et al. | Analyte-Induced desert rose-like Ag nanostructures for surface-enhanced Raman scattering-based biomolecule detection and imaging | |
| CN114410781B (zh) | 用于检测肺癌标志物的免泵sers微流控芯片及其制备方法和使用方法 | |
| Yi et al. | Micro-macro SERS strategy for highly sensitive paper cartridge with trace-level molecular detection | |
| Lv et al. | Enhanced superhydrophobic substrate-based 3D SERS platform for a portable Raman spectrometer-assisted drug detection in plasma | |
| JP2025519090A (ja) | 多結晶構造体を含む分光分析用基板及びその製造方法 | |
| CN110658167B (zh) | 基于银-金属有机骨架材料作为荧光探针应用于叶酸检测的方法 | |
| CN113777034B (zh) | 金纳米双锥阵列基底及其制备方法和应用 | |
| TWI657166B (zh) | 攜帶式拉曼光學檢測試紙及其製法與使用方法 | |
| Wang et al. | SERS hydrogel designed using a microfluidic droplet platform for label-free therapeutic drug monitoring of doxorubicin in human serum | |
| RU2854766C2 (ru) | Подложка для спектроскопического анализа, включающая поликристаллическую структуру, и способ ее получения | |
| Fu et al. | Composite surface enhanced Raman scattering substrate of flower-shaped ZIF-67 and Au nanorods for simultaneous detection of creatinine and urea nitrogen | |
| KR102798902B1 (ko) | 표면증강라만산란 분광용 구조체 및 그 제조방법 | |
| US12005448B2 (en) | Systems and methods of using anisotropic nanostructures in microfluidic devices for binding and optional release of molecules and cells | |
| Tang et al. | Copper hydroxide nanowires assisted molecule enrichment for highly sensitive SERS detection | |
| Lei et al. | A Size-Determined Growth Rule Enables Well-Preserved Silver–Gold Core–Shell Nanocubes for Reliable Surface-Enhanced Raman Scattering Bioanalysis | |
| KR102929032B1 (ko) | 분광분석용 플라즈모닉 웰플레이트 기판 및 이의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20241120 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20251023 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20251028 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20260123 |