JP2023082015A - 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム - Google Patents
免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム Download PDFInfo
- Publication number
- JP2023082015A JP2023082015A JP2023039900A JP2023039900A JP2023082015A JP 2023082015 A JP2023082015 A JP 2023082015A JP 2023039900 A JP2023039900 A JP 2023039900A JP 2023039900 A JP2023039900 A JP 2023039900A JP 2023082015 A JP2023082015 A JP 2023082015A
- Authority
- JP
- Japan
- Prior art keywords
- immune checkpoint
- checkpoint inhibitor
- subject
- free protein
- free
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 title claims abstract description 162
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 title claims abstract description 162
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 title claims abstract description 162
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 title claims abstract description 162
- 238000000034 method Methods 0.000 title claims abstract description 108
- 239000003153 chemical reaction reagent Substances 0.000 title claims abstract description 93
- 238000004590 computer program Methods 0.000 title claims abstract description 25
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 54
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 54
- 239000007788 liquid Substances 0.000 claims abstract description 53
- 239000003446 ligand Substances 0.000 claims abstract description 10
- 238000005259 measurement Methods 0.000 claims description 127
- 206010028980 Neoplasm Diseases 0.000 claims description 86
- 239000012474 protein marker Substances 0.000 claims description 73
- 201000011510 cancer Diseases 0.000 claims description 48
- 239000000126 substance Substances 0.000 claims description 47
- 239000003550 marker Substances 0.000 claims description 35
- 210000004881 tumor cell Anatomy 0.000 claims description 25
- 238000012744 immunostaining Methods 0.000 claims description 19
- 210000004369 blood Anatomy 0.000 claims description 18
- 239000008280 blood Substances 0.000 claims description 18
- 210000004027 cell Anatomy 0.000 claims description 16
- 239000004480 active ingredient Substances 0.000 claims description 15
- 206010014733 Endometrial cancer Diseases 0.000 claims description 12
- 206010014759 Endometrial neoplasm Diseases 0.000 claims description 12
- 208000000461 Esophageal Neoplasms Diseases 0.000 claims description 12
- 206010030155 Oesophageal carcinoma Diseases 0.000 claims description 12
- 201000004101 esophageal cancer Diseases 0.000 claims description 12
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 9
- 201000005202 lung cancer Diseases 0.000 claims description 9
- 208000020816 lung neoplasm Diseases 0.000 claims description 9
- 239000000203 mixture Substances 0.000 claims description 9
- 238000009472 formulation Methods 0.000 claims description 8
- 239000008194 pharmaceutical composition Substances 0.000 claims description 7
- 239000003795 chemical substances by application Substances 0.000 claims description 3
- 230000005746 immune checkpoint blockade Effects 0.000 claims description 2
- 238000004364 calculation method Methods 0.000 claims 2
- 102100040678 Programmed cell death protein 1 Human genes 0.000 description 53
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 53
- 102000008203 CTLA-4 Antigen Human genes 0.000 description 48
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 48
- 210000001519 tissue Anatomy 0.000 description 39
- 239000000523 sample Substances 0.000 description 38
- 238000001514 detection method Methods 0.000 description 31
- 229960003301 nivolumab Drugs 0.000 description 24
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 22
- 238000003018 immunoassay Methods 0.000 description 21
- 239000006249 magnetic particle Substances 0.000 description 21
- 239000007790 solid phase Substances 0.000 description 21
- 239000000872 buffer Substances 0.000 description 17
- 238000011532 immunohistochemical staining Methods 0.000 description 16
- 238000002372 labelling Methods 0.000 description 16
- 102000004190 Enzymes Human genes 0.000 description 15
- 108090000790 Enzymes Proteins 0.000 description 15
- 238000011282 treatment Methods 0.000 description 15
- 230000003287 optical effect Effects 0.000 description 14
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 13
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 13
- 230000008569 process Effects 0.000 description 12
- 230000004083 survival effect Effects 0.000 description 12
- 229960002685 biotin Drugs 0.000 description 11
- 235000020958 biotin Nutrition 0.000 description 11
- 239000011616 biotin Substances 0.000 description 11
- 210000002381 plasma Anatomy 0.000 description 11
- 230000035945 sensitivity Effects 0.000 description 11
- 239000000758 substrate Substances 0.000 description 10
- 229940045513 CTLA4 antagonist Drugs 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 239000013642 negative control Substances 0.000 description 8
- 229960002621 pembrolizumab Drugs 0.000 description 8
- 238000003118 sandwich ELISA Methods 0.000 description 8
- 210000001744 T-lymphocyte Anatomy 0.000 description 7
- 238000004891 communication Methods 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 238000010186 staining Methods 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 238000010586 diagram Methods 0.000 description 6
- 239000002245 particle Substances 0.000 description 6
- 238000011002 quantification Methods 0.000 description 6
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 5
- 239000007995 HEPES buffer Substances 0.000 description 5
- 102000037982 Immune checkpoint proteins Human genes 0.000 description 5
- 108091008036 Immune checkpoint proteins Proteins 0.000 description 5
- 239000007987 MES buffer Substances 0.000 description 5
- 108010090804 Streptavidin Proteins 0.000 description 5
- 239000007853 buffer solution Substances 0.000 description 5
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 5
- 238000012545 processing Methods 0.000 description 5
- 230000004044 response Effects 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 5
- 108090001008 Avidin Proteins 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 239000000427 antigen Substances 0.000 description 4
- 108091007433 antigens Proteins 0.000 description 4
- 102000036639 antigens Human genes 0.000 description 4
- 239000012830 cancer therapeutic Substances 0.000 description 4
- 239000003112 inhibitor Substances 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 239000006228 supernatant Substances 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 102000003992 Peroxidases Human genes 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- 230000006044 T cell activation Effects 0.000 description 3
- 239000012736 aqueous medium Substances 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 238000007796 conventional method Methods 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 3
- 239000000284 extract Substances 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 229940126546 immune checkpoint molecule Drugs 0.000 description 3
- 108040007629 peroxidase activity proteins Proteins 0.000 description 3
- 239000002953 phosphate buffered saline Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- 108091023037 Aptamer Proteins 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical compound C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 2
- 238000011226 adjuvant chemotherapy Methods 0.000 description 2
- 229940125644 antibody drug Drugs 0.000 description 2
- 229960003852 atezolizumab Drugs 0.000 description 2
- 229950002916 avelumab Drugs 0.000 description 2
- 229920001222 biopolymer Polymers 0.000 description 2
- 239000003593 chromogenic compound Substances 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 239000000356 contaminant Substances 0.000 description 2
- UKWLRLAKGMZXJC-QIECWBMSSA-L disodium;[4-chloro-3-[(3r,5s)-1-chloro-3'-methoxyspiro[adamantane-4,4'-dioxetane]-3'-yl]phenyl] phosphate Chemical compound [Na+].[Na+].O1OC2([C@@H]3CC4C[C@H]2CC(Cl)(C4)C3)C1(OC)C1=CC(OP([O-])([O-])=O)=CC=C1Cl UKWLRLAKGMZXJC-QIECWBMSSA-L 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 229950009791 durvalumab Drugs 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 2
- 150000002484 inorganic compounds Chemical class 0.000 description 2
- 229910010272 inorganic material Inorganic materials 0.000 description 2
- 229960005386 ipilimumab Drugs 0.000 description 2
- 239000007791 liquid phase Substances 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 239000011259 mixed solution Substances 0.000 description 2
- 229920000620 organic polymer Polymers 0.000 description 2
- 238000004806 packaging method and process Methods 0.000 description 2
- 238000012856 packing Methods 0.000 description 2
- CMPQUABWPXYYSH-UHFFFAOYSA-N phenyl phosphate Chemical compound OP(O)(=O)OC1=CC=CC=C1 CMPQUABWPXYYSH-UHFFFAOYSA-N 0.000 description 2
- -1 polypropylene Polymers 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- QRXMUCSWCMTJGU-UHFFFAOYSA-L (5-bromo-4-chloro-1h-indol-3-yl) phosphate Chemical compound C1=C(Br)C(Cl)=C2C(OP([O-])(=O)[O-])=CNC2=C1 QRXMUCSWCMTJGU-UHFFFAOYSA-L 0.000 description 1
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- IHPYMWDTONKSCO-UHFFFAOYSA-N 2,2'-piperazine-1,4-diylbisethanesulfonic acid Chemical compound OS(=O)(=O)CCN1CCN(CCS(O)(=O)=O)CC1 IHPYMWDTONKSCO-UHFFFAOYSA-N 0.000 description 1
- UAIUNKRWKOVEES-UHFFFAOYSA-N 3,3',5,5'-tetramethylbenzidine Chemical compound CC1=C(N)C(C)=CC(C=2C=C(C)C(N)=C(C)C=2)=C1 UAIUNKRWKOVEES-UHFFFAOYSA-N 0.000 description 1
- XZKIHKMTEMTJQX-UHFFFAOYSA-N 4-Nitrophenyl Phosphate Chemical compound OP(O)(=O)OC1=CC=C([N+]([O-])=O)C=C1 XZKIHKMTEMTJQX-UHFFFAOYSA-N 0.000 description 1
- QRXMUCSWCMTJGU-UHFFFAOYSA-N 5-bromo-4-chloro-3-indolyl phosphate Chemical compound C1=C(Br)C(Cl)=C2C(OP(O)(=O)O)=CNC2=C1 QRXMUCSWCMTJGU-UHFFFAOYSA-N 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 239000012099 Alexa Fluor family Substances 0.000 description 1
- 206010003445 Ascites Diseases 0.000 description 1
- 102000008096 B7-H1 Antigen Human genes 0.000 description 1
- 108010074708 B7-H1 Antigen Proteins 0.000 description 1
- 108700031361 Brachyury Proteins 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- QXNVGIXVLWOKEQ-UHFFFAOYSA-N Disodium Chemical compound [Na][Na] QXNVGIXVLWOKEQ-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 239000006173 Good's buffer Substances 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 239000007990 PIPES buffer Substances 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- WGLPBDUCMAPZCE-UHFFFAOYSA-N Trioxochromium Chemical compound O=[Cr](=O)=O WGLPBDUCMAPZCE-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- QWXOJIDBSHLIFI-UHFFFAOYSA-N [3-(1-chloro-3'-methoxyspiro[adamantane-4,4'-dioxetane]-3'-yl)phenyl] dihydrogen phosphate Chemical compound O1OC2(C3CC4CC2CC(Cl)(C4)C3)C1(OC)C1=CC=CC(OP(O)(O)=O)=C1 QWXOJIDBSHLIFI-UHFFFAOYSA-N 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- OHDRQQURAXLVGJ-HLVWOLMTSA-N azane;(2e)-3-ethyl-2-[(e)-(3-ethyl-6-sulfo-1,3-benzothiazol-2-ylidene)hydrazinylidene]-1,3-benzothiazole-6-sulfonic acid Chemical compound [NH4+].[NH4+].S/1C2=CC(S([O-])(=O)=O)=CC=C2N(CC)C\1=N/N=C1/SC2=CC(S([O-])(=O)=O)=CC=C2N1CC OHDRQQURAXLVGJ-HLVWOLMTSA-N 0.000 description 1
- YJFXSWKKBWMMCM-UHFFFAOYSA-N azanium;3-ethyl-2h-1,3-benzothiazole-6-sulfonate Chemical compound [NH4+].[O-]S(=O)(=O)C1=CC=C2N(CC)CSC2=C1 YJFXSWKKBWMMCM-UHFFFAOYSA-N 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 102000005936 beta-Galactosidase Human genes 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 238000010241 blood sampling Methods 0.000 description 1
- 230000003139 buffering effect Effects 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 229910000423 chromium oxide Inorganic materials 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 1
- JIQQITINEAMHOX-UHFFFAOYSA-L disodium;(5-bromo-6-chloro-1h-indol-2-yl) phosphate Chemical compound [Na+].[Na+].BrC1=C(Cl)C=C2NC(OP([O-])(=O)[O-])=CC2=C1 JIQQITINEAMHOX-UHFFFAOYSA-L 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 210000001808 exosome Anatomy 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000009093 first-line therapy Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 108091006047 fluorescent proteins Proteins 0.000 description 1
- 102000034287 fluorescent proteins Human genes 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000002523 gelfiltration Methods 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 230000003832 immune regulation Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000011221 initial treatment Methods 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 238000010827 pathological analysis Methods 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 210000004910 pleural fluid Anatomy 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 238000010837 poor prognosis Methods 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 238000009094 second-line therapy Methods 0.000 description 1
- 238000011519 second-line treatment Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000012956 testing procedure Methods 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 229910000859 α-Fe Inorganic materials 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
- G01N33/57488—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites involving compounds identifable in body fluids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57423—Specifically defined cancers of lung
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57442—Specifically defined cancers of the uterus and endometrial
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70503—Immunoglobulin superfamily, e.g. VCAMs, PECAM, LFA-3
- G01N2333/70521—CD28, CD152
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70503—Immunoglobulin superfamily, e.g. VCAMs, PECAM, LFA-3
- G01N2333/70532—B7 molecules, e.g. CD80, CD86
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H50/00—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics
- G16H50/20—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics for computer-aided diagnosis, e.g. based on medical expert systems
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Organic Chemistry (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Oncology (AREA)
- Pathology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Hospice & Palliative Care (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Reproductive Health (AREA)
- Epidemiology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
【課題】免疫チェックポイント阻害剤の奏効性予測を高い精度で判定可能な検査の提供。【解決手段】本発明は、免疫チェックポイント阻害剤の奏効性の判定を補助する方法に関する。被検者から採取した液体試料中の遊離タンパク質マーカーを測定する工程を含み、前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含み、前記被検者に対する免疫チェックポイント阻害剤の奏効性を示唆する、免疫チェックポイント阻害剤の奏効性の判定を補助する方法。また、本発明は、この方法に用いるための試薬キットに関する。さらに、本発明は、免疫チェックポイント阻害剤の奏効性の判定のための装置及びコンピュータプログラムに関する。【選択図】なし
Description
本発明は、免疫チェックポイント阻害剤の奏効性の判定を補助する方法に関する。また、本発明は、この方法に用いるための試薬キットに関する。さらに、本発明は、免疫チェックポイント阻害剤の奏効性の判定のための装置及びコンピュータプログラムに関する。
活性化したT細胞の表面には、PD-1(Programmed cell death-1)と呼ばれる受容体分子が発現している(非特許文献1参照)。PD-1は、T細胞の過剰な活性化を抑制して、生体の免疫応答を負に制御する分子として知られている。また、活性化したT細胞の表面には、CTLA-4(Cytotoxic T lymphocyte antigen-4)と呼ばれる分子も発現している。CTLA-4も、PD-1と同様に、T細胞の活性化を抑制する機能を有する。一方、がん局所の細胞には、PD-1のリガンドであるPD-L1(Programmed cell death-ligand 1)を細胞表面に発現するものがある。そのようながん局所の細胞は、自らのPD-L1とT細胞のPD-1との結合を介してT細胞の活性化を抑制し、T細胞の攻撃を回避することが知られている。その結果、がんは生体内で増大する。実際、がん局所のPD-L1発現量とがん患者の予後不良率には相関関係がある。このように、PD-L1、PD-1及びCTLA-4は、免疫の制御に関与することから、免疫チェックポイント分子とも呼ばれる。
近年、新たながんの治療薬として、免疫チェックポイント分子に対する抗体が注目されている。これらの抗体を有効成分として含む製剤は、免疫チェックポイント阻害剤とも呼ばれる。免疫チェックポイント阻害剤は、T細胞の活性化を抑制する上記の分子を阻害することによりT細胞の活性化を促進して、このT細胞の抗腫瘍応答性を増強させる。すなわち、免疫チェックポイント阻害剤による治療では、上記の抗体の投与によって生体の免疫状態を活性化させることにより、がんを排除する。
Agata Y.ら, Expression of the PD-1 antigen on the surface of stimulated mouse T and B lymphocytes. Int. Immunol., 1996, vol.8, p.765-772
免疫チェックポイント阻害剤の奏効性予測を高い精度で判定可能な検査の開発が望まれる。これまでに、がん患者から採取した腫瘍組織を免疫染色し、PD-L1陽性腫瘍細胞の割合を確認することによって抗PD-1抗体薬や抗PD-L1抗体薬の有効性を予測する方法が知られている。本発明の課題は、免疫チェックポイント阻害剤の奏効性の予測を行うことのできる新規方法を提供することである。
本発明は、被検者から採取した液体試料中の遊離タンパク質マーカーを測定する工程と、測定結果に基づいて、該被検者に対する免疫チェックポイント阻害剤の奏効性を判定する工程とを含み、該遊離タンパク質マーカーが、遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つである、免疫チェックポイント阻害剤の奏効性を判定する方法を提供する。
本発明は、がん患者から採取した液体試料中の遊離タンパク質マーカーを測定する工程と、測定結果に基づいて、該患者に対する免疫チェックポイント阻害剤の奏効性を判定する工程と、免疫チェックポイント阻害剤が奏効すると判定された患者に免疫チェックポイント阻害剤を投与する工程とを含み、該遊離タンパク質マーカーが、遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つである、がんの治療方法を提供する。
本発明は、本実施形態の判定方法により免疫チェックポイント阻害剤が奏効すると判定されたがん患者に投与されることを特徴とする免疫チェックポイント阻害剤を含有するがん治療用医薬組成物、及び本実施形態の判定方法により免疫チェックポイント阻害剤が奏効すると判定されたがん患者に投与されることを特徴とする免疫チェックポイント阻害剤を含有するがん治療剤を提供する。
本発明は、被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得する工程を含み、該遊離タンパク質マーカーが遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つであり、取得した遊離タンパク質マーカーの測定値が、各マーカーに対応する所定の閾値より低いとき、免疫チェックポイント阻害剤が該被検者に奏効することを示唆する、遊離タンパク質マーカーの測定値の取得方法を提供する。
本発明は、遊離CTLA-4に特異的に結合可能な物質を含む試薬、遊離PD-1に特異的に結合可能な物質を含む試薬、及び遊離PD-L1と特異的に結合可能な物質を含む試薬から選択される少なくとも1つの試薬を含む、上記の判定を補助する方法に用いるための試薬キットを提供する。
本発明は、被検者から採取した腫瘍組織の免疫染色を行い、PD-L1陽性腫瘍細胞の割合を算出する工程と、被検者から採取した液体試料中の遊離タンパク質マーカーを測定する工程と、算出結果と測定結果とに基づいて、被検者に対する免疫チェックポイント阻害剤の奏効性を判定する工程とを含み、該遊離タンパク質マーカーが、遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つである、免疫チェックポイント阻害剤の奏効性の判定を補助する方法を提供する。
本発明は、プロセッサ及び該プロセッサの制御下にあるメモリを含むコンピュータを備え、該メモリには、被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得するステップと、該マーカーの測定値に基づいて、該被検者に対する免疫チェックポイント阻害剤の奏効性を判定するステップとを上記コンピュータに実行させるためのコンピュータプログラムが記録されており、該遊離タンパク質マーカーが、遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つである、免疫チェックポイント阻害剤の奏効性の判定装置を提供する。
本発明は、プロセッサ及び該プロセッサの制御下にあるメモリを含むコンピュータを備え、該メモリには、被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得するステップを上記コンピュータに実行させるためのコンピュータプログラムが記録されており、該遊離タンパク質マーカーが、遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つであり、取得した遊離タンパク質マーカーの測定値が、各マーカーに対応する所定の閾値より低いとき、免疫チェックポイント阻害剤が該被検者に奏効することを示唆する、遊離タンパク質マーカーの測定値の取得装置を提供する。
本発明は、コンピュータが読み取り可能な媒体に記録されているコンピュータプログラムであって、該コンピュータプログラムが、被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得するステップと、該マーカーの測定値に基づいて、該被検者に対する免疫チェックポイント阻害剤の奏効性を判定するステップとを該コンピュータに実行させるためのコンピュータプログラムであり、該遊離タンパク質マーカーが、遊離CTLA-4、遊離PD-1及び遊離PD-L1から選択される少なくとも1つである、免疫チェックポイント阻害剤の奏効性の判定のためのコンピュータプログラムを提供する。
本発明によれば、被検者に免疫チェックポイント阻害剤を投与する前に、該被検者に対して免疫チェックポイント阻害剤が奏効するか否かを判定することを可能にする。
[1.免疫チェックポイント阻害剤の奏効性の判定方法]
本実施形態の免疫チェックポイント阻害剤の奏効性の判定方法(以下、「判定方法」ともいう)では、まず、被検者から採取した液体試料中の遊離タンパク質マーカーとして遊離PD-1、遊離CTLA-4及び遊離PD-L1から選択される少なくとも1つを測定する。好ましい実施形態では、遊離PD-1、遊離CTLA-4及び遊離PD-L1から選択される少なくとも2つを測定する。より好ましい実施形態では、遊離PD-1、遊離CTLA-4及び遊離PD-L1を測定する。
本実施形態の免疫チェックポイント阻害剤の奏効性の判定方法(以下、「判定方法」ともいう)では、まず、被検者から採取した液体試料中の遊離タンパク質マーカーとして遊離PD-1、遊離CTLA-4及び遊離PD-L1から選択される少なくとも1つを測定する。好ましい実施形態では、遊離PD-1、遊離CTLA-4及び遊離PD-L1から選択される少なくとも2つを測定する。より好ましい実施形態では、遊離PD-1、遊離CTLA-4及び遊離PD-L1を測定する。
免疫チェックポイント阻害剤は、有効成分として、抗PD-1抗体、抗CTLA-4抗体及び抗PD-L1抗体の少なくとも1種を含む製剤であればよい。有効成分として抗PD-1抗体を含む製剤としては、ニボルマブ、ペムブロリズマブなどが公知である。有効成分として抗PD-L1抗体を含む製剤としては、アテゾリズマブ、アベルマブ、デュルバルマブなどが公知である。有効成分として抗CTLA-4抗体を含む製剤としては、イピリムマブなどが公知である。本実施形態の判定方法は、特に、有効成分として抗PD-1抗体を含む製剤の奏効性の判定に適する。
本実施形態の方法における被検者としては、例えば、がんの罹患が疑われる者及びがん患者が挙げられる。本明細書において「がん患者」は、腫瘍組織の除去後の被検者を含む。腫瘍組織の除去後に、補助化学療法として免疫チェックポイント阻害剤が投与される場合がある。本実施形態の判定方法は、補助化学療法のための免疫チェックポイント阻害剤の奏効性判定にも用いられ得る。がん患者としては、免疫チェックポイント阻害剤による治療を受ける前のがん患者が好ましい。被検者は、免疫チェックポイント阻害剤以外の治療を受けていてもよい。そのような治療としては、手術、放射線照射、化学療法及びこれらの組み合わせなどが挙げられる。がんの種類は特に限定されず、例えば、固形がん及び血液がんなどの種々のがんが挙げられる。固形がんとしては、例えば、肺がん、食道がん、子宮体がん、腎臓がん、卵巣がん、メラノーマ、胃がん、大腸がんなどが挙げられる。血液がんとしては、例えば、白血病、悪性リンパ腫、多発性骨髄腫などが挙げられる。これらの中でも、肺がん(特に非小細胞肺がん)、食道がん及び子宮体がんが本実施形態の判定方法に適している。
上述のように、がん患者から採取した腫瘍組織を免疫染色し、PD-L1陽性腫瘍細胞の割合を確認することにより、免疫チェックポイント阻害剤の有効性を予測する方法が知られている。しかし、この方法には腫瘍組織が用いられるので、例えば身体的負担等の理由により腫瘍組織を採取することができない被検者には適用できない。一方、本実施形態の判定方法では、血液試料など、侵襲性の低い方法で採取された試料を用いることができる。すなわち、本実施形態の判定方法は、腫瘍組織の採取が難しい被検者にも適用できる。また、免疫染色は、検査手技が煩雑であるので自動化に適していない。これに対して、液体試料中の遊離タンパク質マーカーの測定は自動化に適しており、本実施形態の判定方法は、病理検査の効率化を推進するという観点から好適である。
上記の免疫染色と、本実施形態の判定方法とを組み合わせて用いることも可能である。これにより、判定精度が向上し得る。例えば、後述の実施例に示されるように、本実施形態の判定方法は、PD-L1陽性腫瘍細胞の割合が所定の値より低い患者から、免疫チェックポイント阻害剤が奏効する患者を抽出することができる。この場合、被検者は、腫瘍組織の免疫染色により、PD-L1陽性腫瘍細胞の割合が所定の値より低いと判定されたがん患者である。
腫瘍組織の免疫染色は、当該技術分野において公知の免疫組織染色法により行うことができる。特に、病理診断のガイドラインなどに従って、免疫チェックポイント分子を特異的に認識する抗体を用いて免疫組織染色を行うことが好ましい。免疫組織染色は、市販の染色用キットを用いて行ってもよい。腫瘍組織のPD-L1免疫染色を行うためのキットとして、PD-L1 IHC 22C3 pharmDx「ダコ」(Agilent Technologies, Inc.)、PD-L1 IHC 28-8 pharmDx「ダコ」(Agilent Technologies, Inc.)などが公知である。
腫瘍組織のPD-L1免疫染色は、例えば、次のようにして行うことができる。まず、被検者から腫瘍組織を採取し、得られた腫瘍組織を1時間以内に10%中性緩衝ホルマリンで固定する。固定時間は、12時間以上72時間以内とする。固定した腫瘍組織をエタノールにより脱水する。脱水した腫瘍組織をキシレンに浸して透徹処理を行う。処理後の腫瘍組織を、融解したパラフィン(60℃以下)に浸漬して冷却し、ホルマリン固定パラフィン包埋(FFPE)組織標本を得る。得られたFFPE組織標本を厚さ4~5μmで薄切し、スライドガラスに貼り付ける。得られた薄切切片にキシレンを添加して、脱パラフィン処理をする。脱パラフィン処理した薄切切片をエタノールに浸して親水化処理をする。親水化処理した薄切切片を貼り付けたスライドガラスを、市販の抗原賦活化液に入れて加熱することにより、抗原賦活化処理をする。処理後の薄切切片に、抗PD-L1抗体を用いて免疫組織染色を行って、組織標本を得る。
PD-L1陽性腫瘍細胞の割合は、腫瘍組織の免疫染色により得られた組織標本中の全腫瘍細胞に対する、部分的又は完全な細胞膜染色を呈する腫瘍細胞の割合である。PD-L1陽性腫瘍細胞の割合として、PD-L1 IHC 22C3 pharmDx「ダコ」の染色結果判定マニュアルに定義されるTumor Proportion Score(TPS)を用いてもよい。TPSは、下記の式により算出できる。式中、「全腫瘍細胞数」は、腫瘍組織のHE染色により得られた組織標本中の全ての腫瘍細胞の数であり、少なくとも100個であることが必要である。「PD-L1陽性腫瘍細胞数」は、組織標本中の部分的又は完全な細胞膜PD-L1免疫染色を呈する腫瘍細胞の数である。PD-L1陽性腫瘍細胞には、マクロファージ、リンパ球などの腫瘍関連免疫細胞は含まれない。各細胞数は、光学顕微鏡での観察により計数される。
上記の所定の値は、PD-L1陽性腫瘍細胞の割合のカットオフ値である。所定の値自体は、特に限定されず、免疫染色に用いた抗体(又は染色用キット)、及び対象となる癌種などに応じて適宜決定される。例えば、PD-L1 IHC 22C3 pharmDx「ダコ」を用いて非小細胞肺がんの腫瘍組織を免疫染色した場合では、50%のTPSを所定の値として、ペムブロリズマブによる一次治療の対象が決定される。また、1%のTPSを所定の値として、ペムブロリズマブによる二次治療の対象が決定される。具体的には、TPSが50%以上のときはPD-L1陽性(高発現)と判定し、TPS1%以上且つ50%より低いときはPD-L1陽性(低発現)と判定し、TPSが1%より低いときはPD-L1陰性(非発現)と判定する。PD-L1陽性(高発現)と判定された被検者は、ペムブロリズマブによる一次治療の対象となる。PD-L1陽性(低発現)と判定された被検者は、一次治療の対象から除外されるが、ペムブロリズマブによる二次治療の対象となる。PD-L1陰性と判定された被検者は、ペムブロリズマブによる治療の対象から除外される。
本実施形態における被検者は、PD-L1陽性腫瘍細胞の割合が所定の値より低いと判定されたがん患者であり得る。PD-L1陽性腫瘍細胞の割合が所定の値より低いと判定されたがん患者は、免疫チェックポイント阻害剤による一次治療の対象から除外される患者であってもよい。
液体試料は、被検者から採取され、遊離タンパク質が含まれ得る液状の試料であれば特に限定されない。そのような液体試料としては、例えば、血液試料、脳脊髄液、胸水、腹水、リンパ液、尿などが挙げられる。本実施形態では、液体試料としては血液試料が好ましい。血液試料としては、全血、血漿及び血清が挙げられ、特に血漿及び血清が好ましい。
液体試料に細胞などの不溶性の夾雑物が含まれる場合は、例えば、遠心分離、ろ過などの公知の手段により、液体試料から夾雑物を除去してもよい。また、液体試料は、必要に応じて適切な水性媒体で希釈してもよい。そのような水性媒体は、後述の測定を妨げないかぎり特に限定されず、例えば、水、生理食塩水、緩衝液などが挙げられる。緩衝液は、中性付近のpH(例えば6以上8以下のpH)で緩衝作用を有するかぎり、特に限定されない。そのような緩衝液は、例えば、HEPES、MES、Tris、PIPESなどのグッド緩衝液、リン酸緩衝生理食塩水(PBS)などが挙げられる。
遊離PD-1、遊離CTLA-4及び遊離PD-L1は、いずれも遊離タンパク質である。以下、遊離PD-1、遊離CTLA-4及び遊離PD-L1をそれぞれ「sPD-1」、「sCTLA-4」及び「sPD-L1」とも呼ぶ。本明細書において「遊離タンパク質」とは、細胞の表面から脱離して、該細胞の外部(液体試料中)に存在するタンパク質をいう。そのような遊離タンパク質は、液体試料の液体成分(液相)に可溶化したタンパク質、ベシクルに内包されたタンパク質、及びベシクルの表面に存在するタンパク質のいずれであってもよい。ベシクルは、膜で構成された小胞であれば特に限定されない。ベシクルは、内部に液相を含んでいてもよい。好ましいベシクルは細胞外小胞であり、例えば、エクソソーム、マイクロベシクル、アポトーシス小体などが挙げられる。
遊離タンパク質マーカーを測定する手段は、液体試料に含まれる遊離タンパク質マーカーの量又は濃度を反映する値(以下、「マーカーの測定値」ともいう)を取得できるかぎり、特に限定されない。本実施形態では、遊離タンパク質マーカーと特異的に結合可能な物質を用いて、該マーカーを捕捉する方法が好ましい。このような物質により捕捉された遊離タンパク質マーカーを、当該技術において公知の方法で検出することにより、液体試料に含まれる遊離タンパク質マーカーを測定できる。
遊離タンパク質マーカーと特異的に結合可能な物質としては、例えば、抗体、アプタマーなどが挙げられるが、それらの中でも抗体が特に好ましい。PD-1、CTLA-4及びPD-L1の各タンパク質に対する抗体自体は、当該技術において公知であり、一般に入手可能である。遊離タンパク質マーカーに対する抗体は、遊離タンパク質マーカーと特異的に結合できる抗体であれば、特に限定されない。そのような抗体は、モノクローナル抗体、ポリクローナル抗体、及びそれらの断片(例えば、Fab、F(ab')2など)のいずれであってもよい。また、市販の抗体を用いてもよい。
抗体を用いて遊離タンパク質マーカーを測定する方法は、特に限定されず、公知の免疫学的測定法から適宜選択できる。本実施形態においては、酵素結合免疫吸着法(ELISA法)が好ましく、サンドイッチELISA法が特に好ましい。測定工程の一例として、サンドイッチELISA法により、液体試料中の遊離タンパク質マーカーを測定する場合について、以下に説明する。
まず、遊離タンパク質マーカーと、遊離タンパク質マーカーを捕捉するための抗体(以下、「捕捉用抗体」ともいう)と、遊離タンパク質マーカーを検出するための抗体(以下、「検出用抗体」ともいう)とを含む複合体を固相上に形成させる。該複合体は、遊離タンパク質マーカーを含み得る液体試料と、捕捉用抗体と、検出用抗体とを混合することにより形成できる。そして、複合体を含む溶液を、捕捉用抗体を固定できる固相と接触させることにより、上記の複合体を固相上に形成させることができる。あるいは、捕捉用抗体をあらかじめ固定させた固相を用いてもよい。すなわち、捕捉用抗体を固定させた固相と、液体試料と、検出用抗体とを接触することにより、上記の複合体を固相上に形成させることができる。なお、捕捉用抗体及び検出用抗体がいずれもモノクローナル抗体の場合は、互いのエピトープが異なっていることが好ましい。
捕捉用抗体の固相への固定の態様は、特に限定されない。例えば、捕捉用抗体と固相とを直接結合させてもよいし、捕捉用抗体と固相とを別の物質を介して間接的に結合させてもよい。直接の結合としては、例えば、物理的吸着などが挙げられる。間接的な結合としては、例えば、ビオチンと、アビジン又はストレプトアビジン(以下、「アビジン類」ともいう)との組み合わせを介した結合が挙げられる。この場合、捕捉用抗体をあらかじめビオチンで修飾し、固相にアビジン類をあらかじめ結合させておくことにより、ビオチンとアビジン類との結合を介して、捕捉用抗体と固相とを間接的に結合させることができる。
固相の素材は特に限定されず、例えば、有機高分子化合物、無機化合物、生体高分子などから選択できる。有機高分子化合物としては、ラテックス、ポリスチレン、ポリプロピレンなどが挙げられる。無機化合物としては、磁性体(酸化鉄、酸化クロム及びフェライトなど)、シリカ、アルミナ、ガラスなどが挙げられる。生体高分子としては、不溶性アガロース、不溶性デキストラン、ゼラチン、セルロースなどが挙げられる。これらのうちの2種以上を組み合わせて用いてもよい。固相の形状は特に限定されず、例えば、粒子、膜、マイクロプレート、マイクロチューブ、試験管などが挙げられる。それらの中でも粒子が好ましく、磁性粒子が特に好ましい。
本実施形態においては、複合体の形成工程と複合体の検出工程との間に、複合体を形成していない未反応の遊離成分を除去するB/F(Bound/Free)分離を行ってもよい。未反応の遊離成分とは、複合体を構成しない成分をいう。例えば、遊離タンパク質マーカーと結合しなかった捕捉用抗体及び検出用抗体などが挙げられる。B/F分離の手段は特に限定されないが、固相が粒子であれば、遠心分離により、複合体を捕捉した固相だけを回収することによりB/F分離ができる。固相がマイクロプレートやマイクロチューブなどの容器であれば、未反応の遊離成分を含む液を除去することによりB/F分離ができる。また、固相が磁性粒子の場合は、磁石で磁性粒子を磁気的に拘束した状態でノズルによって未反応の遊離成分を含む液を吸引除去することによりB/F分離ができ、自動化の観点で好ましい。未反応の遊離成分を除去した後、複合体を捕捉した固相をPBSなどの適切な水性媒体で洗浄してもよい。
そして、固相上に形成された複合体を、当該技術において公知の方法で検出することにより、液体試料に含まれる遊離タンパク質マーカーの測定値を取得できる。例えば、検出用抗体として、標識物質で標識した抗体を用いた場合は、その標識物質により生じるシグナルを検出することにより、液体試料におけるマーカーの測定値を取得できる。あるいは、検出用抗体に対する標識二次抗体を用いた場合も、同様にして液体試料におけるマーカーの測定値を取得できる。
また、抗体を用いて遊離タンパク質マーカーを測定する方法の例として、特開平1-254868号公報に記載の免疫複合体転移法を用いることもできる。
本明細書において、「シグナルを検出する」とは、シグナルの有無を定性的に検出すること、シグナル強度を定量すること、及び、シグナルの強度を半定量的に検出することを含む。半定量的な検出とは、シグナルの強度を、「シグナル発生せず」、「弱」、「中」、「強」などのように段階的に示すことをいう。本実施形態では、シグナルの強度を定量的又は半定量的に検出することが好ましい。
標識物質は、特に限定されない。標識物質は、例えば、それ自体がシグナルを発生する物質(以下、「シグナル発生物質」ともいう)であってもよいし、他の物質の反応を触媒してシグナルを発生させる物質であってもよい。シグナル発生物質としては、例えば、蛍光物質、放射性同位元素などが挙げられる。他の物質の反応を触媒して検出可能なシグナルを発生させる物質としては、例えば、酵素が挙げられる。酵素としては、アルカリホスファターゼ、ペルオキシダーゼ、β-ガラクトシダーゼ、ルシフェラーゼなどが挙げられる。蛍光物質としては、フルオレセインイソチオシアネート(FITC)、ローダミン、Alexa Fluor(登録商標)などの蛍光色素、GFPなどの蛍光タンパク質などが挙げられる。放射性同位元素としては、125I、14C、32Pなどが挙げられる。それらの中でも、標識物質として、酵素が好ましく、アルカリホスファターゼ及びペルオキシダーゼが特に好ましい。
シグナルを検出する方法自体は、当該技術において公知である。本実施形態では、上記の標識物質に由来するシグナルの種類に応じた測定方法を適宜選択すればよい。例えば、標識物質が酵素である場合、該酵素に対する基質を反応させることによって発生する光、色などのシグナルを、分光光度計などの公知の装置を用いて測定することにより行うことができる。
酵素の基質は、該酵素の種類に応じて公知の基質から適宜選択できる。例えば、酵素としてアルカリホスファターゼを用いる場合、基質として、CDP-Star(登録商標)(4-クロロ-3-(メトキシスピロ[1, 2-ジオキセタン-3, 2'-(5'-クロロ)トリクシロ[3. 3. 1. 13, 7]デカン]-4-イル)フェニルリン酸2ナトリウム)、CSPD(登録商標)(3-(4-メトキシスピロ[1, 2-ジオキセタン-3, 2-(5'-クロロ)トリシクロ[3. 3. 1. 13, 7]デカン]-4-イル)フェニルリン酸2ナトリウム)などの化学発光基質、5-ブロモ-4-クロロ-3-インドリルリン酸(BCIP)、5-ブロモ-6-クロロ-インドリルリン酸2ナトリウム、p-ニトロフェニルリン酸などの発色基質が挙げられる。また、酵素としてペルオキシダーゼを用いる場合、基質としては、ルミノール及びその誘導体などの化学発光基質、2, 2'-アジノビス(3-エチルベンゾチアゾリン-6-スルホン酸アンモニウム)(ABTS)、1, 2-フェニレンジアミン(OPD)、3, 3',5, 5'-テトラメチルベンジジン(TMB)などの発色基質が挙げられる。
標識物質が放射性同位体である場合は、シグナルとしての放射線を、シンチレーションカウンターなどの公知の装置を用いて測定できる。また、標識物質が蛍光物質である場合は、シグナルとしての蛍光を、蛍光マイクロプレートリーダーなどの公知の装置を用いて測定できる。なお、励起波長及び蛍光波長は、用いた蛍光物質の種類に応じて適宜決定できる。
シグナルの検出結果は、マーカーの測定値として用いることができる。例えば、シグナルの強度を定量的に検出する場合は、シグナル強度の測定値自体又は該測定値から取得される値を、マーカーの測定値として用いることができる。シグナル強度の測定値から取得される値としては、例えば、該測定値から陰性対照試料の測定値又はバックグラウンドの値を差し引いた値、該測定値を検量線に当てはめて取得した値などが挙げられる。陰性対照試料は、適宜選択できるが、例えば、健常人から得た液体試料などが挙げられる。
本実施形態では、磁性粒子に固定された捕捉用抗体と、標識物質で標識された検出用抗体とを用いるサンドイッチELISA法により、液体試料に含まれる遊離タンパク質マーカーを測定することが好ましい。この場合、測定は、HISCLシリーズ(シスメックス株式会社製)などの市販の全自動免疫測定装置を用いて行ってもよい。
次いで、本実施形態の判定方法では、測定結果に基づいて、被検者に対する免疫チェックポイント阻害剤の奏効性を判定する。本実施形態では、測定により取得した遊離タンパク質マーカーの測定値と、各マーカーに対応する所定の閾値とを比較し、比較結果に基づいて判定を行うことが好ましい。具体的には、該測定値が該所定の閾値より低いとき、免疫チェックポイント阻害剤が被検者に奏効すると判定してもよい。また、該測定値が該所定の閾値以上であるとき、免疫チェックポイント阻害剤が被検者に奏効しないと判定してもよい。
sPD-1、sCTLA-4及びsPD-L1のうち、いずれか1つの測定値を取得している場合、下記のように判定を行うことができる。
一実施形態において、sPD-1の測定値を取得している場合、sPD-1の測定値と、sPD-1に対応する閾値とを比較する。sPD-1の測定値が閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sPD-1の測定値が閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
別の実施形態において、sCTLA-4の測定値を取得している場合、sCTLA-4の測定値と、sCTLA-4に対応する閾値とを比較する。sCTLA-4の測定値が閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sCTLA-4の測定値が閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
別の実施形態において、sPD-L1の測定値を取得している場合、sPD-L1の測定値と、sPD-L1に対応する閾値とを比較する。sPD-L1の測定値が閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sPD-L1の測定値が閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
sPD-1、sCTLA-4及びsPD-L1のうち、2つ又は3つの測定値を取得している場合、取得したマーカーの測定値の全てが、各マーカーに対応する所定の閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、取得したマーカーの測定値の少なくとも1つが、該マーカーに対応する所定の閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。具体的には、下記のとおりである。
一実施形態において、sPD-1及びsCTLA-4の測定値を取得している場合、sPD-1の測定値と第1の閾値とを比較し、sCTLA-4の測定値と第2の閾値とを比較する。この例において、第1の閾値は、sPD-1に対応する閾値であり、第2の閾値は、sCTLA-4に対応する閾値である。sPD-1の測定値が第1の閾値より低く、且つsCTLA-4の測定値が第2の閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sPD-1の測定値が第1の閾値以上であるか、又はsCTLA-4の測定値が第2の閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
別の実施形態において、sPD-1及びsPD-L1の測定値を取得している場合、sPD-1の測定値と第1の閾値とを比較し、sPD-L1の測定値と第2の閾値とを比較する。この例において、第1の閾値は、sPD-1に対応する閾値であり、第2の閾値は、sPD-L1に対応する閾値である。sPD-1の測定値が第1の閾値より低く、且つsPD-L1の測定値が第2の閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sPD-1の測定値が第1の閾値以上であるか、又はsPD-L1の測定値が第2の閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
別の実施形態において、sCTLA-4及びsPD-L1の測定値を取得している場合、sCTLA-4の測定値と第1の閾値とを比較し、sPD-L1の測定値と第2の閾値とを比較する。この例において、第1の閾値は、sCTLA-4に対応する閾値であり、第2の閾値は、sPD-L1に対応する閾値である。sCTLA-4の測定値が第1の閾値より低く、且つsPD-L1の測定値が第2の閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sCTLA-4の測定値が第1の閾値以上であるか、又はsPD-L1の測定値が第2の閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
別の実施形態において、sPD-1、sCTLA-4及びsPD-L1の測定値を取得している場合、sPD-1の測定値と第1の閾値とを比較し、sCTLA-4の測定値と第2の閾値とを比較し、sPD-L1の測定値と第3の閾値とを比較する。この例において、第1の閾値は、sPD-1に対応する閾値であり、第2の閾値は、sCTLA-4に対応する閾値であり、第3の閾値は、sPD-L1に対応する閾値である。sPD-1の測定値が第1の閾値より低く、sCTLA-4の測定値が第2の閾値より低く、且つsPD-L1の測定値が第3の閾値より低いとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、sPD-1の測定値が第1の閾値以上であるか、sCTLA-4の測定値が第2の閾値以上であるか、又はsPD-L1の測定値が第3の閾値以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
本実施形態では、取得した遊離タンパク質マーカーの測定値と、各マーカーに対応する閾値との比較結果をスコアにしてもよい。例えば、取得した遊離タンパク質マーカーの測定値が、該マーカーに対応する閾値よりも低いとき、スコアを0とする。また、取得した遊離タンパク質マーカーの測定値が、該マーカーに対応する閾値以上であるとき、スコアを1とする。2つ以上の遊離タンパク質マーカーの測定値を取得している場合は、各マーカーのスコアを合計する。例えば、sPD-1及びsCTLA-4の測定値を取得している場合、sPD-1の測定値及びsCTLA-4の測定値の両方が、それぞれに対応する閾値よりも低いとき、スコアは0となる。sPD-1の測定値及びsCTLA-4の測定値のいずれか一方が、それに対応する閾値以上であるとき、スコアは1となる。sPD-1の測定値及びsCTLA-4の測定値の両方が、それぞれに対応する閾値以上であるとき、スコアは2となる。sPD-1の測定値及びsCTLA-4の測定値のいずれか一方に代えてsPD-L1の測定値を取得している場合も、同様にしてスコアを算出できる。
sPD-1、sCTLA-4及びsPD-L1の測定値を取得している場合、sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値の全てが、それぞれに対応する閾値よりも低いとき、スコアは0となる。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値のいずれか1つが、それに対応する閾値以上であるとき、スコアは1となる。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値のいずれか2つが、それぞれに対応する閾値以上であるとき、スコアは2となる。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値の全てが、それぞれに対応する閾値以上であるとき、スコアは3となる。
本実施形態では、スコアが0のとき、免疫チェックポイント阻害剤は被検者に奏効すると判定してもよい。また、スコアが1以上であるとき、免疫チェックポイント阻害剤は被検者に奏効しないと判定してもよい。
上記の各マーカーに対応する所定の閾値は、適宜設定することができる。所定の閾値は、例えば、がん患者から採取した液体試料における遊離タンパク質マーカーのデータに基づいて設定することができる。例えば、次のようにして所定の閾値を設定してもよい。まず、免疫チェックポイント阻害剤を投与されていない複数のがん患者から液体試料を採取する。液体試料の採取後、がん患者に免疫チェックポイント阻害剤を投与して、経過を観察する。腫瘍の大きさの変化、無増悪生存期間(PFS)、全生存期間(OS)などの公知の評価指標に基づいて、免疫チェックポイント阻害剤の奏効性を確認する。そして、液体試料を、免疫チェックポイント阻害剤が奏効した患者の試料と、免疫チェックポイント阻害剤が奏効しなかった患者の試料とに分類する。それぞれの試料について、遊離タンパク質マーカーを測定して測定値を取得する。そして、取得した測定値から、免疫チェックポイント阻害剤が奏効した患者と、免疫チェックポイント阻害剤が奏効しなかった患者とを区別可能な値を求め、その値を所定の閾値として設定する。所定の閾値の設定に際しては、判定の感度、特異度、陽性的中率及び陰性的中率も考慮することが好ましい。
本実施形態の判定方法は、免疫チェックポイント阻害剤が被検者に奏効するか否かを、免疫チェックポイント阻害剤の投与前に判定することを可能にする。これにより、医師などに、免疫チェックポイント阻害剤の奏効性の判定を補助する情報が提供される。また、本実施形態の判定方法は、免疫チェックポイント阻害剤の効果の予測方法と言い換えることができる。
[2.遊離タンパク質マーカーの測定値の取得方法]
上記の判定方法で得られる遊離タンパク質マーカーの測定値は、被検者に対する免疫チェックポイント阻害剤の奏効性に関する情報ともいえる。よって、本発明の範囲には、遊離タンパク質マーカーの測定値の取得方法(以下、「取得方法」ともいう)も含まれる。
上記の判定方法で得られる遊離タンパク質マーカーの測定値は、被検者に対する免疫チェックポイント阻害剤の奏効性に関する情報ともいえる。よって、本発明の範囲には、遊離タンパク質マーカーの測定値の取得方法(以下、「取得方法」ともいう)も含まれる。
本実施形態の取得方法では、まず、被検者から採取した液体試料中の遊離タンパク質マーカーを測定する。遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1から選択される少なくとも1つである。好ましくは、遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1から選択される少なくとも2つである。より好ましくは、遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1である。被検者、液体試料、遊離タンパク質マーカーの測定手段については、上記の判定方法において述べたことと同じである。好ましい実施形態では、被検者は、肺がん(特に非小細胞肺がん)の患者、食道がん患者及び子宮体がん患者である。また、被検者は、腫瘍除去後のがん患者であってもよい。
本実施形態の取得方法において、被検者は、腫瘍組織の免疫染色により、PD-L1陽性腫瘍細胞の割合が所定の値より低いと判定されたがん患者であってもよい。腫瘍組織の免疫染色、PD-L1陽性腫瘍細胞の割合、所定の値、及び被検者のがんの種類については、上記の判定方法において述べたことと同じである。本実施形態では、被検者は、腫瘍組織の免疫染色の結果に基づいて、有効成分として抗PD-1抗体を含む免疫チェックポイント阻害剤による一次治療の対象から除外される患者であってもよい。
本実施形態の取得方法で得られる遊離タンパク質マーカーの測定値は、各マーカーに対応する所定の閾値との比較により、被検者に対する免疫チェックポイント阻害剤の奏効性を示唆する情報となる。例えば、取得した遊離タンパク質マーカーの測定値がいずれも、各マーカーに対応する所定の閾値より低いとき、取得した遊離タンパク質マーカーの測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。
一実施形態において、取得したsPD-1の測定値が、sPD-1に対応する閾値より低いとき、その測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。別の実施形態において、取得したsCTLA-4の測定値が、sCTLA-4に対応する閾値より低いとき、その測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。別の実施形態において、取得したsPD-L1の測定値が、sPD-L1に対応する閾値より低いとき、その測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。
一実施形態において、取得したsPD-1の測定値が第1の閾値よりも低く、且つ取得したsCTLA-4の測定値が第2の閾値よりも低いとき、これらの測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。別の実施形態において、取得したsPD-1の測定値が第1の閾値よりも低く、且つ取得したsPD-L1の測定値が第2の閾値よりも低いとき、これらの測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。別の実施形態において、取得したsCTLA-4の測定値が第1の閾値よりも低く、且つ取得したsPD-L1の測定値が第2の閾値よりも低いとき、これらの測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。
一実施形態において、取得したsPD-1の測定値が第1の閾値よりも低く、且つ取得したsCTLA-4の測定値が第2の閾値よりも低く、且つ取得したsPD-L1の測定値が第3の閾値より低いとき、これらの測定値は、免疫チェックポイント阻害剤が被検者に奏効することを示唆する。なお、所定の閾値については、上記の判定方法において述べたことと同じである。
本実施形態の取得方法において、免疫チェックポイント阻害剤は、有効成分として、抗PD-1抗体、抗CTLA-4抗体及び抗PD-L1抗体の少なくとも1種を含む製剤であり得る。有効成分として抗PD-1抗体を含む製剤としては、ニボルマブ、ペムブロリズマブなどが公知である。有効成分として抗PD-L1抗体を含む製剤としては、アテゾリズマブ、アベルマブ、デュルバルマブなどが公知である。有効成分として抗CTLA-4抗体を含む製剤としては、イピリムマブなどが公知である。
[3.試薬キット]
本発明の範囲には、上記の判定方法に用いるための試薬キットも含まれる。本実施形態の試薬キットは、sPD-1と特異的に結合可能な物質を含む試薬、sCTLA-4と特異的に結合可能な物質を含む試薬、及び遊離PD-L1と特異的に結合可能な物質を含む試薬から選択される少なくとも1つの試薬を含む。好ましくは、試薬キットは、sPD-1と特異的に結合可能な物質を含む試薬、sCTLA-4と特異的に結合可能な物質を含む試薬、及びsPD-L1と特異的に結合可能な物質を含む試薬から選択される少なくとも2つの試薬を含む。より好ましくは、sPD-1と特異的に結合可能な物質を含む試薬、sCTLA-4と特異的に結合可能な物質を含む試薬、及びsPD-L1と特異的に結合可能な物質を含む試薬を含む。各遊離タンパク質マーカーと特異的に結合可能な物質としては、例えば、抗体、アプタマーなどが挙げられる。それらの中でも抗体が特に好ましい。
本発明の範囲には、上記の判定方法に用いるための試薬キットも含まれる。本実施形態の試薬キットは、sPD-1と特異的に結合可能な物質を含む試薬、sCTLA-4と特異的に結合可能な物質を含む試薬、及び遊離PD-L1と特異的に結合可能な物質を含む試薬から選択される少なくとも1つの試薬を含む。好ましくは、試薬キットは、sPD-1と特異的に結合可能な物質を含む試薬、sCTLA-4と特異的に結合可能な物質を含む試薬、及びsPD-L1と特異的に結合可能な物質を含む試薬から選択される少なくとも2つの試薬を含む。より好ましくは、sPD-1と特異的に結合可能な物質を含む試薬、sCTLA-4と特異的に結合可能な物質を含む試薬、及びsPD-L1と特異的に結合可能な物質を含む試薬を含む。各遊離タンパク質マーカーと特異的に結合可能な物質としては、例えば、抗体、アプタマーなどが挙げられる。それらの中でも抗体が特に好ましい。
本実施形態の試薬キットの一例を、図1Aに示す。図1Aにおいて、11は、試薬キットを示し、12は、遊離PD-1と特異的に結合可能な物質を含む試薬を収容した第1容器を示し、13は、遊離CTLA-4と特異的に結合可能な物質を含む試薬を収容した第2容器を示し、14は、梱包箱を示し、15は、添付文書を示す。図示しないが、この例の試薬キットは、遊離PD-L1と特異的に結合可能な物質を含む試薬を収容した第3容器を含んでもよい。
好ましい実施形態では、本実施形態の試薬キットは、各遊離タンパク質マーカーの捕捉用抗体及び検出用抗体を含む。検出用抗体は、標識物質で標識されていてもよい。捕捉用抗体、検出用抗体及び標識物質については、上記の本実施形態の判定方法において述べたことと同じである。また、試薬キットは、固相と、基質とを含んでもよい。固相及び基質については、上記の本実施形態の判定方法において述べたことと同じである。
さらなる実施形態の試薬キットの一例を、図1Bに示す。図1Bにおいて、21は、試薬キットを示し、22は、遊離PD-1の捕捉用抗体を含む試薬を収容した第1容器を示し、23は、遊離PD-1の検出用標識抗体を含む試薬を収容した第2容器を示し、24は、遊離CTLA-4の捕捉用抗体を含む試薬を収容した第3容器を示し、25は、遊離CTLA-4の検出用標識抗体を含む試薬を収容した第4容器を示し、26は、添付文書を示し、27は、梱包箱を示す。図示しないが、この例の試薬キットは、遊離PD-L1の捕捉用抗体を含む試薬を収容した第5容器、及び遊離PD-L1の検出用標識抗体を含む試薬を収容した第6容器を含んでもよい。
上記のいずれの試薬キットにおいても、キャリブレータを含むことが好ましい。キャリブレータの一例としては、遊離PD-1の定量のためのキャリブレータ(PD-1用キャリブレータ)、遊離CTLA-4の定量のためのキャリブレータ(CTLA-4用キャリブレータ)及び遊離PD-L1の定量のためのキャリブレータ(PD-L1用キャリブレータ)が挙げられる。PD-1用キャリブレータは、例えば、PD-1を含まない緩衝液(ネガティブコントロール)と、PD-1を既知濃度で含む緩衝液とを備えていてもよい。CTLA-4用キャリブレータは、例えば、CTLA-4を含まない緩衝液(ネガティブコントロール)と、CTLA-4を既知濃度で含む緩衝液とを備えていてもよい。PD-L1用キャリブレータは、例えば、PD-L1を含まない緩衝液(ネガティブコントロール)と、PD-L1を既知濃度で含む緩衝液とを備えていてもよい。
別のキャリブレータの例は、PD-1、CTLA-4及びPD-L1のいずれも含まない緩衝液(ネガティブコントロール)と、PD-1を既知濃度で含む緩衝液と、CTLA-4を既知濃度で含む緩衝液と、PD-L1を既知濃度で含む緩衝液とを備える。別のキャリブレータの例は、PD-1、CTLA-4及びPD-L1のいずれも含まない緩衝液(ネガティブコントロール)と、PD-1、CTLA-4及びPD-L1から選択される2つをそれぞれ既知濃度で含む緩衝液とを備える。さらに別のキャリブレータの例は、PD-1、CTLA-4及びPD-L1のいずれも含まない緩衝液(ネガティブコントロール)と、PD-1、CTLA-4及びPD-L1をそれぞれ既知濃度で含む緩衝液とを備える。
さらなる実施形態の試薬キットの一例を、図1Cに示す。図1Cにおいて、31は、試薬キットを示し、32は、遊離PD-1の捕捉用抗体を含む試薬を収容した第1容器を示し、33は、遊離PD-1の検出用標識抗体を含む試薬を収容した第2容器を示し、34は、遊離CTLA-4の捕捉用抗体を含む試薬を収容した第3容器を示し、35は、遊離CTLA-4の検出用標識抗体を含む試薬を収容した第4容器を示し、36は、PD-1、CTLA-4及びPD-L1のいずれも含まない緩衝液を収容した第5容器を示し、37は、PD-1及びCTLA-4をそれぞれ所定の濃度で含有する緩衝液を収容した第6容器を示し、38は、梱包箱を示し、39は、添付文書を示す。PD-1、CTLA-4及びPD-L1のいずれも含まない緩衝液と、PD-1及びCTLA-4をそれぞれ所定の濃度で含有する緩衝液は、PD-1及びCTLA-4の定量のためのキャリブレータとして用いることができる。図示しないが、この例の試薬キットは、遊離PD-L1の捕捉用抗体を含む試薬を収容した第7容器、遊離PD-L1の検出用標識抗体を含む試薬を収容した第8容器、及びPD-L1を所定の濃度で含有する緩衝液(PD-L1定量用キャリブレータ)を収容した第9容器を含んでもよい。
[4.装置及びコンピュータプログラム]
本発明の範囲には、上記の本実施形態の判定方法を実施するための装置も含まれる。そのような装置は、免疫チェックポイント阻害剤の奏効性の判定装置(以下、単に「判定装置」ともいう)である。また、本発明の範囲には、上記の本実施形態の判定方法をコンピュータに実行させるためのコンピュータプログラムも含まれる。そのようなコンピュータプログラムは、免疫チェックポイント阻害剤の奏効性の判定のためのコンピュータプログラムである。さらに、本発明の範囲には、上記の本実施形態の取得方法を実施するための装置も含まれる。そのような装置は、遊離タンパク質マーカーの測定値の取得装置である。
本発明の範囲には、上記の本実施形態の判定方法を実施するための装置も含まれる。そのような装置は、免疫チェックポイント阻害剤の奏効性の判定装置(以下、単に「判定装置」ともいう)である。また、本発明の範囲には、上記の本実施形態の判定方法をコンピュータに実行させるためのコンピュータプログラムも含まれる。そのようなコンピュータプログラムは、免疫チェックポイント阻害剤の奏効性の判定のためのコンピュータプログラムである。さらに、本発明の範囲には、上記の本実施形態の取得方法を実施するための装置も含まれる。そのような装置は、遊離タンパク質マーカーの測定値の取得装置である。
以下に、上記の本実施形態の方法を実施するための装置の一例を、図面を参照して説明する。しかし、本実施形態は、この例に示される形態のみに限定されない。図2は、判定装置の概略図である。図2に示された判定装置10は、免疫測定装置20と、該免疫測定装置20と接続されたコンピュータシステム30とを含む。遊離タンパク質マーカーの測定値の取得装置のハードウェア構成も、判定装置10と同様である。
本実施形態において、免疫測定装置の種類は特に限定されず、遊離タンパク質マーカーの測定方法に応じて適宜選択できる。図2に示される例では、免疫測定装置20は、捕捉用抗体を固定した磁性粒子及び酵素標識された検出用抗体を用いるサンドイッチELISA法により生じる化学発光シグナルを検出可能な市販の自動免疫測定装置である。免疫測定装置20は、用いた標識物質に基づくシグナルの検出が可能であれば特に限定されず、標識物質の種類に応じて適宜選択できる。
捕捉用抗体を固定した磁性粒子を含む試薬、酵素標識された検出用抗体を含む試薬及び被検者から採取した液体試料を免疫測定装置20にセットすると、該免疫測定装置20は、各試薬を用いて抗原抗体反応を実行し、遊離タンパク質マーカーと特異的に結合した酵素標識抗体に基づく光学的情報として化学発光シグナルを取得し、得られた光学的情報をコンピュータシステム30に送信する。
コンピュータシステム30は、コンピュータ本体300と、入力部301と、検体情報や判定結果などを表示する表示部302とを含む。コンピュータシステム30は、免疫測定装置20から光学的情報を受信する。そして、コンピュータシステム30のプロセッサは、光学的情報に基づいて、ハードディスク313にインストールされた、免疫チェックポイント阻害剤の奏効性の判定のためのコンピュータプログラムを実行する。なお、コンピュータシステム30は、図2に示されるように、免疫測定装置20とは別個の機器であってもよいし、免疫測定装置20を内包する機器であってもよい。後者の場合、コンピュータシステム30は、それ自体で判定装置10となってもよい。市販の自動免疫測定装置に、免疫チェックポイント阻害剤の奏効性の判定のためのコンピュータプログラムを搭載してもよい。
図3を参照して、コンピュータ本体300は、CPU(Central Processing Unit)310と、ROM(Read Only Memory)311と、RAM(Random Access Memory)312と、ハードディスク313と、入出力インターフェイス314と、読取装置315と、通信インターフェイス316と、画像出力インターフェイス317とを備えている。CPU310、ROM311、RAM312、ハードディスク313、入出力インターフェイス314、読取装置315、通信インターフェイス316及び画像出力インターフェイス317は、バス318によってデータ通信可能に接続されている。また、免疫測定装置20は、通信インターフェイス316により、コンピュータシステム30と通信可能に接続されている。
CPU310は、ROM311又はハードディスク313に記憶されているプログラム及びRAM312にロードされたプログラムを実行することが可能である。CPU310は、遊離タンパク質マーカーの測定値を算出し、ROM311又はハードディスク313に記憶されている各マーカーに対応する所定の閾値を読み出し、免疫チェックポイント阻害剤が被検者に奏効するか否かを判定する。CPU310は、判定結果を出力して表示部302に表示させる。
ROM311は、マスクROM、PROM、EPROM、EEPROMなどによって構成されている。ROM311には、前述のようにCPU310によって実行されるコンピュータプログラム及び当該コンピュータプログラムの実行に用いるデータが記録されている。ROM311には、各遊離タンパク質マーカーに対応する所定の閾値など、後述の判定フローに用いられるデータが記録されていてもよい。
RAM312は、SRAM、DRAMなどによって構成されている。RAM312は、ROM311及びハードディスク313に記録されているプログラムの読み出しに用いられる。RAM312はまた、これらのプログラムを実行するときに、CPU310の作業領域として利用される。
ハードディスク313は、CPU310に実行させるためのオペレーティングシステム、アプリケーションプログラム(上記のがんの判定のためのコンピュータプログラム)などのコンピュータプログラム及び当該コンピュータプログラムの実行に用いるデータがインストールされている。ハードディスク313には、各遊離タンパク質マーカーに対応する所定の閾値など、後述の判定フローに用いられるデータが記録されていてもよい。
読取装置315は、フレキシブルディスクドライブ、CD-ROMドライブ、DVD-ROMドライブなどによって構成されている。読取装置315は、可搬型記録媒体40に記録されたプログラム又はデータを読み取ることができる。
入出力インターフェイス314は、例えば、USB、IEEE1394、RS-232Cなどのシリアルインターフェイスと、SCSI、IDE、IEEE1284などのパラレルインターフェイスと、D/A変換器、A/D変換器などからなるアナログインターフェイスとから構成されている。入出力インターフェイス314には、キーボード、マウスなどの入力部301が接続されている。操作者は、該入力部301により、コンピュータ本体300に各種の指令を入力することが可能である。
通信インターフェイス316は、例えば、Ethernet(登録商標)インターフェイスなどである。コンピュータ本体300は、通信インターフェイス316により、プリンタなどへの印刷データの送信も可能である。
画像出力インターフェイス317は、LCD、CRTなどで構成される表示部302に接続されている。これにより、表示部302は、CPU310から与えられた画像データに応じた映像信号を出力できる。表示部302は、入力された映像信号にしたがって画像(画面)を表示する。
図4Aを参照して、判定装置10により実行される、免疫チェックポイント阻害剤の奏効性の判定フローについて説明する。ここでは、捕捉用抗体を固定した磁性粒子及び酵素標識された検出用抗体を用いるサンドイッチELISA法により生じる化学発光シグナルから、sPD-1の測定値を取得し、取得した測定値を用いて判定を行なう場合を例として説明する。この例において、第1の閾値は、sPD-1に対応する閾値である。しかし、本実施形態は、この例のみに限定されない。sPD-1の測定値に代えて、sCTLA-4の測定値又はsPD-L1の測定値を取得してもよい。
ステップS101において、CPU310は、免疫測定装置20から光学的情報(化学発光シグナル)を取得し、取得した光学的情報からsPD-1の測定値を算出してハードディスク313に記憶する。ステップS102において、CPU310は、算出したsPD-1の測定値と、ハードディスク313に記憶された第1の閾値とを比較する。sPD-1の測定値が第1の閾値より低いとき、処理はステップS103に進行する。ステップS103において、CPU310は、免疫チェックポイント阻害剤が被検者に奏効するとの判定結果をハードディスク313に記憶する。
一方、ステップS102において、sPD-1の測定値が第1の閾値以上であるとき、処理はステップS104に進行する。ステップS104において、CPU310は、免疫チェックポイント阻害剤が被検者に奏効しないとの判定結果をハードディスク313に記憶する。ステップS105において、CPU310は、判定結果を出力し、表示部302に表示させたり、プリンタに印刷させたりする。これにより、免疫チェックポイント阻害剤の奏効性の判定を補助する情報を医師などに提供することができる。
図4Bを参照して、判定装置10により実行される、免疫チェックポイント阻害剤の奏効性の判定フローについて説明する。ここでは、捕捉用抗体を固定した磁性粒子及び酵素標識された検出用抗体を用いるサンドイッチELISA法により生じる化学発光シグナルから、sPD-1及びsCTLA-4の測定値を取得し、取得した測定値を用いて判定を行なう場合を例として説明する。この例において、第1の閾値は、sPD-1に対応する閾値であり、第2の閾値は、sCTLA-4に対応する閾値である。しかし、本実施形態は、この例のみに限定されない。sPD-1及びsCTLA-4の測定値のいずれか一方に代えて、sPD-L1の測定値を取得してもよい。
ステップS201において、CPU310は、免疫測定装置20から光学的情報(化学発光シグナル)を取得し、取得した光学的情報からsPD-1及びsCTLA-4の測定値を算出してハードディスク313に記憶する。ステップS202において、CPU310は、算出したsPD-1の測定値と、ハードディスク313に記憶された第1の閾値とを比較する。sPD-1の測定値が第1の閾値より低いとき、処理はステップS203に進行する。ステップS203において、CPU310は、算出したsCTLA-4の測定値と、ハードディスク313に記憶された第2の閾値とを比較する。sCTLA-4の測定値が第2の閾値より低いとき、処理はステップS204に進行する。ステップS204において、CPU310は、免疫チェックポイント阻害剤が被検者に奏効するとの判定結果をハードディスク313に記憶する。
一方、ステップS202において、sPD-1の測定値が第1の閾値以上であるとき、処理はステップS205に進行する。ステップS203において、sCTLA-4の測定値が第2の閾値以上であるとき、処理はステップS205に進行する。ステップS205において、CPU310は、免疫チェックポイント阻害剤が被検者に奏効しないとの判定結果をハードディスク313に記憶する。ステップS206において、CPU310は、判定結果を出力し、表示部302に表示させたり、プリンタに印刷させたりする。これにより、免疫チェックポイント阻害剤の奏効性の判定を補助する情報を医師などに提供することができる。なお、この例において、ステップS202及びステップS203の処理は順序を入れ替えることができる。
図4Cを参照して、判定装置10により実行される、免疫チェックポイント阻害剤の奏効性の判定フローについて説明する。ここでは、sPD-1及びsCTLA-4の測定値に加えて、さらにsPD-L1の測定値を取得し、取得した測定値を用いて判定を行なう場合を例として説明する。この例において、第1の閾値は、sPD-1に対応する閾値であり、第2の閾値は、sCTLA-4に対応する閾値であり、第3の閾値は、sPD-L1に対応する閾値である。しかし、本実施形態は、この例のみに限定されない。
ステップS301において、CPU310は、免疫測定装置20から光学的情報(化学発光シグナル)を取得し、取得した光学的情報からsPD-1、sCTLA-4及びsPD-L1の測定値を算出してハードディスク313に記憶する。ステップS302において、CPU310は、算出したsPD-1の測定値と、ハードディスク313に記憶された第1の閾値とを比較する。sPD-1の測定値が第1の閾値より低いとき、処理はステップS203に進行する。ステップS303において、CPU310は、算出したsCTLA-4の測定値と、ハードディスク313に記憶された第2の閾値とを比較する。sCTLA-4の測定値が第2の閾値より低いとき、処理はステップS304に進行する。ステップS304において、CPU310は、算出したsPD-L1の測定値と、ハードディスク313に記憶された第3の閾値とを比較する。sPD-L1の測定値が第3の閾値より低いとき、処理はステップS305に進行する。ステップS305において、CPU310は、免疫チェックポイント阻害剤が被検者に奏効するとの判定結果をハードディスク313に記憶する。
一方、ステップS302において、sPD-1の測定値が第1の閾値以上であるとき、処理はステップS306に進行する。ステップS303において、sCTLA-4の測定値が第2の閾値以上であるとき、処理はステップS306に進行する。ステップS304において、sPD-L1の測定値が第3の閾値以上であるとき、処理はステップS306に進行する。ステップS306において、CPU310は、免疫チェックポイント阻害剤が被検者に奏効しないとの判定結果をハードディスク313に記憶する。ステップS307において、CPU310は、判定結果を出力し、表示部302に表示させたり、プリンタに印刷させたりする。なお、この例において、ステップS302、ステップS303及びステップS304の処理は順序を入れ替えることができる。
図5を参照して、遊離タンパク質マーカーの測定値の取得装置10により実行される処理手順について説明する。ここでは、捕捉用抗体を固定した磁性粒子及び酵素標識された検出用抗体を用いるサンドイッチELISA法により生じる化学発光シグナルから、sPD-1の測定値を取得し、取得した測定値を用いて判定を行なう場合を例として説明する。しかし、本実施形態は、この例のみに限定されない。sPD-1の測定値に代えて、sCTLA-4の測定値又はsPD-L1の測定値を取得してもよい。さらなる実施形態では、sPD-1、sCTLA-4及びsPD-L1から選択される2つの遊離タンパク質マーカーの測定値を取得してもよい。あるいは、sPD-1、sCTLA-4及びsPD-L1の測定値を取得してもよい。
ステップS401において、CPU310は、免疫測定装置20から光学的情報(化学発光シグナル)を取得し、取得した光学的情報からsPD-1の測定値を算出してハードディスク313に記憶する。ステップS402において、CPU310は、取得したsPD-1の測定値を出力し、表示部302に表示させたり、プリンタに印刷させたりする。なお、この例において、取得した遊離タンパク質マーカーの測定値と共に、該マーカーに対応する所定の閾値を出力してもよい。
取得装置により得られた遊離タンパク質マーカーの測定値は、各マーカーに対応する所定の閾値との比較により、被検者に対する免疫チェックポイント阻害剤の奏効性を示唆する情報となる。具体的には、本実施形態の取得方法について述べたことと同様である。
本発明において、「免疫チェックポイント阻害剤が被検者に奏効する」とは、「免疫チェックポイント阻害剤が被検者に奏効する可能性が高い」ことを意味し、また「被検者は免疫チェックポイント阻害剤の投与対象として選択される」と言い換えることができる。また、「免疫チェックポイント阻害剤が被検者に奏効しない」は、「免疫チェックポイント阻害剤が被検者に奏効する可能性が低い」ことを意味し、また「被検者は免疫チェックポイント阻害剤の投与対象として選択されない」と言い換えることができる。
[4.がんの治療方法及び医薬組成物]
本発明の一実施形態は、がんの治療方法に関する。本実施形態のがんの治療方法は、がん患者から採取した液体試料中の遊離タンパク質マーカーの測定結果に基づいて、がん患者に免疫チェックポイント阻害剤を投与する工程を含む。この治療方法において、遊離タンパク質マーカーは、遊離PD-1、遊離CTLA-4及び遊離PD-L1から選択される少なくとも1つである。好ましくは、遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1から選択される少なくとも2つである。より好ましくは、遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1である。免疫チェックポイント阻害剤は、有効成分として、抗PD-1抗体、抗CTLA-4抗体及び抗PD-L1抗体の少なくとも1種を含む製剤であり得る。好ましくは、有効成分として抗PD-1抗体を含む製剤であり、一実施形態においてニボルマブであり、またはペムブロリズマブである。
本発明の一実施形態は、がんの治療方法に関する。本実施形態のがんの治療方法は、がん患者から採取した液体試料中の遊離タンパク質マーカーの測定結果に基づいて、がん患者に免疫チェックポイント阻害剤を投与する工程を含む。この治療方法において、遊離タンパク質マーカーは、遊離PD-1、遊離CTLA-4及び遊離PD-L1から選択される少なくとも1つである。好ましくは、遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1から選択される少なくとも2つである。より好ましくは、遊離タンパク質マーカーは、sPD-1、sCTLA-4及びsPD-L1である。免疫チェックポイント阻害剤は、有効成分として、抗PD-1抗体、抗CTLA-4抗体及び抗PD-L1抗体の少なくとも1種を含む製剤であり得る。好ましくは、有効成分として抗PD-1抗体を含む製剤であり、一実施形態においてニボルマブであり、またはペムブロリズマブである。
本実施形態の治療方法において、遊離タンパク質マーカーの測定結果から免疫チェックポイント阻害剤が奏効すると判定された患者に対して、上記の投与工程を実施し得る。この方法における免疫チェックポイント阻害剤の奏効性判定については、上記の判定方法において述べたことと同様である。また、がんの種類、液体試料、遊離タンパク質マーカーの測定手段、判定等については、上記の判定方法において述べたことと同じである。
本実施形態の治療方法は、肺がんの患者、食道がんの患者及び子宮体がん患者に適している。投与工程では、治療上の有効量の免疫チェックポイント阻害剤をがん患者に投与することが好ましい。治療上の有効量は、がんの種類、がんの進行度、免疫チェックポイント阻害剤の種類、治療ガイドラインなどに応じて適宜決定される。
本発明の一実施形態は、上記の判定方法により免疫チェックポイント阻害剤が奏効すると判定されたがん患者に投与されることを特徴とする、免疫チェックポイント阻害剤を含有するがん治療用医薬組成物に関する。本実施形態では、がん治療用医薬組成物は、免疫チェックポイント阻害剤そのものであってもよい。免疫チェックポイント阻害剤の詳細は上述のとおりである。がん治療用医薬組成物は、医薬的に許容される成分を含んでいてもよい。そのような成分は、当該技術分野において公知の医薬品添加物から適宜選択できる。がん治療用医薬組成物は、免疫チェックポイント阻害剤とは異なるがん治療用薬剤をさらに含んでもよい。そのようながん治療用薬剤としては、例えば化学療法剤、分子標的薬などが挙げられる。がん治療用医薬組成物の形態は特に限定されず、結晶、粉末などの固体であってもよいし、溶液、乳化液、懸濁液などの液体であってもよい。
以下に、本発明を実施例により詳細に説明するが、本発明はこれらの実施例に限定されるものではない。
実施例1
非小細胞肺がん患者について、免疫チェックポイント阻害剤の投与前の血液試料中の遊離タンパク質マーカーの濃度と、免疫チェックポイント阻害剤の投与後の治療効果との関連を検討した。
非小細胞肺がん患者について、免疫チェックポイント阻害剤の投与前の血液試料中の遊離タンパク質マーカーの濃度と、免疫チェックポイント阻害剤の投与後の治療効果との関連を検討した。
1.被検者
免疫チェックポイント阻害剤を投与されていない非小細胞肺がんの患者(50例)を被検者とした。実施例1では、全ての患者(50例)に、免疫チェックポイント阻害剤であるニボルマブ(小野薬品工業株式会社)を投与し、無増悪生存期間(PFS)を評価指標として経過を観察した。
免疫チェックポイント阻害剤を投与されていない非小細胞肺がんの患者(50例)を被検者とした。実施例1では、全ての患者(50例)に、免疫チェックポイント阻害剤であるニボルマブ(小野薬品工業株式会社)を投与し、無増悪生存期間(PFS)を評価指標として経過を観察した。
2.液体試料
免疫チェックポイント阻害剤の投与前に、上記の患者(50例)から血液を採取した。得られた血液を常法により分離して、血漿を得た。得られた血漿(50検体)を、液体試料として用いた。
免疫チェックポイント阻害剤の投与前に、上記の患者(50例)から血液を採取した。得られた血液を常法により分離して、血漿を得た。得られた血漿(50検体)を、液体試料として用いた。
3.腫瘍組織のPD-L1免疫染色
免疫チェックポイント阻害剤の投与前に、上記の患者(50例)から腫瘍組織を手術又は生検により採取して、常法によりFFPE組織標本を作製した。得られたFFPE組織標本を薄切し、得られた薄切切片に、常法により脱パラフィン処理、親水化処理及び抗原賦活化処理を行った。処理後の薄切切片に、抗PD-L1抗体(28-8抗体)を用いて免疫組織染色を行って、組織標本を得た。得られた組織標本を光学顕微鏡で観察し、細胞膜が部分的又は完全に染色されている腫瘍細胞を「PD-L1陽性腫瘍細胞」として計数した。上記の式により、PD-L1陽性腫瘍細胞の割合としてTPSを算出した。その結果、50例のうち13例では、TPSが50%以上であった。残りの37例では、TPSが50%未満であった。以下、TPSが50%未満であった患者を「PD-L1陰性症例」とも呼ぶ。
免疫チェックポイント阻害剤の投与前に、上記の患者(50例)から腫瘍組織を手術又は生検により採取して、常法によりFFPE組織標本を作製した。得られたFFPE組織標本を薄切し、得られた薄切切片に、常法により脱パラフィン処理、親水化処理及び抗原賦活化処理を行った。処理後の薄切切片に、抗PD-L1抗体(28-8抗体)を用いて免疫組織染色を行って、組織標本を得た。得られた組織標本を光学顕微鏡で観察し、細胞膜が部分的又は完全に染色されている腫瘍細胞を「PD-L1陽性腫瘍細胞」として計数した。上記の式により、PD-L1陽性腫瘍細胞の割合としてTPSを算出した。その結果、50例のうち13例では、TPSが50%以上であった。残りの37例では、TPSが50%未満であった。以下、TPSが50%未満であった患者を「PD-L1陰性症例」とも呼ぶ。
4.遊離タンパク質マーカーの測定
(4.1) 試薬の調製
(4.1.1) 第1試薬(ビオチン標識抗体溶液)
・PD-1捕捉用第1試薬
捕捉用抗体として、抗PD-1抗体(クローンNo.MIH4)を用いた。この抗体を、Biotin Labeling Kit-SH (Catalog No. LK10、同仁化学社製)を用いてビオチンで標識した。具体的な操作は、該キットに添付のマニュアルに従って行った。得られたビオチン標識抗PD-1抗体を100 mM HEPES(pH 7.5)に添加して、PD-1捕捉用第1試薬(抗体濃度5μg/ml)を調製した。
(4.1) 試薬の調製
(4.1.1) 第1試薬(ビオチン標識抗体溶液)
・PD-1捕捉用第1試薬
捕捉用抗体として、抗PD-1抗体(クローンNo.MIH4)を用いた。この抗体を、Biotin Labeling Kit-SH (Catalog No. LK10、同仁化学社製)を用いてビオチンで標識した。具体的な操作は、該キットに添付のマニュアルに従って行った。得られたビオチン標識抗PD-1抗体を100 mM HEPES(pH 7.5)に添加して、PD-1捕捉用第1試薬(抗体濃度5μg/ml)を調製した。
・CTLA-4捕捉用第1試薬
捕捉用抗体として、抗CTLA-4抗体(クローンNo.BNI3)を用いた。この抗体を、上記と同様にしてビオチンで標識した。得られたビオチン標識抗CTLA-4抗体を100 mM MES(pH 6.5)に添加して、CTLA-4捕捉用第1試薬(抗体濃度5μg/ml)を調製した。
捕捉用抗体として、抗CTLA-4抗体(クローンNo.BNI3)を用いた。この抗体を、上記と同様にしてビオチンで標識した。得られたビオチン標識抗CTLA-4抗体を100 mM MES(pH 6.5)に添加して、CTLA-4捕捉用第1試薬(抗体濃度5μg/ml)を調製した。
・PD-L1捕捉用第1試薬
捕捉用抗体として、抗PD-L1抗体(クローンNo.27A2)を用いた。この抗体を、上記と同様にしてビオチンで標識した。得られたビオチン標識抗PD-L1抗体を100 mM MES(pH 6.5)に添加して、PD-L1捕捉用第1試薬(抗体濃度5μg/ml)を調製した。
捕捉用抗体として、抗PD-L1抗体(クローンNo.27A2)を用いた。この抗体を、上記と同様にしてビオチンで標識した。得られたビオチン標識抗PD-L1抗体を100 mM MES(pH 6.5)に添加して、PD-L1捕捉用第1試薬(抗体濃度5μg/ml)を調製した。
(4.1.2) 第2試薬(ストレプトアビジン結合粒子含有液)
表面にストレプトアビジンが固定された磁性粒子(平均粒子径2μm。磁性粒子1gあたりのストレプトアビジンの量は2.9~3.5 mg。以下、「STA結合磁性粒子」ともいう)を、10 mM HEPES緩衝液(pH 7.5)で3回洗浄した。洗浄後のSTA結合磁性粒子を、ストレプトアビジン濃度が18~22μg/ml(STA結合磁性粒子の濃度が0.48~0.52 mg/ml)となるように、10 mM HEPES(pH 7.5)に添加し、STA結合粒子含有液を得た。
表面にストレプトアビジンが固定された磁性粒子(平均粒子径2μm。磁性粒子1gあたりのストレプトアビジンの量は2.9~3.5 mg。以下、「STA結合磁性粒子」ともいう)を、10 mM HEPES緩衝液(pH 7.5)で3回洗浄した。洗浄後のSTA結合磁性粒子を、ストレプトアビジン濃度が18~22μg/ml(STA結合磁性粒子の濃度が0.48~0.52 mg/ml)となるように、10 mM HEPES(pH 7.5)に添加し、STA結合粒子含有液を得た。
(4.1.3) 第3試薬(アルカリホスファターゼ標識抗体溶液)
・PD-1検出用第3試薬
検出用抗体として、抗PD-1抗体(クローンNo. PD1.3.1.3)を用いた。この抗体を、Alkaline Phosphatase Labeling Kit-SH (Catalog No. LK13、同仁化学社製)を用いてアルカリホスファターゼで標識した。具体的な操作は、該キットに添付のマニュアルに従って行った。得られたアルカリホスファターゼ標識抗PD-1抗体をゲルろ過にて精製した。このアルカリホスファターゼ標識抗PD-1抗体を、100 mM HEPES(pH 7.5)に75倍希釈となるように添加して、PD-1検出用第3試薬を調製した。
・PD-1検出用第3試薬
検出用抗体として、抗PD-1抗体(クローンNo. PD1.3.1.3)を用いた。この抗体を、Alkaline Phosphatase Labeling Kit-SH (Catalog No. LK13、同仁化学社製)を用いてアルカリホスファターゼで標識した。具体的な操作は、該キットに添付のマニュアルに従って行った。得られたアルカリホスファターゼ標識抗PD-1抗体をゲルろ過にて精製した。このアルカリホスファターゼ標識抗PD-1抗体を、100 mM HEPES(pH 7.5)に75倍希釈となるように添加して、PD-1検出用第3試薬を調製した。
・CTLA-4検出用第3試薬
検出用抗体として、抗CTLA-4抗体(クローンNo.14D3)を用いた。この抗体を、上記と同様にしてアルカリホスファターゼで標識し、精製した。得られたアルカリホスファターゼ標識抗CTLA-4抗体を、100 mM MES(pH 6.5)に75倍希釈となるように添加して、CTLA-4検出用第3試薬を調製した。
検出用抗体として、抗CTLA-4抗体(クローンNo.14D3)を用いた。この抗体を、上記と同様にしてアルカリホスファターゼで標識し、精製した。得られたアルカリホスファターゼ標識抗CTLA-4抗体を、100 mM MES(pH 6.5)に75倍希釈となるように添加して、CTLA-4検出用第3試薬を調製した。
・PD-L1検出用第3試薬
検出用抗体として、抗PD-L1抗体(クローンNo. 9L814)を用いた。この抗体を、上記と同様にしてアルカリホスファターゼで標識し、精製した。得られたアルカリホスファターゼ標識抗PD-L1抗体を、100 mM MES(pH 6.5)に75倍希釈となるように添加して、PD-L1検出用第3試薬を調製した。
検出用抗体として、抗PD-L1抗体(クローンNo. 9L814)を用いた。この抗体を、上記と同様にしてアルカリホスファターゼで標識し、精製した。得られたアルカリホスファターゼ標識抗PD-L1抗体を、100 mM MES(pH 6.5)に75倍希釈となるように添加して、PD-L1検出用第3試薬を調製した。
(4.1.4) 第4試薬(測定用緩衝液)
HISCL R4試薬(シスメックス株式会社製)を第4試薬として使用した。
HISCL R4試薬(シスメックス株式会社製)を第4試薬として使用した。
(4.1.5) 第5試薬(基質溶液)
アルカリホスファターゼの化学発光基質としてCDP-Star(登録商標)(アプライドバイオシステムズ社)を含むHISCL R5試薬(シスメックス株式会社製)を、第5試薬として使用した。
アルカリホスファターゼの化学発光基質としてCDP-Star(登録商標)(アプライドバイオシステムズ社)を含むHISCL R5試薬(シスメックス株式会社製)を、第5試薬として使用した。
(4.2) 測定
各遊離タンパク質マーカーの測定は、上記の第1~第5試薬を用いて全自動免疫測定装置HISCL-800(シスメックス株式会社製)により行った。なお、この測定は、磁性粒子上でのサンドイッチELISAをベースとしている。具体的な操作は、次のとおりである。第1試薬(50μL)に血漿(20μL)を加えて混合した後、第2試薬(30μL)を加えて混合した。得られた混合液中の磁性粒子を集磁して上清を除き、HISCL洗浄液(300μL)を加えて磁性粒子を洗浄した。上清を除き、磁性粒子に第3試薬を添加して混合した。各第3試薬の添加量は、次のとおりであった。PD-1検出用第3試薬が100μL、CTLA-4検出用第3試薬が100μL、PD-L1検出用第3試薬が80μL。得られた混合液中の磁性粒子を集磁して上清を除き、HISCL洗浄液(300μL)を加えて磁性粒子を洗浄した。上清を除き、磁性粒子に第4試薬(50μL)及び第5試薬(100μL)を添加し、よく混合して、化学発光強度を測定した。反応時間は全工程を通して17分間であった。得られた化学発光強度を検量線に当てはめて、各遊離タンパク質マーカーの濃度を算出した。
各遊離タンパク質マーカーの測定は、上記の第1~第5試薬を用いて全自動免疫測定装置HISCL-800(シスメックス株式会社製)により行った。なお、この測定は、磁性粒子上でのサンドイッチELISAをベースとしている。具体的な操作は、次のとおりである。第1試薬(50μL)に血漿(20μL)を加えて混合した後、第2試薬(30μL)を加えて混合した。得られた混合液中の磁性粒子を集磁して上清を除き、HISCL洗浄液(300μL)を加えて磁性粒子を洗浄した。上清を除き、磁性粒子に第3試薬を添加して混合した。各第3試薬の添加量は、次のとおりであった。PD-1検出用第3試薬が100μL、CTLA-4検出用第3試薬が100μL、PD-L1検出用第3試薬が80μL。得られた混合液中の磁性粒子を集磁して上清を除き、HISCL洗浄液(300μL)を加えて磁性粒子を洗浄した。上清を除き、磁性粒子に第4試薬(50μL)及び第5試薬(100μL)を添加し、よく混合して、化学発光強度を測定した。反応時間は全工程を通して17分間であった。得られた化学発光強度を検量線に当てはめて、各遊離タンパク質マーカーの濃度を算出した。
5.結果
実施例1では、PFSが6ヶ月以上であった患者を、ニボルマブが奏効した群に分類し、PFSが6ヶ月未満であった患者を、ニボルマブが奏効しなかった群に分類した。全ての患者(50例)のうち、PFSが6ヶ月以上であった患者は21例であり、PFSが6ヶ月未満であった患者は29例であった。また、PD-L1陰性症例(37例)のうち、PFSが6ヶ月以上であった患者は10例であり、PFSが6ヶ月未満であった患者は27例であった。図6A~6Cに、PD-L1陰性症例における、ニボルマブ投与前の血漿中の各遊離タンパク質マーカーの測定値(pg/mL)の分布を示す。図中、「奏効」は、ニボルマブが奏効した群を示し、「非奏効」は、ニボルマブが奏効しなかった群を示す。また、図中、破線は、測定値の中央値を示す。図6A~6Cに示されるように、ニボルマブが奏効した患者では、血液試料中の遊離PD-1、遊離CTLA-4及び遊離PD-L1の測定値が低い傾向にあることが分かった。
実施例1では、PFSが6ヶ月以上であった患者を、ニボルマブが奏効した群に分類し、PFSが6ヶ月未満であった患者を、ニボルマブが奏効しなかった群に分類した。全ての患者(50例)のうち、PFSが6ヶ月以上であった患者は21例であり、PFSが6ヶ月未満であった患者は29例であった。また、PD-L1陰性症例(37例)のうち、PFSが6ヶ月以上であった患者は10例であり、PFSが6ヶ月未満であった患者は27例であった。図6A~6Cに、PD-L1陰性症例における、ニボルマブ投与前の血漿中の各遊離タンパク質マーカーの測定値(pg/mL)の分布を示す。図中、「奏効」は、ニボルマブが奏効した群を示し、「非奏効」は、ニボルマブが奏効しなかった群を示す。また、図中、破線は、測定値の中央値を示す。図6A~6Cに示されるように、ニボルマブが奏効した患者では、血液試料中の遊離PD-1、遊離CTLA-4及び遊離PD-L1の測定値が低い傾向にあることが分かった。
PD-L1陰性症例(37例)を、各遊離タンパク質マーカーの測定値及び6ヶ月PFSにより分類した。また、マーカーの測定値に基づいてニボルマブの奏効性を判定した場合の感度及び特異度を算出した。結果を表1~3に示す。表中、「6ヶ月PFS」では、PFSが6ヶ月以上の被検者を「+」に分類し、PFSが6ヶ月未満の被検者を「-」に分類した。表中、「sPD-1」、「sCTLA-4」及び「sPD-L1」では、測定値が閾値より低かった被検者を「+」に分類し、測定値が閾値より高かった被検者を「-」に分類した。実施例1では、sPD-1に対応する閾値を150 pg/mLとし、sCTLA-4に対応する閾値を0.5 pg/mLとし、sPD-L1に対応する閾値を219 pg/mLとした。
PD-L1陰性症例に分類された37名の患者は、免疫組織染色に基づく従来の予測法では、ニボルマブが奏効しないと判断された患者であった。しかし、本実施例では、sPD-1の測定値を用いる判定により、PD-L1陰性症例から6名をニボルマブが奏効する患者としてさらに抽出することができた。また、sCTLA-4の測定値を用いる判定により9名を、sPD-L1の測定値を用いる判定により7名を、ニボルマブが奏効する患者としてさらに抽出することができた。
実施例2
実施例1の結果に基づいて、免疫チェックポイント阻害剤の奏効性を判定したときの判定精度を確認した。
実施例1の結果に基づいて、免疫チェックポイント阻害剤の奏効性を判定したときの判定精度を確認した。
1.免疫組織染色による奏効性の判定
実施例1で算出したTPSにより、ニボルマブの奏効性を判定した場合の感度及び特異度、を算出した。結果を表4に示す。表中、「6ヶ月PFS」では、PFSが6ヶ月以上の被検者を「+」に分類し、PFSが6ヶ月未満の被検者を「-」に分類した。「免疫組織染色(PD-L1)」では、TPSが50%以上であった被検者を「+」に分類し、TPSが50%未満の被検者を「-」に分類した。
実施例1で算出したTPSにより、ニボルマブの奏効性を判定した場合の感度及び特異度、を算出した。結果を表4に示す。表中、「6ヶ月PFS」では、PFSが6ヶ月以上の被検者を「+」に分類し、PFSが6ヶ月未満の被検者を「-」に分類した。「免疫組織染色(PD-L1)」では、TPSが50%以上であった被検者を「+」に分類し、TPSが50%未満の被検者を「-」に分類した。
表1に示されるように、腫瘍組織におけるPD-L1発現率に基づく判定では、特異度は高いが、感度が低いことが分かる。すなわち、当該判定では、本来は免疫チェックポイント阻害剤が奏効する患者を見落としている。そこで、以下では、免疫組織染色による判定で陰性と判断された被検者(TPS<50%)に対して、遊離マーカータンパク質の測定値に基づく判定をさらに行った。
2.免疫組織染色及び遊離タンパク質マーカーによる奏効性の判定
(2.1) 遊離タンパク質マーカーの測定値のスコア化
実施例1のPD-L1陰性症例(37例)について、血液試料中の遊離タンパク質マーカー(sPD-1及びsCTLA-4)の測定値を、閾値に基づいてスコア化した。実施例2では、閾値として、測定値の中央値を用いた。表5に示すように、sPD-1の測定値及びsCTLA-4の測定値の両方が、それぞれに対応する閾値よりも低い場合、スコアを0とした。sPD-1の測定値及びsCTLA-4の測定値のいずれか一方が、それに対応する閾値よりも低い場合、スコアを1とした。sPD-1の測定値及びsCTLA-4の測定値の両方が、それぞれに対応する閾値よりも高い場合、スコアを2とした。
(2.1) 遊離タンパク質マーカーの測定値のスコア化
実施例1のPD-L1陰性症例(37例)について、血液試料中の遊離タンパク質マーカー(sPD-1及びsCTLA-4)の測定値を、閾値に基づいてスコア化した。実施例2では、閾値として、測定値の中央値を用いた。表5に示すように、sPD-1の測定値及びsCTLA-4の測定値の両方が、それぞれに対応する閾値よりも低い場合、スコアを0とした。sPD-1の測定値及びsCTLA-4の測定値のいずれか一方が、それに対応する閾値よりも低い場合、スコアを1とした。sPD-1の測定値及びsCTLA-4の測定値の両方が、それぞれに対応する閾値よりも高い場合、スコアを2とした。
(2.2) 奏効性の判定
PD-L1陰性症例(37例)を、遊離タンパク質マーカーのスコアと6ヶ月PFSにより分類した。また、スコアに基づいてニボルマブの奏効性を判定した場合の感度及び特異度を算出した。結果を表6に示す。
PD-L1陰性症例(37例)を、遊離タンパク質マーカーのスコアと6ヶ月PFSにより分類した。また、スコアに基づいてニボルマブの奏効性を判定した場合の感度及び特異度を算出した。結果を表6に示す。
表6に示されるように、遊離タンパク質マーカーの測定値による判定では、スコアを0と1以上とに分けた場合、ニボルマブが奏効する患者を感度よく選択できることを見出した。したがって、遊離タンパク質マーカーの測定値による判定では、スコアが0である場合、免疫チェックポイント阻害剤が奏効する可能性が高いと判定され、被検者は免疫チェックポイント阻害剤の投与対象に選択される。一方、スコアが1以上の場合、免疫チェックポイント阻害剤が奏効する可能性が低いと判定され、被検者は免疫チェックポイント阻害剤の投与対象に選択されない。
また、上記(2.1)の免疫組織染色による判定と、遊離タンパク質マーカーの測定値による判定とを組み合わせて、ニボルマブの奏効性を判定した。この組み合わせによる判定のフローを図7に示す。当該判定の感度及び特異度を算出した。結果を表7に示す。表中、「免疫組織染色(PD-L1)及び血中マーカー検査(sPD-1及びsCTLA-4)」では、TPSが50%以上であった被検者及びTPSが50%未満且つスコアが0であった被検者を「+」に分類し、残りの被検者を「-」に分類した。
表7に示されるように、免疫組織染色による判定と、遊離タンパク質マーカーの測定値による判定とを組み合わせてニボルマブの奏効性を判定した場合、感度が顕著に向上した。図7に示すフローのように、免疫組織染色で陰性を示した被検者に対して、血液試料中の遊離タンパク質マーカーの測定値に基づく判定を行うことで、免疫チェックポイント阻害剤が奏効する可能性のある患者を抽出できることが示された。
実施例3
実施例1と同じ被検者(50例)について、sPD-1、sCTLA-4及びsPD-L1の3つのマーカーの測定値に基づいて、ニボルマブの奏効性を判定した。また、3つのマーカーの測定値による判定と、実施例2の免疫組織染色による判定とを組み合わせて、ニボルマブの奏効性を判定した。
実施例1と同じ被検者(50例)について、sPD-1、sCTLA-4及びsPD-L1の3つのマーカーの測定値に基づいて、ニボルマブの奏効性を判定した。また、3つのマーカーの測定値による判定と、実施例2の免疫組織染色による判定とを組み合わせて、ニボルマブの奏効性を判定した。
1.マーカーの測定値による判定
(1.1) 測定値のスコア化
各マーカーの測定値を、閾値に基づいてスコア化した。実施例3では、各マーカーに対応する閾値として、実施例1と同じ閾値を用いた。表8に示すように、sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値の全てが、それぞれに対応する閾値よりも低い場合、スコアを0とした。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値のいずれか1つが、それに対応する閾値よりも高い場合、スコアを1とした。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値のいずれか2つが、それに対応する閾値よりも高い場合、スコアを2とした。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値の全てが、それぞれに対応する閾値よりも高い場合、スコアを3とした。
(1.1) 測定値のスコア化
各マーカーの測定値を、閾値に基づいてスコア化した。実施例3では、各マーカーに対応する閾値として、実施例1と同じ閾値を用いた。表8に示すように、sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値の全てが、それぞれに対応する閾値よりも低い場合、スコアを0とした。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値のいずれか1つが、それに対応する閾値よりも高い場合、スコアを1とした。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値のいずれか2つが、それに対応する閾値よりも高い場合、スコアを2とした。sPD-1の測定値、sCTLA-4の測定値及びsPD-L1の測定値の全てが、それぞれに対応する閾値よりも高い場合、スコアを3とした。
(1.2) 奏効性の判定
被検者(50例)を、遊離タンパク質マーカーのスコアと6ヶ月PFSにより分類した。また、スコアに基づいてニボルマブの奏効性を判定した場合の感度及び特異度を算出した。結果を表9に示す。
被検者(50例)を、遊離タンパク質マーカーのスコアと6ヶ月PFSにより分類した。また、スコアに基づいてニボルマブの奏効性を判定した場合の感度及び特異度を算出した。結果を表9に示す。
表9及び表4に示されるように、血液試料中のマーカーの測定値に基づく判定は、腫瘍組織の免疫染色に基づく判定と同程度の感度及び特異度を有していた。血液の採取は、腫瘍組織の採取に比べて侵襲性が低いので、本実施形態の判定方法は、腫瘍組織の切除ができない患者にも適用し得ることが分かった。
2.マーカーの測定値による判定と免疫組織染色による判定との組み合わせ
上記(1.2)の3つのマーカーの測定値による判定と、実施例2の免疫組織染色による判定とを組み合わせて、ニボルマブの奏効性を判定した。結果を表10に示す。表中、「免疫組織染色及び血中マーカー検査」では、TPSが50%以上であった被検者及びTPSが50%未満且つスコアが0であった被検者を「+」に分類し、残りの被検者を「-」に分類した。
上記(1.2)の3つのマーカーの測定値による判定と、実施例2の免疫組織染色による判定とを組み合わせて、ニボルマブの奏効性を判定した。結果を表10に示す。表中、「免疫組織染色及び血中マーカー検査」では、TPSが50%以上であった被検者及びTPSが50%未満且つスコアが0であった被検者を「+」に分類し、残りの被検者を「-」に分類した。
表10に示されるように、免疫組織染色による判定と、3つの遊離タンパク質マーカーの測定値による判定とを組み合わせることにより、感度及び特異度の両方が高い判定が可能となり、判定精度が向上したと言える。
実施例4
食道がん患者及び子宮体がん患者について、免疫チェックポイント阻害剤の投与前の血液試料中の遊離タンパク質マーカーの濃度と、免疫チェックポイント阻害剤の投与後の治療効果との関連を検討した。
食道がん患者及び子宮体がん患者について、免疫チェックポイント阻害剤の投与前の血液試料中の遊離タンパク質マーカーの濃度と、免疫チェックポイント阻害剤の投与後の治療効果との関連を検討した。
1.被検者
免疫チェックポイント阻害剤を投与されていない食道がんの患者(64例)及び子宮体がんの患者(22例)を被検者とした。全ての患者にニボルマブ(小野薬品工業株式会社)を投与し、全生存期間(OS)を評価指標として経過を観察した。
免疫チェックポイント阻害剤を投与されていない食道がんの患者(64例)及び子宮体がんの患者(22例)を被検者とした。全ての患者にニボルマブ(小野薬品工業株式会社)を投与し、全生存期間(OS)を評価指標として経過を観察した。
2.液体試料及び測定
免疫チェックポイント阻害剤の投与前に、上記の患者から血液を採取し、血漿を調製した。これらの血漿を用いて実施例1と同様にして、遊離タンパク質マーカーの濃度を算出した。
免疫チェックポイント阻害剤の投与前に、上記の患者から血液を採取し、血漿を調製した。これらの血漿を用いて実施例1と同様にして、遊離タンパク質マーカーの濃度を算出した。
3.結果
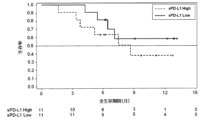
各遊離タンパク質マーカーについて、測定値が高い群と測定値が低い群とを比較したカプラン・マイヤー法による生存率曲線を作成した。結果を図8及び9に示す。図中、横線は、生存率が50%のラインを示す。また、図中、横軸の下に示した各群の数値は、横軸の各時点における生存者の数である。これらの図に示されるように、いずれの遊離タンパク質マーカーについても、測定値が低い群(図中、実線で示される)は、測定値が高い群(図中、破線で示される)に比べて、免疫チェックポイント阻害剤の投与によりOSが長期化する傾向にあることが分かった。これらの結果より、本実施形態の判定方法は、食道がん患者及び子宮体がん患者にも適用できることが示唆された。
各遊離タンパク質マーカーについて、測定値が高い群と測定値が低い群とを比較したカプラン・マイヤー法による生存率曲線を作成した。結果を図8及び9に示す。図中、横線は、生存率が50%のラインを示す。また、図中、横軸の下に示した各群の数値は、横軸の各時点における生存者の数である。これらの図に示されるように、いずれの遊離タンパク質マーカーについても、測定値が低い群(図中、実線で示される)は、測定値が高い群(図中、破線で示される)に比べて、免疫チェックポイント阻害剤の投与によりOSが長期化する傾向にあることが分かった。これらの結果より、本実施形態の判定方法は、食道がん患者及び子宮体がん患者にも適用できることが示唆された。
11、21、31: 試薬キット
12、22、32: 第1容器
13、23、33: 第2容器
24、34: 第3容器
25、35: 第4容器
36: 第5容器
37: 第6容器
14、27、38: 梱包箱
15、26、39: 添付文書
10: 判定装置
20: 免疫測定装置
30: コンピュータシステム
40: 記録媒体
300: コンピュータ本体
301: 入力部
302: 表示部
310: CPU
311: ROM
312: RAM
313: ハードディスク
314: 入出力インターフェイス
315: 読取装置
316: 通信インターフェイス
317: 画像出力インターフェイス
318: バス
12、22、32: 第1容器
13、23、33: 第2容器
24、34: 第3容器
25、35: 第4容器
36: 第5容器
37: 第6容器
14、27、38: 梱包箱
15、26、39: 添付文書
10: 判定装置
20: 免疫測定装置
30: コンピュータシステム
40: 記録媒体
300: コンピュータ本体
301: 入力部
302: 表示部
310: CPU
311: ROM
312: RAM
313: ハードディスク
314: 入出力インターフェイス
315: 読取装置
316: 通信インターフェイス
317: 画像出力インターフェイス
318: バス
Claims (17)
- 被検者から採取した液体試料中の遊離タンパク質マーカーを測定する工程を含み、前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含み、測定結果が、前記被検者に対する免疫チェックポイント阻害剤の奏効性を示唆する、免疫チェックポイント阻害剤の奏効性の判定を補助する方法。
- 前記測定工程で取得した遊離タンパク質マーカーの測定値が、前記マーカーに対応する閾値より低いとき、免疫チェックポイント阻害剤が前記被検者に奏効することを示唆する、請求項1に記載の方法。
- 前記被検者が、腫瘍組織の免疫染色により、PD-L1陽性腫瘍細胞の割合が所定の値より低いと判定されたがん患者である、請求項1又は2に記載の方法。
- 前記被検者が、肺がん患者、食道がん患者又は子宮体がん患者である、請求項1~3のいずれか1項に記載の方法。
- 前記免疫チェックポイント阻害剤が、有効成分として抗PD-1抗体を含む製剤である、請求項1~4のいずれか1項に記載の方法。
- 前記液体試料が、血液試料である請求項1~5のいずれか1項に記載の方法。
- 被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得する工程を含み、
前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含む、
取得した遊離タンパク質マーカーの測定値が、前記マーカーに対応する閾値より低いとき、免疫チェックポイント阻害剤が前記被検者に奏効することを示唆する、
遊離タンパク質マーカーの測定値の取得方法。 - 前記免疫チェックポイント阻害剤が、有効成分として抗PD-1抗体を含む製剤である、請求項7に記載の方法。
- 前記被検者が、肺がん患者、食道がん患者又は子宮体がん患者である、請求項7又は8に記載の方法。
- 前記液体試料が、血液試料である請求項7~9のいずれか1項に記載の方法。
- 被検者から採取した腫瘍組織の免疫染色を行い、PD-L1陽性腫瘍細胞の割合を算出する工程と、
前記被検者から採取した液体試料中の遊離タンパク質マーカーを測定する工程と
を含み、前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含み、
前記算出結果及び前記測定結果が、前記被検者に対する免疫チェックポイント阻害剤の奏効性を示唆する、
免疫チェックポイント阻害剤の奏効性の判定を補助する方法。 - 前記算出工程で取得したPD-L1陽性腫瘍細胞の割合が所定の値より低く、且つ前記測定工程で取得した遊離タンパク質マーカーの測定値が、前記マーカーに対応する閾値より低いとき、免疫チェックポイント阻害剤が前記被検者に奏効することを示唆する、請求項11に記載の方法。
- 遊離PD-L1(Programmed cell death-ligand 1)と特異的に結合可能な物質を含む試薬を含む、請求項1~12のいずれか1項に記載の方法に用いるための試薬キット。
- プロセッサ及び前記プロセッサの制御下にあるメモリを含むコンピュータを備え、前記メモリには、下記のステップ:
被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得するステップと、
前記マーカーの測定値に基づいて、前記被検者に対する免疫チェックポイント阻害剤の奏効性を判定するステップと
を前記コンピュータに実行させるためのコンピュータプログラムが記録されており、
前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含む、
免疫チェックポイント阻害剤の奏効性の判定装置。 - プロセッサ及び前記プロセッサの制御下にあるメモリを含むコンピュータを備え、
前記メモリには、下記のステップ:
被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得するステップを前記コンピュータに実行させるためのコンピュータプログラムが記録されており、
前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含み、
取得した遊離タンパク質マーカーの測定値が、前記マーカーに対応する閾値より低いとき、免疫チェックポイント阻害剤が該被検者に奏効することを示唆する、
遊離タンパク質マーカーの測定値の取得装置。 - コンピュータが読み取り可能な媒体に記録されているコンピュータプログラムであって、
前記コンピュータプログラムが、下記のステップ:
被検者から採取した液体試料中の遊離タンパク質マーカーの測定値を取得するステップと、
前記マーカーの測定値に基づいて、前記被検者に対する免疫チェックポイント阻害剤の奏効性を判定するステップと
を前記コンピュータに実行させるためのコンピュータプログラムであり、
前記遊離タンパク質マーカーが、遊離PD-L1(Programmed cell death-ligand 1)を含む、
免疫チェックポイント阻害剤の奏効性の判定のためのコンピュータプログラム。 - 請求項1~6、11及び12のいずれか1項に記載の方法により免疫チェックポイント阻害剤が奏効すると判定されたがん患者に投与されることを特徴とする、免疫チェックポイント阻害剤を含有するがん治療用医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018059834 | 2018-03-27 | ||
| JP2018059834 | 2018-03-27 | ||
| JP2020098576A JP7251738B2 (ja) | 2018-03-27 | 2020-06-05 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020098576A Division JP7251738B2 (ja) | 2018-03-27 | 2020-06-05 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2023082015A true JP2023082015A (ja) | 2023-06-13 |
Family
ID=68061613
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019547535A Active JP6719117B2 (ja) | 2018-03-27 | 2019-03-14 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
| JP2020098576A Active JP7251738B2 (ja) | 2018-03-27 | 2020-06-05 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
| JP2023039900A Pending JP2023082015A (ja) | 2018-03-27 | 2023-03-14 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019547535A Active JP6719117B2 (ja) | 2018-03-27 | 2019-03-14 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
| JP2020098576A Active JP7251738B2 (ja) | 2018-03-27 | 2020-06-05 | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20210003579A1 (ja) |
| EP (1) | EP3779450A4 (ja) |
| JP (3) | JP6719117B2 (ja) |
| CN (1) | CN111919119A (ja) |
| WO (1) | WO2019188354A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2970873C (en) * | 2005-05-09 | 2022-05-17 | E. R. Squibb & Sons, L.L.C. | Human monoclonal antibodies to programmed death 1 (pd-1) and methods for treating cancer using anti-pd-1 antibodies alone or in combination with other immunotherapeutics |
| TW202021617A (zh) * | 2018-08-10 | 2020-06-16 | 國立大學法人岐阜大學 | 用於預測免疫檢查點阻礙藥之有效性之生物標記 |
| JP2020148631A (ja) * | 2019-03-13 | 2020-09-17 | 学校法人日本医科大学 | 免疫チェックポイント阻害剤の血中モニタリングおよび患者層別化方法 |
| KR20220093122A (ko) * | 2019-11-08 | 2022-07-05 | 아지노모토 가부시키가이샤 | 면역 체크 포인트 저해제의 약리 작용의 평가 방법, 산출 방법, 평가 장치, 산출 장치, 평가 프로그램, 산출 프로그램, 기록 매체, 평가 시스템 및 단말 장치 |
| EP4130024A1 (en) * | 2020-03-26 | 2023-02-08 | JSR Corporation | Method for predicting efficacy of treatment of lung cancer patient using immune checkpoint inhibitor |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2606722B2 (ja) | 1988-04-05 | 1997-05-07 | 栄治 石川 | 超高感度抗原物質の測定法 |
| EP3293275B1 (en) * | 2013-06-06 | 2021-08-04 | Dana-Farber Cancer Institute, Inc. | Compositions and methods for identification, assessment prevention, and treatment of cancer using pd-l1 isoforms |
| RU2744836C2 (ru) * | 2014-05-08 | 2021-03-16 | Новодиакс, Инк. | Прямой иммуногистохимический анализ |
| CN108463724B (zh) * | 2015-12-28 | 2022-02-15 | 国立大学法人京都大学 | 癌的判断方法、癌的判断用装置及计算机程序 |
-
2019
- 2019-03-14 EP EP19774196.0A patent/EP3779450A4/en active Pending
- 2019-03-14 CN CN201980022487.4A patent/CN111919119A/zh active Pending
- 2019-03-14 JP JP2019547535A patent/JP6719117B2/ja active Active
- 2019-03-14 WO PCT/JP2019/010601 patent/WO2019188354A1/ja unknown
-
2020
- 2020-06-05 JP JP2020098576A patent/JP7251738B2/ja active Active
- 2020-09-23 US US17/029,361 patent/US20210003579A1/en active Pending
-
2023
- 2023-03-14 JP JP2023039900A patent/JP2023082015A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20210003579A1 (en) | 2021-01-07 |
| EP3779450A1 (en) | 2021-02-17 |
| CN111919119A (zh) | 2020-11-10 |
| JP7251738B2 (ja) | 2023-04-04 |
| EP3779450A4 (en) | 2022-01-12 |
| WO2019188354A1 (ja) | 2019-10-03 |
| JP2020160076A (ja) | 2020-10-01 |
| JP6719117B2 (ja) | 2020-07-08 |
| JPWO2019188354A1 (ja) | 2020-05-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7251738B2 (ja) | 免疫チェックポイント阻害剤の奏効性の判定を補助する方法、試薬キット、装置及びコンピュータプログラム | |
| CA2623653C (en) | Use of n-myristoyltransferase on non-tumor tissue for cancer diagnosis | |
| US10436806B2 (en) | Method of measuring lipoprotein's capacity to accept cholesterol | |
| US20180299453A1 (en) | Method for determining cancer | |
| CN107271678A (zh) | 肾病发展风险的诊断试剂盒制造用途及辅助诊断方法 | |
| Kolonko et al. | Potential utility of neutrophil-to-lymphocyte, platelet-to-lymphocyte, and neutrophil, lymphocyte, and platelet ratios in differential diagnosis of kidney transplant acute rejection: a retrospective, propensity score matched analysis | |
| Nwachokor et al. | Quantitation of spatial and temporal variability of biomarkers for Barrett's Esophagus | |
| Creaney et al. | Does CA125 binding to mesothelin impact the detection of malignant mesothelioma? | |
| WO2014159907A1 (en) | Systems and methods employing human stem cell markers for detection, diagnosis and treatment of circulating tumor cells | |
| WO2023234422A1 (ja) | 三次リンパ組織の検査方法、及び三次リンパ組織の検査用キット | |
| JP6602481B2 (ja) | 予後診断方法及び該方法において有用なキット | |
| JP6799226B2 (ja) | 骨髄線維症の状態の診断を補助する方法、予後の予測を補助する方法、及び治療効果のモニター方法、並びにそれらの方法に用いるマーカー及び装置 | |
| Yigzaw et al. | Review of Immunohistochemistry Techniques: Applications, Current Status, and Future Perspectives | |
| WO2024011295A1 (en) | Methods and products for determining responsiveness to anti-pd1 immune checkpoint inhibitor immunotherapy | |
| JP2020162420A (ja) | サイクリン依存性キナーゼ4/6阻害剤の感受性を判定するための方法、試薬キット、装置及びコンピュータプログラム | |
| Bozzetti et al. | Determination of Biological Parameters on Fine-Needle Aspirates from Non-Small Cell Lung Cancer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230314 |