JP2021511524A - ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ - Google Patents
ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ Download PDFInfo
- Publication number
- JP2021511524A JP2021511524A JP2020561597A JP2020561597A JP2021511524A JP 2021511524 A JP2021511524 A JP 2021511524A JP 2020561597 A JP2020561597 A JP 2020561597A JP 2020561597 A JP2020561597 A JP 2020561597A JP 2021511524 A JP2021511524 A JP 2021511524A
- Authority
- JP
- Japan
- Prior art keywords
- analyte
- sample
- complex
- assay
- subject
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000003556 assay Methods 0.000 title claims abstract description 284
- 208000035143 Bacterial infection Diseases 0.000 title claims description 16
- 208000022362 bacterial infectious disease Diseases 0.000 title claims description 16
- 208000036142 Viral infection Diseases 0.000 title claims description 13
- 230000003612 virological effect Effects 0.000 title claims description 6
- 238000000034 method Methods 0.000 claims abstract description 82
- 239000012491 analyte Substances 0.000 claims description 399
- 239000012530 fluid Substances 0.000 claims description 189
- 239000002516 radical scavenger Substances 0.000 claims description 140
- 238000012360 testing method Methods 0.000 claims description 139
- 108010074051 C-Reactive Protein Proteins 0.000 claims description 129
- 102100032752 C-reactive protein Human genes 0.000 claims description 129
- 102000046283 TNF-Related Apoptosis-Inducing Ligand Human genes 0.000 claims description 100
- 101710097160 Tumor necrosis factor ligand superfamily member 10 Proteins 0.000 claims description 96
- 238000001514 detection method Methods 0.000 claims description 70
- 238000013096 assay test Methods 0.000 claims description 63
- 239000012634 fragment Substances 0.000 claims description 63
- 230000003287 optical effect Effects 0.000 claims description 44
- 239000003795 chemical substances by application Substances 0.000 claims description 40
- 231100000673 dose–response relationship Toxicity 0.000 claims description 33
- 230000002000 scavenging effect Effects 0.000 claims description 30
- 102000004169 proteins and genes Human genes 0.000 claims description 26
- 108090000623 proteins and genes Proteins 0.000 claims description 26
- 238000004458 analytical method Methods 0.000 claims description 22
- 210000004369 blood Anatomy 0.000 claims description 22
- 239000008280 blood Substances 0.000 claims description 22
- 210000002966 serum Anatomy 0.000 claims description 22
- 230000027455 binding Effects 0.000 claims description 21
- 238000002405 diagnostic procedure Methods 0.000 claims description 19
- 230000001965 increasing effect Effects 0.000 claims description 19
- 210000002381 plasma Anatomy 0.000 claims description 17
- 239000000126 substance Substances 0.000 claims description 17
- 206010061218 Inflammation Diseases 0.000 claims description 14
- 230000004054 inflammatory process Effects 0.000 claims description 14
- 230000007423 decrease Effects 0.000 claims description 13
- 238000003745 diagnosis Methods 0.000 claims description 8
- 201000010099 disease Diseases 0.000 claims description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 7
- 230000008569 process Effects 0.000 claims description 7
- 230000001939 inductive effect Effects 0.000 claims description 6
- 239000003446 ligand Substances 0.000 claims description 6
- 102000008070 Interferon-gamma Human genes 0.000 claims description 5
- 108010074328 Interferon-gamma Proteins 0.000 claims description 5
- 229960003130 interferon gamma Drugs 0.000 claims description 5
- 230000002829 reductive effect Effects 0.000 claims description 5
- 238000005507 spraying Methods 0.000 claims description 5
- 210000003296 saliva Anatomy 0.000 claims description 4
- 210000002700 urine Anatomy 0.000 claims description 4
- 230000006907 apoptotic process Effects 0.000 claims description 3
- 210000004243 sweat Anatomy 0.000 claims description 3
- 238000001035 drying Methods 0.000 claims description 2
- 230000006698 induction Effects 0.000 claims 1
- 238000010586 diagram Methods 0.000 abstract 1
- 239000000523 sample Substances 0.000 description 390
- 241000699666 Mus <mouse, genus> Species 0.000 description 87
- 230000000670 limiting effect Effects 0.000 description 35
- -1 IP-10 Proteins 0.000 description 25
- 239000002245 particle Substances 0.000 description 24
- 238000005259 measurement Methods 0.000 description 23
- 239000013641 positive control Substances 0.000 description 19
- 108010048233 Procalcitonin Proteins 0.000 description 18
- 238000002372 labelling Methods 0.000 description 18
- CWCXERYKLSEGEZ-KDKHKZEGSA-N procalcitonin Chemical compound C([C@@H](C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)NCC(O)=O)[C@@H](C)O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCSC)NC(=O)[C@H]1NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)CNC(=O)[C@@H](N)CSSC1)[C@@H](C)O)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 CWCXERYKLSEGEZ-KDKHKZEGSA-N 0.000 description 18
- 239000000243 solution Substances 0.000 description 15
- 239000007787 solid Substances 0.000 description 13
- 101000858088 Homo sapiens C-X-C motif chemokine 10 Proteins 0.000 description 12
- 102100025248 C-X-C motif chemokine 10 Human genes 0.000 description 11
- 239000003153 chemical reaction reagent Substances 0.000 description 11
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 11
- 239000002105 nanoparticle Substances 0.000 description 11
- 230000009385 viral infection Effects 0.000 description 11
- 150000001413 amino acids Chemical class 0.000 description 10
- 239000011324 bead Substances 0.000 description 10
- 229910052737 gold Inorganic materials 0.000 description 10
- 239000010931 gold Substances 0.000 description 10
- 102100031802 Interferon-induced GTP-binding protein Mx1 Human genes 0.000 description 9
- 210000004027 cell Anatomy 0.000 description 9
- 239000004816 latex Substances 0.000 description 9
- 229920000126 latex Polymers 0.000 description 9
- 239000013642 negative control Substances 0.000 description 9
- 230000009870 specific binding Effects 0.000 description 9
- 101001128393 Homo sapiens Interferon-induced GTP-binding protein Mx1 Proteins 0.000 description 8
- 239000000427 antigen Substances 0.000 description 8
- 238000010790 dilution Methods 0.000 description 8
- 239000012895 dilution Substances 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- 101000830565 Homo sapiens Tumor necrosis factor ligand superfamily member 10 Proteins 0.000 description 7
- 108060003951 Immunoglobulin Proteins 0.000 description 6
- 239000000020 Nitrocellulose Substances 0.000 description 6
- FJWGYAHXMCUOOM-QHOUIDNNSA-N [(2s,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6s)-4,5-dinitrooxy-2-(nitrooxymethyl)-6-[(2r,3r,4s,5r,6s)-4,5,6-trinitrooxy-2-(nitrooxymethyl)oxan-3-yl]oxyoxan-3-yl]oxy-3,5-dinitrooxy-6-(nitrooxymethyl)oxan-4-yl] nitrate Chemical compound O([C@@H]1O[C@@H]([C@H]([C@H](O[N+]([O-])=O)[C@H]1O[N+]([O-])=O)O[C@H]1[C@@H]([C@@H](O[N+]([O-])=O)[C@H](O[N+]([O-])=O)[C@@H](CO[N+]([O-])=O)O1)O[N+]([O-])=O)CO[N+](=O)[O-])[C@@H]1[C@@H](CO[N+]([O-])=O)O[C@@H](O[N+]([O-])=O)[C@H](O[N+]([O-])=O)[C@H]1O[N+]([O-])=O FJWGYAHXMCUOOM-QHOUIDNNSA-N 0.000 description 6
- 230000008901 benefit Effects 0.000 description 6
- 102000044949 human TNFSF10 Human genes 0.000 description 6
- 102000018358 immunoglobulin Human genes 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 229920001220 nitrocellulos Polymers 0.000 description 6
- 238000011546 CRP measurement Methods 0.000 description 5
- 102000004190 Enzymes Human genes 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 5
- 241000283973 Oryctolagus cuniculus Species 0.000 description 5
- 102000036639 antigens Human genes 0.000 description 5
- 108091007433 antigens Proteins 0.000 description 5
- 238000007865 diluting Methods 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 230000007613 environmental effect Effects 0.000 description 5
- 208000015181 infectious disease Diseases 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 238000011002 quantification Methods 0.000 description 5
- 239000000758 substrate Substances 0.000 description 5
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- 102000014150 Interferons Human genes 0.000 description 4
- 108010050904 Interferons Proteins 0.000 description 4
- 108091028043 Nucleic acid sequence Proteins 0.000 description 4
- 108700012411 TNFSF10 Proteins 0.000 description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 4
- 239000012472 biological sample Substances 0.000 description 4
- 229960000074 biopharmaceutical Drugs 0.000 description 4
- 229960002685 biotin Drugs 0.000 description 4
- 239000011616 biotin Substances 0.000 description 4
- 229920002678 cellulose Polymers 0.000 description 4
- 150000001875 compounds Chemical class 0.000 description 4
- 229920001903 high density polyethylene Polymers 0.000 description 4
- 239000004700 high-density polyethylene Substances 0.000 description 4
- 229940088597 hormone Drugs 0.000 description 4
- 239000005556 hormone Substances 0.000 description 4
- 230000002452 interceptive effect Effects 0.000 description 4
- 229940079322 interferon Drugs 0.000 description 4
- 150000007523 nucleic acids Chemical class 0.000 description 4
- 230000035945 sensitivity Effects 0.000 description 4
- 150000003384 small molecules Chemical class 0.000 description 4
- 102000003390 tumor necrosis factor Human genes 0.000 description 4
- 238000011144 upstream manufacturing Methods 0.000 description 4
- FTOAOBMCPZCFFF-UHFFFAOYSA-N 5,5-diethylbarbituric acid Chemical class CCC1(CC)C(=O)NC(=O)NC1=O FTOAOBMCPZCFFF-UHFFFAOYSA-N 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- 241000283707 Capra Species 0.000 description 3
- 208000010201 Exanthema Diseases 0.000 description 3
- 239000004952 Polyamide Substances 0.000 description 3
- 201000005485 Toxoplasmosis Diseases 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 229940098773 bovine serum albumin Drugs 0.000 description 3
- 238000004364 calculation method Methods 0.000 description 3
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 201000005884 exanthem Diseases 0.000 description 3
- 239000007850 fluorescent dye Substances 0.000 description 3
- 208000002672 hepatitis B Diseases 0.000 description 3
- 229940072221 immunoglobulins Drugs 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 238000007837 multiplex assay Methods 0.000 description 3
- 230000010287 polarization Effects 0.000 description 3
- 229920002647 polyamide Polymers 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 206010037844 rash Diseases 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 102000011022 Chorionic Gonadotropin Human genes 0.000 description 2
- 108010062540 Chorionic Gonadotropin Proteins 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 102000009151 Luteinizing Hormone Human genes 0.000 description 2
- 108010073521 Luteinizing Hormone Proteins 0.000 description 2
- 101150112867 MX1 gene Proteins 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 239000004677 Nylon Substances 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 206010036790 Productive cough Diseases 0.000 description 2
- RJKFOVLPORLFTN-LEKSSAKUSA-N Progesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 RJKFOVLPORLFTN-LEKSSAKUSA-N 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 2
- 102000011923 Thyrotropin Human genes 0.000 description 2
- 108010061174 Thyrotropin Proteins 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- VIROVYVQCGLCII-UHFFFAOYSA-N amobarbital Chemical compound CC(C)CCC1(CC)C(=O)NC(=O)NC1=O VIROVYVQCGLCII-UHFFFAOYSA-N 0.000 description 2
- 230000001745 anti-biotin effect Effects 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- TZCXTZWJZNENPQ-UHFFFAOYSA-L barium sulfate Chemical compound [Ba+2].[O-]S([O-])(=O)=O TZCXTZWJZNENPQ-UHFFFAOYSA-L 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 229920002301 cellulose acetate Polymers 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- ZPUCINDJVBIVPJ-LJISPDSOSA-N cocaine Chemical compound O([C@H]1C[C@@H]2CC[C@@H](N2C)[C@H]1C(=O)OC)C(=O)C1=CC=CC=C1 ZPUCINDJVBIVPJ-LJISPDSOSA-N 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- DDRJAANPRJIHGJ-UHFFFAOYSA-N creatinine Chemical compound CN1CC(=O)NC1=N DDRJAANPRJIHGJ-UHFFFAOYSA-N 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 2
- 102000046438 human CXCL10 Human genes 0.000 description 2
- 229940084986 human chorionic gonadotropin Drugs 0.000 description 2
- OROGSEYTTFOCAN-UHFFFAOYSA-N hydrocodone Natural products C1C(N(CCC234)C)C2C=CC(O)C3OC2=C4C1=CC=C2OC OROGSEYTTFOCAN-UHFFFAOYSA-N 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 230000003100 immobilizing effect Effects 0.000 description 2
- 238000003018 immunoassay Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 229940040129 luteinizing hormone Drugs 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 239000002122 magnetic nanoparticle Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 240000004308 marijuana Species 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- 229920005615 natural polymer Polymers 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 229920001778 nylon Polymers 0.000 description 2
- 239000000123 paper Substances 0.000 description 2
- WEXRUCMBJFQVBZ-UHFFFAOYSA-N pentobarbital Chemical compound CCCC(C)C1(CC)C(=O)NC(=O)NC1=O WEXRUCMBJFQVBZ-UHFFFAOYSA-N 0.000 description 2
- DDBREPKUVSBGFI-UHFFFAOYSA-N phenobarbital Chemical compound C=1C=CC=CC=1C1(CC)C(=O)NC(=O)NC1=O DDBREPKUVSBGFI-UHFFFAOYSA-N 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 239000011148 porous material Substances 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 238000000159 protein binding assay Methods 0.000 description 2
- 239000002096 quantum dot Substances 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 239000004627 regenerated cellulose Substances 0.000 description 2
- 229910052711 selenium Inorganic materials 0.000 description 2
- 239000011669 selenium Substances 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 210000003802 sputum Anatomy 0.000 description 2
- 208000024794 sputum Diseases 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 229920001059 synthetic polymer Polymers 0.000 description 2
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 241000712461 unidentified influenza virus Species 0.000 description 2
- 230000000007 visual effect Effects 0.000 description 2
- WRRSFOZOETZUPG-FFHNEAJVSA-N (4r,4ar,7s,7ar,12bs)-9-methoxy-3-methyl-2,4,4a,7,7a,13-hexahydro-1h-4,12-methanobenzofuro[3,2-e]isoquinoline-7-ol;hydrate Chemical compound O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC WRRSFOZOETZUPG-FFHNEAJVSA-N 0.000 description 1
- KWTSXDURSIMDCE-QMMMGPOBSA-N (S)-amphetamine Chemical compound C[C@H](N)CC1=CC=CC=C1 KWTSXDURSIMDCE-QMMMGPOBSA-N 0.000 description 1
- VOXZDWNPVJITMN-ZBRFXRBCSA-N 17β-estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 VOXZDWNPVJITMN-ZBRFXRBCSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 241000272517 Anseriformes Species 0.000 description 1
- 206010003445 Ascites Diseases 0.000 description 1
- 238000012935 Averaging Methods 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- SGHZXLIDFTYFHQ-UHFFFAOYSA-L Brilliant Blue Chemical compound [Na+].[Na+].C=1C=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C(=CC=CC=2)S([O-])(=O)=O)C=CC=1N(CC)CC1=CC=CC(S([O-])(=O)=O)=C1 SGHZXLIDFTYFHQ-UHFFFAOYSA-L 0.000 description 1
- 102000055006 Calcitonin Human genes 0.000 description 1
- 108060001064 Calcitonin Proteins 0.000 description 1
- 241000282832 Camelidae Species 0.000 description 1
- 235000012766 Cannabis sativa ssp. sativa var. sativa Nutrition 0.000 description 1
- 235000012765 Cannabis sativa ssp. sativa var. spontanea Nutrition 0.000 description 1
- 101710132601 Capsid protein Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 108010008978 Chemokine CXCL10 Proteins 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- AUNGANRZJHBGPY-UHFFFAOYSA-N D-Lyxoflavin Natural products OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-UHFFFAOYSA-N 0.000 description 1
- WDJUZGPOPHTGOT-OAXVISGBSA-N Digitoxin Natural products O([C@H]1[C@@H](C)O[C@@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@@](C)([C@H](C6=CC(=O)OC6)CC5)CC4)CC3)CC2)C[C@H]1O)[C@H]1O[C@@H](C)[C@H](O[C@H]2O[C@@H](C)[C@@H](O)[C@@H](O)C2)[C@@H](O)C1 WDJUZGPOPHTGOT-OAXVISGBSA-N 0.000 description 1
- LTMHDMANZUZIPE-AMTYYWEZSA-N Digoxin Natural products O([C@H]1[C@H](C)O[C@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@](C)([C@H](O)C4)[C@H](C4=CC(=O)OC4)CC5)CC3)CC2)C[C@@H]1O)[C@H]1O[C@H](C)[C@@H](O[C@H]2O[C@@H](C)[C@H](O)[C@@H](O)C2)[C@@H](O)C1 LTMHDMANZUZIPE-AMTYYWEZSA-N 0.000 description 1
- 102000043859 Dynamin Human genes 0.000 description 1
- 108700021058 Dynamin Proteins 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000283074 Equus asinus Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 102000008857 Ferritin Human genes 0.000 description 1
- 108050000784 Ferritin Proteins 0.000 description 1
- 238000008416 Ferritin Methods 0.000 description 1
- 102000013446 GTP Phosphohydrolases Human genes 0.000 description 1
- 102000030782 GTP binding Human genes 0.000 description 1
- 108091000058 GTP-Binding Proteins 0.000 description 1
- 108091006109 GTPases Proteins 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- 102100028967 HLA class I histocompatibility antigen, alpha chain G Human genes 0.000 description 1
- 101710197836 HLA class I histocompatibility antigen, alpha chain G Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 241000700721 Hepatitis B virus Species 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 108010093488 His-His-His-His-His-His Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 241000598436 Human T-cell lymphotropic virus Species 0.000 description 1
- 241000725303 Human immunodeficiency virus Species 0.000 description 1
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 101710202180 Interferon-induced GTP-binding protein Mx1 Proteins 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 102000019298 Lipocalin Human genes 0.000 description 1
- 108050006654 Lipocalin Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 229920002302 Nylon 6,6 Polymers 0.000 description 1
- BRUQQQPBMZOVGD-XFKAJCMBSA-N Oxycodone Chemical compound O=C([C@@H]1O2)CC[C@@]3(O)[C@H]4CC5=CC=C(OC)C2=C5[C@@]13CCN4C BRUQQQPBMZOVGD-XFKAJCMBSA-N 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 101800001442 Peptide pr Proteins 0.000 description 1
- CXOFVDLJLONNDW-UHFFFAOYSA-N Phenytoin Chemical compound N1C(=O)NC(=O)C1(C=1C=CC=CC=1)C1=CC=CC=C1 CXOFVDLJLONNDW-UHFFFAOYSA-N 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 239000004695 Polyether sulfone Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- AUNGANRZJHBGPY-SCRDCRAPSA-N Riboflavin Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-SCRDCRAPSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- FOIXSVOLVBLSDH-UHFFFAOYSA-N Silver ion Chemical compound [Ag+] FOIXSVOLVBLSDH-UHFFFAOYSA-N 0.000 description 1
- 241000907663 Siproeta stelenes Species 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 208000000389 T-cell leukemia Diseases 0.000 description 1
- 208000028530 T-cell lymphoblastic leukemia/lymphoma Diseases 0.000 description 1
- 102100024598 Tumor necrosis factor ligand superfamily member 10 Human genes 0.000 description 1
- 108010059993 Vancomycin Proteins 0.000 description 1
- 229930003471 Vitamin B2 Natural products 0.000 description 1
- 229910021536 Zeolite Inorganic materials 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910052910 alkali metal silicate Inorganic materials 0.000 description 1
- 229910052915 alkaline earth metal silicate Inorganic materials 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- WLDHEUZGFKACJH-UHFFFAOYSA-K amaranth Chemical compound [Na+].[Na+].[Na+].C12=CC=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(O)=C1N=NC1=CC=C(S([O-])(=O)=O)C2=CC=CC=C12 WLDHEUZGFKACJH-UHFFFAOYSA-K 0.000 description 1
- 210000004381 amniotic fluid Anatomy 0.000 description 1
- 229960001301 amobarbital Drugs 0.000 description 1
- 229940025084 amphetamine Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 210000003567 ascitic fluid Anatomy 0.000 description 1
- 229960002319 barbital Drugs 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 229940049706 benzodiazepine Drugs 0.000 description 1
- 150000001557 benzodiazepines Chemical class 0.000 description 1
- 210000000941 bile Anatomy 0.000 description 1
- 239000010836 blood and blood product Substances 0.000 description 1
- 229940125691 blood product Drugs 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 description 1
- 229960004015 calcitonin Drugs 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 229930003827 cannabinoid Natural products 0.000 description 1
- 239000003557 cannabinoid Substances 0.000 description 1
- 229940065144 cannabinoids Drugs 0.000 description 1
- FFGPTBGBLSHEPO-UHFFFAOYSA-N carbamazepine Chemical compound C1=CC2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 FFGPTBGBLSHEPO-UHFFFAOYSA-N 0.000 description 1
- 229960000623 carbamazepine Drugs 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000011852 carbon nanoparticle Substances 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920003086 cellulose ether Polymers 0.000 description 1
- 210000003756 cervix mucus Anatomy 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 239000003593 chromogenic compound Substances 0.000 description 1
- 239000004927 clay Substances 0.000 description 1
- 229910052570 clay Inorganic materials 0.000 description 1
- 229960003920 cocaine Drugs 0.000 description 1
- 229960004126 codeine Drugs 0.000 description 1
- OROGSEYTTFOCAN-DNJOTXNNSA-N codeine Natural products C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC OROGSEYTTFOCAN-DNJOTXNNSA-N 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 239000000599 controlled substance Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 229940109239 creatinine Drugs 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 210000002726 cyst fluid Anatomy 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- XLMALTXPSGQGBX-GCJKJVERSA-N dextropropoxyphene Chemical compound C([C@](OC(=O)CC)([C@H](C)CN(C)C)C=1C=CC=CC=1)C1=CC=CC=C1 XLMALTXPSGQGBX-GCJKJVERSA-N 0.000 description 1
- 229960004193 dextropropoxyphene Drugs 0.000 description 1
- NIJJYAXOARWZEE-UHFFFAOYSA-N di-n-propyl-acetic acid Natural products CCCC(C(O)=O)CCC NIJJYAXOARWZEE-UHFFFAOYSA-N 0.000 description 1
- WDJUZGPOPHTGOT-XUDUSOBPSA-N digitoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)CC5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O WDJUZGPOPHTGOT-XUDUSOBPSA-N 0.000 description 1
- 229960000648 digitoxin Drugs 0.000 description 1
- LTMHDMANZUZIPE-PUGKRICDSA-N digoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)[C@H](O)C5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O LTMHDMANZUZIPE-PUGKRICDSA-N 0.000 description 1
- 229960005156 digoxin Drugs 0.000 description 1
- LTMHDMANZUZIPE-UHFFFAOYSA-N digoxine Natural products C1C(O)C(O)C(C)OC1OC1C(C)OC(OC2C(OC(OC3CC4C(C5C(C6(CCC(C6(C)C(O)C5)C=5COC(=O)C=5)O)CC4)(C)CC3)CC2O)C)CC1O LTMHDMANZUZIPE-UHFFFAOYSA-N 0.000 description 1
- XYYVYLMBEZUESM-UHFFFAOYSA-N dihydrocodeine Natural products C1C(N(CCC234)C)C2C=CC(=O)C3OC2=C4C1=CC=C2OC XYYVYLMBEZUESM-UHFFFAOYSA-N 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003256 environmental substance Substances 0.000 description 1
- 229930182833 estradiol Natural products 0.000 description 1
- 229960005309 estradiol Drugs 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 210000003722 extracellular fluid Anatomy 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 229960002428 fentanyl Drugs 0.000 description 1
- IVLVTNPOHDFFCJ-UHFFFAOYSA-N fentanyl citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 IVLVTNPOHDFFCJ-UHFFFAOYSA-N 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- 235000010417 guar gum Nutrition 0.000 description 1
- 229960002154 guar gum Drugs 0.000 description 1
- 210000004209 hair Anatomy 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 210000004251 human milk Anatomy 0.000 description 1
- 235000020256 human milk Nutrition 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- LLPOLZWFYMWNKH-CMKMFDCUSA-N hydrocodone Chemical compound C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC LLPOLZWFYMWNKH-CMKMFDCUSA-N 0.000 description 1
- 229960000240 hydrocodone Drugs 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- WVLOADHCBXTIJK-YNHQPCIGSA-N hydromorphone Chemical compound O([C@H]1C(CC[C@H]23)=O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O WVLOADHCBXTIJK-YNHQPCIGSA-N 0.000 description 1
- 229960001410 hydromorphone Drugs 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- YWXYYJSYQOXTPL-SLPGGIOYSA-N isosorbide mononitrate Chemical compound [O-][N+](=O)O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 YWXYYJSYQOXTPL-SLPGGIOYSA-N 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 125000005647 linker group Chemical group 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000000891 luminescent agent Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000004880 lymph fluid Anatomy 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000006249 magnetic particle Substances 0.000 description 1
- 230000005389 magnetism Effects 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 230000002175 menstrual effect Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 229960005181 morphine Drugs 0.000 description 1
- 210000003097 mucus Anatomy 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 239000002667 nucleating agent Substances 0.000 description 1
- 229940127240 opiate Drugs 0.000 description 1
- 230000005693 optoelectronics Effects 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 229960002085 oxycodone Drugs 0.000 description 1
- 229960005489 paracetamol Drugs 0.000 description 1
- 229960001412 pentobarbital Drugs 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 229960002695 phenobarbital Drugs 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 210000004910 pleural fluid Anatomy 0.000 description 1
- 238000012123 point-of-care testing Methods 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 150000004804 polysaccharides Chemical class 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 229930010796 primary metabolite Natural products 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 239000000186 progesterone Substances 0.000 description 1
- 229960003387 progesterone Drugs 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 210000004908 prostatic fluid Anatomy 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- LOUPRKONTZGTKE-LHHVKLHASA-N quinidine Chemical compound C([C@H]([C@H](C1)C=C)C2)C[N@@]1[C@H]2[C@@H](O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-LHHVKLHASA-N 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000008672 reprogramming Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 229960002477 riboflavin Drugs 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 210000002374 sebum Anatomy 0.000 description 1
- 229960002060 secobarbital Drugs 0.000 description 1
- KQPKPCNLIDLUMF-UHFFFAOYSA-N secobarbital Chemical compound CCCC(C)C1(CC=C)C(=O)NC(=O)NC1=O KQPKPCNLIDLUMF-UHFFFAOYSA-N 0.000 description 1
- 229930000044 secondary metabolite Natural products 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 210000000582 semen Anatomy 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 210000001179 synovial fluid Anatomy 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 210000001138 tear Anatomy 0.000 description 1
- 229910052714 tellurium Inorganic materials 0.000 description 1
- PORWMNRCUJJQNO-UHFFFAOYSA-N tellurium atom Chemical compound [Te] PORWMNRCUJJQNO-UHFFFAOYSA-N 0.000 description 1
- 229960003604 testosterone Drugs 0.000 description 1
- 229960000278 theophylline Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- LLPOLZWFYMWNKH-UHFFFAOYSA-N trans-dihydrocodeinone Natural products C1C(N(CCC234)C)C2CCC(=O)C3OC2=C4C1=CC=C2OC LLPOLZWFYMWNKH-UHFFFAOYSA-N 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 239000013026 undiluted sample Substances 0.000 description 1
- MSRILKIQRXUYCT-UHFFFAOYSA-M valproate semisodium Chemical compound [Na+].CCCC(C(O)=O)CCC.CCCC(C([O-])=O)CCC MSRILKIQRXUYCT-UHFFFAOYSA-M 0.000 description 1
- 229960000604 valproic acid Drugs 0.000 description 1
- MYPYJXKWCTUITO-LYRMYLQWSA-N vancomycin Chemical compound O([C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC1=C2C=C3C=C1OC1=CC=C(C=C1Cl)[C@@H](O)[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@H]3C(=O)N[C@H]1C(=O)N[C@H](C(N[C@@H](C3=CC(O)=CC(O)=C3C=3C(O)=CC=C1C=3)C(O)=O)=O)[C@H](O)C1=CC=C(C(=C1)Cl)O2)=O)NC(=O)[C@@H](CC(C)C)NC)[C@H]1C[C@](C)(N)[C@H](O)[C@H](C)O1 MYPYJXKWCTUITO-LYRMYLQWSA-N 0.000 description 1
- MYPYJXKWCTUITO-UHFFFAOYSA-N vancomycin Natural products O1C(C(=C2)Cl)=CC=C2C(O)C(C(NC(C2=CC(O)=CC(O)=C2C=2C(O)=CC=C3C=2)C(O)=O)=O)NC(=O)C3NC(=O)C2NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(CC(C)C)NC)C(O)C(C=C3Cl)=CC=C3OC3=CC2=CC1=C3OC1OC(CO)C(O)C(O)C1OC1CC(C)(N)C(O)C(C)O1 MYPYJXKWCTUITO-UHFFFAOYSA-N 0.000 description 1
- 229960003165 vancomycin Drugs 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011716 vitamin B2 Substances 0.000 description 1
- 235000019164 vitamin B2 Nutrition 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54386—Analytical elements
- G01N33/54387—Immunochromatographic test strips
- G01N33/54388—Immunochromatographic test strips based on lateral flow
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/84—Systems specially adapted for particular applications
- G01N21/8483—Investigating reagent band
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/4875—Details of handling test elements, e.g. dispensing or storage, not specific to a particular test method
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54393—Improving reaction conditions or stability, e.g. by coating or irradiation of surface, by reduction of non-specific binding, by promotion of specific binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/558—Immunoassay; Biospecific binding assay; Materials therefor using diffusion or migration of antigen or antibody
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/46—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans from vertebrates
- G01N2333/47—Assays involving proteins of known structure or function as defined in the subgroups
- G01N2333/4701—Details
- G01N2333/4737—C-reactive protein
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/52—Assays involving cytokines
- G01N2333/521—Chemokines
- G01N2333/522—Alpha-chemokines, e.g. NAP-2, ENA-78, GRO-alpha/MGSA/NAP-3, GRO-beta/MIP-2alpha, GRO-gamma/MIP-2beta, IP-10, GCP-2, MIG, PBSF, PF-4 or KC
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70575—NGF/TNF-superfamily, e.g. CD70, CD95L, CD153 or CD154
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Biochemistry (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Optics & Photonics (AREA)
- Biophysics (AREA)
- Peptides Or Proteins (AREA)
- Automatic Analysis And Handling Materials Therefor (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
Abstract
Description
本出願は、2018年1月27日出願の米国仮出願第62/622,877号の利益を主張し、その全体が参照により本明細書に組み込まれる。
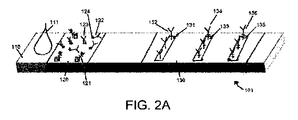
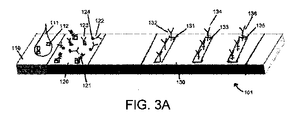
本明細書に記載のラテラルフローアッセイ、試験システム、及び方法は、多重サンドイッチ型ラテラルフローアッセイのこれら及び他の欠点に対処する。図1A−図6Bは、複数の対象分析物の量を正確に測定することができる例示的なラテラルフローアッセイを示し、単一試料中に1つ以上の対象分析物が高濃度で存在し、1つ以上の対象分析物が低濃度で存在する場合を示す。図7A−図7Cは、本明細書に記載のラテラルフローアッセイから測定された光シグナルをグラフで示す例示的な用量応答曲線を提供し、具体的には、捕捉ゾーンで検出された光シグナルの大きさ(y軸に沿って測定される)と、アッセイに適用された試料中の分析物の濃度(x軸に沿って測定される)との間の関係を提供する。本開示によるアッセイは、光シグナルを生成する反射型標識の文脈で説明されるが、本開示によるアッセイは、蛍光シグナル、磁気シグナル、又は任意の他の検出可能なシグナルを生成するように構成された任意の適切な材料の標識を含み得ることが理解されよう。
高濃度と低濃度の両方で蛋白質を定量するためのラテラルフローアッセイの準備
以下の例は、本明細書に記載されるように、複数の対象分析物を定量するためのラテラルフローアッセイの準備を記載する。この非限定的な例において、対象となる分析物は、単一試料中のタンパク質:C反応性タンパク質(CRP)、インターフェロンγ誘導タンパク質10(IP-10)、及びTNF関連アポトーシス誘導リガンド(TRAIL)である。この非限定的な例では、CRPは血清試料中に高められた又は高い濃度で存在し、一方IP-10又はTRAILは血清試料中に低濃度で存在する。
単一マルチプレックスラテラルフローアッセイを用いたCRP、IP−10、又はTRAILの定量
IP−10及びTRAILと比較してCRPの濃度は大幅に変化するため、サンドイッチ型ラテラルフローアッセイは、CRPが高濃度で存在する場合にCRPを定量すると共に、IP−10及びTRAILが(低濃度又は高濃度で)存在する場合にIP−10及びTRAILの濃度を同時に定量するのには一般的に不適当である。典型的な体積の試料中にいかなる濃度で存在する場合でも、IP−10及びTRAILは、1−999pg/mLのオーダーで存在するが、対照的に、CRPは、同じ典型的な体積の試料中に存在する場合、1−999μg/mLのオーダーの濃度で存在する。CRPの上昇した濃度を測定するには、以前は試料の連続希釈を必要としていたため、非効率的かつ面倒なプロセスとなり、また、既に低濃度になっているIP−10及びTRAILの濃度を検出不可能な濃度まで低下させてしまっていた。しかしながら、本明細書に記載されているラテラルフロー装置、試験システム、及び方法を用いて、高濃度のCRP及び大幅に低濃度のIP−10及びTRAIL(例えばCRPの100万分の1の濃度)を、正確に、信頼性よく、かつ迅速に定量することができる。
表1:CRP、IP−10及びTRAILのラテラルフローアッセイ
単一マルチプレックスラテラルフローアッセイを用いたCRP、IP−10、及びTRAILの同時定量
実施例2は、血清試料中のCRP、IP−10、又はTRAILを同時に検出するための単一のマルチプレックスラテラルフローアッセイを示す。この実施例は、さらに、血清試料中のCRP、IP−10、及びTRAILのいずれか1つ以上の組み合わせの存在を検出するための単一のラテラルフローアッセイを示す。
表2:CRP、IP−10、及びTRAILの組み合わせを試験するためのラテラルフローアッセイ
本明細書で提供されるいくつかの実施形態は、医学的状態を診断するためにラテラルフローアッセイを使用する方法に関する。いくつかの態様において、本方法は、本明細書に記載されるようなラテラルフローアッセイを提供することを含む。いくつかの態様において、本方法は、ラテラルフローアッセイの試料リザーバにおいて試料を受け取ることを含む。
本開示によるラテラルフロー装置、試験システム、及び方法は、1つ以上の対象分析物が試料中に高濃度または高濃度で存在し、1つ以上の対象分析物が試料中に低濃度で存在する状況において、複数の対象分析物の存在又は量を正確に決定する。有利には、本明細書に記載されるラテラルフロー装置、試験システム、及び方法は、単一試験事象において単一試料を単一テストストリップなどの単一のラテラルフローアッセイに適用した後に、大幅に異なる濃度で単一試料中に存在する対象分析物の存在又は量を決定する。したがって、本明細書に記載されるラテラルフローアッセイは、分析物が大幅に異なる濃度範囲で存在する場合であっても、単一試料において複数の分析物を同時に検出することができる。試料中に高濃度で存在する1以上の対象分析物の存在又は量を決定する例示的なラテラルフロー装置、試験システム、及び方法は、図1A−図6Bに示した非限定的な実施形態を参照して上述した。さらなる例示的な実施形態は、2018年6月25日に出願された国際出願第PCT/US2018/039347号に記載されており、その全体が参照により本明細書に組み込まれる。
本明細書に記載のラテラルフローアッセイ試験システムは、ラテラルフローアッセイ試験装置(例えばテストストリップ)と、試験装置の全部又は一部を受け入れるように構成されたポートを含むハウジングと、光源及び光検出器を含むリーダと、データ分析器と、それらの組み合わせとを含むことができる。ハウジングは、プラスチック、金属、又は複合材料を含む様々な材料のうちの任意の1つで構成することができる。ハウジングは、診断テストシステムの構成要素のための保護筐体を形成する。ハウジングはまた、テストストリップをリーダに対して機械的に登録するレセプタクルを画定する。レセプタクルは、多種多様な異なるタイプのテストストリップのいずれかを受けるように設計されてもよい。いくつかの実施形態において、筐体は、ベンチ上、現場、家庭、又は家庭、商業、若しくは環境用の施設を含む様々な環境においてラテラルフローアッセイを実施する能力を可能にする可搬型装置である。
本明細書に記載のラテラルフロー装置は、試料リザーバ(試料受容ゾーンとも呼ばれる)を含むことができ、そこで流体試料は、例えばラテラルフロー装置に存在する免疫クロマトグラフィーテストストリップだがこれに限定されないテストストリップに導入される。一例では、試料は、スポイト又は他のアプリケータのように、外部適用によって試料リザーバに導入され得る。試料は、試料リザーバ上に注ぎ込まれ得るか、又は発現され得る。別の例では、テストストリップが試料を保持する容器内に浸漬される場合のように、試料リザーバを試料内に直接浸漬することができる。
Claims (66)
- 試料中に異なる濃度で存在する第1の対象分析物及び第2の対象分析物を検出する方法であって、
ラテラルフローアッセイを提供するステップを含み、
前記ラテラルフローアッセイは、
前記ラテラルフローアッセイの流路に結合された第1の複合体であって、標識と、前記第1の分析物に特異的に結合する抗体又はそのフラグメントと、前記第1の分析物とを含む前記第1の複合体と、
前記流路に結合され、前記第2の分析物に特異的に結合するように構成された第2の標識抗体又はそのフラグメントと、
前記第1の複合体の下流の第1の捕捉ゾーンであって、前記第1の分析物に特異的な第1の固定化捕捉剤を含む、前記第1の捕捉ゾーンと、
前記第2の標識抗体又はそのフラグメントの下流にある第2の捕捉ゾーンであって、前記第2の分析物に特異的な第2の固定化捕捉剤を含む前記第2の捕捉ゾーンと、を有し、
前記方法は、さらに、
前記第1の複合体及び前記第2の標識抗体又はそのフラグメントに前記試料を適用するステップと、
前記第2の標識抗体又はそのフラグメントに前記第2の分析物を結合して第2の複合体を形成するステップと、
前記流体試料及び前記第1の複合体を前記第1の捕捉ゾーンに流すステップであって、前記流体試料中の前記第1の分析物と前記第1の複合体とは、前記第1の捕捉ゾーン内の前記第1の固定化捕捉剤に結合するために競合するステップと、
前記流路内の前記第2の複合体を前記第2の捕捉ゾーンに流し、前記第2の複合体を前記第2の捕捉ゾーン内の前記第2の固定化捕捉剤に結合させるステップと、
前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した前記第1の複合体からの第1のシグナルと、前記第2の捕捉ゾーンにおいて前記第2の固定化捕捉剤に結合した前記第2の複合体からの第2のシグナルとを検出するステップと、
を含む、方法。 - 前記第1の対象分析物が、前記試料中に存在する前記第2の対象分析物の濃度よりも約6桁大きい濃度で前記試料中に存在する、請求項1に記載の方法。
- 前記第1の対象分析物が、1から999μl/mlの間の濃度で前記試料中に存在し、第2の対象分析物が、1から999pg/mlの間の濃度で前記試料中に存在する、請求項1に記載の方法。
- 前記第1の対象分析物が、前記試料中に存在する前記第2の対象分析物の濃度よりも少なくとも1桁大きい濃度で試料中に存在し、その桁は、1桁、2桁、3桁、4桁、5桁、6桁、7桁、8桁、9桁、又は10桁を含む、請求項1に記載の方法。
- さらに、前記第1のシグナルを、前記試料中に存在する前記第1の対象分析物の濃度に相関させるステップと、前記第2のシグナルを、前記試料中の前記第2の対象分析物の濃度に相関させるステップとを含む、請求項1に記載の方法。
- 前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した前記第1の複合体から検出される前記第1のシグナルは、前記試料中の前記第1の分析物の濃度が減少するにつれて減少し、前記第2の捕捉ゾーンにおいて前記第2の固定化捕捉剤に結合した前記第2の複合体から検出される前記第2のシグナルは、前記試料中の前記第2の対象分析物の濃度が増加するにつれて増加する、請求項1に記載の方法。
- さらに、前記試料中の第3の対象分析物を検出する工程を含み、
前記ラテラルフローアッセイは、
前記流路に結合され、前記第3の分析物に特異的に結合するように構成された第3の標識抗体又はそのフラグメントと、
前記第3の標識抗体又はそのフラグメントの下流にある第3の捕捉ゾーンであって、前記第3の分析物に特異的な第3の固定化捕捉剤を含む前記第3の捕捉ゾーンと、を有する、
請求項1に記載の方法。 - 前記第3の標識抗体又はそのフラグメントへ前記試料を適用する工程と、
前記第3の標識抗体又はそのフラグメントに前記第3の分析物を結合して第3の複合体を形成する工程と、
前記流路中の前記第3の複合体を前記第3の捕捉ゾーンに流し、前記第3の複合体を前記第3の捕捉ゾーン内の前記第3の固定化捕捉剤に結合させる工程と、
前記第3の捕捉ゾーンにおいて前記第3の固定化捕捉剤に結合した前記第3の複合体からの第3のシグナルを検出する工程と、
をさらに含む、請求項7に記載の方法。 - 前記第1のシグナル、前記第2のシグナル、及び前記第3のシグナルを、それぞれ、前記試料中の前記第1の分析物の濃度、前記第2の分析物の濃度、及び前記第3の分析物の濃度に相関させる工程をさらに含む、請求項8に記載の方法。
- 前記第1の分析物、前記第2の分析物、及び前記第3の分析物のそれぞれの濃度に基づき、疾患状態、非疾患状態、又は無状態を示す工程をさらに含む、請求項9に記載の方法。
- 前記疾患状態がウイルス感染又は細菌感染であり、前記非疾患状態が炎症である、請求項10に記載の方法。
- 前記第1の対象分析物はC反応性タンパク質(CRP)を含み、前記第2の対象分析物はTNF関連アポトーシス誘導リガンド(TRAIL)を含む、請求項1に記載の方法。
- 前記第3の対象分析物は、インターフェロンγ誘導タンパク質10(IP−10)を含む、請求項7に記載の方法。
- 前記試料は、全血試料、静脈血試料、毛細血管血液試料、血清試料又は血漿試料である、請求項1に記載の方法。
- 前記試料は、前記ラテラルフローアッセイに前記試料を適用する前に希釈されない、請求項1に記載の方法。
- 流体試料中に異なる濃度で存在する第1の対象分析物及び第2の対象分析物を検出するように構成されたラテラルフローアッセイであって、
前記ラテラルフローアッセイの流路に結合され、標識と、前記第1の分析物に特異的に結合する抗体又はそのフラグメントと、前記第1の分析物とを含む、第1の複合体と、
前記流路に結合され、前記第2の分析物に特異的に結合するように構成された第2の標識抗体又はそのフラグメントと、
前記第1の複合体の下流の第1の捕捉ゾーンであって、前記第1の分析物に特異的な第1の固定化捕捉剤を含む前記第1の捕捉ゾーンと、
前記第2の標識抗体又はそのフラグメントの下流の第2の捕捉ゾーンであって、前記第2の分析物に特異的な第2の固定化捕捉剤を含む前記第2の捕捉ゾーンと、
を有するラテラルフローアッセイ。 - 前記第1の複合体及び前記第2の標識抗体又はそのフラグメントは、前記流体試料が前記第1の複合体及び前記第2の標識抗体又はそのフラグメントに適用されたときに、前記ラテラルフローアッセイの前記流路から分離される、請求項16に記載のラテラルフローアッセイ。
- 前記流体試料が前記第1の複合体及び前記第2の標識抗体又はそのフラグメントに適用されるときに、前記第2の標識抗体又はそのフラグメントが前記第2の分析物に結合して第2の複合体を形成する、請求項17に記載のラテラルフローアッセイ。
- 前記流体試料が適用された後、前記第1の捕捉ゾーン内の前記第1の固定化捕捉剤は、前記流体試料内を前記第1の捕捉ゾーンに流れた前記第1の複合体及び前記第1の分析物と競合的に結合する、請求項18に記載のラテラルフローアッセイ。
- 前記流体試料が適用された後、前記第2の捕捉ゾーン内の前記第2の固定化捕捉剤は、前記流体試料内を前記第2の捕捉ゾーンに流れた前記第2の複合体と結合する、請求項19に記載のラテラルフローアッセイ。
- 第1のシグナルは、前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した前記第1の複合体から発せられ、第2のシグナルは、前記第2の捕捉ゾーンにおいて前記第2の固定化捕捉剤に結合した前記第2の複合体から発せられる、請求項20に記載のラテラルフローアッセイ。
- 前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した前記第1の複合体から発せられる前記第1のシグナルは、前記流体試料中の前記第1の分析物の濃度が低下するにつれて低下し、前記第2の捕捉ゾーンにおいて前記第2の固定化捕捉剤に結合した前記第2の複合体から発せられる前記第2のシグナルは、前記流体試料中の前記第2の対象分析物の濃度が上昇するにつれて上昇する、請求項21に記載のラテラルフローアッセイ。
- 前記第1の対象分析物は、前記試料中に存在する前記第2の対象分析物の濃度よりも約6桁大きい濃度で前記試料中に存在する、請求項16に記載のラテラルフローアッセイ。
- 前記第1の対象分析物は1から999μl/mlの間の濃度で前記試料中に存在し、前記第2の対象分析物は1から999pg/mlの間の濃度で前記試料中に存在する、請求項16に記載のラテラルフローアッセイ。
- 前記第1の対象分析物は、前記試料中に存在する前記第2の対象分析物の濃度よりも少なくとも1桁大きい濃度で前記試料中に存在し、その桁は、1桁、2桁、3桁、4桁、5桁、6桁、7桁、8桁、9桁、又は10桁を含む、請求項16に記載のラテラルフローアッセイ。
- 前記第1の対象分析物はC反応性タンパク質(CRP)を含み、前記第2の対象分析物はTNF関連アポトーシス誘導リガンド(TRAIL)を含む、請求項16に記載のラテラルフローアッセイ。
- 前記流体試料は、全血試料、静脈血試料、毛細血管血液試料、血清試料、又は血漿試料である、請求項16に記載のラテラルフローアッセイ。
- 前記試料は、前記ラテラルフローアッセイに適用される前に希釈されない、請求項16に記載のラテラルフローアッセイ。
- 流体試料を受け入れるように構成された流路と、
前記流路に結合された試料受容ゾーンと、
前記試料受容ゾーンの下流で前記流路に結合された検出ゾーンであって、第1の捕捉ゾーン、第2の捕捉ゾーン、及び第3の捕捉ゾーンを備え、前記第1の捕捉ゾーンは、第1の対象分析物に特異的な第1の固定化捕捉剤を含み、前記第2の捕捉ゾーンは、第2の対象分析物に特異的な第2の固定化捕捉剤を含み、前記第3の捕捉ゾーンは、第3の対象分析物に特異的な第3の固定化捕捉剤を含む、前記検出ゾーンと、
第1のフェイズにおいて前記流路に結合され、第2のフェイズにおいて前記流体試料の存在下で前記流路を前記検出ゾーンへ流れるように構成された第1の複合体であって、標識と、前記第1の対象分析物に特異的に結合する第1の抗体又はそのフラグメントと、前記第1の対象分析物を含む前記第1の複合体と、
前記第2の対象分析物に特異的に結合する第2の標識抗体又はそのフラグメントであって、前記第1のフェイズにおいて前記流路に結合され、前記第2のフェイズにおいて前記流体試料の存在下で前記流路を前記検出ゾーンへ流れるように構成された前記第2の標識抗体又はそのフラグメントと、
前記第3の対象分析物に特異的に結合する第3の標識抗体又はそのフラグメントであって、前記第1のフェイズにおいて前記流路に結合され、前記第2のフェイズにおいて前記流体試料の存在下で前記流路を前記検出ゾーンへ流れるように構成された前記第3の標識抗体又はそのフラグメントと、
を有するアッセイテストストリップ。 - 前記流路は、標識されていない前記第1の対象分析物を含む前記流体試料を受け入れるように構成され、前記第1の固定化捕捉剤は、前記流体試料中の前記第1の複合体及び前記標識されていない前記第1の対象分析物と競合的に結合するように構成される、請求項29に記載のアッセイテストストリップ。
- 前記流体試料は、さらに、前記流体試料中の標識されていない前記第1の分析物の濃度より6桁低い濃度で、標識されていない第2の分析物を含む、請求項30に記載のアッセイテストストリップ。
- 前記流体試料は、さらに、前記流体試料中の標識されていない前記第1の分析物の濃度より6桁低い濃度で、標識されていない第3の分析物を含む、請求項30に記載のアッセイテストストリップ。
- 前記第1の複合体は、前記第1の捕捉ゾーンに流れ、第3のフェイズにおいて前記第1の固定化捕捉剤と結合し、前記第2の対象分析物に結合した前記第2の標識抗体又はそのフラグメントは、前記第2の捕捉ゾーンに流れ、前記第3のフェイズにおいて前記第2の固定化捕捉剤と結合する、請求項29に記載のアッセイテストストリップ。
- 前記第1の複合体は、前記第3のフェイズにおいて前記第1の捕捉ゾーンから第1のシグナルを発し、前記第2の対象分析物に結合した前記第2の標識抗体又はそのフラグメントは、前記第3のフェイズにおいて前記第2の捕捉ゾーンから第2のシグナルを発する、請求項33に記載のアッセイテストストリップ。
- 前記流路は、標識されていない第1の対象分析物を含む流体試料を受け入れるように構成され、前記試料中の前記標識されていない第1の対象分析物の濃度が前記流体試料中で増加するにつれて、前記第1の捕捉ゾーンから発せられる前記第1のシグナルは減少する、請求項34に記載のアッセイテストストリップ。
- 前記流体試料は、標識されていない第2の対象分析物をさらに含み、前記流体試料中の前記標識されていない第2の対象分析物の濃度が増加するにつれて、前記第2の捕捉ゾーンから発せられる前記第2のシグナルは増加する、請求項35に記載のアッセイテストストリップ。
- 前記流路は、標識されていない第1の対象分析物を含む流体試料を受け入れるように構成され、前記第1の複合体は、前記第1のフェイズ又は前記第2のフェイズにおいて、前記標識されていない第1の対象分析物に特異的に結合しない、請求項29に記載のアッセイテストストリップ。
- 前記第1の複合体は、前記第2のフェイズにおいて前記標識されていない第1の対象分析物と共に前記流路を前記第1の捕捉ゾーンへ流れるように構成される、請求項37に記載のアッセイテストストリップ。
- 前記第1の複合体は、第3のフェイズにおいて前記第1の捕捉ゾーンで前記第1の固定化捕捉剤に結合するために前記標識されていない第1の対象分析物と競合するように構成される、請求項38に記載のアッセイテストストリップ。
- 前記流体試料中の標識されていない第1の対象分析物の濃度が増加するにつれて、前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した第1の複合体から発せられる第1の光シグナルは減少する、請求項39に記載のアッセイテストストリップ。
- 前記流路は、第1の対象分析物を含む又は含まない流体試料を受け入れるように構成され、前記流体試料が第1の対象分析物を含まない場合、前記第1の複合体は、前記第2のフェイズにおいて前記第1の捕捉ゾーンで前記第1の固定化捕捉剤の全て又は実質的に全てに特異的に結合する、請求項29に記載のアッセイテストストリップ。
- 前記流体試料が第1の対象分析物を含まない場合、前記第1の捕捉ゾーンに結合された前記第1の複合体から発せられる第1の光シグナルは、前記アッセイテストストリップの前記第1の捕捉ゾーンから発せられ得る最大の光シグナルである、請求項41に記載のアッセイテストストリップ。
- 前記流体試料が第1の対象分析物を含む場合、前記第1の捕捉ゾーンに結合された前記第1の複合体から発せられる第1の光シグナルは、前記最大の光シグナルよりも小さい、請求項42に記載のアッセイテストストリップ。
- 前記第1の固定化捕捉剤は、前記第1の対象分析物に特異的に結合する抗体又は抗体のフラグメントを含む、請求項29に記載のアッセイテストストリップ。
- 前記第1の複合体は、第1のフェイズにおいて前記アッセイテストストリップの表面上に結合される、請求項29に記載のアッセイテストストリップ。
- 前記第1の複合体を含む溶液を前記アッセイテストストリップの表面に噴霧し、当該溶液を乾燥することにより、前記第1の複合体が前記アッセイテストストリップの表面に結合される、請求項29に記載のアッセイテストストリップ。
- 前記流体試料は、血液、血漿、尿、汗、及び唾液試料からなる群より選択される、請求項29に記載のアッセイテストストリップ。
- 前記流体試料は、全血、静脈血、毛細血管血、血漿及び血清からなる群より選択される、請求項29に記載のアッセイテストストリップ。
- 前記第1の対象分析物はC反応性タンパク質(CRP)を含み、前記第1の複合体はCRPに結合した抗CRP抗体又はそのフラグメントを含み、前記第2の対象分析物はTNF関連アポトーシス誘導リガンド(TRAIL)を含み、前記第3の対象分析物はインターフェロンγ誘導タンパク質10(IP-10)を含む、請求項29に記載のアッセイテストストリップ。
- 請求項29に記載のアッセイテストストリップと、
光源と検出器とを備えるリーダと、
データ分析器と、
を有する診断テストシステム。 - 前記リーダが前記アッセイテストストリップの前記第1の捕捉ゾーンから第1の光シグナルを検出し、その光シグナルが、前記テストストリップの前記第1の捕捉ゾーンについての用量応答曲線の最大光シグナルである場合、前記データ分析器は、前記流体試料中に第1の対象分析物がないという表示を出力する、請求項50に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第1の捕捉ゾーンからの光シグナルを検出し、その光シグナルが前記最大光シグナルから1%の範囲内である場合、前記データ分析器は、前記流体試料中の第1の対象分析物の濃度が低いことを示す表示を出力する、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第1の捕捉ゾーンからの光シグナルを検出し、その光シグナルが前記最大光シグナルから5%の範囲内である場合、前記データ分析器は、前記流体試料中の第1の対象分析物の濃度が低いことを示す表示を出力する、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第1の捕捉ゾーンからの光シグナルを検出し、その光シグナルが前記最大光シグナルから10%の範囲内である場合、前記データ分析器は、前記流体試料中の第1の対象分析物の濃度が低いことを示す表示を出力する、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第1の捕捉ゾーンからの光シグナルを検出し、その光シグナルが前記最大光シグナルの90%以下である場合、前記データ分析器は、前記流体試料中に高濃度の第1の分析物が存在するという表示を出力する、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第1の捕捉ゾーンからの光シグナルを検出し、その光シグナルが前記最大光シグナル未満である場合、前記データ分析器は、前記流体試料中の第1の対象分析物の濃度の表示を出力する、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第2の捕捉ゾーンから第2の光シグナルを検出した場合、前記データ分析器は、前記流体試料中の第2の対象分析物の濃度の表示を出力し、前記流体試料中の第2の対象分析物の前記表示された濃度は、前記流体試料中の前記第1の対象分析物の前記表示された濃度より6桁低い、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第3の捕捉ゾーンから第3の光シグナルを検出した場合、前記データ分析器は、前記流体試料中の第3の対象分析物の濃度の表示を出力し、前記流体試料中の第3の対象分析物の前記表示された濃度は、前記流体試料中の前記第1の対象分析物の前記表示された濃度より6桁低い、請求項51に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第2の捕捉ゾーンからの第2の光シグナルを検出しない場合、前記データ分析器は、前記流体試料中に第2の対象分析物がないという表示を出力する、請求項50に記載の診断テストシステム。
- 前記リーダが、前記アッセイテストストリップの前記第3の捕捉ゾーンからの第3の光シグナルを検出しない場合、前記データ分析器は、前記流体試料中に第3の対象分析物がないという表示を出力する、請求項50に記載の診断テストシステム。
- 流体試料中の複数の対象分析物の各々の存在又は濃度を決定する方法であって、
前記第1のフェイズにおいて、前記第1の複合体、前記第2の標識抗体又はそのフラグメント、及び前記第3の標識抗体又はそのフラグメントがそれぞれ前記流路に結合されている場合に、請求項29に記載のアッセイテストストリップに前記流体試料を適用する工程と、
前記第2の分析物が前記流体試料中に存在する場合、前記第2の分析物を前記第2の標識抗体又はそのフラグメントに結合し、それにより第2の複合体を形成する工程と、
前記第3の分析物が前記流体試料中に存在する場合、前記第3の分析物を前記第3の標識抗体又はそのフラグメントに結合し、それにより第3の複合体を形成する工程と、
前記第1の複合体と、前記第2の複合体が形成された場合には当該第2の複合体と、前記第3の複合体が形成された場合には当該第3の複合体とを、前記流路から分離する工程と、
前記第2のフェイズにおいて前記流体試料を前記検出ゾーンへ流す工程と、
前記第1の捕捉ゾーンにおける前記第1の固定化捕捉剤に、前記第1の複合体を結合し、前記第2の複合体が形成された場合には、前記第2の捕捉ゾーンにおける前記第2の固定化捕捉剤に前記第2の複合体を結合し、前記第3の複合体が形成された場合には、前記第3の捕捉ゾーンにおける前記第3の固定化捕捉剤に前記第3の複合体を結合する工程と、
前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した前記第1の複合体からの第1のシグナルを検出する工程と、
前記第2の複合体が形成される場合、前記第2の捕捉ゾーンにおいて前記第2の固定化捕捉剤に結合された前記第2の複合体からの第2のシグナルを検出する工程と、
前記第3の複合体が形成される場合、前記第3の捕捉ゾーンにおいて前記第3の固定化捕捉剤に結合された前記第3の複合体からの第3のシグナルを検出する工程と、
を有する方法。 - 前記第1の対象分析物は、前記流体試料中に存在する前記第2の対象分析物の濃度よりも約6桁大きい濃度で前記流体試料中に存在する、請求項61に記載の方法。
- 前記第1の対象分析物は、1から999μl/mlの間の濃度で前記流体試料中に存在し、前記第2の対象分析物は、1から999pg/mlの間の濃度で前記流体試料中に存在する、請求項61に記載の方法。
- 前記第1の対象分析物が、前記流体試料中に存在する前記第2の対象分析物の濃度よりも少なくとも1桁大きい濃度で前記流体試料中に存在し、その桁は、1桁、2桁、3桁、4桁、5桁、6桁、7桁、8桁、9桁、又は10桁を含む、請求項61に記載の方法。
- さらに、前記第1のシグナルを、前記試料中に存在する前記第1の対象分析物の濃度に相関させる工程と、前記第2のシグナルを、前記試料中の前記第2の対象分析物の濃度に相関させる工程とを含む、請求項61に記載の方法。
- 前記第1の捕捉ゾーンにおいて前記第1の固定化捕捉剤に結合した前記第1の複合体から検出される前記第1のシグナルは、前記試料中の前記第1の分析物の濃度が低下するにつれて低下し、前記第2の捕捉ゾーンにおいて前記第2の固定化捕捉剤に結合した前記第2の複合体から検出される前記第2のシグナルは、前記試料中の前記第2の対象分析物の濃度が上昇するにつれて上昇する、請求項61に記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024019231A JP2024057619A (ja) | 2018-01-27 | 2024-02-13 | ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862622877P | 2018-01-27 | 2018-01-27 | |
| US62/622,877 | 2018-01-27 | ||
| PCT/US2019/015005 WO2019147850A1 (en) | 2018-01-27 | 2019-01-24 | Multiplex lateral flow assay for differentiating bacterial infections from viral infections |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024019231A Division JP2024057619A (ja) | 2018-01-27 | 2024-02-13 | ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021511524A true JP2021511524A (ja) | 2021-05-06 |
| JPWO2019147850A5 JPWO2019147850A5 (ja) | 2022-02-21 |
Family
ID=67396274
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020561597A Pending JP2021511524A (ja) | 2018-01-27 | 2019-01-24 | ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ |
| JP2024019231A Pending JP2024057619A (ja) | 2018-01-27 | 2024-02-13 | ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024019231A Pending JP2024057619A (ja) | 2018-01-27 | 2024-02-13 | ウイルス感染と細菌感染を区別するためのマルチプレックスラテラルフローアッセイ |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20200348296A1 (ja) |
| EP (1) | EP3743719A4 (ja) |
| JP (2) | JP2021511524A (ja) |
| CN (2) | CN111801575B (ja) |
| AU (1) | AU2019212375A1 (ja) |
| CA (1) | CA3088124A1 (ja) |
| WO (1) | WO2019147850A1 (ja) |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070243630A1 (en) * | 1997-03-06 | 2007-10-18 | Quidel Corporation | Quantitative lateral flow assays and devices |
| JP2008539424A (ja) * | 2005-04-29 | 2008-11-13 | キンバリー クラーク ワールドワイド インコーポレイテッド | フック効果領域内の検出機能を有するアッセイ装置 |
| JP2011209140A (ja) * | 2010-03-30 | 2011-10-20 | Sekisui Medical Co Ltd | ヒトc反応性タンパク質(crp)測定用イムノクロマト試薬 |
| WO2014070686A1 (en) * | 2012-10-29 | 2014-05-08 | Sri International | Lateral flow assay utilizing infrared dye for multiplex detection |
| JP2016500154A (ja) * | 2012-11-15 | 2016-01-07 | オーソ・クリニカル・ダイアグノスティックス・インコーポレーテッド | 反応時間を使用してアッセイを較正すること |
| JP2016520827A (ja) * | 2013-05-03 | 2016-07-14 | ザリオン ゲーエムベーハー | 移植拒絶反応、神経変性疾患又はうつ病と特に関連する潜在的炎症のインビトロ早期検出方法 |
| WO2017221255A1 (en) * | 2016-06-23 | 2017-12-28 | Memed Diagnostics Ltd. | Measuring trail by lateral flow immunoassay |
| JP2020526742A (ja) * | 2017-06-28 | 2020-08-31 | ベクトン・ディキンソン・アンド・カンパニーBecton, Dickinson And Company | 高濃度の分析物等、分析物を測定するための用量反応曲線の減少信号部分を使用したサンドイッチ型アッセイ |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7239394B2 (en) * | 2003-06-04 | 2007-07-03 | Inverness Medical Switzerland Gmbh | Early determination of assay results |
| US7632687B2 (en) * | 2004-03-23 | 2009-12-15 | Quidel Corporation | Hybrid phase lateral flow assay |
| US20070224701A1 (en) * | 2006-02-16 | 2007-09-27 | Becton, Dickinson And Company | Combination vertical and lateral flow immunoassay device |
| US20130196310A1 (en) * | 2008-05-20 | 2013-08-01 | Rapid Pathogen Screening, Inc. | Method and Device for Combined Detection of Viral and Bacterial Infections |
| CN103052883B (zh) * | 2010-07-15 | 2015-05-20 | 比勒陀利亚大学 | 检测血清样品中替代性标记的方法 |
| EP2780705B1 (en) * | 2011-11-16 | 2018-09-19 | Becton, Dickinson and Company | Methods and systems for detecting an analyte in a sample |
| CA3133249C (en) * | 2012-02-09 | 2023-07-25 | Memed Diagnostics Ltd. | Signatures and determinants for diagnosing infections and methods of use thereof |
| CN105051542A (zh) * | 2012-10-31 | 2015-11-11 | 阿斯图德医疗有限公司 | 定量的侧向流测定法 |
| US20160291010A1 (en) * | 2013-11-12 | 2016-10-06 | Gwangju Institute Of Science And Technology | Immunochromatography strip sensor capable of measuring biomaterial concentration over broad concentration range |
-
2019
- 2019-01-24 AU AU2019212375A patent/AU2019212375A1/en active Pending
- 2019-01-24 WO PCT/US2019/015005 patent/WO2019147850A1/en active Application Filing
- 2019-01-24 JP JP2020561597A patent/JP2021511524A/ja active Pending
- 2019-01-24 CA CA3088124A patent/CA3088124A1/en active Pending
- 2019-01-24 CN CN201980015174.6A patent/CN111801575B/zh active Active
- 2019-01-24 CN CN202311832413.1A patent/CN117783514A/zh active Pending
- 2019-01-24 EP EP19743341.0A patent/EP3743719A4/en active Pending
-
2020
- 2020-07-17 US US16/932,533 patent/US20200348296A1/en active Pending
-
2024
- 2024-02-13 JP JP2024019231A patent/JP2024057619A/ja active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070243630A1 (en) * | 1997-03-06 | 2007-10-18 | Quidel Corporation | Quantitative lateral flow assays and devices |
| JP2008539424A (ja) * | 2005-04-29 | 2008-11-13 | キンバリー クラーク ワールドワイド インコーポレイテッド | フック効果領域内の検出機能を有するアッセイ装置 |
| JP2011209140A (ja) * | 2010-03-30 | 2011-10-20 | Sekisui Medical Co Ltd | ヒトc反応性タンパク質(crp)測定用イムノクロマト試薬 |
| WO2014070686A1 (en) * | 2012-10-29 | 2014-05-08 | Sri International | Lateral flow assay utilizing infrared dye for multiplex detection |
| JP2016500154A (ja) * | 2012-11-15 | 2016-01-07 | オーソ・クリニカル・ダイアグノスティックス・インコーポレーテッド | 反応時間を使用してアッセイを較正すること |
| JP2016520827A (ja) * | 2013-05-03 | 2016-07-14 | ザリオン ゲーエムベーハー | 移植拒絶反応、神経変性疾患又はうつ病と特に関連する潜在的炎症のインビトロ早期検出方法 |
| WO2017221255A1 (en) * | 2016-06-23 | 2017-12-28 | Memed Diagnostics Ltd. | Measuring trail by lateral flow immunoassay |
| JP2020526742A (ja) * | 2017-06-28 | 2020-08-31 | ベクトン・ディキンソン・アンド・カンパニーBecton, Dickinson And Company | 高濃度の分析物等、分析物を測定するための用量反応曲線の減少信号部分を使用したサンドイッチ型アッセイ |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2019212375A1 (en) | 2020-07-30 |
| CN117783514A (zh) | 2024-03-29 |
| CN111801575B (zh) | 2024-01-12 |
| WO2019147850A1 (en) | 2019-08-01 |
| EP3743719A1 (en) | 2020-12-02 |
| CA3088124A1 (en) | 2019-08-01 |
| US20200348296A1 (en) | 2020-11-05 |
| JP2024057619A (ja) | 2024-04-24 |
| CN111801575A (zh) | 2020-10-20 |
| EP3743719A4 (en) | 2021-11-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7451431B2 (ja) | 側方流動アッセイのシグナルを増幅させるシステム、装置および方法 | |
| CN111033237B (zh) | 使用剂量响应曲线的递减信号部分来测量包括高浓度分析物在内的分析物的夹心式测定 | |
| US20200292542A1 (en) | Lateral flow assay and methods for detecting high concentration analytes | |
| CN111801575B (zh) | 区分细菌感染和病毒感染的多重横向流测定物 | |
| CN111936852B (zh) | 区分细菌感染和病毒感染的多重横向流测定物 | |
| JP2023501164A (ja) | 生体サンプルの定量化のための側方流動アッセイシステム及び方法 | |
| JP2024074809A (ja) | 側方流動アッセイのシグナルを増幅させるシステム、装置および方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220124 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220124 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220210 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20221227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230104 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230403 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230525 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230703 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20231012 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240213 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20240415 |