[0010] リードの抜去は、概ね非常に安全な処置である。ただし、どんな侵襲的な処置とも同様に、潜在的なリスクがある。例えば、上記で論じたツールのいずれかを使用してリードを除去する間に、ツールがそれを通って移動している静脈又は動脈を過って突き刺すか、切断するか、又は穿孔する場合があり、それにより患者の血管系から血液が漏れ出るのを可能にする。患者の心臓の近くに過って開口が作られると、血液が漏れ出る速度が速くなる可能性がある。したがって、臨床医は、患者から漏れ出る血液の量を減らすために、状況に迅速に対処し、それによって可能性のある患者への長期的傷害を最小限に抑える必要がある。
[0011] これら及び他に必要なものは、本開示の様々な態様、実施形態、及び構成によって対処される。いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトを備える。第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも一方を受容するよう適合され、第2のルーメンは、膨張流体を受容するよう適合される。第2のルーメンは、カテーテルシャフトの長さに沿った位置で、0.65mm2から1.90mm2の間の断面積を有する。デバイスは、カテーテルシャフトによって保持される膨張可能なバルーンをさらに備える。膨張可能なバルーンは、第2のルーメンから膨張流体を受容するよう適合されている。膨張可能なバルーンは、約65mmから約80mmの作動長さ、及び約20mmから約25mmの膨張した直径を有する。デバイスは、三日月状の形状を有する第2のルーメン内の断面積も有し、第2のルーメンの断面積は約1mm2であり、三日月状の断面形状の半径は、約1mmなど、およそ0.50mmから1.50mmの間の半径を有する。
[0012] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、血流損失の速度を下げて、穿孔の外科的修復を計画して開始するためのより多くの時間を与える、止血組成物でコーティングされた膨張可能なバルーンを備える。止血組成物は、1種又は複数種類の止血血液凝固剤、並びに1種又は複数種類のアジュバント及び/又は賦形剤を含むことができる。
[0013] デバイスの一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0014] 一実施形態では、膨張可能なバルーンは、近位テーパ部分、遠位テーパ部分、並びに近位テーパ部分と遠位テーパ部分との間に配置された作動部分を含み、作動部分は、約20mmから約25mmの膨張した直径を有する。
[0015] 一実施形態では、第1のルーメン及び第2のルーメンは、カテーテルシャフト内に非同心状に配置される。
[0016] 一実施形態では、デバイスは、カテーテルシャフトで保持される少なくとも1つのX線造影マーカをさらに備える。
[0017] 一実施形態では、少なくとも1つのX線造影マーカは、カテーテルシャフトの周囲に延在するバンドを備える。
[0018] 一実施形態では、少なくとも1つのX線造影マーカは、少なくとも第1のX線造影マーカ及び第2のX線造影マーカを備える。
[0019] 一実施形態では、少なくとも1つのX線造影マーカは、少なくとも第3のX線造影マーカをさらに備える。
[0020] 一実施形態では、止血組成物には、血液凝固及び創傷治癒を促進するフィブリンベースの凝固剤(例えば、フィブリン密封材)が含まれる。
[0021] 一実施形態では、止血組成物には、血液凝固及び創傷治癒を促進する1種又は複数種類の凝固剤、及びバルーンを穿孔に隣接して配置する間の止血組成物の早すぎる損失を防ぐコーティング剤が含まれる。
[0022] 一実施形態では、膨張可能なバルーンは、近位部分、遠位部分、及び近位部分と遠位部分との間に配置された中間部分を備え、ここで第1、第2、及び第3のX線造影マーカは膨張可能なバルーン内に保持され、第1のX線造影マーカは近位部分と軸方向に位置合せされ、第2のX線造影マーカは中間部分と軸方向に位置合せされ、第3のX線造影マーカは遠位部分と軸方向に位置合せされる。
[0023] 一実施形態では、膨張可能なバルーンは、近位首部、近位テーパ部分、作動部分、遠位テーパ部分、及び遠位首部を備え、ここで第1、第2、及び第3のX線造影マーカは、膨張可能なバルーン内に保持され、第1のX線造影マーカは、近位首部と近位テーパ部分との交切部と軸方向に位置合せされ、第2のX線造影マーカは、近位テーパ部分と作動部分との交切部と軸方向に位置合せされ、第3のX線造影マーカは、作動部分と遠位テーパ部分との交切部と軸方向に位置合せされる。
[0024] 一実施形態では、デバイスは、膨張可能なバルーンの第1の端部から第2の端部へ容易に血液を通過させるよう適合されている第3のルーメンをさらに有する。
[0025] 一実施形態では、カテーテルシャフトは第3のルーメンを有する。
[0026] 一実施形態では、デバイスは、膨張可能なバルーンによって着脱可能に保持された閉塞パッチをさらに備え、閉塞パッチは、穿孔を閉塞するために膨張可能なバルーンから展開可能である。
[0027] 一実施形態では、閉塞パッチは、血管内で閉塞パッチの位置を維持するよう適合された少なくとも1種の接着剤を含む。
[0028] 一実施形態では、少なくとも1種の接着剤は、熱、pH、及び光のうちの少なくとも1つを与えることで活性化されるよう適合されている。
[0029] 一実施形態では、閉塞パッチは、その中で容易に組織を成長させるよう適合される足場構造物(scaffold structure)を備える。
[0030] 一実施形態では、閉塞パッチには、閉塞パッチの生体吸収を容易にする幹細胞が含まれる。
[0031] 一実施形態では、閉塞パッチには、創傷治癒を促進するよう適合された少なくとも1種のホルモン剤が含まれる。
[0032] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトを備える。第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合され、第2のルーメンは、膨張流体を受容するよう適合される。デバイスは、カテーテルシャフトによって保持される膨張可能なバルーンをさらに備える。膨張可能なバルーンは、第2のルーメンから膨張流体を受容するよう適合される。膨張可能なバルーンには、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれる。
[0033] 一実施形態では、第1のルーメン及び第2のルーメンは、カテーテルシャフト内に非同心状に配置される。
[0034] 一実施形態では、第1のルーメン及び第2のルーメンは、カテーテルシャフト内に非同心状に配置される。
[0035] 一実施形態では、デバイスは、カテーテルシャフトで保持される少なくとも1つのX線造影マーカをさらに備える。
[0036] 一実施形態では、少なくとも1つのX線造影マーカは、カテーテルシャフトの周囲に延在するバンドを備える。
[0037] 一実施形態では、少なくとも1つのX線造影マーカは、少なくとも第1のX線造影マーカ及び第2のX線造影マーカを備える。
[0038] 一実施形態では、少なくとも1つのX線造影マーカは、少なくとも第3のX線造影マーカをさらに備える。
[0039] 一実施形態では、膨張可能なバルーンは、近位部分、遠位部分、及び近位部分と遠位部分との間に配置された中間部分を備え、ここで第1、第2、及び第3のX線造影マーカは膨張可能なバルーン内に保持され、第1のX線造影マーカは近位部分と軸方向に位置合せされ、第2のX線造影マーカは中間部分と軸方向に位置合せされ、第3のX線造影マーカは遠位部分と軸方向に位置合せされる。
[0040] 一実施形態では、デバイスは、膨張可能なバルーンの第1の端部から第2の端部へ容易に血液を通過させるよう適合されている第3のルーメンをさらに有する。
[0041] 一実施形態では、カテーテルシャフトは第3のルーメンを有する。
[0042] 一実施形態では、膨張可能なバルーンは、血流損失の速度を下げるために、止血組成物でコーティングされる。
[0043] 一実施形態では、止血組成物には、フィブリンベースの凝固剤が含まれる。
[0044] 一実施形態では、止血組成物には、コーティング剤が含まれる。
[0045] 一実施形態では、デバイスは、膨張可能なバルーンによって着脱可能に保持された閉塞パッチをさらに備え、閉塞パッチは、穿孔を閉塞するために膨張可能なバルーンから展開可能である。
[0046] 一実施形態では、閉塞パッチは、血管内で閉塞パッチの位置を維持するよう適合された少なくとも1種の接着剤を含む。
[0047] 一実施形態では、少なくとも1種の接着剤は、熱、pH、及び光のうちの少なくとも1つを与えることで活性化されるよう適合されている。
[0048] 一実施形態では、閉塞パッチは、その中で容易に組織を成長させるよう適合される足場構造物を備える。
[0049] 一実施形態では、閉塞パッチには、閉塞パッチの生体吸収を容易にする幹細胞が含まれる。
[0050] 一実施形態では、閉塞パッチには、創傷治癒を促進するよう適合された少なくとも1種のホルモン剤が含まれる。
[0051] いくつかの実施形態では、血管の穿孔を閉塞する方法は、以下のステップを有する。(1)第1のルーメン及び第2のルーメンを有するカテーテルシャフトと、約65mmから約80mmの作動長さを有し、約20mmから約25mmの膨張した直径を有する、カテーテルシャフトによって保持される膨張可能なバルーンとを備える、閉塞バルーンデバイスを準備するステップ、(2)膨張可能なバルーンが穿孔に近接して配置されるまで、血管内でカテーテルシャフトを前進させるステップ、並びに(3)膨張バルーンを膨張させ、それにより穿孔を閉塞するために、第2のルーメンを通して膨張可能なバルーンに膨張流体を送達するステップ。
[0052] 本方法の一実施形態では、膨張流体は、生理食塩水及び造影剤溶液を含む。
[0053] 本方法の一実施形態では、膨張流体は、約80パーセントの生理食塩水及び約20パーセントの造影剤溶液を含む。
[0054] 本方法の一実施形態では、膨張可能なバルーンに膨張流体を送達するステップは、約2から約3気圧の範囲の圧力で膨張流体を送達するステップを有する。
[0055] 本方法の一実施形態では、デバイスは、膨張可能なバルーンの第1の端部から第2の端部へ容易に血液を通過させるよう適合されている第3のルーメンをさらに有する。
[0056] 本方法の一実施形態では、カテーテルシャフトは第3のルーメンを有する。
[0057] 本方法の一実施形態では、膨張可能なバルーンは止血組成物でコーティングされており、ここで膨張流体を膨張可能なバルーンに送達するステップは、止血組成物を穿孔部位で血管組織と接触させる。
[0058] 本方法の一実施形態では、膨張可能なバルーンは、血流損失の速度を下げるために、止血組成物でコーティングされる。
[0059] 本方法の一実施形態では、止血組成物には、フィブリンベースの凝固剤が含まれる。
[0060] 本方法の一実施形態では、止血組成物には、コーティング剤が含まれる。
[0061] 本方法の一実施形態では、閉塞バルーンデバイスは、膨張可能なバルーンで着脱可能に保持される閉塞パッチを備え、膨張流体を膨張可能なバルーンに送達して膨張バルーンを膨張させ、それにより穿孔を閉塞するステップは、膨張可能なバルーンから閉塞パッチを展開するステップ、及びそれによって穿孔を閉塞するステップを有する。
[0062] 本方法の一実施形態では、閉塞パッチは少なくとも1種の接着剤を含み、本方法は、少なくとも1種の接着剤を活性化して血管内に閉塞パッチを固着させるステップをさらに有する。
[0063] 本方法の一実施形態では、少なくとも1種の接着剤を活性化して血管内に閉塞パッチを固着させるステップは、熱、pH、及び光のうちの少なくとも1つを与えるステップを有する。
[0064] 本方法の一実施形態では、閉塞パッチは、その中で容易に組織を成長させるよう適合される足場構造物を備える。
[0065] 本方法の一実施形態では、閉塞パッチには、閉塞パッチの生体吸収を容易にする幹細胞が含まれる。
[0066] 本方法の一実施形態では、閉塞パッチには、創傷治癒を促進するよう適合された少なくとも1種のホルモン剤が含まれる。
[0067] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトによって保持され、第2のルーメンから膨張流体を受容するよう適合された膨張可能なバルーンであって、約115mmから約65mmの長さを有する作動部分を備え、作動部分は、第1の外径から第2の外径へ内向きにテーパ付けされている膨張可能なバルーンとを備える。
[0068] 一実施形態では、作動部分は、一定の勾配で、第1の外径から第2の外径へ内向きにテーパ付けされている。
[0069] 一実施形態では、作動部分は、一定の勾配で、第1の外径から第2の外径へ内向きにテーパ付けされている。
[0070] 一実施形態では、第1の外径は、膨張可能なバルーンの近位部分に配置され、第2の外径は、膨張可能なバルーンの遠位部分に配置される。
[0071] 一実施形態では、第1の外径は、約35mmから約50mmの範囲にある。
[0072] 一実施形態では、第2の外径は、約16mmから約30mmの範囲にある。
[0073] 一実施形態では、デバイスは、カテーテルシャフトで保持される少なくとも1つのX線造影マーカをさらに備える。
[0074] 一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0075] 一実施形態では、膨張可能なバルーンには、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれる。
[0076] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトによって保持され、第2のルーメンから膨張流体を受容するよう適合された膨張可能なバルーンであって、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれ、第1の外径から第2の外径へ内向きにテーパ付けされている作動部分を備える膨張可能なバルーンとを備える。
[0077] 一実施形態では、作動部分は、一定の勾配で、第1の外径から第2の外径へ内向きにテーパ付けされている。
[0078] 一実施形態では、第1の外径は、膨張可能なバルーンの近位部分に配置され、第2の外径は、膨張可能なバルーンの遠位部分に配置される。
[0079] 一実施形態では、第1の外径は、約35mmから約50mmの範囲にある。
[0080] 一実施形態では、第2の外径は、約16mmから約30mmの範囲にある。
[0081] 一実施形態では、カテーテルシャフトで保持される少なくとも1つのX線造影マーカを備える。
[0082] 一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0083] 一実施形態では、膨張可能なバルーンには、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれる。
[0084] いくつかの実施形態では、血管の穿孔を閉塞する方法であって、本方法は、第1のルーメン及び第2のルーメンを有するカテーテルシャフトを備える閉塞バルーンデバイスを準備するステップであって、膨張可能なバルーンはカテーテルシャフトで保持され、膨張可能なバルーンは約115mmから約65mmの長さを有する作動部分を備え、作動部分は第1の外径から第2の外径へ内向きにテーパ付けされる、ステップと、膨張可能なバルーンが穿孔に近接して配置されるまで、血管内でカテーテルシャフトを前進させるステップと、膨張バルーンを膨張させ、それにより穿孔を閉塞するために、第2のルーメンを通して膨張可能なバルーンに膨張流体を送達するステップとを有する。
[0085] 本方法の一実施形態では、膨張流体は、生理食塩水及び造影剤溶液を含む。
[0086] 本方法の一実施形態では、膨張流体は、約80パーセントの生理食塩水及び約20パーセントの造影剤溶液を含む。
[0087] 本方法の一実施形態では、膨張可能なバルーンに膨張流体を送達するステップは、約2から約3気圧の範囲の圧力で膨張流体を送達するステップを有する。
[0088] いくつかの実施形態では、血管の穿孔を閉塞するデバイスであって、デバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトで保持され、第2のルーメンから膨張流体を受容するよう適合され、約115mmから約65mmの長さを有する作動部分を備えた膨張可能なバルーンとを備え、ここで作動部分は、第1の外径から第2の外径へ内向きにテーパ付けされており、膨張可能なバルーンは、長さ対第1の外径が約1.3:1から約3.3:1である第1の比、及び長さ対第2の外径が約2.2:1から約7.2:1である第2の比を有する。
[0089] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトで保持され、第2のルーメンから膨張流体を受容するよう適合され、約125mmから約85mmの長さを有する作動部分を備える膨張可能なバルーンであって、作動部分は、それぞれが異なる外径を有する複数のセクションを備える膨張可能なバルーンとを備える。
[0090] 一実施形態では、作動部分の複数のセクションは、第1の外径を有する第1のセクションと、第2の外径を有する第2のセクションと、第3の外径を有する第3のセクションとを備える。
[0091] 一実施形態では、第1の外径は第2の外径より大きく、第2の外径は第3の外径より大きい。
[0092] 一実施形態では、第1のセクションは、第2のセクションに対して近位方向に配置され、第2のセクションは、第3のセクションに対して近位方向に配置される。
[0093] 一実施形態では、第1の外径は、約60mmから約40mmの範囲にある。
[0094] 一実施形態では、第2の外径は、約30mmから約10mmの範囲にある。
[0095] 一実施形態では、第3の外径は、約26mmから約6mmの範囲にある。
[0096] 一実施形態では、第1のセクションは、約18mmから約25mmの範囲にある長さを有する。
[0097] 一実施形態では、第2のセクションは、約52mmから約60mmの範囲にある長さを有する。
[0098] 一実施形態では、第3のセクションは、約20mmから約40mmの範囲にある長さを有する。
[0099] 一実施形態では、デバイスは、カテーテルシャフトで保持される少なくとも1つのX線造影マーカをさらに備える。
[0100] 一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0101] 一実施形態では、膨張可能なバルーンには、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれる。
[0102] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトによって保持され、第2のルーメンから膨張流体を受容するよう適合された膨張可能なバルーンであって、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれ、それぞれが異なる外径を有する複数のセクションを具備する作動部分を備える膨張可能なバルーンとを備える。
[0103] 一実施形態では、作動部分の複数のセクションは、第1の外径を有する第1のセクションと、第2の外径を有する第2のセクションと、第3の外径を有する第3のセクションとを備える。
[0104] 一実施形態では、第1の外径は第2の外径より大きく、第2の外径は第3の外径より大きい。
[0105] 一実施形態では、第1のセクションは、第2のセクションに対して近位方向に配置され、第2のセクションは、第3のセクションに対して近位方向に配置される。
[0106] 一実施形態では、第1の外径は、約60mmから約40mmの範囲にある。
[0107] 一実施形態では、第2の外径は、約30mmから約10mmの範囲にある。
[0108] 一実施形態では、第3の外径は、約26mmから約6mmの範囲にある。
[0109] 一実施形態では、第1のセクションは、約18mmから約25mmの範囲にある長さを有する。
[0110] 一実施形態では、第2のセクションは、約52mmから約60mmの範囲にある長さを有する。
[0111] 一実施形態では、第3のセクションは、約20mmから約40mmの範囲にある長さを有する。
[0112] 一実施形態では、デバイスは、カテーテルシャフトで保持される少なくとも1つのX線造影マーカをさらに備える。
[0113] 一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0114] 一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0115] 一実施形態では、膨張可能なバルーンには、約85AのショアAデュロメータ硬さを有するポリウレタンが含まれる。
[0116] いくつかの実施形態では、血管の穿孔を閉塞する方法は、閉塞バルーンデバイスを準備するステップであって、閉塞バルーンデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトと、カテーテルシャフトで保持され、約125mmから約85mmの長さを有する作動部分を具備する膨張可能なバルーンとを備え、作動部分は、それぞれが異なる外径を有する複数のセクションを備える、ステップと、膨張可能なバルーンが穿孔に近接して配置されるまで、血管内でカテーテルシャフトを前進させるステップと、膨張バルーンを膨張させ、それにより穿孔を閉塞するために、第2のルーメンを通して膨張可能なバルーンに膨張流体を送達するステップとを有する。
[0117] 一実施形態では、膨張流体は、生理食塩水及び造影剤溶液を含む。
[0118] 一実施形態では、膨張流体は、約80パーセントの生理食塩水及び約20パーセントの造影剤溶液を含む。
[0119] 一実施形態では、膨張可能なバルーンに膨張流体を送達するステップは、約2から約3気圧の範囲の圧力で膨張流体を送達するステップを有する。
[0120] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトで保持され、第2のルーメンから膨張流体を受容するよう適合され、約125mmから約85mmの長さを有する作動部分を備えた膨張可能なバルーンとを備え、ここで作動部分は、第1の外径、長さ対第1の外径が約1.4:1から約3.1:1である第1の比を有する第1のセクションと、第2の外径、長さ対第2の外径が約2.8:1から約12.5:1である第2の比を有する第2のセクションと、第3の外径、長さ対第3の外径が約3.3:1から約20.8:1である第3の比を有する第3のセクションとを備える。
[0121] 一実施形態では、第1のセクションは、第2のセクションに対して近位方向に配置され、第2のセクションは、第3のセクションに対して近位方向に配置される。
[0122] いくつかの実施形態では、血管の穿孔を閉塞するデバイスは、第1のルーメン及び第2のルーメンを有するカテーテルシャフトであって、第1のルーメンは、ガイドワイヤ及び植え込まれた心臓リードの少なくとも1つを受容するよう適合されており、第2のルーメンは、膨張流体を受容するよう適合されているカテーテルシャフトと、カテーテルシャフトで保持され、第2のルーメンから膨張流体を受容するよう適合された膨張可能なバルーンであって、約80mmの作動長さを有し、約20mmの膨張した直径を有する膨張可能なバルーンとを備える。
[0123] 一実施形態では、膨張可能なバルーンはポリウレタンを含む。
[0124] 一実施形態では、膨張可能なバルーンは、近位テーパ部分、遠位テーパ部分、並びに近位テーパ部分と遠位テーパ部分との間に配置された作動部分を備え、作動部分は、約20mmの膨張した直径を有する。
[0125] 一実施形態では、第1のルーメン及び第2のルーメンは、カテーテルシャフト内に非同心状に配置される。
[0126] 一実施形態では、デバイスは、カテーテルシャフトで保持される少なくとも1つのX線造影マーカをさらに備える。
[0127] 一実施形態では、少なくとも1つのX線造影マーカは、カテーテルシャフトの周囲に延在するバンドを備える。
[0128] 一実施形態では、少なくとも1つのX線造影マーカは、少なくとも第1のX線造影マーカ及び第2のX線造影マーカを備える。
[0129] 一実施形態では、少なくとも1つのX線造影マーカは、少なくとも第3のX線造影マーカをさらに備える。
[0130] いくつかの実施形態では、血管の穿孔を治療する方法は、カテーテルシャフト、及びカテーテルシャフトで保持される膨張可能なバルーンを備える閉塞バルーンデバイスを準備するステップを有し、膨張可能なバルーンは、複数の別々に膨張及び収縮可能なバルーン部分を備える。本方法は、膨張可能なバルーンが穿孔に近接して配置されるまで、血管内でカテーテルシャフトを前進させるステップと、膨張可能なバルーンの少なくとも第1のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分を膨張状態まで膨張させるステップと、膨張可能なバルーンの第1のバルーン部分が膨張状態にある間に、膨張可能なバルーンの少なくとも第2のバルーン部分を収縮状態に維持するステップと、膨張可能なバルーンの第1のバルーン部分が膨張状態にあり、且つ膨張可能なバルーンの第2のバルーン部分が収縮状態にある間に、血管に造影剤の流体を送達するステップと、膨張可能なバルーンの第1のバルーン部分が膨張状態にあり、膨張可能なバルーンの第2のバルーン部分が収縮状態にある間に、造影剤の流体が穿孔を通って血管を出るのを観察し、それにより穿孔が膨張可能なバルーンの第2のバルーン部分に隣接していることを判断するステップとをさらに有する。
[0131] 本方法の一実施形態では、膨張流体を送達するステップは、膨張可能なバルーンの少なくとも第1のバルーン部分及び第3のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分及び第3のバルーン部分を膨張させるステップをさらに有する。
[0132] 本方法の一実施形態では、膨張流体を送達するステップは、膨張可能なバルーンの少なくとも第1のバルーン部分、第3のバルーン部分、及び第4のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分、第3のバルーン部分、及び第4のバルーン部分を膨張させるステップをさらに有する。
[0133] 本方法の一実施形態では、膨張流体を送達するステップは、膨張可能なバルーンの複数のバルーン部分のうち第2のバルーン部分を除くすべてに膨張流体を送達し、それにより膨張可能なバルーンの複数のバルーン部分のうち第2のバルーン部分を除くすべてを膨張させるステップをさらに有する。
[0134] 本方法の一実施形態では、造影剤の流体が穿孔を通って血管を出るのを観察するステップの後に、膨張流体を膨張可能なバルーンの第2のバルーン部分に送達し、それにより穿孔を閉塞するステップを有する。
[0135] 一実施形態では、本方法は、造影剤の流体が穿孔を通って血管を出るのを観察するステップの後に、膨張流体を膨張可能なバルーンの第1のバルーン部分から除去し、それにより膨張可能なバルーンの第1のバルーン部分を収縮して、膨張可能なバルーンに対して血管内の血液を灌流することを可能にするステップをさらに有する。
[0136] 本方法の一実施形態では、膨張流体は、生理食塩水を含む。
[0137] 本方法の一実施形態では、造影剤の流体が穿孔を通って血管を出るのを観察するステップは、造影剤の流体を医療画像化によって観察するステップを有する。
[0138] 本方法の一実施形態では、造影剤の流体を医療画像化によって観察するステップは、造影剤の流体をX線透視法によって観察するステップを有する。
[0139] 一実施形態では、本方法は、膨張可能なバルーンの少なくとも第1のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分を膨張状態まで膨張させるステップ、及び膨張可能なバルーンの少なくとも第2のバルーン部分を収縮状態に維持するステップの前に、膨張可能なバルーンの少なくとも第2のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第2のバルーン部分を膨張状態まで膨張させるステップと、膨張可能なバルーンの第2のバルーン部分が膨張状態にある間に、膨張可能なバルーンの少なくとも第1のバルーン部分を収縮状態に維持するステップと、膨張可能なバルーンの第2のバルーン部分が膨張状態にあり、且つ膨張可能なバルーンの第1のバルーン部分が収縮状態にある間に、血管に造影剤の流体を送達するステップと、膨張可能なバルーンの第2のバルーン部分が膨張状態にあり、且つ膨張可能なバルーンの第1のバルーン部分が収縮状態にある間に、造影剤の流体が穿孔を通って血管を出ないことを観察するステップとをさらに有する。
[0140] いくつかの実施形態では、血管の穿孔を治療する方法は、カテーテルシャフト、及びカテーテルシャフトで保持される膨張可能なバルーンを備える閉塞バルーンデバイスを準備するステップを有し、膨張可能なバルーンは、複数の別々に膨張及び収縮可能なバルーン部分を備える。本方法は、膨張可能なバルーンが穿孔に近接して配置されるまで、血管内でカテーテルシャフトを前進させるステップと、膨張可能なバルーンの少なくとも第1のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分を膨張させて穿孔を閉塞するステップと、穿孔を閉塞する一方で、膨張可能なバルーンの少なくとも第2のバルーン部分を収縮状態に維持し、それにより膨張可能なバルーンに対する血管内の血液の灌流を可能にするステップとをさらに有する。
[0141] 一実施形態では、本方法は、膨張可能なバルーンの少なくとも第1のバルーン部分及び第3のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分及び第3のバルーン部分を膨張させるステップをさらに有する。
[0142] 一実施形態では、本方法は、膨張可能なバルーンの少なくとも第1のバルーン部分、第3のバルーン部分、及び第4のバルーン部分に膨張流体を送達し、それにより膨張可能なバルーンの少なくとも第1のバルーン部分、第3のバルーン部分、及び第4のバルーン部分を膨張させるステップをさらに有する。
[0143] 本方法の一実施形態では、膨張流体を送達するステップは、膨張可能なバルーンの複数のバルーン部分のうち第2のバルーン部分を除くすべてに膨張流体を送達し、それにより膨張可能なバルーンの複数のバルーン部分のうち第2のバルーン部分を除くすべてを膨張させるステップをさらに有する。
[0144] 本方法の一実施形態では、膨張流体は、生理食塩水を含む。
[0145] 本方法の一実施形態では、造影剤の流体を医療画像化によって観察するステップでは、灌流するのを確認する。
[0146] 本方法の一実施形態では、造影剤の流体を医療画像化によって観察するステップは、X線透視法によって造影剤の流体を観察し、灌流するのを確認するステップを有する。
[0147] これら及び他の利点は、本明細書に含まれる態様、実施形態、及び構成の開示から明らかとなろう。
[0148] 本明細書で使用される「少なくとも1つの」、「1つ又は複数の」、並びに「及び/又は」は、運用にあたっては、接続的且つ選言的の両方である、無制限の表現である。例えば、「A、B、及びCのうちの少なくとも1つ」、「A、B、又はCのうちの少なくとも1つ」、「A、B、及びCのうちの1つ又は複数」、「A、B、又はCのうちの1つ又は複数」並びに「A、B、及び/又はC」の表現のそれぞれが、A単独、B単独、C単独、AとBと一緒、AとCと一緒、BとCと一緒、又はAとBとCと一緒、を意味する。上記表現におけるA、B、及びCのそれぞれが、X、Y、及びZなどの要素、又はX1−Xn、Y1−Ym、及びZ1−Zoなどの要素のクラスを指す場合、そのフレーズは、X、Y、及びZから選択される単一の要素、同じクラスから選択される要素の組合せ(例えば、X1及びX2)、並びに2つ以上のクラスから選択される要素の組合せ(例えば、Y1及びZo)を指すことを意図している。
[0149] 用語「a」又は「an」のつく実体は、その実体の1つ又は複数を指すことに留意されたい。したがって、用語「a」(又は「an」)、「1つ又は複数」、及び「少なくとも1つ」は、本明細書では互換的に使用され得る。用語「comprising」、「including」、及び「having」もまた、互換的に使用され得ることに留意されたい。
[0150] 「カテーテル」は、血管構造系などの体腔、導管、管腔、又は血管に挿入することができる管を指す。ほとんどの用途では、カテーテルは比較的細い可撓性の管(「ソフト」カテーテル)であるが、用途によっては、より大きく、硬く(より可撓性が低く)、それでもなおできるだけ可撓なカテーテル(「ハード」カテーテル)もある。
[0151] 「リード」は導電性の構造体で、通常は電気的に絶縁されたコイル状のワイヤである。電気的に導電性の材料は、金属及び金属間合金が一般的な、任意の導電性材料であり得る。絶縁材料の外側シースは、生体適合性及び生体安定性があり(例えば、体内で溶解しない)、一般にポリウレタン及びポリイミドなどの有機材料を含む。リードの種類には、非限定的な例として、心外膜及び心内膜のリードが含まれる。リードは一般的に、経皮的又は外科的に体内に植え込まれる。
[0152] 本明細書で使用する用語「手段」は、米国特許法第112条第(f)項にしたがって、可能な限り最も広い解釈が与えられるものとする。したがって、用語「手段」を組み入れた請求項は、本明細書に示すあらゆる構造体、材料、又は振る舞い、及びそれらのすべての均等物を包含するものとする。さらに、その構造体、材料、又は振る舞い、及びそれらの均等物は、概要、図面の簡単な説明、詳細な説明、要約、及び特許請求の範囲自体に記載されているものすべてを含むものとする。
[0153] 本明細書で使用する用語「閉塞する」及びその変形は、血管の穿孔などの、構造体を通る流れを抑制することを指す。
[0154] 本明細書で使用する用語「近接した」は、非常に近いか、且つ/又は隣接することを意味するものとする。例えば、閉塞バルーンは、穿孔の非常に近くにあるか、又は穿孔に隣接し、それにより閉塞バルーンが、膨張時に穿孔を通って流れる血液を閉塞する。
[0155] 本開示全体にわたって与えられる、どの最大数値限度も、あたかも低い数値限度が本明細書に明示的に記載されていたかのように、代替としての何れの低い数値限度も含むものとしてみなされることを理解されたい。本開示全体にわたって与えられる、どの最小数値限度も、あたかも高い数値限度が本明細書に明示的に記載されていたかのように、代替としての何れの高い数値限度も含むものとみなされる。本開示全体にわたって与えられる、どの数値範囲も、あたかも狭い数値範囲が本明細書にすべて明示的に記載されていたかのように、当該数値範囲内にあるどの狭い数値範囲も含むものとみなされる。
[0156] 上記は、本開示のいくつかの態様の理解を可能にするための、本開示の簡略化した概要である。この概要は、本開示及びその様々な態様、実施形態、及び構成の、広範な大要でも網羅的な大要でもない。本開示の重要な又は決定的な要素を特定することも本開示の範囲を描写することも意図していないが、以下に提示するより詳細な説明への導入として、本開示の選択された概念を簡略化した形で提示することを意図したものである。本開示の他の態様、実施形態、及び構成は、上記に示す又は以下に詳細に説明する機能のうちの1つ又は複数を、単独で又は組み合わせて利用することも可能であることが理解されよう。
[0157] 添付図面は、本開示のいくつかの例を示すために本明細書の中に組み入れられ、その一部を形成する。これらの図面は、記述と共に、本開示の原理を説明する。図面は単に、本開示をどのようにして作成し使用することができるかについての好ましい、代替の例を示しているにすぎず、本開示が、図示し説明した例のみに限定されると解釈すべきではない。以下に参照する図面で示すように、より詳しい機能及び利点が、以下の、本開示の種々の態様、実施形態、及び構成のより詳細な説明から明らかとなろう。
[0204] 図1は、一般に、過失で血管102の壁に穿孔する機械的デバイス、レーザデバイス、又はその他の何らかのデバイスを含む、前進してリードを除去するカテーテル104と共に、血管102(上大静脈、無名静脈、頸静脈など)の部分断面図を示す。より具体的には、心臓のリード106が血管102内にある。心臓リード106の遠位端(図示せず)は、患者の心臓の近位にあるペースメーカ又は除細動器などの、外科的に植え込まれたデバイスに結合される。リード除去カテーテル104は、近位端(図示せず)から遠位端に向かってリード106に沿って移動する。リード106は、上大静脈又は右心房の中又は近くなど1箇所又は複数箇所の位置で、血管102の壁の非常に近くに配置される場合がある。かかる状況では、リード除去カテーテル104がリード106に沿って前進するとき、リード除去カテーテル104の先端又は切断器具(図示せず)が誤って血管102の壁に穿孔108を作り、それにより出血110を引き起こす可能性がある。
[0205] 穿孔108が発生する原因となる要因には、リード106の屈曲の鋭さ、リード106が血管102の壁に非常に近い位置にある血管102の壁の構造的に完全な状態、血管102の鋭い屈曲、カテーテル104を前進させるためにリード除去カテーテル104に加えられる速度及び/又は力、並びに/或いはこれらの要因と当業者に知られている他の要因との様々な組合せが含まれる。いずれにせよ、穿孔108を(例えば、X線透視法、血圧監視などによって)検出すると、リード除去カテーテル104を血管構造から直ちに除去し、本開示の実施形態による1つ又は複数の閉塞バルーンデバイスを血管構造に挿入し、穿孔108に隣接して配置して穿孔108を閉塞するために使用する。すなわち、リード除去カテーテル104が血管102内に残っている間に、閉塞バルーンデバイスを血管に挿入して穿孔108を閉塞するか、又は血管102内に閉塞バルーンデバイスを挿入して展開する前に、リード除去カテーテル104を血管102から除去する。
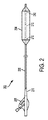
[0206] 図2は、本開示の実施形態による例示的な閉塞バルーンデバイス202の側面図である。閉塞バルーンデバイス202は、一般に、カテーテルシャフト206の遠位部分に保持される膨張可能なバルーン204を備える。閉塞バルーンデバイス202は、カテーテルシャフト206の近位部分に保持される接続ハブ208も備える。接続ハブ208及びカテーテルシャフト206は、それらの間の境界部分に、遠位方向にテーパ付けした歪み緩和部210を保持する。カテーテルシャフト206は、閉塞バルーンデバイス202の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ212も保持する。カテーテルシャフト206は、例えば図2に示すように、3つのX線造影マーカ212を保持する。第1のX線造影マーカ212は、膨張可能なバルーン204の近位部分と軸方向に位置合せされ、第2のX線造影マーカ212は、膨張可能なバルーン204の中間部分と軸方向に位置合せされ、第3のX線造影マーカ212は、膨張可能なバルーン204の遠位部分と軸方向に位置合せされる。
[0207] 図3は、図2の閉塞バルーンデバイス202の膨張可能なバルーン204の側面図であり、ここで膨張可能なバルーン204は膨張状態で描かれている。膨張可能なバルーン204は、壁302、膨張室304、全長305、長さ310を有する近位首部306、長さ328を有する遠位首部324、長さ320を有する作動部分316、近位首部306と作動部分316との間に配置される近位テーパ部分312、並びに遠位首部324と作動部分316との間に配置される遠位テーパ部分322を備える。
[0208] 膨張可能なバルーン204の壁302は、膨張室304を画定する。膨張室304は、バルーンを膨張させる膨張流体(例えば、約80パーセント(すなわち、80パーセント±5パーセント)の生理食塩水及び約20パーセント(すなわち、20パーセント±5パーセント)の造影剤溶液)を受容するよう適合される。臨床医がリード除去カテーテル104を血管構造内に導入し、膨張可能なバルーン204を穿孔108に隣接して配置し、膨張可能なバルーンを膨張させると、膨張可能なバルーン204は穿孔108を容易に閉塞する。
[0209] いくつかの実施形態では、膨張可能なバルーン204は、1種又は複数種類の比較的柔軟な材料で形成される。かかる材料は、比較的高い拡張力を血管に加えることなく、様々な直径の血管、不規則性を有する血管、及び/又は(心臓リードなどの)植え込まれた物体を保持する血管を、容易に満たす。膨張可能なバルーン204は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン204は、例えば、オハイオ州ウィクリフにあるThe Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には80AE Pellethane(登録商標)で形成される。膨張可能なバルーン204は、約85A(すなわち、85A±4A)のショアAデュロメータ硬さを有する。
[0210] 膨張可能なバルーン204は、約98mm(すなわち、98mm±3mm)から約82mm(すなわち、82mm±3mm)の全長305を有する。
[0211] 膨張可能なバルーン204は、(1種又は複数種類の接着剤、圧縮嵌合などによって)カテーテルシャフト206に係合する近位首部306を備える。近位首部306は、約2.5mm(すなわち、2.5mm±0.07mm)の内径308を有する。近位首部306は、約10mm(すなわち、10mm±1mm)の長さ310を有する。近位首部306は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0212] 近位首部306の遠位で、近位首部306は、近位テーパ部分312と連結する。近位テーパ部分312は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン204が膨張すると、近位テーパ部分312は、膨張可能なバルーン204の長手方向軸314に対して約45度(すなわち、45度±0.5度)の角度313で配置される。
[0213] 近位テーパ部分312の遠位で、近位テーパ部分312は、作動部分316と連結する。膨張可能なバルーン204が適切に配置され膨張すると、作動部分316は穿孔108を閉塞する。作動部分316は、20mm(すなわち、20mm±2mm)よりもほぼ大きい、例えば、約20mm(すなわち、20mm±2mm)から約30mm(すなわち、30mm±2mm)の間、さらにできれば約20mm(すなわち、20mm±2mm)から約25mm(すなわち、25mm±2mm)の間の膨張した外径318を有する。作動部分316は、約80mm(すなわち、80mm±3mm)から約65mm(すなわち、65mm±3mm)の長さ320を有する。作動部分316は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。したがって、作動部分302の長さ320に対する膨張状態での膨張可能なバルーン204の外径318の比は、約2.6:1から約4:1である。約80mmから約65mmの長さ320に対する、約20mmから約25mmの比較的一定の膨張した外径318の、この比を有することにより、膨張可能なバルーン204が患者の血管構造内で穿孔108に隣接して配置されて膨張すると、穿孔108を閉塞する可能性が高まる。すなわち、膨張可能なバルーン204の作動部分302の長さ320は、穿孔108よりも大幅に長くなるように設計され、それにより、穿孔を迅速に探し出して閉塞する臨床医の能力を潜在的に高める。
[0214] 前述のように、膨張可能なバルーン204の作動部分316は、20mm(すなわち、20mm±2mm)よりもほぼ大きい、例えば、約20mm(すなわち、20mm±2mm)から約30mm(すなわち、30mm±2mm)の間、さらにできれば約20mm(すなわち、20mm±2mm)から約25mm(すなわち、25mm±2mm)の間の膨張した外径318を有する。膨張可能なバルーン204の作動部分316の外径318をこの直径まで膨張させると、膨張可能なバルーン204の作動部分316が、穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きくなる可能性が高まる。膨張可能なバルーン204の作動部分316の外径318を、穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きく膨張させると、穿孔のサイズを大きくすることなく、膨張可能なバルーン204が穿孔108を塞ぐ可能性が高まる。
[0215] やはり、膨張可能なバルーン204は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン204を上記の直径の範囲まで膨張させるために、膨張可能なバルーン204を、バルーン膨張室304内の圧力が約0psiから約3psiになるまで膨張流体を使って膨張させることも望ましい。膨張可能なバルーン204をかかる圧力まで、且つ/又は所望の直径に膨張させるのに使用される膨張流体の量は、約20ml(cc)から約60ml(cc)である。
[0216] 作動部分316の遠位で、作動部分316は、遠位テーパ部分322と連結する。遠位テーパ部分322は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン204が膨張すると、遠位テーパ部分322は、長手方向軸314に対して約45度(すなわち、45度±0.5度)の角度323で配置される。
[0217] 遠位テーパ部分322の遠位で、遠位テーパ部分322は、(1種又は複数種類の接着剤、圧縮嵌合などによって)カテーテルシャフト206に係合する遠位首部324と連結する。遠位首部324は、約2.5mm(すなわち、2.5mm±0.07mm)の内径326を有する。遠位首部324は、約10mm(すなわち、10mm±1mm)の長さ328を有する。遠位首部324は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0218] 図4は、上記のカテーテルシャフト206として使用されるカテーテルシャフト402の第1の例示的な実施形態の断面図である。カテーテルシャフト402は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。カテーテルシャフト402は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には75D Pellethane(登録商標)で形成される。
[0219] カテーテルシャフト402は、約2.1mm(すなわち、2.1mm±0.038mm)の外径403を有する。カテーテルシャフト402は、約110cm(すなわち、110cm±0.3cm)の長さを有する。
[0220] カテーテルシャフト402は、ガイドワイヤ又は植え込まれた心臓リードを受容し、閉塞バルーンデバイス202を穿孔108に近接した位置に誘導するよう適合された第1のルーメン404を有する。したがって、第1のルーメン504は、ガイドワイヤルーメン又は植込みリードルーメンとも呼ばれる。第1のルーメン404は、カテーテルシャフト402の外径403に対して中心から外れて配置されている。第1のルーメン404がガイドワイヤを受容するよう適合されていることを前提として、第1のルーメン404は円形断面を有し、約0.94mm(すなわち、0.94mm±0.025mm)の直径を有する。やはり、第1のルーメン404がガイドワイヤを受容するよう適合されていることを前提として、第1のルーメン404と外径403との間の最小壁厚405は、約0.15mm(すなわち、0.15mm±0.025mm)である。ただし、第1のルーメン404が植え込まれた心臓リードを受容するよう適合されている場合、心臓リードの直径は通常0.25mmより大きいので、第1のルーメン404は一層大きい円形断面を有する。したがって、第1のルーメン404は、0.25mmより大きい円形断面を有する。また、第1のルーメン404は円形断面を有するように描かれているが、第1のルーメン404の断面形状は、楕円などの非円形断面であってもよい。
[0221] カテーテルシャフト402は、接続ハブ208から膨張流体を受容し、膨張流体をバルーン膨張室304に送達するよう適合された、第2のルーメン406も有する。したがって、第2のルーメン506は、膨張ルーメンとも呼ばれる。第2のルーメン406は、第1のルーメン404及びカテーテルシャフト402の外径403に対して、中心から外れて配置されている。第2のルーメン406は、円形断面、又は三日月状の断面形状などの非円形断面形状を有する。第2のルーメン406が三日月状の断面形状を有していることを前提として、第2のルーメン406は、約1.8mm(すなわち、1.8mm±0.025mm)の幅408を有する。第2のルーメン406は、カテーテルシャフト402を2等分する平面で、約0.76mm(すなわち、0.76mm±0.025mm)の高さ410を有する。できるだけ迅速に膨張可能なバルーンを膨張させ、穿孔によって起こり得る失血を最小限に抑えるために、できるだけ多くの膨張流体を第2のルーメン406を通して膨張可能なバルーンの膨張室へ、できるだけ迅速に導入することが望ましい。したがって、カテーテルシャフト402の所与の外径403に対して、第2のルーメン406の断面積をできるだけ大きくすることが望ましい。例えば、2.1mm(すなわち、2.1mm±0.038mm)の外径403から2.3mm(すなわち、2.3mm±0.038mm)の外径の場合、第2のルーメン406の断面積は0.65mm2から1.90mm2の間、又はそれらの間の、0.66、0.67、0.68、0.69、0.70…1.0…1.5…1.9mm2など、0.01mm2刻みのいずれかであってもよい。
[0222] 第2のルーメン406と第1のルーメン404との間の最小壁厚412は、約0.1mm(すなわち、0.1mm±0.025mm)である。第2のルーメン406と外径403との間の最小壁厚414は、約0.15mm(すなわち、0.15mm±0.025mm)である。第2のルーメン406の三日月状の断面形状、第1のルーメン404と外径403との間の約0.15mmの壁厚405、第2のルーメン406と外径403との間の約0.15mmの壁厚414、並びに第2のルーメン406と第1のルーメン404との間の約0.1mmの壁厚412のうち2つ以上を有することにより、臨床医は、膨張可能なバルーン204の膨張室304を、膨張流体で迅速に膨張させることができる。
[0223] カテーテルシャフト402は、第2のルーメン406をカテーテルシャフト402の外側及びバルーン膨張室304と連結する1つ又は複数の開口部(図示せず)も有する。すなわち、第2のルーメン406は、1つ又は複数の開口部を通して膨張可能なバルーン204に膨張流体を送達する。第2のルーメン406は、カテーテルシャフト402の遠位端で(例えば、別個のカバー、カテーテルシャフト402の壁などによって)蓋をされている。
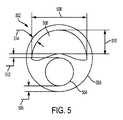
[0224] 図5は、上記のカテーテルシャフト206として使用されるカテーテルシャフト502の第2の例示的な実施形態の断面図である。カテーテルシャフト502は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。カテーテルシャフト502は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には75D Pellethane(登録商標)で形成される。
[0225] カテーテルシャフト502は、約2.3mm(すなわち、2.3mm±0.038mm)の外径503を有する。カテーテルシャフト502は、約110cm(すなわち、110cm±0.3cm)の長さを有する。
[0226] カテーテルシャフト502は、ガイドワイヤ又は植え込まれた心臓リードを受容し、閉塞バルーンデバイス202を穿孔108に近接した位置に誘導するよう適合された第1のルーメン504を有する。第1のルーメン504は、カテーテルシャフト502の外径503に対して中心から外れて配置されている。第1のルーメン504は円形断面を有し、約0.94mm(すなわち、0.94mm±0.025mm)の直径を有する。第1のルーメン504と外径503との間の最小壁厚505は、約0.1mm(すなわち、0.1mm±0.025mm)である。
[0227] カテーテルシャフト502は、接続ハブ208から膨張流体を受容し、膨張流体をバルーン膨張室304に送達するよう適合された、第2のルーメン506も有する。第2のルーメン506は、第1のルーメン504及びカテーテルシャフト502の外径503に対して、中心から外れて配置されている。第2のルーメン506は、三日月状の断面形状などの非円形断面形状を有する。第2のルーメン506は、約2.0mm(すなわち、2.0mm±0.025mm)の幅508を有する。第2のルーメン506は、カテーテルシャフト502を2等分する平面で、約0.94mm(すなわち、0.94mm±0.025mm)の高さ510を有する。第2のルーメン506と第1のルーメン504との間の最小壁厚512は、約0.1mm(すなわち、0.1mm±0.025mm)である。第2のルーメン506と外径503との間の最小壁厚514は、約0.15mm(すなわち、0.15mm±0.025mm)である。第2のルーメン506の三日月状の断面形状、第1のルーメン504と外径503との間の約0.15mmの壁厚505、第2のルーメン506と外径503との間の約0.1mmの壁厚514、並びに第2のルーメン506と第1のルーメン504との間の約0.1mmの壁厚512のうち2つ以上を有することにより、臨床医は、膨張可能なバルーン204の膨張室304を、膨張流体で迅速に膨張させることができる。
[0228] カテーテルシャフト502は、第2のルーメン506をカテーテルシャフト502の外側及びバルーン膨張室304に連結する1つ又は複数の開口部(図示せず)も有する。すなわち、第2のルーメン506は、1つ又は複数の開口部を通して膨張可能なバルーン204に膨張流体を送達する。第2のルーメン506は、カテーテルシャフト502の遠位端で(例えば、別個のカバー、カテーテルシャフト502の壁などによって)蓋をされている。
[0229] いくつかの実施形態では、膨張可能なバルーン204、カテーテルシャフト402、及びカテーテルシャフト502の寸法及び材料特性により、比較的小さなガイドワイヤ及びイントロデューサシースを備えた閉塞バルーンデバイス202の使用、及び膨張流体の膨張可能なバルーン204への比較的迅速な送達(例えば、15秒以内)が容易になる。さらに、閉塞バルーンデバイス202は、対象者の血管構造に入り、血管の穿孔を閉塞するのに十分な強度を有する。
[0230] 図6A及び図6Bは、上記のX線造影マーカ212として使用されるX線造影マーカバンド602の図である。X線造影マーカバンド602は、約90パーセント(すなわち、90パーセント±1パーセント)の白金と、10パーセント(すなわち、10パーセント±1パーセント)のイリジウムとの混合物などの、1種又は複数種類のX線造影材料で形成される。X線造影マーカバンド602は、カテーテルシャフト206の周囲に延在するよう適合された、開放端の円筒形状を有する。X線造影マーカバンド602は、約2.3mm(すなわち、2.3mm±0.01mm)から約2.5mm(すなわち、2.5mm±0.01mm)の範囲の外径604を有する。X線造影マーカバンド602は、約2.2mm(すなわち、2.2mm±0.01mm)から約2.4mm(すなわち、2.4mm±0.01mm)の内径606を有する。X線造影マーカバンド602は、約1.2mm(すなわち、1.2mm±0.05mm)の長さ608を有する。
[0231] 図7A〜図7Dは、接続ハブ208の図である。接続ハブ208は、ポリカーボネート、具体的にはドイツ、ダルムシュタットにあるBayer MaterialScienceから入手可能なMakrolon(登録商標)などの、1種又は複数種類のポリマーで形成される。接続ハブ208は、二股に分かれたルーメンを有し、二股に分かれたルーメンはさらに主ルーメン702及び分岐ルーメン704を有する(図7D参照)。分岐ルーメン704は、主ルーメン702から鋭角に延出している。主ルーメン702は、約2.2mm(すなわち、2.2mm±0.025mm)から約2.4mm(すなわち、2.4mm±0.025mm)の範囲の内径706を有する。主ルーメン704は、接続ハブ208の遠位側の第1のポート708と連結する。第1のポート708は、カテーテルシャフト206及び歪み緩和部210と連結する。主ルーメン704は、接続ハブ208の近位側の第2のポート710と連結する。第2のポート710は、例えば、ISO 594準拠のルアーコネクタであり、ガイドワイヤを受容し、且つ/又は注射筒など、膨張流体源に連結するよう適合される。分岐ルーメン706は、接続ハブ208の近位側の第3のポート712と連結する。第3のポート712は、例えば、ISO 594準拠のルアーコネクタであり、ガイドワイヤを受容し、且つ/又は注射筒など、膨張流体源に連結するよう適合される。
[0232] 図8Aは、本開示の実施形態による、血管の穿孔を閉塞する例示的な方法を示す。本方法は、ブロック802で、上記の図2〜図7に示す閉塞バルーンデバイス202などの閉塞バルーンデバイス、又は以下で説明する図9〜図22に示す閉塞バルーンデバイスなどの閉塞バルーンデバイスのいずれかを準備するステップから始まる。話を簡単にするために、この段落では、閉塞バルーンデバイス202の機能のみを指す。ブロック804では、図8Bに示すように、カテーテルシャフト206及び膨張可能なバルーン204を、血管内で、膨張可能なバルーン204が穿孔に近接して配置されるまで前進させる。引き続き図8Bを参照すると、膨張可能なバルーン204は膨張状態で穿孔108に隣接し、それによって穿孔108に近接している。図8Bでは、膨張可能なバルーン204は、穿孔108全体を隣接して覆うように描かれているが、閉塞バルーンデバイス202は、血管102内で、膨張可能なバルーン204が穿孔108の一部しか覆わないか、又は膨張可能なバルーン204は穿孔108のどんな部分も覆わないが、血管内の血流の上流の位置で穿孔108の非常に近くに配置され、それにより、膨張可能なバルーン204は血流が穿孔108を通って流れるのを閉塞することができるような位置に配置することができる。
[0233] 再び図8Aを参照すると、いくつかの実施形態では、カテーテルシャフト206の第1のルーメン404は、ガイドワイヤ又は植え込まれた心臓リードを受容し、カテーテルシャフト206及び膨張可能なバルーン204は、ガイドワイヤ又は植え込まれた心臓リードに沿って前進する。いくつかの実施形態では、大腿骨イントロデューサシース(例えば、12Fの大腿骨イントロデューサシース)を使用することにより、カテーテルシャフト206を、大腿静脈(例えば、右大腿静脈)を通して穿孔まで前進させる。いくつかの実施形態では、近位側のX線造影マーカ212が上大静脈と右心房との接合部に位置するまで、カテーテルシャフト206を前進させる。ブロック806では、膨張流体(例えば、上記の生理食塩水及び造影剤溶液)は、カテーテルシャフト206の第2のルーメン406を通して膨張可能なバルーン204に送達され、膨張バルーン204を膨張させ、それにより穿孔を閉塞する。いくつかの実施形態では、膨張流体が、バルーン204が血管構造に合うまで、60ml(cc)の注射筒により膨張バルーン204に送達される。いくつかの実施形態では、膨張流体は、約2気圧(すなわち、2気圧±10パーセント)から約3気圧(すなわち、3気圧±10パーセント)の範囲の圧力で、膨張可能なバルーン204に送達される。いくつかの実施形態では、バルーン204の適切な膨張及び穿孔の閉塞を確認するために、造影剤が上静脈のアクセス部位を通って注入される。いくつかの実施形態では、患者の血行動態及び/又は生体情報の安定化を使用して、穿孔の閉塞を確認することができる。いくつかの実施形態では、ブロック808において、本方法は任意選択で、膨張可能なバルーン204から閉塞パッチ(例えば、以下に説明する閉塞パッチ1708)を、血管の穿孔を覆って展開するステップを含み、それにより穿孔を閉塞する。そして、膨張可能なバルーン204が閉塞パッチを備える場合、バルーン204が膨張することにより閉塞パッチが展開される。さらに、いくつかの実施形態では、ブロック810において、本方法は任意選択で、血管構造内のパッチの位置を維持するために、閉塞パッチを血管構造に連結するステップを含む。いくつかの実施形態では、閉塞パッチを血管構造に連結するステップは、以下で説明するやり方のいずれかで、パッチが保持する1種又は複数種類の接着剤を活性化するステップを含む。いくつかの実施形態では、もはや閉塞する必要がなくなると、バルーン204は、60ml(cc)の注射筒を使用して第2のルーメン406に吸引力を加えることにより収縮される。いくつかの実施形態では、バルーン204の収縮は、X線透視法を使用することにより確認される。
[0234] 図9A及び図9Bは、本開示の実施形態による別の例示的な閉塞バルーンデバイス902の、遠位部分の側面図である。閉塞バルーンデバイス902は、概して、上記のバルーンと類似の膨張可能なバルーン904を備える。膨張可能なバルーン904は、カテーテルシャフト906の遠位部分に保持される。閉塞バルーンデバイス902は、上記の接続ハブと類似の接続ハブ(図示せず)も備える。接続ハブは、カテーテルシャフト906の近位部分に保持される。接続ハブ及びカテーテルシャフト906は、それらの間の境界部分で、上記の歪み緩和部と類似の、遠位方向にテーパ付けした歪み緩和部(図示せず)を保持する。カテーテルシャフト906は、閉塞バルーンデバイス902の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ912も保持する。カテーテルシャフト906は、例えば、図9A及び図9Bに示すように、3つのX線造影マーカ912を保持する。第1のX線造影マーカ912は、バルーン904の近位首部914とバルーン904の近位テーパ部分916との交切部と、軸方向に位置合せされる。第2のX線造影マーカ912は、バルーン904の近位テーパ部分916と作動部分918との交切部と、軸方向に位置合せされる。第3のX線造影マーカ912は、バルーン904の作動部分918と遠位テーパ部分920との交切部と、軸方向に位置合せされる。
[0235] 本開示の膨張可能なバルーンは、穿孔部位の治療を支援するために、様々な医薬品及び生物学的薬剤で処理又はコーティングすることができる。いくつかの実施形態では、本開示の膨張可能なバルーンは、血流損失の速度を下げて、穿孔部位の外科的修復を計画して開始するためのより多くの時間を与える、止血組成物でコーティングすることができる。一般に、止血組成物は、1種又は複数種類の止血血液凝固剤(止血剤又は凝固剤とも呼ばれる)を含む。好適な凝固剤が、止血を刺激できるか、又は容易に止血できるように、止血組成物中に有効量だけ含まれる。好適な凝固剤には、トロンビン、又はフィブリノーゲンをフィブリンに変える天然に生じる若しくは合成の任意の薬剤、カルシウム、ナトリウム、マグネシウム、又は止血を刺激する他の化学イオン、硫酸プロタミン、イプシロンアミノカプロン酸、フィブリノーゲン、キチンなどが含まれるが、これらに限定されるものではない。本開示の止血組成物の一部として使用できる止血剤には、フィブリンシーラント(フィブリン糊とも呼ばれる)などのフィブリンベースの薬剤、ゼラチンマトリックストロンビン、ゼラチンスポンジ、酸化セルロース、コラーゲンスポンジ、コラーゲンフリース、組換え因子VIIaなども含まれるが、これらに限定されるものではない。
[0236] いくつかの実施形態では、止血組成物中に、ポリエチレングリコール、シアノアクリレート、フィブロネクチン、フォンウィルブランド因子、プロテインZなどを含むがこれらに限定されない細胞又は組織接着特性を有する、1種又は複数種類の薬剤を含めることも有利である。細胞又は組織接着特性を有する薬剤はさらに、血管の穿孔からの血流損失の速度を下げることはもちろん、穿孔創傷部位の治癒を促進することができる。バルーンが血管系を通って穿孔部位に移動するときに、組成物を安定化し、且つ/又は組成物の早すぎる損失を防ぐために、止血組成物中に、生体適合性ポリマーの添加の有無にかかわらず、ノルジヒドログアイアレチン酸、レスベラトロール、没食子酸プロピルなどの親油性抗酸化剤を含むがこれに限定されない1種又は複数種類のコーティング剤を含めることも有利である。
[0237] 止血組成物の他の成分には、創傷の治癒を促進する成長因子及び他の治療薬などのホルモン剤が含まれ得る。いくつかの実施形態では、止血組成物は、創傷シーラント組成物、並びに/或いは潜在的な反応性表面水酸基、及び場合によっては、例えば流体除去剤、脱水剤、粘着性凝集剤、膨潤剤、ナノ粒子又は微粒子などの薬物送達溶媒、凝血促進組成物、活性化剤又は促進剤などを含む追加の成分が含まれる、シリカナノ粒子の架橋結合剤を含む。他の実施形態では、止血組成物には、ペニシリン、ペニシリン化合物、スルホンアミド、リンコサミド、カルバペネム、テトラサイクリン、アミノグリコシドなどの予防的抗生物質及び殺菌剤、並びに他の好適な抗生物質組成物及びその組合せが含まれ得る。本開示の止血組成物には、好適なアジュバント、並びに防腐剤、湿潤剤、乳化剤、及び分散剤を含む賦形剤、追加の抗生物質単独、又は抗真菌剤、例えばパラベン、クロロブタノール、フェノール、ソルビン酸などとの組合せも含まれ得る。糖、塩化ナトリウムなどの浸透圧調節剤を含むことも可能である。さらに、モノステアリン酸アルミニウム及びゼラチンなどの吸収遅延剤も止血組成物に含まれ得る。当業者は本開示に基づいて容易に認識するように、止血組成物は、穿孔部位に直接塗布することができる粉末、スプレー、エアロゾル、泡、又はゲルになるよう調剤することができる。
[0238] 本開示の止血組成物は、様々なやり方で穿孔部位の組織に送達され得る。例えば、止血組成物は、カテーテルの遠位端に配置された膨張可能なバルーンの外側周辺に塗布することができ、それによりバルーンが膨張して穿孔を閉塞すると、止血組成物が穿孔部位の組織と接触するようになる。止血組成物の様々な成分は、穿孔部位の組織に送達されると、血流損失の速度を下げ、穿孔部位の治癒を促進するために、血液凝固並びに/又は細胞及び組織の接着を促進するなど、その生物学的効果を発揮することができる。いくつかの実施形態では、組成物は、(膨張していない状態の)膨張可能なバルーンの皺に塗布することができ、それによってカテーテルの遠位端を血管構造内に配置している際に、組成物を早すぎる損失から保護する。バルーンを展開すると、組成物が露出し、穿孔部位の組織に送達され得る。
[0239] 他の実施形態では、組成物を穿孔部位の組織へ容易に放散させるために、バルーンに隣接するカテーテルの遠位端にデバイス及び機構を備えることができる。例えば、径方向に伝播して穿孔部位の組織に組成物を送達する衝撃波(例えば、液体媒体のキャビテーション)を作り出すために、1本又は複数本の光ファイバを使用して、膨張可能なバルーン内に収容される液体媒体(例えば、造影剤)に光エネルギーのパルスを照射することができる。当業者が本開示に基づいて認識するように、穿孔部位の組織に止血組成物を送達するための他の手段も使用することができる。
[0240] カテーテルシャフト906は、上記の第1及び第2のルーメンとそれぞれ類似する、第1及び第2のルーメン(図示せず)を有する。カテーテルシャフト906は、第2のルーメンをカテーテルシャフト906の外側及びバルーン膨張室924に連結する1つ又は複数の開口部922も有する。すなわち、第2のルーメンは、1つ又は複数の開口部922を通して膨張可能なバルーン904に膨張流体を送達する。カテーテルシャフト906は、例えば、図9A及び図9Bに示すように、2つの開口部922を有する。第1の開口部922は、バルーン904の近位テーパ部分916と、軸方向に位置合せされる。第2の開口部922は、バルーン904の遠位テーパ部分920と、軸方向に位置合せされる。
[0241] カテーテルシャフト906の遠位端は、カテーテルシャフト906の第2のルーメンを覆う遠位先端部926を保持する。遠位先端部926は、カテーテルシャフト906の第1のルーメンと位置合せされた開口(図示せず)を有する。第1のルーメンと共に、開口は、ガイドワイヤ又は植え込まれた心臓リードを受容するよう適合されている。遠位先端部926は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。遠位先端部926は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には65D Pellethane(登録商標)で形成される。
[0242] 図10は、本開示の実施形態による別の例示的な閉塞バルーンデバイス1002の側面図である。閉塞バルーンデバイス1002は、一般に、カテーテルシャフト1006の遠位部分に保持される膨張可能なバルーン1004を備える。閉塞バルーンデバイス1002は、カテーテルシャフト1006の近位部分に保持される接続ハブ1008も備える。接続ハブ1008及びカテーテルシャフト1006は、それらの間の境界部分に、遠位方向にテーパ付けした歪み緩和部1010を保持する。カテーテルシャフト1006は、閉塞バルーンデバイス1002の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ1012も保持する。カテーテルシャフト1006は、例えば図10に示すように、3つのX線造影マーカ1012を保持する。第1のX線造影マーカ1012は、膨張可能なバルーン1004の近位部分と軸方向に位置合せされ、第2のX線造影マーカ1012は、膨張可能なバルーン1004の中間部分と軸方向に位置合せされ、第3のX線造影マーカ1012は、膨張可能なバルーン1004の遠位部分と軸方向に位置合せされる。
[0243] 図11A及び図11Bはそれぞれ、図10の閉塞バルーンデバイス1002の膨張可能なバルーン1004の部分縦断面図及び正面図であり、ここで膨張可能なバルーン1004は膨張状態で描かれている。膨張可能なバルーン1004は、壁1102、膨張室1104、長さ1110を有する近位首部1106、長さ1128を有する遠位首部1124、長さ1120を有する作動部分1116、近位首部1106と作動部分1116との間に配置される近位テーパ部分1112、並びに遠位首部1124と作動部分1116との間に配置される遠位テーパ部分1122を備える。
[0244] 膨張可能なバルーン1004の壁1102は、膨張室1104を画定する。膨張室1104は、バルーンを膨張させる膨張流体(例えば、約80パーセント(すなわち、80パーセント±5パーセント)の生理食塩水及び約20パーセント(すなわち、20パーセント±5パーセント)の造影剤溶液)を受容するよう適合される。臨床医が、閉塞バルーンデバイス1002を血管構造内に導入し、膨張可能なバルーン1004を穿孔108に隣接して配置し、膨張可能なバルーンを膨張させると、膨張可能なバルーン1004は穿孔108を容易に閉塞する。
[0245] いくつかの実施形態では、膨張可能なバルーン1004は、1種又は複数種類の比較的柔軟な材料で形成される。かかる材料は、比較的高い拡張力を血管に加えることなく、様々な直径の血管、不規則性を有する血管、及び/又は(心臓リードなどの)植え込まれた物体を保持する血管を、容易に満たす。膨張可能なバルーン1004は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン1004は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には80AE Pellethane(登録商標)で形成される。膨張可能なバルーン1004は、約85A(すなわち、85A±4A)のショアAデュロメータ硬さを有する。
[0246] 近位首部1106は、1種又は複数種類の接着剤、圧縮嵌合などによって、カテーテルシャフト1006に係合する。近位首部1106は、約2.5mm(すなわち、2.5mm±0.07mm)の内径1108を有する。近位首部1106は、約10mm(すなわち、10mm±1mm)の長さ1110を有する。近位首部1106は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0247] 近位首部1106の遠位で、近位首部1106は、近位テーパ部分1112と連結する。近位テーパ部分1112は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン1004が膨張すると、近位テーパ部分1112は、膨張可能なバルーン1004の長手方向軸1114に対して約35度(すなわち、35度±10度)の角度1113で配置される。
[0248] 近位テーパ部分1112の遠位で、近位テーパ部分1112は、作動部分1116と連結する。膨張可能なバルーン1004が適切に配置され膨張されると、作動部分1116は穿孔108を閉塞する。作動部分1116は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。作動部分1116は、約115mm(すなわち、115mm±3mm)から約65mm(すなわち、65mm±3mm)の長さ1120を有する。
[0249] 作動部分1116は、第1の外径1130(近位テーパ部分1112との境界部分)から第2の外径1132(遠位テーパ部分1122との境界部分)へと内向きにテーパ付けされている。膨張すると、第1の外径1130は、約35mm(すなわち、35mm±2mm)より大きい、例えば、約35mm(すなわち、35mm±2mm)から約50mm(すなわち、50mm±2mm)の間、さらにできれば約35mm(すなわち、35mm±2mm)から約45mm(すなわち、45mm±2mm)の間である。膨張すると、第2の外径1132は、約16mm(すなわち、16mm±2mm)より大きい、例えば、約16mm(すなわち、16mm±2mm)から約30mm(すなわち、30mm±2mm)の間、さらにできれば約16mm(すなわち、16mm±2mm)から約25mm(すなわち、25mm±2mm)の間である。
[0250] したがって、作動部分1116の長さ1120と、膨張可能なバルーン1004の膨張したときの第1の外径1130との比は、約1.3:1から約3.3:1であり、したがって、作動部分1116の長さ1120と、膨張可能なバルーン1004の膨張したときの第2の外径1132との比は、約2.2:1から約7.2:1である。比較的作動長が長いこれらの比率を有することにより、具体的には、右無名静脈及び右心房腔の上部の、又はその間の穿孔を閉塞するのに好適なバルーンが実現される。すなわち、作動部分1116の遠位部分は、具体的には右無名静脈の穿孔を閉塞するのに好適であり、作動部分1116の近位部分は、具体的には心房腔の上部の穿孔を閉塞するのに好適である。より一般的には、作動部分1116を上記の直径まで膨張させると、作動部分1116が、穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きくなる可能性が高まる。作動部分1116を穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きく膨張させると、穿孔のサイズを大きくすることなく、膨張可能なバルーン1004が穿孔108を塞ぐ可能性が高まる。
[0251] いくつかの実施形態では、図11A及び図11Bに示すように、作動部分は、一定の勾配で第1の外径1130から第2の外径1132へと内向きにテーパ付けされている。別の言い方をすれば、作動部分1116は円錐台形状を有している。いくつかの実施形態では、作動部分は、一定ではない勾配で、第1の外径1130から第2の外径1132へと内向きにテーパ付けされていてもよい。
[0252] やはり、膨張可能なバルーン1004は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン1004を上記の直径の範囲まで膨張させるために、膨張可能なバルーン1004を、バルーン膨張室1104内の圧力が約0psiから約3psiになるまで膨張流体を使って膨張させることも望ましい。膨張可能なバルーン1004をかかる圧力まで、且つ/又は所望の直径に膨張させるのに使用される膨張流体の量は、約20ml(cc)から約60ml(cc)である。
[0253] 作動部分1116の遠位で、作動部分1116は、遠位テーパ部分1122と連結する。遠位テーパ部分1122は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン1004が膨張すると、遠位テーパ部分1122は、長手方向軸1114に対して約30度(すなわち、30度±10度)の角度1123で配置される。
[0254] 遠位首部1124は、1種又は複数種類の接着剤、圧縮嵌合などによって、カテーテルシャフト1006に係合する。遠位首部1124は、約2.5mm(すなわち、2.5mm±0.07mm)の内径1126を有する。遠位首部1124は、約10mm(すなわち、10mm±1mm)の長さ1128を有する。遠位首部1124は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0255] カテーテルシャフト1006、接続ハブ1008、歪み緩和部1010、及びX線造影マーカ1012は、それぞれ、上記のカテーテルシャフト、接続ハブ、歪み緩和部、及びX線造影マーカと類似している。
[0256] 図12A及び図12Bは、本開示の実施形態による別の例示的な閉塞バルーンデバイス1202の、遠位部分の側面図である。閉塞バルーンデバイス1202は、概して、上記のバルーン1004と類似の膨張可能なバルーン1204を備える。膨張可能なバルーン1204は、カテーテルシャフト1206の遠位部分に保持される。閉塞バルーンデバイス1202は、上記の接続ハブと類似の接続ハブ(図示せず)も備える。接続ハブは、カテーテルシャフト1206の近位部分に保持される。接続ハブ及びカテーテルシャフト1206は、それらの間の境界部分で、上記の歪み緩和部と類似の、遠位方向にテーパ付けした歪み緩和部(図示せず)を保持する。カテーテルシャフト1206は、閉塞バルーンデバイス1202の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ1212も保持する。カテーテルシャフト1206は、例えば、図12A及び図12Bに示すように、3つのX線造影マーカ1212を保持する。第1のX線造影マーカ1212は、バルーン1204の近位首部1214とバルーン1204の近位テーパ部分1216との交切部と、軸方向に位置合せされる。第2のX線造影マーカ1212は、バルーン1204の近位テーパ部分1216と作動部分1218との交切部と、軸方向に位置合せされる。第3のX線造影マーカ1212は、バルーン1204の作動部分1218と遠位テーパ部分1220との交切部と、軸方向に位置合せされる。
[0257] カテーテルシャフト1206は、上記の第1及び第2のルーメンとそれぞれ類似する、第1及び第2のルーメン(図示せず)を有する。カテーテルシャフト1206は、第2のルーメンをカテーテルシャフト1206の外側及びバルーン膨張室1224に連結する1つ又は複数の開口部1222も有する。すなわち、第2のルーメンは、1つ又は複数の開口部1222を通して膨張可能なバルーン1204に膨張流体を送達する。カテーテルシャフト1206は、例えば、図12A及び図12Bに示すように、2つの開口部1222を有する。第1の開口部1222は、バルーン1204の近位テーパ部分1216と、軸方向に位置合せされる。第2の開口部1222は、バルーン1204の遠位テーパ部分1220と、軸方向に位置合せされる。
[0258] カテーテルシャフト1206の遠位端は、カテーテルシャフト1206の第2のルーメンを覆う遠位先端部1226を保持する。遠位先端部1226は、カテーテルシャフト1206の第1のルーメンと位置合せされた開口(図示せず)を有する。第1のルーメンと共に、開口は、ガイドワイヤ又は植え込まれた心臓リードを受容するよう適合されている。遠位先端部1226は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。遠位先端部1226は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には65D Pellethane(登録商標)で形成される。
[0259] 閉塞バルーンデバイス1002及び1202に対する、いくつかの変形形態及び修正形態を使用することができる。例えば、カテーテル1002又は1202が非大腿静脈的手法(例えば、頸静脈的手法)を使用して挿入されるべき場合、作動部分は、近位方向に向かって内向きにテーパ付けされていてもよい。
[0260] 図13は、本開示の実施形態による別の例示的な閉塞バルーンデバイス1302の側面図である。閉塞バルーンデバイス1302は、一般に、カテーテルシャフト1306の遠位部分に保持される膨張可能なバルーン1304を備える。閉塞バルーンデバイス1302は、カテーテルシャフト1306の近位部分に保持される接続ハブ1308も備える。接続ハブ1308及びカテーテルシャフト1306は、それらの間の境界部分に、遠位方向にテーパ付けした歪み緩和部1310を保持する。カテーテルシャフト1306は、閉塞バルーンデバイス1302の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ1312も保持する。カテーテルシャフト1306は、例えば図13に示すように、3つのX線造影マーカ1312を保持する。第1のX線造影マーカ1312は、膨張可能なバルーン1304の近位部分と軸方向に位置合せされ、第2のX線造影マーカ1312は、膨張可能なバルーン1304の中間部分と軸方向に位置合せされ、第3のX線造影マーカ1312は、膨張可能なバルーン1304の遠位部分と軸方向に位置合せされる。
[0261] 図14A及び図14Bはそれぞれ、図13の閉塞バルーンデバイス1302の膨張可能なバルーン1304の部分縦断面図及び正面図であり、ここで膨張可能なバルーン1304は膨張状態で描かれている。膨張可能なバルーン1304は、壁1402、膨張室1404、長さ1410を有する近位首部1406、長さ1428を有する遠位首部1424、長さ1420を有し複数の直径をもつ作動部分1416、近位首部1406と作動部分1416との間に配置される近位テーパ部分1412、並びに遠位首部1424と作動部分1416との間に配置される遠位テーパ部分1422を備える。
[0262] 膨張可能なバルーン1304の壁1402は、膨張室1404を画定する。膨張室1404は、バルーンを膨張させる膨張流体(例えば、約80パーセント(すなわち、80パーセント±5パーセント)の生理食塩水及び約20パーセント(すなわち、20パーセント±5パーセント)の造影剤溶液)を受容するよう適合される。臨床医が閉塞バルーンデバイス1302を血管構造内に導入し、膨張可能なバルーン1304を穿孔108に隣接して配置し、膨張可能なバルーンを膨張させると、膨張可能なバルーン1304は穿孔108を容易に閉塞する。
[0263] いくつかの実施形態では、膨張可能なバルーン1304は、1種又は複数種類の比較的柔軟な材料で形成される。かかる材料は、比較的高い拡張力を血管に加えることなく、様々な直径の血管、不規則性を有する血管、及び/又は(心臓リードなどの)植え込まれた物体を保持する血管を、容易に満たす。膨張可能なバルーン1304は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン1304は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には80AE Pellethane(登録商標)で形成される。膨張可能なバルーン1304は、約85A(すなわち、85A±4A)のショアAデュロメータ硬さを有する。
[0264] 近位首部1406は、1種又は複数種類の接着剤、圧縮嵌合などによって、カテーテルシャフト1306に係合する。近位首部1406は、約2.5mm(すなわち、2.5mm±0.07mm)の内径1408を有する。近位首部1406は、約10mm(すなわち、10mm±1mm)の長さ1410を有する。近位首部1406は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0265] 近位首部1406の遠位で、近位首部1406は、近位テーパ部分1412と連結する。近位テーパ部分1412は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン1304が膨張すると、近位テーパ部分1412は、膨張可能なバルーン1304の長手方向軸1414に対して約60度(すなわち、60度±10度)の角度1413で配置される。
[0266] 近位テーパ部分1412の遠位で、近位テーパ部分1412は、複数の直径を有する作動部分1416と連結する。膨張可能なバルーン1304が適切に配置され膨張されると、作動部分1416は穿孔108を閉塞する。作動部分1416は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。作動部分1416は、約125mm(すなわち、125mm±3mm)から約85mm(すなわち、85mm±3mm)の全長1420を有する。
[0267] 作動部分1416は、それぞれが異なる外径を有する複数のセクションを備える。例えば、図に示すように、作動部分1416は、第1の外径1434を有する近位又は第1のセクション1432、第2の外径1438を有する中間又は第2のセクション1436、及び第3の外径1442を有する遠位又は第3のセクション1440を備える。第1の外径1434は第2の外径1438より大きく、第2の外径1438は第3の外径1442より大きい。
[0268] 第1のセクション1432は、約18mm(すなわち、18mm±2mm)より長い、例えば約18mm(すなわち、18mm±2mm)から約25mm(すなわち、25mm±2mm)の間の長さ1444を有する。膨張すると、第1の外径1434は約60mm(すなわち、60mm±2mm)から約40mm(すなわち、40mm±2mm)の間、できれば約50mm(すなわち、50mm±2mm)である。
[0269] 第1のセクション1432の遠位で、第1の中間テーパ部分1446は、第1のセクション1432を第2のセクション1436と連結する。第1の中間テーパ部分1446は、膨張可能なバルーン1304の長手方向軸1414に対して約45度(すなわち、45度±10度)の角度で配置される。
[0270] 第2のセクション1436は、約52mm(すなわち、52mm±2mm)より長い、例えば約52mm(すなわち、52mm±2mm)から約60mm(すなわち、60mm±2mm)の間の長さ1448を有する。膨張すると、第2の外径1438は約30mm(すなわち、30mm±2mm)から約10mm(すなわち、10mm±2mm)の間、できれば約20mm(すなわち、20mm±2mm)である。
[0271] 第2のセクション1436の遠位で、第2の中間テーパ部分1450は、第2のセクション1436を第3のセクション1440と連結する。第2の中間テーパ部分1450は、膨張可能なバルーン1304の長手方向軸1414に対して約45度(すなわち、45度±10度)の角度で配置される。
[0272] 第3のセクション1440は、約40mm(すなわち、40mm±2mm)から約20mm(すなわち、20mm±2mm)の間、できれば約30mm(すなわち、30mm±2mm)の長さ1452を有する。膨張すると、第3の外径1442は約26mm(すなわち、26mm±2mm)から約6mm(すなわち、6mm±2mm)の間、できれば約16mm(すなわち、16mm±2mm)である。
[0273] したがって、作動部分1416の全長1420と、膨張可能なバルーン1304の膨張したときの第1の外径1434との比は、約1.4:1から約3.1:1であり、したがって、作動部分1416の全長1420と、膨張可能なバルーン1304の膨張したときの第2の外径1438との比は、約2.8:1から約12.5:1であり、したがって、作動部分1416の長さ1420と、膨張可能なバルーン1304の膨張したときの第3の外径1442との比は、約3.3:1から約20.8:1である。比較的作動長が長いこれらの比率を有することにより、具体的には、右無名静脈及び右心房腔の上部の、又はその間の穿孔を閉塞するのに好適なバルーンが実現される。すなわち、作動部分1416の第3のセクション1440は、具体的には右無名静脈の穿孔を閉塞するのに好適であり、作動部分1416の第2のセクション1436は、具体的には上大静脈の穿孔を閉塞するのに好適であり、作動部分1416の第1のセクション1432は、具体的には心房腔の上部の穿孔を閉塞するのに好適である。より一般的には、作動部分1416を上記の直径まで膨張させると、作動部分1416が、穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きくなる可能性が高まる。作動部分1416を穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きく膨張させると、穿孔のサイズを大きくすることなく、膨張可能なバルーン1304が穿孔108を塞ぐ可能性が高まる。
[0274] いくつかの実施形態では、作動部分1416の第1のセクション1432は、下大静脈から流れる血液が上大静脈と右心房との接合部の穿孔を通って流出するのを抑制する。すなわち、作動部分1416の第1のセクション1432は、心室内への流れの向きを変える栓又は障壁として作用する。
[0275] やはり、膨張可能なバルーン1304は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン1304を上記の直径の範囲まで膨張させるために、膨張可能なバルーン1304を、バルーン膨張室1404内の圧力が約0psiから約3psiになるまで膨張流体を使って膨張させることも望ましい。膨張可能なバルーン1304をかかる圧力まで、且つ/又は所望の直径に膨張させるのに使用される膨張流体の量は、約20ml(cc)から約60ml(cc)である。
[0276] 作動部分1416の遠位で、作動部分1416は、遠位テーパ部分1422と連結する。遠位テーパ部分1422は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン1304が膨張すると、遠位テーパ部分1422は、長手方向軸1414に対して約45度(すなわち、45度±10度)の角度1423で配置される。
[0277] 遠位首部1424は、1種又は複数種類の接着剤、圧縮嵌合などによって、カテーテルシャフト1306に係合する。遠位首部1424は、約2.5mm(すなわち、2.5mm±0.07mm)の内径1426を有する。遠位首部1424は、約10mm(すなわち、10mm±1mm)の長さ1428を有する。遠位首部1424は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0278] カテーテルシャフト1306、接続ハブ1308、歪み緩和部1310、及びX線造影マーカ1312は、それぞれ、上記のカテーテルシャフト、接続ハブ、歪み緩和部、及びX線造影マーカと類似している。
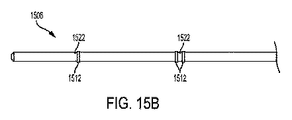
[0279] 図15A及び図15Bは、本開示の実施形態による別の例示的な閉塞バルーンデバイス1502の、遠位部分の側面図である。閉塞バルーンデバイス1502は、概して、上記のバルーン1304と類似の膨張可能なバルーン1504を備える。膨張可能なバルーン1504は、カテーテルシャフト1506の遠位部分に保持される。閉塞バルーンデバイス1502は、上記の接続ハブと類似の接続ハブ(図示せず)も備える。接続ハブは、カテーテルシャフト1506の近位部分に保持される。接続ハブ及びカテーテルシャフト1506は、それらの間の境界部分で、上記の歪み緩和部と類似の、遠位方向にテーパ付けした歪み緩和部(図示せず)を保持する。カテーテルシャフト1506は、閉塞バルーンデバイス1502の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ1512も保持する。カテーテルシャフト1506は、例えば、図15A及び図15Bに示すように、3つのX線造影マーカ1512を保持する。第1のX線造影マーカ1512は、バルーン1504の近位首部1514とバルーン1504の近位テーパ部分1516との交切部と、軸方向に位置合せされる。第2のX線造影マーカ1512は、バルーン1504の近位テーパ部分1516と作動部分の近位セクション1517との交切部と、軸方向に位置合せされる。第3のX線造影マーカ1512は、バルーン1504の作動部分の遠位セクション1519と遠位テーパ部分1520との交切部と、軸方向に位置合せされる。
[0280] カテーテルシャフト1506は、上記の第1及び第2のルーメンとそれぞれ類似する、第1及び第2のルーメン(図示せず)を有する。カテーテルシャフト1506は、第2のルーメンをカテーテルシャフト1506の外側及びバルーン膨張室1524に連結する1つ又は複数の開口部1522も有する。すなわち、第2のルーメンは、1つ又は複数の開口部1522を通して膨張可能なバルーン1504に膨張流体を送達する。カテーテルシャフト1506は、例えば、図15A及び図15Bに示すように、2つの開口部1522を有する。第1の開口部1522は、バルーン1504の近位テーパ部分1516と、軸方向に位置合せされる。第2の開口部1522は、バルーン1504の遠位テーパ部分1520と、軸方向に位置合せされる。
[0281] カテーテルシャフト1506の遠位端は、カテーテルシャフト1506の第2のルーメンを覆う遠位先端部1526を保持する。遠位先端部1526は、カテーテルシャフト1506の第1のルーメンと位置合せされた開口(図示せず)を有する。第1のルーメンと共に、開口は、ガイドワイヤ又は植え込まれた心臓リードを受容するよう適合されている。遠位先端部1526は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。遠位先端部1526は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には65D Pellethane(登録商標)で形成される。
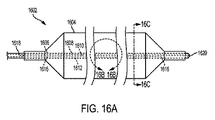
[0282] 図16A及び図16Bは、本開示の実施形態による別の例示的な閉塞バルーンデバイス1602の、遠位部分の図である。閉塞バルーンデバイス1602は、概して、本明細書で説明するバルーンのいずれかと類似の膨張可能なバルーン1604を備える。膨張可能なバルーン1604は、カテーテルシャフト1606の遠位部分に保持される。閉塞バルーンデバイス1602は、上記の接続ハブと類似の接続ハブ(図示せず)も備える。接続ハブは、カテーテルシャフト1606の近位部分に保持される。接続ハブ及びカテーテルシャフト1606は、それらの間の境界部分で、上記の歪み緩和部と類似の、遠位方向にテーパ付けした歪み緩和部(図示せず)を保持する。
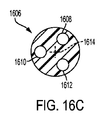
[0283] カテーテルシャフト1606は、第1のルーメン1608、第2のルーメン1610、及び第3のルーメン1612を有する。ルーメン1608、1610、及び1612は、カテーテルシャフト1606の長手方向軸1614の周りに等しい角度で配置されてもよいが、他の配置も考えられる。第1のルーメン1604は、ガイドワイヤ又は植え込まれた心臓リードを受容し、閉塞バルーンデバイス1602を穿孔108に近接した位置に誘導するよう適合されている。第2のルーメン1610は、1つ又は複数の開口部1616を通して膨張可能なバルーン1604に膨張流体を送達する。カテーテルシャフト1606は、例えば、図16Aに示すように、2つの開口部1616を有する。第3のルーメン1612は、血液灌流ルーメンとして作用する。すなわち、第3のルーメン1612は、血液を、カテーテルシャフト1606を通って膨張可能なバルーン1604の一端から他端へ、容易に通過させる。第3のルーメン1612は、バルーンデバイス1602の近位方向に配置された第1の開口部1618、及びバルーンデバイス1602の遠位方向に配置された第2の開口部1620に連結されている。第1の開口部1618は、カテーテルシャフト1606の側部に配置される。第2の開口部1620は、カテーテルシャフト1606の遠位端に配置される。
[0284] カテーテルシャフト1606は、本明細書で説明するやり方のいずれかで、1つ又は複数のX線造影マーカ(図示せず)を保持する。
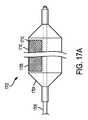
[0285] 図17A及び図17Bは、本開示の実施形態による別の例示的な閉塞バルーンデバイス1702の、遠位部分の図である。閉塞バルーンデバイス1702は、概して、本明細書で説明するバルーンのいずれかと類似する膨張可能なバルーン1704を備える。膨張可能なバルーン1704は、本明細書で説明するカテーテルシャフトのいずれかと類似するカテーテルシャフト1706の、遠位部分に保持される。閉塞バルーンデバイス1702は、上記の接続ハブと類似の接続ハブ(図示せず)も備える。接続ハブは、カテーテルシャフト1706の近位部分に保持される。接続ハブ及びカテーテルシャフト1706は、それらの間の境界部分で、上記の歪み緩和部と類似の、遠位方向にテーパ付けした歪み緩和部(図示せず)を保持する。
[0286] 閉塞バルーンデバイス1702は、膨張可能なバルーン1704の作動部分1710の外面上に、着脱可能に保持される閉塞パッチ1708も備える。膨張可能なバルーン1704は、パッチ1708を血管の穿孔の上に位置させるよう閉塞パッチ1708を(例えば、バルーン1704を膨張させることにより)展開し、それにより穿孔を閉塞する。いくつかの実施形態では、閉塞パッチ1708には、血管構造内でのパッチ1708の位置を維持するために、1種又は複数種類の接着剤が含まれる。1種又は複数種類の接着剤の接着特性は、熱、pH、光などのうちの1つ又は複数を与えることによるなど、様々なやり方で活性化される。いくつかの実施形態では、接着剤は紫外線の照射により活性化される。例えば、本開示の接着剤組成物は、Lang等による「A Blood−Resistant Surgical Glue for Minimally Invasive Repair of Vessels and Heart Defects」、Science Translational Medicine、第6巻、第218号、2014年1月8日、Roche等による「A Light−Reflecting Ballon Catheter for Atraumatic Tissue Defect Repair」、Science Translational Medicine、第7巻、第306号、2015年9月23日、及び国際公開第2015/175662号で説明されるように活性化され、それらが教示するすべて及びあらゆる目的のために、その全体が参照により本明細書に組み入れられる。
[0287] いくつの実施形態では、接着剤には、シアノアクリレート、ウシ血清アルブミン(BSA)−グルタルアルデヒド、フィブリンシーラント、ゼラチンマトリックストロンビン、ゼラチンスポンジ、酸化セルロース、コラーゲンスポンジ、コラーゲンフリース、組換え因子VIIaなどを含むがこれらに限定されない、臨床現場で現在使用されている接着剤が含まれる。いくつかの実施形態では、接着剤には、洗い流されないように、又は主に水性環境(例えば、血管組織)の中でそれらの基質から離脱しないように、ヘキサノイル(Hx、C6)基、パルミトイル(Pam、C16)基、ステアロイル(Ste、C18)基、及びオレオイル(Ole、C18不飽和)基などの疎水性官能基が含まれる。かかる接着剤には、10オレオイル−ジスクシンイミジル酒石酸塩、10ステアロイル−ジスクシンイミジル、及びそれらの変形及び組合せが含まれるが、これらに限定されるものではない。
[0288] 接着剤は、閉塞パッチ1708へ容易に付着させるために、様々な他の化合物と組み合わされる。例えば、接着剤は、閉塞パッチ1708をコーティングするために使用することができる、接着剤を含む溶液又は混合物の生成を補助する様々な化合物(例えば、可溶化剤)と組み合わされる。
[0289] いくつかの実施形態では、生分解性且つ生体適合性の疎水性ポリマーが接着剤として使用される。例えば、生分解性且つ生体適合性の疎水性ポリマーは、UV光を使用して架橋することができるポリ(グリセロールセバケートアクリレート)(PGSA)、又はその変形及び組合せである。閉塞パッチ1708に付着したPGSAを活性化するために、膨張可能なバルーン1704の内部又は外側に配置される紫外線放射カテーテルの遠位端から、紫外線が放射される。紫外線放射カテーテルがバルーン1704の内部に配置される場合、紫外線放射カテーテルは、バルーン1704内にあるカテーテルシャフト1706の一部の中に(部分的又は全体的に)配置されるか、又は紫外線放射カテーテルは、カテーテルシャフト1706とバルーン1704の内側との間に配置される。膨張可能なバルーン1704の壁は、紫外線を紫外線放射カテーテルから閉塞パッチ1708へ容易に透過させるために半透明である。
[0290] いくつかの実施形態では、パッチ1708は、ウシの心膜、ブタの小腸粘膜下組織、ポリエチレンテレフタレート、及びポリ(グリセロールセバケートウレタン)(PGSU)で構成される。さらに、パッチ1708は、その中で容易に組織を成長させるための足場構造物1712を備える。いくつかの実施形態では、パッチ1708には、パッチ1708の生体吸収を容易にする幹細胞が含まれる。いくつかの実施形態では、パッチ1708には、創傷の治癒を促進する成長因子及び他の治療薬などの、1種又は複数種類のホルモン剤が含まれる。特定の実施形態では、ホルモン剤は、ナノ粒子又は微粒子などの送達溶媒を使って送達される。
[0291] 閉塞パッチ1708は、様々な寸法のうちのいずれかを有する。いくつかの実施形態では、図17Aに示すように、閉塞パッチ1708は、膨張可能なバルーン1704の作動部分1710のほぼ全長にわたって延在する。いくつかの実施形態では、閉塞パッチ1708は、膨張可能なバルーン1704の作動部分1710の長さのうち、一部の上にしか延在しない。いくつかの実施形態では、図17Bに示すように、閉塞パッチ1708は、膨張可能なバルーン1704の作動部分1710の周囲の、一部の上にしか延在しない。いくつかの実施形態では、閉塞パッチ1708は、膨張可能なバルーン1704の作動部分1710のほぼ全周にわたって延在する。
[0292] 図17A及び図17Bはただ1つの閉塞パッチ1708だけを示しているが、いくつかの実施形態では、膨張可能なバルーン1704は複数の閉塞パッチ1708を保持する。パッチ1708は、膨張可能なバルーン1704の作動部分1710の長さに沿って、且つ/又は作動部分1710の周囲で、互いにずれていてもよい。
[0293] 閉塞バルーンデバイス1302及び1502に対する、いくつかの変形形態及び修正形態を使用することができる。例えば、カテーテル1302又は1502が非大腿静脈的手法(例えば、頸静脈的手法)を使用して挿入されるべき場合、作動部分は、比較的大きな直径を有する遠位セクション、及び比較的小さな直径を有する近位セクションを備えてもよい。別の例として、灌流ルーメンは、カテーテルシャフトではなくバルーンデバイスの一部として形成することができる。
[0294] 図18は、本開示の実施形態による例示的な閉塞バルーンデバイス1802の側面図である。閉塞バルーンデバイス1802は、一般に、カテーテルシャフト1806の遠位部分に保持される膨張可能なバルーン1804を備える。閉塞バルーンデバイス1802は、カテーテルシャフト1806の近位部分に保持される接続ハブ1808も備える。接続ハブ1808及びカテーテルシャフト1806は、それらの間の境界部分に、遠位方向にテーパ付けした歪み緩和部1810を保持する。カテーテルシャフト1806は、閉塞バルーンデバイス1802の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、3つのX線造影マーカ1812も保持する。第1のX線造影マーカ1812は、バルーン1804の近位首部1814とバルーン1804の近位テーパ部分1816との交切部と、軸方向に近接している。第2のX線造影マーカ1812は、バルーン1804の近位テーパ部分1816と作動部分1818との交切部と、軸方向に近接している。第3のX線造影マーカ1812は、バルーン1804の作動部分1818と遠位テーパ部分1820との交切部と、軸方向に近接している。デバイス1802は、約88cm(すなわち、88cm±1cm)の有効長1822(すなわち、歪み緩和部1810の遠位端とシャフト1806の遠位端との間の長さ)を有する。デバイス1802の最大外径又は横断面(crossing profile)は、約4mm(すなわち、4mm±0.1mm)である。
[0295] 図19は、図18の閉塞バルーンデバイス1802の遠位部分の側面図であり、ここで膨張可能なバルーン1804は膨張状態で描かれている。膨張可能なバルーン1804は、壁1902、膨張室1904、(長さ1906及び外径1907を有する)近位首部1814、長さ1910及び外径1911を有する遠位首部1908、(長さ1912を有する)作動部分1818、近位首部1814と作動部分1818との間に配置される近位テーパ部分1816、並びに遠位首部1908と作動部分1818との間に配置される遠位テーパ部分1820を備える。
[0296] 膨張可能なバルーン1804の壁1902は、膨張室1904を画定する。膨張室1904は、バルーンを膨張させる膨張流体(例えば、約80パーセント(すなわち、80パーセント±5パーセント)の生理食塩水及び約20パーセント(すなわち、20パーセント±5パーセント)の造影剤溶液)を受容するよう適合される。臨床医が、リード除去カテーテル104を血管構造内に導入し、膨張可能なバルーン1804を穿孔108に隣接して配置し、膨張可能なバルーンを膨張させると、膨張可能なバルーン1804は穿孔108を容易に閉塞する。
[0297] いくつかの実施形態では、膨張可能なバルーン1804は、1種又は複数種類の比較的柔軟な材料で形成される。かかる材料は、比較的高い拡張力を血管に加えることなく、様々な直径の血管、不規則性を有する血管、及び/又は(心臓リードなどの)植え込まれた物体を保持する血管を、容易に満たす。膨張可能なバルーン1804は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン1804は、例えば、オハイオ州ウィクリフにあるThe Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には80AE Pellethane(登録商標)で形成される。膨張可能なバルーン1804は、約85A(すなわち、85A±4A)のショアAデュロメータ硬さを有する。
[0298] 膨張可能なバルーン1804は、(1種又は複数種類の接着剤、圧縮嵌合などによって)カテーテルシャフト1806に係合する近位首部1814を備える。近位首部1814は、約2.5mm(すなわち、2.5mm±0.07mm)の内径を有する。近位首部1814は、約10mm(すなわち、10mm±2mm)の長さ1906を有する。近位首部1814は、約3.0mm(すなわち、3.0mm±0.1mm)の外径1907を有する。近位首部1814は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。
[0299] 近位首部1814の遠位で、近位首部1814は、近位テーパ部分1816と連結する。近位テーパ部分1816は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン1804が膨張すると、近位テーパ部分1816は、膨張可能なバルーン1804の長手方向軸に対して約45度(すなわち、45度±0.5度)の角度で配置される。
[0300] 近位テーパ部分1816の遠位で、近位テーパ部分1816は、作動部分1818と連結する。膨張可能なバルーン1804が適切に配置され膨張すると、作動部分1818は穿孔108を閉塞する。作動部分1818は、約20mm(すなわち、20mm±2mm)の膨張した外径1914を有する。作動部分1818は、約80mm(すなわち、80mm±3mm)の長さ1912を有する。作動部分1818は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。したがって、作動部分1818の長さ1912に対する膨張可能なバルーン1804の膨張した状態での外径1914の比は、約4:1である。約80mmの長さ1912に対する、約20mmの比較的一定の膨張した外径1914の、この比を有することにより、膨張可能なバルーン1804が患者の血管構造内で穿孔108に隣接して配置され膨張すると、穿孔108を閉塞する可能性が高まる。すなわち、膨張可能なバルーン1804の作動部分1818の長さ1912は、穿孔108よりも大幅に長くなるように設計され、それにより、穿孔を迅速に探し出して閉塞する臨床医の能力を潜在的に高める。
[0301] 前述のように、膨張可能なバルーン1804の作動部分1818は、約20mm(すなわち、20mm±2mm)の膨張した外径1914を有する。膨張可能なバルーン1804の作動部分1818の外径1914をこの直径まで膨張させると、膨張可能なバルーン1804の作動部分1818が、穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きくなる可能性が高まる。膨張可能なバルーン1804の作動部分1818の外径1914を、穿孔108の位置で、血管102の直径とほぼ同じ直径か、又は血管102の直径よりわずかに大きく膨張させると、穿孔のサイズを大きくすることなく、膨張可能なバルーン1804が穿孔108を塞ぐ可能性が高まる。
[0302] やはり、膨張可能なバルーン1804は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。膨張可能なバルーン1804を上記の直径まで膨張させるために、膨張可能なバルーン1804を、バルーン膨張室1904内の圧力が約0psiから約3psiになるまで膨張流体を使って膨張させることも望ましい。膨張可能なバルーン1804をかかる圧力まで、且つ/又は所望の直径に膨張させるのに使用される膨張流体の量は、約25ml(cc)である。さらに、エラストマ材料は、膨張可能なバルーン1804に、表1に示す伸展特性をもたらす。すなわち、膨張可能なバルーン1804に特定のボリュームの膨張流体を供給することにより、バルーン1804は、表1に示すように特定の直径まで膨張する。
[0303] 作動部分1818の遠位で、作動部分1818は、遠位テーパ部分1820と連結する。遠位テーパ部分1820は、約0.036mm(すなわち、0.036mm±0.0064mm)、約0.041mm(すなわち、0.041mm±0.0064mm)、約0.046mm(すなわち、0.046mm±0.0064mm)、又は約0.051mm(すなわち、0.051mm±0.0064mm)の壁厚を有する。膨張可能なバルーン1804が膨張すると、遠位テーパ部分1820は、膨張可能なバルーン1804の長手方向軸に対して約45度(すなわち、45度±0.5度)の角度で配置される。
[0304] 遠位テーパ部分1820の遠位で、遠位テーパ部分1820は、(1種又は複数種類の接着剤、圧縮嵌合などによって)カテーテルシャフト1806に係合する遠位首部1908と連結する。遠位首部1908は、約2.5mm(すなわち、2.5mm±0.07mm)の内径を有する。遠位首部1908は、約10mm(すなわち、10mm±2mm)の長さ1910を有する。遠位首部1908は、約3.0mm(すなわち、3.0mm±0.1mm)の外径1911を有する。遠位首部1908は、約0.24mm(すなわち、0.24mm±0.01mm)の壁厚を有する。膨張可能なバルーン1804は、遠位首部1908と近位首部1814との間で約100mm(すなわち、100mm±1mm)の長さ1916を有する。
[0305] 第1のX線造影マーカ1812は、近位首部1814と近位テーパ部分1816との交切部から、約1mm(すなわち、1mm±1mm)の距離1918だけずれている。第2のX線造影マーカ1812は、第1のX線造影マーカ1812から約10.27mm(すなわち、10.27mm±1mm)の距離1920だけずれている。第3のX線造影マーカ1812は、第1のX線造影マーカ1812から約86mm(すなわち、86mm±1mm)の距離1922だけずれている。
[0306] 図20A〜図20Dは、カテーテルシャフト1806の図である。カテーテルシャフト1806は、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。カテーテルシャフト1806は、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には75D Pellethane(登録商標)で形成される。
[0307] カテーテルシャフト1806は、約2.286mm(すなわち、2.286mm±0.04mm)の外径2002を有する。カテーテルシャフト1806は、約110cm(すなわち、110cm±0.3cm)の長さを有する。
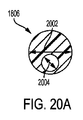
[0308] カテーテルシャフト1806は、ガイドワイヤ又は植え込まれた心臓リードを受容し、閉塞バルーンデバイス1802を穿孔108に近接した位置に誘導するよう適合された第1のルーメン2004を有する。第1のルーメン2004は、カテーテルシャフト1806の外径2002に対して中心から外れて配置されている。第1のルーメン2004が、約0.9mm(0.035インチ)の直径を有するガイドワイヤを受容するよう適合されていることを前提として、第1のルーメン2004は円形断面を有し、約0.954mm(すなわち、0.954mm±0.04mm)の直径を有する。しかし、第1のルーメン2004が植え込まれた心臓リードを受容するよう適合されている場合、第1のルーメン2004は、異なる断面直径を有する。しかも、第1のルーメン2004は、円形断面を有するように描かれているが、第1のルーメン2004の断面形状は、楕円などの非円形断面であってもよい。第1のルーメン2004と外径2002との間の最小壁厚は、約0.15mm(すなわち、0.15mm±0.025mm)である。
[0309] カテーテルシャフト1806は、接続ハブ1808から膨張流体を受容し、膨張流体をバルーン膨張室1904に送達するよう適合された、第2のルーメン2006も有する。第2のルーメン2006は、第1のルーメン2004及びカテーテルシャフト1806の外径2002に対して、中心から外れて配置されている。第2のルーメン2006は、円形断面、又は三日月状の断面形状又は半円形状などの非円形断面形状を有する。第2のルーメン2006が三日月状の断面形状又は半円形状を有していることを前提として、第2のルーメン2006は、約1.8mm(すなわち、1.8mm±0.025mm)の幅を有する。第2のルーメン2006は、カテーテルシャフト1806を2等分する平面で、約0.76mm(すなわち、0.76mm±0.025mm)の高さを有する。できるだけ迅速に膨張可能なバルーンを膨張させ、穿孔によって起こり得る失血を最小限に抑えるために、できるだけ多くの膨張流体を第2のルーメン2006を通して膨張可能なバルーンの膨張室内へ、できるだけ迅速に導入することが望ましい。したがって、カテーテルシャフト1806の所与の外径2002に対して、第2のルーメン2006の断面積をできるだけ大きくすることが望ましい。例えば、約2.286mm(すなわち、2.286mm±0.04mm)の外径2002の場合、第2のルーメン2006の断面積は0.65mm2から1.90mm2の間、又はそれらの間の、0.66、0.67、0.68、0.69、0.70…1.0…1.5…1.9mm2など、0.01mm2刻みのいずれかであってもよい。
[0310] 第2のルーメン2006と第1のルーメン2004との間の最小壁厚は、約0.1mm(すなわち、0.1mm±0.025mm)である。第2のルーメン2006と外径2002との間の最小壁厚は、約0.15mm(すなわち、0.15mm±0.025mm)である。第2のルーメン2006と外径2002との間の最小厚さが約0.15mmであり、約1mmの三日月状の断面形状又は半円形状の半径は、約1.4mm2から1.7mm2の間であるルーメン2006の断面積と相関することを前提として、また第2のルーメン2006と第1のルーメン2004との間の壁厚に応じて、約1mmの三日月状の断面形状又は半円形状の半径は、約1.50mm2から1.60mm2の間であり約1.55mm2であるルーメン2006の断面積と相関する。或いは、三日月状の断面形状又は半円形状は、およそ0.50mmから1.50mmの間の半径を有してもよい。
[0311] カテーテルシャフト1806は、第2のルーメン2006をカテーテルシャフト1806の外側及びバルーン膨張室1904に連結する2つの開口部1924も有する。すなわち、第2のルーメン2006は、開口部1924を通して膨張可能なバルーン1804に膨張流体を送達する。図19を簡単に参照すると、第1の開口部1924は、バルーン1804の近位テーパ部分1816と軸方向に位置合せされ、第2の開口部1924は、バルーン1804の遠位テーパ部分1820と軸方向に位置合せされる。具体的に図20Dを参照すると、各開口部1924は、約5mm(すなわち、5mm±1mm)の軸方向長さ2008及び約1.8mm(すなわち、1.8mm±0.3mm)の横幅2010を有する。第2のルーメン2006は、カテーテルシャフト1806の遠位端で(例えば、別個のカバー1926、カテーテルシャフト1806の壁などによって)蓋をされている。カテーテルシャフト1806が別個のカバー1926を備える場合、カバー1926は、約10mm(すなわち、10mm±2mm)の距離1928だけ遠位首部1908からずらされる。カバー1926は、約5mm(すなわち、5mm±2mm)の軸方向の長さ1930を有する。カテーテルシャフト1806は、接続ハブ1808のルーメンからの膨張流体を容易に受容するために、接続ハブ1808内に配置された第3の開口部(図示せず)も有する。
[0312] いくつかの実施形態では、膨張可能なバルーン1804及びカテーテルシャフト1806の寸法及び材料特性により、比較的小さなガイドワイヤ及びイントロデューサシースを備えた閉塞バルーンデバイス1802の使用、及び膨張流体の膨張可能なバルーン1804への比較的迅速な送達(例えば、40秒以内)が容易になる。第2のルーメン2006が三日月状の断面形状であることと、第1のルーメン2004と外径2002との間の壁厚は約0.15mmであることと、第2のルーメン2006と外径2002との間の壁厚は約0.15mmであることと、第2のルーメン2006と第1のルーメン2004との間の壁厚は約0.1mmであることと、開口部1924は約5mmの軸方向長さ2008及び約1.8mmの横幅2010を有し、一方の開口部1924は近位テーパ部分1816と軸方向に位置合せされ、他方の開口部1924は遠位テーパ部分1820と軸方向に位置合せされていることとのうち2つ以上を有することにより、臨床医は、膨張可能なバルーン1804を、膨張流体を使って迅速に膨張させることができる。テストでは、かかる特性を有する閉塞バルーンデバイスは、閉塞バルーンを直径31.1mmまで容易に膨張させるために、平均時間25.6秒、標準偏差1.3秒で、60mlの(80%の生理食塩水及び20%の造影剤溶液である)膨張流体を受容できることが実証された。さらに、閉塞バルーンデバイス1802は、対象者の血管構造に入り、血管の穿孔を閉塞するのに十分な強度を有する。
[0313] X線造影マーカ1812は、上記のX線造影マーカバンド602と類似している。X線造影マーカ1812は、約90パーセント(すなわち、90パーセント±1パーセント)の白金と、10パーセント(すなわち、10パーセント±1パーセント)のイリジウムとの混合物などの、1種又は複数種類のX線造影材料で形成される。X線造影マーカ1812は、カテーテルシャフト1806の周囲に延在するよう適合された、開放端の円筒形状を有する。X線造影マーカ1812はそれぞれ、約2.489mm(すなわち、2.489mm±0.1mm)の範囲の外径を有する。X線造影マーカ1812はそれぞれ、約2.2mm(すなわち、2.2mm±0.01mm)から約2.4mm(すなわち、2.4mm±0.01mm)の内径を有する。X線造影マーカ1812はそれぞれ、約1.2mm(すなわち、1.2mm±0.05mm)の長さを有する。
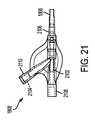
[0314] 図21は、接続ハブ1808の図である。接続ハブ1808は、ポリカーボネート、具体的にはドイツ、ダルムシュタットにあるBayer MaterialScienceから入手可能なMakrolon(登録商標)などの、1種又は複数種類のポリマーで形成される。接続ハブ1808は、二股に分かれたルーメンを有し、二股に分かれたルーメンはさらに主ルーメン2102及び分岐ルーメン2104を有する。分岐ルーメン2104は、主ルーメン2102から鋭角に延出している。主ルーメン2102は、約2.2mm(すなわち、2.2mm±0.025mm)から約2.4mm(すなわち、2.4mm±0.025mm)の範囲の内径を有する。主ルーメン2104は、接続ハブ1808の遠位側の第1のポート2108と連結する。第1のポート2108は、カテーテルシャフト1806及び歪み緩和部1810と連結する。主ルーメン2104は、接続ハブ1808の近位側の第2のポート2108と連結する。第2のポート2108は、例えば、ISO 594−1、594−2準拠のルアーコネクタであり、ガイドワイヤを受容し、且つ/又は注射筒、具体的には60ml(cc)注射筒など、膨張流体源に連結するよう適合される。分岐ルーメン2104は、接続ハブ1808の近位側の第3のポート2110と連結する。第3のポート2110は、例えば、ISO 594−1、594−2準拠のルアーコネクタであり、ガイドワイヤを受容し、且つ/又は注射筒、具体的には60ml(cc)注射筒など、膨張流体源に結合するよう適合される。
[0315] 図22は、デバイス1802が医療施術者に提供される状態での、閉塞バルーンデバイス1802の図である。具体的には、デバイス1802は、膨張可能なバルーン1804の周りに配置された保護カバー2202を備える。保護カバー2202は、バルーン1804の近位端を越えて近位方向に、またバルーン1804の遠位端を越えて遠位方向に延在する。
[0316] 図23A及び図23Bは、本開示の実施形態による例示的な閉塞バルーンデバイス2302の図である。閉塞バルーンデバイス2302は、一般に、カテーテルシャフト2306の遠位部分に保持される膨張可能なバルーン2304を備え、膨張可能なバルーン2304は膨張した状態で描かれている。閉塞バルーンデバイス2302は、カテーテルシャフト2306の近位部分に保持される接続ハブ2308も備える。接続ハブ2308及びカテーテルシャフト2306は、それらの間の境界部分に、遠位方向にテーパ付けした歪み緩和部2310を保持する。カテーテルシャフト2306は、閉塞バルーンデバイス2302の位置を医療画像化によって(例えば、X線透視法によって)判断できるように、1つ又は複数のX線造影マーカ2312も保持する。カテーテルシャフト2306は、例えば図23Aに示すように、3つのX線造影マーカ2312を保持する。カテーテルシャフト2306は、ガイドワイヤ又は植え込まれた心臓リードを受容し、閉塞バルーンデバイス2302を血管の穿孔に近接した位置に誘導するよう適合された第1のルーメン2307も有する。
[0317] 膨張可能なバルーン2304は、別々に膨張及び収縮可能な複数のバルーン部分を備える。いくつかの実施形態では、図23A及び図23Bに示すように、膨張可能なバルーン2304は、4つのバルーン部分、具体的には第1のバルーン部分2305A、第2のバルーン部分2305B、第3のバルーン部分2305C、及び第4のバルーン部分2305Dを備える。話を簡単にするために、以下の説明は、これら4つのバルーン部分2305A、2305B、2305C、及び2305D、並びに関連する構成要素を例示的に参照する。しかし、他の実施形態では、膨張可能なバルーンは、2つ、3つ、又は5つ以上のバルーン部分など、異なる数のバルーン部分を備え、当業者は、以下の説明がそれに応じて一般化できることを理解するであろう。
[0318] いくつかの実施形態では、バルーン部分2305A、2305B、2305C、及び2305Dは、カテーテルシャフト2306の周囲に、ほぼ等しい角度幅(すなわち、±5パーセント以内の、等しい角度幅)を有する。具体例として、図23A及び図23Bに示すように、各バルーン部分2305A、2305B、2305C、及び2305Dは、ほぼ45度の角度幅を有する。他の実施形態では、バルーン部分2305A、2305B、2305C、又は2305Dのうちの1つ又は複数は、バルーン部分2305A、2305B、2305C、又は2305Dのうちの他の1つ又は複数と異なる角度幅を有する。
[0319] バルーン部分2305A、2305B、2305C、及び2305Dは、それぞれ、膨張室2316A、2316B、2316C、及び2316Dを画定する壁2314A、2314B、2314C、及び2314Dを備える。膨張室2316A、2316B、2316C、及び2316Dは、それぞれ、バルーン部分2305A、2305B、2305C、及び2305Dを膨張させる膨張流体(例えば、約80パーセント(すなわち、80パーセント±5パーセント)の生理食塩水及び約20パーセント(すなわち、20パーセント±5パーセント)の造影剤溶液)を受容するよう適合される。以下でさらに詳細に説明するように、膨張室2316A、2316B、2316C、及び2316Dは、バルーン部分2305A、2305B、2305C、及び2305Dを容易に別々に膨張及び収縮させるように、互いに選択的に分離できる。したがって、バルーン部分2305A、2305B、2305C、及び2305Dは、単一のバルーンの部分ではなく、別々のバルーンと見なされる。
[0320] いくつかの実施形態では、バルーン部分の壁2314A、2314B、2314C、及び2314Dは、1種又は複数種類の比較的柔軟な材料で形成される。かかる材料は、比較的高い拡張力を血管に加えることなく、様々な直径の血管、不規則性を有する血管、及び/又は(心臓リードなどの)植え込まれた物体を保持する血管を、容易に満たす。バルーン部分2305A、2305B、2305C、及び2305Dは、ポリウレタンなどの1種又は複数種類のエラストマ材料で形成される。バルーン部分2305A、2305B、2305C、及び2305Dは、例えば、The Lubrizol Corporationから入手可能な、Pellethane(登録商標)、具体的には80AE Pellethane(登録商標)で形成される。
[0321] 上記で簡単に説明したように、膨張室2316A、2316B、2316C、及び2316Dは、バルーン部分2305A、2305B、2305C、及び2305Dを容易に別々に膨張及び収縮させるように、互いに選択的に分離できる。いくつかの実施形態では、このように容易に別々に膨張及び収縮させるために、閉塞バルーンデバイス2302は、図23Cの水圧回路図に模式的に示す構成要素を備える。より具体的には、閉塞バルーンデバイス2302のハブ2308は、膨張流体源2320(例えば、注射筒)に着脱可能に連結する注入ポート2318を備える。膨張流体源2320は、ハブ2308及びカテーテルシャフト2306内の膨張ルーメン2322に膨張流体を送達する。バルーン部分2305A、2305B、2305C、及び2305Dは、それぞれ流量調整器(例えば、弁)2324A、2324B、2324C、及び2324D(例えば、2位置、2方向弁)を通って膨張ルーメン2322に連結される。いくつかの実施形態では、バルーン部分2305A、2305B、2305C、及び2305Dがそれぞれ膨張し、各バルーン部分2305A、2305B、2305C、及び2305Dが別々に収縮できる場合、弁2324A、2324B、2324C、及び2324Dは、自動的に閉じることができる。いくつかの実施形態では、弁2324A、2324B、2324C、及び2324Dは、手動で閉じ、且つ/又は開くことができる。いくつかの実施形態では、弁2324A、2324B、2324C、及び2324Dは、コントローラ2326及び1つ又は複数のユーザ入力2328(作動可能な釦など)によって制御され得る。
[0322] いくつかの実施形態では、別の例として、閉塞バルーンデバイス2302は、図24の水圧回路図に模式的に示す構成要素を備える。より具体的には、閉塞バルーンデバイス2302のハブ2308は、1つ又は複数の膨張流体源2420(例えば、注射筒)に着脱可能に連結する第1のポート2418A、第2のポート2418B、第3のポート2418C、及び第4のポート2418Dを備える。単一の膨張流体源2420が、相異なる時間にポート2418A、2418B、2418C、2418Dに連結するか、又は複数の膨張流体源2420が、1つ又は複数のポート2418A、2418B、2418C、2418Dに同時に連結する。いずれの場合でも、膨張流体源2420は、ハブ2308及びカテーテルシャフト2306内に配置されている、ポート2418A、2418B、2418C、2418Dにそれぞれ連結された第1の膨張ルーメン2422A、第2の膨張ルーメン2422B、第3の膨張ルーメン2422C、及び第4の膨張ルーメン2422Dに膨張流体を送達する。膨張ルーメン2422A、2422B、2422C、及び2422Dは、それぞれ、弁2424A、2424B、2424C、及び2424D(例えば、2位置、2方向弁)を通って、バルーン部分2305A、2305B、2305C、及び2305Dにそれぞれ連結される。いくつかの実施形態では、弁2424A、2424B、2424C、及び2424Dは、膨張流体源2420に連結されると自動的に開き、膨張流体源2420から連結解除されると自動的に閉じることができる。いくつかの実施形態では、弁2424A、2424B、2424C、及び2424Dは、手動で閉じ、且つ/又は開くことができる。
[0323] 図25A〜図25Cは、本開示の実施形態による、血管の穿孔を治療する例示的な方法を示す。本方法は、ブロック2502で、上記の図23A〜図23C及び図24に描かれた閉塞バルーンデバイス2302などの閉塞バルーンデバイスを準備するステップから始まる。話を簡単にするために、この段落では、閉塞バルーンデバイス2302の機能を参照する。ブロック2504で、図25Bに示すように、カテーテルシャフト2306及び膨張していないバルーン2304を、血管102内で、膨張可能なバルーン2304が穿孔108に近接して配置されるまで前進させる。いくつかの実施形態では、カテーテルシャフト2306の第1のルーメン2307は、ガイドワイヤ又は植え込まれた心臓リードを受容し、カテーテルシャフト2306及び膨張可能なバルーン2304は、ガイドワイヤ又は植え込まれた心臓リードに沿って前進する。いくつかの実施形態では、大腿骨イントロデューサシース(例えば、12Fの大腿骨イントロデューサシース)を使用することにより、カテーテルシャフト2306を、大腿静脈(例えば、右大腿静脈)を通して穿孔まで前進させる。ブロック2506で、膨張流体(例えば、上記のような生理食塩水及び造影剤溶液)が、バルーン部分2305A、2305B、2305C、及び2305Dのすべて、又は1つを除くすべてに送達され、それにより、バルーン部分2305A、2305B、2305C、及び2305Dを膨張状態まで膨張させる。例えば、膨張流体は、バルーン部分2305A、2305B、2305C、及び2305Dのすべてに送達され、それにより、バルーン部分2305A、2305B、2305C、及び2305Dのすべてを膨張状態まで膨張させる。別の例として、膨張流体は、バルーン部分2305A、2305B、及び2305Cに送達され、それにより、バルーン部分の1つを除くすべてを膨張状態まで膨張させる。ブロック2508で、バルーン部分の1つ、例えばバルーン部分2305Dは、膨張したバルーン部分、例えばバルーン部分2305A、2305B、及び2305Cが膨張状態にある間、収縮状態に維持される。バルーン部分は、以前に膨張状態にあった場合は、バルーン部分を収縮させた後に収縮状態に維持されるか、又はバルーン部分は、以前から膨張状態にない。ブロック2510で、収縮したバルーン部分、例えば、バルーン部分2305Dが収縮状態にあり、他のバルーン部分、例えば、バルーン部分2305A、2305B、及び2305Cが膨張状態にある間に、造影剤の流体が血管102に送達される。ブロック2512で、収縮したバルーン部分、例えば、バルーン部分2305Dが収縮状態にあり、他のバルーン部分、例えば、バルーン部分2305A、2305B、及び2305Cが膨張状態にある間に、造影剤の流体の流路を観察する。造影剤の流体は、医療画像化、具体的にはX線透視法によって観察される。判断ブロック2514で、造影剤の流体が穿孔108を通って血管102から出る場合、それにより、図25Cに示すように、穿孔108が収縮したバルーン部分、例えばバルーン部分2305Dに隣接していると判断される。次いで、本方法は、膨張流体を以前に収縮していたバルーン部分、例えばバルーン部分2305Dに送達するステップによるブロック2516に進み、それにより、バルーン部分2305A、2305B、2305C、及び2305Dのすべてを膨張状態まで膨張させる。ブロック2518で、膨張したバルーン部分、例えば、バルーン部分2305A、2305B、及び2305Dが膨張状態にある間に、以前に収縮していたバルーン部分以外のバルーン部分のうちの1つ、例えばバルーン部分2305Cが、例えば、膨張流体をそこから除去するステップにより、収縮状態まで収縮される。本方法は、ブロック2510(血管102へ造影剤の流体を送達するステップ)、ブロック2512(造影剤の流体の流路を観察するステップ)、及び判断ブロック2514(造影剤の流体が穿孔108を通って血管102から出るかどうかを検討するステップ)を繰り返すステップに進む。造影剤の流体が穿孔108を通って血管102から出る場合(これは、デバイス2302が血管120に対して移動していない限り起こり難い)、本方法はブロック2516、ブロック2518などを繰り返す。しかし、造影剤の流体が穿孔108を通って血管102から出ない場合(上記の最初の段階を含む、判断ブロック2514のいずれかの段階で)、それにより、デバイス2302が穿孔108を閉塞したと判断される。かかる状況で、本方法は、収縮したバルーン部分、例えば、バルーン部分2305Cを収縮状態に維持するステップによるブロック2520に進み、収縮したバルーン部分に対する、又は収縮したバルーン部分を通った血管102内の血液の灌流を可能にする。いくつかの状況では、バルーンデバイス2302は、外科医が穿孔108を修復する準備ができるまで、かかる構成のまま保持される。ブロック2522で、例えば、そこから膨張流体を除去するステップによって膨張したバルーン部分を収縮させ、バルーンデバイス2302を血管102から除去する。
[0324] 上記の方法は、様々なやり方で変更され得る。例えば、相異なる数のバルーン部分が、同時に膨張状態又は収縮状態になり得る。より具体的には、1つを除くすべてよりも少ない数のバルーン部分が同時に膨張状態にあってもよく、バルーン部分のうちの2つ以上が同時に収縮状態にあってもよい。
[0325] 場合によっては、上記の方法は、どのバルーン部分が血管の穿孔に隣接しているかを必ずしも判断しないであろう。すなわち、判断ブロック2514の最初の段階で造影剤の流体が穿孔を通って血管から出ない場合(すなわち、複数のバルーン部分の最初の膨張で穿孔が閉塞される場合)、どのバルーン部分が穿孔を閉塞していたかは明らかではない。しかし、状況によっては、どのバルーン部分が血管の穿孔に隣接しているかを判断することは重要である(例えば、外科医による修復を容易にするため)。かかる状況では、バルーンデバイスは下記に説明する方法にしたがって使用される。
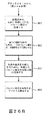
図26A〜図26Bは、本開示の実施形態による、血管の穿孔を治療する例示的な方法を示す。本方法は、ブロック2602で、上記の図23A〜図23C及び図24に描かれた閉塞バルーンデバイス2302などの閉塞バルーンデバイスを準備するステップから始まる。話を簡単にするために、この段落では、閉塞バルーンデバイス2302の機能を参照する。ブロック2604では、カテーテルシャフト2306及び膨張していないバルーン2304を、血管内で、膨張可能なバルーン2304が穿孔に近接して配置されるまで前進させる。いくつかの実施形態では、カテーテルシャフト2306の第1のルーメン2307は、ガイドワイヤ又は植え込まれた心臓リードを受容し、カテーテルシャフト2306及び膨張可能なバルーン2304は、ガイドワイヤ又は植え込まれた心臓リードに沿って前進する。いくつかの実施形態では、大腿骨イントロデューサシース(例えば、12Fの大腿骨イントロデューサシース)を使用することにより、カテーテルシャフト2306を、大腿静脈(例えば、右大腿静脈)を通して穿孔まで前進させる。ブロック2606で、膨張流体(例えば、上記のような生理食塩水及び造影剤溶液)が、バルーン部分2305A、2305B、2305C、及び2305Dのすべて、又は1つを除くすべてに送達され、それにより、バルーン部分2305A、2305B、2305C、及び2305Dを膨張状態まで膨張させる。例えば、膨張流体は、バルーン部分2305A、2305B、2305C、及び2305Dのすべてに送達され、それにより、バルーン部分2305A、2305B、2305C、及び2305Dのすべてを膨張状態まで膨張させる。別の例として、膨張流体は、バルーン部分2305A、2305B、及び2305Cに送達され、それにより、1つを除くすべてのバルーン部分を膨張状態まで膨張させる。ブロック2608で、バルーン部分の1つ、例えばバルーン部分2305Dは、膨張したバルーン部分、例えばバルーン部分2305A、2305B、及び2305Cが膨張した状態にある間、収縮状態に維持される。バルーン部分は、以前に膨張状態にあった場合は、バルーン部分を収縮させた後に収縮状態に維持されるか、又はバルーン部分は、以前から膨張状態にない。ブロック2610で、収縮したバルーン部分、例えば、バルーン部分2305Dが収縮状態にあり、他のバルーン部分、例えば、バルーン部分2305A、2305B、及び2305Cが膨張状態にある間に、造影剤の流体が血管に送達される。ブロック2612で、収縮したバルーン部分、例えば、バルーン部分2305Dが収縮状態にあり、他のバルーン部分、例えば、バルーン部分2305A、2305B、及び2305Cが膨張状態にある間に、造影剤の流体の流路を観察する。造影剤の流体は、医療画像化、具体的にはX線透視法によって観察される。標的とされる血管構造内への造影剤のボーラスの注入は、造影剤源(例えば、ポートを介した注射筒)又は異なる医療器具と連通する閉塞バルーンデバイス2302のノズルを通して実行される。代替実施形態では、医療画像化は、コンピュータ断層撮影血管造影を含む放射線血管造影(RA)、磁気共鳴血管造影(MRA)、又は超音波画像化(UI)など、十分に確立された技法を使って行われる。それぞれの画像化モダリティについて、造影剤、例えばRA用の放射線造影剤、MRA用のガドリニウムベースの物質、体外又は体内UI用のマイクロバブルを含むエコー源性造影剤が利用可能である。
判断ブロック2614で、造影剤の流体が穿孔を通って血管から出ない場合、どのバルーン部分が穿孔に隣接し、それにより穿孔を閉塞していたかは明らかではない。次いで、本方法は、膨張流体を以前に収縮していたバルーン部分、例えばバルーン部分2305Dに送達するステップによるブロック2616に進み、それにより、バルーン部分2305A、2305B、2305C、及び2305Dのすべてを膨張状態まで膨張させる。ブロック2618で、膨張したバルーン部分、例えば、バルーン部分2305A、2305B、及び2305Dが膨張状態にある間に、以前に収縮していたバルーン部分以外のバルーン部分のうちの1つ、例えばバルーン部分2305Cは、例えば、膨張流体をそこから除去するステップにより、収縮状態まで収縮される。本方法は、ブロック2610(血管へ造影剤の流体を送達するステップ)、ブロック2612(造影剤の流体の流路を観察するステップ)、及び判断ブロック2614(造影剤の流体が穿孔を通って血管から出るかどうかを検討するステップ)を繰り返すステップに進む。本方法は、造影剤の流体が穿孔を通って血管から出ない場合、ブロック2616、ブロック2618などを繰り返す。しかし、造影剤の流体が穿孔を通って血管から出る場合、それにより穿孔が収縮したバルーン部分に隣接していると判断される。かかる状況で、本方法は、膨張流体を以前に収縮していたバルーン部分(すなわち、穿孔に隣接するバルーン部分)に送達するステップによるブロック2620に進み、それにより、バルーン部分2305A、2305B、2305C、及び2305Dのすべてを膨張状態まで膨張させ、穿孔を閉塞する。ブロック2622で、穿孔に隣接するバルーン部分以外のバルーン部分の1つが、他のバルーン部分が膨張状態にある間に、例えば、膨張流体をそこから除去するステップにより、収縮状態まで収縮される。本方法は、収縮したバルーン部分を収縮状態に維持するステップによるブロック2624に進み、収縮したバルーン部分に対する、又は収縮したバルーン部分を通った血管内の血液の灌流を可能にする。いくつかの状況では、バルーンデバイス2302は、外科医が穿孔を修復する準備ができるまで、かかる構成のまま保持される。ブロック2626で、例えば、そこから膨張流体を除去するステップによって膨張したバルーン部分を収縮させ、バルーンデバイス2302を血管から除去する。
[0326] 本開示のいくつかの変形形態及び修正形態を使用することができる。本開示のいくつかの機能を、他の機能を実現することなく、提供することが可能である。
[0327] 本開示は、様々な態様、実施形態、及び構成において、様々な態様、実施形態、構成、それらの部分的組合せ及びそれらのサブセットを含む、本明細書に実質的に示され説明された構成要素、方法、プロセス、システム及び/又は装置を含む。当業者は、本開示を理解した後に、様々な態様、実施形態、及び構成をどのようにして作成し使用するかを理解するであろう。本開示は、様々な態様、実施形態、及び構成において、例えば、性能を向上する、容易さを達成する、且つ/又は実施コストを低減するための、以前のデバイス又はプロセスで使用されてきたようなものがない場合を含む、本明細書に、又は本明細書の様々な態様、実施形態、構成に示されていない、且つ/又は説明されていないものがないデバイス及びプロセスの提供を含む。
[0328] 本開示の前述の説明は、例示及び説明の目的で提示されている。上記は、本開示を本明細書に開示された形態、又は複数の形態に限定することを意図したものではない。例えば前述の、発明を実施するための形態において、本開示の様々な特徴は、本開示を合理化する目的で、1つ又は複数の態様、実施形態、及び構成にまとめられている。本開示の態様、実施形態、及び構成の特徴は、上記で論じたもの以外の代替の態様、実施形態、及び構成に組み合わせてもよい。この開示の方法は、請求された開示が、各請求項に明示的に列挙されているものよりも多くの特徴を必要とするという意図を反映していると解釈されるべきではない。むしろ、以下の特許請求の範囲が反映するように、発明の態様は、単一の前述の開示された態様、実施形態、及び構成のすべての特徴より少ない部分にある。したがって、以下の特許請求の範囲はここに、この発明を実施するための形態に組み入れられ、各請求項は、本開示の別々の好ましい実施形態としてそれ自体で成り立つ。
[0329] さらに、本開示の説明は、1つ又は複数の態様、実施形態、又は構成並びに特定の変形形態及び修正形態の説明を含んでいるが、他の変形形態、組合せ、及び修正形態が、例えば、本開示を理解した後の、当業者の技能及び知識の範囲内にあるように、本開示の範囲内にある。請求されたものに対する代替の、交換可能な、且つ/又は同等の構造、機能、範囲、又はステップを含む、許容される範囲での代替の態様、実施形態、及び構成を含む権利を取得することを意図しており、かかる代替の、交換可能な、且つ/又は同等の構造、機能、範囲、又はステップが、本明細書に開示されているか否かにかかわらず、特許性のあるいかなる主題をも公に捧げることを意図するものではない。