JP2020007240A - ベンズアミド化合物の製造方法 - Google Patents
ベンズアミド化合物の製造方法 Download PDFInfo
- Publication number
- JP2020007240A JP2020007240A JP2018127418A JP2018127418A JP2020007240A JP 2020007240 A JP2020007240 A JP 2020007240A JP 2018127418 A JP2018127418 A JP 2018127418A JP 2018127418 A JP2018127418 A JP 2018127418A JP 2020007240 A JP2020007240 A JP 2020007240A
- Authority
- JP
- Japan
- Prior art keywords
- methyl
- compound
- pyridin
- amino
- pyrimidin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Abstract
Description
[1] 4-メチル-N-[3-(4-メチル-1H-イミダゾール-1-イル)-5-(トリフルオロメチル)フェニル]-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}ベンズアミド(ニロチニブ)の製造方法であって、
(1)オレフィン化合物の存在下で、4-メチル-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}-安息香酸に塩化チオニルを反応させて、4-メチル-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}-安息香酸クロリドを得る工程、及び
(2)工程(1)で得られた4-メチル-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}-安息香酸クロリドに、3-(4-メチル-1H-イミダゾール-1-イル)-5-(トリフルオロメチル)アニリンを反応させる工程、
を包含する、製造方法。
[2] オレフィン化合物が、シクロヘキセン又はスチレンである、[1]に記載の製造方法。
[3] 4-メチル-N-[3-(4-メチル-1H-イミダゾール-1-イル)-5-(トリフルオロメチル)フェニル]-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}ベンズアミド中の核塩素化物の含有量が0.06%未満である、[1]又は[2]に記載の製造方法。
工程1では、化合物[1]と塩化チオニルとを、オレフィン化合物の存在下に反応させて化合物[2]を得る。工程1の反応は、化合物[1]とオレフィン化合物との混合物に塩化チオニルを添加する方法で実施するのが好ましい。
工程2では、工程1で得られた化合物[2]及び化合物[3]を混合することにより、化合物[4]を得る。
<高速液体クロマトグラフィー(HPLC)分析条件>
・測定機器:島津製作所製LC20A
・カラム:InertSustain C18 4.6×150mm, 3μm
・移動相:A液 炭酸アンモニウム水(1.57g/1L)
B液 メタノール
・グラジエント条件:
N-メチル-2-ピロリドン 400mLに、化合物[1] 80.0g (261mmol)、及びシクロヘキセン0.43g (5.2mmol)を加え、20-40℃において塩化チオニル43.5g(366mmol)を滴下後、60℃に昇温し、1h反応した。反応終点を確認後、反応マスに、化合物[3] 63.0g (261mmol)をN-メチル-2-ピロリドン400mLに溶解した溶液を滴下し、60℃で3h反応した。反応マスに水 400mLを流入後、80℃まで昇温し、20%KOH水溶液83.0gを滴下し、80℃で3h以上保温した。続いて、20%KOH水溶液112.3gを1h以上かけて滴下した。60℃に冷却後、40%K2CO3水溶液45.2gを滴下した後、約2hかけて40℃まで冷却し、保温後、濾過し、40℃に保温した20%メタノール水 480mL、メタノール320mLで洗浄した。得られた結晶を減圧乾燥し、化合物[4] (ニロチニブ)128.6g(収率 93.0%)を得た。LCクロマトグラムにおける目的物のピークの面積百分率は、99.96%(核塩素化物は、検出されなかった)であった。
シクロヘキセンを用いないこと以外は、上記実施例1と同様に反応を行った。LCクロマトグラムにおける目的物のピークの面積百分率: 99.85%(核塩素化物 0.06%-LC/MS:ESI(+) 564[M+H]+)
ニロチニブ80.0g(151.1mmol)、メタノール969mL、及びアセトン 242mLを仕込み、50℃に昇温した。この混合物に35%塩酸 17.3g(166.2mmol)を滴下し、1h保温することによりほぼ溶液となった。濾過により不溶成分を除去し、メタノール40mLで洗浄した。濾洗液はあらかじめアセトン 1274mL、水 8.8mLを仕込み50℃に温調した溶液中に受け入れた。この溶液を45℃に冷却し、種晶を接種後、保温により結晶を析出させた。スラリー液を約6hかけて-10℃に冷却し、保温後、濾過し、-10℃に調整したアセトン320mL及び水5.6mLの混媒で洗浄した。得られた結晶を減圧乾燥してニロチニブ塩酸塩水和物76.3g (収率84.6%)を得た。LCクロマトグラムにおける目的物のピークの面積百分率は、100%であった。
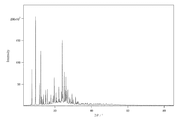
測定範囲 : 3.0 〜 84.993°/2θ, ステップ幅 : 0.017°, 積算時間 : 10664.6 sec. , 管電圧・管電流 : 40kV, 40mA
ニロチニブ50.0g(94.4mmol)、及びメタノール750mLを仕込み、55℃に昇温した。この混合物に35%塩酸 10.8g(103.9mmol)を滴下し、1h保温することによりほぼ溶液となった。濾過により不溶成分を除去し、メタノール25mLで洗浄した。この溶液を40℃に冷却し、種晶を接種後、保温により結晶を析出させた。スラリー液を約5hかけて-10℃に冷却し、保温後、濾過し、-10℃に調整したメタノール 200mLで洗浄した。得られた結晶を恒量となるまで減圧乾燥した後、40%RH以上に調湿した窒素を通気させてニロチニブ塩酸塩水和物47.4g (収率86.0%)を得た。LCクロマトグラムにおける目的物のピークの面積百分率は、99.96%であった。
測定範囲 : 3.0 〜 84.993°/2θ, ステップ幅 : 0.017°, 積算時間 : 14930.4 sec. , 管電圧・管電流 : 40kV, 40mA
Claims (3)
- 4-メチル-N-[3-(4-メチル-1H-イミダゾール-1-イル)-5-(トリフルオロメチル)フェニル]-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}ベンズアミドの製造方法であって、
(1)オレフィン化合物の存在下で、4-メチル-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}-安息香酸に塩化チオニルを反応させて、4-メチル-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}-安息香酸クロリドを得る工程、及び
(2)工程(1)で得られた4-メチル-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}-安息香酸クロリドに、3-(4-メチル-1H-イミダゾール-1-イル)-5-(トリフルオロメチル)アニリンを反応させる工程、
を包含する、製造方法。 - オレフィン化合物が、シクロヘキセン又はスチレンである、請求項1に記載の製造方法。
- 4-メチル-N-[3-(4-メチル-1H-イミダゾール-1-イル)-5-(トリフルオロメチル)フェニル]-3-{[4-(ピリジン-3-イル)ピリミジン-2-イル]アミノ}ベンズアミド中の核塩素化物の含有量が0.06%未満である、請求項1又は2に記載の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018127418A JP2020007240A (ja) | 2018-07-04 | 2018-07-04 | ベンズアミド化合物の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018127418A JP2020007240A (ja) | 2018-07-04 | 2018-07-04 | ベンズアミド化合物の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2020007240A true JP2020007240A (ja) | 2020-01-16 |
Family
ID=69150651
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018127418A Ceased JP2020007240A (ja) | 2018-07-04 | 2018-07-04 | ベンズアミド化合物の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2020007240A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113214225A (zh) * | 2020-01-21 | 2021-08-06 | 安礼特(上海)医药科技有限公司 | 一种制备尼洛替尼单盐酸盐二水合物晶型a的方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08208538A (ja) * | 1989-04-07 | 1996-08-13 | Mitsui Toatsu Chem Inc | 芳香族側鎖塩素化物の安定化方法 |
| WO2004005281A1 (en) * | 2002-07-05 | 2004-01-15 | Novartis Ag | Inhibitors of tyrosine kinases |
| WO2006135641A2 (en) * | 2005-06-09 | 2006-12-21 | Novartis Ag | PROCESS FOR THE SYNTHESIS OF 5- (METHYL-lH-IMIDAZOL-l-YL) -3- (TRI FLUOROME TH YL) -BENZENEAMINE |
| WO2007015870A2 (en) * | 2005-07-20 | 2007-02-08 | Novartis Ag | Crystalline forms of 4-methyl-n-[3-(4-methyl-imidazol-1-yl)-5-trifluoromethyl-phenyl]-3-(4-pyridin-3-yl-pyrimidin-2-ylamino)-benzamide |
| WO2010009402A2 (en) * | 2008-07-17 | 2010-01-21 | Teva Pharmaceutical Industries Ltd. | Nilotinib intermediates and preparation thereof |
-
2018
- 2018-07-04 JP JP2018127418A patent/JP2020007240A/ja not_active Ceased
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08208538A (ja) * | 1989-04-07 | 1996-08-13 | Mitsui Toatsu Chem Inc | 芳香族側鎖塩素化物の安定化方法 |
| WO2004005281A1 (en) * | 2002-07-05 | 2004-01-15 | Novartis Ag | Inhibitors of tyrosine kinases |
| WO2006135641A2 (en) * | 2005-06-09 | 2006-12-21 | Novartis Ag | PROCESS FOR THE SYNTHESIS OF 5- (METHYL-lH-IMIDAZOL-l-YL) -3- (TRI FLUOROME TH YL) -BENZENEAMINE |
| WO2007015870A2 (en) * | 2005-07-20 | 2007-02-08 | Novartis Ag | Crystalline forms of 4-methyl-n-[3-(4-methyl-imidazol-1-yl)-5-trifluoromethyl-phenyl]-3-(4-pyridin-3-yl-pyrimidin-2-ylamino)-benzamide |
| WO2010009402A2 (en) * | 2008-07-17 | 2010-01-21 | Teva Pharmaceutical Industries Ltd. | Nilotinib intermediates and preparation thereof |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113214225A (zh) * | 2020-01-21 | 2021-08-06 | 安礼特(上海)医药科技有限公司 | 一种制备尼洛替尼单盐酸盐二水合物晶型a的方法 |
| CN113214225B (zh) * | 2020-01-21 | 2023-12-22 | 江苏希迪制药有限公司 | 一种制备尼洛替尼单盐酸盐二水合物晶型a的方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10626116B2 (en) | Crystalline form of BTK kinase inhibitor and preparation method thereof | |
| US11149017B2 (en) | Solid state forms of apalutamide | |
| US11542245B2 (en) | Preparative process | |
| CN107074776B (zh) | Copanlisib及其二盐酸盐的合成 | |
| TW201617319A (zh) | (2s,3s)7-氟-2-(4-氟苯基)-3-(1-甲基-1h-1,2,4-三唑-5-基)-4-側氧基-1,2,3,4-四氫喹啉-5-羧酸甲酯之共形成體鹽及其製備方法 | |
| EP3303304A1 (en) | Methods of making protein deacetylase inhibitors | |
| US11198684B2 (en) | Intermediates useful for the synthesis of a selective inhibitor against protein kinase and processes for preparing the same | |
| JP2014509642A (ja) | イマチニブ及びそのメシル酸塩の生成のための改良方法 | |
| US10144708B2 (en) | Crystalline arylalkylamine compound and process for producing the same | |
| US10710998B2 (en) | Compound and process | |
| WO2013065063A1 (en) | Anhydrous form of dasatinib, process for its preparation and its use | |
| JP2020007240A (ja) | ベンズアミド化合物の製造方法 | |
| WO2015011659A1 (en) | Crystalline polymorphic forms of regorafenib and processes for the preparation of polymorph i of regorafenib | |
| CN112654603A (zh) | 乐伐替尼的制备方法 | |
| WO2021241611A1 (ja) | 複素環化合物の製造方法 | |
| JP3884063B2 (ja) | セフカペンピボキシルのメタンスルホン酸塩 | |
| EP4063351A1 (en) | Preparation method of quinoline derivative compounds | |
| CN112624968B (zh) | 一种5-氨基-3-氰基吡啶甲酸甲酯盐酸盐的合成方法 | |
| EP4073051B1 (en) | Process and intermediate for the preparation of oxetan-2-ylmethanamine | |
| EP3584241B1 (en) | Method for producing indazole compound, and indazole compound | |
| EP3287448A1 (en) | Method for producing dicarboxylic acid compound | |
| WO2006072833A1 (en) | Imidazole derivatives as enzyme reverse transcriptase modulators | |
| EP3266773B1 (en) | Process for the preparation of lapatinib ditosylate monohydrate by means of an improved crystallization procedure | |
| JP2020040923A (ja) | オルメサルタンメドキソミルの製造方法 | |
| KR20240027678A (ko) | 4-아미노-n-(1-((3-클로로-2-플루오로페닐)아미노)-6-메틸이소퀴놀린-5-일)티에노[3,2-d]피리미딘-7-카르복스아미드의비스-메실레이트 염 및 이의 중간체의 합성 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210219 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20211111 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211207 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220104 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220517 |
|
| A045 | Written measure of dismissal of application [lapsed due to lack of payment] |
Free format text: JAPANESE INTERMEDIATE CODE: A045 Effective date: 20220927 |