JP2016522958A - 改質多結晶リチウム金属リン酸塩を含むセラミック電解質材料 - Google Patents
改質多結晶リチウム金属リン酸塩を含むセラミック電解質材料 Download PDFInfo
- Publication number
- JP2016522958A JP2016522958A JP2016505507A JP2016505507A JP2016522958A JP 2016522958 A JP2016522958 A JP 2016522958A JP 2016505507 A JP2016505507 A JP 2016505507A JP 2016505507 A JP2016505507 A JP 2016505507A JP 2016522958 A JP2016522958 A JP 2016522958A
- Authority
- JP
- Japan
- Prior art keywords
- modified
- lithium ion
- ion conductive
- polycrystalline
- polycrystalline lithium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Abandoned
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0561—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of inorganic materials only
- H01M10/0562—Solid materials
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M12/00—Hybrid cells; Manufacture thereof
- H01M12/04—Hybrid cells; Manufacture thereof composed of a half-cell of the fuel-cell type and of a half-cell of the primary-cell type
- H01M12/06—Hybrid cells; Manufacture thereof composed of a half-cell of the fuel-cell type and of a half-cell of the primary-cell type with one metallic and one gaseous electrode
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M50/00—Constructional details or processes of manufacture of the non-active parts of electrochemical cells other than fuel cells, e.g. hybrid cells
- H01M50/40—Separators; Membranes; Diaphragms; Spacing elements inside cells
- H01M50/403—Manufacturing processes of separators, membranes or diaphragms
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M50/00—Constructional details or processes of manufacture of the non-active parts of electrochemical cells other than fuel cells, e.g. hybrid cells
- H01M50/40—Separators; Membranes; Diaphragms; Spacing elements inside cells
- H01M50/409—Separators, membranes or diaphragms characterised by the material
- H01M50/431—Inorganic material
- H01M50/434—Ceramics
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M50/00—Constructional details or processes of manufacture of the non-active parts of electrochemical cells other than fuel cells, e.g. hybrid cells
- H01M50/40—Separators; Membranes; Diaphragms; Spacing elements inside cells
- H01M50/489—Separators, membranes, diaphragms or spacing elements inside the cells, characterised by their physical properties, e.g. swelling degree, hydrophilicity or shut down properties
- H01M50/497—Ionic conductivity
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02T—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO TRANSPORTATION
- Y02T10/00—Road transport of goods or passengers
- Y02T10/60—Other road transportation technologies with climate change mitigation effect
- Y02T10/70—Energy storage systems for electromobility, e.g. batteries
Abstract
少なくとも1つの表面;結晶粒界を備える多結晶リチウムイオン伝導性材料;及び少なくとも1つの改質相を備える、リチウム‐空気バッテリ用の多結晶リチウムイオン伝導性膜であって、ここで(a)少なくとも1つの改質相は、改質された結晶粒界を備える改質多結晶リチウムイオン導電性材料を形成するために結晶粒界に組み込まれるか;(b)少なくとも1つの改質相は、改質された表面を形成するために少なくとも1つの表面に組み込まれるか;又は(a)及び(b)の両方である、多結晶リチウムイオン伝導性膜を開示する。リチウムイオン、リチウム‐空気及びリチウム‐水バッテリを含む様々なリチウム系バッテリを開示し、また、多結晶リチウムイオン伝導性膜をこのようなバッテリ用途に使用できるようにするために改質するための方法も開示する。
Description
本出願は、米国特許法第120条の下で、2013年3月28日出願の米国特許出願第13/852491号の優先権の利益を主張するものであり、上記出願の内容全体は参照によって本出願に援用される。
本開示は一般に、リチウム‐空気セル中の固体電解質として使用するための、改質多結晶材料に関する。例示的な実施形態は、少なくとも1つの改質相の濃度が、多結晶材料の表面において又は結晶粒界に沿って上昇した、多結晶材料を含む。本開示の多結晶材料を用いて作製されたリチウムバッテリ、及び上記改質多結晶材料を作製する方法も開示される。
リチウムバッテリは、理論上のエネルギ密度及び比容量が高く、従って、ハイブリッド先進的電気自動車及び再生可能エネルギにおけるその応用の可能性に世界的な注目が集まっている。
リチウム‐空気(「Li‐空気」)、リチウム‐水(「Li‐水」)又はハイブリッドLi‐空気/Li‐水バッテリのいずれにおいて、リチウム金属アノードを使用してよく、またリチウム金属アノードは、その有利な電気化学的特性により好ましい場合が多い。しかしながらリチウム金属は、水との反応性が高い反応性アルカリ金属であり、リチウム金属を環境から隔離することが有益である。1つのアプローチは、アノードとカソードとの間に気密性シールを提供する固体電解質を使用することを含んでよい。
従来の固体電解質は環境安定性が低く、例えば水への曝露又は水中への浸漬時に溶解する、崩壊する、又は導電率の低下を示す。この低い環境安定性は、良好でない気密性シールによって湿気がリチウム金属アノードに到達できてしまう場合に、バッテリ性能の低下のみならず、潜在的な安全性の問題をもたらし得る。従って、固体電解質の環境安定性を改善することが望ましい。
本開示は、様々な実施形態において、リチウム‐空気(「Li‐空気」)、リチウム‐水(「Li‐水」)及び/又はハイブリッドLi‐空気/Li‐水セルのための固体電解質として使用するための、多結晶リチウムイオン伝導性膜に関する。この多結晶リチウムイオン伝導性膜は、少なくとも1つの表面と、結晶粒界を有する複数の粒子とを備え、金属酸化物又はリン酸塩から選択される少なくとも1つの改質相を更に備え、ここで上記金属は、Ge、Al、Ca、Y、Si、Mg、Ga、若しくは2価カチオン、3価カチオン、4価カチオン及び/又は5価カチオンを形成できる他のいずれの金属、並びにその組合せであり、上記少なくとも1つの改質相は:改質された結晶粒界を備える改質多結晶リチウムイオン伝導性材料を形成するために結晶粒界に組み込まれるか、又は結晶粒界及び少なくとも1つの表面の両方に組み込まれる。
様々な実施形態において、多結晶リチウムイオン伝導性膜は、未改質多結晶リチウムイオン伝導性材料よりも低い水によるエッチング速度、及び/又は未改質多結晶リチウムイオン伝導性材料よりも高い導電率を呈する。特定の実施形態では、改質された結晶粒界は、多結晶リチウムイオン伝導性材料の結晶粒界よりも低い水によるエッチング速度を呈する。
一実施形態では、多結晶リチウムイオン伝導性材料は、Li1+xAlxTi2‐x(PO4)3を含むリチウム金属リン酸塩であり、ここで0<x<0.6である。一実施形態では、改質された表面相はLi1+xAlxGeyTi2‐x‐y(PO4)3を含み、ここで0<x<0.6及び0<y<2であり、また改質された結晶粒界相は、ゲルマニウムに富む1つ又は複数の酸化物又はリン酸塩相、例えばGeO2を含む。
様々な実施形態において、改質された表面の厚さは約15マイクロメートル未満である。一実施形態では、多結晶リチウムイオン伝導性膜は、多結晶リチウムイオン伝導性膜の2つの対向する表面上に位置する2つの改質された表面を備え、これによって改質相濃度の勾配を有する構造が形成され、上記濃度は、上記構造の中央よりも上記対向する側部において高い。
様々な実施形態において、多結晶リチウムイオン伝導性材料は、多結晶リチウムイオン伝導性材料の理論上の密度の少なくとも92%の密度を示し、約5μm〜約500μmの厚さを有し、多結晶リチウムイオン伝導性膜を通したヘリウムの拡散が約10‐2cm3/m2/日となるように気密性であり、及び/又は約10‐4S/cmを超える導電率を有する。
固体電解質として上記多結晶リチウムイオン伝導性膜を備えるリチウムバッテリも開示される。このリチウムバッテリは、リチウムイオンバッテリ、リチウム‐空気バッテリ及び/又はリチウム‐水バッテリであってよい。
多結晶リチウムイオン伝導性膜を改質するための方法も開示される。この方法は:金属酸化物若しくはリン酸塩又はこれらの前駆体を含む組成物を調製するステップであって、ここで上記金属は、Ge、Al、Ca、Y、Si、Mg、Ga、若しくは2価カチオン、3価カチオン、4価カチオン及び/又は5価カチオンを形成できる他のいずれの金属、並びにその組合せである、ステップ;多結晶リチウムイオン伝導性膜の少なくとも1つの表面に上記組成物を塗布することによって、被覆された多結晶リチウムイオン伝導性膜を形成するステップ;並びに上記被覆された多結晶リチウムイオン伝導性膜をアニーリングして、改質相を備える改質された表面、改質相を備える結晶粒界、又は改質された表面及び改質された結晶粒界の両方を形成するステップを有してなる。
一実施形態では、上記組成物は、ゲルマニウムイソプロポキシド前駆体を用いたゾル‐ゲルプロセスによって作製されたGeO2粒子を含む。このGeO2粒子の平均粒径は20〜100nmであってよい。
一実施形態では、上記アニーリングは、温度が約700℃〜約1000℃の炉内において、約0.5〜12時間の時間に亘って実施される。
更なる目的及び利点は、その一部が以下の説明において列挙され、またその一部が以下の説明から明らかとなるか、又は本開示を実施することによって把握できる。これらの目的及び利点は、添付の請求項において特に指摘される要素及び組合せを用いて実現及び達成できる。
以上の概説及び以下の詳細な説明はいずれも単なる例示及び説明であり、請求されている本開示を制限するものではないことを理解されたい。
本明細書に組み込まれて本明細書の一部を構成する添付の図面は、いくつかの実施形態を図示しており、本説明と併せて、本開示の原理を説明する役割を果たす。
これより、本開示の実施形態に対する詳細な言及を行う。これらの実施形態の実施例は添付の図面に図示されている。可能な限り、全ての図面を通して、同一の又は同様の部分を指すために同一の参照番号を使用する。
本出願において使用される用語「リチウム‐空気セル(lithium‐air cell)」、「Li‐空気セル(Li‐air cell)」、「Li‐空気バッテリ(Li‐air battery)」及びその変化形は:リチウム系電極、例えばアノード;電解質;及び空気又は酸化剤含有ガスに対して開放されている多孔性電極、例えばカソードを含む、電気化学セルを意味する。
本出願において使用される用語「リチウム‐水セル(lithium‐water cell)」、「Li‐水セル(Li‐water cell)」、「Li‐水バッテリ(Li‐water battery)」及びその変化形は:リチウム系電極、例えばアノード;電解質;及び水又は酸化剤含有水溶液に対して開放されている多孔性電極、例えばカソードを含む、電気化学セルを意味する。
本出願において使用される用語「リチウムイオンセル(lithium‐ion cell)」、「Liイオンセル(Li‐ion cell)」、「Liイオンバッテリ(Li‐ion battery)」及びその変化形は:層間挿入されたリチウム化合物系電極、例えばアノード;電解質;及び電極、例えばカソードを含む、電気化学セルを意味する。
本出願において使用される用語「電解質(electrolyte)」及びその変化形は、リチウムイオンの輸送を可能とする材料を意味する。
本出願において使用される用語「カソード(cathode)」、「空気電極(air electrode)」、「水電極(water electrode)」及びその変化形は、Li‐空気セル、Li‐水セル及び/又はハイブリッドLi‐空気/Li‐水セルの、セルの放電中に酸素の還元が起こり、セルの充電中にO2の生成が起こる電極を意味する。
本出願において使用される用語「改質相(modifying phase)」及びその変化形は、改質されるバルク材料の組成とは異なる全体的な組成を有する固体材料を意味する。
本出願において使用される用語「多結晶(polycrystalline)」及びその変化形は、様々なサイズ及び配向の多数の粒子又は結晶子からなる材料を意味する。本出願において使用される用語「結晶粒界(grain boundary)」及びその変化形は、多結晶材料中の2つの粒子又は結晶子の間の境界面を意味する。
本出願において使用される用語「気密性(hermetic)」及びその変化形は、実質的に空気を通さない、及び/又は実質的に湿気に対して不浸透性であることを意味する。
本開示は、様々な例示的実施形態において、リチウム‐空気(「Li‐空気」)、リチウム‐水(「Li‐水」)及び/又はハイブリッドLi‐空気/Li‐水セルのための固体電解質として使用するための、改質多結晶材料に関する。改質相による多結晶材料の改質により、上記改質相で改質された結晶粒界及び/又は上記改質相で改質された表面若しくは領域を得ることができ、改質多結晶材料は、未改質多結晶材料よりも低い水によるエッチング速度及び/又は未改質多結晶材料よりも高い導電率を呈する。特定の実施形態では、改質多結晶材料のエッチングの速度が比較的低いことは、少なくとも部分的に、改質された結晶粒界が、未改質多結晶材料の結晶粒界よりも低い水によるエッチング速度を呈することによる。
多くの現実的な電気化学的対のうち、Li‐空気は、比容量及びエネルギ密度が最も高い。Li‐空気バッテリの理論上のエネルギ密度は、電解質及び反応生成物の性質に応じて5800〜11400Wh/kgであり、これはリチウムイオンの理論上のエネルギ密度である約400Wh/kgを大きく上回る。従ってLi‐空気セルは世界的に注目を集めており、ハイブリッド先進的電気自動車及び再生可能エネルギにおける応用の可能性は高い。
Li‐空気セルでは、放電中、リチウムはリチウム金属アノードにおいて酸化され、環境から直接取得された酸素は空気カソードにおいて還元されて、電流が生成される。電解質は電極間でリチウムイオンを輸送する。非プロトン性、水性、混合水性‐非プロトン性及び固体を含む、4つの主要なタイプのLi‐空気セルが存在する。非プロトン性Li‐空気セルは一般に、リチウム金属アノード、液体有機及び/又は非水性電解質、並びに多孔性炭素カソードを含む。水性Li‐空気セルは、水性電解質を使用すること以外は非プロトン性セルと同様である。混合水性‐非プロトン性Li‐空気セルは典型的には、リチウム金属アノード側の有機電解質、カソード側の水性電解質、及び有機電解質を水性電解質から分離するリチウム伝導性膜を含む。固体Li‐空気セルは、リチウムアノード、セラミック及び/又はガラスから作製される固体電解質、並びに多孔性炭素カソードを含む。
Li‐水セルもまた、極めて高いエネルギ密度及び大きな比容量を有する。Li‐水バッテリでは、放電中、リチウムはリチウム金属アノードにおいて酸化され、水又は食塩水若しくは海水等の水溶液から取得された酸素は水カソードにおいて還元されて、電流が生成される。Li‐空気バッテリと同様に、電解質は電極間でリチウムイオンを輸送する。Li‐水バッテリの1つのタイプは、ハイブリッドLi‐空気/Li‐水セルであり、これには、リチウム金属アノード及び任意に固体又は液体の境界面を含むLi‐空気側と、固体電解質及び水カソードを含むLi‐水側とが組み込まれる。上記任意の固体又は液体の中間層は、リチウム金属アノードと固体電解質との間又はリチウム金属アノードとカソードとの間に位置し、リチウム金属アノードをLi‐水側から隔離できる。
Li‐空気、Li‐水又はハイブリッドLi‐空気/Li‐水セルのいずれにおいて、リチウム金属アノードを使用してよく、またリチウム金属アノードは、その有利な電気化学的特性により好ましい場合が多い。しかしながらリチウム金属は、水との反応性が高い反応性アルカリ金属であり、リチウム金属アノードから湿気を離間させて維持することは必須である。Li‐空気バッテリを用いた場合の魅力的な電気的特性結果が示されているものの、これらの結果は、乾燥した純粋な酸素又は乾燥した酸素及び窒素の混合ガス下で得られたものである。例えば電気自動車といった多くの実際の応用において、空気カソード上の空気中の全ての湿気を回避することは困難であり、また本来的に、又はカソードからの水の輸送によって、電解質も水を含有する場合がある。水カソードからの湿気もまた同様に、リチウム金属アノードから隔離するべきである。
従って、現実的な動作のためのLi‐空気、Li‐水及びハイブリッドLi‐空気/Li‐水バッテリの実際の使用を制限し得る課題は、水及び/又は湿気を含有する条件におけるリチウムアノードの安定性である。この課題の1つの解決策は、アノードとカソードとの間に気密性シールを提供する固体電解質を用いることを含み得る。
カソードは、空気、若しくは例えば酸素である酸化剤を含有する他のいずれのガスに対して開放されている空気カソード、又は水、若しくは例えば酸素である酸化剤を含有する水溶液に対して開放されている水カソードとすることができる。空気、ガス、水及び/又は水溶液からの湿気は、カソードに浸透して固体電解質に到達する。従って、現実的な動作のためのLi‐空気、Li‐水及びハイブリッドLi‐空気/Li‐水バッテリの実際の使用を制限する別の課題は、水及び/又は湿気を含有する条件における固体電解質の安定性である。
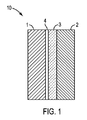
提案される1つの解決策は、NASICONタイプLiM2(PO4)3をベースとした水安定性リチウム伝導性固体電解質を用いて保護リチウム電極(「PLE」)を形成することを含み、ここでMはTi、Ge、Sn、Zr及び/又はHfである。この構造は、MO6八面体及びPO4四面体の開放型3次元フレームワークからなる。これらの多面体はこれらの角によって連結されて、3次元チャネルを提供する[M2(PO4)3]‐剛性スケルトンを形成し、上記3次元チャネルを通してリチウムイオンが移動できる。PLEバッテリ系の主要な構成要素は、高いリチウム伝導性、気密性膜及び水中での高い安定性を必要とする固体電解質である。図1は、保護リチウム電極(PLE)バッテリの概略図である。しかしながら、好適かつ水安定性の固体電解質の不在により、このようなPLEバッテリの開発は妨げられてきた。
Li、Al、Ti及びPを含む固体電解質の安定性は、水に曝露された場合に悪影響を受ける場合があることが公知である。例えば固体電解質Li1+x+yAlxTi2‐xP3‐ySiyO12は、1ヶ月に亘る水中での浸漬後、導電率の低下を呈し、又はゾル‐ゲルプロセスを経たLATP(Li1.3Al0.3Ti1.7(PO4)3)は、100時間に亘る蒸留水中での浸漬後、その重量を有意に失う場合がある。ガラス‐セラミックプロセスによって調製されたLATP膜においても、水道水への65日間の曝露後に僅かな変質が発生した。
LiTi2(PO4)3の誘導体であるLi1.4Al0.4Ti1.6(PO4)3(「LATP」)のセラミック膜は、10‐4S/cmという高い導電率及び低い多孔率を呈し、また染色試験による漏れを全く呈しない。しかしながら、リチウムバッテリのセラミック電解質としてのLATP膜の安定性試験は、LATP膜が、水性電解質中で室温で試験した場合の溶解によって、有意量のリチウム及びリンを溶出させてしまうことを示している。
代替的な固体電解質膜であるLi1.4Al0.4Ge1.6(PO4)3(「LAGP」)は、2000時間を超える水性電解質試験において、少ない溶出を示した。従ってLAGPは、Li‐空気、Li‐水又はハイブリッドLi‐空気/Li‐水セルにおける使用のための高い安定性を有する、有望なセラミック電解質である。しかしながら、LAGPの調製に使用されるゲルマニウムのコストの高さは、経済的効率を低下させ、市場での大規模な実行可能性を妨げる可能性がある。
従って、例えば表面改質によってLATP膜を改質して、セラミック電解質のバルク組成物及び構造を変化させるのではなく、その環境安定性を改善することが望ましい。
現行の表面改質戦略は、大まかに以下の3つのカテゴリに分類できる:1)表面に望ましい材料機能を付与するもの;2)既存の表面をより望ましい組成及び/又はトポグラフィーに変換するもの;並びに3)表面材料を除去することによって表面トポグラフィーを変化させるもの。表面を改質するために、物理蒸着、プラズマスプレーコーティング、イオン注入、表面機械加工、グリットブラスト処理、パルスレーザ堆積、圧縮成形プロセス、ナノ及びマイクロ押込、スパッタリング、電気化学堆積、化学蒸着、化学エッチング、ゾル‐ゲルプロセス並びに高分子吸着を含む、様々な物理的及び化学的技術が適用されている。
これらの技術のうち、ゾル‐ゲルプロセスは、その独自の特徴により極めて魅力的である。物理蒸着法又は化学蒸着法と比較して、ゾル‐ゲル技術は、いずれの高真空系を必要とせず、また:様々な基材にコーティングを容易に塗布できること:面積が大きい基材を被覆できること;コスト効率の高さ;必要な前駆体の量が少ないこと;結果として得られる薄く密で均一なフィルム;低温加工;コーティングが呈する割れが少ないこと;基材への強力な接着;及び表面材料の特性を変化させる能力の大きさといった、複数のその他の利点を有する。
GeO2を調製するために、様々なゾル‐ゲル法を使用してよく、上記ゾル‐ゲル法は、ITO及び/又はガラス基材上に前駆体ゾルをスピンコート堆積するステップ;並びに結果として得られたフィルムを500℃〜700℃の様々な温度でアニーリングするステップを含む、ゲルマニウムイソプロポキシド及び2‐プロパノールを用いる方法を含む。更に、電界紡糸法及びそれに続く高温でのか焼によって、ポリ(酢酸ビニル)及び二酸化ゲルマニウムゾルを用いて、GeO2のマイクロメートルスケールからサブマイクロメートルスケールの繊維を合成できる。ゲルマニウムメトキシドの制御された加水分解、及びそれに続く、反応溶媒アセトニトリルの高速超臨界抽出による、モノリシックな3次元GeO2ナノ構造化エアロゲルのゾル‐ゲル合成が報告されている。ゾル‐ゲル由来のGeO2:SiO2ガラス質フィルムが開発されており、これは光学的な用途のためにケイ素又はIII‐V基材上にスピンコートされる。他の用途としては:PVPゾル‐ゲルコーティング法を用いた、Li1+xAlxTi2‐x(PO4)3固体電解質上のLiMn2O4薄層電極の調製;及びLiMn2O4粉末をLATPコーティング溶液中に混合した後、この材料をアニーリングすることによる、Li1.3Al0.3Ti1.7(PO4)3被覆LiMn2O4の調製が挙げられる。最後に、LATP‐ポリアクリロニトリル(「PAN」)複合繊維系不織膜を、PAN溶液中でのLATP粒子の電界紡糸分散によって調製できる。
表面改質は、Li‐空気、Li‐水及び/又はハイブリッドLi‐空気/Li‐水セル中の固体電解質膜の安定性を改善し得るが、表面改質だけでは、バルク特性に対して十分な利益、例えば改善された導電率を与えることはできない場合がある。従って、セラミック電解質のバルク組成及び構造を変化させることなく、LATP膜を改質してその環境安定性及びその他のバルク特性を改善することが望ましい。
図1は、一実施形態によるリチウム‐空気(「Li‐空気」)、リチウム‐水(「Li‐水」)及び/又はハイブリッドLi‐空気/Li‐水セル10の概略図である。アノード1及びカソード2は、電解質3及び任意に中間層4によって分離されている。特定の実施形態では、アノード1はリチウム系アノードであり、例えばリチウム金属アノードである。様々な実施形態において、カソード2は、空気電極、水電極及び海水電極から選択される。例示的実施形態では、電解質3は固体電解質である。任意の中間層4は、アノード1を例えば水又は湿気といった物質から隔離するもののリチウムイオンを通過させることができる、固体又は液体層である。
様々な実施形態において、固体電解質は、多結晶材料を含む膜である。この多結晶材料は、リチウムイオン伝導性であり、電極間のリチウムイオンの輸送を可能とするものである。特定の実施形態では、この膜は、カソードからのアノードの物理的及び化学的分離を提供する。
特定の実施形態では、固体電解質は、アノードと湿気との間の気密性障壁を提供する。様々な例示的実施形態では、この膜は、この膜を通したヘリウムの発散及び/又は拡散を、約10‐2cm3/m2/日未満、又は約10‐3cm3/m2/日未満に制限できる。
様々な実施形態においてこの膜は、膜が形成される材料の理論上の密度の少なくとも約92%、少なくとも約95%、少なくとも約97%又は少なくとも約99%の密度を有する。膜の密度が、膜が形成される材料の理論上の密度の約92%未満である場合、膜は気密性障壁又はシールを提供できない。特定の例示的実施形態では、膜は、膜が形成される材料の理論上の密度の少なくとも95%の密度を有する。
特定の実施形態では、膜の厚さは約1μm〜約500μm、約5μm〜約400μm、約10μm〜約300μm又は約50μm〜約200μmである。
様々な例示的実施形態では、膜の導電率は少なくとも1×10‐4S/cm、少なくとも2×10‐4S/cm、少なくとも3×10‐4S/cm、少なくとも4×10‐4S/cm又は少なくとも5×10‐4S/cmである。
特定の実施形態では、多結晶材料は、リチウム金属リン酸塩を含む。いくつかの例示的実施形態では、リチウム金属リン酸塩はLi1+xAlxTi2‐x(PO4)3であり、ここでx>0である。
様々な実施形態において、改質多結晶材料は、少なくとも1つの改質相を含む少なくとも1つの改質領域を有する、多結晶材料を含む。いくつかの例示的実施形態では、改質相は、金属酸化物又はリン酸塩から選択され、ここで上記金属は、Ge、Al、Ca、Y、若しくは2価カチオン、3価カチオン、4価カチオン及び/又は5価カチオンを形成できる他のいずれの金属、並びにその組合せである。特定の実施形態では、改質領域は表面及び/又は結晶粒界である。いくつかの実施形態では、改質相は、多結晶材料の結晶粒界に組み込まれる。様々な実施形態において、改質相は、多結晶材料の改質された表面層に組み込まれる。
特定の例示的実施形態では、改質相はGe、例えばGeO2を含み、改質された結晶粒界及び/又は表面層は、Li1+xAlxGeyTi2‐x‐y(PO4)3を含み、ここで0<x<0.6及び0<y<2である。
様々な例示的実施形態では、改質相の濃度の勾配が存在し、多結晶材料の表面付近の濃度が最も高く、多結晶材料のコア付近の濃度が最も低い。いくつかの実施形態では、改質相の最高濃度は多結晶材料の第1の表面付近であり、最低濃度は多結晶材料の第2の表面付近である。他の実施形態では、改質相は、多結晶材料全体に亘って、結晶粒界に均一又は略均一に分散されている。
いくつかの実施形態では、多結晶材料の表面からコアへの結晶粒界中の改質相の濃度の勾配は、結晶粒界中の改質相の均一な濃度に対して、例えば環境安定性、水中での溶出若しくはエッチングへの耐性、及び/又は導電率といった特定の特性に関して利点を提供する。
様々な実施形態は、多結晶材料を改質する方法を含む。改質プロセスの特定の実施形態は、多結晶材料を調製するステップ、改質相又はその前駆体を多結晶材料の少なくとも1つの表面に導入するステップ、及び多結晶材料を加熱するステップを含む。
特定の実施形態では、多結晶材料は、リチウム金属リン酸塩膜に点火することによって調製される。いくつかの実施形態では、この点火は、リチウム金属リン酸塩膜の微細構造を変化させるか、又は実質的に変化させることができる。
様々な実施形態において、改質相は、改質相又は改質相の前駆体を含む組成物を調製し、この組成物を多結晶材料に塗布することによって、被覆多結晶材料を形成することによって、多結晶材料に導入される。特定の実施形態では、上記組成物は、上記組成物を多結晶材料上に浸漬コーティング、スプレーコーティング、スピンコーティングすることによって塗布される。他の実施形態では、上記組成物を、スパッタリング等の物理蒸着法によって塗布してよい。
例示的実施形態では、上記組成物は、改質相又は改質相の前駆体を含むゾル‐ゲルである。いくつかの実施形態では、上記組成物は粒子、例えばナノ粒子を含む。
様々な実施形態において、加熱は、改質相を形成すること、及び/又は改質相を表面から多結晶材料の結晶粒界中に拡散することによって改質された結晶粒界を形成することを可能とする、アニーリングである。
特定の例示的実施形態では、加熱は、温度が約700℃〜約1000℃の炉内において、約0.5〜12時間の時間に亘って実施される。
加熱の時間及び温度は、多結晶材料の結晶粒界中及び/又は表面上の改質相の分散及び/又は均一性に影響し得る。
いくつかの実施形態では、加熱は、多結晶材料の微細構造を変化させるか、又は実質的に変化させることができる。他の実施形態では、加熱は、多結晶材料の微細構造を変化させず、又は実質的に変化させない。
図2は、多結晶リチウム金属リン酸塩材料を、ゾル‐ゲルプロセスによって合成された酸化ゲルマニウム(「GeO2」)ナノ粒子で改質するためのプロセスの概略図である。ステップ1では、前駆体溶液20は、エタノール及び水の混合物に添加されたゲルマニウムイソプロポキシドを含む。ステップ2において縮合反応が起こり、結果として得られるゾル22中でGeO2ナノ粒子24が形成される。ステップ3では、リチウム金属リン酸塩基材30は、その片側又は両側32、32’をゾル22で被覆され、これにより表面32上にGeO2ナノ粒子24の層が形成される。被覆された基材をステップ4でアニーリングして、リチウム金属リン酸塩基材30の結晶粒界中へのGeの拡散を誘発する。結果として得られる改質リチウム金属リン酸塩基材40は、結晶粒界に組み込まれたGeを含む。結果としてGeの濃度勾配が発生し得、改質リチウム金属リン酸塩基材40の表面42、42’上及び表面42、42’付近の結晶粒界内においてGeの濃度が高く、改質リチウム金属リン酸塩基材40のコア44付近の結晶粒界においてGeの濃度が低くなる。
GeO2ナノ粒子の調製
ナノ酸化ゲルマニウム(「GeO2」)コロイドゾルを、以下のゾル‐ゲル法によって調製した。ゲルマニウム(IV)イソプロポキシドを、エタノール及び脱イオン(「DI」)水の溶液に滴下し、磁力によって激しく撹拌して、スラリー溶液を形成した。エタノールとDi水とのモル比は1:50〜100:10であった。ある量のHClをスラリー溶液に点火して、溶液のpHを約3に調整し、pH調整溶液を形成した。このpH調整溶液に蓋をし、室温で24時間連続して撹拌して、ゾル溶液を形成した。アルミニウムの走査電子顕微鏡(「SEM」)スタッブ上でゾル溶液の滴を乾燥させ、オーブン内において50℃で約10分間乾燥させることにより、試料を調製した。導電性炭素コーティングを試料上に蒸着して、帯電を低減した。調製されたままの状態の酸化ゲルマニウムの組織形態を、Zeiss 1500VP SEM上で観察した。
ナノ酸化ゲルマニウム(「GeO2」)コロイドゾルを、以下のゾル‐ゲル法によって調製した。ゲルマニウム(IV)イソプロポキシドを、エタノール及び脱イオン(「DI」)水の溶液に滴下し、磁力によって激しく撹拌して、スラリー溶液を形成した。エタノールとDi水とのモル比は1:50〜100:10であった。ある量のHClをスラリー溶液に点火して、溶液のpHを約3に調整し、pH調整溶液を形成した。このpH調整溶液に蓋をし、室温で24時間連続して撹拌して、ゾル溶液を形成した。アルミニウムの走査電子顕微鏡(「SEM」)スタッブ上でゾル溶液の滴を乾燥させ、オーブン内において50℃で約10分間乾燥させることにより、試料を調製した。導電性炭素コーティングを試料上に蒸着して、帯電を低減した。調製されたままの状態の酸化ゲルマニウムの組織形態を、Zeiss 1500VP SEM上で観察した。
図3(a)及び(b)は、ゾル‐ゲル法によって合成されたGeO2ナノ粒子のSEM画像であり、図3(c)は、上記GeO2ナノ粒子のエネルギ分散型X線分光器(「EDX」)スペクトルである。図3aは、密に詰まった粒子の凝塊の典型的画像を示し、またゾル‐ゲルプロセスによって合成されたナノ粒子の大規模生産を更に示す。これはゾル‐ゲルプロセスを用いたGeO2ナノ粒子の合成を、例えば大規模製造に拡張できることを示唆している。図3bは、調製されたままの状態の個々のナノ粒子の粒径が約20nm〜約100nmであることを示す。図3cは、ナノ粒子中にGe及びOのみが存在することを示し、これは、調製されたままの状態のゾルの組成が酸化ゲルマニウムであることを示す。
比較例1
Li1.4Al0.4Ti1.6(PO4)3(「LATP」)粉末をテープキャストすることによって、厚さ150マイクロメートルの多結晶膜を調製した。この膜を900℃で2時間焼結した。
Li1.4Al0.4Ti1.6(PO4)3(「LATP」)粉末をテープキャストすることによって、厚さ150マイクロメートルの多結晶膜を調製した。この膜を900℃で2時間焼結した。
実施例1
比較例1の多結晶LATP材料を、上記ゲルマニウムゾル溶液に約5分間浸漬し、LATP材料をゾル溶液から約6〜約30mm/分の速度で引き出すことにより、上記ゾル溶液を上記LATP材料上に浸漬コーティングした。浸漬コーティングされたLATPを、50℃で少なくとも1時間、空気中で乾燥させた。乾燥した被覆LATP材料を、850℃の炉内で約2時間アニーリングして、酸化ゲルマニウムナノ粒子をLATPと反応させ、LATP材料の表面上及び結晶粒界内に、リチウムアルミニウムゲルマニウムチタニウムリン酸塩(「LAGTP」)を形成した。
比較例1の多結晶LATP材料を、上記ゲルマニウムゾル溶液に約5分間浸漬し、LATP材料をゾル溶液から約6〜約30mm/分の速度で引き出すことにより、上記ゾル溶液を上記LATP材料上に浸漬コーティングした。浸漬コーティングされたLATPを、50℃で少なくとも1時間、空気中で乾燥させた。乾燥した被覆LATP材料を、850℃の炉内で約2時間アニーリングして、酸化ゲルマニウムナノ粒子をLATPと反応させ、LATP材料の表面上及び結晶粒界内に、リチウムアルミニウムゲルマニウムチタニウムリン酸塩(「LAGTP」)を形成した。
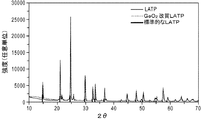
Geによる改質前(比較例1)及び後(実施例1)の組成物について、電力設定40kV 40mAのBruker D4 Endeavor X線回折計を用いて特徴決定した。図4a及び4bは、比較例1及び実施例1による未改質及び改質LATP材料の表面上で得られたX線回折(「XRD」)パターンのグラフを示す。図4aに示すように、実施例1のGe改質LATP表面は、比較例1の未改質LATP試料と同様の回折パターンを示し、これらは共に、LiTi2(PO4)3菱面体晶相(R3c)(PCPDF#01‐072‐6140)として簡単に表示して差し支えない。図4bは、実施例1のGe改質LATP表面が、比較例1と比べて、より小さい格子パラメータへの僅かなピークシフトを有することを示す。表1に、実施例1及び比較例1について計算された格子定数a及びc並びに計算されたセル容積を示す。実施例1は、比較例1に比べて約0.6%の単位セル容積の減少を示し、これは、LATP表面に薄いLAGTPコーティングが形成されたことを示唆する。
図5は、a)比較例1による未改質LATP材料、及びb)実施例1による改質LATP材料の、表面のSEM画像、並びにc)比較例1による未改質LATP材料、及びd)実施例1による改質LATP材料の、破断面のSEM画像を示す。図5に示すように、b)及びd)に示された実施例1の改質LATPは、a)及びc)に示された比較例1の未改質LATPと比較した場合に、膜の結晶上又は膜の結晶間に明らかな組織形態の差異を示さなかった。a)及びb)に示されている表面並びにc)及びd)に示されている断面は共に、実施例1及び比較例1において同様の結晶組織形態及び構造を有する。
図6は、比較例1及び実施例1によるa)未改質及びb)改質LATP材料の表面のエネルギ分散型X線分光器(「EDX」)スペクトルを示す。EDX分析により、a)に示されている実施例1の改質LATPの表面においてゲルマニウムが検出されたが、b)に示されている比較例1の未改質LATPの表面上ではゲルマニウムは検出されなかった。
図7に、実施例1の改質LATPの破断面に対して実施されたEDX分析を示す。図7aは、実施例1による改質LATP材料の破断面のSEM画像を示す。図7b及び7cはそれぞれ、図7a上でマーキングされた領域1及び3のEDXスペクトルを示す。実施例1の改質LATPの表面付近で試料採取された領域1ではゲルマニウムが検出されたが、改質LATPの表面から約15μm超のEDXによってはゲルマニウムは検出されなかった。図6及び7に示されているEDXの結果は、図4に示されている、XRDによるごく僅かなピークシフトの観察と良好に符合しており、これは、改質LATPの表面上にLAGTPの極めて薄い層が存在していることを示唆する。領域2(図示せず)から収集されたEDXデータは、領域1からのデータと同様であった。
水又は湿気への曝露による固体電解質の変質は、溶解によって起こり得るため、脱イオン水に多結晶材料を曝露して、得られる浸出液の導電性を測定することによって、実施例1及び比較例1の安定性を決定した。溶解した多結晶材料は、浸出液の導電性を上昇させ得る。浸出液の導電性の相当な上昇は、この試料は水中で不安定であると考えられることを示す。浸出液の導電性が比較的低いことは、水中での溶解が少ないことを示し、これは、多結晶材料をリチウム‐空気又はリチウム‐水セル内の固体電解質として使用した場合の変質が少ないことを示唆する。従って、浸出液の導電性が低いほど、電解質材料の安定性が高いことが示唆される。浸出実験において、実施例1及び比較例1の改質及び未改質LATP膜それぞれ約50mgを、約30mlの脱イオン水(「DI H2O」)中に浸漬し、浸出液の導電性を長時間に亘って測定した。
図8は、比較例1及び実施例1による未改質及び改質LATP材料(それぞれ3つの試料)に関する、時間に対する脱イオン水中での浸出液の導電率を示す。図8に示すように、実施例1の改質LATPは、比較例1の未改質LATPに比べて低下した浸出液の導電率を示す。約400時間に亘るDI H2O中での浸漬後、改質された試料と改質されていない試料との間で、LATP1に関する浸出液の導電率は約50.8%低下し、LATP2に関する浸出液の導電率は約58.3%低下した。約700時間に亘るDI H2O中での浸漬後、改質LATP1は、未改質LATP1(図示せず)に比べて約54.3%低下した浸出液の導電率を示した。浸出試験の結果は、多結晶材料の本開示の表面及び/又は結晶粒界改質が、水性又は湿潤環境における安定性の改善のための有用なアプローチであることを示す。
図9は、比較例1及び実施例1による未改質及び改質LATP材料に関するACインピーダンスを示すグラフである。図9及び表2に示すように、実施例1の改質LATPに関してインピーダンス分光法によって測定された全リチウムイオン伝導率は、比較例1の未改質LATPに比べて有意に高かった。表2において改質LATP2材料は未改質LATP2材料に比べて20%上昇した伝導率を示した。
本出願において使用される名詞は、複数及び単数を包含することを意図している。換言すると、名詞は、単に論及を容易にするために、「ある多結晶材料」、「ある要素」、「上記カソード」等のように本出願において使用され得るが、そうでないことが明示されていない限り、これは、「少なくとも1つの多結晶材料」、「少なくとも1つの要素」、「上記少なくとも1つのカソード」のように、「少なくとも1つの」を意味することを意図している。これは、ある例において用語「少なくとも1つの」が使用され、かつ別の例、例えば同一の段落又は節において「ある」又は「上記」が使用される場合であっても当てはまる。更に、本出願において使用される句「少なくとも1つの」は、1つ又は複数を意味し、従って個々の構成要素並びに混合物及び/又は組合せを含む。
本出願において使用される用語「備える、含む(comprising)」(及びその文法的変化形)は、「有する(having)」又は「含む(including)」を包括した意味で使用され、「有する」又は「含む」と交換可能に使用され得る。これらの用語は、そのように言明されていない限り、「…のみからなる(consisting only of)」という排他的な意味で使用されていると解釈してはならない。
明示されている場合を除いて、成分及び/又は反応条件の量を表す全ての数は、全ての例において用語「約(about)」で改質されているものとして理解されたい。これは、「全て(all)」又は「いずれも・・・ない(none)」といった用語及びこれらの変化形を含む。本出願において使用される改質語「約」は、定義された特定の量に関して当業者が想定するであろう限界内を意味し、これは、様々な実施形態において例えば、指示されている数の±10%、指示されている数の±5%、指示されている数の±2%、指示されている数の±1%、指示されている数の±0.5%、又は指示されている数の±0.1%であってよい。
更に、範囲が与えられている場合、その範囲の終点は追加の実施形態を定義すること、及び明確に挙げられていないものを含む部分範囲もまた追加の実施形態を含むことを意図していることを理解されたい。
本出願において使用される「…から形成される(formed from)」、「…によって生成される(generated by)」及びこれらの変化形は、化学反応によって得られたことを意味し、ここで「化学反応(chemical reaction)」は、自発的な化学反応及び誘発された化学反応を含む。本出願において使用される句「…から形成される」及び「…によって生成される」は非制限的なものであり、組成物の構成要素を、列挙されているものに限定しない。
本開示による組成物および方法は、本出願に記載された要素及び限定、並びに本出願に記載の又は記載されていなくても当該技術分野で公知のいずれの追加の又は任意の成分、構成要素又は限定を備えるか、これらからなるか、又はこれらから本質的になることができる。
そうでないことが言明されていない限り、本出願に記載の様々な方法のステップは、いずれの順序で実施してよく、全てのステップを実施する必要はなく、それでもこれらの方法は本開示の範囲内にあることが意図されていることを理解されたい。
以上に開示した特徴及び機能並びにその他の特徴及び機能の変形例、又はこれらの代替例を、他の異なる多数の系又は応用に組み合わせてよいことが理解されるだろう。当業者は、現時点で予測されない又は予期しない様々な代替例、修正例、変形例又は改善例を後に実施してよく、これらもまた、以下の請求項によって包含されることを意図している。
1 アノード
2 カソード
3 電解質
4 中間層
10 リチウム‐空気(「Li‐空気」)、リチウム‐水(「Li‐水」)及び/又はハイブリッドLi‐空気/Li‐水セル
22 ゾル
24 GeO2ナノ粒子
30 リチウム金属リン酸塩基材
32、32’ リチウム金属リン酸塩基材の表面
40 改質リチウム金属リン酸塩基材
42、42’ 改質リチウム金属リン酸塩基材の表面
44 改質リチウム金属リン酸塩基材のコア
2 カソード
3 電解質
4 中間層
10 リチウム‐空気(「Li‐空気」)、リチウム‐水(「Li‐水」)及び/又はハイブリッドLi‐空気/Li‐水セル
22 ゾル
24 GeO2ナノ粒子
30 リチウム金属リン酸塩基材
32、32’ リチウム金属リン酸塩基材の表面
40 改質リチウム金属リン酸塩基材
42、42’ 改質リチウム金属リン酸塩基材の表面
44 改質リチウム金属リン酸塩基材のコア
Claims (5)
- 多結晶リチウムイオン伝導性膜であって:
少なくとも1つの表面;
結晶粒界を備える、多結晶リチウムイオン伝導性材料;並びに
金属酸化物及び金属リン酸塩から選択される、少なくとも1つの改質相
を備え、
前記金属は、Ge、Al、Ca、Y、Si、Mg、Ga、若しくは2価カチオン、3価カチオン、4価カチオン及び/又は5価カチオンを形成できる他のいずれの金属、並びにその組合せを含み、
(a)前記少なくとも1つの改質相は、改質された結晶粒界を備える改質多結晶リチウムイオン導電性材料を形成するために前記結晶粒界に組み込まれるか;
(b)前記少なくとも1つの改質相は、改質された表面を形成するために前記少なくとも1つの表面に組み込まれるか;又は
(a)及び(b)の両方である、多結晶リチウムイオン伝導性膜。 - 前記多結晶リチウムイオン伝導性材料は、Li1+xAlxTi2‐x(PO4)3を含むリチウム金属リン酸塩を含み、ここでx>0である、請求項1に記載の多結晶リチウムイオン伝導性膜。
- 前記改質相は、Li1+xAlxGeyTi2‐x‐y(PO4)3を含み、ここで0<x<0.6及び0<y<2である、請求項1に記載の多結晶リチウムイオン伝導性膜。
- 前記多結晶リチウムイオン伝導性膜は、前記改質多結晶リチウムイオン伝導性膜の2つの対向する表面上に位置する2つの改質された表面を備え、これによって改質相濃度の勾配を有する構造が形成され、
前記濃度は、前記構造の中央よりも前記対向する表面において高い、請求項1に記載の多結晶リチウムイオン伝導性膜。 - 少なくとも1つの表面;及び
結晶粒界を備える、多結晶リチウムイオン伝導性材料
を備える多結晶リチウムイオン伝導性膜を改質するための方法であって、
前記方法は:
改質相又は改質相の前駆体を含む組成物を調製するステップであって、ここで前記改質相は金属酸化物及び金属リン酸塩から選択され、前記金属は、Ge、Al、Ca、Y、Si、Mg、Ga、若しくは2価カチオン、3価カチオン、4価カチオン及び/又は5価カチオンを形成できる他のいずれの金属、並びにその組合せを含むものである、ステップ;
前記多結晶リチウムイオン伝導性膜の前記少なくとも1つの表面に前記組成物を塗布することによって、被覆された多結晶リチウムイオン伝導性膜を形成するステップ;並びに
前記被覆された多結晶リチウムイオン伝導性膜をアニーリングして、(e)前記改質相を備える改質された表面、(f)前記改質相を備える改質された結晶粒界、又は(e)及び(f)の両方を形成するステップ
を有してなる方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13/852,491 | 2013-03-28 | ||
| US13/852,491 US9905883B2 (en) | 2013-03-28 | 2013-03-28 | Ceramic electrolyte material comprising a modified polycrystalline lithium metal phosphate |
| PCT/US2014/031405 WO2014160598A1 (en) | 2013-03-28 | 2014-03-21 | A ceramic electrolyte material comprising a modified polycrystalline lithium metal phosphate |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016522958A true JP2016522958A (ja) | 2016-08-04 |
| JP2016522958A5 JP2016522958A5 (ja) | 2017-04-27 |
Family
ID=50687677
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016505507A Abandoned JP2016522958A (ja) | 2013-03-28 | 2014-03-21 | 改質多結晶リチウム金属リン酸塩を含むセラミック電解質材料 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9905883B2 (ja) |
| EP (1) | EP2979317A1 (ja) |
| JP (1) | JP2016522958A (ja) |
| KR (1) | KR20150135493A (ja) |
| CN (1) | CN105190940A (ja) |
| TW (1) | TW201503456A (ja) |
| WO (1) | WO2014160598A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3360185A1 (en) * | 2015-10-08 | 2018-08-15 | Electrijet Flight Systems Inc | Battery system |
| JP6524026B2 (ja) * | 2016-02-29 | 2019-06-05 | スズキ株式会社 | 固体電解質 |
| US10033066B2 (en) * | 2016-02-29 | 2018-07-24 | Suzuki Motor Corporation | Solid electrolyte and method of manufacturing solid electrolyte |
| CN111423110A (zh) * | 2016-04-08 | 2020-07-17 | 康宁股份有限公司 | 包含金属氧化物浓度梯度的玻璃基制品 |
| US10749199B2 (en) | 2017-11-29 | 2020-08-18 | International Business Machines Corporation | Li1+xAlxTi2-x(PO4)3 solid-state thin film electrolyte for 3D microbattery and method of fabrication |
| KR102626920B1 (ko) | 2018-09-14 | 2024-01-18 | 삼성전자주식회사 | 금속-공기 전지 |
| CN112490585A (zh) * | 2020-11-27 | 2021-03-12 | 南京林业大学 | 一种用于锂金属电池的陶瓷隔膜及其制备方法 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4496639A (en) | 1983-07-05 | 1985-01-29 | Ceramatec, Inc. | Hydrogen selenide treatment of electrolytes |
| DE4119498A1 (de) | 1991-06-13 | 1992-12-17 | Abb Patent Gmbh | Verfahren zur herstellung einer brennstoffzellen-luftelektrode |
| US6599664B2 (en) | 1997-08-22 | 2003-07-29 | Yardney Technical Products, Inc. | Inorganic gel-polymer electrolyte |
| JP2001282139A (ja) | 2000-01-27 | 2001-10-12 | Sharp Corp | アクティブマトリックス基板およびその製造方法、並びに、液晶表示装置 |
| JP2002267842A (ja) | 2001-03-12 | 2002-09-18 | Nippon Sheet Glass Co Ltd | 偏光素子及びその製造方法 |
| US6803138B2 (en) | 2001-07-02 | 2004-10-12 | Nextech Materials, Ltd. | Ceramic electrolyte coating methods |
| KR100666821B1 (ko) | 2004-02-07 | 2007-01-09 | 주식회사 엘지화학 | 유/무기 복합 다공성 코팅층이 형성된 전극 및 이를포함하는 전기 화학 소자 |
| US7871735B2 (en) | 2004-10-29 | 2011-01-18 | Nextech Materials, Ltd. | Ceramic laminate structures |
| WO2007062220A2 (en) | 2005-11-23 | 2007-05-31 | Polyplus Battery Company | Li/air non-aqueous batteries |
| RU2403653C2 (ru) * | 2005-12-06 | 2010-11-10 | Эл Джи Кем, Лтд. | Органическо/неорганический композитный разделитель, имеющий градиент морфологии, способ его изготовления и содержащее его электрохимическое устройство |
| US8337939B2 (en) | 2007-09-13 | 2012-12-25 | General Electric Company | Method of processing a ceramic layer and related articles |
| CN102612782B (zh) * | 2009-11-27 | 2014-12-03 | 株式会社村田制作所 | 固体电池 |
| US9502729B2 (en) * | 2012-08-29 | 2016-11-22 | Corning Incorporated | Ion-conducting composite electrolyte comprising path-engineered particles |
-
2013
- 2013-03-28 US US13/852,491 patent/US9905883B2/en active Active
-
2014
- 2014-03-21 JP JP2016505507A patent/JP2016522958A/ja not_active Abandoned
- 2014-03-21 EP EP14723219.3A patent/EP2979317A1/en not_active Withdrawn
- 2014-03-21 KR KR1020157030812A patent/KR20150135493A/ko not_active Application Discontinuation
- 2014-03-21 CN CN201480017952.2A patent/CN105190940A/zh active Pending
- 2014-03-21 WO PCT/US2014/031405 patent/WO2014160598A1/en active Application Filing
- 2014-03-27 TW TW103111550A patent/TW201503456A/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| WO2014160598A1 (en) | 2014-10-02 |
| EP2979317A1 (en) | 2016-02-03 |
| TW201503456A (zh) | 2015-01-16 |
| US20140295286A1 (en) | 2014-10-02 |
| KR20150135493A (ko) | 2015-12-02 |
| US9905883B2 (en) | 2018-02-27 |
| CN105190940A (zh) | 2015-12-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Yubuchi et al. | Lithium-ion-conducting argyrodite-type Li6PS5X (X= Cl, Br, I) solid electrolytes prepared by a liquid-phase technique using ethanol as a solvent | |
| JP7279115B2 (ja) | アノード活物質、カソード活物質及び固体電解質のためのナノ加工コーティング並びにナノ加工コーティングを含む電池の製造方法 | |
| JP2016522958A (ja) | 改質多結晶リチウム金属リン酸塩を含むセラミック電解質材料 | |
| JP5741685B2 (ja) | 電極活物質の製造方法 | |
| KR101624805B1 (ko) | 고체 전해질층을 포함하는 이차전지 | |
| Xu et al. | Enhanced electrochemical performance of LiNi0. 5Mn1. 5O4 cathode material by YPO4 surface modification | |
| JP5730538B2 (ja) | リチウム二次電池電極用焼結体、当該焼結体を含むリチウム二次電池用電極、及び当該電極を備えるリチウム二次電池 | |
| JP2020532067A (ja) | 安全性及びサイクル安定性の向上のための正極材料上の四ホウ酸リチウムガラスコーティング | |
| He et al. | Preparation and electrochemical performance of monodisperse Li 4 Ti 5 O 12 hollow spheres | |
| KR102405440B1 (ko) | 이온 삽입 배터리 전극 및 이의 제조방법 | |
| JP5614646B2 (ja) | 電極用薄膜、全固体リチウム電池、および電極用薄膜の製造方法 | |
| US10062904B2 (en) | Scaffold-free 3D porous electrode and method of making a scaffold-free 3D porous electrode | |
| Chen et al. | Facile synthesis of Cu2O nanorod arrays on Cu foam as a self-supporting anode material for lithium ion batteries | |
| Cheng et al. | Oxidation–reduction assisted exfoliation of LiCoO 2 into nanosheets and reassembly into functional Li-ion battery cathodes | |
| CN110235295B (zh) | 锂离子固体蓄电池及其制造方法 | |
| Borhani-Haghighi et al. | Synthesis of nanostructured LiMn2O4 thin films by glancing angle deposition for Li-ion battery applications | |
| CN108064422A (zh) | 制备纳米结构化层的方法 | |
| Rangasamy et al. | Synthesis and processing of battery materials: giving it the plasma touch | |
| Kimilita et al. | Electrochemical property of solid-state MnO2-Zn battery with the combination of improved cathode and solid electrolyte | |
| KR20170095865A (ko) | 박막의 습식 증착 방법 | |
| WO2019163967A1 (ja) | 積層体とその製造方法 | |
| Yang et al. | Preparation and electrochemical properties of ceria coated Li3V2 (PO4) 3/C cathode materials for lithium-ion batteries | |
| Wei et al. | Enhanced electrochemical performance of La2O3-modified Li4Ti5O12 anode material for Li-ion batteries | |
| KR101738228B1 (ko) | 티타늄-니오비늄 메조 포러스 산화물 및 그 제조 방법 | |
| KR102251048B1 (ko) | 다공성 구조를 가지는 SnO2 나노입자 및 그 제조 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170317 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170317 |
|
| A762 | Written abandonment of application |
Free format text: JAPANESE INTERMEDIATE CODE: A762 Effective date: 20171101 |