JP2016508488A - ラジカル軌道スイッチング - Google Patents
ラジカル軌道スイッチング Download PDFInfo
- Publication number
- JP2016508488A JP2016508488A JP2015555501A JP2015555501A JP2016508488A JP 2016508488 A JP2016508488 A JP 2016508488A JP 2015555501 A JP2015555501 A JP 2015555501A JP 2015555501 A JP2015555501 A JP 2015555501A JP 2016508488 A JP2016508488 A JP 2016508488A
- Authority
- JP
- Japan
- Prior art keywords
- neg
- rad
- radical
- anion
- energy
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/16—Purine radicals
- C07H19/20—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
- C07H19/207—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids the phosphoric or polyphosphoric acids being esterified by a further hydroxylic compound, e.g. flavine adenine dinucleotide or nicotinamide-adenine dinucleotide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/06—Free radical scavengers or antioxidants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/46—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with hetero atoms directly attached to the ring nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/44—Iso-indoles; Hydrogenated iso-indoles
- C07D209/46—Iso-indoles; Hydrogenated iso-indoles with an oxygen atom in position 1
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/92—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with a hetero atom directly attached to the ring nitrogen atom
- C07D211/94—Oxygen atom, e.g. piperidine N-oxide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/92—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with a hetero atom directly attached to the ring nitrogen atom
- C07D211/96—Sulfur atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/04—Ortho- or peri-condensed ring systems
- C07D221/06—Ring systems of three rings
- C07D221/10—Aza-phenanthrenes
- C07D221/12—Phenanthridines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/091—Esters of phosphoric acids with hydroxyalkyl compounds with further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)]
- C07F9/3804—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)] not used, see subgroups
- C07F9/3808—Acyclic saturated acids which can have further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/50—Organo-phosphines
- C07F9/53—Organo-phosphine oxides; Organo-phosphine thioxides
- C07F9/5325—Aromatic phosphine oxides or thioxides (P-C aromatic linkage)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/553—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having one nitrogen atom as the only ring hetero atom
- C07F9/572—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/553—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having one nitrogen atom as the only ring hetero atom
- C07F9/576—Six-membered rings
- C07F9/59—Hydrogenated pyridine rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6561—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings
- C07F9/65616—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings containing the ring system having three or more than three double bonds between ring members or between ring members and non-ring members, e.g. purine or analogs
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6568—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms
- C07F9/65685—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms the ring phosphorus atom being part of a phosphine oxide or thioxide
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Pyridine Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
開殻種、例えば、ラジカルでは不対電子を収容する分子軌道(MO)(半占軌道、すなわちSOMO)が通常エネルギー的に最高被占軌道(HOMO)であることは周知である。
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(Doubly-Occupied Molecular Orbital)(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、
式(I)の構造が提供される。
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、
式(I)の構造が提供される。
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、中和可能である負の点電荷を含み、
LがNEGおよびRADを連結し、
RADのラジカルがNEGの負の点電荷とπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーが、NEGの負の点電荷が中和されているときの式(I)の対応する構造における該エネルギーより低い、
式(I)の構造が提供される。
RAD-L-NEG
(I)
の構造を有するラジカル保護基であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合していないときに、保護対象のラジカルが脱保護可能である、
式(I)の構造を有するラジカル保護基が提供される。
一酸化窒素;
二酸化窒素;
一酸化窒素および/もしくは二酸化窒素ラジカルを含む構造;または
非ステロイド性抗炎症薬(NSAID)
の群より選択される、前記で定義されたプロセスが提供される。
RAD-L-NEG
(I)
の構造を特定するための計算手段の使用であって、
式中、RAD、NEG、およびLが、本発明の前の局面のいずれか1つに従って定義される、
使用が提供される。
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、本発明の第3の局面に従って定義される、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RAD、NEG、およびLが、本発明の前の局面のいずれか1つに従って定義される、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、本発明の前の局面のいずれか1つに従って定義される、方法が提供される。
式(I)
RAD-L-NEG
(I)
の構造における、中和されているNEGの点電荷から中和の原因を除去することによって、RADの半占軌道のエネルギー準位を下げる方法であって、式中、RAD、NEG、およびLが、本発明の第3の局面に従って定義される、方法が提供される。
RAD-L-NEG
(I)
の構造における、NEGのアニオンからプロトンおよび/または他のカチオンを除去することによって、NEGの二重被占軌道のエネルギー準位をRADの半占軌道のエネルギー準位より高く上げる方法であって、式中、RAD、NEG、およびLが、本発明の前の局面のいずれか1つに従って定義される、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、生体高分子が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法が提供される。
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法が提供される。
の群より選択されるラジカル、DNA/RNA塩基ベースのラジカルを含むか、またはアミノ酸ベースのラジカルである、前記で定義された方法、使用、プロセス、構造、または保護基が提供される。
2,2',6,6'-テトラメチルピペリジン-N-オキシル(TEMPO)、
2,2',5,5'-テトラメチルピロリジン-N-オキシル(PROXYL)、
2,2,5,5-テトラメチル-4-フェニル-3-アザヘキサン-3-オキシル(TIPNO)、
N,N-(1,1-ジメチルエチル-1)-(1-ジエチル-ホスホノ-2,2-ジメチル-プロピル-1)-N-オキシル(SG1)、
グアニンベースまたはグリシルベースのラジカル
を含む群より選択されるラジカル基を含む、前記で定義された方法、使用、プロセス、構造、または保護基が提供される。
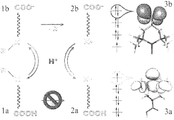
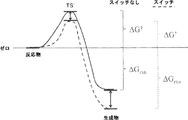
図1は、本発明において考察される化学的側面および分子軌道を図でまとめたものを示す。図の左下隅から始めて、酸基(COOH)がリンカーによって基Xと連結され、基Xが基Rと結合した分子が示されている。酸基は大まかに言って本発明のNEG基に一致し、リンカー構造は大まかに言って本発明のL基に一致し、X基(非結合状態のときは、すなわち・X)は基RADに対応する。
で示した)があることが分かる。次いで、・X-----COO-種にプロトンが付加されれば、新たな種・X-----COOHが形成される。これもまた、この種の隣に、軌道のエネルギー準位図と分子軌道の図を示した。この場合、非充填軌道(すなわち、
で示した)はHOMOになっており、これはプロトン付加によって引き起こされたことが分かる。すなわち、プロトンは種の電子拘束(electronic stricture)を変えるように、従って、種の化学特性を変えるように働いた。
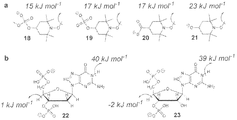
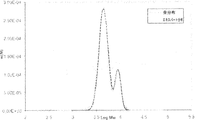
コンホメーション、ならびに対応する非結合TEMPO...CH3COOH複合体(●)のM06-2X/6-31+G(d)最適化構造およびBDE-スイッチ(電子エネルギーに換算した、kJmol-1)。b、aの種および完全カルボキシ-TEMPO同族列(n=0〜10の伸びきり鎖配座異性体)のメチルBDE計算値(kJmol-1)。
SOMO≠HOMO時の状態と比較したSOMO=HOMO時の状態のエネルギー差は、これらの状態を有する2つの種の反応性の差を示している。
NEGのアニオンとプロトン(および他のカチオン)との結合性によっても、式(I)の構造の特性をさらに操作することが可能である。様々なクラスのアニオンが当業者に公知であろう。
式(I)の構造は、調整されるRADのラジカルの性質を提供する。様々なラジカルタイプが公知であり、これらの基の安定性は異なる。様々なクラスのラジカルが当業者に公知であろう。
リンカーLの性質は式(I)の構造のさらなる操作を可能にする。
結果として生じた、「変換」ラジカルの余分な安定性のために、このラジカルは結合形成反応に関与する可能性が低く、そしてさらには、関与している結合から(ホモリシス)開裂する可能性が高い。
負に荷電している官能基とπ-π共役していない、安定化ラジカルを含有するディストニックラジカルアニオンが、pHによって切り替え可能なSOMO-HOMO変換を示すかどうか試験するために、2つの特異なタイプの安定ラジカル種-立体障害性環式アミノキシル(「ニトロキシド」、R1R2NO・とも知られる)および非環式第1級ペルオキシル(RCH2OO・)を検討した。π共役の可能性を排除し、それによって、調べられたラジカルと供与体部分との間の長距離相互作用だけを確保するために、それぞれの種に、ラジカル中心から十分に離れている、遠く離れたカルボン酸基を導入した。単参照および多参照アブイニシオおよびDFT計算に従って、カルボン酸アニオンが高エネルギー二重被占軌道を提供し、これにプロトンが付加されると、通常の軌道構成が回復することが見出された(例えば、SOMO=HOMO、図2a〜b、および実施例1〜実施例4を参照されたい)。
pHによって制御されるSOMO-HOMOエネルギー準位変換をもつフリーラジカルが設計されたので、切り替え型および非切り替え型における安定性を調査した。ラジカル安定性の代表的な実際に役に立つ尺度は、メチル、・CH3などの単純な炭素中心ラジカルとの結合解離自由エネルギー(BDFE)である。従って、気相中、25℃で、中性型および脱プロトン化型におけるカルボキシ-アミノキシルおよびカルボキシ-ペルオキシルラジカルのメチルBDFEを計算し、カルボキシル基の脱プロトン化(従って、通常の軌道構成から変換軌道構成への切り替え)によって・CH3との結合が弱まることが見出された。ラジカルCOOH-X・について[BDFE(COOH-X-R)-BDFE(COO--X-R)]と定義された、このBDFE-スイッチの大きさは、アミノキシルの場合、約20kJmol-1、ペルオキシルの場合、15kJmol-1である(またはKeqでは約3.5および2.0オーダー。表6を参照されたい)。従って、脱プロトン化ラジカルにおけるSOMO-HOMO変換は安定性を高める。これは、空間分離、およびアニオン部分とラジカル部分との間の明白なπ共役相互作用の非存在を考慮すると予期せぬ発見であった。この点に関して、計算によって、遠く離れたアニオンにスピン密度がないことが裏付けられた(実施例2aおよび実施例2bを参照されたい)。
pHによって誘導される軌道スイッチングはラジカル部分の安定性およびカルボン酸基の酸性度に影響を及ぼす。これは、カルボキシ-アミノキシルおよびそのアルコキシアミンの脱プロトン化の気相エンタルピー(すなわち、気相酸性度すなわちGPA)差と、プロトン化型および脱プロトン化型の同じアルコキシアミンの気相BDE差と関連づける簡単なサーモサイクルによって証明された(図5aおよび実施例9)。従って、反応速度論的方法を用いて求められたGPA-スイッチの値は、理論的に予測されたBDE-スイッチの直接の尺度である。GPA差を測定するために、陰イオンエレクトロスプレーイオン化を用いて二量体複合体[A-H+B-]を合成し、タンデム質量分析計で衝突誘起解離に供した。AHがBHより酸性度が高ければ、解離平衡はA-+BH生成物チャネルに有利になり、従って、A-およびB-生成物イオンの存在量を比較することによって、この対のGPA-スイッチを確かめることができる。カルボキシアミノキシルにおけるBDE-スイッチを評価するために、Aがそのアミノキシルであり、Bがそのアルコキシアミンであるプロトン結合二量体を調製した。これを、図5bでは、カルボキシ-TEMPO 4およびそのメチルアルコキシアミン17について説明した。図5bから、計算(正のBDE-スイッチ)と一致して、4は17より酸性度が高い(正のGPA-スイッチ)ことが分かる。
理論的手順
全てのアブイニシオ理論計算および密度汎関数法理論計算を、Gaussian 09、QChem 3.2、Molpro 2009.1、およびGAMESS 2010ソフトウェアパッケージを用いて行った。垂直酸化生成物を除く全種の構造を、M06-2X/6-31+G(d)、選択的にBMK/6-31+G(2df,p)法を用いて完全に最適化し、振動数を同じレベルで計算し、推奨される倍率によってスケール変更した。同族列については、(CH2)n鎖を伸びきったコンホメーション(extended conformation)に保ったのに対して、本研究にある他の全ての種について全コンホメーション検索を分解能(resolution)60°で行った。正確な電子エネルギーを、DFTおよびMP2から高レベル複合G3(MP2)RAD、G3(MP2,CC)、およびG4(MP2)-6X法に及ぶ様々な方法を用いて計算した。ラジカルに対する計算は、制限開殻波動関数を使用した「R」接頭辞で示した場合を除いて、非制限波動関数を用いて行った。高レベル複合計算が計算により実行できない大きな系(15〜20個の重原子を超える)の場合、代わりに2レイヤーONIOM型法を適用し、MP2/6-311+G(3df, 2p)法を完全な系に使用した。報告した熱化学値(気相結合解離エネルギー、酸性度、および相対イオン化エネルギー)は、調和振動子近似下の理想気体の統計熱力学について標準的な教科書に載っている式と最適化構造およびスケール変更した振動数(scaled frequency)を用いて得た25℃での気相エントロピーおよび熱補正と併用して計算した。記載の方法は実験データに対して広範囲に試験されており、化学的精度内で結果を出すことが示されている(結合解離エネルギーについては約5kJmol-1、酸化還元電位については0.050V)。ここで研究された事例の大半において、上述の熱化学パラメータの絶対値と、より重要なことには、その相対的差異(例えば、BDE-スイッチおよびGPA-スイッチ)は両方とも、反応性の傾向および結論に影響を及ぼすことなく、理論的方法に応じて7kJmol-1というごくわずかな範囲内で変化することを強調すべきである。
アルコキシアミンを、文献に書いてある標準的な手順によってアミノキシルラジカル前駆体から合成した。アミノキシルラジカルおよびアルコキシアミンの等モル混合物をメタノールに溶解して最終濃度が約10μMになるように二つ一組で調製した。これらのメタノール含有溶液をWaters QuattroMicro(Manchester, UK)三連四重極型質量分析計のイオン源に5μL min-1の速度で注入したときに、陰イオンエレクトロスプレーイオン化によってプロトン結合二量体が生成された。質量分析計を陰イオンモードで操作し、MicromassMassLynxソフトウェア(Version4.1)によって制御した。望ましいプロトン結合クラスターイオンの生成を最適化するために、キャピラリー電圧を-3.0kV、コーン電圧を-20V、供給源温度(source temperature)を80℃、脱溶媒和温度を110℃に設定した。乾燥ガスとして窒素を300L h-1の流速で使用したのに対して、衝突誘起解離(CID)実験では、必要に応じて5〜25Vの実験室系エネルギー、衝突ガスとしてアルゴンを使用した(3.0±0.1mTorr)。ここで報告した全ての質量スペクトルおよびイオン存在量比は少なくとも200回の累積スキャンの平均である。質量選別されたクラスターイオンの競合的解離に起因する相対イオン存在量に基づいて相対気相脱プロトン化エンタルピーおよび絶対気相脱プロトン化エンタルピーを求めるために、反応速度論的方法を使用した。
方法
試作カルボキシ-アミノキシルおよびカルボキシ-ペルオキシルディストニックラジカルアニオンの軌道構成を確かめるために、最初に、非制限単参照アブイニシオ法およびDFT法を使用した。具体的には、αスピン電子およびβスピン電子を、そのエネルギーおよび形状によって突き合わせた。占有α軌道と対をなす占有β軌道があるときはいつでも、これらは二重被占軌道を形成するのに対して、低いところにある非占有β軌道と対をなす1つの占有α軌道はラジカルのSOMOに対応する。この手順は、UHFおよびUMP2波動関数ベースの方法ならびにUM06-2X密度汎関数法とSTO-3G〜6-311+G(3df,2p)に及ぶ基底関数を、同じ理論レベルで最適化された構造と併用して行った。全ての場合で、半占軌道より高いエネルギーを有する多数の二重被占軌道をもたらす軌道構成変換が観察された。選択された例を実施例1に示した。スピン密度をGaussView 5.0を用いてプロットし、軌道プロットをIQmol 2.1ビジュアリゼーションパッケージを用いて構築した。
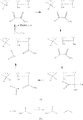
試作ディストニックラジカルアニオンの単参照分子軌道
試作カルボキシ-ペルオキシル(上)およびカルボキシ-アミノキシル(下)ラジカルのUHF/STO-3G(左)およびUM06-2X/6-31+G(d)(右)スピン密度(透明表面(transparent surface))ならびにαおよびβ分子軌道(固体表面(solid surface))。太字の数字は軌道数であり(エネルギーが増加する順)、イタリック体の数字は軌道エネルギーである。半占軌道に対応する数字に下線を引いた。
試作ディストニックラジカルアニオンのMCSCFおよびMRPT2分子軌道
試作カルボキシ-ペルオキシル(左)およびカルボキシ-アミノキシル(右)ラジカルのMCSCF(9,5)/6-31+G(d)最適化分子軌道ならびにMCSCF(9,5)/6-31+G(d)およびMRPT2(9,5)/6-31+G(d)最適化軌道構成のプロット。
試作ディストニックラジカルアニオンのCASSCF分子軌道
試作カルボキシペルオキシル(左)およびカルボキシアミノキシル(右)ラジカルのCASSCF(7,8)/STO-3G最適化分子軌道および主構成と太字フォントで示したその固有値。
試作プロトン化ラジカルの多参照分子軌道
プロトン化カルボキシペルオキシル(上)およびカルボキシ-アミノキシル(下)ラジカルの最適化MCSCF(9,5)/6-31+G(d)分子軌道、MCSCF(9,5)/6-31+G(d)およびMRPT2(9,5)/6-31+G(d)軌道構成のプロット、ならびにCASSCF(7,8)/STO-3G最適化分子軌道プロットおよび主構成と太字フォントで示したその固有値。MacMolPlt v.7.4.2およびGaussView 5.0パッケージを用いて軌道を構築した。
参照カルボキシ-アルコキシルラジカルの多参照分子軌道
カルボキシル基のプロトン化状態にある参照アルコキシルラジカルのMCSCF(9,5)/6-31+G(d)およびMRPT2(9,5)/6-31+G(d)最適化軌道構成、ならびにCASSCF(7,8)/STO-3G主要最適化構成と太字フォントで示したその固有値。
方法
試作種の普通でない軌道構成の追加試験として、そのイオン化(一電子酸化)を調べた。両基質について、本発明者らは、ビラジカル生成物には三重項基底状態があることを見出した(実施例6を参照されたい)。一重項ビラジカルについての計算は、対称性の破れDFTアプローチと最適化三重項ビラジカル構造を用いて行った。脱プロトン化カルボキシTEMPOの場合、垂直酸化生成物および断熱(adiabatic)酸化生成物の両方を首尾良くモデル化することができた。これらは安定な波動関数および平衡構造をもつと特徴付けられた。原子電荷およびスピン密度の計算値(図2を参照されたい)ならびにS2値によって、位置づけられた構造は真の閉殻双性イオンおよび開殻ビラジカルであることが確かめられた。両種とも、双性イオンの場合、窒素の平坦化(planarization)を伴う構造緩和時には安定している。計算方法とは無関係に、三重項ビラジカルは双性イオンより(約10〜25kJmol-1)安定であることが見出された。これは親カルボキシアミノキシルにおける軌道変換と一致する。しかしながら、酸素原子にある局在化正電荷が関与するこのような生成物の極端な不安定性のために、双性イオンへの試作カルボキシペルオキシルの酸化は成し遂げることができない。構造緩和時に、CO2が放出され、分子内環化が起こる。従って、親カルボキシペルオキシルにおける軌道構成のダイアグノスティック(diagnostic)において双性イオンを使用することはできない。それにもかかわらず、三重項ビラジカル生成物は凍結(frozen)構造と緩和構造の両方で安定している(実施例6を参照されたい)。
一電子酸化開殻生成物および閉殻生成物の特性
SOMO-HOMOエネルギー準位変換ディストニックアニオンラジカルから閉殻(一重項)双性イオンおよび開殻(三重項および一重項)ビラジカルへの一電子酸化(イオン化)の競合的経路。酸化生成物については、その最適化UM06-2X/6-31+G(d)構造を示した。構造の隣にある数字は、UM06-2X/6-31+G(d)およびUMP2/GTMP2Large(括弧内)マリケン原子スピン密度および電荷(イタリック体)である。開殻種におけるスピン混入(spin contamination)は、そのS2(UM06-2X/6-31+G(d)、括弧内にはUMP2/GTMP2Large)およびT1ダイアグノスティック(UCCSD(T)/6-31+G(d))値で反映される。酸化生成物の相対電子エネルギー(kJmol-1)を、UM06-2X/6-31+G(d)および改良されたG3(MP2,CC)(+)法を用いて計算した。
方法
試作ラジカルがメチルと形成する結合の正確なエネルギー特性を得るために、いくつかの高レベル複合法を使用した。最初に、G3(MP2)-RADおよびG3(MP2,CC)法といくつかの改良法を適用した。具体的には、アニオン種を正確に説明するには、分散関数(diffuse function)を基底関数に導入することが必要であり、従って、全計算において、デフォルト6-31G(d)基底の代わりに6-31+G(d)基底を使用した。これらをG3(MP2)-RAD(+)およびG3(MP2,CC)(+)法と呼ぶ。B3LYP汎関数の代わりにM06-2X密度汎関数を使用することも選択した。最も一般的に用いられる方法の1つではあるが、B3LYPには多数の重大な欠点があることが知られている。これに対して、ミネソタ(Minnesota)汎関数の新たな一群は、特に、ラジカル反応の熱化学に対して優れた性能を示す。これは本研究の結果によって裏付けられた(下記を参照されたい)。さらに、基底関数補正を介したダブル-ζ基底関数を用いた計算からの大きなトリプル-ζ基底を用いた標準的なG3(MP2)法近似CCSD(T)計算をR(O)MP2(G3(MP2)-RAD)およびUMP2(G3(MP2,CC)レベルで行った。両手順ともモルプロ(Molpro)コードを用いて計算したURCCSD(T)エネルギーを使用し、前者の方法はラジカル反応専用にパラメータ化されていたので、G3(MP2,CC)計算ではG3(MP2)-RAD法の高レベル補正(HLC)値も使用した。次に、最近のG4(MP2)-6X法を使用した。G3-ファミリーとの主な違いは、1)構造および振動数にBMK/6-31+G(2df,p)法が用いられること、2)完全基底関数極限まで外挿されたハートリー-フォック極限エネルギー推定値が複合エネルギーの基本成分であることである。この方法はG3(MP2)法より計算に費用がかかり、従って、小さなペルオキシル種にのみ実行することができ、アミノキシルには実行できなかった。最後に、正確な電子エネルギーを、調和振動子近似と最適化構造およびスケール変更した振動数下で計算したエントロピーおよび熱補正で補った。2つの試作種-プロトン化型および脱プロトン化型のカルボキシペルオキシルおよびアミノキシル-の絶対結合解離エネルギーおよびその差(BDE-スイッチ、前記で定義した)の結果を表6に集めた。G3(MP2)-RAD(+)およびG3(MP2,CC)(+)の結果は有意差がなく(4kJmol-1以内)、G4法から絶対値でわずかに大きく変動した(約7〜8kJmol-1)。重要なことに、BDE-スイッチの値を得るための方法全てを用いて、1kJmol-1未満の変動の範囲内で非常に良好な一致が得られた。
a閉殻脱プロトン化化合物を示した。b第1番目の縦列に示したような脱プロトン化型。c完全プロトン化型; d開殻種では分子内電子移動が起こる。
スイッチングを伴う反応を太字で示した。aG3(MP2)-RAD(+)法とUM06-2X/6-31+G(d)最適化構造およびスケール変更した振動数を用いて計算した。bトンネル効果に合わせて補正した速度定数。
a全ての値は25℃でのものであり、kJmol-1で示した。b切断結合(breaking bond)を曲がった矢印で示した。cM06-2X/6-31+G(d)(カルボキシ-TEMPO-Rおよびフェノールの場合)ならびにUMP2/6-311+G(3df,2p)レベルでのG3(MP2,CC)(+)エネルギーに対するONIOM近似値(コアとしてTEMPO-CH3を用いたTTF-CH=N-TEMPO-CH3および参照非切り替え系の場合)を用いて計算した。cUAKS-CPCM/B3LYP/6-31G(d)法と推奨される倍率(水の場合、1.2、トルエンの場合、1.3)を用いて計算した。eR(O)MP2/6-311+G(3df,2p)理論レベルでのG3(MP2)-RADエネルギーに対するONIOM近似値を用いて計算した。fUAHF-CPCM/UHF/6-31+G(d)法と推奨される倍率(1.4)を用いて計算した。gUAKS-CPCM/B3LYP/6-31+G(d)法と推奨される倍率(水の場合、1.2、トルエンの場合、1.3)を用いて計算した。
スイッチングを伴う反応を太字で示した。aR(O)MP2/6-311+G(3df,2p)法とUB3LYP/6-31G(d)最適化構造およびスケール変更した振動数を用いて、G3(MP2)-RAD電子エネルギーに対するONIOM近似値を用いて計算した。b完全プロトン化。c第1番目の縦列に示したように二重脱プロトン化。d
方法
試作カルボキシペルオキシルおよびアミノキシルラジカルにおけるpHスイッチングの性質を調べるために、これらを、脱プロトン化時に軌道変換を示さない、構造が似ているカルボキシアルコキシルラジカルと対にした。「試験セット」を、ラジカル部分とカルボキシ部分とを分ける(CH2)n鎖の長さが異なる同族列にも広げた(図3および実施例7aを参照されたい)。結合エネルギー特性計算値の1/r依存性を研究するために、これらの鎖を、伸びきったコンホメーションに保った。式中、rは、ラジカル部分とカルボキシ部分との間の(スルースペース)距離である。
そのプロトン化型におけるBDEは、弱い水素結合相互作用があるために他の同族体よりわずかに小さい。この相互作用は、対応する脱プロトン化種では不可能であるので、そのBDEでのpHスイッチはわずかに減少する(実施例7cを参照されたい)。にもかかわらず、脱プロトン化酢酸を含む超分子のメチルBDEは、伸びきり鎖n=4同族体のメチルBDEより1.5kJmol-1未満大きく
、従って、軌道変換スイッチング効果の主としてスルースペースな性質およびスルーボンドσ補助からのごくわずかな寄与が確かめられた。
同族体の構造
a、変換カルボキシアミノキシルおよびカルボキシ-ペルオキシルラジカルの同族列ならびにこれらの参照環式および非環式カルボキシアルコキシルラジカル。b、非環式アルコキシル系列にあるn=4同族体の最適化M06-2X/6-31+G(d)およびBMK/6-31+G(2df, p)構造(カルボキシル基の脱プロトン化型およびプロトン化型のラジカル種および対応するメチルエーテルを示した)。最小エネルギーcおよび伸びきり鎖、d(上)、n=4のアミノキシル同族体の配座異性体、ならびにTEMPOおよび酢酸の超分子、d(下)の最適化M06-2X/6-31+G(d)構造。カルボキシル基の脱プロトン化型およびプロトン化型のラジカル種および対応するメチルエーテルを示した。
アミノキシル同族体のBDE
アミノキシル同族列:伸びきり鎖配座異性体(○)、n=4の最小気相エネルギー配座異性体(□)、ならびにTEMPOおよび酢酸からなる超分子(◇)のM06-2X/6-31+G(d)結合解離電子エネルギー計算値。
カルボキシル基プロトン化状態にある非環式試作ペルオキシルラジカルおよび参照アルコキシルラジカルを対象にしたX-CH3結合ホモリシスの電子エネルギー計算値、kJmol-1。
a実施例7aにある構造を示す。b6-31+G(d)基底関数。cGTMP2Large基底関数。dG3-RADはG3(MP2)-RAD(+)法を表す。eG3-CCはG3(MP2,CC)(+)を表す。fG4はG4(MP2)-6X法を表す。
カルボキシル基プロトン化状態にある環式試作アミノキシルラジカルおよび参照アルコキシルラジカルを対象にしたX-CH3結合ホモリシスの電子エネルギー計算値、kJmol-1。
a実施例7aにある構造を示す。b 6-31+G(d)基底関数。c 6-311+G(3df,2p)基底関数。d G3-RADはG3(MP2)-RAD(+)法を表す。e G3-CCはG3(MP2,CC)(+)を表す。f UMP2/6-311+G(3df,2p)レベルで処理した高級同族体のコアとして、G3(MP2,CC(+)理論レベルで処理した非置換TEMPO(A)または1番目の同族体(n=0,B)を用いたONIOM近似値。g最小エネルギー配座異性体、実施例7cを参照されたい。h超分子、実施例7dを参照されたい。均衡補正を用いてエネルギーを基底関数の重ね合わせ誤差(BSSE)に合わせて補正した。
電子エネルギーに換算した試作系列および参照系列のBDE-スイッチ計算値、kJmol-1。
a実施例7aにある構造を示す。b6-31+G(d)基底関数。c全HF成分と同じ基底で計算したαおよびβ交換の合計。d完全基底関数まで外挿されたHFエネルギー(アルコキシルセットについてM06-2X構造のHF/GTMP2Large値を示す)。eG3-CCはG3(MP2,CC)(+)法を表す。fG4はG4(MP2)-6X法を表す。gTZは6-311+G(3df,2p)基底関数を表す。hUMP2/6-311+G(3df,2p)レベルで処理した高級同族体のコアとしてG3(MP2,CC)(+)理論レベルで処理した1番目の同族体(n=0)を用いたONIOM近似値。i最小エネルギー配座異性体、実施例7cを参照されたい。j超分子、実施例7dを参照されたい。均衡補正を用いてエネルギーをBSSEに合わせて補正した。
サーモサイクル
結果の実験検証は、カルボキシル化されたアミノキシルおよびアルコキシアミン対の(エンタルピーに換算した)相対気相酸性度の測定値に基づいた。これは、図5aに示したサーモサイクルに従って、これらのアルコキシアミンにおける結合解離のエンタルピー計算値と直接比較することができる。結果として生じた関係の導出を以下の実施例9に示した。
実施例10に示したセットからの化合物対を対象にして実験を行った。4-カルボキシ-2,2',6,6'-テトラメチルピペリジン-N-オキシルラジカル(カルボキシ-TEMPO)および3-カルボキシ-2,2',5,5'-テトラメチルピロリジン-N-オキシルラジカル(カルボキシ-PROXYL)を含む全試薬をSigma Aldrich(Castle Hill, Australia)から購入し、特にことわらない限り受領したように使用した。全アルコキシアミンを、文献に書いてある標準的な手順によって、そのアミノキシルラジカル前駆体から調製した。質量分析用メタノールはHPLCグレードであり、Crown Scientific(現在は、VWR, Queensland, Australia)から購入し、受領したように使用した。
試験セット
アミノキシルおよびアルコキシアミン。質量分析実験での研究。
原稿に記載のように、型(A-+H++B-)-のプロトン結合二量体から得た衝突誘起解離質量スペクトルを入手した。式中、A-およびB-は、アミノキシルラジカルおよび/または関連アルコキシアミンから形成された任意の共役塩基対である。結果として生じた質量スペクトル中の生成物イオン存在量[A-]および[B-]の比を表10に示した。式1にまとめたように、これらのデータに反応速度論的方法を適用すると、イオン存在量比を用いて、2つの共役酸の気相酸性度差(形式上、ΔacidH2-ΔacidH1で示した脱プロトン化エンタルピー)を導き出すことが可能になる。この反応速度論的方法の関係は、(i)逆方向の活性化障壁が存在しないこと;(ii)クラスターのアイソマー型が全く存在しないこと;(iii)競合的解離チャネルのエントロピー差がごくわずかであること(すなわち、Δ(ΔacidG)がΔ(ΔacidH)に単純化する)に頼っている。単純なプロトン結合二量体の解離およびここで研究されている系について、仮定(i)および(ii)はロバストであると一般にみなされる。単純な二量体解離だけが観察された。このことは、(iii)もこの実験に適用されることを示唆している。
ターゲットガスとしてアルゴンを用いた三連四重極型質量分析計における10V(実験室系)衝突エネルギーでのプロトン結合二量体の衝突誘起解離から得たイオン存在量比(I1:I2)。報告した比は少なくとも200回の累積スキャンの平均であり、試料溶液の反復注入を含む。1より大きな比は、ΔacidH1>ΔacidH2を意味する。最も重要な比は、アミノキシルラジカル(A&E)をアルコキシアミンと比較した比である。内的一貫性のための相互参照としてアルコキシアミン対間の選択された、さらなる比を報告する。
実施例10からのアミノキシルおよびアルコキシアミン対の実験的GPA-スイッチおよびBDE-スイッチ計算値(25℃での気相エンタルピー、kJmol-1)。
それに対応して、全種の絶対GPAおよび絶対BDEを、前記のように、G3(MP2)-RAD(+)法またはそれに対するONIOM近似値を用いて25℃、気相中で計算した(表12)。GPA計算のために、プロトンの熱化学をフェルミ-ディラック統計下での電子規則に従って考慮した。最後に、これらの種の様々な対のBDE-スイッチを計算し、実験により求めたGPA-スイッチと比較した(表11)。得られた理論結果および実験結果は非常によく一致しており、全ての場合で、アミノキシルラジカルがその閉殻アルコキシアミンより酸性度が高いか、またはラジカル安定性の点から見るとCOOH基の脱プロトン化がアルコキシアミンにおけるBDEを下げることを裏付けている。
下記式を用いて、二次反応速度定数測定値と剛体球衝突速度(khs)を比較することによって、酸素がシクロヘキシルラジカルに付加する反応効率を見積もった。
式中、σAB 2=(RA+RB)2であり、RAは、1.74Åとしたシクロヘキシルラジカルの分子半径であり、RBは2.90Åとした二酸素の分子半径であり、kBはボルツマン定数であり、Tは絶対温度であり、μは、換算質量
である。
図6bの種の結合解離電子エネルギー計算値(気相、kJmol-1)。
a2個のリン酸基のプロトン化を、脱プロトン化状態の場合は(-)、プロトン化状態の場合は(H)で示した。bR(O)MP2/6-311+G(3df,2p)法を用いたG3(MP2)-RADエネルギーに対する2レイヤーONIOM近似値。
モデルDNAラジカルの一電子酸化生成物
デオキシグアノシン二リン酸の塩基ラジカルおよび糖ラジカルの垂直一電子酸化(イオン化)生成物。閉殻双性イオンの場合、三重項ビラジカルの静電ポテンシャル地図-スピン密度をプロットした。全てUB3LYP/6-31+G(d)構造と併用した。UB3LYP/6-31+G(d)およびUHF/6-31+G(d)(括弧内)レベルでのUB3LYP/6-31+G(d)双極子モーメント(μ, デバイ)および相対エネルギー(Er, kJmol-1)も示した。
B3LYP/6-31+G(d)およびUHF/6-31+G(d)(括弧内)レベルでの双極子モーメント(D, デバイ)および相対エネルギー(E, kJmol-1)。
室温での、CuBrおよびPMDETAを含む100%Tol中でのNRC反応(スキーム1)
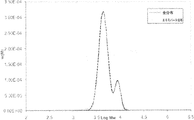
100mgのPMA-Br(Mn=4000, 2.5x10-5mol)、5.0mgの4-カルボン酸TEMPO(2.5x10-5mol)、およびPMDETA 6.3μL(3.0x10-5mol)を1.0mLトルエンに溶解し、Arで10分間パージした。次いで、4.3mgのCuBr(3.0x10-5mol)をAr下で添加した。次いで、30分で反応物をサンプリングし、20時間で反応を止めた。反応物をTHFで希釈し、銅を除去するためにAl2O3に通した。次いで、溶液をSECで分析した。
スキーム1。室温での、CuBr/PMDETAを含むTol中でのPMA-Brと4-カルボン酸TEMPOとのNRC反応。
室温での、CuBrおよびMe6TRENを含む100%DMSO中でのNRC反応(スキーム2)
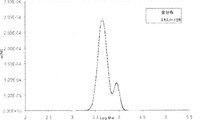
85mgのPMA-Br(Mn=4000,2.125x10-5mol)、5.0mgの4-カルボン酸TEMPO(2.5x10-5mol)、およびMe6TREN 6.3μL(3.0x10-5mol)を1.0mLのDMSOに溶解し、Arで10分間パージした。次いで、4.3mgのCuBr(3.0x10-5mol)をAr下で添加した。次いで、30分で反応物をサンプリングし、20時間で反応を止めた。反応物をTHFで希釈し、銅を除去するためにAl2O3に通した。次いで、溶液をSECで分析した。
スキーム2。室温での、CuBr/Me6TRENを含むDMSO中でのPMA-Brと4-カルボン酸TEMPOとのNRC反応。
室温での、Me6TRENを含む100%DMSO中での解離反応(スキーム3)
約50mgのPMA-ON-COOH(Mn=4200)を1.0mLのDMSOに溶解し、Arで10分間パージした。次いで、50μLのMe6TRENをAr下で添加した。次いで、6時間で反応物をサンプリングし、20時間で反応を止めた。次いで、溶液をSECで分析した。
スキーム3。室温での、DMSO Me6TREN中でのPMA-ON-COOHのアルコキシルアミン解離反応。
全ての値をハートリーで示した。
aG3(MP2)-RADパラメータを用いて計算した。c6-31+G(d)基底関数と併用した。bGTMP2Large基底関数と併用した。dG3(MP2,CC)(+)電子エネルギー。
T1ダイアグノスティック以外の全ての値をハートリーで示した。同族体を以下の通りに命名した。最初の文字はアルコキシル(A)およびペルオキシル(P)種を示し、2番目の状態はアニオン性(A)およびプロトン化(H)カルボキシル基を示す。数字は実施例7aのnに対応する。Rはラジカル種を示し、Mは、対応するメチルエーテルを示す。
aCCSD(T)/6-31+G(d)計算からのT1ダイアグノスティック。bDFT-D3法とBJダンピングを用いて計算した、B3LYPに対する分散補正。c6-31+G(d)基底関数を用いて計算した。dGTMP2Large基底関数を用いて計算した。eHF/CBSエネルギーへのαおよびβ交換寄与。
T1ダイアグノスティック以外の全ての値をハートリーで示した。同族体を以下の通りに命名した。最初の文字はアルコキシル(O)およびアミノキシル(N)種を示し、2番目の状態はアニオン性(A)およびプロトン化(H)カルボキシル基を示す。数字は実施例7aのnに対応する。Rはラジカル種を示し、Mは、対応するメチルエーテルを示す。
aCCSD(T)/6-31+G(d)計算からのT1ダイアグノスティック。bDFT-D3法とBJダンピングを用いて計算した、B3LYPに対する分散補正。c6-31+G(d)基底関数を用いて計算した。d6-311+G(3df,2p)基底関数を用いて計算した。e対応するHFエネルギーへのαおよびβ交換寄与。fアミノキシル系列の場合、コア層は非置換TEMPOである。アルコキシル系列の場合、コア層はこの系列の1番目の同族体である。gカルボキシ-TEMPO n=4同族体の最小エネルギー配座異性体。hTEMPOおよび酢酸の超分子複合体。示したM06-2Xエネルギーを、均衡補正を用いてBSSEに合わせて補正した。
T1ダイアグノスティック以外の全ての値をハートリーで示した。
aCCSD(T)/6-31+G(d)計算からのT1ダイアグノスティック。b6-311+G(3df,2p)基底関数を用いて計算した。cG3(MP2)-RAD(+)電子エネルギーまたはR(O)MP2/6-311+G(3df,2p)理論レベルでの、それに対するONIOM近似値(色付きの太字で示した)。
T1ダイアグノスティック以外の全ての値をハートリーで示した。種を以下の通りに命名した。アニオン性系列では、最初の単語はアニオン性断片に対応し、最初の文字はアニオン性(A)状態およびプロトン化(H)状態を示し、2番目の文字はラジカル(R)種および対応するメチルエーテル(M)種を示す。核酸系列では、Gはグアニンを表し、dはデオキシリボースを表し、rはリボース部分を表す。aは脱プロトン化リン酸基を示し、4はC4糖ラジカルを指し、1はN1塩基ラジカルを指し、コアはONIOMコア種を示す。
aCCSD(T)/6-31+G(d)計算からのT1ダイアグノスティック。b6-31+G(d)基底関数を用いて計算した。c6-311+G(3df,2p)基底関数を用いて計算した。d6-31G(d)基底関数を用いて計算した。eR(O)MP2/6-311+G(3df,2p)理論レベルでのG3(MP2)-RAD電子エネルギーに対するONIOM近似値。
25℃、60℃、および100℃で、気相および様々な溶媒中でのM06-2X/6-31+G(d)電子エネルギーおよびギブズ自由エネルギーから計算した絶対X-RBDEおよびBDE-スイッチ。全てkJmol-1で示した。
a(-)は酸-塩基基の脱プロトン化状態に対応し、(H)は酸-塩基基のプロトン化状態に対応する。b溶媒和のギブズ自由エネルギーを、UAKS-(C)PCM/B3LYP/6-31+G(d)法を用いて計算した。c「DMSO」はジメチルスルホキシドを表し、「ACN」はアセトニトリルを表し、「DCA」はジクロロエタンを表す。
全種に、振動数から求めた0仮想振動数があった。各エントリーに理論レベルを含め、それに対応して、化合物の一部については2つのエントリー(M06-2XおよびBMK)を割り当てた。この点に関しては、本明細書と共に参照により本明細書に組み入れられるNature Chemistry刊行物 (Gryn'ova G., Marshall D., Blanksby, SJ, Coote M.L. Nature Chem.(2013), 5, 474-481)を、これと一緒に公表されたサポート情報を含めて参照されたい。
より選択される構造を含む、前記で定義された方法、使用、プロセス、構造、または保護基が提供される。
[本発明1001]
式(I)
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、中和可能である負の点電荷を含み、
LがNEGおよびRADを連結し、
RADのラジカルがNEGの負の点電荷とπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーが、NEGの負の点電荷が中和されているときの式(I)の対応する構造における該エネルギーより低い、
式(I)の構造。
[本発明1002]
NEGが、負の点電荷を帯びることができるおよび/または保持することができる表面または構造であり、かつ負の点電荷が中和可能である、本発明1001の式(I)の構造。
[本発明1003]
負の点電荷が、電子、電荷、負電位、または負のクーロン電荷を含む群より選択され、かつ負の点電荷が、その電荷の実質的な除去、散逸、または反転によって中和可能である、本発明1001または1002の式(I)の構造。
[本発明1004]
負の点電荷を帯びることができるおよび/または保持することができる表面または構造が、電極である、本発明1001〜1003のいずれかの式(I)の構造。
[本発明1005]
負の点電荷を帯びることができるおよび/または保持することができる表面または構造が、金属または非金属である、本発明1001〜1004のいずれかの式(I)の構造。
[本発明1006]
負の点電荷を帯びることができるおよび/または保持することができる表面または構造が、グラフェンを含む、本発明1001〜1005のいずれかの式(I)の構造。
[本発明1007]
負の点電荷が、プロトンまたは他のカチオンに結合することによって中和可能であるアニオンを含む基である、本発明1001の式(I)の構造。
[本発明1008]
式(I)
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、
式(I)の構造。
[本発明1009]
式(I)
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、
式(I)の構造。
[本発明1010]
保護されたラジカルを生じるように、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGの負の点電荷が中和されていないときに、保護対象のラジカルとの結合が弱まる、
本発明1001〜1007のいずれかの式(I)の構造を有するラジカル保護基。
[本発明1011]
保護されたラジカルを生じるように、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGの負の点電荷が中和されていないときに、保護対象のラジカルが脱保護可能である、
本発明1001〜1007および本発明1010のいずれかの式(I)の構造を有するラジカル保護基。
[本発明1012]
ラジカルを保護するための本発明1010または1011のラジカル保護基の使用であって、負の点電荷が中和されている、使用。
[本発明1013]
中和されている負の点電荷から中和の原因を除去することによって、本発明1010または1011のラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1014]
負の点電荷を除去すること;負の点電荷を散逸させること;または負の点電荷から正の点電荷へと反転させることを含む、本発明1010または1011のいずれかのラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1015]
ラジカルを本発明1010または1011のラジカル保護基と反応させることによってラジカルを保護する方法であって、負の点電荷が中和されている、方法。
[本発明1016]
負の点電荷を中和することによって、本発明1010または1011のラジカル保護基を活性化する方法。
[本発明1017]
式(I)
RAD-L-NEG
(I)
の構造を有するラジカル保護基であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、保護されたラジカルを生じるように、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合していないときに、保護対象のラジカルが脱保護可能である、
ラジカル保護基。
[本発明1018]
ラジカルを保護するための本発明1017のラジカル保護基の使用であって、NEGのアニオンがプロトンまたは他のカチオンと結合している、使用。
[本発明1019]
NEGのアニオンに結合しているプロトンまたは他のカチオンを除去することによって、本発明1017のラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1020]
反応媒体のpHを上げて、NEGのアニオンに結合しているプロトンを除去することによって、本発明1017のラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1021]
金属キレートを反応媒体に添加して、NEGのアニオンに結合している金属カチオンを除去することによって、本発明1017のラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1022]
アニオンを反応媒体に添加し、添加されたアニオンが、反応媒体中に存在するカチオンと共に沈殿物を形成し、それによって、これらのカチオンをNEGのアニオンとの結合から除去することによって、本発明1017のラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1023]
ラジカルを本発明1017のラジカル保護基と反応させることによってラジカルを保護する方法であって、NEGのアニオンがプロトンまたは他のカチオンと結合している、方法。
[本発明1024]
プロトンまたは他のカチオンを反応媒体に添加することによって、本発明1017のラジカル保護基を活性化する方法であって、添加されたプロトンまたは他のカチオンにNEGのアニオンが結合する、方法。
[本発明1025]
反応媒体のpHを下げて、NEGのアニオンをプロトン化することによって、本発明1017のラジカル保護基を活性化する方法。
[本発明1026]
NEGのアニオンに結合しているプロトンまたは他のカチオンがそのアニオンから解離するように反応媒体の極性を上げることによって、本発明1001〜1008のいずれかのラジカル保護基で保護されたラジカルを脱保護する方法。
[本発明1027]
反応媒体中のプロトンまたは他のカチオンがNEGのアニオンに結合するように反応媒体の極性を下げることによって、本発明1017のラジカル保護基を活性化する方法。
[本発明1028]
本発明1013〜1016、1019〜1027のいずれかの方法の1つまたは複数が用いられる、方法。
[本発明1029]
脱保護されたラジカルが、それ自身と反応するか、または反応媒体中の1種もしくは複数種の試薬と反応する、本発明1013、1014、1019〜1022、1026、および1028のいずれかの方法。
[本発明1030]
ラジカル反応が、ラジカルカップリング;ウルツ反応;ニトロキシドを介した重合;ニトロキシドラジカルカップリング;二重結合付加;環化反応;原子引抜き;および酸化を含む群より選択される、本発明1029の方法。
[本発明1031]
脱保護されたラジカルが重合反応に関与する、本発明1029の方法。
[本発明1032]
鎖延長ポリマーラジカルが、本発明1001のラジカル保護基でキャッピングされる、本発明1030または1031の方法。
[本発明1033]
キャッピングされたラジカルが脱保護されて、さらに、その脱保護されたラジカルが重合される、本発明1032の方法。
[本発明1034]
キャッピング前のポリマー基質が脱保護後のポリマー基質と異なる、本発明1033の方法。
[本発明1035]
本発明1013〜1016および1019〜1034のいずれかの方法の1つまたは複数が用いられる、方法。
[本発明1036]
重合反応がブロック共重合である、本発明1030〜1035のいずれかの方法。
[本発明1037]
最高で120℃までの温度範囲、好ましくは、25〜80℃の範囲で重合が行われる、本発明1030〜1036のいずれかの方法。
[本発明1038]
反応媒体が緩衝化されている、本発明1019〜1037のいずれかの方法。
[本発明1039]
カチオンが、金属イオン種もしくは金属含有イオン種であるか、またはアンモニウムイオンもしくはホスホニウムイオンである、本発明1019〜1038のいずれかの方法。
[本発明1040]
保護されたラジカル、保護対象のラジカル、またはラジカル保護基が、センサーによって検出可能である、本発明1013〜1016および1019〜1039のいずれかの方法。
[本発明1041]
センサーがプロ蛍光(profluorescent)プローブを含む、本発明1040の方法。
[本発明1042]
センサーが、pHの決定;医用画像処理;酸化または還元の程度;存在し得るフリーラジカル種の検出および定量において有用である、本発明1040または1041の方法。
[本発明1043]
センサーがpHの決定において有用である、本発明1040〜1042のいずれかの方法。
[本発明1044]
本発明1040〜1043のいずれかの保護されたラジカル、保護対象のラジカル、もしくはラジカル保護基;またはこれらの種から生じた1種もしくは複数種の生成物のうちの1つまたは複数の濃度を測定することによって、媒体のpHをモニタリングする方法。
[本発明1045]
保護対象のラジカルまたはラジカル保護基が抗酸化剤である、本発明1013〜1016および1019〜1044のいずれかの方法。
[本発明1046]
保護対象のラジカルまたはラジカル保護基が、光安定剤を含む産業用抗酸化剤である、本発明1045の方法。
[本発明1047]
保護対象のラジカルまたはラジカル保護基が、生物学的に活性な抗酸化剤である、本発明1045の方法。
[本発明1048]
ラジカルスカベンジャーとしての、本発明1010、1011、および1017のいずれかの保護対象のラジカルおよび/またはラジカル保護基の使用。
[本発明1049]
保護対象のラジカルもしくはラジカル保護基;結果として生じたその代謝産物;または結果として生じたその生成物のうちの1つまたは複数が生物学的に活性である、本発明1013〜1016、1019〜1029、1031、1035、1038〜1040、1045、1047、および1048のいずれかの方法。
[本発明1050]
生物学的に活性な種が体内に放出される、本発明1049の方法。
[本発明1051]
生物学的に活性な種が、生理学的状態の変化に応答して、特に、pH上昇の結果として体内に放出される、本発明1050の方法。
[本発明1052]
生物学的に活性な種が、
一酸化窒素;
二酸化窒素;
一酸化窒素および/もしくは二酸化窒素ラジカルを含む構造;または
非ステロイド性抗炎症薬(NSAID)
の群より選択される、本発明1050または1051の方法。
[本発明1053]
ビラジカル種を生じるように電子を除去することによる、本発明1001〜1011および1017のいずれかの式(I)の構造の酸化方法。
[本発明1054]
負の点電荷が中和されており、かつ酸化によって不対電子が除去される、本発明1053の式(I)の酸化方法。
[本発明1055]
NEGがプロトンまたは他のカチオンと結合しており、かつ酸化によって不対電子が除去される、本発明1053の式(I)の酸化方法。
[本発明1056]
本発明1053〜1055のいずれかの方法の1つまたは複数が用いられる、方法。
[本発明1057]
本発明1053において酸化される種および本発明1054において酸化される種が、負の点電荷の導入または除去によって相互変換可能である、本発明1056の方法。
[本発明1058]
本発明1053において酸化される種および本発明1055において酸化される種が、プロトンまたは他のカチオンの付加または除去によって相互変換可能である、本発明1056の方法。
[本発明1059]
太陽電池を含む分子電子用途において使用するための、本発明1053〜1058のいずれかの方法。
[本発明1060]
式(I)
RAD-L-NEG
(I)
の構造を特定するための計算手段の使用であって、
式中、RAD、NEG、およびLが、本発明1001〜1011および1017のいずれかに従って定義される、
使用。
[本発明1061]
本発明1060の方法に従う、結果として生じた構造。
[本発明1062]
ラジカルを含む構造に負の点電荷を導入することを含む、ラジカルを含む構造を安定化させる方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、本発明1001〜1007、1010、および1011のいずれかに従って定義される、方法。
[本発明1063]
ラジカルを含む構造にアニオンを組み込むことを含む、ラジカルを含む構造を安定化させる方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、本発明1007〜1009および1017のいずれかに従って定義される、方法。
[本発明1064]
本発明1062または1063の方法に従う、結果として生じた構造。
[本発明1065]
共役塩基を含む構造にラジカルを組み込むことを含む、共役塩基を含む構造のpK b を上げる方法であって、結果として生じる構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、本発明1001〜1011および1017のいずれかに従って定義される、方法。
[本発明1066]
本発明1065の方法に従う、結果として生じた構造。
[本発明1067]
式(I)
RAD-L-NEG
(I)
の構造における、中和されているNEGの点電荷から中和の原因を除去することによって、RADの半占軌道のエネルギー準位を下げる方法であって、式中、RAD、NEG、およびLが、本発明1001〜1007、1010、および1011のいずれかに従って定義される、方法。
[本発明1068]
式(I)
RAD-L-NEG
(I)
の構造における、NEGのアニオンからプロトンおよび/または他のカチオンを除去することによって、NEGの二重被占軌道のエネルギー準位をRADの半占軌道のエネルギー準位より高く上げる方法であって、式中、RAD、NEG、およびLが、本発明1001〜1009および1017のいずれかに従って定義される、方法。
[本発明1069]
本発明1067または1068の方法に従う、結果として生じた構造。
[本発明1070]
生体高分子にラジカルを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1071]
生体高分子にラジカルを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1072]
生体高分子にアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1073]
生体高分子にアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1074]
生体高分子にラジカルおよびアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1075]
生体高分子にラジカルおよびアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1076]
生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1077]
生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1078]
結果として生じる生体高分子が基質と複合体を形成するように生体高分子を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1079]
結果として生じる生体高分子が基質と複合体を形成するように生体高分子を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1080]
結果として生じる改変された基質が生体高分子と複合体を形成するように基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1081]
結果として生じる改変された基質が生体高分子と複合体を形成するように基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1082]
結果として生じる改変された生体高分子および基質が複合体を形成するように生体高分子および基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。
[本発明1083]
結果として生じる改変された生体高分子および基質が複合体を形成するように生体高分子および基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。
[本発明1084]
改変が生体高分子の活性部位に対する改変である、本発明1070〜1079、1082、および1083のいずれかの生体高分子を改変する方法。
[本発明1085]
本発明1070〜1084のいずれかの改変された生体高分子および/または改変された基質。
[本発明1086]
本発明1085の改変された生体高分子および/または改変された基質の使用。
[本発明1087]
RADのラジカルが安定化される、本発明1001〜1086のいずれかの方法、使用、構造、または保護基。
[本発明1088]
RADのラジカルが非局在化される、本発明1001〜1087のいずれかの方法、使用、構造、または保護基。
[本発明1089]
RADのラジカルがLと共役している、本発明1001〜1088のいずれかの方法、使用、構造、または保護基。
[本発明1090]
RADが、立体的および/または電子的に安定化されたラジカルを含む、本発明1001〜1089のいずれかの方法、使用、構造、または保護基。
[本発明1091]
RADのラジカルが、そのラジカルに近接する基によって電子的および/または立体的に安定化される、本発明1001〜1090のいずれかの方法、使用、構造、または保護基。
[本発明1092]
RADが、電子的に安定化されたラジカルを含む、本発明1001〜1091のいずれかの方法、使用、構造、または保護基。
[本発明1093]
RADが、
の群より選択されるラジカル、DNA/RNA塩基ベースのラジカルを含むか、またはアミノ酸ベースのラジカルである、本発明1001〜1092のいずれかの方法、使用、構造、または保護基。
[本発明1094]
DNA/RNA塩基がグアニン(G)、アデニン(A)、シトシン(C)、チミン(T)、またはウラシル(U)より選択される、本発明1093の方法、使用、構造、または保護基。
[本発明1095]
RADが、
2,2',6,6'-テトラメチルピペリジン-N-オキシル(TEMPO)、
2,2',5,5'-テトラメチルピロリジン-N-オキシル(PROXYL)、
2,2,5,5-テトラメチル-4-フェニル-3-アザヘキサン-3-オキシル(TIPNO)、
N,N-(1,1-ジメチルエチル-1)-(1-ジエチル-ホスホノ-2,2-ジメチル-プロピル-1)-N-オキシル(SG1)、
グアニンベースまたはグリシルベースのラジカル
の群より選択されるラジカル基を含む、本発明1001〜1094のいずれかの方法、使用、構造、または保護基。
[本発明1096]
NEGのアニオンが不安定化される、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1095のいずれかの方法、使用、構造、または保護基。
[本発明1097]
NEGのアニオンの負電荷が、そのアニオンの外側にあるいかなる基にも非局在化されない、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1096のいずれかの方法、使用、構造、または保護基。
[本発明1098]
NEGのアニオンがLとπ共役していない、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1097のいずれかの方法、使用、構造、または保護基。
[本発明1099]
NEGが、立体的および/または電子的に不安定化されたアニオンを含む、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1098のいずれかの方法、使用、構造、または保護基。
[本発明1100]
NEGのアニオンが、そのアニオンに近接する基によって電子的および/または立体的に不安定化される、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1099のいずれかの方法、使用、構造、または保護基。
[本発明1101]
NEGが、電子的に不安定化されたアニオンを含む、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1100のいずれかの方法、使用、構造、または保護基。
[本発明1102]
NEGが、
を含む群より選択されるアニオンを含む、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1101のいずれかの方法、使用、構造、または保護基。
[本発明1103]
LがRADとの共役を含む、本発明1001〜1102いずれかの方法、使用、構造、または保護基。
[本発明1104]
LがNEGとのπ共役を含まない、本発明1001〜1103のいずれかの方法、使用、構造、または保護基。
[本発明1105]
Lが2個以上の部分で構成され、かつ該部分の少なくとも2個が非共有結合により一緒に結合される、本発明1001〜1104のいずれかの方法、使用、構造、または保護基。
[本発明1106]
非共有結合が水素結合または静電結合である、本発明1105の方法、使用、構造、または保護基。
[本発明1107]
1つまたは複数の部分が、1つまたは複数のDNA/RNA塩基、アミノ酸、ペプチド、補因子、酵素、酵素断片、活性化酵素、生体高分子、または酵素基質を含み、該部分が、天然のものであるか、天然のものから改変されているか、または合成のものである、本発明1105または1079の方法、使用、構造、または保護基。
[本発明1108]
Lが2個以上の部分で構成され、かつ該部分の少なくとも2個が1つまたは複数の金属中心に結合する、本発明1001〜1107のいずれかの方法、使用、構造、または保護基。
[本発明1109]
金属中心が、アルカリ金属カチオンおよび遷移金属カチオンを含む群より選択される、本発明1108の方法、使用、構造、または保護基。
[本発明1110]
Lが複数のNEG基および/またはRAD基を連結する、本発明1001〜1109のいずれかの方法、使用、構造、または保護基。
[本発明1111]
Lが1つまたは複数のポリマー部分を含む、本発明1001〜1110のいずれかの方法、使用、構造、または保護基。
[本発明1112]
Lが、結合、水素結合、非共有結合、静電結合、金属結合、アルキル、環式アルキル、アリール、アルケン、アルキン、複素環式化合物、複素環式芳香族化合物、糖、金属錯体のうちの1つもしくは複数を含むか、またはスルースペース相互作用である、本発明1001〜1111のいずれかの方法、使用、構造、または保護基。
[本発明1113]
Lが、結合、フェニル、ビフェニル、C 1 -C 20 アルキル、C 3 -C 20 シクロアルキル、RNAベースの糖、DNAベースの糖を含む群より選択される、本発明1001〜1112のいずれかの方法、使用、構造、または保護基。
[本発明1114]
式(I)の構造が
を含む群より選択される、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1113のいずれかの方法、使用、構造、または保護基。
[本発明1115]
本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1114のいずれかの式(I)の構造を含む治療的有効量の化合物を投与することを含む、医学的状態の医学的処置方法。
[本発明1116]
医学的状態を処置および/または予防するための医薬を製造するための、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1114のいずれかの式(I)の構造を含む化合物の使用。
[本発明1117]
療法において使用するための、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1114のいずれかの式(I)の構造を含む化合物の使用。
[本発明1118]
医学的状態を処置するための、本発明1007〜1009、1017〜1053、1055、1056、1058〜1061、1063〜1066、1068〜1100のいずれかの式(I)の構造を含む化合物の使用。
Claims (118)
- 式(I)
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、中和可能である負の点電荷を含み、
LがNEGおよびRADを連結し、
RADのラジカルがNEGの負の点電荷とπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーが、NEGの負の点電荷が中和されているときの式(I)の対応する構造における該エネルギーより低い、
式(I)の構造。 - NEGが、負の点電荷を帯びることができるおよび/または保持することができる表面または構造であり、かつ負の点電荷が中和可能である、請求項1に記載の式(I)の構造。
- 負の点電荷が、電子、電荷、負電位、または負のクーロン電荷を含む群より選択され、かつ負の点電荷が、その電荷の実質的な除去、散逸、または反転によって中和可能である、請求項1または2に記載の式(I)の構造。
- 負の点電荷を帯びることができるおよび/または保持することができる表面または構造が、電極である、請求項1〜3のいずれか一項に記載の式(I)の構造。
- 負の点電荷を帯びることができるおよび/または保持することができる表面または構造が、金属または非金属である、請求項1〜4のいずれか一項に記載の式(I)の構造。
- 負の点電荷を帯びることができるおよび/または保持することができる表面または構造が、グラフェンを含む、請求項1〜5のいずれか一項に記載の式(I)の構造。
- 負の点電荷が、プロトンまたは他のカチオンに結合することによって中和可能であるアニオンを含む基である、請求項1に記載の式(I)の構造。
- 式(I)
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、
式(I)の構造。 - 式(I)
RAD-L-NEG
(I)
の構造であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、
式(I)の構造。 - 保護されたラジカルを生じるように、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGの負の点電荷が中和されていないときに、保護対象のラジカルとの結合が弱まる、
請求項1〜7のいずれか一項に記載の式(I)の構造を有するラジカル保護基。 - 保護されたラジカルを生じるように、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGの負の点電荷が中和されていないときに、保護対象のラジカルが脱保護可能である、
請求項1〜7および請求項10のいずれか一項に記載の式(I)の構造を有するラジカル保護基。 - ラジカルを保護するための請求項10または11に記載のラジカル保護基の使用であって、負の点電荷が中和されている、使用。
- 中和されている負の点電荷から中和の原因を除去することによって、請求項10または11に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- 負の点電荷を除去すること;負の点電荷を散逸させること;または負の点電荷から正の点電荷へと反転させることを含む、請求項10または11のいずれか一項に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- ラジカルを請求項10または11に記載のラジカル保護基と反応させることによってラジカルを保護する方法であって、負の点電荷が中和されている、方法。
- 負の点電荷を中和することによって、請求項10または11に記載のラジカル保護基を活性化する方法。
- 式(I)
RAD-L-NEG
(I)
の構造を有するラジカル保護基であって、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、保護されたラジカルを生じるように、RADのラジカルが保護対象のラジカルとの結合を形成することができ、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合していないときに、保護対象のラジカルが脱保護可能である、
ラジカル保護基。 - ラジカルを保護するための請求項17に記載のラジカル保護基の使用であって、NEGのアニオンがプロトンまたは他のカチオンと結合している、使用。
- NEGのアニオンに結合しているプロトンまたは他のカチオンを除去することによって、請求項17に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- 反応媒体のpHを上げて、NEGのアニオンに結合しているプロトンを除去することによって、請求項17に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- 金属キレートを反応媒体に添加して、NEGのアニオンに結合している金属カチオンを除去することによって、請求項17に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- アニオンを反応媒体に添加し、添加されたアニオンが、反応媒体中に存在するカチオンと共に沈殿物を形成し、それによって、これらのカチオンをNEGのアニオンとの結合から除去することによって、請求項17に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- ラジカルを請求項17に記載のラジカル保護基と反応させることによってラジカルを保護する方法であって、NEGのアニオンがプロトンまたは他のカチオンと結合している、方法。
- プロトンまたは他のカチオンを反応媒体に添加することによって、請求項17に記載のラジカル保護基を活性化する方法であって、添加されたプロトンまたは他のカチオンにNEGのアニオンが結合する、方法。
- 反応媒体のpHを下げて、NEGのアニオンをプロトン化することによって、請求項17に記載のラジカル保護基を活性化する方法。
- NEGのアニオンに結合しているプロトンまたは他のカチオンがそのアニオンから解離するように反応媒体の極性を上げることによって、請求項1〜8のいずれか一項に記載のラジカル保護基で保護されたラジカルを脱保護する方法。
- 反応媒体中のプロトンまたは他のカチオンがNEGのアニオンに結合するように反応媒体の極性を下げることによって、請求項17に記載のラジカル保護基を活性化する方法。
- 請求項13〜16、19〜27のいずれか一項に記載の方法の1つまたは複数が用いられる、方法。
- 脱保護されたラジカルが、それ自身と反応するか、または反応媒体中の1種もしくは複数種の試薬と反応する、請求項13、14、19〜22、26、および28のいずれか一項に記載の方法。
- ラジカル反応が、ラジカルカップリング;ウルツ反応;ニトロキシドを介した重合;ニトロキシドラジカルカップリング;二重結合付加;環化反応;原子引抜き;および酸化を含む群より選択される、請求項29に記載の方法。
- 脱保護されたラジカルが重合反応に関与する、請求項29に記載の方法。
- 鎖延長ポリマーラジカルが、請求項1に記載のラジカル保護基でキャッピングされる、請求項30または31に記載の方法。
- キャッピングされたラジカルが脱保護されて、さらに、その脱保護されたラジカルが重合される、請求項32に記載の方法。
- キャッピング前のポリマー基質が脱保護後のポリマー基質と異なる、請求項33に記載の方法。
- 請求項13〜16および19〜34のいずれか一項に記載の方法の1つまたは複数が用いられる、方法。
- 重合反応がブロック共重合である、請求項30〜35のいずれか一項に記載の方法。
- 最高で120℃までの温度範囲、好ましくは、25〜80℃の範囲で重合が行われる、請求項30〜36のいずれか一項に記載の方法。
- 反応媒体が緩衝化されている、請求項19〜37のいずれか一項に記載の方法。
- カチオンが、金属イオン種もしくは金属含有イオン種であるか、またはアンモニウムイオンもしくはホスホニウムイオンである、請求項19〜38のいずれか一項に記載の方法。
- 保護されたラジカル、保護対象のラジカル、またはラジカル保護基が、センサーによって検出可能である、請求項13〜16および19〜39のいずれか一項に記載の方法。
- センサーがプロ蛍光(profluorescent)プローブを含む、請求項40に記載の方法。
- センサーが、pHの決定;医用画像処理;酸化または還元の程度;存在し得るフリーラジカル種の検出および定量において有用である、請求項40または41に記載の方法。
- センサーがpHの決定において有用である、請求項40〜42のいずれか一項に記載の方法。
- 請求項40〜43のいずれか一項に記載の保護されたラジカル、保護対象のラジカル、もしくはラジカル保護基;またはこれらの種から生じた1種もしくは複数種の生成物のうちの1つまたは複数の濃度を測定することによって、媒体のpHをモニタリングする方法。
- 保護対象のラジカルまたはラジカル保護基が抗酸化剤である、請求項13〜16および19〜44のいずれか一項に記載の方法。
- 保護対象のラジカルまたはラジカル保護基が、光安定剤を含む産業用抗酸化剤である、請求項45に記載の方法。
- 保護対象のラジカルまたはラジカル保護基が、生物学的に活性な抗酸化剤である、請求項45に記載の方法。
- ラジカルスカベンジャーとしての、請求項10、11、および17のいずれか一項に記載の保護対象のラジカルおよび/またはラジカル保護基の使用。
- 保護対象のラジカルもしくはラジカル保護基;結果として生じたその代謝産物;または結果として生じたその生成物のうちの1つまたは複数が生物学的に活性である、請求項13〜16、19〜29、31、35、38〜40、45、47、および48のいずれか一項に記載の方法。
- 生物学的に活性な種が体内に放出される、請求項49に記載の方法。
- 生物学的に活性な種が、生理学的状態の変化に応答して、特に、pH上昇の結果として体内に放出される、請求項50に記載の方法。
- 生物学的に活性な種が、
一酸化窒素;
二酸化窒素;
一酸化窒素および/もしくは二酸化窒素ラジカルを含む構造;または
非ステロイド性抗炎症薬(NSAID)
の群より選択される、請求項50または51に記載の方法。 - ビラジカル種を生じるように電子を除去することによる、請求項1〜11および17のいずれか一項に記載の式(I)の構造の酸化方法。
- 負の点電荷が中和されており、かつ酸化によって不対電子が除去される、請求項53に記載の式(I)の酸化方法。
- NEGがプロトンまたは他のカチオンと結合しており、かつ酸化によって不対電子が除去される、請求項53に記載の式(I)の酸化方法。
- 請求項53〜55のいずれか一項に記載の方法の1つまたは複数が用いられる、方法。
- 請求項53において酸化される種および請求項54において酸化される種が、負の点電荷の導入または除去によって相互変換可能である、請求項56に記載の方法。
- 請求項53において酸化される種および請求項55において酸化される種が、プロトンまたは他のカチオンの付加または除去によって相互変換可能である、請求項56に記載の方法。
- 太陽電池を含む分子電子用途において使用するための、請求項53〜58のいずれか一項に記載の方法。
- 式(I)
RAD-L-NEG
(I)
の構造を特定するための計算手段の使用であって、
式中、RAD、NEG、およびLが、請求項1〜11および17のいずれか一項に従って定義される、
使用。 - 請求項60に記載の方法に従う、結果として生じた構造。
- ラジカルを含む構造に負の点電荷を導入することを含む、ラジカルを含む構造を安定化させる方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、請求項1〜7、10、および11のいずれか一項に従って定義される、方法。 - ラジカルを含む構造にアニオンを組み込むことを含む、ラジカルを含む構造を安定化させる方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、請求項7〜9および17のいずれか一項に従って定義される、方法。 - 請求項62または63に記載の方法に従う、結果として生じた構造。
- 共役塩基を含む構造にラジカルを組み込むことを含む、共役塩基を含む構造のpKbを上げる方法であって、結果として生じる構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、RAD、NEG、およびLが、請求項1〜11および17のいずれか一項に従って定義される、方法。 - 請求項65に記載の方法に従う、結果として生じた構造。
- 式(I)
RAD-L-NEG
(I)
の構造における、中和されているNEGの点電荷から中和の原因を除去することによって、RADの半占軌道のエネルギー準位を下げる方法であって、式中、RAD、NEG、およびLが、請求項1〜7、10、および11のいずれか一項に従って定義される、方法。 - 式(I)
RAD-L-NEG
(I)
の構造における、NEGのアニオンからプロトンおよび/または他のカチオンを除去することによって、NEGの二重被占軌道のエネルギー準位をRADの半占軌道のエネルギー準位より高く上げる方法であって、式中、RAD、NEG、およびLが、請求項1〜9および17のいずれか一項に従って定義される、方法。 - 請求項67または68に記載の方法に従う、結果として生じた構造。
- 生体高分子にラジカルを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 生体高分子にラジカルを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 生体高分子にアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 生体高分子にアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 生体高分子にラジカルおよびアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 生体高分子にラジカルおよびアニオンを組み込むことを含む、生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 生体高分子を改変する方法であって、結果として生じる形成された構造が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 結果として生じる生体高分子が基質と複合体を形成するように生体高分子を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 結果として生じる生体高分子が基質と複合体を形成するように生体高分子を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 結果として生じる改変された基質が生体高分子と複合体を形成するように基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 結果として生じる改変された基質が生体高分子と複合体を形成するように基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 結果として生じる改変された生体高分子および基質が複合体を形成するように生体高分子および基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーが、NEGのアニオンがプロトンまたは他のカチオンと結合しているときの式(I)の対応する構造における該エネルギーより低い、方法。 - 結果として生じる改変された生体高分子および基質が複合体を形成するように生体高分子および基質を改変する方法であって、結果として生じる形成された基質-複合体が、式(I)
RAD-L-NEG
(I)
であり、
式中、
RADが、ラジカルを含む基であり、
NEGが、プロトンまたは他のカチオンに結合することができるアニオンを含む基であり、
LがNEGおよびRADを連結し、
RADのラジカルがNEGのアニオンとπ共役せず、かつ
改変後に、RADの最低半占軌道(SOMO)のエネルギーがNEGの二重被占軌道(DOMO)のエネルギーより低く、かつ
NEGのアニオンがプロトンまたは他のカチオンと結合しているときに、RADのSOMOのエネルギーがNEGのDOMOのエネルギーより高い、方法。 - 改変が生体高分子の活性部位に対する改変である、請求項70〜79、82、および83のいずれか一項に記載の生体高分子を改変する方法。
- 請求項70〜84のいずれか一項に記載の改変された生体高分子および/または改変された基質。
- 請求項85に記載の改変された生体高分子および/または改変された基質の使用。
- RADのラジカルが安定化される、請求項1〜86のいずれか一項に記載の方法、使用、構造、または保護基。
- RADのラジカルが非局在化される、請求項1〜87のいずれか一項に記載の方法、使用、構造、または保護基。
- RADのラジカルがLと共役している、請求項1〜88のいずれか一項に記載の方法、使用、構造、または保護基。
- RADが、立体的および/または電子的に安定化されたラジカルを含む、請求項1〜89のいずれか一項に記載の方法、使用、構造、または保護基。
- RADのラジカルが、そのラジカルに近接する基によって電子的および/または立体的に安定化される、請求項1〜90のいずれか一項に記載の方法、使用、構造、または保護基。
- RADが、電子的に安定化されたラジカルを含む、請求項1〜91のいずれか一項に記載の方法、使用、構造、または保護基。
- DNA/RNA塩基がグアニン(G)、アデニン(A)、シトシン(C)、チミン(T)、またはウラシル(U)より選択される、請求項93に記載の方法、使用、構造、または保護基。
- RADが、
2,2',6,6'-テトラメチルピペリジン-N-オキシル(TEMPO)、
2,2',5,5'-テトラメチルピロリジン-N-オキシル(PROXYL)、
2,2,5,5-テトラメチル-4-フェニル-3-アザヘキサン-3-オキシル(TIPNO)、
N,N-(1,1-ジメチルエチル-1)-(1-ジエチル-ホスホノ-2,2-ジメチル-プロピル-1)-N-オキシル(SG1)、
グアニンベースまたはグリシルベースのラジカル
の群より選択されるラジカル基を含む、請求項1〜94のいずれか一項に記載の方法、使用、構造、または保護基。 - NEGのアニオンが不安定化される、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜95のいずれか一項に記載の方法、使用、構造、または保護基。
- NEGのアニオンの負電荷が、そのアニオンの外側にあるいかなる基にも非局在化されない、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜96のいずれか一項に記載の方法、使用、構造、または保護基。
- NEGのアニオンがLとπ共役していない、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜97のいずれか一項に記載の方法、使用、構造、または保護基。
- NEGが、立体的および/または電子的に不安定化されたアニオンを含む、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜98のいずれか一項に記載の方法、使用、構造、または保護基。
- NEGのアニオンが、そのアニオンに近接する基によって電子的および/または立体的に不安定化される、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜99のいずれか一項に記載の方法、使用、構造、または保護基。
- NEGが、電子的に不安定化されたアニオンを含む、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜100のいずれか一項に記載の方法、使用、構造、または保護基。
- LがRADとの共役を含む、請求項1〜102いずれか一項に記載の方法、使用、構造、または保護基。
- LがNEGとのπ共役を含まない、請求項1〜103のいずれか一項に記載の方法、使用、構造、または保護基。
- Lが2個以上の部分で構成され、かつ該部分の少なくとも2個が非共有結合により一緒に結合される、請求項1〜104のいずれか一項に記載の方法、使用、構造、または保護基。
- 非共有結合が水素結合または静電結合である、請求項105に記載の方法、使用、構造、または保護基。
- 1つまたは複数の部分が、1つまたは複数のDNA/RNA塩基、アミノ酸、ペプチド、補因子、酵素、酵素断片、活性化酵素、生体高分子、または酵素基質を含み、該部分が、天然のものであるか、天然のものから改変されているか、または合成のものである、請求項105または79に記載の方法、使用、構造、または保護基。
- Lが2個以上の部分で構成され、かつ該部分の少なくとも2個が1つまたは複数の金属中心に結合する、請求項1〜107のいずれか一項に記載の方法、使用、構造、または保護基。
- 金属中心が、アルカリ金属カチオンおよび遷移金属カチオンを含む群より選択される、請求項108に記載の方法、使用、構造、または保護基。
- Lが複数のNEG基および/またはRAD基を連結する、請求項1〜109のいずれか一項に記載の方法、使用、構造、または保護基。
- Lが1つまたは複数のポリマー部分を含む、請求項1〜110のいずれか一項に記載の方法、使用、構造、または保護基。
- Lが、結合、水素結合、非共有結合、静電結合、金属結合、アルキル、環式アルキル、アリール、アルケン、アルキン、複素環式化合物、複素環式芳香族化合物、糖、金属錯体のうちの1つもしくは複数を含むか、またはスルースペース相互作用である、請求項1〜111のいずれか一項に記載の方法、使用、構造、または保護基。
- Lが、結合、フェニル、ビフェニル、C1-C20アルキル、C3-C20シクロアルキル、RNAベースの糖、DNAベースの糖を含む群より選択される、請求項1〜112のいずれか一項に記載の方法、使用、構造、または保護基。
- 請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜114のいずれか一項に記載の式(I)の構造を含む治療的有効量の化合物を投与することを含む、医学的状態の医学的処置方法。
- 医学的状態を処置および/または予防するための医薬を製造するための、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜114のいずれか一項に記載の式(I)の構造を含む化合物の使用。
- 療法において使用するための、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜114のいずれか一項に記載の式(I)の構造を含む化合物の使用。
- 医学的状態を処置するための、請求項7〜9、17〜53、55、56、58〜61、63〜66、68〜100のいずれか一項に記載の式(I)の構造を含む化合物の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2013900373 | 2013-02-06 | ||
| AU2013900373A AU2013900373A0 (en) | 2013-02-06 | Radical orbital switching | |
| AU2013900371 | 2013-02-06 | ||
| AU2013900371A AU2013900371A0 (en) | 2013-02-06 | Radical orbital switching | |
| PCT/AU2014/000085 WO2014121327A1 (en) | 2013-02-06 | 2014-02-06 | Radical orbital switching |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016508488A true JP2016508488A (ja) | 2016-03-22 |
| JP2016508488A5 JP2016508488A5 (ja) | 2017-02-09 |
Family
ID=51299075
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015555501A Pending JP2016508488A (ja) | 2013-02-06 | 2014-02-06 | ラジカル軌道スイッチング |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20160075732A1 (ja) |
| EP (1) | EP2953916A4 (ja) |
| JP (1) | JP2016508488A (ja) |
| CN (1) | CN105209410A (ja) |
| AU (1) | AU2014214532B2 (ja) |
| CA (1) | CA2900272A1 (ja) |
| WO (1) | WO2014121327A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020089048A1 (en) * | 2018-10-29 | 2020-05-07 | Universiteit Gent | Admixture for a cementitious material to influence the rheology properties of the cementitious material |
| CN110265646B (zh) * | 2019-06-25 | 2022-09-16 | 西南大学 | 一种氮掺杂类石墨烯活性碳材料及其制备方法和应用 |
| CN113707226B (zh) * | 2021-08-24 | 2024-08-06 | 西安热工研究院有限公司 | 一种建立木糖-木酮糖相互转化时微观动力学模型的方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10195136A (ja) * | 1996-12-26 | 1998-07-28 | Elf Atochem Sa | (メタ)アクリル単量体、ビニル単量体、ビニリデン単量体、及びジエン単量体を制御下でラジカル重合又は共重合する方法並びに該方法により得られる(共)重合体 |
| JP2001514697A (ja) * | 1997-03-11 | 2001-09-11 | カーネギー メロン ユニヴァーシティー | 原子または基転移ラジカル重合の改良 |
| WO2002079284A1 (en) * | 2001-03-30 | 2002-10-10 | Zipat Ab | New material |
| JP2003096054A (ja) * | 2001-09-25 | 2003-04-03 | Nof Corp | アルコキシアミンおよびその製造方法 |
| WO2009111725A1 (en) * | 2008-03-07 | 2009-09-11 | Carnegie Mellon University | Improved controlled radical polymerization processes |
| CN102746515A (zh) * | 2012-07-16 | 2012-10-24 | 浙江大学 | 一种嵌段共聚物的制备方法 |
-
2014
- 2014-02-06 AU AU2014214532A patent/AU2014214532B2/en not_active Ceased
- 2014-02-06 US US14/765,967 patent/US20160075732A1/en not_active Abandoned
- 2014-02-06 WO PCT/AU2014/000085 patent/WO2014121327A1/en not_active Ceased
- 2014-02-06 JP JP2015555501A patent/JP2016508488A/ja active Pending
- 2014-02-06 CN CN201480019844.9A patent/CN105209410A/zh active Pending
- 2014-02-06 CA CA2900272A patent/CA2900272A1/en not_active Abandoned
- 2014-02-06 EP EP14748562.7A patent/EP2953916A4/en not_active Withdrawn
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10195136A (ja) * | 1996-12-26 | 1998-07-28 | Elf Atochem Sa | (メタ)アクリル単量体、ビニル単量体、ビニリデン単量体、及びジエン単量体を制御下でラジカル重合又は共重合する方法並びに該方法により得られる(共)重合体 |
| JP2001514697A (ja) * | 1997-03-11 | 2001-09-11 | カーネギー メロン ユニヴァーシティー | 原子または基転移ラジカル重合の改良 |
| WO2002079284A1 (en) * | 2001-03-30 | 2002-10-10 | Zipat Ab | New material |
| JP2003096054A (ja) * | 2001-09-25 | 2003-04-03 | Nof Corp | アルコキシアミンおよびその製造方法 |
| WO2009111725A1 (en) * | 2008-03-07 | 2009-09-11 | Carnegie Mellon University | Improved controlled radical polymerization processes |
| CN102746515A (zh) * | 2012-07-16 | 2012-10-24 | 浙江大学 | 一种嵌段共聚物的制备方法 |
Non-Patent Citations (9)
| Title |
|---|
| AKDOGAN, YASAR ET AL.: "The solvation of nitroxide radicals in ionic liquids studied by high-field EPR spectroscopy", PHYSICAL CHEMISTRY CHEMICAL PHYSICS, vol. 12(28), JPN6017044043, 2010, pages 7874 - 82, ISSN: 0003814553 * |
| ATIK, SAMIR ET AL.: "Fluorescence quenching by nitroxyl radicals in micellar environments. A useful probe for studyi", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 100(10), JPN6017044040, 1978, pages 3234 - 5, ISSN: 0003814551 * |
| EDELEVA, MARIYA V. ET AL.: "pH-Sensitive C-ON Bond Homolysis of Alkoxyamines of Imidazoline Series with Multiple Ionizable Group", JOURNAL OF ORGANIC CHEMISTRY, vol. 76(14), JPN6017044033, 2011, pages 5558 - 73, ISSN: 0003814547 * |
| FUJITA, W. ET AL.: "Intercalation of stable organic radicals into layered copper hydroxides", SYNTHETIC METALS, vol. 122(3), JPN6017044039, 2001, pages 569 - 72, ISSN: 0003814550 * |
| GRYN'OVA, GANNA ET AL.: "Origin and Scope of Long-Range Stabilizing Interactions and Associated SOMO-HOMO Conversion in D", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 135(41), JPN6017044050, 2013, pages 15392 - 403, ISSN: 0003683732 * |
| KIRK, BENJAMIN B.; HARMAN, DAVID. G.; BLANKSBY, STEPHEN J.: "Direct Observation of the Gas Phase Reaction of the Cyclohexyl Radical with Dioxygen using a Dis", JOURNAL OF PHYSICAL CHEMISTRY A, vol. 114(3), JPN6017044046, 2010, pages 1446 - 56, ISSN: 0003683731 * |
| LAGERCRANTZ, CARL ET AL.: "Formation of aminoxyl radicals in alkaline water solutions from spin traps and short-lived radic", ACTA CHEMICA SCANDINAVICA, vol. 49(6), JPN6017044041, 1995, pages 399 - 404, ISSN: 0003814552 * |
| POREL, MINTU ET AL.: "Interaction between Encapsulated Excited Organic Molecules and Free Nitroxides: Communication Across", LANGMUIR, vol. 27(17), JPN6017044035, 2011, pages 10548 - 55, ISSN: 0003814548 * |
| STREHMEL, VERONIKA ET AL.: "Temperature dependence of interactions between stable piperidine-1-yloxyl derivatives and an ionic l", CHEMPHYSCHEM, vol. 9(9), JPN6017044037, 2008, pages 1294 - 302, ISSN: 0003814549 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN105209410A (zh) | 2015-12-30 |
| CA2900272A1 (en) | 2014-08-14 |
| US20160075732A1 (en) | 2016-03-17 |
| AU2014214532B2 (en) | 2018-02-22 |
| WO2014121327A1 (en) | 2014-08-14 |
| AU2014214532A1 (en) | 2015-08-20 |
| EP2953916A4 (en) | 2016-10-26 |
| EP2953916A1 (en) | 2015-12-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Gryn'ova et al. | Switching radical stability by pH-induced orbital conversion | |
| Escobar et al. | Molecular recognition in water using macrocyclic synthetic receptors | |
| Cockroft et al. | Substituent effects on aromatic stacking interactions | |
| Baytekin et al. | Mass spectrometric studies of non-covalent compounds: why supramolecular chemistry in the gas phase? | |
| Kimura et al. | Selective and Efficient Recognition of Thymidylylthymidine (TpT) by Bis (ZnII‐cyclen) and Thymidylylthymidylylthymidine (TpTpT) by Tris (ZnII‐cyclen) at Neutral pH in Aqueous Solution | |
| Liang et al. | Synthesis, physicochemical properties, and hydrogen bonding of 4 (5)‐substituted 1‐H‐imidazole‐2‐carboxamide, a potential universal reader for DNA sequencing by recognition tunneling | |
| JP2016508488A (ja) | ラジカル軌道スイッチング | |
| Molawi et al. | Tin‐Free Radical Alkoxyamine Addition and Isomerization Reactions by Using the Persistent Radical Effect: Variation of the Alkoxyamine Structure | |
| ES2616707T3 (es) | Líquido iónico que contiene el anión alilsulfonato | |
| Pozharskii et al. | Proton sponges and hydrogen transfer phenomena | |
| Chandra et al. | Potential inhibitors of DNA topoisomerase II: ruthenium (II) poly-pyridyl and pyridyl-azine complexes | |
| Prasad et al. | Flexible versus rigid G‐quadruplex DNA ligands: synthesis of two series of bis‐indole derivatives and comparison of their interactions with G‐quadruplex DNA | |
| Vušurović et al. | Interactions of protonated guanidine and guanidine derivatives with multiply deprotonated RNA probed by electrospray ionization and collisionally activated dissociation | |
| Žabka et al. | Ternary complexes of chiral disulfonimides in transfer-hydrogenation of imines: the relevance of late intermediates in ion pair catalysis | |
| Gronert et al. | The gas phase acid/base properties of 1, 3,-dimethyluracil, 1-methyl-2-pyridone, and 1-methyl-4-pyridone: relevance to the mechanism of orotidine-5′-monophosphate decarboxylase | |
| Huang et al. | Uv–vis photodissociation action spectroscopy reveals cytosine–guanine hydrogen transfer in dna tetranucleotide cation radicals upon one-electron reduction | |
| Bagryanskaya et al. | Can the first addition of alkyl radicals play a role in the fate of NMP? | |
| Sun et al. | Reaction kinetics, product branching, and potential energy surfaces of 1O2-induced 9-methylguanine–lysine cross-linking: a combined mass spectrometry, spectroscopy, and computational study | |
| Nguyen et al. | Comparison of collision-induced dissociation and electron-induced dissociation of singly charged mononucleotides | |
| Aggarwal et al. | Novel pyridinium oximes: synthesis, molecular docking and in vitro reactivation studies | |
| Bacon et al. | Homolysis and decomposition of alkoxyamines containing PROXYL and TEMPO residues: A comparison | |
| Parchami et al. | Effect of intramolecular hydrogen bonding of α, ω–diamines on the structure and exchange affinity of 18–crown–6-amine host-guest complexes in gas phase: A collision cross section measurements by ion mobility spectrometry | |
| Bandopadhyay et al. | Unprecedented copper (ii) coordination induced nucleophilic cleavage of a quinoxaline heterocycle: structural and computational studies | |
| US7132540B1 (en) | Hindered spiro-ketal nitroxides | |
| Leavell et al. | Determination of phosphate position in hexose monosaccharides using an FTICR mass spectrometer: ion/molecule reactions, labeling studies, and dissociation mechanisms |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161216 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20161216 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20171026 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20171120 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180412 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180611 |