JP2015529556A - Selective catalytic deoxygenation of biomass and catalyst therefor - Google Patents
Selective catalytic deoxygenation of biomass and catalyst therefor Download PDFInfo
- Publication number
- JP2015529556A JP2015529556A JP2015525874A JP2015525874A JP2015529556A JP 2015529556 A JP2015529556 A JP 2015529556A JP 2015525874 A JP2015525874 A JP 2015525874A JP 2015525874 A JP2015525874 A JP 2015525874A JP 2015529556 A JP2015529556 A JP 2015529556A
- Authority
- JP
- Japan
- Prior art keywords
- pyrolysis
- hydrotalcite
- catalyst
- calcined
- metals
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/84—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with arsenic, antimony, bismuth, vanadium, niobium, tantalum, polonium, chromium, molybdenum, tungsten, manganese, technetium or rhenium
- B01J23/847—Vanadium, niobium or tantalum or polonium
- B01J23/8474—Niobium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J21/00—Catalysts comprising the elements, oxides, or hydroxides of magnesium, boron, aluminium, carbon, silicon, titanium, zirconium, or hafnium
- B01J21/16—Clays or other mineral silicates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/007—Mixed salts
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/10—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of rare earths
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/16—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of arsenic, antimony, bismuth, vanadium, niobium, tantalum, polonium, chromium, molybdenum, tungsten, manganese, technetium or rhenium
- B01J23/24—Chromium, molybdenum or tungsten
- B01J23/28—Molybdenum
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/16—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of arsenic, antimony, bismuth, vanadium, niobium, tantalum, polonium, chromium, molybdenum, tungsten, manganese, technetium or rhenium
- B01J23/32—Manganese, technetium or rhenium
- B01J23/34—Manganese
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/78—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with alkali- or alkaline earth metals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/83—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with rare earths or actinides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0201—Impregnation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0201—Impregnation
- B01J37/0207—Pretreatment of the support
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0201—Impregnation
- B01J37/0213—Preparation of the impregnating solution
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/08—Heat treatment
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/08—Heat treatment
- B01J37/082—Decomposition and pyrolysis
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10B—DESTRUCTIVE DISTILLATION OF CARBONACEOUS MATERIALS FOR PRODUCTION OF GAS, COKE, TAR, OR SIMILAR MATERIALS
- C10B49/00—Destructive distillation of solid carbonaceous materials by direct heating with heat-carrying agents including the partial combustion of the solid material to be treated
- C10B49/16—Destructive distillation of solid carbonaceous materials by direct heating with heat-carrying agents including the partial combustion of the solid material to be treated with moving solid heat-carriers in divided form
- C10B49/20—Destructive distillation of solid carbonaceous materials by direct heating with heat-carrying agents including the partial combustion of the solid material to be treated with moving solid heat-carriers in divided form in dispersed form
- C10B49/22—Destructive distillation of solid carbonaceous materials by direct heating with heat-carrying agents including the partial combustion of the solid material to be treated with moving solid heat-carriers in divided form in dispersed form according to the "fluidised bed" technique
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10B—DESTRUCTIVE DISTILLATION OF CARBONACEOUS MATERIALS FOR PRODUCTION OF GAS, COKE, TAR, OR SIMILAR MATERIALS
- C10B53/00—Destructive distillation, specially adapted for particular solid raw materials or solid raw materials in special form
- C10B53/02—Destructive distillation, specially adapted for particular solid raw materials or solid raw materials in special form of cellulose-containing material
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10B—DESTRUCTIVE DISTILLATION OF CARBONACEOUS MATERIALS FOR PRODUCTION OF GAS, COKE, TAR, OR SIMILAR MATERIALS
- C10B57/00—Other carbonising or coking processes; Features of destructive distillation processes in general
- C10B57/04—Other carbonising or coking processes; Features of destructive distillation processes in general using charges of special composition
- C10B57/06—Other carbonising or coking processes; Features of destructive distillation processes in general using charges of special composition containing additives
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10C—WORKING-UP PITCH, ASPHALT, BITUMEN, TAR; PYROLIGNEOUS ACID
- C10C5/00—Production of pyroligneous acid distillation of wood, dry distillation of organic waste
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10G—CRACKING HYDROCARBON OILS; PRODUCTION OF LIQUID HYDROCARBON MIXTURES, e.g. BY DESTRUCTIVE HYDROGENATION, OLIGOMERISATION, POLYMERISATION; RECOVERY OF HYDROCARBON OILS FROM OIL-SHALE, OIL-SAND, OR GASES; REFINING MIXTURES MAINLY CONSISTING OF HYDROCARBONS; REFORMING OF NAPHTHA; MINERAL WAXES
- C10G1/00—Production of liquid hydrocarbon mixtures from oil-shale, oil-sand, or non-melting solid carbonaceous or similar materials, e.g. wood, coal
- C10G1/02—Production of liquid hydrocarbon mixtures from oil-shale, oil-sand, or non-melting solid carbonaceous or similar materials, e.g. wood, coal by distillation
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10G—CRACKING HYDROCARBON OILS; PRODUCTION OF LIQUID HYDROCARBON MIXTURES, e.g. BY DESTRUCTIVE HYDROGENATION, OLIGOMERISATION, POLYMERISATION; RECOVERY OF HYDROCARBON OILS FROM OIL-SHALE, OIL-SAND, OR GASES; REFINING MIXTURES MAINLY CONSISTING OF HYDROCARBONS; REFORMING OF NAPHTHA; MINERAL WAXES
- C10G1/00—Production of liquid hydrocarbon mixtures from oil-shale, oil-sand, or non-melting solid carbonaceous or similar materials, e.g. wood, coal
- C10G1/08—Production of liquid hydrocarbon mixtures from oil-shale, oil-sand, or non-melting solid carbonaceous or similar materials, e.g. wood, coal with moving catalysts
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10G—CRACKING HYDROCARBON OILS; PRODUCTION OF LIQUID HYDROCARBON MIXTURES, e.g. BY DESTRUCTIVE HYDROGENATION, OLIGOMERISATION, POLYMERISATION; RECOVERY OF HYDROCARBON OILS FROM OIL-SHALE, OIL-SAND, OR GASES; REFINING MIXTURES MAINLY CONSISTING OF HYDROCARBONS; REFORMING OF NAPHTHA; MINERAL WAXES
- C10G1/00—Production of liquid hydrocarbon mixtures from oil-shale, oil-sand, or non-melting solid carbonaceous or similar materials, e.g. wood, coal
- C10G1/08—Production of liquid hydrocarbon mixtures from oil-shale, oil-sand, or non-melting solid carbonaceous or similar materials, e.g. wood, coal with moving catalysts
- C10G1/086—Characterised by the catalyst used
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J27/00—Catalysts comprising the elements or compounds of halogens, sulfur, selenium, tellurium, phosphorus or nitrogen; Catalysts comprising carbon compounds
- B01J27/20—Carbon compounds
- B01J27/232—Carbonates
- B01J27/236—Hydroxy carbonates
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E50/00—Technologies for the production of fuel of non-fossil origin
- Y02E50/10—Biofuels, e.g. bio-diesel
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P30/00—Technologies relating to oil refining and petrochemical industry
- Y02P30/20—Technologies relating to oil refining and petrochemical industry using bio-feedstock
Abstract
本発明は、バイオマスの熱分解での使用に適合させた新しい効果的な熱分解触媒、そのような触媒の調製、並びに空気の添加、分子状酸素の添加、及び分子状水素の添加及び水のような液体の添加を除外したバイオマスの熱分解でのそのような触媒の使用を提供する。触媒は、金属の特定の対を含浸させている層状のHTC及び関連物質であり、含浸させた層状のHTC及び関連物質は空気中にて高温で焼成されている。【選択図】図1The present invention relates to a new and effective pyrolysis catalyst adapted for use in biomass pyrolysis, the preparation of such a catalyst, and the addition of air, addition of molecular oxygen, and addition of molecular hydrogen and water. The use of such a catalyst in the pyrolysis of biomass, excluding the addition of such liquids, is provided. A catalyst is a layered HTC and related material impregnated with a specific pair of metals, and the impregnated layered HTC and related material is calcined at high temperature in air. [Selection] Figure 1
Description
本発明は、バイオマスの熱分解で使用するのに適合した新しい効果的な熱分解触媒、そのような触媒の調製、及び空気の添加、分子状酸素の添加、分子状水素の添加及び/又は水のような液体の添加を除外したバイオマスの熱分解におけるそのような触媒の使用に関する。 The present invention provides a new and effective pyrolysis catalyst adapted for use in biomass pyrolysis, the preparation of such a catalyst, and the addition of air, the addition of molecular oxygen, the addition of molecular hydrogen and / or water. To the use of such catalysts in the pyrolysis of biomass, excluding the addition of liquids such as
長年にわたる鋭意研究にもかかわらず、バイオマスを効果的に触媒的に熱分解して選択的に集中させた、炭化水素及び/又は炭化水素前駆体に富む熱分解流体を形成する問題が依然として存在する。熱分解の生成物及び工程を改善する試みにおいて、水又は水素の添加を伴って又は伴わずに低い熱分解温度を使用することが提案されてきた。我々の研究室では、残念ながら、少なくとも水又は水素の非存在下では、低温の使用はコークスに変換される炭素の量を実質的に増やし、それによって炭素含量に関する極めて低い効率の処理を生じることが見いだされている。これは同様に、製造される炭化水素様の生成物の低い収率のために炭化水素様の輸送燃料を製造するための熱分解処理の有用性に対して有害な効果を有する。 Despite years of diligent research, there remains a problem of forming pyrolysis fluids rich in hydrocarbons and / or hydrocarbon precursors that effectively catalytically pyrolyze and selectively concentrate biomass. . In attempts to improve pyrolysis products and processes, it has been proposed to use low pyrolysis temperatures with or without the addition of water or hydrogen. In our laboratory, unfortunately, at least in the absence of water or hydrogen, the use of low temperatures can substantially increase the amount of carbon that is converted to coke, thereby resulting in a very low efficiency treatment for carbon content. Has been found. This also has a detrimental effect on the usefulness of pyrolysis processes for producing hydrocarbon-like transportation fuels due to the low yield of hydrocarbon-like products produced.
好適な種類のバイオマスの熱分解の間に、特定の選択された方向にて熱分解脱酸素を触媒的に集中させ、指図し、又は誘導することが可能であることが今や見いだされている。これは同様に、種々の方法で濃縮される気体様の生成物(一酸化炭素、二酸化炭素及び水)の形成を可能にする。さらに、たとえば、低い酸性、低い酸素含量、低下した腐食性、及び所望の炭素/水素比のような改善された特性を有する熱分解油を生じることができる。その結果、必要とされる熱分解油の後処理が少なく、熱分解油における酸素を含有する極性化合物の量が低下するので化石燃料とのさらに良好な相溶性/混和性が達成される。 It has now been found that pyrolysis deoxygenation can be catalytically concentrated, directed or directed in a specific selected direction during the pyrolysis of a suitable type of biomass. This likewise allows the formation of gaseous products (carbon monoxide, carbon dioxide and water) that are concentrated in various ways. In addition, pyrolytic oils can be produced that have improved properties such as, for example, low acidity, low oxygen content, reduced corrosivity, and the desired carbon / hydrogen ratio. As a result, less post-treatment of pyrolysis oil is required and better compatibility / miscibility with fossil fuels is achieved because the amount of oxygen-containing polar compounds in the pyrolysis oil is reduced.
本発明は、とりわけ、固体状態のバイオマス物質を熱分解して、改善された特性を有する熱分解油と気体様のCO、CO2及び/又はH2Oの混合物とを生じる方法を提供することによって、これらの利点の達成を可能にする。そのような方法は、
(I)熱分解反応器にて撹拌のもとで
(A)任意の乾燥及び/又は破砕を除いて未処理である粒子状の又は細かく分けた固体状態のバイオマス物質;
(B)反応器に装填される際(すなわち、装填される直前)、(1)単一対の金属、(2)単一対の金属それぞれの少なくとも1つの酸化物又は(3)(a)単一対の金属の一方若しくは双方の少なくとも1つの酸化物と(b)単一対の金属の一方若しくは双方の少なくとも1つの遊離の金属を含浸した又は運ぶ、少なくとも1つの焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含む、それから本質的に成る、又はそれから成る焼成生成物である、含浸された又はドープされた固体状態の焼成熱分解触媒と、(その際、前記焼成生成物は、遊離の酸素の存在下(たとえば、空気又は酸素と窒素、ネオン、アルゴン若しくはクリプトンから選択される少なくとも1つの不活性気体の混合物)で前記対の金属の塩を含浸させている又はそれを運ぶ、少なくとも1つの予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を焼成することによって形成され、(1)、(2)又は(3)の単一対の金属は、以下の群:CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYから選択され);及び
(C)固体状態の粒子状熱媒を接触させることによって混合物を形成することと、
(II)空気の添加、分子状酸素の添加、分子状水素の添加、及び/又は水のような液体の希釈剤若しくは担体の添加を除外して(を伴わずに)熱分解反応器の中で約500℃を超える1以上の温度にて(I)の前記混合物の少なくとも一部を迅速に又は瞬時に熱分解し、それによって流体の熱分解生成物を形成することを含む。言い換えれば、以下のいずれも添加しない:(i)空気、(ii)分子状酸素、(iii)分子状水素、(iv)水のような液体希釈剤。
上記(I)(B)にて特定された個々の触媒を用いるそのような方法のそれぞれが本発明の個々の実施形態を構成する。前述の方法は、(1)改善された品質の及び/又は炭化水素含量が豊富な熱分解油、及び/又は(2)一酸化炭素又は二酸化炭素又は水、又は一酸化炭素、二酸化炭素、水のうち2つ又はすべての混合物が選択的に豊富な気相を含む流体の熱分解生成物の形成を可能にする。
The present invention provides, inter alia, a method for pyrolyzing solid state biomass material to produce pyrolysis oils with improved properties and mixtures of gaseous CO, CO 2 and / or H 2 O. Makes it possible to achieve these advantages. Such a method is
(I) under agitation in a pyrolysis reactor (A) particulate or finely divided solid biomass material that is untreated except for any drying and / or crushing;
(B) When loaded into the reactor (ie, just prior to loading): (1) a single pair of metals, (2) at least one oxide of each single pair of metals, or (3) (a) a single pair At least one calcined hydrotalcite or hydrotalcite impregnated or carrying at least one oxide of one or both of the metals and (b) at least one free metal of one or both of a single pair of metals Impregnated or doped solid state calcination comprising, consisting essentially of, or consisting of a calcination product comprising such compounds, layered dihydroxides, anionic clays, or mixtures of two or more thereof A pyrolysis catalyst, wherein the calcined product is selected in the presence of free oxygen (eg air or oxygen and nitrogen, neon, argon or krypton At least one pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide impregnated with or carrying a salt of said pair of metals with a mixture of at least one inert gas) , An anionic clay, or a mixture of two or more thereof, and a single pair of metals of (1), (2), or (3) is composed of the following groups: Ca and Ce, Ca and Cu, Selected from Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, Ni and Y And (C) forming a mixture by contacting the solid state particulate heat medium;
(II) In the pyrolysis reactor, excluding (without) the addition of air, molecular oxygen, molecular hydrogen, and / or the addition of a liquid diluent or carrier such as water. At least one portion of the mixture of (I) at a temperature of one or more above about 500 ° C. rapidly or instantaneously pyrolyzing, thereby forming a fluid pyrolysis product. In other words, none of the following is added: (i) liquid diluent such as air, (ii) molecular oxygen, (iii) molecular hydrogen, (iv) water.
Each such method using the individual catalysts identified in (I) and (B) above constitutes an individual embodiment of the present invention. The above-described methods may include (1) pyrolysis oil of improved quality and / or rich hydrocarbon content, and / or (2) carbon monoxide or carbon dioxide or water, or carbon monoxide, carbon dioxide, water Two or all of the mixtures allow the formation of a pyrolysis product of a fluid containing a selectively rich gas phase.
クレームを含む本明細書で使用されるとき、語句「再水和された、含浸された又はドープされた固体状態の焼成熱分解触媒」における用語「再水和された」は、触媒組成物の形成を完了する最終的な焼成工程の前で触媒調製の好適な段階にて、触媒を活性化させる再水和が行われることを意味する。 As used herein, including the claims, the term “rehydrated” in the phrase “rehydrated, impregnated or doped solid state calcined pyrolysis catalyst” refers to the catalyst composition. It means that rehydration is performed to activate the catalyst at a suitable stage of catalyst preparation prior to the final calcination step to complete formation.
単語「触媒」が使用される場合はいつでも、使用の際、種々の反応条件下でそれ(「触媒」)は他の物質に暴露されるので、言及される物質は触媒前駆体とみなされるべきであることが理解され、正しく認識されるべきである。従って、反応器に装填される際、それ(「触媒」)は、上記(B)の成分(1)、(2)又は(3)を含浸させた又はそれで運ばれる少なくとも1つのハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物から形成される焼成生成物を含む、それから本質的に成る、又は成るけれども、それ(「触媒」)は熱分解反応器に存在する特定の反応条件下で化学変化を受けてもよい。 Whenever the word “catalyst” is used, the material referred to should be considered a catalyst precursor because in use it (“catalyst”) is exposed to other materials under various reaction conditions. It should be understood and recognized correctly. Thus, when charged to the reactor, it (“catalyst”) is impregnated with or carried by component (1), (2) or (3) of (B) above or at least one hydrotalcite It comprises, consists essentially of, or consists of a calcined product formed from a hydrotalcite-like compound, a layered dihydroxide, an anionic clay, or a mixture of two or more thereof ("catalyst") May undergo chemical changes under certain reaction conditions present in the pyrolysis reactor.
用語「ハイドロタルサイト」、「ハイドロタルサイト様の化合物」、「層状二水酸化物」及び「アニオン性粘土」は生成物のよく認識されたカテゴリーについての代替的な表現として当該技術でみなされる。実際、層状の二重水酸化物及びアニオン性粘土のような種々の他の名称も当該技術ではこれらの物質に適用されている。これに関連してRives,V.;Ed.“Layered Double Hydroxides: Present and Future”,Nova Science Publishers,Inc.,New York,2001の第1章を参照のこと。これらの物質は当該技術で周知であり、十分に記載され、性状分析されているので、そのような物質に関するさらなる情報を所望する人は誰でも本発明の実践に有用な天然の及び合成の材料を理解するのに利用できる十二分な源材料を有する。そのような情報の他の有用な供給源は、F.Cavaniら、 “Hydrotalcite−Type Anionic Clays:Preparation,Properties and Applications”,Catalysis Today,11(1991) Elsevier Science Publishers B.V.Amsterdam;及びJ.P.Besseら、Anionic Clays: Trends in Pillary Chemistry, its Synthesis and Microporous Solids (1992),2,108,editors:M.I.Occelli,H.E.Robson,Van Nostrand Reinhold,N.Y.である。都合上、用語「ハイドロタルサイト」、「ハイドロタルサイト様の化合物」又は「HTC」は単数であろうと複数であろうと、本文書では物質のカテゴリー全体(ハイドロタルサイト、ハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土)を表すのに使用される。これらの物質が異なってもよい程度まで、もしあれば、その混合物を使用してもよい。合成の「HTC」が一般に好まれるが、天然の及び合成のハイドロタルサイトはこのカテゴリ
ーに含まれる。さらに好ましくは、使用されるHTCは、その酸化物を形成する2つの金属がマグネシウム及びアルミニウムである合成ハイドロタルサイトである。
The terms “hydrotalcite”, “hydrotalcite-like compound”, “layered dihydroxide” and “anionic clay” are considered in the art as alternative expressions for well-recognized categories of products . Indeed, various other names such as layered double hydroxides and anionic clays have also been applied to these materials in the art. In this context, Rivers, V.M. Ed. “Layered Double Hydroxides: Present and Future”, Nova Science Publishers, Inc. , New York, 2001, Chapter 1. Because these materials are well known in the art and are well described and characterized, anyone who wants more information about such materials can use natural and synthetic materials useful in the practice of the present invention. Have enough source material available to understand. Other useful sources of such information are F.I. Cavani et al., “Hydroitalite-Type Anionic Clays: Preparation, Properties and Applications”, Catalysis Today, 11 (1991) Elvis Science Publishers B. V. Amsterdam; and J.P. Besse et al., Anionic Clays: Trends in Pillar Chemistry, it's Synthesis and Microporous Solids (1992), 2, 108, editors: I. Occelli, H.C. E. Robson, Van Nostrand Reinhold, N.A. Y. It is. For convenience, the term “hydrotalcite”, “hydrotalcite-like compound” or “HTC”, whether singular or plural, is used in this document to refer to the entire category of substance (hydrotalcite, hydrotalcite-like compound). , Layered dihydroxide, anionic clay). To the extent that these materials may differ, mixtures thereof, if any, may be used. Synthetic "HTC" is generally preferred, but natural and synthetic hydrotalcites are included in this category. More preferably, the HTC used is a synthetic hydrotalcite in which the two metals forming the oxide are magnesium and aluminum.
上記で言及された熱分解法を実施することにおいて操作は迅速な又は瞬時の熱分解条件下で実施される。従って、温度は常温から秒当たり少なくとも100℃の速度で500℃を超えて上昇し、好ましくは約650℃よりも高くない。迅速な又は瞬時の熱分解を達成する別の方法は、熱分解反応器の中での熱分解生成物の平均滞留時間が非常に短い、通常30秒以下、好ましくは20秒以下、さらに好ましくは10秒以下であるように操作を行うことである。反応器の設計及び採用される補助装置に応じて、一層さらに短い平均滞留時間が可能である。普通、約700℃を超える熱分解温度は稀にしか使用されない。望ましくは、本発明で使用される最高熱分解温度は約650℃であり、好ましくは約575℃以下である。望ましい及び好まれる温度範囲は実質的に常圧で約500℃〜約600℃であり、約510℃〜約575℃の範囲である。使用することができる反応器には、流動床反応器、オージエ反応器、発泡反応器等が挙げられる。このうち、流動床反応器は非常に良好な成績を提供することが見いだされている。所望であれば、熱分解反応器から取り出した直後、水のような好適な液体によって熱分解生成物を冷ますことができる。 In carrying out the pyrolysis method mentioned above, the operation is carried out under rapid or instantaneous pyrolysis conditions. Thus, the temperature rises from room temperature at a rate of at least 100 ° C. per second, exceeding 500 ° C., and preferably not higher than about 650 ° C. Another way to achieve rapid or instantaneous pyrolysis is that the average residence time of the pyrolysis products in the pyrolysis reactor is very short, usually 30 seconds or less, preferably 20 seconds or less, more preferably The operation is to be 10 seconds or less. Depending on the reactor design and the auxiliary equipment employed, even shorter average residence times are possible. Usually, pyrolysis temperatures above about 700 ° C. are rarely used. Desirably, the maximum pyrolysis temperature used in the present invention is about 650 ° C, preferably about 575 ° C or less. A desirable and preferred temperature range is from about 500 ° C. to about 600 ° C. at substantially normal pressure and in the range of about 510 ° C. to about 575 ° C. Reactors that can be used include fluidized bed reactors, Auger reactors, foam reactors and the like. Of these, fluidized bed reactors have been found to provide very good performance. If desired, the pyrolysis product can be cooled with a suitable liquid, such as water, immediately after removal from the pyrolysis reactor.
操作の望ましい方式では、熱分解は実質的に常圧で行い、たとえば、乾燥窒素のような不活性無水担体ガス又はネオン、アルゴン若しくはクリプトンのような他の不活性無水担体ガスの流れにて固体状態のバイオマス物質を熱分解反応器に運び入れる。 In the preferred mode of operation, the pyrolysis is carried out at substantially atmospheric pressure and is solid, for example, in a stream of an inert anhydrous carrier gas such as dry nitrogen or other inert anhydrous carrier gas such as neon, argon or krypton. The biomass material in the state is brought into the pyrolysis reactor.
焼成後の得られた触媒組成物におけるHTCの量とは区別されるような追加対の2つの金属(金属として焼成される)の量は変化することができるが、通常、約1〜約10重量%の範囲、好ましくは4〜約9重量%の範囲であり、これらの比率は焼成組成物の総重量に基づく。含浸させ、焼成されたHTC触媒組成物における追加対の2つの金属(再び金属として焼成される)の互いに対する原子比は、通常約1:15〜約15:1の範囲であり、好ましくは約1:7〜約7:1の範囲であり、さらに好ましくは約1:3〜約3:1の範囲である。 The amount of the additional pair of two metals (calcined as a metal) as distinguished from the amount of HTC in the resulting catalyst composition after calcination can vary, but is usually from about 1 to about 10 In the range of wt%, preferably in the range of 4 to about 9 wt%, these ratios are based on the total weight of the fired composition. The atomic ratio of the additional pair of two metals (fired again as metal) to each other in the impregnated and calcined HTC catalyst composition is usually in the range of about 1:15 to about 15: 1, preferably about It is in the range of 1: 7 to about 7: 1, more preferably in the range of about 1: 3 to about 3: 1.
本文書の全体を通して使用されるとき、用語「固体状態のバイオマス」、「固体バイオマス」、「バイオマス」及び「バイオマス物質」は「固体状態のバイオマス物質」を指すのに使用されることがある。 As used throughout this document, the terms “solid state biomass”, “solid biomass”, “biomass” and “biomass material” may be used to refer to “solid state biomass material”.
種々の種類の固体状態のバイオマス物質を使用することができるけれども、リグノセルロース系バイオマスは本発明の熱分解法で使用するバイオマス物質の好ましい種類である。代表的なリグノセルロース系バイオマスはほぼ45重量%の炭素、ほぼ6%の水素及びほぼ49%の酸素を含有するが、他の類似のリグノセルロース系バイオマス物質も同様に代表的であり、使用に好ましいと思われる。 Although various types of solid state biomass material can be used, lignocellulosic biomass is a preferred type of biomass material for use in the pyrolysis process of the present invention. A typical lignocellulosic biomass contains approximately 45% by weight carbon, approximately 6% hydrogen and approximately 49% oxygen, although other similar lignocellulosic biomass materials are also representative and are in use. It seems preferable.
使用することができる固体状態の粒子状熱媒(伝熱剤とも呼ばれることがある)のうちで、砂(たとえば、シリカ砂)は豊富であり、非常に効果的である。たとえば、火山灰、粉砕岩、粉砕コンクリート等のような他の物質も所望であれば使用することができる。異なる固体状態の粒子状熱媒の混合物を所望であれば使用することができる。 Of the solid-state particulate heat media that can be used (sometimes referred to as heat transfer agents), sand (eg, silica sand) is abundant and very effective. For example, other materials such as volcanic ash, crushed rock, crushed concrete and the like can be used if desired. Mixtures of different solid state particulate heating media can be used if desired.
本発明の別の実施形態に従って、固体状態のバイオマス物質の熱分解を炭化水素が豊富な熱分解油の形成に向かって選択的に方向づけ、含酸素生成物及び/又は改善された特性を有する熱分解油のその中での形成から離れるように選択的に方向づけるように適合させた固体状態の熱分解触媒組成物;及び/又はCO、CO2及び/又はH2Oの1以上が選択的に豊富である熱分解気体の形成が提供される。反応器に装填された際(すなわち、装填される直前)の形態でのこれらの新しい触媒は、以下の群:CaとCe、CaとCu、C
aとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYから選択される金属の対の塩、好ましくは無機塩を含浸させた又は運ぶ少なくとも1つの予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含む、それから本質的に成る、又は成る少なくとも1つの触媒前駆体から形成される焼成触媒を含む、それから本質的に成る、又は成る。触媒前駆体の焼成は、金属の対の一方又は双方の少なくとも一部の1以上の酸化物が酸化物に変換されるように遊離の酸素(たとえば、空気又は酸素と窒素、ネオン、アルゴン若しくはクリプトンから選択される少なくとも1つの不活性気体の混合物)の存在下で実施される。この段落で言及される各焼成された触媒は本発明の個々の実施形態を構成する。
In accordance with another embodiment of the present invention, the pyrolysis of biomass material in the solid state is selectively directed towards the formation of a hydrocarbon-rich pyrolysis oil, heat with oxygenated products and / or improved properties. A solid state pyrolysis catalyst composition adapted to selectively direct away from formation of cracked oil therein; and / or one or more of CO, CO 2 and / or H 2 O is selectively Abundant pyrolysis gas formation is provided. These new catalysts in the form when loaded into the reactor (ie just before loading) are the following groups: Ca and Ce, Ca and Cu, C
a and Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, Ni and Y At least one pre-calcined hydrotalcite or hydrotalcite-like compound impregnated or carrying an inorganic salt, preferably an inorganic salt, layered dihydroxide, anionic clay, or two or more thereof Comprising, consisting essentially of, or consisting of a calcined catalyst formed from at least one catalyst precursor comprising, consisting essentially of, or consisting of. Calcination of the catalyst precursor is performed by free oxygen (eg, air or oxygen and nitrogen, neon, argon or krypton) such that at least a portion of one or both of the metal pair is converted to an oxide. In the presence of a mixture of at least one inert gas selected from: Each calcined catalyst referred to in this paragraph constitutes an individual embodiment of the present invention.
本発明の触媒は、一般式:[MII (1-x)MIII x(OH)2]x+[AII-]x/n・mH2Oによって通常表されるHTCから形成され、式中、MIIは、Mg2+、Co2+、Cu2+、Ni2+、Zn2+等のような二価の金属であり、MIIIはAl3+、Cr3+、Ga3+、Fe3+であり;AII-は有機イオン及び/又は無機イオンである。たとえば、Rives,V.,Editor.Layered Double Hydroxides:Present and Future,Nova Science Publishers,Inc.,New York,2001におけるA.Monzonらによる「LDHから調製される混合酸化物による水素化触媒」と題するものの第II章;Valenteら、Layered Double Hydroxides:Properties,Applications and Synthetic Procedures,SciTopics,Retrieved January 6,2012を参照のこと。 The catalyst of the present invention is formed from an HTC usually represented by the general formula: [M II (1-x) M III x (OH) 2 ] x + [A II− ] x / n · mH 2 O, , M II is a divalent metal such as Mg 2+ , Co 2+ , Cu 2+ , Ni 2+ , Zn 2+ , and M III is Al 3+ , Cr 3+ , Ga 3+ , Fe 3+ ; A II− is an organic ion and / or an inorganic ion. See, for example, Rivers, V .; , Editor. Layered Double Hydroxides: Present and Future, Nova Science Publishers, Inc. , New York, 2001; Monzon et al., Chapter II of what is entitled "Hydrogenation Catalysts with Mixed Oxides Prepared from LDH"; Valente et al.
本発明のさらに別の実施形態は、空気、分子状酸素、分子状水素又は水のような液体の添加を除外して、任意の乾燥及び/又は破砕以外は未処理である粒子状の又は細かく分けた固体状態のバイオマス物質から熱分解生成物を生じるように適合させた触媒組成物を調製する方法である。触媒組成物を調製する方法は、
(A)個々に見て又は集合的に見て、溶解された選択された金属の対、同一であっても異なっていてもよい、蒸発可能な溶媒、好ましくは水であるそのような溶液の溶媒を提供する1以上の溶液(通常、1つの溶液又は2つの別々の溶液)を製造すること又は提供すること(前記1以上の溶液の金属の中身は、CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYから成る群から選択される溶解された金属の対である)と、
(B)上記(A)の1以上の前記溶液を用いた初期湿りによって(予備焼成された)粉状の又は粒子状のハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含浸させて湿り混合物を形成し、得られた湿り混合物を乾燥させて生成物混合物を形成し、次いで遊離の酸素(たとえば、空気又は酸素と窒素、ネオン、アルゴン若しくはクリプトンから選択される少なくとも1つの不活性気体の混合物)の存在下で生成物混合物を焼成することとを含む。乾燥させた混合物のこの焼成は、上記(A)の前記1以上の溶液の溶解された金属の対の一方又は双方に相当する遊離の金属の任意での共存在と共に、金属の選択された対の塩をそのような金属の酸化物に変換する。
上記(A)におけるような個々の触媒前駆体を調製する上記方法のそれぞれは、本発明の個々の実施形態を構成する。空気、分子状酸素、分子状水素又は水のような液体の添加を除外することに関連して、偶発的な量の空気、分子状酸素、分子状水素又は水のような液体が、たとえば、バイオマス物質に由来して存在し得ることが理解される。
Yet another embodiment of the present invention excludes the addition of liquids such as air, molecular oxygen, molecular hydrogen or water, and is particulate or fine that is untreated except for any drying and / or crushing. A method of preparing a catalyst composition adapted to produce a pyrolysis product from a separated solid state biomass material. The method of preparing the catalyst composition includes:
(A) a pair of selected metals dissolved, viewed individually or collectively, of such a solution, which may be the same or different, an evaporable solvent, preferably water Producing or providing one or more solutions that provide a solvent (usually one solution or two separate solutions) (the metal contents of the one or more solutions are Ca and Ce, Ca and Cu, Ca And Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, Ni and Y Selected molten metal pair), and
(B) Powdered or particulate hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anion by initial wetting using one or more of the solutions of (A) above Impregnated with a clay, or a mixture of two or more thereof to form a wet mixture, the resulting wet mixture is dried to form a product mixture, and then free oxygen (eg, air or oxygen and nitrogen, neon) Calcining the product mixture in the presence of a mixture of at least one inert gas selected from argon or krypton). This calcination of the dried mixture is performed with the optional pair of metals together with the optional co-existence of free metal corresponding to one or both of the dissolved metal pairs of the one or more solutions of (A) above. Is converted to such a metal oxide.
Each of the above methods for preparing individual catalyst precursors as in (A) above constitutes an individual embodiment of the present invention. In connection with excluding the addition of liquids such as air, molecular oxygen, molecular hydrogen or water, accidental quantities of liquids such as air, molecular oxygen, molecular hydrogen or water are, for example, It is understood that it can be derived from biomass material.
本発明のさらなる実施形態は固体状態のバイオマス物質を少なくとも以下に変換する方法である。 A further embodiment of the invention is a method for converting solid state biomass material to at least:
(AA)1以上の流体炭化水素生成物、方法は、任意の乾燥及び/又は破砕以外は未処理である粒子状の又は細かく分けた固体状態のバイオマス物質を、迅速な又は瞬時の操作条件下で約500℃を超える温度で操作する反応器に導入することを含み、前記反応器は、(1)反応器に最初に導入される際、
(A)個々に見て又は集合的に見て、金属の溶解された選択された対と、同一であっても異なっていてもよい蒸発可能な溶媒、好ましくは水であるそのような溶液の溶媒を提供する1以上の溶液(通常、1つの溶液又は2つの別々の溶液)を製造すること又は提供すること(前記1以上の溶液の金属の中身は、CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYから成る群から選択される溶解された金属の対である)と、
(B)上記(A)の1以上の前記溶液を用いた初期湿りによって(予備焼成された)粉状の又は粒子状のハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含浸させて湿り混合物を形成し、湿り混合物を乾燥させて生成物混合物を形成し、次いで遊離の酸素(たとえば、空気又は酸素と窒素、ネオン、アルゴン若しくはクリプトンから選択される少なくとも1つの不活性気体の混合物)の存在下で生成物混合物を焼成することとを含む方法によって形成される触媒である焼成された熱分解触媒と
(2)固体状態の粒子状熱媒との流体化混合物を含有し、
その際、熱分解は、空気の添加、分子状酸素の添加、分子状水素の添加、及び/又は水のような液体の希釈剤若しくは担体の添加を除外して実施される。それによって流体の熱分解生成物が形成される。
(AA) One or more fluid hydrocarbon products, methods, can be used to process a particulate or finely divided solid state biomass material that is untreated except for any drying and / or crushing, under rapid or instantaneous operating conditions. In a reactor operating at a temperature above about 500 ° C., said reactor being (1) when first introduced into the reactor,
(A) of a solution, such as water, preferably an evaporable solvent, preferably water, which may be the same as or different from the selected pair of metals, either individually or collectively. Producing or providing one or more solutions that provide a solvent (usually one solution or two separate solutions) (the metal contents of the one or more solutions are Ca and Ce, Ca and Cu, Ca And Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, Ni and Y Selected molten metal pair), and
(B) Powdered or particulate hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anion by initial wetting using one or more of the solutions of (A) above An impregnated clay, or a mixture of two or more thereof to form a wet mixture, the wet mixture is dried to form a product mixture, and then free oxygen (eg, air or oxygen and nitrogen, neon, argon or Calcined pyrolysis catalyst which is a catalyst formed by a process comprising calcining a product mixture in the presence of a mixture of at least one inert gas selected from krypton) and (2) solid state particles Containing a fluidized mixture with a heating medium,
In doing so, the pyrolysis is carried out excluding the addition of air, the addition of molecular oxygen, the addition of molecular hydrogen and / or the addition of a liquid diluent or carrier such as water. Thereby, a pyrolysis product of the fluid is formed.
(AB)金属の前記対が、CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、FeとY、MoとZn、及びMnとYから選択される(AA)の方法。 (AB) The metal pair is selected from Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Fe and Y, Mo and Zn, and Mn and Y ( Method AA).
(AC)金属の前記対が、CaとCu及びCaとFeから選択される(AB)の方法。 (AC) The method of (AB), wherein the pair of metals is selected from Ca and Cu and Ca and Fe.
(AD)前記予備焼成したハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物の含有金属がマグネシウム及びアルミニウムである(AA)、(AB)又は(AC)のいずれかの方法。 (AD) The pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof is magnesium and aluminum (AA), (AB) ) Or (AC).
(AE)前記迅速な又は瞬時の操作条件が実質的に常圧で500℃を超えて約650℃迄の温度を含み、バイオマス物質が、不活性の無水担体ガス、好ましくは、窒素、アルゴン、ネオン又はクリプトン又はその2以上の混合物と共に熱分解反応器に装填され、前記固体状態の粒子状熱媒が砂であり、反応器に装填されるような前記焼成熱分解触媒の平均粒度が、約40〜約400ミクロンの範囲、好ましくは約50〜約150ミクロンの範囲であり、熱分解反応器に装填されるような前記焼成熱分解触媒が再水和によって活性化されており、熱分解反応器内での平均滞留時間が、30秒以下、好ましくは20秒以下、さらに好ましくは10秒以下である(AA)、(AB)又は(AC)のいずれかの方法。 (AE) The rapid or instantaneous operating conditions comprise a temperature substantially above 500 ° C. to about 650 ° C. at atmospheric pressure, and the biomass material is an inert anhydrous carrier gas, preferably nitrogen, argon, The average particle size of the calcined pyrolysis catalyst as loaded into a pyrolysis reactor with neon or krypton or a mixture of two or more thereof, wherein the solid state particulate heating medium is sand and loaded into the reactor is about In the range of 40 to about 400 microns, preferably in the range of about 50 to about 150 microns, and the calcined pyrolysis catalyst as loaded in the pyrolysis reactor has been activated by rehydration, The method of any one of (AA), (AB), or (AC), wherein the average residence time in the vessel is 30 seconds or less, preferably 20 seconds or less, and more preferably 10 seconds or less.
(AF)前記予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物の含有金属がマグネシウム及びアルミニウムであり、前記迅速な又は瞬時の操作条件が実質的に常圧で500℃を超えて約650℃迄の温度を含み、バイオマス物質が、不活性の無水担体ガス、好ましくは、窒素、アルゴン、ネオン又はクリプトン又はその2以上の混合物と共に熱分解反応器に装填され、前記固体状態の粒子状熱媒が砂であり、反応器に装填されるような前記焼成熱分解触媒の平均粒度が、約40〜約400ミクロンの範囲、好ましくは約50〜約150ミクロンの範囲であり、熱分解反応器に装填されるような前記焼成熱分解触媒が再
水和によって活性化されており、熱分解反応器内での平均滞留時間が、30秒以下、好ましくは20秒以下、さらに好ましくは10秒以下である(AA)、(AB)又は(AC)のいずれかの方法。
(AF) The metal contained in the pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof is magnesium and aluminum, The instantaneous operating conditions comprise a temperature substantially above 500 ° C. to about 650 ° C. at atmospheric pressure, and the biomass material is an inert anhydrous carrier gas, preferably nitrogen, argon, neon or krypton or more The solid state particulate heating medium is sand and the average particle size of the calcined pyrolysis catalyst as loaded in the reactor is in the range of about 40 to about 400 microns. The calcined pyrolysis catalyst, preferably in the range of about 50 to about 150 microns, as loaded in the pyrolysis reactor, has been activated by rehydration. The average residence time in the pyrolysis reactor is 30 seconds or less, preferably 20 seconds or less, more preferably not more than 10 seconds (AA), one of the methods of (AB) or (AC).
都合上、金属及び/又は金属塩の対を好適に含浸させ、1以上の好適な高温で焼成されているHTCから構成される触媒は、本明細書では「本発明の二元金属触媒」と呼ばれることがある。用語「本発明の二元金属触媒」は、2つの異なる金属又は異なる金属対が唯一の金属形態であることを意味しないことが理解されるべきである。代わりに、この用語は、本発明の二元金属触媒が、使用されるのに先立って1以上の好適な高温にて、大気中で又は酸素を含有する、たとえば、窒素、アルゴン、ネオン又はクリプトンのような不活性気体中で焼成されるので、反応器に装填される際(すなわち、装填される直前)、金属の対に存在する2つの金属元素があり、それらの一方又は双方が部分的に又は全体的に1以上の酸化物の形態であり得ることを意味する。要するに、対の遊離の金属及び/又はそのような金属の一方又は双方の1以上の酸化物は、本発明の二元金属触媒にて含浸されたコーティングとして存在することができる。 For convenience, a catalyst composed of HTC that is preferably impregnated with a pair of metals and / or metal salts and calcined at one or more suitable high temperatures is referred to herein as a “bimetallic catalyst of the invention”. Sometimes called. It should be understood that the term “bimetallic catalyst of the present invention” does not mean that two different metals or different metal pairs are the only metal form. Instead, this term refers to the bimetallic catalyst of the present invention containing one or more suitable elevated temperatures in the atmosphere or oxygen prior to use, such as nitrogen, argon, neon or krypton. Is fired in an inert gas such as when there are two metal elements present in a metal pair when loaded into the reactor (ie, just prior to loading), one or both of which are partially Meaning that it may be in the form of one or more oxides in whole or in total. In short, the free metal of the pair and / or one or more oxides of one or both of such metals can be present as a coating impregnated with the bimetallic catalyst of the present invention.
上述の実施形態のそれぞれでは、本発明の二元金属触媒の平均粒度は、望ましくは約40〜約400ミクロンの範囲に入り、好ましくは約50〜約150ミクロンの範囲に入る。 In each of the above embodiments, the average particle size of the bimetallic catalyst of the present invention desirably falls in the range of about 40 to about 400 microns, preferably in the range of about 50 to about 150 microns.
本発明の二元金属触媒を形成するのに使用される焼成温度は変化することができる。通常、好適な焼成温度は約550℃〜約800℃の範囲である。好ましい温度は約575℃〜約700℃の範囲である。約575℃〜約625℃の範囲、たとえば、600℃の温度がさらに好ましい。 The calcination temperature used to form the bimetallic catalyst of the present invention can vary. Usually, a suitable firing temperature is in the range of about 550 ° C to about 800 ° C. A preferred temperature is in the range of about 575 ° C to about 700 ° C. More preferred is a temperature in the range of about 575 ° C to about 625 ° C, for example 600 ° C.
上記の焼成温度は、本発明の二元金属触媒を形成するのに使用されるハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を予備焼成するのに使用することにも好適である。 The above calcination temperature is obtained by using hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof used to form the bimetallic catalyst of the present invention. It is also suitable for use in pre-baking.
上記及び他の特徴、実施形態及び/又は利点は、以下の説明、添付のクレーム及び添付の図面からさらに明らかになるであろう。 These and other features, embodiments and / or advantages will become more apparent from the following description, the appended claims and the accompanying drawings.
発明の詳細な説明
本発明は、とりわけ、固体状態のバイオマス物質(たとえば、リグノセルロース系バイオマス又は他のバイオマス物質、特に陸上の供給源に由来し、熱分解で実質的な量の炭化水素を提供する潜在性を有するもの)を単一の反応工程にて炭化水素及び少なくとも1つの、好ましくは1を超える炭化水素前駆体(すなわち、一酸化炭素、二酸化炭素及び/又は水)が豊富な生成物に変換する固体状態のバイオマスの変換の方法を提供する。これに
は、本発明の触媒を用いた1以上に好適な高い反応温度にて、空気の添加、分子状酸素の添加、分子状水素の添加、分子オゾンの添加及び水のような液体の添加を除外した好適な固体状態のバイオマス物質の熱分解、特に迅速熱分解を行うことが伴う。
DETAILED DESCRIPTION OF THE INVENTION The present invention provides, inter alia, solid state biomass material (eg, lignocellulosic biomass or other biomass material, particularly from terrestrial sources, and provides a substantial amount of hydrocarbons upon pyrolysis. Products rich in hydrocarbons and at least one, preferably more than one hydrocarbon precursor (ie, carbon monoxide, carbon dioxide and / or water) in a single reaction step. A method of converting solid state biomass to be converted to is provided. This includes the addition of air, the addition of molecular oxygen, the addition of molecular hydrogen, the addition of molecular ozone and the addition of liquids such as water at a high reaction temperature suitable for one or more using the catalyst of the present invention. Is accompanied by the pyrolysis of a suitable solid state biomass material, especially rapid pyrolysis.
種々の種類、大きさ及び水分含量の広範囲のバイオマス原料を本発明の実践で利用することができる。固体状態のバイオマス物質原料には、成長の早い材木(たとえば、ヤナギ及びポプラ)、材木収穫残材又は林業廃棄物、針葉樹チップ、広葉樹チップ、樹木の枝、樹木の切り株、葉、樹皮、オガクズ、規格外紙パルプ、農業廃棄物、トウモロコシ、トウモロコシ茎葉、小麦藁、米藁、サトウキビ絞りかす、スイッチグラス、都市ゴミ、商業廃棄物、ブドウ絞りかす、アーモンドの殻、ピーカンの殻、ココナッツの殻、コーヒー絞りかす、草ペレット、干し草ペレット、材木ペレット、段ボール及び紙から選択される1以上の物質を挙げることができる。セルロース性バイオマス物質も同様に使用され得る。しかしながら、そのような物質は熱分解の間に粘着性の残留物を形成する傾向があることが分かっている。従って、セルロース性バイオマス物質を使用する場合、熱分解反応器及び攪拌機のような関連する器具の慎重な温度制御及び頻繁な清掃等が推奨される。一般に言えば、リグノセルロース系バイオマス物質及び実質的な量の炭化水素を熱分解で提供することが可能である類似の物質が使用には好まれる。そのような物質は所望のようにバッチ、半バッチ又は連続で処理され得る。 A wide range of biomass feedstocks of various types, sizes and moisture contents can be utilized in the practice of the present invention. Solid biomass materials include fast-growing timber (eg, willows and poplars), timber harvest residue or forestry waste, coniferous chips, hardwood chips, tree branches, tree stumps, leaves, bark, sawdust, Nonstandard paper pulp, agricultural waste, corn, corn stover, wheat straw, rice bran, sugarcane pomace, switchgrass, municipal waste, commercial waste, grape pomace, almond shell, pecan shell, coconut shell, Mention may be made of one or more substances selected from coffee grounds, grass pellets, hay pellets, timber pellets, cardboard and paper. Cellulosic biomass materials can be used as well. However, it has been found that such materials tend to form sticky residues during pyrolysis. Therefore, when using cellulosic biomass materials, careful temperature control and frequent cleaning of related equipment such as pyrolysis reactors and agitators are recommended. Generally speaking, lignocellulosic biomass materials and similar materials that are capable of providing substantial amounts of hydrocarbons by pyrolysis are preferred for use. Such materials can be processed in batches, semi-batches or continuously as desired.
代わりの実施形態では、陸上植物によってセルロース系バイオマス物質が形成される。陸上植物は実際上例外なく、一般にリグノセルロース系バイオマスと呼ばれるリグニンとセルロースの組み合わせを形成する。本発明の工程での使用に食用作物を使用することができるが、エネルギー作物物質、農業廃棄物又は林業廃棄物を使用することが経済的に及び倫理的に言及される。好適なエネルギー作物物質の例には、スイッチグラス及びたとえば、ヤナギやポプラのような成長の早い材木が挙げられる。 In an alternative embodiment, cellulosic biomass material is formed by land plants. Terrestrial plants have practically no exception, and form a combination of lignin and cellulose, commonly called lignocellulosic biomass. Although food crops can be used for use in the process of the present invention, it is economically and ethically mentioned to use energy crop material, agricultural waste or forestry waste. Examples of suitable energy crop materials include switchgrass and fast growing timber such as willow and poplar.
本発明に従って選択された固体状態のバイオマス物質の任意の予備処理は2種類の予備処理に限定される。そのような予備処理の1つは熱分解での使用に先立ってバイオマス物質を予備乾燥させることである。これには、熱の適用、好適な長さの時間好適な温度のもとでの保存、吹き付け乾燥又は他の類似の風乾法等の使用が伴い得る。他の予備処理は、熱分解での使用の前にバイオマス物質の大きさを縮小することである。これには通常、たとえば、製粉、すりつぶすこと、混錬、切り刻むこと、のこぎりで切ること、又は破砕の他の物理的な方法、又はそれらの組み合わせのような好適な機械的処理が関与する。 The optional pretreatment of the solid state biomass material selected according to the present invention is limited to two types of pretreatment. One such pretreatment is to predry the biomass material prior to use in pyrolysis. This may involve the use of heat application, a suitable length of time, storage at a suitable temperature, spray drying or other similar air drying methods. Another pretreatment is to reduce the size of the biomass material prior to use in pyrolysis. This usually involves suitable mechanical processing such as milling, grinding, kneading, chopping, sawing, or other physical methods of crushing, or combinations thereof.
上記で言及したように、熱分解を達成するのに使用される本発明の触媒は、1以上の粉状又は粒子状のHTCであり、それは、熱分解容器に導入する際、特定の金属の対及び/又は金属の対の一方又は双方の1以上の酸化物のコーティングを運ぶ、又それでドープされる。 As mentioned above, the catalyst of the present invention used to achieve pyrolysis is one or more powdered or particulate HTCs, which, when introduced into the pyrolysis vessel, are made of certain metals. It carries and is doped with one or more oxide coatings of one or both of the pairs and / or metal pairs.
選択された好適な固体状態のバイオマス物質と共に本発明に従って使用される触媒系の主要な機能は、特定の選択された方向に熱分解脱酸素を触媒的に集中させ、指図し、又は誘導し、それによって熱分処理にて又は処理にて形成される流体生成物(気体及び液体)の質にて、又は双方にて有利な結果が得られることである。 The primary function of the catalyst system used in accordance with the present invention with selected suitable solid state biomass material is to catalytically concentrate, direct or induce pyrolytic deoxygenation in a particular selected direction, Thereby, advantageous results are obtained in the heat treatment or in the quality of the fluid products (gas and liquid) formed in the treatment or both.
本発明の熱分解法のすべてにおいて、本発明の二元金属触媒のすべてにおいて及び本発明の二元金属触媒を調製する方法すべてにおいて、予備焼成されたHTCに含浸させる又はドープさせるのに使用される追加の金属成分の好ましい対は、以下の9の個々の金属対:CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、FeとY、MoとZn、及びMnとYの水溶性化合物(たとえば、塩、酸化物又は水酸化物)である。本発明のこれらの二元金属触媒は、所望の対合した金属の追加成分(通常、塩)によ
る基質への含浸によって形成されるだけではなく、含浸された基質はその後焼成されて金属及び/又は金属酸化物の触媒表面を形成するが、基質は、
(a)二価の金属化合物と三価の金属化合物の物理的混合物を製粉する又はさもなければ破砕する工程と、
(b)200〜800℃の範囲の温度にて、製粉された又はさもなければ破砕された物理的混合物を焼成する工程と、
(c)焼成された混合物を水性懸濁液にて再水和する工程とを含む方法によって形成されている予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物であり、その際、追加の対は物理的混合物及び/又は工程(c)の水性懸濁液に存在する。
非常に小さな粒子形態での触媒組成物を活性化するのに役立つが、本発明の特定の追加の組み合わせを使用しないこの方法は、2008年2月7日に公開されたJoneらの米国公開特許出願番号US2008/0032884にて記載されている。都合上、工程(a)、(b)及び(c)が関与するこの方法は以後「触媒活性化法」と呼ばれることがある。この方法では、用語「物理的混合物」は、どの化合物も焼成の前に互いに有意な程度には反応しない乾燥状態又は水性状態での(a)の化合物の混合物を指す。従って、物理的混合物は時を経て、焼成前に予備焼成されるハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を形成することはない。
Used in all of the pyrolysis processes of the present invention, in all of the bimetallic catalysts of the present invention and in all of the processes of preparing the bimetallic catalysts of the present invention, to impregnate or dope the pre-fired HTC. Preferred pairs of additional metal components are the following nine individual metal pairs: Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Fe and Y, Mo and Zn , And water-soluble compounds of Mn and Y (for example, salts, oxides or hydroxides). These bimetallic catalysts of the present invention are not only formed by impregnation of the substrate with an additional component (usually a salt) of the desired paired metal, but the impregnated substrate is then calcined to produce the metal and / or Or form a metal oxide catalyst surface, but the substrate is
(A) milling or otherwise crushing a physical mixture of a divalent metal compound and a trivalent metal compound;
(B) firing the milled or otherwise crushed physical mixture at a temperature in the range of 200-800 ° C;
(C) pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anion formed by a method comprising rehydrating the calcined mixture with an aqueous suspension Clay, or a mixture of two or more thereof, wherein an additional pair is present in the physical mixture and / or the aqueous suspension of step (c).
This method, useful for activating catalyst compositions in very small particle form, but without the use of certain additional combinations of the present invention, is disclosed in the US published patent of Jone et al., Published Feb. 7, 2008. Application No. US2008 / 0032884. For convenience, this process involving steps (a), (b) and (c) may be referred to hereinafter as the “catalyst activation process”. In this method, the term “physical mixture” refers to a mixture of compounds of (a) in a dry or aqueous state in which none of the compounds react with each other to a significant extent prior to calcination. Thus, the physical mixture may, over time, form a hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof that is pre-fired before firing. Absent.
従って、直前の段落で言及された9つの金属対のいずれかを有する二元金属触媒は望ましい金属及び/又は金属酸化物が含浸された表面を有し、好ましくは、直前の段落で記載された触媒活性化法に従って再水和によって活性化もされている。さらに好ましくは、これらの予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物の金属の中身はマグネシウム及びアルミニウムである。 Thus, a bimetallic catalyst having any of the nine metal pairs mentioned in the immediately preceding paragraph has a surface impregnated with the desired metal and / or metal oxide, preferably as described in the immediately preceding paragraph. It is also activated by rehydration according to the catalyst activation method. More preferably, the metal contents of these pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof are magnesium and aluminum.
触媒調製の手順の説明
本発明の二元金属触媒を調製する好適な手順を説明するために、3つの異なる触媒調製方法を採用した。そのような方法の2つにはロボット器具を用いたロボットプレート含浸が関与した。
Description of Catalyst Preparation Procedures To illustrate the preferred procedure for preparing the bimetallic catalyst of the present invention, three different catalyst preparation methods were employed. Two such methods involved robotic plate impregnation using robotic instruments.
第1のそのような方法(以後、触媒調製方法Aと呼ぶことがある)では、Mg/Al/HTC粉末(125〜400ミクロン)をプレート上に堆積させた。バイアル中の必要とされる量の含浸溶液を合計49液滴の小液滴の形態で支持触媒(HTC)の表面すべてにわたって広げる。次いで触媒を含浸溶液と共に30分間の間、静置した。湿潤粉体をよく混合し、次いで、1分当たり5℃の温度傾斜で90分間の間、600℃で空気中にて焼成した。この操作で使用した含浸溶液は、二元金属の中身による含浸に使用される溶液における金属酸化物前駆体としての2つの金属を用いた金属硝酸塩だった。 In the first such method (hereinafter sometimes referred to as Catalyst Preparation Method A), Mg / Al / HTC powder (125-400 microns) was deposited on the plate. The required amount of impregnation solution in the vial is spread across the surface of the supported catalyst (HTC) in the form of a total of 49 droplets. The catalyst was then left with the impregnation solution for 30 minutes. The wet powder was mixed well and then calcined in air at 600 ° C. for 90 minutes with a temperature ramp of 5 ° C. per minute. The impregnation solution used in this operation was a metal nitrate using two metals as metal oxide precursors in the solution used for impregnation with the contents of the binary metal.
第2の方法(以後、触媒調製方法Bと呼ぶことがある)には、この目的で製造された市販の器具を用いたロボット振盪含浸が関与した。この方法では、1.6gのHTCを試験管に入れた。HTCの孔容量を用いて算出された量の水と共に、必要とされる量の、2つの金属前駆体及び/又は金属酸化物前駆体の1つを加えた。回転/振動モードにてロボット器具を用いて、初期の湿り法に従って含浸を開始した。得られた生成物を試験管の中で120℃にて1時間乾燥させた。第2の金属及び/又は金属酸化物前駆体を用いてこの手順を繰り返した。乾燥の後、次いで乾燥させた生成物を1分当たり5℃の温度傾斜で90分間の間、600℃で焼成した。 The second method (hereinafter sometimes referred to as Catalyst Preparation Method B) involved robotic shaking impregnation using a commercial instrument manufactured for this purpose. In this method, 1.6 g of HTC was placed in a test tube. The required amount of one of the two metal precursors and / or metal oxide precursors was added along with the amount of water calculated using the pore volume of the HTC. Impregnation was started according to the initial wetting method using a robotic instrument in rotation / vibration mode. The resulting product was dried in a test tube at 120 ° C. for 1 hour. This procedure was repeated using a second metal and / or metal oxide precursor. After drying, the dried product was then calcined at 600 ° C. for 90 minutes with a temperature ramp of 5 ° C. per minute.
さらに大きな実験室レベルの触媒の調製については、以下の第3の方法(以後、方法C
又は「実験室レベルの方法」と呼ぶことがある)を含浸及び触媒の形成に使用した。各調製は約60gの触媒を提供した。約120gの篩過したHTCをさらに大きなフラスコに入れた。含浸溶液は、必要とされる量の第1の金属及び/又は金属酸化物の前駆体をHTCの孔容量から算出された最少量の水と混合することによって形成し、その後、湿潤混合物の振盪を含む含浸溶液による初期の湿りが続き、その後、100℃での5時間の乾燥が続いた。2つの金属及び/又は金属酸化物の前駆体の混合物を調製するために、第2の前駆体による含浸についてこの方法を繰り返した。第2の乾燥が終わった後、600℃で焼成を行った。前に言及したように、特に追加の対が、CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、FeとY、MoとZn、及びMnとYから選択される場合、予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を形成することにおいて上述の触媒活性化法が好ましくは使用される。触媒活性化法を使用する別の利点は、その中で使用される製粉工程又は他の破砕工程が通常40〜400ミクロンの範囲、好ましくは50〜150ミクロンの範囲での望ましく小さな粒度を持つ触媒を提供することである。一層さらに大きな触媒の調製については、従来の大型の含浸及び/又はドープ触媒の調製手順が当該技術で既知であり、採用することができる。
For the preparation of larger laboratory level catalysts, the following third method (hereinafter Method C) is used.
(Sometimes referred to as “laboratory method”) was used for impregnation and catalyst formation. Each preparation provided about 60 g of catalyst. About 120 g of sieved HTC was placed in a larger flask. The impregnation solution is formed by mixing the required amount of the first metal and / or metal oxide precursor with the minimum amount of water calculated from the pore volume of the HTC and then shaking the wet mixture. Followed by an initial wetting with an impregnating solution containing, followed by drying at 100 ° C. for 5 hours. This process was repeated for impregnation with a second precursor to prepare a mixture of two metal and / or metal oxide precursors. After the second drying, baking was performed at 600 ° C. As mentioned before, especially additional pairs are from Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Fe and Y, Mo and Zn, and Mn and Y. If selected, the catalyst activation method described above is preferred in forming a pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof. Is used. Another advantage of using a catalyst activation method is that the milling or other crushing process used therein is a catalyst with a desirably small particle size, usually in the range of 40-400 microns, preferably in the range of 50-150 microns. Is to provide. For the preparation of even larger catalysts, conventional large impregnation and / or dope catalyst preparation procedures are known in the art and can be employed.
触媒試験手順
図1に示す結果は、3gの粒子状の未処理のリグノセルロース系バイオマスを窒素気体の流れと共に、迅速熱分解流動床反応器(図3を参照)の最上部に導入するバイオマス脱酸素実験の使用によって得られた。流動床は、25重量%の本発明の二元金属触媒と75%の砂の重量比にて触媒(12g)と砂(36g)の混合物で構成された。流動床の温度は実質的に常圧にて約515℃に維持された。平均滞留時間は30秒未満だった。
Catalyst Testing Procedure The results shown in FIG. 1 show that the biomass desorption of 3 g of particulate untreated lignocellulosic biomass with nitrogen gas flow at the top of a rapid pyrolysis fluidized bed reactor (see FIG. 3). Obtained by use of oxygen experiments. The fluidized bed consisted of a mixture of catalyst (12 g) and sand (36 g) in a weight ratio of 25 wt% bimetallic catalyst of the present invention and 75% sand. The fluidized bed temperature was maintained at about 515 ° C. at substantially normal pressure. The average residence time was less than 30 seconds.
図2に示す結果は、以下:リグノセルロース系バイオマス(10mg)と、触媒調製方法Bによって調製されたCa/Nb/HTC触媒以外の、報告された触媒すべてについて触媒調製方法Aを用いて調製された10mgの二元金属触媒、のように行ったバイオマス脱酸素実験の使用によって得られた。各触媒を調製して金属の目標の1:1重量比を提供した。バイオマスと触媒の重量比は1:1(各10mg)だった。80mL/分の流速ですべて窒素(N2)中にて熱重量分析(TGA)カップ内でこれらの混合物を迅速に500℃に加熱した。120℃で辿った配管を介して、形成された熱分解蒸気をフーリエ変換赤外分光セル(FTIR)(容量15mL、150℃に加熱したKBrウインドウ付き)に通し、その後、FTIRスペクトルを記録した:1スペクトル/2秒間隔(0.5cm-1の分解能で5走査から成る)。報告されたスペクトルはすべてバイオマス含量について補正された。バイオマスの量に対して基準化した後、一酸化炭素におけるC=O振動に特異的な範囲2244〜2142cm-1で、二酸化炭素におけるC=O振動に特異的な2392〜2258cm-1の範囲で、及び形成された水分子におけるO−H振動に特異的な3856〜3853cm-1の範囲で特定の振動について積分ピーク面積を比較した。
The results shown in FIG. 2 are prepared using Catalyst Preparation Method A for all reported catalysts except for the following: lignocellulosic biomass (10 mg) and Ca / Nb / HTC catalyst prepared by Catalyst Preparation Method B. Obtained by use of biomass deoxygenation experiments conducted as in 10 mg of bimetallic catalyst. Each catalyst was prepared to provide a 1: 1 weight ratio of the metal target. The weight ratio of biomass to catalyst was 1: 1 (10 mg each). These mixtures were rapidly heated to 500 ° C. in a thermogravimetric analysis (TGA) cup in nitrogen (N 2 ) all at a flow rate of 80 mL / min. Through the piping traced at 120 ° C., the formed pyrolysis vapor was passed through a Fourier transform infrared spectroscopic cell (FTIR) (
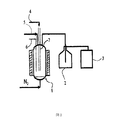
図3では、好ましい半断熱流動床の性能試験装置の断面の側面図を示す。装置は、反応器1、生成物リザーバ2及び気体バッグ3を含む。反応器1はバイオマス供給ライン4、熱媒供給ライン5、熱電温度計6、ディプレグ7及び窒素気体(N2)流入口を有する。
FIG. 3 shows a cross-sectional side view of a preferred semi-insulated fluidized bed performance test apparatus. The apparatus includes a reactor 1, a
熱分解気体はガスクロマトグラフィ法によって分析し、CO及びCO2の収率は供給量(湿量基準)に対する重量%として定量する。液体(熱分解油)はテトラヒドロフラン(THF)による希釈によって均質化する。均質化した液体を水含量及び酸性度について分析する。熱分解油にて見いだされた水の総収率(THF希釈について補正された)は標準のKarl−Fischerの滴定によって決定し、供給量(湿量基準)に対する重量%として報告する。酸性度は、滴定曲線の同等な時点での液体生成物のグラム当たりのmgKOHとして報告される。 The pyrolysis gas is analyzed by gas chromatography, and the yields of CO and CO 2 are quantified as% by weight with respect to the feed rate (wet basis). The liquid (pyrolytic oil) is homogenized by dilution with tetrahydrofuran (THF). The homogenized liquid is analyzed for water content and acidity. The total yield of water found in the pyrolysis oil (corrected for THF dilution) is determined by standard Karl-Fischer titration and reported as weight percent relative to feed (wet basis). Acidity is reported as mg KOH per gram of liquid product at equivalent time points in the titration curve.
そのような熱分解実験によって達成される酸素除去(バイオマス供給量からの)は以下の方法で表現される:
O除去は、除去された酸素の重量%である(供給量における酸素を基にした重量%)
MO:Oのモル質量=15.999(g/モル)
XCO:COの収率(供給量に対する重量%)
MCO:COのモル質量=28.01(g/モル)
XCO2:CO2収率(供給量に対する重量%)
MCO2:CO2のモル質量=44.01(g/モル)
XH2O:H2Oの収率(供給量に対する重量%)
MH2O:H2Oのモル質量=18.02(g/モル)
O供給:49重量%がリグノセルロース系の供給量である供給されたバイオマスにおける酸素含量(重量%)
Oxygen removal (from biomass feed) achieved by such pyrolysis experiments is expressed in the following way:
O removal is the weight percent of oxygen removed (weight percent based on oxygen in the feed rate).
M O : Molar mass of O = 15.999 (g / mol)
X CO : CO yield (% by weight with respect to the supply amount)
M CO : molar mass of CO = 28.01 (g / mol)
X CO2 : CO 2 yield (% by weight with respect to the supply amount)
M CO2 : Mole mass of CO 2 = 44.01 (g / mol)
X H2O: H 2 O yield (wt% with respect to the supply amount)
M H2O : Molar mass of H 2 O = 18.02 (g / mol)
O supply : Oxygen content (wt%) in supplied biomass where 49 wt% is the lignocellulosic supply
以下の実施例は、本発明の種々の個々の実施形態を説明する。これらの実施例は、これらの実施例にて記載される実施形態にのみ本発明を限定するようには意図されない。これらの実施例では、用語HTCは2つの水酸化物の金属がMg及びAlであるハイドロタルサイト又はハイドロタルサイト様の化合物を指す。そのようなHTCは、1又は2の工程にて2つの異なる追加の金属化合物を含浸させられており、その後、使用される調製方法に応じて1又は2回焼成される。使用される含浸化合物の金属の例としてCa及びCuを用いて、追加の金属化合物のこの対によるHTCの含浸に由来する最終的な焼成生成物は、実際の化学構造が通常、たぶん若干の遊離金属を伴って酸化物を含むにもかかわらず、Ca/Cu/HTCと呼ばれる。あらゆる場合において、触媒合成は1:1の重量比で金属を提供することを目標とする各量にて含浸化合物を使用した。 The following examples illustrate various individual embodiments of the present invention. These examples are not intended to limit the invention to only the embodiments described in these examples. In these examples, the term HTC refers to a hydrotalcite or hydrotalcite-like compound in which the two hydroxide metals are Mg and Al. Such HTCs are impregnated with two different additional metal compounds in one or two steps and then calcined once or twice depending on the preparation method used. Using Ca and Cu as examples of impregnating compound metals used, the final calcined product derived from impregnation of HTC with this pair of additional metal compounds will usually have a slight chemical structure. It is called Ca / Cu / HTC despite containing oxide with metal. In all cases, the catalyst synthesis used impregnated compounds in each amount targeted to provide the metal in a 1: 1 weight ratio.
実施例1〜7
触媒調の方法Cを用い、Mg/Al/HTCと2つの異なる水溶性金属塩の水溶液を用いて、本発明の二元金属触媒を製造する量にて本発明の7つの異なる二元金属触媒を調製した。使用したHTCは550℃で1時間あらかじめ焼成し、デシケータにて保持して湿気及びCO2との相互作用を回避していた。含浸は、追加の金属の選択された対の硝酸塩、アンモニウム塩及び/又はシュウ酸塩と共に周知の初期湿り法を用いて実施した。空気中、又は上記で言及した遊離の酸素を含有する不活性気体中における600℃での焼成の間、遊離金属の一方又は双方の一部の存在を完全に除外することはできないが、金属塩は金属酸化物に転換される。含浸された又はドープされたHTCを焼成し、水和によって活性化した後、湿気及びCO2のような気体との相互作用を回避するようにデシケータのような不活性条件下でそれを保持した。次いで図3にて模式的に描いた実験室レベルの熱分解装置で7つの焼成した触媒を個々に性能について評価した。個々の熱分解の実行のすべてにおいて、室温での3gのバイオマスを515℃に予備加熱した触媒流動床の最上部に供給した。流動床は、36gの砂と一緒に12gの本発明の二元金属触媒で構成された。3バールの窒素パージ用いて、供給ディプレグを介した流動床への固体供給物の導入を達成した。30秒未満の迅速熱分解の滞留時間の後、窒素で流動床を洗い流した。操作の間、液体生成物を濃縮し、冷却トラップを装備した生成物リザーバに回収した。熱分解気体及び窒素は気体バッグにて回収した。ガスクロマトグラフィ法を用いて熱分解気体を分析した。液体生成物を酸性度、水の測定及びFTIR又はGC−MSの解析に供した。触媒
を燃焼させることによるコークスについて消費された触媒を分析した。実際に測定されたコークスの量は、触媒におけるコークスと炭化物(変換されないバイオマス)双方の合計を表した。対照として、砂だけを用いて実験を行い、焼成されたHTCのみを用いて別の実験を行った。
Examples 1-7
Seven different bimetallic catalysts of the present invention in an amount to produce the bimetallic catalyst of the present invention using an aqueous solution of Mg / Al / HTC and two different water soluble metal salts using catalyst-like method C Was prepared. The HTC used was pre-fired at 550 ° C. for 1 hour and held in a desiccator to avoid interaction with moisture and CO 2 . The impregnation was carried out using the well-known initial wetting method with selected pairs of nitrates, ammonium salts and / or oxalates of additional metals. During firing at 600 ° C. in air or in an inert gas containing free oxygen as mentioned above, the presence of a part of one or both of the free metals cannot be ruled out completely. Is converted to a metal oxide. After the impregnated or doped HTC was calcined and activated by hydration, it was kept under inert conditions such as a desiccator to avoid interaction with moisture and gases such as CO 2 . The seven calcined catalysts were then individually evaluated for performance in the laboratory-level pyrolysis apparatus depicted schematically in FIG. In all individual pyrolysis runs, 3 g of biomass at room temperature was fed to the top of the catalyst fluidized bed preheated to 515 ° C. The fluidized bed consisted of 12 g of the bimetallic catalyst of the present invention together with 36 g of sand. A 3 bar nitrogen purge was used to achieve introduction of the solid feed into the fluidized bed via the feed prepreg. After a rapid pyrolysis residence time of less than 30 seconds, the fluidized bed was flushed with nitrogen. During operation, the liquid product was concentrated and collected in a product reservoir equipped with a cold trap. Pyrolysis gas and nitrogen were collected in a gas bag. The pyrolysis gas was analyzed using gas chromatography. The liquid product was subjected to acidity, water measurement and FTIR or GC-MS analysis. The spent catalyst was analyzed for coke by burning the catalyst. The actual amount of coke measured represents the sum of both coke and carbide (non-converted biomass) in the catalyst. As a control, an experiment was conducted using only sand, and another experiment was conducted using only calcined HTC.
実施例1〜7に関するさらなる詳細を表1に要約する。触媒における金属の量は誘導結合プラズマ(ICP)法の使用によって決定した。 Further details regarding Examples 1-7 are summarized in Table 1. The amount of metal in the catalyst was determined by using an inductively coupled plasma (ICP) method.
同一条件下で調べた場合、ゼオライトZSM−5が10.2重量%(湿量基準)のCOと8.7重量%(湿量基準)のCO2のCOx(xは普通1又は2である)分布を生じることを言及するのは興味深い。従って、この周知の広範に調べられたゼオライト触媒は多量の毒性一酸化炭素を含有するCOx分布を生じた。際立って対照的に、本発明の実践は
多量の二酸化炭素を含有するCOx分布の形成を可能にする。
When examined under identical conditions, the COx (x of CO 2 zeolite ZSM-5 is 10.2 wt% CO and 8.7% by weight of (wet basis) (wet basis) is usually 1 or 2 It is interesting to mention that it produces a distribution. Therefore, this well-known extensively investigated zeolite catalyst produced a COx distribution containing a large amount of toxic carbon monoxide. In marked contrast, the practice of the present invention allows the formation of COx distributions containing large amounts of carbon dioxide.
実施例8〜11
触媒調製方法A又は触媒調製方法Bを用い、それぞれ、Mg/Al/HTCと2つの異なる水溶性金属塩の水溶液を用いて、本発明の二元金属触媒を製造する量にて本発明の4つの異なる二元金属触媒を調製した。これらの触媒は、Ca/Cu/HTC、Ce/Y/HTC、Cu/Nb/HTC及びNi/Y/HTCだった。触媒を作製するのに使用した追加の金属塩並びに触媒を作製するのに使用した金属対の重量比率及び原子比を表2に示す。次いで4つの焼成された触媒を性能について個々に評価した。これらの操作では、バイオマス脱酸素実験は、以下:リグノセルロース系バイオマス(10mg)と、触媒調製方法Bによって調製されたCa/Nb/HTC触媒を除いて報告された触媒すべてについて触媒調製方法Aを用いて調製された10mgの二元金属触媒、のように行った。金属の目標の1:1重量比を提供するように各触媒を調製した。バイオマスと触媒の重量比は1:1だった。80mL/分の流速ですべて窒素(N2)中にて熱重量分析(TGA)カップ内でこれらの混合物を迅速に500℃に加熱した。120℃で辿った配管を介して、形成された熱分解蒸気をフーリエ変換赤外分光セル(FTIR)(容量15mL、150℃に加熱したKBrウインドウ付き)に通し、その後、FTIRスペクトルを記録した:1スペクトル/2秒間隔(0.5cm-1の分解能で5走査から成る)。報告されたスペクトルはすべてバイオマス含量について補正された。バイオマスの量に対して基準化した後、表2にて示す積分ピーク面積を、形成された水分子におけるO−H振動に特異的な3856〜3853cm-1の範囲での特定の振動について比較した。また、本発明の4つの上記二元金属触媒の金属以外の金属を用いて同様に13の他のバイオマス脱酸素実験を行った。1群では、本発明のCa/Cu/HTC及びCu/Nb/HTCと本発明のではない7つの他の銅二元金属触媒を含む9回の試験を行った。本発明のではない7つの二元金属触媒は、式Cu/M/HTCで表され、式中、Mはカルシウム及びニオビウム以外の7つの異なる金属のそれぞれであり、これら他の金属の1つはアルカリ金属(Li)である。他の群では、本発明のCe/Y/HTC及びNi/Y/HTCを含む8回の試験を同様に行った。この群では、本発明のではない6つの二元金属触媒は式Y/M/HTCによって表され、式中、Mはセシウム及びニッケル以外の6つの異なる金属のそれぞれであり、これら他の金属の1つはアルカリ金属(Li)である。
Examples 8-11
Using catalyst preparation method A or catalyst preparation method B, respectively, an aqueous solution of Mg / Al / HTC and two different water-soluble metal salts is used to produce the bimetallic catalyst of the present invention in an amount of 4 of the present invention. Two different bimetallic catalysts were prepared. These catalysts were Ca / Cu / HTC, Ce / Y / HTC, Cu / Nb / HTC and Ni / Y / HTC. The additional metal salts used to make the catalyst and the weight and atomic ratios of the metal pair used to make the catalyst are shown in Table 2. The four calcined catalysts were then individually evaluated for performance. In these operations, the biomass deoxygenation experiments consisted of the following: catalyst preparation method A for all reported catalysts except for lignocellulosic biomass (10 mg) and the Ca / Nb / HTC catalyst prepared by catalyst preparation method B. As 10 mg of the bimetallic catalyst prepared with. Each catalyst was prepared to provide a 1: 1 weight ratio of the metal target. The weight ratio of biomass to catalyst was 1: 1. These mixtures were rapidly heated to 500 ° C. in a thermogravimetric analysis (TGA) cup in nitrogen (N 2 ) all at a flow rate of 80 mL / min. Through the piping traced at 120 ° C., the formed pyrolysis vapor was passed through a Fourier transform infrared spectroscopic cell (FTIR) (
実施例8〜11に関するさらなる詳細を表2に要約する。 Further details regarding Examples 8-11 are summarized in Table 2.
実施例12〜13
触媒調製方法Aを用い、予備焼成されたMg/Al/HTCと2つの異なる水溶性金属塩の水溶液を用いて、本発明の二元金属触媒を製造する量にて本発明の2つの異なる二元金属触媒を調製した。これらの触媒はCe/Fe/HTC及びCe/Ni/HTCだった。触媒を作製するのに使用した追加の金属塩並びに触媒を作製するのに使用した金属対の重量比率及び原子比を表3に示す。次いで2つの焼成された触媒を性能について個々に評価した。これらの操作では、バイオマス脱酸素実験は、以下:リグノセルロース系バイオマス(10mg)と、双方の触媒について触媒調製方法Aを用いて調製された10mgの二元金属触媒、のように行った。金属の目標の1:1重量比を提供するように各触媒を調製した。バイオマスと触媒の重量比は1:1だった。表3に示す積分ピーク面積を二酸化炭素におけるC=O振動に特異的な2392〜2258cm-1の範囲で特定の振動について比較したことを除いて、これらの混合物を実施例8〜11にて使用され、記載されたのと同じ試験手順に供した。
Examples 12-13
Using catalyst preparation method A, the pre-calcined Mg / Al / HTC and an aqueous solution of two different water-soluble metal salts are used to produce the two different two-metal catalysts of the present invention in an amount to produce the bimetallic catalyst of the present invention. An original metal catalyst was prepared. These catalysts were Ce / Fe / HTC and Ce / Ni / HTC. Table 3 shows the additional metal salts used to make the catalyst and the weight and atomic ratios of the metal pair used to make the catalyst. The two calcined catalysts were then individually evaluated for performance. In these operations, biomass deoxygenation experiments were performed as follows: lignocellulosic biomass (10 mg) and 10 mg bimetallic catalyst prepared using Catalyst Preparation Method A for both catalysts. Each catalyst was prepared to provide a 1: 1 weight ratio of the metal target. The weight ratio of biomass to catalyst was 1: 1. These mixtures were used in Examples 8-11, except that the integrated peak areas shown in Table 3 were compared for specific vibrations in the range of 2392-2258 cm −1 specific for C═O vibrations in carbon dioxide. And subjected to the same test procedure as described.
実施例14〜15
触媒調製の方法Cを用い、予備焼成されたMg/Al/HTCと2つの異なる水溶性金属塩の水溶液を用いて、本発明の二元金属触媒を製造する量にて本発明の2つの異なる二元金属触媒を調製した。使用したHTCは550℃で1時間あらかじめ焼成し、デシケータにて保持して湿気及びCO2との相互作用を回避しておいた。含浸は、追加の金属の選択された対の硝酸塩、アンモニウム塩及び/又はシュウ酸塩と共に周知の初期湿り法を用いて実施した。次いで、実施例1〜7で使用したのと同様の方法で、同様の試験系で及び同様の条件下で、実験室レベルの熱分解装置にて2つの焼成された触媒を性能について個々に評価した。
Examples 14-15
Using the catalyst preparation method C, the two different metal oxides of the present invention are produced in amounts to produce the bimetallic catalyst of the present invention using pre-calcined Mg / Al / HTC and an aqueous solution of two different water soluble metal salts. A bimetallic catalyst was prepared. The HTC used was pre-fired at 550 ° C. for 1 hour and held in a desiccator to avoid interaction with moisture and CO 2 . The impregnation was carried out using the well-known initial wetting method with selected pairs of nitrates, ammonium salts and / or oxalates of additional metals. The two calcined catalysts were then individually evaluated for performance in a laboratory-level pyrolysis apparatus in the same manner as used in Examples 1-7, under similar test systems and under similar conditions. did.
図1〜3を参照して上記で記載された実験で使用されたのと同じバイオマスを使用して515℃での迅速熱分解条件下でこの触媒を利用した。この操作で使用した物質は、空気、分子状酸素、分子状水素及び液体の溶媒又は希釈剤の非存在下でバイオマス試料が供給される伝熱剤としての75重量%の砂と25重量%のFe/Ca/HTC触媒の混合物だった。使用したこれらの物質の量は、36gの砂、12gのFe/Ca/HTC触媒及び3gのバイオマスだった。この迅速熱分解試験手順には以下の操作が関与した。 The catalyst was utilized under rapid pyrolysis conditions at 515 ° C. using the same biomass used in the experiments described above with reference to FIGS. The material used in this operation was 75% by weight sand and 25% by weight sand as a heat transfer agent supplied with biomass samples in the absence of air, molecular oxygen, molecular hydrogen and liquid solvent or diluent. It was a mixture of Fe / Ca / HTC catalyst. The amount of these materials used was 36 g sand, 12 g Fe / Ca / HTC catalyst and 3 g biomass. This rapid pyrolysis test procedure involved the following operations.
表4は、追加の触媒成分なしで同じ量の同じHTCを用いて形成された生成物と比較した上記の迅速熱分解手順で形成された生成物の特徴を要約する。 Table 4 summarizes the characteristics of the product formed with the above rapid pyrolysis procedure compared to the product formed with the same amount of the same HTC without additional catalyst components.
表4から、Fe/Ca/HTC触媒は、無添加のHTC物質と比べてはるかに大きな収率のCO、CO2及び酸素の除去を生じることが言及されるであろう。方法で形成されるバイオオイルの酸性度はFe/Ca/HTC触媒を用いた場合、有意に低いことも分かるであろう。 From Table 4 it will be noted that the Fe / Ca / HTC catalyst results in a much greater yield of CO, CO 2 and oxygen removal compared to the unadded HTC material. It will also be seen that the bio-oil formed by the process has a significantly lower acidity when using Fe / Ca / HTC catalyst.
本発明の追加の実施形態には以下が挙げられる。 Additional embodiments of the present invention include:
(BA)固体状態のバイオマス物質から1以上の流体炭化水素生成物を製造する方法で
あって、前記方法は、
(I)熱分解反応器にて撹拌のもとで
(A)任意の乾燥及び/又は破砕を除いて未処理である粒子状の又は細かく分けた固体状態のバイオマス物質;
(B)反応器に装填される際、(1)単一対の金属、(2)単一対の前記金属それぞれの少なくとも1つの酸化物又は(3)(a)単一対の金属の一方若しくは双方の少なくとも1つの酸化物と(b)単一対の金属の一方若しくは双方の少なくとも1つの遊離の金属を含浸させた又は運ぶ、少なくとも1つの焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含む、それから本質的に成る、又はそれから成る焼成生成物である、再水和させ、含浸させた又はドープさせた固体状態の焼成された熱分解触媒と、(その際、前記焼成生成物は、遊離の酸素の存在下(たとえば、空気又は酸素と窒素、ネオン、アルゴン若しくはクリプトンから選択される少なくとも1つの不活性気体の混合物)で、前記対の金属の塩を含浸させた又はそれを運ぶ、少なくとも1つの予備焼成したハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を焼成することによって形成され、(1)、(2)又は(3)の単一対の金属は、以下の群:CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYから選択され);及び
(C)固体状態の粒子状熱媒を接触させることによって混合物を形成することと、
(II)空気の添加、分子状酸素の添加、分子状水素の添加、及び/又は水のような液体希釈剤若しくは担体の添加を除外して(を伴わずに)熱分解反応器の中で約500℃を超える1以上の温度にて(I)の前記混合物の少なくとも一部を迅速に又は瞬時に熱分解し、それによって流体の熱分解生成物を形成することを含む方法。
(BA) A method of producing one or more fluid hydrocarbon products from a biomass material in a solid state, the method comprising:
(I) Under stirring in a pyrolysis reactor (A) Particulate or finely divided solid biomass material that is untreated except for any drying and / or crushing;
(B) when loaded into the reactor, (1) a single pair of metals, (2) a single pair of at least one oxide of each of the metals, or (3) (a) one or both of a single pair of metals. At least one calcined hydrotalcite or hydrotalcite-like compound, layered two impregnated or carrying at least one oxide and (b) at least one free metal of one or both of a single pair of metals A rehydrated, impregnated or doped solid state calcined product comprising, consisting essentially of, or consisting of a hydroxide, anionic clay, or a mixture of two or more thereof. (Wherein the calcined product is in the presence of free oxygen (eg air or oxygen and a small amount selected from nitrogen, neon, argon or krypton). At least one pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anion impregnated with or carrying the metal salt of said pair with a mixture of inert gases) A single pair of metals of (1), (2) or (3) is formed from the following groups: Ca and Ce, Ca and Cu, and Ca. Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, Ni and Y); And (C) forming a mixture by contacting a solid state heating medium in a solid state;
(II) in the pyrolysis reactor, excluding (without) the addition of air, molecular oxygen, molecular hydrogen, and / or the addition of a liquid diluent or carrier such as water A method comprising rapidly or instantaneously pyrolyzing at least a portion of said mixture of (I) at one or more temperatures greater than about 500 ° C. thereby forming a fluid pyrolysis product.
(BB)(1)、(2)又は(3)の金属の前記単一対がCaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、FeとY、MoとZn、及びMnとYから選択される(BA)のような方法。 (BB) The single pair of metals of (1), (2) or (3) is Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Fe and Y, Mo And a method such as (BA) selected from Zn and Mn and Y.
(BC)(1)、(2)又は(3)の金属の前記単一対がCaとCu及びCaとFeから選択される(BB)のような方法。 (BC) A method as in (BB), wherein the single pair of metals of (1), (2) or (3) is selected from Ca and Cu and Ca and Fe.
(BD)前記予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物がマグネシウム及びアルミニウムの金属を含有する(BA)〜(BC)のいずれかのような方法。 (BD) The pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof contains magnesium and aluminum metals (BA) to ( BC).
(BE)前記迅速な又は瞬時の熱分解が実質的に常圧で500℃を超えて約650℃迄の温度にて行われ、バイオマス物質が、不活性の無水担体ガス、好ましくは、窒素、アルゴン、ネオン又はクリプトン又はそれらの2以上の混合物と共に熱分解反応器に装填され、前記固体状態の粒子状熱媒が砂であり、反応器に装填される際の前記焼成された熱分解触媒が約40〜約400ミクロンの、好ましくは約50〜150ミクロンの範囲の平均粒度を有し、前記焼成された熱分解触媒が熱分解反応器に装填される際、再水和によって活性化されており、方法が、30秒以下、好ましくは20秒以下、又はさらに好ましくは10秒以下の熱分解反応器内での滞留時間で実施される(BA)〜(BC)のいずれかのような方法。 (BE) The rapid or instantaneous pyrolysis is carried out at a temperature substantially above 500 ° C. to about 650 ° C. at atmospheric pressure, and the biomass material is an inert anhydrous carrier gas, preferably nitrogen, The pyrolysis reactor is loaded together with argon, neon or krypton or a mixture of two or more thereof, the solid particulate heat transfer medium is sand, and the calcined pyrolysis catalyst when loaded into the reactor is Having an average particle size in the range of about 40 to about 400 microns, preferably about 50 to 150 microns, and activated by rehydration when the calcined pyrolysis catalyst is loaded into the pyrolysis reactor. And the process is carried out with a residence time in the pyrolysis reactor of 30 seconds or less, preferably 20 seconds or less, or more preferably 10 seconds or less, as in any of (BA) to (BC) .
(BF)前記温度が約510℃〜約575℃の範囲内である(BA)〜(BC)のいずれかのような方法。 (BF) The method as in any one of (BA) to (BC), wherein the temperature is in the range of about 510 ° C to about 575 ° C.
(CA)CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、
CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、及びNiとYから選択される金属の対の塩、好ましくは無機塩を含浸させている又はドープさせている、及び金属の対の一方又は双方の少なくとも一部の1以上の酸化物が酸化物に変換されるように乾燥させた後1以上の高温で遊離の酸素(たとえば、空気又は酸素と窒素、ネオン、アルゴン若しくはクリプトンから選択される少なくとも1つの不活性気体の混合物)の存在下で焼成されている少なくとも1つの予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物から形成される焼成生成物を含む、それから本質的に成る、又はそれから成る固体状態の熱分解触媒組成物。
(CA) Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn,
Impregnated with a salt of a metal pair selected from Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, and Ni and Y, preferably an inorganic salt. Free oxygen (eg, air) at one or more elevated temperatures after being dried such that at least a portion of one or both of one or both of the metal pair is doped or doped and is converted to an oxide. Or a mixture of at least one inert gas selected from oxygen and nitrogen, neon, argon or krypton), or at least one pre-calcined hydrotalcite or hydrotalcite-like compound, layered Solid state pyrolysis catalyst comprising, consisting essentially of or consisting of a calcined product formed from a dihydroxide, an anionic clay, or a mixture of two or more thereof Narubutsu.
(CB)金属の前記対がCaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、FeとY、MoとZn、及びMnとYから選択される(CA)のような触媒組成物。 (CB) The metal pairs are selected from Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Fe and Y, Mo and Zn, and Mn and Y (CA ) Catalyst composition.
(CC)金属の前記対がCaとCu及びCaとFeから選択される(CB)のような触媒組成物。 (CC) A catalyst composition such as (CB), wherein the pair of metals is selected from Ca and Cu and Ca and Fe.
(CD)前記予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物がマグネシウム及びアルミニウムの金属を含有する(CA)〜(CC)のいずれかのような触媒組成物。 (CD) The pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof contains magnesium and aluminum metals (CA) to ( CC).
本明細書又はクレームにおけるどこかでの化学名又は化学式によって言及される成分は、単数で言及されようと複数で言及されようと、化学名又は化学的な種類によって言及される別の物質(たとえば、別の成分、溶媒等)と接触する前にそれらが存在するように特定される。得られた混合物又は溶液にてどの化学変化、変換及び/又は反応が、もしあれば、生じるかは、そのような変化変換及び/又は反応が本開示に従って要求される条件下で特定された成分と一緒にすることの自然の結果なので、問題ではない。 A component referred to by a chemical name or formula anywhere in this specification or claim, whether referred to in the singular or in the plural, is another substance referred to by chemical name or chemical type (e.g., Before they come into contact with other components, solvents, etc.). Which chemical changes, transformations and / or reactions, if any, occur in the resulting mixture or solution are components identified under the conditions under which such transformations and transformations and / or reactions are required according to the present disclosure. It is not a problem because it is the natural result of being together.
本発明は、本明細書で引用された物質及び/又は手順を含み得るし、それから成り得るし、又は本質的にそれから成り得る。 The present invention can include, consist of, or consist essentially of the materials and / or procedures cited herein.
別のやり方で明白に指示され得るのを除いて、冠詞「a」又は「an」は、本明細書で使用するのであれば又は使用するとき、限定することを意図するものではなく、クレームを冠詞が指す単一要素に限定すると解釈されるべきではない。むしろ、冠詞「a」又は「an」は、本明細書で使用するのであれば又は使用するとき、本文が明白に指示しない限り、1以上のそのような要素を網羅するように意図される。 Except as expressly indicated otherwise, the article “a” or “an” is not intended to be limiting, if used or used herein, and claims It should not be construed as limited to the single element that the article points to. Rather, the article “a” or “an”, as used herein or when used, is intended to cover one or more such elements, unless the text clearly indicates otherwise.
本発明はその実践において相当な変化の影響を受け易い。従って、前述の記載は限定するように意図されるのではなく、上文に提示した特定の例示にのみ本発明を限定すると解釈されるべきではない。 The present invention is susceptible to considerable changes in practice. Accordingly, the foregoing description is not intended to be limiting and should not be construed to limit the invention to the specific illustrations presented above.
Claims (20)
(I)熱分解反応器にて撹拌のもとで
(A)任意の乾燥及び/又は破砕を除いて未処理である粒子状の又は細かく分けた固体状態のバイオマス物質;
(B)反応器に装填される際、(1)単一対の金属、(2)単一対の前記金属それぞれの少なくとも1つの酸化物、又は(3)(a)単一対の金属の一方若しくは双方の少なくとも1つの酸化物と(b)単一対の金属の一方若しくは双方の少なくとも1つの遊離の金属との組み合わせを含浸させた又は運ぶ、少なくとも1つの焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含む、それから本質的に成る、又はそれから成る焼成生成物である、再水和させ、含浸させた又はドープさせた固体状態の焼成された熱分解触媒と、(その際、前記焼成生成物は、遊離の酸素の存在下で前記対の金属の塩を含浸させている又はそれを運ぶ少なくとも1つの予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を焼成することによって形成され、(1)、(2)又は(3)の単一対の金属は、以下の群:CaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYから選択され);及び
(C)固体状態の粒子状熱媒を接触させることによって混合物を形成することと、
(II)空気の添加、分子状酸素の添加、分子状水素の添加、又は液体の希釈剤若しくは担体の添加を伴わずに熱分解反応器の中で約500℃を超える1以上の温度にて(I)の前記混合物の少なくとも一部を迅速に又は瞬時に熱分解し、それによって流体の熱分解生成物を形成することを含む、前記方法。 A method for producing one or more fluid hydrocarbon products from a biomass material in a solid state, the method comprising:
(I) Under stirring in a pyrolysis reactor (A) Particulate or finely divided solid biomass material that is untreated except for any drying and / or crushing;
(B) When loaded into the reactor, (1) a single pair of metals, (2) a single pair of at least one oxide of each of the metals, or (3) (a) one or both of a single pair of metals. At least one calcined hydrotalcite or hydrotalcite-like impregnated or carrying a combination of at least one oxide of (b) and at least one free metal of one or both of a single pair of metals Rehydrated, impregnated or doped solids comprising, consisting essentially of or consisting of compounds, layered dihydroxides, anionic clays, or mixtures of two or more thereof A calcined pyrolysis catalyst in the state, wherein the calcined product is impregnated with or carries the pair of metal salts in the presence of free oxygen (1), (2) or (3) formed by firing the formed hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or a mixture of two or more thereof. The single pairs of metals are the following groups: Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb , Fe and Y, Mo and Zn, Mn and Y, Ni and Y); and (C) forming a mixture by contacting a solid state heating medium in a solid state;
(II) at one or more temperatures above about 500 ° C. in the pyrolysis reactor without the addition of air, molecular oxygen, molecular hydrogen, or liquid diluent or support The method comprising rapidly or instantaneously pyrolyzing at least a portion of the mixture of (I), thereby forming a fluid pyrolysis product.
から選択される金属の対の塩を含浸させている又はドープさせている、及び金属の対の一方又は双方の少なくとも一部の1以上の酸化物が酸化物に変換されるように乾燥させた後1以上の高温で遊離の酸素の存在下で焼成されている、少なくとも1つの予備焼成されたハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物から形成される焼成生成物を含む、それから本質的に成る、又はそれから成る固体状態の熱分解触媒組成物。 Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, Ce and Fe, Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, and Mn Y and Ni and Y
Impregnated or doped with a salt of a metal pair selected from and dried so that one or more oxides of at least part of one or both of the metal pairs are converted to oxides At least one pre-calcined hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or two thereof, which is subsequently calcined in the presence of free oxygen at one or more high temperatures A solid state pyrolysis catalyst composition comprising, consisting essentially of, or consisting of a calcined product formed from the above mixture.
(A)個々に見れば、又は集合的に見れば、溶解された金属の対を提供する1以上の溶液を作り出すこと又は提供すること(前記溶液は同一であっても異なっていてもよく、蒸発可能な溶媒である溶媒を含み、前記1以上の溶液の溶解された金属の対はCaとCe、CaとCu、CaとFe、CaとMn、CaとY、CaとZn、CeとFe、CeとNi、CeとY、CuとNb、FeとY、MoとZn、MnとY、NiとYからから成る群から選択される)と、
(B)上記(A)の前記溶液の1以上を用いた初期湿り法で粉状の又は粒子状のハイドロタルサイト若しくはハイドロタルサイト様の化合物、層状二水酸化物、アニオン性粘土、又はそれらの2以上の混合物を含浸させて湿り混合物を形成し、湿り混合物を乾燥させて生成物混合物を形成し、次いで遊離の酸素の存在下で生成物混合物を焼成することとを含む方法。 Producing pyrolysis products from untreated particulate or finely divided solid state biomass material except for any drying and / or crushing without the addition of air, molecular oxygen, molecular hydrogen or liquid A method of preparing a catalyst composition adapted to
(A) creating or providing one or more solutions that provide dissolved metal pairs, either individually or collectively, (the solutions may be the same or different; The dissolved metal pairs of the one or more solutions include Ca and Ce, Ca and Cu, Ca and Fe, Ca and Mn, Ca and Y, Ca and Zn, and Ce and Fe. , Ce and Ni, Ce and Y, Cu and Nb, Fe and Y, Mo and Zn, Mn and Y, and Ni and Y).
(B) Powdered or particulate hydrotalcite or hydrotalcite-like compound, layered dihydroxide, anionic clay, or the like by an initial wetting method using one or more of the solutions of (A) above Impregnating a mixture of two or more of to form a wet mixture, drying the wet mixture to form a product mixture, and then calcining the product mixture in the presence of free oxygen.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261681064P | 2012-08-08 | 2012-08-08 | |
| US61/681,064 | 2012-08-08 | ||
| PCT/EP2013/066532 WO2014023758A2 (en) | 2012-08-08 | 2013-08-07 | Selective catalytic deoxygenation of biomass and catalysts therefor |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015529556A true JP2015529556A (en) | 2015-10-08 |
| JP2015529556A5 JP2015529556A5 (en) | 2016-09-08 |
Family
ID=48979733
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015525874A Pending JP2015529556A (en) | 2012-08-08 | 2013-08-07 | Selective catalytic deoxygenation of biomass and catalyst therefor |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20150190788A1 (en) |
| EP (1) | EP2882827A2 (en) |
| JP (1) | JP2015529556A (en) |
| CN (1) | CN104718275A (en) |
| BR (1) | BR112015002752A2 (en) |
| CA (1) | CA2878793A1 (en) |
| IN (1) | IN2015DN00325A (en) |
| WO (1) | WO2014023758A2 (en) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10040735B2 (en) * | 2014-05-08 | 2018-08-07 | Exxonmobil Research And Engineering Company | Method of producing an alcohol-containing pyrolisis product |
| EP3169753B1 (en) | 2014-07-17 | 2020-06-10 | SABIC Global Technologies B.V. | Upgrading hydrogen deficient streams using hydrogen donor streams in a hydropyrolysis process |
| EP3400273A2 (en) * | 2015-10-05 | 2018-11-14 | University Of Pretoria | Oxygenate reduction catalyst and process |
| CN108855101B (en) * | 2016-07-18 | 2020-10-20 | 山东省科学院能源研究所 | Method for online upgrading bio-oil by using iron-based composite catalyst |
| ES2932125A1 (en) * | 2021-06-29 | 2023-01-13 | Univ Cordoba | NEW HYDROTALCITES AND THEIR USE AS CATALYSTS FOR TRANSESTERIFICATION OF OIL (Machine-translation by Google Translate, not legally binding) |
| CN114797878B (en) * | 2022-03-24 | 2023-02-24 | 华北电力大学 | Method for preparing tar catalytic cracking reforming hydrogen production and carbon dioxide adsorption dual-function catalyst by using biomass ash |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007534595A (en) * | 2004-04-26 | 2007-11-29 | アルベマーレ ネザーランズ ビー.ブイ. | Method for preparing additive-containing anionic clay |
| WO2011123508A2 (en) * | 2010-03-31 | 2011-10-06 | Exxonmobil Research And Engineering Company | Methods for producing pyrolysis products |
| WO2012082377A1 (en) * | 2010-12-13 | 2012-06-21 | Exxonmobil Research And Engineering Company | Phosphorus recovery from hydrothermal treatment of biomass |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5340466A (en) * | 1993-04-19 | 1994-08-23 | Texaco Inc. | Hydrodesulfurization of cracked naphtha with hydrotalcite-containing catalyst |
| US6028023A (en) * | 1997-10-20 | 2000-02-22 | Bulldog Technologies U.S.A., Inc. | Process for making, and use of, anionic clay materials |
| KR100972705B1 (en) * | 2002-06-28 | 2010-07-28 | 알베마를 네덜란드 비.브이. | Fcc catalyst for reducing the sulfur content in gasoline and diesel |
| EP2105486A1 (en) * | 2008-03-25 | 2009-09-30 | KiOR Inc. | Low total acid number bio-crude |
| US8236173B2 (en) * | 2011-03-10 | 2012-08-07 | Kior, Inc. | Biomass pretreatment for fast pyrolysis to liquids |
-
2013
- 2013-08-07 BR BR112015002752A patent/BR112015002752A2/en active Search and Examination
- 2013-08-07 WO PCT/EP2013/066532 patent/WO2014023758A2/en active Application Filing
- 2013-08-07 JP JP2015525874A patent/JP2015529556A/en active Pending
- 2013-08-07 US US14/417,725 patent/US20150190788A1/en not_active Abandoned
- 2013-08-07 IN IN325DEN2015 patent/IN2015DN00325A/en unknown
- 2013-08-07 CA CA2878793A patent/CA2878793A1/en not_active Abandoned
- 2013-08-07 CN CN201380041666.5A patent/CN104718275A/en active Pending
- 2013-08-07 EP EP13748009.1A patent/EP2882827A2/en not_active Withdrawn
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007534595A (en) * | 2004-04-26 | 2007-11-29 | アルベマーレ ネザーランズ ビー.ブイ. | Method for preparing additive-containing anionic clay |
| WO2011123508A2 (en) * | 2010-03-31 | 2011-10-06 | Exxonmobil Research And Engineering Company | Methods for producing pyrolysis products |
| WO2012082377A1 (en) * | 2010-12-13 | 2012-06-21 | Exxonmobil Research And Engineering Company | Phosphorus recovery from hydrothermal treatment of biomass |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104718275A (en) | 2015-06-17 |
| CA2878793A1 (en) | 2014-02-13 |
| US20150190788A1 (en) | 2015-07-09 |
| IN2015DN00325A (en) | 2015-06-12 |
| EP2882827A2 (en) | 2015-06-17 |
| WO2014023758A3 (en) | 2014-04-17 |
| BR112015002752A2 (en) | 2017-07-04 |
| WO2014023758A2 (en) | 2014-02-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2015529556A (en) | Selective catalytic deoxygenation of biomass and catalyst therefor | |
| US8293952B2 (en) | Methods for producing pyrolysis products | |
| Kuo et al. | Cellulose-to-HMF conversion using crystalline mesoporous titania and zirconia nanocatalysts in ionic liquid systems | |
| AU2017279755B2 (en) | Catalyst Compositions And Use Thereof In Catalytic Biomass Pyrolysis | |
| JP6342394B2 (en) | Catalytic pyrolysis process and pyrolysis products formed thereby | |
| Afari et al. | Comparative kinetic studies of solid absorber catalyst (K/MgO) and solid desorber catalyst (HZSM-5)-aided CO2 absorption and desorption from aqueous solutions of MEA and blended solutions of BEA-AMP and MEA-MDEA | |
| Norouzi et al. | Catalytic upgrading of bio-products derived from pyrolysis of red macroalgae Gracilaria gracilis with a promising novel micro/mesoporous catalyst | |
| US10040735B2 (en) | Method of producing an alcohol-containing pyrolisis product | |
| Cheng et al. | Directly catalytic upgrading bio-oil vapor produced by prairie cordgrass pyrolysis over Ni/HZSM-5 using a two stage reactor | |
| Behnia et al. | Supercritical water gasification of aqueous fraction of pyrolysis oil in the presence of a Ni‐Ru catalyst | |
| JP2015529556A5 (en) | ||
| Dada et al. | Thermo-catalytic co-pyrolysis of ironbark sawdust and plastic waste over strontium loaded hierarchical Y-zeolite | |
| Li et al. | Catalytic pyrolysis of rice straw for high yield of aromatics over modified ZSM-5 catalysts and its kinetics | |
| JP6460879B2 (en) | Regeneration method for tar-containing gas reforming catalyst | |
| JP5817794B2 (en) | Method for demethylation or demethoxylation of aromatic compound having methoxy group | |
| JP2013523960A (en) | Method for producing pyrolysis product | |
| US20210214622A1 (en) | Process of upgrading light hydrocarbons and oxygenates produced during catalytic pyrolysis of biomass | |
| Ogonowski et al. | Catalytic dehydrogenation of isobutane in the presence of carbon dioxide | |
| Genel et al. | Catalytic effect of metal powder and MCM‐41/metal catalysts on the pyrolysis of cellulose | |
| JP5892277B2 (en) | Catalyst for demethylation or demethoxylation reaction in a liquid phase of a mixture containing guaiacol as a main component, and method for producing phenol or catechol using the same | |
| JP2023011517A (en) | Hydrocarbon-containing gas reforming catalyst, production method of hydrocarbon-containing gas reforming catalyst, and reforming method of hydrocarbon-containing gas using hydrocarbon-containing gas reforming catalyst | |
| Santamaría Moreno et al. | Effect of CeO2 and MgO promoters on the performance of a Ni/Al2O3 catalyst in the steam reforming of biomass pyrolysis volatiles | |
| Gonzalez Borja | Understanding Catalytic Strategies for Bio-oil Upgrading: Model Compound Studies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160720 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160720 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20170614 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170621 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180131 |