JP2015523058A - 間葉系幹細胞の骨形成分化 - Google Patents
間葉系幹細胞の骨形成分化 Download PDFInfo
- Publication number
- JP2015523058A JP2015523058A JP2015511419A JP2015511419A JP2015523058A JP 2015523058 A JP2015523058 A JP 2015523058A JP 2015511419 A JP2015511419 A JP 2015511419A JP 2015511419 A JP2015511419 A JP 2015511419A JP 2015523058 A JP2015523058 A JP 2015523058A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- vesicles
- osteogenic differentiation
- extracellular vesicles
- target cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 230000009818 osteogenic differentiation Effects 0.000 title claims abstract description 32
- 210000002901 mesenchymal stem cell Anatomy 0.000 title claims description 38
- 238000000034 method Methods 0.000 claims abstract description 29
- 230000001939 inductive effect Effects 0.000 claims abstract description 8
- 230000001737 promoting effect Effects 0.000 claims abstract description 8
- 210000004027 cell Anatomy 0.000 claims description 108
- 210000001808 exosome Anatomy 0.000 claims description 77
- 210000001616 monocyte Anatomy 0.000 claims description 44
- 239000007943 implant Substances 0.000 claims description 22
- 210000000988 bone and bone Anatomy 0.000 claims description 21
- 210000000130 stem cell Anatomy 0.000 claims description 20
- 239000002158 endotoxin Substances 0.000 claims description 16
- 229920006008 lipopolysaccharide Polymers 0.000 claims description 16
- 210000002540 macrophage Anatomy 0.000 claims description 14
- 102000004127 Cytokines Human genes 0.000 claims description 10
- 108090000695 Cytokines Proteins 0.000 claims description 10
- 230000011164 ossification Effects 0.000 claims description 9
- 102000019034 Chemokines Human genes 0.000 claims description 7
- 108010012236 Chemokines Proteins 0.000 claims description 7
- 230000006378 damage Effects 0.000 claims description 6
- 210000004969 inflammatory cell Anatomy 0.000 claims description 6
- 230000008439 repair process Effects 0.000 claims description 6
- 208000001132 Osteoporosis Diseases 0.000 claims description 5
- 239000011248 coating agent Substances 0.000 claims description 5
- 238000000576 coating method Methods 0.000 claims description 5
- 238000012258 culturing Methods 0.000 claims description 5
- 230000004936 stimulating effect Effects 0.000 claims description 5
- 239000011800 void material Substances 0.000 claims description 5
- 210000004369 blood Anatomy 0.000 claims description 4
- 239000008280 blood Substances 0.000 claims description 4
- 201000010099 disease Diseases 0.000 claims description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 4
- 239000000945 filler Substances 0.000 claims description 4
- 230000002757 inflammatory effect Effects 0.000 claims description 4
- 239000000203 mixture Substances 0.000 claims description 4
- 208000027418 Wounds and injury Diseases 0.000 claims description 3
- 230000004927 fusion Effects 0.000 claims description 3
- 208000014674 injury Diseases 0.000 claims description 3
- 210000001519 tissue Anatomy 0.000 claims description 3
- 230000008468 bone growth Effects 0.000 claims description 2
- 210000003127 knee Anatomy 0.000 claims description 2
- 201000008482 osteoarthritis Diseases 0.000 claims description 2
- 210000003625 skull Anatomy 0.000 claims description 2
- 239000003636 conditioned culture medium Substances 0.000 description 22
- 210000004271 bone marrow stromal cell Anatomy 0.000 description 17
- 239000002609 medium Substances 0.000 description 13
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 12
- 239000003102 growth factor Substances 0.000 description 10
- 238000000684 flow cytometry Methods 0.000 description 8
- 102100025222 CD63 antigen Human genes 0.000 description 7
- 101000934368 Homo sapiens CD63 antigen Proteins 0.000 description 7
- -1 IL-14 Proteins 0.000 description 7
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 6
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 6
- 238000010586 diagram Methods 0.000 description 6
- 108020004999 messenger RNA Proteins 0.000 description 6
- 239000002679 microRNA Substances 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 102100027221 CD81 antigen Human genes 0.000 description 5
- 101000914479 Homo sapiens CD81 antigen Proteins 0.000 description 5
- 101000738354 Homo sapiens CD9 antigen Proteins 0.000 description 5
- 238000001514 detection method Methods 0.000 description 5
- 230000014509 gene expression Effects 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 108091032955 Bacterial small RNA Proteins 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 238000004113 cell culture Methods 0.000 description 4
- 230000004069 differentiation Effects 0.000 description 4
- 239000007850 fluorescent dye Substances 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 230000001965 increasing effect Effects 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 230000001105 regulatory effect Effects 0.000 description 4
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 3
- 108010049931 Bone Morphogenetic Protein 2 Proteins 0.000 description 3
- 102100024506 Bone morphogenetic protein 2 Human genes 0.000 description 3
- 102000015775 Core Binding Factor Alpha 1 Subunit Human genes 0.000 description 3
- 108010024682 Core Binding Factor Alpha 1 Subunit Proteins 0.000 description 3
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 3
- 108700011259 MicroRNAs Proteins 0.000 description 3
- 108020004459 Small interfering RNA Proteins 0.000 description 3
- 210000001789 adipocyte Anatomy 0.000 description 3
- 230000008568 cell cell communication Effects 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 230000035876 healing Effects 0.000 description 3
- 210000003630 histaminocyte Anatomy 0.000 description 3
- 230000028993 immune response Effects 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 108091070501 miRNA Proteins 0.000 description 3
- 238000012758 nuclear staining Methods 0.000 description 3
- 239000002773 nucleotide Substances 0.000 description 3
- 125000003729 nucleotide group Chemical group 0.000 description 3
- 210000002997 osteoclast Anatomy 0.000 description 3
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 2
- 102100037904 CD9 antigen Human genes 0.000 description 2
- 102100030703 Interleukin-22 Human genes 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000012620 biological material Substances 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 230000010478 bone regeneration Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 238000004891 communication Methods 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000001962 electrophoresis Methods 0.000 description 2
- 210000003743 erythrocyte Anatomy 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000000017 hydrogel Substances 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 239000004816 latex Substances 0.000 description 2
- 229920000126 latex Polymers 0.000 description 2
- 230000033001 locomotion Effects 0.000 description 2
- 238000007885 magnetic separation Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 239000000021 stimulant Substances 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- 208000020084 Bone disease Diseases 0.000 description 1
- 102100031172 C-C chemokine receptor type 1 Human genes 0.000 description 1
- 101710149814 C-C chemokine receptor type 1 Proteins 0.000 description 1
- 102100031151 C-C chemokine receptor type 2 Human genes 0.000 description 1
- 101710149815 C-C chemokine receptor type 2 Proteins 0.000 description 1
- 102100024167 C-C chemokine receptor type 3 Human genes 0.000 description 1
- 101710149862 C-C chemokine receptor type 3 Proteins 0.000 description 1
- 102100037853 C-C chemokine receptor type 4 Human genes 0.000 description 1
- 101710149863 C-C chemokine receptor type 4 Proteins 0.000 description 1
- 102100035875 C-C chemokine receptor type 5 Human genes 0.000 description 1
- 101710149870 C-C chemokine receptor type 5 Proteins 0.000 description 1
- 102100036849 C-C motif chemokine 24 Human genes 0.000 description 1
- 102100021935 C-C motif chemokine 26 Human genes 0.000 description 1
- 102000034342 Calnexin Human genes 0.000 description 1
- 108010056891 Calnexin Proteins 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 102000012422 Collagen Type I Human genes 0.000 description 1
- 108010022452 Collagen Type I Proteins 0.000 description 1
- 102100023688 Eotaxin Human genes 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 101000713078 Homo sapiens C-C motif chemokine 24 Proteins 0.000 description 1
- 101000897493 Homo sapiens C-C motif chemokine 26 Proteins 0.000 description 1
- 101000978392 Homo sapiens Eotaxin Proteins 0.000 description 1
- 101001002470 Homo sapiens Interferon lambda-1 Proteins 0.000 description 1
- 101000853002 Homo sapiens Interleukin-25 Proteins 0.000 description 1
- 101000853000 Homo sapiens Interleukin-26 Proteins 0.000 description 1
- 101000998139 Homo sapiens Interleukin-32 Proteins 0.000 description 1
- 101000958041 Homo sapiens Musculin Proteins 0.000 description 1
- 101001128431 Homo sapiens Myeloid-derived growth factor Proteins 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 102000000589 Interleukin-1 Human genes 0.000 description 1
- 108090000174 Interleukin-10 Proteins 0.000 description 1
- 102000003814 Interleukin-10 Human genes 0.000 description 1
- 108090000177 Interleukin-11 Proteins 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 108090000176 Interleukin-13 Proteins 0.000 description 1
- 108090000172 Interleukin-15 Proteins 0.000 description 1
- 101800003050 Interleukin-16 Proteins 0.000 description 1
- 102000013691 Interleukin-17 Human genes 0.000 description 1
- 108050003558 Interleukin-17 Proteins 0.000 description 1
- 108090000171 Interleukin-18 Proteins 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 102000013264 Interleukin-23 Human genes 0.000 description 1
- 108010065637 Interleukin-23 Proteins 0.000 description 1
- 108010066979 Interleukin-27 Proteins 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 101710181613 Interleukin-31 Proteins 0.000 description 1
- 108010067003 Interleukin-33 Proteins 0.000 description 1
- 101710181549 Interleukin-34 Proteins 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- 108010002586 Interleukin-7 Proteins 0.000 description 1
- 108090001007 Interleukin-8 Proteins 0.000 description 1
- 108010002335 Interleukin-9 Proteins 0.000 description 1
- 208000029725 Metabolic bone disease Diseases 0.000 description 1
- 102000004067 Osteocalcin Human genes 0.000 description 1
- 108090000573 Osteocalcin Proteins 0.000 description 1
- 206010049088 Osteopenia Diseases 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 108700030796 Tsg101 Proteins 0.000 description 1
- 101150072717 Tsg101 gene Proteins 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229940096422 collagen type i Drugs 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000001493 electron microscopy Methods 0.000 description 1
- 230000002121 endocytic effect Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000000799 fluorescence microscopy Methods 0.000 description 1
- 239000001056 green pigment Substances 0.000 description 1
- 102000046949 human MSC Human genes 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 230000003100 immobilizing effect Effects 0.000 description 1
- 230000003832 immune regulation Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000035992 intercellular communication Effects 0.000 description 1
- 102000004114 interleukin 20 Human genes 0.000 description 1
- 108090000681 interleukin 20 Proteins 0.000 description 1
- 108010074108 interleukin-21 Proteins 0.000 description 1
- 108010074109 interleukin-22 Proteins 0.000 description 1
- 210000002510 keratinocyte Anatomy 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 239000004579 marble Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 238000002493 microarray Methods 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 210000002487 multivesicular body Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 210000003098 myoblast Anatomy 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 210000000963 osteoblast Anatomy 0.000 description 1
- 230000036542 oxidative stress Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 230000000153 supplemental effect Effects 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 238000004627 transmission electron microscopy Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 238000005199 ultracentrifugation Methods 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0654—Osteocytes, Osteoblasts, Odontocytes; Bones, Teeth
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/32—Bones; Osteocytes; Osteoblasts; Tendons; Tenocytes; Teeth; Odontoblasts; Cartilage; Chondrocytes; Synovial membrane
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L24/00—Surgical adhesives or cements; Adhesives for colostomy devices
- A61L24/0005—Ingredients of undetermined constitution or reaction products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L24/00—Surgical adhesives or cements; Adhesives for colostomy devices
- A61L24/001—Use of materials characterised by their function or physical properties
- A61L24/0015—Medicaments; Biocides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/005—Ingredients of undetermined constitution or reaction products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/16—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0635—B lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/15—Cells of the myeloid line, e.g. granulocytes, basophils, eosinophils, neutrophils, leucocytes, monocytes, macrophages or mast cells; Myeloid precursor cells; Antigen-presenting cells, e.g. dendritic cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/60—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a special physical form
- A61L2300/64—Animal cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/02—Materials or treatment for tissue regeneration for reconstruction of bones; weight-bearing implants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/05—Adjuvants
- C12N2501/052—Lipopolysaccharides [LPS]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/11—Coculture with; Conditioned medium produced by blood or immune system cells
- C12N2502/1157—Monocytes, macrophages
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/13—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from connective tissue cells, from mesenchymal cells
- C12N2506/1346—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from connective tissue cells, from mesenchymal cells from mesenchymal stem cells
- C12N2506/1384—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from connective tissue cells, from mesenchymal cells from mesenchymal stem cells from adipose-derived stem cells [ADSC], from adipose stromal stem cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Surgery (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Rheumatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Pharmacology & Pharmacy (AREA)
- Immunology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Cell Biology (AREA)
- Heart & Thoracic Surgery (AREA)
- Vascular Medicine (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Materials Engineering (AREA)
- Hematology (AREA)
- Virology (AREA)
- Developmental Biology & Embryology (AREA)
- Pain & Pain Management (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本発明は、細胞外小胞を使用して骨形成分化を誘発するおよび/または促進するための方法ならびにその使用に関する。
Description
本発明は、細胞の分化を誘発するまたは促進するための方法、前記分化を誘発するまたは促進するのに使用するための細胞外小胞、前記小胞の使用、および前記小胞を使用する治療の方法に関する。
序論
インプラント表面または傷害の部位での初期の骨形成のメカニズムならびに骨−インプラントの接触、安定性、および機能の維持に影響を及ぼす因子は、完全には理解されていない。炎症細胞および幹細胞および前駆細胞がインプラントの表面で連絡する経路についての知識の増加は、臨床上の使用のための次世代のインプラントをどのように最適化するべきかを理解するのに重要である。より優れた知識により、将来、発明者らは、うまく行けば、骨結合の改善のための新しくてよりよいインプラントまたは骨治癒のためのよりよい薬剤を産生することができるであろう。
インプラント表面または傷害の部位での初期の骨形成のメカニズムならびに骨−インプラントの接触、安定性、および機能の維持に影響を及ぼす因子は、完全には理解されていない。炎症細胞および幹細胞および前駆細胞がインプラントの表面で連絡する経路についての知識の増加は、臨床上の使用のための次世代のインプラントをどのように最適化するべきかを理解するのに重要である。より優れた知識により、将来、発明者らは、うまく行けば、骨結合の改善のための新しくてよりよいインプラントまたは骨治癒のためのよりよい薬剤を産生することができるであろう。
単球/マクロファージ系は、バイオマテリアル表面で、宿主防御、創傷治癒、および免疫調節における中心的な役割を果たす。単球および間葉系幹細胞は、移植された物質表面に速やかに移動し、細胞外マトリックスの沈着および骨形成の前に、互いにすぐ近くに局在化する。たとえば炎症促進性サイトカインを含有する、ヒト単球由来の条件培地が、ヒト間葉系幹細胞(hMSC)の骨形成分化を促進することが示された。単球およびMSCが直接的な細胞間接触の非存在下において連絡することが示唆されているが、単球がMSCとどのように連絡するかは完全には決定されていない。
エキソソームを含む細胞外小胞(EV)は、細胞間の連絡において重要な役割を果たす。細胞間の連絡について示唆される一般的なメカニズムは、おそらく微小環境においてであるが、可能性として少し離れてでも起こるであろう、エキソソームを通しての移動によるRNAの送達に関係する。エキソソームは、多胞体の形質膜との融合に際して細胞外環境へ放出される、エンドサイトーシス起源の小さな膜小胞(40〜100nm)である。エキソソームは、細胞間の連絡の手段を提供し、ここで、一方の細胞は、微小環境におけるまたはある距離を置いた他方の細胞に影響を及ぼすことができるエキソソームを放出することができる。
エキソソームは、多くの細胞から放出され、それらの機能は、それらに細胞の特徴的な組成物を与える産生細胞についての細胞起源および状態に依存する。たとえば、酸化ストレスに曝露された細胞に起源を持つエキソソームは、ストレスに対する保護的なメッセージをレシピエント細胞に伝えることが示された。
しかしながら、EVがレシピエント細胞の分化に影響を及ぼすかどうか、また、どのように影響を及ぼすのかは、ほとんど知られていない。
本発明の目的は、細胞、好ましくは間葉系幹細胞、より好ましくはヒト間葉系幹細胞(hMSC)の骨形成分化を誘発するおよび/または促進するための方法を提供することである。本発明はまた、骨再生を増加させ、かつインプラントの骨結合を支持するための、細胞外小胞の使用に関する。
第1の態様において、本発明は、標的幹細胞の骨形成分化を誘発するおよび/または促進するための方法において、
a.非標的細胞の細胞培養由来の条件培地または非標的細胞から単離された細胞外小胞を提供するステップと、
b.培地または細胞外小胞を標的幹細胞に追加するステップと、を含む方法に関する。
a.非標的細胞の細胞培養由来の条件培地または非標的細胞から単離された細胞外小胞を提供するステップと、
b.培地または細胞外小胞を標的幹細胞に追加するステップと、を含む方法に関する。
第2の態様において、本発明は、標的幹細胞の骨形成分化において使用するための単離細胞外小胞に関する。
第3の態様において、本発明は、標的幹細胞の骨形成分化において使用するための、非標的細胞によって得られた細胞外小胞を含む培地に関する。
第4の態様において、本発明は、細胞外小胞に曝露されたコーティングを含むインプラント表面に関する。
第5の態様において、本発明は、エキソソームを産生することができる、固定され刺激された単球、マクロファージ、または間葉系幹細胞のコーティングを含むインプラント表面に関する。
第6の態様において、本発明は、患者を治療するための方法において、血液または組織サンプルを患者から収集するステップと、非標的細胞を単離するステップと、非標的細胞を培養し、かつ刺激するステップと、非標的細胞によって産生されたエキソソームを単離するステップと、エキソソームを患者に投与するステップと、を含む方法に関する。
第7の態様において、本発明は、骨損傷、骨粗しょう症、骨形成の治療のためのまたは骨修復における単離細胞外小胞の使用に関する。
第8の態様において、本発明は、骨損傷、骨空隙、骨粗しょう症、または骨形成の治療のための単離細胞外小胞を含む組成物に関する。
第9の態様において、本発明は、単離細胞外小胞を含む骨空隙充填剤に関する。
本発明において、用語「標的幹細胞」は、非標的細胞由来の条件培地または細胞外小胞によって骨形成分化が誘発される細胞を意味する。
用語「条件培地」は、培養細胞を除去した後に、細胞培養に使用される培地を意味する。
細胞へのシグナル伝達は、一般に、可溶性の形態でおよび/または細胞の形質膜であるもしくはマトリックス結合性である表面上に示される分子の効果と見なされる。本発明は、たとえばタンパク質、mRNA、およびマイクロRNAを含有する、細胞由来の約20〜400nmまたは50〜200nmの細胞外小胞によって媒介される細胞間連絡に関する。小胞は、標的細胞に付着し、融合し、または標的細胞によって内部移行され、標的細胞において調節作用を及ぼす。この連絡は、幹細胞、とりわけヒト間葉系幹細胞などのような細胞の骨形成分化を誘発し得るおよび/または促進し得る。
本発明者らは、標的細胞の骨形成分化を誘発するおよび/または促進するための方法を開発した。方法は、非標的細胞の細胞培養物由来の条件培地または非標的細胞から放出された単離細胞外小胞を提供するステップを含む。一実施形態において、細胞外小胞が、エキソソームである。細胞外小胞は、前記小胞を放出させるために、任意選択での非標的細胞の刺激の間に、非標的細胞を培養することおよび条件培地または小胞の単離によって、提供される。非標的細胞は、様々な時間、たとえば1時間以上または1日以上または2日以上または3日以上、培養されてもよい。培地または小胞は、幹細胞であってもよい標的細胞に追加されてもよいまたはそれと接触させてもよい。次いで、小胞は、標的細胞によって取込まれまたはそれに付着し、骨形成分化を誘発するおよび/または促進する。
標的細胞は、任意の適した細胞型であってもよいが、細胞型はまた、前駆細胞もしくは幹細胞であってもよい。細胞は、たとえば、骨芽細胞、破骨細胞、肥満細胞、筋細胞、脂肪細胞、またはヒトMSCなどのような間葉系幹細胞(MSC)であってもよい。
本発明者らの知る限りでは、骨形成分化を誘発するおよび/または促進するための、細胞外エキソソームまたは同様の特性を有する他の細胞外小胞を介しての、炎症細胞および間葉系幹細胞などのような標的細胞などのような細胞の間のクロストーク(cross−talk)について記載している刊行物はない。発明者らは、炎症細胞などのような細胞が、間葉系幹細胞などのような他の細胞にメッセージを送り、レシピエント細胞、たとえば幹細胞における骨分化遺伝子の発現の増加をもたらすことを発見した。これらのメッセージは、エキソソームおよび/または他の細胞外小胞である。
本発明による標的幹細胞の骨形成分化の誘発および/または促進は、本明細書において非標的細胞と呼ばれる、標的細胞以外の細胞を刺激することによって実行されてもよい。これらの刺激非標的細胞は、任意の適した細胞であってもよく、たとえば単球、マクロファージ、赤血球、破骨細胞、肥満細胞、筋芽細胞、ケラチノサイト、脂肪細胞、または任意の他の炎症細胞もしくは非炎症細胞および幹細胞、たとえば間葉系幹細胞とすることができる。好ましくは、非標的細胞は、単球、マクロファージ、または幹細胞であり、好ましい実施形態において、これらは、ヒト単球、マクロファージ、または幹細胞、たとえばhMSCである。方法は、インビボにおいてまたインビトロにおいて実行することができる。
理論によって拘束されないが、標的または非標的細胞の表現型は、骨形成分化の誘発および/または促進の成功において役割を果たし得る。異なる表現型を有する非標的細胞由来のEVがまた、異なる表現型および機能をも有することが知られている。さらに、標的細胞の表現型は、EVが標的細胞に結合し、それらのメッセージを送達することができるかどうかおよびさらに、標的細胞を特異的な方向に向けることができるかどうかに影響を及ぼし得る。本発明の一実施形態において、非標的細胞が、自己由来または非自己由来のものである。他の実施形態において、標的細胞が、自己由来または非自己由来のものである。自己由来のものを使用することの有益性は、免疫応答が限られているということとなり得るが、健康な人または治療される疾患に罹患していない人由来の非自己由来の細胞は、再生または治癒プロセスに関しては、有益となり得る。
細胞は、様々な方法において、たとえば、リポ多糖(LPS)、サイトカイン、ケモカイン、もしくは任意の他の刺激薬またはその組み合わせなどのような刺激剤の使用によって刺激することができる。刺激剤の量は、1〜100ng/mlの範囲、たとえば1ng/ml以上または5ng/ml以上または10ng/ml以上または20ng/ml以上または100ng/ml以下または70ng/ml以下または50ng/ml以下または30ng/ml以下であってもよい。一実施形態において、刺激剤の濃度範囲が、1〜20ng/mlであり、他の実施形態において、濃度が、5〜50ng/mlであり、他の実施形態において、濃度が、5〜15ng/mlである。
理論によって拘束されないが、非標的細胞、とりわけ刺激非標的細胞は、細胞から放出された細胞膜の小さな嚢である分化刺激細胞外小胞、たとえばエキソソームを産生し、これは、標的幹細胞と接触した場合にまたはそれによって取込まれた場合に、骨形成分化を誘発すると考えられる。これらの小胞、骨形成分化を促進するおよび/または誘発する小胞は、非標的細胞、たとえば単球、マクロファージ、赤血球、破骨細胞、肥満細胞、脂肪細胞、および幹細胞、たとえば間葉系幹細胞のいずれか由来の条件培地から単離することができる。小胞は、増殖因子などのような他の生体分子と混合することができる。細胞外小胞のサイズは、20〜400nmの範囲、たとえば20nm以上または50nm以上または80nm以上または100nm以上または400nm以下または300nm以下または250nm以下または200nm以下または150nm以下であってもよい。図1は、条件培地から単離されたエキソソームを明らかにする。
一実施形態において、単離EVが、2つ以上の異なる細胞型から放出されたEVの組み合わせである。他の実施形態において、単離EVが、2つ以上の異なるタイプの刺激剤を使用して刺激された細胞から放出されたEVの組み合わせである。他の実施形態において、単離EVが、2つ以上の異なる細胞型から放出されたEVの組み合わせであり、それぞれの細胞型が、少なくとも1つの異なるタイプの刺激剤を使用して刺激される。
分化を担うサイトカイン、増殖因子、もしくは他のシグナル物質または物質の組み合わせは、まだ完全には決定されていない。サイトカイン、増殖因子、および他のシグナル物質はまた、たとえば特異的な表現型および/または機能を有する細胞外小胞を放出するように、非標的性細胞を刺激するために使用されてもよい。他のシグナル物質は、たとえばホルモンとすることができる。可能性のあるサイトカインは、IL−1、IL−2、IL−3、IL−4、IL−5、IL−6、IL−7、IL−8、IL−9、IL−10、IL−11、IL−12、IL−13、IL−14、IL−15、IL−16、IL−17、IL−18、Il−19、IL−20、IL−21、IL−22、IL−23、IL−24、IL−25、IL−26、IL−27、IL−28、IL−29、IL−30、IL−31、IL−32、IL−33、IL−34、IL−35、もしくはIFN型またはその組み合わせである。可能性のある増殖因子は、BMP、TGF、VEGF、TNF、もしくはFGFまたはその組み合わせである。ケモカインの例は、CCL 2、CCL 3、CCL 5、CCL 7、CCL 8、CCL11、CCL 13、CCL 17、CCL 22、CCL24、CCL26、CCR1、CCR2、CCR3、CCR4、CCR5、またはその組み合わせなどのような、型CC、CXC、CX3C、およびXCのいずれか1つとなるであろう。他のシグナル物質は、たとえばホルモンとすることができる。
小胞は、他のタンパク質、増殖因子(BMP、TGF、VEGF、TNF、もしくはFGFまたはその組み合わせ)、mRNA、miRNA、またはsiRNAもしくは他の小さな調節性RNAなどのような他の物質を含む。
一実施形態において、非標的性細胞が、リポ多糖(LPS)、サイトカイン、ケモカイン、増殖因子(BMP、TGF、VEGF、TNF、もしくはFGFまたはその組み合わせ)、または任意の他の刺激薬またはその組み合わせを使用して、タンパク質、増殖因子(BMP、TGF、VEGF、TNF、もしくはFGFまたはその組み合わせ)、mRNA、miRNA、またはsiRNAもしくは他の小さな調節性RNAまたはその組み合わせを含有する細胞外小胞を放出するように、刺激される。
他の実施形態において、非標的性細胞が、リポ多糖(LPS)、サイトカイン、ケモカイン、増殖因子(BMP、TGF、VEGF、TNF、もしくはFGFまたはその組み合わせ)、または任意の他の刺激薬またはその組み合わせを使用して、タンパク質、増殖因子(BMP、TGF、VEGF、TNF、もしくはFGFまたはその組み合わせ)、mRNA、miRNA、またはsiRNAもしくは他の小さな調節性RNAまたはその組み合わせを含有する細胞外小胞を放出するように、刺激される。次いで、これらの小胞は、リポ多糖(LPS)、サイトカイン、ケモカイン、増殖因子、もしくは任意の他の刺激薬またはその組み合わせと組み合わせて、標的細胞に追加されるまたはそれと接触させられる。
本発明者らは、MSCおよび単球の両方が、RNAを含有する細胞外小胞を放出することを示し、図1〜8、また、本発明者らはまた、標的MSCが、放出された細胞外小胞を取込むことをも示した、図9〜10。本発明者らはまた、RUNX2およびBMP−2の遺伝子発現の増加によって例証されるように、hMSCを本発明に従って処理した場合に、骨形成分化が促進されたことをも示した(図12)。
細胞外小胞は、PBSバッファーまたは任意の他の食塩水バッファーまたは任意の他の培地などのような細胞培養培地(または調整培地)と混合することができる。培地は、2つ以上のタイプの非標的細胞、たとえば2つ、3つ、または4つの細胞型由来の小胞を含有してもよい。たとえば、培地は、単球およびhMSCまたは単球、hMSC、およびマクロファージ由来の小胞の混合物を含有してもよい。細胞外小胞は、インビトロおよびインビボの両方において、標的細胞に提供されてもよい。
非標的の細胞培養由来の条件培地または単離細胞外小胞は、骨再生が必要とされる部位に追加することができる。条件培地または小胞はまた、標的細胞と一緒に送達することもできる。標的細胞が位置する部位に培地または小胞を送達することによって、骨形成分化が誘発されるであろう。送達は、送達ビヒクルの注射によってまたは移植を通して行うことができる。エキソソームなどのような細胞外小胞は、たとえば合成のリポソームと比較して、中程度の免疫応答しか引き起こさないまたは免疫応答を全く引き起こさないという有益性を有する。
細胞外小胞は、骨形成分化を誘発するおよび/または促進するのに十分な量で、標的細胞に追加されるまたはそれと接触させられる。
さらに、小胞は、表面上に、たとえばインプラント表面上に小胞をコーティングするもしくは固定することによってまたは薬剤送達系の一部として、幹細胞に提供されてもよい。インプラント表面は、チタンもしくは酸化チタンなどのような金属表面またはリン酸カルシウム表面などのようなセラミック表面とすることができる。薬剤送達系は、たとえば、小胞をゆっくり放出するヒドロゲルまたは生分解性物質とすることができる。ヒドロゲルは、たとえばヒアルロン酸またはキトサンまたはポリビニルアルコールまたはその組み合わせとすることができる。他の実施形態において、インプラント表面が、細胞外小胞のインビボにおける放出のために、細胞でコーティングされるまたは固定される。たとえば、表面は、インプラントの部位で骨形成分化を誘発するおよび/または促進するために、数が増加したエキソソームを放出するであろう刺激単球、マクロファージ、または間葉系幹細胞でコーティングされてもよいまたは固定されてもよい。
本発明による方法はまた、患者を治療するために使用されてもよい。方法は、
−ヒト、たとえば患者彼自身から、任意の利用可能な適した技術を使用して、血液または組織サンプルを収集するステップと、
−促進するおよび/または誘発する細胞外小胞を産生するために、非標的細胞を単離し、細胞を培養し、任意選択で、非標的細胞を刺激するステップと、
−非標的細胞によって産生された前記細胞外小胞を単離するステップと、
−細胞外小胞を患者に投与するステップと、を含む。
−ヒト、たとえば患者彼自身から、任意の利用可能な適した技術を使用して、血液または組織サンプルを収集するステップと、
−促進するおよび/または誘発する細胞外小胞を産生するために、非標的細胞を単離し、細胞を培養し、任意選択で、非標的細胞を刺激するステップと、
−非標的細胞によって産生された前記細胞外小胞を単離するステップと、
−細胞外小胞を患者に投与するステップと、を含む。
投与は、全身的にまたは局所的に、任意の適した技術によって、たとえば注射器によって、骨形成分化が必要とされるまたは求められる位置に対して実行されてもよい。
本発明は、骨手術、インプラント手術、骨治癒治療、または骨もしくは歯の修復治療の間の補足の治療として使用することができる。単離細胞外小胞は、歯などのような歯科用の適用のためのインプラント、股関節または膝または任意の他の骨インプラントなどのような、様々な足場およびインプラント上に固定することができる。小胞はまた、ねじまたは修復プレートなどのような骨修復インプラント上に固定することもできる。さらに、本発明は、骨空隙充填物質、骨増殖体、頭蓋骨癒合症、変形性関節症、様々な骨炎疾患、大理石骨病、骨減少症、骨粗しょう症、または骨形成などのような、様々な骨関連性の疾患および損傷を治療するために使用することができる。
実施例1
プロセスについての一般的な説明
単球の単離および培養:単球は、磁気分離を使用してヒト血液から単離し、異なるバイオマテリアル上で、刺激(たとえばLPS)ありまたはなしで培養する。間葉系幹細胞は、勾配分離によってヒト骨髄から得る。72時間後、細胞を収集し、エキソソームを条件培地から単離する。
プロセスについての一般的な説明
単球の単離および培養:単球は、磁気分離を使用してヒト血液から単離し、異なるバイオマテリアル上で、刺激(たとえばLPS)ありまたはなしで培養する。間葉系幹細胞は、勾配分離によってヒト骨髄から得る。72時間後、細胞を収集し、エキソソームを条件培地から単離する。
エキソソーム単離および検出:エキソソームは、繰り返しの遠心分離およびろ過のステップに基づく方法を使用して、細胞デブリ、アポトーシス小体などを除去し、その後、超遠心分離を使用して、エキソソームをペレットにして、単離する。代替の単離方法もまた、使用されてもよい。エキソソームは、電子顕微鏡観察ならびにフローサイトメトリーおよびウェスタンブロットを使用する、エキソソーム上でよく見つけられる多くのマーカー(たとえばCD9、CD63、CD81、Tsg101)およびエキソソームに不在であるはずである多くのマーカー(カルネキシン)についての検出を含む方法の組み合わせを使用して検出する。
エキソソームのmRNAおよびマイクロRNAの含有量:マイクロアレイは、mRNAおよびマイクロRNAの含有量を評価するために、異なる刺激に曝露された単球およびMSC由来のエキソソームに対して実行する。
取込み実験:単離エキソソームに蛍光色素を標識し、培養中のMSCに追加し、取込みを、様々な時点の後に、蛍光顕微鏡観察およびフローサイトメトリーを使用して分析した。
骨形成の評価:組織学的染色(フォン コッサ)および骨形成についてのマーカー(オステオカルシン、runx2、コラーゲンI型)をRT−PCRを使用して評価する。
材料&方法
ヒト単球は、磁気分離によってバフィーコートから得た(純度90〜95%、n=4)。単球をLPS(10ng/ml)により72時間処理し、条件培地(CM)を収集した。ヒト脂肪由来間葉系幹細胞(MSC)を培養し、条件培地を収集した。エキソソームを繰り返しの遠心分離およびろ過のステップによってCMから単離し、フローサイトメトリーを使用して検出した。フローサイトメトリー分析については、エキソソームを抗CD63ラテックスビーズにコンジュゲートし、テトラスパニンCD9、CD63、およびCD81に対して免疫染色した。エキソソームはまた、透過型電子顕微鏡観察およびナノ粒子トラッキング分析を使用して視覚化した。様々なタイプの小胞およびそれらのドナー細胞由来のRNAを抽出し、サイズ分布パターンをバイオアナライザーを使用して分析した。hMSCは、単球エキソソームを補足した培地、CM、またはコントロール培地において72時間、培養した。骨形成分化を、リアルタイムPCR分析を使用して評価した(Runx2、BMP−2、n=4)。標的遺伝子発現の相対的な定量化について、dd−Ct法によって計算した。別々の実験において、ヒト単球またはhMSCを、PKH67染色小胞を補足した培地において培養し、取込みを、フローサイトメトリーおよび顕微鏡観察を使用して検査した。
ヒト単球は、磁気分離によってバフィーコートから得た(純度90〜95%、n=4)。単球をLPS(10ng/ml)により72時間処理し、条件培地(CM)を収集した。ヒト脂肪由来間葉系幹細胞(MSC)を培養し、条件培地を収集した。エキソソームを繰り返しの遠心分離およびろ過のステップによってCMから単離し、フローサイトメトリーを使用して検出した。フローサイトメトリー分析については、エキソソームを抗CD63ラテックスビーズにコンジュゲートし、テトラスパニンCD9、CD63、およびCD81に対して免疫染色した。エキソソームはまた、透過型電子顕微鏡観察およびナノ粒子トラッキング分析を使用して視覚化した。様々なタイプの小胞およびそれらのドナー細胞由来のRNAを抽出し、サイズ分布パターンをバイオアナライザーを使用して分析した。hMSCは、単球エキソソームを補足した培地、CM、またはコントロール培地において72時間、培養した。骨形成分化を、リアルタイムPCR分析を使用して評価した(Runx2、BMP−2、n=4)。標的遺伝子発現の相対的な定量化について、dd−Ct法によって計算した。別々の実験において、ヒト単球またはhMSCを、PKH67染色小胞を補足した培地において培養し、取込みを、フローサイトメトリーおよび顕微鏡観察を使用して検査した。
結果
フローサイトメトリー分析は、LPS刺激単球およびMSCが、エキソソーム検出のためによく使用されるマーカーであるテトラスパニンCD9、CD63、およびCD81についてポジティブなエキソソームを放出することを明らかにした。図2および5を参照されたい。
フローサイトメトリー分析は、LPS刺激単球およびMSCが、エキソソーム検出のためによく使用されるマーカーであるテトラスパニンCD9、CD63、およびCD81についてポジティブなエキソソームを放出することを明らかにした。図2および5を参照されたい。
図11は、単球/マクロファージ由来のエキソソームが、間葉系幹細胞に取込まれる/付着することを明らかにする。緑色PKH67染色エキソソームの存在下において培養したMSCは、ネガティブコントロールと比較して、FL−1においてポジティブであり、エキソソームがMSCに付着するもしくはそれと融合するまたはMSCによって内部移行されることを示す。さらに、PKH67標識緑色MSCエキソソームを補足した培地におけるhMSCの培養は、MSCが緑色色素についてポジティブであることを示し、MSCがエキソソームを介して他のMSCと連絡することを示唆する。図10を参照されたい。そのうえ、緑色MSCエキソソームとの単球の培養はまた、単球の一部分が緑色エキソソームを取込んだまたは内部移行したことをも明らかにした。図9を参照されたい。
単球CMまたはCMから単離した純粋なエキソソームを補足した培地における72時間のhMSCの培養は、Runx2(それぞれ1.7±0.3および1.4±0.2倍の変化)ならびにBMP−2(それぞれ15.4±1.7および2.3±0.3倍の変化)の発現レベルの有意な増加をコントロール培地と比較してもたらした。図12を参照されたい。
結果は、LPS刺激ヒト単球が、間葉系幹細胞の骨形成分化を増強する因子を放出することおよびこの効果の少なくとも一部がエキソソームを介しての連絡によるものであることを実証する。
実施例2
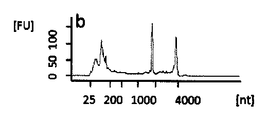
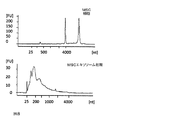
ヒト初代LPS刺激単球。エキソソームを3日間の培養の後に単離し、RNAを抽出した。細胞およびエキソソームの全RNAおよび小型RNAのBioanalyzer分析を実行した。電気泳動図、図4は、(a)エキソソームおよび細胞(b)における全RNAならびにエキソソーム(c)および細胞(d)における小型RNAのヌクレオチドにおけるサイズ分布(nt)ならびに蛍光強度(FU)を示す。
ヒト初代LPS刺激単球。エキソソームを3日間の培養の後に単離し、RNAを抽出した。細胞およびエキソソームの全RNAおよび小型RNAのBioanalyzer分析を実行した。電気泳動図、図4は、(a)エキソソームおよび細胞(b)における全RNAならびにエキソソーム(c)および細胞(d)における小型RNAのヌクレオチドにおけるサイズ分布(nt)ならびに蛍光強度(FU)を示す。
Claims (20)
- 標的細胞の骨形成分化を誘発するおよび/または促進するための方法において、
a.非標的細胞から放出された、骨形成分化を誘発するおよび/または促進する単離細胞外小胞を提供するステップと、
b.前記細胞外小胞を前記標的細胞に追加するステップと、を含むことを特徴とする方法。 - 請求項1に記載の方法において、前記非標的細胞が、刺激単球、マクロファージ、もしくは間葉系幹細胞または他の炎症細胞もしくは非炎症細胞であることを特徴とする方法。
- 請求項2に記載の方法において、前記非標的細胞が、リポ多糖、サイトカイン、ケモカイン、または任意の他の刺激薬により刺激されることを特徴とする方法。
- 請求項2に記載の方法において、前記非標的細胞が、間葉系幹細胞の骨形成分化を促進するおよび/または誘発する細胞外小胞を放出するように、任意の他の方法によって刺激されるまたは修飾されることを特徴とする方法。
- 請求項1乃至4の何れか一項に記載の方法において、前記細胞外小胞が、単球から放出されることを特徴とする方法。
- 請求項1乃至4の何れか一項に記載の方法において、提供される前記小胞が、2つ以上の異なるタイプの細胞から放出された小胞の組み合わせであるまたは2つ以上の異なるタイプの刺激剤を使用して刺激された細胞から放出された小胞の組み合わせであるまたは2つ以上の異なる細胞型から放出されたEVの組み合わせであって、それぞれの細胞型が、少なくとも1つの異なるタイプの刺激剤を使用して刺激される、EVの組み合わせであることを特徴とする方法。
- 請求項1乃至6の何れか一項に記載の方法において、前記細胞外小胞が、エキソソームであることを特徴とする方法。
- 標的細胞の骨形成分化のための、非標的細胞由来の、単離された、骨形成分化を促進するおよび/または誘発する細胞外小胞の使用。
- 請求項8に記載の小胞において、前記非標的細胞が、刺激単球、マクロファージ、もしくは間葉系幹細胞または他の炎症細胞もしくは非炎症細胞であることを特徴とする小胞。
- 請求項9に記載の小胞において、前記非標的細胞が、リポ多糖、サイトカイン、ケモカイン、または任意の他の刺激薬により刺激されることを特徴とする小胞。
- 請求項8乃至10の何れか一項に記載の小胞において、前記小胞が、エキソソームであることを特徴とする小胞。
- 請求項8乃至11の何れか一項に記載の小胞において、前記小胞が、培地中に懸濁されることを特徴とする小胞。
- 骨形成分化を誘発するおよび/または促進する細胞外小胞に曝露されたコーティングを含むことを特徴とするインプラント。
- 骨形成分化を誘発するおよび/または促進する細胞外小胞を産生することができる、固定され刺激された単球、マクロファージ、または間葉系幹細胞のコーティングを含むことを特徴とするインプラント。
- 請求項13または14に記載のインプラントにおいて、前記インプラントが、歯科用の適用、股関節、膝、ねじ、または修復プレートのためのインプラントであることを特徴とするインプラント。
- 請求項8乃至12の何れか一項に記載の使用において、損傷、骨粗しょう症、骨形成の治療のためのまたは骨修復におけることを特徴とする使用。
- 骨損傷、骨空隙充填物質、骨増殖体、頭蓋骨癒合症、変形性関節症、様々な骨炎疾患、骨粗しょう症、または骨形成の治療のための、単離された、骨形成分化を促進するおよび/または誘発する細胞外小胞を含むことを特徴とする組成物。
- 単離された、骨形成分化を促進するおよび/または誘発する細胞外小胞を含むことを特徴とする骨空隙充填剤。
- 請求項18に記載の骨空隙充填剤において、標的性幹細胞をさらに含むことを特徴とする骨空隙充填剤。
- 患者を治療するための方法において、血液または組織サンプルを前記患者から収集するステップと、非標的細胞を単離するステップと、前記非標的細胞を培養し、かつ刺激するステップと、前記非標的細胞によって産生された細胞外小胞を単離するステップと、前記細胞外小胞を前記患者に投与するステップと、を含むことを特徴とする方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SE1250477 | 2012-05-10 | ||
| SE1250477-5 | 2012-05-10 | ||
| PCT/SE2013/050526 WO2013169202A1 (en) | 2012-05-10 | 2013-05-10 | Osteogenic differentiation of mesenchymal stem cells |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2015523058A true JP2015523058A (ja) | 2015-08-13 |
Family
ID=49551066
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015511419A Pending JP2015523058A (ja) | 2012-05-10 | 2013-05-10 | 間葉系幹細胞の骨形成分化 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20150093363A1 (ja) |
| EP (1) | EP2847320A4 (ja) |
| JP (1) | JP2015523058A (ja) |
| CN (1) | CN104487569A (ja) |
| WO (1) | WO2013169202A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022531846A (ja) * | 2020-05-25 | 2022-07-12 | シーケイ-エクソジーン カンパニー リミテッド | 間葉系幹細胞由来のエキソソーム生産方法およびこれから製造された培養液 |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10865383B2 (en) | 2011-07-12 | 2020-12-15 | Lineage Cell Therapeutics, Inc. | Methods and formulations for orthopedic cell therapy |
| US20160120805A1 (en) * | 2013-06-05 | 2016-05-05 | The Trustees Of Columbia University In The City Of New York | Exosomes for orofacial diagnostics and therapeutics |
| WO2016157142A1 (en) * | 2015-04-02 | 2016-10-06 | Stegi-Ra Trust | Composition for use in treating celiac disease |
| CA2988778A1 (en) * | 2015-06-09 | 2016-12-15 | Orthocyte Corporation | Osteogenic graft forming unit |
| WO2016203414A1 (en) * | 2015-06-16 | 2016-12-22 | Fondazione Città Della Speranza - Onlus | Extracellular vesicles derived from osteoblastic lineage cells for therapeutic and diagnostic use |
| WO2016210256A1 (en) * | 2015-06-25 | 2016-12-29 | The University Of Florida Research Foundation, Inc. | Conductive nonwoven mat and method of using the conductive nonwoven mat |
| WO2017189842A1 (en) * | 2016-04-27 | 2017-11-02 | The Scripps Research Institute | Extracellular vesicles from young stem cells or serum for age-related therapies |
| CN106047802B (zh) * | 2016-06-15 | 2019-07-02 | 北京大学口腔医院 | 一种促进间充质干细胞成骨分化的材料及其制备方法和应用 |
| FR3055805B1 (fr) * | 2016-09-09 | 2020-05-15 | Assistance Publique - Hopitaux De Paris (Ap-Hp) | Biomateriau a usage therapeutique |
| WO2018115871A1 (en) * | 2016-12-20 | 2018-06-28 | The University Of Birmingham | Composition and method for bone production |
| CN108324735B (zh) * | 2017-01-20 | 2024-02-09 | 李莉 | 用于疾病治疗的胞外体制剂及其应用 |
| KR20190011213A (ko) * | 2017-07-24 | 2019-02-01 | 한양대학교 에리카산학협력단 | 줄기세포로부터 추출된 엑소좀을 유효성분으로 포함하는 골다공증 예방 또는 치료용 조성물 |
| EP3801589A4 (en) * | 2018-06-01 | 2022-03-02 | Memorial Sloan Kettering Cancer Center | METHODS AND COMPOSITIONS FOR THE TREATMENT OF OSTEOPETROSIS |
| EP3866816A4 (en) * | 2018-10-18 | 2022-07-20 | NantBio, Inc. | EXOSOMES FROM MESENCHYMATOUS STEM CELLS AND METHODS |
| CN109568665B (zh) * | 2018-12-28 | 2021-12-10 | 中国医科大学附属第一医院 | 负载脂肪干细胞外泌体的温敏型可注射水凝胶及其制备方法和应用 |
| CN112175899A (zh) * | 2019-07-04 | 2021-01-05 | 陕西佰傲干细胞再生医学有限公司 | 间充质干细胞成骨定向分化诱导液及其应用 |
| CN110951685A (zh) * | 2019-10-28 | 2020-04-03 | 天津市康婷生物工程集团有限公司 | 一种应用于间充质干细胞成骨分化的单核细胞源外泌体制剂 |
| WO2022055238A1 (ko) * | 2020-09-09 | 2022-03-17 | 주식회사 셀렉소바이오 | 경막외 지방 중간엽 줄기세포 유래 엑소좀을 포함하는 골 질환 치료용 조성물 |
| CN112190596A (zh) * | 2020-09-14 | 2021-01-08 | 陕西佰傲干细胞再生医学有限公司 | 一种用于治疗关节炎的间充质干细胞制剂及其制备方法 |
| CN113440653B (zh) * | 2021-07-01 | 2022-08-05 | 山西医科大学口腔医院 | 一种促进骨结合的钛基种植体及其制备方法和应用 |
| CN114591905B (zh) * | 2022-04-01 | 2022-09-02 | 北京大学口腔医学院 | 一种人红细胞制备凋亡囊泡的方法与应用 |
| WO2023212637A1 (en) * | 2022-04-29 | 2023-11-02 | CryoHeart Laboratories, Inc. | Systems, methods, and devices of exosome delivery for filling bone fracture voids |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8409847B2 (en) * | 2000-10-06 | 2013-04-02 | ICE Development Technologies, LLC | System and method for controlling the diameter of a mammilian hybrid coronary bypass graft |
| ES2444090T3 (es) * | 2001-01-18 | 2014-02-24 | Georg Watzek | Fármaco para fomentar la regeneración de tejidos |
| WO2009087361A1 (en) * | 2008-01-04 | 2009-07-16 | Lydac Neuroscience Limited | Microvesicles |
| CN101636041B (zh) * | 2008-07-24 | 2011-05-11 | 富葵精密组件(深圳)有限公司 | 基板表面平坦化系统及基板表面平坦化方法 |
| CN102232970A (zh) * | 2010-04-22 | 2011-11-09 | 董运海 | 一种治疗骨损伤细胞注射剂及其制备方法 |
| WO2012020307A2 (en) * | 2010-08-13 | 2012-02-16 | The University Court Of The University Of Glasgow | Therapeutic uses of microvesicles and related micrornas |
-
2013
- 2013-05-10 US US14/398,896 patent/US20150093363A1/en not_active Abandoned
- 2013-05-10 CN CN201380028009.7A patent/CN104487569A/zh active Pending
- 2013-05-10 EP EP13786931.9A patent/EP2847320A4/en not_active Withdrawn
- 2013-05-10 WO PCT/SE2013/050526 patent/WO2013169202A1/en active Application Filing
- 2013-05-10 JP JP2015511419A patent/JP2015523058A/ja active Pending
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022531846A (ja) * | 2020-05-25 | 2022-07-12 | シーケイ-エクソジーン カンパニー リミテッド | 間葉系幹細胞由来のエキソソーム生産方法およびこれから製造された培養液 |
| US11879138B2 (en) | 2020-05-25 | 2024-01-23 | Ck-Exogene Co., Ltd. | Method for preparing mesenchymal stem cell-derived exosomes and culture solution produced from the same |
| JP7449590B2 (ja) | 2020-05-25 | 2024-03-14 | シーケイ-エクソジーン カンパニー リミテッド | 間葉系幹細胞由来のエキソソーム生産方法およびこれから製造された培養液 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2013169202A1 (en) | 2013-11-14 |
| EP2847320A4 (en) | 2015-12-30 |
| US20150093363A1 (en) | 2015-04-02 |
| EP2847320A1 (en) | 2015-03-18 |
| CN104487569A (zh) | 2015-04-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2015523058A (ja) | 間葉系幹細胞の骨形成分化 | |
| Daneshmandi et al. | Emergence of the stem cell secretome in regenerative engineering | |
| Soares et al. | Biological analysis of simvastatin-releasing chitosan scaffold as a cell-free system for pulp-dentin regeneration | |
| Li et al. | Exosomes from adipose-derived stem cells regulate M1/M2 macrophage phenotypic polarization to promote bone healing via miR-451a/MIF | |
| Zhang et al. | Electrical stimulation of adipose‐derived mesenchymal stem cells and endothelial cells co‐cultured in a conductive scaffold for potential orthopaedic applications | |
| Zhou et al. | Effect of tetrahedral DNA nanostructures on proliferation and osteo/odontogenic differentiation of dental pulp stem cells via activation of the notch signaling pathway | |
| Wu et al. | MicroRNA functionalized microporous titanium oxide surface by lyophilization with enhanced osteogenic activity | |
| Gholami et al. | Extracellular vesicles in bone and periodontal regeneration: current and potential therapeutic applications | |
| Shen et al. | Titania nanotubes promote osteogenesis via mediating crosstalk between macrophages and MSCs under oxidative stress | |
| Bao et al. | The role and therapeutic potential of MSC-derived exosomes in osteoarthritis | |
| Qiao et al. | Magnesium-doped nanostructured titanium surface modulates macrophage-mediated inflammatory response for ameliorative osseointegration | |
| Shen et al. | Applications of biomaterials for immunosuppression in tissue repair and regeneration | |
| Jiang et al. | Bone response to the multilayer BMP‐2 gene coated porous titanium implant surface | |
| Cui et al. | A pilot study of macrophage responses to silk fibroin particles | |
| Wu et al. | Chitosan-miRNA functionalized microporous titanium oxide surfaces via a layer-by-layer approach with a sustained release profile for enhanced osteogenic activity | |
| Hosseinpour et al. | Modulating osteoimmune responses by mesoporous silica nanoparticles | |
| ES2385450T3 (es) | Células madre mesenquimatosas y sus utilizaciones | |
| Xie et al. | Regulation of cellular behaviors of fibroblasts related to wound healing by sol–gel derived bioactive glass particles | |
| Xiao et al. | Osteoimmunomodulation role of exosomes derived from immune cells on osseointegration | |
| Zhao et al. | Improvement of bone formation by bionic hydroxyapatite nanorod via the regulation of macrophage polarization | |
| Zhu et al. | Exosomes derived from mesenchymal stromal cells promote bone regeneration by delivering miR-182–5p-inhibitor | |
| Zhang et al. | A n in vitro investigation of the marked impact of dendritic cell interactions with bone grafts | |
| Cha et al. | Generation of bioactive MSC-EVs for bone tissue regeneration by tauroursodeoxycholic acid treatment | |
| Ren et al. | MSC-Exos: Important active factor of bone regeneration | |
| Wang et al. | MicroRNA-loaded biomaterials for osteogenesis |