関連する出願の相互参照
本出願は、2011年10月3日に出願されたアメリカ合衆国仮特許出願シリアル番号第61/542,678号の恩恵と優先権を主張するものであり、その開示内容全体が参考としてこの明細書に含まれている。
本発明は、分析物に対する貴金属の反応の分野、特にグルコースと反応するように設計したバイオセンサーと、そのバイオセンサーを製造する方法に関する。
人体が機能するには、さまざまな化学物質の極めて微妙なバランスのもとで処理、輸送、代謝が行なわれる必要がある。人体内でカギとなる代謝産物のレベルは、身体の諸器官が正常に働くことによってのみ、既知の生理学的範囲内に適切に維持される。そうした既知の化学物質の濃度が予想される範囲からたびたび変化するのは、一般に病気の兆候である。
運動不足があり、さらに加工食品の不健康な摂取が多くの家庭の通常の健康的な食品に取って代わっている現代社会において、急速に増えているありふれた病気は糖尿病である。糖尿病は、単純に、膵臓におけるインスリンの産生が不十分である(またはない)結果として、または場合によってはインスリン抵抗性により、血糖値が上昇しているという特徴を持つ。実際、身体の血中化学物質は、定期的にそのような化学物質の正常範囲から外れる。
国際糖尿病連盟によれば、世界中に現在2.46億人の糖尿病患者がおり、その数は2025年までに3.8億人に達すると予想されている。多くの場合、慢性糖尿病でさえ、身体の機能を正しくモニタし、適切なときにグルコース(またはインスリン)を身体に供給する限りは十分に制御可能な疾患である。しかし身体の要求に正しく応えるには、身体のその要求を明らかにする必要がある。糖尿病患者の現在の血中化学物質を明らかにするため、彼らは血液から定期的にサンプルを採取し、化学分析を行なってグルコースが過剰(または不足)であるかどうかを調べる。グルコースの過剰が検出された場合には、インスリンを(特別な注射によって、または設置したポンプを通じて、または他の手段で)患者の血流に添加してグルコースのレベルを正常範囲に戻すよう試みることができる。同様に、血中グルコースのレベルが低すぎる場合には、その人は炭水化物を摂取してそのレベルを正常範囲に再び戻すことができる。
血中化学物質は外部から調節できるため、糖尿病は一般に制御可能であると見なされているが、制御されていない糖尿病の効果は、短期間でさえ、悲劇的になる可能性がある。糖尿病は一般に血管と神経にダメージを与えるため、多くの糖尿病患者は、非常に進行するまで存在が認識されることのない損傷に苦しみ、侵襲性で人生を変えてしまう治療(四肢の切断)が必要となる可能性がある。糖尿病の制御に失敗するとより重大な合併症(例えば腎不全、失明、脳損傷、心筋梗塞、死)になる可能性もある。上記のことから明らかなように、このように常時厳しく制御するための前提条件は、血中グルコースのレベルを正確かつ頻繁にモニタすることである。というのも、そうすることで治療計画(すなわちインスリンの用量)がわかるとともに、あらゆる不均衡を迅速に正すことで、生じるダメージを最小にできるからである。
血糖値を定期的にモニタする必要があるため、血中グルコースの量を正確に測定できる製品が非常に強く望まれている。そのような装置は一般にグルコース計と呼ばれており、最新のものは、本人に一滴の血液(指先から得られることが多い)を採取してもらってそれをグルコースと反応するストリップの上に置くことによって動作する。すると反応の量が検出され、グルコース計は、血液中のグルコースのレベルを示す。そこで糖尿病患者は食物を摂取するかインスリンを用いて不均衡を正す。明らかなように、使い捨てバイオセンサー用ストリップを用いて血液を一日に何回も試験する必要があるため、ストリップが大量に必要となる。
試験ストリップの形態になった使い捨てグルコース・バイオセンサーは、一般に、似た構成パターンに従う。試験ストリップは、一般に、酵素(グルコースオキシダーゼまたはグルコースデヒドロゲナーゼであることが多い)と、メディエータ(フェリシアン化物であることが多い)と、インディケータと、多くの追加成分を、基板上に配置された複数の乾燥層の形態で含んでいる。次にこれら乾燥層を2つ以上の電極と化学的に接触させる。電極は、グルコース計の中で電気的に接続されている。
試験ストリップの測定法は、一般に、測光法と電気化学法である。どちらの方法でも似た設計の検出領域が使用される。測光システムでは、測定は、LEDからの狭い範囲の波長の光束を用いて反応するサンプルに光を照射することによってなされる。散乱反射光の一部が光検出器に到達して電流に変換される。
より一般的な電流測定システムでは、測定で反応生成物を再び酸化した形態に変換する。この反応は、試験ストリップ上の電極の表面で起こるため、還元された化学物質を表面に輸送し、酸化されたメディエータをその表面から追い出すのに拡散が必要とされる。原則として、これは、測光法における瞬時の観察と比べて遅いプロセスである。しかし反応は数秒以下で終了させることができるため、実現するのがよりロバストでより簡単であることがしばしばある。
電気化学的測定の品質は、乾燥化学物質と測定法(その中に評価アルゴリズムが含まれる)の間の密な協力の結果である。電気化学用試験ストリップの設計は非常に多彩なものにすることができ、特に、試薬および血液サンプルと接触させるのに用いる電極の数と、ストリップから測定値を得る方法はさまざまである。しかしたいていの試験ストリップでは、グルコース計の具体的な設計から生じる設計上の制約の範囲内でさえ、同じ一般原則を利用する。
一般に、試験ストリップでは、酵素(グルコースオキシダーゼ)がグルコースの酸化を触媒し、グルコースをグルコノラクトンと酸化還元補因子にする。その後グルコノラクトンは加水分解されてグルコン酸になる。加水分解は、電子をグルコースからメディエータ(フェリシアン化物)に移動させるのに役立ち、このようにして輸送されたグルコースの各分子につき既知量のインディケータ(フェロシアン化物)が生成する。試薬層の中でフェリシアン化物からフェロシアン化物に還元されることで酵素が再び酸化される。
どの場合でも、グルコースのレベルに関する測定電流、したがって較正値は、試験ストリップ中の作用電極の面積に比例する。作用電極は、血中グルコースの量に比例した電気化学反応が起こる電極である。
補助電極は、作用電極が血中グルコースのレベルを正確に測定できるよう、適切に機能せねばならない。実際、補助電極では、作用電極で反応が続くよう、逆反応が起こらねばならない。これらの電極は一般に1つ以上の基板の上に配置された後、乾燥成分(とおそらくは追加基板)を用いて合体されて試験ストリップを形成する。図1は、反応がどのようにして起こり、グルコース・レベルの電気化学的測定が、フェリシアン化物の還元中に生成するフェロシアン化物の消費量に基づいてどのようになされるかのブロック・ダイヤグラムを示している。
システムの電極に電位を印加した後、電流を測定する。補助電極の電位は、電極表面におけるフェリシアン化物とフェロシアン化物の比によって決まる。印加する電位は、拡散によって制限される電流を作用電極に供給するため、フェロシアン化物の濃度を二電流測定によって求めることができる。計測器は作用電極の電流を測定する。この電流はフェロシアン化物の濃度に比例するため、グルコースの濃度と直接関係している。一般に試験ストリップとグルコース計に固有のアルゴリズムを使用してグルコースの濃度を明らかにし、ユーザーに知らせることができる。
この測定法の1つの利点は、試験ストリップの構造中の両方の電極を同じ金属にできることである。すると構成が簡単になる。具体的には、電極と基板を大きなロールその他の構造体の中に形成し、それを試験ストリップで使用するための望ましい構造体に切断することができる。どちらが作用電極、補助電極になるかの選択は、単純に、得られる試験ストリップの中での位置によって決まり、一実施態様では2つの電極は実質的に同じである。
メディエータであるフェリシアン化物は、両方の電極で同じように反応する必要がある。したがって構造を簡単にするため両方の電極で同じ材料(と構成)にすることが有利である。現在あるたいていのグルコース計では、電極として機能するよう、金などの貴金属を市販されている一般に最も純粋な形態にして覆ったプラスチック基板が用いられる。
メディエータから電極の表面への電子の輸送と、作用電極上へのフェロシアン化物の拡散速度に関し、基板上の被覆の品質とその活性が、血中グルコースのレベルの正確な測定に重要な役割を果たす。具体的には、電極上にフェロシアン化物を正確に拡散させることができると、フェロシアン化物分子のカウント数、したがってグルコースの量が正確になる。カウント数がより正確になるほど、電極の位置におけるセンサーの感度が増大する。
さらに、グルコース計は、分子の数を直接測定するのではなく、電気化学的特性を測定しているため、ストリップは、電位の測定値とグルコース濃度の間の関係が安定したものになるような電気的特性を持つことも重要である。多くの点において、読み取り値の安定性は、アルゴリズムによってグルコース濃度を求めるとき、読み取り値の生の感度よりも重要とは言わないまでも、それと同じくらい重要である。電位の読み取り値が安定していると、感度が低下する場合でさえ、結果がより安定したものになり、したがってより正確になる。
試験ストリップの読み取り値の安定性に関する1つの懸念は、元の(または完成した)試験ストリップの製品または成分の経時変化である。ストリップは化学的に反応性を持つように設計されているため、ストリップで用いる材料は時間が経過すると化学組成が変化する可能性があり、その結果としてその電気的特性が変化する可能性があるため、得られる出力測定が変化する可能性がある。計測器がストリップの経時変化を考慮する(または判断する)ことは一般に不可能であるため、試験ストリップの製造者は、(例えば使用期限を印字することで)実質的に古くなったストリップを使わないよう勧める以外、店舗または最終ユーザーの元での製品の保管期間を正確に制御することは不可能であることがわかるはずである。さらに、販売前に確実に一定のレベルまで経時変化しているようにするため、使用前に強制的にある待機期間だけ保管しておくのは非効率的である。
ある種の純粋な(またはほぼ純粋な)貴金属電極(例えばパラジウム)では、時間経過とともに金属が酸化して導電特性が変化すると考えられる。実験により、そのような変化が主に最初の100日間に起こることが明らかになった。一般に、商業的な理由で、グルコース計を較正することにより(常に新しい製品よりも)一定の経時変化をした製品を受け入れるとともに、最終ユーザーに継続して使用してもらう問題を処理するほうが容易であるため、電極が経時変化した後(特に少なくとも100日間が経過した後)も追加の経時関連効果を示すことなく製造時と同じように振る舞う試験ストリップ(実質的に“あらかじめ経時変化している”もの)を製造することが望ましい。このようにすると、新製品と経時製品の両方を同じ安定したレベルで使用できるため、最終ユーザーにとって製品の保管期間と読み取り値の安定性が改善される。
従来はこのような問題や他の問題があったため、この明細書では特に、電気化学式グルコース・バイオセンサーとして、導電層が上に載った非導電性で化学的に不活性な基板を有する第1の電極と;貴金属元素を含有する金属層を含む導電層が上に載った非導電性で化学的に不活性な基板を有する第2の電極と;第1の電極と第2の電極を接続するグルコース反応性ストリップを備えるバイオセンサーを説明する。第1の電極の導電層は、貴金属を含有する金属層と;その金属層と直接接触する配置の非金属導電層を含んでいる。
いくつかの実施態様では、第1の電極の貴金属元素はパラジウムである。
第1と第2の電極の両方の貴金属を含有する金属層の厚さはさまざまである。いくつかの実施態様では、厚さは約10ナノメートル〜約10ミクロンである。別の実施態様では、厚さは約10ナノメートル〜約50ナノメートルである。さらに別の実施態様では、厚さは約20ナノメートル〜約30ナノメートルである。
非金属導電層の厚さもさまざまにすることができる。いくつかの実施態様では、厚さは約1ナノメートル〜約10ナノメートルである。
グルコース反応性ストリップは、酵素と、メディエータと、インディケータを含むことができる。いくつかの実施態様では、酵素はグルコースオキシダーゼである。メディエータはフェリシアン化物にしてもよい。
別の一実施態様では、第2の電極の導電層は、金属層と直接接触する配置の非金属導電層をさらに備えることができる。そのような一実施態様では、第1と第2の電極の両方の非金属導電層は炭素を含むことができる。
いくつかの実施態様では、第2の電極の貴金属元素は金を含んでいる。別の実施態様では、非金属導電層は炭素を含んでいる。さらに別の実施態様では、基板は熱可塑性ポリマーを含むことができる。
この明細書には、活性化された電気化学式グルコース・バイオセンサーを形成する方法として、基板を用意し;その基板上に、貴金属元素を含有する金属層を含むか、非金属導電層を含む第1の層をスパッタリングで形成し;その第1の層の上に、貴金属元素を含有する金属層を含むか、非金属導電層を含む第2の層をスパッタリングで形成する操作を含む方法も開示されている。この方法では、第1の層が非金属導電層である場合には、第2の層は貴金属元素を含有する金属層であり;第1の層が貴金属元素を含有する金属層である場合には、第2の層は非金属導電層である。
いくつかの実施態様では、第1と第2のスパッタリング・ステップを真空中で実施する。別の実施態様では、貴金属元素はパラジウムである。
この明細書には、電気化学式グルコース・バイオセンサーとして、導電層を有する第1の電極と;貴金属元素を含有する金属層を含む導電層を有する第2の電極と;第1の電極と第2の電極を接続するグルコース反応性ストリップを備えるバイオセンサーも開示されている。この実施態様では、第1の電極の導電層は、パラジウムを含有する金属層と;その金属層と直接接触する配置の非金属導電層を含んでいる。いくつかの実施態様では、第2の電極の貴金属元素は金を含んでいる。別の実施態様では、非金属導電層は炭素を含んでおり、その非金属導電層の厚さは約1ナノメートル〜約10ナノメートルである。
グルコース計における試験ストリップの化学作用と動作の機能ブロック・ダイヤグラムを示す。
本発明による電極のさまざまな実施態様の断面図を示す。
本発明による電極のさまざまな実施態様の断面図を示す。
本発明による電極のさまざまな実施態様の断面図を示す。
本発明による電極のさまざまな実施態様の断面図を示す。
本発明による電極の作製に使用できるロールからロールへ方式のスパッタリング室の機能ダイヤグラムを示す。
金属層を堆積させた後の電極の一実施態様の断面図を示す。
金属層の上に非金属層を堆積させた後の電極の一実施態様の断面図を示す。
パラジウムと炭素を含む電極と、炭素なしの経時変化したパラジウム電極と、炭素なしの新しいパラジウム電極のEIS分析の結果を示すグラフである。
パラジウム/炭素サンプルと経時変化したパラジウム・サンプルを比較したCV試験のグラフであり、似た性質であることをさらに示している。
本発明の一実施態様による電極を含む試験ストリップのブロック・ダイヤグラムを示す。
この明細書には、糖尿病試験ストリップの電極として使用できる貴金属層を製造して活性化させる方法が記載されている。その貴金属層は、別の形態でグルコースをモニタするため、またはそのような活性化が望ましい別の用途のためにも使用できる。この明細書で使用する“活性化させる”という用語には、電極を、実際には経時変化していないのに、その電極が特定の時間だけ経時変化したかのようにうまく機能させることが含まれる。したがって活性化された製品は、最初に製造されたとき(“新”製品)に、ある期間にわたって標準的な保管と包装の条件下に置いた製品(“経時変化した”製品)と同様に機能する製品であると考えられる。ある種の包装技術、製造技術、その他の技術を利用して製品に対する経時変化の効果をなくしたり減らしたりできることに注意されたい。しかし本発明はそうしたことには関係がない。なぜなら望みは、新しいときに既知で安定性のある“あらかじめ経時変化した”特徴を持つ製品を製造し、その製品がさらなる時間経過が原因で変化するのを実質的に阻止することだからである。
活性化の考え方は、電極に対する経時効果をうまく取り込んで製品を最初から経時曲線に沿って変化してしまっているように設計するというものである。いくつかの貴金属電極(まだ活性化されたことがないもの)の反応性(貴金属によって異なる)は、一般に、製造直後により大きく、変化量は時間経過とともに減少する。より具体的には、いくつかの貴金属電極(例えばパラジウム)では、変化は、製造後の最初の100日間のほうが、100日を超える長期間におけるよりもはるかに顕著であることがわかった。さらに、それよりもはるかに長く経時変化させた製品は、印刷した製品期限を守らせることで使用されないようにできることがしばしばある。したがって本発明の一実施態様では、“経時変化した”製品は、当業者に知られているタイプの電極を、そのような製品にとって標準的な保管条件下に100日間にわたって放置した状態のものを備えている。“新”製品には、包装されたときに最初からそのような条件に置かれた製品が含まれる。“活性化された”製品は、新しい状態のとき、経時変化した活性化されていない製品の特徴をまねた製品である。
注意すべき1つの点は、ここで考える電極は、経時変化していて少なくとも一部が酸化した従来の電極と同様に振る舞うことである。しかしこの明細書の方法は、貴金属を酸化させる機能は持たない。そうではなく、この明細書で議論する電極のいくつかは、最初に貴金属を堆積され、次いで非金属層で被覆されることで、酸化の必要なしに、特定の動作モードに限定されることなく経時変化した電極をまねた電極になる。しかしいくつかの貴金属(例えば金、銀など)では一般に時間が経過しても反応性は同じままであるため、被覆された非金属層は不要である。
図2に、試験ストリップの一部として使用できるさまざまな電極(801)の断面図を示してある。特に、これらの電極は、図1と図8に示したように、作用電極と補助電極のいずれかを含むことができる。図2A〜図2Cに示してあるように、電極(801)は、金属層(201)と非金属層(203)の両方を含んでいる。金属層(201)と非金属層(203)は、電極材料の活性が最大となるよう、基板(205)上に、金属/非金属(図2A)、または非金属/金属(図2B)、または金属/非金属/金属(図2C)の順番で配置される。追加の金属層または非金属層と配置を利用して、電極の望ましい動作と性質(例えば時間経過のシミュレーション)によって異なる別の配置にできることが認識されよう。図2Dからわかるように、電極(801)(例えば金を含む電極)によっては非金属層を省略することが好ましかろう。
一般に、試験ストリップ(800)は、少なくとも2つの電極(801)を備えていて、一般に、表面に化学成分(例えば酵素やメディエータ)も堆積される基板を備えることになる。この試験ストリップは、図2に示したのとは異なる位置に堆積された化学物質を含む基板(205)を備えるか、化学作用のための土台として機能し、試験ストリップの設計に応じて基板(205)に取り付けられる別の基板を備えることができる。さらに、各ストリップ(800)は、少なくとも2つのほぼ同じ電極(801)(具体的には、補助電極と作用電極の両方が同じ例えばパラジウムという貴金属からなる)、または少なくとも2つの異なる電極(具体的には、例えばパラジウムからなる補助電極と、例えば金からなる作用電極)を含むことができる。それに加え、ストリップ(800)は、そのストリップ(800)を用いて動作させるグルコース計の設計に応じ、3つ以上の電極、または形が異なる2つ以上の電極、または構成が異なる2つ以上の電極を備えていてもよい。試験ストリップの一実施態様を図8に示す。
基板(205)(と、存在する場合の他のあらゆる基板)は、一般に非導電性で、想定される上記の反応に対して化学的に不活性な任意の材料(可撓性のあるもの、または堅固なもの)を含むことができる。それはプラスチックの形態であることがしばしばあり、その中には、ポリエステル、ポリエチレン、ポリカーボネート、ポリプロピレン、ナイロンや、これら以外のポリマーが含まれるが、例がこれらに限定されることはない。
一般に、金属層(201)は貴金属を含むことになる。貴金属の具体例として、ルテニウム、ロジウム、パラジウム、銀、オスミウム、イリジウム、白金、金や、これらの任意の組み合わせが挙げられるが、これらに限定されない。いくつかの実施態様では、金属は、堆積時には、酸化した形態を除外するため、市販されている最も純粋な形態で提供される。金属は、公知のさまざまな堆積技術を利用して可撓性基板の上に非常に薄い層として堆積させることができる。その厚さは、一般に約10ナノメートル〜約10ミクロンだが、約10ナノメートル〜約50ナノメートルであることが好ましく、約20ナノメートル〜約30ナノメートルであることがより好ましい。金属層は、基板の表面に堆積させた貴金属の表面に堆積させた非金属導電層によって活性化させることができる。しかし上に指摘したように、場合によっては、非金属層を堆積させて金属層を活性化させる必要はない可能性がある。
非金属層は、存在する場合には、一般に、当業者に知られている任意の導電性非金属材料を含むことになる。その例として、透明な導電性被覆材料(例えば炭素(グラファイトの形態であることがしばしばある)と導電性ポリマー)が挙げられるが、別の実施態様では、他の導電性非金属材料や、それらの組み合わせを使用することもできる。非金属導電層は、一般に、金属層よりもはるかに薄い層を含み、通常は1ナノメートル〜10ナノメートルの範囲であり、パラジウム電極では15ナノメートル〜100ナノメートルの範囲である。
図3は、プラスチック基板の上に金属層と非金属層の両方を制御して堆積させる方法としてのスパッタリングに使用できるロールからロールへ方式の被覆システムの一実施態様を示している。このようなロールからロールへ方式の被覆システムでは、一般に、ロールからロールへ形態のプラスチック・フィルムの上に原子レベルの被覆が生成するため、材料のコストが低下する。したがってこのシステムは、電極の構成にとって好ましい一実施態様である。次にロールを公知のやり方で切断して各試験ストリップの具体的な電極部を形成することができる。スパッタリングを適用することにより、一般に、環境因子による汚染がほとんどないかまったくない非常にクリーンかつ一様な層が生成する。なぜなら、どの層も真空中または不活性環境中で堆積されてより純粋な被覆になるからである。しかし当業者であれば、電極を構成するのにスパッタリングを利用する必要はなく、他の堆積法を利用できることが理解できよう。
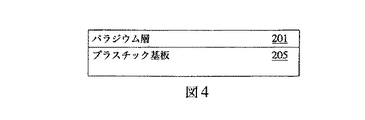
図4と図5は、図3の装置を公知の方法で操作して形成した材料の配置を示している。図4では、最初の金属層は、第1のスパッタリング・ステップで堆積された。図5では、非金属層は、第2のスパッタリング・ステップでその上に配置された。金属層は任意の貴金属を用いて構成されるが、図4の実施態様では、それはパラジウムを含んでいる。この層は、非常に一様であって一般に厚さが一定であることが好ましい。図5では、金属層の上に非金属層(ここでは炭素)が配置されている。非金属層は、同じスパッタリング法によって厚さを制御して堆積され、堆積には非金属導電材料が用いられる。図5では、非金属材料層は厚さが1ミクロン以下である。厚さは1オングストローム〜1ミクロンであることが好ましく、5オングストローム〜50ナノメートルであることがより好ましい。しかしそうである必要はなく、他の厚さにしてもよい。
層になったパラジウムと炭素を含む電極は、電気的特性が、経時に関連した変化に対して非金属層を含まない電極よりも抵抗性があることと、経時変化した(100日間)純粋なパラジウム電極と同様の電気的特性を示すことがわかっている。すなわち、このような構造体は上記のようにして活性化される。
図6はEIS分析の結果であり、炭素層電極を有する新しいサンプル(製造後72時間未満)のパラジウム層(約28ナノメートル)(炭素層の厚さが異なる3種類のサンプル)と、炭素層のない経時変化した(製造後150日)パラジウム層(約26〜28ナノメートル)と、炭素のない新しい(製造後72時間未満)パラジウム層(約28ナノメートル)が示されている。この図からわかるように、経時変化していないパラジウム層/炭素層電極(炭素層の厚さは0.5ミクロン)は、経時変化したパラジウム電極の性能を非常によく再現している。図7は、同じパラジウム/炭素サンプルと経時変化したパラジウム・サンプルを比較したCV試験の結果であり、やはり同様の性質を示している。
図6から明らかなように、炭素層の使用によって電極の経時変化を“シミュレーション”できるだけでなく、炭素層の厚さを変えることでわずかに異なった特性を得ることが可能になる。
本発明をいくつかの実施態様(その中には、現在好ましい実施態様と考えられるものが含まれる)の説明とともに開示してきたが、詳細な説明は例示であり、本発明の範囲を制限すると理解してはならない。当業者であればわかるように、この明細書で詳細に説明した以外の実施態様も本発明に含まれる。ここに開示した任意の発明の精神と範囲を逸脱することなく、記載した実施態様の改変やバリエーションが可能である。
さらに、本発明のどの単一の要素に関して与えたどの範囲、数値、特徴も、本発明の他の任意の要素に関して与えた任意の範囲、数値、性質と同じように使用し、矛盾がなければ、この明細書全体に与えられている個々の要素について規定された数値を持つ一実施態様を形成できることが理解されよう。さらに、ある属またはカテゴリーについて与えられている範囲は、特に断わらない限り、そのカテゴリーの属またはメンバーの中の種にも適用できる。