JP2014503195A5 - - Google Patents
Download PDFInfo
- Publication number
- JP2014503195A5 JP2014503195A5 JP2013539983A JP2013539983A JP2014503195A5 JP 2014503195 A5 JP2014503195 A5 JP 2014503195A5 JP 2013539983 A JP2013539983 A JP 2013539983A JP 2013539983 A JP2013539983 A JP 2013539983A JP 2014503195 A5 JP2014503195 A5 JP 2014503195A5
- Authority
- JP
- Japan
- Prior art keywords
- cell
- light
- cells
- wavelength
- mid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Description
本願はまた、米国仮特許出願第61/628,259号の利益を主張する(出願日2011年10月27日);
細胞を識別し分類する光学的手法を使用することは多くの潜在的な長所(速度、選択性/特異性およびそれらの非侵入性の性質)を持つ。その結果、光を使用して細胞を調べて決定的な情報を決定する多くの方法が実証された。そのような1つの方法は蛍光マーカーを使用する。それは、標的細胞内の特定構造または合成物に結合し、細胞の混合物に導入される化学薬品である。混合物は引き続き洗浄して超過の蛍光マーカーを取り除く。また、細胞は重要な測定値および細胞を分類するために強いUVあるいは他の短い波長の放射線に露出される。化学的マーカーはよい特異性を提供する。しかしながら、これらの化学的マーカーは標的細胞の機能を傷つけるか変化させ、その損傷又は変化は実際の細胞選別には特に不利になる。試験では、マーカーとしてDNAに使用された染料は、例えば、染色体に損傷をもたらした。さらに、細胞内のマーカーのレベルを読む強いUVか可視光線は細胞に破損を与えることがあり、特にDNA損傷は高エネルギーのUVあるいは可視光への露出に起因する。波長のために、さらにいわゆる蛍光活性化細胞選別(FACS)システムに使用される波長のために、定量的測定(特定の抗体用の二者選択的測定値というよりも)は非常に困難になる。なぜなら照明の波長および放射された蛍光の両方が散乱し、細胞の構成要素に吸収されるからである。これは、細胞定位が正確に測定する際に重要な要因になり、劇的にシステムの有効性を低減しうることを意味する。例えば、XおよびY-保有精子の精細胞選別(細胞間のDNA差異を測定する)は、まさに特定の定位(細胞の10%だけが典型的に定位基準を満たす)を必要とし、ヒトについては70-90%の範囲内だけの正確さを提供する。
図23a及びbは、フロー内のコアまたはシース流体に添加物を使用して、中赤外サブシステムによって直接測定できる「トレーサー」を作成する本発明の実施形態を示す。したがって、コア流量の位置およびフローの形および位置の変化の正確なリアルタイムのキャリブレーション/補償ができる。
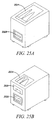
図25a及びbは、ミクロフローチップ・システムの2つの配置例である。図25aは、ユーザーによって、測定されかつ/または選択される細胞サンプルがあらかじめ組み込まれたミクロフローチップを受け入れるツールを示す。これは、比較的小さなボリュームのサンプル用の一般的な配置で、この配置は 単一のミクロフローチップ上に含まれていてよく、それで選別してもよい。スロット2502は測定/選別方式へチップを読み込んでよい。ディスプレイ2504は、細胞内DNA内容に関するヒストグラムおよび他の指標を示す。ディスプレイは、 ユーザーが選択設定ポイントを作り、データのグラフィック表示を設定し、およびスタートと停止ができるタッチスクリーン・ディスプレイであってよい。ツールは、 コンピューターへの(またはコンピューターでコントロールされる)データ転送、またはUSBメモリスティックへデータの転送もしくはバックアップができるUSBインターフェース、などのインターフェースを含んでいてよい。 無線通信ネットワーキング・インターフェースも同様に含まれていてよい。
図26a及びbは、ツールのユーザーに見せるDNA含量のディスプレイ例を示す。図26aは DNA対細胞数がヒストグラム・フォーマットで表示される配置を示す。この例におけるX軸2602は、細胞のDNA含量を表わしている。Y軸2604はサンプルの累積細胞数を表わす。測定された細胞の分布は2608に示されている (ここでは活発に分裂している細胞の分布標本を示す、 またその内いくつかの細胞は、一番左端の小さなピークによって指し示される異数性を示し、これは異常に低DNA数を示す )。このヒストグラムはそれ自体で、ユーザーが細胞サンプルを迅速に評価するのに貴重である。さらに、各状態の細胞のパーセンテージを評価するために、測定後にリアルタイムもしくはオフラインで、曲線あてはめアルゴリズムを手動もしくは自動的に適用できる。
図29a及びbは、本発明で使用されるミクロフローチップ用のいくつかのフォーマット例を示す。
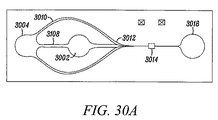
図30a及びbは、本発明で使用されるミクロフローチップの追加の配置例を示す。
図38a-cは、本発明が特に回避しようと設計した表面効果に悩まされている他者が使用しているいくつかの配置サンプルを示す。図38aは、中赤外でフーリエ変換赤外分光(FTIR)分光法を使う液体または固体を測定するのにしばしば使用される減衰全反射法ATR配置を示す。ここで、それは、流速を示す液体のマイクロ経路に接して断面図で示される。システムでは通常であるように、インターフェースの近くの速度は非常に低いだろう。さらに、ATRプリズムから液体フローへの一過性の場の限定的な浸透が示される。従来のFTIRシステムでATRを使用するという利点は、液体の吸収が非常に高い場合でさえ、光がこの配置でほとんど吸収されることはないことである。この図から明白な大きな不都合は、フローのコアへの浸透厚が制限されていることであろう。図 38bは、多くのグループによって使用されるより最近の配置を示す。それは類似しているが、吸収を向上させるプラズモン層(パターン化された金属導電層)を使用する。これによって、プラズモン・フィルターと直接接触するサンプルの吸収識別特性は非常に向上させられる。再び、しかしながら、中赤外の場は液体への浸透を非常に制限されている。この例の生物学的細胞のうちの1つによって示されるような基板に付着させられ静止している細胞の測定について、これによって時系列測定ができるようになる。しかしながら、液体のマイクロ経路を通り抜ける細胞の高速検知について、これは、吸収は強い深さ依存がありおよびその深さに制限があるために、適切な構成ではないかもしれない。図38cは、いくつかのグループによる中赤外測定に使用されてきた本当の伝送構成を示す。この「半透過」構成で、中赤外光は中赤外サンプルを通過し、反射する基板(それは可視で伝送可能)によって反射され、次に検知器に移る前にサンプルを通る第二のパスがなされる。この構成に基づいてHolmanらは「開経路」測定について記述した、トップのウィンドウがない場合、それは反射基板上を限度内の距離だけ開いたおよび液体フローである。この利点は改善された伝送およびより単純な構築であろう。大きな短所は、液体層厚さの中のどんなばらつきもサンプルの吸収における大規模な明白な変化を生じる点である。しかしながら、半透過構成に関するより本質的な問題は反射基板に起因する干渉効果に由来する。例えば、電場は低レベルに落ちているに違いない反射面に非常に近い細胞は、比較的小さな中赤外光を吸収できる。反対に、基板からの一定距離の細胞は、光を最大限吸収するだろう。深さへの依存性は、補正が難しい信号のばらつきを引き起こすだろう。さらに、この構成では、どの光がサンプルによって反射されるのか、サンプルによって散乱するのか、またはサンプルを通って伝達されるか識別するのは難しい。本発明は、これらの構成が抱えるほとんどの問題を取り除く努力をしている。
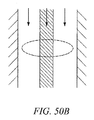
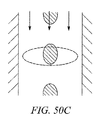
図40a-cは、できるだけ位置依存がQCLに基づいた流体の測定システムから取り出されるように、どのようにミクロフロー空洞が最適化されて共振光学効果を縮小させているかを示す。図40aは、検知波長(それはピーク反響かもしれない)の4分の1波の倍数でさえありうるミクロフロー・ギャップを示す。図40aの左側の図形は電場を示し、図40bに示されるように、光強度は右に示す。図にみられるように、流体のギャップの中心の近くに強いピークがあってもよい。一般に、それは、そのような強い空間の依存性を回避し、液体の吸収のより一様なサンプリングを行うことが望ましい(粒子が経路内の様々な高さに配置される場合、浮流が測定されている時、これは特に重要かもしれない)。図40cは、検知波長で共振しないギャップを使用し、 流体経路の内容のより一様なサンプリングを保証する場合の好ましい配置を示す。この配置は、記述されたようなAR被膜および角度と共にもちろん使用してもよい。
図43a-bは、本発明で使用される複数波長の例を示す。個別の波長は、同調可能なQCL(例えば特に本明細書に記述されたバーニヤ配置)、個々にパッケージ化された一定波長QCL、またはチップ上のモノリシックのQCLアレイによって生じて、個別ビームとして伝達されるか、一つのスポットに合成して伝達される。この図のために、横軸は中赤外周波数を表わす。また、垂直軸は吸光度を表わす。図43aは、吸収スペクトルが対象とする4302の吸収ピークで測定される場合(3点はピーク上で測定される)の配置を示す。これによって形状導関数または二次導関数、同様に絶対吸収が測定できる二次導関数は広域バックグラウンド信号が存在する状態で吸収ピークを測定するのにしばしば使用される。さらに、ローカルの吸収最小限4304はシステム波長のうちの1つで検知される。これによって、例えば、測定ボリュームへ細胞または微粒子を運ぶ液媒の背景吸収レベルが測定できる。図 43bは、ピーク吸収波長4308および参照波長4310だけがサンプリングされるより最小の配置を示す。
図45a-bは、中赤外光での分子吸収ピークの概略例を示す。図45aは、粒子(標的分子の一部分から成り立つ)の吸収、およびそれが測定される媒体の吸収を、両方とも光周波数の関数として示す。図45bは、粒子と媒体の導かれた実際の屈折率を示す。図45bで示されるように、吸収ピークの中心のまわりの粒子屈折率に変動がある。粒子には媒体のそれと異なる基線屈折率(「無限大でのインデックス」)がある。ある応用については、媒体を変更して粒子からの屈折率をより近く(より少ない散乱)またはより遠く(より多くの散乱)することが望ましい。直線の吸収測定が望まれる場合、 散乱の影響を最小限にするようにインデックスの不整合を少なくすることが望ましい。他方では、例えば粒度の散乱に基づいた測定が望まれる場合、次に粒子インデックスに対する媒体インデックスを低下させることは有用である。
Claims (19)
- ミクロフロー経路及び前記ミクロフロー経路において測定領域の媒体にある単一の精細胞を無ラベルで連続的に提示する設備を含むミクロ流体処理システムと、
前記精細胞のDNAにおける結合振動を誘導する1つ以上の波長で中赤外光ビームを放射するように構成され、前記測定領域に含まれる連続した細胞の各々を順に照射するように動作する少なくとも1つの量子カスケードレーザ(QCL)源と、
前記ミクロフロー経路を介した前記光ビームの方向に実質的に垂直である方向に測定すると20ミクロ以下の長さを持つ、前記測定領域にあるスポットに、放射された前記中赤外光ビームを導くビーム形成光学系と、
前記精細胞の各々を介して個別的に伝達された中赤外光の量を量的に測定するように構成される検知機能と、
前記DNAの結合振動の識別特性に対して、伝達されて測定された前記中赤外光を分析して、前記精細胞の各々に保有されるDNA含有量を決定し、それによって精細胞の各々がX染色体またはY染色体を保有するかを識別するように構成されたプロセッサと、
を備える細胞測定システム。 - 前記精細胞を、識別されたその染色体それぞれに従って選別する選別機能を更に有する、ことを特徴とする請求項1に記載の細胞測定システム。
- 第2のレーザーソースを更に備え、
前記少なくとも1つのQCL源は、精細胞のDNAについての共振吸収に対応する波長で、放射するように構成され、前記第2のレーザーソースは、第2の波長で放射するように構成され、前記第2の波長で伝達されて測定された信号は、別の分析物及びシステムの人為要素からのバックグラウンド信号を相殺するために用いられる、
ことを特徴とする請求項1に記載の細胞測定システム。 - 第2の発光源及び第2の検知器をさらに備え、
前記第2の発光源は、前記精細胞によるミー散乱を誘導する波長で放射するように構成され、前記第2の検知器は、ミー散乱に起因する光を検知し、ミー散乱に起因する、検知された光は、前記プロセッサによって用いられて、前記測定領域内の単一の精細胞の存在を識別し、
前記検知機能による測定は、前記測定領域における単一の精細胞の識別された前記存在に対応してゲート制御される、
ことを特徴とする請求項1に記載の細胞測定システム。 - 前記プロセッサは、ミー散乱に起因する、検知された光を用いて、精細胞の特性を識別するようにさらに構成され、前記精細胞の特性は、サイズ、細胞型、細胞の密度及び細胞の定位の1つ以上を備える、
ことを特徴とする請求項4に記載の細胞測定システム。 - 前記第2の発光源は、1つ以上のVIS、UVおよびNIRレーザーソースである、
ことを特徴とする請求項4に記載の細胞数測定システム。 - 細胞が保有する、識別された染色体に基づいて精細胞を選択的に無能化し、ミー散乱に起因する、検知された光に応じて、制御される細胞破壊機能をさらに含む、請求項4に記載の細胞数測定システム。
- 前記細胞破壊機能はレーザーである、請求項7に記載の細胞数測定システム。
- ミクロフロー経路を含み、前記ミクロフロー経路内にある、50ミクロ以下の厚さである測定領域を介して、無ラベルの細胞のフローを提供するように構成されるミクロ流体処理システムと、
前記細胞の各々の1以上の分析物によって共振吸収を誘導する中赤外波長の光ビームを放射するように構成され、前記細胞の各々の1以上の分析物によって共振中赤外吸収を誘導するために、前記測定領域に含まれる連続的なセルの各々を順に照明するように動作する少なくとも1つの量子カスケードレーザ(QCL)光源と、
前記ミクロフロー経路を介した前記光ビームの方向に実質的に垂直である方向に測定すると20ミクロ以下の長さを持つ、前記測定領域にあるスポットに、放射された前記中赤外光ビームを導くビーム形成光学系と、
前記細胞の各々を介して個別的に伝達された中赤外波長光の大きさを測定するように構成される中赤外検知機能と、
伝達されて測定された前記中赤外波長光を分析して、前記細胞の各々の分析物の特性を識別するプロセッサと、
を備える細胞数測定システム。 - 前記少なくとも1つのQCL光源は、第1のQCL光源と、第2のQCL光源とを備え、前記第1のQCL光源は、目標分析物の共振吸収に対応する波長で放射するように構成され、前記第2のQCL光源は、第2の波長で放射するように構成され、伝達されて測定された第2の波長の信号は、別の分析物及びシステムの人為要素からのバックグラウンド信号を相殺するために使用される、
ことを特徴とする請求項9に記載の細胞数測定システム。 - 単一の前記細胞を、識別されたその特性それぞれに従って選別する選別機能を更に有する、
ことを特徴とする請求項9に記載の細胞測定システム。 - 前記ミクロ流体処理システムは、形状、サイズ、表面性状及び細胞膜完全性の内の少なくとも1つに基づいて前記測定領域から細胞を除外するフィルターをさらに備える、
ことを特徴とする請求項9に記載の細胞測定システム。 - 前記プロセッサは、核酸、タンパク質、脂質、代謝産物、溶解ガス、栄養素及びそれらの組合せの1つである分析物を識別するように構成される、
ことを特徴とする請求項9に記載の細胞測定システム。 - 識別された前記特性に基づいて細胞を選択的に無能化する細胞破壊機能をさらに備える、
ことを特徴とする請求項9に記載の細胞測定システム。 - 前記細胞破壊機能はレーザーである、
ことを特徴とする請求項14に記載の細胞数測定システム。 - 細胞が前記測定領域内にあるときに、ミー散乱を誘導する波長で光を放射するように構成される第2の光源と、ミー散乱光を測定する付随検知器とをさらに備え、
測定された前記ミー散乱光は、前記プロセッサによって、分析されて、細胞の特性を識別し、前記特性は、サイズ、細胞型、細胞の密度及び細胞の定位の1つ以上を備える、
ことを特徴とする請求項9に記載の細胞測定システム。 - 前記第2の発光源は、1つ以上のVIS、UVおよびNIRレーザーソースである、
ことを特徴とする請求項16に記載の細胞数測定システム。 - 前記付随検知器は、前記第2の光源の前記波長に対してシフトしない波長を有する散乱光の大きさ及び角度を測定する、
ことを特徴とする請求項16に記載の細胞数測定システム。 - 細胞が前記測定領域内にあるときに、ミー散乱を誘導する波長で光を放射するように構成される第2の光源と、前記測定領域にある前記細胞からのミー散乱光の大きさを測定する付随検知器とをさらに備え、
前記プロセッサは、測定された前記散乱光及び伝達されて測定された前記中赤外光を分析して、前記セルの各々の分析特性を識別する、
ことを特徴とする請求項16に記載の細胞数測定システム。
Applications Claiming Priority (13)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US45699710P | 2010-11-16 | 2010-11-16 | |
| US61/456,997 | 2010-11-16 | ||
| US201161464775P | 2011-03-09 | 2011-03-09 | |
| US61/464,775 | 2011-03-09 | ||
| US201161516623P | 2011-04-05 | 2011-04-05 | |
| US61/516,623 | 2011-04-05 | ||
| US201161519567P | 2011-05-25 | 2011-05-25 | |
| US61/519,567 | 2011-05-25 | ||
| US201161571051P | 2011-06-20 | 2011-06-20 | |
| US61/571,051 | 2011-06-20 | ||
| US201161575799P | 2011-08-29 | 2011-08-29 | |
| US61/575,799 | 2011-08-29 | ||
| PCT/US2011/061046 WO2012068287A2 (en) | 2010-11-16 | 2011-11-16 | System for identifying and sorting living cells |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016198323A Division JP2017012197A (ja) | 2010-11-16 | 2016-10-06 | 生細胞の識別および選別用システム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2014503195A JP2014503195A (ja) | 2014-02-13 |
| JP2014503195A5 true JP2014503195A5 (ja) | 2015-04-23 |
Family
ID=46048107
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013539983A Pending JP2014503195A (ja) | 2010-11-16 | 2011-11-16 | 生細胞の識別および選別用システム |
| JP2016198323A Pending JP2017012197A (ja) | 2010-11-16 | 2016-10-06 | 生細胞の識別および選別用システム |
| JP2018220397A Active JP6911254B2 (ja) | 2010-11-16 | 2018-11-26 | 生細胞の識別および選別用システム |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016198323A Pending JP2017012197A (ja) | 2010-11-16 | 2016-10-06 | 生細胞の識別および選別用システム |
| JP2018220397A Active JP6911254B2 (ja) | 2010-11-16 | 2018-11-26 | 生細胞の識別および選別用システム |
Country Status (4)
| Country | Link |
|---|---|
| EP (3) | EP3708674B1 (ja) |
| JP (3) | JP2014503195A (ja) |
| SG (3) | SG190015A1 (ja) |
| WO (1) | WO2012068287A2 (ja) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11243494B2 (en) | 2002-07-31 | 2022-02-08 | Abs Global, Inc. | Multiple laminar flow-based particle and cellular separation with laser steering |
| US8941062B2 (en) | 2010-11-16 | 2015-01-27 | 1087 Systems, Inc. | System for identifying and sorting living cells |
| US10908066B2 (en) | 2010-11-16 | 2021-02-02 | 1087 Systems, Inc. | Use of vibrational spectroscopy for microfluidic liquid measurement |
| US20120225475A1 (en) | 2010-11-16 | 2012-09-06 | 1087 Systems, Inc. | Cytometry system with quantum cascade laser source, acoustic detector, and micro-fluidic cell handling system configured for inspection of individual cells |
| GB2519460B (en) * | 2012-07-09 | 2018-02-21 | Thermo Electron Scient Instruments Llc | Motorized variable path length cell for spectroscopy |
| US9194786B2 (en) * | 2012-08-01 | 2015-11-24 | Owl biomedical, Inc. | Particle manipulation system with cytometric capability |
| US8961904B2 (en) | 2013-07-16 | 2015-02-24 | Premium Genetics (Uk) Ltd. | Microfluidic chip |
| US11796449B2 (en) | 2013-10-30 | 2023-10-24 | Abs Global, Inc. | Microfluidic system and method with focused energy apparatus |
| JP6691053B2 (ja) | 2014-03-18 | 2020-04-28 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニアThe Regents Of The University Of California | 無線周波数多重化を用いた並行フローサイトメーター |
| KR20170039250A (ko) * | 2014-08-28 | 2017-04-10 | 시스멕스 가부시키가이샤 | 입자 촬상 장치 및 입자 촬상 방법 |
| WO2016063322A1 (ja) * | 2014-10-20 | 2016-04-28 | 株式会社日立製作所 | 光学分析装置及び生体分子解析装置 |
| WO2016115397A1 (en) * | 2015-01-14 | 2016-07-21 | Hartley Frank Thomas | Apparatus for drawing of a bodily fluid and method therefor |
| JP2018509615A (ja) * | 2015-02-19 | 2018-04-05 | プレミアム ジェネティクス (ユーケー) リミテッド | 走査型赤外線測定システム |
| EP4194801A1 (en) | 2015-02-24 | 2023-06-14 | The University of Tokyo | Dynamic high-speed high-sensitivity imaging device and imaging method |
| JP6713730B2 (ja) | 2015-05-20 | 2020-06-24 | シスメックス株式会社 | 細胞検出装置および細胞検出方法 |
| ES2925353T3 (es) | 2015-10-13 | 2022-10-17 | Omega Biosystems Incorporated | Sistema de citometría de flujo de imágenes de fluorescencia multimodal |
| WO2017073737A1 (ja) | 2015-10-28 | 2017-05-04 | 国立大学法人東京大学 | 分析装置 |
| BR112018014870A2 (pt) * | 2016-01-21 | 2018-12-11 | Protein Dynamic Solutions Llc | método e sistema para análise de dados espectrais |
| CN109863384B (zh) | 2016-06-10 | 2022-10-28 | 加利福尼亚大学董事会 | 基于图像的细胞分选系统和方法 |
| EP3516369B1 (en) * | 2016-09-22 | 2022-11-02 | IMEC vzw | Particle detection using thin lenses |
| CN108458963B (zh) * | 2018-04-13 | 2023-06-06 | 大连海事大学 | 一种基于纳米-微米通道组合进行颗粒和细胞顺序分离和计数的微流控芯片装置和方法 |
| EP3796998A1 (en) | 2018-05-23 | 2021-03-31 | ABS Global, Inc. | Systems and methods for particle focusing in microchannels |
| CN112638529B (zh) * | 2018-06-13 | 2023-05-30 | 新克赛特株式会社 | 细胞计数的方法和系统 |
| EP3955735B1 (en) | 2019-04-18 | 2024-05-22 | ABS Global, Inc. | System and process for continuous addition of cryoprotectant |
| JP2022540601A (ja) | 2019-07-10 | 2022-09-16 | ベクトン・ディキンソン・アンド・カンパニー | 細胞選別分類を調整するための再構成可能な集積回路 |
| US11628439B2 (en) | 2020-01-13 | 2023-04-18 | Abs Global, Inc. | Single-sheath microfluidic chip |
| US11662297B2 (en) * | 2020-04-28 | 2023-05-30 | Becton, Dickinson And Company | Method for index sorting unique phenotypes and systems for same |
| KR102450943B1 (ko) * | 2020-07-30 | 2022-10-04 | 아주대학교산학협력단 | 바이오 센서, 이의 제조방법 및 이를 이용한 분석 방법 |
| US20230333006A1 (en) * | 2020-09-28 | 2023-10-19 | Jasco Corporation | Infrared circular dichroism measurement apparatus |
| KR102564301B1 (ko) * | 2021-11-18 | 2023-08-07 | 고등기술연구원연구조합 | 필터파손측정장치 및 이를 이용한 필터파손측정방법 |
| CN114778422B (zh) * | 2022-04-19 | 2023-09-08 | 北京理工大学 | 一种基于微液滴操控技术的自动化细胞分选系统及其方法 |
| WO2023220536A2 (en) * | 2022-05-08 | 2023-11-16 | The General Hospital Corporation | Systems and methods for sorting using laser particles or cells |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4765737A (en) * | 1987-03-30 | 1988-08-23 | Cornell Research Foundation | Cell size measurements using light in flow cytometry and cell sorting |
| FI98765C (fi) * | 1995-01-16 | 1997-08-11 | Erkki Soini | Virtaussytometrinen menetelmä ja laite |
| US6031232A (en) * | 1995-11-13 | 2000-02-29 | Bio-Rad Laboratories, Inc. | Method for the detection of malignant and premalignant stages of cervical cancer |
| JP3454173B2 (ja) * | 1998-11-09 | 2003-10-06 | 三菱電機株式会社 | 光学式ほこりセンサ光学系 |
| US6853654B2 (en) | 1999-07-27 | 2005-02-08 | Intel Corporation | Tunable external cavity laser |
| CA2408939C (en) * | 2000-05-09 | 2011-11-08 | Xy, Inc. | High purity x-chromosome bearing and y-chromosome bearing populations of spermatozoa |
| US6749565B2 (en) * | 2000-07-08 | 2004-06-15 | Victor Chudner | Method for blood infrared spectroscopy diagnosing of inner organs pathology |
| AU2002234621A1 (en) * | 2001-01-22 | 2002-07-30 | Ralf Masuch | Rapid test for biological substances using ftir |
| US7812312B2 (en) * | 2002-04-03 | 2010-10-12 | Johann Wolfgang Goethe-Universitaet | Infrared measuring device, especially for the spectrometry of aqueous systems, preferably multiple component systems |
| US7699767B2 (en) * | 2002-07-31 | 2010-04-20 | Arryx, Inc. | Multiple laminar flow-based particle and cellular separation with laser steering |
| ES2918578T3 (es) * | 2003-03-28 | 2022-07-19 | Inguran Llc | Aparato y métodos para proporcionar esperma animal clasificado por sexo |
| NZ544103A (en) * | 2003-05-15 | 2010-10-29 | Xy Llc | Efficient haploid cell sorting for flow cytometer systems |
| EP1650597A4 (en) * | 2003-08-01 | 2007-09-05 | Nippon Telegraph & Telephone | LASER LIGHT SOURCE |
| JP5046645B2 (ja) * | 2003-09-04 | 2012-10-10 | アリックス インコーポレイテッド | 血液や細胞等の液体混合物を構成成分に分離する方法、装置およびシステム。 |
| NZ530972A (en) * | 2004-02-05 | 2005-04-29 | Embrionics Ltd | A method and apparatus for orientating and selecting cells |
| US7623234B2 (en) * | 2004-03-22 | 2009-11-24 | Quantaspec, Inc. | System and method for detecting and identifying an analyte |
| JP4921307B2 (ja) * | 2007-10-02 | 2012-04-25 | 日本電信電話株式会社 | 光吸収分析装置 |
| CN103153086B (zh) * | 2010-10-20 | 2016-06-22 | 荷兰联合利华有限公司 | 包含疏水蛋白的发泡剂 |
| EP3933038A1 (en) * | 2020-07-02 | 2022-01-05 | Technische Universität München | Modified terpene synthases and their use for production of pseudopterosin intermediates and/or pseudopterosins |
-
2011
- 2011-11-16 EP EP20167363.9A patent/EP3708674B1/en active Active
- 2011-11-16 EP EP11841869.8A patent/EP2640844B1/en active Active
- 2011-11-16 JP JP2013539983A patent/JP2014503195A/ja active Pending
- 2011-11-16 SG SG2013031927A patent/SG190015A1/en unknown
- 2011-11-16 EP EP23169267.4A patent/EP4227666A1/en active Pending
- 2011-11-16 SG SG10201912164UA patent/SG10201912164UA/en unknown
- 2011-11-16 WO PCT/US2011/061046 patent/WO2012068287A2/en active Application Filing
- 2011-11-16 SG SG10201509185UA patent/SG10201509185UA/en unknown
-
2016
- 2016-10-06 JP JP2016198323A patent/JP2017012197A/ja active Pending
-
2018
- 2018-11-26 JP JP2018220397A patent/JP6911254B2/ja active Active
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2014503195A5 (ja) | ||
| US20230296494A1 (en) | Flow Cytometer With Optical Equalization | |
| US9766223B2 (en) | Analysis of bioparticles in an optical microcavity | |
| US9372143B2 (en) | Scanning image flow cytometer | |
| US7386199B2 (en) | Providing light to channels or portions | |
| US7399600B2 (en) | Optical detection and analysis of particles | |
| CN103823051B (zh) | 利用红细胞内含有的血红蛋白的本征色素沉着来确定血样的红细胞指数的方法及设备 | |
| US8209128B1 (en) | Nanolaser spectroscopy and micro-optical resonators for detecting, analyzing, and manipulating bioparticles | |
| JP2018509615A (ja) | 走査型赤外線測定システム | |
| JP6100658B2 (ja) | 血球分析装置および血球分析方法 | |
| Gnyawali et al. | Simultaneous acoustic and photoacoustic microfluidic flow cytometry for label-free analysis | |
| JP5260949B2 (ja) | 光計測装置および光計測方法 | |
| US10324020B2 (en) | Fluidic optical cartridge | |
| EP2726852B1 (en) | Multiple examinations of a sample | |
| EP2843410B1 (en) | Sample analyzing method and sample analyzer | |
| JP2016522893A (ja) | 全内部反射を使用して光を収集するための方法およびシステム | |
| US8211708B2 (en) | Optical measuring device and method therefor | |
| CN212321444U (zh) | 表面增强拉曼散射结合spr传感的检测装置 | |
| US9068915B2 (en) | Method and system for calibrating a flow cytometer | |
| RU2347224C2 (ru) | Способ проведения анализов крови и анализатор крови | |
| JP2022520504A (ja) | 流体中の粒子の存在を検出するシステムおよび方法 | |
| EP3913044A1 (en) | Device and method for determining a viability and/or a cell count of biological cells in a cell suspension culture by means of collimated transmission | |
| Tsuyama et al. | Nanofluidic optical diffraction interferometry for detection and classification of individual nanoparticles in a nanochannel | |
| JP2003028796A (ja) | サンプル分析器内のサンプル高さを較正する方法 | |
| Then | Waveguide-based single molecule detection in flow |