JP2012509666A - 生体外におけるヒトbリンパ球産生培養システム - Google Patents
生体外におけるヒトbリンパ球産生培養システム Download PDFInfo
- Publication number
- JP2012509666A JP2012509666A JP2011537633A JP2011537633A JP2012509666A JP 2012509666 A JP2012509666 A JP 2012509666A JP 2011537633 A JP2011537633 A JP 2011537633A JP 2011537633 A JP2011537633 A JP 2011537633A JP 2012509666 A JP2012509666 A JP 2012509666A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- cell
- population
- hspc
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 210000003719 b-lymphocyte Anatomy 0.000 title claims abstract description 244
- 238000000338 in vitro Methods 0.000 title claims abstract description 51
- 238000004519 manufacturing process Methods 0.000 title description 11
- 238000000034 method Methods 0.000 claims abstract description 90
- 210000000130 stem cell Anatomy 0.000 claims abstract description 36
- 210000004027 cell Anatomy 0.000 claims description 373
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 claims description 125
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 claims description 125
- 108091033319 polynucleotide Proteins 0.000 claims description 79
- 102000040430 polynucleotide Human genes 0.000 claims description 79
- 239000002157 polynucleotide Substances 0.000 claims description 79
- 239000013598 vector Substances 0.000 claims description 74
- 230000004936 stimulating effect Effects 0.000 claims description 46
- 210000004180 plasmocyte Anatomy 0.000 claims description 40
- 239000012190 activator Substances 0.000 claims description 39
- 239000003102 growth factor Substances 0.000 claims description 39
- 210000001948 pro-b lymphocyte Anatomy 0.000 claims description 38
- 238000012258 culturing Methods 0.000 claims description 35
- 108010029697 CD40 Ligand Proteins 0.000 claims description 30
- 102100032937 CD40 ligand Human genes 0.000 claims description 30
- 210000003297 immature b lymphocyte Anatomy 0.000 claims description 29
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 claims description 25
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 claims description 25
- 108020004414 DNA Proteins 0.000 claims description 23
- 210000003720 plasmablast Anatomy 0.000 claims description 23
- 108090000174 Interleukin-10 Proteins 0.000 claims description 21
- 108010002350 Interleukin-2 Proteins 0.000 claims description 21
- 108010002386 Interleukin-3 Proteins 0.000 claims description 20
- 102000000646 Interleukin-3 Human genes 0.000 claims description 20
- 210000003958 hematopoietic stem cell Anatomy 0.000 claims description 20
- 102000036693 Thrombopoietin Human genes 0.000 claims description 17
- 108010041111 Thrombopoietin Proteins 0.000 claims description 17
- 210000002536 stromal cell Anatomy 0.000 claims description 17
- 101710162577 Fms-related tyrosine kinase 3 ligand protein Proteins 0.000 claims description 14
- 102100020715 Fms-related tyrosine kinase 3 ligand protein Human genes 0.000 claims description 14
- 108010002586 Interleukin-7 Proteins 0.000 claims description 12
- 102100021592 Interleukin-7 Human genes 0.000 claims description 12
- 230000003248 secreting effect Effects 0.000 claims description 12
- 210000004700 fetal blood Anatomy 0.000 claims description 10
- 108090001005 Interleukin-6 Proteins 0.000 claims description 9
- 230000001177 retroviral effect Effects 0.000 claims description 9
- 102000003815 Interleukin-11 Human genes 0.000 claims description 8
- 108090000177 Interleukin-11 Proteins 0.000 claims description 8
- 230000008093 supporting effect Effects 0.000 claims description 8
- 210000000224 granular leucocyte Anatomy 0.000 claims description 7
- 102000007644 Colony-Stimulating Factors Human genes 0.000 claims description 6
- 108010071942 Colony-Stimulating Factors Proteins 0.000 claims description 6
- 108090000172 Interleukin-15 Proteins 0.000 claims description 6
- 210000002798 bone marrow cell Anatomy 0.000 claims description 6
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 claims 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 claims 1
- 101001105486 Homo sapiens Proteasome subunit alpha type-7 Proteins 0.000 abstract description 14
- 102100021201 Proteasome subunit alpha type-7 Human genes 0.000 abstract description 14
- 239000000203 mixture Substances 0.000 abstract description 11
- 210000004369 blood Anatomy 0.000 abstract description 4
- 239000008280 blood Substances 0.000 abstract description 4
- PZNPLUBHRSSFHT-RRHRGVEJSA-N 1-hexadecanoyl-2-octadecanoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[C@@H](COP([O-])(=O)OCC[N+](C)(C)C)COC(=O)CCCCCCCCCCCCCCC PZNPLUBHRSSFHT-RRHRGVEJSA-N 0.000 abstract 1
- 230000014509 gene expression Effects 0.000 description 65
- 239000005090 green fluorescent protein Substances 0.000 description 55
- 108091007433 antigens Proteins 0.000 description 50
- 102000036639 antigens Human genes 0.000 description 50
- 108090000623 proteins and genes Proteins 0.000 description 49
- 239000000427 antigen Substances 0.000 description 48
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 30
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 30
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 30
- 241000700605 Viruses Species 0.000 description 27
- 108090000765 processed proteins & peptides Proteins 0.000 description 24
- 108700019146 Transgenes Proteins 0.000 description 22
- 102000004196 processed proteins & peptides Human genes 0.000 description 22
- 201000010099 disease Diseases 0.000 description 20
- 229920001184 polypeptide Polymers 0.000 description 20
- 102000004169 proteins and genes Human genes 0.000 description 20
- 150000007523 nucleic acids Chemical class 0.000 description 18
- 229940076264 interleukin-3 Drugs 0.000 description 17
- 208000015181 infectious disease Diseases 0.000 description 16
- 102000039446 nucleic acids Human genes 0.000 description 16
- 108020004707 nucleic acids Proteins 0.000 description 15
- 230000003612 virological effect Effects 0.000 description 14
- 230000011712 cell development Effects 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 239000003623 enhancer Substances 0.000 description 13
- 238000001514 detection method Methods 0.000 description 12
- 102100031585 ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Human genes 0.000 description 11
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 11
- 101000777636 Homo sapiens ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Proteins 0.000 description 11
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 11
- 101000599951 Homo sapiens Insulin-like growth factor I Proteins 0.000 description 11
- 102100037852 Insulin-like growth factor I Human genes 0.000 description 11
- 102000003729 Neprilysin Human genes 0.000 description 11
- 108090000028 Neprilysin Proteins 0.000 description 11
- 230000010261 cell growth Effects 0.000 description 11
- 238000003501 co-culture Methods 0.000 description 11
- 229940100994 interleukin-7 Drugs 0.000 description 11
- 241000725303 Human immunodeficiency virus Species 0.000 description 10
- 108060003951 Immunoglobulin Proteins 0.000 description 10
- 208000035475 disorder Diseases 0.000 description 10
- 102000018358 immunoglobulin Human genes 0.000 description 10
- 102100027207 CD27 antigen Human genes 0.000 description 9
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 9
- 241000713666 Lentivirus Species 0.000 description 9
- 241000124008 Mammalia Species 0.000 description 9
- 230000024245 cell differentiation Effects 0.000 description 9
- 238000000684 flow cytometry Methods 0.000 description 9
- 239000002609 medium Substances 0.000 description 9
- 230000001105 regulatory effect Effects 0.000 description 9
- 239000013603 viral vector Substances 0.000 description 9
- 102000004127 Cytokines Human genes 0.000 description 8
- 108090000695 Cytokines Proteins 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 238000002965 ELISA Methods 0.000 description 7
- 101000874179 Homo sapiens Syndecan-1 Proteins 0.000 description 7
- 206010028980 Neoplasm Diseases 0.000 description 7
- 102100035721 Syndecan-1 Human genes 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- 230000027455 binding Effects 0.000 description 7
- 150000001875 compounds Chemical class 0.000 description 7
- 238000011534 incubation Methods 0.000 description 7
- 229940074383 interleukin-11 Drugs 0.000 description 7
- 230000001737 promoting effect Effects 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 241001430294 unidentified retrovirus Species 0.000 description 7
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 6
- 108091026890 Coding region Proteins 0.000 description 6
- 241001529936 Murinae Species 0.000 description 6
- 108091028043 Nucleic acid sequence Proteins 0.000 description 6
- 108090000848 Ubiquitin Proteins 0.000 description 6
- 102000044159 Ubiquitin Human genes 0.000 description 6
- 210000001185 bone marrow Anatomy 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- 230000018109 developmental process Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 230000010354 integration Effects 0.000 description 6
- 239000013612 plasmid Substances 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 230000000638 stimulation Effects 0.000 description 6
- 238000013518 transcription Methods 0.000 description 6
- 230000035897 transcription Effects 0.000 description 6
- 238000010361 transduction Methods 0.000 description 6
- 230000026683 transduction Effects 0.000 description 6
- 241000710198 Foot-and-mouth disease virus Species 0.000 description 5
- 241000282412 Homo Species 0.000 description 5
- 238000004113 cell culture Methods 0.000 description 5
- 239000001963 growth medium Substances 0.000 description 5
- 230000028993 immune response Effects 0.000 description 5
- 230000003834 intracellular effect Effects 0.000 description 5
- 150000002632 lipids Chemical class 0.000 description 5
- 230000001566 pro-viral effect Effects 0.000 description 5
- 230000028327 secretion Effects 0.000 description 5
- 241000713800 Feline immunodeficiency virus Species 0.000 description 4
- 108091092584 GDNA Proteins 0.000 description 4
- 102000007651 Macrophage Colony-Stimulating Factor Human genes 0.000 description 4
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 description 4
- 102100037935 Polyubiquitin-C Human genes 0.000 description 4
- 241000713311 Simian immunodeficiency virus Species 0.000 description 4
- 108010056354 Ubiquitin C Proteins 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 229940098773 bovine serum albumin Drugs 0.000 description 4
- 235000014633 carbohydrates Nutrition 0.000 description 4
- 150000001720 carbohydrates Chemical class 0.000 description 4
- 210000000349 chromosome Anatomy 0.000 description 4
- 239000012228 culture supernatant Substances 0.000 description 4
- 238000003745 diagnosis Methods 0.000 description 4
- 230000004069 differentiation Effects 0.000 description 4
- 230000007613 environmental effect Effects 0.000 description 4
- 239000012737 fresh medium Substances 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 230000001939 inductive effect Effects 0.000 description 4
- 244000000056 intracellular parasite Species 0.000 description 4
- 230000003472 neutralizing effect Effects 0.000 description 4
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- 150000003384 small molecules Chemical class 0.000 description 4
- 238000010186 staining Methods 0.000 description 4
- 238000001890 transfection Methods 0.000 description 4
- 230000009466 transformation Effects 0.000 description 4
- 241000894006 Bacteria Species 0.000 description 3
- 241000283707 Capra Species 0.000 description 3
- 206010059866 Drug resistance Diseases 0.000 description 3
- 102100022297 Integrin alpha-X Human genes 0.000 description 3
- 108010047761 Interferon-alpha Proteins 0.000 description 3
- 102000006992 Interferon-alpha Human genes 0.000 description 3
- 102100040604 Myotubularin-related protein 5 Human genes 0.000 description 3
- 108050003253 Myotubularin-related protein 5 Proteins 0.000 description 3
- 102000016971 Proto-Oncogene Proteins c-kit Human genes 0.000 description 3
- 108010014608 Proto-Oncogene Proteins c-kit Proteins 0.000 description 3
- 210000001744 T-lymphocyte Anatomy 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 230000001580 bacterial effect Effects 0.000 description 3
- 201000011510 cancer Diseases 0.000 description 3
- 230000004186 co-expression Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 210000004443 dendritic cell Anatomy 0.000 description 3
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 3
- 241001493065 dsRNA viruses Species 0.000 description 3
- 210000003527 eukaryotic cell Anatomy 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 229940072221 immunoglobulins Drugs 0.000 description 3
- 210000000265 leukocyte Anatomy 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 238000006386 neutralization reaction Methods 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 230000001717 pathogenic effect Effects 0.000 description 3
- 210000005259 peripheral blood Anatomy 0.000 description 3
- 239000011886 peripheral blood Substances 0.000 description 3
- 239000002953 phosphate buffered saline Substances 0.000 description 3
- 239000002243 precursor Substances 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 230000014616 translation Effects 0.000 description 3
- 241000701161 unidentified adenovirus Species 0.000 description 3
- 238000011144 upstream manufacturing Methods 0.000 description 3
- 102100022749 Aminopeptidase N Human genes 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- 241000701022 Cytomegalovirus Species 0.000 description 2
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 description 2
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 241000283086 Equidae Species 0.000 description 2
- 241000713730 Equine infectious anemia virus Species 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- 101000757160 Homo sapiens Aminopeptidase N Proteins 0.000 description 2
- 101100059511 Homo sapiens CD40LG gene Proteins 0.000 description 2
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 2
- 241000713340 Human immunodeficiency virus 2 Species 0.000 description 2
- 241000829100 Macaca mulatta polyomavirus 1 Species 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 241000714177 Murine leukemia virus Species 0.000 description 2
- TTZMPOZCBFTTPR-UHFFFAOYSA-N O=P1OCO1 Chemical compound O=P1OCO1 TTZMPOZCBFTTPR-UHFFFAOYSA-N 0.000 description 2
- 108700026244 Open Reading Frames Proteins 0.000 description 2
- 241001494479 Pecora Species 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 208000007452 Plasmacytoma Diseases 0.000 description 2
- 241001505332 Polyomavirus sp. Species 0.000 description 2
- 238000000692 Student's t-test Methods 0.000 description 2
- 102000002663 Surrogate Immunoglobulin Light Chains Human genes 0.000 description 2
- 108010018324 Surrogate Immunoglobulin Light Chains Proteins 0.000 description 2
- 239000004098 Tetracycline Substances 0.000 description 2
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 2
- 230000010530 Virus Neutralization Effects 0.000 description 2
- 239000013566 allergen Substances 0.000 description 2
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 2
- 229960000723 ampicillin Drugs 0.000 description 2
- 230000036436 anti-hiv Effects 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 230000020411 cell activation Effects 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 210000000805 cytoplasm Anatomy 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 210000004667 early pro-b cell Anatomy 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 210000001671 embryonic stem cell Anatomy 0.000 description 2
- 239000013604 expression vector Substances 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- 210000003918 fraction a Anatomy 0.000 description 2
- 238000001476 gene delivery Methods 0.000 description 2
- 210000004602 germ cell Anatomy 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- 230000003394 haemopoietic effect Effects 0.000 description 2
- 230000016784 immunoglobulin production Effects 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 210000000014 large pre-b cell Anatomy 0.000 description 2
- 210000002202 late pro-b cell Anatomy 0.000 description 2
- 208000014018 liver neoplasm Diseases 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 210000003738 lymphoid progenitor cell Anatomy 0.000 description 2
- 210000003519 mature b lymphocyte Anatomy 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 210000001806 memory b lymphocyte Anatomy 0.000 description 2
- 230000000813 microbial effect Effects 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 238000010369 molecular cloning Methods 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- OHDXDNUPVVYWOV-UHFFFAOYSA-N n-methyl-1-(2-naphthalen-1-ylsulfanylphenyl)methanamine Chemical compound CNCC1=CC=CC=C1SC1=CC=CC2=CC=CC=C12 OHDXDNUPVVYWOV-UHFFFAOYSA-N 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 210000003705 ribosome Anatomy 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000002356 single layer Substances 0.000 description 2
- 210000000345 small pre-b cell Anatomy 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 210000001082 somatic cell Anatomy 0.000 description 2
- 238000012353 t test Methods 0.000 description 2
- 229960002180 tetracycline Drugs 0.000 description 2
- 229930101283 tetracycline Natural products 0.000 description 2
- 235000019364 tetracycline Nutrition 0.000 description 2
- 150000003522 tetracyclines Chemical class 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- UAIUNKRWKOVEES-UHFFFAOYSA-N 3,3',5,5'-tetramethylbenzidine Chemical compound CC1=C(N)C(C)=CC(C=2C=C(C)C(N)=C(C)C=2)=C1 UAIUNKRWKOVEES-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 108091023043 Alu Element Proteins 0.000 description 1
- 206010003571 Astrocytoma Diseases 0.000 description 1
- 241000713842 Avian sarcoma virus Species 0.000 description 1
- 108091008875 B cell receptors Proteins 0.000 description 1
- 102100025218 B-cell differentiation antigen CD72 Human genes 0.000 description 1
- 102100038080 B-cell receptor CD22 Human genes 0.000 description 1
- 230000003844 B-cell-activation Effects 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 241000713704 Bovine immunodeficiency virus Species 0.000 description 1
- 241000701822 Bovine papillomavirus Species 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 241000589562 Brucella Species 0.000 description 1
- 101150013553 CD40 gene Proteins 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- 241000606161 Chlamydia Species 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 102100032768 Complement receptor type 2 Human genes 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 238000001712 DNA sequencing Methods 0.000 description 1
- 241000450599 DNA viruses Species 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 208000006168 Ewing Sarcoma Diseases 0.000 description 1
- 108091029865 Exogenous DNA Proteins 0.000 description 1
- 108010042634 F2A4-K-NS peptide Proteins 0.000 description 1
- 241001523858 Felipes Species 0.000 description 1
- 241000700662 Fowlpox virus Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 102100021519 Hemoglobin subunit beta Human genes 0.000 description 1
- 108091005904 Hemoglobin subunit beta Proteins 0.000 description 1
- 241000700721 Hepatitis B virus Species 0.000 description 1
- 101000934359 Homo sapiens B-cell differentiation antigen CD72 Proteins 0.000 description 1
- 101000884305 Homo sapiens B-cell receptor CD22 Proteins 0.000 description 1
- 101000941929 Homo sapiens Complement receptor type 2 Proteins 0.000 description 1
- 101000878605 Homo sapiens Low affinity immunoglobulin epsilon Fc receptor Proteins 0.000 description 1
- 101000633778 Homo sapiens SLAM family member 5 Proteins 0.000 description 1
- 101000884271 Homo sapiens Signal transducer CD24 Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 241000701085 Human alphaherpesvirus 3 Species 0.000 description 1
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 1
- 241000701027 Human herpesvirus 6 Species 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 1
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 1
- 102100029571 Immunoglobulin J chain Human genes 0.000 description 1
- 101710132152 Immunoglobulin J chain Proteins 0.000 description 1
- 102100029567 Immunoglobulin kappa light chain Human genes 0.000 description 1
- 101710189008 Immunoglobulin kappa light chain Proteins 0.000 description 1
- 102000004218 Insulin-Like Growth Factor I Human genes 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 241000589248 Legionella Species 0.000 description 1
- 208000007764 Legionnaires' Disease Diseases 0.000 description 1
- 241000222722 Leishmania <genus> Species 0.000 description 1
- 241000186781 Listeria Species 0.000 description 1
- 102100038007 Low affinity immunoglobulin epsilon Fc receptor Human genes 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 241000712079 Measles morbillivirus Species 0.000 description 1
- 101000687343 Mus musculus PR domain zinc finger protein 1 Proteins 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 241000186359 Mycobacterium Species 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 108700019961 Neoplasm Genes Proteins 0.000 description 1
- 102000048850 Neoplasm Genes Human genes 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 101150012195 PREB gene Proteins 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 241001631646 Papillomaviridae Species 0.000 description 1
- 241000224016 Plasmodium Species 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 108010076039 Polyproteins Proteins 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 102000000434 Pre-B Cell Receptors Human genes 0.000 description 1
- 108010016231 Pre-B Cell Receptors Proteins 0.000 description 1
- 102000029797 Prion Human genes 0.000 description 1
- 108091000054 Prion Proteins 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 241000125945 Protoparvovirus Species 0.000 description 1
- 230000004570 RNA-binding Effects 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 201000000582 Retinoblastoma Diseases 0.000 description 1
- 241000606701 Rickettsia Species 0.000 description 1
- 241000710799 Rubella virus Species 0.000 description 1
- 102100029216 SLAM family member 5 Human genes 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- 102100038081 Signal transducer CD24 Human genes 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- 108091081024 Start codon Proteins 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 208000000389 T-cell leukemia Diseases 0.000 description 1
- 208000028530 T-cell lymphoblastic leukemia/lymphoma Diseases 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 241000223996 Toxoplasma Species 0.000 description 1
- 241000223104 Trypanosoma Species 0.000 description 1
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 241000713325 Visna/maedi virus Species 0.000 description 1
- 208000008383 Wilms tumor Diseases 0.000 description 1
- 241001492404 Woodchuck hepatitis virus Species 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 210000000628 antibody-producing cell Anatomy 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 102000023732 binding proteins Human genes 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- -1 carboxymethyl ester Chemical class 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 239000013553 cell monolayer Substances 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000003113 dilution method Methods 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- BFMYDTVEBKDAKJ-UHFFFAOYSA-L disodium;(2',7'-dibromo-3',6'-dioxido-3-oxospiro[2-benzofuran-1,9'-xanthene]-4'-yl)mercury;hydrate Chemical compound O.[Na+].[Na+].O1C(=O)C2=CC=CC=C2C21C1=CC(Br)=C([O-])C([Hg])=C1OC1=C2C=C(Br)C([O-])=C1 BFMYDTVEBKDAKJ-UHFFFAOYSA-L 0.000 description 1
- NAGJZTKCGNOGPW-UHFFFAOYSA-N dithiophosphoric acid Chemical compound OP(O)(S)=S NAGJZTKCGNOGPW-UHFFFAOYSA-N 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 206010014599 encephalitis Diseases 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000002073 fluorescence micrograph Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 102000034287 fluorescent proteins Human genes 0.000 description 1
- 108091006047 fluorescent proteins Proteins 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 210000002980 germ line cell Anatomy 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 239000003547 immunosorbent Substances 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 210000004324 lymphatic system Anatomy 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- YACKEPLHDIMKIO-UHFFFAOYSA-L methylphosphonate(2-) Chemical compound CP([O-])([O-])=O YACKEPLHDIMKIO-UHFFFAOYSA-L 0.000 description 1
- 210000005087 mononuclear cell Anatomy 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 238000007857 nested PCR Methods 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 238000003752 polymerase chain reaction Methods 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 230000001124 posttranscriptional effect Effects 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 210000005211 primary lymphoid organ Anatomy 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 210000001938 protoplast Anatomy 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 1
- 208000015347 renal cell adenocarcinoma Diseases 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 108010056030 retronectin Proteins 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 210000005212 secondary lymphoid organ Anatomy 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 108091008023 transcriptional regulators Proteins 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 238000005199 ultracentrifugation Methods 0.000 description 1
- 229940035893 uracil Drugs 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
- C07K16/1036—Retroviridae, e.g. leukemia viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
- C07K16/1036—Retroviridae, e.g. leukemia viruses
- C07K16/1045—Lentiviridae, e.g. HIV, FIV, SIV
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0635—B lymphocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/05—Adjuvants
- C12N2501/056—Immunostimulating oligonucleotides, e.g. CpG
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/125—Stem cell factor [SCF], c-kit ligand [KL]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/145—Thrombopoietin [TPO]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/22—Colony stimulating factors (G-CSF, GM-CSF)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/26—Flt-3 ligand (CD135L, flk-2 ligand)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/52—CD40, CD40-ligand (CD154)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/13—Coculture with; Conditioned medium produced by connective tissue cells; generic mesenchyme cells, e.g. so-called "embryonic fibroblasts"
- C12N2502/1394—Bone marrow stromal cells; whole marrow
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
- C12N2510/02—Cells for production
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Virology (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Medicinal Chemistry (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- AIDS & HIV (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
本出願は、特許法合衆国法典第35巻(35U.S.C.)§119(e)の基、2008年11月21日に出願した米国出願第61/199,932号を主張し、本明細書に参考文献として明確に組み込むものとする。
本出願は、電子形式にて配列表と共に出願している。配列表は、2009年11月19日に作成され、サイズ4.0KbのSEQLISTING.TXTと称するファイルとして提供する。配列表の電子形式の情報を、本明細書に参考文献としてそれを完全に組み込むものとする。
本出願は、一般的に免疫および遺伝子導入の分野に関する。より詳細には、本出願は、プログラミングヒトB細胞が関連のある抗体を生成する生体外におけるヒトBリンパ球生成培養システムに関する。
抗体は、感染症と戦い、病原因子を取り除くことにおいて重要な役割を果たす免疫系によって産生される自然発生のタンパク質である。抗体は、それらの機能を、タンパク質または非タンパク質抗原を結合し、防御反応を誘発することによって発揮する。
本出願は、抗体産生B細胞を生体外において生成するためのシステム、方法および組成物を提供する。本明細書に記載のシステムおよび方法に従って生成される抗体産生B細胞は、治療、診断、産業、法医学的および環境への適用を含有する多岐に渡る実用性を有する。いくつかの非制限的例の実用性は、病原体に対する生命体の免疫反応への刺激;特定の疾病または疾患、例えば病原性感染症であり、HIV感染等または癌に対する免疫反応の提供;および特定の疾病、疾患の検出および/または特定の疾病、疾患の進行のモニタリングである。本明細書に記載のシステムおよび方法に従って産生された抗体を、例えば法医学的/環境のサンプルにおける生命体および/または抗原(例えば、ポリペプチド、炭水化物、脂質または核酸)の存在の同定、酵素の活性化状態の検出の同定ならびに精製されたタンパク質の産生の同定に、適用して使用することができる。
本出願のいくつかの実施形態は、生体外における抗体産生B細胞の集団を生成するシステム、方法および組成物に関する。抗体産生B細胞の集団を、標的細胞の集団、好ましくは造血幹/前駆細胞(HSPC)の集団から生成することができる。いくつかの実施形態において、ヒトB系統発生を、HSPCから抗体産生B細胞までで、形質芽球および/または血漿細胞を含有して支持する生体外の培養システムを提供する。
特に規定しない限り、本明細書において使用した専門的且つ科学的な用語は、本発明が帰属する当業者に一般的に理解されるような同様の意味を有する。例えばSingleton et al., Dictionaiy of Microbiology and Molecular Biology 2nd ed., J. Wiley & Sons (New York, NY 1994);Sambrook et al., Molecular Cloning, A Laboratory Manual, Cold Springs Harbor Press (Cold Springs Harbor, NY 1989)を参照とする。本明細書に記載のものと同様または同等のあらゆる方法、装置および成分を、本明細書に開示した実施形態の実施で使用することができる。
本明細書に使用したように、「ポリヌクレオチドデリバリーシステム」は、ポリヌクレオチド、特に抗体をコード化するポリヌクレオチドを標的細胞内に導入することが可能であるあらゆるシステムである。ポリヌクレオチドデリバリーシステムは、ウイルス性および非ウイルス性のデリバリーシステムの双方を含有する。当業者は、特定の抗体をコード化するポリヌクレオチドを標的細胞内に効果的に導入ために使用することができるポリヌクレオチドデリバリーシステムの種類を決定することが可能であるだろう。
ポリヌクレオチドデリバリーシステムは、1以上のベクターを含むことができる。ベクターは、抗体をコード化するポリヌクレオチド配列、コード化配列の発現を導く1以上の制御要素と任意に関連のあるものを含有することができる。真核生物細胞発現ベクターは、従来技術にて知られていて、数々の市販の資源から利用できる。抗体をコード化するポリヌクレオチド配列が実施可能な状態で結合するベクターおよび/または発現制御配列の選択は、従来技術にて良く知られているように、例えばタンパク質発現といった所望の機能的特徴および形質転換される標的細胞に直接依存する。本発明で予測される好ましいベクターは、標的細胞の染色体内に抗体をコード化するポリヌクレオチドの挿入、および抗体をコード化するポリヌクレオチドによってコード化される抗体の発現を導くことができる。
標的細胞は、生殖細胞系細胞および細胞株と体細胞およびその細胞株との双方を含有する。標的細胞は、いずれかの複製起点から由来する幹細胞であることができる。標的細胞が生殖細胞系細胞であるとき、標的細胞が単一細胞胚および胚性幹細胞(ES)からなる群から選択されることが好ましい。標的細胞が体細胞であるとき、細胞は例えばプレB、プロB、未成熟、ナイーブB細胞および活性化B細胞を含有するが、これらに限定されない未成熟または成熟したリンパ球を含む。
以下に記載するように、本明細書に開示したような抗体産生B細胞を生成する方法は、疾病または疾患の検出および/または疾病または疾患の進行の観測に実用的である関連の抗体を生成することができる。本明細書にて使用したように、「診断」という語句は、疾病または疾患の存在または性質を同定することとする。疾病または疾患と関連のある抗原(例えば、抗原タンパク質、抗原核酸配列、抗原ペプチド、抗原脂質、抗原炭水化物および抗原小分子)の検出は、疾病または疾患の診断の手段を提供する。前記検出法を、例えば状態の初期診断で使用して、対象が疾病または疾患を罹るかどうかを決定し、疾病または疾患の進行、治療プロトコルの進行を観測し、疾病または疾患の重症度を評価し、疾病または疾患の予後および/または回復の見込みを予測するか、または対象のための適切な治療を決定の補助することが可能である。検出は生体外または生体内にて発生することができる。
以下の実験方法を下記の実施例1〜4に使用した。
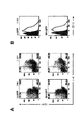
抗HFV抗体b12の軽鎖および重鎖の可変配列を増幅し、ヒトκ鎖定常部および分泌IgG1定常部の上流にそれぞれ挿入した。2つの結果として生じる遺伝子は、自己切断F2Aペプチドによって結合し、バイシストロニックユニットを形成した。その後結合した遺伝子を、FUWレンチウイルスベクター内にサブクローンし、ユビキチンCプロモーター(U)を含有するレンチウイルスベクターFUW−b12(本明細書にて「U−b12」ともする)を作成した(図1B)。また、FMHWレンチウイルスベクターを、マトリックス会合領域(MAR)の側面に位置されるEμエンハンサーの前に、FUW内のユビキチンCプロモーターをヒトμ重鎖プロモーター(MHプロモーター)と置換することによって構成した。同様に、FEEKWベクターを、エンハンサーおよびMARの前に、FUW内のユビキチンCプロモーターを、ヒトκ軽鎖プロモーター(EEKプロモーター)を置換することによって構成した。その後b12のバイシストロニックユニットを、FMHWおよびFEEKW内にサブクローンし、レンチウイルスベクターFMHW−b12(本明細書において「MH−b12」ともする)およびFEEKW−b12(本明細書において「EEK−b12」ともする)をそれぞれ生成した(図1B)。さらに緑色蛍光タンパク質(GFP)を、FUW、FMHWおよびFEEKW内にサブクローンし、レンチウイルスベクターFUWG(本明細書において「U−GFP」ともする)、FMHWG(また本明細書において「MH−GFP」ともする)およびFEEKWG(本明細書において「EEK−GFP」ともする)を生成した。全てのコンストラクトを、Nalm−6(プレB)、Ramos(ナイーブB)、Dakiki(形質細胞腫)およびJurkat細胞株にて、ヒトHSPC内に導入する前に試験した。
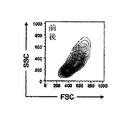
レンチウイルスを、リン酸カルシウム沈殿物によるHEK293T細胞のトランスフェクションによって生成した。高滴定濃度ウイルスを調製するため、ウイルスの上清を超遠心分離によって90分間、5000×gで濃縮した。ヒト臍帯血CD34+HSPCを感染の前24時間未満で、10%ウシ胎仔血清およびサイトカインを含有するIscove’s modified Dulbecco medium(IMDM)にて保持した。サイトカインは、ヒト組み換え型インターロイキン−3(IL−3;10ng/mL)、Flt3リガンド(10ng/mL)、トロンボポエチン(10ng/mL)、幹細胞因子(SCF;5ng/mL)、および顆粒白血球コロニー刺激因子(G−CSF;5ng/mL)を含み、感染中一日おきに与えた。濃縮レンチウイルス粒子による感染多重度で0.3〜0.4×106のHSPC/穴の1000の2つの一連の感染を、Retronectin50μg/mLでプレコートした48穴プレートにて実行した。HSPCを感染後3日目に収集し、フローサイトメトリーによって分析した。感染細胞は、それらの前駆表現型を維持した。
全ヒトIgM、IgGおよびIgAを、商業用酵素結合の免疫吸着剤分析(ELISA)のキットを使用して分析した。b12−IgG1を検出するためのELISAを、Selvarajah et al., J Virol., 2005, 79:12148-12163から修正した。分析にて、プレートを、一晩、4℃にて単量体gp120MN、2μg/mLで、リン酸緩衝生理食塩水(PBS)内で被覆した。穴を、0.05%のTween−20を含むPBS(PBS−T)で洗浄し、3%ウシ血清アルブミン(BSA)で、1時間、室温にて阻害した。BSAを吸引後、サンプルの希釈剤、および1%BSAを含むPBS−Tにおけるb12標準を添加し、37℃にて3時間インキュベートした。b12標準培地を、293T細胞とU−b12をトランスフェクションすることによって得て、その濃度をBiacore gp120結合分析によって測定した。穴を再度洗浄し、セイヨウワサビペルオキシダーゼと結合するヤギ抗ヒトIgG F(ab’)2を1:1000で希釈して添加し、1時間37℃にてインキュベートした。プレートを3,3’,5,5’−テトラメチルベンジジン溶液の添加によって発現した。2MのH2SO4を添加することによって、反応を中止し、プレートを450nmでSpectroMax Reader上にて読み込んだ。
プロウイルスのコピー数を、修飾されたAlu長い末端反復(LTR)ネステッド−ポリメラーゼ連鎖反応(PCR)のプロトコルで測定した。PCRの最初のラウンドは、Alu配列(Alu-fw: 5'- TCCCAGCTACTGGGGAGGCTGAGG-3')およびウイルスが組み込まれた後の5’LTRのすぐ下流の配列(PBS-bw: 5'-GAGTCCTGCGTCGAGAGAG-3')の間で最長3kbまでの増幅を可能とした。第二ラウンドは、SYBR greenに基づく定量PCRを使用して、プロウイルスLTRの143bp配列を検出した(late-RT-fw: 5'-TGTGTGCCCGTCTGTTGTGT-3'およびlate-RT-bw: 5'- GAGTCCTGCGTCGAGAGAGC-3')。検量線を確立するため、組み込まれたgDNA標準を、6ヶ月間維持した組み込みFUWで安定なTHP−I細胞株からgDNAを抽出することによって生成し、標準gDNAにおけるプロウイルスのコピー数を、線状FUWプラスミドの連続希釈法をLTRコピーの既知の数で使用して決定した。無関係なベクトルで形質導入されたTHP−1株のゲノムDNAを、陰性対照として使用した。β−グロビンをローディングコントロールとして使用した。前記Alu−LTRネステッドPCRのプロトコルの検出範囲は、50ngのgDNAにつき500〜6×104コピーである。B細胞発生の異なる段階におけるゲノムDNAの量および細胞数の間の相互関係を、実験的に決定した。
第一段階:B系統関与のための刺激、およびHSPCのレンチウイルス形質導入によるヒトB細胞のプログラミング
この実施例において、CD34+臍帯血細胞を、前記工程(a)にてレンチウイルスコンストラクトとトランスフェクションし、前記工程(b)にて約5日間B系統発生で刺激して、B細胞刺激因子、例えばIL−3、Flt3リガンド、トロンボポエチン、SCFおよびG−CSFの存在下で関与した。
第二段階:刺激したHSPCからMS5間質細胞でヒトB細胞の発生
この実施例において、B系統成長因子IL−7を発現するネズミの間質MS5細胞を使用して、工程(c)にて刺激したHSPCから、ヒトのプロB、プレBおよび未成熟B細胞の、一連の生成を支持した。刺激したCD34+HSPCを、3〜4週間MS5細胞で培養した後、HSPC23〜28%が、プロB細胞となった。またインキュベーションから更に2〜3週間後、CD19+細胞65〜69%は、プレBおよび未成熟B細胞の混合物を示した。
第三段階:生体外における発生したヒトB細胞の活性化および血漿細胞分化
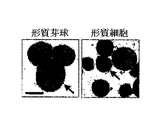
この実施例において、IL−2、IL−10およびCpG DNAを含むB細胞活性剤を、CD40Lを発現するMS5細胞と共に使用して、プロB、プレBおよび未成熟B細胞の活性化および最終分化を形質芽球および形質細胞に支持した。MS40L細胞との共培養2〜3週以内に、第2段階から得たB細胞約90%は、抗体分泌形質芽球(35〜37%)および形質細胞(16〜23%)を含有する活性化B細胞内に発生した。
抗HIV抗体b12−IgG1を産生するためのヒトB細胞のプログラミング
生体外培養システムの異なる時点でB細胞のゲノムDNAにおける、組み込まれたレンチウイルスの分析は、プロウイルスがB細胞発生を通して存在することを示した(図10)。明らかに生存し且つ発生した組み込み部位をもたらす細胞は、第3段階の終わりで細胞あたりのプロウイルスコピー数のように、平均的にはそれらの前駆細胞のものから統計学的に異ならなかった(P=0.26)。これは、抗HIV中和抗体をコード化するレンチウイルスの安定した組み込みを、HSPCから抗体分泌B細胞まで維持することができることを示唆した。
刺激されていないHSPCからのIg分泌ヒトB細胞の発生
ヒト臍帯血からのCD34+細胞を播種し、B系統成長因子IL−7を発現するMS5ネズミ間質細胞単分子層上にて培養した。細胞培養を週2回行い、新鮮な培地を添加したり、次に培養穴からの培地80%を吸引し、新鮮な培地を添加した。細胞培養を、CD19+細胞の出現に関して観察した。細胞集団の有意なパーセンテージが、CD34−CD19+になるとき、長期の培養細胞を収集し、MiniMacs細胞分離システムを使用して、CD19+細胞を増加させた。
プロB、プレBおよび/または未成熟B細胞から抗体産生ヒトB細胞への発生
プロB、プレBまたは未成熟B細胞を播種し、B系統成長因子IL−7を発現するMS5ネズミ間質細胞単分子層上で培養した。細胞培養を週に2回行い、新鮮な培地を添加したり、培養穴から培地80%を吸引し、新鮮な培地を添加した。細胞培養を、CD19+μ+δ+細胞の増加に関して観察した。細胞集団の有意なパーセンテージが、CD19+μ+δ+になるとき、細胞を収集し、MiniMacs細胞分離システムを使用して、CD19+μ+δ+細胞を増加した。
ナイーブB細胞から抗体産生ヒトB細胞への発生
関連の抗体をコード化する遺伝子をもたらすナイーブB細胞を播種し、IL−2、IL−10およびCpG DNAを含有するB細胞活性剤の存在で、CD40L(例えば、MS40L−低およびMS40L−高)を発現するMS5細胞と共に、実施例3に記載したように培養した。関連の抗体をコード化する遺伝子を、ナイーブB細胞内に、従来の遺伝子デリバリー技術、例えば関連の抗体がコード化される遺伝子を含有するレンチウイルスベクターとナイーブB細胞をトランスフェクションすることによって導入した。MS5細胞は、関連の抗体を産生する形質芽球および形質細胞に、ナイーブB細胞の活性化および末端分化を支持すると予期した。
Claims (25)
- 抗体産生B細胞の集団を生体外にて生成する方法において、
(a)血液生成の幹細胞/前駆細胞(HSPC)の集団と生体外にてポリヌクレオチドデリバリーシステムを接触させ、前記ポリヌクレオチドデリバリーシステムは関連の抗体をコード化するポリヌクレオチドを含む工程と;
(b)1以上のB系統成長因子を発現する第一支持細胞の集団とHSPCを、HSPCの少なくとも約20%がCD19+μ+になるまで共培養する工程と;
(c)前記工程(b)で得られたCD19+μ+細胞とCD40Lを発現する第二支持細胞の集団を、1以上のB細胞の活性剤の存在下にて、CD19+μ+細胞の少なくとも約20%が関連の抗体を産生するB細胞になるまで共培養する工程と
を含有する方法。 - HSPCは、臍帯血からのCD34+細胞である、請求項1に記載の方法。
- HSPCは一次骨髄細胞である、請求項1に記載の方法。
- (d)HSPCを1以上のB細胞刺激因子の存在下にて、前記工程(b)の前に培養することをさらに含有する、請求項1に記載の方法。
- 少なくとも1つのB細胞刺激因子は、IL−3、Flt3リガンド、トロンボポイエチン、幹細胞因子(SCF)、顆粒白血球コロニー刺激因子(G−CSF)、顆粒白血球コロニー刺激因子(GM−CSF)、IL−7およびIL−11からなる群から選択される、請求項4に記載の方法。
- HSPCを、B細胞刺激因子IL−3、Flt3リガンド、トロンボポイエチン、SCFおよびG−CSFの存在下にて培養する、請求項4に記載の方法。
- HSPCを、1以上のB系統成長因子を発現する第一支持細胞の集団と、HSPC少なくとも約30%がCD19+μ+になるまで共培養する、請求項4に記載の方法。
- 第一支持細胞は、間質細胞である、請求項1に記載の方法。
- 第一支持細胞は、B系統成長因子IL−7を発現する間質細胞である、請求項8に記載の方法。
- 少なくとも1つのB細胞活性剤は、CpG DNA、IL−2、IL−10、IL−15、IL−6、IFNαおよび抗CD40Lからなる群から選択される、請求項1に記載の方法。
- B細胞活性剤は、CpG DNA、IL−2およびIL−10である、請求項10に記載の方法。
- B細胞活性剤の1つは、CpG DNAである、請求項10に記載の方法。
- 工程(b)から得られたCD19+μ+細胞の少なくとも約40%は、CD19+μ+VプレB +プレB細胞またはCD19+μ+κ/λ+未成熟B細胞である、請求項1に記載の方法。
- 関連の抗体を産生するB細胞の少なくとも約40%は、抗体分泌形質芽球および形質細胞である、請求項1に記載の方法。
- ポリヌクレオチドデリバリーシステムは、レトロウイルスベクターである、請求項1に記載の方法。
- レトロウイルスベクターは、レンチウイルスベクターである、請求項15に記載の方法。
- レンチウイルスベクターは、B細胞特異的プロモーターを含む、請求項16に記載の方法。
- B細胞特異的プロモーターは、EKKプロモーターである、請求項17に記載の方法。
- B細胞の集団を生体外にて生成する方法において、
(a)血液生成の幹細胞/前駆細胞(HSPC)の集団を、1以上のB刺激因子の存在下にて培養する工程と、
(b)HSPCと、1以上のB系統成長因子を発現する第一支持細胞を共培養する工程と、
(c)前記工程(b)から得られたCD19+μ+細胞とCD40Lを発現する第二支持細胞の集団を、1以上のB細胞活性剤の存在下にて共培養することと
を含有する方法。 - B細胞刺激因子は、IL−3、Flt3リガンド、トロンボポイエチン、SCFおよびG−CSFから選択される、請求項19に記載の方法。
- HSPCを、前記工程(b)にて第一支持細胞の集団と、HSPCの少なくとも約20%がCD19+μ+になるまで共培養する、請求項19に記載の方法。
- CD19+μ+細胞を、前記工程(c)にて第二支持細胞の集団と、1以上のB細胞活性剤の存在下にて、CD19+μ+細胞の20%が活性化B細胞になるまで共培養する、請求項19に記載の方法。
- 抗体産生B細胞を生成する方法において、
標的細胞の集団を生体外にてポリヌクレオチドデリバリーシステムとトランスフェクションする工程であって、前記ポリヌクレオチドデリバリーシステムは関連の抗体をコード化するポリヌクレオチドである工程と;
標的細胞とCD40Lを発現する支持細胞の集団を、1以上のB細胞活性剤の存在下にて、標的細胞の少なくとも約20%が関連の抗体を産生するB細胞になるまで共培養する工程と
を含有する方法。 - 標的細胞は、プロB、プレB、未成熟BおよびナイーブB細胞から選択される、請求項23に記載の方法。
- 少なくとも1つのB細胞活性剤は、CpG DNA、IL−2、IL−10、IL−15、IL−6、IFNαおよび抗CD40Lからなる群から選択される、請求項23に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US19993208P | 2008-11-21 | 2008-11-21 | |
| US61/199,932 | 2008-11-21 | ||
| PCT/US2009/065217 WO2010059876A2 (en) | 2008-11-21 | 2009-11-19 | In vitro human b lymphopoiesis culture system |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012509666A true JP2012509666A (ja) | 2012-04-26 |
| JP2012509666A5 JP2012509666A5 (ja) | 2013-01-10 |
| JP5726744B2 JP5726744B2 (ja) | 2015-06-03 |
Family
ID=42198808
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011537633A Active JP5726744B2 (ja) | 2008-11-21 | 2009-11-19 | 生体外におけるヒトbリンパ球産生培養システム |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8133727B2 (ja) |
| EP (1) | EP2358868B1 (ja) |
| JP (1) | JP5726744B2 (ja) |
| WO (1) | WO2010059876A2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016513476A (ja) * | 2013-03-14 | 2016-05-16 | イミュソフト コーポレーション | インビトロでのメモリーb細胞分化方法およびvsv−g偽型ウイルスベクターを用いる形質導入方法 |
| JP2019054804A (ja) * | 2012-05-04 | 2019-04-11 | ファイザー・インク | 前立腺関連抗原およびワクチンに基づく免疫療法レジメン |
| JP2022132351A (ja) * | 2015-04-03 | 2022-09-08 | デイナ ファーバー キャンサー インスティチュート,インコーポレイテッド | B細胞のゲノム編集のための組成物及び方法 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9074223B2 (en) | 2010-01-08 | 2015-07-07 | Immusoft Corporation | Vectors and methods for transducing B cells |
| US20140134638A1 (en) * | 2012-11-13 | 2014-05-15 | Genentech, Inc. | Enrichment of antigen-specific plasmablasts |
| EP4177336A1 (en) | 2014-12-19 | 2023-05-10 | Immusoft Corporation | B cells for in vivo delivery of therapeutic agents |
| JP7215994B2 (ja) | 2016-09-06 | 2023-01-31 | ザ チルドレンズ メディカル センター コーポレーション | 人工多能性幹細胞由来の免疫細胞 |
| WO2018102612A1 (en) | 2016-12-02 | 2018-06-07 | Juno Therapeutics, Inc. | Engineered b cells and related compositions and methods |
| WO2019178613A1 (en) | 2018-03-16 | 2019-09-19 | Immusoft Corporation | B cells genetically engineered to secrete follistatin and methods of using the same to treat follistatin-related diseases, conditions, disorders and to enhance muscle growth and strength |
| CN109234232A (zh) * | 2018-09-30 | 2019-01-18 | 杭州华安单抗生物技术有限公司 | 兔外周血b细胞的培养体系及培养方法、抗体的制备方法和应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005525800A (ja) * | 2001-12-22 | 2005-09-02 | 4−アンチボディ アーゲー | 遺伝的に修飾された脊椎動物前駆体リンパ球の生成方法及び異種結合タンパク質の産生を目的としたその使用。 |
| US20070116690A1 (en) * | 2001-12-10 | 2007-05-24 | Lili Yang | Method for the generation of antigen-specific lymphocytes |
| WO2007134220A2 (en) * | 2006-05-11 | 2007-11-22 | University Of Maryland Biotechnology Institute | A general method for generating human antibody responses in vitro |
-
2009
- 2009-11-19 WO PCT/US2009/065217 patent/WO2010059876A2/en active Application Filing
- 2009-11-19 JP JP2011537633A patent/JP5726744B2/ja active Active
- 2009-11-19 EP EP09828251.0A patent/EP2358868B1/en active Active
- 2009-11-19 US US12/622,379 patent/US8133727B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070116690A1 (en) * | 2001-12-10 | 2007-05-24 | Lili Yang | Method for the generation of antigen-specific lymphocytes |
| JP2005525800A (ja) * | 2001-12-22 | 2005-09-02 | 4−アンチボディ アーゲー | 遺伝的に修飾された脊椎動物前駆体リンパ球の生成方法及び異種結合タンパク質の産生を目的としたその使用。 |
| WO2007134220A2 (en) * | 2006-05-11 | 2007-11-22 | University Of Maryland Biotechnology Institute | A general method for generating human antibody responses in vitro |
Non-Patent Citations (5)
| Title |
|---|
| JPN6014018360; Fluckiger et al: Blood VOl. 92, No. 12, 19981215, p. 4509-4520 * |
| JPN6014018362; Johnson et al: The journal of immunology Vol. 175, 2005, p. 7325-7331 * |
| JPN6014018367; Grassinger et al: Eur J Haematol Vol. 77, 2006, p. 134-144 * |
| JPN6014018370; Nishihara et al: Eur J Immunol Vol. 28, 1998, p. 855-864 * |
| JPN6014018373; Luo et al: Blood Vol. 113, No. 7, 20081204, p. 1422-1431 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019054804A (ja) * | 2012-05-04 | 2019-04-11 | ファイザー・インク | 前立腺関連抗原およびワクチンに基づく免疫療法レジメン |
| JP2016513476A (ja) * | 2013-03-14 | 2016-05-16 | イミュソフト コーポレーション | インビトロでのメモリーb細胞分化方法およびvsv−g偽型ウイルスベクターを用いる形質導入方法 |
| JP2018075039A (ja) * | 2013-03-14 | 2018-05-17 | イミュソフト コーポレーション | インビトロでのメモリーb細胞分化方法およびvsv−g偽型ウイルスベクターを用いる形質導入方法 |
| JP2022132351A (ja) * | 2015-04-03 | 2022-09-08 | デイナ ファーバー キャンサー インスティチュート,インコーポレイテッド | B細胞のゲノム編集のための組成物及び方法 |
| JP7463442B2 (ja) | 2015-04-03 | 2024-04-08 | デイナ ファーバー キャンサー インスティチュート,インコーポレイテッド | B細胞のゲノム編集のための組成物及び方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2358868A2 (en) | 2011-08-24 |
| WO2010059876A3 (en) | 2010-10-14 |
| US8133727B2 (en) | 2012-03-13 |
| WO2010059876A2 (en) | 2010-05-27 |
| EP2358868A4 (en) | 2012-09-05 |
| EP2358868B1 (en) | 2014-11-12 |
| JP5726744B2 (ja) | 2015-06-03 |
| US20100203630A1 (en) | 2010-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5726744B2 (ja) | 生体外におけるヒトbリンパ球産生培養システム | |
| Luo et al. | Engineering human hematopoietic stem/progenitor cells to produce a broadly neutralizing anti-HIV antibody after in vitro maturation to human B lymphocytes. | |
| US7939059B2 (en) | Method for the generation of antigen-specific lymphocytes | |
| KR100445712B1 (ko) | 바이러스-매개된dna전이를증가시키기위한작제물및이를위한배양배지 | |
| US20230203537A1 (en) | Stable pseudotyped lentiviral particles and uses thereof | |
| CN105316362B (zh) | 一种Dual-RMCE介导的TCR基因置换系统及其方法 | |
| JP2011527905A (ja) | Bright/arid3a機能の阻害による多能性細胞の作製方法 | |
| Fusil et al. | A lentiviral vector allowing physiologically regulated membrane-anchored and secreted antibody expression depending on B-cell maturation status | |
| JP2021502799A (ja) | レトロウイルスベクター | |
| CN114230658B (zh) | 新型冠状病毒特异性t细胞受体和其用途 | |
| JP2024019533A (ja) | 膜結合型IL-10を発現する遺伝子的にリプログラミングされたTreg | |
| WO2011052545A1 (ja) | 抗原特異的b細胞集団の製造方法 | |
| JP2022530139A (ja) | 同種異系car-t細胞、その調製及び応用 | |
| CN113195712A (zh) | 突变型piggyBac转座酶 | |
| US12084681B2 (en) | Ex vivo antibody production | |
| JP2022501067A (ja) | Bcma及びcd19を標的とするキメラ抗原受容体、並びにその使用 | |
| JP2024050551A (ja) | マウス定常領域を伴うtcrを発現する細胞を選択的に増幅するための方法 | |
| WO2021259334A1 (zh) | 自我调节型嵌合抗原受体及其在肿瘤免疫中的应用 | |
| JP2019509729A (ja) | 抗体産生のためにb細胞を拡張及び分化する方法 | |
| EP2470562A1 (en) | Production of monoclonal antibodies in vitro | |
| JP6684211B2 (ja) | B細胞集団の製造方法 | |
| US20130196380A1 (en) | In vitro process for the preparation of antibodies of the igg type | |
| JP2021500905A (ja) | ベクター | |
| JP2022540012A (ja) | SIRPαがサイレンシングされたナチュラルキラー(NK)細胞 | |
| Kvell | Examination of B cell and virus interactions through transformation by a pathogen (EBV) and transduction by a lentiviral vector (HIV-1) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121113 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121113 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140507 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140804 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140811 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140903 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150310 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150401 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5726744 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |