JP2012144452A - 抗真菌剤 - Google Patents
抗真菌剤 Download PDFInfo
- Publication number
- JP2012144452A JP2012144452A JP2011002077A JP2011002077A JP2012144452A JP 2012144452 A JP2012144452 A JP 2012144452A JP 2011002077 A JP2011002077 A JP 2011002077A JP 2011002077 A JP2011002077 A JP 2011002077A JP 2012144452 A JP2012144452 A JP 2012144452A
- Authority
- JP
- Japan
- Prior art keywords
- group
- carbon atoms
- malassezia
- acid
- antifungal agent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Cosmetics (AREA)
Abstract
Description
従って、従来から硫化セレン、硫化カドミウム、ジンクピリジニウム−1−チオール−N−オキサイド、オクトピロックスなどの抗菌剤や、殺菌剤を添加した頭髪化粧料がフケ防止用頭髪化粧料として使用されてきた。
しかしながら、これらの脂肪酸がマラセチア属菌に対して抗菌性を示すことやフケ抑制剤として使用できることは全く知られていない。
1)下記の一般式(1):
で表される脂肪酸誘導体又はその塩を有効成分とするマラセチア属菌に対する抗真菌剤。
2)Xが炭素数4〜10のアルキル基であり、Yが炭素数1〜7のアルキレン基である上記1)の抗真菌剤。
3)マラセチア属菌が、マラセチア・フルフル(Malassezia furfur)である上記1)又は2)の抗真菌剤。
4)下記の一般式(1):
で表される脂肪酸誘導体又はその塩を有効成分とするフケ抑制剤。
5)上記1)の抗真菌剤又は上記4)のフケ抑制剤を含有する皮膚外用剤。
尚、下記式中、Zで示されるハロゲン原子としては、フッ素原子、塩素原子、臭素原子が挙げられ、このうち臭素原子が好ましい。
当該反応は、溶媒存在下又は非存在下に行うことができる。
溶媒を使用する場合の溶媒は、反応に影響を及ばさないものであれば特に限定されないが、例えば、テトラヒドロフラン、ジエチルエーテル、ジメチルエーテル、メトキシエタン、t−ブチルメチルエーテル、イソプロピルエーテル、ジオキサン等のエーテル類;ヘキサン、シクロヘキサン、ヘプタン、イソオクタン、デカン等の炭化水素類;ベンゼン、トルエン、キシレンのような芳香族炭化水素類及びこれらの混合物等が挙げられる。
ここで、抗菌活性を有するとは、例えば抗菌性評価においてコントロールに比して菌数を1/10以下に減少させることをいい、抗菌活性を有しないとは、例えば抗菌性評価においてコントロールに比して菌数を1/10以下に減少させないことをいう。
また、当該医薬には、他の薬効成分、例えば鎮痛消炎剤、殺菌消毒剤、収斂剤、皮膚軟化剤、ホルモン剤、抗生物質等を必要に応じて適宜配合することができる。
窒素雰囲気下、デカノール20mLに水酸化カリウム2.4g(40mmol)を添加し、80℃にて加熱攪拌、水酸化カリウムが溶解後、6-ブロモヘキサン酸2.0g(10mmol)を添加し、100℃に昇温した。GC分析にて原料6-ブロモヘキサン酸の消失を確認した後、クロロホルム50mL、1N硫酸25mL(50mmol)を加え、酸性化し、水洗を行なった。濃縮後、蒸留にて主留分を得たが(GC純度94%)、着色していたためシリカゲルカラム精製を行ない、下記の6-デシロキシ-ヘキサン酸(化合物1)1.7g(GC純度98%、収率64%)を得た。
IR(cm-1, ATR法) : 2924, 2854, 1709, 1465, 1114;
1H-NMR(CDCL3, ppm) : 0.85(t, J=7Hz, 3H), 1.20-1.47(m, 16H), 1.52-1.70(m, 6H), 2.33 (t, J=8Hz, 2H), 3.35-3.45(m, 4H).
製造例1と同様にして、6-ブロモヘキサン酸を2-クロロ酢酸に変更して、2-デシロキシ-酢酸(化合物2)1.5g(GC純度99%、収率15%)を合成した。
IR(cm-1, ATR法) : 2915, 2848, 1698, 1470, 1130;
1H-NMR(CDCL3, ppm) : 0.85(t, J=7Hz, 3H), 1.18-1.36(m, 14H), 1.57-1.65(m, 2H), 3.52 (t, J=7Hz, 2H), 4.09(s, 2H).
製造例1と同様にして、デカノールの代わりにオクタノール、6-ブロモヘキサン酸を2-ブロモプロピオン酸に変更して、2-メチル-2-オクチロキシ-酢酸(化合物3)3.2g(GC純度90%、収率53%)を合成した。
IR(cm-1, ATR法) : 2925, 2856, 1717, 1458, 1125 ;
1H-NMR(CDCL3, ppm) : 0.86(t, J=7Hz, 3H), 1.18-1.36(m, 10H), 1.43(d, J=7Hz, 3H), 1.56-1.63(m, 2H), 3.42-3.48(m, 1H), 3.51-3.57(m, 1H), 3.98(q, J=7Hz, 1H).
製造例1と同様にして、6-ブロモヘキサン酸を2-ブロモプロピオン酸に変更して、2-デシロキシ-2-メチル-酢酸(化合物4)2.7g(GC純度90%、収率27%)を合成した。
IR(cm-1, ATR法) : 2923, 2855, 1720, 1458, 1126 ;
1H-NMR(CDCL3, ppm) : 0.86(t, J=7Hz, 3H), 1.18-1.36(m, 14H), 1.43(d, J=7Hz, 3H), 1.56-1.63(m, 2H), 3.42-3.48(m, 1H), 3.51-3.57(m, 1H), 3.98(q, J=7Hz, 1H).
製造例1と同様にして、デカノールの代わりにオクタノールに変更して、下記の6-オクチロキシ-ヘキサン酸(化合物5)1.2g(GC純度、98%、収率50%)を合成した。
IR(cm-1, ATR法) : 2931, 2858, 1708, 1113 ;
1H-NMR(CDCL3, ppm) : 0.85(t, J=7Hz, 3H), 1.20-1.34(m, 10H), 1.35-1.43(m, 2H), 1.50−1.60(m, 4H), 1.60-1.67(m, 2H), 2.34(t, J=7Hz, 2H), 3.34-3.40(m, 4H).
製造例1と同様にして、デカノールの代わりにヘキサノールに変更して、下記の6-ヘキシロキシ-ヘキサン酸(化合物6)1.7g(GC純度、98%、収率77%)を合成した。
IR(cm-1, ATR法) : 2931, 2858, 1708, 1113 ;
1H-NMR(CDCL3, ppm) : 0.86(t, J=7Hz, 3H), 1.22-1.33(m, 6H), 1.35-1.42(m, 2H), 1.50-1.60(m, 4H), 1.60-1.67(m, 2H), 2.34(t, J=7Hz, 2H), 3.34-3.40(m, 4H).
製造例1と同様にして、デカノールの代わりにブタノール、6-ブロモヘキサン酸を8−ブロモオクタン酸に変更して、8-ブトキシ-オクタン酸(化合物7)1.8g(GC純度97%、収率29%)を合成した。
IR(cm-1, ATR法) : 2932, 2858, 1708, 1113 ;
1H-NMR(CDCL3, ppm) : 0.89(t, J=7Hz, 3H), 1.26-1.38(m, 8H), 1.49-1.57(m, 4H), 1.57-1.65(m, 2H), 2.32(t, J=7Hz, 2H), 3.34-3.40(m, 4H).
製造例1と同様にして、デカノールの代わりにエタノール、6-ブロモヘキサン酸を10−ブロモデカン酸に変更して、10-エトキシ-デカン酸(化合物8)1.3g(GC純度95%、収率35%)を合成した。
IR(cm-1, ATR法) : 2916, 2851, 1709, 1107 ;
1H-NMR(CDCL3, ppm) : 1.18(t, J=7Hz, 3H), 1.23-1.34(m, 10H), 1.50-1.57(m, 2H), 1.57-1.64(m, 2H), 2.32(t, J=8Hz, 2H), 3.38(t, J=7Hz, 2H), 3.44(q, J=7Hz, 2H).
製造例1と同様にして、デカノールの代わりにオクタノール、6-ブロモヘキサン酸を2−クロロ酢酸に変更して、2-オクチロキシ-酢酸(化合物9)1.0g(GC純度99%、収率19%)を合成した。
IR(cm-1, ATR法) : 2925, 2856, 1729, 1431, 1125;
1H-NMR(CDCL3, ppm) : 0.86(t, J=7Hz, 3H), 1.18-1.36(m, 10H), 1.57-1.65(m, 2H), 3.53 (t, J=7Hz, 2H), 4.09(s, 2H).
製造例1と同様にして、デカノールの代わりに2-ヘキシロキシ-エタノールに変更して、6-(2-ヘキシロキシ-エトキシ)-ヘキサン酸(比較化合物1)0.9g(GC純度99%、収率36%)を合成した。
IR(cm-1, ATR法) : 2931, 2860, 1736, 1708, 1458, 1115 ;
1H-NMR(CDCL3, ppm) : 0.86(t, J=7Hz, 3H), 1.20-1.50(m, 10H), 1.50-1.75(m, 4H), 2.32(t, J=7Hz, 2H), 3.39-3.54(m, 4H), 3.55(bs, 4H).
製造例1と同様にして、デカノールの代わりに2-ヘキシロキシ-エタノール、6-ブロモヘキサン酸を8-ブロモオクタン酸に変更して、8-(2-ヘキシロキシ-エトキシ)-オクタン酸(比較化合物2)1.9g(GC純度98%、収率65%)を合成した。
IR(cm-1, ATR法) : 2930, 2857, 1737, 1709, 1457, 1113 ;
1H-NMR(CDCL3, ppm) : 0.86(t, J=7Hz, 3H), 1.20-1.38(m, 12H), 1.50-1.65(m, 6H), 2.32(t, J=7Hz, 2H), 3.39-3.48(m, 4H), 3.55(bs, 4H).
(1)使用菌株
表皮ブドウ球菌としてStaphyllococus epidermidis NBRC12993、マラセチア菌としてMalassezia furfur NBRC101593を使用した。
表皮ブドウ球菌の培養にはSCD寒天培地(ダイゴ社製)を、マラセチア菌の培養にはYM寒天培地(DIFCO社製)又はYMOLP寒天培地(YM寒天4.1%、LP希釈液(ダイゴ社製)3.0%、オリーブ油1.0%)を使用した。菌体数の計測には、上記寒天培地にLP希釈液を添加させたものを使用した。
pH=6に調整した50mMリン酸緩衝液(1カリウム及び2カリウム)4.5mLにソルビタンモノステアレートを終濃度0.1%、サンプル濃度0.01%になるように添加した(コントロールはソルビタンモノステアレートのみを終濃度0.01%で添加)。30℃で2日間培養した表皮ブドウ球菌を生理食塩水に終濃度105〜107個/mLとなるように懸濁し、この懸濁液0.5mLを上記調製液に接種した。十分に混合し、所定時間30℃で放置した後、その液より50μL採取した。5mLのLP希釈液にて不活性化した後、LP希釈液にて適宜希釈して菌体数計測用寒天培地に塗布した。30℃で培養した後、生育したコロニー数を計測した。
その結果、表皮ブドウ球菌に対しては、どの化合物も抗菌性を示さなかった(図1、図2)。
pH=6に調整した50mMリン酸緩衝液(1カリウム及び2カリウム)4.5mLにソルビタンモノステアレートを終濃度0.01%、サンプル濃度0.01%〜0.1%になるように添加した(コントロールはソルビタンモノステアレートのみを終濃度0.01%で添加)。32℃で5日間培養したマラセチア菌を生理食塩水に終濃度105〜107個/mLとなるように懸濁し、この懸濁液0.5mLを上記調製液に接種した。十分に混合し、所定時間32℃で放置した後、その液より50μL採取した。5mLのLP希釈液にて不活性化した後、LP希釈液にて適宜希釈して菌体数計測用寒天培地に塗布した。32℃で培養した後、生育したコロニー数を計測した。
その結果、化合物1に濃度の上昇に伴い、抗マラセチア活性が認められた(図3)。
また、化合物2〜5についても高い抗マラセチア活性が認められた(図4)。
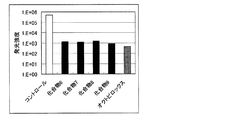
YM培地(+Tween-60 0.5%添加、10mL)に、マラセチア菌1白金耳を懸濁させたもの90μLを96wellプレートに注入し、さらに評価サンプル(10mMのエタノール溶液、N=2)10μL加え、恒温機で30℃1昼夜培養。培養後、ATP抽出/発光試薬(BacTiter-GloTM Microbial Cell Viability Assay)100μLを加え、発光量を測定した(WALLAC ARVOTMSX 1420 MULTILABEL COUNTER)。発光強度が弱いものほど、ATP量が少なく、抗菌活性が高いということになる。図5の棒グラフの高さは発光強度の対数表示で示した。ポジティブコントロールとして、オクトピロックス(Clariant Produkte)を用いた。
その結果、化合物6〜9にポジティブコントロールと同様に高いマラセチア菌抑制効果が認められた(図5)。
Claims (5)
- Xが炭素数4〜10のアルキル基であり、Yが炭素数1〜7のアルキレン基である請求項1記載の抗真菌剤。
- マラセチア属菌が、マラセチア・フルフル(Malassezia furfur)である請求項1又は2記載の抗真菌剤。
- 請求項1記載の抗真菌剤又は請求項4記載のフケ抑制剤を含有する皮膚外用剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011002077A JP5718064B2 (ja) | 2011-01-07 | 2011-01-07 | 抗真菌剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011002077A JP5718064B2 (ja) | 2011-01-07 | 2011-01-07 | 抗真菌剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012144452A true JP2012144452A (ja) | 2012-08-02 |
| JP5718064B2 JP5718064B2 (ja) | 2015-05-13 |
Family
ID=46788419
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011002077A Active JP5718064B2 (ja) | 2011-01-07 | 2011-01-07 | 抗真菌剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5718064B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR9301059A (pt) | 1993-05-07 | 1994-11-29 | Brasil Compressores Sa | Sistema de acionamento de válvula de descarga para compressores herméticos |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005539093A (ja) * | 2002-07-17 | 2005-12-22 | ユニリーバー・ナームローゼ・ベンノートシヤープ | 分枝状アルコールのカルボキシアルキレート及び/またはそのアルコキシレートを含有するスキンケア用化粧組成物 |
-
2011
- 2011-01-07 JP JP2011002077A patent/JP5718064B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005539093A (ja) * | 2002-07-17 | 2005-12-22 | ユニリーバー・ナームローゼ・ベンノートシヤープ | 分枝状アルコールのカルボキシアルキレート及び/またはそのアルコキシレートを含有するスキンケア用化粧組成物 |
Non-Patent Citations (1)
| Title |
|---|
| JPN6014051521; The Journal of Biological Chemistry Vol.267, No.24, pp.17159-17169, 1992 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5718064B2 (ja) | 2015-05-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7459581B2 (en) | Anti-bacterial compounds | |
| US8911715B2 (en) | L-menthyl-N-(2-hydroxyphenyl)carbamate | |
| JP2008120811A (ja) | 抗菌組成物 | |
| US7119123B2 (en) | Antimicrobially active 4-methyl-4-aryl-2-pentanols, their preparation and use | |
| JP2907640B2 (ja) | 尋常性ざ瘡用皮膚外用剤 | |
| KR101851010B1 (ko) | 항염증 및 항균활성을 가지는 조성물 | |
| JP5718064B2 (ja) | 抗真菌剤 | |
| EP2974713B1 (en) | Ceramide-like function imparting agent | |
| JP5718065B2 (ja) | 抗菌剤及びこれを含有する皮膚外用剤 | |
| US7722893B2 (en) | Use of substitute 2,4-bis (alkylamino) pyrimidines or quinzolines as antimicrobials | |
| WO2021089501A1 (en) | Novel method | |
| CA3083192A1 (en) | Propanediol monoacetate mononitrate | |
| WO2008065527A2 (en) | Gallic acid esters of fragrant alcohols | |
| AU2003254560B2 (en) | Pyridyl-triazine derivatives as microbicidal active substances | |
| US20070276045A1 (en) | Anti-Bacterial Compounds | |
| JP2004189656A (ja) | 抗アクネ菌組成物 | |
| GB2401865A (en) | Antibacterial and antifungal glycerol monocarbonates | |
| US20220193025A1 (en) | Use of dianhydrohexitol to eliminate the cosmetic effects of acne, dandruff and bad odors | |
| JP2010013359A (ja) | 防腐殺菌剤並びに該防腐殺菌剤を配合した化粧料、医薬品及び食品 | |
| JP2012523391A (ja) | レゾルシノールの硫化誘導体、その製造及びその美容用途 | |
| ES2781860T3 (es) | Nuevos derivados de benzoato de bencilo | |
| JPWO2015159384A1 (ja) | 新規な化合物、これを含有する化粧料及び皮膚外用剤 | |
| JPS6045174B2 (ja) | 新規なヒドロキシ安息香酸エステルおよびこれを有効成分とする工業製品の防腐防バイ剤 | |
| JPS6045176B2 (ja) | 新規なオキシ安息香酸エステルおよびこれを有効成分とする工業製品の防腐防バイ剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20131220 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141209 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150206 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150310 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150318 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 5718064 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |