JP2011503162A - 固体組成物 - Google Patents
固体組成物 Download PDFInfo
- Publication number
- JP2011503162A JP2011503162A JP2010533657A JP2010533657A JP2011503162A JP 2011503162 A JP2011503162 A JP 2011503162A JP 2010533657 A JP2010533657 A JP 2010533657A JP 2010533657 A JP2010533657 A JP 2010533657A JP 2011503162 A JP2011503162 A JP 2011503162A
- Authority
- JP
- Japan
- Prior art keywords
- dosage form
- solid
- excipients
- active substance
- eye
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000008247 solid mixture Substances 0.000 title 1
- 239000000546 pharmaceutical excipient Substances 0.000 claims abstract description 107
- 239000013543 active substance Substances 0.000 claims abstract description 106
- 239000002552 dosage form Substances 0.000 claims abstract description 103
- 239000007787 solid Substances 0.000 claims abstract description 64
- 238000000338 in vitro Methods 0.000 claims abstract description 13
- 239000003826 tablet Substances 0.000 claims description 131
- NITYDPDXAAFEIT-DYVFJYSZSA-N ilomastat Chemical compound C1=CC=C2C(C[C@@H](C(=O)NC)NC(=O)[C@H](CC(C)C)CC(=O)NO)=CNC2=C1 NITYDPDXAAFEIT-DYVFJYSZSA-N 0.000 claims description 81
- 229940124761 MMP inhibitor Drugs 0.000 claims description 80
- 239000007909 solid dosage form Substances 0.000 claims description 79
- 229960003696 ilomastat Drugs 0.000 claims description 75
- 239000000126 substance Substances 0.000 claims description 64
- 230000036573 scar formation Effects 0.000 claims description 61
- 238000000034 method Methods 0.000 claims description 49
- 238000011282 treatment Methods 0.000 claims description 41
- 238000001356 surgical procedure Methods 0.000 claims description 39
- 238000002513 implantation Methods 0.000 claims description 37
- 239000000203 mixture Substances 0.000 claims description 34
- 230000001225 therapeutic effect Effects 0.000 claims description 34
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 33
- 201000010099 disease Diseases 0.000 claims description 32
- 238000001727 in vivo Methods 0.000 claims description 32
- 239000003814 drug Substances 0.000 claims description 31
- 102000002274 Matrix Metalloproteinases Human genes 0.000 claims description 28
- 108010000684 Matrix Metalloproteinases Proteins 0.000 claims description 28
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 25
- 238000004519 manufacturing process Methods 0.000 claims description 24
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 claims description 23
- 229960002949 fluorouracil Drugs 0.000 claims description 22
- 230000002265 prevention Effects 0.000 claims description 21
- 208000010412 Glaucoma Diseases 0.000 claims description 20
- 229940121386 matrix metalloproteinase inhibitor Drugs 0.000 claims description 20
- 239000003771 matrix metalloproteinase inhibitor Substances 0.000 claims description 20
- 239000008194 pharmaceutical composition Substances 0.000 claims description 18
- 229940079593 drug Drugs 0.000 claims description 17
- 238000001914 filtration Methods 0.000 claims description 17
- 239000007892 solid unit dosage form Substances 0.000 claims description 12
- 239000002260 anti-inflammatory agent Substances 0.000 claims description 8
- 239000002246 antineoplastic agent Substances 0.000 claims description 8
- 102000004169 proteins and genes Human genes 0.000 claims description 8
- 108090000623 proteins and genes Proteins 0.000 claims description 8
- XFILPEOLDIKJHX-QYZOEREBSA-N batimastat Chemical compound C([C@@H](C(=O)NC)NC(=O)[C@H](CC(C)C)[C@H](CSC=1SC=CC=1)C(=O)NO)C1=CC=CC=C1 XFILPEOLDIKJHX-QYZOEREBSA-N 0.000 claims description 7
- 238000007906 compression Methods 0.000 claims description 7
- 230000006835 compression Effects 0.000 claims description 7
- NEAQRZUHTPSBBM-UHFFFAOYSA-N 2-hydroxy-3,3-dimethyl-7-nitro-4h-isoquinolin-1-one Chemical group C1=C([N+]([O-])=O)C=C2C(=O)N(O)C(C)(C)CC2=C1 NEAQRZUHTPSBBM-UHFFFAOYSA-N 0.000 claims description 6
- 230000015556 catabolic process Effects 0.000 claims description 6
- 239000003795 chemical substances by application Substances 0.000 claims description 6
- 238000006731 degradation reaction Methods 0.000 claims description 6
- 230000001613 neoplastic effect Effects 0.000 claims description 6
- 239000002253 acid Substances 0.000 claims description 5
- 239000003242 anti bacterial agent Substances 0.000 claims description 5
- 230000009467 reduction Effects 0.000 claims description 5
- 230000000699 topical effect Effects 0.000 claims description 5
- GTXSRFUZSLTDFX-HRCADAONSA-N (2s)-n-[(2s)-3,3-dimethyl-1-(methylamino)-1-oxobutan-2-yl]-4-methyl-2-[[(2s)-2-sulfanyl-4-(3,4,4-trimethyl-2,5-dioxoimidazolidin-1-yl)butanoyl]amino]pentanamide Chemical compound CNC(=O)[C@H](C(C)(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](S)CCN1C(=O)N(C)C(C)(C)C1=O GTXSRFUZSLTDFX-HRCADAONSA-N 0.000 claims description 4
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 claims description 4
- 229940088710 antibiotic agent Drugs 0.000 claims description 4
- -1 antibody molecules Substances 0.000 claims description 4
- 229950001858 batimastat Drugs 0.000 claims description 4
- 229950003608 prinomastat Drugs 0.000 claims description 4
- 150000003431 steroids Chemical class 0.000 claims description 4
- 238000002560 therapeutic procedure Methods 0.000 claims description 4
- 239000011701 zinc Substances 0.000 claims description 4
- 229910052725 zinc Inorganic materials 0.000 claims description 4
- GFUITADOEPNRML-SJORKVTESA-N (2r,3r)-3-(cyclopentylmethyl)-n-hydroxy-4-oxo-4-piperidin-1-yl-2-[(3,4,4-trimethyl-2,5-dioxoimidazolidin-1-yl)methyl]butanamide Chemical compound O=C1C(C)(C)N(C)C(=O)N1C[C@H](C(=O)NO)[C@H](C(=O)N1CCCCC1)CC1CCCC1 GFUITADOEPNRML-SJORKVTESA-N 0.000 claims description 3
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 claims description 3
- 239000004480 active ingredient Substances 0.000 claims description 3
- 229960003957 dexamethasone Drugs 0.000 claims description 3
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 claims description 3
- 229960002009 naproxen Drugs 0.000 claims description 3
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical group C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 claims description 3
- 229960005294 triamcinolone Drugs 0.000 claims description 3
- GFNANZIMVAIWHM-OBYCQNJPSA-N triamcinolone Chemical compound O=C1C=C[C@]2(C)[C@@]3(F)[C@@H](O)C[C@](C)([C@@]([C@H](O)C4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 GFNANZIMVAIWHM-OBYCQNJPSA-N 0.000 claims description 3
- 230000001678 irradiating effect Effects 0.000 claims description 2
- 210000001519 tissue Anatomy 0.000 description 62
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 39
- 238000004090 dissolution Methods 0.000 description 28
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 23
- 239000000499 gel Substances 0.000 description 22
- 239000002609 medium Substances 0.000 description 22
- 239000000243 solution Substances 0.000 description 21
- 208000002352 blister Diseases 0.000 description 20
- 238000002474 experimental method Methods 0.000 description 20
- 239000007864 aqueous solution Substances 0.000 description 17
- 230000008602 contraction Effects 0.000 description 17
- 230000000694 effects Effects 0.000 description 17
- 238000004128 high performance liquid chromatography Methods 0.000 description 15
- 239000003112 inhibitor Substances 0.000 description 15
- 231100000241 scar Toxicity 0.000 description 15
- 230000008901 benefit Effects 0.000 description 14
- 238000002347 injection Methods 0.000 description 13
- 239000007924 injection Substances 0.000 description 13
- 241000283973 Oryctolagus cuniculus Species 0.000 description 11
- 210000004027 cell Anatomy 0.000 description 11
- 210000002950 fibroblast Anatomy 0.000 description 11
- 229960004857 mitomycin Drugs 0.000 description 11
- 229960000397 bevacizumab Drugs 0.000 description 10
- 238000011088 calibration curve Methods 0.000 description 10
- 230000002401 inhibitory effect Effects 0.000 description 10
- 238000013268 sustained release Methods 0.000 description 10
- 239000012730 sustained-release form Substances 0.000 description 10
- 210000001742 aqueous humor Anatomy 0.000 description 9
- 150000001875 compounds Chemical class 0.000 description 9
- 230000001954 sterilising effect Effects 0.000 description 9
- 206010052428 Wound Diseases 0.000 description 8
- 208000027418 Wounds and injury Diseases 0.000 description 8
- 230000008569 process Effects 0.000 description 8
- 230000037390 scarring Effects 0.000 description 8
- 238000004659 sterilization and disinfection Methods 0.000 description 8
- 229940124597 therapeutic agent Drugs 0.000 description 8
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 7
- 239000001856 Ethyl cellulose Substances 0.000 description 7
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- 229940120638 avastin Drugs 0.000 description 7
- 229920001249 ethyl cellulose Polymers 0.000 description 7
- 235000019325 ethyl cellulose Nutrition 0.000 description 7
- 229920002674 hyaluronan Polymers 0.000 description 7
- 229960003160 hyaluronic acid Drugs 0.000 description 7
- 239000011550 stock solution Substances 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 102000012422 Collagen Type I Human genes 0.000 description 6
- 108010022452 Collagen Type I Proteins 0.000 description 6
- 230000000340 anti-metabolite Effects 0.000 description 6
- 229940100197 antimetabolite Drugs 0.000 description 6
- 239000002256 antimetabolite Substances 0.000 description 6
- 230000001186 cumulative effect Effects 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 230000035876 healing Effects 0.000 description 6
- 230000004410 intraocular pressure Effects 0.000 description 6
- 238000012404 In vitro experiment Methods 0.000 description 5
- 206010061218 Inflammation Diseases 0.000 description 5
- 102000000380 Matrix Metalloproteinase 1 Human genes 0.000 description 5
- 102100039364 Metalloproteinase inhibitor 1 Human genes 0.000 description 5
- 239000000512 collagen gel Substances 0.000 description 5
- 238000011065 in-situ storage Methods 0.000 description 5
- 208000015181 infectious disease Diseases 0.000 description 5
- 230000004054 inflammatory process Effects 0.000 description 5
- 230000014759 maintenance of location Effects 0.000 description 5
- 230000003389 potentiating effect Effects 0.000 description 5
- 238000012384 transportation and delivery Methods 0.000 description 5
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 4
- 102000008186 Collagen Human genes 0.000 description 4
- 108010035532 Collagen Proteins 0.000 description 4
- 108010016113 Matrix Metalloproteinase 1 Proteins 0.000 description 4
- 206010028980 Neoplasm Diseases 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 4
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 4
- 230000027455 binding Effects 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 239000002775 capsule Substances 0.000 description 4
- 239000006143 cell culture medium Substances 0.000 description 4
- 229920001436 collagen Polymers 0.000 description 4
- 210000000795 conjunctiva Anatomy 0.000 description 4
- 239000008367 deionised water Substances 0.000 description 4
- 229910021641 deionized water Inorganic materials 0.000 description 4
- 239000012530 fluid Substances 0.000 description 4
- 230000005764 inhibitory process Effects 0.000 description 4
- 208000014674 injury Diseases 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 239000008188 pellet Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 238000001542 size-exclusion chromatography Methods 0.000 description 4
- 230000002459 sustained effect Effects 0.000 description 4
- 231100000419 toxicity Toxicity 0.000 description 4
- 230000001988 toxicity Effects 0.000 description 4
- 230000008733 trauma Effects 0.000 description 4
- 230000010388 wound contraction Effects 0.000 description 4
- 102100026802 72 kDa type IV collagenase Human genes 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 201000004569 Blindness Diseases 0.000 description 3
- GUTLYIVDDKVIGB-OUBTZVSYSA-N Cobalt-60 Chemical compound [60Co] GUTLYIVDDKVIGB-OUBTZVSYSA-N 0.000 description 3
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 3
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 108010031374 Tissue Inhibitor of Metalloproteinase-1 Proteins 0.000 description 3
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 3
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 3
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 210000002159 anterior chamber Anatomy 0.000 description 3
- 239000000427 antigen Substances 0.000 description 3
- 102000036639 antigens Human genes 0.000 description 3
- 108091007433 antigens Proteins 0.000 description 3
- 230000006907 apoptotic process Effects 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 231100000673 dose–response relationship Toxicity 0.000 description 3
- 210000002744 extracellular matrix Anatomy 0.000 description 3
- 230000036512 infertility Effects 0.000 description 3
- OCSMOTCMPXTDND-OUAUKWLOSA-N marimastat Chemical compound CNC(=O)[C@H](C(C)(C)C)NC(=O)[C@H](CC(C)C)[C@H](O)C(=O)NO OCSMOTCMPXTDND-OUAUKWLOSA-N 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 210000000651 myofibroblast Anatomy 0.000 description 3
- 239000013642 negative control Substances 0.000 description 3
- 230000002980 postoperative effect Effects 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 238000004062 sedimentation Methods 0.000 description 3
- 238000010561 standard procedure Methods 0.000 description 3
- 230000003637 steroidlike Effects 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 238000011287 therapeutic dose Methods 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- 231100000331 toxic Toxicity 0.000 description 3
- 230000002588 toxic effect Effects 0.000 description 3
- 238000005303 weighing Methods 0.000 description 3
- 230000029663 wound healing Effects 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 208000009043 Chemical Burns Diseases 0.000 description 2
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 2
- 102000029816 Collagenase Human genes 0.000 description 2
- 108060005980 Collagenase Proteins 0.000 description 2
- 208000001708 Dupuytren contracture Diseases 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 206010014989 Epidermolysis bullosa Diseases 0.000 description 2
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 2
- 206010063560 Excessive granulation tissue Diseases 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 101000627872 Homo sapiens 72 kDa type IV collagenase Proteins 0.000 description 2
- 101001013150 Homo sapiens Interstitial collagenase Proteins 0.000 description 2
- 101000669513 Homo sapiens Metalloproteinase inhibitor 1 Proteins 0.000 description 2
- 101000990915 Homo sapiens Stromelysin-1 Proteins 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- 102000000422 Matrix Metalloproteinase 3 Human genes 0.000 description 2
- 102100026262 Metalloproteinase inhibitor 2 Human genes 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- 206010063562 Radiation skin injury Diseases 0.000 description 2
- 206010039710 Scleroderma Diseases 0.000 description 2
- 101710151387 Serine protease 1 Proteins 0.000 description 2
- 102100032491 Serine protease 1 Human genes 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 206010053615 Thermal burn Diseases 0.000 description 2
- 108010031372 Tissue Inhibitor of Metalloproteinase-2 Proteins 0.000 description 2
- 206010066901 Treatment failure Diseases 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 101710119665 Trypsin-1 Proteins 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 230000002776 aggregation Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 206010003246 arthritis Diseases 0.000 description 2
- 230000000975 bioactive effect Effects 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- FAKRSMQSSFJEIM-RQJHMYQMSA-N captopril Chemical compound SC[C@@H](C)C(=O)N1CCC[C@H]1C(O)=O FAKRSMQSSFJEIM-RQJHMYQMSA-N 0.000 description 2
- 229960000830 captopril Drugs 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 230000037319 collagen production Effects 0.000 description 2
- 229960002424 collagenase Drugs 0.000 description 2
- 239000002442 collagenase inhibitor Substances 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 206010012601 diabetes mellitus Diseases 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 239000003889 eye drop Substances 0.000 description 2
- 229940012356 eye drops Drugs 0.000 description 2
- 210000000744 eyelid Anatomy 0.000 description 2
- 230000002349 favourable effect Effects 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 230000019305 fibroblast migration Effects 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 210000001126 granulation tissue Anatomy 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 229920001477 hydrophilic polymer Polymers 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 230000028709 inflammatory response Effects 0.000 description 2
- 230000002427 irreversible effect Effects 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 229950008959 marimastat Drugs 0.000 description 2
- 208000001491 myopia Diseases 0.000 description 2
- 230000004379 myopia Effects 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 108091007196 stromelysin Proteins 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 125000002730 succinyl group Chemical group C(CCC(=O)*)(=O)* 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 239000007916 tablet composition Substances 0.000 description 2
- 210000002435 tendon Anatomy 0.000 description 2
- 230000009772 tissue formation Effects 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 210000004127 vitreous body Anatomy 0.000 description 2
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- 101710151806 72 kDa type IV collagenase Proteins 0.000 description 1
- ZKRFOXLVOKTUTA-KQYNXXCUSA-N 9-(5-phosphoribofuranosyl)-6-mercaptopurine Chemical compound O[C@@H]1[C@H](O)[C@@H](COP(O)(O)=O)O[C@H]1N1C(NC=NC2=S)=C2N=C1 ZKRFOXLVOKTUTA-KQYNXXCUSA-N 0.000 description 1
- 102100033312 Alpha-2-macroglobulin Human genes 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 229930183010 Amphotericin Natural products 0.000 description 1
- QGGFZZLFKABGNL-UHFFFAOYSA-N Amphotericin A Natural products OC1C(N)C(O)C(C)OC1OC1C=CC=CC=CC=CCCC=CC=CC(C)C(O)C(C)C(C)OC(=O)CC(O)CC(O)CCC(O)C(O)CC(O)CC(O)(CC(O)C2C(O)=O)OC2C1 QGGFZZLFKABGNL-UHFFFAOYSA-N 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 101000645291 Bos taurus Metalloproteinase inhibitor 2 Proteins 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 208000018380 Chemical injury Diseases 0.000 description 1
- 208000032544 Cicatrix Diseases 0.000 description 1
- 229940122097 Collagenase inhibitor Drugs 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 206010010733 Conjunctival scar Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 208000028006 Corneal injury Diseases 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 102000009123 Fibrin Human genes 0.000 description 1
- 108010073385 Fibrin Proteins 0.000 description 1
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 1
- 102000016359 Fibronectins Human genes 0.000 description 1
- 108010067306 Fibronectins Proteins 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 206010016717 Fistula Diseases 0.000 description 1
- 208000005422 Foreign-Body reaction Diseases 0.000 description 1
- 108010026132 Gelatinases Proteins 0.000 description 1
- 102000013382 Gelatinases Human genes 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 101000990902 Homo sapiens Matrix metalloproteinase-9 Proteins 0.000 description 1
- 101000990908 Homo sapiens Neutrophil collagenase Proteins 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 108010016165 Matrix Metalloproteinase 2 Proteins 0.000 description 1
- 108010015302 Matrix metalloproteinase-9 Proteins 0.000 description 1
- 102000001776 Matrix metalloproteinase-9 Human genes 0.000 description 1
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 1
- 206010062575 Muscle contracture Diseases 0.000 description 1
- 102100030411 Neutrophil collagenase Human genes 0.000 description 1
- 101710118230 Neutrophil collagenase Proteins 0.000 description 1
- 102000056189 Neutrophil collagenases Human genes 0.000 description 1
- 108030001564 Neutrophil collagenases Proteins 0.000 description 1
- 102000016979 Other receptors Human genes 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 208000031481 Pathologic Constriction Diseases 0.000 description 1
- 206010034277 Pemphigoid Diseases 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 108010015078 Pregnancy-Associated alpha 2-Macroglobulins Proteins 0.000 description 1
- 206010038848 Retinal detachment Diseases 0.000 description 1
- 206010038933 Retinopathy of prematurity Diseases 0.000 description 1
- 125000000066 S-methyl group Chemical group [H]C([H])([H])S* 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 208000007107 Stomach Ulcer Diseases 0.000 description 1
- 208000004350 Strabismus Diseases 0.000 description 1
- 102100030416 Stromelysin-1 Human genes 0.000 description 1
- 239000012505 Superdex™ Substances 0.000 description 1
- 208000021945 Tendon injury Diseases 0.000 description 1
- 206010047139 Vasoconstriction Diseases 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 238000005054 agglomeration Methods 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 229940009444 amphotericin Drugs 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000002399 angioplasty Methods 0.000 description 1
- 230000002942 anti-growth Effects 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 239000003782 beta lactam antibiotic agent Substances 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 238000006065 biodegradation reaction Methods 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000000337 buffer salt Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- 229960004630 chlorambucil Drugs 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 208000006111 contracture Diseases 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 239000002254 cytotoxic agent Substances 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 229920006237 degradable polymer Polymers 0.000 description 1
- 239000007857 degradation product Substances 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 229960001259 diclofenac Drugs 0.000 description 1
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 229960003722 doxycycline Drugs 0.000 description 1
- XQTWDDCIUJNLTR-CVHRZJFOSA-N doxycycline monohydrate Chemical compound O.O=C1C2=C(O)C=CC=C2[C@H](C)[C@@H]2C1=C(O)[C@]1(O)C(=O)C(C(N)=O)=C(O)[C@@H](N(C)C)[C@@H]1[C@H]2O XQTWDDCIUJNLTR-CVHRZJFOSA-N 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 206010014801 endophthalmitis Diseases 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000002532 enzyme inhibitor Substances 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 229960003276 erythromycin Drugs 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000013401 experimental design Methods 0.000 description 1
- 208000030533 eye disease Diseases 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 229950003499 fibrin Drugs 0.000 description 1
- 210000000630 fibrocyte Anatomy 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 230000001497 fibrovascular Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 230000003890 fistula Effects 0.000 description 1
- 230000005251 gamma ray Effects 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 201000005917 gastric ulcer Diseases 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 229940089982 healon Drugs 0.000 description 1
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 201000001371 inclusion conjunctivitis Diseases 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 229940025708 injectable product Drugs 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 229960004752 ketorolac Drugs 0.000 description 1
- OZWKMVRBQXNZKK-UHFFFAOYSA-N ketorolac Chemical compound OC(=O)C1CCN2C1=CC=C2C(=O)C1=CC=CC=C1 OZWKMVRBQXNZKK-UHFFFAOYSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 239000003120 macrolide antibiotic agent Substances 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 208000002780 macular degeneration Diseases 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 239000003475 metalloproteinase inhibitor Substances 0.000 description 1
- MGJXBDMLVWIYOQ-UHFFFAOYSA-N methylazanide Chemical compound [NH-]C MGJXBDMLVWIYOQ-UHFFFAOYSA-N 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 239000005445 natural material Substances 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 238000011587 new zealand white rabbit Methods 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 208000030346 palmar fibromatosis Diseases 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 150000002960 penicillins Chemical class 0.000 description 1
- 230000002572 peristaltic effect Effects 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000002135 phase contrast microscopy Methods 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920002503 polyoxyethylene-polyoxypropylene Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 238000004080 punching Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- HDOUGSFASVGDCS-UHFFFAOYSA-N pyridin-3-ylmethanamine Chemical compound NCC1=CC=CN=C1 HDOUGSFASVGDCS-UHFFFAOYSA-N 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 238000009790 rate-determining step (RDS) Methods 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 208000014733 refractive error Diseases 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 210000001525 retina Anatomy 0.000 description 1
- 230000004264 retinal detachment Effects 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 230000037387 scars Effects 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- YWIVKILSMZOHHF-QJZPQSOGSA-N sodium;(2s,3s,4s,5r,6r)-6-[(2s,3r,4r,5s,6r)-3-acetamido-2-[(2s,3s,4r,5r,6r)-6-[(2r,3r,4r,5s,6r)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2- Chemical compound [Na+].CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 YWIVKILSMZOHHF-QJZPQSOGSA-N 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 230000036262 stenosis Effects 0.000 description 1
- 208000037804 stenosis Diseases 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000013269 sustained drug release Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000012622 synthetic inhibitor Substances 0.000 description 1
- 238000012385 systemic delivery Methods 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 239000012085 test solution Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 230000036575 thermal burns Effects 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 230000000451 tissue damage Effects 0.000 description 1
- 231100000827 tissue damage Toxicity 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 210000001585 trabecular meshwork Anatomy 0.000 description 1
- 206010044325 trachoma Diseases 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 210000000626 ureter Anatomy 0.000 description 1
- 230000025033 vasoconstriction Effects 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 230000004393 visual impairment Effects 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 238000007805 zymography Methods 0.000 description 1
- 239000002132 β-lactam antibiotic Substances 0.000 description 1
- 229940124586 β-lactam antibiotics Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/513—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim having oxo groups directly attached to the heterocyclic ring, e.g. cytosine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
- A61K9/0051—Ocular inserts, ocular implants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Ophthalmology & Optometry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Dermatology (AREA)
- Immunology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Endocrinology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
【選択図】図13
Description
i.マトリックスメタロプロテイナーゼインヒビター及び存在する場合は賦形剤を含有する圧縮剤形、例えば錠剤を製造し、そして、
ii.その圧縮剤形をガンマ線照射することにより滅菌する、
ことを含んでなる。
i.実質上水不溶性の治療物質の固体錠剤を形作り;そして、
ii.この錠剤をガンマ線で照射して滅菌する、
ことを含んでなる、実質上水不溶性の治療物質を含んでなる滅菌された固体医薬組成物を製造する方法を提供する。
溶解性実験は、イロマスタット及びその他のMMPインヒビターの治療用量が、固体錠剤形態のイロマスタット又はその他のMMPインヒビターの遅速溶解によって達成できる可能性を示唆した。クリアランスがインビトロフローセルにおいて5分未満で起こる単純な注射と比較して、この錠剤形態のイロマスタットでは長期放出が達成されることが証明された。次に、臨床的に検証されたインビボGFSモデルを用いて、最長30日間の様々な時点での、手術部位における長期放出の効果を調べた。GFSに関してイロマスタットは毒性でないことが見出されているが、この教示は、種々のMMPインヒビター及びその他の実質上水不溶性治療物質にも適用できる。
流動システム
放出動態について幾らかの指標を得るために、50〜200μl容量の流動リグを用いてブレブのモデルとした。イロマスタット錠剤(1リグあたり1個の錠剤)をフローチェンバー内に置いた。2本の管を各リグに接続する。一方は水溶液を導入する蠕動ポンプに接続し、他方はリグからこの溶液を排出させる。流速を利用して、結膜下腔への、及び結膜下腔から強膜静脈に至るこの水溶液の流動をモデル化する。溶液がリグから流出する際に試料を採取し、この徐放系におけるイロマスタットの濃度を決定する。
錠剤用パンチ及びダイを使用し、固体イロマスタットをダイに置き、パンチを取り付ける。この固体イロマスタットは、ダイに置く前に精確に秤量した。次に、取り付けたパンチ−ダイを錠剤圧縮機中に入れ、約10秒間5barの圧力で圧縮した。
幾つかの逆相カラム及び移動相を評価し、イロマスタットのHPLC分離に必要な最適条件を決定した。C−18カラム(SIGMA)及び25%アセトニトリル水性移動相が良好な基線分離を与えることが判明した。移動相は以下のように調製した。緩衝液1000mlを作製するために、酢酸アンモニウム(Fluka)1.54gm、99.5%トリエチルアミン6ml(Sigma Aldrich)、脱イオン水〜950mlを混合し、次いで100%酢酸(Analar BDH)およそ10mlを加え、この緩衝液のpHを5.0±0.1に調節した。pHを調節する際、脱イオン水を加えて緩衝液の容量を1000mlとした。各試料のアリコート(0.1ml)をHPLCバイアルに移し、次にこれをHPLCオートサンプラーに入れた。移動相を1ml/分で溶出し、UV検出機を280nmに設定し、イロマスタット溶液の濃度を決定した(Galardy et al. 1994b)。各時点で3回の注入(各10μl)を評価した。UV検出機にコンピューターを接続し、プログラムChrom+を使用してピーク面積を解析し、イロマスタットの量を決定した。ピーク表面は、被験溶液中のイロマスタットの濃度を表す。3個の測定値の平均を用いてイロマスタットの量を決定した。
欧州及び米国薬局方の規定に従い、投与される薬物の最終剤形は無菌である必要がある。錠剤製造は無菌条件で実施される訳ではなく、滅菌イロマスタットは市販されていないため、イロマスタット錠をガンマ線照射によって滅菌する必要があった。ガンマ線照射は、無菌処理及び濾過よりも優れた製品滅菌の確実性といった著明な利点を持つこと、製造された最終製品の内部を貫通すること、低温プロセスであること、そして単純な検証プロセスを有することから、幅広く利用されている。さらに、例えばエチレンオキシド滅菌の場合のような除去すべき残留物がない。潜在的な1つの不都合は、ガンマ線照射は試料内部の化学構造の改変を導き得る化学反応を開始させ得ることである。一般に、最低限の無菌性保証レベルSAL=10−6(処理後にその物体が非無菌である確率が百万分の一)の達成には25kGyの線量が必要である。より低い線量は、適当な無菌試験を使用して検証できる。欧州及び米国薬局方の規定の下では、25kGy線量の照射が無菌性を保証する(2000a;2000b)。英国のクランフィールド大学と協力して、コバルト60ガンマ線源を利用した。これは、薬物及び生体材料を照射により滅菌するのに好適であると考えられる。よってイロマスタットを未加工粉末及び製造済み錠剤として照射した。コバルト60ガンマ線源は1時間あたり約4500kGyの照射にあたることから、25kGyの暴露を達成するために試料をコバルト60パノラマ式チェンバーに約5時間35分間放置した。
1.ヒトテノン線維芽細胞(HTF)
インビトロ培養用にヒトテノン線維芽細胞(HTF)を使用した。これらの細胞は結膜下瘢痕形成に関与している。ヘルシンキ宣言の信条(1989)の下にモアフィールド病院アイバンクから取得したドナー眼由来の0.5cm3の組織外植片を使用して、HTF単離及び増殖の処理を実施した。0.5cm3の外植片を、25cm3のフラスコの底に、カバースリップを載せて2時間保持した。各フラスコには、10%牛胎児血清、2mM L−グルタミン、100U/mlペニシリン、50mg/mlゲンタマイシン、100μg/mlストレプトマイシン及び0.25μg/mlアムホテリシンを加えたダルベッコ改良イーグル培地(DMEM)で構成される通常培地5mlを入れた。フラスコを、37℃及び空気中5%加湿CO2のインキュベーターに入れた。培地を3日毎に交換し、コンフルエントになった時に(通常1ヶ月以内)、新たなフラスコに継代し、直接実験に使用するか、液体窒素中に保存した。
HTFがコンフルエントに達した後、培地を吸引し、単層をトリプシン1x(Gibco)1mlで洗浄し、このトリプシンを約15秒間速やかに吸引した。次に、トリプシン1x(Gibco)2mlを各フラスコに加え、37℃及び空気中5%加湿CO2で2分間インキュベートすることにより、HTFをフラスコから剥離させた。x10倍率のLeica顕微鏡を用いる位相差顕微鏡検査によって、細胞がフラスコの底から剥離し、それらが球形を獲得したことを確認した後、細胞培地2mlを加えてトリプシン処理を中和した。細胞懸濁液を15ml遠心管(STARLAB GMBH)に移し、1600rpmで5分間遠心分離した。次いでこの細胞ペレットを細胞培地10mlに再懸濁し、4個の異なる75cm3フラスコに分けた(1:4の拡大)。各フラスコに細胞培地7.5mlを加えた。フラスコを37℃及び空気中5%加湿CO2のインキュベーターに入れ、3日毎に培地を交換した。コンフルエントに到達させるために継代から継代までに必要な時間は平均1週間であった。
ノイバウエルプレートを用いて6.2x104HTFを計数し、次いで50mlユニバーサル管に入れたFBS170μlに再懸濁した。濃縮培地(160μl)を加えた(3.5mlDMEM(x10原液)、0.35mlグルタミン(2mM原液)及び0.9ml重炭酸ナトリウム(7.5%原液)より成る保存溶液)。次に、First LinkI型コラーゲン溶液のコラーゲン(0.6%酢酸中原液2.2mg/ml)830μlを加え、気泡ができないよう、この溶液を回転させて混合した。滅菌1M NaOH(75〜80μl)を速やかに添加して溶液の酸性pHを変化させた。これにより溶液はピンク色となり、元の黄色には戻らなかった。直ちにコラーゲンゲル溶液150μlをMattek皿のウェルに流し入れ、ピペットチップを用いてこのゲルが確実に中央溝の隅に入っているようにした。ゲルをチップから排出する際、気泡の生成を回避せねばならない。気泡ができた場合はそれらを吸入除去した。通常、ゲル懸濁液1.2mlから6個のゲルが容易にできる。この処理の後、ゲルの入ったMakket皿のウェルをインキュベーターに入れ、少なくとも10〜15分間(最長30分間)で固まらせた。黄色のチップを用いて中央溝の隅からゲルを剥離し、ポリマー化しなかった過剰の溶液を吸引除去した。細胞培地2mlを加え、皿を37℃及び空気中5%加湿CO2のインキュベーターに入れた。培地は3日毎に交換した。
一般に固体イロマスタットは培地に添加する前にDMSOで希釈するが、この実験では、イロマスタットをDMSOを含まない通常培地に直接溶解できた。培地及び滅菌しておいた固体イロマスタット、並びに培地及び非照射固体イロマスタットを、異なる50mlユニバーサル管に入れ、約5〜6時間攪拌した。次いで両試料の濃度をHPLCで確認した。
コラーゲンIゲルのHTF収縮に及ぼす非照射イロマスタットの阻害効果が知られている。照射したイロマスタットと比較するため、3つの異なるコラーゲンゲルの処置群による実験を行った。各処置群はHTFを伴う3つのコラーゲンIゲルを有していた。第一群のゲルはイロマスタット無しの培地で処理し(負の対照)、第二群のゲルは非照射イロマスタットを加えた培地で処理し(正の対照)、そして第三群のゲルは照射したイロマスタットを加えた培地で処理した。
1.実験設計
左目に緑内障ドレナージ手術を受ける4匹のウサギによってランダムな1ブロック研究の設計を実施した。動物を30日間観察した。この実験は、マスキングされた観察者を用いるランダム化盲検対照研究として実施した。一人の観察者を臨床データの評価に利用した。
4匹の雌性ニュージーランドホワイトウサギ(Harlan UK Ltd; c.2〜2.2kg、12〜14週齢)を使用した。動物を眼科用BRUユニットに収容し、通常必要とされる順応期間7日間を与えた。
表1に示すように動物を2群の何れかにランダムに割り付けた。A群の動物には賦形剤不含イロマスタット錠(ペレットとも称する)を投与し、B群には対照としてエチルセルロース錠を投与した。エチルセルロースは水溶液に溶解しない賦形剤であり、MMPに対して既知の阻害活性を持たない。エチルセルロース錠のサイズは30日間のインビボ実験の間不変であった。単に不活性エチルセルロース錠を入れたためではなく、イロマスタット自体がブレブ及びその機能性を維持したのかどうかを判定するために、対照ペレットはイロマスタットペレットと同サイズとした。
手術は、文献に詳細に記載されている標準法を用いて実施する。外科的手技及びウサギにおけるその使用を一致させることにより、過去の研究とのおおよその比較が可能となる。このモデルは臨床的に検証されており、且つこの外科的手技は広く臨床使用されていることから、このことは特に重要である。
HPLCでイロマスタットの検出を行うため、第30日目の実験終了時に、房水、硝子体及び血液を採取した。
検量線
DMSOを含まないpH7.6の水溶液中でのイロマスタットの検量線を図1に示す。この曲線は、Chrom+と称するソフトウェアと共に上記の移動相及びUV検出機(280nm)を使用するHPLCカラム(C18)から溶出するイロマスタットを測定することにより作製した。
全般的な狙いは、緑内障濾過手術後に結膜下腔に純粋な圧縮イロマスタットで作られた小錠剤を配置したならば、イロマスタットが房水に持続放出する結果となるかどうかを確定することであった。イロマスタットは極めて高価な化合物であるため、イロマスタット錠の製造に先立ち、5−FUのような他の化合物を用いる小錠剤製造において経験を得た。6.5mg、5.6mg及び3.2mgの固体イロマスタットを用いて3種の賦形剤不含イロマスタット錠を製造した。標準的な錠剤用パンチ及びダイ並びに適用圧力5barのプレス機を使用した。第一の錠剤は直径3mm、厚さ0.87mm及び重量4.8mgであった。第二の錠剤は同じ直径、厚さ0.62mm及び重量4.1mgであった。第三の錠剤は直径3mm、厚さ0.4mm及び重量2.3mgであった。少量のイロマスタットがパンチ及びダイの表面に残留した。第一の錠剤の製造に用いられたイロマスタットの量は、30日間のあらゆる時点でイロマスタットが水溶液(約100μM)中で理論上最大の溶解性を維持するという仮説に基づいた。
試験された2個の錠剤が流動リグ内で30日後に完全に溶解していないことが判明したため、本発明者等は、2.3mgのイロマスタットを使用して、より柔らかい錠剤を作ろうと試みた。本発明者等はこの錠剤を200μl容量の流動リグに配置し、この系を流速2μl/分に設定した。この錠剤の放出プロファイルを表4に示す。
緑内障濾過手術中にイロマスタット錠を埋め込むためには、この錠剤が無菌である必要があった。医薬品規制調和国際会議(ICH)は、照射された製品と照射されていない製品の特性解明及び比較に、高速液体クロマトグラフィー(HPLC)、質量分析又はガスクロマトグラフィーの使用を推奨している。これらの指針に従い、ガンマ線照射イロマスタットをpH7.6の水溶液に溶解し、それをHPLCで評価した。照射されたイロマスタットのクロマトグラムを非照射イロマスタットのクロマトグラムと比較した。照射イロマスタットのクロマトグラムは、イロマスタット全体と比較して、照射後に形成される0.25%の微量生成物を表す追加のピークを示した。これは、米国及び欧州薬局方何れの基準にも適合する。
イロマスタットを0.1mMの濃度でDMSO又は水に溶解した溶液は、4℃で1ヶ月あたり1%が分解し、37℃ではこれが一日あたり1%に増大する(Caldiochemのデータ)。37℃の湿潤環境で数日間放置した場合のイロマスタット固体錠剤の安定性を記載したデータは公表されていない。イロマスタット錠を、37℃の水性環境で30日間潜在的分解について評価した。第二の錠剤から試料を採取した後、本発明者等は、リグから残存固体を除去し、それを水溶液(pH7.6)に溶解した。残存イロマスタット化合物を含むこの水溶液の第30日目におけるクロマトグラム及び第一の時点においてリグから採取された水溶液のクロマトグラムを比較した。両クロマトグラムは極めて似通っており、この30日間で分解が起こらなかったことを示唆した(データは記載されていない)。
DMSO無しで直接媒質に溶解した照射イロマスタット粉末及び照射イロマスタット錠がインビトロで収縮を阻害する能力
3種類の処置カテゴリー(通常媒質、非照射及び照射イロマスタット)のゲルはすぐには収縮を開始させなかった。この理由により、3つの処置群において第1日目までは著明な変化が見られなかった。第2日目からゲルが収縮し始め、照射及び非照射イロマスタットの阻害効果が明らかとなった。実験が終了した7日目までに、負の対照群及びイロマスタット群の収縮に統計的有意差があった。
インビボ実験におけるイロマスタット錠の有効性
1.臨床的観察
エチルセルロース錠(対照)を投与されたウサギのブレブは、緑内障濾過手術の10日後に不全となった。対照的に、イロマスタット錠を投与された3匹のウサギのブレブは不全とならなかった。30日後、計画された実験は終了した。1匹のウサギにおいて、7日目に強膜の縫合が裂け、管が前房に落下した。これが起こった場合、通常の予想ではブレブが不全になる。しかしながら驚くべき事に、良好な構造のブレブが30日目までこのウサギに存続した。処置群及び対照群のウサギに角膜上皮症は観察されなかった。さらに、ブレブ領域上部の結膜は正常で無血管性ではなかった。緑内障濾過手術においてMMCを使用した後には無血管性ブレブが観察されてきた。そのうえ、柔らかい眼は観察されなかった。
上記のHPLC法を使用したところ、30日目にウサギの左(手術された)眼から採取した前房由来の房水、硝子体又は血液試料にはイロマスタットが検出されなかった。先に述べたようにイロマスタットの保持時間は6.5〜8分間であり、その時点付近でピークは検出されなかった。これらの観察は、GFS処置について、いかなる潜在的局所毒性も回避できるという結果を伴ってイロマスタットの流出が起こることを示している。
本発明者等は、試験された錠剤からのイロマスタットの持続放出を観察した。これらの錠剤は、賦形剤を使用せずに製造された。放出期間(30日間)の間、イロマスタットの治療用量(10μM)が達成された。固体形態のイロマスタットの使用は、複数回の注射を必要としない組織瘢痕形成の防止方法を提供する。過去のインビトロ及びインビボ実験とは対照的に、本発明者等は実験全体を通じてDMSOの使用を回避したが、それは、眼科での臨床使用が認可されていないためである。
5−FUを用いたインビトロ実験
上に指摘したように、固体5−FUの錠剤を上記と同じ技術を用いて製造した。次にこの錠剤の溶解速度を上記と同じリグを用いて測定した。
検量線
DMSOを含まないpH7.6の水溶液における5−FU溶解の検量線を図6に示す。この曲線は、ソフトウェアPC Chrom+を使用してHPLC読み取り機で5−FUのピークを測定することにより作製した。
第一の錠剤(錠剤A)は、直径3mm、厚さ0.71mm及び重量7.1mgであった。第二の錠剤(錠剤B)は、同じ直径、厚さ0.88mm及び重量8.7mgであった。第三の錠剤(錠剤C)は、直径3mm、厚さ0.76mm及び重量7mgであった。
賦形剤を含まない錠剤からの活性物質の持続放出
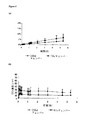
図9〜13は、フロースルー溶解リグを使用し、賦形剤不含錠剤(上に記載のとおり)として製剤化された様々な化学的に無関係の活性物質を用いて得られた結果を示す。各々の場合において、(a)は錠剤中の総薬物含有量のパーセントとして薬物の累積放出を示し、(b)は、各時点でのフロースルーセル中の濃度を示す。
固体抗体を含有する錠剤組成物
ベバシズマブの水性注射剤(アバスチンとして市販されている)を出発材料として使用した。賦形剤(例えばトレハロース)を除去するため、医薬品アバスチン(25mg/mlを50μl)をカットオフ10000ダルトンの膜を付けたスピンカラム(Vivascience社製Vivaspin 10000)に入れた。蒸留水(4ml)を加え、カラムを4000rpmで4分間遠心分離した。この工程を2回反復した。薄層クロマトグラフィー(TLC;水性メタノール90%)でトレハロースの除去を確認した。種々の濃度のトレハロース及び未処理アバスチンを対照に使用した。TLCフィルムを硫酸(10%)及びエタノール(90%)の混合物に浸し、次いで加熱した。
試料の注入容量:150μl
移動相:リン酸緩衝液(NaH2PO4、25mM、pH6.8及びNaCl 150mM)
流速:1mL/分
カラム:(Hiload TM、Superdex TM 200)
UV検出機:280nm
図16のデータは、製剤化されたベバシズマブの分子量は、アバスチン対照溶液と比較して変化がない、即ち、精製及び錠剤化工程はこの抗体の凝集を導いていないことを裏付けている。実施例4に示した結果でも同様であるが、本実施例に従って製造された剤形の埋め込み部位への滞留は、例えば点眼剤や眼科用注射剤よりはるかに長いであろう。これは著しい臨床上の利益を提供することになるであろう。
Claims (58)
- 固体の埋め込み可能な剤形であって、固体形態の治療活性物質を、任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなり、前記の1又は2以上の賦形剤が存在する場合は、インビトロで試験した時に、賦形剤を含有しない同等の剤形と比較して、活性物質放出の著明な遅延又は延長を導かない、剤形。
- 疾患の局所的予防又は治療に好適な、請求項1に記載の剤形。
- 眼への、眼周囲への、又は眼内への埋め込みに好適な、請求項1又は請求項2に記載の剤形。
- 滅菌されている、請求項1〜3の何れかに記載の剤形。
- 1又は2以上の賦形剤が、それが存在する場合、インビボ埋め込み後に生分解性及び/又は生体吸収性である、請求項1〜4の何れかに記載の剤形。
- 圧縮により製造される、請求項1〜5の何れかに記載の剤形。
- 錠剤である、請求項6に記載の剤形。
- 0.1mm3〜1.5cm3の体積を持ち、及び/又は5mm以下の最大寸法を有し、及び/又は10mg以下の重量を有する、請求項1〜7の何れかに記載の剤形。
- 実質上賦形剤を含まない、請求項1〜8の何れかに記載の剤形。
- 活性物質が実質上水不溶性である、請求項1〜9の何れかに記載の剤形。
- 活性物質がマトリックスメタロプロテイナーゼインヒビターである、請求項1〜10の何れかに記載の剤形。
- マトリックスメタロプロテイナーゼインヒビターが、マトリックスメタロプロテイナーゼの活性部位において亜鉛と可逆的に結合するヒドロキサム酸誘導体である、請求項11に記載の剤形。
- マトリックスメタロプロテイナーゼインヒビターが右側結合体である、請求項12に記載のマトリックスメタロプロテイナーゼインヒビター。
- 活性物質が、イロマスタット、バチマスタット、マリマスタット、プリノマスタット、タノマスタット、トロケード(シペマスタット)、AG3340、CGs227023A、BAY12−9566、及びBMS−275291より成る群、又はそれらの任意の機能的誘導体から選ばれる、請求項11に記載の剤形。
- 活性物質が、抗癌剤、ステロイド、抗生物質、抗体分子、抗炎症物質及び抗瘢痕形成物質より成る群から選ばれる、請求項1〜10の何れかに記載の剤形。
- 抗癌剤が5−フルオロウラシルであり、ステロイドがトリアムシノロン及びデキサメタゾンから選ばれ、そして、抗炎症物質がナプロキセンである、請求項15に記載の剤形。
- 治療に使用するための、請求項1〜16の何れかに記載の剤形。
- 組織瘢痕形成を防止又は低減させるための、請求項11〜14の何れかに記載の剤形。
- 瘢痕形成が眼、眼周囲又は眼内である、請求項18に記載の剤形。
- 該剤形を緑内障濾過手術後に埋め込む、請求項18又は請求項19に記載の剤形。
- 該剤形を結膜下腔に埋め込む、請求項19又は請求項20に記載の剤形。
- 眼への、眼周囲への、又は眼内への埋め込みによる治療に使用するための埋め込み可能な固体剤形であって、固体形態の治療活性物質を、任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、剤形。
- 活性物質が実質上水不溶性である、請求項22に記載の剤形。
- 活性物質がマトリックスメタロプロテイナーゼインヒビターである、請求項22又は請求項23に記載の剤形。
- 疾患の局所的予防又は治療のための埋め込み用薬剤の製造における、請求項1〜10、又は15の何れかに記載の剤形の使用。
- 組織瘢痕形成の局所的予防又は治療のための埋め込み用薬剤の製造における、請求項11〜14の何れかに記載の剤形の使用。
- 固体形態の治療活性物質を任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、埋め込み可能な固体剤形の使用であって、眼への、眼周囲への、又は眼内への埋め込みによる疾患の局所的予防又は治療のための埋め込み用薬剤の製造のための使用。
- 患者において疾患を局所的に予防又は治療する方法であって、請求項1〜10、又は15の何れかに記載の固体剤形を、該疾患を予防又は治療するに充分な量で、埋め込みにより患者に投与することを含んでなる方法。
- 患者において瘢痕形成を局所的に防止する方法であって、請求項11〜14の何れかに記載の固体剤形を、該瘢痕形成の改善に充分な量で、埋め込みにより患者に投与することを含んでなる方法。
- 該剤形を眼への、眼周囲への、又は眼内への埋め込みにより投与する、請求項29に記載の方法。
- 該剤形を結膜下腔に埋め込む、請求項30に記載の方法。
- 瘢痕形成が緑内障濾過手術後のものである、請求項29〜31の何れかに記載の方法。
- 請求項1〜15の何れかに記載の固体剤形の製造におけるマトリックスメタロプロテイナーゼインヒビターの使用。
- 患者において疾患を局所的に予防又は治療する方法であって、固体形態の治療活性物質を任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる埋め込み可能な固体剤形を、眼への、眼周囲への、又は眼内への埋め込みにより投与することを含んでなる方法。
- 活性物質が実質上水不溶性である、請求項34に記載の方法。
- 活性物質がマトリックスメタロプロテイナーゼインヒビターである、請求項34又は請求項35に記載の方法。
- 患者において組織瘢痕形成を局所的に予防又は治療する方法であって、マトリックスメタロプロテイナーゼインヒビターを任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる埋め込み可能な固体剤形を、局所埋め込みにより投与することを含んでなる方法。
- 組織瘢痕形成の局所的防止又は低減に使用するためのMMPインヒビターであって、MMPインヒビターが、局所埋め込みのための、任意により1又は2以上の医薬的に許容し得る賦形剤を含有していてもよい埋め込み可能な固体薬剤として製剤化される、MMPインヒビター。
- マトリックスメタロプロテイナーゼインヒビターを任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、滅菌されている埋め込み可能な固体剤形。
- 請求項39に記載の剤形を製造する方法であって、
i.マトリックスメタロプロテイナーゼインヒビター及び存在する場合には賦形剤を含有する圧縮剤形、例えば錠剤を製造し、そして、
ii.その圧縮剤形をガンマ線で照射することにより滅菌する、
ことを含んでなる方法。 - 請求項11〜14の何れか1項に記載の剤形及び緑内障濾過手術の実施に必要な手術用機器を含んでなるキット。
- 固体形態の抗体を、任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、固体単位剤形の医薬組成物。
- 抗体がモノクローナル抗体である、請求項42に記載の組成物。
- 抗体が、腫瘍性疾患の予防又は治療を適応とする、例えば抗VEGF抗体である、請求項42又は43に記載の組成物。
- 滅菌されている、請求項42〜44の何れかに記載の組成物。
- 1又は2以上の賦形剤が、それが存在する場合、インビボ埋め込み後に生分解性及び/又は生体吸収性である、請求項42〜45の何れかに記載の組成物。
- 実質上賦形剤を含まない、請求項42〜45の何れかに記載の組成物。
- 圧縮により製造される、請求項42〜47の何れかに記載の組成物。
- 錠剤である、請求項48に記載の組成物。
- 各固体単位剤形が、0.1mm3〜1.5cm3の体積を持ち、及び/又は、5mm以下の最大寸法を有し、及び/又は、10mg以下の重量を有する、請求項42〜49の何れかに記載の組成物。
- 抗体又は非抗体の、固体形態又は非固体形態の、1又は2以上のさらなる治療活性成分を含有する、請求項42〜50の何れかに記載の組成物。
- 治療に使用するための、請求項42〜51の何れかに記載の組成物。
- 腫瘍性疾患の予防又は治療に使用するための、請求項44に記載の組成物。
- 患者において腫瘍性疾患を予防又は治療する方法であって、請求項44に記載の医薬組成物を該患者に投与することを含んでなる方法。
- 固体形態の治療活性物質を、任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、埋め込み可能な固体剤形であって、前記1又は2以上の賦形剤が存在する場合、その1又は2以上の賦形剤の化学的又は生化学的分解により活性物質の放出が制御されない、剤形。
- 固体形態の治療活性物質を任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、埋め込み可能な固体剤形であって、圧縮により製造される剤形。
- 固体形態の治療用又は診断用蛋白物質、例えば抗体を、任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる、固体単位剤形の医薬組成物であって、該剤形が圧縮により製造される医薬組成物。
- インビボ部位を冒している状態を局所的に予防又は治療するために、治療活性物質を前記インビボ部位にデリバリーする方法であって、固体形態の治療活性物質を任意により1又は2以上の医薬的に許容し得る賦形剤と共に含んでなる固体剤形を該部位に埋め込むことを含んでなる方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0722484.3A GB0722484D0 (en) | 2007-11-15 | 2007-11-15 | Solid compositions |
| PCT/GB2008/003851 WO2009063222A2 (en) | 2007-11-15 | 2008-11-17 | Solid compositions |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011503162A true JP2011503162A (ja) | 2011-01-27 |
| JP2011503162A5 JP2011503162A5 (ja) | 2013-11-28 |
Family
ID=38896404
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010533657A Pending JP2011503162A (ja) | 2007-11-15 | 2008-11-17 | 固体組成物 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20100278896A1 (ja) |
| EP (1) | EP2219644A2 (ja) |
| JP (1) | JP2011503162A (ja) |
| CN (1) | CN102316854A (ja) |
| CA (1) | CA2704510A1 (ja) |
| GB (1) | GB0722484D0 (ja) |
| WO (1) | WO2009063222A2 (ja) |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7431710B2 (en) | 2002-04-08 | 2008-10-07 | Glaukos Corporation | Ocular implants with anchors and methods thereof |
| US20100098772A1 (en) * | 2008-10-21 | 2010-04-22 | Allergan, Inc. | Drug delivery systems and methods for treating neovascularization |
| US9636255B2 (en) | 2009-02-13 | 2017-05-02 | Dose Medical Corporation | Uveoscleral drug delivery implant and methods for implanting the same |
| US10206813B2 (en) | 2009-05-18 | 2019-02-19 | Dose Medical Corporation | Implants with controlled drug delivery features and methods of using same |
| GB201017048D0 (en) | 2010-10-08 | 2010-11-24 | Ucl Business Plc | Composition |
| EP2654715B1 (en) | 2010-11-24 | 2017-01-25 | Dose Medical Corporation | Drug eluting ocular implant |
| US10245178B1 (en) | 2011-06-07 | 2019-04-02 | Glaukos Corporation | Anterior chamber drug-eluting ocular implant |
| WO2013177170A2 (en) * | 2012-05-21 | 2013-11-28 | Dcb-Usa Llc | Methods for drug screen using zebrafish model and the compounds screened thereform |
| US10517759B2 (en) | 2013-03-15 | 2019-12-31 | Glaukos Corporation | Glaucoma stent and methods thereof for glaucoma treatment |
| US11548940B2 (en) | 2014-05-15 | 2023-01-10 | Rani Therapeutics, Llc | Anti-interleukin antibody preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US10058595B2 (en) | 2014-05-15 | 2018-08-28 | Incube Labs, Llc | Pharmaceutical compositions and methods for fabrication of solid masses comprising TNF-inhibiting antibodies |
| US10689460B2 (en) | 2014-05-15 | 2020-06-23 | Incube Labs, Llc | PCSK9 antibody preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| EP3677229A1 (en) | 2014-05-29 | 2020-07-08 | Glaukos Corporation | Implants with controlled drug delivery features |
| US9840553B2 (en) | 2014-06-28 | 2017-12-12 | Kodiak Sciences Inc. | Dual PDGF/VEGF antagonists |
| JP7202070B2 (ja) * | 2015-05-01 | 2023-01-11 | ラニ セラピューティクス, エルエルシー | ポリペプチドおよび/またはタンパク質を含む固体塊の製作のための薬学的組成物および方法 |
| CA2984422C (en) * | 2015-05-08 | 2023-10-17 | Incube Labs, Llc | Anti-interleukin antibody preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| WO2017040853A1 (en) | 2015-09-02 | 2017-03-09 | Glaukos Corporation | Drug delivery implants with bi-directional delivery capacity |
| US11564833B2 (en) | 2015-09-25 | 2023-01-31 | Glaukos Corporation | Punctal implants with controlled drug delivery features and methods of using same |
| WO2017117464A1 (en) | 2015-12-30 | 2017-07-06 | Kodiak Sciences Inc. | Antibodies and conjugates thereof |
| JP7003110B2 (ja) | 2016-04-20 | 2022-01-20 | ドーズ メディカル コーポレーション | 生体吸収性眼球薬物送達デバイス |
| US12071476B2 (en) | 2018-03-02 | 2024-08-27 | Kodiak Sciences Inc. | IL-6 antibodies and fusion constructs and conjugates thereof |
| JP2022553640A (ja) | 2019-10-10 | 2022-12-26 | コディアック サイエンシーズ インコーポレイテッド | 眼障害を処置する方法 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58157715A (ja) * | 1982-02-25 | 1983-09-19 | メルク・パテント・ゲゼルシヤフト・ミツト・ベシユレンクテル・ハフツング | デポ薬剤 |
| JPS58165869A (ja) * | 1982-03-18 | 1983-09-30 | メルク・エンド・カムパニ−・インコ−ポレ−テツド | 浸透薬品投与装置 |
| JPH04504103A (ja) * | 1988-07-01 | 1992-07-23 | ファルマシア・アンド・アップジョン・カンパニー | 植込錠から制御放出される抗生物質塩 |
| JPH06505274A (ja) * | 1991-02-21 | 1994-06-16 | ユニバーシティ オブ ケンタッキー リサーチ ファウンデーション | 持続性放出医薬デリバリー装置 |
| JPH11512711A (ja) * | 1995-09-27 | 1999-11-02 | コントロール デリヴァリー システムズ インコーポレイテッド | 身体の内部位置まで薬物を直接供給するための埋め込み可能な放出制御デバイス |
| US6194384B1 (en) * | 1996-06-14 | 2001-02-27 | Theratechnologies, Inc. | Long-acting galenical formulation for GRF peptides |
| US20050048099A1 (en) * | 2003-01-09 | 2005-03-03 | Allergan, Inc. | Ocular implant made by a double extrusion process |
| JP2007523911A (ja) * | 2004-02-26 | 2007-08-23 | アドバンスト アキュラー システムズ リミテッド | 眼病変治療用テトラサイクリン誘導体 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4599361A (en) * | 1985-09-10 | 1986-07-08 | G. D. Searle & Co. | Hydroxamic acid based collagenase inhibitors |
| US4743587A (en) * | 1985-09-10 | 1988-05-10 | G. D. Searle & Co. | Hydroxamic acid based collagenase inhibitors |
| GB8827308D0 (en) * | 1988-11-23 | 1988-12-29 | British Bio Technology | Compounds |
| US5183900A (en) * | 1990-11-21 | 1993-02-02 | Galardy Richard E | Matrix metalloprotease inhibitors |
| US5114953A (en) * | 1990-11-21 | 1992-05-19 | University Of Florida | Treatment for tissue ulceration |
| US5189178A (en) * | 1990-11-21 | 1993-02-23 | Galardy Richard E | Matrix metalloprotease inhibitors |
| US6607748B1 (en) * | 2000-06-29 | 2003-08-19 | Vincent Lenaerts | Cross-linked high amylose starch for use in controlled-release pharmaceutical formulations and processes for its manufacture |
| US6713081B2 (en) * | 2001-03-15 | 2004-03-30 | The United States Of America As Represented By The Department Of Health And Human Services | Ocular therapeutic agent delivery devices and methods for making and using such devices |
| CZ20032901A3 (en) * | 2001-04-26 | 2004-07-14 | Bristol-Myers Squibb Company | Control of compactability through crystallization |
| US20030199449A1 (en) * | 2002-04-19 | 2003-10-23 | Tarcha Peter J. | Combination of ablation and controlled drug delivery for the treatment of cancer |
| US20040253293A1 (en) * | 2003-06-16 | 2004-12-16 | Afshin Shafiee | Rate controlled release of a pharmaceutical agent in a biodegradable device |
| DE10351448A1 (de) * | 2003-11-04 | 2005-06-09 | Bayer Healthcare Ag | Geschmackstoffhaltige Arzneimittelformulierungen mit verbesserten pharmazeutischen Eigenschaften |
-
2007
- 2007-11-15 GB GBGB0722484.3A patent/GB0722484D0/en not_active Ceased
-
2008
- 2008-11-17 EP EP08850655A patent/EP2219644A2/en not_active Withdrawn
- 2008-11-17 CN CN2008801161268A patent/CN102316854A/zh active Pending
- 2008-11-17 WO PCT/GB2008/003851 patent/WO2009063222A2/en active Application Filing
- 2008-11-17 JP JP2010533657A patent/JP2011503162A/ja active Pending
- 2008-11-17 US US12/743,147 patent/US20100278896A1/en not_active Abandoned
- 2008-11-17 CA CA2704510A patent/CA2704510A1/en not_active Abandoned
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58157715A (ja) * | 1982-02-25 | 1983-09-19 | メルク・パテント・ゲゼルシヤフト・ミツト・ベシユレンクテル・ハフツング | デポ薬剤 |
| JPS58165869A (ja) * | 1982-03-18 | 1983-09-30 | メルク・エンド・カムパニ−・インコ−ポレ−テツド | 浸透薬品投与装置 |
| JPH04504103A (ja) * | 1988-07-01 | 1992-07-23 | ファルマシア・アンド・アップジョン・カンパニー | 植込錠から制御放出される抗生物質塩 |
| JPH06505274A (ja) * | 1991-02-21 | 1994-06-16 | ユニバーシティ オブ ケンタッキー リサーチ ファウンデーション | 持続性放出医薬デリバリー装置 |
| JPH11512711A (ja) * | 1995-09-27 | 1999-11-02 | コントロール デリヴァリー システムズ インコーポレイテッド | 身体の内部位置まで薬物を直接供給するための埋め込み可能な放出制御デバイス |
| US6194384B1 (en) * | 1996-06-14 | 2001-02-27 | Theratechnologies, Inc. | Long-acting galenical formulation for GRF peptides |
| US20050048099A1 (en) * | 2003-01-09 | 2005-03-03 | Allergan, Inc. | Ocular implant made by a double extrusion process |
| JP2007523911A (ja) * | 2004-02-26 | 2007-08-23 | アドバンスト アキュラー システムズ リミテッド | 眼病変治療用テトラサイクリン誘導体 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009063222A3 (en) | 2009-07-30 |
| EP2219644A2 (en) | 2010-08-25 |
| US20100278896A1 (en) | 2010-11-04 |
| CN102316854A (zh) | 2012-01-11 |
| CA2704510A1 (en) | 2009-05-22 |
| WO2009063222A2 (en) | 2009-05-22 |
| GB0722484D0 (en) | 2007-12-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2011503162A (ja) | 固体組成物 | |
| JP5696121B2 (ja) | α−2アドレナリン受容体アゴニスト含有生分解性眼内インプラント | |
| JP6986758B2 (ja) | デンドリマー−生体接着性ポリマーヒドロゲルナノ接着剤およびその使用 | |
| JP6570513B2 (ja) | 持続的眼内放出のためのマイクロスフェア薬剤送達システム | |
| AU2007223057B2 (en) | Ocular therapy using sirtuin-activating agents | |
| JP5485314B2 (ja) | 2ヶ月を超える期間の長期持続放出を与えるステロイド眼内インプラント | |
| RU2389479C2 (ru) | Глазной имплантат, изготавливаемый способом двойной экструзии | |
| JP2015013863A (ja) | 増大した前眼部クリアランス速度を有するα−2アドレナリン受容体アゴニストを用いる眼科治療 | |
| JP2007523911A (ja) | 眼病変治療用テトラサイクリン誘導体 | |
| TW200826963A (en) | Water insoluble polymer matrix for drug delivery | |
| MX2007003789A (es) | Suministro ocular de formulaciones polimericas para suministro. | |
| Fedorchak et al. | 28-day intraocular pressure reduction with a single dose of brimonidine tartrate-loaded microspheres | |
| CN105682645A (zh) | 含前列腺酰胺的眼内植入物及其使用方法 | |
| JP2024001149A (ja) | 抗菌剤及び抗炎症剤を含む眼内投与のための医薬組成物 | |
| JP2013535485A (ja) | 薬物の持続送達のためのコラーゲン系インプラント | |
| Eperon et al. | A biodegradable drug delivery system for the treatment of postoperative inflammation | |
| Garg et al. | In-situ gel: a smart carrier for drug delivery | |
| Zhang et al. | Prophylaxis of posterior capsule opacification through autophagy activation with indomethacin-eluting intraocular lens | |
| Mukherjee et al. | Chitosan-based nanomedicine in the management of age-related macular degeneration: a review | |
| Sha et al. | In situ gels: The next new frontier in ophthalmic drug delivery system | |
| JP2005538160A (ja) | 眼組織を治癒するための抗炎症性マイクロスフェア含有組成物 | |
| AU2010289618B2 (en) | Ketorolac tromethamine compositions for treating or preventing ocular pain | |
| US20160317438A1 (en) | Injectable sustained release intraocular device | |
| Zhang et al. | Preparation and evaluation of a novel biodegradable long-acting intravitreal implant containing ligustrazine for the treatment of proliferative vitreoretinopathy | |
| KR102191180B1 (ko) | 안질환 치료용 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111110 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20111110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121001 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130621 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130709 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20131009 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131210 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140513 |