JP2010511707A - 亜塩素酸塩および過酸化水素を含む相乗的抗菌製剤 - Google Patents
亜塩素酸塩および過酸化水素を含む相乗的抗菌製剤 Download PDFInfo
- Publication number
- JP2010511707A JP2010511707A JP2009540253A JP2009540253A JP2010511707A JP 2010511707 A JP2010511707 A JP 2010511707A JP 2009540253 A JP2009540253 A JP 2009540253A JP 2009540253 A JP2009540253 A JP 2009540253A JP 2010511707 A JP2010511707 A JP 2010511707A
- Authority
- JP
- Japan
- Prior art keywords
- formulation
- weight
- chlorite
- hydrogen peroxide
- ophthalmic formulation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N59/00—Biocides, pest repellants or attractants, or plant growth regulators containing elements or inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/726—Glycosaminoglycans, i.e. mucopolysaccharides
- A61K31/728—Hyaluronic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/14—Alkali metal chlorides; Alkaline earth metal chlorides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/20—Elemental chlorine; Inorganic compounds releasing chlorine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/22—Boron compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/40—Peroxides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L12/00—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor
- A61L12/08—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor using chemical substances
- A61L12/10—Halogens or compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L12/00—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor
- A61L12/08—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor using chemical substances
- A61L12/12—Non-macromolecular oxygen-containing compounds, e.g. hydrogen peroxide or ozone
- A61L12/124—Hydrogen peroxide; Peroxy compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/04—Artificial tears; Irrigation solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
Abstract
Description
(関連出願の相互参照)
本発明は、1999年10月4日出願の米国特許出願第09/412,174号の部分継続出願である、2001年7月23日出願の米国特許出願第09/911,638号の部分継続出願である、2003年7月7日に出願の米国特許出願第10/614,646号の部分継続出願であり、それぞれの開示全体が参照により本明細書に明確に組み込まれている。
(連邦政府支援による研究/開発に関する記述)
該当なし
従来技術としては、様々な物品の殺菌および治癒、もしくはそのいずれかを助けるために微生物の増殖を予防または防止することが望ましい皮膚疾患(例えば、創傷、火傷、擦過傷、感染症)の消毒および治療、もしくはそのいずれかのための生物への局所的施用に使用可能と言われてきた多数の抗菌剤があった。当該の局所的抗菌剤は、ヨウ素、マーキュロクロム、過酸化水素、および二酸化塩素などの多種多様な活性殺菌成分を含んでいた。
i.従来の二酸化塩素製剤
二酸化塩素の前駆物質である亜塩素酸塩は、飲料水の殺菌剤として、またコンタクトレンズの防腐剤として使用可能であることが知られている。しかし、亜塩素酸塩は皮膚への局所施用において許容可能で安全な範囲の濃度(例えば、50〜1000百万分率)では弱い殺菌活性しか示さない。そのため亜塩素酸塩は、皮膚への局所施用のための製剤の活性殺菌成分として通常使われてこなかった。
許文献4に記載されているように、二酸化塩素は(a)2つの炭素原子間の二重結合の酸化;(b)不飽和脂肪酸(脂質)の2つの炭素原子間の二重結合における酸化;(c)カルボン酸無水物の加水分解の加速;(d)対応するカルボン酸へのアルデヒド類の酸化;(e)アルコール類の酸化;(f)アミン類の酸化;(g)フェノール類、フェノール誘導体、およびチオフェノール化合物の酸化;(h)ヒドロキノン類の穏やかな酸化;(i)アミノ酸、タンパク質、およびポリアミド類の酸化;(j)硝酸塩および硫化物の酸化;ならびに(k)炭水化物のCHOおよびCH2OHラジカルからカルボン酸官能基を生じる変化に利用することができる。
されている。デ・グェバラの特許によると、安定化された二酸化塩素の消毒液は、ホウ素化合物および二酸化塩素が反応活性錯体として溶液中に存在する、二酸化塩素および無機ホウ素化合物の水溶液から作ることができる。この安定状態に固定された二酸化塩素が、消毒液の必須成分である。デ・グェバラの特許は、二酸化塩素をin situで発生させることによって、または二酸化塩素ガスを溶液中に通気させて外部で発生させた二酸化塩素を溶液中に取り入れることによって、二酸化塩素を配合に取り入れることもできることを開示している。外部での二酸化塩素の生成には、硫酸と塩素酸カリウムの反応または塩素酸塩と含水シュウ酸の反応など様々な方法を採用することができる。あるいは、二酸化塩素は、塩素酸カリウムと硫酸の反応によりin situで生成することもできる。二酸化塩素がin situで生成されようと外部で生成されようと、基本的に酸で誘発される塩素酸カリウムからの二酸化塩素の遊離であることに留意されたい。
ii.抗生物質製剤
抗生化合物も、火傷、創傷、ならびに皮膚および眼の感染症の治療上の処置として一般的に用いられてきた。抗生物質は効果的な治療をもたらす一方で、抗生物質の臨床環境における使用にはしばしばいくつかの危険を伴う。これらの危険としては、それだけには限られないが、(1)身体の正常なフローラが変化し、抗生物質耐性生物の増殖による「重感染」を引き起こす;(2)特に、種類によっては腎臓、肝臓、および神経組織への損傷が生じる可能性がある抗生物質の長期使用による、抗生物質の直接的な毒性;(3)抗生物質によるさらなる治療が効かない、抗生物質耐性微生物集団の発生などを挙げることができる。
B.創傷、火傷、擦過傷および感染症以外の治療が困難な皮膚疾患
特定の患者および特定の健康状態下、もしくはそのいずれかでは、軽微な創傷および擦過傷でさえも治療が困難になる場合がある一方で、治療を成功させるのが特に困難である乾癬および皮膚潰瘍などのよく知られた皮膚疾患がある。
i.乾癬
乾癬は、銀白色の鱗屑で覆われた、炎症を起こして腫れた皮膚病変として最も一般的に現れる、非伝染性皮膚疾患である。この最も一般的な種類の乾癬は、「尋常性乾癬」と呼ばれる。乾癬は、多種多様で様々な重症度で出現する。様々な種類の乾癬が、膿様の水膨れ(膿疱性乾癬)、皮膚の重症の腐肉形成(乾癬性紅皮症)、滴状の斑点(滴状乾癬)、および炎症を起こした滑らかな病変部(インバス乾癬)などの特徴を呈する。
ii.皮膚潰瘍
皮膚潰瘍は、圧力、摩耗、または原発性/続発性血管疾患の結果として生じることが知られている。皮膚潰瘍は一般的に、以下のような病因によって分類される。
C.コンタクトレンズの保存および殺菌
コンタクトレンズを眼から取り外した時には、再度着用するまでコンタクトレンズを保存殺菌溶液中にいつも入れておかなければならない。保存殺菌溶液には以下の機能がある。
2.細菌で汚染されたレンズによる眼の感染症を予防すること;および
3.着用中にレンズが達する水和平衡状態を維持すること。
D.コンタクトレンズの洗浄
刺激、灼熱感、および赤みによりレンズ着用を不快にする粘液物質、脂質およびタンパク質がレンズ着用中にコンタクトレンズに蓄積する。その結果、視野がかすむ。不快な問題を軽減するためには、ソフトまたはハードコンタクトレンズを眼から取り出して、酵素的洗浄剤および殺菌液を用いて定期的に洗浄して殺菌しなければならない。ソフトレンズに関連する重篤な合併症の一つは、巨大乳頭結膜炎(GPC)であろう。巨大乳頭結膜炎の発生は、主にソフトコンタクトレンズの合併症に関連する炎症反応によると考えられている。これはほとんどの場合、コンタクトレンズへのタンパク質の沈着によって引き起こされる。GPCは無症候から痒み、上眼瞼浮腫、眼の充血、粘液様分泌物、進行性のコンタクトレンズ不耐性におよぶ症状を生じる。本発明の眼内洗浄剤は、タンパク質の沈着を効果的に洗浄し、角膜表面を微生物の感染から守ると同時に分子状酸素を供給することによって角膜上皮細胞を健康に保ち、その結果としてソフトおよびハードコンタクトレンズ両方の着用者に利便性と利益をもたらす。
E.眼疾患の治療
i.ドライアイ
ドライアイは涙液の産生が不十分であるか、または角膜および結膜を適切に湿らせるのに涙液の組成が不適切である症候群である。涙液に関連する様々な眼疾患が、眼の乾燥、眼内に生じた異物の存在による不快感を引き起こす。大部分の症例では、涙液層が正常な連続性を失って急速に途切れ、自発的な瞬きの間隔にその構造を維持することができない。これら全ての涙液の異常は、複数の原因があろう。おそらく最も一般的なドライアイのタイプは、涙液中の水溶性成分の減少によるものである。未治療のドライアイは、さらに微生物感染によってより複雑化する可能性もある、より重症の上皮びらん、糸状の上皮細胞、および角膜上の局所的なドライスポットへとさらに悪化させる可能性もある。しかし、より軽いタイプのドライアイでは、眼の乾燥感および刺激感は人工涙液で解決することもできる。したがって、角膜潤滑性を備える広域スペクトル抗菌活性を持った人工涙液は、快適性だけでなく損傷を受けた角膜表面の回復に有益な効果ももたらすことができる。ii.アレルギー性結膜炎
大気中アレルゲンまたは手を介したアレルゲンは、通常、IgEを介した過敏反応によりアレルギー性結膜炎を引き起こす。アレルギー性結膜炎は、眼瞼の腫れ、結膜充血、乳頭反応、キモシン、および粘着性の粘液様分泌物などを含む、掻痒および流涙を伴い乾燥し粘ついた眼を呈する。人工涙液の製剤中に含まれる、涙液中のヒアルロン酸の存在は、アレルゲンとの接触から角膜表面を保護するだろう。本発明の広域スペクトル抗菌剤は、角膜表面の細菌感染を防ぎ、分子状酸素を供給することによって角膜上皮細胞を健康に保つ。したがって、アレルゲンに過敏な眼に対して、有益な効果をもたらす。
iii.細菌侵入
細菌性角膜炎は、世界の失明の主要原因の一つである。先進国でのコンタクトレンズ着用の人気が罹患率上昇の原因となり、合衆国では毎年推定30,000症例が発生している。統計調査によると、合衆国では100,000人のコンタクトレンズ着用者に対して、毎年約30人が潰瘍性角膜炎を発症することが示されており、その結果、潜在的に失明する可能性があるという観点から、この疾患は重大な公衆衛生問題となっている。眼瞼、眼瞼のまばたき、ならびに角膜および結膜上皮細胞は、微生物の侵入に対する障壁となっているが、この防衛機構の1つまたは複数が損なわれる場合がある。このような弱体化としては、眼瞼の異常、角膜表面の露出、涙液の生成不足、上皮の問題、薬剤の毒性、外傷、および切開手術などを挙げることができる。細菌性角膜炎の眼症状の徴候は、重篤な侵入および時間と共に穿孔を引き起こす可能性もある壊死を引き起こす傾向があるブドウ球菌(staphylococcus)および連鎖球菌(streptococcus)の感染で認められる。緑膿菌性(pseudomonal)角膜炎は、急速に進行する傾向がある。この生物は、プロテアーゼ、リパーゼおよびエラスターゼなどの破壊酵素、ならびに壊死性潰瘍および穿孔をもたらす外毒素を生成する。セラチア(serratia)角膜炎は、悪性の潰瘍および穿孔を形成する場合もある外毒素およびプロテアーゼを分泌しながら、傍中心の表在性潰瘍として始まる。細菌性角膜炎が成立するためには、微生物付着が宿主細胞の受容体に結合しなければならない。この接着が一旦生じると、炎症、壊死および血管新生の破壊的プロセスが続いて起こる可能性がある。
さらに、本発明によると、本発明の亜塩素酸塩/過酸化水素製剤の施用または投与により、瘢痕形成を防止する方法が提供される。
れた製品の製剤が提供される。
また、本発明によると、本発明の亜塩素酸塩/過酸化水素製剤の施用または投与により眼の感染症、眼の穿孔および炎症を防止する方法が提供される。
は、好ましくは約0.005から約0.06%(重量/体積)の亜塩素酸塩を含み、また好ましくは約0.0002から約0.05%(重量/体積)の過酸化水素を含む。この場合もやはり、過酸化水素の存在は、涙液中のカタラーゼと接触して、角膜に対して有益な酸素分子をもたらす。
A.製剤
本発明の亜塩素酸塩/過酸化物製剤は、溶液、ゲル、軟膏、クリーム、スプレーなどの様々な方法で製剤することができる。以下、本発明に従って調製されるであろう具体的な製剤タイプの数例を説明する。
i.安定な亜塩素酸塩/過酸化物溶液
以下の処方1は、本発明の亜塩素酸塩/過酸化物溶液の第1の好適な製剤である。
処方1
亜塩素酸ナトリウム・・・0.005%〜0.10%
過酸化水素・・・0.005%〜0.05%
Methocel A・・・0.05%〜0.2%
ホウ酸・・・0.15%
塩化ナトリウム・・・0.75%
Pluronic F 68/F-127・・・0.1%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
以下の処方2は、本発明の亜塩素酸塩/過酸化物溶液の第2の好適な製剤である。
処方2
亜塩素酸ナトリウム・・・0.05%
過酸化水素・・・0.02%
カルボキシメチルセルロース・・・0.01%
ホウ酸・・・0.15%
塩化ナトリウム・・・0.75%
Pluronic F 68/F-127・・・0.1%
HClまたはNaOH・・・pH7.3に調整
精製水・・・所定体積まで十分量
上記の好適な製剤の溶液などの本発明の亜塩素酸塩/過酸化物溶液は、必ずしもそれに限られないが、a)コンタクトレンズ、医用/歯科用機器、調理台、診療台、くしやブラシなどの物品もしくは表面の殺菌;皮膚または身体の一部の消毒(例えば、手洗い用殺菌洗剤、消毒スクラブ洗顔料など)およびb)創傷、火傷、感染症、潰瘍、口唇ヘルペス、乾癬、座瘡などの皮膚(すなわち、皮膚もしくは粘膜)疾患の治療または予防、およびc)瘢痕形成の防止または予防、およびd)眼疾患(例えば、感染症または細菌性角膜炎により生じた炎症)の治療など、様々な医学的および非医学的用途に用いることができる。
ii.安定な亜塩素酸塩/過酸化物ゲル
以下の処方3は、現在のところ、本発明の亜塩素酸塩/過酸化物ゲルの好適な製剤であ
る。
処方3
亜塩素酸ナトリウム・・・0.02%〜0.10%
過酸化水素・・・0.005%〜0.05%
Methocel A・・・2.0%
ホウ酸・・・0.15%
塩化ナトリウム・・・0.75%
Pluronic F 68/F-127・・・0.1%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
本発明のいずれの製剤も、周知のリポソーム形成手法に従って調製したリポソームを形成することにより、および薬剤的に許容可能で効果的な量(例えば、一般的には1〜20重量%)のポリマーマトリックスまたは下記の1つもしくは複数の持続放出成分を製剤に加えることにより、もしくはその一方で、活性成分を持続放出するよう製剤することもできる。
セルロースエステル;
ヒドロキシメチルプロピルセルロース;
メチルヒドロキシエチルセルロース;
ヒドロキシプロピルセルロース;
ヒドロキシエチルセルロース;
カルボキシメチルセルロース;
セルロースエステルの塩;
酢酸セルロース;
ヒドロキシプロピルメチルセルロースフタレート;
メタクリル酸‐メチルメタクリレートコポリマー;
メタクリル酸‐酢酸エチルコポリマー;
ポリビニルピロリドン;
ポリビニルアルコール;
ヒアルロン酸;
リン脂質;
コレステロール;
中性電荷を持つリン脂質;
負電荷を持つリン脂質;
ジパルミトイルホスファチジルコリン;
ジパルミトイルホスファチジルセリン;および
それらのナトリウム塩。
iii.安定な眼科用亜塩素酸塩/過酸化物溶液
以下の処方4は、現在のところ、眼の中にある、または眼から取り出したコンタクトレンズの洗浄に使用する亜塩素酸塩/過酸化物コンタクトレンズ殺菌液の好適な製剤である。この製剤は、更にドライアイの対象者において潤滑のための涙液製品として機能する。処方4
亜塩素酸ナトリウム・・・0.002%〜0.20%
過酸化水素・・・0.005%〜0.05%
ヒアルロン酸・・・0.001%〜0.50%
ホウ酸・・・0.15%
塩化ナトリウム・・・0.75%
Pluronic 127・・・0.05%〜2.0%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
先に示したように、本発明の亜塩素酸塩/過酸化物製剤は、溶液、ゲル、軟膏、クリー
ム、スプレーなどのいずれの形に製剤されていようと、室温で保存中に二酸化塩素を発生せずに、活性成分として亜塩素酸ナトリウムなどの亜塩素酸塩および過酸化水素をpH5.0〜8.8の範囲に維持するよう特別に構成される。例として、特定の範囲内でpHレベルが異なる処方2に従った亜塩素酸塩/過酸化水素溶液について、複数の実験を実施した。しかし、当該の実験は、溶液の形のみに限られることはなく、pHレベルが異なる本亜塩素酸塩/過酸化物製剤の様々な形態において二酸化塩素が生成されないことを説明するために行われたものであることを本明細書において明確に述べておく。
ボ溶液を更に用いた。
プラシーボ溶液
過酸化水素・・・0.02%
カルボキシメチルセルロース・・・0.01%
ホウ酸・・・0.15%
塩化ナトリウム・・・0.75%
Pluronic F 68/F-127・・・0.1%
HClまたはNaOH・・・pH7.3に調整
精製水・・・所定体積まで十分量
実験例1:pHレベル7.3
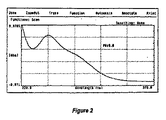
実験:第1のキュベットをプラシーボ溶液で満たし、キュベットをきれいに拭って分光光度計の標準ビーム経路に置く。第2のキュベットを亜塩素酸ナトリウム/過酸化水素溶液で満たし、キュベットをきれいに拭って分光光度計の試料ビーム経路に置く。200nmから400nmまで溶液をスキャンし、結果を記録する。図1に示すグラフに示すように、結果をプロットしプリントアウトする。
亜塩素酸ナトリウムは、260nmに吸収極大があり、一方、亜塩素酸ナトリウムの分解産物である二酸化塩素は、355nm〜358nmに吸収極大がある。
解釈:亜塩素酸ナトリウム/過酸化水素溶液は、260nmの亜塩素酸ナトリウムのピークを示すが、355nm〜358nmの二酸化塩素のピークは全く示さない。
実験例2:pHレベル8.0
実験:プラシーボ溶液を25mLおよび亜塩素酸ナトリウム/過酸化水素溶液を25mL、2つの清浄な容器に分注する。各容器に0.1規定濃度の水酸化ナトリウム溶液を加え、プラシーボ溶液および亜塩素酸ナトリウム/過酸化水素溶液双方のpHレベルを8.0に調整する。
解釈:亜塩素酸ナトリウム/過酸化水素溶液は、260nmの亜塩素酸ナトリウムのピークを示すが、355nm〜358nmの二酸化塩素のピークは全く示さない。これは、pHレベル8.0では亜塩素酸ナトリウム/過酸化水素溶液は亜塩素酸ナトリウムのみを含み、二酸化塩素は多少なりとも含まないことを明らかに示す。これは、亜塩素酸ナトリウムがpHレベル8.0で安定であり、亜塩素酸ナトリウムが分解して二酸化塩素を形成していないという明らかな証拠である。
実験例3:pHレベル8.8
プラシーボ溶液を25mLおよび亜塩素酸ナトリウム/過酸化水素溶液を25mL、2つの清浄な容器に分注する。各容器に0.1規定濃度の水酸化ナトリウム溶液を加え、プラシーボ溶液および亜塩素酸ナトリウム/過酸化水素溶液双方のpHレベルを8.8に調整する。
論じたように、亜塩素酸ナトリウムは、260nmに吸収極大があり、一方、亜塩素酸ナトリウムの分解産物である二酸化塩素は、355nm〜358nmに吸収極大がある。
解釈:亜塩素酸ナトリウム/過酸化水素溶液は、260nmの亜塩素酸ナトリウムのピークを示すが、355nm〜358nmの二酸化塩素のピークは全く示さない。これは、pHレベル8.8では亜塩素酸ナトリウム/過酸化水素溶液は亜塩素酸ナトリウムのみを含み、二酸化塩素は多少なりとも含まないことを明らかに示す。これは、亜塩素酸ナトリウムがpHレベル8.8で安定であり、亜塩素酸ナトリウムが分解して二酸化塩素を形成していないという明らかな証拠である。
実験例4:pHレベル7.0
実験:プラシーボ溶液を25mLおよび亜塩素酸ナトリウム/過酸化水素溶液を25mL、2つの清浄な容器に分注する。各容器に0.1規定濃度の塩酸溶液を加え、プラシーボ溶液および亜塩素酸ナトリウム/過酸化水素溶液双方のpHレベルを7.0に調整する。
実験:プラシーボ溶液を25mLおよび亜塩素酸ナトリウム/過酸化水素溶液を25mL、2つの清浄な容器に分注する。各容器に0.1規定濃度の塩酸溶液を加え、プラシーボ溶液および亜塩素酸ナトリウム/過酸化水素溶液双方のpHレベルを6.44に調整する。
プラシーボ溶液は活性成分として過酸化水素、ならびにpH=6.44で緩衝剤および等張化剤を含んでいた。過酸化水素は200nmから400nmの範囲では吸収がなく、したがって、過酸化水素の吸収ピークは検出されなかった。亜塩素酸ナトリウムは、260nmに吸収極大があり、一方、亜塩素酸ナトリウムの分解産物である二酸化塩素は、355nm〜358nmに吸収極大がある。
解釈:亜塩素酸ナトリウム/過酸化水素溶液は、260nmの亜塩素酸ナトリウムのピークを示すが、355nm〜358nmの二酸化塩素のピークは全く示さない。これは、pH6.44では溶液は亜塩素酸ナトリウムのみを含み、二酸化塩素は多少なりとも含まないことを明らかに示す。これは、亜塩素酸ナトリウムがpH6.44で安定であり、亜塩素酸ナトリウムが分解して二酸化塩素を形成していないという明らかな証拠である。
実験例6:pHレベル6.0
実験:プラシーボ溶液を25mLおよび亜塩素酸ナトリウム/過酸化水素溶液を25mL、2つの清浄な容器に分注する。各容器に0.1規定濃度の塩酸溶液を加え、プラシーボ溶液および亜塩素酸ナトリウム/過酸化水素溶液双方のpHレベルを6.0に調整する。
実験:プラシーボ溶液を25mLおよび亜塩素酸ナトリウム/過酸化水素溶液を25mL、2つの清浄な容器に分注する。各容器に0.1規定濃度の塩酸溶液を加え、プラシーボ溶液および殺菌溶液双方のpHを1.5に調整する。
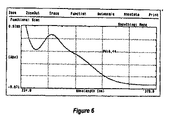
の標準ビーム経路に置く。第2のキュベットを亜塩素酸ナトリウム/過酸化水素溶液で満たし、キュベットをきれいに拭って分光光度計の試料ビーム経路に置く。200nmから400nmまで溶液をスキャンし、結果を記録する。図7に示すグラフに示すように、結果をプロットしプリントアウトする。
実験例1〜7の結果
亜塩素酸ナトリウム/過酸化水素溶液は、活性成分として亜塩素酸ナトリウムおよび過酸化水素を、ならびにpHレベル1.5、6.0、6.44、7.0、7.3、8.0、および8.8で緩衝剤および等張化剤を含んでいた。
亜塩素酸ナトリウムは、260nmに吸収極大があり、一方、二酸化塩素は、355nm〜358nmに吸収極大がある。
実験例1〜7の結果の解釈
pHレベル6.0、6.44、7.0、7.3、8.0、および8.8の亜塩素酸ナトリウム/過酸化水素溶液は、260nmの亜塩素酸ナトリウムのピークを示すが、355nm〜358nmの二酸化塩素のピークの存在は示さない。
実験例1〜7の結果の結論
結果は、pHレベル1.5、6.0、6.44、7.0、7.3、8.0、および8.8の亜塩素酸ナトリウム/過酸化水素溶液に存在する亜塩素酸ナトリウムおよび二酸化塩素のレベルを定量的に測定できることを明確に示している。
B.治療用途の実施例
以下は、本発明の亜塩素酸塩/過酸化物製剤の治療用途の具体的な実施例である。
i.実施例1:乾癬の治療‐非クロスオーバー実験
両腕に乾癬プラークがある患者を以下のように治療する。
過酸化水素・・・0.01%
HPMC・・・2.0%
ホウ酸・・・0.15%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
市販の0.1%トリアムシノロンアセトニドクリームを1日2回、右腕のプラークのみに塗布する。
ii.実施例2:乾癬の治療‐クロスオーバー実験
両腕に乾癬プラークがある患者を以下のように2週間治療する。
過酸化水素・・・0.01%
HPMC・・・2.0%
ホウ酸・・・0.15%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量/100%
市販の0.1%トリアムシノロンアセトニドクリームを1日2回、右腕のプラークのみに塗布する。
本実施例で上述した同一の市販の0.1%トリアムシノロンアセトニドクリームを1日2回、左腕のプラークのみに塗布する。
第2の治療期間の開始から24時間以内に、右腕の乾癬病巣は正常な状態に戻りはじめた。3日目までに、および第2の2週間の治療期間の終わりまで継続して、右腕の乾癬病巣は実質的に消失した。
iii.実施例3:口唇ヘルペスの治療
唇に痛みを伴った、中に液体を含む口唇ヘルペス(すなわち、下疳)がある患者を、上記処方1に従って調製した亜塩素酸塩/過酸化物製剤を1日2回、口唇に塗布することによって治療した。
iv.実施例4:静脈性潰瘍の治療
右足に9〜12ヶ月前から存在する直径3〜4cmの静脈性潰瘍がある患者に対して、上記処方1に従って調製した亜塩素酸塩/過酸化物溶液をガーゼに浸して1日2回、潰瘍に貼り付けて治療した。
v.実施例5:糖尿病性褥瘡性潰瘍の治療
12〜18ヶ月間、両脚部および何本かの足指に褥瘡性潰瘍がある歩行不能の糖尿病患者について、清浄な滅菌ガーゼを潰瘍に貼り付けて、毎日1日3回、上記処方1に従って調製した亜塩素酸塩/過酸化物溶液をガーゼに染みこませることにより治療した。亜塩素酸塩/過酸化水素治療開始後4から7日以内に、潰瘍の赤みが縮小し、きれいに乾燥し始めた。亜塩素酸塩/過酸化水素治療開始後約7から10日後、肉芽組織が潰瘍内に形成し始めた。12から14日以内に、特に重症で足指の骨にまで潰瘍が浸潤していた一本の足指を除いて、再上皮形成が潰瘍領域内で始まったのが認められた。治療開始から30から45日以内に、重症の足指の潰瘍を除く全ての潰瘍が完全に閉じ、異常な瘢痕形成もなく、再上皮形成化した。また治療開始後30から45日で、足指の潰瘍も実質的により小さくなり(しかし、完全には閉鎖されなかった)、患者は歩行することができた。処方1および2などの本発明の液体、およびゲル製剤もしくはそのいずれかは、創傷、火傷、座瘡、感染症、外傷、外科的切開、または他の瘢痕を形成しつつある病巣もしくは疾患による瘢痕形成を予防するために局所的に施用することもできる。
vi.実施例6
a.ドライアイ症状の治療
ドライアイ症状の患者には、眼にむずむずおよびちくちくする痒みがある。極端な症例では、健康維持を妨げかねないさらに深刻な問題を抱えている。以下の処方の好適な涙液製品で患者の治療を行った。
処方:
亜塩素酸ナトリウム・・・0.005〜0.02%
過酸化水素・・・0.01%
メチルセルロースA4M・・・0.075%
ヒアルロン酸・・・0.10%〜0.125%
ホウ酸・・・0.15%
塩化ナトリウム、米国薬局方・・・0.75%
Pluronic 127・・・0.10%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
ローズベンガル染色またはフルオレセインを用いて検査することにより、ドライアイ患者の角膜上皮の健康状態に関する良い指標が得られ、さらに、ローズベンガル染色により角膜および結膜上の死んだ上皮細胞の数の良い指標が得られる。
b.アレルギー性結膜炎の治療
上記の好適な涙液製品によるドライアイ症状の治療に加え、この製品はアレルギー性結膜炎による症状の治療についてもテストされた。具体的には、眼にむずむずおよびちくちくする痒みがあり、常時流涙がある二人のアレルギー性結膜炎患者に、1日3回、2滴の本製品を施用した。この投薬の結果、症状が消失した。
C.コンタクトレンズ洗浄の実施例
i.実施例1:浸漬、洗浄、および殺菌
以下の処方が、従来の浸漬によるコンタクトレンズの洗浄に適用可能な、好適な殺菌溶液である。
亜塩素酸ナトリウム・・・0.005%
過酸化水素・・・0.02%
メチルセルロースA4M・・・0.075%
ヒアルロン酸・・・0.05%〜0.10%
ホウ酸・・・0.15%
Pluronic 127・・・0.25%〜0.50%
塩化ナトリウム、米国薬局方・・・0.75%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
親水性のソフトコンタクトレンズを使用する6人の被験者が、レンズを上記の殺菌溶液に浸し、次いで、レンズを眼内に直接装着した。浸漬は毎晩行うか、または必要に応じて随時行った。6人の被験者全員が、レンズが非常に快適に感じ、また有害影響(例えば、灼熱感、刺すような感覚、赤み、痛み)は経験しなかったと報告した。また、溶液は、レンズの快適さと清浄状態を、他の市販の殺菌液で得られるよりも数週間延長させた。
ii.実験例2:着用時の洗浄
以下の処方は、眼に溶液を入れることで、コンタクトレンズ着用状態での洗浄に適用可能な、好適な眼内殺菌溶液である。
亜塩素酸ナトリウム・・・0.02%
過酸化水素・・・0.01〜0.02%
メチルセルロースA4M・・・0.075%
ヒアルロン酸・・・0.075%〜0.10%
ホウ酸・・・0.15%
塩化ナトリウム、米国薬局方・・・0.75%
Pluronic 127・・・0.75%
HClまたはNaOH・・・pH7.4に調整
精製水・・・所定体積まで十分量
4人の被験者が、上記の眼内溶液をコンタクトレンズに1日3回2滴ずつ30日間コンタクトレンズ着用時に施用した。被験者全員の検査結果は、刺激、灼熱感、刺すような痛み、または他のあらゆる種類の有害影響を示さなかった。この被験者らは、さらに、溶液が心地よく、滑らかで潤いがあると感じたことを報告した。
D.In vitroおよびin vivoでの抗菌効果
i.相乗的活性
表IおよびIIは、(a)400ppmの亜塩素酸ナトリウム単独、(b)200ppmの過酸化水素単独、ならびに(c)400ppmの亜塩素酸ナトリウムおよび200ppmの過酸化水素の併用について、共にヒトの感染症を起こした眼から単離されたスタフィロコッカス・ヘモリチカス(staphylococcus haemolyticus)(表I)および緑膿菌(pseudomonas aeruginosa)(表II)の抗生物質耐性株に対する抗菌効果を比較している。表IおよびIIは、試験液の導入後1時間および2時間時点での抗菌作用についてまとめている。
素酸ナトリウム‐過酸化水素併用は、本実験で用いられた緑膿菌の株に対して相乗作用を示したと結論される。
ii.動物試験
ウサギ12匹のそれぞれ右眼に50,000CFU/mlのスタフィロコッカス・ヘモリチカスを含むブロスを擦り傷をつけた角膜上に滴下して、スタフィロコッカス・ヘモリチカス角膜炎を誘発した。24時間後、全ての角膜が同じように感染した。ウサギをランダムに3つの群に分けた。グループIのウサギ(5匹)は、コンタクトレンズを装着した状態で洗浄する際に、上で定義した亜塩素酸‐過酸化水素処方で処置し(ここで、「殺菌剤」と称する);グループIIのウサギ(5匹)は、市販の0.3%オフロキサシン抗生物質点眼薬で処置し;グループIIIのウサギ(2匹)は、コントロールとするため無処置とした。
i.高濃度過酸化水素の眼における耐容性
以前は、ヒトの眼における過酸化水素の耐容性の上限は、約100ppm(0.01重量%)であると考えられた。パウ J.R.(Paugh,J.R.)、ブレナン N.A.(Brennan,N.A.)、エフロン N(Efron,N.)、Ocular
Response to Hydrogen Peroxide、Am.J.Optom.Physiol.Opt.1988年2月;第65(2)版:91〜8ページを参照のこと。しかし、以下の実験は、亜塩素酸ナトリウムと組み合わせた場合、ヒトの眼は500ppm(0.05重量%)までの濃度の過酸化水素に良好な耐容性を示すことを示している。以下の全ての実験において、過酸化水素は、pH7.4の0.2%ホウ酸に400ppm(0.04重量%)の亜塩素酸ナトリウムと配合され、0.2μmのAcrodiscシリンジフィルターで濾過された。次いで、各処方を2滴ずつ正常なヒトの両眼の盲嚢に置いた。液滴を滴下した時に、被験者は眼瞼を閉じるよう指示された。被験者の処理を行った眼の症状を、滴下後1時間以上にわたって、灼熱感および刺すような感覚、痛
み、赤み、流涙、痒み、光視症、羞明、分泌物、および異物感について観察および評価した。観察結果を以下に示す。
ii.眼内での過酸化水素/亜塩素酸ナトリウムの分解
以下の実験は、ヒトの眼内に入れた場合の過酸化水素/亜塩素酸ナトリウム製剤の自己分解速度を測定する目的、および「眼内」コンタクトレンズ洗浄剤製品または人工涙液製品に使用された場合に、製剤に関連した眼の総合的症状のレベルを測定する目的で設計された。
実験1:「眼内」コンタクトレンズ洗浄剤
100mLの滅菌水中に0.5gのカルボキシメチルセルロース、0.5gのPluronic、および0.05gの過酸化水素/亜塩素酸ナトリウム混合物を含む、「眼内」コンタクトレンズ洗浄剤を準備した。洗浄剤は、400ppmの亜塩素酸ナトリウムおよび100ppmの過酸化水素、合計500ppmの過酸化水素/亜塩素酸ナトリウム混合物を含んだ。洗浄剤2滴を正常なヒトの両眼の盲嚢に置いた。液滴を滴下した時に、被験者は眼瞼を閉じ、人差し指で内眼角を圧迫し、涙点を塞いで涙が涙管に行かないように止めた。
実験2:人工涙液製品
100mLの滅菌水中に0.15gのヒアルロン酸ナトリウム、0.50gの保護剤、および0.06gの過酸化水素/亜塩素酸ナトリウム混合物を含む、人工涙液製品を準備した。人工涙液製品は、400ppmの亜塩素酸ナトリウムおよび200ppmの過酸化水素、合計600ppmの過酸化水素/亜塩素酸ナトリウム混合物を含んだ。洗浄剤2滴を6人の正常なヒトの眼の盲嚢に置いた。液滴を滴下した時に、被験者は眼瞼を閉じ、人差し指で内眼角を圧迫し、涙点を塞いで涙が涙管に行かないように止めた。
びスーパーオキシドジスムターゼ酵素の存在に起因すると考えられる。液滴が患者の眼に置かれた時、カタラーゼおよび他の酵素が過酸化水素/亜塩素酸ナトリウム製剤の迅速な酵素分解を開始する。それによって、およそ3分の間に処理を行った被験者の涙液中のレベルは、ほとんど検出不能なレベルになる。この実験結果は、どちらかといえば、眼内への滴下時に、過酸化水素/亜塩素酸ナトリウム混合物が、最終産物が水、酸素、塩化ナトリウムである自己分解性保存料のように振る舞うことを示している。
Claims (76)
- 眼科用製品に使用する抗菌保存料であって、前記保存料が約0.005重量%から約0.20重量%の亜塩素酸化合物および約0.005重量%から約0.05重量%の過酸化化合物を含み、前記保存料が二酸化塩素を生成せず、かつ前記保存料がpH約6.0から約8.8の間の範囲である、抗菌保存料。
- 前記亜塩素酸化合物が亜塩素酸金属である、請求項1に記載の保存料。
- 前記金属がナトリウムである、請求項2に記載の保存料。
- 前記金属がカリウム、カルシウム、およびマグネシウムから成る群から選択される、請求項2に記載の保存料。
- 前記過酸化化合物が過酸化水素である、請求項1に記載の保存料。
- 前記眼科用製品が人工涙液溶液である、請求項1に記載の保存料。
- 前記眼科用製品がコンタクトレンズ殺菌液である、請求項1に記載の保存料。
- 前記眼科用製品がコンタクトレンズ洗浄剤液である、請求項1に記載の保存料。
- 前記洗浄剤液が生物の眼に着用されたコンタクトレンズに直接施用される、請求項8に記載の保存料。
- 生物の眼に直接施用される抗菌眼科用配合であって、前記配合が約0.005重量%から約0.20重量%の亜塩素酸化合物および約0.005重量%から約0.05重量%の過酸化化合物を含み、前記配合が二酸化塩素を生成せず、かつ前記配合がpH約6.0から約8.8の間の範囲である、抗菌眼科用配合。
- 前記亜塩素酸化合物が亜塩素酸金属である、請求項10に記載の抗菌眼科用配合。
- 前記金属がナトリウムである、請求項11に記載の抗菌眼科用配合。
- 前記金属がカリウム、カルシウム、およびマグネシウムから成る群から選択される、請求項11に記載の抗菌眼科用配合。
- 前記過酸化化合物が過酸化水素である、請求項10に記載の抗菌眼科用配合。
- 非イオン性ポリマー潤滑剤、アニオン性ポリマー潤滑剤、およびそれらの組合せから成る群から選択される潤滑剤をさらに含む、請求項10に記載の抗菌眼科用配合。
- ブロック重合体ベースの界面活性剤をさらに含む、請求項15に記載の抗菌眼科用配合。
- 前記眼科用配合が、
潤滑剤 0.05重量%〜0.3重量%と;
ホウ酸 0.15重量%〜0.3重量%と;
塩化ナトリウム 0.50重量%〜0.8重量%と;
界面活性剤 0.05重量%〜0.3重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項15に記載の抗菌眼科用配合。 - 約0.001重量%から約0.50重量%のヒアルロン酸ナトリウムをさらに含む、請求項17に記載の抗菌眼科用配合。
- 前記眼科用配合が、
潤滑剤 0.05重量%〜0.30重量%と;
リン酸2水素ナトリウム 0.10重量%〜0.25重量%と;
リン酸水素2ナトリウム 0.10重量%〜0.40重量%と;
塩化ナトリウム 0.50重量%〜0.80重量%と;
界面活性剤 0.05重量%〜0.30重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項15に記載の抗菌眼科用配合。 - 約0.001重量%から約0.50重量%のヒアルロン酸ナトリウムをさらに含む、請求項19に記載の抗菌眼科用配合。
- 前記配合が眼の乾燥を治療するために眼に施用される、請求項10に記載の抗菌眼科用配合。
- 前記配合が眼の感染症を治療するために眼に施用される、請求項10に記載の抗菌眼科用配合。
- 前記感染症が細菌角膜炎によって引き起こされる、請求項22に記載の抗菌眼科用配合。
- 前記感染症がウイルスによって引き起こされる、請求項22に記載の抗菌眼科用配合。
- 前記感染症が糸状菌によって引き起こされる、請求項22に記載の抗菌眼科用配合。
- 前記配合が、眼に装着されたコンタクトレンズを洗浄をするために眼に施用される、請求項10に記載の抗菌眼科用配合。
- 生物の眼の乾燥の治療方法であって、前記方法が、抗菌眼科用配合を眼に施用するステップを含み、前記配合が約0.005重量%から約0.20重量%の亜塩素酸化合物および約0.005重量%から約0.05重量%の過酸化化合物を含み、前記配合が二酸化塩素を生成せず、かつ前記配合がpH約6.0から8.8の間の範囲である方法。
- 前記眼科用配合の前記亜塩素酸化合物が亜塩素酸金属である、請求項27に記載の方法。
- 前記金属がナトリウムである、請求項28に記載の方法。
- 前記金属がカリウム、カルシウム、およびマグネシウムから成る群から選択される、請求項28に記載の方法。
- 前記眼科用配合の前記過酸化化合物が過酸化水素である、請求項27に記載の方法。
- 前記眼科用配合が非イオン性ポリマー潤滑剤、アニオン性ポリマー潤滑剤、およびそれらの組合せから成る群から選択される潤滑剤をさらに含む、請求項27に記載の方法。
- 前記眼科用配合がブロック重合体ベースの界面活性剤をさらに含む、請求項32に記載の方法。
- 前記眼科用配合が、
潤滑剤 0.05重量%〜0.3重量%と;
ホウ酸 0.15重量%〜0.3重量%と;
塩化ナトリウム 0.50重量%〜0.8重量%と;
界面活性剤 0.05重量%〜0.3重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項33に記載の方法。 - 前記眼科用配合が約0.001重量%から約0.50重量%のヒアルロン酸ナトリウムをさらに含む、請求項34に記載の方法。
- 前記眼科用配合が、
潤滑剤 0.05重量%〜0.30重量%と;
リン酸2水素ナトリウム 0.10重量%〜0.25重量%と;
リン酸水素2ナトリウム 0.10重量%〜0.40重量%と;
塩化ナトリウム 0.50重量%〜0.80重量%と;
界面活性剤 0.05重量%〜0.30重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項33に記載の方法。 - 前記眼科用配合が約0.001重量%から約0.50重量%のヒアルロン酸ナトリウムをさらに含む、請求項36に記載の方法。
- 生物の眼に装着されたコンタクトレンズの洗浄方法であって、前記方法が、抗菌眼科用配合をレンズ上に施用するステップを含み、前記配合が約0.005重量%から約0.20重量%の亜塩素酸化合物および約0.005重量%から約0.05重量%の過酸化化合物を含み、前記配合が二酸化塩素を生成せず、かつ前記配合がpH約6.0から8.8の間の範囲である方法。
- 前記眼科用配合の前記亜塩素酸化合物が亜塩素酸金属である、請求項38に記載の方法。
- 前記金属がナトリウムである、請求項39に記載の方法。
- 前記金属がカリウム、カルシウム、およびマグネシウムから成る群から選択される、請求項39に記載の方法。
- 前記眼科用配合の前記過酸化化合物が過酸化水素である、請求項38に記載の方法。
- 前記眼科用配合が非イオン性ポリマー潤滑剤、アニオン性ポリマー潤滑剤、およびそれらの組合せから成る群から選択される潤滑剤をさらに含む、請求項38に記載の方法。
- 前記眼科用配合が、亜塩素酸塩および過酸化水素が酸素の生成に利用可能になる速度を制限する持続的送達成分をさらに含む、請求項38に記載の方法。
- 前記持続的送達成分がポリマーマトリクスである、請求項44に記載の方法。
- 前記持続的送達成分がリポソームである、請求項44に記載の方法。
- 前記持続的送達成分が軟膏である、請求項44に記載の方法。
- 前記持続的送達成分が、セルロースエステル、ヒドロキシメチルプロピルセルロース、メチルヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシエチルセルロース、カルボキシメチルセルロース、セルロースエステルの塩、酢酸セルロース、ヒドロキシプロピルメチルセルロースフタレート、メタクリル酸‐酢酸エチルコポリマー、ポリビニルピロリドン、ポリビニルアルコール、ヒアルロン酸、リン脂質、中性電荷を持つリン脂質、負電荷を持つリン脂質、ジパルミトイルホスファチジルコリン、ジパルミトイルホスファチジルセリン、およびそれらのナトリウム塩から成る群から選択される、請求項44に記載の方法。
- 前記持続的送達成分が、製剤の1重量パーセントから20重量パーセントを構成する、請求項44に記載の方法。
- 前記眼科用配合が、
亜塩素酸ナトリウム 0.005重量%〜0.200重量%と;
過酸化水素 0.005重量%〜0.050重量%と;
HPMC 0.05重量%〜0.20重量%と;
リン酸2水素ナトリウム一水和物 0.01重量%〜0.30重量%と;
HClまたはNaOH pH7.4に調整
精製水 所定体積まで十分量
とをさらに含む、請求項47に記載の方法。 - 前記眼科用配合がブロック重合体ベースの界面活性剤をさらに含む、請求項38に記載の方法。
- 前記眼科用配合が
潤滑剤 0.05重量%〜0.30重量%と;
ホウ酸 0.15重量%〜0.30重量%と;
塩化ナトリウム 0.50重量%〜0.80重量%と;
界面活性剤 0.05重量%〜0.30重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項51に記載の方法。 - 前記眼科用配合が約0.001重量%から約0.50重量%のヒアルロン酸ナトリウムをさらに含む、請求項52に記載の方法。
- 前記眼科用配合が、
潤滑剤 0.05重量%〜0.30重量%と;
リン酸2水素ナトリウム 0.10重量%〜0.25重量%と;
リン酸水素2ナトリウム 0.10重量%〜0.40重量%と;
塩化ナトリウム 0.50重量%〜0.80重量%と;
界面活性剤 0.05重量%〜0.30重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項51に記載の方法。 - 前記眼科用配合が約0.001重量%から約0.50重量%のヒアルロン酸ナトリウムをさらに含む、請求項54に記載の方法。
- 皮膚科用製品に使用する抗菌保存料であって、前記保存料が約0.005重量%から約0.20重量%の亜塩素酸化合物および約0.005重量%から約0.05重量%の過酸化化合物を含み、前記保存料が二酸化塩素を生成せず、かつ前記保存料がpH約5.0から約8.8の間の範囲である、抗菌保存料。
- 前記亜塩素酸化合物が亜塩素酸金属である、請求項56に記載の保存料。
- 前記金属がナトリウムである、請求項57に記載の保存料。
- 前記金属がカリウム、カルシウム、およびマグネシウムから成る群から選択される、請求項57に記載の保存料。
- 前記過酸化化合物が過酸化水素である、請求項56に記載の保存料。
- 前記皮膚科用製品が褥瘡ゲルまたはクリームである、請求項56に記載の保存料。
- 皮膚症状の治療方法であって、前記方法が、抗菌皮膚科用配合を皮膚患部に施用するステップを含み、前記配合が約0.005重量%から約0.20重量%の亜塩素酸化合物および約0.005重量%から約0.05重量%の過酸化化合物を含み、前記配合が二酸化塩素を生成せず、かつ前記配合がpH約5.0から約8.8の間の範囲である方法。
- 前記皮膚科用配合の前記亜塩素酸化合物が亜塩素酸金属である、請求項62に記載の方法。
- 前記金属がナトリウムである、請求項63に記載の方法。
- 前記金属がカリウム、カルシウム、およびマグネシウムから成る群から選択される、請求項63に記載の方法。
- 前記皮膚科用配合の前記過酸化化合物が過酸化水素である、請求項62に記載の方法。
- 前記皮膚科用配合が褥瘡ゲルまたはクリームである、請求項62に記載の方法。
- 前記皮膚科用配合が
潤滑剤 0.05重量%〜0.30重量%と;
ホウ酸 0.15重量%〜0.30重量%と;
塩化ナトリウム 0.50重量%〜0.80重量%と;
界面活性剤 0.05重量%〜0.30重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項67に記載の方法。 - 前記皮膚科用配合が、
潤滑剤 0.05重量%〜0.30重量%と;
リン酸2水素ナトリウム 0.10重量%〜0.25重量%と;
リン酸水素2ナトリウム 0.10重量%〜0.40重量%と;
塩化ナトリウム 0.50重量%〜0.80重量%と;
界面活性剤 0.05重量%〜0.30重量%と;
HClまたはNaOH pH調整用と;
精製水 所定体積まで十分量
とをさらに含む、請求項67に記載の方法。 - 前記皮膚科用配合が、亜塩素酸塩および過酸化水素が酸素の生成に利用可能になる速度を制限する持続的送達成分をさらに含む、請求項62に記載の方法。
- 前記持続的送達成分がポリマーマトリクスを含む、請求項70に記載の方法。
- 前記持続的送達成分がリポソームを含む、請求項70に記載の方法。
- 前記持続的送達成分が軟膏を含む、請求項70に記載の方法。
- 前記持続的送達成分が、セルロースエステル、ヒドロキシメチルプロピルセルロース、メチルヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシエチルセルロース、カルボキシメチルセルロース、セルロースエステルの塩、酢酸セルロース、ヒドロキシプロピルメチルセルロースフタレート、メタクリル酸‐酢酸エチルコポリマー、ポリビニルピロリドン、ポリビニルアルコール、ヒアルロン酸、リン脂質、中性電荷を持つリン脂質、負電荷を持つリン脂質、ジパルミトイルホスファチジルコリン、ジパルミトイルホスファチジルセリン、およびそれらのナトリウム塩から成る群から選択される、請求項70に記載の方法。
- 前記持続的送達成分が、製剤の1重量パーセントから20重量パーセントを構成する、請求項70に記載の方法
- 前記眼科用配合が、
亜塩素酸ナトリウム 0.005重量%〜0.200重量%と;
過酸化水素 0.005重量%〜0.050重量%と;
HPMC 0.05重量%〜0.20重量%と;
リン酸2水素ナトリウム一水和物 0.01重量%〜0.30重量%と;
HClまたはNaOH pH7.4に調整
精製水 所定体積まで十分量
とをさらに含む、請求項73に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/633,355 US20070104798A1 (en) | 1999-10-04 | 2006-12-04 | Synergistic antimicrobial preparations containing chlorite and hydrogen peroxide |
| PCT/US2007/024815 WO2008070063A1 (en) | 2006-12-04 | 2007-12-04 | Synergistic antimicrobial preparations containing chlorite and hydrogen peroxide |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010511707A true JP2010511707A (ja) | 2010-04-15 |
| JP2010511707A5 JP2010511707A5 (ja) | 2011-01-27 |
Family
ID=39492544
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009540253A Pending JP2010511707A (ja) | 2006-12-04 | 2007-12-04 | 亜塩素酸塩および過酸化水素を含む相乗的抗菌製剤 |
Country Status (8)
| Country | Link |
|---|---|
| US (8) | US20070104798A1 (ja) |
| EP (2) | EP2099296B1 (ja) |
| JP (1) | JP2010511707A (ja) |
| CN (1) | CN101600348A (ja) |
| ES (1) | ES2551120T3 (ja) |
| HK (1) | HK1222131A1 (ja) |
| MX (1) | MX2009005836A (ja) |
| WO (1) | WO2008070063A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016526036A (ja) * | 2013-05-20 | 2016-09-01 | 本部三慶株式会社 | 亜塩素酸水含有ウイルス殺傷剤 |
| JP2018052994A (ja) * | 2018-01-15 | 2018-04-05 | 保土谷化学工業株式会社 | 殺菌組成物 |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070104798A1 (en) | 1999-10-04 | 2007-05-10 | S.K. Pharmaceuticals, Inc. | Synergistic antimicrobial preparations containing chlorite and hydrogen peroxide |
| US20090004288A1 (en) * | 2007-06-29 | 2009-01-01 | Collins Gary L | Stabilized ophthalmic solutions |
| US20090220618A1 (en) * | 2008-02-29 | 2009-09-03 | Erning Xia | Pharmaceutical formulations comprising polyanionic materials and source of hydrogen peroxide |
| US20090239775A1 (en) * | 2008-03-19 | 2009-09-24 | Collins Gary L | Ophthalmic solutions displaying improved efficacy |
| WO2010064636A1 (ja) * | 2008-12-02 | 2010-06-10 | ロート製薬株式会社 | 眼科用組成物 |
| US20100226999A1 (en) * | 2009-03-06 | 2010-09-09 | Tracy Quevillon-Coleman | Process for forming stabilized ophthalmic solutions |
| TW201127423A (en) | 2009-12-17 | 2011-08-16 | Alcon Res Ltd | Ophthalmic solutions with improved disinfection profiles |
| CN101785786B (zh) * | 2010-02-20 | 2012-09-05 | 北京欧凯纳斯科技有限公司 | 一种用于治疗脚气的二氧化氯软膏 |
| US9675065B2 (en) | 2011-02-14 | 2017-06-13 | Truox, Inc. | Biocide and bleach compositions and related methods |
| BR112014015333A2 (pt) * | 2011-12-22 | 2017-06-13 | Nuvo Res Gmbh | composições lipossomais de clorito ou clorato |
| US9433643B2 (en) | 2013-04-30 | 2016-09-06 | Truox, Inc. | Microbicidal composition comprising hydrogen peroxide and aminocarboxylic acids |
| US10131574B2 (en) | 2013-06-17 | 2018-11-20 | Corning Incorporated | Antimicrobial glass articles and methods of making and using same |
| GB2534049B (en) * | 2013-10-03 | 2020-05-06 | Halliburton Energy Services Inc | Solvent extraction and analysis of formation fluids from formation solids at a well site |
| CN106773120A (zh) * | 2015-11-25 | 2017-05-31 | 鸿富锦精密工业(深圳)有限公司 | 隐形眼镜镜片材料及隐形眼镜镜片 |
| CN108552216B (zh) * | 2018-01-25 | 2021-05-25 | 湖北荷普药业股份有限公司 | 一种杀孢子剂及其制备方法与应用 |
| CA3099166A1 (en) * | 2018-05-02 | 2019-11-07 | Ocusoft, Inc. | Hypochlorous acid-based eyelid cleansers |
| WO2020069079A1 (en) * | 2018-09-27 | 2020-04-02 | Medivators Inc. | Peracetic acid stabilized compositions with stable lining |
| WO2020069078A1 (en) * | 2018-09-27 | 2020-04-02 | Medivators Inc. | Peracetic acid stabilized compositions with polymeric resins chelators |
| CN109846847B (zh) * | 2019-04-04 | 2021-08-10 | 石家庄卫科生物科技有限公司 | 一种用于治疗动物皮肤病的泡腾片及其制备方法 |
| EP3958915A4 (en) * | 2019-04-22 | 2023-01-11 | Allegro Ophthalmics, LLC | COMPOSITIONS AND METHODS USABLE FOR THE TREATMENT OF DRY EYE |
| WO2021214536A1 (en) * | 2020-04-21 | 2021-10-28 | Lifeactivus Private Limited | Pharmaceutical composition of chlorine for treatment of respiratory viral infection |
| CN111602655A (zh) * | 2020-05-09 | 2020-09-01 | 武汉中科先进技术研究院有限公司 | 抗病毒双壳微胶囊及其制备方法和具有该抗病毒双壳微胶囊的消毒涂料及其制备方法和应用 |
| CN113491711A (zh) * | 2021-06-09 | 2021-10-12 | 广州丰歌生物科技有限责任公司 | 一种抗菌氧溶液及其制备方法和应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003522109A (ja) * | 1998-10-08 | 2003-07-22 | エル. キャラグーチアン、ハンパー | 亜塩素酸塩と過酸化水素とを含有する共同作用抗菌性皮膚科・眼科製剤 |
| JP2004536137A (ja) * | 2001-07-23 | 2004-12-02 | エル. キャラグーチアン、ハンパー | 亜塩素酸塩および過酸化水素を含有する相乗的抗菌性眼科用および皮膚科用製剤 |
| WO2005007174A2 (en) * | 2003-07-07 | 2005-01-27 | Karagoezian Hampar J | Synergistic antimicrobial ophthalmic combination |
Family Cites Families (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2701781A (en) * | 1949-12-30 | 1955-02-08 | Charles Van Buren | Aqueous chlorine dioxide antiseptic compositions and production thereof |
| US3271242A (en) * | 1963-03-29 | 1966-09-06 | Alexander R Reed Iii | Stable chlorine dioxide composition and method of making same |
| US3585147A (en) * | 1969-10-01 | 1971-06-15 | Int Dioxcide Inc | Stabilized chlorine dioxide solutions containing a chloride and processes of making and using same |
| US3920810A (en) * | 1974-04-23 | 1975-11-18 | Burton Parsons And Company Inc | Polyacrylamide containing ophthalmic solutions |
| US4084747A (en) | 1976-03-26 | 1978-04-18 | Howard Alliger | Germ killing composition and method |
| USRE31779E (en) * | 1976-03-26 | 1984-12-25 | Alcide Corporation | Germ-killing composition and method |
| US4250269A (en) * | 1979-11-26 | 1981-02-10 | Buckman Laboratories, Inc. | Water-soluble mixtures of quaternary ammonium polymers, nonionic and/or cationic vinyl-addition polymers, and nonionic and/or cationic surfactants |
| US4317814A (en) * | 1980-06-12 | 1982-03-02 | Felipe Laso | Preparation and method for treating burns |
| US4499077A (en) * | 1981-02-03 | 1985-02-12 | Stockel Richard F | Anti-microbial compositions and associated methods for preparing the same and for the disinfecting of various objects |
| US4670185A (en) * | 1982-07-19 | 1987-06-02 | Lion Corporation | Aqueous vesicle dispersion having surface charge |
| US4574084A (en) * | 1983-02-25 | 1986-03-04 | Peter Berger | Process for the preparation of a modified aqueous chlorite solution, the solution prepared by this process and the use thereof |
| US4654208A (en) * | 1983-03-01 | 1987-03-31 | Stockel Richard F | Anti-microbial compositions comprising an aqueous solution of a germicidal polymeric nitrogen compound and a potentiating oxidizing agent |
| US4574804A (en) * | 1984-02-27 | 1986-03-11 | Board Of Regents, The University Of Texas System | Optic nerve clamp |
| US4585482A (en) * | 1984-05-25 | 1986-04-29 | Southern Research Institute | Long-acting biocidal compositions and method therefor |
| US4855135A (en) * | 1984-07-30 | 1989-08-08 | Ratcliff Perry A | Method for debriding |
| US4978535A (en) * | 1984-07-30 | 1990-12-18 | Ratcliff Perry A | Method for cleaning contact lenses |
| CA1224415A (en) * | 1984-08-23 | 1987-07-21 | Peter Berger | Process for the preparation of a modified aqueous chlorite solution, the solution prepared by this process and the use thereof |
| US4956348A (en) * | 1986-02-19 | 1990-09-11 | Eye Research Institute Of Retina Foundation | Stimulation of tear secretion with cyclic nucleotides |
| US4756844A (en) * | 1986-12-29 | 1988-07-12 | The Dow Chemical Company | Controlled-release composition having a membrane comprising submicron particles |
| US4891216A (en) * | 1987-04-14 | 1990-01-02 | Alcide Corporation | Disinfecting compositions and methods therefor |
| US4963287A (en) | 1987-05-26 | 1990-10-16 | The Drackett Company | Aqueous alkali metal halogenite compositions |
| US4956184A (en) * | 1988-05-06 | 1990-09-11 | Alcide Corporation | Topical treatment of genital herpes lesions |
| US5607698A (en) * | 1988-08-04 | 1997-03-04 | Ciba-Geigy Corporation | Method of preserving ophthalmic solution and compositions therefor |
| US4880638A (en) * | 1988-08-23 | 1989-11-14 | Bioxy International, Ltd. | Biocidal composition and method for disinfecting articles |
| FR2637533B1 (fr) | 1988-10-10 | 1990-12-07 | Solvay | Procede pour realiser, par extrusion soufflee, une gaine en resine a base de chlorure de vinyle dont au moins une face presente un aspect mat |
| US5078908A (en) * | 1989-10-02 | 1992-01-07 | Allergan, Inc. | Methods for generating chlorine dioxide and compositions for disinfecting |
| US4997626A (en) * | 1990-01-05 | 1991-03-05 | Allergan, Inc. | Methods to disinfect contact lenses |
| US5279673A (en) * | 1990-01-05 | 1994-01-18 | Allergan, Inc. | Methods to disinfect contact lenses |
| US5246662A (en) * | 1989-10-02 | 1993-09-21 | Allergan, Inc. | Methods for generating chlorine dioxide and compositions for disinfecting |
| US5152912A (en) * | 1990-01-05 | 1992-10-06 | Allergan, Inc. | Chlorine dioxide precursor containing compositions useful in disinfecting contact lenses |
| US5009895A (en) * | 1990-02-02 | 1991-04-23 | Merck & Co., Inc. | Sustained release with high and low viscosity HPMC |
| US5225055A (en) * | 1990-02-09 | 1993-07-06 | Abbott Laboratories | Method of cleaning and disinfecting contact lenses |
| US5145644A (en) * | 1990-12-20 | 1992-09-08 | Allergan, Inc. | Hydrogen peroxide destroying compositions and methods of making and using same |
| US5281353A (en) * | 1991-04-24 | 1994-01-25 | Allergan, Inc. | Compositions and methods for disinfecting/cleaning of lenses and for destroying oxidative disinfectants |
| US5270002A (en) * | 1991-10-03 | 1993-12-14 | Allergan, Inc. | Apparatus and method useful in disinfecting contact lenses |
| EP0591956B1 (en) * | 1992-10-08 | 1998-08-26 | Tomei Sangyo Kabushiki Kaisha | Method for cleaning, preserving and disinfecting contact lenses |
| EP0674532B1 (en) * | 1992-12-17 | 2003-05-28 | Advanced Medical Optics, Inc. | Contact lens disinfecting solution containing an oxidizing agent and polyvinyl pyrrolidone |
| US5472703A (en) * | 1993-03-02 | 1995-12-05 | Johnson & Johnson Vision Products, Inc. | Ophthalmic lens with anti-toxin agent |
| US5736165A (en) * | 1993-05-25 | 1998-04-07 | Allergan | In-the-eye use of chlorine dioxide-containing compositions |
| CA2125060C (en) | 1993-07-02 | 1999-03-30 | Henry P. Dabrowski | Ophthalmic solution for artificial tears |
| US5616568A (en) * | 1993-11-30 | 1997-04-01 | The Research Foundation Of State University Of New York | Functionalized derivatives of hyaluronic acid |
| US5639481A (en) * | 1994-10-17 | 1997-06-17 | Symbollon Corporation | Method for the therapeutic treatment of a mammalian eye using an admixed composition containing free molecular iodine |
| US5855922A (en) * | 1995-12-07 | 1999-01-05 | Bio-Cide International, Inc. | Antiseptic composition and process for prophylaxis and therapeutic treatment of dermal disorders |
| US6096328A (en) * | 1997-06-06 | 2000-08-01 | The Procter & Gamble Company | Delivery system for an oral care substance using a strip of material having low flexural stiffness |
| US6033704A (en) * | 1998-08-14 | 2000-03-07 | Charvid Limited Liability Co. | Method and apparatus for preserving fruits and vegetables |
| DE69923987T2 (de) * | 1998-10-08 | 2006-11-02 | Karagoezian, Hampar L., San Juan Capistrano | Synergistische antimikrobielle, dermatologische und ophtahalmologische zubereitung, die ein chlorit und wasserstoffperoxid enthalten |
| US20070104798A1 (en) | 1999-10-04 | 2007-05-10 | S.K. Pharmaceuticals, Inc. | Synergistic antimicrobial preparations containing chlorite and hydrogen peroxide |
| CA2565944C (en) | 2004-05-07 | 2011-07-19 | S.K. Pharmaceuticals, Inc. | Stabilized hyaluronan preparations and related methods |
-
2006
- 2006-12-04 US US11/633,355 patent/US20070104798A1/en not_active Abandoned
-
2007
- 2007-12-04 CN CNA2007800489270A patent/CN101600348A/zh active Pending
- 2007-12-04 JP JP2009540253A patent/JP2010511707A/ja active Pending
- 2007-12-04 MX MX2009005836A patent/MX2009005836A/es active IP Right Grant
- 2007-12-04 ES ES07862490.5T patent/ES2551120T3/es active Active
- 2007-12-04 EP EP07862490.5A patent/EP2099296B1/en not_active Revoked
- 2007-12-04 EP EP15186300.8A patent/EP2990044A1/en active Pending
- 2007-12-04 WO PCT/US2007/024815 patent/WO2008070063A1/en active Application Filing
-
2010
- 2010-09-02 US US12/874,443 patent/US8460701B2/en not_active Expired - Lifetime
- 2010-09-10 US US12/879,989 patent/US20110008420A1/en not_active Abandoned
-
2012
- 2012-10-23 US US13/658,609 patent/US20130195995A1/en not_active Abandoned
-
2013
- 2013-12-31 US US14/145,126 patent/US8784901B2/en not_active Expired - Fee Related
-
2014
- 2014-06-18 US US14/307,706 patent/US9072712B2/en not_active Expired - Fee Related
-
2015
- 2015-05-21 US US14/718,852 patent/US9622480B2/en not_active Expired - Lifetime
-
2016
- 2016-09-01 HK HK16110425.6A patent/HK1222131A1/zh unknown
-
2017
- 2017-03-09 US US15/454,859 patent/US10010081B2/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003522109A (ja) * | 1998-10-08 | 2003-07-22 | エル. キャラグーチアン、ハンパー | 亜塩素酸塩と過酸化水素とを含有する共同作用抗菌性皮膚科・眼科製剤 |
| JP2004536137A (ja) * | 2001-07-23 | 2004-12-02 | エル. キャラグーチアン、ハンパー | 亜塩素酸塩および過酸化水素を含有する相乗的抗菌性眼科用および皮膚科用製剤 |
| WO2005007174A2 (en) * | 2003-07-07 | 2005-01-27 | Karagoezian Hampar J | Synergistic antimicrobial ophthalmic combination |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016526036A (ja) * | 2013-05-20 | 2016-09-01 | 本部三慶株式会社 | 亜塩素酸水含有ウイルス殺傷剤 |
| JP2018052994A (ja) * | 2018-01-15 | 2018-04-05 | 保土谷化学工業株式会社 | 殺菌組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| US8460701B2 (en) | 2013-06-11 |
| WO2008070063A1 (en) | 2008-06-12 |
| EP2099296B1 (en) | 2015-10-21 |
| US9072712B2 (en) | 2015-07-07 |
| HK1222131A1 (zh) | 2017-06-23 |
| US20070104798A1 (en) | 2007-05-10 |
| US20150264936A1 (en) | 2015-09-24 |
| US20110008420A1 (en) | 2011-01-13 |
| EP2990044A1 (en) | 2016-03-02 |
| EP2099296A1 (en) | 2009-09-16 |
| US20140322350A1 (en) | 2014-10-30 |
| US9622480B2 (en) | 2017-04-18 |
| CN101600348A (zh) | 2009-12-09 |
| US20130195995A1 (en) | 2013-08-01 |
| US10010081B2 (en) | 2018-07-03 |
| ES2551120T3 (es) | 2015-11-16 |
| US20140127319A1 (en) | 2014-05-08 |
| MX2009005836A (es) | 2009-10-08 |
| EP2099296A4 (en) | 2009-12-23 |
| US20170172150A1 (en) | 2017-06-22 |
| US8784901B2 (en) | 2014-07-22 |
| US20110014276A1 (en) | 2011-01-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10010081B2 (en) | Synergistic antimicrobial preparations containing chlorite and hydrogen peroxide | |
| JP5002114B2 (ja) | 亜塩素酸塩および過酸化水素を含有する相乗的抗菌性眼科用および皮膚科用製剤 | |
| US7648716B2 (en) | Synergistic antimicrobial ophthalmic and dermatologic preparations containing chlorite and hydrogen peroxide | |
| EP1119347B1 (en) | Synergistic antimicrobial, dermatological and ophthalmic preparations containing chlorite and hydrogen peroxide | |
| US20070264226A1 (en) | Synergistically enhanced disinfecting solutions | |
| MXPA06000228A (es) | Antibioticos de oxazolidinona sustituidos con un grupo ciclopropilo y derivados de los mismos. | |
| JP4727816B2 (ja) | 亜塩素酸塩と過酸化水素とを含有する共同作用抗菌性皮膚科・眼科製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101206 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101206 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20120127 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20121107 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121113 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130212 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130308 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130402 |