JP2010019864A - 神経変性の分別診断 - Google Patents
神経変性の分別診断 Download PDFInfo
- Publication number
- JP2010019864A JP2010019864A JP2009247559A JP2009247559A JP2010019864A JP 2010019864 A JP2010019864 A JP 2010019864A JP 2009247559 A JP2009247559 A JP 2009247559A JP 2009247559 A JP2009247559 A JP 2009247559A JP 2010019864 A JP2010019864 A JP 2010019864A
- Authority
- JP
- Japan
- Prior art keywords
- tau
- amyloid
- disease
- antibody
- neurological
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 230000004770 neurodegeneration Effects 0.000 title abstract description 51
- 238000003748 differential diagnosis Methods 0.000 title abstract description 38
- 230000000926 neurological effect Effects 0.000 claims abstract description 121
- 238000000034 method Methods 0.000 claims abstract description 104
- 239000003550 marker Substances 0.000 claims abstract description 87
- 238000011895 specific detection Methods 0.000 claims abstract description 62
- 238000011002 quantification Methods 0.000 claims abstract description 45
- 210000001124 body fluid Anatomy 0.000 claims abstract description 40
- 239000010839 body fluid Substances 0.000 claims abstract description 36
- 238000012360 testing method Methods 0.000 claims abstract description 18
- 210000001175 cerebrospinal fluid Anatomy 0.000 claims description 157
- 102000013498 tau Proteins Human genes 0.000 claims description 146
- 108010026424 tau Proteins Proteins 0.000 claims description 146
- 208000024827 Alzheimer disease Diseases 0.000 claims description 108
- 102000013455 Amyloid beta-Peptides Human genes 0.000 claims description 101
- 108010090849 Amyloid beta-Peptides Proteins 0.000 claims description 101
- 101150004420 RAB3A gene Proteins 0.000 claims description 91
- 108010057722 Synaptosomal-Associated Protein 25 Proteins 0.000 claims description 83
- 102000004183 Synaptosomal-Associated Protein 25 Human genes 0.000 claims description 83
- 108090000623 proteins and genes Proteins 0.000 claims description 72
- 102000004169 proteins and genes Human genes 0.000 claims description 71
- 238000001514 detection method Methods 0.000 claims description 44
- 230000000946 synaptic effect Effects 0.000 claims description 44
- 238000011282 treatment Methods 0.000 claims description 35
- 206010012289 Dementia Diseases 0.000 claims description 33
- 238000009007 Diagnostic Kit Methods 0.000 claims description 29
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 25
- 238000003745 diagnosis Methods 0.000 claims description 20
- 239000000872 buffer Substances 0.000 claims description 16
- -1 or -tau Proteins 0.000 claims description 15
- 230000008105 immune reaction Effects 0.000 claims description 9
- 230000008878 coupling Effects 0.000 claims description 8
- 238000010168 coupling process Methods 0.000 claims description 8
- 238000005859 coupling reaction Methods 0.000 claims description 8
- 238000012544 monitoring process Methods 0.000 claims description 7
- 238000010606 normalization Methods 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 2
- 238000003556 assay Methods 0.000 abstract description 25
- 239000013068 control sample Substances 0.000 abstract description 3
- 102000003802 alpha-Synuclein Human genes 0.000 description 74
- 108090000185 alpha-Synuclein Proteins 0.000 description 74
- 235000018102 proteins Nutrition 0.000 description 60
- 102100023206 Neuromodulin Human genes 0.000 description 50
- 101710144282 Neuromodulin Proteins 0.000 description 50
- 239000000523 sample Substances 0.000 description 50
- 108010022181 Phosphopyruvate Hydratase Proteins 0.000 description 36
- 102000012288 Phosphopyruvate Hydratase Human genes 0.000 description 36
- 238000002512 chemotherapy Methods 0.000 description 33
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 28
- 230000001900 immune effect Effects 0.000 description 28
- 208000018737 Parkinson disease Diseases 0.000 description 25
- 208000009829 Lewy Body Disease Diseases 0.000 description 24
- 201000002832 Lewy body dementia Diseases 0.000 description 24
- 210000004556 brain Anatomy 0.000 description 23
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 23
- 201000010099 disease Diseases 0.000 description 22
- 238000009593 lumbar puncture Methods 0.000 description 21
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 20
- 230000026683 transduction Effects 0.000 description 18
- 238000010361 transduction Methods 0.000 description 18
- 201000011240 Frontotemporal dementia Diseases 0.000 description 15
- 238000011160 research Methods 0.000 description 15
- 210000003719 b-lymphocyte Anatomy 0.000 description 14
- 208000028564 B-cell non-Hodgkin lymphoma Diseases 0.000 description 13
- 208000012902 Nervous system disease Diseases 0.000 description 13
- 238000004458 analytical method Methods 0.000 description 13
- 238000003118 sandwich ELISA Methods 0.000 description 13
- 210000003169 central nervous system Anatomy 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 12
- 208000011580 syndromic disease Diseases 0.000 description 12
- 241000588724 Escherichia coli Species 0.000 description 11
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 11
- FEWOUVRMGWFWIH-ILZZQXMPSA-N amyloid-beta polypeptide 40 Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(O)=O)[C@@H](C)CC)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 FEWOUVRMGWFWIH-ILZZQXMPSA-N 0.000 description 11
- 239000000427 antigen Substances 0.000 description 11
- 102000036639 antigens Human genes 0.000 description 11
- 108091007433 antigens Proteins 0.000 description 11
- 230000006870 function Effects 0.000 description 11
- 230000005855 radiation Effects 0.000 description 11
- 210000002966 serum Anatomy 0.000 description 11
- 208000024891 symptom Diseases 0.000 description 11
- 201000004810 Vascular dementia Diseases 0.000 description 10
- 150000001413 amino acids Chemical class 0.000 description 10
- 230000000626 neurodegenerative effect Effects 0.000 description 10
- 102000004196 processed proteins & peptides Human genes 0.000 description 10
- 208000000172 Medulloblastoma Diseases 0.000 description 9
- 235000001014 amino acid Nutrition 0.000 description 9
- 238000011156 evaluation Methods 0.000 description 9
- 201000010374 Down Syndrome Diseases 0.000 description 8
- 206010058314 Dysplasia Diseases 0.000 description 8
- 208000017604 Hodgkin disease Diseases 0.000 description 8
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 8
- 206010021143 Hypoxia Diseases 0.000 description 8
- 206010028980 Neoplasm Diseases 0.000 description 8
- 208000025966 Neurological disease Diseases 0.000 description 8
- 241000283973 Oryctolagus cuniculus Species 0.000 description 8
- 238000004587 chromatography analysis Methods 0.000 description 8
- 229940079593 drug Drugs 0.000 description 8
- 239000003814 drug Substances 0.000 description 8
- 230000014509 gene expression Effects 0.000 description 8
- 238000003018 immunoassay Methods 0.000 description 8
- 206010027175 memory impairment Diseases 0.000 description 8
- 230000035772 mutation Effects 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 8
- 208000019553 vascular disease Diseases 0.000 description 8
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 7
- 208000006332 Choriocarcinoma Diseases 0.000 description 7
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 7
- 208000000527 Germinoma Diseases 0.000 description 7
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 7
- 150000001875 compounds Chemical class 0.000 description 7
- 230000004069 differentiation Effects 0.000 description 7
- 239000000499 gel Substances 0.000 description 7
- 201000003115 germ cell cancer Diseases 0.000 description 7
- 208000014752 hemophagocytic syndrome Diseases 0.000 description 7
- 210000000265 leukocyte Anatomy 0.000 description 7
- 210000000278 spinal cord Anatomy 0.000 description 7
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 102000019355 Synuclein Human genes 0.000 description 6
- 108050006783 Synuclein Proteins 0.000 description 6
- 201000000053 blastoma Diseases 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 208000029028 brain injury Diseases 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 201000008184 embryoma Diseases 0.000 description 6
- 102000004963 gamma-Synuclein Human genes 0.000 description 6
- 108090001121 gamma-Synuclein Proteins 0.000 description 6
- 208000032839 leukemia Diseases 0.000 description 6
- 208000016344 lissencephaly with cerebellar hypoplasia Diseases 0.000 description 6
- 230000007774 longterm Effects 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 230000003287 optical effect Effects 0.000 description 6
- 102000013415 peroxidase activity proteins Human genes 0.000 description 6
- 108040007629 peroxidase activity proteins Proteins 0.000 description 6
- 210000001525 retina Anatomy 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- 230000007470 synaptic degeneration Effects 0.000 description 6
- 206010028923 Neonatal asphyxia Diseases 0.000 description 5
- 208000037212 Neonatal hypoxic and ischemic brain injury Diseases 0.000 description 5
- 201000011510 cancer Diseases 0.000 description 5
- 230000034994 death Effects 0.000 description 5
- 230000003247 decreasing effect Effects 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 238000011534 incubation Methods 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 210000004558 lewy body Anatomy 0.000 description 5
- 201000006417 multiple sclerosis Diseases 0.000 description 5
- 210000005044 neurofilament Anatomy 0.000 description 5
- 210000002569 neuron Anatomy 0.000 description 5
- 208000033300 perinatal asphyxia Diseases 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000035945 sensitivity Effects 0.000 description 5
- 102000004899 14-3-3 Proteins Human genes 0.000 description 4
- 208000003174 Brain Neoplasms Diseases 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- 102000001708 Protein Isoforms Human genes 0.000 description 4
- 108010029485 Protein Isoforms Proteins 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 210000005013 brain tissue Anatomy 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 238000002405 diagnostic procedure Methods 0.000 description 4
- 230000004064 dysfunction Effects 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- 230000009251 neurologic dysfunction Effects 0.000 description 4
- 208000015015 neurological dysfunction Diseases 0.000 description 4
- 102000003137 synaptotagmin Human genes 0.000 description 4
- 108060008004 synaptotagmin Proteins 0.000 description 4
- 230000002792 vascular Effects 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- 238000001262 western blot Methods 0.000 description 4
- 241000283707 Capra Species 0.000 description 3
- 101800005309 Carboxy-terminal peptide Proteins 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 101000891579 Homo sapiens Microtubule-associated protein tau Proteins 0.000 description 3
- 101710115937 Microtubule-associated protein tau Proteins 0.000 description 3
- 102100040243 Microtubule-associated protein tau Human genes 0.000 description 3
- 208000028389 Nerve injury Diseases 0.000 description 3
- 208000028017 Psychotic disease Diseases 0.000 description 3
- 108010010469 Qa-SNARE Proteins Proteins 0.000 description 3
- 108010005730 R-SNARE Proteins Proteins 0.000 description 3
- 108010090804 Streptavidin Proteins 0.000 description 3
- 208000006011 Stroke Diseases 0.000 description 3
- 102000002215 Synaptobrevin Human genes 0.000 description 3
- 102000050389 Syntaxin Human genes 0.000 description 3
- 210000001744 T-lymphocyte Anatomy 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- 206010044688 Trisomy 21 Diseases 0.000 description 3
- 239000002246 antineoplastic agent Substances 0.000 description 3
- 102000003799 beta-Synuclein Human genes 0.000 description 3
- 108090000182 beta-Synuclein Proteins 0.000 description 3
- 230000006931 brain damage Effects 0.000 description 3
- 231100000874 brain damage Toxicity 0.000 description 3
- 210000004899 c-terminal region Anatomy 0.000 description 3
- 238000003759 clinical diagnosis Methods 0.000 description 3
- 239000002299 complementary DNA Substances 0.000 description 3
- 229940127089 cytotoxic agent Drugs 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 238000005194 fractionation Methods 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- 102000057063 human MAPT Human genes 0.000 description 3
- 210000004408 hybridoma Anatomy 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 208000015181 infectious disease Diseases 0.000 description 3
- 230000009545 invasion Effects 0.000 description 3
- 230000002503 metabolic effect Effects 0.000 description 3
- 230000008764 nerve damage Effects 0.000 description 3
- 230000001537 neural effect Effects 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 239000013612 plasmid Substances 0.000 description 3
- 238000001959 radiotherapy Methods 0.000 description 3
- 239000012723 sample buffer Substances 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 3
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- 102000009027 Albumins Human genes 0.000 description 2
- 108010088751 Albumins Proteins 0.000 description 2
- 206010073478 Anaplastic large-cell lymphoma Diseases 0.000 description 2
- 240000003291 Armoracia rusticana Species 0.000 description 2
- 235000011330 Armoracia rusticana Nutrition 0.000 description 2
- 206010003497 Asphyxia Diseases 0.000 description 2
- 208000035473 Communicable disease Diseases 0.000 description 2
- 102100031675 DnaJ homolog subfamily C member 5 Human genes 0.000 description 2
- 208000035366 Familial hemophagocytic lymphohistiocytosis Diseases 0.000 description 2
- 102000053171 Glial Fibrillary Acidic Human genes 0.000 description 2
- 101710193519 Glial fibrillary acidic protein Proteins 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 208000032004 Large-Cell Anaplastic Lymphoma Diseases 0.000 description 2
- 102000029749 Microtubule Human genes 0.000 description 2
- 108091022875 Microtubule Proteins 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- 108010088373 Neurofilament Proteins Proteins 0.000 description 2
- 102000008763 Neurofilament Proteins Human genes 0.000 description 2
- 206010060860 Neurological symptom Diseases 0.000 description 2
- 206010029350 Neurotoxicity Diseases 0.000 description 2
- 239000000020 Nitrocellulose Substances 0.000 description 2
- 208000037273 Pathologic Processes Diseases 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 102000011070 Rab3 Human genes 0.000 description 2
- 108050001276 Rab3 Proteins 0.000 description 2
- 201000000582 Retinoblastoma Diseases 0.000 description 2
- 229920002684 Sepharose Polymers 0.000 description 2
- 102000001435 Synapsin Human genes 0.000 description 2
- 108050009621 Synapsin Proteins 0.000 description 2
- 206010044221 Toxic encephalopathy Diseases 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 210000003050 axon Anatomy 0.000 description 2
- 210000004227 basal ganglia Anatomy 0.000 description 2
- 230000003542 behavioural effect Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000007413 biotinylation Methods 0.000 description 2
- 230000006287 biotinylation Effects 0.000 description 2
- 238000005422 blasting Methods 0.000 description 2
- 210000000133 brain stem Anatomy 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 239000005018 casein Substances 0.000 description 2
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 2
- 235000021240 caseins Nutrition 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 208000015114 central nervous system disease Diseases 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 229940052810 complex b Drugs 0.000 description 2
- 238000002591 computed tomography Methods 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 210000005046 glial fibrillary acidic protein Anatomy 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 230000002267 hypothalamic effect Effects 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 239000002198 insoluble material Substances 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 230000003211 malignant effect Effects 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 210000004688 microtubule Anatomy 0.000 description 2
- 210000000478 neocortex Anatomy 0.000 description 2
- 210000005036 nerve Anatomy 0.000 description 2
- 210000002682 neurofibrillary tangle Anatomy 0.000 description 2
- 230000002981 neuropathic effect Effects 0.000 description 2
- 230000002887 neurotoxic effect Effects 0.000 description 2
- 231100000228 neurotoxicity Toxicity 0.000 description 2
- 230000007135 neurotoxicity Effects 0.000 description 2
- 229920001220 nitrocellulos Polymers 0.000 description 2
- 210000004940 nucleus Anatomy 0.000 description 2
- 230000008520 organization Effects 0.000 description 2
- 230000009054 pathological process Effects 0.000 description 2
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 238000002203 pretreatment Methods 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 210000004129 prosencephalon Anatomy 0.000 description 2
- 230000017854 proteolysis Effects 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 201000000980 schizophrenia Diseases 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- KISWVXRQTGLFGD-UHFFFAOYSA-N 2-[[2-[[6-amino-2-[[2-[[2-[[5-amino-2-[[2-[[1-[2-[[6-amino-2-[(2,5-diamino-5-oxopentanoyl)amino]hexanoyl]amino]-5-(diaminomethylideneamino)pentanoyl]pyrrolidine-2-carbonyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]-5-(diaminomethylideneamino)p Chemical compound C1CCN(C(=O)C(CCCN=C(N)N)NC(=O)C(CCCCN)NC(=O)C(N)CCC(N)=O)C1C(=O)NC(CO)C(=O)NC(CCC(N)=O)C(=O)NC(CCCN=C(N)N)C(=O)NC(CO)C(=O)NC(CCCCN)C(=O)NC(C(=O)NC(CC(C)C)C(O)=O)CC1=CC=C(O)C=C1 KISWVXRQTGLFGD-UHFFFAOYSA-N 0.000 description 1
- UAIUNKRWKOVEES-UHFFFAOYSA-N 3,3',5,5'-tetramethylbenzidine Chemical compound CC1=C(N)C(C)=CC(C=2C=C(C)C(N)=C(C)C=2)=C1 UAIUNKRWKOVEES-UHFFFAOYSA-N 0.000 description 1
- YNTLVCDWTWUMDV-UHFFFAOYSA-N 4-(4-aminophenyl)-n,2,3-trimethylaniline Chemical compound CC1=C(C)C(NC)=CC=C1C1=CC=C(N)C=C1 YNTLVCDWTWUMDV-UHFFFAOYSA-N 0.000 description 1
- 102000012440 Acetylcholinesterase Human genes 0.000 description 1
- 108010022752 Acetylcholinesterase Proteins 0.000 description 1
- 208000037259 Amyloid Plaque Diseases 0.000 description 1
- 101710137189 Amyloid-beta A4 protein Proteins 0.000 description 1
- 101710151993 Amyloid-beta precursor protein Proteins 0.000 description 1
- 102100022704 Amyloid-beta precursor protein Human genes 0.000 description 1
- 108010032595 Antibody Binding Sites Proteins 0.000 description 1
- 208000002109 Argyria Diseases 0.000 description 1
- 206010003694 Atrophy Diseases 0.000 description 1
- 208000025324 B-cell acute lymphoblastic leukemia Diseases 0.000 description 1
- 208000003950 B-cell lymphoma Diseases 0.000 description 1
- 208000024806 Brain atrophy Diseases 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- 102100025570 Cancer/testis antigen 1 Human genes 0.000 description 1
- 108010007718 Chromogranins Proteins 0.000 description 1
- 102000007345 Chromogranins Human genes 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 206010010071 Coma Diseases 0.000 description 1
- 101710082261 Competence-stimulating peptide Proteins 0.000 description 1
- 201000009343 Cornelia de Lange syndrome Diseases 0.000 description 1
- 208000010859 Creutzfeldt-Jakob disease Diseases 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 208000003471 De Lange Syndrome Diseases 0.000 description 1
- 101710138858 DnaJ homolog subfamily C member 5 Proteins 0.000 description 1
- 101100326341 Drosophila melanogaster brun gene Proteins 0.000 description 1
- 208000027534 Emotional disease Diseases 0.000 description 1
- 108700042658 GAP-43 Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 206010053759 Growth retardation Diseases 0.000 description 1
- 208000002250 Hematologic Neoplasms Diseases 0.000 description 1
- 208000036066 Hemophagocytic Lymphohistiocytosis Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000856237 Homo sapiens Cancer/testis antigen 1 Proteins 0.000 description 1
- 101000652315 Homo sapiens Synaptosomal-associated protein 25 Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 206010022773 Intracranial pressure increased Diseases 0.000 description 1
- 208000032382 Ischaemic stroke Diseases 0.000 description 1
- 206010023249 Juvenile chronic myelomonocytic leukaemia Diseases 0.000 description 1
- 238000012313 Kruskal-Wallis test Methods 0.000 description 1
- 201000005099 Langerhans cell histiocytosis Diseases 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 102000006386 Myelin Proteins Human genes 0.000 description 1
- 108010083674 Myelin Proteins Proteins 0.000 description 1
- 102000003729 Neprilysin Human genes 0.000 description 1
- 108090000028 Neprilysin Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 108090000526 Papain Proteins 0.000 description 1
- 206010033799 Paralysis Diseases 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 241000276498 Pollachius virens Species 0.000 description 1
- 108010050254 Presenilins Proteins 0.000 description 1
- 102000015499 Presenilins Human genes 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 241000269319 Squalius cephalus Species 0.000 description 1
- 241000191940 Staphylococcus Species 0.000 description 1
- 102000004874 Synaptophysin Human genes 0.000 description 1
- 108090001076 Synaptophysin Proteins 0.000 description 1
- 102000001317 Synaptotagmin I Human genes 0.000 description 1
- 108010055170 Synaptotagmin I Proteins 0.000 description 1
- 108010006785 Taq Polymerase Proteins 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- OIPILFWXSMYKGL-UHFFFAOYSA-N acetylcholine Chemical compound CC(=O)OCC[N+](C)(C)C OIPILFWXSMYKGL-UHFFFAOYSA-N 0.000 description 1
- 229960004373 acetylcholine Drugs 0.000 description 1
- 229940022698 acetylcholinesterase Drugs 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000003470 adrenal cortex hormone Substances 0.000 description 1
- 229960002684 aminocaproic acid Drugs 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- DZHSAHHDTRWUTF-SIQRNXPUSA-N amyloid-beta polypeptide 42 Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O)[C@@H](C)CC)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 DZHSAHHDTRWUTF-SIQRNXPUSA-N 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 208000037849 arterial hypertension Diseases 0.000 description 1
- 230000000712 assembly Effects 0.000 description 1
- 238000000429 assembly Methods 0.000 description 1
- 230000037444 atrophy Effects 0.000 description 1
- 230000008335 axon cargo transport Effects 0.000 description 1
- 230000007844 axonal damage Effects 0.000 description 1
- 230000003376 axonal effect Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000005549 barrier dysfunction Effects 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000002146 bilateral effect Effects 0.000 description 1
- 230000008499 blood brain barrier function Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 238000004820 blood count Methods 0.000 description 1
- 210000001772 blood platelet Anatomy 0.000 description 1
- 210000001218 blood-brain barrier Anatomy 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 238000010322 bone marrow transplantation Methods 0.000 description 1
- 230000005978 brain dysfunction Effects 0.000 description 1
- 201000008273 brain germinoma Diseases 0.000 description 1
- UDSAIICHUKSCKT-UHFFFAOYSA-N bromophenol blue Chemical compound C1=C(Br)C(O)=C(Br)C=C1C1(C=2C=C(Br)C(O)=C(Br)C=2)C2=CC=CC=C2S(=O)(=O)O1 UDSAIICHUKSCKT-UHFFFAOYSA-N 0.000 description 1
- 230000002308 calcification Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000007910 cell fusion Effects 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 230000003727 cerebral blood flow Effects 0.000 description 1
- 210000003710 cerebral cortex Anatomy 0.000 description 1
- 208000026106 cerebrovascular disease Diseases 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 201000002797 childhood leukemia Diseases 0.000 description 1
- 230000001713 cholinergic effect Effects 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 230000003930 cognitive ability Effects 0.000 description 1
- 230000006999 cognitive decline Effects 0.000 description 1
- 208000010877 cognitive disease Diseases 0.000 description 1
- 230000006998 cognitive state Effects 0.000 description 1
- 238000009096 combination chemotherapy Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- RKHQGWMMUURILY-UHRZLXHJSA-N cortivazol Chemical compound C([C@H]1[C@@H]2C[C@H]([C@]([C@@]2(C)C[C@H](O)[C@@H]1[C@@]1(C)C2)(O)C(=O)COC(C)=O)C)=C(C)C1=CC1=C2C=NN1C1=CC=CC=C1 RKHQGWMMUURILY-UHRZLXHJSA-N 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 108010059354 cysteine string protein Proteins 0.000 description 1
- 230000002380 cytological effect Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000003436 cytoskeletal effect Effects 0.000 description 1
- 230000003412 degenerative effect Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000003291 dopaminomimetic effect Effects 0.000 description 1
- 210000003372 endocrine gland Anatomy 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 206010015037 epilepsy Diseases 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 208000029944 familial hemophagocytic lymphohistiocytosis type 1 Diseases 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 210000005153 frontal cortex Anatomy 0.000 description 1
- 210000001652 frontal lobe Anatomy 0.000 description 1
- 238000002825 functional assay Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 231100000001 growth retardation Toxicity 0.000 description 1
- 201000010235 heart cancer Diseases 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 208000024348 heart neoplasm Diseases 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 230000000971 hippocampal effect Effects 0.000 description 1
- 235000014304 histidine Nutrition 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 102000053886 human SNAP25 Human genes 0.000 description 1
- 210000003917 human chromosome Anatomy 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 201000005992 juvenile myelomonocytic leukemia Diseases 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 238000011866 long-term treatment Methods 0.000 description 1
- 210000004880 lymph fluid Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 230000015654 memory Effects 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000037353 metabolic pathway Effects 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000003032 molecular docking Methods 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 210000005012 myelin Anatomy 0.000 description 1
- 210000000944 nerve tissue Anatomy 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 210000002241 neurite Anatomy 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 230000001272 neurogenic effect Effects 0.000 description 1
- 238000010984 neurological examination Methods 0.000 description 1
- 231100000878 neurological injury Toxicity 0.000 description 1
- 230000016273 neuron death Effects 0.000 description 1
- 230000014511 neuron projection development Effects 0.000 description 1
- 230000003955 neuronal function Effects 0.000 description 1
- 230000007514 neuronal growth Effects 0.000 description 1
- 230000003961 neuronal insult Effects 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 231100000189 neurotoxic Toxicity 0.000 description 1
- 230000003957 neurotransmitter release Effects 0.000 description 1
- 201000003077 normal pressure hydrocephalus Diseases 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 230000008557 oxygen metabolism Effects 0.000 description 1
- 229940055729 papain Drugs 0.000 description 1
- 235000019834 papain Nutrition 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007310 pathophysiology Effects 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 230000009984 peri-natal effect Effects 0.000 description 1
- 210000002856 peripheral neuron Anatomy 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 238000011458 pharmacological treatment Methods 0.000 description 1
- NMHMNPHRMNGLLB-UHFFFAOYSA-N phloretic acid Chemical compound OC(=O)CCC1=CC=C(O)C=C1 NMHMNPHRMNGLLB-UHFFFAOYSA-N 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 230000004793 poor memory Effects 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 210000000063 presynaptic terminal Anatomy 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 235000004252 protein component Nutrition 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 230000033764 rhythmic process Effects 0.000 description 1
- 102220005373 rs33938574 Human genes 0.000 description 1
- 102220020469 rs397508332 Human genes 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000011896 sensitive detection Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- CMZUMMUJMWNLFH-UHFFFAOYSA-N sodium metavanadate Chemical compound [Na+].[O-][V](=O)=O CMZUMMUJMWNLFH-UHFFFAOYSA-N 0.000 description 1
- 210000004989 spleen cell Anatomy 0.000 description 1
- 230000007480 spreading Effects 0.000 description 1
- 238000003892 spreading Methods 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 210000003523 substantia nigra Anatomy 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 210000000225 synapse Anatomy 0.000 description 1
- 230000003977 synaptic function Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 229960002180 tetracycline Drugs 0.000 description 1
- 229930101283 tetracycline Natural products 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 238000003325 tomography Methods 0.000 description 1
- 201000008757 transient arthritis Diseases 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
- 229910000166 zirconium phosphate Inorganic materials 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
- G01N33/6896—Neurological disorders, e.g. Alzheimer's disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/28—Neurological disorders
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/28—Neurological disorders
- G01N2800/2835—Movement disorders, e.g. Parkinson, Huntington, Tourette
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Chemical & Material Sciences (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measurement And Recording Of Electrical Phenomena And Electrical Characteristics Of The Living Body (AREA)
- Eye Examination Apparatus (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Peptides Or Proteins (AREA)
Abstract
【解決手段】本発明は、個体の1またはそれ以上の体液中の少なくとも3つの神経学的マーカーを検出する組み合わせアッセイを用いる、個体における神経変性の特異的検出、定量および/または分別診断のための新たな方法であって、神経変性のタイプおよび程度が対照試料と比較して該神経学的マーカーのすべてのレベルの量的変化により反映されるものである方法。
【選択図】なし
Description
本発明のもう1つの目的は、個体におけるアルツハイマー病の、より特異的な検出、定量および/または分別診断のための方法を提供することである。
本発明のもう1つの目的は、個体におけるレービー小体疾患の、より特異的な検出、定量および/または分別診断のための方法を提供することである。
本発明のもう1つの目的は、個体におけるパーキンソン病の、より特異的な検出、定量および/または分別診断のための方法を提供することである。
本発明のもう1つの目的は、個体における前頭側頭葉痴呆の、より特異的な検出、定量および/または分別診断のための方法を提供することである。
本発明のもう1つの目的は、パーキンソン病とアルツハイマー病との分別方法を提供することである。
本発明のもう1つの目的は、レービー小体疾患とアルツハイマー病との分別方法を提供することである。
本発明のもう1つの目的は、アルツハイマー病における血管の問題の特異的検出または定量のための方法、ならびに異なる形態のアルツハイマー病の分別診断のための方法を提供することである。
本発明のもう1つの目的は、化学療法により、あるいは化合物または放射線照射に対する曝露により誘発された神経変性の診断方法を提供することである。
本発明のもう1つの目的は、白血病または脳腫瘍の治療を受けた個体における、化学療法により誘発された神経変性の診断方法を提供することである。
本発明のもう1つの目的は、周産期仮死により生じる神経変性の診断方法を提供することである。
本発明のもう1つの目的は、脳脊髄液中のシナプス蛋白Rab3aの新たな検出方法を提供することである。
本発明のもう1つの目的は、個体における神経変性の、より特異的検出、定量および/または分別診断を可能にする、脳脊髄液中のRab3aの新たな検出方法を提供することである。
本発明のもう1つの目的は、アルツハイマー病の、より特異的検出、定量および/または分別診断を可能にする、脳脊髄液中のRab3aの新たな検出方法を提供することである。
本発明のもう1つの目的は、脳脊髄液中のシナプス蛋白α−シヌクレインの新たな検出方法を提供することである。
本発明のもう1つの目的は、個体におけるより特異的な検出、定量、および/または分別診断を可能にする、脳脊髄液中のα−シヌクレインの新たな検出方法を提供することである。
本発明のもう1つの目的は、アルツハイマー病および/またはレービー小体疾患の、より特異的な検出または定量を可能にする、ならびに/あるいはレービー小体疾患とアルツハイマー病との分別診断を可能にする、脳脊髄液中のα−シヌクレインの新たな検出方法を提供することである。
本発明のもう1つの目的は、上記方法を行うための診断キットを提供することである。
本発明のもう1つの目的は、特定の治療の有効性の治療モニタリングおよび/または決定のための方法を提供することである。
(1) 個体におけるアルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための方法であって、
該個体からの体液試料中の少なくとも3種の神経学的マーカーのレベルを、該神経学的マーカーを特異的に認識する抗体を用いて決定する工程を含み、
該神経学的マーカーがタウ、β−アミロイド(1−42)、およびシナプス蛋白である、方法;
(2) 該シナプス蛋白が、Rab3aまたはSNAP25である、(1)に記載の方法;
(3) 該体液試料が、脳脊髄液試料である、(1)または(2)に記載の方法;
(4) (1)〜(3)のいずれか1に記載の方法であって、
−脳脊髄液試料中のタウ、β−アミロイド(1−42)、およびRab3aのレベルを決定する、または
−脳脊髄液試料中のタウ、β−アミロイド(1−42)、およびSNAP25のレベルを決定する、方法;
(5) アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のためのキットであって、
異なる神経学的マーカーをそれぞれ認識する、少なくとも3種の抗体を含み、
該神経学的マーカーがタウ、β−アミロイド(1−42)、およびシナプス蛋白である、診断キット;
(6) 該シナプス蛋白が、Rab3aまたはSNAP25である、(5)に記載の診断キット;
(7) 該神経学的マーカーが、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、である、(5)または(6)に記載の診断キット。
(8) アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための診断キットであって、
−異なる神経学的マーカーをそれぞれ認識する、少なくとも3種の一次抗体(補足抗体)を一緒にあるいは別個に含む支持体、および
−神経学的マーカー−一次抗体複合体の1つをそれぞれ認識する二次抗体(ディテクター抗体)を含み、
該神経学的マーカーがタウ、β−アミロイド(1−42)、およびシナプス蛋白である、診断キット;
(9) 該シナプス蛋白が、Rab3aまたはSNAP25である、(8)に記載の診断キット;
(10)
該神経学的マーカーが、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、である、(8)または(9)に記載の診断キット;
(11) 該2次抗体に特異的、にタグを付するまたはカップリングするためのマーカーをさらに含む(8)〜(10)のいずれか1に記載の診断キット;
(12) 一次抗体と体液試料、二次抗体と神経学的マーカー−一次抗体複合体、および/または結合二次抗体とマーカー間の免疫学的反応を行うための適切な緩衝液をさらに含む(8)〜(11)のいずれか1に記載の診断キット;
(13) 標準化の目的のために、神経学的マーカーの検出に使用されるキットの抗体により特異的に認識される精製蛋白または合成ペプチドをさらに含む、(8)〜(12)のいずれか1に記載の診断キット;
(14) (1)〜(4)のいずれか1に記載の方法を行うために特異的に設計された(8)〜(13)のいずれか1に記載の診断キット;
(15) アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための、タウ、β−アミロイド(1−42)、およびシナプス蛋白を特異的に認識する抗体の使用;
(16) 該シナプス蛋白が、Rab3aまたはSNAP25である、(15)に記載の使用;
(17) 該抗体が、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、を特異的に認識する、(15)または(16)に記載の使用;
(18) アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための診断キットの製造のための、タウ、β−アミロイド(1−42)、およびシナプス蛋白を特異的に認識する抗体の使用;
(19) 該シナプス蛋白が、Rab3aまたはSNAP25である、(18)に記載の使用;
(20) 該抗体が、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、を特異的に認識する、(18)または(19)に記載の使用;
(21) 特定の治療の、治療モニタリングおよび/または有効性の決定のための、(1)〜(14)のいずれか1に記載の方法または診断キットの使用;
を提供するものである。
本明細書の表現「神経変性の定量」は、特定の神経変性的症状による神経の機能不全の程度が測定されることを意味する。
本明細書の表現「神経変性の分別診断」は、神経学的障害の特定の疾患または特定の原因が特定の神経変性的症状に関連している種々の神経変性的症状を識別することをいう。
該個体から1またはそれ以上の体液試料を得ること;および
抗原−抗体複合体の生成に適した条件下において、体液試料中の異なる神経学的マーカーをそれぞれ認識する少なくとも3種の抗体(一次抗体または捕捉抗体)に該体液試料を接触させること;および
該体液試料に対する該抗体の免疫学的結合を検出すること;
対照試料と比較して、該神経学的マーカーすべてのレベルの量的変化に反映される神経変性のタイプおよび程度を該体液中の該神経学的マーカーのレベルに基づいて推断すること。
a)二次抗体(またはディテクター抗体)
*該二次抗体は、抗原−抗体複合体の特異的エピトープを認識するが、単独の一次抗体を認識しないモノクローナル抗体であってもよく、あるいは
*抗原−抗体複合体の特異的エピトープを認識するが、単独の一次抗体を認識しないポリクローナル抗体であって、好ましくは固定化された神経学的マーカーまたは神経学的マーカー−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたポリクローナル抗体であってもよい
b)該二次抗体に特異的にタグを付する、あるいは特異的にカップリングするマーカーであって、当業者に知られたいずれかのマーカー
c)抗体と体液試料との間、二次抗体と神経学的マーカー−一次抗体複合体との間および/または結合二次抗体とマーカーとの間の免疫学的反応、を行うための適当な緩衝液;および
d)また可能ならば、標準化する目的で、神経学的マーカーの検出に使用する抗体と反応する精製蛋白または合成ペプチド。
本明細書の表現「認識」、「〜と反応」、「免疫学的結合」または「抗原−抗体複合体」は、抗体および抗原の免疫学的特性を考慮したすべての条件下で抗原と抗体との間の結合が起こることと解釈すべきである。
用語「体液」は、血液、リンパ液、尿および脳脊髄液(CSF)(これらに限らない)を包含する人体に存在するすべての液体をいう。
タウ、β−アミロイド(1−42)、およびニューロモジュリン;あるいは
タウ、ニューロン特異的エノラーゼおよびニューロモジュリン;あるいは
タウ、ホスホタウおよびβ−アミロイド(1−42)。
個体から脳脊髄液試料を得ること;次いで、
抗原−抗体複合体の生成に適した条件下で、Rab3aを認識するモノクローナル抗体(一次抗体または捕捉抗体)に該脳脊髄液試料を接触させること;次いで、
該脳脊髄液試料への該抗体の免疫学的結合を検出すること。
a)二次抗体(またはディテクター抗体)
*該二次抗体(またはディテクター抗体)は、抗原−抗体複合体のエピトープを認識するが、単独の一次抗体を認識しないモノクローナル抗体であってもよく、あるいは
*該二次抗体(またはディテクター抗体)は、抗原−抗体複合体のエピトープを認識するが、単独の一次抗体を認識しないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、Rab3aまたはRab3a−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
b)該二次抗体に特異的にタグを付しあるいはカップリングするマーカーであって、当業者に知られたいずれかの使用可能なマーカー
c)抗体と脳脊髄液との間、二次抗体と神経学的マーカー−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液;および
d)さらに可能ならば、標準化を目的として、Rab3aを認識する抗体と反応する精製蛋白または合成ペプチド。
個体から脳脊髄液試料を得ること;次いで、
抗原−抗体複合体の生成に適した条件下で、SNAP25を認識するモノクローナル抗体(一次抗体または捕捉抗体)に該脳脊髄液試料を接触させること;次いで、
該脳脊髄液試料への該抗体の免疫学的結合を検出すること。
a)二次抗体(またはディテクター抗体)
*該二次抗体(またはディテクター抗体)は、抗原−抗体複合体のエピトープを認識するが、単独の一次抗体を認識しないモノクローナル抗体であってもよく、あるいは
*該二次抗体(またはディテクター抗体)は、抗原−抗体複合体のエピトープを認識するが、単独の一次抗体を認識しないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、SNAP25またはSNAP25−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
b)該二次抗体に特異的にタグを付しあるいはカップリングするマーカーであって、当業者に知られたいずれかの使用可能なマーカー
c)抗体と脳脊髄液との間、二次抗体と神経学的マーカー−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液;および
d)さらに可能ならば、標準化を目的として、SNAP25を認識する抗体と反応する精製蛋白または合成ペプチド。
個体から脳脊髄液試料を得ること;次いで、
抗原−抗体複合体の生成に適した条件下で、α−シヌクレインを認識するモノクローナル抗体(一次抗体または捕捉抗体)に該脳脊髄液試料を接触させること;次いで、
該脳脊髄液試料への該抗体の免疫学的結合を検出すること。
a)二次抗体(またはディテクター抗体)
*該二次抗体(またはディテクター抗体)は、抗原−抗体複合体のエピトープを認識するが、単独の一次抗体を認識しないモノクローナル抗体であってもよく、あるいは
*該二次抗体(またはディテクター抗体)は、抗原−抗体複合体のエピトープを認識するが、単独の一次抗体を認識しないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、α−シヌクレインまたはα−シヌクレイン−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
b)該二次抗体に特異的にタグを付しあるいはカップリングするマーカーであって、当業者に知られたいずれかの使用可能なマーカー
c)抗体と脳脊髄液との間、二次抗体と神経学的マーカー−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液;および
d)さらに可能ならば、標準化を目的として、α−シヌクレインを認識する抗体と反応する精製蛋白または合成ペプチド。
タウ、ホスホタウ、NSE、β−アミロイド(1−42)、β−アミロイド(1−40)、ニューロモジュリンまたはRab3a;あるいは
タウ、ホスホタウ、NSE、β−アミロイド(1−42)、β−アミロイド(1−40)、ニューロモジュリンまたはSNAP25;あるいは
タウ、ホスホタウ、NSE、β−アミロイド(1−42)、β−アミロイド(1−40)、ニューロモジュリンまたはα−シヌクレイン。
脳脊髄液試料中の少なくともα−シヌクレインのレベルが決定され;および/または
脳脊髄液試料中のタウ、β−アミロイド(1−42)およびα−シヌクレインのレベルが決定される。
脳脊髄液試料中のタウ、β−アミロイド(1−42)およびRab3aのレベルが決定され;あるいは
脳脊髄液試料中のタウ、β−アミロイド(1−42)およびSNAP25のレベルが決定される。
脳脊髄液試料中のタウおよびβ−アミロイド(1−42)のレベルが定量的に決定され、血漿試料中のβ−アミロイド(1−42)のレベルが定量的に決定され;あるいは
脳脊髄液試料中のホスホタウおよびβ−アミロイド(1−42)のレベルが定量的に決定され、血漿試料中のβ−アミロイド(1−42)のレベルが定量的に決定され;あるいは
脳脊髄液試料中のタウおよびホスホタウのレベルが定量的に決定され、血漿試料中のβ−アミロイド(1−42)のレベルが定量的に決定され;あるいは
脳脊髄液中のタウ、ホスホタウおよびβ−アミロイド(1−42)のレベルが定量的に決定される。
異なる神経学的マーカーをそれぞれ認識する、一緒にされたあるいは別個のウェル中にある少なくとも3つの抗体(一次抗体または捕捉抗体)を含むマイクロタイタープレートのごとき支持体、
神経学的マーカー−一次抗体複合体の1つをそれぞれ認識する二次抗体(ディテクター抗体)
*該二次抗体は神経学的マーカー−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないモノクローナル抗体であってもよく、あるいは
*該二次抗体は神経学的マーカー−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、固定化された神経学的マーカーまたは神経学的マーカー−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
可能ならば、該二次抗体に特異的にタグを付するあるいはカップリングするためのマーカー、
可能ならば、一次抗体と体液試料との間、二次抗体と神経学的マーカー−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液、
可能ならば、標準化を目的として、神経学的マーカーの検出に使用されるキットの抗体により特異的に認識される精製蛋白または合成ペプチド。
α−シヌクレイン;あるいは
タウ、β−アミロイド(1−42)およびα−シヌクレイン;あるいは
タウ、β−アミロイド(1−42)およびRab3a;あるいは
タウ、β−アミロイド(1−42)およびSNAP25;あるいは
タウ、β−アミロイド(1−42)およびニューロモジュリン;あるいは
タウ、ニューロン特異的エノラーゼおよびニューロモジュリン;あるいは
タウ、ホスホタウおよびβ−アミロイド(1−42);あるいは
タウおよびβ−アミロイド(1−42)。
少なくとも、Rab3aを認識するモノクローナル抗体(一次抗体または捕捉抗体)を含むマイクロタイタープレートのごとき支持体
二次抗体(またはディテクター抗体)
*該二次抗体はRab3a−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないモノクローナル抗体であってもよく、あるいは
*該二次抗体はRab3a−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、固定化されたRab3aまたはRab3a−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
可能ならば、該二次抗体に特異的にタグを付するあるいはカップリングするためのマーカー、
可能ならば、一次抗体と体液試料との間、ニ次抗体とRab3a−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液、
可能ならば、標準化を目的として、Rab3aの検出に使用されるキットの抗体により特異的に認識される精製蛋白または合成ペプチド。
少なくとも、SNAP25を認識するモノクローナル抗体(一次抗体または捕捉抗体)を含むマイクロタイタープレートのごとき支持体
二次抗体(またはディテクター抗体)
*該二次抗体はSNAP25−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないモノクローナル抗体であってもよく、あるいは
*該二次抗体はSNAP25−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、固定化されたSNAP25またはSNAP25−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
可能ならば、該二次抗体に特異的にタグを付するあるいはカップリングするためのマーカー、
可能ならば、一次抗体と体液試料との間、ニ次抗体とSNAP25−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液、
可能ならば、標準化を目的として、SNAP25の検出に使用されるキットの抗体により特異的に認識される精製蛋白または合成ペプチド。
少なくとも、α−シヌクレインを認識するモノクローナル抗体(一次抗体または捕捉抗体)を含むマイクロタイタープレートのごとき支持体
二次抗体(またはディテクター抗体)
*該二次抗体はα−シヌクレイン−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないモノクローナル抗体であってもよく、あるいは
*該二次抗体はα−シヌクレイン−一次抗体複合体のエピトープと免疫学的複合体を形成できるが、単独の一次抗体とは免疫学的複合体を形成できないポリクローナル抗体であってもよく、該ポリクローナル抗体は、好ましくは、固定化されたα−シヌクレインまたはα−シヌクレイン−一次抗体複合体を用いる免疫アフィニティークロマトグラフィーにより精製されたものである
可能ならば、該二次抗体に特異的にタグを付するあるいはカップリングするためのマーカー、
可能ならば、一次抗体と体液試料との間、二次抗体とα−シヌクレイン−一次抗体複合体との間、および/または結合二次抗体とマーカーとの間の免疫学的反応を行うための適当な緩衝液、
可能ならば、標準化を目的として、α−シヌクレインの検出に使用されるキットの抗体により特異的に認識される精製蛋白または合成ペプチド。
1.1 Rab3aおよびSNAP25のクローニング
製造者の増幅プロトコルに従ってQuick-ScreenTMヒトcDNAライブラリー(Clontech, Palo Alto, CA, USA;カタログ番号K1003-1)からRab3aおよびSNAP25コーディング配列を増幅するために特別なプライマーを使用した。簡単に説明すると、94℃で45秒、60℃で45秒アニーリング、次いでTaqポリメラーゼ(Stratagene, Amsterdam, The Netherlands;カタログ番号600131)を用いて72℃で2分伸長からなるサイクルを35サイクル行った。72℃で7分間のポリメラーゼ伸長反応にてプログラムを終了した。Perkin-Elmer(Ueberlingen, Germany)DNAサーマルサイクラー(480型)にて反応を行った。Rab3aを増幅するためのプライマーの配列はヒトRab3a配列(Zahraoui et al., 1989)に基づくものであった:ATGプライマーとしてATG GCA TCG GCC ACA GAC TCG CGC TAT GGG (Tm=76℃)および逆プライマーとしてCGCG TCTAG AGG CTC TCA GCA GGC GCA GTC CTG GTG CGG (Tm=77℃)。SNAP25を増幅するためのプライマーの配列はヒトSNAP25配列(Zhao et al., 1994)に基づくものであった:ATGプライマーとしてATG GCC GAA GAC GCA GAC ATG CGC AAT GAG (Tm=75℃)および逆プライマーとしてCGCG CTAG ACA CTT AAC CAC TTC CCA GCA TCT TTG TTG (Tm=59℃)。
PCR生成物を再増幅して十分な量のPCR生成物を得て、T4 DNAポリメラーゼで仕上げを行い、XbaIで切断し、NcoIで平滑末端化され、XbaIで切断されたpIGRHISA(Innogenetics, Gent, Belgium;カタログ番号2075)中に連結した。これにより、Rab3aに関してpIGRHISARab3a(Innogenetics, Gent, Belgium;カタログ番号3008)を、SNAP25に関してpIGRH6SNAP25a(Innogenetics, Gent, Belgium;カタログ番号2941)を得た。連結生成物をDH1(λ)(Bachmann, 1987)中に形質転換し、テトラサイクリン耐性コロニーをインサートの存在について分析した。インサートを配列決定し、正しい配列(Zahraoui et al., 1989; Zhao et al., 1994)を含むプラスミドをさらに使用した。Rab3aに関しては、PCRによるいくつかの人工的要因が存在した。2つのクローンから正しい配列を組み立てた。
PLに基づく発現系pIGRHISARab3aおよびpIGRH6SNAP25aを用いてRab3aおよびSNAP25をそれぞれイー・コリにおいて発現させた。温度感受性cIリプレッサーを有するMC1061 pACI(Wertman et al., 1986)中に正しいプラスミドを形質転換した。約25kDaのクーマシー染色可能なバンドが12.5%アクリルアミドゲル上に可視化され、合理的な発現レベルが示された。組み換え蛋白は、NiIMACカラムでの精製を迅速ならしめる6個の付加ヒスチジン残基を含む融合蛋白として得られた。3リットルの熱誘導イー・コリ(Houchi, 1988; Van Gelder et al., 1993)を用いて、10mgよりも多い組み換えRab3aおよびSNAP25を精製し、少なくとも95%の均質性であった。
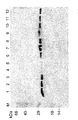
Rab3aおよびSNAP25に対する抗体をウサギにおいて生成させた。50μgの精製蛋白を2匹のウサギに腹腔内注射した(100μg/ウサギ1匹)。4週間ごとに注射を行い、ELISAで力価を測定した。抗体は脳抽出物により特徴づけられた。Rab3a免疫反応性に関する結果を図1に示す。アルツハイマー病患者および対照患者からの組織試料を、5倍体積の1% SDS、1% バナジン酸ナトリウム、10mM Tris pH7.4中で迅速にホモジナイズし、次いで、水浴にて5分間煮沸することにより調製した。ホモジネートを5分間遠心分離(12000g、室温)して不溶性物質を除去した。少量の上清を用いてBCA法(Pierce, Rockford, Illinois, USA)により蛋白濃度を測定した。上清を水で希釈して蛋白濃度を2mg/mlとし、同体積の2x試料緩衝液(250mM Tris pH6.8、3% SDS、10%グリセロール、0.006%ブロモフェノールブルーおよび2% β−メルカプトエタノール)を添加した。10〜12.5%ゲルのLaemmli系によりゲル電気泳動を行った。半乾燥ブロッティング法により蛋白をニトロセルロース(Schleicher and Schull, Dassel, Germany;カタログ番号401196)に移行させた。10mM Tris pH7.5,150mM NaCl中の1% BSAでニトロセルロースフィルターをブロックした。1% BSA中適当濃度(±1μg/ml)の一次抗体およびニ次抗体を添加した。
0.3M NaHCO3,pH8.6中で精製組み換え抗原を透析した。透析前後においてOD280値を測定して蛋白量を評価した。Mini-Leak-Medium(KEM-EN-TEC Biozyme, Vancouver, BC, Canada;カタログ番号10127、ロット番号60232-5)を用い、製造者の指示に従って免疫精製を行った。抗体の一部をビオチン化させた(Amersham, Place Little Chalfont ]Buckinghamshire, UK;カタログ番号RPN 2202)。銀染色およびウエスタンブロットにより精製および標識化をモニターした(データ示さず)。
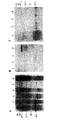
特異的モノクローナル抗体(Transduction Labs, Lexington, KY, USA; R35520およびS35020)を捕捉抗体として用い、免疫精製されたポリクローナルウサギ抗血清をディテクター抗体として用いて、CSF中に添加したシナプス蛋白Rab3aおよびSNAP25の安定性を、37℃で一晩インキュベーションした後に評価した。濃度500pg/mlにおいて、SNAP25およびRab3aに対する組み換え体の免疫反応性は試験したCSF中で一晩置いても変化しなかった(図2)。
50mlのCSFからのアルブミンおよびIgGの抽出ならびにカラムでの分画により、両蛋白がCSF中に存在するという直接的証拠を得た。フラクションを乾燥させ、試料緩衝液に溶解し、12%アクリルアミドゲルで泳動し、ブロッティングした。Rab3aおよびSNAP25モノクローナル抗体を用いてPVDF膜をプローブした。予想分子量およびpIの免疫反応性バンドが検出された。
モノクローナルRab3aまたはSNAP25抗体を捕捉抗体とし、免疫アフィニティー精製されたビオチン化ポリクローナル抗体をディテクター抗体とするサンドイッチELISAを開発した。MaxisporpマイクロタイタープレートをAffini Pureヤギ抗マウスIgG(Jackson Immuno Research Laboratories, Inc., West Grove, Pennsylvania, USA; カタログ番号115-035-144)で被覆した。PBS中1% BSA(臨床用グレード 98% 脂肪酸不含; ICN, Biomedical Research Products, Costa Mesa, CA, USA; カタログ番号 105033, ロット番号 6p384)をブロッキング緩衝液として使用した。ブロッキング緩衝液で1/1000に希釈したマウス抗Rab3a(Transduction Labs, Lexington, KY, USA; カタログ番号 R35520, IgG2a, クローン 9, ロット番号 606-259-1550 ロット 2)または抗SNAP25(Transduction Labs, Lexington, KY, USA; カタログ番号 S35020, IgG1, クローン 20)を添加した。インキュベーション後、組み換え抗原を異なる濃度で添加した(濃度範囲40000〜2.56pg/ml)。同時に、アフィニティー精製されたウサギ抗Rab3aまたは抗SNAP25抗血清を最適バックグラウンドシグナル比となるように選択した濃度で添加した。次いで、1/2000に希釈したセイヨウワサビ標識ストレプトアビジン(Immuno Research Laboratories, Inc., West Grove, Pennsylvania, USA; カタログ番号 016-030-084)によりビオチン化ウサギ抗体を検出した。カップリングしたペルオキシダーゼを、TMB H2O2基質溶液により検出した。30分後に2N H2SO4で反応を停止し、吸光度を450nmで測定した。このELISAに基づいて10pg/ml程度のRab3aを検出することができた。SNAP25のアッセイは同じ原理に基づくものであった。
2.1 α−シヌクレインに対する特異性に関する市販抗体の評価
異なるシヌクレインのイソ形態(isoform)に対する市販モノクローナル抗体(Transduction Labs, Lexington, KY, USA; カタログ番号 S63320, IgG1)の特異性を評価した。公表された配列のデータ(α-synuclein: accession number L08850; β-synuclein: accession number S69965; γ-synuclein: accession number AF010126)に基づくプライマーを用いて、α−シヌクレイン、β−シヌクレイン、γ−シヌクレインのオープンリーディングフレーム(ATGから停止コドンまで)をヒト脳cDNAライブラリー(HL5018; Clontech, Palo Alto, CA, USA)から増幅した。報告されたように、いくつかの重要なアミノ酸変化がγ−シヌクレインのオリジナル配列に存在した:このクローンにはK12EおよびK68Eがあり、このクローンのアミノ酸109の多型性はE109Vであった。アミノ末端に6個のさらなるヒスチジンを付加するPLベースの発現系(ICCG 3307; Innogenetics, Gent, Belgium)中にインサートをサブクローンした。Hisタグを付したシヌクレイン融合蛋白をイー・コリにおいて発現させた。次いで、イー・コリ蛋白をSDS−PAGEで泳動し、Transduction Labs (Lexington, KY, USA)から市販されているモノクローナル抗体を用いてイムノブロッテイングした。このモノクローナル抗体はα−シヌクレインに対して特異性を示し、シヌクレイン蛋白のカルボキシ末端半分をマッピングしている(図3)。
数人の患者からのCSFをプールした。Rotophorを用いて200mlのプールしたCSFを等電点により分離した。次いで、得られたフラクションをSDS−PAGEで泳動し、Transduction Labs (Lexington, KY, USA)から市販されているモノクローナル抗体を用いてイムノブロッテイングした。2つの免疫反応性バンドが19kDaの範囲に検出され、pIは4ないし6の範囲であった(図4)。いくつかの負に荷電したアミノ酸(最後の20個のアミノ酸中に6つのE)はpIをより塩基性のほうへシフトさせるので、低い方のバンドはC末端切断形態である可能性があった。この免疫反応性に基づいて、α−シヌクレインの濃度範囲をpg/mlの範囲で評価した。
3リットルの誘導イー・コリ培養からα−シヌクレインを精製したところ、10mgよりも多いα−シヌクレインが精製された(クーマシーおよび銀染色ゲルから評価すると純度は90%より高い)。いくつかの免疫スキーム(表3)に従って蛋白をマウスに注射した。4回注射後、コーティングELISAにおいてα−シヌクレインに対する力価を評価した。6匹のマウスは100000以上の力価を有していた(バックグラウンドの2倍のODが得られる血清の希釈率として力価を定義)。
最後の注射から3日後、動物312(m3)から脾臓細胞を取り、Koehler and Milstein (1975)により記載された方法に大まかに準じて細胞融合に使用した。最初のスクリーニングラウンドでは、直接コーティングアッセイにおいて特異的抗体の存在についてハイブリドーマを試験した。次いで、α−、β−、γ−シヌクレインおよびα−シヌクレイン由来の欠失変異体を含有するイー・コリ溶解物のドットブロットによりそれらを再試験して、シヌクレイン蛋白上の異なるエピトープを認識する抗体を生成するハイブリドーマを選択した。
ドットブロットにおいてα−シヌクレインに特異的であった2つのハイブリドーマ3B5(IgG2a)および9B6(IgG1)を単離した。その正確なエピトープを決定するために、カルボキシ末端部分(位置64から140まで)を、10個の重複するペプチドとして合成した(図5)。それらのペプチドはアミノ酸14個の長さで、7個のアミノ酸が重複していた。ビオチン化ペプチドを、1μg/mlの濃度でストレプトアビジン被覆プレート上に捕捉した。これらのペプチド上でα−シヌクレイン特異的抗体をインキュベーションし、次いで、抗マウス酵素結合抗体を用いて検出した。トリメチルベンジジンを基質として用いて酵素セイヨウワサビペルオキシダーゼを定量した。3B5および9B6は両方とも、配列LEDMPVDPDNEAYE(位置113〜126)を含むペプチドを認識し、このモノクローナル抗体に対する直鎖状エピトープが示唆された(図6)。同じセットの実験において、α−シヌクレインを認識することがすでに示されている市販抗体(Clone 42, IgG1, Transduction Labs, Lexington, KY, USA; カタログ番号 S63320)もまた、直鎖状エピトープ(配列AGSIAAATGFVKKD)(図6)にマップできた。
第2および第3ラウンドのサブクローニング後、10〜20mgの抗体を精製するために抗体の生成を1〜2リットルまでスケールアップする。Mini-Leak-Medium(KEM-EN-TEC Biozyme, Vancouver, BC, Canada; カタログ番号 10127, ロット番号 60232-5)を用いて、製造者により提供される説明に従って抗体を免疫精製する。
十分に確立された方法(Bonhard et al., 1984)に従って、D−ビオチニル−エタ−アミノカプロン酸N−ヒドロキシサクシンイミドエステル(Boehringer-Mannheim, Brussels, Belgium; カタログ番号 1008960)を用いてビオチン化を行う。
α−シヌクレイン抗体を捕捉抗体とし、ビオチン化モノクローナル抗体の1つをディテクター抗体とするサンドイッチELISAを開発する。MaxisporpマイクロタイタープレートをAffini Pureヤギ抗マウスIgG(Jackson Immuno Research Laboratories, Inc., West Grove, Pennsylvania, USA; カタログ番号115-035-144)で被覆する。PBS中1% BSA(臨床用グレード 98% 脂肪酸不含; ICN, Biomedical Research Products, Costa Mesa, CA, USA; カタログ番号 105033, ロット番号 6p384)+1%マウス血清をブロッキング緩衝液として使用する。ブロッキング緩衝液で1/1000に希釈した抗α−シヌクレイン(Transduction Labs, Lexington, KY, USA)を添加する。インキュベーション後、組み換え抗原を異なる濃度で添加する(濃度範囲1000〜2pg/ml)。同時に、1%マウス抗体の存在下においてビオチン化抗α−シヌクレインモノクローナル抗体を最適バックグラウンドシグナル比となるように選択した濃度で添加する。次いで、1/2000に希釈したセイヨウワサビ標識ストレプトアビジン(Immuno Research Laboratories, Inc., West Grove, Pennsylvania, USA; カタログ番号 016-030-084)によりビオチン化ウサギ抗体を検出する。カップリングしたペルオキシダーゼを、TMB H2O2基質溶液により検出する。30分後に2N H2SO4で反応を停止し、吸光度を450nmで測定する。
3.1 タウおよびホスホタウ
AT120を捕捉抗体とし、ビオチン化HT7−BT2をディテクター抗体として用いて、タウ抗原試験(INNOTEST hTau antigen, Innogenetics, Gent, Belgium)により全タウを測定した。モノクローナル抗体AT120は、正常ヒトタウ蛋白および過剰にリン酸化されたヒトタウ蛋白の両方と等しく十分に反応し(Vandermeeren et al., 1993)、モノクローナル抗体HT7もまた、正常ヒトタウ蛋白および過剰にリン酸化されたヒトタウ蛋白の両方と等しく十分に反応するが、モノクローナル抗体BT2は優先的に正常タウを認識する(Goedert et al., 1994)。すでに記載されたようにして(Mercken et al., 1992b)調製された、アフィニティー精製されたタウ蛋白を標準物質として使用した。
HT7を捕捉抗体とし、ビオチン化AT270をディテクター抗体として用いるサンドイッチELISA(INNOTEST phospho-tau(181), Innogenetics, Gent, Belgium)を用いてホスホタウを測定した。AT270はホスホタウを特異的に認識する(国際公開 WO 95/17429)。
Innotest β-amyloid(1-42)(Innogenetics, Gent, Belgium)を用いてβ−アミロイド(1−42)濃度を測定した。アッセイはサンドイッチ型ELISAであり、該アッセイにおいて第1のモノクローナル抗体21F12(アミロイドのカルボキシ末端に特異的)を捕捉抗体として使用し、ビオチン化抗体3D6(アミノ末端に特異的)をディテクター抗体として使用する。21F12/3D6の組み合わせはアミロイド(1−42)ペプチドの特異的検出を可能にする。いくぶんかの交差反応性がアミロイド(1−42)に関して観察されるが、短いペプチドに関しては観察されない(Citron et al., 1997; Johnson-Wood et al., 1997)。簡単に説明すると、21F12抗体を10mM Tris−10mM NaClに懸濁し、4℃で一晩かけてNunc Maxisorbsマイクロタイタープレートを被覆した。1回洗浄工程を行った後、25℃で2時間、PBS−0.1%カゼインでプレートをブロックした。75μlのビオチン化3D6および25μlのCSFまたは標準物質を同時インキュベーション(25℃で1時間)することにより試験を行った。数回洗浄工程を行った後、100μlのHRP−ストレプトアビジン(RDI, Flanders, New York, NY, USA)を添加することにより結合抗体量を調べた。インキュベーションを25℃で30分継続した。次いで、100μlの0.42mM 3,5,3’,5’−テトラメチルベンジジンをペルオキシダーゼ基質として添加した。30分後に50μlの0.9N H2SO4で反応を停止した。
Quality Controlled Biochemicals (QCB, Hopkinton, MA, USA)から得た、C末端に特異的な、アフィニティー精製されたポリクローナル抗体を捕捉抗体として用い、3D6(Citron et al., 1997; Johnson-Wood et al., 1997)をディテクター抗体として用いて、β−アミロイド(1−40)濃度を測定した。10mM Tris−10mM NaCl緩衝液中で25℃で2時間かけてNunc Maxisorbsマイクロタイタープレートを5μg/mlのアフィニティー精製されたヤギ抗ウサギIgG(H+L)(Jackson Immuno Research Laboratories, Inc., West Grove, Pennsylvania, USA; カタログ番号 111-005-144)で被覆した。その後、4℃で一晩、プレートをPBS−0.1%カゼインでブロックした。ウサギポリクローナル抗体(QCB, Hopkinton, MA, USA; カタログ番号 44-348-20)を0.5μg/mlの濃度で添加し、25℃で1時間置いた。数回洗浄工程を行った後、100μlのCSFまたは標準物質を25℃で2時間インキュベーションした。100μlのビオチン化3D6抗体を添加(抱合体希釈物中0.1μg/mlの濃度で添加)して25℃で1時間置くことにより結合アミロイド量を調べた。プレートをさらに5回洗浄した。100μlのSV−AP(Gibco, Rockville, MD, USA; カタログ番号 JK-4410)を添加することにより結合抗体量を調べた。インキュベーションを25℃で1時間継続した。最後の洗浄工程(5回)の後、基質緩衝液に溶解した100μlのTMBをペルオキシダーゼ基質として添加した。30分後に50μlの0.9N H2SO4で反応を停止した。
2種のエピトープ特異的モノクローナル抗体(NM2、NM4;Oestreicher et al., 1994)を用いてニューロモジュリンについても測定した。捕捉抗体としてNM2を選択し、ディテクター抗体としてビオチン化NM4を選択した。組み換えニューロモジュリンを標準物質として使用した。
NSEの測定は、抗NSEモノクローナル抗体2E7を捕捉抗体として用い、ペルオキシダーゼ標識抗NSEモノクローナル抗体10C1をディテクター抗体として用いるサンドイッチELISAの測定は、抗NSEモノクローナル抗体2E7を捕捉抗体として用い、ペルオキシダーゼ標識抗NSEモノクローナル抗体10C1をディテクター抗体として用いるサンドイッチELISAに基づくものであった。ヒト脳から精製したNSEを標準物質として使用した(Vanmechelen et al., 1997)。
BCA蛋白試薬(Pierce, Rockford, Illinois, USA)を用いて蛋白濃度を決定した。
4.1 患者および対照患者
アルツハイマー病(AD)群は32人の患者からなり、男性15人、女性17人で、平均年齢±SDは75.0±6.6歳であった。血管性痴呆(VAD)群は20人の患者からなり、男性10人、女性10人で、平均年齢±SDは81.0±7.0歳であった。対照群は18個体を含み、男性7人、女性11人で、平均年齢±SDは67.5±5.5歳であった。NINCDS−ADRDA判断基準(McKhann et al., 1984)に従って排除を行うことにより可能性のあるADの診断を行った。痴呆の進展、および/または大規模な梗塞および/または多発性裂口のCT所見、および/または重症の血管性疾患の臨床的所見、例えば、合併症を伴う動脈高血圧または糖尿病に関連した一時的な虚血発作および/または卒中エピソードを有する患者においてVADを診断した。対照群は精神病または神経学的疾患、悪性疾患、または全身性疾患(例えば、リューマチ性関節炎、感染性疾患)の病歴、症状または徴候のない個体からなっていた。60歳以上の個体において、Multi-Mental state examination (Folstein et al., 1975)を用いて認識状態を試験した。28点以下のスコアを有する患者は参加させなかった。University of Goeteberg(Goeteberg, Swedec)のEthic Committeeにより当該研究は承認された。患者(または彼らに最も近い親類)および対照群の個体は研究に参加するためのインフォームドコンセントを受けた。
手順はDavidsson et al., 1996に詳述されている。簡単に説明すると、5〜10mlのCSFをBlue Sepharoseカラム(Pharmacia, Uppsala, Sweden)に供してアルブミンを選択的に除去した。次いで、アルブミン不含フラクションを、Sepharose 4B(Pharmacia, Uppsala, Sweden)に共有結合したスタフィロコッカス蛋白Gのカラムに供してIgGを吸着させた。mRPC C2/C18カラム(内径2.1x100mm、ゲル体積0.35ml、粒子サイズ3mm)を装備したSMARTシステム(Pharmacia LKB technology)を用いるmR−HPLCにより未吸着蛋白を分離した。2回のトリフルオロ酢酸のグラジエントにより蛋白を溶離した。全部で40個のフラクションをSavant Speed Vac Concentratorで乾燥させた。フラクションをSDS−PAGE試料緩衝液に溶解し、超音波処理し、15分煮沸して、12%ポリアクリルアミドゲルで分離した。
サンドイッチELISAを用いることにより、CSF−Rab3a、CSF−SNAP25、CSF−タウおよびCSF−β−アミロイド(1−42)を32人のAD患者、20人のVAD患者および11人の対照のCSF試料中で測定した。すべてのマーカーの平均レベルを表4にまとめる。個体のタウおよびRab3a値を図7に示す。
AD患者に関する最高感度および対照患者に関する最高特異性により決定されたカットオフ値に基づいて、確度比を決定した(表5)。Rab3aレベルとSNAP25レベルとが相関関係を有しているので、Rab3aまたはSNAP25のいずれかをタウおよびβ−アミロイドと組み合わせるだけでよい(図8)。かくして、Rab3aとSNAP25の組み合わせに関する確度比を調べなかった。個々のマーカー1つだけあるいは2つだけの組み合わせに関する確度比と比較した場合の、3つの神経学的マーカーの組み合わせ、タウ−β−アミロイド(1−42)−Rab3aならびにタウ−β−アミロイド(1−42)−SNAP25の増加した確度比は、これらの3つのマーカーの組み合わせによりアルツハイマー病のより特異的かつ感度の良い検出が可能になることを示す。
依存的変数、因子としての性別、共分散としての年齢および最小精神的スコア(MMSE; Folstein et al., 1975)のようなすべてのマーカーを有する、十分に階乗的な変数の多数分析(ANOVA)は、異なる群において、これらのパラメーターが共分散しないことを示した。さらに、タウ、β−アミロイド(1−42)およびRab3a/SNAP25の間の有為な相関関係は、各群においても、全群を一緒にしても検出できなかった。
Rab3aおよびSNAP25に対するさらなる抗体を単離する。CSF−Rab3a、CSF−SNAP25、CSF−タウおよびCSF−β−アミロイド(1−42)のレベルを、許容される試料のサイズにより統計学的に有意な比較が可能な十分に定義された臨床診断群において研究する。
5.1 患者および対照患者
1996年8月から1998年9月までの間、the Pediatric Hemato-oncology Department of the Catholic University of Leuven, Belgiumにおいて癌の治療を受けた83人の小児から448のCSF試料を得た。すべての患者は診断時点において完全に臨床的評価を受けていた。親のインフォームドコンセントが得られた。
悪性疾患の分類および治療のために、計画された腰椎せん刺(LP)のコースに試料を供した。血液学的悪性疾患を有する患者の異なる群を本研究に参加させた(表6)。第1群は、United Kingdom Children Cancers group (UKCCSG 9602) NHL protocolに従って治療された9人のB細胞非ホジキンリンパ腫患者(B−NHL)からなっていた(表7a)。この群において、4人の患者がB細胞リンパ腫を有し、3人の患者がBurkittリンパ腫を、2人の患者が未分化ラージ細胞リンパ腫(ALCL)を有していた。これらの患者のうち8人は長期にわたり研究された。第2および最後の群は、'European Organization for Research and Treatment of Cancer' (EORTC) protocol 58881に従って治療された非B細胞急性リンパ芽球白血病/非ホジキンリンパ腫(NB ALL/NHL)の42人の患者からなっていた(表7b)。この第2群において、18人の小児はCD10(+)ブラストまたは通常のNB ALLを有し、2人の患者はダウン症候群(DS)を有し、1人の患者はBrachmann-de Lange症候群を有し、3人の患者は通常のB細胞ブラストを有し、1人の患者はT細胞ブラストを有し、2人の患者はプロB細胞ブラストを有し、9人の患者はプレB細胞ブラストを有し、8人の患者はT細胞ブラストを有していた。38人の小児が白血病を有し、5人の患者が非ホジキンリンパ腫段階II(1人)、段階III(3人)または段階(IV)(1人)であり、それらのうち1人の患者は、CSF中の悪性細胞に関する研究プロトコル、眼底検査およびコントラストカプテーション(contrast captation)により定義された明らかなCNSの疾病(CNS+)を有していた。5人の患者は、治療プロトコルにおいて定義された判断基準によれば非常に危険性の高い(VHR)患者であった(2人の患者はT細胞ブラスト、3人の患者はコルチコイド耐性)。この群中の患者のうち27人は長期にわたり追跡できた。第3の患者群は急性骨髄性白血病(AML)の6人の小児からなっており、そのうち1人の患者はCNSの疾病を有し、2人の患者はダウン症候群であった。M0表現型を有する3人の患者、およびM1、M2またはM7表現型が1人ずついた。これらすべての患者はEORTC 58921プロトコルにより治療され、長期にわたり追跡された。他の患者は異種の小児群(n=18)からなり、治療前後の感染の診断および段階分けのために臨床的理由により腰椎せん刺を行った。この群は5人の髄芽細胞腫の小児(3人が段階分け中、1人が治療中、1人がフォローアップ中)、3人のホジキン病の小児(段階分け中)、3人の横紋筋肉腫(2人が段階分け中、1人が治療中)、2人の脊髄形成異常(MDS)の小児(段階分け中)、2人のランゲルハンス細胞組織球炎(LCH/HLH、段階分け中)、1人の若年性慢性骨髄性白血病(CML)の小児(治療中)、絨毛癌(フォローアップ中)の小児、または胚細胞腫(段階分け中)の小児であった。健康な新生児の大きな群は利用できなかった。なぜなら、これらの患者から脳脊髄液を採取することは倫理に反するからである。対照として、髄膜炎を有する疑いがあるが陰性である小児(n=4)、局所的網膜芽細胞腫(n=1)の小児および家族性ヘモファゴサイティックリンパ組織炎球増多症(n=1)の小児を参加させた。親のインフォームドコンセンサスが得られた。
見込のある、かつ長期の単一中心研究計画を用いた。研究に入る前に患者は治療を受けなかった。今回の調査研究において、58人の小児から得たCSF試料を治療前に利用した(診断的腰椎せん刺またはLP1)(さらなる詳細は表7参照)。大部分の患者に関してすべての時点において残りの試料が利用できなかった。失われた値は小児の疾病の状態によるのではなく、サンプリングまたは試料の保存の間の人為的要因によるものであった。
診断ワークアップのためのベースラインまたは化学療法のIT投与直前のいずれかにおいて、ルーチンな分析のために腰椎せん刺を行った。別々のポリプロピレンチューブに5mlのCSFを集めた。1の試料を即座に1500rpmで2分間遠心分離して細胞および他の不溶性物質を除去した。引き続いて行う分析のために上清を−70℃で保存した。凍結/融解サイクルの数を最小限とした。ルーチンなCSF測定は、細胞学的項目、蛋白濃度、グルコース等を包含した。
診断群にかかわらずすべての神経学的マーカーのデータに関する正規化が拒否されたので、非パラメトリック統計を分析に使用した。Kruskal-Wallis検定を用いて、エフェクト変数(タウ、ニューロモジュリン、蛋白等)に関する群の差異を調べた。Wilcoxonサインドランクス検定、マッチド−ペアー(Wilcoxon signed ranks test, matched-pairs)を用いて、最初の診断LPとその後のLPとの間の相違をチェックした。Prismソフトウェアv2.01(Graphpad Software Inc., San Diego, CA, USA)、Systatバージョン7(SPSS, Chicago, IL, USA)を用いて分析を行った。
治療前の神経学的マーカーのレベル
まず、感染性疾患(しかしながら、ウイルスおよび細菌培養陰性)(n=4)の小児から得たCSF試料に関してタウの正常な上限を調べた。1人の患者は非常に局部的な網膜芽細胞腫を有し、1人の小児は家族性HLHに関してスクリーニングされた者であった。対照小児における平均タウ値は106.2pg/ml(95% CI=34.3〜178.0)であった。任意のカットオフ正常値は312pg/ml(平均+3SD)であり、それは成人において観察される値の範囲内である。正常成人対照の80%が352pg/ml未満のタウ値を有するが、425pg/ml(p25−p75:274−713,n=150)がアルツハイマー病患者のメジアンタウレベルである(Hulstaert et al.,1999)。まず、患者数に関係なく試料を分析し、その後、1の患者から得たすべての試料を1のイムノプレート上でさらに分析した。104個の試料のセットに関する第1のアプローチと第2のアプローチとの間の相関係数は0.901(95% CI:0.856−0.933)であった。
診断時のタウレベルを患者の各サブグループに関して分析した(図9)。診断時のタウレベルは66から1500pg/mlの範囲であった。タウ、ニューロモジュリン、β−アミロイド(1−42)、β−アミロイド(1−40)、血清LDHおよびCSF白血球カウントに関するデータ(図10)は、ダウン症候群を有するまたは有しない患者群において、あるいは診断群間において、明らかな相違を示さない。さらに、タウレベルとWBCまたはLDHレベルとの間にも相関関係が見出されなかった。タウ濃度と小児の年齢との間にも有意な相関関係が見出されなかった。2人のMDS患者、明らかなCNS侵襲(CNS+)であるがAMLでない小児は、診断時においてタウレベルが著しく上昇していた。また、後方窩における髄芽細胞腫のために頭蓋内圧が上昇して入院した3人の患者から、段階分けのためにCSFを取ったところ、非常に高いCSF−タウ濃度であった(823、1397、1500)。しかしながら、非B ALL/NHLを有する21人中7人の小児、非常に高い危険性を有する非B ALL/NHL患者4人のうち1人、AMLの患者4人のうち2人、およびB細胞NHLの患者8人のうち2人が312pg/ml以上のタウレベルを有していたが、古典的な診断手順を用いるとCNS侵襲は検出されなかった。
非B ALL/NHLを有する27人の患者あるいはB細胞 NHLを有する9人の患者に関しては(データ示さず)、白血球カウント(p=0.935,n=40)または血清LDH(p=0.855,n=39)によって反映されるように、診断時のタウレベルは腫瘍負荷と相関関係がなかった。LP1において、タウとニューロモジュリンとの間の非常に有意な相関関係が存在し[r=0.793;95% CI:0.658−0.928,n=50]、両方の蛋白の分泌がある程度相互関係があることが示された。タウとβ−アミロイド(1−42)との間には相関関係が見られなかった(p=0.1032,n=52)。
化学療法により誘導されたCSF中のタウの増加に関する最も明確な相違がB細胞NHL患者において検出された。ベースライン試料および9日目のLP(=LP2)におけるフォローアップ試料の両方が利用可能であった3人の患者に関する結果を図11aに示す。9日目、すなわちIV MTXおよびビンクリスチンとともにMTXおよびヒドロコルチゾンをIT投与した後には、すでに最大タウ増加が測定可能であった。タウのさらなる増加はその後測定されなかった。ニューロモジュリン(図11b)およびニューロン特異的エノラーゼ(図11c)に関する同様の知見によっても、化学療法により誘導された神経代謝活性に対する効果が確認された。さらに、タウとニューロモジュリンとの間(r=0.722, 95% CI: 0.553-0.834, n=49)あるいはニューロモジュリンとニューロン特異的エノラーゼとの間(r=0.622, 95% CI: 0.247-0.835, n=20)に明確な相関関係があった。
全治療期間にわたるデータ(前後試料)が、EORTCプロトコル58881により治療を受けた13人の非B細胞ALL患者に関して利用可能であった。個々の患者について、異なるフェーズまたは治療に関するメジアンタウ値を図12aに示す。治療前(LP1)と比較して(p=0.048)、あるいはメンテナンス期間と比較して(p=0.040)、誘導期間中にタウレベルが有意に増加した。1人の患者は治療開始前からすでにタウレベルが上昇しており(893pg/ml)、おそらく神経学的機能不全がすでに開始していたことを反映するものであろう。また、治療前と誘導期間との間のニューロモジュリンレベルの増加傾向もあった(図12b)。治療開始時に高いタウレベルが存在した患者もまた、化学療法開始時において高いニューロモジュリンレベルを示した。LP1およびLP2に関するNSEのデータが利用可能であった2人の患者において[LP1 (4.0 ng/ml, 3.4 ng/ml); LP2 (11.7 ng/ml, 9.6 ng/ml)]、NSEの明確な増加が観察された。
非B細胞ALL患者からのすべてのデータの分析により、誘導期間において最高タウ濃度が見られることが明らかとなった。誘導期間中、分析した試料の41%(28/68)が500pg/mlよりも高かった。その後、インターバル期間においてこのパーセンテージは18.9%(14/74)まで低下し、再誘導期間中に16.7%(3/18)となり、最後に、メンテナンス期間中に9.7%(7/72)となった(図13a)。治療開始前にすでに上昇したタウ(>500pg/ml)を有していた3人の患者におけるタウ値は化学療法後に正常化した。β−アミロイド(1−42)、非B ALL患者におけるニューロモジュリンおよびNSEレベルに関するデータを図13b、図13cおよび図13dにそれぞれ示す。ここでもやはりタウとニューロモジュリン(r=0.658, 95% CI = 0.580-0.725,n=251)またはNSE(r=0.589, 95% CI = 0.363-0.749, n=47)との間に明確な相関関係があった。
非常に高い危険性を有する5人の非B ALL小児を、本研究において長期にわたり試験した。最初の治療フェーズはEORTC 58881と同様であった。同様の化学療法により誘導されたタウレベルの変化が5人中4人の患者において観察され、タウとニューロモジュリンとの間の高く有意な相関関係も観察された(n=55; r=0.880, 95% CI: 0.802-0.929)。
1人のダウン症候群−非B ALL患者は診断時に70pg/mlのタウ濃度を有していた。すべての非B ALL患者における平均タウ増加は、長期研究の8日目で250%(95% CI = 130%-370%, n=13)、21日目で200%(95% CI = 150%-260%, n=8)であったが、ダウン症候群患者のタウ増加パーセンテージは8日目および21日目においてそれぞれ820%および1200%であった。
高い白血球負荷(610000WBC/mm3)のため、1人の特別な患者を、1日目にIT MTXを使用せずにプレドニソロンで8日間治療した。治療8日後にタウレベルは低いまま、すなわち155pg/mlであった。その後、この患者は他の非B ALL患者と同様にEORTCプロトコル(次の週からMTXをIT注射することを含む)に入った。タウレベルは急激に増加し、12、15、18、22および44日目にはそれぞれ744、948、1120、861および1023pg/mlとなった。別のセンターで治療を受け、MTXでの治療後に明らかな神経毒性に苦しんでおり、しかも両側麻痺であった小児から1のCSF試料が利用可能であった。この小児のタウおよびミューロモジュリンのレベルは使用した最高標準値(タウについて1500pg/ml、ニューロモジュリンについて8000pg/ml)を超え、大規模な神経変性を反映していた。
図14aは、AMLを有する個々の患者におけるタウの消長を示す。患者11、12および23は治療期間中有意なタウの増加を示さなかった(表7c)。1日目および8日目にLPを取った患者12は激しい疾病を有しており、骨髄移植後間もなく死亡した。ダウン症候群の2人の患者のうち1人から、長期にわたるデータが利用可能であり、この患者は300pg/mlをわずかに上回るタウレベルを有しており、患者11および23のCSF中のタウレベルの消長とは対照的であった。診断時にCNS侵襲の証拠があった患者69はCSF中のタウおよびニューロモジュリンの劇的な増加を示した(図14b)。この小児はまだ治療中であり、現在完全に軽快している。
我々は、長期の研究において、体液中のタウ、ニューロモジュリンおよびNSEレベルの有意な増加を見出し、それは化学療法に関連した神経のダメージを反映している可能性が最も高く、主にIV コルチコステロイドおよび化学療法剤と組み合わせてIT MTXを投与した場合に誘導されたが、インターバル治療期間中の高用量のIVおよびIT MTX投与期間中には誘導されなかった。
周産期仮死は神経損傷に関連している可能性がある。電脳図および神経放射線学的データに加えて、CSF神経学的マーカーは低酸素−虚血イベントを評価する際の臨床データを補完しうるものである(Garcia-Alix, 1994)。変化した脳の代謝活性はCSF中の成分の変化を反映するものであるという証拠が増えつつある。CSFマーカーの周産期レベルおよび仮死による変化の分布を評価する。
7.1 患者および対照患者
109の個体からCSFを得た。個体を4群に分けた:(i)痴呆に関する神経学的対照と定義される群(n=70)。この群は、多発性硬化症、Guillan-Barre症候群、多発性ニューロパシーおよびてんかんの患者を含んでいた。他の群は、(ii)記憶障害の老人患者(n=7)、(iii)アルツハイマー病(AD)患者(n=27)、および(iv)血管性痴呆(VAD)の患者(n=5)からなっていた。International Classification of Diseases, version 9 (Manual of the international statistical classification of diseases, injuries, and causes of death: based on recommendations of the Ninth Revision Conference; 1975, and adopted by the Twenty-Ninth World Health Assembly. Geneva: World Health Organization, 1977)により決定された判断基準に従ってすべての患者を診断した。AD群において、2人の患者は1の家族からの者であり、プレセニリン変異により疾病の早期発症がわかっている。これらの患者のうち1人は徴候前であった。
神経学的試験の一環としてCSFをルーチンに採取した。CSFの残りについてすべての試験を行った。ポリプロピレンチューブ中に正しく保存され、1回だけ凍結されたCSF試料においてのみβ−アミロイド(1−42)を測定した。
これらの患者のCSF中のタウ、β−アミロイド(1−42)およびニューロモジュリン(GAP−43)を調べた。各群の平均CSFレベルを表8に示す。β−アミロイド(1−42)、タウおよびニューロモジュリンの個人レベルを図15a、15bおよび15cにそれぞれ示す。
AD患者においてCSF−タウおよびCSF−β−アミロイド(1−42)が有意に変化していた。また、ADにおいてCSF−ニューロモジュリンが有意に増加していた。対照的に、老人性記憶障害患者においてはCSF−ニューロモジュリンにおける有意な影響は観察されなかったが、対照患者と比較してCSF−タウレベルが有意に増加していた。7人の記憶障害患者のうち3人が対照群により決定された最大レベル(280pg/ml)よりも高いCSF−タウレベルを有していた。正しくない保存のため、CSF−β−アミロイド(1−42)レベルは3人の記憶障害の患者においてしか調べることができなかった。3人の患者のうち2人において、300pg/ml未満のレベルがみられた。これらの患者のうち1人は上昇したCSF−タウレベルも有していた。他の患者は278pg/mlのCSF−タウレベルを有しており、すなわち、対照群により決定された最大レベルよりもわずかに低かった。徴候前の家族性AD患者において、327pg/mlのCSF−タウレベルにまで増加しており、β−アミロイド(1−42)レベルは300pg/ml未満であった。少ない記憶障害個体の試料についてのこの分析は、タウ、β−アミロイド(1−42)およびニューロモジュリンの組み合わせ使用はアルツハイマー病の存在に関するより良いインジケーターであることを示す。統計学的に有意であるように、1群あたりより多数の試料を分析中である(1の診断群あたり少なくとも50の試料)。
8.1 患者および対照患者
60人のアルツハーマー病患者、23人のパーキンソン病患者および年齢の合った32人の対照患者からCSFを得た。これらの患者のCSF中のタウ、β−アミロイド(1−42)およびニューロモジュリン(GAP−43)を調べた。各群の平均CSFレベルを表9に示す。
対照と比較すると、AD患者においてタウが有意に増加していたが、β−アミロイド(1−42)レベルが減少していた。NMレベルは両群間で有意には異ならなかった。しかしながら、NMとタウのレベルは有意に相関関係があった(図16)。図16は、AD患者に関する値が対照患者に関する値とは異なる可能性を示す。後退判別分析(backward discriminant analysis)(Marrisonら,1976年)を用いて、タウ、β−アミロイド(1−42)、ニューロモジュリンまたはタウ/ニューロモジュリンのいすれの変数が最も良くアルツハイマー病患者を対照患者から識別するものであるかを調べた。変数タウ/ニューロモジュリンおよびβ−アミロイド(1−42)を選択し、アルツハイマー患者58人中55人(感度94.8%、CI 85.6%〜98.9%)および対照患者31人中30人(特異性96.8%、CI 83.3%〜99.9%)を正しく分類した(図17)。より多くの試料をさらに分析すれば、これら3つのマーカーを用いることによるアルツハイマー病の診断の統計学的に有意な改善が可能になるであろう。
後退判別分析(Morrison, 1976)を用いて、いずれの変数がパーキンソン病患者と対照患者とを最適に識別するものであるかを調べた。変数タウ/ニューロモジュリンおよびβ−アミロイド(1−42)を選択した。パーキンソン病患者23人中14人が正しく分類され(感度60.9%、CI 38.6%〜80.3%)、対照患者31人中27人が正しく分類された(特異性87.1%、CI 70.2%〜96.4%)(図17)。より多くの試料をさらに分析すれば、これら3つのマーカーを用いることによるパーキンソン病の診断の統計学的に有意な改善が可能になるであろう。
β−アミロイド(1−42)およびニューロモジュリンを選択して、アルツハイマー病患者をパーキンソン病患者から分別し、アルツハイマー病患者について感度94.8%(CI 85.6〜98.9%)、パーキンソン病患者について特異性78.3%(CI 56.3%〜92.5%)であった。より多くの試料をさらに分析すれば、これら3つのマーカーを用いることによるアルツハイマー病とパーキンソン病の分別の統計学的に有意な改善が可能になるであろう。
9.1 患者および対照患者
30〜40人のアルツハイマー患者、10〜20人のレービー小体痴呆患者および10〜20人の年齢の合った対照からCSFを得る。
患者群および対照群からのCSF中のα−シヌクレイン濃度を定量する。レービー小体痴呆群のα−シヌクレインレベルに関する値の平均値とアルツハイマー病群のα−シヌクレインレベルに関する値の平均値との有意な相違により、両方のタイプの痴呆を分別することが可能である。α−シヌクレインの定量と少なくとも2種の他の神経学的マーカー(タウおよびβ−アミロイド(1−42)のごとき)の定量を組み合わせることにより、アルツハイマー病とレービー小体痴呆との分別がさらに改善される。
10.1 患者および対照患者
30〜40人の前頭側頭葉痴呆患者および10〜20人の年齢の合った対照からCSFを得る。
前頭側頭葉痴呆患者および対照患者のCSF中のβ−アミロイド(1−42)、タウおよびホスホ−タウのレベルを定量する。対照患者のタウおよびホスホ−タウのレベルの平均値と比較した場合、前頭側頭葉痴呆患者のタウおよびホスホ−タウのレベルの平均値が有意に増加している。前頭側頭葉痴呆患者は、対照患者と比較すると、β−アミロイド(1−42)のレベル低下を示す。
11.1 患者および対照患者
アルツハイマー病の血管性疾患の患者30〜40人、他の形態のアルツハイマー病患者30〜40人および年齢の合った対照10〜20人からCSFおよび血漿を得る。
血管性疾患の患者、他の形態のアルツハイマー病の患者、ならびに対照患者のCSF中のタウおよびβ−アミロイド(1−42)のレベルならびに血漿中のβ−アミロイド(1−42)のレベルを定量する。血漿−β−アミロイド(1−42)、CSF−タウおよびCSF−β−アミロイド(1−42)の定量的に異なったレベルは、血管性疾患の患者と他の形態のアルツハイマー病の患者との分別を可能にする。
Abbruzzese M, Ferri S, Scarone S (1997) Neuropsychologia 35: 907-912.
Asami-Odaka A, Ishibashi Y, Kikuchi T (1995) Biochemistry 34: 10272-10278.
Auld DS, Kar S, Quirion R (1998) Trends Neurosci 21: 43-49.
Andreadis A, Brown W, Kosik K (1992) Biochem 31: 10626-10633.
Bachmann BJ (1987) In: E. coli and S. typhimurium, Cellular and molecular biology. Ed. Neidhardt FC et al., ASM 1190-1219.
Ballard C, Grace J, McKeith I, Holmes C (1998) Lancet 351: 1032-1033.
Basi GS (1987) Cell 49: 785-791.
Benowitz LI, Perrone-Bizzozero NI, Finklestein SP, Bird ED (1989) J Neurosci 9: 990-995.
Blennow K, Davidson P, Wallin A, Ekman R (1995) Dementia 6: 306-311.
Blennow K, Bogdanovic N, Alafuzoff I, Ekman R, Davidson P (1996) J Neural Transm 103: 603-618.
Bonhard C et al (1984) In: Immunolabeling for Electron Microscopy. Eds. Polak JM, Varndell JM. Elsevier Scientific Publishers, Amsterdam, p. 95.
Bramblett G, Trojanowski J, Lee V (1992) Lab Invest 66: 212-222.
Bramblett G, Goedert M, Jakes R, Merrick S, Trojanowski J, Lee V (1993) Neuron 10: 1089-1099.
Brion J, Passareiro J, Nunez J and Flament-Durand J (1985) Arch Biol 95: 229-235.
Brun A (1993) Dementia 4: 126-131.
Citron M, Diehl TS, Gordon G, Biere AL, Seubert P, Selkoe DJ (1996) Proc Natl Acad Sci 93: 13170-13175.
Citron M, Westaway D, Xia W, Carlson G, Diehl T, Levesque G, Johnson-Wood K, Lee M, Suebert P, Davis A, Kholodenko D, Motter R, Sherrington R, Perry B, Yao H, Strome R, Lieberburg I, Rommens J, Kim S, Schenk D, Fraser P, StGeorge Hyslop P, Selkoe DJ (1997) Nature Medicine 3: 67-72.
Coleman PD, Kazee AM, Lapham L, Eskin T, Rogers K (1992) Neurobiol aging 13: 631-639.
Davidsson P, Jahn R, Bergquist J, Ekman R, Blennow K (1996) Mol Chem Neuropathol 27: 195-210.
Delacourte A, Defossez A (1986) J. Neurol. Sci. 76: 173-180.
Delacourte A, Flament S, Dibe E, Hublau P, Sablonniere B, Hemon B, Sherrer V, Defossez A (1990) Acta Neuropathol 80: 111-117.
Ferrer I, Marti E, Tortosa A, Blasi J (1998) J Neuropathol Exp Neurol 57: 218-225.
Flament S, Delacourte A, Mann D (1990) Brain Res 516: 15-19.
Fletcher JM, Copeland DR (1988) J Clin Exp neuropsychol 10: 495-537.
Folstein M, Folstein S, McHugh P.(1975) J Psychol Res 12: 189-198.
Friedland RP, Majocha RE, Reno JM, Lyle LR, Marotta CA (1994) Mol Neurobiol 9: 107-113.
Ghanbari H, Kozuk T, Miller B, Riesing S (1990) J Clin Laboratory Anal 4: 189-192.
Garcia-Alix A, Cabanas F, Pellicer A, Hernanz A, Stiris TA, Quero J (1994) Pediatrics 93: 234-240.
Goedert M, Spillantini M, Jakes R, Rutherford D, Crowther R (1989) Neuron 3: 519-526.4055.
Goedert M, Cohen E, Jakes R, Cohen P (1992) FEBS Lett. 312: 95-99.
Goedert M, Jakes R, Crowther R, Six J, Lubke U, Vandermeeren M, Cras P, Trojanowski JQ, Lee V (1993) Proc Natl Acad Sci (USA) 90: 5066-5070.
Goedert M, Jakes R, Crowther RA, Cohen P, Vanmechelen E, Vandermeeren M, Cras P (1994) Biochem J 301: 871-877.
Greenberg S, Davies P (1990) Proc Natl Acad Sci USA 87: 5827-5831.
Grundke-Iqbal I, Iqbal K, Quinlan M, Tung Y, Zaidi M, Wisniewski H (1986) J Biol Chem 261: 6084-6089.
Harrington C, Mukaetova E, Hills R, Edwards P, Montejo de Garcini E, Novak M, Wischik C (1991) Proc Natl Acad Sci (USA) 88: 5842-5846.
Hasegawa M, Morishima-Kawashima M, Takio K, Suzuki M, Titani K, Ihara Y (1992) J Biol Chem 267: 17047-17054.
Himmler A (1989) Mol Cell Biol 9: 1389-1396.
Hooten WM, Lyketsos CG (1998) Dement Geriatr Cogn Disord 9: 164-174.
Hulstaert F, Blennow K, Ivanoiu A, Schoonderwaldt HC, Riemenschneider M, De Deyn PP, Bancher C, Cras P, Wiltfang J, Mehta PD, Iqbal K, Pottel H, Vanmechelen E, Vanderstichele H (1999) Neurology 52: 1555-1562.
Hochuli E (1988) J Chromatogr 444: 293-302.
Iqbal K, Grundke-Iqbal I, Smith A, George L, Tung Y, Zaidi T (1989) Proc Natl Acad Sci (USA) 86: 5646-5650.
Jannoun L 1983 Arch Dis Child 58: 953-958.
Jensen PH, Nielsen MS, Jahes R, Dotti CG, Goedert M (1998) J Biol Chem 273: 26292-26294.
Johnson-Wood K, Lee M, Motter R, Hu K, Gordon G, Barbour R, Khan K, Gordon M, Tan H, Games D, Lieberburg I, Schenk D, Seubert P, McConlogue L (1997) Proc Natl Acad Sci 94: 1550-1555.
Kaiser E, Kuzmits R, Pregant P, Burghuber O, Worofka W (1989) Clin Chim Acta 183: 13-32.
Kato K, Suzuki F, Umeda Y (1981) J Neurochem 36: 793-797.
Kim KS, Wen GW, Bancher C, Chen CMJ, Sapienza HH, Hong H, Wisniewski HM (1990) Neurosci Res Comm 7: 113-122.
Knopman DS (1993) Dementia 4: 132-136.
Kondo J, Honda T, Mori H, Hamada Y, Miura R, Ogawara M, Ihara Y (1988) Neuron 1: 82.
Kohler G, Milstein C (1975 Nature 256: 495-497.
Konig G, Graham P, Bushnell A, Webster S, Wunderlich D, Perlmutter LS (1996) Ann NY Acad Sci 777: 344-355.
Kosik K, Joachim C, Selkoe (1986) Proc Natl Acad Sci (USA) 83: 4044-4048.
Ksiezak-Reding H, Liu WK, Yen SH (1992) Brain Res 597: 209-219.
Lannfelt-L, Basun-H, Wahlund-LO, Rowe-BA, Wagner-SL (1995) NatMed 1: 829-832.
Lee V, Balin B, Otvos L, Trojanowski J (1991) Science 251: 675-678.
Levy R, Eagger S, Griffiths M, Perry E, Honavar M, Daen A, Lantos P (1994) Lancet 343: 176-178.
Lewis S, Wang D, Cowan N (1988) Science 242: 936-939.
Majocha RE, Reno JM, Friedland RP, VanHaight C, Lyle LR, Marotta CA (1992) J Nucl Med 33: 2184-2189.
McKeith IG, Galasko D, Kosaka K, Perry EK, Dickson DW, Hansen LA, Salmon DP, Lowe J, Mirra SS, Byrne EJ, Lennox G, Quinn NP, Edwardson JA, Ince PG, Bergeron C, Burns A, Miller BL, Lovestone S, Collerton D, Jansen EN, Ballard C, de Vos RA, Wilcock GK, Jellinger KA, Perry RH (1996) Neurology 47: 1113-1124.
McKhann G, Drachman D, Folstein M, Katzman R, Price D, Stadlan EM (1984) Neurology 34: 939-944.
Mercken M, Lubke U, Vandermeeren M, Gheuens J, Oestreicher AB (1992a) J Neurobiol 23: 309-321.
Mercken M, Vandermeeren M, Lubke U, Six J, Boons J, Vanmechelen E, Van De Voorde A, Gheuens J (1992b) J Neurochem 58: 548-553.
Moore I, Kramer JH, Ablin A (1986) Oncol Nurs Forum 12: 45-51.
Morrison DF (1976) Multivariate statistical methods. McGraw-Hill, New York, NY, USA.
Motter R, Vigo-Pelfrey C, Kholodenko D, Barbour R, Johnson-Wood K, Galasko D, Chang L, Miller B, Clark C, Green R, Olson D, Southwick P, Wolfert R, Munroe B, Lieberburg I, Seubert P, Schenk D (1995) Ann Neurol 38: 643-648.
Nara T, Nozaki H, Nakae Y, Arai T, Ohashi T (1988) AJDC 142: 173-174.
Ochs J, Mulhern R, Fairclough D, Parvey L, Whitaker J, Ch'ien L, Mauer A, Simone J (1991) J Clin Oncol 9: 145-151.
Oestreicher AB, Hens JJH, Marquart A (1994) J Neurochem. 62: 881-889.
Perry EK, Haroutunian V, Davis KL, Levy R, Lantos P, Eagger S, Honavar M, Dean A, Griffiths M, McKeith IG, et al (1994) Neuroreport 5: 747-749.
Schoonjans F, Zalata A, Depuydt CE, Comhaire FH (1995) Comput Methods Programs Biomed 48: 257-62.
Selden S, Pollard T (1983) J Biol Chem 258(11): 7064-7071.
Shimohama S, Kamiya S, Taniguchi T, Akagawa K, Kimura J (1997) Biochem Biophys Res Comm 236: 239-242.
Skene JH, Willard M (1981) J Neurosci 1: 419-26.
Six J, Lubke U, Lenders M-B, Vandermeeren M, Mercken M, Villanova M, Van de Voorde A, Gheuens J, Martin J-J, Cras P (1992) Neurodegeneration, impairment of neuronal function 1: 247-255.
Sjogren M, Edman A, Wallin A (1997) Psychiatry 12: 656-661.
Soji M, Matsubara E, Kanai M, Watanabe M, Nakamura T, Tomidokoro Y, Shizuka M, Wakabayashi K, Igeta Y, Ikeda Y, Mizushima K, Amari M, Ishiguro K, Kawarabayashi T, Harigaya Y, Okamotot K, Hirai S (1998) J Neurol Sci 158: 134-140.
Stern RA, Trojanowski J,; Lee VM (1990) FEBS-Lett. 264: 43-7.
Suzuki N, Cheung TT, Cai X-D, Odaka A, Otvos L, Eckman C, Golde TE, Younkin SG (1994) Science 264: 1336-1340.
Terry RD, Masliah E, Salmon DP, Butters N, DeTeresa R, Hill R, Hansen LA, Katzman R (1991) Ann Neurol 30: 572-580.
Vandermeeren M, Mercken M, Vanmechelen E, Six J, Van de Voorde A, Martin J, Cras P (1993) J Neurochem 61: 1828-1834.
Van de Voorde A, Vanmechelen E, Vandermeeren M, Dessaint F, Beeckman W, Cras P (1995) Detection of tau in cerebrospinal fluid. Research Advances in Alzheimer's disaese and related disorders, Ed. Ibqal, Mortimer, Winblad & Wisniewski, John Wiley & Sons Ltd.
Van Gelder P, Bosman F, de Meuter F, van Heuverswyn H, Herion P (1993) J Clin Microbiol 31: 9-15.
Vanmechelen E, Blennow K, Davidsson P, Cras P, Van De Voorde A (1997) Alzheimer's Disease: biology, diagnosis and therapeutics. Edited by K Iqbal, B Winblad, T Nishimura, M Takeda, HM Wisniewski, John Wiley & Sons, Ltd. pp.197-203.
Wertman KF, Wyman AR, Botstein D (1986) Gene 49: 253-262.
Wilcock GK, Scott MI (1994) Lancet 344: 544-544.
Wilson JD, Braunwald E, Isselbacher KJ, Petersdorf RG, Martin JB, Fauci AS, Root RK (1991) Harrison's Principles of Internal Medicine, 12th Edition, McGraw-Hill Inc, NY, USA.
Wood J, Mirra S, Pollock N, Binder L (1986) Proc Natl Acad Sci (USA) 83: 4040-4043.
Zahraoui A, Touchot N, Chardin P and Tavitian A (1989) J Biol Chem 264: 12394-12401.
Zhao N, Hashida H, Takahashi N and Sakaki Y (1994) Gene 145: 313-314.
Claims (21)
- 個体におけるアルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための方法であって、
該個体からの体液試料中の少なくとも3種の神経学的マーカーのレベルを、該神経学的マーカーを特異的に認識する抗体を用いて決定する工程を含み、
該神経学的マーカーがタウ、β−アミロイド(1−42)、およびシナプス蛋白である、方法。 - 該シナプス蛋白が、Rab3aまたはSNAP25である、請求項1に記載の方法。
- 該体液試料が、脳脊髄液試料である、請求項1または2に記載の方法。
- 請求項1〜3のいずれか1項に記載の方法であって、
−脳脊髄液試料中のタウ、β−アミロイド(1−42)、およびRab3aのレベルを決定する、または
−脳脊髄液試料中のタウ、β−アミロイド(1−42)、およびSNAP25のレベルを決定する、方法。 - アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のためのキットであって、
異なる神経学的マーカーをそれぞれ認識する、少なくとも3種の抗体を含み、
該神経学的マーカーがタウ、β−アミロイド(1−42)、およびシナプス蛋白である、診断キット。 - 該シナプス蛋白が、Rab3aまたはSNAP25である、請求項5に記載の診断キット。
- 該神経学的マーカーが、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、である、請求項5または6に記載の診断キット。 - アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための診断キットであって、
−異なる神経学的マーカーをそれぞれ認識する、少なくとも3種の一次抗体(補足抗体)を一緒にあるいは別個に含む支持体、および
−神経学的マーカー−一次抗体複合体の1つをそれぞれ認識する二次抗体(ディテクター抗体)を含み、
該神経学的マーカーがタウ、β−アミロイド(1−42)、およびシナプス蛋白である、診断キット。 - 該シナプス蛋白が、Rab3aまたはSNAP25である、請求項8に記載の診断キット。
- 該神経学的マーカーが、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、である、請求項8または9に記載の診断キット。 - 該2次抗体に特異的、にタグを付するまたはカップリングするためのマーカーをさらに含む請求項8〜10のいずれか1項に記載の診断キット。
- 一次抗体と体液試料、二次抗体と神経学的マーカー−一次抗体複合体、および/または結合二次抗体とマーカー間の免疫学的反応を行うための適切な緩衝液をさらに含む請求項8〜11のいずれか1項に記載の診断キット。
- 標準化の目的のために、神経学的マーカーの検出に使用されるキットの抗体により特異的に認識される精製蛋白または合成ペプチドをさらに含む、請求項8〜12のいずれか1項に記載の診断キット。
- 請求項1〜4のいずれか1項に記載の方法を行うために特異的に設計された請求項8〜13のいずれか1項に記載の診断キット。
- アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための、タウ、β−アミロイド(1−42)、およびシナプス蛋白を特異的に認識する抗体の使用。
- 該シナプス蛋白が、Rab3aまたはSNAP25である、請求項15に記載の使用。
- 該抗体が、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、を特異的に認識する、請求項15または16に記載の使用。 - アルツハイマー病の特異的検出または定量のため、および/またはアルツハイマー病と他の痴呆との分別検査のための診断キットの製造のための、タウ、β−アミロイド(1−42)、およびシナプス蛋白を特異的に認識する抗体の使用。
- 該シナプス蛋白が、Rab3aまたはSNAP25である、請求項18に記載の使用。
- 該抗体が、
−タウ、β−アミロイド(1−42)、およびRab3a、または
−タウ、β−アミロイド(1−42)、およびSNAP25、を特異的に認識する、請求項18または19に記載の使用。 - 特定の治療の、治療モニタリングおよび/または有効性の決定のための、請求項1〜14のいずれか1項に記載の方法または診断キットの使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP98870148 | 1998-07-03 | ||
| EP98870236 | 1998-11-03 | ||
| EP99870069 | 1999-04-09 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005326503A Division JP2006091025A (ja) | 1998-07-03 | 2005-11-10 | 神経変性の分別診断 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010019864A true JP2010019864A (ja) | 2010-01-28 |
| JP4580455B2 JP4580455B2 (ja) | 2010-11-10 |
Family
ID=27239769
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000558397A Pending JP2002519702A (ja) | 1998-07-03 | 1999-06-29 | 神経変性の分別診断 |
| JP2005326503A Pending JP2006091025A (ja) | 1998-07-03 | 2005-11-10 | 神経変性の分別診断 |
| JP2009247559A Expired - Lifetime JP4580455B2 (ja) | 1998-07-03 | 2009-10-28 | 神経変性の分別診断 |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000558397A Pending JP2002519702A (ja) | 1998-07-03 | 1999-06-29 | 神経変性の分別診断 |
| JP2005326503A Pending JP2006091025A (ja) | 1998-07-03 | 2005-11-10 | 神経変性の分別診断 |
Country Status (11)
| Country | Link |
|---|---|
| EP (1) | EP1095278B1 (ja) |
| JP (3) | JP2002519702A (ja) |
| CN (1) | CN1316055A (ja) |
| AT (1) | ATE312349T1 (ja) |
| AU (1) | AU754062B2 (ja) |
| BR (1) | BR9911291A (ja) |
| CA (1) | CA2329523A1 (ja) |
| DE (1) | DE69928809T2 (ja) |
| DK (1) | DK1095278T3 (ja) |
| ES (1) | ES2255280T3 (ja) |
| WO (1) | WO2000002053A2 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013524220A (ja) * | 2010-04-01 | 2013-06-17 | バンヤン・バイオマーカーズ・インコーポレイテッド | 神経毒性を検出するためのマーカーおよびアッセイ |
| EP3540441A1 (en) | 2014-05-22 | 2019-09-18 | Shimadzu Corporation | Surrogate biomarker for evaluating intracerebral amyloid ss peptide accumulation and method for analysis thereof |
| EP3598137A1 (en) | 2015-09-16 | 2020-01-22 | Shimadzu Corporation | Multiplex biomarker for use in evaluation of state of accumulation of amyloid b in brain, and analysis method for said evaluation |
| US10646555B2 (en) | 2010-01-26 | 2020-05-12 | Bioregency, Inc. | Compositions and methods relating to argininosuccinate synthetase |
| US10942190B2 (en) | 2014-01-21 | 2021-03-09 | Shimadzu Corporation | Measurement method for amyloid precursor protein cleavage peptides |
Families Citing this family (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10041478A1 (de) | 2000-08-24 | 2002-03-14 | Sanol Arznei Schwarz Gmbh | Neue pharmazeutische Zusammensetzung |
| US20040146935A1 (en) * | 2001-03-15 | 2004-07-29 | Roberts Rosalinda Cusido | Disease associated gene |
| CA2468088A1 (en) * | 2001-11-20 | 2003-05-30 | Atgen Co., Ltd. | Novel peptides conferring environmental stress resistance and fusion proteins including said peptides |
| GB0203446D0 (en) * | 2002-02-14 | 2002-04-03 | Univ Lancaster | Detection and/or monitoring of synuclein-related diseases |
| US9034337B2 (en) | 2003-10-31 | 2015-05-19 | Prothena Biosciences Limited | Treatment and delay of outset of synucleinopathic and amyloidogenic disease |
| WO2005001483A2 (en) * | 2003-06-27 | 2005-01-06 | Georg-August-Universität Göttingen Stiftung Öffentlichen Rechts | Methods for diagnisis and differential diagnosis of dementia disorders |
| WO2005047860A2 (en) | 2003-11-08 | 2005-05-26 | Elan Pharmaceuticals, Inc. | Antibodies to alpha-synuclein |
| US20060094064A1 (en) * | 2003-11-19 | 2006-05-04 | Sandip Ray | Methods and compositions for diagnosis, stratification, and monitoring of alzheimer's disease and other neurological disorders in body fluids |
| EP2211183B1 (en) * | 2003-11-19 | 2013-03-06 | Satoris, Inc. | Method for diagnosis and monitoring of Alzheimer's disease |
| DE10361258A1 (de) | 2003-12-24 | 2005-07-28 | Schwarz Pharma Ag | Verwendung von substituierten 2-Aminotetralinen zur vorbeugenden Behandlung von Morbus Parkinson |
| AT500321B1 (de) * | 2003-12-30 | 2006-02-15 | Red Bull Gmbh | Verfahren zur diagnose des down-syndroms |
| DE102004014841B4 (de) | 2004-03-24 | 2006-07-06 | Schwarz Pharma Ag | Verwendung von Rotigotin zur Behandlung und Prävention des Parkinson-Plus-Syndroms |
| US8399241B2 (en) * | 2004-12-01 | 2013-03-19 | Whitehead Institute For Biomedical Research | Modulators of alpha-synuclein toxicity |
| CA2669848A1 (en) * | 2006-11-17 | 2008-05-22 | Friedrich-Alexander-Universitaet Erlangen-Nuernberg | Method of differentially diagnosing dementias |
| PL2583978T3 (pl) * | 2007-02-23 | 2016-07-29 | Prothena Biosciences Ltd Co | Profilaktyka i leczenie chorób synukleinopatycznych i amyloidogennych |
| EP2020602A1 (en) * | 2007-08-02 | 2009-02-04 | Araclon Biotech | High sensitivty immunoassays and kits for the determination of peptides and proteins of biological interest |
| JP2009052933A (ja) * | 2007-08-24 | 2009-03-12 | Rakuno Gakuen | プリオン病の検出方法及び診断キット |
| WO2009039586A2 (en) * | 2007-09-28 | 2009-04-02 | Powmri Limited | Biomarkers for parkinson's disease |
| US8501465B2 (en) | 2007-12-21 | 2013-08-06 | Whitehead Institute For Biomedical Research | Modulators of alpha-synuclein toxicity |
| PT2282758T (pt) * | 2008-04-29 | 2019-02-12 | Bioarctic Ab | Anticorpos e vacinas para uso em métodos terapêuticos e diagnósticos para perturbações relacionadas com a alfa-sinucleína |
| WO2009152607A1 (en) * | 2008-06-16 | 2009-12-23 | Ottawa Hospital Research Institute | Methods and kits for diagnosing neurodegenerative disease |
| WO2011033252A1 (en) * | 2009-09-16 | 2011-03-24 | United Arab Emirates University | Diagnostic agent for parkinson's disease |
| HUE038313T2 (hu) | 2010-02-26 | 2018-10-29 | Bioarctic Neuroscience Ab | Protofibril-kötõ antitestek és alkalmazásuk Parkinson-kór, Lewy-testes demencia és más alfa-szinukleinopátiák terápiás és diagnosztikai eljárásaiban |
| GB201011420D0 (en) | 2010-07-06 | 2010-08-18 | United Arab Emirates Universit | Method for diagnosis |
| RU2441240C1 (ru) * | 2010-10-05 | 2012-01-27 | Государственное образовательное учреждение высшего профессионального образования "Московский государственный медико-стоматологический университет" Министерства здравоохранения и социального развития Российской Федерации | Способ диагностики аксонально-демиелинизирующих полиневропатий |
| UA118441C2 (uk) * | 2012-10-08 | 2019-01-25 | Протена Біосаєнсиз Лімітед | Антитіло, що розпізнає альфа-синуклеїн |
| WO2016038084A1 (en) * | 2014-09-10 | 2016-03-17 | AbbVie Deutschland GmbH & Co. KG | Rgma fragment based diagnostic assay |
| EP3242134A1 (en) * | 2016-05-04 | 2017-11-08 | Euroimmun Medizinische Labordiagnostika AG | Assay for the diagnosis of a neurological disease |
| WO2018094120A1 (en) * | 2016-11-16 | 2018-05-24 | Nanosomix, Inc. | Quantification of subpopulations of exosomes and diagnosis of neurodegenerative disorders |
| US10364286B2 (en) * | 2016-12-22 | 2019-07-30 | H. Lundbeck A/S | Monoclonal anti-alpha-synuclein antibodies for preventing tau aggregation |
| GB201814807D0 (en) * | 2018-09-12 | 2018-10-24 | Univ Newcastle | Dementia Biomarkers |
| EP3660509B1 (en) * | 2018-11-29 | 2022-03-09 | Hugel Inc. | A cell-based method for determining an activity of botulinum toxin |
| GB202005732D0 (en) * | 2020-04-20 | 2020-06-03 | Synpromics Ltd | Regulatory nucleic acid sequences |
| MX2022016005A (es) | 2020-06-26 | 2023-02-02 | Bioarctic Ab | Anticuerpos de fijacion a protofibrillas de \03b1-sinucleina. |
| US20240003918A1 (en) * | 2020-11-30 | 2024-01-04 | Enigma Biointelligence, Inc. | Non-invasive assessment of alzheimer's disease |
-
1999
- 1999-06-29 JP JP2000558397A patent/JP2002519702A/ja active Pending
- 1999-06-29 AT AT99934543T patent/ATE312349T1/de active
- 1999-06-29 DE DE69928809T patent/DE69928809T2/de not_active Expired - Lifetime
- 1999-06-29 AU AU50290/99A patent/AU754062B2/en not_active Ceased
- 1999-06-29 DK DK99934543T patent/DK1095278T3/da active
- 1999-06-29 WO PCT/EP1999/004483 patent/WO2000002053A2/en not_active Ceased
- 1999-06-29 BR BR9911291-4A patent/BR9911291A/pt not_active IP Right Cessation
- 1999-06-29 CA CA002329523A patent/CA2329523A1/en not_active Abandoned
- 1999-06-29 EP EP99934543A patent/EP1095278B1/en not_active Expired - Lifetime
- 1999-06-29 CN CN99810286.5A patent/CN1316055A/zh active Pending
- 1999-06-29 ES ES99934543T patent/ES2255280T3/es not_active Expired - Lifetime
-
2005
- 2005-11-10 JP JP2005326503A patent/JP2006091025A/ja active Pending
-
2009
- 2009-10-28 JP JP2009247559A patent/JP4580455B2/ja not_active Expired - Lifetime
Non-Patent Citations (2)
| Title |
|---|
| JPN5001015740, Journal of the Neurological Sciences, 1998, Vol.158, p134−140 * |
| JPN5001015741, TAKEDA A, AMERICAN JOURNAL OF PATHOLOGY, 19981201, V152 N12, P367−372 * |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10646555B2 (en) | 2010-01-26 | 2020-05-12 | Bioregency, Inc. | Compositions and methods relating to argininosuccinate synthetase |
| JP2013524220A (ja) * | 2010-04-01 | 2013-06-17 | バンヤン・バイオマーカーズ・インコーポレイテッド | 神経毒性を検出するためのマーカーおよびアッセイ |
| US10942190B2 (en) | 2014-01-21 | 2021-03-09 | Shimadzu Corporation | Measurement method for amyloid precursor protein cleavage peptides |
| EP3540441A1 (en) | 2014-05-22 | 2019-09-18 | Shimadzu Corporation | Surrogate biomarker for evaluating intracerebral amyloid ss peptide accumulation and method for analysis thereof |
| EP3540442A1 (en) | 2014-05-22 | 2019-09-18 | Shimadzu Corporation | Surrogate biomarker for evaluating intracerebral amyloid beta peptide accumulation and method for analysis thereof |
| EP3783364A2 (en) | 2014-05-22 | 2021-02-24 | Shimadzu Corporation | Surrogate biomarker for evaluating intracerebral amyloid beta peptide accumulation and method for analysis thereof |
| US11231413B2 (en) | 2014-05-22 | 2022-01-25 | Shimadzu Corporation | Surrogate biomarker for evaluating intracerebral amyloid ß peptide accumulation and method for analysis thereof |
| EP4040157A1 (en) | 2014-05-22 | 2022-08-10 | Shimadzu Corporation | Surrogate biomarker for evaluating intracerebral amyloid beta peptide accumulation and method for analysis thereof |
| EP3598137A1 (en) | 2015-09-16 | 2020-01-22 | Shimadzu Corporation | Multiplex biomarker for use in evaluation of state of accumulation of amyloid b in brain, and analysis method for said evaluation |
| US11268965B2 (en) | 2015-09-16 | 2022-03-08 | Shimadzu Corporation | Multiplex biomarker for use in evaluation of state of accumulation of amyloid B in brain, and analysis method for said evaluation |
| EP4424704A2 (en) | 2015-09-16 | 2024-09-04 | Shimadzu Corporation | Multiplex biomarker for use in evaluation of state of accumulation of amyloid b in brain, and analysis method for said evaluation |
Also Published As
| Publication number | Publication date |
|---|---|
| DE69928809T2 (de) | 2006-08-31 |
| AU5029099A (en) | 2000-01-24 |
| JP2006091025A (ja) | 2006-04-06 |
| DK1095278T3 (da) | 2006-04-18 |
| ES2255280T3 (es) | 2006-06-16 |
| CN1316055A (zh) | 2001-10-03 |
| EP1095278B1 (en) | 2005-12-07 |
| WO2000002053A3 (en) | 2000-02-24 |
| EP1095278A2 (en) | 2001-05-02 |
| JP4580455B2 (ja) | 2010-11-10 |
| AU754062B2 (en) | 2002-10-31 |
| JP2002519702A (ja) | 2002-07-02 |
| BR9911291A (pt) | 2001-12-04 |
| CA2329523A1 (en) | 2000-01-13 |
| DE69928809D1 (de) | 2006-01-12 |
| WO2000002053A2 (en) | 2000-01-13 |
| HK1036834A1 (en) | 2002-01-18 |
| ATE312349T1 (de) | 2005-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4580455B2 (ja) | 神経変性の分別診断 | |
| US20040014142A1 (en) | Differential diagnosis of neurodegeneration | |
| Mori et al. | Tau in cerebrospinal fluids: establishment of the sandwich ELISA with antibody specific to the repeat sequence in tau | |
| AU2007279287B2 (en) | Biomarkers of mild cognitive impairment and Alzheimer's disease | |
| JP2021523357A (ja) | 部位特異的タウリン酸化に基づく診断法及び治療方法 | |
| Liu et al. | An ultra‐sensitive immunoassay detects and quantifies soluble Aβ oligomers in human plasma | |
| Wang et al. | Synaptic vesicle glycoprotein 2 A in serum is an ideal biomarker for early diagnosis of Alzheimer’s disease | |
| JP4624559B2 (ja) | 初期cnsダメージのマーカーとしてのタウ | |
| US20230132508A1 (en) | Uses of Tau Phosphosites as Biomarkers for Alzheimer's Disease | |
| Mehta et al. | Biological markers of Alzheimer's disease | |
| AU2003200041B2 (en) | Differential Diagnosis of Neurodegeneration | |
| HK1036834B (en) | Differential diagnosis of neurodegeneration | |
| US9618522B2 (en) | Diagnostic testing in dementia and methods related thereto | |
| JP4851052B2 (ja) | 神経学的疾患の分別診断 | |
| Mehta | Amyloid beta and tau proteins in Alzheimer’s disease and Down syndrome | |
| Mehta | Amyloid beta and tau proteins in | |
| WO2024108311A1 (en) | Extracellular vesicles for the diagnosis of alzheimer's disease | |
| AU2013205062A1 (en) | Biomarkers of mild cognitive impairment and Alzheimer's disease | |
| Chu et al. | O2-02-04 Increased α7 nicotinic acetylcholine receptor protein levels in Alzheimer's disease patients |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091028 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100413 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100713 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100810 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100827 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130903 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4580455 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |