JP2009185178A - カーボンブラック組成物 - Google Patents
カーボンブラック組成物 Download PDFInfo
- Publication number
- JP2009185178A JP2009185178A JP2008026800A JP2008026800A JP2009185178A JP 2009185178 A JP2009185178 A JP 2009185178A JP 2008026800 A JP2008026800 A JP 2008026800A JP 2008026800 A JP2008026800 A JP 2008026800A JP 2009185178 A JP2009185178 A JP 2009185178A
- Authority
- JP
- Japan
- Prior art keywords
- group
- substituent
- carbon black
- hydrogen atom
- alkyl group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Landscapes
- Compositions Of Macromolecular Compounds (AREA)
- Pigments, Carbon Blacks, Or Wood Stains (AREA)
Abstract
【解決手段】カーボンブラックと結合剤、溶剤および下特定の構造式で表されるベンゾイソインドール誘導体を用いてなることを特徴とするカーボンブラック組成物。
さらに、カーボンブラック100重量部に対し、上記ベンゾイソインドール誘導体を0.1から20重量部含有することを特徴とするカーボンブラック組成物。
【選択図】なし
Description
しかしながら、表面電荷の異なる多様な顔料や添加剤を使用するインキ・塗料工業にあっては、全塗料の表面電荷を制御することが困難なこともあって、十分な分散安定性を得るには、未だ到っていない。
しかしながら、これまでの方法で得られた表面が被覆してなるカーボンブラックは、他の物質との親和性が期待した程には改良されず、必ずしも満足する結果は得られていないのが現状である。
(式中、Yは、直接結合、−O−、−S(O)m−(ここでmは、0から3の整数を表す)、−CO−、−NR14−、−CONR14−、−SO2NR14−、−NR14CO−、−NR14SO2−(ここでR14は、水素原子、アルキル基、またはヒドロキシアルキル基を表す)、炭素数1から12の直鎖または枝分かれしたアルキレン基あるいは、アルキル基、アミノ基、ニトロ基、水酸基、アルコキシ基、またはハロゲン原子で置換されていてもよいベンゼン残基あるいはトリアジン残基、またはこれらの結合基を2個以上組み合わせた結合基を表す。Zはハロゲン原子、置換基を有してもよいアルキル基、置換基を有してもよいアリール基、置換基を有してもよいフタルイミドメチル気、−NR15R16、SO3・M/n、または−COO・M/nを表し、R15とR16はそれぞれ独立に水素原子、置換基を有してもよいアルケニル基、置換基を有してもよいフェニル基、またはR15とR16とで一体となって更なる窒素、酸素または硫黄原子を含んでもよく、置換基を有してもよい複素環を表し、Mは水素イオン、1から3価の金属イオン、または少なくとも1つがアルキル基で置換されているアンモニウムイオンを表し、nはMの価数を表す。kは1または2の整数を表す。)
R11は、水素原子、ハロゲン原子、ニトロ基、シアノ基、水酸基、置換基を有してもよいアルコキシ基、置換基を有してもよいアルールオキシ基、−S(O)mR17、−NR18R19、またはN2 +X−である。ただし、mは0から3までの整数であり、R17は水素原子、置換基を有してもよいアルキル基、置換基を有してもよいアリール基、またはハロゲン原子である。さらに、R18とR19は、互いに独立に、水素原子、または置換基を有してもよいアルキル基、またはR18とR19とで一体となって更なる窒素、酸素または硫黄原子を含んでもよい複素環を表す。Xは、ハロゲン原子を表す。]
(式中、Yは、直接結合、−O−、−S(O)m−(ここでmは、0から3の整数を表す)、−CO−、−NR14−、−CONR14−、−SO2NR14−、−NR14CO−、−NR14SO2−(ここでR14は、水素原子、アルキル基、またはヒドロキシアルキル基を表す)、炭素数1から12の直鎖または枝分かれしたアルキレン基あるいは、アルキル基、アミノ基、ニトロ基、水酸基、アルコキシ基、またはハロゲン原子で置換されていてもよいベンゼン残基あるいはトリアジン残基、またはこれらの結合基を2個以上組み合わせた結合基を表す。Zはハロゲン原子、置換基を有してもよいアルキル基、置換基を有してもよいアリール基、置換基を有してもよいフタルイミドメチル気、−NR15R16、SO3・M/n、または−COO・M/nを表し、R15とR16はそれぞれ独立に水素原子、置換基を有してもよいアルケニル基、置換基を有してもよいフェニル基、またはR15とR16とで一体となって更なる窒素、酸素または硫黄原子を含んでもよく、置換基を有してもよい複素環を表し、Mは水素イオン、1から3価の金属イオン、または少なくとも1つがアルキル基で置換されているアンモニウムイオンを表し、nはMの価数を表す。kは1または2の整数を表す。)
R11は、水素原子、ハロゲン原子、ニトロ基、シアノ基、水酸基、置換基を有してもよいアルコキシ基、置換基を有してもよいアルールオキシ基、−S(O)mR17、−NR18R19、またはN2 +X−である。ただし、mは0から3までの整数であり、R17は水素原子、置換基を有してもよいアルキル基、置換基を有してもよいアリール基、またはハロゲン原子である。さらに、R18とR19は、互いに独立に、水素原子、または置換基を有してもよいアルキル基、またはR18とR19とで一体となって更なる窒素、酸素または硫黄原子を含んでもよい複素環を表す。Xは、ハロゲン原子を表す。]
ソペンチルオキシ基、ヘキシルオキシキ、ヘプチルオキシ基、オクチルオキシ基、2−エチルヘキシルオキシ基、デシルオキシ基、ドデシルオキシ基、オクタデシルオキシ基、エトキシカルボニルメチル基、2−エチルヘキシルオキシカルボニルメチルオキシ基、アミノカルボニルメチルオキシ基、N,N−ジブチルアミノカルボニルメチルオキシ基、N−メチルアミノカルボニルメチルオキシ基、N−エチルアミノカルボニルメチルオキシ基、N−オクチルアミノカルボニルメチルオキシ基、N−メチル−N−ベンジルアミノカルボニルメチルオキシ基、ベンジルオキシ基、シアノメチルオキシ基等が挙げられる。
ボニル基、フェノキシカルボニル基等のアルコキシカルボニル基、アセトキシ基、プロピオニルオキシ基、ベンゾイルオキシ基等のアシルオキシ基、アセチル基、ベンゾイル基、イソブチリル基、アクリロイル基、メタクリロイル基、メトキサリル基等のアシル基、メチルスルファニル基、tert−ブチルスルファニル基等のアルキルスルファニル基、フェニルスルファニル基、p−トリルスルファニル基等のアリールスルファニル基、メチルアミノ基、シクロヘキシルアミノ基等のアルキルアミノ基、ジメチルアミノ基、ジエチルアミノ基、モルホリノ基、ピペリジノ基等のジアルキルアミノ基、フェニルアミノ基、p−トリルアミノ基等のアリールアミノ基、メチル基、エチル基、tert−ブチル基、ドデシル基等のアルキル基、フェニル基、p−トリル基、キシリル基、クメニル基、ナフチル基、アンスリル基、フェナントリル基等のアリール基、フリル基、チエニル基等の複素環基等の他、ヒドロキシ基、カルボキシ基、ホルミル基、メルカプト基、スルホ基、メシル基、p−トルエンスルホニル基、アミノ基、ニトロ基、シアノ基、トリフルオロメチル基、トリクロロメチル基、トリメチルシリル基、ホスフィニコ基、ホスホノ基、トリメチルアンモニウミル基、ジメチルスルホニウミル基、トリフェニルフェナシルホスホニウミル基等が挙げられる。
−2−イルアミノメチル基等が挙げられる。
この中で、広範な樹脂に対し優れた分散性を示すだけでなく、非集合性、非結晶性、粘度適性、塗膜光沢、鮮明性、貯蔵安定性に優れたインキ及び塗料を得ることが容易に達成できる本発明のベンゾイソインドール誘導体は、R4が
、一般式(3)または一般式(4)で表される置換基を有するものである。
式中、Yは、直接結合、−O−、−S(O)m−(ここでmは、0から3の整数を表す)、−CO−、−NR14−、−CONR14−、−SO2NR14−、−NR14CO−、−N
R14SO2−(ここでR1は、水素原子、アルキル基、またはヒドロキシアルキル基を表す)、炭素数が1〜12の直鎖または枝分かれしたアルキレン基、およびアルキル基、アミノ基、ニトロ基、水酸基、アルコキシ基、またはハロゲン原子で置換されてもよいベンゼン残基あるいはトリアジン残基、またはこれらの結合基を2個以上組み合わせた結合基を表す。R15とR16はそれぞれ独立に水素原子、置換基を有してもよいアルキル基、置換基を有してもよいアルケニル基、置換基を有してもよいフェニル基、またはR15とR16とで一体となって更なる窒素、酸素または硫黄原子を含んでもよく、置換基を有してもよい複素環を表す。kは1または2の整数を表す。
式中、Yは、直接結合、−O−、−S(O)m−(ここでmは、0から3の整数を表す)、−CO−、−NR14−、−CONR14−、−SO2NR14−、−NR14CO−、−N
R14SO2−(ここでR1は、水素原子、アルキル基、またはヒドロキシアルキル基を表す)、炭素数1〜12の直鎖または枝分かれしたアルキレン基、およびアルキル基、アミノ基、ニトロ基、水酸基、アルコキシ基、またはハロゲン原子で置換されてもよいベンゼン残基あるいはトリアジン残基、またはこれらの結合基を2個以上組み合わせた結合基を表す。Mは水素イオン、1〜3価の金属イオン、または少なくとも1つがアルキル基で置換されているアンモニウムイオンを表し、nはMの価数を表す。kは1または2の整数を表す。
(ただし、Meはメチル基、Etはエチル基、n−Prはノルマルプロピル基、i−Prは2−プロピル基、Buはブチル基、Hexはヘキシル基、Tolはパラトリル基、Acはアセチル基、Bzはベンゾイル基、Phはフェニル基を表す)。
以下に、実施例により、本発明をさらに詳細に説明するが、以下の実施例は本発明の権利範囲を何ら制限するものではない。なお、実施例における「部」は、「重量部」を表す。
[実施例1]
下記の原料(アクリル樹脂は酸化16mgKOH/g、重量平均分子量60000、固形分50%ものを用いた。以下の列中のアクリル樹脂も全て同じもの)の混合物にスチールビーズを加え、ペイントシェカー(レッドデビル社製)を用いて90分間分散しカーボンブラック組成物を作製した。
カーボンブラック(FW−200 デグサ社製) 10.0部
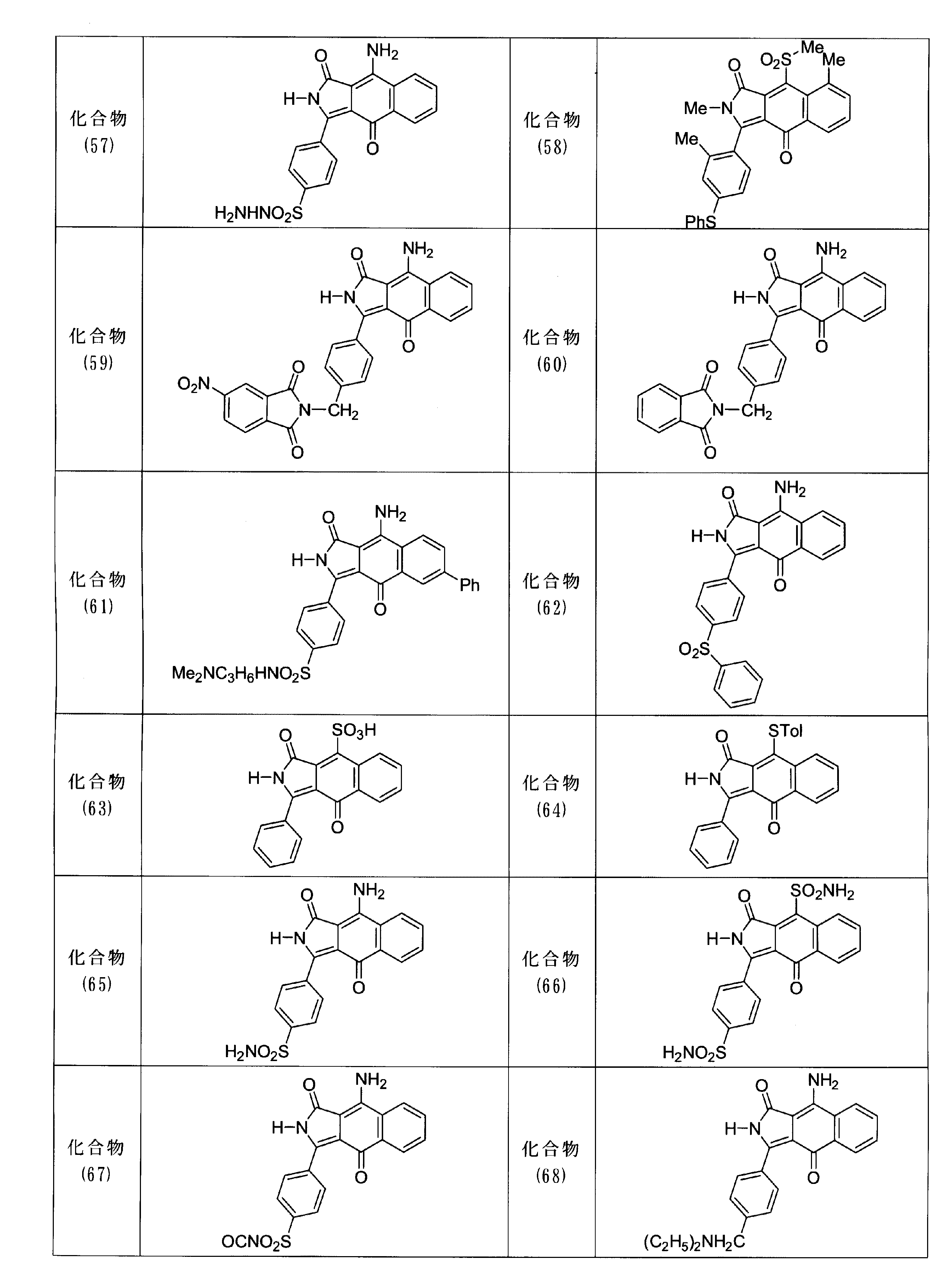
ベンゾイソインドール誘導体[表1の化合物57] 1.0部
アクリル樹脂 60.0部
トルエン 20.0部
酢酸エチル 10.0部
実施例1におけるベンゾイソインゾール誘導体[表1の化合物57]を[表1の化合物33]に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[実施例3]
実施例1におけるベンゾイソインゾール誘導体[表1の化合物57]を[表1の化合物25]に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[実施例4]
実施例1におけるベンゾイソインゾール誘導体[表1の化合物57]を[表1の化合物79]に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[実施例5]
実施例1におけるベンゾイソインゾール誘導体[表1の化合物57]を1.0部から0.5部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
実施例2におけるベンゾイソインゾール誘導体[表1の化合物33]を1.0部から0.5部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[実施例7]
実施例3におけるベンゾイソインゾール誘導体[表1の化合物25]を1.0部から0.5部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[実施例8]
実施例4におけるベンゾイソインゾール誘導体[表1の化合物79]を1.0部から0.5部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
実施例1におけるベンゾイソインゾール誘導体を除く以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例2]
実施例1におけるベンゾイソインゾール誘導体[表1の化合物57]を1.0部から0.05部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例3]
実施例2におけるベンゾイソインゾール誘導体[表1の化合物33]を1.0部から0.05部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例4]
実施例3におけるベンゾイソインゾール誘導体[表1の化合物25]を1.0部から0.05部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例5]
実施例4におけるベンゾイソインゾール誘導体[表1の化合物79]を1.0部から0.05部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
実施例1におけるベンゾイソインゾール誘導体[表1の化合物57]を1.0部から25.0部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例7]
実施例2におけるベンゾイソインゾール誘導体[表1の化合物33]を1.0部から25.0部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例8]
実施例3におけるベンゾイソインゾール誘導体[表1の化合物25]を1.0部から25.0部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
[比較例9]
実施例4におけるベンゾイソインゾール誘導体[表1の化合物79]を1.0部から25.0部に変更した以外は実施例1と同様にしてカーボンブラック組成物を作製した。
尚、評価方法としては下記の通り行った。
カーボンブラック組成物と下記原料(ユーバン20SE60は三井サイテック社製のメ
ラミン樹脂)を混合し、アクリル/メラミン系の濃色塗料を得た。
カーボンブラック組成物 43.5部
アクリル樹脂 34.8部
ユーバン20SE60 21.7部
[淡色塗料配合]
濃色塗料中のカーボンブラックと酸化チタンの比率が1/10になるように下記酸化チ
タン塗料と混合し淡色塗料を得た。
濃色塗料 15.8部
酸化チタン塗料 84.2部
[酸化チタン塗料組成]
酸化チタン(タイペーク R−670 石原産業社製)18.8部
アクリル樹脂 34.8部
ユーバン20SE60 21.7部
トルエン 5.6部
酢酸エチル 2.8部
[塗装方法]
上記で作製した濃色塗料をPETフィルムに乾燥塗膜の膜厚が約10μmとなるように
バーコーターで塗装し、10分予備乾燥後、140℃30分乾燥し塗膜を作製した。
10分予備乾燥後、140℃30分乾燥し塗膜を作製した。
[光沢(60°鏡面反射率)]光沢計[日本電色工業(株)GlossMeter VG2000]により60°−60°反射率を測定した。
[ヘイズ]濁度計[日本電色工業(株)300A]によりヘイズを測定した。
[着色力]測色計[日本電色工業(株)SpctrophotoMeter SE2000]にて比較例1との明度指数差L値を測定し、下式により着色力を求めた。この数値が大きい程、分散性は良好である。
着色力=100−(△L値×10)
[保存安定性]各比較例及び実施例より作製したカーボンブラック組成物の初期粘度と40℃1ヶ月保存した経時粘度を測定し、初期粘度と経時粘度との比較より経時増粘率を算出した。経時増粘率=経時粘度/初期粘度 尚、粘度の測定はカーボンブラック組成物を25℃に調整した後にBL型粘度計において60prm1分後の値を測定する。
Claims (2)
- カーボンブラックと結合剤、溶剤および下記一般式(1)で表されるベンゾイソインドール誘導体を用いてなることを特徴とするカーボンブラック組成物
式(1)
式中、R1は水素原子、置換基を有してもよいアルキル基、または置換基を有してもよいアシル基を表す。
R2、R3、R5、R6、R7、R8、R9、R10は、互いに独立に、水素原子、置換基を有してもよいアルキル基、フェニル基、ハロゲン原子、シアノ基、置換基を有してもよいアルコキシ基、または−NR12R13である。ただし、R12とR13は、互いに独立に、水素原子、または置換基を有してもよいアルキル基、またはR12とR13とで一体となって更なる窒素、酸素または硫黄原子を含んでもよい複素環を表す。
R4は、水素原子、置換基を有してもよいアルキル基、置換基を有してもよいアシル基、または、一般式(2)で表される置換基を表す。
−Y−(Z)k 一般式(2)
(式中、Yは、直接結合、−O−、−S(O)m−(ここでmは、0から3の整数を表す)、−CO−、−NR14−、−CONR14−、−SO2NR14−、−NR14CO−、−NR14SO2−(ここでR14は、水素原子、アルキル基、またはヒドロキシアルキル基を表す)、炭素数1から12の直鎖または枝分かれしたアルキレン基あるいは、アルキル基、アミノ基、ニトロ基、水酸基、アルコキシ基、またはハロゲン原子で置換されていてもよいベンゼン残基あるいはトリアジン残基、またはこれらの結合基を2個以上組み合わせた結合基を表す。Zはハロゲン原子、置換基を有してもよいアルキル基、置換基を有してもよいアリール基、置換基を有してもよいフタルイミドメチル気、−NR15R16、SO3・M/n、または−COO・M/nを表し、R15とR16はそれぞれ独立に水素原子、置換基を有してもよいアルケニル基、置換基を有してもよいフェニル基、またはR15とR16とで一体となって更なる窒素、酸素または硫黄原子を含んでもよく、置換基を有してもよい複素環を表し、Mは水素イオン、1から3価の金属イオン、または少なくとも1つがアルキル基で置換されているアンモニウムイオンを表し、nはMの価数を表す。kは1または2の整数を表す。)
R11は、水素原子、ハロゲン原子、ニトロ基、シアノ基、水酸基、置換基を有してもよいアルコキシ基、置換基を有してもよいアルールオキシ基、−S(O)mR17、−NR18R19、またはN2 +X−である。ただし、mは0から3までの整数であり、R17は水素原子、置換基を有してもよいアルキル基、置換基を有してもよいアリール基、またはハロゲン原子である。さらに、R18とR19は、互いに独立に、水素原子、または置換基を有してもよいアルキル基、またはR18とR19とで一体となって更なる窒素、酸素または硫黄原子を含んでもよい複素環を表す。Xは、ハロゲン原子を表す。] - カーボンブラック100重量部に対し、一般式(1)で表されるベンゾイソインドール誘導体を0.1から20重量部含有することを特徴とする請求項1記載のカーボンブラック組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008026800A JP2009185178A (ja) | 2008-02-06 | 2008-02-06 | カーボンブラック組成物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008026800A JP2009185178A (ja) | 2008-02-06 | 2008-02-06 | カーボンブラック組成物 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2009185178A true JP2009185178A (ja) | 2009-08-20 |
Family
ID=41068738
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008026800A Pending JP2009185178A (ja) | 2008-02-06 | 2008-02-06 | カーボンブラック組成物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2009185178A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL422003A1 (pl) * | 2017-06-24 | 2019-01-02 | Instytut Chemii Organicznej Polskiej Akademii Nauk | Nowe emitery światła pomarańczowego i czerwonego na bazie izoindolo[5,8]dionów oraz sposób ich otrzymywania |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004292672A (ja) * | 2003-03-27 | 2004-10-21 | Mikuni Color Ltd | カーボンブラック分散液 |
| JP2005213405A (ja) * | 2004-01-30 | 2005-08-11 | Toyo Ink Mfg Co Ltd | カーボンブラック分散液の製造方法 |
| JP2007009096A (ja) * | 2005-07-01 | 2007-01-18 | Toyo Ink Mfg Co Ltd | 顔料組成物およびそれを用いた顔料分散体 |
| JP2007277221A (ja) * | 2006-03-17 | 2007-10-25 | Toyo Ink Mfg Co Ltd | ベンゾイソインドール系化合物およびその製造法 |
| JP2008069343A (ja) * | 2006-08-18 | 2008-03-27 | Toyo Ink Mfg Co Ltd | ベンゾイソインドール誘導体を含む顔料組成物およびそれを用いた着色組成物 |
| JP2009057477A (ja) * | 2007-08-31 | 2009-03-19 | Toyo Ink Mfg Co Ltd | 顔料組成物、顔料分散体およびインキ |
| JP2009057478A (ja) * | 2007-08-31 | 2009-03-19 | Toyo Ink Mfg Co Ltd | 顔料組成物、顔料分散体およびインキ |
-
2008
- 2008-02-06 JP JP2008026800A patent/JP2009185178A/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004292672A (ja) * | 2003-03-27 | 2004-10-21 | Mikuni Color Ltd | カーボンブラック分散液 |
| JP2005213405A (ja) * | 2004-01-30 | 2005-08-11 | Toyo Ink Mfg Co Ltd | カーボンブラック分散液の製造方法 |
| JP2007009096A (ja) * | 2005-07-01 | 2007-01-18 | Toyo Ink Mfg Co Ltd | 顔料組成物およびそれを用いた顔料分散体 |
| JP2007277221A (ja) * | 2006-03-17 | 2007-10-25 | Toyo Ink Mfg Co Ltd | ベンゾイソインドール系化合物およびその製造法 |
| JP2008069343A (ja) * | 2006-08-18 | 2008-03-27 | Toyo Ink Mfg Co Ltd | ベンゾイソインドール誘導体を含む顔料組成物およびそれを用いた着色組成物 |
| JP2009057477A (ja) * | 2007-08-31 | 2009-03-19 | Toyo Ink Mfg Co Ltd | 顔料組成物、顔料分散体およびインキ |
| JP2009057478A (ja) * | 2007-08-31 | 2009-03-19 | Toyo Ink Mfg Co Ltd | 顔料組成物、顔料分散体およびインキ |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL422003A1 (pl) * | 2017-06-24 | 2019-01-02 | Instytut Chemii Organicznej Polskiej Akademii Nauk | Nowe emitery światła pomarańczowego i czerwonego na bazie izoindolo[5,8]dionów oraz sposób ich otrzymywania |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101184803B (zh) | 官能化的纳米颗粒 | |
| KR100803934B1 (ko) | 채색 특성이 개선된 안료 및 이의 제조방법 | |
| EP1572810B1 (de) | Phthalocyaninpigmentzubereitungen | |
| US8203125B2 (en) | Light to heat conversion layer incorporating modified pigment | |
| EP1940968B1 (de) | Pigmentzubereitungen auf basis von diketopyrrolopyrrolen | |
| JP4844499B2 (ja) | ベンゾイソインドール誘導体を含む顔料組成物およびそれを用いた着色組成物 | |
| DE102007011067A1 (de) | Pigmentzubereitungen auf Basis von Diketopyrrolopyrrolen | |
| DE102007001851A1 (de) | Feinteilige Epsilon-Kupferphthalocyanin-Komposition (Pigment Blau 15:6) zur Verwendung als Pigment | |
| WO2013166348A2 (en) | Surface modification of pigments and compositions comprising the same | |
| JP2004505157A (ja) | 透明な顔料の熱安定性を改善する分散剤組成物 | |
| JP2009185178A (ja) | カーボンブラック組成物 | |
| EP2658928B1 (en) | Surface-modified pigment preparations | |
| EP1892240B1 (en) | Benzoisoindole derivative, pigment composition comprising the same and colored composition | |
| JP2008081565A (ja) | 顔料分散剤、及び顔料分散体 | |
| JP2009057478A (ja) | 顔料組成物、顔料分散体およびインキ | |
| CN114466843B (zh) | 异吲哚啉衍生物 | |
| MXPA03001995A (es) | Composiciones polimericas pigmentadas estabilizadas. | |
| WO2008107073A1 (de) | Verfahren zur direkten herstellung feinteiliger diketopyrrolopyrrolpigmente | |
| JP2010254835A (ja) | 顔料分散剤 | |
| JP4983631B2 (ja) | 磁気記録媒体用塗料組成物およびそれを用いてなる磁気記録媒体 | |
| WO2008107075A2 (de) | Pigmentzubereitungen auf basis von diketopyrrolopyrrolen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101004 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110729 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120823 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120828 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130108 |