JP2007526460A - 細胞集団のタンパク質発現プロファイルの作成のための分析用プラットフォームおよび方法 - Google Patents
細胞集団のタンパク質発現プロファイルの作成のための分析用プラットフォームおよび方法 Download PDFInfo
- Publication number
- JP2007526460A JP2007526460A JP2007501122A JP2007501122A JP2007526460A JP 2007526460 A JP2007526460 A JP 2007526460A JP 2007501122 A JP2007501122 A JP 2007501122A JP 2007501122 A JP2007501122 A JP 2007501122A JP 2007526460 A JP2007526460 A JP 2007526460A
- Authority
- JP
- Japan
- Prior art keywords
- solid support
- different
- lysate
- proteins
- protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6845—Methods of identifying protein-protein interactions in protein mixtures
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/566—Immunoassay; Biospecific binding assay; Materials therefor using specific carrier or receptor proteins as ligand binding reagents where possible specific carrier or receptor proteins are classified with their target compounds
- G01N33/567—Immunoassay; Biospecific binding assay; Materials therefor using specific carrier or receptor proteins as ligand binding reagents where possible specific carrier or receptor proteins are classified with their target compounds utilising isolate of tissue or organ as binding agent
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6842—Proteomic analysis of subsets of protein mixtures with reduced complexity, e.g. membrane proteins, phosphoproteins, organelle proteins
Abstract
-1以上の細胞集団の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-実質的に平面の固体支持体を提供すること、
-希釈または非希釈形態にて該固体支持体に直接的に、または、該固体支持体上にアプライされた接着促進層上に、少量の細胞可溶化液を別々の部位に沈着させ、それによって該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイを作成すること、
-例えば、シグナル伝達系路の大域解析または、最高の特異性、選択性および親和性についてのタンパク質標的に対する抗体セット/ライブラリーのスクリーニングのために、別々の測定領域における細胞可溶化液に含まれる検出すべきタンパク質の特異的結合パートナーとして複数の結合試薬をアプライすること、および適当であるならば、該1以上の測定領域のアレイに1以上の検出試薬をアプライすること、該結合試薬および該検出試薬は、1以上のアレイの別々の測定領域に逐次的にアプライされるか、または検出試薬が結合試薬に結合した後、単一添加工程にてアプライされる、そして、
-該1以上のアレイの別々の測定領域から生じる光シグナルを局所的に分解した様式で測定および記録すること、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。
Description
-1以上の細胞集団の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-実質的に平面の固体支持体を提供すること、
-希釈または非希釈形態にて該固体支持体上に直接的に、または、該固体支持体上にアプライされた接着促進層上に、少量の細胞可溶化液を別々の部位に沈着させ、それによって該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイを作成すること、
-別々の測定領域における細胞可溶化液に含まれる検出すべきタンパク質の特異的結合パートナーとして複数の結合試薬をアプライすること、および、適当であるならば、該1以上の測定領域のアレイに1以上の検出試薬をアプライすること、該結合試薬および該検出試薬は、1以上のアレイの別々の測定領域に逐次的にアプライされるか、または検出試薬が結合試薬に結合した後、単一添加工程にてアプライされる、そして、
-該1以上のアレイの別々の測定領域から生じる光シグナルを局所的に分解した様式で測定および記録すること、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。
本発明は、具体的には、生物または組織または細胞アセンブリーに対する薬剤の医薬効果および/または毒性効果の理解の向上または促進を補助するものである。本発明は、特に、細胞シグナル伝達カスケードの調査およびその元の形態または細胞発達過程の結果、および適当であるならば、これらの過程を修飾するための外部から指示された誘導の結果、翻訳後修飾された形態における非常に多様なタンパク質の検出に関する。
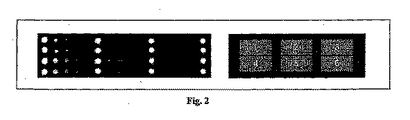
図1は、本発明による分析用プラットフォームおよび本発明による分析用プラットフォームとしての一般的な固体支持体上の(沈着させたサンプルにしたがって) 6つの同一の測定領域のアレイの配置を示す。作成した測定領域の配置の形状は2つの拡大図に示す(詳細な説明については明細書の記載を参照されたい)。
本発明の第一の対象は、以下を含む1以上の細胞集団の定性的および/または定量的タンパク質発現プロファイルの作成方法である:
-1以上の細胞集団の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-実質的に平面の固体支持体を提供すること、
-希釈または非希釈形態にて、該固体支持体上に直接的に、または、該固体支持体上にアプライされた接着促進層上に、少量の細胞可溶化液を沈着サンプルとして別々の部位に沈着させ、それによって該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイを作成すること、
-別々の測定領域における細胞可溶化液に含まれる検出すべきタンパク質の特異的結合パートナーとして複数の(即ち1以上の) 結合試薬をアプライすること、および適当であるならば、該1以上の測定領域のアレイに1以上の検出試薬をアプライすること、該結合試薬および該検出試薬は、1以上のアレイの別々の測定領域に逐次的にアプライされるか、または検出試薬が結合試薬に結合した後、単一添加工程にてアプライされる、そして、
-該1以上のアレイの別々の測定領域から生じる光シグナルを局所的に分解した様式で測定および記録すること、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。
-細胞集団の第一の可溶化液を作成すること、該可溶化液は、それぞれの細胞集団によって発現される複数のタンパク質を含む、
-さらなる細胞集団の第二または第三以上の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-実質的に平面の固体支持体を提供すること、
-希釈または非希釈形態にて、該固体支持体上に直接的に、または、該固体支持体上にアプライされた接着促進層上に、少量の細胞可溶化液を沈着サンプルとして別々の部位に沈着させ、それによって該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイを作成すること、
-別々の測定領域における細胞可溶化液に含まれる検出すべきタンパク質の特異的結合パートナーとして複数の結合試薬をアプライすること、および、適当であるならば、該1以上の測定領域のアレイに1以上の検出試薬をアプライすること、該結合試薬および該検出試薬は、1以上のアレイの別々の測定領域に逐次的にアプライされるか、または検出試薬が結合試薬に結合した後、単一添加工程にてアプライされる、そして、
-希釈または非希釈形態にて、少量の第一の可溶化液の沈着によって作成された測定領域から生じる光シグナルの第一の群を局所的に分解した様式で測定および記録すること、
-希釈または非希釈形態にて、少量の第二または第三以上の可溶化液の沈着によって作成された測定領域から生じる光シグナルの第二または第三以上の群を局所的に分解した様式で測定および記録すること、
-光シグナルの第一の群の測定値と光シグナルの第二または第三以上の群の測定値を比較すること、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。
Y-B-OPO3 H2 (IA)
または一般式 I (B)の有機ホスホン酸:
Y-B-PO3 H2 (IB)
の群の化合物およびそれらの塩も含み得、式中、Bは、アルキル、アルケニル、アルキニル、アリール、アラルキル、ヘテロアリール(hetaryl)、またはヘテロアリールアルキル(hetarylalkyl)残基であり、Yは水素または以下のシリーズの官能基である:例えば、ヒドロキシ、カルボキシ、アミノ、低級アルキルによって置換されていてもよいモノまたはジアルキルアミノ、チオール、または以下のシリーズ負の酸性基である:例えば、エステル、ホスファート、ホスフォナート、スルファート、スルフォナート、マレイミド、スクシンイミジル、エポキシまたはアクリラート。これら化合物は国際特許出願 PCT/EP 01/10077により詳細に記載されており、その開示全体を引用により本明細書に含める。
-実質的に平面の固体支持体、
-該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイ、該アレイは、少量の細胞可溶化液が、希釈または非希釈形態にて、別々の部位に該固体支持体上に直接に沈着するか、または、固体支持体上に前もってアプライされた接着促進層上に沈着することによって作成され、該細胞可溶化液は1以上の細胞集団由来であり、かかる細胞集団によって発現される複数のタンパク質を含む、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。
-実質的に平面の固体支持体、
-該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイ、該アレイは少量の2以上の細胞可溶化液を、希釈または非希釈形態にて、別々の部位に該固体支持体上に直接に沈着することまたは前もって固体支持体上にアプライされた接着促進層上に沈着することによって作成され、該細胞可溶化液は2以上の細胞集団由来であり、かかる細胞集団によって発現される複数のタンパク質を含む、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。
Y-B-OPO3 H2 (IA)
または一般式 I (B)の有機ホスホン酸の群の化合物:
Y-B-PO3 H2 (IB)
およびそれらの塩も含み得、ここで、Bは、アルキル、アルケニル、アルキニル、アリール、アラルキル、ヘテロ(het)アリール、またはヘテロ(het)アリールアルキル残基、Yは水素または以下のシリーズの官能基、例えば、ヒドロキシ、カルボキシ、アミノ、低級アルキルによって置換されていてもよいモノまたはジアルキルアミノ、チオール、または以下のシリーズの負の酸性基、例えば、エステル、ホスファート、ホスフォナート、スルファート、スルフォナート、マレイミド、スクシンイミジル、エポキシまたはアクリラートである。これら化合物は国際特許出願 PCT/EP 01/10077により詳細に記載されており、その開示全体を引用により本明細書に含める。
1.1.組織可溶化液サンプル
示差的タンパク質発現プロファイルを調べるために2種類の組織可溶化液を用いた。可溶化液は共通の細胞集団に由来する細胞亜種団から得た: 癌組織 (= 共通の細胞集団)を2つの細胞亜種団に分け、これらを互いに独立に培養した。その一方はさらなる処理に供さず、対照サンプル (「腫瘍可溶化液1」)の作成に用いた。他方の細胞亜種団は化学的に処理し、第二可溶化液サンプル(「腫瘍可溶化液2」)の作成に用いた。これらサンプルは以下の特徴を有していた:
以下のマーカー特異的抗体を選択し、特異的結合試薬として用いた(CST = Cell Signaling Technology、Inc.、Beverly、MA 01915、USA、BD = BD Biosciences、Basel、Switzerland):
α-P-p44/42 MAPK (CST # 9101) ウサギ
α-P-Akt (CST #4051) マウス IgG2b
α-P-p38 (CST #9211) ウサギ
α-P-SAPK/JNK (CST #9251) ウサギ
α-P-IκB-α (CST #9241) ウサギ
α-P-Stat3 (CST #9138) マウス IgG1
α-P-ヒストン H3 (CST #9706) マウス IgG1
α-P-Rb (CST #9308) ウサギ
α-P-p53/Ser15 (CST #9284) ウサギ
α-サイクリン D1 (CST #2926) マウス IgG2a
α-切断カスパーゼ3 (CST #9664) ウサギ
α-切断PARP (CST #9541) ウサギ
α-α-カテニン (BD #6101193)
α-β-カテニン (CST #9562)。
Cy3-α-β-アクチン (内部標識)
Alexa Fluor 647 (α-ウサギ IgG); Molecular Probes #Z-25308
Alexa Fluor 647 (α-マウス IgG1); Molecular Probes #Z-25008
Alexa Fluor 647 (α-マウス IgG2a); Molecular Probes #Z-25108
Alexa Fluor 647 (α-マウス IgG2b); Molecular Probes #Z-25208。
本発明による分析用プラットフォームの部分としての実質的に平面の固体支持体として、平面状膜導波路を用い、この大きさは、幅14 mm x 長さ57 mm x厚さ0.7 mmであった。これら薄膜導波路は、ガラス基体(AF 45、第二の光学的に透明の層 (b))および(b)の上に沈着する150 nmの厚さの、屈折率の高い五酸化タンタル層(第一の光学的に透明の層 (a))を含む。2つの表面レリーフ格子(格子構造(c)および(c’))は、これらプレートの長さに平行に、ガラス基体上に互いに9 mmの距離に調整される (格子周期: 318 nm、格子深度: 12 nm +/- 2 nm)。光の屈折率の高い層へのインカップリングのための回折格子として役立つこれら構造は、該屈折率の高い層の沈着の結果、該五酸化タンタル層の表面に導入される。
3.1.タンパク質定量
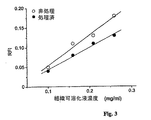
組織可溶化液のタンパク質濃度は標準として10倍希釈溶解バッファー中のBSAを用いてPIERCE Coomassie Plus Kit (PIERCE # 23238)により測定した。組織可溶化液を比色分析試薬の添加に先立ってリン酸緩衝食塩水 (PBS)に10倍に希釈した。結果はセクション 1.1に示す。
組織可溶化液を希釈して、セクション 2に記載の接着促進層を備えた固体支持体上に沈着 (「スポッティング」)させるための可溶化液終濃度とした。スポッティング溶液のタンパク質濃度は、尿素含有スポッティングバッファー中それぞれ0.26 mg/ml、0.21 mg/ml、0.16 mg/mlおよび0.10 mg/mlとした。別々の測定領域(「スポット」)はインクジェット・スポッターを用いて約400 pl容積の一滴の沈着により固体支持体上に作成した。各可溶化液溶液から2つの複製スポットを、共通の列に互いに隣接するように作成し、常に4種類の希釈度の可溶化液から4つの測定領域が1つの行において生じるようにした(図1参照)。2つのさらなる、相異なる処理をした細胞可溶化液(「非開示細胞可溶化液」として図1の上の拡大図に示す)をアッセイ性能についての内部陽性対照としてスポットした。陽性対照は典型的には、シグナル伝達経路マーカータンパク質であるP-Akt およびP-Erk2レベルの処理による上方制御を明らかにする。陰性対照となる測定領域はバッファー溶液(細胞または組織可溶化液を含まない)をスポッティングすることにより作成した。
可溶化液アレイの質的制御、即ち、欠損したスポット、スポット形状および均一性ならびにアプライされる相対タンパク質濃度の測定を、ハウスキーピングタンパク質としてβ-アクチンを検出することにより行った。β-アクチンの検出は5% BSAを含むアッセイバッファー中に500倍希釈したCy3-α-β-アクチン抗体の測定領域の1つのアレイへの添加(アプライ濃度: 6 nM)、次いで1時間25℃でのインキュベーションによって一工程アッセイにて行った。過剰の蛍光標識化抗体を5% BSAを含むアッセイバッファーにより除去した後、アレイを励起および結果として生じる蛍光シグナルの ZeptoREADERTM を用いた(以下参照)検出による検出工程に供した。
様々な測定領域のアレイからの蛍光シグナルをZeptoREADERTM (Zeptosens AG、Benkenstrasse 254、CH-4108 Witterswil)を用いて自動的に連続して測定した。主要な測定工程は以下の通りである:各測定領域のアレイについて、本発明による分析用プラットフォームを、光の導波路である五酸化タンタル層へのインカップリングのための共鳴条件のマッチングおよび測定領域における利用可能な励起光の最大化のために調整する。次いで、各アレイについて、対応するアレイからの蛍光シグナルのイメージを作成し、ここで、使用者は様々な露光時間および作成するイメージの数を選択することが出来る。本実施例についての測定の場合、励起波長はCy5またはAlexa Fluor 647 蛍光標識の励起のためには633 nm、Cy3 蛍光標識の励起のためには532 nmとした。Cy5またはAlexa Fluor 647の蛍光波長での蛍光検出はカメラのレンズの前に位置する散乱光を抑制するために、冷却カメラ、干渉フィルター(透過 675 nm +/- 25 nm、「赤色検出チャネル」)を用いて行う。532 nmにて励起されたCy3 蛍光標識から生じる蛍光の検出には、 透過 572 nm +/- 25 nm (「緑色検出チャネル」)の干渉フィルターを用いる。作成された蛍光イメージは、制御コンピュータのディスクに自動的に記憶される。光学システム(ZeptoREADERTM)のさらなる詳細については国際特許出願 PCT/EP 01/10012に記載されており、本明細書にその内容を引用により含める。
測定領域(スポット)からの可溶化液サンプル分析物濃度の相対濃度に対応する蛍光シグナル強度を複数の測定領域のアレイからの蛍光イメージの自動化分析を可能とするイメージ分析ソフトウェア(ZeptoVIEWTM、Pro 2.0 Release 2.0、Zeptosens AG、CH-4108 Witterswil)を用いて測定した。
4.1. 組織可溶化液アレイの生産-質的対照
スポットした可溶化液アレイの質(例えば、欠損したスポットの数、スポット形状、スポット形態、相対タンパク質濃度)をハウスキーピングタンパク質としてのβ-アクチンの発現レベルを測定するアッセイにて調べた。測定は、図1において「非開示細胞可溶化液」と称される測定領域のアレイにアプライされるCy3-標識抗-β-アクチン抗体を検出試薬として用いてZeptoREADERTMの緑色検出チャネルにて行った。
・欠損したスポットが無い
・スポット形状が良好である
・スポットの均一性が良好である。
・シグナル生成のダイナミックレンジの指定、および、
・単一地点測定(即ち、個々のタンパク質濃度についてのみ測定される蛍光強度)ではなく用量依存的シグナル勾配を用いることによるより正確なシグナルの抽出。
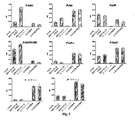
ひとつの測定領域のアレイを、特異的結合試薬としてアプライされた各異なる抗体および沈着したサンプルにおける検出すべきタンパク質について測定した。以下において、各測定したマイクロアレイから得たバー・プロット・プロファイルを各タンパク質分析物について示す。
図8は、14種類のタンパク質分析物への結合およびそれらの検出のための、14種類のマーカー抗体によりプロファイリングされた2種の異なる処理済大腸癌組織可溶化液について得られた結果を要約する。「シグナル倍数」変化は、対照可溶化液サンプルのシグナルに対する処理済可溶化液サンプルのシグナルの比として算出したものであり、したがって目的のタンパク質の示差的発現プロファイルを表す。破線はタンパク質 発現の有意な上方制御および下方制御の限界を示す:
上方制御の限界= 1.24
下方制御の限界= 0.81。
Claims (69)
- 以下を含む、1以上の細胞集団の定性的および/または定量的タンパク質発現プロファイルを作成する方法:
-1以上の細胞集団の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-実質的に平面の固体支持体を提供すること、
-希釈または非希釈形態にて、該固体支持体上に直接的に、または、該固体支持体上にアプライされた接着促進層上に、少量の細胞可溶化液を沈着サンプルとして別々の部位に沈着させ、それによって該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイを作成すること、
-別々の測定領域における細胞可溶化液に含まれる検出すべきタンパク質の特異的結合パートナーとして複数の結合試薬をアプライすること、および、適当であるならば、該1以上の測定領域のアレイに1以上の検出試薬をアプライすること、該結合試薬および該検出試薬は、1以上のアレイの別々の測定領域に逐次的にアプライされるか、または検出試薬が結合試薬に結合した後、単一添加工程にてアプライされる、および、
-該1以上のアレイの別々の測定領域から生じる光シグナルを局所的に分解した様式で測定および記録すること、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。 - 以下を含む、2以上の細胞集団の定性的および/または定量的示差的タンパク質発現プロファイルを作成する方法:
-細胞集団の第一の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-さらなる細胞集団の第二または第三以上の可溶化液を作成すること、該可溶化液はそれぞれの細胞集団によって発現される複数のタンパク質を含む、
-実質的に平面の固体支持体を提供すること、
-希釈または非希釈形態にて、該固体支持体上に直接的に、または、該固体支持体上にアプライされた接着促進層上に、少量の細胞可溶化液を沈着サンプルとして別々の部位に沈着させ、それによって該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイを作成すること、
-別々の測定領域における細胞可溶化液に含まれる検出すべきタンパク質の特異的結合パートナーとして複数の結合試薬をアプライすること、および、適当であるならば、該1以上の測定領域のアレイに1以上の検出試薬をアプライすること、該結合試薬および該検出試薬は、1以上のアレイの別々の測定領域に逐次的にアプライされるか、または検出試薬が結合試薬に結合した後、単一添加工程にてアプライされる、および、
-希釈または非希釈形態にて、少量の第一の可溶化液の沈着によって作成された測定領域から生じる光シグナルの第一の群を局所的に分解した様式で測定および記録すること、
-希釈または非希釈形態にて、少量の第二または第三以上の可溶化液の沈着によって作成された測定領域から生じる光シグナルの第二または第三以上の群を局所的に分解した様式で測定および記録すること、および、
-光シグナルの第一の群の測定値と光シグナルの第二または第三以上の群の測定値を比較すること、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。 - 相異なるタンパク質に対する特異的結合パートナーとして相異なる結合試薬が各相異なる検出すべきタンパク質についての相異なるアレイ上にアプライされる請求項1または2の方法。
- アレイ上に相異なる識別可能な検出試薬をアプライすることにより共通のアレイにおいて相異なるタンパク質を検出し、検出すべき相異なるタンパク質の数が、アプライされる相異なる識別可能な標識の数に対応する、請求項1または2の方法。
- 測定領域のアレイ上の相異なるタンパク質および/または相異なる識別可能な検出試薬の検出のために相異なるアレイ上に相異なるタンパク質に対する特異的結合パートナーとして相異なる結合試薬をアプライすることにより、複数の相異なるタンパク質を複数の測定領域のアレイにおいて検出する、請求項1または2の方法。
- 相異なる可溶化液が関連しない細胞集団から作成される、請求項1〜5のいずれかの方法。
- 相異なる可溶化液が共通の細胞集団から得られた相異なる細胞亜集団から作成される、請求項1〜5のいずれかの方法。
- 相異なる可溶化液が共通の細胞集団から相異なる時点にて得られた相異なる細胞亜集団から作成される、請求項7の方法。
- 相異なる可溶化液が共通の細胞集団から得られ、相異なる試薬によって処理または刺激された、および/または、相異なる培養条件に曝された、相異なる細胞亜集団から作成される、請求項7または8の方法。
- 相異なる可溶化液が疾患および健康細胞集団から作成される請求項1〜9のいずれかの方法。
- 可溶化液の作成の由来である健康または疾患および/または処理または非処理および/または刺激された細胞集団が、以下を含む群に由来する、請求項1〜10のいずれかの方法:細菌を含む原核細胞、およびヒト、動物、または植物細胞を含む真核細胞、特に器官、皮膚、毛または骨組織を含むヒトまたは動物組織、または植物組織、および血液、血清または血漿、滑液、涙液、尿、唾液、組織液、リンパ液を含む細胞含有体液またはその構成成分。
- 固体支持体上または該固体支持体上の接着促進層上の別々の部位に希釈または非希釈形態にて沈着される可溶化液が、その中で検出すべきタンパク質を該可溶化液が由来する細胞集団と同一の相対的な分子の組成にて有する請求項1〜11のいずれかの方法。
- 可溶化液が、例えば、較正目的に使用することができる添加剤として、測定すべき分析物と類似の、追加された既知の濃度の化合物を(標準として)含む請求項1〜11のいずれかの方法。
- 単一の測定領域に沈着させる材料が1000 細胞未満のタンパク質含量に対応する請求項1〜13のいずれかの方法。
- 複数の測定領域のアレイが希釈または非希釈細胞可溶化液の沈着部位の同一の形状にて配置されており、2つの相異なるアレイにおける測定領域の行および列に関する類似の位置が、そこに沈着させた同一の(希釈または非希釈)細胞可溶化液からの沈着させた量に対応する、請求項1−14のいずれかの方法。
- 固体支持体上にアプライされる接着促進層の厚さが200 nm未満、好ましくは20 nm未満である請求項1−15のいずれかの方法。
- 該接着促進層が以下の群の化合物を含む請求項16の方法:シラン、官能化シラン、エポキシド、官能化荷電または極性ポリマーおよび「自立性受動的または官能化単層または多層」、チオール、アルキルホスファートおよびアルキルホスフォナート、ポリ(L)リジン/ポリエチレングリコールを含む多官能性ブロックコポリマー。
- サンプルが固体支持体上に直接に、または、固体支持体上に沈着させた接着促進層上に、横方向に選択的に、別々の測定領域に、以下を含む群から選択される方法によって沈着される、請求項16または17のいずれかの方法:インクジェットスポッティング、ペン、ピンまたはキャピラリーによる機械的スポッティング、「ミクロ接触プリンティング」、平行または交差マイクロチャンネルにおける、圧力差または電位または電磁ポテンシャルの印加によるその供給を介した測定領域とサンプルとの流体接触、および光化学的またはフォトリソグラフィー固定化方法。
- 別々の測定領域の間の領域が、結合試薬および/または検出試薬の非特異的結合を最小にするために「不動態化」されており、即ち、分析物(即ちタンパク質)および沈着したサンプルのその他の含有物および結合試薬、ならびに適当であるならば、検出試薬に対して「化学的に中立」(即ち非結合性)の化合物が横方向に分離した測定領域の間に沈着されている、請求項1−18のいずれかの方法。
- 検出すべきであって別々の測定領域に沈着している希釈または非希釈可溶化液に含まれるタンパク質が以下を含むタンパク質の群の化合物である請求項1−19のいずれかの方法:細胞質タンパク質、核タンパク質および膜タンパク質、体液中の分泌タンパク質(細胞質タンパク質および膜結合型細胞タンパク質、特にキナーゼを含む、細胞におけるシグナル伝達過程に関与するタンパク質)、タンパク質のリン酸化、グリコシル化、メチル化、およびアセチル化形態を含む翻訳後修飾タンパク質、特に処理の下で過剰発現および/または過小発現するタンパク質、抗体、人工的に過剰発現させたタンパク質、さらなる結合部位により官能化されたタンパク質を含む人工的に過剰発現させた修飾タンパク質(「ヒスチジンタグタンパク質」を含む「タグタンパク質」)、および蛍光タンパク質(「緑色蛍光タンパク質」、GFPを含む)。
- 検出すべきであって、別々の測定領域に沈着している希釈または非希釈可溶化液に含まれるタンパク質が、添加された特異的結合試薬、および適当であるならば、逐次的に添加されたか、あるいは検出試薬の結合試薬への結合の後に単一添加工程にて添加された検出試薬の結合工程において、分析すべき希釈または非希釈の沈着された可溶化液に含まれるそのリン酸化および/または非リン酸化形態および/またはグリコシル化および/または非グリコシル化形態および/またはメチル化および/または非メチル化形態および/またはアセチル化および/または非アセチル化形態の存在によって識別される、請求項1−20のいずれかの方法。
- 検出すべきであって別々の測定領域に沈着している希釈または非希釈可溶化液に含まれるタンパク質が、添加した特異的結合試薬、および適当であるならば、逐次的に添加されたか、あるいは検出試薬の結合試薬への結合の後に単一添加工程にて添加された検出試薬の結合工程において、分析すべき希釈または非希釈の沈着された可溶化液に含まれるそのリン酸化または非リン酸化形態および/またはグリコシル化または非グリコシル化形態および/またはメチル化または非メチル化形態および/またはアセチル化または非アセチル化形態の存在によって識別されない、請求項1−20のいずれかの方法。
- 直接にまたは接着促進層に媒介されて作成された測定領域に物理的に接触している実質的に平面の固体支持体の材料が実質的に光学的に透明の材料である、請求項1−22のいずれかの方法。
- 固体支持体上にアプライされる接着層の材料が実質的に光学的に透明の材料である、請求項16−23のいずれかの方法。
- 実質的に光学的に透明の固体支持体の材料が、以下を含む群からの材料を含む請求項1−24のいずれかの方法:成形可能、噴霧可能または製粉可能プラスチック、金属、金属酸化物、ガラス、石英またはセラミックスを含むケイ酸塩。
- 1以上の多色または単色光源からのプローブ光が1以上の測定領域のアレイにおける1以上の測定領域に向けられており、該1以上の測定領域のアレイから生じる光シグナルおよび/またはかかる光シグナルの変化が測定および記録される、請求項1−25のいずれかの方法。
- プローブ光が落射照明立体配置にて送達される請求項26の方法。
- プローブ光が透光立体配置にて送達される請求項26の方法。
- 別々の測定領域における1以上のタンパク質の検出が、1以上の発光の強度または発光の強度の変化の検出に基づく、請求項1−28のいずれかの方法。
- 別々の測定領域における1以上のタンパク質の検出が、該測定領域上または測定領域から1μm未満の距離内での屈折率変化の検出に基づく、請求項1−28のいずれかの方法。
- 該測定領域上または測定領域から1μm未満の距離内での屈折率変化の検出が、アプライされた特異的結合パートナーの結合または脱離または移動に起因する、異なる屈折率の材料との接触面から生じる光と測定領域の領域から生じる光との位相差の変化によって生じる、該接触面から生じる光による、固体支持体上に作成された測定領域の領域における平面状の固体支持体から生じる光の干渉パターンの変化の検出に基づき、ここで、相異なる領域から生じる干渉光が、局所的に、および適当であるならば、スペクトル的に分解された様式で測定される、請求項30の方法。
- 固体支持体に、好ましくは銀または金、好ましくは厚さ20 nm〜200 nmの金属薄層が備えられており、該金属薄層が直接にまたは接着促進層に媒介されて測定領域と接触しており、該測定領域上または測定領域から1μm未満の距離内での屈折率変化の検出が該金属層における表面プラズモン共鳴の発生の条件下での変化の検出に基づく、請求項1−30のいずれかの方法。
- 固体支持体が連続した光導波路または個々の導波路領域へと分割される光導波路を含む、請求項1−32のいずれかの方法。
- 光導波路が第一の実質的に光学的に透明の層 (a)よりも屈折率が低い第二の実質的に光学的に透明の層 (b)上にあり、別々の測定領域を担持する表面に面している層 (a)を備えた光学膜導波路である、請求項33の方法。
- プローブ光の光学的に透明の層 (a)へのインカップリングのために、この層が以下を含む群から選択される1以上の光学的インカップリング要素と光学的に接触している請求項34の方法:プリズムカップラー、オーバーラップするエバネセント場を有する光導波路を組み合わせて含むエバネセントカップラー、集束レンズを含む接合部カップラー、好ましくは、導波路層の一面の前に配置されたシリンダーレンズ、および格子カップラー。
- プローブ光が光学的に透明の層 (a)に、光学的に透明の層 (a)に備えられている1以上の格子構造(c)を用いてインカップリングする、請求項35の方法。
- 光学的に透明の層(a)中に導かれる光が光学的に透明の層 (a) に備えられている1以上の格子構造(c')を用いてアウトカップリングする、請求項34−36のいずれかの方法。
- 測定領域におけるタンパク質の検出が、膜導波路として形成された固体支持体の層(a)へのプローブ光のインカップリングのための、または、層(a)において導かれる光のアウトカップリングのための、共鳴条件における変化に基づく、光学膜導波路の層(a)に形成された格子構造を介して行われ、該変化が結合試薬および/またはさらなる検出試薬の、測定領域に含まれるタンパク質との結合に起因する、請求項34−37のいずれかの方法。
- 該光導波路が第一の光学的に透明の層 (a)より屈折率の低い第二の光学的に透明の層(b)上に層 (a)を備えた光学膜導波路として設計され、ここでプローブ光が光学的に透明の層 (a)に備えられた1以上の格子構造の補助によって光学的に透明の層 (a)にさらにインカップリングされ、その上に位置する測定領域 (d)に導波として送達され、ここで、該導波のエバネセント場において生じた発光可能な分子の発光が、さらに1以上の検出器を用いて測定され、そして測定領域に含まれるタンパク質の相対量がこれら発光シグナルの強度から判定される、請求項34−37のいずれかの方法。
- 測定領域における検出すべきタンパク質に特異的に結合している結合試薬と結合した検出試薬の励起により発光が生じ、検出試薬が300 nm〜1100 nmの波長にて励起され得、かつ放射し得る発光標識として用いられる発光色素または発光ナノ粒子を含む、請求項39の方法。
- 相異なる識別可能な検出試薬が、相異なる放射波長および/または相異なる放射半減期を特徴とする、 請求項40の方法。
- プローブ光が持続時間1フェムト秒〜10分間のパルスにて送達され、測定領域からの放射光が時間分解様式で測定される、請求項1−41のいずれかの方法。
- 以下を含む、1以上の細胞集団の光シグナル読み取りおよび定性的および/または定量的タンパク質発現プロファイルの作成のための分析用プラットフォーム:
-実質的に平面の固体支持体、
-該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイ、該アレイは直接に該固体支持体上の、または、固体支持体上にあらかじめアプライされた接着促進層上の別々の部位に、希釈または非希釈形態にて少量の細胞可溶化液を沈着させることによって作成され、該細胞可溶化液は1以上の細胞集団由来であり、かつ、それら細胞集団によって発現される複数のタンパク質を含む、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。 - 以下を含む、光シグナル読み取りおよび1以上の細胞集団の定性的および/または定量的示差的タンパク質発現プロファイルの作成のための分析用プラットフォーム:
-実質的に平面の固体支持体、
-該固体支持体上の別々の測定領域の1以上の1次元または2次元アレイ、該アレイは直接に該固体支持体上の、または、固体支持体上にあらかじめアプライされた接着促進層上の別々の部位に、希釈または非希釈形態にて少量の2以上の細胞可溶化液を沈着させることによって作成され、該細胞可溶化液は2以上の細胞集団由来であり、かつ、それら細胞集団によって発現される複数のタンパク質を含む、
ここで該実質的に平面の固体支持体は無孔性であり、かつ、アプライしてもよい接着促進層は厚さ1μm未満である。 - 相異なる沈着された可溶化液が関連しない細胞集団から作成されたものである請求項43または44の分析用プラットフォーム。
- 相異なる沈着された可溶化液が共通の細胞集団から得た相異なる細胞亜集団から作成されたものである請求項43または44の分析用プラットフォーム。
- 相異なる沈着された可溶化液が共通の細胞集団から相異なる時点にて得られた相異なる細胞亜集団から作成されたものである請求項46の分析用プラットフォーム。
- 相異なる沈着された可溶化液が共通の細胞集団から得られ、その後、相異なる試薬によって処理または刺激された、および/または、相異なる培養条件に曝された、相異なる細胞亜集団から作成されたものである請求項46または47の分析用プラットフォーム。
- 相異なる沈着された可溶化液が疾患細胞集団および健康細胞集団から作成されたものである請求項43−48のいずれかの分析用プラットフォーム。
- 沈着された可溶化液の作成の由来である健康または疾患および/または処理済または非処理および/または刺激細胞集団が、以下を含む群由来である請求項43−49のいずれかの分析用プラットフォーム:細菌を含む原核細胞、およびヒト、動物、または植物細胞を含む真核細胞、特に、器官、皮膚、毛または骨組織を含むヒトまたは動物組織または植物組織、そして血液、血清または血漿、滑液、涙液、尿、唾液、組織液、リンパ液を含む細胞-含有体液またはその構成成分。
- 固体支持体上または該固体支持体上の接着促進層上の別々の部位に沈着された希釈または非希釈形態の可溶化液が、可溶化液の作成由来である細胞集団と、その中で検出すべきタンパク質が同一の相対的な分子の組成を有する、請求項43−50のいずれかの分析用プラットフォーム。
- 沈着された可溶化液がろ過および/または分画および/または希釈以外のさらなるサンプル処理工程に供されていないものである請求項43−50のいずれかの分析用プラットフォーム。
- 一つの測定領域に沈着させた材料が1000未満の細胞のタンパク質含量に対応する請求項43−52のいずれかの分析用プラットフォーム。
- 複数の測定領域のアレイが希釈または非希釈細胞可溶化液の沈着部位が同一の形状となるよう配置され、2つの相異なるアレイにおける測定領域の行および列に関する類似の位置が、その中に沈着させた同一の(希釈または非希釈)細胞可溶化液からの沈着量に対応する、請求項43−53のいずれかの分析用プラットフォーム。
- 固体支持体上にアプライされる接着促進層の厚さが200 nm未満、好ましくは20 nm未満である請求項43−54のいずれかの分析用プラットフォーム。
- 該接着促進層が以下の群の化合物を含む請求項55の分析用プラットフォーム:シラン、官能化シラン、エポキシド、官能化、荷電または極性ポリマーおよび「自立性受動的または官能化単層または多層」、チオール、アルキルホスファートおよびアルキルホスフォナート、ポリ(L)リジン/ポリエチレングリコールを含む多官能性ブロックコポリマー。
- 別々の測定領域の間の領域がトレーサー化合物の非特異的結合を最小にするために「不動態化」されており、即ち、結合試薬および、適当であるならば検出試薬に対して「化学的に中立」(即ち非結合性)の化合物が横方向に分離した測定領域の間に沈着されている請求項43−56のいずれかの分析用プラットフォーム。
- 検出すべきであって、別々の測定領域に沈着させた希釈または非希釈可溶化液に含まれるタンパク質が以下を含むタンパク質の群の化合物である請求項43−57のいずれかの分析用プラットフォーム:細胞質タンパク質、核タンパク質および膜タンパク質、体液中に分泌されたタンパク質(細胞質タンパク質および膜結合型細胞タンパク質、特にキナーゼを含む細胞におけるシグナル伝達過程に関与するタンパク質)、リン酸化、グリコシル化、メチル化、およびアセチル化形態のタンパク質を含む翻訳後修飾タンパク質、特に処理の下で過剰発現および/または過小発現したタンパク質、抗体、人工的に過剰発現させたタンパク質、さらなる結合部位を備えた官能化タンパク質を含む人工的に過剰発現させた修飾タンパク質(「ヒスチジンタグタンパク質」を含む「タグタンパク質」)、および蛍光タンパク質(「緑色蛍光タンパク質」、GFPを含む)。
- 直接にまたは接着促進層に媒介されて作成された測定領域と物理的に接触している実質的に平面の固体支持体の材料が実質的に光学的に透明である請求項43−58のいずれかの分析用プラットフォーム。
- 固体支持体上にアプライされた接着層の材料が実質的に光学的に透明である請求項43−59のいずれかの分析用プラットフォーム。
- 実質的に光学的に透明の固体支持体の材料が以下を含む群からの材料を含む請求項43−60のいずれかの分析用プラットフォーム:成形可能、噴霧可能または製粉可能プラスチック、金属、金属酸化物、ガラス、石英またはセラミックスを含むケイ酸塩。
- 固体支持体が、好ましくは銀または金であり、好ましくは厚さが20 nm〜200 nmである、金属薄層を備えており、該金属薄層が直接にまたは接着促進層に媒介されて測定領域と接触しており、プラットフォームが該金属層における表面プラズモン共鳴の生成のために作動可能である請求項43−61のいずれかの分析用プラットフォーム。
- 固体支持体が連続した光導波路または個々の導波路領域へと分割される光導波路を含む請求項43−62のいずれかの分析用プラットフォーム。
- 光導波路が第一の実質的に光学的に透明の層 (a)よりも屈折率が低い第二の実質的に光学的に透明の層 (b)上にあり、別々の測定領域を担持する表面に面している層 (a)を備えた光学膜導波路である請求項63の分析用プラットフォーム。
- プローブ光の光学的に透明の層 (a)へのインカップリングのために、層 (a)が以下を含む群からの1以上の光学的インカップリング要素と光学的に接触している請求項64の分析用プラットフォーム:プリズムカップラー、オーバーラップするエバネセント場を備える光導波路と組み合わされたエバネセントカップラー、集束レンズ、好ましくは、導波路層の一面の前に配置されたシリンダーレンズを備える接合部カップラー、および格子カップラー。
- 1以上の格子構造 (c)がプローブ光の光学的に透明の層 (a)へのインカップリングを可能とするために光学的に透明の層 (a)に備えられている請求項65の分析用プラットフォーム。
- 1以上の格子構造(c')が光学的に透明の層 (a)に備えられており、光学的に透明の層 (a)において導かれた光のアウトカップリングを可能とする請求項64−66のいずれかの分析用プラットフォーム。
- 該光導波路が第一の光学的に透明の層 (a)より屈折率が低い第二の光学的に透明の層 (b)上の層 (a)を備えた光学膜導波路として設計されており、分析用プラットフォームが光学的に透明の層 (a)に備えられた1以上の格子構造の補助による光学的に透明の層 (a)へのプローブ光のインカップリング、該プローブ光の導波としての測定領域(d)への送達、および該導波のエバネセント場における発光可能な分子の発光の励起に対して作動可能である、請求項64−67のいずれかの分析用プラットフォーム。
- 医薬研究におけるスクリーニング方法、コンビナトリアルケミストリー、臨床および前臨床開発におけるタンパク質およびその修飾形態の測定のため、リアルタイム結合研究および親和性スクリーニングおよび研究における動力学的パラメーターの測定のため、特にプロテオームにおけるプロテオームの差異の測定のため、タンパク質-DNA 相互作用の測定のため、タンパク質 (生)合成の制御メカニズムの判定のため、生物学的および化学的マーカー化合物のスクリーニングのため、医薬品開発における患者の層別化のため、および治療薬選択のための、請求項1−42のいずれかの方法および/または請求項43−68のいずれかの分析用プラットフォームの、定量的および/または定性的分析のための使用。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/EP2004/002127 WO2005095965A1 (en) | 2004-03-03 | 2004-03-03 | Analytical platform and method for generating protein expression profiles of cell populations |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007526460A true JP2007526460A (ja) | 2007-09-13 |
| JP2007526460A5 JP2007526460A5 (ja) | 2011-02-24 |
Family
ID=34957113
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007501122A Pending JP2007526460A (ja) | 2004-03-03 | 2004-03-03 | 細胞集団のタンパク質発現プロファイルの作成のための分析用プラットフォームおよび方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20080020409A1 (ja) |
| EP (1) | EP1730530A1 (ja) |
| JP (1) | JP2007526460A (ja) |
| CN (1) | CN1954213A (ja) |
| AU (1) | AU2004318038A1 (ja) |
| CA (1) | CA2559803A1 (ja) |
| WO (1) | WO2005095965A1 (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014516644A (ja) * | 2011-04-29 | 2014-07-17 | セブンス センス バイオシステムズ,インコーポレーテッド | 血斑または他の体液の収集および/または操作のためのデバイスおよび方法 |
| US9730624B2 (en) | 2009-03-02 | 2017-08-15 | Seventh Sense Biosystems, Inc. | Delivering and/or receiving fluids |
| US9775551B2 (en) | 2009-03-02 | 2017-10-03 | Seventh Sense Biosystems, Inc. | Devices and techniques associated with diagnostics, therapies, and other applications, including skin-associated applications |
| JP2017536106A (ja) * | 2014-06-03 | 2017-12-07 | 韓国科学技術院Korea Advanced Institute Of Science And Technology | シグナル伝達経路の活性化状態の分析方法およびこれを用いた個人向け治療剤の選定方法 |
| US10543310B2 (en) | 2011-12-19 | 2020-01-28 | Seventh Sense Biosystems, Inc. | Delivering and/or receiving material with respect to a subject surface |
| US10835163B2 (en) | 2011-04-29 | 2020-11-17 | Seventh Sense Biosystems, Inc. | Systems and methods for collecting fluid from a subject |
| US11177029B2 (en) | 2010-08-13 | 2021-11-16 | Yourbio Health, Inc. | Systems and techniques for monitoring subjects |
| US11202895B2 (en) | 2010-07-26 | 2021-12-21 | Yourbio Health, Inc. | Rapid delivery and/or receiving of fluids |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BRPI0717416A2 (pt) | 2006-09-21 | 2013-11-12 | Prometheus Lab Inc | Método para realizar um imunoensaio complexo de alta produtividade, e, arranjo |
| EP2064549B1 (en) * | 2006-09-21 | 2012-10-24 | Prometheus Laboratories, Inc. | Antibody-based arrays for detecting multiple signal transducers in rare circulating cells |
| WO2011008990A1 (en) | 2009-07-15 | 2011-01-20 | Prometheus Laboratories Inc. | Drug selection for gastric cancer therapy using antibody-based arrays |
| RU2519647C2 (ru) | 2007-07-13 | 2014-06-20 | Нестек С.А. | Выбор лекарственных средств для терапии рака легких с помощью матриц на основе антител |
| CA2923248A1 (en) | 2008-02-25 | 2009-09-03 | Nestec S.A. | Methods for detecting truncated receptors |
| WO2012046412A1 (ja) * | 2010-10-07 | 2012-04-12 | パナソニック株式会社 | プラズモンセンサ |
| US9719995B2 (en) | 2011-02-03 | 2017-08-01 | Pierian Holdings, Inc. | Drug selection for colorectal cancer therapy using receptor tyrosine kinase profiling |
| WO2013033623A1 (en) | 2011-09-02 | 2013-03-07 | Nestec S.A. | Profiling of signal pathway proteins to determine therapeutic efficacy |
| EP2573565A1 (en) | 2011-09-23 | 2013-03-27 | Gerhard Matthias Kresbach | Immune detection method for common epitopes of two or more analytes in samples of complex compositions, device, and kit for enabling said immune detection method |
| US20150347680A1 (en) * | 2013-01-10 | 2015-12-03 | Emory University | Systems, methods and computer readable storage media for analyzing a sample |
| JP2016148655A (ja) * | 2015-02-05 | 2016-08-18 | 日東電工株式会社 | 計測装置 |
| AU2017298742A1 (en) * | 2016-07-19 | 2019-01-31 | National Agriculture And Food Research Organization | Method for introducing substance into plant cell using plasma |
| US10520514B2 (en) * | 2017-02-01 | 2019-12-31 | Korea Institute Of Science And Technology | Method for monitoring post-translational modification of protein |
| US11391735B2 (en) * | 2017-09-06 | 2022-07-19 | AimPlex Biosciences, Inc. | Methods for improving the dynamic range of biological assays |
| KR102342302B1 (ko) * | 2018-09-28 | 2021-12-24 | 주식회사 스몰머신즈 | 정량 분석용 단백질 칩 |
| CN110609078B (zh) * | 2019-09-20 | 2022-03-11 | 南京谱利健生物技术有限公司 | 一种检测蛋白磷酸化和乙酰氨基葡萄糖化关联作用的方法 |
| CN114112305B (zh) * | 2021-12-06 | 2024-02-06 | 西南石油大学 | 一种内外流夹击的柔性立管流固耦合效应测试装置及方法 |
| CN113970644B (zh) * | 2021-12-24 | 2022-05-27 | 天德瑞(北京)生物科技有限公司 | 基于hrp标记蛋白的工作浓度检测方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001092870A2 (de) * | 2000-06-02 | 2001-12-06 | Zeptosens Ag | Kit und verfahren zur multianalytbestimmung |
| WO2002023199A2 (en) * | 2000-09-14 | 2002-03-21 | Reverse Proteomics Research Institute Co., Ltd. | Method, system, apparatus and device for discovering and preparing chemical compounds |
| WO2004009639A1 (ja) * | 2002-07-18 | 2004-01-29 | Cellfree Sciences Co., Ltd. | 単鎖抗体およびその利用 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2190362A1 (en) * | 1994-05-27 | 1995-12-07 | Gert L. Duveneck | Process for detecting evanescently excited luminescence |
| PL323257A1 (en) * | 1995-05-12 | 1998-03-16 | Ciba Geigy Ag | Detection platform for simultaneously detecting plurality of analytes using hypercritically excited luminescence |
| DE19628928A1 (de) * | 1996-07-18 | 1998-01-22 | Basf Ag | Feste Träger für analytische Meßverfahren, ein Verfahren zu ihrer Herstellung sowie ihre Verwendung |
| US6395558B1 (en) * | 1996-08-29 | 2002-05-28 | Zeptosens Ag | Optical chemical/biochemical sensor |
| US6087102A (en) * | 1998-01-07 | 2000-07-11 | Clontech Laboratories, Inc. | Polymeric arrays and methods for their use in binding assays |
| CA2317816C (en) * | 1998-01-09 | 2009-02-17 | Tvw Telethon Institute For Child Health Research | Peptide detection method |
| US6197599B1 (en) * | 1998-07-30 | 2001-03-06 | Guorong Chin | Method to detect proteins |
| AU757052B2 (en) * | 1998-09-09 | 2003-01-30 | Dart Neuroscience (Cayman) Ltd | Substituted gamma-phenyl-delta-lactones and analogs thereof and uses related thereto |
| US20030027214A1 (en) * | 1999-02-17 | 2003-02-06 | Kamb Carl Alexander | Methods for substrate-ligand interaction screening |
| US6972198B2 (en) * | 1999-02-26 | 2005-12-06 | Cyclacel, Ltd. | Methods and compositions using protein binding partners |
| GB0007088D0 (en) * | 2000-03-23 | 2000-05-17 | Torsana A S | Detection of immunological memory determining the position of loci of pathologyand therapeutic t-cell conjugates |
| WO2001084197A1 (en) * | 2000-04-28 | 2001-11-08 | Edgelight Biosciences, Inc. | Micro-array evanescent wave fluorescence detection device |
| DE50113602D1 (de) * | 2000-09-05 | 2008-03-27 | Bayer Technology Services Gmbh | Verfahren zur abscheidung von mono- und mehrfachscd deren salzen sowie deren verwendung |
| US7070740B1 (en) * | 2000-09-28 | 2006-07-04 | Beckman Coulter, Inc. | Method and apparatus for processing biomolecule arrays |
| US7332286B2 (en) * | 2001-02-02 | 2008-02-19 | University Of Pennsylvania | Peptide or protein microassay method and apparatus |
| WO2003091418A2 (en) * | 2002-04-26 | 2003-11-06 | Bristol-Myers Squibb Company | Novel essential fungal polynucleotides, polypeptides, and methods of use |
| WO2004023143A2 (de) * | 2002-09-03 | 2004-03-18 | Zeptosens Ag | Analytische plattform und nachweisverfahren |
| US6956651B2 (en) * | 2002-09-07 | 2005-10-18 | Hilary S. Lackritz | Bioanalysis systems including optical integrated circuit |
-
2004
- 2004-03-03 WO PCT/EP2004/002127 patent/WO2005095965A1/en active Application Filing
- 2004-03-03 CN CNA2004800422474A patent/CN1954213A/zh active Pending
- 2004-03-03 EP EP04716582A patent/EP1730530A1/en not_active Withdrawn
- 2004-03-03 JP JP2007501122A patent/JP2007526460A/ja active Pending
- 2004-03-03 CA CA002559803A patent/CA2559803A1/en not_active Abandoned
- 2004-03-03 AU AU2004318038A patent/AU2004318038A1/en not_active Abandoned
- 2004-03-03 US US10/598,418 patent/US20080020409A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001092870A2 (de) * | 2000-06-02 | 2001-12-06 | Zeptosens Ag | Kit und verfahren zur multianalytbestimmung |
| WO2002023199A2 (en) * | 2000-09-14 | 2002-03-21 | Reverse Proteomics Research Institute Co., Ltd. | Method, system, apparatus and device for discovering and preparing chemical compounds |
| WO2004009639A1 (ja) * | 2002-07-18 | 2004-01-29 | Cellfree Sciences Co., Ltd. | 単鎖抗体およびその利用 |
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9730624B2 (en) | 2009-03-02 | 2017-08-15 | Seventh Sense Biosystems, Inc. | Delivering and/or receiving fluids |
| US9775551B2 (en) | 2009-03-02 | 2017-10-03 | Seventh Sense Biosystems, Inc. | Devices and techniques associated with diagnostics, therapies, and other applications, including skin-associated applications |
| US10799166B2 (en) | 2009-03-02 | 2020-10-13 | Seventh Sense Biosystems, Inc. | Delivering and/or receiving fluids |
| US11202895B2 (en) | 2010-07-26 | 2021-12-21 | Yourbio Health, Inc. | Rapid delivery and/or receiving of fluids |
| US11177029B2 (en) | 2010-08-13 | 2021-11-16 | Yourbio Health, Inc. | Systems and techniques for monitoring subjects |
| JP2014516644A (ja) * | 2011-04-29 | 2014-07-17 | セブンス センス バイオシステムズ,インコーポレーテッド | 血斑または他の体液の収集および/または操作のためのデバイスおよび方法 |
| US10188335B2 (en) | 2011-04-29 | 2019-01-29 | Seventh Sense Biosystems, Inc. | Plasma or serum production and removal of fluids under reduced pressure |
| US10835163B2 (en) | 2011-04-29 | 2020-11-17 | Seventh Sense Biosystems, Inc. | Systems and methods for collecting fluid from a subject |
| US11253179B2 (en) | 2011-04-29 | 2022-02-22 | Yourbio Health, Inc. | Systems and methods for collection and/or manipulation of blood spots or other bodily fluids |
| US10543310B2 (en) | 2011-12-19 | 2020-01-28 | Seventh Sense Biosystems, Inc. | Delivering and/or receiving material with respect to a subject surface |
| JP2017536106A (ja) * | 2014-06-03 | 2017-12-07 | 韓国科学技術院Korea Advanced Institute Of Science And Technology | シグナル伝達経路の活性化状態の分析方法およびこれを用いた個人向け治療剤の選定方法 |
| JP2020156490A (ja) * | 2014-06-03 | 2020-10-01 | 韓国科学技術院Korea Advanced Institute Of Science And Technology | シグナル伝達経路の活性化状態の分析方法およびこれを用いた個人向け治療剤の選定方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1954213A (zh) | 2007-04-25 |
| EP1730530A1 (en) | 2006-12-13 |
| AU2004318038A1 (en) | 2005-10-13 |
| WO2005095965A1 (en) | 2005-10-13 |
| US20080020409A1 (en) | 2008-01-24 |
| CA2559803A1 (en) | 2005-10-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2007526460A (ja) | 細胞集団のタンパク質発現プロファイルの作成のための分析用プラットフォームおよび方法 | |
| US7955837B2 (en) | Process for determining one or more analytes in samples of biological origin having complex composition, and use thereof | |
| JP2005537487A (ja) | 試料中において任意には分画された後の試料中において、固定化特異的結合パートナーとして測定される分析対象物を用いる分析プラットフォーム及び検出法 | |
| JP5006494B2 (ja) | 複数の分析物を測定するためのデバイス及び方法 | |
| JP2007526460A5 (ja) | ||
| US7175811B2 (en) | Micro-array evanescent wave fluorescence detection device | |
| US7396675B2 (en) | Kit and method for determining a plurality of analytes | |
| JP2004510130A5 (ja) | ||
| JP2005537486A (ja) | 分析対象物が試料中で固定化された特異的結合パートナーとして測定される分析プラットフォーム及び検出法 | |
| EP1512012B1 (en) | Biomolecular kinetics method using a flow-through microarray | |
| US9823241B2 (en) | Processing of a sample fluid with target components | |
| ES2369494T3 (es) | Plataforma analítica y procedimiento de detección con analitos a detectar en una muestra eventualmente después del fraccionamiento como asociados de unión específicos inmovilizados. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091027 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100126 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100202 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100301 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100308 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100329 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101005 |
|
| A524 | Written submission of copy of amendment under section 19 (pct) |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20110105 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110920 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120228 |