JP2005015460A - Sgltホモログ用途 - Google Patents
Sgltホモログ用途 Download PDFInfo
- Publication number
- JP2005015460A JP2005015460A JP2003366734A JP2003366734A JP2005015460A JP 2005015460 A JP2005015460 A JP 2005015460A JP 2003366734 A JP2003366734 A JP 2003366734A JP 2003366734 A JP2003366734 A JP 2003366734A JP 2005015460 A JP2005015460 A JP 2005015460A
- Authority
- JP
- Japan
- Prior art keywords
- sglt
- glucose
- seq
- protein
- present
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
【解決手段】Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害または促進する化合物またはその塩を含有してなる小腸でのグルコース取り込み阻害または促進剤など。
【選択図】なし
Description
日本臨床 55, 1997、増刊号、糖尿病I、59-64
(1)Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩を含有してなる小腸でのグルコース取り込み阻害剤;
(2)Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を阻害する化合物またはその塩を含有してなる小腸でのグルコース取り込み阻害剤;
(3)食後過血糖改善剤である前記(1)または(2)記載の剤;
(4)糖尿病または高脂血症予防・治療剤である前記(1)ないし(3)記載の剤;
(5)Na+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩を含有してなる小腸でのグルコース取り込み促進剤;
(6)Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を促進する化合物またはその塩を含有してなる小腸でのグルコース取り込み促進剤;
(7)グルコースの吸収促進剤である前記(5)または(6)記載の剤;
(8)Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:1で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である前記(1)ないし(7)記載の剤;
(9)Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:3で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である前記(1)ないし(7)記載の剤;
(10)Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:5または配列番号:50で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である前記(1)ないし(7)記載の剤;
(11)Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドの塩基配列に相補的もしくは実質的に相補的な塩基配列またはその一部分を含有するアンチセンスポリヌクレオチドを含有してなる小腸でのグルコース取り込み阻害剤;
(12)食後過血糖改善剤である前記(11)記載の剤;
(13)糖尿病または高脂血症の予防・治療剤である前記(11)または(12)記載の剤;
(14)Na+/グルコーストランスポーター (SGLT)ホモログをコードするポリヌクレオチドが配列番号:2、配列番号:4、配列番号:6または配列番号:51で表される塩基配列と同一もしくは実質的に同一の塩基配列を含有するポリヌクレオチドである前記(11)ないし(13)記載の剤;
(15)Na+/グルコーストランスポーター (SGLT) ホモログに対する抗体を含有してなる小腸でのグルコース取り込み阻害剤;
(16)食後過血糖改善剤である前記(15)記載の剤;
(17)糖尿病または高脂血症予防・治療剤である前記(15)または(16)記載の剤;
(18)Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:1、配列番号:3、配列番号:5または配列番号:50で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である前記(15)ないし(17)記載の剤;
(19)Na+/グルコーストランスポーター (SGLT) ホモログに対する抗体を含有してなる食後過血糖の診断薬;
(20)Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドを含有してなる食後過血糖の診断薬;
(21)Na+/グルコーストランスポーター (SGLT) ホモログを用いることを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング方法;
(22)Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:1、配列番号:3、配列番号:5または配列番号:50で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である前記(21)記載のスクリーニング方法;
(23)Na+/グルコーストランスポーター (SGLT) ホモログを含有することを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング用キット;
(24)前記(21)もしくは(22)記載のスクリーニング方法または前記(23)記載のスクリーニング用キットを用いて得られうる化合物またはその塩;
(25)前記(24)記載の化合物またはその塩を含有してなる医薬;
(26)食後過血糖改善剤である前記(25)記載の医薬;
(27)糖尿病または高脂血症予防・治療剤である前記(25)または(26)記載の医薬;
(28)Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドを用いることを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング方法;
(29)Na+/グルコーストランスポーター (SGLT)ホモログをコードするポリヌクレオチドが配列番号:2、配列番号:4、配列番号:6または配列番号:51で表される塩基配列と同一もしくは実質的に同一の塩基配列を含有するポリヌクレオチドである前記(28)記載のスクリーニング方法;
(30)Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドを用いることを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング用キット;
(31)前記(28)もしくは(29)記載のスクリーニング方法または前記(30)記載のスクリーニング用キットを用いて得られうる化合物またはその塩;
(32)前記(31)記載の化合物またはその塩を含有してなる医薬;
(33)食後過血糖改善剤である前記(32)記載の医薬;
(34)糖尿病または高脂血症予防・治療剤である前記(32)または(33)記載の医薬;
(35)Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害することを特徴とする小腸でのグルコース取り込み阻害方法;
(36)Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を阻害することを特徴とする小腸でのグルコース取り込み阻害方法;
(37)食後過血糖改善方法である前記(35)または(36)記載の方法;
(38)糖尿病または高脂血症予防・治療方法である前記(35)ないし(37)記載の方法;
(39)Na+/グルコーストランスポーター (SGLT) ホモログの活性を促進することを特徴とする小腸でのグルコース取り込み促進方法;
(40)Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を促進することを特徴とする小腸でのグルコース取り込み促進方法;
(41)グルコースの吸収促進方法である前記(39)または(40)記載の方法;
(42)Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み阻害方法;
(43)Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を阻害する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み阻害方法;
(44)食後過血糖改善方法である前記(42)または(43)記載の方法;
(45)糖尿病または高脂血症予防・治療方法である前記(42)ないし(44)記載の方法;
(46)Na+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み促進方法;
(47)Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を促進する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み促進方法;
(48)グルコースの吸収促進方法である前記(46)または(47)記載の方法;
(49)小腸でのグルコース取り込み阻害剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩の使用;
(50)小腸でのグルコース取り込み阻害剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩の使用;
(51)小腸でのグルコース取り込み阻害剤が食後過血糖改善剤である前記(49)または(50)記載の使用;
(52)小腸でのグルコース取り込み阻害剤が糖尿病または高脂血症予防・治療剤である前記(49)ないし(51)記載の使用;
(53)小腸でのグルコース取り込み促進剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩の使用;
(54)小腸でのグルコース取り込み促進剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩の使用;
(55)小腸でのグルコース取り込み促進剤がグルコースの吸収促進剤である前記(53)または(54)記載の使用;などに関する。
(i)M. Bodanszky および M.A. Ondetti、ペプチド・シンセシス (Peptide Synthesis), Interscience Publishers, New York (1966年)
(ii)SchroederおよびLuebke、ザ・ペプチド(The Peptide), Academic Press, New York (1965年)
(iii)泉屋信夫他、ペプチド合成の基礎と実験、 丸善(株) (1975年)
(iv)矢島治明 および榊原俊平、生化学実験講座 1、 タンパク質の化学IV、 205、(1977年)
(v)矢島治明監修、続医薬品の開発、第14巻、ペプチド合成、広川書店
また、反応後は通常の精製法、例えば、溶媒抽出・蒸留・カラムクロマトグラフィー・液体クロマトグラフィー・再結晶などを組み合わせて本発明で用いられる部分ペプチドを精製単離することができる。上記方法で得られる部分ペプチドが遊離体である場合は、公知の方法あるいはそれに準じる方法によって適当な塩に変換することができるし、逆に塩で得られた場合は、公知の方法あるいはそれに準じる方法によって遊離体または他の塩に変換することができる。
〔モノクローナル抗体の作製〕
(a)モノクローナル抗体産生細胞の作製
本発明のタンパク質は、温血動物に対して投与により抗体産生が可能な部位にそれ自体あるいは担体、希釈剤とともに投与される。投与に際して抗体産生能を高めるため、完全フロイントアジュバントや不完全フロイントアジュバントを投与してもよい。投与は通常2〜6週毎に1回ずつ、計2〜10回程度行われる。用いられる温血動物としては、例えば、サル、ウサギ、イヌ、モルモット、マウス、ラット、ヒツジ、ヤギ、ニワトリが挙げられるが、マウスおよびラットが好ましく用いられる。
(b)モノクローナル抗体の精製
モノクローナル抗体の分離精製は、自体公知の方法、例えば、免疫グロブリンの分離精製法〔例、塩析法、アルコール沈殿法、等電点沈殿法、電気泳動法、イオン交換体(例、DEAE)による吸脱着法、超遠心法、ゲルろ過法、抗原結合固相あるいはプロテインAあるいはプロテインGなどの活性吸着剤により抗体のみを採取し、結合を解離させて抗体を得る特異的精製法〕に従って行なうことができる。
〔ポリクローナル抗体の作製〕
本発明のポリクローナル抗体は、それ自体公知あるいはそれに準じる方法に従って製造することができる。例えば、免疫抗原(タンパク質抗原)自体、あるいはそれとキャリアー蛋白質との複合体をつくり、上記のモノクローナル抗体の製造法と同様に温血動物に免疫を行ない、該免疫動物から本発明のタンパク質に対する抗体含有物を採取して、抗体の分離精製を行なうことにより製造することができる。
(1)本発明のタンパク質が関与する各種疾病の予防・治療剤
本発明のタンパク質は、Na+/グルコーストランスポーターとしてグルコースの能動輸送活性を有し、小腸においては、グルコース取り込みに寄与している。
本明細書において、「小腸」とは広義の小腸(即ち、十二指腸を含む)を示してもよいが、好ましくは狭義の小腸(即ち、十二指腸を含まない)を示す。また、グルコースの取り込みは、単糖類(例えば、グルコース、マンノース、フルクトース、ソルボース、ガラクトース、リボース、アラビノース、キシロースなど)の取り込みに読み替えてもよいが、好ましくはグルコースの取り込みを示す。
(2)疾病に対する医薬候補化合物のスクリーニング
本発明のタンパク質の活性を調節(促進または阻害、好ましくは阻害)する化合物もしくはその塩、本発明のタンパク質の遺伝子の発現を調節(促進または阻害、好ましくは阻害)する化合物もしくはその塩は、例えば、食後過血糖改善剤またはグルコースの吸収促進剤などとして使用することができる。好ましくは食後過血糖改善剤などである。
(1)本発明のタンパク質を用いることを特徴とする本発明のタンパク質の活性(例えば、グルコースの能動輸送活性など)を促進または阻害する化合物またはその塩(以下、それぞれ促進剤、阻害剤と略記する場合がある)のスクリーニング方法を提供し、より具体的には、例えば、
(2)(i)本発明のタンパク質を産生する能力を有する細胞の糖取り込み活性と(ii)本発明のタンパク質を産生する能力を有する細胞と試験化合物の混合物の糖取り込み活性の比較を行なうことを特徴とする促進剤または阻害剤のスクリーニング方法を提供する。
(i)本発明のタンパク質を産生する能力を有する細胞に、3H標識したグルコースまたはグルコース類縁体を取り込ませると同時もしくは取り込ませる前に、グルコースの能動輸送活性阻害剤を添加した場合と、(ii) 本発明のタンパク質を産生する能力を有する細胞に、3H標識したグルコースまたはグルコース類縁体を取り込ませると同時もしくは取り込ませる前に、グルコースの能動輸送活性賦活化剤または阻害剤、および試験化合物を添加した場合とを比較し、その取り込み量の変化を測定することを特徴とする促進剤または阻害剤のスクリーニング方法を提供する。
(2a)本発明のタンパク質、その部分ペプチドまたはその塩の定量
本発明のタンパク質に対する抗体(以下、本発明の抗体と略記する場合がある)は、本発明のタンパク質を特異的に認識することができるので、被検液中の本発明のタンパク質の定量、特にサンドイッチ免疫測定法による定量などに使用することができる。
(i)本発明の抗体と、被検液および標識化された本発明のタンパク質とを競合的に反応させ、該抗体に結合した標識化された本発明のタンパク質の割合を測定することを特徴とする被検液中の本発明のタンパク質の定量法、および
(ii)被検液と担体上に不溶化した本発明の抗体および標識化された本発明の別の抗体とを同時あるいは連続的に反応させたのち、不溶化担体上の標識剤の活性を測定することを特徴とする被検液中の本発明のタンパク質の定量法を提供する。
(3)遺伝子診断薬
本発明のDNAは、例えば、プローブとして使用することにより、ヒトまたは温血動物(例えば、ラット、マウス、モルモット、ウサギ、トリ、ヒツジ、ブタ、ウシ、ウマ、イヌ、ネコ、サル、チンパンジーなど)における本発明のタンパク質または部分ペプチドをコードするDNAまたはmRNAの異常(遺伝子異常)を検出することができるので、例えば、該DNAまたはmRNAの損傷、突然変異あるいは発現低下や、該DNAまたはmRNAの増加あるいは発現過多などの遺伝子診断薬として有用である。
(4)アンチセンスポリヌクレオチドを含有する医薬
本発明のDNAに相補的に結合し、該DNAの発現を調節することができるアンチセンスポリヌクレオチドは低毒性であり、生体内における本発明のタンパク質または本発明のDNAの機能を調節(好ましくは抑制)することができるので、例えば、食後過血糖改善剤などとして使用することができる。
例えば、該アンチセンスポリヌクレオチドを用いる場合、該アンチセンスポリヌクレオチドを単独あるいはレトロウイルスベクター、アデノウイルスベクター、アデノウイルスアソシエイテッドウイルスベクターなどの適当なベクターに挿入した後、常套手段にしたがって、ヒトまたは哺乳動物(例えば、ラット、ウサギ、ヒツジ、ブタ、ウシ、ネコ、イヌ、サルなど)に対して経口的または非経口的に投与することができる。該アンチセンスポリヌクレオチドはそのままで、あるいは摂取促進のために補助剤などの生理学的に認められる担体とともに製剤化し、遺伝子銃やハイドロゲルカテーテルのようなカテーテルによって投与できる。あるいは、エアロゾル化して吸入剤として気管内に局所投与することもできる。
(5)本発明の抗体を含有する医薬
本発明のタンパク質の活性を中和する作用を有する本発明の抗体は、例えば食後過血糖改善剤などの予防・治療剤などの医薬もしくは診断薬として使用することができる。
(6)DNA転移動物
本発明は、外来性の本発明のタンパク質をコードするDNA(以下、本発明の外来性DNAと略記する)またはその変異DNA(本発明の外来性変異DNAと略記する場合がある)を有する非ヒト哺乳動物を提供する。
(1)本発明の外来性DNAまたはその変異DNAを有する非ヒト哺乳動物、
(2)非ヒト哺乳動物がゲッ歯動物である第(1)記載の動物、
(3)ゲッ歯動物がマウスまたはラットである第(2)記載の動物、および
(4)本発明の外来性DNAまたはその変異DNAを含有し、哺乳動物において発現しうる組換えベクターを提供するものである。
1)組織培養のための細胞源としての使用、
2)本発明のDNA転移動物の組織中のDNAもしくはRNAを直接分析するか、またはDNAにより発現されたペプチド組織を分析することによる、本発明のタンパク質により特異的に発現あるいは活性化するペプチドとの関連性についての解析、
3)DNAを有する組織の細胞を標準組織培養技術により培養し、これらを使用して、一般に培養困難な組織からの細胞の機能の研究、
4)上記3)記載の細胞を用いることによる細胞の機能を高めるような薬剤のスクリーニング、および
5)本発明の変異タンパク質を単離精製およびその抗体作製などが考えられる。
(7)ノックアウト動物
本発明は、本発明のDNAが不活性化された非ヒト哺乳動物胚幹細胞および本発明のDNA発現不全非ヒト哺乳動物を提供する。
(1)本発明のDNAが不活性化された非ヒト哺乳動物胚幹細胞、
(2)該DNAがレポーター遺伝子(例、大腸菌由来のβ−ガラクトシダーゼ遺伝子)を導入することにより不活性化された第(1)項記載の胚幹細胞、
(3)ネオマイシン耐性である第(1)項記載の胚幹細胞、
(4)非ヒト哺乳動物がゲッ歯動物である第(1)項記載の胚幹細胞、
(5)ゲッ歯動物がマウスである第(4)項記載の胚幹細胞、
(6)本発明のDNAが不活性化された該DNA発現不全非ヒト哺乳動物、
(7)該DNAがレポーター遺伝子(例、大腸菌由来のβ−ガラクトシダーゼ遺伝子)を導入することにより不活性化され、該レポーター遺伝子が本発明のDNAに対するプロモーターの制御下で発現しうる第(6)項記載の非ヒト哺乳動物、
(8)非ヒト哺乳動物がゲッ歯動物である第(6)項記載の非ヒト哺乳動物、
(9)ゲッ歯動物がマウスである第(8)項記載の非ヒト哺乳動物、および
(10)第(7)項記載の動物に、試験化合物を投与し、レポーター遺伝子の発現を検出することを特徴とする本発明のDNAに対するプロモーター活性を促進または阻害する化合物またはその塩のスクリーニング方法を提供する。
(8a)本発明のDNAの欠損や損傷などに起因する疾病に対して治療・予防効果を有する化合物のスクリーニング方法
本発明のDNA発現不全非ヒト哺乳動物は、本発明のDNAの欠損や損傷などに起因する疾病に対して治療・予防効果を有する化合物のスクリーニングに用いることができる。
(8b)本発明のDNAに対するプロモーターの活性を促進または阻害する化合物をスクリーニング方法
本発明は、本発明のDNA発現不全非ヒト哺乳動物に、試験化合物を投与し、レポーター遺伝子の発現を検出することを特徴とする本発明のDNAに対するプロモーターの活性を促進または阻害する化合物またはその塩のスクリーニング方法を提供する。
DNA :デオキシリボ核酸
cDNA :相補的デオキシリボ核酸
A :アデニン
T :チミン
G :グアニン
C :シトシン
RNA :リボ核酸
mRNA :メッセンジャーリボ核酸
dATP :デオキシアデノシン三リン酸
dTTP :デオキシチミジン三リン酸
dGTP :デオキシグアノシン三リン酸
dCTP :デオキシシチジン三リン酸
ATP :アデノシン三リン酸
EDTA :エチレンジアミン四酢酸
SDS :ドデシル硫酸ナトリウム
Gly :グリシン
Ala :アラニン
Val :バリン
Leu :ロイシン
Ile :イソロイシン
Ser :セリン
Thr :スレオニン
Cys :システイン
Met :メチオニン
Glu :グルタミン酸
Asp :アスパラギン酸
Lys :リジン
Arg :アルギニン
His :ヒスチジン
Phe :フェニルアラニン
Tyr :チロシン
Trp :トリプトファン
Pro :プロリン
Asn :アスパラギン
Gln :グルタミン
pGlu :ピログルタミン酸
Sec :セレノシステイン(selenocysteine)
また、本明細書中で繁用される置換基、保護基および試薬を下記の記号で表記する。
Me :メチル基
Et :エチル基
Bu :ブチル基
Ph :フェニル基
TC :チアゾリジン−4(R)−カルボキサミド基
Tos :p−トルエンスルフォニル
CHO :ホルミル
Bzl :ベンジル
Cl2-Bzl :2,6−ジクロロベンジル
Bom :ベンジルオキシメチル
Z :ベンジルオキシカルボニル
Cl−Z :2−クロロベンジルオキシカルボニル
Br−Z :2−ブロモベンジルオキシカルボニル
Boc :t−ブトキシカルボニル
DNP :ジニトロフェニル
Trt :トリチル
Bum :t−ブトキシメチル
Fmoc :N−9−フルオレニルメトキシカルボニル
HOBt :1−ヒドロキシベンズトリアゾール
HOOBt :3,4−ジヒドロ−3−ヒドロキシ−4−オキソ−1,2,3−ベンゾトリアジン
HONB :1-ヒドロキシ-5-ノルボルネン-2,3-ジカルボキシイミド
DCC :N,N’−ジシクロヘキシルカルボジイミド
本願明細書の配列表の配列番号は、以下の配列を示す。
〔配列番号:1〕
ヒトSGLTホモログタンパク質のアミノ酸配列を示す。
〔配列番号:2〕
配列番号:1で表されるアミノ酸配列を有するヒトSGLTホモログタンパク質をコードするDNAの塩基配列を示す。
〔配列番号:3〕
マウスSGLTホモログタンパク質のアミノ酸配列を示す。
〔配列番号:4〕
配列番号:3で表されるアミノ酸配列を有するマウスSGLTホモログタンパク質をコードするDNAの塩基配列を示す。
〔配列番号:5〕
ラットSGLTホモログタンパク質のアミノ酸配列を示す。
〔配列番号:6〕
配列番号:5で表されるアミノ酸配列を有するラットSGLTホモログタンパク質をコードするDNAの塩基配列を示す。
〔配列番号:7〕
実施例2(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:8〕
実施例2(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:9〕
実施例2(1)で用いられたプローブの塩基配列を示す。
〔配列番号:10〕
実施例2(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:11〕
実施例2(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:12〕
実施例2(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:13〕
実施例2(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:14〕
実施例2(2)で用いられたプローブの塩基配列を示す。
〔配列番号:15〕
実施例2(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:16〕
実施例2(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:17〕
実施例4で用いられたペプチドのアミノ酸配列を示す。
〔配列番号:18〕
実施例5(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:19〕
実施例5(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:20〕
実施例5(1)で用いられたプローブの塩基配列を示す。
〔配列番号:21〕
実施例5(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:22〕
実施例5(1)で用いられたプライマーの塩基配列を示す。
〔配列番号:23〕
実施例5(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:24〕
実施例5(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:25〕
実施例5(2)で用いられたプローブの塩基配列を示す。
〔配列番号:26〕
実施例5(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:27〕
実施例5(2)で用いられたプライマーの塩基配列を示す。
〔配列番号:28〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:29〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:30〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:31〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:32〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:33〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:34〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:35〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:36〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:37〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:38〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:39〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:40〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:41〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:42〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:43〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:44〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:45〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:46〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:47〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:48〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:49〕
実施例6で用いられたプライマーの塩基配列を示す。
〔配列番号:50〕
ハムスターSGLTホモログタンパク質のアミノ酸配列を示す。
〔配列番号:51〕
配列番号:50で表されるアミノ酸配列を有するハムスターSGLTホモログタンパク質をコードするDNAの塩基配列を示す。
〔配列番号:52〕
ハムスターSGLT1タンパク質のアミノ酸配列を示す。
〔配列番号:53〕
配列番号:53で表されるアミノ酸配列を有するハムスターSGLT1タンパク質をコードするDNAの塩基配列を示す。
〔配列番号:54〕
実施例10で用いられたプライマーの塩基配列を示す。
〔配列番号:55〕
実施例10で用いられたプライマーの塩基配列を示す。
〔配列番号:56〕
実施例10で用いられたプライマーの塩基配列を示す。
〔配列番号:57〕
実施例10で用いられたプライマーの塩基配列を示す。
WO02/53738の実施例4に記載の方法に従って、ヒトSGLT ホモログ(hSGLTh)、マウスSGLT ホモログ(mSGLTh)、 ラットSGLT ホモログ(rSGLTh)、ヒトSGLT1(hSGLT1)、ヒトSGLT2(hSGLT2)発現CHO細胞株を作製し、実験に用いた。SGLTによって選択的に細胞内に取りこまれるグルコースアナログであるα-Methyl Glucose の取り込み実験は、Am. J. Physiol. 270 : G833-G843, 1996およびJ. Clin. Invest 93 : 397-404, 1994 の方法に従って行った。細胞を96well プレートに1×105 細胞 / well 、100μl 10% FBS 添加DMEM 培地で播種し、37℃、一夜培養した。細胞をバッファー (125 mM N-Methyl-D-Glucamine, 1.2mM KH2PO4, 2.5mM CaCl2, 1.2mM MgSO4, 4mM Glutamine, 10mM HEPES (pH 7.2) , 0.1mg/ml BSA) 150μlで3回洗浄後同バッファーで1時間培養し、残存するグルコースを除去した。バッファーを除去し、同バッファーおよびN-Methyl-D-Glucamine (NMDG)をNaCl あるいは NaCl + Phlorizin (Sigma 社) に置き換えたバッファー 90μl を添加した。1mM α-Methyl Glucose を各well に10μl ( [14C]α-Methyl Glucose (アマシャム ファルマシア バイオテク社) 0.02μCi を含む) 添加し1時間後、冷PBS バッファー 200μlで3回洗浄した。各well に液体シンチレータ100μl を添加し、細胞に取り込まれた14Cのカウントを測定した。
〔表1〕hSGLT1, hSGLT2, hSGLThのフロリジン耐性度の比較
α-Methyl Glucoseの取込量
(control 群に対する%表示)
hSGLT1 hSGLT2 hSGLTh
control群(NMDG添加・NaCl非添加群) 100± 18 100±15 100± 12
NaCl添加群 1039±186 830±99 767± 85
NaCl+フロリジン 3μM添加群 244± 48 139±23 570±142
NaCl+フロリジン 100μM添加群 60± 14 48± 8 124± 19
〔表2〕mSGLTh, rSGLThのフロリジン耐性度の比較
α-Methyl Glucoseの取込量
(control 群に対する%表示)
mSGLTh rSGLTh
control群(NMDG添加・NaCl非添加群) 100± 6 100± 1
NaCl添加群 819±54 953± 0
NaCl+フロリジン 15μM添加群 521±35 643±76
NaCl+フロリジン 500μM添加群 78± 8 118± 6
表1および表2から明らかなように、ヒト、マウス、ラットSGLT ホモログは、hSGLT1, hSGLT2 と同様に、Na+濃度に依存してα-Methyl Glucose を取り込んだが、Phlorizin への耐性がSGLT1、SGLT2よりも強いことが証明された。
(1)TaqMan PCR によるヒトSGLTホモログの発現量の解析
TaqMan PCR に用いるプライマーおよびプローブは、Primer Express ver. 1.0 (PE バイオシステムジャパン)を用いて検索し、プライマー cccgatgctttccacatgcttc(配列番号:7)、プライマー acaatgacctggtctgtgcacc(配列番号:8)、プローブ acatcccttggccaggtctcattttcgg(配列番号:9)を選択した。プローブのリポーター色素として、FAM (6-carboxyfluorescein) を付加した。
(2)TaqMan PCR によるヒトSGLT1の発現量の解析
TaqMan PCR に用いるプライマーおよびプローブは、Primer Express ver. 1.0 (PE バイオシステムジャパン)を用いて検索し、プライマー agcaccctcttcaccatgga(配列番号:12)、プライマー aaacaaccttccggcaatcat(配列番号:13)、プローブ ccaaggtccgcaagagagcatctga(配列番号:14)を選択した。プローブのリポーター色素として、FAM (6-carboxyfluorescein) を付加した。
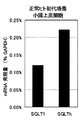
正常ヒト小腸上皮細胞(Cell System-IE Cells)は、大日本製薬から購入した。コラーゲンコートプレート(24穴プレート)にCS-2.0培地(25mM グルコース、10%FBSおよび抗生物質添加)で2x105cells/well播種し、2日置きに培地交換し13日間培養した。RNAeasy mini キット(Quiagen)を用いて、トータルRNA を抽出し、TaqMan Gold RT-PCR キット (PE biosystems) を用い、TaqMan PCR 法でヒトSGLT(hSGLT)ホモログ、hSGLT1の発現量を測定した。図2に示すとおり、正常ヒト小腸上皮細胞(Cell System-IE Cells)において、hSGLTホモログ(hSGLTh)は、hSGLT1と同等以上に発現していた。
(1)抗ヒトSGLTホモログペプチド抗体の作製
ヒトSGLTホモログの261-275番目のペプチドの275番目のアミノ酸残基にシステインをつけたもの(クラボウ社)を免疫原ペプチド〔H-HisAsnLeuArgAspProValSerGlyAspIleProTrpGlyCys(配列番号:17)-NH2= H-HNLRDPVSGDIPWGC-NH2〕として使用した。N-(γ-マレイミドブチリロキシ)サクシニミド(GMBS) とKeyhole Limpet Hemocyanin (KLH) を混合し、室温で40分反応した。セファデックスG-25カラムで分画し、マレイミド基の導入されたKLHを得た。免疫原ペプチド5mgとマレイミド基の導入されたKLHを等量混合し4℃で1日間反応した。PBS buffer で2日間透析し、PBS bufferに1mg/mlの濃度で懸濁した。
糖尿病患者では、小腸からの糖吸収の亢進が認められている( Am J Physiol Gastrointest Liver Physiol 282:G241-G248 2002)。糖尿病モデルマウスであるKKAyと正常マウスのC57/BL6および糖尿病モデルラットであるWistar fatty と正常ラットのWistar lean の小腸におけるSGLTホモログの発現量をTaqMan PCR法で比較した。
(1)TaqMan PCRによるマウスSGLTホモログの発現量の解析
TaqMan PCRに用いるプライマーおよびプローブは、Primer Express ver.1.0(PE バイオシステムズジャパン)を用いて検索し、
プライマー(5’-tgcacagaccaggtgattgtg-3’)〔配列番号:18〕
プライマー(5’-gcacggagcctcccttg-3’)〔配列番号:19〕
プローブ (5’-ctcgcagccaacaatctttcacatg-3’) 〔配列番号:20〕
を選択した。プローブのリポーター色素として、FAM(6-carboxyfluorescein)を付加した。
(2)TaqMan PCRによるラットSGLTホモログの発現量の解析
TaqMan PCRに用いるプライマーおよびプローブは、Primer Express ver.1.0(PE バイオシステムズジャパン)を用いて検索し、
プライマー (5’-ctcacagtcttggccacctg-3’)〔配列番号:23〕
プライマー(5’-agaaccggctctctctggag-3’)〔配列番号:24〕
プローブ (5’-tgcacggaccaggtgattgtgc-3’)〔配列番号:25〕
を選択した。プローブのリポーター色素として、FAM(6-carboxyfluorescein)を付加した。
ヒト、マウス、ラット、ハムスター、サル小腸におけるSGLT1, SGLTホモログの発現量をRT-PCR 法で比較した。
RT-PCRによる小腸におけるSGLTホモログの発現解析
ヒトSGLTホモログについては、ヒト空腸cDNA(DCA社)を鋳型とし、プライマー1 gggggccagaggatccaggtgta〔配列番号:28〕、およびプライマー2 aaaatagccccagaggaagatgttga〔配列番号:29〕を用いてPCR反応を行った。この反応における反応液の組成は上記cDNA 1μlを鋳型として使用し、Pfu Turbo DNA Polymerase(STRATAGENE社)1μl量、プライマー1およびプライマー2を各0.5μM、dNTPsを200μM、および酵素に添付のバッファーを5μl加え、50μlの液量とした。PCR反応は、94℃・1分の後、96℃・20秒、62℃・30秒、72℃・1.5分のサイクルを40回繰り返し、最後に72℃・7分の伸長反応を行った。同様にヒトSGLT1(NM_000343)についてはプライマー3 atcctgactgggtttgcttt〔配列番号:30〕およびプライマー4 atgctgatgccaatcagcac〔配列番号:31〕を用いてPCRを行い、反応条件は96℃・20秒、55℃・30秒、72℃・30秒を40回繰り返し、他の条件はヒトSGLTホモログの条件と同様とした。
ヒトactinについてはプライマー5 agagctacgagctgcctgac〔配列番号:32〕およびプライマー6 acatctgctggaaggtggac〔配列番号:33〕を用いてPCRを行い、反応条件は96℃・20秒、64℃・30秒、72℃・30秒を40回繰り返し、他の条件はヒトSGLTホモログの条件と同様とした。
ハムスターSGLTホモログ
forward:tgccacagtacttgaagaaacgat〔配列番号:34〕
reverse:tgaagaacattgggaggatt〔配列番号:35〕
95℃ 20秒、50℃ 30秒、72℃ 30秒 を40回繰り返し
ハムスターSGLT1
forward:caatgaagtaggagggtatgagg〔配列番号:36〕
reverse:tggcgctgttgaagatggaggtc〔配列番号:37〕
95℃ 20秒、56℃ 30秒、72℃ 1分 を40回繰り返し
サルSGLTホモログおよびSGLT1はカニクイザル小腸より抽出したRNAを鋳型としてTaqMan reverse transcription reagents を用いてランダムプライマーからcDNAを合成した。このcDNAを鋳型として以下に記すPCRプライマーと反応条件でPCR反応を行った。
サルSGLTホモログ
forward:atctctaatgtccagcaatgtg〔配列番号:38〕
reverse:gcaatcatcagcccccgcagac〔配列番号:39〕
95℃ 20秒、57℃ 30秒、72℃ 1分 を40回繰り返し
サルSGLT1
forward:atcctgactgggtttgcttt〔配列番号:40〕
reverse:atgctgatgccaatcagcac〔配列番号:41〕
95℃ 20秒、55℃ 30秒、72℃ 1分 を40回繰り返し
マウスSGLTホモログおよびSGLT1は8週齢 雄性KKAyマウス小腸より抽出したRNAを鋳型としてTaqMan reverse transcription reagents を用いてランダムプライマーからcDNAを合成した。このcDNAを鋳型として以下に記すPCRプライマーと反応条件でPCR反応を行った。
マウスSGLTホモログ
forward:ggcaatggaaccaggagtgtc〔配列番号:42〕
reverse:tcacgcaaaatagccccagagaaag〔配列番号:43〕
95℃ 20秒、60℃ 30秒、72℃ 2.5分 を40回繰り返し
マウスSGLT1(NM_019810)
forward:atggacagtagcaccttgagcc〔配列番号:44〕
reverse:tcaggcaaaataggcatggcag〔配列番号:45〕
95℃ 20秒、55℃ 30秒、72℃ 2.5分 を40回繰り返し
ラットSGLTホモログおよびSGLT1は22週齢 雄性Wistar fatty ラット小腸より抽出したRNAを鋳型としてTaqMan reverse transcription reagents を用いてランダムプライマーからcDNAを合成した。このcDNAを鋳型として以下に記すPCRプライマーと反応条件でPCR反応を行った。
ラットSGLTホモログ
forward:caatggaacctggagcttcaag〔配列番号:46〕
reverse: tcacgcaaaatagccccagagaaag〔配列番号:47〕
95℃ 20秒、60℃ 30秒、72℃ 2.5分 を40回繰り返し
ラットSGLT1(NM_013033)
forward: atggacagtagcaccttgagcc〔配列番号:48〕
reverse: tcaggcaaaataggcgtggcag〔配列番号:49〕
95℃ 20秒、55℃ 30秒、72℃ 2.5分 を40回繰り返し
図6に示す結果のとおり、マウス、ラットでは、SGLTホモログに比べてSGLT1の発現が高いが、サルではヒトと同様にSGLT1, SGLTホモログの発現が同等で、ハムスターではSGLT1以上にSGLTホモログの発現が認められた。
小腸器官培養系による糖取り込み量の測定は、Peptides, 19 : 1249-1253 1998および J. Agric. Food Chem. 48 : 5618-5623 2000の方法に従った。マウス、ラット、モルモット、ハムスターは、エーテル麻酔後頚動脈を切断して安楽死させた。空腸領域を切り出し、腸間膜脂肪を取り除き、管を切り開いて内容物を洗浄し、1cm 長に切り分けた。空腸切片をバッファー (125 mM N-Methyl-D-Glucamine (NMDG), 1.2mM KH2PO4, 2.5mM CaCl2, 1.2mM MgSO4, 4mM Glutamine, 10mM HEPES (pH 7.2) , 0.1mg/ml BSA) で3回洗浄後、48-wellプレートに1個ずつ移した。同バッファーおよびNMDGをNaCl あるいは NaCl + Phlorizin 30μM) に置き換えたバッファー 270μl を添加した。10mM α-Methyl Glucose, 10mM D-mannitol を各well に30μl ( [14C]α-Methyl Glucose (AMG)(アマシャム ファルマシア バイオテク社) 0.12μCi , [3H]D-mannitol (Perkin Elmer LifeSciences)0.3μCi を含む) を添加し、37℃、10分間培養後、冷PBS バッファー 300ulで3回洗浄した。空腸切片を液体シンチレーション測定用ミニバイアルに移し、組織溶解剤 Solvable (Perkin Elmer LifeSciences)500μlを添加し、50℃で2時間処理して溶解した。液体シンチレータUltima Gold-XR (Perkin Elmer LifeSciences) 5ml を添加し、空腸切片に取り込まれた14C、3Hのカウントを測定した。図7に示す結果のとおり、ハムスターの小腸では、フロリジンに耐性の強いSGLT活性が認められ、SGLTホモログの糖取り込み活性が確認された。
ヒトSGLTホモログまたはヒトSGLT1導入COS7細胞を作製しそれぞれの基質特異性を検討した。α-Methyl Glucoseの取り込み実験は、Am. J. Physiol. 270:G833-G843, 1996およびJ. Clin. Invest. 93:397-404, 1994の方法に従って行った。細胞を96穴プレートに3×104細胞/well、100μl 10% FBS添加DMEM培地で播種し、37℃で一夜培養した。各wellを125 mM のN-Methyl-D-Glucamineを添加した反応緩衝液(1.2 mM KH2PO4, 2.5 mM CaCl2, 1.2 mM MgSO4, 4 mM Glutamine, 10 mM HEPES (pH7.2), 0.1 mg/ml BSA)で3回洗浄後、同緩衝液でさらに1時間培養し、細胞に残存するグルコースを除去した。次に150 mMの NaClを添加した上記反応緩衝液にGlucoseまたはGalactoseを0, 1, 10 mMを添加したものを調製し、それぞれ各wellに90μl添加した。さらに0.02μCiの[14C]-α-Methyl Glucose(アマシャム ファルマシア バイオテク社)を含有する終濃度1 mM α-Methyl Glucoseを各wellに10μlずつ添加し、1時間の糖取り込み反応を行った。200μlの冷PBSで3回洗浄した後、液体シンチレータを各wellに100μlずつ添加し、細胞に取り込まれた14Cの量をシンチレーションカウンターで測定した。その結果、SGLT1がGlucoseとGalactoseに対し親和性を持つのに対し、SGLTホモログはGlucoseに親和性はあるもののGalactoseに対する親和性はほとんど無いことが示された。
ヒトSGLTホモログまたはヒトSGLT1導入COS7細胞を作製しそれぞれの糖取り込みの速度論的解析を行った。α-Methyl Glucoseの取り込み実験は、Am. J. Physiol. 270:G833-G843, 1996およびJ. Clin. Invest. 93:397-404, 1994の方法に従って行った。細胞を96穴プレートに3×104細胞/well、100μl 10% FBS添加DMEM培地で播種し、37℃で一夜培養した。各wellを125 mM のN-Methyl-D-Glucamineを添加した反応緩衝液(1.2 mM KH2PO4, 2.5 mM CaCl2, 1.2 mM MgSO4, 4 mM Glutamine, 10 mM HEPES (pH7.2), 0.1 mg/ml BSA)で3回洗浄後、同緩衝液でさらに1時間培養し、細胞に残存するグルコースを除去した。次に150 mMの NaClを添加した上記反応緩衝液にα-Methyl Glucoseを0-20 mMを添加したものを調製し、それぞれ各wellに90μl添加した。さらに0.02μCiの[14C]-α-Methyl Glucose(アマシャム ファルマシア バイオテク社)を含有する終濃度1 mM α-Methyl Glucoseを各wellに10μlずつ添加し、1時間の糖取り込み反応を行った。200μlの冷PBSで3回洗浄した後、液体シンチレータを各wellに100μlずつ添加し、細胞に取り込まれた14Cの量をシンチレーションカウンターで測定し、糖取り込みのKmとVmaxを測定した。その結果、SGLT1がKm = 1.8 mM, Vmax = 3.9 nmol/hour/106 cellsであったのに対し、SGLTホモログはKm = 7.9 mM, Vmax = 8.0 nmol/hour/106 cellsであった。これらのことからSGLT1が高親和性、低輸送能のトランスポーターであるのに対し、SGLTホモログが低親和性、高輸送能のトランスポーターであることが示された。
鋳型となるcDNAは、9週齢、雄性シリアンハムスター小腸よりRNeasyキット(QIAGEN社)のマニュアルに従って抽出したRNAをもとに、TaqMan reverse transcription reagents (Applied Biosystems社) を用いてランダムプライマーから合成した。このハムスター小腸cDNAを鋳型とし、SGLTホモログのクローニングにはプライマーA (5’-gcaatggagcctggagattcag-3’)〔配列番号:54〕およびプライマーB (5’-agcctgcctctggtcttg-3’) 〔配列番号:55〕のセットを用いて、またSGLT1のクローニングのためにはプライマーC (5’-atggacagtagcaccttgagccccgcggtca-3’) 〔配列番号:56〕およびプライマーD (5’-gattcaagcaaaatatccgtggcaaaaga-3’) 〔配列番号:57〕を用いてPCRを行った。該反応における反応液の組成は上記cDNA 10 ngを鋳型として使用し、Pfu Turbo DNA Polymerase (STRATAGENE社)を1μl、プライマーを各0.5μM、dNTPsを200μM、および酵素に添付のバッファーを5μl加え、50μlの液量とした。反応は、94℃, 1分の後、96℃, 20秒、58℃, 30秒、72℃, 2分30秒のサイクルを40回繰り返し、最後に72℃, 7分の伸長反応を行った。該反応産物を1%アガロースゲル電気泳動で分離し、DNA断片を切り出し、ゲルエクストラクションキット(QIAGEN社)を用いてゲルから抽出した。抽出したDNAをTOPOライゲーションキット(インビトロジェン社)の処方に従い、pCR BluntIIベクターへサブクローニングした。これを大腸菌T0P10に導入し、cDNAクローンを得た。ハムスターSGLTホモログcDNAから予測されるアミノ酸配列を配列番号:50に、配列番号:50で示されるアミノ酸配列をコードする領域の塩基配列を配列番号:51に示す。ハムスターSGLTホモログのアミノ酸配列のヒト、マウス、ラットのSGLTホモログのアミノ酸配列に対する相同性はそれぞれ86.4%, 88.4%, 88.3%であった。またハムスターSGLT1 cDNAから予測されるアミノ酸配列を配列番号:52に、配列番号:52で示されるアミノ酸配列をコードする領域の塩基配列を配列番号:53に示す。ハムスターSGLT1のアミノ酸配列のヒト、マウス、ラットのSGLT1のアミノ酸配列に対する相同性はそれぞれ83.9%, 89.7%, 90.6%であった。
ハムスターSGLTホモログ糖取り込み量は以下の手法で測定できる。ハムスター小腸cDNAよりクローニングしたハムスターSGLTホモログまたはSGLT1を動物細胞発現ベクターpcDNA3.1(インビトロジェン社)にサブクローニングすることによりハムスターSGLTホモログまたはSGLT1を動物細胞で発現せしめるベクターを構築する。該発現ベクター各1μgをFuGENE6試薬(Roche社)でCOS7細胞(5×105細胞)に導入しそれぞれの発現細胞を得る。ハムスターSGLTホモログまたはSGLT1導入COS7細胞のα-Methyl Glucoseの取り込み実験は、Am. J. Physiol. 270:G833-G843, 1996およびJ. Clin. Invest. 93:397-404, 1994の方法に従って行う。細胞を96穴プレートに3×104細胞/well、100μl 10% FBS添加DMEM培地で播種し、37℃で一夜培養する。細胞を125 mM のN-Methyl-D-Glucamineを添加した反応緩衝液(1.2 mM KH2PO4, 2.5 mM CaCl2, 1.2 mM MgSO4, 4 mM Glutamine, 10 mM HEPES (pH7.2), 0.1 mg/ml BSA)で3回洗浄後、同緩衝液でさらに1時間培養し、細胞に残存するグルコースを除去する。150 mMの NaClを添加した反応緩衝液にphlorizin(Sigma社)を0, 0.1, 1 mMを添加したものをそれぞれ各wellに90μl添加する。さらに0.02μCiの[14C]-α-Methyl Glucose(アマシャム ファルマシア バイオテク社)を含有する終濃度1 mM α-Methyl Glucoseを各wellに10μlずつ添加し、1時間の糖取り込み反応を行う。200μlの冷PBSで3回洗浄した後、液体シンチレータを各wellに100μlずつ添加し、細胞に取り込まれた14Cの量をシンチレーションカウンターで測定する。
Claims (48)
- Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩を含有してなる小腸でのグルコース取り込み阻害剤。
- Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を阻害する化合物またはその塩を含有してなる小腸でのグルコース取り込み阻害剤。
- 食後過血糖改善剤である請求項1または2記載の剤。
- 糖尿病、肥満症または高脂血症予防・治療剤である請求項1ないし3記載の剤。
- Na+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩を含有してなる小腸でのグルコース取り込み促進剤。
- Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を促進する化合物またはその塩を含有してなる小腸でのグルコース取り込み促進剤。
- グルコースの吸収促進剤である請求項5または6記載の剤。
- Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:1で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である請求項1ないし7記載の剤。
- Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:3で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である請求項1ないし7記載の剤。
- Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:5で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である請求項1ないし7記載の剤。
- Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:50で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である請求項1ないし7記載の剤。
- Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドの塩基配列に相補的もしくは実質的に相補的な塩基配列またはその一部分を含有するアンチセンスポリヌクレオチドを含有してなる小腸でのグルコース取り込み阻害剤。
- 食後過血糖改善剤である請求項12記載の剤。
- 糖尿病、肥満症または高脂血症の予防・治療剤である請求項12または13記載の剤。
- Na+/グルコーストランスポーター (SGLT)ホモログをコードするポリヌクレオチドが配列番号:2、配列番号:4、配列番号:6または配列番号:51で表される塩基配列と同一もしくは実質的に同一の塩基配列を含有するポリヌクレオチドである請求項12ないし14記載の剤。
- Na+/グルコーストランスポーター (SGLT) ホモログに対する抗体を含有してなる小腸でのグルコース取り込み阻害剤。
- 食後過血糖改善剤である請求項16記載の剤。
- 糖尿病、肥満症または高脂血症予防・治療剤である請求項16または17記載の剤。
- Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:1、配列番号:3、配列番号:5または配列番号:50で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である請求項16ないし18記載の剤。
- Na+/グルコーストランスポーター (SGLT) ホモログに対する抗体を含有してなる食後過血糖の診断薬。
- Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドを含有してなる食後過血糖の診断薬。
- Na+/グルコーストランスポーター (SGLT) ホモログを用いることを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング方法。
- Na+/グルコーストランスポーター (SGLT)ホモログが配列番号:1、配列番号:3、配列番号:5または配列番号:50で表されるアミノ酸配列と同一もしくは実質的に同一のアミノ酸配列を含有するタンパク質もしくはその部分ペプチドまたはその塩である請求項22記載のスクリーニング方法。
- Na+/グルコーストランスポーター (SGLT) ホモログを含有することを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング用キット。
- Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドを用いることを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング方法。
- Na+/グルコーストランスポーター (SGLT)ホモログをコードするポリヌクレオチドが配列番号:2、配列番号:4、配列番号:6または配列番号:51で表される塩基配列と同一もしくは実質的に同一の塩基配列を含有するポリヌクレオチドである請求項25記載のスクリーニング方法。
- Na+/グルコーストランスポーター (SGLT) ホモログをコードするポリヌクレオチドを用いることを特徴とする、該ホモログの小腸でのグルコース取り込み活性を調節する化合物またはその塩のスクリーニング用キット。
- Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害することを特徴とする小腸でのグルコース取り込み阻害方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を阻害することを特徴とする小腸でのグルコース取り込み阻害方法。
- 食後過血糖改善方法である請求項28または29記載の方法。
- 糖尿病、肥満症または高脂血症予防・治療方法である請求項28ないし30記載の方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの活性を促進することを特徴とする小腸でのグルコース取り込み促進方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を促進することを特徴とする小腸でのグルコース取り込み促進方法。
- グルコースの吸収促進方法である請求項32または33記載の方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み阻害方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を阻害する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み阻害方法。
- 食後過血糖改善方法である請求項35または36記載の方法。
- 糖尿病、肥満症または高脂血症予防・治療方法である請求項35ないし37記載の方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み促進方法。
- Na+/グルコーストランスポーター (SGLT) ホモログの遺伝子の発現を促進する化合物またはその塩の有効量を哺乳動物に投与することを特徴とする小腸でのグルコース取り込み促進方法。
- グルコースの吸収促進方法である請求項39または40記載の方法。
- 小腸でのグルコース取り込み阻害剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩の使用。
- 小腸でのグルコース取り込み阻害剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を阻害する化合物またはその塩の使用。
- 小腸でのグルコース取り込み阻害剤が食後過血糖改善剤である請求項42または43記載の使用。
- 小腸でのグルコース取り込み阻害剤が糖尿病、肥満症または高脂血症予防・治療剤である請求項42ないし44記載の使用。
- 小腸でのグルコース取り込み促進剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩の使用。
- 小腸でのグルコース取り込み促進剤の製造のためのNa+/グルコーストランスポーター (SGLT) ホモログの活性を促進する化合物またはその塩の使用。
- 小腸でのグルコース取り込み促進剤がグルコースの吸収促進剤である請求項46または47記載の使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003366734A JP2005015460A (ja) | 2002-10-29 | 2003-10-28 | Sgltホモログ用途 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002314041 | 2002-10-29 | ||
| JP2003156306 | 2003-06-02 | ||
| JP2003366734A JP2005015460A (ja) | 2002-10-29 | 2003-10-28 | Sgltホモログ用途 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005015460A true JP2005015460A (ja) | 2005-01-20 |
| JP2005015460A5 JP2005015460A5 (ja) | 2006-12-14 |
Family
ID=34198694
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003366734A Pending JP2005015460A (ja) | 2002-10-29 | 2003-10-28 | Sgltホモログ用途 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005015460A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007010628A1 (ja) * | 2005-07-22 | 2007-01-25 | Japanese Foundation For Cancer Research | 癌の予防・治療剤 |
| JP2013504769A (ja) * | 2009-09-15 | 2013-02-07 | ジヤンセン・フアーマシユーチカ・ナームローゼ・フエンノートシヤツプ | グルコースの吸収および排泄の指標としてのα−メチルグルコシド(AMG)の使用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002053738A1 (fr) * | 2000-12-28 | 2002-07-11 | Takeda Chemical Industries, Ltd. | Nouvelles proteines et adn correspondant |
-
2003
- 2003-10-28 JP JP2003366734A patent/JP2005015460A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002053738A1 (fr) * | 2000-12-28 | 2002-07-11 | Takeda Chemical Industries, Ltd. | Nouvelles proteines et adn correspondant |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007010628A1 (ja) * | 2005-07-22 | 2007-01-25 | Japanese Foundation For Cancer Research | 癌の予防・治療剤 |
| JP2013504769A (ja) * | 2009-09-15 | 2013-02-07 | ジヤンセン・フアーマシユーチカ・ナームローゼ・フエンノートシヤツプ | グルコースの吸収および排泄の指標としてのα−メチルグルコシド(AMG)の使用 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4767019B2 (ja) | 動脈硬化の予防・治療用医薬 | |
| US7247705B2 (en) | Proteins having glucose transporter activity | |
| JP2008237022A (ja) | 非小細胞肺がんの予防・治療剤および診断薬 | |
| JP4829780B2 (ja) | 呼吸器疾患の予防・治療剤 | |
| EP1241257A1 (en) | Novel tachykinin-like polypeptides and use thereof | |
| JP2005015460A (ja) | Sgltホモログ用途 | |
| EP1557178A1 (en) | Use of sglt homolog | |
| JP4530631B2 (ja) | 新規タンパク質および癌の予防・治療剤 | |
| JP4353697B2 (ja) | がんの予防・治療剤 | |
| JP4445291B2 (ja) | 新規タンパク質およびそのdna | |
| JP4300008B2 (ja) | 新規タンパク質およびそのdna | |
| EP1600165A1 (en) | Medicinal use of mip-3alpha inhibitor and method of screening brain/nerve cell protective agent | |
| JP2004217634A (ja) | がんの予防・治療剤 | |
| JP4676608B2 (ja) | 新規タヒキニン様ポリペプチドおよびその用途 | |
| JP2005151826A (ja) | C1qtnf5の用途 | |
| JP2004026692A (ja) | Mepeの新規用途 | |
| JP2004089182A (ja) | がんの予防・治療剤 | |
| JPWO2006101273A1 (ja) | 癌の予防・治療剤 | |
| JP2001299363A (ja) | 新規タンパク質およびそのdna | |
| JP2004075675A (ja) | 骨・関節疾患の予防・治療剤 | |
| JP2004121245A (ja) | 新規タンパク質およびそのdna | |
| JP2004041003A (ja) | 新規タンパク質、そのdnaおよびその用途 | |
| JP2004261172A (ja) | 疾患関連遺伝子の用途 | |
| JP2004135666A (ja) | 神経変性疾患の予防・治療剤 | |
| JP2004187680A (ja) | 新規タンパク質およびそのdna |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20061026 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061026 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20061026 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100202 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100601 |