JP2004004057A - バイオセンサ、それに用いるアダプタ、および測定装置 - Google Patents
バイオセンサ、それに用いるアダプタ、および測定装置 Download PDFInfo
- Publication number
- JP2004004057A JP2004004057A JP2003119871A JP2003119871A JP2004004057A JP 2004004057 A JP2004004057 A JP 2004004057A JP 2003119871 A JP2003119871 A JP 2003119871A JP 2003119871 A JP2003119871 A JP 2003119871A JP 2004004057 A JP2004004057 A JP 2004004057A
- Authority
- JP
- Japan
- Prior art keywords
- substrate
- biosensor
- lead
- electrode
- measuring device
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
【課題】簡易な構成により、測定装置と容易に接続することができる対向型バイオセンサ、それに用いるアダプタおよび測定装置を提供する。
【解決手段】作用極34と対極基板40上に配置された対極35とが相互に対向する位置に配置されたバイオセンサ3をアダプタ2を介して測定装置1に挿入すると、押さえ部21により対極基板40が押さえられて、対極基板40上に配置された第2の対極リード33と作用極基板39上に配置された第1の対極リード32とが接触する。
【選択図】 図4
【解決手段】作用極34と対極基板40上に配置された対極35とが相互に対向する位置に配置されたバイオセンサ3をアダプタ2を介して測定装置1に挿入すると、押さえ部21により対極基板40が押さえられて、対極基板40上に配置された第2の対極リード33と作用極基板39上に配置された第1の対極リード32とが接触する。
【選択図】 図4
Description
【0001】
【発明の属する技術分野】
本発明は、試料中に含まれる基質を迅速かつ高精度に定量するためのバイオセンサ、それに用いるアダプタ、および測定装置に関する。
【0002】
【従来の技術】
スクロース、グルコースなど糖類の定量分析法として、施光度計法、比色法、還元滴定法および各種クロマトグラフィーを用いた方法などが開発されている。しかし、これらの方法は、いずれも糖類に対する特異性があまり高くなく、精度に劣る。また、これらの方法のうち、施光度計法においては、操作は簡便ではあるが、操作時の温度の影響を大きく受ける。したがって、施光度計法は、一般の人々が家庭などで簡易に糖類を定量する方法としては適切でない。
近年、酵素の有する特異的触媒作用を利用した種々のタイプのバイオセンサが開発されている。以下に、試料中の基質の定量法の一例としてグルコースの定量法について説明する。電気化学的なグルコースの定量法としては、酵素であるグルコースオキシダーゼ(EC1.1.3.4、GOD)と酸素電極または過酸化水素電極とを使用して行う方法が一般に知られている。
【0003】
GODは、酸素を電子伝達体として、基質であるβ−D−グルコースをD−グルコノ−δ−ラクトンに選択的に酸化する。酸素の存在下、GODによる酸化反応過程において、酸素は過酸化水素に還元される。酸素電極によって、この酸素の減少量を計測するか、または過酸化水素電極によって過酸化水素の増加量を計測する。酸素の減少量および過酸化水素の増加量は、試料中のグルコースの含有量に比例するため、酸素の減少量または過酸化水素の増加量からグルコースの定量を行うことができる。
上記方法では、酵素反応の特異性を利用することにより、精度良く試料中のグルコースを定量することができる。しかし、反応過程からも推測できるように、測定結果は試料に含まれる酸素濃度の影響を大きく受けるという欠点があり、試料に酸素が存在しない場合は測定が不可能となる。
【0004】
そこで、酸素を電子伝達体として用いず、フェリシアン化カリウム、フェロセン誘導体およびキノン誘導体などの有機化合物や金属錯体を電子伝達体として用いる新しいタイプのグルコースセンサが開発されてきた。このタイプのセンサでは、酵素反応の結果生じた電子伝達体の還元体を作用極上で酸化することにより、その酸化電流量から試料中に含まれるグルコース濃度が求められる。
この際、対極上では、電子伝達体の酸化体が還元され、電子伝達体の還元体の生成する反応が進行する。このような有機化合物や金属錯体を酸素の代わりに電子伝達体として用いることにより、既知量のGODとそれらの電子伝達体を安定な状態で正確に電極上に担持させて試薬層を形成することが可能となり、試料中の酸素濃度の影響を受けることなく、精度良くグルコースを定量することができる。
【0005】
また、この場合、酵素および電子伝達体を含有する試薬層を乾燥状態に近い状態で電極系と一体化させることもできるため、この技術に基づいた使い捨て型のグルコースセンサが近年多くの注目を集めている。その代表的な例が、特許文献1に示されるバイオセンサである。使い捨て型のグルコースセンサにおいては、測定装置に着脱可能に接続されたセンサに試料を導入するだけで容易にグルコース濃度を測定装置で測定することができる。
上記のようなグルコースセンサを用いた測定では、数μlオーダーの試料量で試料中の基質濃度を容易に求めることが可能である。しかし、近年、さらに微量(1μl以下)な試料での測定が可能なバイオセンサの開発が各方面において切望されている。
【0006】
従来の電気化学グルコースセンサは、殆どの場合、一平面上に電極系が配置された平面型バイオセンサであり、極微量の試料における測定では電極間の電荷移動(主にイオンの移動)に対する抵抗が大きくなることにより、測定感度が低下したり、測定結果にバラツキが生じる場合があった。
そこで、例えば特許文献2においては、作用極と対極が相互に対向する位置に配置されたバイオセンサ(対向型バイオセンサ)が提案されている。このタイプのセンサでは、作用極と対極とを相互に対向する位置に配置したことにより作用極−対極間のイオン移動が円滑になるなどの理由から、従来の平面型バイオセンサよりも、高精度かつ高感度で試料中に含まれるグルコース等の基質を定量することができる。
【0007】
しかし、対向型バイオセンサは、センサと測定装置とを電気的に接続する際、作用極と対極が同一平面状に無いために、センサのリード形状または測定装置の接続端子形状を平面型バイオセンサとは異なる形状にする必要がある。例えば特許文献2には、作用極基板および対極基板に、他方の基板上に形成された作用極リードまたは対極リードをそれぞれ表裏逆向きに外部に臨ませる貫通孔を設けた対向型バイオセンサが開示されている。また、特許文献3には、それぞれ作用極または対極が形成された2枚の絶縁性基板に、対向する絶縁性基板が有する接続端子を露出させるように切欠部が形成され、両絶縁性基板の接続端子がそれぞれ表裏逆向きに露出している対向型バイオセンサが開示されている。これらのバイオセンサでは、作用極リード用の接続端子および対極リード用の接続端子が表裏逆向きに露出しているため、測定装置側の作用極用の接続端子と対極用の接続端子とを上下逆方向を向くように、平面型バイオセンサとは異なる特殊な形状にする必要があった。
【0008】
さらに、特許文献4には、長い下部基板と短い上部基板を具備するバイオセンサが開示されており、下部基板の端部と上部基板の端部とは重なっておらず、作用極および対極のリード部が、長い下部基板の内側に形成されている。また、作用極および対極が短い上部基板上に形成されており、接着層またはスペーサが、それらの基板の間に介在している。そして、作用極および対極のリード部は、前記接着剤層またはスペーサを貫通して電気的に接続される。
また、測定装置側の接続端子の形状は、平面型バイオセンサと同じであってよいが、センサ側にリードを形成するとともに、これらリードを接着層、スペーサまたは基板などを貫通させる必要があるため、製造プロセスを煩雑かつ複雑にしていた。
【0009】
【特許文献1】
特開平3−202764号公報(特許第2517153号)
【特許文献2】
特開平11−352093号公報
【特許文献3】
特開平9−159642号公報
【特許文献4】
特開平11−125618号公報
【0010】
【発明が解決しようとする課題】
以上のように、従来の対向型バイオセンサにおいては、平面型バイオセンサと異なり、センサのリードまたは測定装置の接続端子の形状を特殊な形状にする必要があった。このような状況に鑑み、本発明は、単純なリードを有し、かつ測定装置に容易に接続し得る平面型バイオセンサ、それに用いるアダプタならびに測定装置を提供することを目的とする。
【0011】
【課題を解決するための手段】
上記の問題を解決すべく、本発明は、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、
前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、
前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記第1電極または前記第2電極の一方が作用極として機能し、他方が対極として機能し、前記第1の基板および/または前記第2の基板をいずれかの基板に向けて押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触することを特徴とするバイオセンサを提供する。
【0012】
前記バイオセンサにおいては、前記第3のリードが複数に分割されており、前記第2のリードを複数個有することが有効である。
また、前記第1の基板と前記第2の基板との間にスペーサ部材を有することが有効である。
また、前記スペーサ部材が、前記第1の基板および前記第2の基板の少なくとも一方と一体化されていることが有効である。
前記スペーサ部材は、前記第1の基板と一体化されていてもよく、また、前記第2の基板と一体化されていてもよい。
【0013】
また、前記バイオセンサにおいては、前記第2の基板が、長手方向において、前記第1の基板よりも短いことが有効である。逆に、前記第1の基板が前記2の基板よりも短くてもよい。
また、前記試料供給部内に、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼおよびアミノ酸オキシダーゼよりなる群から選択される酵素を含む試薬を具備することが有効である。
【0014】
つぎに、本発明は、バイオセンサを挿入するセンサ差し込み口と、押さえ部と、測定装置と接続するための接続口とを具備することを特徴とするアダプタを提供する。
このアダプタにおいては、前記センサ差し込み口に挿入された前記バイオセンサを受け、
前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、例えば撓ませたり曲げたりすることによって、他方の基板に向けて移動させることが有効である。
このアダプタに用いるバイオセンサは、上述した構成を有するのが有効である。
【0015】
さらに、本発明は、バイオセンサと、押さえ部を含むアダプタと、測定手段とを具備することを特徴とする測定装置を提供する。
この測定装置においても、前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、例えば撓ませたり曲げたりすることによって他方の基板に向けて移動させ得ることが有効である。
【0016】
この測定装置において用いるバイオセンサも、上述のようなバイオセンサの構成を有するのが有効であり、前記測定装置は、試料液中の基質を測定するものであるのが有効である。
さらに、前記測定装置は、前記バイオセンサの前記第1の電極に電気的に接続される第1の端子と、前記バイオセンサの前記第2の電極にそれぞれ電気的に接続される少なくとも1つの第2の端子とを具備することが有効である。
【0017】
また、前記測定手段が、前記第1の端子および前記少なくとも1つの第2の端子を介して、前記バイオセンサの前記第1の電極および前記第2の電極の間に電圧を印加する手段と、前記第1の電極および前記第2の電極の間の電気的変化を測定する手段を具備することが有効である。
また、前記測定装置が、前記第2の端子を複数個有することが有効である。
また、前記測定装置が、前記第1の端子および前記複数個の第2の端子の間の電気的変化を測定する手段を具備することが有効である。
さらに、前記複数個の第2の端子のうち前記第1の端子に電気的に接続された第1の端子を検知する手段と、検知された第2の端子の数および位置に基づいてバイオセンサの種類を決定する手段と、前記種類に応じて測定結果を補正する手段とを具備することが有効である。
【0018】
さらにまた、本発明は、押さえ部と、
第1の電極に電気的に接続された第1のリード、第2のリード、第2の電極に電気的に接続された第3のリードを具備するバイオセンサを受けるセンサ差し込み口と、
前記バイオセンサの前記第1のリードを前記測定装置に電気的に接続する第1の端子と、
前記バイオセンサの前記第2のリードを前記測定装置に電気的に接続する第2の端子と、
前記第1の電極および前記第2の電極の間に電圧を印加する手段と、
前記第1の電極および前記第2の電極の間の電気的変化を測定する手段とを具備することを特徴とする測定装置を提供する。
【0019】
この測定装置も、前記第2の端子を複数個具備することが有効である。
また、前記第1の端子および前記複数個の第2の端子の間の電気的変化を測定する手段とを具備することが有効である。
また、前記押さえ部が弾性体で構成されていることが有効である。
また、前記第2の端子が前記押さえ部として機能することが有効である。
【0020】
この測定装置において用いるバイオセンサも、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、例えば撓ませたり曲げたりすることによって、他方の基板に向けて移動させ得ることが有効である。
【0021】
また、ここで用いるバイオセンサも、上述のようなバイオセンサの構成を有するのが有効である。
また、この測定装置は、前記バイオセンサの前記第1の基板または前記第2の基板の少なくとも一部を押さえて前記第2の電極および前記第3の電極を電気的に接続し、前記バイオセンサの前記試料供給部に供給された試料液中の基質を測定することが有効である。
【0022】
また、前記複数個の第2の端子のうち前記第1の端子に電気的に接続された第2の端子を検知する手段と、検知された第2の端子の数および位置に基づいてバイオセンサの種類を決定する手段と、前記種類に応じて測定結果を補正する手段とを具備することが有効である。
さらに、前記押さえ部が可動し、前記バイオセンサの前記第1の基板および/または前記第2の基板において押さえられる部分が、前記押さえ部によって決定され得ることが有効である。
【0023】
【発明の実施の形態】
本発明に係るバイオセンサは、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、
前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、
前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記第1電極または前記第2電極の一方が作用極として機能し、他方が対極として機能し、前記第1の基板および/または前記第2の基板をいずれかの基板に向けて押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触することを特徴とする。
【0024】
より具体的には、本発明は、第1の基板、第2の基板、第1の電極、第2の電極、前記第1の電極と電気的に接続された第1のリード、第2のリード、前記第2の電極と電気的に接続された第3のリード、前記第1の基板と前記第2の基板との間に設けられ試料供給部を形成するスペーサ部材、および少なくとも一部が前記試料供給部に露出するように設けられた少なくとも酵素を含む試薬を具備し、
前記第1の基板上であって前記第2の基板と対向する面側に、前記第1の電極、前記第1のリード、および前記第2のリードが設けられ、
前記第2の基板上であって前記第1の基板と対向する面側に、前記第2の電極および前記第3のリードが設けられ、
前記第1の電極および前記第2の電極のうち、いずれか一方が作用極、他方が対極として機能し、
前記第1の基板および/または前記第2の基板の少なくとも一部を押さえることにより、前記第1のリードおよび前記第2のリードの少なくとも端部が外部に露出した状態で、前記第2のリードと前記第3のリードとが電気的に接触することを特徴とするバイオセンサを提供する。
上記バイオセンサにおいては、前記第3のリードが複数に分割されており、前記第2のリードを複数個有することが有効である。
【0025】
このような本発明に係るバイオセンサにおいては、第1の端子および/または第2の基板の少なくとも一部を押さえることにより、第2のリードと第3のリードとが電気的に接触するため、第1の基板の同じ面上に設けた第1のリードおよび第2のリードの端部を用いて測定装置側の接続端子との電気的な接続が可能になり、従来の平面型バイオセンサと同じ測定装置を用いることができる。
【0026】
また、リードを導通させるための貫通孔や切欠部をセンサ側に設ける必要がないため、センサの製造工程が容易になる。
ここで、第3のリードが複数に分割されており、複数の第2のリードを有することが好ましい。このようにすると、複数の第2のリードのうち、第3のリードと接触させる第2のリードをセンサの製造ロットに対応して変化させ、センサを測定装置に挿入した際に、複数の第2のリードの内、第3のリードと接続しているものを測定装置側で検出することにより、測定装置においてセンサの製造ロットの判定を行うことができる。したがって、測定前にロット番号を測定装置に手入力したり、ロット番号が判別可能な補正用のチップを測定前に測定装置に挿入したりする手間をなくすことができる。
【0027】
つぎに、本発明は、バイオセンサを挿入するセンサ差し込み口と、押さえ部と、測定装置と接続するための接続口とを具備することを特徴とするアダプタに関する。
さらに具体的には、本発明は、前記バイオセンサの少なくとも一部を挿入するセンサ差し込み口、挿入された前記バイオセンサの前記第1の基板および/または前記第2の基板の少なくとも一部を押さえて、前記第2のリードと前記第3のリードとを電気的に接触させる押さえ部、および測定装置と接続する接続口を有することを特徴とするアダプタをも提供する。
【0028】
このようにすると、このアダプタのセンサ差し込み口に本発明のバイオセンサを挿入することによりセンサの第1の基板および/または第2の基板が押さえられるので、センサの第2のリードと第3のリードとを容易に接触させることができる。
ここで、押さえ部の一部が弾性体により構成されることが好ましい。このようにすると、より確実にバイオセンサを押さえることが可能となり、センサの第2のリードと第3のリードとをより確実に接触させることができる。
【0029】
さらに、本発明は、バイオセンサと、押さえ部を含むアダプタと、測定手段とを具備することを特徴とする測定装置に関する。
詳細には、この測定装置は、前記バイオセンサを前記アダプタを介して着脱可能に接続し、前記試料供給部に供給される試料液中に含まれる基質を測定する測定装置であって、
前記バイオセンサの前記第1のリードと電気的に接続する第1の端子、
前記バイオセンサの前記複数個の第2のリードとそれぞれ電気的に接続する複数個の第2の端子、
前記第1の端子および前記複数個の第2の端子を介して前記バイオセンサの前記第1の電極と前記第2の電極との間に電圧を印加する手段、ならびに
前記第1の電極と前記第2の電極との間の電気的変化を測定する手段を有することを特徴とする。
【0030】
このようにすると、センサの製造ロットに対応して、押さえ部が設けられている位置が異なるアダプタを用い、そのアダプタを介して、第3のリードが複数に分割されており、複数の第2のリードを有するバイオセンサを測定装置に接続し、複数の第2のリードの内、第3の対極リードと接続しているものを複数の第2の端子を用いて測定装置側で検出することにより、測定装置においてセンサの製造ロットの判定を行うことができる。したがって、測定前にロット番号を測定装置に手入力したり、ロット番号が判別可能な補正用のチップを測定前に測定装置に挿入したりする手間をなくすことができる。
【0031】
さらに、本発明は、押さえ部と、
第1の電極に電気的に接続された第1のリード、第2のリード、第2の電極に電気的に接続された第3のリードを具備するバイオセンサを受けるセンサ差し込み口と、
前記バイオセンサの前記第1のリードを前記測定装置に電気的に接続する第1の端子と、
前記バイオセンサの前記第2のリードを前記測定装置に電気的に接続する第2の端子と、
前記第1の電極および前記第2の電極の間に電圧を印加する手段と、
前記第1の電極および前記第2の電極の間の電気的変化を測定する手段とを具備することを特徴とする測定装置を提供する。
【0032】
詳細には、この測定装置は、前記バイオセンサを着脱可能に接続し、前記バイオセンサの前記試料供給部に供給される試料液中に含まれる基質を測定する測定装置であって、
前記バイオセンサの前記第1のリードと電気的に接続する第1の端子、
前記バイオセンサの前記第2のリードと電気的に接続する第2の端子、
前記バイオセンサの前記第1の電極と前記第2の電極との間に電圧を印加する手段、
前記第1の電極と前記第2の電極との間の電気的変化を測定する手段、
前記バイオセンサの少なくとも一部を挿入するセンサ差し込み口、ならびに
挿入された前記バイオセンサの前記第1の基板および/または前記第2の基板の少なくとも一部を押さえて、前記第2のリードと前記第3のリードとを電気的に接触させる押さえ部を有することを特徴とする。
このようにすると、アダプタを用いることなく、本発明のバイオセンサを用いて、容易に試料液中に含まれる基質を測定することができる。
【0033】
ここで、押さえ部の一部が弾性体により構成されることが好ましい。このようにすると、より確実にバイオセンサを押さえることが可能となり、センサの第2のリードと第3のリードとをより確実に接触させることができる。
また、押さえ部が可動であることが好ましい。このようにすると、より確実にバイオセンサを押さえることが可能となり、容易に試料液中に含まれる基質を測定することができる。
また、第2の端子が押さえ部を兼ねていてもよい。このようにすると、測定装置の部材を減らすことができるため、測定装置の構成をより簡易にすることができる。
【0034】
本発明において、第1の基板としては、電気絶縁性を有し、保存および測定時に充分な剛性を有する材料であれば用いることができる。さらに、第2の基板としては第1の基板の条件に加え、第2の基板と空間を開けて設置された第1の基板上に設けられた第2のリードと第2の基板上に設けられた第3のリードとが接触するように、基板表面に垂直な方向からの力により撓むことが可能な柔軟性と、撓んだ際に基板表面に垂直な方向にかかる応力に耐える強度とを有していればよい。
【0035】
第1の基板および第2の基板の材料としては、例えば、ポリエチレン、ポリスチレン、ポリ塩化ビニル、ポリアミド、飽和ポリエステル樹脂などの熱可塑性樹脂、または尿素樹脂、メラミン樹脂、フェノール樹脂、エポキシ樹脂、不飽和ポリエステル樹脂などの熱硬化性樹脂があげられる。なかでも、電極との密着性の点から、ポリエチレンテレフタレートが好ましい。
また、弾性体としては、バネなどを用いることができる。
【0036】
以下、本発明を図面を用いてさらに詳しく説明する。なお、以下の実施の形態においては、一例としてグルコースの定量に用いるバイオセンサ、アダプタ、測定装置および定量法について説明するが、基質はグルコースに限定されない。
また、一例として、第1の電極が作用極、第2の電極が対極であって、第1の基板、第2の基板、第1のリード、第2のリード、第3のリード、第1の端子、および第2の端子がそれぞれ、作用極基板、対極基板、作用極リード、第1の対極リード、第2の対極リード、作用極端子、および対極端子である場合について示すが、これに限定されず、第1の電極が対極、第2の電極が作用極であって、第1の基板、第2の基板、第1のリード、第2のリード、第3のリード、第1の端子、および第2の端子がそれぞれ、対極基板、作用極基板、対極リード、第1の作用極リード、第2の作用極リード、対極端子、および作用極端子であってもよい。
【0037】
実施の形態1
本発明の実施の形態1について図1〜6を用いて説明する。図1は本実施の形態で用いたバイオセンサ、アダプタおよび測定装置の構成を示す概略図である。図2は、バイオセンサの試薬層および界面活性剤層を除いた分解斜視図である。また、図3および4は、アダプタおよび測定装置のセンサ差し込み口近傍の構成を示す概略図である。
【0038】
特に、図3は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに分離された状態を示す縦断面図であり、図4は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに接続された状態を示す縦断面図である。図5は、図3および4における測定装置1のセンサ差し込み口の一部透明概略斜視図であり、図6はアダプタのセンサ差し込み口方向から見た正面図である。
【0039】
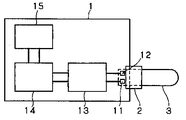
図1において、測定装置1は、作用極端子11、対極端子12、測定部13、演算部14、およびデータ表示部15を備えており、従来の平面型バイオセンサ用の測定装置と同様の構成を有している。
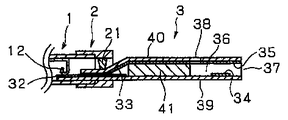
バイオセンサ3は、アダプタ2を介して測定装置1に着脱可能に接続される。図2において、バイオセンサ3は、作用極基板39、対極基板40、作用極リード31、第1の対極リード32、第2の対極リード33、作用極34、対極35、試薬層(図示せず)、試料供給部36を構成するためのスリットを有するスペーサ部材41、試料供給部36に連通した開口部である空気孔38、および試料供給口37を備えている。
【0040】
作用極基板39上に、スパッタリングによりパラジウム薄膜を堆積した後、フォトリソグラフィおよびドライエッチングによりパターニングし、作用極リード31、第1の対極リード32および作用極34を形成した。同様に、対極基板40上全面にスパッタリングによりパラジウム薄膜を堆積し、第2の対極リード33および対極35を形成した。対極基板40の長手方向の長さは作用極基板39よりも短くなっている。また、対極基板40にはスリットが設けられており、第2の対極リード33の端部の幅を第1の対極リード32の幅以下とした。
【0041】
ここで、作用極基板39上に形成したパラジウム薄膜パターンおよび対極基板40上に形成したパラジウム薄膜のうち、バイオセンサ3を組み立てた際に試料供給部36に面する部分が、それぞれ作用極34および対極35として機能する。
酸化還元酵素であるGODおよび電子伝達体であるフェリシアン化カリウムを含有する水溶液を作用極34上に滴下した後乾燥することにより試薬層を形成した。さらに、試料供給を円滑に行うことを目的として、試薬層上および試料供給部36に面する作用極基板39上に、界面活性剤であるレシチンを含有する界面活性剤層を形成した。
最後に、作用極基板39、スペーサ部材41および対極基板40を接着することにより、バイオセンサ3を作製した。
【0042】
アダプタ2は、バイオセンサの一部をリードが設けられた方向から挿入するセンサ差し込み口22、測定装置と接続する接続口23、および挿入されたバイオセンサの対極基板40の少なくとも一部を押さえる押さえ部21を有している。測定時には、アダプタ2の接続口23側を測定装置1に装着し、バイオセンサ3をアダプタ2のセンサ差し込み口22から装着する。すると、押さえ部21により対極基板40の一部が押さえられて対極基板40の端部が撓み、第1の対極リード32と第2の対極リード33とが接触する。
【0043】
このとき、対極基板40の長手方向の長さは作用極基板39よりも短くなっているため、作用極基板39上に設けられた作用極リード31および第1の対極リード32の端部がセンサ外部に露出する。作用極リード31および第1の対極リード32の露出した部分がセンサ側の接続端子となり、それぞれ測定装置1側の作用極端子11および対極端子12と接続する(図2、4および5参照)。この状態で作用極端子11−対極端子12間に電圧を印加すると、作用極34−対極35間に電圧を印加することが可能となる。
【0044】
つぎに、試料液としてβ−D−グルコース水溶液を用い、試料液中のβ−D−グルコース濃度の定量を行った。まず、β−D−グルコース濃度の異なる数種の試料液をそれぞれ調整し、試料液をバイオセンサ3の試料供給口37に接触させた。空気孔38は試料供給部36に連通しているので、試料供給口37に導入された試料液は、毛管現象によって内部に浸透し、試料供給部36に供給された。つぎに、測定装置1の測定部13により、対極35を基準にして300mVの電圧を作用極34に印加し、この時に作用極34に流れる電流値を、測定部13を用いて測定した。測定部13で得た値を、あらかじめ記憶している検量線を参照することにより演算部14において濃度に変換し、得られた結果をデータ表示部15に表示した。
【0045】
実施の形態2
本発明の実施の形態2について、図7〜13を用いて説明する。実施の形態1との違いは、バイオセンサの第1の対極リードが3つに分割されており、それに対応して3つの第2の対極リードを備えた点、および測定装置において3つの対極端子を備えた点である。図7は本実施の形態で用いたバイオセンサ、アダプタおよび測定装置の構成を示す概略図である。
【0046】
図8は、バイオセンサの試薬層および界面活性剤層を除いた分解斜視図であり、図9は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに分離された状態を示す縦断面図である。また、図10は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに接続された状態を示す縦断面図であり、図11〜13は、押さえ部の位置が異なる3種類のアダプタのセンサ差し込み口方向から見た正面図である。
【0047】
図7において、測定装置1は、作用極端子11、対極端子a121、対極端子b122、対極端子c123、測定部13、演算部14、およびデータ表示部15を備えている。
実施の形態1と同様に、バイオセンサ3はアダプタ2を介して測定装置1に着脱可能に接続される。バイオセンサ3は、作用極基板39、対極基板40、作用極リード31、第1の対極リードa321、第1の対極リードb322、第1の対極リードc323、第2の対極リードa331、第2の対極リードb332、第2の対極リードc333、作用極34、対極35、試薬層(図示せず)、試料供給部36を構成するためのスリットを有するスペーサ部材41、試料供給部36に連通した開口部である空気孔38、および試料供給口37を備えている。
【0048】
作用極基板39上に3つ第1の対極リード321、322、323が設けられ、それに対向する対極基板40上の位置に3つの第2の対極リード331、332、333が形成されるように、対極基板40に3本のスリットが設けられている点以外は、実施の形態1と同様にして、バイオセンサ3を作製した。
本実施の形態のアダプタ201、202、203は、実施の形態1と同様にセンサ差し込み口22、接続口23および押さえ部21を有しているが、実施の形態1よりも押さえ部21の幅が狭い。
【0049】
ここで、バイオセンサ3の製造工程において、特性検査の結果から性能に応じて、例えば3段階のロット番号A、B、Cを付与しておく。測定に用いようとするバイオセンサ3のロット番号がAの場合は、図11に示したアダプタ201を用いる。アダプタ201は、センサ差し込み口22方向から見て最も左側寄りに押さえ部21が設けられており、アダプタ201を測定装置1に装着し、バイオセンサ3をアダプタ201に挿入すると、押さえ部21により対極基板40の一部が押さえられて対極基板40の端部がたわみ、第1の対極リードa321と第2の対極リードa331とが接触する。
【0050】
また、測定に用いようとするバイオセンサ3のロット番号がBの場合は、図12に示したアダプタ202を用いる。アダプタ202は、センサ差し込み口22方向から見て中央部に押さえ部21が設けられており、アダプタ202を測定装置1に装着し、バイオセンサ3をアダプタ202に挿入すると、第1の対極リードb322と第2の対極リードb332とが接触する。
【0051】
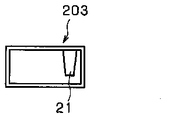
同様に、測定に用いようとするバイオセンサ3のロット番号がCの場合は、図13に示したアダプタ203を用いる。アダプタ203は、センサ差し込み口22方向から見て最も右側寄りに押さえ部21が設けられており、アダプタ203を測定装置1に装着し、バイオセンサ3をアダプタ203に挿入すると、押さえ部21により対極基板40の一部が押さえられて対極基板40の端部がたわみ、第1の対極リードc323と第2の対極リードc333とが接触する。
【0052】
つぎに、実施の形態1と同様にして、試料液としてβ−D−グルコース水溶液を用い、試料液中のβ−D−グルコース濃度の定量を行った。試料液をバイオセンサ3の試料供給口37に接触させることにより、試料供給部36に試料液を導入した。一定時間後、作用極34と対極35に試料液が接触した状態で、測定装置1において作用極端子11−対極端子a121間、作用極端子11−対極端子b122間、および作用極端子11−対極端子c123間の抵抗値等を測定することにより、3つの第2の対極リード331、332、333のうち、第1の対極リードと接続しているものを測定装置1側で検出した。このようにすることにより、測定装置1においてセンサのロット番号がA、B、Cのいずれであるかを判定することができた。
【0053】
つぎに、測定装置1の測定部13により、対極35を基準にして300mVの電圧を作用極34に印加し、この時に作用極34に流れる電流値を、測定部13を用いて測定した。判定されたロット番号に応じて、あらかじめ測定装置1内に記憶されているロット番号に対応した検量線が自動的に選択され、測定部13で得られた電流値が、選択された検量線を参照することにより演算部14において濃度に変換された後、得られた結果がデータ表示部15に表示された。したがって、本実施の形態では、用いるアダプタを選択するだけで、バイオセンサの製造ロットに応じた補正が行われるため、容易に正確な基質の定量を行うことができる。
【0054】
実施の形態3
本発明の実施の形態3について、図14〜16を用いて説明する。図14〜16は、本実施の形態で用いたバイオセンサおよび測定装置の構成を示す概略図であり、図14は押さえ部が閉じた状態の測定装置の斜視図、図15は押さえ部が開いた状態の測定装置の斜視図、図16はバイオセンサと測定装置が互いに接続された状態を示す斜視図である。
【0055】
なお、本実施の形態では、実施の形態1と同様のバイオセンサを使用した。
測定時の手順を以下に示す。まず測定装置71の押さえ部72を開け、バイオセンサ3の一部をリード方向からセンサ差し込み口73に差し込む。その時、バイオセンサ3の作用極リード31および第1の対極リード32が、測定装置71側の作用極端子(図示せず)および対極端子(図示せず)と接続する。ここで、作用極端子と対極端子は、測定装置71の内部であってセンサ差し込み口73の近傍に位置している。
【0056】
つぎに、開いていた押さえ部72を閉じると、押さえ部72によりバイオセンサ3の対極基板40の一部が押さえられて対極基板40の端部が撓み、第1の対極リード32と第2の対極リード33とが接触する。この状態で作用極端子−対極端子間に電圧を印加すると、作用極34−対極35間に電圧を印加することが可能となる。
【0057】
つぎに、試料液としてβ−D−グルコース水溶液を用い、実施の形態1と同様の方法を用いて試料液中のβ−D−グルコース濃度の定量を行った。
このようにすると、アダプタを用いることなく、本発明のバイオセンサを直接測定装置に接続して、試料液中に含まれる基質の測定を行うことができる。
【0058】
なお、実施の形態3において、作用極端子または対極端子の一部を押さえ部として使用可能な構成としてもよい。このようにすると、測定装置を構成する部材を減らすことができる。
また、本実施の形態3においては、複数存在する第1の対極リードと第2の対極リードの接触は一箇所だけである場合について記載したが、これに限定されるものではない。例えば、接触する対極リードが複数箇所あってもよい。実施の形態2を用いて説明すると、第1の対極リード321、322と第2の対極リード331、332がそれぞれ接触するようなアダプタ(図示せず)を用いた場合、センサの新たなロット番号Dを更に識別することが可能となる。
【0059】
また、実施の形態2において、第1の対極リードが3つに分割されている場合を示したが、本発明はこれに限定されず、2つ以上に分割されていれば同様の効果を得ることができる。ここで、分割されている数が多い程、バイオセンサの製造ロットの違いによる測定値の補正を細かく行うことができるので好ましい。
【0060】
また、実施の形態1および2においては、挿入されたバイオセンサの対極基板の少なくとも一部を押さえて、第1の対極リードと第2の対極リードとを接触させる押さえ部が設けられたアダプタを用いたが、これに代えて、上記押さえ部が測定装置のセンサ差し込み口内に設けられてもよい。このようにすると、アダプタを用いることなく、本発明のバイオセンサを直接測定装置に接続して、試料液中に含まれる基質の測定を行うことができる。その際、実施の形態3のように押さえ部を含んだ部材が可動してもよい。このようにすると、より確実に端子を押さえることができる。また、端子の一部を押さえ部として使用可能な構成としてもよい。このようにすると、測定装置を構成する部材を減らすことができる。
【0061】
また、実施の形態2においては、バイオセンサの製造ロットを判別する例を示したが、これに限らない。例えば、バイオセンサの測定対象を判別してもよい。その場合、例えば、測定対象物である基質がグルコース、乳酸、あるいはコレステロールである3種類のバイオセンサを一つの測定装置で測定することが可能となる。この場合、測定装置1内に記憶されている検量線はロット番号ではなく基質に対応した検量線となっている。またこの場合も製造ロット判別の時と同様に、第1の対極リードの分割数は3に限定されるものではない。
【0062】
また、以上の実施の形態において、作用極34への印加電圧を対極35を基準に300mVとしたが、これに限定されず、電子伝達体が作用極34上で電極反応可能な電圧であればよい。
また、空気孔38の位置は、図に示した位置に限定されず、試料供給部36と通じており、試料供給部36に対して試料供給口37と反対側に位置していればよい。
【0063】
さらに、以上の実施の形態では、酸化還元酵素を含む溶液を塗布および乾燥することにより試薬層を形成したが、これに限定されず、例えばインクジェット方式により、試薬を含んだ溶液を塗布してもよい。このようにすると、塗布する溶液量が微量であっても試薬層の正確な位置制御が可能となる。また、試薬を含んだ溶液をガラスろ紙に担持し、乾燥したガラスろ紙を試料供給部36内に位置させてもよい。
【0064】
さらにまた、導電材料と試薬を混合することにより電極を形成してもよい。試薬の担持位置としては、作用極34または対極35上にあることが好ましいが、それに限らず、試料と接することが可能な位置であれば、試料供給部36内の作用極34および対極35上以外の場所でもよい。
スペーサ部材41としては、電気絶縁性を有し、保存および測定時に充分な剛性を有する材料であれば用いることができる。例えば、ポリエチレン、ポリスチレン、ポリ塩化ビニル、ポリアミド、飽和ポリエステル樹脂などの熱可塑性樹脂、または尿素樹脂、メラミン樹脂、フェノール樹脂、エポキシ樹脂、不飽和ポリエステル樹脂などの熱硬化性樹脂があげられる。
【0065】
作用極としては、電子伝達体を酸化する際にそれ自身が酸化されない導電性材料であれば用いることができる。対極としては、パラジウム、銀、白金、カーボン等の一般的に用いられる導電性材料であれば用いることができる。また、電気絶縁性の材料の表面をこれらの導電性材料で被覆しても良い。
また、以上の実施の形態では、電極系の形成方法としてフォトリソグラフィを使用したがそれに限定されない。例えば、パラジウムなどの貴金属を基板上にスパッタリングした後、レーザートリミングにより電極パターンを形成する方法や、基板上に導電ペースト等をスクリーン印刷することにより電極パターンを形成する等の製造方法を用いてもよい。
【0066】
さらに、以上の実施の形態では、第2の基板は第1の基板よりも長手方向に短くなっている構成であったが、これに限定されず、第2のリードと第3のリードとを電気的に接触させるために第2の基板の少なくとも一部を押さえたとき、第1のリードおよび第2のリードの少なくとも端部が外部に露出するように、第1の基板および第2の基板の寸法、配置などが調整されていればよい。
【0067】
酸化還元酵素としては、試料中に含まれる測定対象物である基質に対応したものが用いられ、例えば、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼ、アミノ酸オキシダーゼ等が挙げられる。
【0068】
電子伝達体としては、フェリシアン化カリウム、p−ベンゾキノン、フェナジンメトサルフェート、メチレンブルー、フェロセン誘導体等があげられる。また、酸素を電子伝達体とした場合にも電流応答が得られる。電子伝達体は、これらの一種または二種以上が使用される。
【0069】
また、以上の実施の形態では試料としてβ−D−グルコース水溶液を使用したが、これに限定されない。例えば、全血、血漿、血清、間質液、唾液、尿などの生体試料に対しても使用可能である。ここで、全血としては、例えば、指先や腕の皮膚を穿刺し採取した毛細血、あるいは静脈血、動脈血などを用いることができる。
【0070】
【発明の効果】
以上のように、本発明によれば、簡易な構成により、測定装置と容易に接続することができる対向型バイオセンサ、それに用いるアダプタおよび測定装置を提供することができる。
【図面の簡単な説明】
【図1】本発明の一実施の形態によるバイオセンサ、アダプタおよび測定装置の構成を示す概略図
【図2】同実施の形態におけるバイオセンサの試薬層および界面活性剤層を除いた分解斜視図
【図3】同実施の形態におけるアダプタおよび測定装置のセンサ差し込み口近傍の構成を示す概略図
【図4】同実施の形態におけるアダプタおよび測定装置のセンサ差し込み口近傍の構成を示す別の概略図
【図5】図3および4における測定装置1のセンサ差し込み口の一部透明概略斜視図
【図6】アダプタのセンサ差し込み口方向から見た正面図
【図7】本発明の他の実施の形態で用いたバイオセンサ、アダプタおよび測定装置の構成を示す概略図
【図8】バイオセンサの試薬層および界面活性剤層を除いた分解斜視図
【図9】測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに分離された状態を示す縦断面図
【図10】測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに接続された状態を示す縦断面図
【図11】アダプタのセンサ差し込み口方向から見た正面図
【図12】押さえ部の位置が異なるアダプタのセンサ差し込み口方向から見た正面図
【図13】押さえ部の位置が異なる別のアダプタのセンサ差し込み口方向から見た正面図
【図14】本発明のさらに別の実施の形態における測定装置の構成を示す概略図
【図15】同実施の形態における測定装置の構成を示す別の概略図
【図16】同実施の形態における測定装置とバイオセンサの構成を示す概略図
【符号の説明】
1、71 測定装置
11 作用極端子
12 対極端子
121 対極端子a
122 対極端子b
123 対極端子c
13 測定部
14 演算部
15 データ表示部
2、201、202、203 アダプタ
21、72 押さえ部
22、73 センサ差し込み口
23 接続口
3 バイオセンサ
31 作用極リード
32 第1の対極リード
321 第1の対極リードa
322 第1の対極リードb
323 第1の対極リードc
33 第2の対極リード
331 第2の対極リードa
332 第2の対極リードb
333 第2の対極リードc
34 作用極
35 対極
36 試料供給部
37 試料供給口
38 空気孔
39 作用極基板
40 対極基板
41 スペーサ部材
【発明の属する技術分野】
本発明は、試料中に含まれる基質を迅速かつ高精度に定量するためのバイオセンサ、それに用いるアダプタ、および測定装置に関する。
【0002】
【従来の技術】
スクロース、グルコースなど糖類の定量分析法として、施光度計法、比色法、還元滴定法および各種クロマトグラフィーを用いた方法などが開発されている。しかし、これらの方法は、いずれも糖類に対する特異性があまり高くなく、精度に劣る。また、これらの方法のうち、施光度計法においては、操作は簡便ではあるが、操作時の温度の影響を大きく受ける。したがって、施光度計法は、一般の人々が家庭などで簡易に糖類を定量する方法としては適切でない。
近年、酵素の有する特異的触媒作用を利用した種々のタイプのバイオセンサが開発されている。以下に、試料中の基質の定量法の一例としてグルコースの定量法について説明する。電気化学的なグルコースの定量法としては、酵素であるグルコースオキシダーゼ(EC1.1.3.4、GOD)と酸素電極または過酸化水素電極とを使用して行う方法が一般に知られている。
【0003】
GODは、酸素を電子伝達体として、基質であるβ−D−グルコースをD−グルコノ−δ−ラクトンに選択的に酸化する。酸素の存在下、GODによる酸化反応過程において、酸素は過酸化水素に還元される。酸素電極によって、この酸素の減少量を計測するか、または過酸化水素電極によって過酸化水素の増加量を計測する。酸素の減少量および過酸化水素の増加量は、試料中のグルコースの含有量に比例するため、酸素の減少量または過酸化水素の増加量からグルコースの定量を行うことができる。
上記方法では、酵素反応の特異性を利用することにより、精度良く試料中のグルコースを定量することができる。しかし、反応過程からも推測できるように、測定結果は試料に含まれる酸素濃度の影響を大きく受けるという欠点があり、試料に酸素が存在しない場合は測定が不可能となる。
【0004】
そこで、酸素を電子伝達体として用いず、フェリシアン化カリウム、フェロセン誘導体およびキノン誘導体などの有機化合物や金属錯体を電子伝達体として用いる新しいタイプのグルコースセンサが開発されてきた。このタイプのセンサでは、酵素反応の結果生じた電子伝達体の還元体を作用極上で酸化することにより、その酸化電流量から試料中に含まれるグルコース濃度が求められる。
この際、対極上では、電子伝達体の酸化体が還元され、電子伝達体の還元体の生成する反応が進行する。このような有機化合物や金属錯体を酸素の代わりに電子伝達体として用いることにより、既知量のGODとそれらの電子伝達体を安定な状態で正確に電極上に担持させて試薬層を形成することが可能となり、試料中の酸素濃度の影響を受けることなく、精度良くグルコースを定量することができる。
【0005】
また、この場合、酵素および電子伝達体を含有する試薬層を乾燥状態に近い状態で電極系と一体化させることもできるため、この技術に基づいた使い捨て型のグルコースセンサが近年多くの注目を集めている。その代表的な例が、特許文献1に示されるバイオセンサである。使い捨て型のグルコースセンサにおいては、測定装置に着脱可能に接続されたセンサに試料を導入するだけで容易にグルコース濃度を測定装置で測定することができる。
上記のようなグルコースセンサを用いた測定では、数μlオーダーの試料量で試料中の基質濃度を容易に求めることが可能である。しかし、近年、さらに微量(1μl以下)な試料での測定が可能なバイオセンサの開発が各方面において切望されている。
【0006】
従来の電気化学グルコースセンサは、殆どの場合、一平面上に電極系が配置された平面型バイオセンサであり、極微量の試料における測定では電極間の電荷移動(主にイオンの移動)に対する抵抗が大きくなることにより、測定感度が低下したり、測定結果にバラツキが生じる場合があった。
そこで、例えば特許文献2においては、作用極と対極が相互に対向する位置に配置されたバイオセンサ(対向型バイオセンサ)が提案されている。このタイプのセンサでは、作用極と対極とを相互に対向する位置に配置したことにより作用極−対極間のイオン移動が円滑になるなどの理由から、従来の平面型バイオセンサよりも、高精度かつ高感度で試料中に含まれるグルコース等の基質を定量することができる。
【0007】
しかし、対向型バイオセンサは、センサと測定装置とを電気的に接続する際、作用極と対極が同一平面状に無いために、センサのリード形状または測定装置の接続端子形状を平面型バイオセンサとは異なる形状にする必要がある。例えば特許文献2には、作用極基板および対極基板に、他方の基板上に形成された作用極リードまたは対極リードをそれぞれ表裏逆向きに外部に臨ませる貫通孔を設けた対向型バイオセンサが開示されている。また、特許文献3には、それぞれ作用極または対極が形成された2枚の絶縁性基板に、対向する絶縁性基板が有する接続端子を露出させるように切欠部が形成され、両絶縁性基板の接続端子がそれぞれ表裏逆向きに露出している対向型バイオセンサが開示されている。これらのバイオセンサでは、作用極リード用の接続端子および対極リード用の接続端子が表裏逆向きに露出しているため、測定装置側の作用極用の接続端子と対極用の接続端子とを上下逆方向を向くように、平面型バイオセンサとは異なる特殊な形状にする必要があった。
【0008】
さらに、特許文献4には、長い下部基板と短い上部基板を具備するバイオセンサが開示されており、下部基板の端部と上部基板の端部とは重なっておらず、作用極および対極のリード部が、長い下部基板の内側に形成されている。また、作用極および対極が短い上部基板上に形成されており、接着層またはスペーサが、それらの基板の間に介在している。そして、作用極および対極のリード部は、前記接着剤層またはスペーサを貫通して電気的に接続される。
また、測定装置側の接続端子の形状は、平面型バイオセンサと同じであってよいが、センサ側にリードを形成するとともに、これらリードを接着層、スペーサまたは基板などを貫通させる必要があるため、製造プロセスを煩雑かつ複雑にしていた。
【0009】
【特許文献1】
特開平3−202764号公報(特許第2517153号)
【特許文献2】
特開平11−352093号公報
【特許文献3】
特開平9−159642号公報
【特許文献4】
特開平11−125618号公報
【0010】
【発明が解決しようとする課題】
以上のように、従来の対向型バイオセンサにおいては、平面型バイオセンサと異なり、センサのリードまたは測定装置の接続端子の形状を特殊な形状にする必要があった。このような状況に鑑み、本発明は、単純なリードを有し、かつ測定装置に容易に接続し得る平面型バイオセンサ、それに用いるアダプタならびに測定装置を提供することを目的とする。
【0011】
【課題を解決するための手段】
上記の問題を解決すべく、本発明は、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、
前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、
前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記第1電極または前記第2電極の一方が作用極として機能し、他方が対極として機能し、前記第1の基板および/または前記第2の基板をいずれかの基板に向けて押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触することを特徴とするバイオセンサを提供する。
【0012】
前記バイオセンサにおいては、前記第3のリードが複数に分割されており、前記第2のリードを複数個有することが有効である。
また、前記第1の基板と前記第2の基板との間にスペーサ部材を有することが有効である。
また、前記スペーサ部材が、前記第1の基板および前記第2の基板の少なくとも一方と一体化されていることが有効である。
前記スペーサ部材は、前記第1の基板と一体化されていてもよく、また、前記第2の基板と一体化されていてもよい。
【0013】
また、前記バイオセンサにおいては、前記第2の基板が、長手方向において、前記第1の基板よりも短いことが有効である。逆に、前記第1の基板が前記2の基板よりも短くてもよい。
また、前記試料供給部内に、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼおよびアミノ酸オキシダーゼよりなる群から選択される酵素を含む試薬を具備することが有効である。
【0014】
つぎに、本発明は、バイオセンサを挿入するセンサ差し込み口と、押さえ部と、測定装置と接続するための接続口とを具備することを特徴とするアダプタを提供する。
このアダプタにおいては、前記センサ差し込み口に挿入された前記バイオセンサを受け、
前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、例えば撓ませたり曲げたりすることによって、他方の基板に向けて移動させることが有効である。
このアダプタに用いるバイオセンサは、上述した構成を有するのが有効である。
【0015】
さらに、本発明は、バイオセンサと、押さえ部を含むアダプタと、測定手段とを具備することを特徴とする測定装置を提供する。
この測定装置においても、前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、例えば撓ませたり曲げたりすることによって他方の基板に向けて移動させ得ることが有効である。
【0016】
この測定装置において用いるバイオセンサも、上述のようなバイオセンサの構成を有するのが有効であり、前記測定装置は、試料液中の基質を測定するものであるのが有効である。
さらに、前記測定装置は、前記バイオセンサの前記第1の電極に電気的に接続される第1の端子と、前記バイオセンサの前記第2の電極にそれぞれ電気的に接続される少なくとも1つの第2の端子とを具備することが有効である。
【0017】
また、前記測定手段が、前記第1の端子および前記少なくとも1つの第2の端子を介して、前記バイオセンサの前記第1の電極および前記第2の電極の間に電圧を印加する手段と、前記第1の電極および前記第2の電極の間の電気的変化を測定する手段を具備することが有効である。
また、前記測定装置が、前記第2の端子を複数個有することが有効である。
また、前記測定装置が、前記第1の端子および前記複数個の第2の端子の間の電気的変化を測定する手段を具備することが有効である。
さらに、前記複数個の第2の端子のうち前記第1の端子に電気的に接続された第1の端子を検知する手段と、検知された第2の端子の数および位置に基づいてバイオセンサの種類を決定する手段と、前記種類に応じて測定結果を補正する手段とを具備することが有効である。
【0018】
さらにまた、本発明は、押さえ部と、
第1の電極に電気的に接続された第1のリード、第2のリード、第2の電極に電気的に接続された第3のリードを具備するバイオセンサを受けるセンサ差し込み口と、
前記バイオセンサの前記第1のリードを前記測定装置に電気的に接続する第1の端子と、
前記バイオセンサの前記第2のリードを前記測定装置に電気的に接続する第2の端子と、
前記第1の電極および前記第2の電極の間に電圧を印加する手段と、
前記第1の電極および前記第2の電極の間の電気的変化を測定する手段とを具備することを特徴とする測定装置を提供する。
【0019】
この測定装置も、前記第2の端子を複数個具備することが有効である。
また、前記第1の端子および前記複数個の第2の端子の間の電気的変化を測定する手段とを具備することが有効である。
また、前記押さえ部が弾性体で構成されていることが有効である。
また、前記第2の端子が前記押さえ部として機能することが有効である。
【0020】
この測定装置において用いるバイオセンサも、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、例えば撓ませたり曲げたりすることによって、他方の基板に向けて移動させ得ることが有効である。
【0021】
また、ここで用いるバイオセンサも、上述のようなバイオセンサの構成を有するのが有効である。
また、この測定装置は、前記バイオセンサの前記第1の基板または前記第2の基板の少なくとも一部を押さえて前記第2の電極および前記第3の電極を電気的に接続し、前記バイオセンサの前記試料供給部に供給された試料液中の基質を測定することが有効である。
【0022】
また、前記複数個の第2の端子のうち前記第1の端子に電気的に接続された第2の端子を検知する手段と、検知された第2の端子の数および位置に基づいてバイオセンサの種類を決定する手段と、前記種類に応じて測定結果を補正する手段とを具備することが有効である。
さらに、前記押さえ部が可動し、前記バイオセンサの前記第1の基板および/または前記第2の基板において押さえられる部分が、前記押さえ部によって決定され得ることが有効である。
【0023】
【発明の実施の形態】
本発明に係るバイオセンサは、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、
前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、
前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記第1電極または前記第2電極の一方が作用極として機能し、他方が対極として機能し、前記第1の基板および/または前記第2の基板をいずれかの基板に向けて押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触することを特徴とする。
【0024】
より具体的には、本発明は、第1の基板、第2の基板、第1の電極、第2の電極、前記第1の電極と電気的に接続された第1のリード、第2のリード、前記第2の電極と電気的に接続された第3のリード、前記第1の基板と前記第2の基板との間に設けられ試料供給部を形成するスペーサ部材、および少なくとも一部が前記試料供給部に露出するように設けられた少なくとも酵素を含む試薬を具備し、
前記第1の基板上であって前記第2の基板と対向する面側に、前記第1の電極、前記第1のリード、および前記第2のリードが設けられ、
前記第2の基板上であって前記第1の基板と対向する面側に、前記第2の電極および前記第3のリードが設けられ、
前記第1の電極および前記第2の電極のうち、いずれか一方が作用極、他方が対極として機能し、
前記第1の基板および/または前記第2の基板の少なくとも一部を押さえることにより、前記第1のリードおよび前記第2のリードの少なくとも端部が外部に露出した状態で、前記第2のリードと前記第3のリードとが電気的に接触することを特徴とするバイオセンサを提供する。
上記バイオセンサにおいては、前記第3のリードが複数に分割されており、前記第2のリードを複数個有することが有効である。
【0025】
このような本発明に係るバイオセンサにおいては、第1の端子および/または第2の基板の少なくとも一部を押さえることにより、第2のリードと第3のリードとが電気的に接触するため、第1の基板の同じ面上に設けた第1のリードおよび第2のリードの端部を用いて測定装置側の接続端子との電気的な接続が可能になり、従来の平面型バイオセンサと同じ測定装置を用いることができる。
【0026】
また、リードを導通させるための貫通孔や切欠部をセンサ側に設ける必要がないため、センサの製造工程が容易になる。
ここで、第3のリードが複数に分割されており、複数の第2のリードを有することが好ましい。このようにすると、複数の第2のリードのうち、第3のリードと接触させる第2のリードをセンサの製造ロットに対応して変化させ、センサを測定装置に挿入した際に、複数の第2のリードの内、第3のリードと接続しているものを測定装置側で検出することにより、測定装置においてセンサの製造ロットの判定を行うことができる。したがって、測定前にロット番号を測定装置に手入力したり、ロット番号が判別可能な補正用のチップを測定前に測定装置に挿入したりする手間をなくすことができる。
【0027】
つぎに、本発明は、バイオセンサを挿入するセンサ差し込み口と、押さえ部と、測定装置と接続するための接続口とを具備することを特徴とするアダプタに関する。
さらに具体的には、本発明は、前記バイオセンサの少なくとも一部を挿入するセンサ差し込み口、挿入された前記バイオセンサの前記第1の基板および/または前記第2の基板の少なくとも一部を押さえて、前記第2のリードと前記第3のリードとを電気的に接触させる押さえ部、および測定装置と接続する接続口を有することを特徴とするアダプタをも提供する。
【0028】
このようにすると、このアダプタのセンサ差し込み口に本発明のバイオセンサを挿入することによりセンサの第1の基板および/または第2の基板が押さえられるので、センサの第2のリードと第3のリードとを容易に接触させることができる。
ここで、押さえ部の一部が弾性体により構成されることが好ましい。このようにすると、より確実にバイオセンサを押さえることが可能となり、センサの第2のリードと第3のリードとをより確実に接触させることができる。
【0029】
さらに、本発明は、バイオセンサと、押さえ部を含むアダプタと、測定手段とを具備することを特徴とする測定装置に関する。
詳細には、この測定装置は、前記バイオセンサを前記アダプタを介して着脱可能に接続し、前記試料供給部に供給される試料液中に含まれる基質を測定する測定装置であって、
前記バイオセンサの前記第1のリードと電気的に接続する第1の端子、
前記バイオセンサの前記複数個の第2のリードとそれぞれ電気的に接続する複数個の第2の端子、
前記第1の端子および前記複数個の第2の端子を介して前記バイオセンサの前記第1の電極と前記第2の電極との間に電圧を印加する手段、ならびに
前記第1の電極と前記第2の電極との間の電気的変化を測定する手段を有することを特徴とする。
【0030】
このようにすると、センサの製造ロットに対応して、押さえ部が設けられている位置が異なるアダプタを用い、そのアダプタを介して、第3のリードが複数に分割されており、複数の第2のリードを有するバイオセンサを測定装置に接続し、複数の第2のリードの内、第3の対極リードと接続しているものを複数の第2の端子を用いて測定装置側で検出することにより、測定装置においてセンサの製造ロットの判定を行うことができる。したがって、測定前にロット番号を測定装置に手入力したり、ロット番号が判別可能な補正用のチップを測定前に測定装置に挿入したりする手間をなくすことができる。
【0031】
さらに、本発明は、押さえ部と、
第1の電極に電気的に接続された第1のリード、第2のリード、第2の電極に電気的に接続された第3のリードを具備するバイオセンサを受けるセンサ差し込み口と、
前記バイオセンサの前記第1のリードを前記測定装置に電気的に接続する第1の端子と、
前記バイオセンサの前記第2のリードを前記測定装置に電気的に接続する第2の端子と、
前記第1の電極および前記第2の電極の間に電圧を印加する手段と、
前記第1の電極および前記第2の電極の間の電気的変化を測定する手段とを具備することを特徴とする測定装置を提供する。
【0032】
詳細には、この測定装置は、前記バイオセンサを着脱可能に接続し、前記バイオセンサの前記試料供給部に供給される試料液中に含まれる基質を測定する測定装置であって、
前記バイオセンサの前記第1のリードと電気的に接続する第1の端子、
前記バイオセンサの前記第2のリードと電気的に接続する第2の端子、
前記バイオセンサの前記第1の電極と前記第2の電極との間に電圧を印加する手段、
前記第1の電極と前記第2の電極との間の電気的変化を測定する手段、
前記バイオセンサの少なくとも一部を挿入するセンサ差し込み口、ならびに
挿入された前記バイオセンサの前記第1の基板および/または前記第2の基板の少なくとも一部を押さえて、前記第2のリードと前記第3のリードとを電気的に接触させる押さえ部を有することを特徴とする。
このようにすると、アダプタを用いることなく、本発明のバイオセンサを用いて、容易に試料液中に含まれる基質を測定することができる。
【0033】
ここで、押さえ部の一部が弾性体により構成されることが好ましい。このようにすると、より確実にバイオセンサを押さえることが可能となり、センサの第2のリードと第3のリードとをより確実に接触させることができる。
また、押さえ部が可動であることが好ましい。このようにすると、より確実にバイオセンサを押さえることが可能となり、容易に試料液中に含まれる基質を測定することができる。
また、第2の端子が押さえ部を兼ねていてもよい。このようにすると、測定装置の部材を減らすことができるため、測定装置の構成をより簡易にすることができる。
【0034】
本発明において、第1の基板としては、電気絶縁性を有し、保存および測定時に充分な剛性を有する材料であれば用いることができる。さらに、第2の基板としては第1の基板の条件に加え、第2の基板と空間を開けて設置された第1の基板上に設けられた第2のリードと第2の基板上に設けられた第3のリードとが接触するように、基板表面に垂直な方向からの力により撓むことが可能な柔軟性と、撓んだ際に基板表面に垂直な方向にかかる応力に耐える強度とを有していればよい。
【0035】
第1の基板および第2の基板の材料としては、例えば、ポリエチレン、ポリスチレン、ポリ塩化ビニル、ポリアミド、飽和ポリエステル樹脂などの熱可塑性樹脂、または尿素樹脂、メラミン樹脂、フェノール樹脂、エポキシ樹脂、不飽和ポリエステル樹脂などの熱硬化性樹脂があげられる。なかでも、電極との密着性の点から、ポリエチレンテレフタレートが好ましい。
また、弾性体としては、バネなどを用いることができる。
【0036】
以下、本発明を図面を用いてさらに詳しく説明する。なお、以下の実施の形態においては、一例としてグルコースの定量に用いるバイオセンサ、アダプタ、測定装置および定量法について説明するが、基質はグルコースに限定されない。
また、一例として、第1の電極が作用極、第2の電極が対極であって、第1の基板、第2の基板、第1のリード、第2のリード、第3のリード、第1の端子、および第2の端子がそれぞれ、作用極基板、対極基板、作用極リード、第1の対極リード、第2の対極リード、作用極端子、および対極端子である場合について示すが、これに限定されず、第1の電極が対極、第2の電極が作用極であって、第1の基板、第2の基板、第1のリード、第2のリード、第3のリード、第1の端子、および第2の端子がそれぞれ、対極基板、作用極基板、対極リード、第1の作用極リード、第2の作用極リード、対極端子、および作用極端子であってもよい。
【0037】
実施の形態1
本発明の実施の形態1について図1〜6を用いて説明する。図1は本実施の形態で用いたバイオセンサ、アダプタおよび測定装置の構成を示す概略図である。図2は、バイオセンサの試薬層および界面活性剤層を除いた分解斜視図である。また、図3および4は、アダプタおよび測定装置のセンサ差し込み口近傍の構成を示す概略図である。
【0038】
特に、図3は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに分離された状態を示す縦断面図であり、図4は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに接続された状態を示す縦断面図である。図5は、図3および4における測定装置1のセンサ差し込み口の一部透明概略斜視図であり、図6はアダプタのセンサ差し込み口方向から見た正面図である。
【0039】
図1において、測定装置1は、作用極端子11、対極端子12、測定部13、演算部14、およびデータ表示部15を備えており、従来の平面型バイオセンサ用の測定装置と同様の構成を有している。
バイオセンサ3は、アダプタ2を介して測定装置1に着脱可能に接続される。図2において、バイオセンサ3は、作用極基板39、対極基板40、作用極リード31、第1の対極リード32、第2の対極リード33、作用極34、対極35、試薬層(図示せず)、試料供給部36を構成するためのスリットを有するスペーサ部材41、試料供給部36に連通した開口部である空気孔38、および試料供給口37を備えている。
【0040】
作用極基板39上に、スパッタリングによりパラジウム薄膜を堆積した後、フォトリソグラフィおよびドライエッチングによりパターニングし、作用極リード31、第1の対極リード32および作用極34を形成した。同様に、対極基板40上全面にスパッタリングによりパラジウム薄膜を堆積し、第2の対極リード33および対極35を形成した。対極基板40の長手方向の長さは作用極基板39よりも短くなっている。また、対極基板40にはスリットが設けられており、第2の対極リード33の端部の幅を第1の対極リード32の幅以下とした。
【0041】
ここで、作用極基板39上に形成したパラジウム薄膜パターンおよび対極基板40上に形成したパラジウム薄膜のうち、バイオセンサ3を組み立てた際に試料供給部36に面する部分が、それぞれ作用極34および対極35として機能する。
酸化還元酵素であるGODおよび電子伝達体であるフェリシアン化カリウムを含有する水溶液を作用極34上に滴下した後乾燥することにより試薬層を形成した。さらに、試料供給を円滑に行うことを目的として、試薬層上および試料供給部36に面する作用極基板39上に、界面活性剤であるレシチンを含有する界面活性剤層を形成した。
最後に、作用極基板39、スペーサ部材41および対極基板40を接着することにより、バイオセンサ3を作製した。
【0042】
アダプタ2は、バイオセンサの一部をリードが設けられた方向から挿入するセンサ差し込み口22、測定装置と接続する接続口23、および挿入されたバイオセンサの対極基板40の少なくとも一部を押さえる押さえ部21を有している。測定時には、アダプタ2の接続口23側を測定装置1に装着し、バイオセンサ3をアダプタ2のセンサ差し込み口22から装着する。すると、押さえ部21により対極基板40の一部が押さえられて対極基板40の端部が撓み、第1の対極リード32と第2の対極リード33とが接触する。
【0043】
このとき、対極基板40の長手方向の長さは作用極基板39よりも短くなっているため、作用極基板39上に設けられた作用極リード31および第1の対極リード32の端部がセンサ外部に露出する。作用極リード31および第1の対極リード32の露出した部分がセンサ側の接続端子となり、それぞれ測定装置1側の作用極端子11および対極端子12と接続する(図2、4および5参照)。この状態で作用極端子11−対極端子12間に電圧を印加すると、作用極34−対極35間に電圧を印加することが可能となる。
【0044】
つぎに、試料液としてβ−D−グルコース水溶液を用い、試料液中のβ−D−グルコース濃度の定量を行った。まず、β−D−グルコース濃度の異なる数種の試料液をそれぞれ調整し、試料液をバイオセンサ3の試料供給口37に接触させた。空気孔38は試料供給部36に連通しているので、試料供給口37に導入された試料液は、毛管現象によって内部に浸透し、試料供給部36に供給された。つぎに、測定装置1の測定部13により、対極35を基準にして300mVの電圧を作用極34に印加し、この時に作用極34に流れる電流値を、測定部13を用いて測定した。測定部13で得た値を、あらかじめ記憶している検量線を参照することにより演算部14において濃度に変換し、得られた結果をデータ表示部15に表示した。
【0045】
実施の形態2
本発明の実施の形態2について、図7〜13を用いて説明する。実施の形態1との違いは、バイオセンサの第1の対極リードが3つに分割されており、それに対応して3つの第2の対極リードを備えた点、および測定装置において3つの対極端子を備えた点である。図7は本実施の形態で用いたバイオセンサ、アダプタおよび測定装置の構成を示す概略図である。
【0046】
図8は、バイオセンサの試薬層および界面活性剤層を除いた分解斜視図であり、図9は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに分離された状態を示す縦断面図である。また、図10は、測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに接続された状態を示す縦断面図であり、図11〜13は、押さえ部の位置が異なる3種類のアダプタのセンサ差し込み口方向から見た正面図である。
【0047】
図7において、測定装置1は、作用極端子11、対極端子a121、対極端子b122、対極端子c123、測定部13、演算部14、およびデータ表示部15を備えている。
実施の形態1と同様に、バイオセンサ3はアダプタ2を介して測定装置1に着脱可能に接続される。バイオセンサ3は、作用極基板39、対極基板40、作用極リード31、第1の対極リードa321、第1の対極リードb322、第1の対極リードc323、第2の対極リードa331、第2の対極リードb332、第2の対極リードc333、作用極34、対極35、試薬層(図示せず)、試料供給部36を構成するためのスリットを有するスペーサ部材41、試料供給部36に連通した開口部である空気孔38、および試料供給口37を備えている。
【0048】
作用極基板39上に3つ第1の対極リード321、322、323が設けられ、それに対向する対極基板40上の位置に3つの第2の対極リード331、332、333が形成されるように、対極基板40に3本のスリットが設けられている点以外は、実施の形態1と同様にして、バイオセンサ3を作製した。
本実施の形態のアダプタ201、202、203は、実施の形態1と同様にセンサ差し込み口22、接続口23および押さえ部21を有しているが、実施の形態1よりも押さえ部21の幅が狭い。
【0049】
ここで、バイオセンサ3の製造工程において、特性検査の結果から性能に応じて、例えば3段階のロット番号A、B、Cを付与しておく。測定に用いようとするバイオセンサ3のロット番号がAの場合は、図11に示したアダプタ201を用いる。アダプタ201は、センサ差し込み口22方向から見て最も左側寄りに押さえ部21が設けられており、アダプタ201を測定装置1に装着し、バイオセンサ3をアダプタ201に挿入すると、押さえ部21により対極基板40の一部が押さえられて対極基板40の端部がたわみ、第1の対極リードa321と第2の対極リードa331とが接触する。
【0050】
また、測定に用いようとするバイオセンサ3のロット番号がBの場合は、図12に示したアダプタ202を用いる。アダプタ202は、センサ差し込み口22方向から見て中央部に押さえ部21が設けられており、アダプタ202を測定装置1に装着し、バイオセンサ3をアダプタ202に挿入すると、第1の対極リードb322と第2の対極リードb332とが接触する。
【0051】
同様に、測定に用いようとするバイオセンサ3のロット番号がCの場合は、図13に示したアダプタ203を用いる。アダプタ203は、センサ差し込み口22方向から見て最も右側寄りに押さえ部21が設けられており、アダプタ203を測定装置1に装着し、バイオセンサ3をアダプタ203に挿入すると、押さえ部21により対極基板40の一部が押さえられて対極基板40の端部がたわみ、第1の対極リードc323と第2の対極リードc333とが接触する。
【0052】
つぎに、実施の形態1と同様にして、試料液としてβ−D−グルコース水溶液を用い、試料液中のβ−D−グルコース濃度の定量を行った。試料液をバイオセンサ3の試料供給口37に接触させることにより、試料供給部36に試料液を導入した。一定時間後、作用極34と対極35に試料液が接触した状態で、測定装置1において作用極端子11−対極端子a121間、作用極端子11−対極端子b122間、および作用極端子11−対極端子c123間の抵抗値等を測定することにより、3つの第2の対極リード331、332、333のうち、第1の対極リードと接続しているものを測定装置1側で検出した。このようにすることにより、測定装置1においてセンサのロット番号がA、B、Cのいずれであるかを判定することができた。
【0053】
つぎに、測定装置1の測定部13により、対極35を基準にして300mVの電圧を作用極34に印加し、この時に作用極34に流れる電流値を、測定部13を用いて測定した。判定されたロット番号に応じて、あらかじめ測定装置1内に記憶されているロット番号に対応した検量線が自動的に選択され、測定部13で得られた電流値が、選択された検量線を参照することにより演算部14において濃度に変換された後、得られた結果がデータ表示部15に表示された。したがって、本実施の形態では、用いるアダプタを選択するだけで、バイオセンサの製造ロットに応じた補正が行われるため、容易に正確な基質の定量を行うことができる。
【0054】
実施の形態3
本発明の実施の形態3について、図14〜16を用いて説明する。図14〜16は、本実施の形態で用いたバイオセンサおよび測定装置の構成を示す概略図であり、図14は押さえ部が閉じた状態の測定装置の斜視図、図15は押さえ部が開いた状態の測定装置の斜視図、図16はバイオセンサと測定装置が互いに接続された状態を示す斜視図である。
【0055】
なお、本実施の形態では、実施の形態1と同様のバイオセンサを使用した。
測定時の手順を以下に示す。まず測定装置71の押さえ部72を開け、バイオセンサ3の一部をリード方向からセンサ差し込み口73に差し込む。その時、バイオセンサ3の作用極リード31および第1の対極リード32が、測定装置71側の作用極端子(図示せず)および対極端子(図示せず)と接続する。ここで、作用極端子と対極端子は、測定装置71の内部であってセンサ差し込み口73の近傍に位置している。
【0056】
つぎに、開いていた押さえ部72を閉じると、押さえ部72によりバイオセンサ3の対極基板40の一部が押さえられて対極基板40の端部が撓み、第1の対極リード32と第2の対極リード33とが接触する。この状態で作用極端子−対極端子間に電圧を印加すると、作用極34−対極35間に電圧を印加することが可能となる。
【0057】
つぎに、試料液としてβ−D−グルコース水溶液を用い、実施の形態1と同様の方法を用いて試料液中のβ−D−グルコース濃度の定量を行った。
このようにすると、アダプタを用いることなく、本発明のバイオセンサを直接測定装置に接続して、試料液中に含まれる基質の測定を行うことができる。
【0058】
なお、実施の形態3において、作用極端子または対極端子の一部を押さえ部として使用可能な構成としてもよい。このようにすると、測定装置を構成する部材を減らすことができる。
また、本実施の形態3においては、複数存在する第1の対極リードと第2の対極リードの接触は一箇所だけである場合について記載したが、これに限定されるものではない。例えば、接触する対極リードが複数箇所あってもよい。実施の形態2を用いて説明すると、第1の対極リード321、322と第2の対極リード331、332がそれぞれ接触するようなアダプタ(図示せず)を用いた場合、センサの新たなロット番号Dを更に識別することが可能となる。
【0059】
また、実施の形態2において、第1の対極リードが3つに分割されている場合を示したが、本発明はこれに限定されず、2つ以上に分割されていれば同様の効果を得ることができる。ここで、分割されている数が多い程、バイオセンサの製造ロットの違いによる測定値の補正を細かく行うことができるので好ましい。
【0060】
また、実施の形態1および2においては、挿入されたバイオセンサの対極基板の少なくとも一部を押さえて、第1の対極リードと第2の対極リードとを接触させる押さえ部が設けられたアダプタを用いたが、これに代えて、上記押さえ部が測定装置のセンサ差し込み口内に設けられてもよい。このようにすると、アダプタを用いることなく、本発明のバイオセンサを直接測定装置に接続して、試料液中に含まれる基質の測定を行うことができる。その際、実施の形態3のように押さえ部を含んだ部材が可動してもよい。このようにすると、より確実に端子を押さえることができる。また、端子の一部を押さえ部として使用可能な構成としてもよい。このようにすると、測定装置を構成する部材を減らすことができる。
【0061】
また、実施の形態2においては、バイオセンサの製造ロットを判別する例を示したが、これに限らない。例えば、バイオセンサの測定対象を判別してもよい。その場合、例えば、測定対象物である基質がグルコース、乳酸、あるいはコレステロールである3種類のバイオセンサを一つの測定装置で測定することが可能となる。この場合、測定装置1内に記憶されている検量線はロット番号ではなく基質に対応した検量線となっている。またこの場合も製造ロット判別の時と同様に、第1の対極リードの分割数は3に限定されるものではない。
【0062】
また、以上の実施の形態において、作用極34への印加電圧を対極35を基準に300mVとしたが、これに限定されず、電子伝達体が作用極34上で電極反応可能な電圧であればよい。
また、空気孔38の位置は、図に示した位置に限定されず、試料供給部36と通じており、試料供給部36に対して試料供給口37と反対側に位置していればよい。
【0063】
さらに、以上の実施の形態では、酸化還元酵素を含む溶液を塗布および乾燥することにより試薬層を形成したが、これに限定されず、例えばインクジェット方式により、試薬を含んだ溶液を塗布してもよい。このようにすると、塗布する溶液量が微量であっても試薬層の正確な位置制御が可能となる。また、試薬を含んだ溶液をガラスろ紙に担持し、乾燥したガラスろ紙を試料供給部36内に位置させてもよい。
【0064】
さらにまた、導電材料と試薬を混合することにより電極を形成してもよい。試薬の担持位置としては、作用極34または対極35上にあることが好ましいが、それに限らず、試料と接することが可能な位置であれば、試料供給部36内の作用極34および対極35上以外の場所でもよい。
スペーサ部材41としては、電気絶縁性を有し、保存および測定時に充分な剛性を有する材料であれば用いることができる。例えば、ポリエチレン、ポリスチレン、ポリ塩化ビニル、ポリアミド、飽和ポリエステル樹脂などの熱可塑性樹脂、または尿素樹脂、メラミン樹脂、フェノール樹脂、エポキシ樹脂、不飽和ポリエステル樹脂などの熱硬化性樹脂があげられる。
【0065】
作用極としては、電子伝達体を酸化する際にそれ自身が酸化されない導電性材料であれば用いることができる。対極としては、パラジウム、銀、白金、カーボン等の一般的に用いられる導電性材料であれば用いることができる。また、電気絶縁性の材料の表面をこれらの導電性材料で被覆しても良い。
また、以上の実施の形態では、電極系の形成方法としてフォトリソグラフィを使用したがそれに限定されない。例えば、パラジウムなどの貴金属を基板上にスパッタリングした後、レーザートリミングにより電極パターンを形成する方法や、基板上に導電ペースト等をスクリーン印刷することにより電極パターンを形成する等の製造方法を用いてもよい。
【0066】
さらに、以上の実施の形態では、第2の基板は第1の基板よりも長手方向に短くなっている構成であったが、これに限定されず、第2のリードと第3のリードとを電気的に接触させるために第2の基板の少なくとも一部を押さえたとき、第1のリードおよび第2のリードの少なくとも端部が外部に露出するように、第1の基板および第2の基板の寸法、配置などが調整されていればよい。
【0067】
酸化還元酵素としては、試料中に含まれる測定対象物である基質に対応したものが用いられ、例えば、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼ、アミノ酸オキシダーゼ等が挙げられる。
【0068】
電子伝達体としては、フェリシアン化カリウム、p−ベンゾキノン、フェナジンメトサルフェート、メチレンブルー、フェロセン誘導体等があげられる。また、酸素を電子伝達体とした場合にも電流応答が得られる。電子伝達体は、これらの一種または二種以上が使用される。
【0069】
また、以上の実施の形態では試料としてβ−D−グルコース水溶液を使用したが、これに限定されない。例えば、全血、血漿、血清、間質液、唾液、尿などの生体試料に対しても使用可能である。ここで、全血としては、例えば、指先や腕の皮膚を穿刺し採取した毛細血、あるいは静脈血、動脈血などを用いることができる。
【0070】
【発明の効果】
以上のように、本発明によれば、簡易な構成により、測定装置と容易に接続することができる対向型バイオセンサ、それに用いるアダプタおよび測定装置を提供することができる。
【図面の簡単な説明】
【図1】本発明の一実施の形態によるバイオセンサ、アダプタおよび測定装置の構成を示す概略図
【図2】同実施の形態におけるバイオセンサの試薬層および界面活性剤層を除いた分解斜視図
【図3】同実施の形態におけるアダプタおよび測定装置のセンサ差し込み口近傍の構成を示す概略図
【図4】同実施の形態におけるアダプタおよび測定装置のセンサ差し込み口近傍の構成を示す別の概略図
【図5】図3および4における測定装置1のセンサ差し込み口の一部透明概略斜視図
【図6】アダプタのセンサ差し込み口方向から見た正面図
【図7】本発明の他の実施の形態で用いたバイオセンサ、アダプタおよび測定装置の構成を示す概略図
【図8】バイオセンサの試薬層および界面活性剤層を除いた分解斜視図
【図9】測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに分離された状態を示す縦断面図
【図10】測定装置のセンサ差し込み口近傍、アダプタおよびバイオセンサが互いに接続された状態を示す縦断面図
【図11】アダプタのセンサ差し込み口方向から見た正面図
【図12】押さえ部の位置が異なるアダプタのセンサ差し込み口方向から見た正面図
【図13】押さえ部の位置が異なる別のアダプタのセンサ差し込み口方向から見た正面図
【図14】本発明のさらに別の実施の形態における測定装置の構成を示す概略図
【図15】同実施の形態における測定装置の構成を示す別の概略図
【図16】同実施の形態における測定装置とバイオセンサの構成を示す概略図
【符号の説明】
1、71 測定装置
11 作用極端子
12 対極端子
121 対極端子a
122 対極端子b
123 対極端子c
13 測定部
14 演算部
15 データ表示部
2、201、202、203 アダプタ
21、72 押さえ部
22、73 センサ差し込み口
23 接続口
3 バイオセンサ
31 作用極リード
32 第1の対極リード
321 第1の対極リードa
322 第1の対極リードb
323 第1の対極リードc
33 第2の対極リード
331 第2の対極リードa
332 第2の対極リードb
333 第2の対極リードc
34 作用極
35 対極
36 試料供給部
37 試料供給口
38 空気孔
39 作用極基板
40 対極基板
41 スペーサ部材
Claims (50)
- 第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、
前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、
前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記第1の電極または前記第2の電極の一方が作用極として機能し、他方が対極として機能し、前記第1の基板および/または前記第2の基板をいずれかの基板に向けて押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触することを特徴とするバイオセンサ。 - 前記第3のリードが複数に分割されており、前記第2のリードを複数個有することを特徴とする請求項1記載のバイオセンサ。
- 前記第1の基板と前記第2の基板との間にスペーサ部材を有することを特徴とする請求項1記載のバイオセンサ。
- 前記スペーサ部材が、前記第1の基板および前記第2の基板の少なくとも一方と一体化されていることを特徴とする請求項3記載のバイオセンサ。
- 前記スペーサ部材が、前記第1の基板と一体化されていることを特徴とする請求項4記載のバイオセンサ。
- 前記スペーサ部材が、前記第2の基板と一体化されていることを特徴とする請求項4記載のバイオセンサ。
- 前記第2の基板が、長手方向において、前記第1の基板よりも短いことを特徴とする請求項1記載のバイオセンサ。
- 前記試料供給部内に、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼおよびアミノ酸オキシダーゼよりなる群から選択される酵素を含む試薬を具備することを特徴とする請求項1記載のバイオセンサ。
- バイオセンサを挿入するセンサ差し込み口と、押さえ部と、測定装置と接続するための接続口とを具備することを特徴とするアダプタ。
- 前記アダプタが前記センサ差し込み口に挿入された前記バイオセンサを受け、
前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、他方の基板に向けて移動させることを特徴とする請求項9記載のアダプタ。 - 前記第3のリードが複数に分割されており、前記第2のリードを複数個有することを特徴とする請求項10記載のアダプタ。
- 前記第1の基板と前記第2の基板との間にスペーサ部材を有することを特徴とする請求項10記載のアダプタ。
- 前記スペーサ部材が、前記第1の基板および前記第2の基板の少なくとも一方と一体化されていることを特徴とする請求項12記載のアダプタ。
- 前記スペーサ部材が、前記第1の基板と一体化されていることを特徴とする請求項13記載のアダプタ。
- 前記スペーサ部材が、前記第2の基板と一体化されていることを特徴とする請求項13記載のアダプタ。
- 前記第2の基板が、長手方向において、前記第1の基板よりも短いことを特徴とする請求項10記載のアダプタ。
- 前記押さえ部が弾性体で構成されていることを特徴とする請求項9記載のアダプタ。
- バイオセンサと、押さえ部を含むアダプタと、測定手段とを具備することを特徴とする測定装置。
- 前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、他方の基板に向けて移動させることを特徴とする請求項18記載の測定装置。 - 前記第3のリードが複数に分割されており、前記バイオセンサが前記第2のリードを複数個有することを特徴とする請求項19記載の測定装置。
- 前記バイオセンサの前記第1の基板と前記第2の基板との間にスペーサ部材を有することを特徴とする請求項19記載の測定装置。
- 前記バイオセンサの前記スペーサ部材が、前記第1の基板および前記第2の基板の少なくとも一方と一体化されていることを特徴とする請求項21記載の測定装置。
- 前記バイオセンサの前記スペーサ部材が、前記第1の基板と一体化されていることを特徴とする請求項22記載の測定装置。
- 前記バイオセンサの前記スペーサ部材が、前記第2の基板と一体化されていることを特徴とする請求項22記載の測定装置。
- 前記第2の基板が、長手方向において、前記第1の基板よりも短いことを特徴とする請求項19記載の測定装置。
- 前記押さえ部が弾性体で構成されていることを特徴とする請求項18記載の測定装置。
- 前記試料供給部内に、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼおよびアミノ酸オキシダーゼよりなる群から選択される酵素を含む試薬を具備することを特徴とする請求項19記載の測定装置。
- 試料液中の基質を測定することを特徴とする請求項19記載の測定装置。
- 前記バイオセンサの前記第1の電極に電気的に接続される第1の端子と、前記バイオセンサの前記第2の電極にそれぞれ電気的に接続される少なくとも1つの第2の端子とを具備することを特徴とする請求項19または20記載の測定装置。
- 前記測定手段が、前記第1の端子および前記少なくとも1つの第2の端子を介して、前記バイオセンサの前記第1の電極および前記第2の電極の間に電圧を印加する手段と、前記第1の電極および前記第2の電極の間の電気的変化を測定する手段を具備することを特徴とする請求項19記載の測定装置。
- 前記測定装置が、前記第2の端子を複数個有することを特徴とする請求項29記載の測定装置。
- 前記測定装置が、前記第1の端子および前記複数個の第2の端子の間の電気的変化を測定する手段を具備することを特徴とする請求項31記載の測定装置。
- 前記複数個の第2の端子のうち前記第1の端子に電気的に接続された第2の端子を検知する手段と、検知された第2の端子の数および位置に基づいてバイオセンサの種類を決定する手段と、前記種類に応じて測定結果を補正する手段とを具備することを特徴とする請求項31記載の測定装置。
- 押さえ部と、
第1の電極に電気的に接続された第1のリード、第2のリード、第2の電極に電気的に接続された第3のリードを具備するバイオセンサを受けるセンサ差し込み口と、
前記バイオセンサの前記第1のリードを前記測定装置に電気的に接続する第1の端子と、
前記バイオセンサの前記第2のリードを前記測定装置に電気的に接続する第2の端子と、
前記第1の電極および前記第2の電極の間に電圧を印加する手段と、
前記第1の電極および前記第2の電極の間の電気的変化を測定する手段とを具備することを特徴とする測定装置。 - 前記第2の端子を複数個具備することを特徴とする請求項34記載の測定装置。
- 前記第1の端子および前記複数個の第2の端子の間の電気的変化を測定する手段とを具備することを特徴とする請求項35記載の測定装置。
- 前記押さえ部が弾性体で構成されていることを特徴とする請求項34記載の測定装置。
- 前記第2の端子が前記押さえ部として機能することを特徴とする請求項34記載の測定装置。
- 前記バイオセンサが、第1の基板、第2の基板ならびに前記第1の基板および前記第2の基板によって形成された試料供給部と、前記第1の基板上であって前記第2の基板に対向する面側に設けられた第1の電極、第1のリードおよび第2のリードと、前記第2の基板上であって前記第1の基板に対向する面側に設けられた第2の電極および第3のリードとを具備し、
前記押さえ部によって押さえることにより、前記第2のリードおよび前記第3のリードが電気的に接触し、前記押さえ部が前記第1の基板および/または前記第2の基板の少なくとも一部を、他方の基板に向けて移動させることを特徴とする請求項34記載の測定装置。 - 前記バイオセンサの前記第3のリードが複数に分割されており、前記バイオセンサが前記第2のリードを複数個有することを特徴とする請求項39記載の測定装置。
- 前記バイオセンサの前記第1の基板と前記第2の基板との間にスペーサ部材を有することを特徴とする請求項39記載の測定装置。
- 前記バイオセンサの前記スペーサ部材が、前記第1の基板および前記第2の基板の少なくとも一方と一体化されていることを特徴とする請求項41記載の測定装置。
- 前記バイオセンサの前記スペーサ部材が、前記第1の基板と一体化されていることを特徴とする請求項42記載の測定装置。
- 前記バイオセンサの前記スペーサ部材が、前記第2の基板と一体化されていることを特徴とする請求項42記載の測定装置。
- 前記第2の基板が、長手方向において、前記第1の基板よりも短いことを特徴とする請求項39記載の測定装置。
- 前記試料供給部が、フルクトースデヒドロゲナーゼ、グルコースオキシダーゼ、グルコースデヒドロゲナーゼ、アルコールオキシダーゼ、乳酸オキシダーゼ、コレステロールオキシダーゼ、キサンチンオキシダーゼおよびアミノ酸オキシダーゼよりなる群から選択される酵素を含む試薬を具備することを特徴とする請求項39載の測定装置。
- 試料液中の基質を測定することを特徴とする請求項39記載の測定装置。
- 前記バイオセンサの前記第1の基板および/または前記第2の基板の少なくとも一部を押さえて前記第2の電極および前記第3の電極を電気的に接続し、前記バイオセンサの前記試料供給部に供給された試料液中の基質を測定することを特徴とする請求項47記載の測定装置。
- 前記複数個の第2の端子のうち前記第1の端子に電気的に接続された第2の端子を検知する手段と、検知された第2の端子の数および位置に基づいてバイオセンサの種類を決定する手段と、前記種類に応じて測定結果を補正する手段とを具備することを特徴とする請求項35記載の測定装置。
- 前記押さえ部が可動し、前記バイオセンサの前記第1の基板および/または前記第2の基板において押さえられる部分が、前記押さえ部によって決定されることを特徴とする請求項39記載の測定装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003119871A JP2004004057A (ja) | 2002-04-26 | 2003-04-24 | バイオセンサ、それに用いるアダプタ、および測定装置 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002126810 | 2002-04-26 | ||
| JP2003119871A JP2004004057A (ja) | 2002-04-26 | 2003-04-24 | バイオセンサ、それに用いるアダプタ、および測定装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004004057A true JP2004004057A (ja) | 2004-01-08 |
| JP2004004057A5 JP2004004057A5 (ja) | 2006-04-06 |
Family
ID=30447534
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003119871A Withdrawn JP2004004057A (ja) | 2002-04-26 | 2003-04-24 | バイオセンサ、それに用いるアダプタ、および測定装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2004004057A (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100656104B1 (ko) | 2005-09-02 | 2006-12-11 | 주식회사 인포피아 | 바이오센서 |
| WO2008016137A1 (fr) * | 2006-08-03 | 2008-02-07 | Panasonic Corporation | Dispositif de mesure et procédé d'éjection de capteur |
| WO2008126682A1 (ja) * | 2007-03-28 | 2008-10-23 | Arkray, Inc. | 分析装置 |
| JP2012511146A (ja) * | 2008-12-05 | 2012-05-17 | アカノスティクス・リミテッド | 装置 |
-
2003
- 2003-04-24 JP JP2003119871A patent/JP2004004057A/ja not_active Withdrawn
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100656104B1 (ko) | 2005-09-02 | 2006-12-11 | 주식회사 인포피아 | 바이오센서 |
| WO2008016137A1 (fr) * | 2006-08-03 | 2008-02-07 | Panasonic Corporation | Dispositif de mesure et procédé d'éjection de capteur |
| JPWO2008016137A1 (ja) * | 2006-08-03 | 2009-12-24 | パナソニック株式会社 | 測定装置、およびセンサ排出方法 |
| KR101065111B1 (ko) * | 2006-08-03 | 2011-09-16 | 파나소닉 주식회사 | 측정 장치 및 센서 배출 방법 |
| US8562814B2 (en) | 2006-08-03 | 2013-10-22 | Panasonic Corporation | Measurement device and sensor ejection method |
| JP5439814B2 (ja) * | 2006-08-03 | 2014-03-12 | パナソニック株式会社 | 測定装置、およびセンサ排出方法 |
| WO2008126682A1 (ja) * | 2007-03-28 | 2008-10-23 | Arkray, Inc. | 分析装置 |
| JPWO2008126682A1 (ja) * | 2007-03-28 | 2010-07-22 | アークレイ株式会社 | 分析装置 |
| US8293194B2 (en) | 2007-03-28 | 2012-10-23 | Arkray, Inc. | Analyzer |
| JP5212990B2 (ja) * | 2007-03-28 | 2013-06-19 | アークレイ株式会社 | 分析装置 |
| KR101470370B1 (ko) * | 2007-03-28 | 2014-12-08 | 아크레이 가부시키가이샤 | 분석장치 |
| JP2012511146A (ja) * | 2008-12-05 | 2012-05-17 | アカノスティクス・リミテッド | 装置 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3677500B2 (ja) | 分析素子、それを用いた測定器および基質定量法 | |
| JP4177662B2 (ja) | バイオセンサ | |
| KR100340174B1 (ko) | 전기화학적 바이오센서 테스트 스트립, 그 제조방법 및 전기화학적 바이오센서 | |
| JP3690683B2 (ja) | バイオセンサ | |
| US6416641B1 (en) | Biosensor | |
| JP3842989B2 (ja) | クロマトグラフィー機能の多孔性薄膜を備えたバイオセンサー | |
| JP3267936B2 (ja) | バイオセンサ | |
| JP3389106B2 (ja) | 電気化学分析素子 | |
| JP2001183330A (ja) | バイオセンサ | |
| JP2005517181A (ja) | 液体サンプルの分析のための電気化学式バイオセンサストリップ | |
| JPH10185860A (ja) | バイオセンサ | |
| JP2003528312A (ja) | 認識電極を有する電気化学的バイオセンサーテストストリップ及びこれを利用する測定器 | |
| JP4061816B2 (ja) | バイオセンサ | |
| JP2001330581A (ja) | 基質濃度定量法 | |
| EP1357194A2 (en) | Adapter for the connection of a biosensor to a measuring device | |
| JP3267933B2 (ja) | 基質の定量法 | |
| JP2001249103A (ja) | バイオセンサ | |
| JP2004004057A (ja) | バイオセンサ、それに用いるアダプタ、および測定装置 | |
| KR100739865B1 (ko) | 바이오센서 | |
| JP4036883B2 (ja) | バイオセンサ | |
| JPH08338824A (ja) | バイオセンサ、バイオセンサの製造方法および特定化合物の定量法 | |
| JP2007232628A (ja) | バイオセンサー |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060217 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060217 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20061204 |