ES2954785T3 - Compuestos organolépticos novedosos - Google Patents
Compuestos organolépticos novedosos Download PDFInfo
- Publication number
- ES2954785T3 ES2954785T3 ES19850359T ES19850359T ES2954785T3 ES 2954785 T3 ES2954785 T3 ES 2954785T3 ES 19850359 T ES19850359 T ES 19850359T ES 19850359 T ES19850359 T ES 19850359T ES 2954785 T3 ES2954785 T3 ES 2954785T3
- Authority
- ES
- Spain
- Prior art keywords
- oxy
- dodecan
- trimethyltricyclo
- fragrance
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims description 48
- 239000003205 fragrance Substances 0.000 claims abstract description 76
- -1 (4,4,8-trimethyltricyclo[6.3.1.02,5]dodecan-1-yl)oxy Chemical group 0.000 claims abstract description 22
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 101
- 239000000203 mixture Substances 0.000 claims description 68
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 claims description 46
- AMQJEAYHLZJPGS-UHFFFAOYSA-N N-Pentanol Chemical compound CCCCCO AMQJEAYHLZJPGS-UHFFFAOYSA-N 0.000 claims description 36
- 238000009472 formulation Methods 0.000 claims description 32
- JYVLIDXNZAXMDK-UHFFFAOYSA-N pentan-2-ol Chemical compound CCCC(C)O JYVLIDXNZAXMDK-UHFFFAOYSA-N 0.000 claims description 22
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 claims description 15
- 238000002360 preparation method Methods 0.000 claims description 15
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 claims description 14
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 claims description 13
- ZSIAUFGUXNUGDI-UHFFFAOYSA-N hexan-1-ol Chemical compound CCCCCCO ZSIAUFGUXNUGDI-UHFFFAOYSA-N 0.000 claims description 12
- 125000004432 carbon atom Chemical group C* 0.000 claims description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 9
- 229910052739 hydrogen Inorganic materials 0.000 claims description 9
- 239000001257 hydrogen Substances 0.000 claims description 9
- 239000007788 liquid Substances 0.000 claims description 9
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 8
- 238000000034 method Methods 0.000 claims description 8
- 239000002781 deodorant agent Substances 0.000 claims description 7
- 239000002304 perfume Substances 0.000 claims description 7
- 239000000344 soap Substances 0.000 claims description 7
- 239000002537 cosmetic Substances 0.000 claims description 6
- 239000000499 gel Substances 0.000 claims description 6
- 125000000217 alkyl group Chemical group 0.000 claims description 5
- 239000003795 chemical substances by application Substances 0.000 claims description 5
- 229920000642 polymer Polymers 0.000 claims description 5
- 125000004400 (C1-C12) alkyl group Chemical group 0.000 claims description 4
- 239000000377 silicon dioxide Substances 0.000 claims description 4
- 229920002472 Starch Polymers 0.000 claims description 3
- 230000001166 anti-perspirative effect Effects 0.000 claims description 3
- 239000003213 antiperspirant Substances 0.000 claims description 3
- 238000004140 cleaning Methods 0.000 claims description 3
- 239000000645 desinfectant Substances 0.000 claims description 3
- 230000002708 enhancing effect Effects 0.000 claims description 3
- 235000013305 food Nutrition 0.000 claims description 3
- 235000019698 starch Nutrition 0.000 claims description 3
- 238000005406 washing Methods 0.000 claims description 3
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 claims description 2
- 229920001661 Chitosan Polymers 0.000 claims description 2
- 108010010803 Gelatin Proteins 0.000 claims description 2
- 229920000084 Gum arabic Polymers 0.000 claims description 2
- 239000004952 Polyamide Substances 0.000 claims description 2
- 239000004721 Polyphenylene oxide Substances 0.000 claims description 2
- 229920002396 Polyurea Polymers 0.000 claims description 2
- 235000010489 acacia gum Nutrition 0.000 claims description 2
- 239000000205 acacia gum Substances 0.000 claims description 2
- 229940072056 alginate Drugs 0.000 claims description 2
- 229920000615 alginic acid Polymers 0.000 claims description 2
- 235000010443 alginic acid Nutrition 0.000 claims description 2
- 239000006260 foam Substances 0.000 claims description 2
- 229920000159 gelatin Polymers 0.000 claims description 2
- 239000008273 gelatin Substances 0.000 claims description 2
- 235000019322 gelatine Nutrition 0.000 claims description 2
- 235000011852 gelatine desserts Nutrition 0.000 claims description 2
- 230000036541 health Effects 0.000 claims description 2
- 235000016709 nutrition Nutrition 0.000 claims description 2
- 229920000747 poly(lactic acid) Polymers 0.000 claims description 2
- 229920002401 polyacrylamide Polymers 0.000 claims description 2
- 229920000058 polyacrylate Polymers 0.000 claims description 2
- 229920002647 polyamide Polymers 0.000 claims description 2
- 229920000728 polyester Polymers 0.000 claims description 2
- 229920000570 polyether Polymers 0.000 claims description 2
- 229920002635 polyurethane Polymers 0.000 claims description 2
- 239000004814 polyurethane Substances 0.000 claims description 2
- 239000008107 starch Substances 0.000 claims description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 2
- QNVRIHYSUZMSGM-UHFFFAOYSA-N hexan-2-ol Chemical compound CCCCC(C)O QNVRIHYSUZMSGM-UHFFFAOYSA-N 0.000 claims 2
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims 1
- 241000978776 Senegalia senegal Species 0.000 claims 1
- 239000000463 material Substances 0.000 abstract description 13
- 150000001298 alcohols Chemical class 0.000 abstract description 6
- 239000000047 product Substances 0.000 description 57
- 238000005160 1H NMR spectroscopy Methods 0.000 description 29
- 238000005481 NMR spectroscopy Methods 0.000 description 17
- 235000019645 odor Nutrition 0.000 description 17
- 230000003595 spectral effect Effects 0.000 description 17
- SGIIQKAMTIJXBU-UHFFFAOYSA-N pentan-2-ol Chemical compound CC[CH]C(C)O SGIIQKAMTIJXBU-UHFFFAOYSA-N 0.000 description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 12
- 239000004615 ingredient Substances 0.000 description 9
- 230000000052 comparative effect Effects 0.000 description 8
- 239000002023 wood Substances 0.000 description 8
- YXXPNGIZHZHBTQ-UHFFFAOYSA-N butan-2-ol Chemical compound CC[C](C)O YXXPNGIZHZHBTQ-UHFFFAOYSA-N 0.000 description 7
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 239000007921 spray Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 241000218645 Cedrus Species 0.000 description 5
- 239000002386 air freshener Substances 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 239000003599 detergent Substances 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- VPKMGDRERYMTJX-CMDGGOBGSA-N 1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)-1-penten-3-one Chemical compound CCC(=O)\C=C\C1C(C)=CCCC1(C)C VPKMGDRERYMTJX-CMDGGOBGSA-N 0.000 description 4
- 239000004215 Carbon black (E152) Substances 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- QMVPMAAFGQKVCJ-UHFFFAOYSA-N citronellol Chemical compound OCCC(C)CCC=C(C)C QMVPMAAFGQKVCJ-UHFFFAOYSA-N 0.000 description 4
- 230000000295 complement effect Effects 0.000 description 4
- 239000012043 crude product Substances 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 229930195733 hydrocarbon Natural products 0.000 description 4
- 230000005923 long-lasting effect Effects 0.000 description 4
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 4
- 230000003472 neutralizing effect Effects 0.000 description 4
- NPNUFJAVOOONJE-ZIAGYGMSSA-N β-(E)-Caryophyllene Chemical compound C1CC(C)=CCCC(=C)[C@H]2CC(C)(C)[C@@H]21 NPNUFJAVOOONJE-ZIAGYGMSSA-N 0.000 description 4
- KHQDWCKZXLWDNM-KPKJPENVSA-N (e)-2-ethyl-4-(2,2,3-trimethylcyclopent-3-en-1-yl)but-2-en-1-ol Chemical compound CC\C(CO)=C/CC1CC=C(C)C1(C)C KHQDWCKZXLWDNM-KPKJPENVSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 239000000443 aerosol Substances 0.000 description 3
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 3
- 235000019568 aromas Nutrition 0.000 description 3
- 125000000753 cycloalkyl group Chemical group 0.000 description 3
- SNRUBQQJIBEYMU-UHFFFAOYSA-N dodecane Chemical compound CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 3
- 238000001030 gas--liquid chromatography Methods 0.000 description 3
- HGCQWDFNEHWQDP-UHFFFAOYSA-N hexan-2-ol Chemical compound [CH2]C(O)CCCC HGCQWDFNEHWQDP-UHFFFAOYSA-N 0.000 description 3
- 230000002045 lasting effect Effects 0.000 description 3
- 239000006210 lotion Substances 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 239000001993 wax Substances 0.000 description 3
- WCVRQHFDJLLWFE-RXMQYKEDSA-N (2r)-pentane-1,2-diol Chemical compound CCC[C@@H](O)CO WCVRQHFDJLLWFE-RXMQYKEDSA-N 0.000 description 2
- WCVRQHFDJLLWFE-YFKPBYRVSA-N (2s)-pentane-1,2-diol Chemical compound CCC[C@H](O)CO WCVRQHFDJLLWFE-YFKPBYRVSA-N 0.000 description 2
- YBUIAJZFOGJGLJ-SWRJLBSHSA-N 1-cedr-8-en-9-ylethanone Chemical compound C1[C@]23[C@H](C)CC[C@H]3C(C)(C)[C@@H]1C(C)=C(C(C)=O)C2 YBUIAJZFOGJGLJ-SWRJLBSHSA-N 0.000 description 2
- VSIXJPFQJMODCS-UHFFFAOYSA-N 3-methyl-4-phenylbutan-2-ol Chemical compound CC(O)C(C)CC1=CC=CC=C1 VSIXJPFQJMODCS-UHFFFAOYSA-N 0.000 description 2
- OXYRENDGHPGWKV-UHFFFAOYSA-N 3-methyl-5-phenylpentan-1-ol Chemical compound OCCC(C)CCC1=CC=CC=C1 OXYRENDGHPGWKV-UHFFFAOYSA-N 0.000 description 2
- NVEQFIOZRFFVFW-UHFFFAOYSA-N 9-epi-beta-caryophyllene oxide Natural products C=C1CCC2OC2(C)CCC2C(C)(C)CC21 NVEQFIOZRFFVFW-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- 241000402754 Erythranthe moschata Species 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- NBBJYMSMWIIQGU-UHFFFAOYSA-N Propionic aldehyde Chemical compound CCC=O NBBJYMSMWIIQGU-UHFFFAOYSA-N 0.000 description 2
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- FAMPSKZZVDUYOS-UHFFFAOYSA-N alpha-Caryophyllene Natural products CC1=CCC(C)(C)C=CCC(C)=CCC1 FAMPSKZZVDUYOS-UHFFFAOYSA-N 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- NPNUFJAVOOONJE-UHFFFAOYSA-N beta-cariophyllene Natural products C1CC(C)=CCCC(=C)C2CC(C)(C)C21 NPNUFJAVOOONJE-UHFFFAOYSA-N 0.000 description 2
- 125000002619 bicyclic group Chemical group 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- NPNUFJAVOOONJE-UONOGXRCSA-N caryophyllene Natural products C1CC(C)=CCCC(=C)[C@@H]2CC(C)(C)[C@@H]21 NPNUFJAVOOONJE-UONOGXRCSA-N 0.000 description 2
- 229940117948 caryophyllene Drugs 0.000 description 2
- MIZGSAALSYARKU-UHFFFAOYSA-N cashmeran Chemical compound CC1(C)C(C)C(C)(C)C2=C1C(=O)CCC2 MIZGSAALSYARKU-UHFFFAOYSA-N 0.000 description 2
- 150000005829 chemical entities Chemical class 0.000 description 2
- 235000000484 citronellol Nutrition 0.000 description 2
- 238000004040 coloring Methods 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 125000000392 cycloalkenyl group Chemical group 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 239000002979 fabric softener Substances 0.000 description 2
- ONKNPOPIGWHAQC-UHFFFAOYSA-N galaxolide Chemical compound C1OCC(C)C2=C1C=C1C(C)(C)C(C)C(C)(C)C1=C2 ONKNPOPIGWHAQC-UHFFFAOYSA-N 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 150000002430 hydrocarbons Chemical class 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- KVWWIYGFBYDJQC-UHFFFAOYSA-N methyl dihydrojasmonate Chemical compound CCCCCC1C(CC(=O)OC)CCC1=O KVWWIYGFBYDJQC-UHFFFAOYSA-N 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- JHJNPOSPVGRIAN-SFHVURJKSA-N n-[3-[(1s)-1-[[6-(3,4-dimethoxyphenyl)pyrazin-2-yl]amino]ethyl]phenyl]-5-methylpyridine-3-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1C1=CN=CC(N[C@@H](C)C=2C=C(NC(=O)C=3C=C(C)C=NC=3)C=CC=2)=N1 JHJNPOSPVGRIAN-SFHVURJKSA-N 0.000 description 2
- 230000009965 odorless effect Effects 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 239000002453 shampoo Substances 0.000 description 2
- 238000010898 silica gel chromatography Methods 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000000606 toothpaste Substances 0.000 description 2
- 239000002699 waste material Substances 0.000 description 2
- DNIAPMSPPWPWGF-VKHMYHEASA-N (+)-propylene glycol Chemical compound C[C@H](O)CO DNIAPMSPPWPWGF-VKHMYHEASA-N 0.000 description 1
- FINOAUDUYKVGDS-UHFFFAOYSA-N (2-tert-butylcyclohexyl) acetate Chemical compound CC(=O)OC1CCCCC1C(C)(C)C FINOAUDUYKVGDS-UHFFFAOYSA-N 0.000 description 1
- ZSKAJFSSXURRGL-PKNBQFBNSA-N (2e)-1,1-dimethoxy-3,7-dimethylocta-2,6-diene Chemical compound COC(OC)\C=C(/C)CCC=C(C)C ZSKAJFSSXURRGL-PKNBQFBNSA-N 0.000 description 1
- KJBPYIUAQLPHJG-SECBINFHSA-N (2r)-1-phenylmethoxypropan-2-ol Chemical compound C[C@@H](O)COCC1=CC=CC=C1 KJBPYIUAQLPHJG-SECBINFHSA-N 0.000 description 1
- KJBPYIUAQLPHJG-VIFPVBQESA-N (2s)-1-phenylmethoxypropan-2-ol Chemical compound C[C@H](O)COCC1=CC=CC=C1 KJBPYIUAQLPHJG-VIFPVBQESA-N 0.000 description 1
- VHBOIZSCWFNPBM-PTNGSMBKSA-N (2z)-2-[(4-methylphenyl)methylidene]heptanal Chemical compound CCCCC\C(C=O)=C\C1=CC=C(C)C=C1 VHBOIZSCWFNPBM-PTNGSMBKSA-N 0.000 description 1
- JIYIHILAGIZIMD-CLFYSBASSA-N (4z)-cyclopentadec-4-en-1-one Chemical compound O=C1CCCCCCCCCC\C=C/CC1 JIYIHILAGIZIMD-CLFYSBASSA-N 0.000 description 1
- IHPKGUQCSIINRJ-CSKARUKUSA-N (E)-beta-ocimene Chemical compound CC(C)=CC\C=C(/C)C=C IHPKGUQCSIINRJ-CSKARUKUSA-N 0.000 description 1
- QMVPMAAFGQKVCJ-SNVBAGLBSA-N (R)-(+)-citronellol Natural products OCC[C@H](C)CCC=C(C)C QMVPMAAFGQKVCJ-SNVBAGLBSA-N 0.000 description 1
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 1
- XEJGJTYRUWUFFD-FNORWQNLSA-N (e)-1-(2,6,6-trimethyl-1-cyclohex-3-enyl)but-2-en-1-one Chemical compound C\C=C\C(=O)C1C(C)C=CCC1(C)C XEJGJTYRUWUFFD-FNORWQNLSA-N 0.000 description 1
- MTVBNJVZZAQKRV-BJMVGYQFSA-N (e)-2-methyl-4-(2,2,3-trimethylcyclopent-3-en-1-yl)but-2-en-1-ol Chemical compound OCC(/C)=C/CC1CC=C(C)C1(C)C MTVBNJVZZAQKRV-BJMVGYQFSA-N 0.000 description 1
- LIWYPQFTKLABSJ-WAYWQWQTSA-N (z)-1-(2-methylprop-2-enoxy)hex-3-ene Chemical compound CC\C=C/CCOCC(C)=C LIWYPQFTKLABSJ-WAYWQWQTSA-N 0.000 description 1
- FVUGZKDGWGKCFE-UHFFFAOYSA-N 1-(2,3,8,8-tetramethyl-1,3,4,5,6,7-hexahydronaphthalen-2-yl)ethanone Chemical compound CC1(C)CCCC2=C1CC(C(C)=O)(C)C(C)C2 FVUGZKDGWGKCFE-UHFFFAOYSA-N 0.000 description 1
- FXCYGAGBPZQRJE-ZHACJKMWSA-N 1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)-1,6-heptadien-3-one Chemical compound CC1=CCCC(C)(C)C1\C=C\C(=O)CCC=C FXCYGAGBPZQRJE-ZHACJKMWSA-N 0.000 description 1
- OEVIJAZJVZDBQL-UHFFFAOYSA-N 1-(5,5-dimethylcyclohexen-1-yl)pent-4-en-1-one Chemical compound CC1(C)CCC=C(C(=O)CCC=C)C1 OEVIJAZJVZDBQL-UHFFFAOYSA-N 0.000 description 1
- SOHNFTXQJSQZHZ-UHFFFAOYSA-N 1-[(4,4,8-trimethyl-1-tricyclo[6.3.1.02,5]dodecanyl)oxy]butan-2-ol Chemical compound CC1(CC2C3(CCCC(CCC12)(C3)C)OCC(CC)O)C SOHNFTXQJSQZHZ-UHFFFAOYSA-N 0.000 description 1
- KQLJHUKZAHRXJM-UHFFFAOYSA-N 1-[(4,4,8-trimethyl-1-tricyclo[6.3.1.02,5]dodecanyl)oxy]hexan-2-ol Chemical compound C(CCC(COC12CCCC(C)(C2)CCC2C(C)(C)CC12)O)C KQLJHUKZAHRXJM-UHFFFAOYSA-N 0.000 description 1
- GQQHYCCEMXZWOS-UHFFFAOYSA-N 1-[(4,4,8-trimethyl-1-tricyclo[6.3.1.02,5]dodecanyl)oxy]pentan-2-ol Chemical compound CC1(CC2C3(CCCC(CCC12)(C3)C)OCC(CCC)O)C GQQHYCCEMXZWOS-UHFFFAOYSA-N 0.000 description 1
- MBVBLQFHVRGNLW-UHFFFAOYSA-N 1-methyl-3-(4-methylpent-3-enyl)cyclohex-3-ene-1-carbaldehyde Chemical compound CC(C)=CCCC1=CCCC(C)(C=O)C1 MBVBLQFHVRGNLW-UHFFFAOYSA-N 0.000 description 1
- VUIWFNRBSGUSIN-UHFFFAOYSA-N 1-methyl-4-(4-methylpent-3-enyl)cyclohex-3-ene-1-carbaldehyde Chemical compound CC(C)=CCCC1=CCC(C)(C=O)CC1 VUIWFNRBSGUSIN-UHFFFAOYSA-N 0.000 description 1
- GWCCFAFCQHECBM-UHFFFAOYSA-N 2,2-dimethyl-4-phenylpentanenitrile Chemical compound N#CC(C)(C)CC(C)C1=CC=CC=C1 GWCCFAFCQHECBM-UHFFFAOYSA-N 0.000 description 1
- CLUKHRLTJBCIBD-UHFFFAOYSA-N 2-(3-methylbutoxy)acetic acid Chemical compound CC(C)CCOCC(O)=O CLUKHRLTJBCIBD-UHFFFAOYSA-N 0.000 description 1
- IVXLPXQDGKUAMK-UHFFFAOYSA-N 2-[(4,4,8-trimethyl-1-tricyclo[6.3.1.02,5]dodecanyl)oxy]pentan-1-ol Chemical compound CC1(CC2C3(CCCC(CCC12)(C3)C)OC(CO)CCC)C IVXLPXQDGKUAMK-UHFFFAOYSA-N 0.000 description 1
- YCOHHRPARVZBHK-JOEFCEOISA-N 2-methyl-3-[[(1S,2R,4S)-1,7,7-trimethyl-2-bicyclo[2.2.1]heptanyl]oxy]propan-1-ol Chemical compound CC(CO)CO[C@@H]1C[C@@H]2CC[C@]1(C2(C)C)C YCOHHRPARVZBHK-JOEFCEOISA-N 0.000 description 1
- IXIYWQIFBRZMNR-UHFFFAOYSA-N 3,4,5,6,6-pentamethylhept-3-en-2-one Chemical compound CC(C)(C)C(C)C(C)=C(C)C(C)=O IXIYWQIFBRZMNR-UHFFFAOYSA-N 0.000 description 1
- JFTSYAALCNQOKO-UHFFFAOYSA-N 3-(4-ethylphenyl)-2,2-dimethylpropanal Chemical compound CCC1=CC=C(CC(C)(C)C=O)C=C1 JFTSYAALCNQOKO-UHFFFAOYSA-N 0.000 description 1
- NWMCCMGWYCKNJR-UHFFFAOYSA-N 3-(4-ethylphenyl)-2,2-dimethylpropanenitrile Chemical compound CCC1=CC=C(CC(C)(C)C#N)C=C1 NWMCCMGWYCKNJR-UHFFFAOYSA-N 0.000 description 1
- JRJBVWJSTHECJK-PKNBQFBNSA-N 3-Methyl-4-(2,6,6-trimethyl-2-cyclohexen-1-yl)-3-buten-2-one Chemical compound CC(=O)C(\C)=C\C1C(C)=CCCC1(C)C JRJBVWJSTHECJK-PKNBQFBNSA-N 0.000 description 1
- PNWHKYXFQWRXMV-UHFFFAOYSA-N 3-[(4,4,8-trimethyl-1-tricyclo[6.3.1.02,5]dodecanyl)oxy]butan-2-ol Chemical compound CC1(CC2C3(CCCC(CCC12)(C3)C)OC(C(C)O)C)C PNWHKYXFQWRXMV-UHFFFAOYSA-N 0.000 description 1
- QXTRBFWMEPONIE-UHFFFAOYSA-N 3-[(4,4,8-trimethyl-1-tricyclo[6.3.1.02,5]dodecanyl)oxy]pentan-2-ol Chemical compound C(C(OC12CCCC(C)(C2)CCC2C(C)(C)CC12)CC)(O)C QXTRBFWMEPONIE-UHFFFAOYSA-N 0.000 description 1
- ORMHZBNNECIKOH-UHFFFAOYSA-N 4-(4-hydroxy-4-methylpentyl)cyclohex-3-ene-1-carbaldehyde Chemical compound CC(C)(O)CCCC1=CCC(C=O)CC1 ORMHZBNNECIKOH-UHFFFAOYSA-N 0.000 description 1
- YVSNOTITPICPTB-UHFFFAOYSA-N 4-methyl-2-(2-methylpropyl)oxan-4-ol Chemical compound CC(C)CC1CC(C)(O)CCO1 YVSNOTITPICPTB-UHFFFAOYSA-N 0.000 description 1
- REINJUBMDBESCN-UHFFFAOYSA-N 4-methyl-8-methylideneadamantan-2-ol Chemical compound C1C(C2=C)CC3C(C)C1CC2C3O REINJUBMDBESCN-UHFFFAOYSA-N 0.000 description 1
- MBZRJSQZCBXRGK-UHFFFAOYSA-N 4-tert-Butylcyclohexyl acetate Chemical compound CC(=O)OC1CCC(C(C)(C)C)CC1 MBZRJSQZCBXRGK-UHFFFAOYSA-N 0.000 description 1
- NXFZLSLXLZRDPX-UHFFFAOYSA-N 8-cyclooctyl-8-(cyclopenten-1-ylmethyl)-2,2,3-trimethyloxocane Chemical compound O1C(C)(C)C(C)CCCCC1(C1CCCCCCC1)CC1=CCCC1 NXFZLSLXLZRDPX-UHFFFAOYSA-N 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 235000011468 Albizia julibrissin Nutrition 0.000 description 1
- 244000144725 Amygdalus communis Species 0.000 description 1
- 235000011437 Amygdalus communis Nutrition 0.000 description 1
- 244000099147 Ananas comosus Species 0.000 description 1
- 235000007119 Ananas comosus Nutrition 0.000 description 1
- 241000205585 Aquilegia canadensis Species 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical compound CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- XWCDCDSDNJVCLO-UHFFFAOYSA-N Chlorofluoromethane Chemical compound FCCl XWCDCDSDNJVCLO-UHFFFAOYSA-N 0.000 description 1
- WTEVQBCEXWBHNA-UHFFFAOYSA-N Citral Natural products CC(C)=CCCC(C)=CC=O WTEVQBCEXWBHNA-UHFFFAOYSA-N 0.000 description 1
- 235000009917 Crataegus X brevipes Nutrition 0.000 description 1
- 235000013204 Crataegus X haemacarpa Nutrition 0.000 description 1
- 235000009685 Crataegus X maligna Nutrition 0.000 description 1
- 235000009444 Crataegus X rubrocarnea Nutrition 0.000 description 1
- 235000009486 Crataegus bullatus Nutrition 0.000 description 1
- 235000017181 Crataegus chrysocarpa Nutrition 0.000 description 1
- 235000009682 Crataegus limnophila Nutrition 0.000 description 1
- 240000000171 Crataegus monogyna Species 0.000 description 1
- 235000004423 Crataegus monogyna Nutrition 0.000 description 1
- 235000002313 Crataegus paludosa Nutrition 0.000 description 1
- 235000009840 Crataegus x incaedua Nutrition 0.000 description 1
- 241000612152 Cyclamen hederifolium Species 0.000 description 1
- 235000009355 Dianthus caryophyllus Nutrition 0.000 description 1
- 240000006497 Dianthus caryophyllus Species 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000919496 Erysimum Species 0.000 description 1
- 239000001242 FEMA 4410 Substances 0.000 description 1
- 235000016623 Fragaria vesca Nutrition 0.000 description 1
- 240000009088 Fragaria x ananassa Species 0.000 description 1
- 235000011363 Fragaria x ananassa Nutrition 0.000 description 1
- 240000001972 Gardenia jasminoides Species 0.000 description 1
- 241000147041 Guaiacum officinale Species 0.000 description 1
- 244000215562 Heliotropium arborescens Species 0.000 description 1
- 241001632576 Hyacinthus Species 0.000 description 1
- 235000010254 Jasminum officinale Nutrition 0.000 description 1
- 240000005385 Jasminum sambac Species 0.000 description 1
- 240000006568 Lathyrus odoratus Species 0.000 description 1
- 244000165082 Lavanda vera Species 0.000 description 1
- 235000010663 Lavandula angustifolia Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 241000234435 Lilium Species 0.000 description 1
- 241000218378 Magnolia Species 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 241000220225 Malus Species 0.000 description 1
- 235000011430 Malus pumila Nutrition 0.000 description 1
- 235000015103 Malus silvestris Nutrition 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000014749 Mentha crispa Nutrition 0.000 description 1
- 244000078639 Mentha spicata Species 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- 240000005852 Mimosa quadrivalvis Species 0.000 description 1
- 241000234479 Narcissus Species 0.000 description 1
- 241000233855 Orchidaceae Species 0.000 description 1
- 241000218657 Picea Species 0.000 description 1
- 235000008331 Pinus X rigitaeda Nutrition 0.000 description 1
- 241000018646 Pinus brutia Species 0.000 description 1
- 235000011613 Pinus brutia Nutrition 0.000 description 1
- 235000016067 Polianthes tuberosa Nutrition 0.000 description 1
- 244000014047 Polianthes tuberosa Species 0.000 description 1
- 239000004146 Propane-1,2-diol Substances 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 235000014443 Pyrus communis Nutrition 0.000 description 1
- 240000001987 Pyrus communis Species 0.000 description 1
- 235000002182 Reseda odorata Nutrition 0.000 description 1
- 240000008801 Reseda odorata Species 0.000 description 1
- 235000001466 Ribes nigrum Nutrition 0.000 description 1
- 241001312569 Ribes nigrum Species 0.000 description 1
- 241000220317 Rosa Species 0.000 description 1
- 240000007651 Rubus glaucus Species 0.000 description 1
- 235000011034 Rubus glaucus Nutrition 0.000 description 1
- 235000009122 Rubus idaeus Nutrition 0.000 description 1
- 235000004338 Syringa vulgaris Nutrition 0.000 description 1
- 244000297179 Syringa vulgaris Species 0.000 description 1
- 241000219793 Trifolium Species 0.000 description 1
- 229920001807 Urea-formaldehyde Polymers 0.000 description 1
- 235000009499 Vanilla fragrans Nutrition 0.000 description 1
- 244000263375 Vanilla tahitensis Species 0.000 description 1
- 235000012036 Vanilla tahitensis Nutrition 0.000 description 1
- 244000172533 Viola sororia Species 0.000 description 1
- 235000009754 Vitis X bourquina Nutrition 0.000 description 1
- 235000012333 Vitis X labruscana Nutrition 0.000 description 1
- 240000006365 Vitis vinifera Species 0.000 description 1
- 235000014787 Vitis vinifera Nutrition 0.000 description 1
- 229910021536 Zeolite Inorganic materials 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000003570 air Substances 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000004702 alkoxy alkyl carbonyl group Chemical group 0.000 description 1
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000005083 alkoxyalkoxy group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000005078 alkoxycarbonylalkyl group Chemical group 0.000 description 1
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- 125000004471 alkyl aminosulfonyl group Chemical group 0.000 description 1
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 description 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 1
- 125000004656 alkyl sulfonylamino group Chemical group 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 235000020224 almond Nutrition 0.000 description 1
- UZFLPKAIBPNNCA-BQYQJAHWSA-N alpha-ionone Chemical compound CC(=O)\C=C\C1C(C)=CCCC1(C)C UZFLPKAIBPNNCA-BQYQJAHWSA-N 0.000 description 1
- WUOACPNHFRMFPN-UHFFFAOYSA-N alpha-terpineol Chemical compound CC1=CCC(C(C)(C)O)CC1 WUOACPNHFRMFPN-UHFFFAOYSA-N 0.000 description 1
- 125000002431 aminoalkoxy group Chemical group 0.000 description 1
- 125000004103 aminoalkyl group Chemical group 0.000 description 1
- 125000005160 aryl oxy alkyl group Chemical group 0.000 description 1
- FUQAYSQLAOJBBC-MYZSUADSSA-N beta-Caryophyllene alcohol Natural products O[C@@]12[C@H]3[C@@H](C(C)(C)C3)CC[C@@](C)(C1)CCC2 FUQAYSQLAOJBBC-MYZSUADSSA-N 0.000 description 1
- JGQFVRIQXUFPAH-UHFFFAOYSA-N beta-citronellol Natural products OCCC(C)CCCC(C)=C JGQFVRIQXUFPAH-UHFFFAOYSA-N 0.000 description 1
- 235000013361 beverage Nutrition 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000004061 bleaching Methods 0.000 description 1
- 239000007844 bleaching agent Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- BMRWNKZVCUKKSR-UHFFFAOYSA-N butane-1,2-diol Chemical compound CCC(O)CO BMRWNKZVCUKKSR-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 125000004181 carboxyalkyl group Chemical group 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- IEPWIPZLLIOZLU-ARJAWSKDSA-N cis-3-Hexenyl salicylate Chemical compound CC\C=C/CCOC(=O)C1=CC=CC=C1O IEPWIPZLLIOZLU-ARJAWSKDSA-N 0.000 description 1
- 229940043350 citral Drugs 0.000 description 1
- 239000012459 cleaning agent Substances 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 229930186364 cyclamen Natural products 0.000 description 1
- BLBJUGKATXCWET-UHFFFAOYSA-N cyclaprop Chemical compound C12CC=CC2C2CC(OC(=O)CC)C1C2 BLBJUGKATXCWET-UHFFFAOYSA-N 0.000 description 1
- 125000000000 cycloalkoxy group Chemical group 0.000 description 1
- 125000006310 cycloalkyl amino group Chemical group 0.000 description 1
- 125000005144 cycloalkylsulfonyl group Chemical group 0.000 description 1
- 125000001047 cyclobutenyl group Chemical group C1(=CCC1)* 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000298 cyclopropenyl group Chemical group [H]C1=C([H])C1([H])* 0.000 description 1
- SQIFACVGCPWBQZ-UHFFFAOYSA-N delta-terpineol Natural products CC(C)(O)C1CCC(=C)CC1 SQIFACVGCPWBQZ-UHFFFAOYSA-N 0.000 description 1
- 230000002951 depilatory effect Effects 0.000 description 1
- 230000000249 desinfective effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 125000004473 dialkylaminocarbonyl group Chemical group 0.000 description 1
- AQIXEPGDORPWBJ-UHFFFAOYSA-N diethyl carbinol Natural products CCC(O)CC AQIXEPGDORPWBJ-UHFFFAOYSA-N 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- 238000004851 dishwashing Methods 0.000 description 1
- 238000005108 dry cleaning Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 230000003028 elevating effect Effects 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 230000001815 facial effect Effects 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000000834 fixative Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 238000005227 gel permeation chromatography Methods 0.000 description 1
- WTEVQBCEXWBHNA-JXMROGBWSA-N geranial Chemical compound CC(C)=CCC\C(C)=C\C=O WTEVQBCEXWBHNA-JXMROGBWSA-N 0.000 description 1
- HIGQPQRQIQDZMP-UHFFFAOYSA-N geranil acetate Natural products CC(C)=CCCC(C)=CCOC(C)=O HIGQPQRQIQDZMP-UHFFFAOYSA-N 0.000 description 1
- 230000003370 grooming effect Effects 0.000 description 1
- 229940091561 guaiac Drugs 0.000 description 1
- 230000037308 hair color Effects 0.000 description 1
- 125000004994 halo alkoxy alkyl group Chemical group 0.000 description 1
- 125000004438 haloalkoxy group Chemical group 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 125000004992 haloalkylamino group Chemical group 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 125000001072 heteroaryl group Chemical group 0.000 description 1
- 125000005326 heteroaryloxy alkyl group Chemical group 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- 125000005885 heterocycloalkylalkyl group Chemical group 0.000 description 1
- XOYYHTTVCNEROD-UHFFFAOYSA-N hex-1-enyl 2-hydroxybenzoate Chemical compound CCCCC=COC(=O)C1=CC=CC=C1O XOYYHTTVCNEROD-UHFFFAOYSA-N 0.000 description 1
- FHKSXSQHXQEMOK-UHFFFAOYSA-N hexane-1,2-diol Chemical compound CCCCC(O)CO FHKSXSQHXQEMOK-UHFFFAOYSA-N 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000000976 ink Substances 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 239000001102 lavandula vera Substances 0.000 description 1
- 235000018219 lavender Nutrition 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 235000013372 meat Nutrition 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 239000011279 mineral tar Substances 0.000 description 1
- 230000000116 mitigating effect Effects 0.000 description 1
- 239000002324 mouth wash Substances 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- BOPPSUHPZARXTH-UHFFFAOYSA-N ocean propanal Chemical compound O=CC(C)CC1=CC=C2OCOC2=C1 BOPPSUHPZARXTH-UHFFFAOYSA-N 0.000 description 1
- 150000007823 ocimene derivatives Chemical class 0.000 description 1
- JNEHELHRDRBJNC-UHFFFAOYSA-N pentan-3-ol Chemical compound C[CH]C(O)CC JNEHELHRDRBJNC-UHFFFAOYSA-N 0.000 description 1
- WCVRQHFDJLLWFE-UHFFFAOYSA-N pentane-1,2-diol Chemical compound CCCC(O)CO WCVRQHFDJLLWFE-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 230000008447 perception Effects 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- ODGAOXROABLFNM-UHFFFAOYSA-N polynoxylin Chemical compound O=C.NC(N)=O ODGAOXROABLFNM-UHFFFAOYSA-N 0.000 description 1
- 244000144977 poultry Species 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960004063 propylene glycol Drugs 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000009877 rendering Methods 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 150000003902 salicylic acid esters Chemical class 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000009991 scouring Methods 0.000 description 1
- VIDTVPHHDGRGAF-UHFFFAOYSA-N selenium sulfide Chemical compound [Se]=S VIDTVPHHDGRGAF-UHFFFAOYSA-N 0.000 description 1
- 229960005265 selenium sulfide Drugs 0.000 description 1
- 235000011888 snacks Nutrition 0.000 description 1
- KWVISVAMQJWJSZ-VKROHFNGSA-N solasodine Chemical compound O([C@@H]1[C@@H]([C@]2(CC[C@@H]3[C@@]4(C)CC[C@H](O)CC4=CC[C@H]3[C@@H]2C1)C)[C@@H]1C)[C@]11CC[C@@H](C)CN1 KWVISVAMQJWJSZ-VKROHFNGSA-N 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000035900 sweating Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 229940116411 terpineol Drugs 0.000 description 1
- 239000004753 textile Substances 0.000 description 1
- 238000009988 textile finishing Methods 0.000 description 1
- 230000002110 toxicologic effect Effects 0.000 description 1
- 231100000027 toxicology Toxicity 0.000 description 1
- XJPBRODHZKDRCB-UHFFFAOYSA-N trans-alpha-ocimene Natural products CC(=C)CCC=C(C)C=C XJPBRODHZKDRCB-UHFFFAOYSA-N 0.000 description 1
- 238000011282 treatment Methods 0.000 description 1
- 239000011800 void material Substances 0.000 description 1
- 239000000341 volatile oil Substances 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
- FUQAYSQLAOJBBC-PAPYEOQZSA-N β-caryophyllene alcohol Chemical compound C1C[C@](C2)(C)CCC[C@]2(O)[C@H]2CC(C)(C)[C@@H]21 FUQAYSQLAOJBBC-PAPYEOQZSA-N 0.000 description 1
- IHPKGUQCSIINRJ-UHFFFAOYSA-N β-ocimene Natural products CC(C)=CCC=C(C)C=C IHPKGUQCSIINRJ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/18—Ethers having an ether-oxygen atom bound to a carbon atom of a ring other than a six-membered aromatic ring
- C07C43/196—Ethers having an ether-oxygen atom bound to a carbon atom of a ring other than a six-membered aromatic ring containing hydroxy or O-metal groups
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/34—Alcohols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q13/00—Formulations or additives for perfume preparations
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/56—Ring systems containing bridged rings
- C07C2603/58—Ring systems containing bridged rings containing three rings
- C07C2603/76—Ring systems containing bridged rings containing three rings containing at least one ring with more than six ring members
- C07C2603/78—Ring systems containing bridged rings containing three rings containing at least one ring with more than six ring members containing seven-membered rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Birds (AREA)
- Epidemiology (AREA)
- Emergency Medicine (AREA)
- Wood Science & Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Fats And Perfumes (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Cosmetics (AREA)
- Detergent Compositions (AREA)
Abstract
La presente invención se refiere a nuevos ((4,4,8-trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)alcoholes y su uso como materiales de fragancia. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Compuestos organolépticos novedosos
Campo de la invención
La presente invención se refiere a nuevas entidades químicas, y la incorporación y el uso de las nuevas entidades químicas como materiales de fragancia.
Antecedentes de la invención
Nomura M, Tara T, Hamada T, Fujihara Y, Tajima K, Otani T, Journal of the Chemical Society of Japan, N° 10, 1993 1175-1183 (doi: 10.1246/nikkashi.1993.1175) proporciona compuestos que se evaluaron sobre la base de su olor. Bhatia SP y Letizia CS, Api AM. Food Chem Toxicol. Nov de 2008;46 Suμl. 11 :S95-6. (doi: 10.1016/j .fct.2008.06.030) proporciona una revision toxicological y dermatológica de alcohol de beta-cariofileno cuando se utiliza con un ingrediente de fragancia.
En la industria de las fragancias es necesario proporcionar nuevos productos químicos de forma continua para permitir a los perfumistas y otras personas crear nuevas fragancias para perfumes, colonias y productos de aseo personal. Los expertos en la técnica aprecian cómo las diferencias en la estructura química de la molécula pueden provocar diferencias significativas en el olor, las notas y las características de una molécula. Estas variaciones y la continua necesidad de descubrir y utilizar los nuevos productos químicos en el desarrollo de nuevas fragancias permiten a los perfumistas aplicar los nuevos compuestos en la creación de nuevas fragancias.
Compendio de la invención
La presente invención proporciona compuestos novedosos y su inesperado uso ventajoso en la potenciación, mejora o modificación de la fragancia de perfumes, colonias, agua de tocador, productos para el cuidado de la ropa, productos personales y similares.
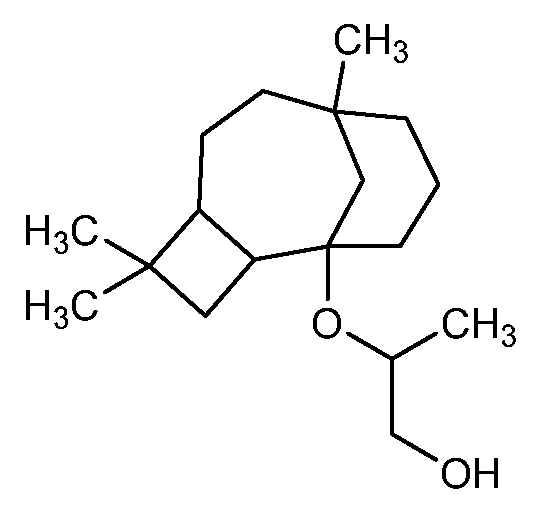
Más específicamente, la presente invención se refiere a ((4,4,8-trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)alcoholes novedosos representados por la Fórmula I que se expone a continuación:
donde R1, R2, R3 y R4 se seleccionan independientemente del grupo que consiste en hidrógeno y un grupo alquilo C1-12 lineal o ramificado, con la condición de que R1, R2, R3 y R4 juntos contengan 1-12 átomos de carbono.
Otra realización de la presente invención se refiere a un subgénero de la Fórmula I anterior representado por la Fórmula II que se expone a continuación:
donde R1', R2', R3' y R4’ se seleccionan independientemente del grupo que consiste en hidrógeno y un grupo alquilo Ci-6 lineal o ramificado, con la condición de que R1', R2', R3' y R4’ juntos contengan 1 -6 átomos de carbono.
Otra realización de la presente invención se refiere a un compuesto novedoso seleccionado del grupo que consiste en 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-1 -ol;
1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-2-ol;
2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-1-ol;
1- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol;
2- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)pentan-1 -ol;
1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)pentan-2-ol;
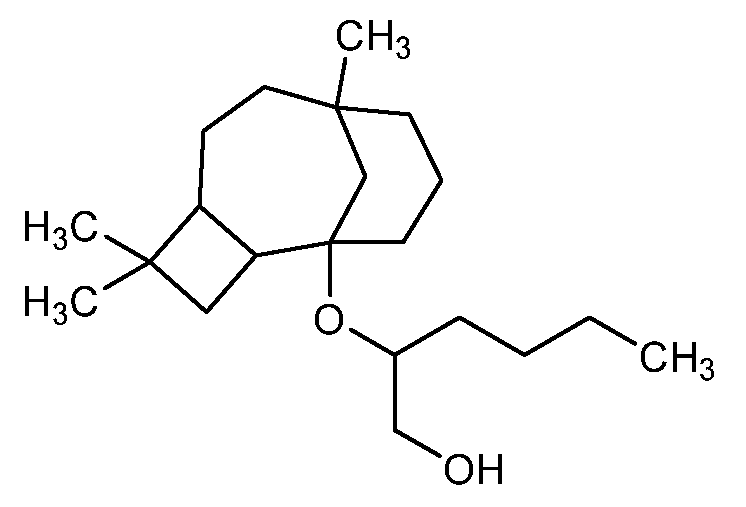
2- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-1-ol;
1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-2-ol;
3- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol;
y
una mezcla de estos.
Otra realización de la presente invención se refiere a una formulación de fragancia que comprende los compuestos novedosos proporcionados anteriormente.
Otra realización de la presente invención se refiere a un producto de fragancia que comprende los compuestos novedosos proporcionados anteriormente.
Otra realización de la presente invención se refiere a un método de mejora, potenciación o modificación de una formulación de fragancia a través de la adición de una cantidad olfativa aceptable de los compuestos novedosos proporcionados anteriormente.
Estas y otras realizaciones de la presente invención serán evidentes al leer la siguiente memoria descriptiva.
Descripción detallada de la invención
Los ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)alcoholes representados pro la Fórmula I y Fórmula II de la presente invención se ilustran, por ejemplo, con los siguientes ejemplos.
2-((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-1 -ol (Estructura 1)
1-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)propan-1-ol (Estructura 2)
2-((4,4,8-Trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)butan-1-ol (Estructura 3)
1-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)butan-2-ol (Estructura 4)
2-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)pentan-1-ol (Estructura 5)
1-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)pentan-2-ol (Estructura 6)
2-((4,4,8-Trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)hexan-1-ol (Estructura 7)
1-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)hexan-2-ol (Estructura 8)
3-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan--il)oxi)butan-2-ol (Estructura 9)
2-((4,4,8-Trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)pentan-3-ol (Estructura 10)
3-((4,4,8-Trimetiltriciclo[6.3.1.02,5]dodecan-1-il)oxi)pentan-2-ol (Estructura 11)
2-Met¡l-1-((4,4,8-tr¡metiltr¡c¡clo[6.3.1.02'5]dodecan-1-il)oxi)propan-2-ol(Estructura 12)
Los ((4,4,8-trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)alcoholes de la presente invención se pueden preparar mediante un esquema general como el representado a continuación:
donde R1, R2, R3 y R4 se definen como anteriormente.
Los expertos en la técnica reconocerán que algunos de los compuestos de la presente invención contienen centros quirales, lo que proporciona varios estereoisómeros de los compuestos reivindicados. Los isómeros individuales pueden separarse utilizando técnicas conocidos por los expertos en la técnica. Las técnicas adecuadas incluyen cromatografía tal como cromatografía de líquidos de alta resolución, a la que se hace referencia como HPLC, particularmente cromatografía en gel de sílice, y captura por cromatografía de gases conocida como captura GC. Sin embargo, las versiones comerciales de tales productos se ofrecen en su mayoría como mezclas.
En estos preparados, los compuestos de la presente invención se pueden utilizar solos o combinados con otras composiciones perfumantes, disolventes, adyuvantes y similares. Los expertos en la técnica conocen la naturaleza y la variedad de los otros ingredientes que también se pueden emplear. Se pueden emplear muchos tipos de fragancias en la presente invención, siendo la única limitación la compatibilidad con los otros componentes que se estén empleando. Las fragancias adecuadas incluyen, sin carácter limitante, frutos tales como almendra, manzana, cereza, uva, pera, piña, naranja, fresa, frambuesa; almizcle, aromas florales tales como el característico de lavanda, el característico de rosa, el característico de iris, el característico de clavel. Otros aromas agradables incluyen aromas herbarios y forestales derivados de olores forestales a pino, abeto y otros. Las fragancias también se pueden derivar de diferentes aceites, tales como aceites esenciales, o de materiales vegetales tales como menta, hierbabuena y similares.
Se proporciona una lista de fragancias adecuadas en la Pat. de EE. UU. N ° 4534891. Otra fuente de fragancias adecuadas se encuentra en Perfumes, Cosmetics and Soaps, Segunda Edición, editado por W. A. Poucher, 1959. Entre las fragancias proporcionadas en este tratado se encuentran la acacia, cassis, chipre, ciclamen, helecho, gardenia, espino, heliotropo, madreselva, jacinto, jazmín, lila, lirio, magnolia, mimosa, narciso, heno recién cortado, flor de azahar, orquídea, reseda, chícharo dulce, trébol, nardo, vainilla, violeta, alhelí y similares.
Los compuestos de la presente invención se pueden utilizar combinados con un compuesto de fragancia complementario. La expresión “compuesto de fragancia complementario”, tal como se utiliza en la presente, se define como un compuesto de fragancia seleccionado del grupo que consiste en 2-[(4-metilfenil)metileno]heptanal (Acalea), éster alílico de ácido isoamiloxiacético (Glicolato de alilo y amilo), 4,4,10,10,11,12,12-heptametil-3-oxatriciclo[7.3.0.0<2,6>]dodecano (Amber Xtreme), propan-1,3-dioato de (3,3-dimetilciclohexil)etilo y etilo (Applelide), (£/Z)-1-etoxi-1-deceno (Arctical), 2-etil-4-(2,2,3-trimetil-3-ciclopenten-1-il)-2-buten-1-ol (Bacdanol), 2-metil-3-[(1,7,7-trimetilbiciclo[2.2.1]hept-2-il)oxi]exo-1-propanol (Bornafix), 1,2,3,5,6,7-hexahidro-1,1,2,3,3-pentametil-4H-inden-4-ona (Cashmeran), trimetilciclopentenilmetiloxabiciclooctano (Cassiffix), 1,1-dimetoxi-3,7-dimetil-2,6-octadieno (Citral DMA), 3,7-dimetil-6-octen-1-ol (Citronelol), acetato de 3^,4,5,6,7,7^-hexahidro-4,7-metano-fH-inden-5/6-ilo (Cyclacet), propionato de 3A4,5,6,7,7^-hexahidro-4,7-metano-7H-inden-5/6-¡lo (Cyclaprop), butirato de 3^,4,5,6,7,7^-hexahidro-4,7-metano-1 G-inden-5/6-ilo (Ciclobutanato), 1 -(2,6,6-trimetil-3-ciclohexen-1 -il)-2-buten-1 -ona (Delta Damascona), 3-(4-etilfenil)-2,2-dimetilpropanonitrilo (Fleuranil), 3-(O/P-etilfenil)-2,2-dimetilpropionaldehído (Floralozona), tetrahidro-4-metil-2-(2-metilpropil)-2H-piran-4-ol (Florifol), 1,3,4,6,7,8-hexahidro-4,6,6,7,8,8-hexametilciclopenta-gamma-2-benzopirano (Galaxolida), 1 -(5,5-dimetil-1 -ciclohexen-1 -il)pent-4-en-1 -ona (Galbascona), acetato de £/Z-3,7-dimetil-2,6-octadien-1-ilo (Acetato de geranilo), a-metil-1,3-benzodioxol-5-propanal (Helional), 1-(2,6,6-trimetil-2-ciclohexen-1-il)-1,6-heptadien-3-ona (Hexalon), 2-hidroxibenzoato de (Z)-3-hexenilo (Salicilato de hexenilo, CIS-3), 4-(2,6,6-trimetil-2-ciclohexen-1-il)-3-buten-2-ona (lonona a), 1-(1,2,3,4,5,6,7,8-octahidro-2,3,8,8-tetrametil-2-naftalenil)etan-1-ona (Iso E Super), 3-oxo-2-pentilciclopentanacetato de metilo (Kharismal), 2,2,4-trimetil-4-fenilbutanonitrilo (Khusinil), 3,4,5,6,6-pentametilhept-3-en-2-ona (Koavone), 3/4-(4-hidroxi-4-metilpentil)ciclohexen-1 -carboxaldehído (Lyral), 3-metil-4-(2,6,6-trimetil-2-ciclohexen-1 -il)-3-buten-2-ona (MetiliononaY), 1-(2,6,6-trimetil-2-ciclohexen-1-il)pent-1-en-3-ona (Metilionona a Extra, Metilionona N), 3-metil-4-fenilbutan-2-ol (Muguesia), ciclopentadec-4-en-1-ona (Almizcle Z4), 3,3,4,5,5-pentametil-11,13-dioxatriciclo[7.4.0.0<2,6>]tridec-2(6)-eno (Nebulona), acetato de 3,7-dimetil-2,6-octadien-1-ilo (Acetato de nerilo), 3,7-dimetil-1,3,6-octatrieno (Ocimeno), orfo-toliletanol (Peomosa), 3-metil-5-fenilpentanol (Fenoxanol), 1-metil-4-(4-metil-3-pentenil)ciclohex-3-en-1-carboxaldehído (Preciclemona B), 4-metil-8-metilen-2-adamantanol (Prismantol), 2-etil-4-(2,2,3-trimetil-3-ciclopenten-1 -il)-2-buten-1 -ol (Sanjinol), 2-metil-4-(2,2,3-trimetil-3-ciclopenten-1 -il)-2-buten-1 -ol (Santaliff), 3-[c/'s-4-(2-metilpropil)ciclohexil]propanal (Starfleur), Terpineol, 2,4-dimeil-3-ciclohexen-1-carboxaldehído (Triplal), decahidro-2,6,6,7,8,8-hexametil-2H-indeno[4,5-fi]furano (Trisamber), acetato de 2-ferf-butilciclohexilo (Verdox), (3£)-4-metildec-3-en-5-ona (Veridian), acetato de 4-ferf-butilciclohexilo (Vertenex), acetilcedreno (Vertofix), 3,6/4,6-dimetilciclohex-3-en-1-carboxaldehído (Vertoliff) y (3Z)-1-[(2-metil-2-propenil)oxi]-3-hexeno (Vivaldie).
Tal como se utiliza en la presente, se entiende que el término “un” o “uno/a” se refiere a uno o más.Se entiende que la expresión “un compuesto” se refiere a uno o más de los compuestos representados por la Fórmula I o Fórmula II como se describen en la presente. La preparación de los compuestos de la presente invención se detalla en los Ejemplos. Los materiales se adquirieron en Aldrich Chemical Company, a menos que se indique lo contrario.
El término “alquilo” se refiere a un hidrocarburo monovalente saturado lineal o ramificado. Los ejemplos incluyen, por ejemplo, sin carácter limitante, metilo, etilo, propilo, 2-propilo, butilo (incluidas todas las formas isoméricas), pentilo (incluidas todas las formas isoméricas), hexilo (incluidas todas las formas isoméricas) y similares. El término “alquenilo” se refiere a un hidrocarburo alifático, insaturado, lineal o ramificado que contiene al menos un doble enlace carbonocarbono. El término “alquileno” se refiere a alquilo bivalente. Los ejemplos incluyen, sin carácter limitante, -C H 2-, -CH2CH2- , -C H 2CH2CH2- , -CH2(CH3)CH2-, -C H 2CH2CH2CH2- y similares.
El término “cicloalquilo” se refiere a un radical hidrocarbonado monovalente monocíclico, bicíclico fusionado o tricíclico fusionado, saturado de tres a catorce átomos anulares de carbono. A menos que se indique lo contrario, la valencia del grupo puede estar situada en cualquier átomo de cualquier anillo dentro del radical, mientras lo permitan las reglas de la valencia. Más específicamente, los ejemplos incluyen, por ejemplo, sin carácter limitante, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo, decahidronaftilo (por ejemplo, decahidronaft-1 -ilo, decahidronaft-2-ilo y similares), norbornilo y similares. El anillo cicloalquilo no está sustituido o puede estar sustituido con uno o más sustituyentes de sistema anular que pueden ser el mismo o diferentes, y son tal como se definen en la presente. El término “cicloalquenilo” se refiere a un radical hidrocarbonado monovalente monocíclico, bicíclico fusionado o tricíclico fusionado, de tres a catorce átomos anulares de carbono que contiene uno o más dobles enlaces. A menos que se indique lo contrario, la valencia del grupo puede estar situada en cualquier átomo de cualquier anillo dentro del radical, mientras lo permitan las reglas de la valencia. Más específicamente, los ejemplos incluyen, por ejemplo, sin carácter limitante, ciclopropenilo, ciclobutenilo, ciclopentenilo, ciclohexenilo y similares. El anillo cicloalquenilo no está sustituido o puede estar sustituido con uno o más sustituyentes de sistema anular que pueden ser el mismo o diferentes, y son tal como se definen en la presente.
La expresión “sustituyente de sistema anular” se refiere a un sustituyente unido a un sistema anular aromático o no aromático, que, por ejemplo, reemplaza un hidrógeno disponible en el sistema anular. Los sustituyentes de sistema anular pueden ser el mismo o diferentes, siendo cada uno independientemente, por ejemplo, —C(=NH)(NH2), — NHC(=NH)(NH2), alquilo, alquenilo, alquinilo, alcoxi, acilo, alquilcarbonilamino, carboxi, carboxialquilo, alcoxicarbonilo, alcoxicarbonilalquilo, ciano, nitro, alquiltio, halo, haloalquilo, haloalcoxi, amino, alquilamino, dialquilamino, aminocarbonilo, alquilaminocarbonilo, dialquilaminocarbonilo, alquilsulfonilo, cicloalquilsulfonilo, alquilsulfonilamino, alquilaminosulfonilo, haloalquilamino, oxo, hidroxi, hidroxialquilo, hidroxialquiloxi, hidroxialquiloxialquilo, alcoxialquiloxialquilo, arilo, heteroarilo, cicloalquilo, cicloalquilamino, cicloalquiloxi, heteroaralquiloxi, aminoalquilo, aminoalquiloxi, alcoxialquilo, alcoxialquilcarbonilo, alcoxialquiloxi, haloalcoxialquilo, ariloxialquilo, heteroariloxialquilo, heterocicloalquilo, heterocicloalquiloxialquilo, heterocicloalquilalquilo, heterocicloalquilalquiloxi o heterocicloalquiloxi. “Sustituyente de sistema anular” también se puede referir a un único resto que reemplaza simultáneamente dos hidrógenos disponibles en dos átomos de carbono adyacentes (un H en cada carbono) en un sistema anular. Los ejemplos de tales restos son metilenodioxi y etilenodioxi.
Las expresiones “formulación de fragancia”, “composición de fragancia” y “composición de perfume” significan lo mismo y se refieren a una composición de consumo que es una mezcla de compuestos que incluyen, por ejemplo, alcoholes, aldehídos, cetonas, ésteres, éteres, lactonas, nitrilos, aceites naturales, aceites sintéticos y mercaptanos, que se mezclan de modo que los olores combinados de los componentes individuales produzcan una fragancia agradable o deseada. La formulación de fragancia de la presente invención es una composición de consumo que comprende un compuesto de la presente invención. La formulación de fragancia de la presente invención comprende un compuesto de la presente invención y además un compuesto de fragancia complementario tal como se ha definido anteriormente.
Las expresiones “producto de fragancia” y “producto funcional” significan lo mismo y se refieren a un producto de consumo que contiene un ingrediente de fragancia que añade fragancia o enmascara el mal olor. Los productos de fragancia pueden incluir, por ejemplo, perfumes, colonias, agua de tocador, jabones en pastilla, jabones líquidos, geles de ducha, baños de espuma, cosméticos, productos para el cuidado de la piel y aseo personal tales como cremas, lociones y productos de afeitado, productos para el cuidado del cabello para lavar con champú, aclarar, acondicionar, decolorar, colorear, teñir y peinar, desodorantes y antiperspirantes, productos de higiene femenina tales como tampones y toallitas femeninas, productos para el cuidado de bebés tales como pañales, baberos y toallitas, productos para el cuidado familiar tales como papel higiénico, pañuelos faciales, pañuelos de papel o papel absorbente, productos para el cuidado de la ropa tales como suavizantes y ambientadores para la ropa, productos para el cuidado del aire tales como ambientadores del aire y sistemas de suministro de fragancias, preparados cosméticos, productos de limpieza y desinfectantes tales como detergentes, materiales de lavavajillas, composiciones para fregar, productos para la limpieza de vidrio y metal tales como limpiacristales, limpiadores de encimeras, limpiadores de pisos y alfombras, limpiadores de baños y aditivos de lejías, agentes de lavado tales como agentes de lavado multiuso, extrafuertes y de lavado a manoo lavado de ropa delicada que incluyen detergentes y aditivos de aclarado para la ropa, productos de higiene bucodental tales como pastas de dientes, geles de dientes, sedas dentales, limpiadores de
prótesis dentales, adhesivos para prótesis dentales, dentífricos, blanqueantes y enjuagues bucales, productos sanitarios y nutricionales, y productos alimenticios tales como refrigerios y bebidas. El producto de fragancia de la presente invención es un producto de consumo que contiene un compuesto de la presente invención. El producto de fragancia de la presente invención contiene un compuesto de la presente invención y además un compuesto de fragancia complementario tal como se ha definido anteriormente.
Se entiende que el término “mejora” en la frase “mejora, potenciación o modificación de una formulación de fragancia” significa elevar la formulación de fragancia a un carácter más deseable. Se entiende que el término “potenciación” significa hacer que la formulación de fragancia tenga una eficacia superior o proporcionar a la formulación de fragancia un carácter mejorado. Se entiende que el término “modificación” significa proporcionar a la formulación de fragancia un cambio de carácter.
Se entiende que la expresión “cantidad olfativa aceptable” significa la cantidad de un compuesto en una formulación de fragancia, donde el compuesto contribuirá a sus características olfativas individuales. Sin embargo, el efecto olfativo de la formulación de fragancia será la suma del efecto de cada uno de los ingredientes de fragancia. Por tanto, el compuesto de la presente invención se puede utilizar para mejorar o potenciar las características de aroma de la formulación de fragancia, o mediante la modificación de la reacción olfativa a la que contribuyen otros ingredientes en la formulación. La cantidad olfativa aceptable puede variar dependiendo de muchos factores que incluyen otros ingredientes, sus cantidades relativas y el efecto olfativo que se desee.
La cantidad de los compuestos de la presente invención empleada en una formulación de fragancia varía de aproximadamente un 0.005 a aproximadamente un 70 por ciento en peso, preferentemente de un 0.005 a aproximadamente un 50 por ciento en peso, más preferentemente de aproximadamente un 0.5 a aproximadamente un 25 por ciento en peso, e incluso más preferentemente de aproximadamente un 1 a aproximadamente un 10 por ciento en peso. Los expertos en la técnica serán capaces de emplear la cantidad deseada para proporcionar el efecto y la intensidad de fragancia deseados. Además de los compuestos de la presente invención, también se pueden utilizar otros materiales junto con la formulación de fragancia para encapsular y/o suministrar la fragancia. Algunos materiales muy conocidos son, por ejemplo, sin carácter limitante, polímeros, oligómeros, otros compuestos no poliméricos tales como surfactantes, emulsionantes, lípidos que incluyen grasas, ceras y fosfolípidos, aceites orgánicos, aceites minerales, vaselina, aceites naturales, fijadores del perfume, fibras, almidones, azúcares y materiales de superficie sólida tales como zeolita y sílice. Algunos polímeros preferidos incluyen poliacrilato, poliurea, poliuretano, poliacrilamida, poliéster, poliéter, poliamida, poli(acrilato-co-acrilamida), almidón, sílice, gelatina y goma arábiga, alginato, quitosano, polilactida, poli(melamina-formaldehído), poli(urea-formaldehído) o una combinación de estos.
Cuando se utilizan en una formulación de fragancia, estos ingredientes proporcionan notas adicionales para crear una formulación de fragancia más deseable y perceptible, y añadir la percepción de valor. Las cualidades de olor encontradas en estos materiales ayudan a embellecer e incrementar los acordes acabados así como mejorar la actuación de los otros materiales en la fragancia.
Además, también se ha descubierto sorprendentemente que los compuestos de la presente invención proporcionan un rendimiento superior de los ingredientes y poseen ventajas inesperadas en aplicaciones para neutralizar el mal olor tales como la sudoración corporal, el olor ambiental tal como moho y hongos, baño, y etc. Los compuestos de la presente invención eliminan sustancialmente la percepción de malos olores y/o evitan la formación de tales malos olores, por tanto, se pueden utilizar con un gran número de productos funcionales.
En la presente se proporcionan ejemplos de los productos funcionales para ilustrar los diferentes aspectos de la presente invención. Sin embargo, no se pretende que limiten el alcance de la presente invención. Los productos funcionales pueden incluir, por ejemplo, una composición de ambientador (o desodorante) para cuartos convencional tal como espráis ambientadores, un aerosol u otro espray, difusores de fragancia, una mecha u otro sistema líquido, o un sólido, por ejemplo, velas o un base de cera como en pomanders y plásticos, polvos como en bolsitas o espráis secos o geles, como en palos de gel sólido, desodorantes de la ropa como los aplicados mediante aplicaciones de lavadora tales como en detergentes, polvos, líquidos, blanqueantes o suavizantes de la ropa, refrescantes de la ropa, espráis para sábanas, bloques para armario, espráis de aerosol para armarios o zonas de almacenamiento de ropa o en el lavado en seco para superar las notas residuales de disolvente en la ropa, accesorios de baño tales como toallas de papel, pañuelos de baño, toallitas sanitarias, toallitas húmedas, paños para lavar desechables, pañales desechables y desodorantes para el cubo de los pañales, limpiadores tales como desinfectantes y limpiadores de la taza del inodoro, productos cosméticos tales como antiperspirantes y desodorantes, desodorantes corporales generales en forma de polvos, aerosoles, líquidos o sólidos, o productos para el cuidado del cabello tales como lacas, acondicionadores, enjuagues, colorantes y tintes para el cabello, moldeadores, productos depilatorios, alisadores del cabello, aplicaciones de acicalar el cabello tales como pomada, cremas y lociones, productos para el cuidado del cabello medicados que contienen ingredientes tales como sulfuro de selenio, alquitrán mineral o salicilatos, o champús, o productos para el cuidado de los pies tales como polvos, líquidos o colonias para pies, lociones para después del afeitado y lociones corporales, o jabones y detergentes sintéticos tales como pastillas, líquidos, espumas o polvos, el control del olor tal como durante procesos de fabricación, tal como en la industria de los acabados textiles y la industria de impresión (tintas y papel), el control de efluentes tal como en procesos que intervienen en tratamientos para la fabricación del papel, el depósito de materiales y cárnicos, depuración de aguas, bolsas de basura o eliminación de
residuos, o en el control del olor de productos como en mercancías textiles acabadas, mercancías de goma acabadas o ambientadores de automóviles, productos para el cuidado de mascotas y agrícolas tales como residuos de corral y perros, y productos para el cuidado de mascotas y animales domesticados tales como desodorantes, champú o agentes de limpieza, o material de lecho de animales y en sistemas de circuito de aire cerrado a gran escala tales como auditorios, y metros y sistemas de transporte.
Por tanto, se observará que la composición de la invención suele ser una en la que el neutralizador del mal olor está presente junto con un portador por medio del cual o a partir del cual se puede introducir el neutralizador del mal olor en un hueco en el que el mal olor está presente, o un sustrato sobre el que se ha depositado el mal olor. Por ejemplo, el portador puede ser un propulsor de aerosol tal como clorofluorometano, o un sólido tal como una cera, material plástico, goma, gel o polvo inerte. En un ambientador del aire de tipo mecha, el portador es un líquido sustancialmente inodoro de baja volatilidad. En varias aplicaciones, una composición de la invención contiene un agente tensioactivo o un desinfectante, mientras que en otras, el neutralizador del mal olor está presente sobre un sustrato fibroso. En muchas composiciones de la invención también hay presente un componente de fragancia que confiere una fragancia a la composición.
Se pueden emplear todas las fragancias indicadas anteriormente.
Se entiende que la cantidad eficaz que neutraliza el mal olor se refiere a la cantidad del neutralizador del mal olor innovador empleado en un producto funcional que es organolépticamente eficaz para mitigar un mal olor dado reduciendo a la vez la intensidad combinada del nivel de olor, donde el mal olor dado está presente en un hueco o se ha depositado sobre un sustrato. La cantidad exacta de agente neutralizador del mal olor empleado puede variar dependiendo del tipo de neutralizador del mal olor, el tipo de portador empleado y el nivel de neutralización del mal olor deseado. En general, la cantidad de agente neutralizador del mal olor presente es la dosificación ordinaria requerida para obtener el resultado deseado. Tal dosificación es conocida por el profesional capacitado en la técnica. En una realización preferida, cuando se utilizan junto con productos funcionales sólidos o líquidos malolientes, por ejemplo, jabón y detergente, los compuestos de la presente invención pueden estar presentes en una cantidad que varía de aproximadamente un 0.005 a aproximadamente un 50 por ciento en peso, preferentemente de aproximadamente un 0.01 a aproximadamente un 20 por ciento en peso y más preferentemente de aproximadamente un 0.05 a aproximadamente un 5 por ciento en peso, y cuando se utilizan junto con productos funcionales gaseoso malolientes, los compuestos de la presente invención pueden estar presentes en una cantidad que varía de aproximadamente 0.1 a 10 mg por metro cúbico de aire.
Las siguientes se proporcionan como realizaciones específicas de la presente invención y realizaciones comparativas que no entran dentro del alcance de las reivindicaciones. Tal como se utilizan en la presente todos los porcentajes son porcentajes en peso a menos que se indique lo contrario, se entiende que ppm se refiere a partes por millón, se entiende que L es litro, se entiende que mL es mililitro, se entiende que g es gramo, se entiende que Kg es kilogramo, se entiende que mol es mol, se entiende que mmol es milimol, se entiende que psi es libra-fuerza por pulga cuadrada y mmHg son milímetros (mm) de mercurio (Hg). Se entiende que IFF, tal como se utiliza en los ejemplos, significa International Flavors&Fragrances Inc., Nueva York, NY, EE. UU.
Ejemplo I
Preparación de 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)propan-1-ol (Estructura 1) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)propan-2-ol (Estructura 2):
Se cargaron cariofileno (500 g, 2.4 mol) y propano-1,2-diol (292 g, 3.8 mol) en un reactor. Se añadió ácido fosfórico (8.29 g, 85 % de pureza). La mezcla de reacción se calentó hasta 125 °C durante 8-16 horas. El avance y finalización de la reacción se controlaron mediante cromatografía gas-líquido (GLC). La reacción se enfrió a continuación hasta 80 °C, se diluyó con acetato de etilo (100 mL) y se lavó con bicarbonato de sodio para desactivar el ácido fosfórico. La capa orgánica se separó, se lavó con salmuera, se destiló apresuradamente para obtener el producto crudo (463
g). El producto crudo se fraccionó adicionalmente para proporcionar una mezcla de isómeros de posición que contenía los productos mayoritarios 2-((4,4,8-trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)propan-1-ol (Estructura 1) (~23 %) y 1-((4,4,8-trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)propan-2-ol (Estructura 2) (~60 %), y los productos minoritarios 2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.02’5]dodecan-8-il)oxi)propan-1(o 2)-ol (~10 %) y 2(o 1)-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)propan-1(o 2)-ol (~7 %). La mezcla tuvo un punto de ebullición de 140 °C a 1.0 mmgHg. Cada uno de los isómeros (donde * indica uncentro quiral) puedecontenerademásestereosiómeros que incluyen (2R)-2(o 1)-(((1 S,8S)-, (2R)-2(o 1)-(((1 S,8R)-, (2R)-2(o 1)-(((1 R,8R)-, (2R)-2(o 1)-(((1 R,8S)-, (2S)-2(o 1)-(((1 S,8S)-, (2S)-2(o 1)-(((1 S,8R)-, (2S)-2(o 1)-(((1 R,8R)- y (2S)-2(o 1)-(((1 R,8S)-4,4,8-trimetiltriciclo[6.3.1.025]dodecanil)oxi)propanol.
1H RMN (500 MHz, CDCla) 5: 3.67-3.95 (m, 1H), 2.97-3.37 (m, 2H), 2.05-2.29 (m, 1H), 1.17-1.90 (m, 12H), 0.99-1.17 (m, 6H), 0.98 (s, 3H), 0.97 (s, 3H), 0.87 (s, 3H).
En la descripción de la mezcla obtenida así como también cada isómero se indicó que tenían notas ámbar, madera, cedro y secas. Entre todos los isómeros, la Estructura 1 mostró notas especialmente fuertes y duraderas.
Ejemplo II
Preparación de (2fí)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1a) y (2R)-1-((4,4,8-trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)propan-2-ol (Estructura 2a):
Una mezcla isómerica preparada de manera similar de acuerdo con el EJEMPLO I con (R)-propano-1,2-diol contuvo los productos mayoritarios (2fí)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1a) (~22 %) y (2R)-1-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-2-ol (Estructura 2) (~60 %), y los productos minoritarios (2R)-2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.02’5]dodecan-8-il)oxi)propan-1(o 2)-ol (~3 %), (2R)-2-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)propan-1-ol (~8 %) y (2R)-1-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)propan-2-ol (~7 %).
(2R)-2-((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1a)tuvo las siguientes características espectrales de RMN:
1H RMN (500 MHz, CDCla) 5: 3.73-3.80 (m, 1H), 3.47-3.54 (m, 1H), 3.33-3.39 (m, 1H), 2.18-2.30 (m, 1H), 2.07-2.14 (m, 1H), 1.61-1.82 (m, 4H), 1.21-1.60 (m, 8H), 1.18 (d, J=12.9 Hz, 1H), 1.00-1.16 (m, 5H), 0.99 (s, 3H), 0.98 (s, 3H), 0.88 (s, 3H).
(2R)-1-((4,4,8-Trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)propan-2-ol (Estructura 2a) tuvo las siguientes características espectrales de RMN:
1H RMN (400 MHz, CDCh) 5: 3.83-4.00 (m, 1H), 3.11-3.29 (m, 2H), 2.45-2.65 (s a, 1H), 2.10-2.33 (m, 2H), 1.21-1.95 (m, 11H), 0.95-1.20 (m, 12H), 0.90 (s, 3H).
En la descripción de la mezcla obtenida se indicó que tenía notas ámbar, madera y similares al serrín. Entre todos los isómeros, la Estructura 1a mostró las notas más fuertes y más duraderas.
Ejemplo III
Preparación de (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1b) y (2S)-1-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-2-ol (Estructura 2b):
Una mezcla isomérica preparada de manera similar de acuerdo con el EJEMPLO I con (S)-propano-1,2-diol contuvo los productos (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)propan-1-ol (Estructura 1b) (~6 %), (2S)-1-((4,4,8-trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)propan-2-ol (Estructura 2b) (~80 %), (2S)-2(o 1 )-((1,4,4-trimetiltriciclo[6.3.1.02’5]dodecan-8-il)oxi)propan-1(o 2)-ol (trazas) y (2S)-2(o 1)-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)propan-1(o 2)-ol (~14 %).
(2S)-2-((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1b) tuvo las siguientes características espectrales de RMN:
1H RMN (500 MHz, CDCh) 5: 3.70-3.82 (m, 1H), 3.42-3.50 (m, 1H), 3.27-3.35 (m, 1H), 2.18-2.31 (m, 1H), 1.99-2.11 (m, 1H), 1.78-1.87 (m, 1H), 1.60-1.78 (m, 4H), 1.28-1.59 (m, 7H), 1.06-1.16 (m, 5H), 1.00-1.08 (m, 1H), 0.99 (s, 3H), 0.98 (s, 3H), 0.89 (s, 3H).
(2S)-1-((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-2-ol (Estructura 2b) tuvo las siguientes características espectrales de RMN:
1H RMN (400 MHz, CDCh) 5: 3.80-3.99 (m, 1H), 3.38 (dd, J=9.0, 3.3 Hz, 1H), 3.08 (dd, J=9.0, 8.7 Hz, 1H), 2.60 (s a,
1H), 2.14-2.27 (m, 1H), 1.78-1.93 (m, 1H), 1.67-1.78 (m, 3H), 1.18-1.67 (m, 8H), 1.02-1.18 (m, 6H), 1.01 (s, 3H), 1.00 (s, 3H), 0.90 (s, 3H).
En la descripción de la mezcla obtenida se indicó que tenía una nota de madera. Entre todos los isómeros, la Estructura 1b mostró las notas más fuertes y más duraderas.
Ejemplo IV
Preparación de 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-1-ol (Estructura 3) y 1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol (Estructura 4):
Una mezcla isoméricapreparada de manera similar de acuerdo con el EJEMPLO I con butano-1,2-diol contuvo los productos mayoritarios 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-1-ol (Estructura 3) (~20 %) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol (Estructura 4) (~50 %), y los productos minoritarios 2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.025]dodecan-8-il)oxi)butan-1(o 2)-ol (~18 %) y 2(o 1)-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)butan-1(o 2)-ol (~12 %).
2-((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-1-ol (Estructura 3) tuvo las siguientes características espectrales de RMN:
1H RMN (500 MHz, CDCla) 5: 3.50-3.58 (m, 1H), 3.00-3.45 (m, 2H), 1.94-2.31 (m, 1H), 1.19-1.88 (m, 14H), 1.00-1.17 (m, 3H), 0.92-1.00 (m, 9H), 0.88 (s, 3H).
1- ((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol (Estructura 4) tuvo las siguientes características espectrales de RMN:
1H RMN (500 MHz, CDCla) 5: 3.58-3.71 (m, 1H), 3.00-3.45 (m, 2H), 1.94-2.31 (m, 1H), 1.19-1.88 (m, 14H), 1.00-1.17 (m, 3H), 0.92-1.00 (m, 9H), 0.88 (s, 3H).
En la descripción de la mezcla obtenida se indicó que tenía fuertes notas ámbar, madera, cedro y secas. Entre todos los isómeros, la Estructura 3 mostró notas especialmente fuertes y duraderas.
Ejemplo V
Preparación de 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol (Estructura 5) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6):
Una mezcla isoméricapreparada de manera similar de acuerdo con el EJEMPLO I con pentano-1,2-diol contuvo los productos mayoritarios 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol (Estructura 5) (~20 %) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6) (~52 %), y los productos minoritarios 2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.025]dodecan-8-il)oxi)pentan-1(o 2)-ol (~22 %) y 2(o 1)-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-1(o 2)-ol (~6 %).
2-((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol (Estructura 5) tuvo las siguientes características espectrales de RMN:
1H RMN (400 MHz, CDCh) 5: 3.53-3.86 (m, 1H), 2.96-3.48 (m, 2H), 2.35-2.66 (m, 1H), 1.95-2.32 (m, 1H), 1.19-1.93 (m, 17H), 0.60-1.18 (m, 14H).
1-((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6) tuvo las siguientes características espectrales de RMN:
1H RMN (400 MHz, CDCh) 5: 3.53-3.86 (m, 1H), 2.96-3.48 (m, 2H), 2.35-2.66 (m, 1H), 1.95-2.32 (m, 1H), 1.19-1.93 (m, 17H), 0.60-1.18 (m, 14H).
En la descripción de la mezcla obtenida se indicó que tenía fuertes notas ámbar, madera, cedro y secas. Entre todos los isómeros, la Estructura 5 mostró notas especialmente fuertes y duraderas.
Ejemplo VI
Preparación de (2R)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)pentan-1-ol (Estructura 5a) y (2R)-1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6a):
Se preparó en primer lugar (R)-pentano-1,2-diol de acuerdo con Shausef al. (Journalofthe American Chemical Society (2002) 124: 1307-1315). A continuación, se preparó de manera similar una mezcla isómerica de acuerdo con el EJEMPLO I con (R)-pentano-1,2-diol que contuvo los productos mayoritarios (2R)-2-((4,4,8trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)pentan-1-ol (Estructura 5a) (~16 %) y (2R)-1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6a) (~58 %), y los productos minoritarios (2fí)-2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.025]dodecan-8-il)oxi)pentan-1(o 2)-ol (~19 %), (2R)-2-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-1-ol (~2 %) y (2R)-1-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-2-ol (~5 %).
(2R)-2-((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)pentan-1-ol (Estructura 5a) tuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCla) 5 : 3.56-3.64 (m, 2H), 3.39-3.50 (m, 1H), 2.22-2.34 (m, 1H), 2.10-2.20 (m, 1H), 1.74-1.87 (m, 2H), 1.62-1.74 (m, 2H), 1.24-1.61 (m, 12H), 1.20 (d, J=12.4 Hz, 1H), 1.10-1.17 (m, 1H), 1.02-1.08 (m, 1H), 1.01 (s, 3H), 1.0 (s, 3H), 0.91 (t, J=7.3 Hz, 3H), 0.90 (s, 3H).
(2R)-1-((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)pentan-2-ol (Estructura 6a) tuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCla) 5 : 3.70-3.79 (m, 1H), 3.27 (dd, J=9.0, 3.1 Hz, 1H), 3.21 (dd, J=9.0, 8.3 Hz, 1H), 2.52 (s, 1H), 2.11-2.26 (m, 1H), 1.79-1.90 (m, 1H), 1.60-1.76 (m, 5H), 1.28-1.59 (m, 10H), 1.11-1.19 (m, 2H), 1.03-1.10 (m, 2H), 1.01 (s, 3H), 1.00 (s, 3H), 0.95 (t, J=7.2 Hz, 3H), 0.90 (s, 3H).
(2R)-2(o 1)-((1,4,4-Trimetiltriciclo[6.3.1.025]dodecan-8-il)oxi)pentan-1(o 2)-oltuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCls) 5 : 3.62-3.73 (m, 1H), 3.40 (dd, J=8.8, 3.1 Hz, 1H), 3.21 (dd, 8.8, 8.6 Hz, 1H), 2.50 (s a, 1H), 2.00-2.09 (m, 1H), 1.79-1.85 (m, 1H), 1.72-1.78 (m 2H), 1.65-1.71 (m, 3H), 1.56-1.65 (m, 2H), 1.44-1.55 (m, 3H), 1.29-1.44 (m, 6H), 1.07-1.13 (m, 1H), 1.04 (d, J=12.8 Hz, 1H), 1.00 (s, 3H), 0.99 (s, 3H), 0.95 (t, J=7.1 Hz, 3H), 0.83 (3H).
(2R)-2-((1,1,7-T rimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-1 -ol tuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCls) 5 : 3.64-3.76 (m, 1H), 3.50 (dd, J=9.8. 5.6 Hz, 1H), 3.44-3.48 (m, 1H), 3.38-3.43 (m, 1H), 1.67 (dd, J=11.9, 5.6 Hz, 1H), 1.14-1.64 (m, 16H), 1.06 (s, 3H), 0.98-1.03 (m, 2H), 0.94 (t, J=7.2 Hz, 3H), 0.90 (s, 3H), 0.87 (s, 3H).
(2R)-1 -((1,1,7-T rimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-2-ol tuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCls) 5 : 3.75-3.82 (m, 1H), 3.51 (dd, J=9.3, 3.1 Hz, 1H), 3.41 (dd, J=9.3, 5.5 Hz, 1H), 3.24 (dd, J=9.3, 8.0 Hz, 1H), 1.12-1.78 (m, 14H), 0.99-1.10 (m, 8H), 0.96 (t, J=6.9 Hz, 3H), 0.90 (s, 3H), 0.88 (s, 3H).
En la descripción de la mezcla obtenida se indicó que tenía notas muy fuertes ámbar, madera, cedro y secas. Entre todos los isómeros, la Estructura 5a mostró notas especialmente fuertes y duraderas.
Ejemplo VII
Preparación de (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)pentan-1-ol (Estructura 5b) y (2S)-1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6b):
Se preparó en primer lugar (S)-pentano-1,2-diol de acuerdo con Shausef al. (Journalofthe American Chemical Society (2002) 124: 1307-1315). A continuación, se preparó de manera similar una mezcla isómerica de acuerdo con el EJEMPLO I con (S)-pentano-1,2-diol que contuvo los productos mayoritarios (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol (Estructura 5b) (~17 %) y (2S)-1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6b) (~56 %), y los productos minoritarios (2S)-2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.025]dodecan-8-il)oxi)pentan-1 (o 2)-ol (~20 %), (2S)-2-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-1-ol (<2 %) y (2S)-1-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-2-ol (~5 %).
(2S)-2-((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol (Estructura 5b) tuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCls) 5 : 3.60-3.67 (m, 1H), 3.51-3.57 (m, 1H), 3.36-3.44 (m, 1H), 2.21-2.33 (m, 1H), 2.03 (s a, 1H), 1.83-1.89 (m, 1H), 1.75-1.82 (m, 1H), 1.66-1.75 (m, 2H), 1.61 -1.66 (m, 1H), 1.45-1.60 (m, 6H), 1.30-1.44 (m, 5H), 1.10-1.20 (m, 2H), 1.02-1.07 (m, 1H), 1.01 (s, 3H), 1.00 (s, 3H), 0.96 (t, J=7.3 Hz, 3H), 0.92 (s, 3H).
(2S)-1-((4,4,8-Trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6b) tuvo las siguientes características
espectrales de RMN:
1H RMN (600 MHz, CDCI3) 5: 3.68-3.78 (m, 1H), 3.41 (dd, J=9.0, 3.2 Hz, 1H), 3.11 (dd, J=9.0, 9.0 Hz, 1H), 2.15-2.24 (m, 1H), 1.81-1.88 (m, 1H), 1.68-1.79 (m, 3H), 1.60-1.67 (m, 2H), 1.26-1.56 (m, 10H), 1.13-1.18 (m, 1H), 1.12 (d, J=12.8 Hz, 1H), 1.04-1.10 (m, 1H), 1.01 (s, 3H), 1.00 (s, 3H), 0.95 (t, J=7.1 Hz, 3H), 0.91 (s, 3H).
(2S)-2(o 1)-((1,4,4-Trimetiltriciclo[6.3.1.02’5]dodecan-8-il)oxi)pentan-1(o 2)-oltuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCla) 5: 3.63-3.71 (m, 1H), 3.43 (dd, J=8.8, 3.1 Hz, 1H), 3.18 (dd, J=8.8, 8.2 Hz, 1H), 2.47 (s a, 1H), 1.97-2.08 (m, 1H), 1.58-1.80 (m, 8H), 1.24-1.54 (m, 9H), 1.04-1.14 (m, 2H), 1.00 (s, 3H), 0.99 (s, 3H), 0.95 (t, J=7.1 Hz, 3H), 0.83 (s, 3H).
(2S)-1 -((1,1,7-T rimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)pentan-2-ol tuvo las siguientes características espectrales de RMN:
1H RMN (600 MHz, CDCla) 5: 3.73-3.80 (m, 1H), 3.46 (dd, J=9.3, 3.1 Hz, 1H), 3.42 (dd, J=9.3, 5.5 Hz, 1H), 3.28 (dd, J=9.3, 7.9 Hz, 1H), 2.39 (s a, 1H), 1.71 (dd, J=12.2, 5.5 Hz, 1H), 1.17-1.67 (m, 16H), 1.05 (s, 3H), 0.99-1.05 (m, 2H), 0.96 (t, J=7.1 Hz, 3H), 0.90 (s, 3H), 0.87 (s, 3H).
En la descripción de la mezcla obtenida se indicó que tenía fuertes notas ámbar, madera, ligeramente ahumado y guayaco. Entre todos los isómeros, la Estructura 5b mostró las notas más fuertes y más duraderas.
Ejemplo VIII
Preparación de 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-1-ol (Estructura 7) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-2-ol (Estructura 8):
Una mezcla isomérica preparada de manera similar de acuerdo con el EJEMPLO I con hexano-1,2-diol contuvo los productos mayoritarios 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-1-ol (Estructura 7) (~21 %) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-2-ol (Estructura 8) (~45 %), y los productos minoritarios 2(o 1)-((1,4,4-trimetiltriciclo[6.3.1.02-5]dodecan-8-il)oxi)hexan-1(o 2)-ol (~28 %) y 2(o 1)-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)hexan-1(o 2)-ol (~6 %).
1H RMN (500 MHz, CDCL) 5: 3.53-3.78 (m, 1H), 3.00-3.45 (m, 2H), 2.37-2.63 (m, 1H), 1.93-2.32 (m, 1H), 1.17-1.90 (m, 18H), 0.61-1.16 (m, 15H).
En la descripción de la mezcla obtenida se indicó que tenía notas ámbar y madera.
Ejemplo IX
Preparación de (2fí)-2-((4,4,8-tr¡metiltr¡c¡clo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1a):
Se cargaron cariofileno (2 g, 9.4 mmol) y (R)-1-(benciloxi)propan-2-ol (1.3 g, 7.8 mol) en un reactor. Se añadió ácido fosfórico (40 mg, 85 % de pureza). La mezcla de reacción se calentó hasta 125 °C durante 8 horas. El avance y finalización de la reacción se controlaron mediante GLC. La reacción se enfrió a continuación hasta 80 °C, se diluyó con acetato de etilo (10 mL) y se lavó con bicarbonato de sodio. La capa orgánica se separó, se lavó con salmuera y se concentró para proporcionar un primer producto crudo, que se purificó mediante cromatografía en gel de sílice utilizando un gradietne de hexanos y acetato de etilo. El producto bencilado aislado se hidrogenó utilizando paladio al 5 % sobre carbono (Pd/C) a 30 °C e hidrógeno (100 psi (689 kPa)) para proporcionar un segundo producto crudo, que se concentró y a continuación se purificó mediante cromatografía en gel de sílice utilizando un gradiente de hexanos y acetato de etilo par generar el producto (2R)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1a) (~99 %).
1H RMN (500 MHz, CDCI3) 5: 3.73-3.80 (m, 1H), 3.47-3.54 (m, 1H), 3.33-3.39 (m, 1H), 2.18-2.30 (m, 1H), 2.07-2.14 (m, 1H), 1.61-1.82 (m, 4H), 1.21-1.60 (m, 8H), 1.18 (d, J=12.9 Hz, 1H), 1.00-1.16 (m, 5H), 0.99 (s, 3H), 0.98 (s, 3H), 0.88 (s, 3H)
En la descripción de (2fí)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol se indicó que tenía fuertes notas ámbar, de madera seca y cedro.
Ejemplo X
Preparación de (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura 1b):
Se preparó de manera similar (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)propan-1-ol (Estructura 1b) (~99 %) de acuerdo con el EJEMPLO IX con (S)-1 -(benciloxi)propan-2-ol.
1H RMN (500 MHz, CDCla) 5: 3.70-3.82 (m, 1H), 3.42-3.50 (m, 1H), 3.27-3.35 (m, 1H), 2.18-2.31 (m, 1H), 1.99-2.11 (m, 1H), 1.78-1.87 (m, 1H), 1.60-1.78 (m, 4H), 1.28-1.59 (m, 7H), 1.06-1.16 (m, 5H), 1.00-1.08 (m, 1H), 0.99 (s, 3H), 0.98 (s, 3H), 0.89 (s, 3H).
En la descripción del (2S)-2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol obtenido se indicó que tenía una nota ámbar efímera.
Ejemplo XI
Preparación de 2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)etan-1-ol (Estructura comparativa A):
Una mezcla isomérica preparada de manera similar de acuerdo con el EJEMPLO I con etilenglicol contuvo un producto mayoritario 2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)etan-1-ol (~80 %) y un producto minoritario 2-((1,1,7-trimetildecahidro-3a,7-metanociclopenta[8]anulen-3-il)oxi)etan-1 -ol (~20 %).
1H RMN (400 MHz, CDCla) 5: 3.61-3.79 (m, 2H), 3.47-3.59 (m, 1H), 3.30-3.47 (m, 1H), 2.10-2.29 (m, 1H), 1.80-1.90 (m, 1H), 1.45-1.80 (m, 8H), 1.20- 1.45 (m, 3H), 1.03-1.19 (m, 3H), 1.01 (s, 3H), 1.00 (s, 3H), 0.90 (s, 3H)
En la descripción de la mezcla obtenida se indicó que era inodora.
Ejemplo XII
Además, se prepararon los siguientes análogos de manera similar.
3-((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)butan-2-ol (Estructura 9)
1H RMN (400 MHz, CDCh) 5: 3.67-3.83 (m, 1H), 3.55-3.66 (m, 1H), 2.16-2.30 (m, 1H), 1.02-1.90 (m, 21H), 1.01 (s, 3H), 1.00 (s, 3H), 0.88-0.92 (m, 3H).
3- ((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)propan-1-ol (Estructura comparativa B)
1H RMN (400 MHz, CDCh) 5: 3.71 -3.86 (m, 2H), 3.57-3.70 (m, 1H), 3.43-3.54 (m, 1H), 2.10-2.25 (m, 1H), 1.03-1.90 (m, 17H), 1.01 (s, 3H), 1.00 (s, 3H), 0.89 (s, 3H).
4- ((4,4,8-Trimetiltriciclo[6.3.1.02-5]dodecan-1-il)oxi)butan-2-ol (Estructura comparativa C)
1H RMN (400 MHz, CDCh) 5: 3.92-4.10 (m, 1H), 3.37-3.92 (m, 2H), 2.12-2.42 (m, 1H), 1.03-1.91 (m, 20H), 0.94-1.01 (m, 6H), 0.85-0.93 (m, 3H).
2-Metil-3-((4,4,8-trimetiltriciclo[6.3.1.02'5]dodecan-1-il)oxi)propan-1-ol (Estructura comparativa D)
1H RMN (400 MHz, CDCla) 5 : 3.18-3.72 (m, 4H), 2.11-2.27 (m, 1H), 1.91-2.09 (m, 1H), 1.02-1.89 (m, 15H), 0.95-1.02 (m, 6H), 0.88 (s, 3H), 0.78-0.86 (m, 3H).
2,2-Dimetil-3-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-1 -ol (Estructura comparativa E)
1H RMN (400 MHz, CDCla) 5 : 3.13-3.59 (m, 4H), 1.96-2.26 (m, 1H), 1.02-1.92 (m, 15H), 0.79-1.01 (m, 15H).
(1-(((4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)metil)ciclopropil)metanol (Estructura comparativa F)
1H RMN (500 MHz, CDCls) 5 : 3.19-3.61 (m, 4H), 2.10-2.21 (m, 1H), 1.78-1.88 (m, 1H), 1.02-1.77 (m, 14H), 1.00 (s, 3H), 0.98 (s, 3H), 0.88 (s, 3H), 0.39-0.57 (m, 4H).
W-(4,4,8-Trimetiltriciclo[6.3.1.02’5]dodecan-1-il)acetamida (Estructura comparativa G)
1H RMN (400 MHz, CDCls) 5 : 5.23-5.45 (s a, 1H), 2.25-2.40 (m, 2H), 1.91 (s, 3H), 1.65-1.83 (m, 4H), 1.29-1.65 (m, 6H), 1.17-1.29 (m, 2H), 1.25 (dd, J=10.3, 10.3 Hz, 1H), 1.20 (d, J=12.9 Hz, 1H), 0.97 (s, 3H), 0.96 (s, 3H), 0.86 (s, 3H).
Ejemplo XIII
Las propiedades de fragancia de los compuestos anteriores se evaluaron utilizando (i) una intensidad de olor de 0 a 10, donde 0 = ninguno, 1 = muy débil, 5 = moderado, 10 = extremadamente fuerte; y (ii) un level de complejidad, donde 0 = ninguno, 1 = muy bajo, 5 = moderado, 10 = extremadamente elevado. A continuación se presentan los puntajes promediados:
Como se ha mostrado anteriormente, los ((4,4,8-trimetiltriciclo[6.3.1,02’5]dodecan-1-il)oxi)alcoholes de Estructuras 1-9 e isómeros de estos mostraron notas ámbar y madera únicas y sumamente deseables, que estuvieron ausentes en las Estructuras A-G. Los perfiles de olor de la Estructura 5/Estructura 6 son particularmente fuertes y complejos. Tales propiedades ventajosas son inesperadas.
Ejemplo XIV
La fórmula de fragancia ejemplificada como se indica a continuación demuestra que 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol (Estructura 5) y 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol (Estructura 6) (obtenidos en el EJEMPLO V) proporcionaron un redondeo y riqueza iniciales al olor. El acorde estuvo envuelto agradablemente, dio lugar a un volumen y olor lineales en el tiempo que prolongaron la sustantividad de las notas florales.
EJEMPLO XV
La fórmula de fragancia ejemplificada como se indica a continuación demuestra que 2-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)pentan-1-ol (Estructura 5) y 1-((4,4,8-trimetiltriciclo[6.3.1.02’5]dodecan-1-il)oxi)pentan-2-ol (Estructura 6) (obtenidos en el EJEMPLO V) confirieron un brillo y aumento de volumen generales a las notas superiores. Las notas de musgo y madera estuvieron potenciadas por la creación de un carácter ámbarmadera, que proporciona atractivos caracteres de secado (dry-down).
Claims (14)
2. Una formulación de fragancia que comprende una cantidad olfativa aceptable de un compuesto que tiene la Fórmula I:
donde R1, R2, R3 y R4 se seleccionan independientemente del grupo que consiste en hidrógeno y un grupo alquilo C1-12 lineal o ramificado, con la condición de que R1, R2, R3 y R4 juntos contengan 1-12 átomos de carbono.
3. El compuesto de la reivindicación 1 que tiene la Fórmula II, o la formulación de fragancia de la reivindicación 2 donde el compuesto tiene la Fórmula II:
donde R1', R2', R3' y R4’ se seleccionan independientemente del grupo que consiste en hidrógeno y un grupo alquilo C1-6 lineal o ramificado, con la condición de que R1', R2', R3' y R4’ juntos contengan 1 -6 átomos de carbono.
4. El compuesto de la reivindicación 3 seleccionado del grupo que consiste en, o la formulación de fragancia de la reivindicación 3, donde el compuesto se selecciona del grupo que consiste en
2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-1 -ol;
1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-2-ol;
2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-1-ol;
1- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol;
2- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)pentan-1 -ol;
1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)pentan-2-ol;
2- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-1-ol;
1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-2-ol;
3- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol;
y
una mezcla de estos.
5. El compuesto de la reivindicación 4 donde el compuesto es 2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-1-ol, 1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)pentan-2-ol, o una mezcla de estos.
6. La formulación de fragancia de la reivindicación 2, donde la cantidad olfativa aceptable es de
(i) aproximadamente un 0.005 a aproximadamente un 50 por ciento en peso de la formulación de fragancia.
(ii) aproximadamente un 0.5 a aproximadamente un 25 por ciento en peso de la formulación de fragancia, o (iii) aproximadamente un 1 a aproximadamente un 10 por ciento en peso de la formulación de fragancia.
7. La formulación de fragancia de la reivindicación 2 que comprende además un polímero.
8. La formulación de fragancia de la reivindicación 7, donde el polímero se selecciona del grupo que consiste en poliacrilato, poliurea, poliuretano, poliacrilamida, poliéster, poliéter, poliamida, poli(acrilato-co-acrilamida), almidón, sílice, gelatina y goma arábiga, alginato, quitosano, polilactida, poli(melamina-formaldehído), poli(urea-formaldehído) y una combinación de estos.
9. Un método de mejora, potenciación o modificación de una formulación de fragancia que comprende el paso de añadir a la formulación de fragancia una cantidad olfativa aceptable de un compuesto que tiene la Fórmula I:
donde R1, R2, R3 y R4 se seleccionan independientemente del grupo que consiste en hidrógeno y un grupo alquilo C1-12 lineal o ramificado, con la condición de que R1, R2, R3 y R4 juntos contengan 1-12 átomos de carbono.
10. El método de la reivindicación 9, donde el compuesto tiene la Fórmula II
donde R1', R2', R3' y R4’ se seleccionan independientemente del grupo que consiste en hidrógeno y un grupo alquilo Ci-6 lineal o ramificado, con la condición de que R1', R2', R3' y R4’ juntos contengan 1 -6 átomos de carbono.
11. El método de la reivindicación 10, donde el compuesto se selecciona del grupo que consiste en
2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-1 -ol;
1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)propan-2-ol;
2-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-1-ol;
1- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol;
2- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)pentan-1 -ol;
1 -((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1 -il)oxi)pentan-2-ol;
2- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-1-ol;
1-((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)hexan-2-ol;
3- ((4,4,8-trimetiltriciclo[6.3.1.025]dodecan-1-il)oxi)butan-2-ol;
y
una mezcla de estos.
12. El método de la reivindicación 9, donde la cantidad olfativa aceptable es de aproximadamente
(i) un 0.005 a aproximadamente un 50 por ciento en peso de la formulación de fragancia.
(ii) un 0.5 a aproximadamente un 25 por ciento en peso de la formulación de fragancia, o
(iii) un 1 a aproximadamente un 10 por ciento en peso de la formulación de fragancia.
13. Un producto de fragancia que contiene el compuesto de la reivindicación 1.
14. El producto de fragancia de la reivindicación 13, donde el producto de fragancia se selecciona del grupo que consiste en un perfume, una colonia, agua de tocador, un jabón en pastilla, un jabón líquido, un gel de ducha, un baño de espuma, un producto cosmético, un producto para el cuidado personal, un producto para el cuidado de la piel, un producto para el cuidado del cabello, un desodorante, un antiperspirante, un producto de higiene femenina, un producto para el cuidado de bebés, un producto para el cuidado familiar, un producto para la ropa, un producto para el cuidado del aire, un sistema de suministro de fragancia, un preparado cosmético, un producto de limpieza, un desinfectante, un agente de lavado, un producto de higiene bucodental, un producto sanitario y nutricional y un producto alimenticio.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862765037P | 2018-08-17 | 2018-08-17 | |
| PCT/US2019/046601 WO2020037098A1 (en) | 2018-08-17 | 2019-08-15 | Novel organoleptic compounds |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2954785T3 true ES2954785T3 (es) | 2023-11-24 |
Family
ID=69525880
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19850359T Active ES2954785T3 (es) | 2018-08-17 | 2019-08-15 | Compuestos organolépticos novedosos |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11286225B2 (es) |
| EP (1) | EP3837234B1 (es) |
| CN (1) | CN112689621B (es) |
| BR (1) | BR112021002867B1 (es) |
| ES (1) | ES2954785T3 (es) |
| MX (1) | MX2021001874A (es) |
| WO (1) | WO2020037098A1 (es) |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4534891A (en) | 1982-11-12 | 1985-08-13 | International Flavors & Fragrances Inc. | Branched C13 -alk-1-en-5-ones and use thereof in perfumery |
| JP2003137758A (ja) * | 2001-10-29 | 2003-05-14 | Kiyomitsu Kawasaki | 頭髪化粧料用のマスキング組成物及び該マスキング組成物を含有する頭髪化粧料並びに頭髪化粧料のマスキング方法。 |
| US9714401B2 (en) * | 2015-10-19 | 2017-07-25 | The Procter & Gamble Company | Particles for malodor reduction |
-
2019
- 2019-08-15 CN CN201980054414.3A patent/CN112689621B/zh active Active
- 2019-08-15 MX MX2021001874A patent/MX2021001874A/es unknown
- 2019-08-15 WO PCT/US2019/046601 patent/WO2020037098A1/en unknown
- 2019-08-15 ES ES19850359T patent/ES2954785T3/es active Active
- 2019-08-15 EP EP19850359.1A patent/EP3837234B1/en active Active
- 2019-08-15 US US17/268,739 patent/US11286225B2/en active Active
- 2019-08-15 BR BR112021002867-6A patent/BR112021002867B1/pt active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| EP3837234A4 (en) | 2022-05-18 |
| MX2021001874A (es) | 2021-04-19 |
| CN112689621A (zh) | 2021-04-20 |
| US20210179521A1 (en) | 2021-06-17 |
| WO2020037098A1 (en) | 2020-02-20 |
| US11286225B2 (en) | 2022-03-29 |
| BR112021002867A2 (pt) | 2021-05-11 |
| EP3837234A1 (en) | 2021-06-23 |
| CN112689621B (zh) | 2023-04-04 |
| EP3837234B1 (en) | 2023-06-07 |
| BR112021002867B1 (pt) | 2022-08-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2687171T3 (es) | Compuestos organolépticos | |
| ES2595528T3 (es) | 3-(ciclohex-1-en-1-il)propionatos y su uso en composiciones de perfume | |
| ES2797925T3 (es) | Nuevos compuestos de octahidroindenil propanal | |
| ES2954785T3 (es) | Compuestos organolépticos novedosos | |
| US10982172B2 (en) | Organoleptic compounds | |
| ES2781089T3 (es) | Composición de fragancia | |
| ES2743377T3 (es) | Compuestos organolépticos novedosos | |
| ES2751901T3 (es) | Compuestos organolépticos noveles | |
| CN112639064B (zh) | 感官化合物 | |
| ES2831311T3 (es) | Compuestos organolépticos novedosos | |
| US11111458B2 (en) | Cyclopropylmethoxy derivatives | |
| ES2835103T3 (es) | Nuevos compuestos organolépticos | |
| WO2023091387A1 (en) | Novel organoleptic compounds | |
| WO2021108472A2 (en) | Novel organoleptic compounds | |
| ES2712870T3 (es) | Nuevos compuestos organolépticos |