ES2931815T3 - Composiciones para tratar y/o prevenir enfermedades de agregación de proteínas - Google Patents
Composiciones para tratar y/o prevenir enfermedades de agregación de proteínas Download PDFInfo
- Publication number
- ES2931815T3 ES2931815T3 ES19730826T ES19730826T ES2931815T3 ES 2931815 T3 ES2931815 T3 ES 2931815T3 ES 19730826 T ES19730826 T ES 19730826T ES 19730826 T ES19730826 T ES 19730826T ES 2931815 T3 ES2931815 T3 ES 2931815T3
- Authority
- ES
- Spain
- Prior art keywords
- disease
- composition
- protein aggregation
- use according
- sulfatase inhibitor
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/366—Lactones having six-membered rings, e.g. delta-lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/366—Lactones having six-membered rings, e.g. delta-lactones
- A61K31/37—Coumarins, e.g. psoralen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/27—Esters, e.g. nitroglycerine, selenocyanates of carbamic or thiocarbamic acids, meprobamate, carbachol, neostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Psychology (AREA)
- Emergency Medicine (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Plant Substances (AREA)
Abstract
Las proteopatías cubren un amplio espectro de afecciones, que incluyen enfermedades neurodegenerativas (p. ej., Alzheimer, Parkinson, enfermedades poliglutamínicas tales como la Huntingtina en la enfermedad de Huntington, enfermedades priónicas); amiloidosis de otras proteínas del sistema no nervioso como Į1-antitripsina, cadenas ligeras y pesadas de inmunoglobulina, lactadherina, apolipoproteína, gelsolina, lisozima, fibrinógeno, factor natriurético auricular, queratina, lactoferrina y microglobulina beta-2, entre otras); enfermedad de célula falciforme; cataratas; fibrosis quística; retinitis pigmentosa; y diabetes insípida nefrogénica. Sorprendentemente, la administración de un inhibidor de sulfatasa es adecuada para tratar y/o prevenir la proteotoxicidad comúnmente asociada con las proteopatías. La presente invención, por lo tanto, (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Composiciones para tratar y/o prevenir enfermedades de agregación de proteínas
Campo técnico
La presente invención se enmarca dentro del campo de la medicina y proporciona una composición para su uso en los tratamientos y/o la prevención de enfermedades de agregación de proteínas.
Antecedentes de la técnica
El buen funcionamiento de los órganos y las células dentro de un organismo se basa en el buen funcionamiento de las proteínas. Una proteína es una entidad biológica que tiene una secuencia de aminoácidos primaria; una estructura secundaria que forma dominios proteicos e incluye, lo más importante, hélices alfa y láminas beta; y una estructura terciaria, resultado de un plegamiento complejo de la cadena peptídica en tres dimensiones que implica interacciones entre la estructura principal de la cadena polipeptídica y la cadena lateral de aminoácidos. Algunas proteínas funcionan en un complejo de múltiples subunidades, donde la disposición de múltiples proteínas en una estructura cuaternaria se vuelve crucial para su buen funcionamiento.
El fallo de las proteínas para plegarse para dar estructuras tridimensionales correctas puede conducir a enfermedades denominadas proteopatías (a veces también denominadas enfermedades de agregación de proteínas, enfermedades de plegamiento incorrecto de proteínas, proteinopatías o trastornos conformacionales de proteínas). El fallo puede deberse a una o más mutaciones en el gen de las proteínas o a factores ambientales tales como estrés oxidativo, alcalosis, acidosis, cambio de pH y choque osmótico. El plegamiento incorrecto de las proteínas a veces puede conducir a la aglutinización o agregación en placas o fibrillas de amiloide que pueden exacerbar una enfermedad. Las proteopatías cubren un amplio espectro de afecciones, incluyendo enfermedades neurodegenerativas (por ejemplo, enfermedad de Alzheimer, enfermedad de Parkinson, enfermedades poliglutamínicas tales como la huntingtina en la enfermedad de Huntington, enfermedades priónicas); amiloidosis de otras proteínas distintas a las del sistema nervioso tales como I1-antitripsina, cadenas ligeras y pesadas de inmunoglobulina, lactadherina, apolipoproteína, gelsolina, lisozima, fibrinógeno, factor natriurético auricular, queratina, lactoferrina y microglobulina beta-2, entre otras); anemia drepanocítica; cataratas; fibrosis quística; retinitis pigmentosa; y diabetes insípida nefrogénica.
La amiloidosis se refiere a la deposición patológica de proteínas en forma de fibrillas verdes birrefringentes congofílicas, cuando se tiñen con rojo Congo, ya sea dispersas o en forma de amiloidomas localizados. Tales depósitos son sintomáticos de varias enfermedades, por ejemplo, enfermedad de Alzheimer, amiloide asociado a inflamación, diabetes tipo II, encefalopatía espongiforme bovina (EEB), enfermedad de Creutzfeld-Jakob (ECJ), encefalopatía espongiforme ovina y amiloidosis primaria.
Las amiloidosis se clasifican generalmente en tres grupos: amiloidosis sistémicas principales, amiloidosis localizadas principales y amiloidosis misceláneas. Las amiloidosis sistémicas principales incluyen: estados inflamatorios crónicos (por ejemplo, tuberculosis, osteomielitis, etc.); estados no infecciosos tales como artritis reumatoide juvenil, espondiloartritis anquilosante y enfermedad de Crohn, etc.; poliserositis familiar recurrente, discrasia de células plasmáticas (amiloidosis primaria) y diversas polineuropatías y miocardiopatías hereditarias. Las amiloidosis localizadas principales incluyen: amiloidosis relacionada con la diálisis, enfermedad de Alzheimer, síndrome de Down, hemorragia cerebral hereditaria (tipo holandesa) y hemorragia cerebral atraumática de los ancianos. Las amiloidosis misceláneas incluyen: polineuropatía hereditaria (tipo Iowa), amiloidosis hereditaria (tipo finlandesa), hemorragia cerebral hereditaria (tipo islandesa), ECJ, carcinoma medular de la tiroides, amiloide auricular y diabetes mellitus (insulinomas). Otras amiloidosis incluyen aquellas a las que se hace referencia en Louis W. Heck, “The Amyloid Diseases” en Cecil's Textbook of Medicine 1504-6 (W.B. Saunders & Co., Filadelfia, Pa.; 1996).
Las encefalopatías espongiformes transmisibles que provocan ECJ y enfermedad de Gerstmann-Strassler-Scheinker (GSS) se describen por B. Chesebro et al., “Transmissible Spongiform Encephalopathies: A Brief Introduction” en FIELD'S VIROLOGY 2845-49 (3a edición; Raven Publishers, Filadelfia, Pa.; 1996) y en D. C. Gajdusek, “ Infectious amyloids: Subacute Spongiform Encephalopathies as Transmissible Cerebral Amyloidoses”, 2851-2900 en FIELDS VIROLOGY (1996). Muchas de estas enfermedades están mediadas probablemente por priones, una proteína infecciosa. Véase S. B. Prusineri, “Prions” en FIELDS VIROLOGY 2901-50 (1996) y las referencias contenidas en el mismo.
Intentar eliminarfibrillas específicas ha sido el objetivo de investigación significativa sobre la amiloidosis, pero sin éxito. El tratamiento actual de la amiloidosis implica agentes de quimioterapia o esteroides, tales como melfalán y dexametasona. Sin embargo, un tratamiento de este tipo no es apropiado para todos los pacientes y no es eficaz en muchos casos debido a la falta de especificidad (documento WO 2017/075540 A1). De manera similar, el tratamiento de otras proteopatías que no se asocian necesariamente con la formación de amiloides también han tenido un éxito limitado. Por tanto, existe una gran necesidad de alternativas que puedan tratar o prevenir de manera segura y eficaz las proteopatías.
Los inventores de la presente invención se interesaron inicialmente en desentrañar nuevos elementos que rigen el control genético del envejecimiento para mejorar nuestra comprensión de este intrincado proceso biológico. Con este objetivo, aislaron mutantes termotolerantes e identificaron un alelo del gen sul-2 (un gen que codifica para uno de los tres miembros de la familia de sulfatasas de Caenorhabditis elegans) que contenía una mutación puntual inactivante. Los inventores hallaron que los gusanos que portaban la versión inactivada del gen sul-2 vivieron más tiempo que los de tipo natural.
Las sulfatasas son una gran familia de proteínas implicadas en diferentes procesos biológicos y afectan a una amplia gama de sustratos. La colocación de sul-2 en el árbol filogenético de la sulfatasa es incierto. Sin embargo, en comparación con las sulfatasas de mamíferos, sul-2 se agrupa cercano a las arilsulfatasas de tipo H, F, E, D y a la sulfatasa esteroidea de tipo C que probablemente se originan a partir de un gen progenitor común. Los inventores plantearon la hipótesis de que sul-2 puede ejercer su actividad modificando las hormonas esteroideas sulfatadas.
Se ha demostrado que el inhibidor de la sulfatasa esteroidea DU-14 protege la memoria espacial y la plasticidad sináptica de la interrupción por la proteína p amiloide en ratas macho (Xing-Hua Yue et al., Hormones and Behavior 83 (2016) 83-92).
Las sulfatasas de hormonas esteroideas son proteínas conservadas que participan en diferentes procesos, tales como estimular la proliferación de cánceres dependientes de hormonas (Mueller et al., 2015. Endocr Rev. 36(5):526-63). Se han generado inhibidores específicos para este tipo de enzima, uno de ellos es STX64 (Nussbaumer y Billich, 2004. Med Res Rev. 24(4):529-76). STX64 se ha usado para tratar a pacientes con cánceres dependientes de hormonas (Stanway et al., 2006. Clin Cancer Res. 12(5):1585-92). Los inventores trataron gusanos de tipo natural con STX64 y observaron los mismos efectos de longevidad que en los mutantes con sul-2. Sin embargo, STX64 no aumentó adicionalmente la longevidad de los mutantes con deleción de sul-2, lo que indica que el mecanismo por el que STX64 aumenta la longevidad es mediante la inhibición de la actividad sulfatasa de SUL-2 (documento WO 2014/154927 A1).
Figuras
Figura 1: La reducción de la actividad sulfatasa de hormonas esteroideas (STS) mejora los síntomas de proteotoxicidad en una cepa modelo NL5901 de C. elegans para la enfermedad de Parkinson (Van Ham et al., 2010. Cell 142: 601 612). Los nematodos que expresan a -sinucleína en las células musculares padecen una movilidad reducida a medida que envejecen (medida como el número de veces por minuto que la cabeza del gusano cruza el eje longitudinal del cuerpo (cabeceos)), pero la velocidad se ralentiza cuando (A) el nematodo comprende el alelo sul-2(gk187) y (B) los nematodos se tratan con STX64. n = 20; *** representa p<0,001.
Figura 2: La reducción de la actividad sulfatasa de hormonas esteroideas (STS) altera la manera en que la a-sinucleína se agrega en una cepa modelo NL5901 de C. elegans para la enfermedad de Parkinson (Van Ham et al., 2010. Celk 142: 601-612). Los gráficos muestran (A) el número total de agregados, (B) el número de agregados con un tamaño > 3 |i m y (C) el número de agregados con un tamaño < 1 |i m de nematodos que expresan a-sinucleína fusionada con YFP y nematodos que expresan el mismo constructo de a-sinucleína que comprende adicionalmente un alelo inactivo de sul-2, es decir, sul-2(gk187). n = 20; *** representa p<0,001; * representa p<0,05.
Figura 3: La reducción de la actividad sulfatasa de hormonas esteroideas (STS) altera la manera en que la a-sinucleína se agrega en una cepa modelo NL5901 de C. elegans para la enfermedad de Parkinson (Van Ham et al., 2010. Cell 142: 601-612). Los gráficos muestran (A) el número total de agregados, (B) el número de agregados con un tamaño > 3 |i m y (C) el número de agregados con un tamaño < 1 |i m de nematodos que expresan a-sinucleína fusionada con YFP tratados con DMSO y nematodos que expresan el mismo constructo de a-sinucleína que se han tratado adicionalmente con STX64. n = 20; *** significa que p<0,001; * representa p<0,05.
Figura 4: La reducción de la actividad sulfatasa de hormonas esteroideas (STS) mejora los síntomas de proteotoxicidad en una cepa modelo UA44 de C. elegans para la enfermedad de Parkinson (Cooper et al., 2006. Science 313: 324 328). (A) La supervivencia de las neuronas dopaminérgicas marcadas con GFP que expresan a-sinucleína humana aumenta cuando el nematodo comprende el alelo inactivo sul-2(gk187). El gráfico representa el número de neuronas vivas en los nematodos que están en el día 6 cuando el nematodo comprende el alelo de tipo natural de sul-2 o el alelo inactivo sul-2(gk187). (B) Una imagen representativa de un nematodo que comprende el alelo sul-2 de tipo natural y un nematodo que comprende el alelo inactivo sul-2(gk187) en el día 9. Las flechas negras apuntan hacia las neuronas dopaminérgicas vivas. n = 37; p<0,0001.
Figura 5: La reducción de la actividad sulfatasa de hormonas esteroideas (STS) mejora los síntomas de proteotoxicidad en una cepa modelo AM140 de C. elegans para la enfermedad de Huntington (Morley et al. 2002. PNAS. 99: 10417 10422). Los nematodos se han modificado para expresar una repetición de poliglutamina de 35 residuos fusionada con YFP y el número de agregados fluorescentes se contó en el día 5 de la etapa adulta. (A) El gráfico muestra una comparación entre un nematodo que comprende el alelo de tipo natural de sul-2 y un nematodo que comprende el alelo mutante inactivo de sul-2. (B) El gráfico muestra una comparación entre un nematodo que comprende el alelo de tipo natural de sul-2 y un nematodo que comprende el alelo de tipo natural de sul-2 que se trató adicionalmente con
STX64. n = 20; *** representa p<0,001.
Figura 6: La reducción de la actividad sulfatasa de hormonas esteroideas (STS) mejora los síntomas de proteotoxicidad en una cepa modelo CL2006 de C. elegans para la enfermedad de Alzheimer (Link, 1995. PNAS. 92: 9368-9372). Los nematodos que expresan p-amiloide en células musculares padecen parálisis a medida que envejecen, pero la velocidad se ralentiza cuando (A) los nematodos comprenden el alelo sul-2(gk187) y (B) los nematodos se tratan con STX64. n = 50; p<0,001.
Figura 7: El tratamiento con STX64 alivió la deposición de p-amiloide y la deficiencia cognitiva en modelos de ratón con enfermedad de Alzheimer. (A) El efecto de la administración intrahipocámpica y oral de STX64 en la prueba de evitación pasiva en ratones de tipo natural a los que se les inyectaron oligómeros de p-amiloide en el hipocampo. El número de ratones en cada grupo era >5. (B) Imágenes inmunorreactivas de p-amiloide representativas evaluadas en la corteza frontal y el hipocampo de ratones APP-PS1 mayores de 15 meses después de 3-4 semanas de ingesta de vehículo o STX64 (0,005 mg/ml en el agua para beber). (C)-(E) Cuantificación del porcentaje de área de p-amiloide (C), densidad de deposición (D) y tamaño promedio de placa (E) en la corteza frontal y el hipocampo de ratones APP-PS1 de >15 meses después de 3-4 semanas de administración oral con STX64 o vehículo. n=4 ratones por grupo. (F) Evolución temporal de la deposición de p-amiloide en ratones APP-PS1 y el efecto del tratamiento oral con STX64 de 3-4 semanas sobre el área de p-amiloide en la corteza frontal y el hipocampo. El número de microfotografías usadas era de más de 3 por ratón. (G) Efecto de la administración oral con STX64 en ratones APP-PS1 de más de 15 meses, y comparación con ratones APP-PS1 y de tipo natural mayores de 15 meses en la prueba de evitación pasiva. El número de ratones en cada grupo era >5. En el análisis histológico, * representa diferencias estadísticamente significativas entre el vehículo y STX64 administrados a ratones APP-PS1. En la prueba de comportamiento, * representa diferencias estadísticamente significativas entre las sesiones de memoria a corto plazo y a largo plazo (STM y LTM, respectivamente) y la sesión de entrenamiento en el mismo grupo experimental; y representa diferencias estadísticamente significativas entre las sesiones de STM y LTM entre cada grupo experimental y el grupo de p-amiloide. Un símbolo representa p<0,05; dos repeticiones del símbolo representan p<0,01 y tres repeticiones del símbolo representan p<0,001.
Figura 8: STX64 previene el deterioro de la actividad motora en un modelo de ratón de enfermedad de Huntington. Se trataron diariamente ratones R6/1 de un mes con agua potable que comprendía STX64 o el propio vehículo. A la edad de 2 meses, se sometió a prueba la actividad motora de los ratones. n >5 ratones por grupo. El resultado representa media+EEM. *, p<0,05.
Figura 9: Una comparación entre STX64 y EMATE en un modelo de enfermedad de Alzheimer, es decir, la cepa GMC101 de C. elegans (McColl et al., 2012. Mol Neurodegener. 7:57). (A) En el contexto de deleción de sul-2(gk187) se redujo el número de gusanos paralizados. El gráfico muestra el número total obtenido de tres muestras biológicas, n = 100 gusanos. Ji cuadrado, bilateral, valor de p = 0,0161. (B) El tratamiento con STX64 a 1 |ig/ml redujo el número de gusanos paralizados. El gráfico muestra el número total obtenido de tres muestras biológicas, n > 120 gusanos. Ji cuadrado, bilateral, valor de p = 0,0014. (C) El tratamiento con EMATE a 1 |ig/ml redujo el número de gusanos paralizados. El gráfico muestra el número total obtenido de tres muestras biológicas, n > 117 gusanos. Ji cuadrado, bilateral, valor de p = 0,0091.
Sumario de la invención
Sorprendentemente, los inventores hallaron que STX64 es capaz de tratar o prevenir la formación de oligómeros y/o amiloides en un modelo de C. elegans para enfermedad de Parkinson, un modelo de C. elegans para enfermedad de Huntington y un modelo de C. elegans para enfermedad de Alzheimer (véanse las figuras 1-6). En la enfermedad de Parkinson, la enfermedad de Huntington y la enfermedad de Alzheimer, la patogenia está dirigida por la producción y/o deposición de agregados de proteínas (Murphy y Levine, 2010. J Alzheimers Dis. 19(1):311; Stefanis, 2012. Cold Spring Harb Perspect Med. 2(2): a009399; Daldin et al., 2017. Sci Rep. 7(1):5070). Por tanto, el tratamiento o la prevención de especies de agregados en estos modelos hace plausible que pueda usarse STX64 para tratar y/o prevenir estas enfermedades de agregación de proteínas. Esto se confirmó en un modelo de ratón para la enfermedad de Alzheimer en el que se halló que STX64 disminuyó la formación de placas de p-amiloide y revirtió las deficiencias cognitivas provocadas por la administración intrahipocámpica de oligómeros de p-amiloide y en un modelo de ratón transgénico de enfermedad de Alzheimer (véase la figura 7). Además, los C. elegans que comprenden mutaciones de inactivación en un gen de sulfatasa fueron igualmente menos propensos a formar agregados dañinos, haciendo plausible que este efecto no sólo esté asociado STX64, sino que se sea aplicable a cualquier inhibidor de sulfatasa. El hecho de que este efecto preventivo/terapéutico se obtuvo en modelos para tres enfermedades de agregación de proteínas diferentes en las que las proteínas tóxicas se expresaron en células musculares o células neuronales hace plausible que pueda usarse un inhibidor de sulfatasa para tratar y/o prevenir cualquier enfermedad de agregación de proteínas.
Por tanto, en un primer aspecto, la presente invención proporciona una composición que comprende un inhibidor de sulfatasa para su uso en el tratamiento y/o la prevención de una enfermedad de agregación de proteínas,
preferiblemente en un paciente y/o animal, en la que el inhibidor de sulfatasa es un compuesto de fórmula (I) tal como se define en las reivindicaciones.
Además, en un segundo aspecto, la presente invención proporciona un kit para su uso en la fabricación de un medicamento para el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, que comprende (i) un inhibidor de sulfatasa; y (ii) un portador y/o diluyente farmacéuticamente aceptable, en el que el inhibidor de sulfatasa es un compuesto de fórmula (I) tal como se define en las reivindicaciones.
Descripción detallada de la invención
Definiciones
Los términos “individuo”, “paciente” o "sujeto” se usan de manera intercambiable en la presente solicitud para designar a un ser humano y no pretenden ser limitativos de ninguna manera. El “individuo”, “paciente” o ”sujeto” puede ser de cualquier edad, sexo y estado físico. El término “animal”, tal como se usa en la presente solicitud, se refiere a cualquier heterótrofo eucariota multicelular que no sea un humano. En una realización preferida, el animal se selecciona del grupo que consiste en gatos, perros, cerdos, hurones, conejos, jerbos, hámsteres, cobayas, caballos, gusanos, ratas, ratones, vacas, ovejas, cabras, alpacas, camellos, burros, llamas, yaks, jirafas, elefantes, suricatos, lémures, leones, tigres, canguros, koalas, murciélagos, monos, chimpancés, gorilas, osos, dugones, manatís, focas y rinocerontes.
Tal como se usa en el presente documento, “portador farmacéuticamente aceptable” o “diluyente farmacéuticamente aceptable” significa todos y cada uno de disolventes, medios de dispersión, recubrimientos, agentes antibacterianos y antifúngicos, agentes isotónicos y retardantes de la absorción, compatibles con la administración farmacéutica. El término “excipiente farmacéuticamente aceptable” se refiere a cualquier sustancia formulada junto con el principio activo de un medicamento, incluido con el propósito de estabilización a largo plazo, aumentar el volumen de formulaciones sólidas que contienen principios activos potentes en pequeñas cantidades, o para conferir una mejora terapéutica en el principio activo en la forma de dosificación final, tal como facilitar la absorción de fármaco, reducir la viscosidad o mejorar la solubilidad. Los excipientes también pueden ser útiles en el procedimiento de fabricación, para ayudar en la manipulación del principio activo en cuestión, tal como facilitando la fluidez del polvo o las propiedades antiadherentes, además de ayudar a la estabilidad in vitro, tal como prevención de la desnaturalización o agregación a lo largo de la vida útil esperada. El uso de tales medios y agentes para principios farmacéuticamente activos se conoce bien en la técnica. Los portadores, excipientes o estabilizadores aceptables no son tóxicos para los receptores en las dosificaciones y concentraciones empleadas y, sin limitar el alcance de la presente invención, incluyen: agentes de tamponamiento adicionales; conservantes; codisolventes; antioxidantes, incluyendo ácido ascórbico y metionina; agentes quelantes tales como EDTA; complejos metálicos (por ejemplo, complejos Zn-proteína); polímeros biodegradables, tales como poliésteres; contraiones que forman sales, tales como sodio, alcoholes de azúcar polihidroxilados; aminoácidos, tales como alanina, glicina, glutamina, asparagina, histidina, arginina, lisina, ornitina, leucina, 2-fenilalanina, ácido glutámico y treonina; alcoholes de azúcar o azúcares orgánicos, tales como lactitol, estaquiosa, manosa, sorbosa, xilosa, ribosa, ribitol, mioinisitosa, mioinisitol, galactosa, galactitol, glicerol, ciclitoles (por ejemplo, inositol), polietilenglicol; agentes reductores que contienen azufre, tales como urea, glutatión, ácido tióctico, tioglicolato de sodio, tioglicerol, [alfa]-monotioglicerol y tiosulfato de sodio; proteínas de bajo peso molecular, tales como albúmina sérica humana, albúmina sérica bovina, gelatina u otras inmunoglobulinas; y polímeros hidrófilos, tales como polivinilpirrolidona. También pueden incluirse otros portadores, excipientes o estabilizadores farmacéuticamente aceptables, tales como los descritos en Remington: The Science and Practice of Pharmacy 22a edición, Pharmaceutical press (2012), ISBN-13: 9780857110626.
Los términos “tratamiento” y “terapia”, tal como se usan en la presente solicitud, se refieren a un conjunto de medios higiénicos, farmacológicos, quirúrgicos y/o físicos usados con la intención de curar y/o aliviar una enfermedad y/o síntomas con el objetivo de remediar el problema de salud. Los términos “tratamiento” y “terapia” incluyen métodos preventivos y curativos, ya que ambos están dirigidos al mantenimiento y/o restablecimiento de la salud de un individuo o animal. Independientemente del origen de los síntomas, enfermedad y discapacidad, la administración de un medicamento adecuado para aliviar y/o curar un problema de salud debe interpretarse como una forma de tratamiento o terapia en el contexto de esta solicitud.
El término “prevención”, tal como se usa en la presente solicitud, se refiere a un conjunto de medios higiénicos, farmacológicos, quirúrgicos y/o físicos usados para prevenir la aparición y/o el desarrollo de una enfermedad y/o síntomas. El término “prevención” abarca los métodos profilácticos, ya que estos se usan para mantener la salud de un animal o individuo.
El término “inhibidor de sulfatasa” se refiere a cualquier sustancia capaz de reducir la actividad de una enzima de la clase esterasa que cataliza la hidrólisis de ésteres sulfato. La sustancia puede ser una molécula que se une a cualquiera de los siguientes elementos: el gen que codifica para la enzima sulfatasa, factores de transcripción de dicho gen, cualquiera de los productos de expresión de dicho gen, por ejemplo, sin limitarse a, el ARN mensajero o la enzima sulfatasa, y disminuye o inhibe la expresión y la actividad de la molécula a la que se une, y/o su señalización intracelular o extracelular, conduciendo de ese modo a la inhibición total o parcial de la actividad de la enzima sulfatasa. El inhibidor puede seleccionarse de la lista que consiste en, sin limitarse a: antagonistas contra la enzima sulfatasa
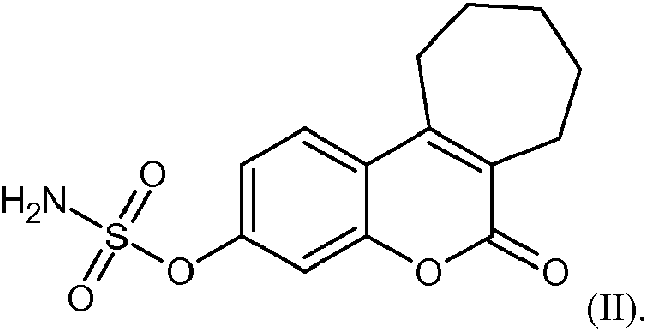
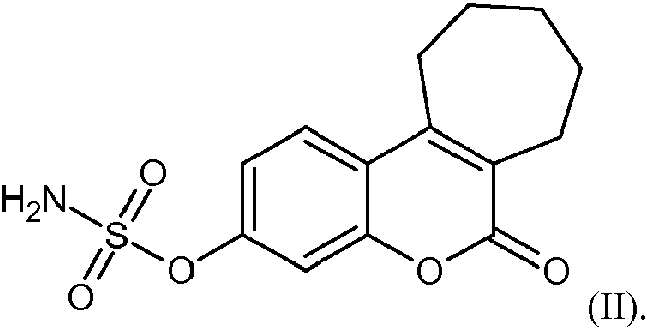
(preferiblemente químicos), ARN silenciador o un anticuerpo específico contra la enzima sulfatasa (preferiblemente, el anticuerpo es monoclonal); en la presente invención, este anticuerpo puede definirse como un anticuerpo neutralizante contra el efecto de la enzima sulfatasa. Ejemplos de inhibidores químicos de la actividad de la enzima sulfatasa son, sin limitarse a, sustratos alternativos tales como los de la serie 2-(hidroxifenil) indol sulfato, esteroides sintéticos o naturales que presentan actividad inhibidora contra STS, tales como 5-androsteno-3p, 17p-diol-3 sulfato, inhibidores competitivos tales como E1-MTP o EMATE, inhibidores no estrogénicos tales como DU-14 (n.° CAS: 186303-55-9), COUMATE (4-metilcumarin-7-O-sulfamato) o STX64 (es decir, el compuesto de fórmula (II)), u otros, tales como KW-2581 o STX213, cuyas CI50 contra la enzima sulfatasa se han determinado en diferentes estudios (Purohit y Foster, 2012, J. Endocrinol., 212(2):99-110).
El término “sulfatasa de hormonas esteroideas” (“STS”) se refiere a cualquier enzima sulfatasa implicada en el metabolismo de los esteroides. En particular, las enzimas catalizan la conversión de precursores de esteroides sulfatados en un esteroide libre. Se ha secuenciado una STS a modo de ejemplo hallada en humanos, se ha caracterizado y los datos se han depositado en la base de datos UniProtKB con el número de registro P08842. El término “inhibidor de sulfatasa de hormonas esteroideas” se refiere a cualquier sustancia capaz de reducir la actividad de una sulfatasa de hormonas esteroideas. La sustancia puede ser una molécula que se une a cualquiera de los siguientes elementos: el gen que codifica para la enzima STS, factores de transcripción de dicho gen, cualquiera de los productos de expresión de dicho gen, por ejemplo, sin limitarse a, el ARN mensajero o la enzima STS, y disminuye o inhibe la expresión y la actividad de la molécula a la que se une, y/o su señalización intracelular, conduciendo de ese modo a la inhibición total o parcial de la actividad de la enzima STS. El inhibidor puede seleccionarse de la lista que consiste en, sin limitarse a: antagonistas contra la enzima STS (preferiblemente químicos), ARN silenciador o un anticuerpo específico contra la enzima STS (preferiblemente, el anticuerpo es monoclonal); en la presente invención, este anticuerpo puede definirse como un anticuerpo neutralizante contra el efecto de la enzima STS. Ejemplos de inhibidores químicos de la actividad de la enzima STS son, sin limitarse a, sustratos alternativos tales como los de la serie 2-(hidroxifenil) indol sulfato, esteroides sintéticos o naturales que presentan actividad inhibidora contra STS, tales como 5-androsteno-3p, 17p-diol-3 sulfato, inhibidores competitivos tales como E1-MTP o EMATE, inhibidores no estrogénicos tales como DU-14, COUMATE (4-metilcumarin-7-O-sulfamato) o STX64 (es decir, el compuesto de fórmula (II)), u otros, tales como KW-2581 o STX213, cuyas CI50 contra la enzima sulfatasa se han determinado en diferentes estudios (Purohit y Foster, 2012, J. Endocrinol., 212(2):99-110).
Los términos “enfermedad de agregación de proteínas”, “proteopatía”, “proteinopatía” o “enfermedades de plegamiento incorrecto de proteínas” se refieren a cualquier enfermedad en la que determinadas proteínas se vuelven estructuralmente anómalas y alteran de ese modo la función de células, tejidos y órganos del cuerpo. A menudo las proteínas no pueden plegarse en su configuración normal; en este estado de plegamiento incorrecto, las proteínas pueden volverse tóxicas de alguna manera o pueden perder su función normal. Los ejemplos no limitativos de enfermedades de agregación de proteínas incluyen amiloidosis AL sistémica, enfermedad de Alzheimer, diabetes mellitus tipo 2, enfermedad de Parkinson, encefalopatía espongiforme transmisible, por ejemplo, encefalopatía espongiforme bovina, insomnio familiar letal, enfermedad de Huntington, carcinoma medular de la tiroides, arritmias cardiacas, ateroesclerosis, artritis reumatoide, amiloide medial aórtico, prolactinomas, polineuropatía amiloidea familiar, amiloidosis sistémica no neuropática hereditaria, amiloidosis relacionada con la diálisis, amiloidosis de tipo finlandesa, distrofia reticular de la córnea, angiopatía amiloidea cerebral, angiopatía amiloidea cerebral (tipo islandesa), miositis esporádica por cuerpos de inclusión, esclerosis lateral amiotrófica (ELA), encefalopatías espongiformes o relacionadas con priones, tales como Creutzfeld-Jacob, demencia con cuerpos de Lewy, demencia frontotemporal con parkinsonismo, ataxias espinocerebelosas, ataxia espinocerebelosa, atrofia muscular vertebral y bulbar, atrofia dentatorubro-pálidoluisiana hereditaria, demencia familiar de tipo británica, demencia familiar de tipo danesa, enfermedades localizadas no neuropáticas, tales como en diabetes mellitus tipo II, carcinoma medular de la tiroides, amiloidosis auricular, hemorragia cerebral hereditaria con amiloidosis, prolactinoma hipofisario, amiloidosis localizada por inyección, amiloidosis medial aórtica, distrofia reticular de la córnea hereditaria, amiloidosis de la córnea asociada con triquiasis, cataratas, tumores odontógenos epiteliales calcificantes, proteinosis alveolar pulmonar, miositis con cuerpos de inclusión, amiloidosis cutánea de liquen y amiloidosis sistémica no neuropática, tal como amiloidosis AL, amiloidosis AA, poliserositis familiar recurrente, amiloidosis sistémica senil, polineuropatía amiloidótica hereditaria, amiloidosis relacionada con la hemodiálisis, amiloidosis de ApoAI, amiloidosis de ApoAII, amiloidosis de ApoAIV, amiloidosis hereditaria de tipo finlandesa, amiloidosis por lisozima, amiloidosis por fibrinógeno, angiopatía amiloidea cerebral hereditaria de tipo islandesa, amiloidosis hereditaria y amiloidosis sistémica que se produce en múltiples tejidos, tal como amiloidosis de cadena ligera, y otros diversos trastornos neurodegenerativos.
El término “agregado de proteínas” se refiere a cualquier acumulación de proteínas plegadas de manera anómala que provocan y/o se asocian con la progresión negativa de una enfermedad de agregación de proteínas.
El término “amiloide” se refiere a una forma de agregados de proteínas en la que los agregados forman fibras no ramificadas que se unen a rojo Congo y luego muestran birrefringencia verde cuando se visualizan entre polarizadores cruzados (por ejemplo, véanse Eisenberg y Jucker, 2012. Cell. 148(6):1188-203 y Sipe et al., 2012. Amyloid. 19(4):167-70).
El término “oligómero” se refiere a cualquier acumulación de proteínas plegadas de manera anómala que provocan y/o se asocian con la progresión negativa de una enfermedad de agregación de proteínas y no satisface la definición
de un amiloide. Por ejemplo, los oligómeros de poliglutamina provocan y/o se asocian con la progresión negativa de la enfermedad de Huntington (véase Hoffner y Dijan, 2014. Brain Sci. 4(1): 91-122).
Composición y kit
En un primer aspecto, la presente invención proporciona una composición que comprende un inhibidor de sulfatasa para su uso en el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, en la que el inhibidor de sulfatasa es un compuesto de fórmula (I) tal como se define en las reivindicaciones.
En un segundo aspecto, la presente invención proporciona un kit para su uso en la fabricación de un medicamento para el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, que comprende (i) un inhibidor de sulfatasa; y (ii) un portador y/o diluyente farmacéuticamente aceptable, en el que el inhibidor de sulfatasa es un compuesto de fórmula (I) tal como se define en las reivindicaciones.
En una realización preferida, el kit comprende además un excipiente farmacéuticamente aceptable.
A continuación se proporcionan realizaciones preferidas para los kits y las composiciones de la presente invención. Inhibidor de sulfatasa
El inhibidor de sulfatasa o inhibidor de sulfatasa de hormonas esteroideas es un compuesto de fórmula (I):
en la que:
(a) Ri -R6 se seleccionan independientemente de hidrógeno, halógeno (flúor, cloro, bromo, yodo o astato), hidroxilo, sulfamato (OSO2NH2), alquilo y sales de los mismos;
(b) al menos uno de R1-R6 es un grupo sulfamato; y
dos o más de Ri -R6 se unen entre sí para formar una estructura cíclica adicional.
En una realización preferida, R1 y R2 forman una estructura cíclica adicional que comprende 3-10 carbonos. En una realización preferida, R6 es OSO2NH2. En una realización preferida, el alquilo es un alquilo C1-C6.
En una realización preferida, el inhibidor de sulfatasa es el compuesto de fórmula (II):
Se han divulgado métodos de síntesis de los compuestos anteriores de fórmula (I) y (II) en el documento WO 97/30041. Enfermedad de agregación de proteínas
Los agregados de proteínas tales como amiloides y oligómeros se han asociado con varias enfermedades. En algunos casos, estos agregados de proteínas pueden volverse tóxicos y pueden provocar un daño significativo a células y tejido. Se piensa que esta toxicidad es uno de los factores contribuyentes que provocan y/o contribuyen a la patología de enfermedades de agregación de proteínas.
Además, el procesamiento y plegamiento anómalos de una proteína vinculada a una enfermedad de agregación de proteínas puede comenzar décadas antes de que puedan observarse síntomas externos de la enfermedad de agregación de proteínas (Jack et al., 2010. Lancet Neurol. 9(1):119-28). Por tanto, en una realización preferida, se
eliminan amiloides y/u oligómeros y/o se previene su formación en el paciente y/o animal como resultado de administrar una cualquiera de las composiciones de la presente invención. Además, en una realización preferida, el inhibidor de sulfatasa trata y/o previene la proteotoxicidad en una enfermedad de agregación de proteínas. El término “proteotoxicidad" se refiere a cualquier deterioro de la función celular provocado por el plegamiento incorrecto de una proteína.
Al seleccionar como diana directamente la formación de agregados de proteínas, las composiciones y los kits de la presente invención son capaces de tratar y/o prevenir una enfermedad de agregación de proteínas en pacientes y/o animales que están en los estadios iniciales de una enfermedad de agregación de proteínas, pero todavía no muestran ningún síntoma externo. Además, las composiciones y los kits de la presente invención también tratan los estadios avanzados de una enfermedad de agregación de proteínas tal como se demuestra en el ejemplo 2 y en las figuras 7F y 7G.
En una realización preferida, el paciente y/o animal han experimentado los cambios fisiopatológicos que provocan la agregación de proteínas, pero aún no ha alcanzado el estadio de la enfermedad en el que pueden observarse los síntomas externos. Dicho de otro modo, el paciente y/o animal está en un estadio inicial de la enfermedad. El término “síntoma externo" se refiere a cualquier síntoma que puede observar un médico usando cualquier procedimiento no invasivo.
En una realización preferida, el inhibidor de sulfatasa ralentiza la progresión de una enfermedad de agregación de proteínas inhibiendo la formación de agregados de proteínas y/o el inhibidor de sulfatasa retrasa la aparición de una enfermedad de agregación de proteínas inhibiendo la formación de agregados de proteínas.
En una realización preferida, la enfermedad de agregación de proteínas se selecciona de una lista que consiste en amiloidosis AL sistémica, enfermedad de Alzheimer, diabetes mellitus tipo 2, enfermedad de Parkinson, encefalopatía espongiforme transmisible, por ejemplo, encefalopatía espongiforme bovina, insomnio familiar letal, enfermedad de Huntington, carcinoma medular de la tiroides, arritmias cardiacas, ateroesclerosis, artritis reumatoide, amiloide medial aórtico, prolactinomas, polineuropatía amiloidea familiar, amiloidosis sistémica no neuropática hereditaria, amiloidosis relacionada con la diálisis, amiloidosis de tipo finlandesa, distrofia reticular de la córnea, angiopatía amiloidea cerebral, angiopatía amiloidea cerebral (tipo islandesa), miositis esporádica por cuerpos de inclusión, esclerosis lateral amiotrófica (ELA), encefalopatías espongiformes o relacionadas con priones, tales como Creutzfeld-Jacob, demencia con cuerpos de Lewy, demencia frontotemporal con parkinsonismo, ataxias espinocerebelosas, ataxia espinocerebelosa, atrofia muscular vertebral y bulbar, atrofia dentatorubro-pálidoluisiana hereditaria, demencia familiar de tipo británica, demencia familiar de tipo danesa, enfermedades localizadas no neuropáticas, tales como en diabetes mellitus tipo II, carcinoma medular de la tiroides, amiloidosis auricular, hemorragia cerebral hereditaria con amiloidosis, prolactinoma hipofisario, amiloidosis localizada por inyección, amiloidosis medial aórtica, distrofia reticular de la córnea hereditaria, amiloidosis de la córnea asociada con triquiasis, cataratas, tumores odontógenos epiteliales calcificantes, proteinosis alveolar pulmonar, miositis con cuerpos de inclusión, amiloidosis cutánea de liquen y amiloidosis sistémica no neuropática, tal como amiloidosis AL, amiloidosis AA, poliserositis familiar recurrente, amiloidosis sistémica senil, polineuropatía amiloidótica hereditaria, amiloidosis relacionada con la hemodiálisis, amiloidosis de ApoAI, amiloidosis de ApoAII, amiloidosis de ApoAIV, amiloidosis hereditaria de tipo finlandesa, amiloidosis por lisozima, amiloidosis por fibrinógeno, angiopatía amiloidea cerebral hereditaria de tipo islandesa, amiloidosis hereditaria y amiloidosis sistémica que se produce en múltiples tejidos, tal como amiloidosis de cadena ligera, y otros diversos trastornos neurodegenerativos. Preferiblemente, la enfermedad de agregación de proteínas se selecciona de una lista que consiste en la enfermedad de Alzheimer, la enfermedad de Parkinson y la enfermedad de Huntington. En una realización preferida, la enfermedad de agregación de proteínas no es la enfermedad de Alzheimer ni ningún tipo de cáncer.
En una realización preferida, la enfermedad de agregación de proteínas se selecciona de una lista que consiste en la enfermedad de Alzheimer, la enfermedad de Parkinson y la enfermedad de Huntington. En una realización preferida, se eliminan amiloides y/u oligómeros y/o se previene su formación en pacientes con enfermedad de Alzheimer, enfermedad de Parkinson o enfermedad de Huntington.
En una realización preferida, la enfermedad de agregación de proteínas es una enfermedad de agregación de proteínas localizada en el sistema nervioso central. En una realización preferida, la enfermedad de agregación de proteínas también es una enfermedad neurodegenerativa. El término “enfermedad neurodegenerativa" se refiere a cualquier trastorno caracterizado por la pérdida progresiva de la estructura o función de las neuronas, incluyendo la muerte de neuronas. Por ejemplo, la enfermedad de Alzheimer es un ejemplo de una enfermedad de agregación de proteínas y un ejemplo de una enfermedad neurodegenerativa.
Realizaciones combinadas de inhibidores de sulfatasa y enfermedades de agregación de proteínas
En una realización preferida, el inhibidor de sulfatasa es un compuesto de fórmula (I):
en la que:
(a) R1-R6 se seleccionan independientemente de hidrógeno, halógeno (flúor, cloro, bromo, yodo o astato), hidroxilo, sulfamato (OSO2NH2), alquilo y sales de los mismos;
(b) al menos uno de R1-R6 es un grupo sulfamato; y
dos o más de R1-R6 se unen entre sí para formar una estructura cíclica adicional; y
la enfermedad de agregación de proteínas se selecciona de una lista que consiste en enfermedad de Alzheimer, enfermedad de Huntington y enfermedad de Parkinson.
En una realización preferida, el inhibidor de sulfatasa es STX64 (es decir, el compuesto de fórmula (II)) y la enfermedad de agregación de proteínas se selecciona de una lista que consiste en enfermedad de Alzheimer, enfermedad de Huntington y enfermedad de Parkinson. En una realización preferida, el inhibidor de sulfatasa es STX64 y la enfermedad de agregación de proteínas es enfermedad de Alzheimer. En una realización preferida, el inhibidor de sulfatasa es STX64 y la enfermedad de agregación de proteínas es enfermedad de Huntington. En una realización preferida, el inhibidor de sulfatasa es STX64 y la enfermedad de agregación de proteínas es enfermedad de Parkinson.
Composiciones farmacéuticas
En una realización preferida, la composición es una composición farmacéutica que comprende además un portador y/o diluyente farmacéuticamente aceptable. Preferiblemente, la composición farmacéutica puede comprender además un excipiente farmacéuticamente aceptable.
Una composición farmacéutica tal como se describe en el presente documento también puede contener otras sustancias. Estas sustancias incluyen, pero no se limitan a, crioprotectores, lioprotectores, tensioactivos, agentes de carga, antioxidantes y agentes estabilizantes. En algunas realizaciones, puede liofilizarse la composición farmacéutica.
El término “crioprotector”, tal como se usa en el presente documento, incluye agentes que proporcionan estabilidad a las composiciones contra las agresiones inducidas por congelación. Los crioprotectores también pueden ofrecer protección durante el secado primario y secundario y el almacenamiento del producto a largo plazo. Los ejemplos no limitativos de crioprotectores incluyen azúcares, tales como sacarosa, glucosa, trehalosa, manitol, manosa y lactosa; polímeros, tales como dextrano, hidroxietil-almidón y polietilenglicol; tensioactivos, tales como polisorbatos (por ejemplo, PS-20 o PS-80); y aminoácidos, tales como glicina, arginina, leucina y serina. Se usa generalmente un crioprotector que presenta baja toxicidad en sistemas biológicos.
En una realización, se añade un lioprotector a una composición farmacéutica descrita en el presente documento. El término “lioprotector”, tal como se usa en el presente documento, incluye agentes que proporcionan estabilidad a las composiciones durante el procedimiento de secado por congelación o de deshidratación (ciclos de secado por congelación primario y secundario). Esto ayuda a minimizar la degradación del producto durante el ciclo de liofilización y a mejorar la estabilidad del producto a largo plazo. Los ejemplos no limitativos de lioprotectores incluyen azúcares, tales como sacarosa o trehalosa; un aminoácido, tal como glutamato de monosodio, histidina o glicina no cristalina; una metilamina, tal como betaína; una sal liotrópica, tal como sulfato de magnesio; un poliol, tal como alcoholes de azúcar trihidroxilados o superiores, por ejemplo, glicerina, eritritol, glicerol, arabitol, xilitol, sorbitol y manitol; propilenglicol; polietilenglicol; Pluronics; y combinaciones de los mismos. La cantidad de lioprotector añadida a una composición farmacéutica es generalmente una cantidad que no conduce a una cantidad inaceptable de degradación cuando se liofiliza la composición farmacéutica.
En algunas realizaciones, se incluye un agente de carga en la composición farmacéutica. El término “agente de carga”, tal como se usa en el presente documento, incluye agentes que proporcionan la estructura del producto secado por congelación sin interactuar directamente con el producto farmacéutico. Además de proporcionar una torta farmacéuticamente elegante, los agentes de carga también pueden conferir cualidades útiles con respecto a modificar la temperatura de colapso, proporcionando protección en la congelación-descongelación, y mejorando la estabilidad durante el almacenamiento a largo plazo. Los ejemplos no limitativos de agentes de carga incluyen manitol, glicina, lactosa y sacarosa. Los agentes de carga pueden ser cristalinos (tales como glicina, manitol o cloruro de sodio) o
amorfos (tales como dextrano, hidroxietil-almidón) y se usan generalmente en formulaciones en una cantidad de desde el 0,5% hasta el 10%.
También pueden incluirse otros portadores, excipientes o estabilizadores farmacéuticamente aceptables, tales como los descritos en Remington's Pharmaceutical Sciences 16a edición, Osol, A. Ed. (1980) o en Remington: The Science and Practice of Pharmacy 22a edición, Pharmaceutical press (2012), ISBN-13: 9780857110626, en una composición farmacéutica descrita en el presente documento, siempre que no afecten de manera adversa a las características deseadas de la composición farmacéutica.
Para las composiciones farmacéuticas sólidas, pueden usarse portadores sólidos no tóxicos convencionales que incluyen, por ejemplo, calidades farmacéuticas de manitol, lactosa, almidón, estearato de magnesio, sacarina sódica, talco, celulosa, glucosa, sacarosa, carbonato de magnesio, y similares. Para la disolución para inyección, la composición farmacéutica puede comprender además crioprotectores, lioprotectores, tensioactivos, agentes de carga, antioxidantes, agentes estabilizantes y portadores farmacéuticamente aceptables. Para la administración por aerosol, las composiciones farmacéuticas se administran generalmente en una forma finamente dividida junto con un tensioactivo y un propelente. Por supuesto, el tensioactivo no debe ser tóxico, y es generalmente soluble en el propelente. Representativos de tales agentes son los ésteres o ésteres parciales de ácidos grasos que contienen desde 6 hasta 22 átomos de carbono, tales como los ácidos caproico, octanoico, láurico, palmítico, esteárico, linoleico, linolénico, olestérico y oleico con un alcohol polihidroxilado alifático o su anhídrido cíclico. Pueden emplearse ésteres mixtos, tales como glicéridos mixtos o naturales. También puede incluirse un portador, según se desee, tal como, por ejemplo, lecitina para la administración intranasal. Para los supositorios, pueden incluirse aglutinantes y portadores tradicionales, por ejemplo, polialcalenglicoles o triglicéridos.
En una realización preferida, la composición de la presente invención se prepara para administración oral, sublingual, bucal, intranasal, intravenosa, intramuscular, intraperitoneal y/o mediada por inhalación.
Administración
La composición de la presente invención puede administrarse usando cualquier vía conocida para el experto en la técnica. En una realización preferida, la composición de la presente invención se administra por vía transdérmica, sublingual, intravenosa, intranasal, intracerebroventricular, intraarterial, intracerebral, intramuscular, intraperitoneal, oral o a través de inhalación.
En una realización preferida, la composición de la presente invención se administra por vía transdérmica, sublingual, intravenosa, intraperitoneal, oral o a través de inhalación. Cuando la composición se administra a través de inhalación, la composición puede aerosolizarse y administrarse a través de, por ejemplo, una mascarilla de anestesia.
En una realización preferida, la composición de la presente invención se administra por vía transdérmica, sublingual, intravenosa, subcutánea, oral o a través de inhalación. Preferiblemente, la composición se administra por vía oral o sublingual.
En una realización preferida, la composición comprende una cantidad terapéuticamente eficaz de inhibidor de sulfatasa. El término “cantidad terapéuticamente eficaz” se refiere a una cantidad de inhibidor de sulfatasa en una composición que tiene un efecto terapéutico y que es capaz de tratar y/o prevenir una enfermedad de agregación de proteínas. En una realización preferida, se administra al paciente una dosis de 0,01 a 100 mg/kg del inhibidor de sulfatasa. Preferiblemente, se administra al paciente una dosis de 0,01 a 10 mg/kg. Más preferiblemente, se administra al paciente una dosis de 0,05 a 1 mg/kg.
En una realización preferida, la composición se usa en una terapia de combinación con cualquier otro tratamiento o terapia usados habitualmente para tratar y/o prevenir una enfermedad de agregación de proteínas. En una realización preferida, la composición se usa en una terapia de combinación con donepezilo, rivastigmina, galantamina, memantina, levodopa, carbidopa y/o tetrabenazina.
Las composiciones de la presente invención pueden administrarse una vez o más de una vez. Un experto en la técnica será capaz de determinar la pauta posológica más eficaz para el paciente. Por ejemplo, la pauta posológica más eficaz puede ser una en la que se administra al paciente la composición dos veces al día, una vez al día, una vez cada tres días, una vez a la semana, una vez al mes, una vez cada tres meses, una vez cada seis meses o una vez cada año.
Los siguientes puntos están abarcados por la presente invención.
[1] Una composición que comprende un inhibidor de sulfatasa de fórmula (I) para su uso en el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, en la que:
(i) se eliminan amiloides y/u oligómeros y/o se impide su formación en el paciente y/o animal; y/o
(ii) el inhibidor de sulfatasa trata y/o previene la proteotoxicidad en una enfermedad de agregación de proteínas.
[2] La composición para su uso según el punto [1], en la que el inhibidor de sulfatasa ralentiza la progresión de una enfermedad de agregación de proteínas inhibiendo la formación de agregados de proteínas y/o el inhibidor de sulfatasa retrasa la aparición de una enfermedad de agregación de proteínas inhibiendo la formación de agregados de proteínas.
[3] La composición para su uso según uno cualquiera de los puntos [1]-[2], en la que la enfermedad de agregación de proteínas es una enfermedad de agregación de proteínas localizada en el sistema nervioso central.
[4] La composición para su uso según uno cualquiera de los puntos [1]-[3], en la que se eliminan amiloides y/u oligómeros y/o se previene su formación en pacientes con enfermedad de Alzheimer, enfermedad de Parkinson o enfermedad de Huntington; o en la que la enfermedad de agregación de proteínas es enfermedad de Alzheimer, enfermedad de Parkinson o enfermedad de Huntington.
[5] La composición para su uso según uno cualquiera de los puntos [1]-[4], en la que el inhibidor de sulfatasa es un compuesto de fórmula (I):
en la que:
(a) R1-R6 se seleccionan independientemente de hidrógeno, halógeno, hidroxilo, sulfamato, alquilo y sales de los mismos;
(b) al menos uno de R1-R6 es un grupo sulfamato; y
(c) dos o más de R1-R6 se unen entre sí para formar una estructura cíclica adicional.
[6] La composición para su uso según el punto [5], en la que R1 y R2 forman una estructura cíclica adicional que comprende 3-10 carbonos.
[7] La composición para su uso según uno cualquiera de los puntos [5]-[6], en la que R6 es OSO2NH2.
[8] La composición para su uso según uno cualquiera de los puntos [5]-[7], en la que el inhibidor de sulfatasa es el compuesto de fórmula (II):
[9] La composición para su uso según uno cualquiera de los puntos [1]-[8], en la que la composición es una composición farmacéutica que comprende el inhibidor de sulfatasa según uno cualquiera de los puntos [1]-[8] y un portador y/o diluyente farmacéuticamente aceptable.
[10] La composición para su uso según uno cualquiera de los puntos [1]-[9], en la que la composición se administra por vía oral.
[11] La composición para su uso según uno cualquiera de los puntos [1]-[10], en la que se administra al paciente una dosis de 0,01 a 100 mg/kg, preferiblemente de 0,01 a 10 mg/kg, más preferiblemente de 0,05 a 1 mg/kg.
[12] La composición para su uso según uno cualquiera de los puntos [1]-[11], en la que la composición se usa en una terapia de combinación con donepezilo, rivastigmina, galantamina, memantina, levodopa, carbidopa y/o tetrabenazina.
[13] Un kit para su uso en la fabricación de un medicamento para el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, que comprende (i) un inhibidor de sulfatasa de fórmula (I); y (ii) un portador y/o diluyente farmacéuticamente aceptable.
[14] El kit para su uso según el punto [13], en el que el inhibidor de sulfatasa es un compuesto de fórmula (I):
en la que:
(a) R1-R6 se seleccionan independientemente de hidrógeno, halógeno, hidroxilo, sulfamato, alquilo y sales de los mismos;
(b) al menos uno de R1-R6 es un grupo sulfamato; y
dos o más de R1-R6 se unen entre sí para formar una estructura cíclica adicional.
[15] El kit para su uso según el punto [14], en el que el inhibidor de sulfatasa es el compuesto de fórmula (II):
Ejemplos
Se generaron C. elegans que contenían un alelo inactivado sul-2(gk187) (ID de WormBase: WBVar00145594) mediante el consorcio de atenuación génica de C. elegans (The C. elegans Deletion Mutant Consortium, 2012. G3: GENES, GENOMES, GENETICS. 2(11):1415-1425) y se depositaron en el Caenorhabidits Genetic Center (https://cbs.umn.edu/cgc/home). El alelo sul-2(gk187) consiste en una deleción de 131 aminoácidos que incluye el núcleo catalítico de la sulfatasa. La deleción genera un marco de lectura y sólo se conservan los cuatro primeros aminoácidos de la secuencia original. Por tanto, se considera que sul-2(gk187) es un alelo mutante nulo de sul-2. La lesión mutante está disponible en Wormbase (http://www.wormbase.org/species/c elegans/variation/WBVar00145594#02-45-3).
Ejemplo 1: Efectos de STX64 sobre modelos de nematodo de enfermedades neurodegenerativas
Modelos de C. elegans de enfermedad de Parkinson: se sometió a prueba si las mutaciones de sul-2 o el tratamiento con STX64 (n.° de cat. de Sigma S1950) a una concentración de 1 ^g/ml disuelto en DMSO mejoraba los síntomas provocados por la sobreexpresión de a -sinucleína humana en células musculares (véanse las siguientes referencias para información del modelo usado: van Ham et al., 2008. PLoS Genet. 4(3):e1000027; Gidalevitz et al., 2009. PLoS Genet. 5(3):e1000399; van Ham et al., 2010. Cell. 142(4):601 -12). En particular, se sincronizaron nematodos a 20°C y se monitorizaron cada dos días. En cada día de monitorización, se colocó un nematodo en una gota de tampón M9, permitiendo 30 segundos de acomodación y posteriormente contando el número de cabeceos en un minuto, suponiendo que un cabeceo se produce cuando la cabeza del nematodo cruza el eje axial. N=20 para cada día evaluado y condición (este protocolo se adaptó de Van Ham et al., 2010. Cell. 142: 601-612). Tal como puede observarse en las figuras 1A y 1B, la mutación de sul-2 o el tratamiento con STX64 mejoró significativamente la movilidad.
Además, se sometió a prueba el efecto de la deleción de sul-2 y la administración de STX64 sobre la agregación de a -sinucleína. Para cuantificar los agregados, se transfirieron los animales a almohadillas que comprendían agarosa al 2% y se inmovilizaron usando levamisol 25 mM. Se determinó el número de agregados de a-sinucleína contando los agregados fluorescentes a un aumento de 40x, desde el primer bulbo faríngeo hasta el segundo bulbo. La pérdida de función o inhibición de SUL-2 disminuyó el número de agregados más pequeños mientras que aumentó el número de agregados más grandes de a-sinucleína (véanse las figuras 2 y 3), lo que sugiere una mejor manipulación de los agregados de proteínas en animales con actividad STS reducida (Roberts y Brown, 2015. Biomolecules. 5(2):282-305; Moll et al., 2016. FASEB J. 30(4):1656-69).
En un modelo alternativo de C. elegans de enfermedad de Parkinson que expresa a-sinucleína en neuronas dopaminérgicas marcadas con GFP, se halló que las neuronas dopaminérgicas mueren debido a la toxicidad de la asinucleína (Cooper et al., 2006. Science. 313(5785):324-8). De acuerdo con los hallazgos previos, los mutantes de sul-2 mostraron una supervivencia de neuronas aumentada (véase la figura 4), lo que indica una acción neuroprotectora de la reducción de la actividad STS.
Modelo de C. elegans de enfermedad de Huntington: en un modelo de enfermedad de Huntington que expresa repeticiones de poliglutamina (poliQ) de 35 residuos fusionadas con una proteína fluorescente, se halló que tanto la mutación de sul-2 como la administración de STX64 a una concentración de 1 |ig/ml disuelto en DMSO redujo el número total de agregados (véase la figura 5). Para cuantificar los agregados, se transfirieron los animales a almohadillas que comprendían agarosa al 2% y se inmovilizaron usando levamisol 25 mM. Se determinó el número de agregados de poliQ contando los agregados fluorescentes a un aumento de 10x, desde el primer bulbo faríngeo hasta el segundo bulbo.
Modelo de C. elegans de enfermedad de Alzheimer: también se sometió a prueba un modelo de enfermedad de Alzheimer que expresa proteína p-amiloide en células musculares que provoca la parálisis en el nematodo a medida que envejece. Se sincronizaron los nematodos a 20°C. Se monitorizó la parálisis desde el primer día de la etapa adulta, observando si hay una falta de movimiento después de que se estimulara el nematodo con una púa de platino. Además, para rastrear a los nematodos paralizados, se visualizó que los nematodos tenían un halo de bacterias alrededor de su cabeza ya que la parálisis impide el desplazamiento de la comida. De acuerdo con los datos previos de los inventores, la mutación de sul-2 y el tratamiento con STX64 retrasaron la parálisis (véase la figura 6).
Ejemplo 2: Efectos de STX64 sobre modelos de mamífero de enfermedades neurodegenerativas
Razas de ratones y condiciones: los ratones macho Swiss (CD1) y APP-PS1 (Blanchard et al., 2003. Exp Neurol.
184(1):247-63) usados en este estudio se adquirieron de un proveedor autorizado (Universidad de Sevilla, España) y se habituaron a las condiciones convencionales de alojamiento de animales durante 2-3 semanas (un ciclo de 12 h de luz/oscuridad, temperatura y humedad). Se realizaron estudios de comportamiento con ratones Swiss de 8 semanas, y ratones APP-PS1 de >15 meses en un contexto C57Black. Para los estudios histológicos, se usaron ratones APP-PS1 macho desde 2 hasta >15 meses. Todos los experimentos se realizaron según las directrices de la Unión Europea (2010/63/UE) y según las regulaciones españolas para el uso de animales de laboratorio en experimentos crónicos (RD 53/2013 sobre el cuidado de animales de experimentación: BOE 08/02/2013), y se obtuvo la aprobación de los comités de cuidado animal de la Universidad Pablo de Olavide antes de realizar este estudio.
Infusión local de fármaco en ratones: se anestesió a los ratones con hidrato de cloral al 4% (10 |il/kg de peso corporal, i.p.), y cuando se anestesiaron completamente, se situaron en un marco estereotáctico. Para lesionar el hipocampo, se inyectaron de manera bilateral 0,5 |il de disolución 5 |iM de oligómeros de p-amiloide en el hipocampo dorsal de los ratones en las siguientes coordenadas estereotácticas: AP = -2,2 mm, ML = 1,5 mm, V = -1,5 mm a partir del bregma. Luego se permitió a los ratones recuperarse durante al menos 15 días. A los ratones que también recibieron STX64 se les administraron 0,5 |il de una disolución 1 mg/ml de STX6420 minutos antes de que se les administraran oligómeros de p-amiloide. Se infusionó STX64 en las mismas coordenadas del hipocampo rostral. Se administraron STX64 y oligómeros de p-amiloide a una velocidad de 0,2 |il/min a través de una jeringa de inyección (Hamilton), y se dejaron en el lugar durante 2,5 min tras la infusión.
Administración oral de STX a ratones: se disolvió STX64 en agua potable a 0,005 mg/ml. Se expuso a los ratones a una disolución de STX durante 3-4 semanas y se registró la ingesta de agua cada día durante el tratamiento. La dosis diaria estimada de STX64 era de entre 1-2 mg/kg de peso corporal.
Prueba de evitación pasiva (PA) de pasar al otro lado: los ratones tienen una preferencia innata por entornos oscuros y cerrados. Durante la fase de habituación, se manipuló a los ratones y se dejó que se movieran libremente durante 1 minuto en una cámara (47x18x26 cm, fabricada por Ugo Basile) que se dividió de manera simétrica en un compartimento con luz y uno oscuro (midiendo cada uno 28,5 cmx18 cmx26 cm). Durante la fase de entrenamiento, se confinó brevemente a los ratones en el compartimento con luz y luego, 30 segundos más tarde, se abrió la puerta que separaba los compartimentos oscuro-con luz. Una vez que los ratones entraron en el compartimento oscuro, se cerró la puerta de manera automática y los ratones recibieron una estimulación eléctrica (0,5 mA, 5 s y 0,3 mA, 5 s para ratones Swiss y C57Black, respectivamente) administrada a través del suelo metálico. En las pruebas de retención realizadas en los momentos indicados, los ratones que recordaron la experiencia de descarga eléctrica cuando regresaron al compartimento con luz evitaron, o al menos tardaron más en, entrar en el compartimiento oscuro. Por tanto, la latencia para entrar en el compartimento oscuro (latencia de escape) es una medida de la retención en la memoria o el aprendizaje de información dependiendo de cuánto tiempo después de la sesión de entrenamiento se llevó a cabo la prueba. Se representan la latencia de escape (s), las sesiones de entrenamiento, la memoria a corto y largo plazo (STM y LTM, respectivamente).
Inmunohistoquímica y análisis histológico: para la inmunohistoquímica, se usó un anticuerpo contra p-amiloide (1:3000, Sigma-Aldrich). Se visualizó la tinción del anticuerpo con H2O2 y diaminobencidina, y se mejoró con níquel. Para
minimizar la variabilidad, se analizaron al menos 5 secciones por ratón bajo un microscopio de campo claro DMRB RFY HC (Leica). En cada sección, se cuantificaron el área en porcentaje ocupada por el p-amiloide, la densidad y el tamaño promedio de acumulaciones de p-amiloide usando el software Image-J (descargado como un programa de software libre del dominio público: http://rsb.info.nih.gov/ij/download.html).
Resultados: debido a que STX64 mostró un efecto terapéutico significativo en los modelos de neurodegeneración de C. elegans, se sometió a prueba el efecto de este fármaco sobre alteraciones cognitivas provocadas por la infusión intrahipocámpica de oligómeros de p-amiloide, un modelo de ratón de enfermedad de Alzheimer (EA) aguda (figura 7A). Ambos tratamientos local y sistémico con STX64 revirtieron las deficiencias cognitivas provocadas por la administración intrahipocámpica de oligómeros de p-amiloide.
Para evaluar el efecto del tratamiento oral con STX64 sobre una patología amiloidea en un modelo de ratón de EA crónica, se evaluó el efecto de 3-4 semanas de administración oral de STX64 sobre la deposición de amiloides en la neocorteza (la corteza cerebral y el hipocampo) de ratones APP-PS1 de >15 meses (figura 7B). A la edad de más de 15 meses, que también se asocia con un estadio tardío de deposición de amiloides en la neocorteza del modelo APP-PS1, el análisis del área inmunorreactiva de p-amiloides, la densidad y el tamaño de placa reveló una reducción significativa, excepto para el tamaño de placa en el hipocampo, en los ratones tratados con STX64 (figuras 7C-E). Resulta interesante que, cuando se comparó la deposición de p-amiloides en ratones APP-PS1 viejos (>15 meses) tratados con STX64 con la tasa de deposición normal de amiloides de ratones APP-PS1 sin tratar, se observó que STX64 redujo la deposición de p-amiloides en los ratones APP-PS1 mayores de 15 meses con respecto a lo observado en ratones APP-PS1 de 10-12 meses (figura 7F).
Todos estos resultados indicaron que el tratamiento con STX64 en ratones APP-PS1 reduce la deposición de pamiloides. Para evaluar si la mejora histológica se correlacionaba con la mejora del déficit cognitivo conductual, se comparó la capacidad cognitiva de ratones APP-PS1 mayores de 15 meses tratados con vehículo o STX64 durante 3-4 semanas. Mientras que los ratones APP-PS1 tratados con vehículo mostraron un déficit en la prueba de evitación pasiva (figura 7G), los ratones tratados con STX64 revirtieron por completo las deficiencias cognitivas, alcanzando niveles similares a los de los ratones de tipo natural <15 meses. Todos estos resultados apuntan a que las alteraciones en el metabolismo de p-amiloides provocadas por STX64 reducen las deficiencias cognitivas conductuales inducidas por la acumulación de p-amiloides en modelos de ratón de EA aguda y crónica, lo que indica que es plausible que STX64 y otros inhibidores de sulfatasa puedan usarse para tratar proteopatías.
Ejemplo 3: Efectos de STX64 sobre un modelo de ratón de enfermedad de Huntington
Razas de ratones y condiciones: los ratones R6/1 (Yi Li et al., 2005. NeuroRX. 2(3): 447-464; Mangiarini et al., 1996. Cell. 87(3):493-506) usados en este estudio se compraron a un proveedor autorizado y se habituaron a las condiciones convencionales de alojamiento de los animales durante 2-3 semanas (un ciclo de luz/oscuridad de 12 h, temperatura y humedad). Los estudios de actividad motora se realizaron con ratones R6/1 de 2 meses. Todos los experimentos se realizaron según las directrices de la Unión Europea (2010/63/UE) y según las regulaciones españolas para el uso de animales de laboratorio en experimentos crónicos (RD 53/2013 sobre el cuidado de animales de experimentación: BOE 08/02/2013), y se obtuvo la aprobación de los comités de cuidado animal de la Universidad Pablo de Olavide antes de realizar este estudio.
Administración oral de STX a ratones: se disolvió STX64 en agua potable a 0,005 mg/ml. Se expusieron ratones de 1 mes a una disolución de STX durante 1 mes y se registró la ingesta de agua cada día durante el tratamiento. La dosis diaria estimada de STX64 era de entre 1-2 mg/kg de peso corporal.
Prueba de actividad motora: se sometió a prueba la actividad locomotora en un campo abierto no estresante (56x40x40 cm) durante 15 minutos. La distancia recorrida por los ratones se estimó con el software de videoseguimiento Smart (Panlab).
Resultados: los ratones R6/1 presentan una disminución de su actividad a los 2 meses. Esta disminución de la actividad motora puede evitarse administrando por vía oral STX64 una vez que cumplen 1 mes (véase la figura 8). Este ejemplo proporciona evidencias adicionales de que las composiciones de la presente invención son adecuadas para tratar enfermedades de agregación de proteínas.
Ejemplo 4: Comparación de STX64 con EMATE en un modelo de C. elegans de enfermedad de Alzheimer
Introducción: para determinar el efecto de diferentes inhibidores de sulfatasas esteroideas (STS) sobre la agregación de proteínas, se sometió a prueba EMATE (número CAS: 148672-09-7) en la cepa GMC101, un modelo mejorado de EA en C. elegans (McColl et al., 2012. Mol Neurodegener. 7:57). EMATE, también denominado sulfamato de estrona, es un potente inhibidor irreversible de la estrona sulfatasa (E1-STS) y la deshidroepiandrosterona sulfatasa (DHA-STS), pero con una fuerte actividad estrogénica.
Cepa: GMC101, genotipo: dvIs100 [pCL354(unc-54:DA-Ap1-42) pCL26(mtl-2: GFP)].
Ensayo de parálisis: los gusanos se hicieron crecer a una temperatura no restrictiva de 16°C hasta que alcanzaron la etapa de adulto joven L4. A continuación, la temperatura se cambió a 25°C. Se contó el número de animales paralizados y no paralizados después de una incubación de 18 horas a la temperatura restrictiva de 25°C.
Análisis estadístico: los datos se analizaron usando una prueba de Ji cuadrado bilateral en una tabla de contingencia. El análisis estadístico se realizó usando el software GraphPad Prism (versión 7.00).
Resultados: se sometió a prueba el fenotipo de parálisis dependiente de la temperatura en diferentes contextos y condiciones. La ausencia de sul-2 mejora los síntomas de parálisis en la cepa GMC101 (véase la figura 9A). Se observaron efectos similares para STX64 (véase la figura 9B) y EMATE (véase la figura 9C). Aunque STX64 parecía tener el mayor efecto.
Claims (10)
- REIVINDICACIONESi. Composición que comprende un inhibidor de sulfatasa para su uso en el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, en la que se eliminan amiloides y/u oligómeros y/o se previene su formación en el paciente y/o animal;en la que el inhibidor de sulfatasa es un compuesto de fórmula (I):en la que:(d) Ri-R6se seleccionan independientemente de hidrógeno, halógeno, hidroxilo, sulfamato, alquilo y sales de los mismos;(e) al menos uno de Ri-R6 es un grupo sulfamato; ydos o más de Ri -R6 se unen entre sí para formar una estructura cíclica adicional.
- 2. Composición para su uso según la reivindicación 1, en la que el inhibidor de sulfatasa trata y/o previene la proteotoxicidad en una enfermedad de agregación de proteínas.
- 3. Composición para su uso según la reivindicación 1 ó 2, en la que el inhibidor de sulfatasa ralentiza la progresión de una enfermedad de agregación de proteínas inhibiendo la formación de agregados de proteínas y/o el inhibidor de sulfatasa retrasa la aparición de una enfermedad de agregación de proteínas inhibiendo la formación de agregados de proteínas.
- 4. Composición para su uso según una cualquiera de las reivindicaciones 1-3, en la que la enfermedad de agregación de proteínas es una enfermedad de agregación de proteínas localizada en el sistema nervioso central.
- 5. Composición para su uso según una cualquiera de las reivindicaciones 1-4, en la que se previene la formación de amiloides y/u oligómeros en pacientes con enfermedad de Alzheimer, enfermedad de Parkinson o enfermedad de Huntington; o en la que la enfermedad de agregación de proteínas es enfermedad de Alzheimer, enfermedad de Parkinson o enfermedad de Huntington.
- 6. Composición para su uso según una cualquiera de las reivindicaciones 1-5, en la que R1 y R2 forman una estructura cíclica adicional que comprende 3-10 carbonos.
- 7. Composición para su uso según una cualquiera de las reivindicaciones 1-6, en la que R6 es OSO2NH2.
- 9. Composición para su uso según una cualquiera de las reivindicaciones 1-8, en la que la composición es una composición farmacéutica que comprende el inhibidor de sulfatasa según una cualquiera de las reivindicaciones 1-8 y un portador y/o diluyente farmacéuticamente aceptable.
- 10. Composición para su uso según una cualquiera de las reivindicaciones 1-9, en la que la composición se administra por vía oral.Composición para su uso según una cualquiera de las reivindicaciones 1-10, en la que se administra al paciente una dosis de 0,01 a 100 mg/kg, preferiblemente de 0,01 a 10 mg/kg, más preferiblemente de 0,05 a 1 mg/kg.Composición para su uso según una cualquiera de las reivindicaciones 1-11, en la que la composición se usa en una terapia de combinación con donepezilo, rivastigmina, galantamina, memantina, levodopa, carbidopa y/o tetrabenazina.Medicamento para su uso en el tratamiento y/o la prevención de una enfermedad de agregación de proteínas, en el que el medicamento se fabrica usando un kit que comprende (i) un inhibidor de sulfatasa; y (ii) un portador y/o diluyente farmacéuticamente aceptable;en el que el inhibidor de sulfatasa es un compuesto de fórmula (I):en la que:(c) Ri -R6 se seleccionan independientemente de hidrógeno, halógeno, hidroxilo, sulfamato, alquilo y sales de los mismos;(d) al menos uno de Ri-R6 es un grupo sulfamato; ydos o más de R1-R6 se unen entre sí para formar una estructura cíclica adicional; yen el que se eliminan amiloides y/u oligómeros y/o se previene su formación en el paciente y/o animal. Medicamento para su uso según la reivindicación 13, en el que el inhibidor de sulfatasa es el compuesto de fórmula (II):
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18382439 | 2018-06-19 | ||
| PCT/EP2019/066271 WO2019243453A1 (en) | 2018-06-19 | 2019-06-19 | Compositions for treating and/or preventing protein-aggregation diseases |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2931815T3 true ES2931815T3 (es) | 2023-01-02 |
Family
ID=62716030
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES22186334T Active ES3044215T3 (en) | 2018-06-19 | 2019-06-19 | Compositions for treating and/or preventing protein-aggregation diseases |
| ES19730826T Active ES2931815T3 (es) | 2018-06-19 | 2019-06-19 | Composiciones para tratar y/o prevenir enfermedades de agregación de proteínas |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES22186334T Active ES3044215T3 (en) | 2018-06-19 | 2019-06-19 | Compositions for treating and/or preventing protein-aggregation diseases |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US20210251953A1 (es) |
| EP (2) | EP3810128B1 (es) |
| JP (2) | JP2021528442A (es) |
| CN (2) | CN118845759A (es) |
| AU (1) | AU2019291061B2 (es) |
| BR (1) | BR112020026066A2 (es) |
| CA (1) | CA3103834A1 (es) |
| DK (1) | DK3810128T3 (es) |
| ES (2) | ES3044215T3 (es) |
| HR (1) | HRP20251214T1 (es) |
| HU (1) | HUE073261T2 (es) |
| MX (1) | MX2020014070A (es) |
| PL (2) | PL4094754T3 (es) |
| PT (1) | PT3810128T (es) |
| RS (1) | RS67299B1 (es) |
| SM (1) | SMT202500382T1 (es) |
| WO (1) | WO2019243453A1 (es) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019023247A1 (en) | 2017-07-25 | 2019-01-31 | Immutics, Inc. | TREATMENT OF CANCER BY BLOCKING THE INTERACTION OF TIM-3 AND ITS LIGAND |
| EP3810128B1 (en) * | 2018-06-19 | 2022-08-03 | Universidad Pablo de Olavide | Compositions for treating and/or preventing protein-aggregation diseases |
| JP2022523333A (ja) | 2019-01-30 | 2022-04-22 | トゥルーバインディング,インコーポレイテッド | 抗gal3抗体およびその使用 |
| EP4157338A4 (en) | 2020-05-26 | 2024-11-13 | TrueBinding, Inc. | METHOD FOR TREATING INFLAMMATORY DISEASES BY GALECTIN-3 BLOCKING |
| EP3988096A1 (en) | 2020-10-26 | 2022-04-27 | Universidad Pablo de Olavide OTRI | Sulfated c19 steroid hormones to treat and/or prevent proteotoxicity in protein-aggregation diseases |
| CN112552272B (zh) * | 2020-12-22 | 2023-06-27 | 四川大学 | 香豆素类化合物及其制备方法和应用、药物组合物 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9603325D0 (en) | 1996-02-16 | 1996-04-17 | Imperial College | A compound |
| US5556847A (en) * | 1994-10-27 | 1996-09-17 | Duquesne University Of The Holy Ghost | Methods of effecting memory enhancement mediated by steroid sulfatase inhibitors |
| JP4320089B2 (ja) * | 1999-07-06 | 2009-08-26 | あすか製薬株式会社 | フェニルスルファメート誘導体 |
| DK1311272T3 (da) * | 2000-03-03 | 2007-02-26 | Eisai R&D Man Co Ltd | Hidtil ukendte fremgangsmåder hvor der anvendes cholinesteraseinhibitorer |
| US20060183776A9 (en) * | 2000-03-03 | 2006-08-17 | Eisai Co., Ltd. | Liquid dosage formulations of donepezil |
| GB0511190D0 (en) * | 2005-06-01 | 2005-07-06 | Sterix Ltd | Use |
| ES2514140B1 (es) * | 2013-03-26 | 2015-08-03 | Universidad Pablo De Olavide | Uso del inhibidor de sulfatasas esteroideas STX64 para el tratamiento del envejecimiento |
| US10155936B2 (en) * | 2014-12-05 | 2018-12-18 | An2H Discovery Limited | Parkin ligase activation methods and compositions |
| WO2017075540A1 (en) | 2015-10-30 | 2017-05-04 | Ultragenyx Pharmaceutical Inc. | Methods and compositions for the treatment of amyloidosis |
| US10780094B2 (en) * | 2016-07-22 | 2020-09-22 | New York University | Use of carbonic anhydrase inhibitors for treatment of neurological and psychiatric disorders |
| EP3810128B1 (en) * | 2018-06-19 | 2022-08-03 | Universidad Pablo de Olavide | Compositions for treating and/or preventing protein-aggregation diseases |
-
2019
- 2019-06-19 EP EP19730826.5A patent/EP3810128B1/en active Active
- 2019-06-19 PT PT197308265T patent/PT3810128T/pt unknown
- 2019-06-19 EP EP22186334.3A patent/EP4094754B1/en active Active
- 2019-06-19 PL PL22186334.3T patent/PL4094754T3/pl unknown
- 2019-06-19 HU HUE22186334A patent/HUE073261T2/hu unknown
- 2019-06-19 RS RS20250996A patent/RS67299B1/sr unknown
- 2019-06-19 MX MX2020014070A patent/MX2020014070A/es unknown
- 2019-06-19 ES ES22186334T patent/ES3044215T3/es active Active
- 2019-06-19 DK DK19730826.5T patent/DK3810128T3/da active
- 2019-06-19 HR HRP20251214TT patent/HRP20251214T1/hr unknown
- 2019-06-19 US US17/253,378 patent/US20210251953A1/en not_active Abandoned
- 2019-06-19 SM SM20250382T patent/SMT202500382T1/it unknown
- 2019-06-19 JP JP2020571600A patent/JP2021528442A/ja active Pending
- 2019-06-19 BR BR112020026066-5A patent/BR112020026066A2/pt unknown
- 2019-06-19 CN CN202410870792.1A patent/CN118845759A/zh active Pending
- 2019-06-19 CN CN201980054686.3A patent/CN112601521A/zh active Pending
- 2019-06-19 ES ES19730826T patent/ES2931815T3/es active Active
- 2019-06-19 AU AU2019291061A patent/AU2019291061B2/en active Active
- 2019-06-19 WO PCT/EP2019/066271 patent/WO2019243453A1/en not_active Ceased
- 2019-06-19 CA CA3103834A patent/CA3103834A1/en active Pending
- 2019-06-19 PL PL19730826.5T patent/PL3810128T3/pl unknown
-
2024
- 2024-02-22 JP JP2024025631A patent/JP2024059803A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| HUE073261T2 (hu) | 2026-01-28 |
| EP3810128A1 (en) | 2021-04-28 |
| DK3810128T3 (da) | 2022-10-31 |
| CN118845759A (zh) | 2024-10-29 |
| ES3044215T3 (en) | 2025-11-26 |
| PL3810128T3 (pl) | 2023-01-30 |
| PT3810128T (pt) | 2022-11-09 |
| WO2019243453A1 (en) | 2019-12-26 |
| EP4094754A1 (en) | 2022-11-30 |
| CN112601521A (zh) | 2021-04-02 |
| MX2020014070A (es) | 2021-05-27 |
| JP2024059803A (ja) | 2024-05-01 |
| EP4094754C0 (en) | 2025-08-06 |
| PL4094754T3 (pl) | 2026-01-05 |
| AU2019291061A1 (en) | 2021-02-04 |
| EP3810128B1 (en) | 2022-08-03 |
| JP2021528442A (ja) | 2021-10-21 |
| BR112020026066A2 (pt) | 2021-03-23 |
| EP4094754B1 (en) | 2025-08-06 |
| AU2019291061B2 (en) | 2025-04-10 |
| SMT202500382T1 (it) | 2025-11-10 |
| HRP20251214T1 (hr) | 2025-12-19 |
| US20210251953A1 (en) | 2021-08-19 |
| RS67299B1 (sr) | 2025-11-28 |
| CA3103834A1 (en) | 2019-12-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2931815T3 (es) | Composiciones para tratar y/o prevenir enfermedades de agregación de proteínas | |
| Shen et al. | Control of the structural landscape and neuronal proteotoxicity of mutant Huntingtin by domains flanking the polyQ tract | |
| US12070456B2 (en) | Compositions and methods for treating Helicobacter pylori infection | |
| ES2833408T3 (es) | Tratamiento de enfermedades neurológicas | |
| ITMI20122065A1 (it) | Uso dei correttori del cftr nel trattamento delle patologie del muscolo striato | |
| Liu et al. | Depression exacerbates AD pathology through lactate-dependent activation of microglial Kv1. 3 to promote Aβ-containing exosome spreading | |
| HK40085227A (en) | Compositions for treating and/or preventing protein-aggregation diseases | |
| US20230405020A1 (en) | Sulfated c19 steroid hormones to treat and/or prevent proteotoxicity in protein-aggregation diseases | |
| ES2804541T3 (es) | Compuesto para su uso en la prevención y el tratamiento de enfermedades neurodegenerativas | |
| BR112021005932A2 (pt) | composição farmacêutica, combinação farmacêutica neuroprotetora, inibidor da acetilcolinesterase e agonista receptor de 5-ht4 | |
| Aria et al. | A prodrug targeting CIM6P/IGF2R enhances memory in healthy mice and reverses deficits in an Angelman syndrome mouse model | |
| US20240108637A1 (en) | Epitestosterone sulphate and/or a steroid sulfatase inhibitor for use in treating or improving age related cognitive impairment | |
| ES2896224T3 (es) | Composición farmacéutica que comprende arginina para su uso en el tratamiento de la enfermedad de PolyQ | |
| Préville | Modelling spinal muscular atrophy (sma) in zebrafish | |
| WO2008145789A1 (es) | Uso de compuestos derivados de benzamidina metanosulfonato o su sal farmacéuticamente aceptable, por ejemplo mesilato de imatinib, para preparar un medicamento para el tratamiento de la enfermedad neurodegenerativa de niemann pick de tipo c ( npc). |