ES2925626T3 - Acidos isoxazol-O-carbamoilciclohexílicos como antagonistas de LPA - Google Patents
Acidos isoxazol-O-carbamoilciclohexílicos como antagonistas de LPA Download PDFInfo
- Publication number
- ES2925626T3 ES2925626T3 ES18830675T ES18830675T ES2925626T3 ES 2925626 T3 ES2925626 T3 ES 2925626T3 ES 18830675 T ES18830675 T ES 18830675T ES 18830675 T ES18830675 T ES 18830675T ES 2925626 T3 ES2925626 T3 ES 2925626T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- lpa
- haloalkyl
- mmol
- fibrosis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D261/00—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings
- C07D261/02—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings
- C07D261/06—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members
- C07D261/08—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
- A61K31/422—Oxazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pulmonology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
La presente invención proporciona compuestos de Fórmula (Ia) o (Ib) o un estereoisómero, tautómero o sal o solvato farmacéuticamente aceptable del mismo, en donde X1, X2, X3 y X4 son cada uno independientemente CR6 o N; siempre que no más de dos de X1, X2, X3 o X4 sean N; L es alquileno C1-4 sustituido con 0 a 4 R7; R1 es (-CH2)aR9; a es un número entero de 0 o 1; cada uno de R2 es independientemente halo, ciano, hidroxilo, amino, alquilo C1-6, cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxi, alcoxialquilo, haloalcoxialocilo o haloalcoxi; n es un número entero de 0, 1 o 2; R3 es hidrógeno, alquilo C1-6, alquilo C1-6 deuterado, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi, y el alquilo, por sí mismo o como parte de otro resto, está opcionalmente sustituido con deuterio parcial o completamente; R4 es alquilo C1-10, alquilo deuterado C1-10, haloalquilo C1-10, alquenilo C1-10, cicloalquilo C3-8, arilo de 6 a 10 miembros, heterociclilo de 3 a 8 miembros, -(alquileno C1-6)- (cicloalquilo C3-8), -(alquileno C1-6)-(arilo de 6 a 10 miembros), -(alquileno C1-6)-(heterociclilo de 3 a 8 miembros), o -(alquileno C1-6)- (heteroarilo de 5 a 6 miembros); en el que cada uno de los alquilo, alquileno, alquenilo, cicloalquilo, arilo, heterociclilo y heteroarilo, por sí mismo o como parte de otro resto, está sustituido independientemente con 0 a 3 R8; o alternativamente, R3 y R4, tomados junto con el átomo de N al que están unidos, forman un resto de anillo heterocíclico de 4 a 9 miembros que está sustituido con 0 a 3 R; cada uno de R5 y R6 es independientemente hidrógeno, halo, ciano, hidroxilo, amino, alquilo C1-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; R7 es halo, oxo, ciano, hidroxilo, amino, alquilo C1-6, cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; R8 son cada uno independientemente deuterio, halo, hidroxilo, amino, ciano, alquilo C1-6, alquilo C1-6 deuterado, alquenilo C2-6, alquinilo C2-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi , fenilo o heteroarilo de 5 a 6 miembros; o alternativamente, dos R8, tomados junto con los átomos a los que están unidos, forman un anillo carbocíclico de 3 a 6 miembros o un anillo heterocíclico de 3 a 6 miembros, cada uno de los cuales está sustituido independientemente con 0 a 3 R12; R9 se selecciona de -CN, -C(O)OR10, -C(O)NR11aR11b, -CO-NH-CO-Re, -CO-NH-SO2-Re, -CO-NH-SO-Re, -SO2 -OH, -SO2-NH-CO-Re, -P(O)(OH)2, tetrazol-5-ilo, -CH2-CO-NH-CO-Re, -CH2-CO-NH-SO2-Re, CH2-CO-NH-SO-Re, -CH2-SO2-OH, -CH2-SO2-NH-CO-Re, -CH2-P(O)(OH)2, tetrazol-5-ilmetileno; Re es alquilo C1-6, cicloalquilo C3-6, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo o haloalcoxialquilo; R10 es hidrógeno o alquilo C1-10; y R11a y R11b son cada uno independientemente hidrógeno, alquilo C1-6, cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; y R12 es halo, ciano, hidroxilo, amino, alquilo C1-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi, fenilo o heteroarilo de 5 a 6 miembros. Estos compuestos son inhibidores selectivos del receptor LPA. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Ácidos isoxazol-O-carbamoilcidohexílicos como antagonistas de LPA
Campo de la invención
La presente invención se refiere a nuevos compuestos de isoxazol sustituidos como se definen en las reivindicaciones, a composiciones que los contienen y a estos compuestos para su uso en terapia, por ejemplo, para el tratamiento de trastornos asociados a uno o más de los receptores del ácido lisofosfatídico (LPA).
Antecedentes de la invención
Los lisofosfolípidos son mediadores lipídicos bioactivos derivados de la membrana, de los cuales uno de los más importantes desde el punto de vista médico es el ácido lisofosfatídico (LPA). El LPA no es una entidad molecular única, sino una colección de variantes estructurales endógenas con ácidos grasos de longitudes y grados de saturación variados (Fujiwara et al., J Biol. Chem., 2005, 280, 35038-35050). El esqueleto estructural de los LPA deriva de fosfolípidos basados en glicerol tales como la fosfatidilcolina (PC) o el ácido fosfatídico (PA).
Los LPA son lípidos bioactivos (lípidos de señalización) que regulan varias vías de señalización celular al unirse a la misma clase de receptores acoplados a proteínas G del dominio 7-transmembrana (GPCR) (Chun, J., Hla, T., Spiegel, S., Moolenaar, W., Editores, Lysophospholipid Receptors: Signaling and Biochemistry, 2013, Wiley; ISBN: 978-0-470 56905-4 y Zhao, Y. et al, Biochim. Biophys. Acta (BBA)-Mol. Cell Biol. Of Lipids, 2013, 1831, 86-92). Los receptores LPA conocidos actualmente se designan como LPA1 , LPA2 , LPA3 , LPA4, LPA5 y LPA6 (Choi, J. W., Annu. Rev. Pharmacol. Toxicol., 2010, 50, 157-186; Kihara, Y., et al, Br. J. Pharmacol., 2014, 171, 3575-3594).
Los LPA5 se conocen desde hace mucho tiempo como precursores de la biosíntesis de fosfolípidos en las células eucariotas y procariotas, pero los LPA5 han emergido recientemente como moléculas de señalización que las células activadas producen y liberan rápidamente, especialmente las plaquetas, para influir en las células diana al actuar sobre receptores específicos de la superficie celular (véase, por ejemplo, Moolenaar et al., BioEssays, 2004, 26, 870-881 y van Leewen et al., Biochem. Soc. Trans., 2003, 31, 1209-1212). Además de sintetizarse y procesarse a fosfolípidos más complejos en el retículo endoplasmático, los LPA pueden generarse a través de la hidrólisis de fosfolípidos preexistentes después de la activación celular; por ejemplo, a la posición sn-2 le falta comúnmente un resto de ácido graso debido a la desacilación, dejando solo el hidroxilo sn-1 esterificado a un ácido graso. También, una enzima clave en la producción de LPA, la autotaxina (lysoPLD/NPP2), puede ser el producto de un oncogén, ya que muchos tipos de tumor regulan positivamente la autotaxina (Brindley, D., J. Cell Biochem. 2004, 92, 900-12). Se han informado las concentraciones de LPA en plasma y suero humano así como en el líquido de lavado broncoalveolar (BALF, del inglés "bronchoalveolar lavage fluid") humano, incluyendo determinaciones hechas usando procedimientos de CL/EM y CL/EN/EM sensibles y específicos (Baker et al. Anal. Biochem., 2001,292, 287-295; Onorato et al., J. Lipid Res., 2014, 55, 1784-1796).
El LPA influye en una amplio abanico de respuestas biológicas, que van desde la inducción de la proliferación celular, la estimulación de la migración celular y la retracción de neuritas, el cierre de la unión de huecos e incluso quimiotaxis de moho limo (Goetzl, et al., Scientific World J., 2002, 2, 324-338; Chun, J., Hla, T., Spiegel, S., Moolenaar, W., Editores, Lysophospholipid Receptors: Signaling and Biochemistry, 2013, Wiley; ISBN: 978-0-470-56905-4). El cuerpo de conocimiento sobre la biología de LPA continúa creciendo a medida que se prueban más y más sistemas celulares para determinar la capacidad de respuesta de LPA. Por ejemplo, ahora se sabe que, además de estimular el crecimiento y la proliferación celular, los LPA5 promueven la tensión celular y la unión de fibronectina a la superficie celular, que son eventos importantes en la reparación y regeneración de heridas (Moolenaar et al., BioEssays, 2004, 26, 870-881). Recientemente, la actividad antiapoptótica también se ha atribuido a LPA y recientemente se ha informado que P P A R y es un receptor/diana para L p A (Simon et al., J. Biol. Chem., 2005, 280, 14656-14662).
La fibrosis es el resultado de un proceso de curación de tejido descontrolado que conduce a una acumulación excesiva y una resorción insuficiente de la matriz extracelular (MEC) que finalmente da como resultado el fallo terminal del órgano (Rockey, D. C., et al., New Engl. J. Med., 2015, 372, 1138-1149). Se ha informado que el receptor LPA1 está sobreexpresado en pacientes con fibrosis pulmonar idiopática (IPF). Los ratones de inactivación génica del receptor LPA1 estaban protegidos de la fibrosis pulmonar inducida por bleomicina (Tager et al., Nature Med., 2008, 14, 45-54). Se demostró que el antagonista de LPA1 BMS-986020 reduce significativamente la tasa de disminución de la FVC (capacidad vital forzada) en un ensayo clínico de 26 semanas en pacientes con IPF (Palmer et al., Chest, 2018, 154, 1061-1069). Se demostró que los inhibidores de la ruta de LPA (por ejemplo, un antagonista de LPA1 ) demostraron ser agentes antifibróticos quimiopreventivos en el tratamiento del carcinoma hepatocelular en un modelo de rata (Nakagawa et al., Cancer Cell, 2016, 30, 879-890).
De esta manera, antagonizar el receptor LPA1 puede ser útil para el tratamiento de la fibrosis tales como fibrosis pulmonar, fibrosis hepática, fibrosis renal, fibrosis arterial y esclerosis sistémica y por lo tanto las enfermedades que resultan de la fibrosis (fibrosis pulmonar-fibrosis pulmonar idiopática [IPF, del inglés "Idiopathic Pulmonary Fibrosis"]), fibrosis hepática: esteatohepatitis no alcohólica [NASH, del inglés "Non-alcoholic Steatohepatitis"], fibrosis renalnefropatía diabética, esclerosis sistémica-esclerodermia, etc.).
Los documentos WO2014/145873, WO2011/017350, EP1258484A1 y US2006/0194850A1 desvelan inhibidores de LPA.
Sumario de la invención
La presente invención proporciona nuevos compuestos de isoxazol sustituidos como se definen en las reivindicaciones, que incluyen estereoisómeros, tautómeros y sales farmacéuticamente aceptables o solvatos de los mismos, que son útiles como antagonistas frente a uno o más de los receptores de ácido lisofosfatídico (LPA), en especial el receptor LPA1.
La presente invención también proporciona composiciones farmacéuticas que comprenden un vehículo farmacéuticamente aceptable y al menos uno de los compuestos de la presente invención o estereoisómeros, tautómeros, sales farmacéuticamente aceptables o solvatos de los mismos.
Los compuestos de la invención se pueden usar en el tratamiento de afecciones en que las que el LPA desempeña una función.
Los compuestos de la presente invención se pueden usar en terapia.
Los compuestos de la presente invención se pueden usar para la fabricación de un medicamento para el tratamiento de una afección en la que la inhibición de la actividad fisiológica del LPA es útil, tal como enfermedades en las que participa un receptor de LPA, está implicada en la etiología o patología de la enfermedad o está asociada de otro modo con al menos un síntoma de la enfermedad.
En otro aspecto, la presente invención se refiere a un compuesto de la invención para su uso en un método para tratar la fibrosis de órganos (hígado, riñón, pulmón, corazón y similares así como piel), enfermedades hepáticas (hepatitis aguda, hepatitis crónica, fibrosis hepática, cirrosis hepática, hipertensión portal, falla regenerativa, esteatohepatitis no alcohólica (NASH), hipofunción hepática, trastorno del flujo sanguíneo hepático y similares), enfermedad de las células proliferativas [cáncer (tumor sólido, metástasis tumoral sólida, fibroma vascular, mieloma, mieloma múltiple, sarcoma de Kaposi, leucemia, leucemia linfocítica crónica (CLL) y similares) y metástasis invasiva de células cancerosas y similares], enfermedad inflamatoria (psoriasis, nefropatía, pneumonía y similares), enfermedad del tracto gastrointestinal (síndrome del intestino irritable (IBS), enfermedad inflamatoria del intestino (IBD), secreción pancreática anormal y similares), enfermedad renal, enfermedad asociada al tracto urinario (hiperplasia prostática benigna o síntomas asociados a la enfermedad de la vejiga neuropática, tumor de la médula espinal, hernia de disco intervertebral, estenosis del canal espinal, síntomas derivados de la diabetes, enfermedad del tracto urinario inferior (obstrucción de tracto urinario inferior y similares), enfermedad inflamatoria del tracto urinario inferior, disuria, micción frecuente y similares), enfermedad pancreática, enfermedad asociada a angiogénesis anormal (obstrucción arterial y similares), esclerodermia, enfermedad asociada al cerebro (infarto cerebral, hemorragia cerebral y similares), dolor neuropático, neuropatía periférica y similares, enfermedad ocular (degeneración macular relacionada con la edad (AMD), retinopatía diabética, vitreorretinopatía proliferativa (PVR), penfigoide cicatricial, cicatrización por cirugía de filtración de glaucoma y similares).
En otro aspecto, la presente invención se refiere a un compuesto de la invención para su uso en un método para tratar enfermedades, trastornos o afecciones en los que la activación de al menos un receptor de LPA por LPA contribuye a la sintomatología o progresión de la enfermedad, el trastorno o la afección. Estas enfermedades, trastornos o afecciones se pueden originar a partir de una o más de una etiología genética, iatrogénica, inmunológica, infecciosa, metabólica, oncológica, tóxica, quirúrgica y/o traumática.
En otro aspecto, la presente invención se refiere a un compuesto de la invención para su uso en un método para tratar renal fibrosis, fibrosis pulmonar, fibrosis hepática, fibrosis arterial y esclerosis sistémica, que comprende administrar a un paciente que necesita dicho tratamiento un compuesto de la presente invención como se ha descrito anteriormente.
En un aspecto, la presente invención proporciona compuestos, composiciones farmacéuticas y medicamentos descritos en el presente documento que comprenden antagonistas de los receptores de LPA, en especial antagonistas de LPA1.
Los compuestos de la invención pueden usarse solos, en combinación con otros compuestos de la presente invención o en combinación con uno o más, preferentemente uno o dos agentes distintos.
Estas y otras características de la invención se explicarán de forma extendida conforme continúa la divulgación.
Descripción detallada de la invención
I. COMPUESTOS DE LA INVENCIÓN
En un aspecto, la presente invención proporciona, entre otros, compuestos de fórmula (Ia) o (Ib):
o un estereoisómero, tautómero o sal farmacéuticamente aceptable o solvato del mismo, en donde
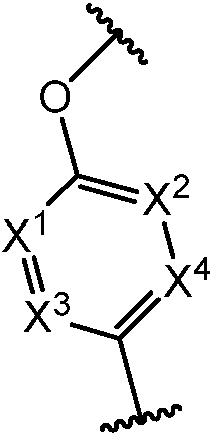
X1, X2, X3 y X4 son cada uno independientemente CR6 o N; con la condición de que no más de dos de X1, X2 , X3 o X4 son N;
L es alquileno C1-4 sustituido con de 0 a 4 R7;
R1 es (-CH2 )aR9;
a es un número entero de 0 o 1;
cada R2 es independientemente halo, ciano, hidroxilo, amino, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxi, alcoxialquilo, haloalcoxialquilo o haloalcoxi;
n es un número entero de 0 , 1 o 2 ;
R3 es hidrógeno, alquilo C1 -6 , alquilo C1-6 deuterado (completa o parcialmente deuterado), haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi y el alquilo, por sí mismo o como parte de otro resto, está opcionalmente sustituido con deuterio de manera parcial o completa;
R4 es alquilo C1 -10 , alquilo C1 -10 deuterado (completa o parcialmente deuterado), haloalquilo C1 -10 , alquenilo C1 -10 , cicloalquilo C3-8, arilo de 6 a 10 miembros, heterociclilo de 3 a 8 miembros, -(alquilen C ^H cicloalquilo C3-8), -(alquilen C1 -6 )-(arilo de 6 a 10 miembros), -(alquilen C ^H heterociclilo de 3 a 8 miembros) o -(alquilen C1-6)-(heteroarilo de 5 a 6 miembros);
en donde cada uno del alquilo, alquileno, alquenilo, cicloalquilo, arilo, heterociclilo y heteroarilo, por sí mismo o como parte de otro resto, está independientemente sustituido con de 0 a 3 R8 ; o, como alternativa, R3 y R4, tomados junto con los átomos de N a los que están unidos, forman un resto anillo heterocíclico de 4 a 9 miembros que está sustituido con de 0 a 3 R8;
R5 y R6 son cada uno independientemente hidrógeno, halo, ciano, hidroxilo, amino, alquilo C1-6 , alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi;
R7 es halo, oxo, ciano, hidroxilo, amino, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi;
cada uno de R8 es independientemente deuterio, halo, hidroxilo, amino, ciano, alquilo C1 -6 , alquilo C1-6 deuterado (completa o parcialmente deuterado), alquenilo C2-6, alquinilo C2-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi, fenilo o heteroarilo de 5 a 6 miembros; o, como alternativa, dos R8 , tomados junto con los átomos a los que están unidos, forman un anillo carbocíclico de 3 a 6 miembros o un anillo heterocíclico de 3 a 6 miembros cada uno de los cuales está independientemente sustituido con de 0 a 3 R12;
R9 se selecciona entre -CN, -C(O)OR10, -C(O)NR11 a R11 b ,
Re es alquilo C1 -6 , cicloalquilo C3-6, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo o haloalcoxialquilo; R10 es hidrógeno o alquilo C1 -10 ; y
R11 a y R11b son cada uno independientemente hidrógeno, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; y R12 es halo, ciano, hidroxilo, amino, alquilo C1-6 , alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi, fenilo o heteroarilo de 5 a 6 miembros;
en donde,
un grupo alquilo, cuando está presente como parte de otro grupo seleccionado entre alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxi, alcoxialquilo, haloalcoxialquilo o haloalcoxi, es un grupo alquilo que tiene de 1 a 10 átomos de carbono.
En una realización de fórmula (la) o (Ib), X1 es CR6, donde R6 es hidrógeno, alquilo C1-4 o halo.
En una cualquiera de las realizaciones anteriores de fórmula (la) o (Ib), L es metileno.
En una cualquiera de las realizaciones anteriores de fórmula (la) o (Ib), n es 0 o 1.
En una cualquiera de las realizaciones anteriores de fórmula (la) o (Ib), R2 es halo.
En una cualquiera de las realizaciones anteriores de fórmula (Ia) o (Ib), a es 0.
En una cualquiera de las realizaciones anteriores de fórmula (Ia) o (Ib), R1 es CO2 H o tetrazolilo.
En una cualquiera de las realizaciones anteriores de fórmula (Ia) o (Ib), R5 es alquilo C1 -4. En una realización, R5 es metilo.
En una cualquiera de las realizaciones anteriores de fórmula (Ia) o (Ib), R4 es alquilo C1 -10 , haloalquilo C1 -10 , cicloalquilo C3-6, -(alquilen C1 -4 )-(cicloalquilo C3-6) o bencilo; en donde el alquilo, alquileno, cicloalquilo y bencilo está cada uno independientemente sustituido con de 0 a 3 R8; y cada R8 es independientemente halo, hidroxilo, amino, ciano, alquilo C1 -6 , alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi o fenilo; o, como alternativa, dos R8, tomados junto con los átomos a los que están unidos, forman un anillo carbocíclico de 3 a 6 miembros. Cada uno del alquilo y el alquileno es independientemente de cadena lineal o ramificada; y el metileno y los restos fenilo del bencilo están cada uno independientemente sustituidos con de 0 a 3 R8.
En una cualquiera de las realizaciones anteriores de fórmula (Ia) o (Ib), el compuesto se representa por la fórmula (IIa) o (IIb):
cada R7a es independientemente hidrógeno, halo, oxo, ciano, hidroxilo, amino, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; f es un número entero de 1, 2 o 3; n es 0 o 1; R3 es hidrógeno, alquilo C1-4 o alquilo C1-4 deuterado (completa o parcialmente deuterado); R5 es alquilo C1 -4 ; y R1, R2, n, R4, X1, X2 , X3 y X4 somo como se ha definido anteriormente. En una realización de fórmula (IIa) o (IIb), R1 es CO2 H.
En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), X1 es CR6 , donde R6 es hidrógeno o alquilo C1 -4. En una realización, X1 es CH o CCH3.
En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), X3 es N.
En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), X1, X2, X3 y X4 son CR6, donde cada R6 es independientemente hidrógeno o alquilo C1 -4. En una realización, X1, X2, X3 y X4 son CH.
En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), el resto
se selecciona entre
cada R6a es independientemente halo, ciano, hidroxilo, amino, alquilo C1-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; y
d es un número entero de 0, 1 o 2.
En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), el resto
se selecciona entre
Cada R6 es independientemente hidrógeno, halo, ciano, hidroxilo, amino, alquilo C1-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi.
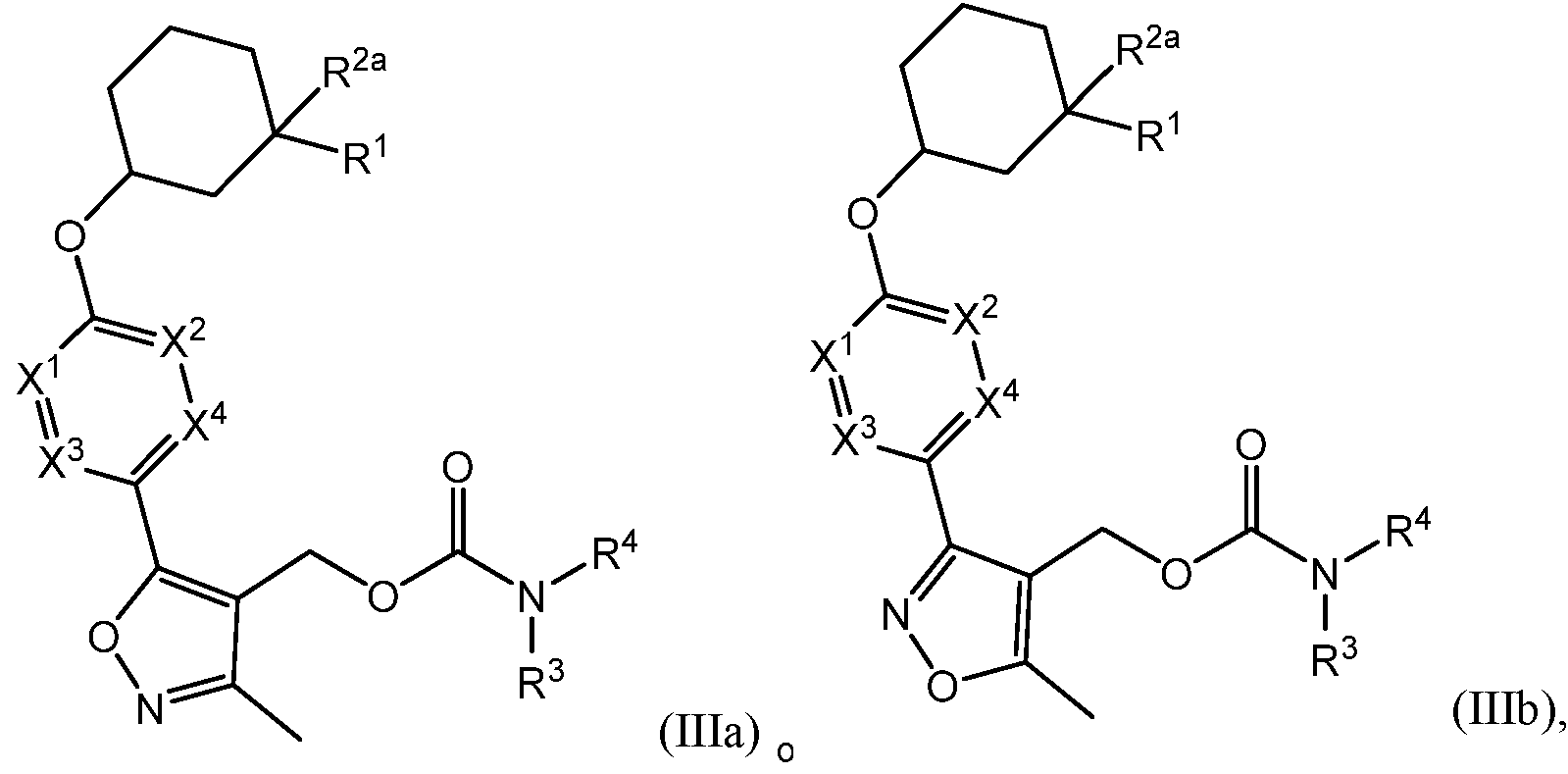
En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), f es 1. En una realización, R7a es hidrógeno. En una cualquiera de las realizaciones anteriores de fórmula (IIa) o (IIb), el compuesto se representa por la fórmula (IIIa) o la fórmula (IIIb):
R2a es hidrógeno o halo (por ejemplo, fluoro);
R3 es hidrógeno, CH3 o CD3; y
R1, R4, X1, X2, X3 y X4 somo como se ha definido anteriormente.
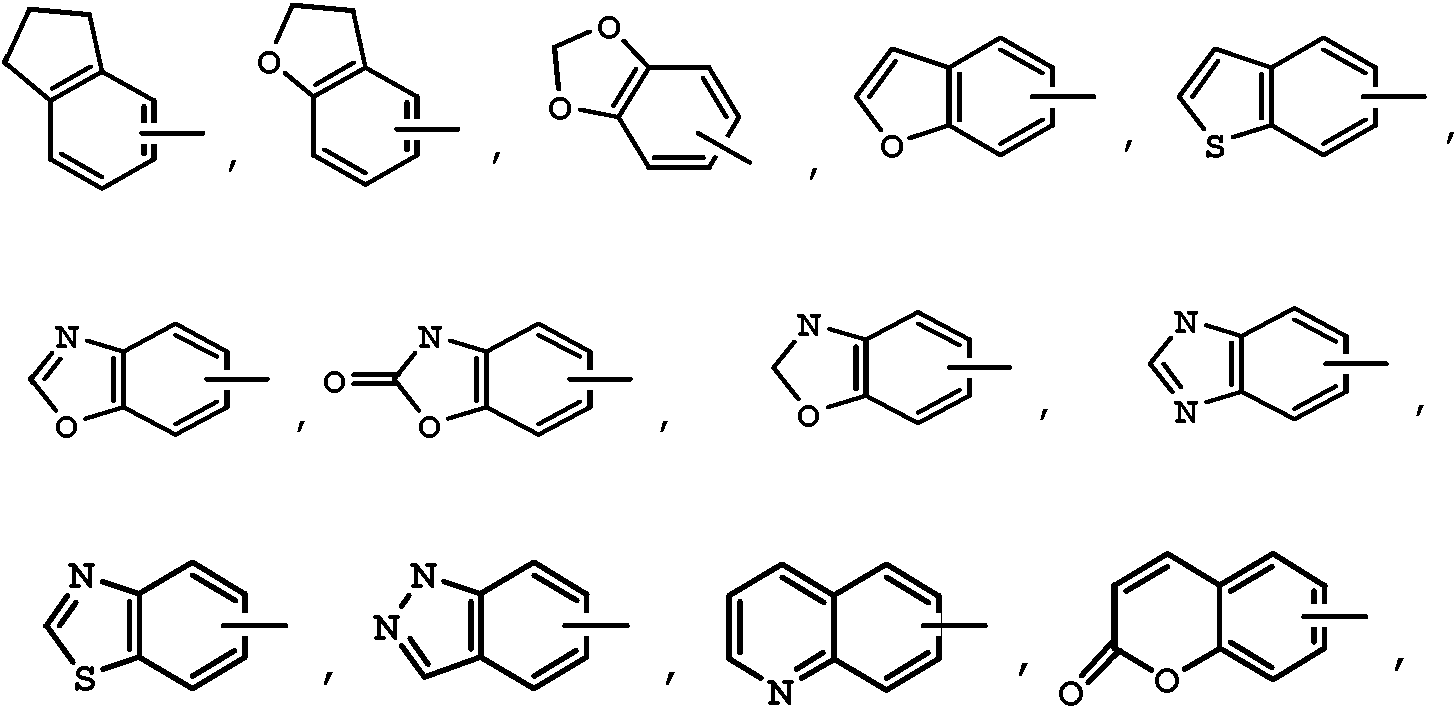
En una cualquiera de las realizaciones anteriores de fórmula (IIIa) o (IIIb), el resto
se selecciona entre
En una cualquiera de las realizaciones anteriores de fórmula (Illa) o (IIIb), R1 es CO2H.
En una cualquiera de las realizaciones anteriores de fórmula (IIIa) o (IIIb), el resto
se selecciona entre
; y R6 es metilo, etilo, flúor o cloro.
En una cualquiera de las realizaciones anteriores de fórmula (IIIa) o (IIIb), R4 es alquilo C3 -10 , haloalquilo C3 -10 , cicloalquilo C3-6, -(alquilen C1 -4 )-(alcoxi C1 -3 ), -(alquilen C1 -4)-(alquilamino C1 -6 ), -(alquilen C1 -4 )-(cicloalquilo C3-6) o -(alquilen C1 -4 )-fenilo; en donde el alquilo, alquileno, cicloalquilo y fenilo está cada uno independientemente sustituido con de 0 a 3 R8 ; y cada R8 es independientemente deuterio, halo, alquilo C1 -6 , cicloalquilo C3-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi. Cada uno del alquilo y el alquileno es independientemente de cadena lineal o ramificada; y el metileno y los restos fenilo del bencilo están cada uno independientemente sustituidos con de 0 a 3 R8
En una cualquiera de las realizaciones anteriores de fórmula (IIIa) o (IIIb), R4 es alquilo C3 -10 , haloalquilo C3 -10 ,
ciclobutilo, ciclopentilo, -(CH2 )1 -2 -(alquilamino C2-6), -C(HR8a)1 -2 -ciclopropilo, -C(HR8a)-ciclobutilo, -C(HR8a)-pentilo o -C(HR8)-fenilo; en donde el ciclopropilo, ciclobutilo, ciclopentilo y fenilo está cada uno independientemente sustituido con de 0 a 3 R8 ; cada R8a es independientemente hidrógeno, metilo, ciclopropilo; y cada R8 es independientemente halo, alquilo C1-4 o haloalquilo C1 -4.
En una realización de la presente invención, el compuesto se selecciona entre uno cualquiera de los ejemplos que se describen en la memoria descriptiva o un estereoisómero, un tautómero o una sal o solvato farmacéuticamente aceptable del mismo.
En otra realización de la presente invención, el compuesto se selecciona entre los ejemplos 1 a 76 que se describen en la memoria descriptiva o un estereoisómero, un tautómero o una sal o solvato farmacéuticamente aceptable del mismo.
En otra realización de la presente invención, el compuesto se selecciona entre los ejemplos 1 a 46 que se describen en la memoria descriptiva o un estereoisómero, un tautómero o una sal o solvato farmacéuticamente aceptable del mismo.
En una realización, los compuestos de la presente invención tienen valores de CI50 de hLPA1 < 5000 nM, usando el ensayo de antagonista funcional de LPA1 ; en otra realización, los compuestos de la presente invención tienen valores de CI 50 de hLPA1 < 1000 nM; en otra realización, los compuestos de la presente invención tienen valores de CI50 de hLPA1 < 500 nM; en otra realización, los compuestos de la presente invención tienen valores de CI50 de hLPA1 < 200 nM; en otra realización, los compuestos de la presente invención tienen valores de CI50 de hLPA1 < 100 nM; en otra realización, los compuestos de la presente invención tienen valores de CI50 de hLPA1 < 50 nM.
II. OTRAS REALIZACIONES DE LA INVENCIÓN
En algunas realizaciones, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, es un antagonista de al menos un receptor de LPA. En algunas realizaciones, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, es un antagonista de LPA1. En algunas realizaciones, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, es un antagonista de LPA2. En algunas realizaciones, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, es un antagonista de LPA3.
En algunas realizaciones, se presentan en el presente documento compuestos seleccionados entre tautómeros, sales farmacéuticamente aceptables o solvatos de un compuesto de fórmula (Ia) o (Ib).
En otra realización, la presente invención proporciona una composición que comprende al menos uno de los compuestos de la presente invención o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo.
En otra realización, la presente invención proporciona una composición farmacéutica, que comprende un vehículo farmacéuticamente aceptable y una cantidad terapéuticamente eficaz de al menos uno de los compuestos de la presente invención o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo.
En otra realización, la presente invención proporciona una composición farmacéutica que comprende además un agente o agentes terapéuticos adicionales.
En otra realización, la presente invención proporciona un compuesto de la invención para su uso en un método para el tratamiento de una afección asociada a fibrosis mediada por el receptor de LPA, que comprende administrar a un paciente que necesita dicho tratamiento una cantidad terapéuticamente eficaz de al menos uno de los compuestos de la presente invención o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo. Tal como se usa en el presente documento, el término "paciente" incluye todas las especies de mamíferos.
En otra realización, la presente invención proporciona un compuesto de la invención para su uso en un método para tratar una enfermedad, trastorno o afección asociada a desregulación del receptor 1 del ácido lisofosfatídico (LPA1 ) en un paciente que lo necesita, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de la presente invención o un estereoisómero, tautómero o una sal farmacéuticamente aceptable o solvato del mismo, al paciente. En una realización, la enfermedad, trastorno o afección está relacionada con fibrosis, rechazo de trasplante, cáncer, osteoporosis o trastornos inflamatorios. En una realización, la fibrosis patológica es fibrosis pulmonar, hepática, renal, cardíaca, dérmica, ocular o pancreática. En una realización, la enfermedad, trastorno o afección es fibrosis pulmonar idiopática (IPF), esteatohepatitis no alcohólica (NASH), esteatosis hepática no alcohólica (NAFLD), enfermedad renal crónica, enfermedad renal diabética y esclerosis sistémica. En una realización, el cáncer es de vejiga, sangre, hueso, cerebro, mama, sistema nervioso central, cuello del útero, colon, endometrio, esófago, vesícula biliar, genitales, tracto genitourinario, cabeza, riñón, laringe, hígado, pulmón, tejido muscular, cuello, mucosa oral o nasal, ovario, páncreas, próstata, piel, bazo, intestino delgado, intestino grueso, estómago, testículo o tiroides.
En otra realización, la presente invención proporciona un compuesto de la invención para su uso en un método para tratar fibrosis en un mamífero, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de la presente invención o un estereoisómero, tautómero o una sal farmacéuticamente aceptable o solvato del mismo, al mamífero que lo necesita. En una realización, la fibrosis es fibrosis pulmonar idiopática (IPF), esteatohepatitis no alcohólica (NASH), enfermedad renal crónica, enfermedad renal diabética y esclerosis sistémica.
En otra realización, la presente invención proporciona un compuesto de la invención para su uso en un método para tratar fibrosis pulmonar (fibrosis pulmonar idiopática), asma, enfermedad pulmonar obstructiva crónica (EPOC), fibrosis renal, lesión renal aguda, enfermedad renal crónica, fibrosis hepática (esteatohepatitis no alcohólica), fibrosis de la piel, fibrosis del intestino, cáncer de mama, cáncer de páncreas, cáncer de ovario, cáncer de próstata, glioblastoma, cáncer de huesos, cáncer de colon, cáncer de intestino, cáncer de cabeza y cuello, melanoma, mieloma múltiple, leucemia linfocítica crónica, dolor por cáncer, metástasis tumoral, rechazo de trasplante de órgano, esclerodermia, fibrosis ocular, degeneración macular relacionada con la edad (AMD), retinopatía diabética, enfermedad vascular por colágeno, aterosclerosis, fenómeno de Raynaud o dolor neuropático en un mamífero, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de la presente invención o un estereoisómero, tautómero o una sal farmacéuticamente aceptable o solvato del mismo, al mamífero que lo necesita.
Tal como se usa en el presente documento, "tratar" o "tratamiento" cubre el tratamiento de un estado patológico en un mamífero, en particular en un ser humano e incluyen: (a) inhibir el estado patológico, es decir, detener su desarrollo; y/o (b) aliviar la patología, es decir, provocar la regresión del estado patológico. Tal como se usa en el presente documento, "tratar" o "tratamiento" también incluye el tratamiento protector de un estado patológico para reducir y/o minimizar el riesgo y/o la reducción del riesgo de recurrencia de un estado patológico mediante la administración a un paciente de una cantidad terapéuticamente eficaz de al menos uno de los compuestos de la presente invención o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo. Los pacientes se pueden seleccionar para dicha terapia protectora basándose en factores que se sabe que aumentan el riesgo de sufrir un estado patológico clínico en comparación con la población general. Para el tratamiento protector, las afecciones del estado patológico clínico pueden estar o no presentes todavía. El tratamiento protector se puede dividir en (a) profilaxis primaria y (b) profilaxis secundaria. La profilaxis primaria se define como el tratamiento para reducir o minimizar el riesgo de un estado patológico en un paciente que todavía no ha presentado un estado patológico clínico, mientras que la profilaxis secundaria se define como minimizar o reducir el riesgo de una recurrencia o segunda ocurrencia del mismo o similar estado patológico clínico.
La presente invención se puede realizar de otras formas específicas. Esta invención abarca todas las combinaciones de los aspectos preferidos de la invención indicados en el presente documento. Se entiende que cualquiera y todas las realizaciones de la presente invención se pueden tomar en conjunto con cualquier otra realización o realizaciones para describir realizaciones adicionales. También debe entenderse que cada elemento individual de las realizaciones es su propia realización independiente. Además, cualquier elemento de una realización tiene por objeto combinarse con cualquiera y todos los otros elementos de cualquier realización para describir una realización adicional.
III. QUÍMICA
A lo largo de la memoria descriptiva y las reivindicaciones adjuntas, una fórmula o nombre químico dado abarcará todos los estereoisómeros e isómeros ópticos y racematos del mismo cuando existan dichos isómeros. A menos que se indique de otro modo, todas las formas quirales (enantioméricas y diastereoméricas) y racémicas están dentro del alcance de la invención. Muchos isómeros geométricos de dobles enlaces C=C, dobles enlaces C=N, sistemas de anillos y similares pueden estar presentes también en los compuestos y todos estos isómeros estables están contemplados en la presente invención. Se describen los isómeros geométricos cis y trans (o E y Z) de los compuestos de la presente invención y se pueden aislar en forma de una mezcla de isómeros o como formas isoméricas separadas. Los presentes compuestos se pueden aislar en formas ópticamente activas o racémicas. Las formas ópticamente activas se pueden preparar por resolución de las formas racémicas o mediante síntesis a partir de materiales de partida ópticamente activos. Cuando se preparan productos enantioméricos o diastereoméricos, estos se pueden separar por métodos convencionales, por ejemplo, por cromatografía o cristalización fraccionada. Dependiendo de las condiciones de proceso los productos finales de la presente invención se obtienen tanto en forma libre (neutral) como de sal. Tanto la forma libre como las sales de estos productos finales están dentro del alcance de la invención. Si se desea, una forma de un compuesto se puede convertir en otra forma. Una base libre o ácida se puede convertir en una sal; una sal se puede convertir en el compuesto libre o en otra sal; una mezcla de compuestos isoméricos de la presente invención se puede separar en los isómeros individuales. Los compuestos de la presente invención, las formas libres y las sales de los mismos, pueden existir en múltiples formas tautoméricas, en las que los átomos de hidrógeno se transponen a otras partes de las moléculas y los enlaces químicos entre los átomos de las moléculas se reordenan en consecuencia. Debe entenderse que todas las formas tautoméricas, en la medida en que puedan existir, se incluyen dentro de la invención.
El término "estereoisómero" se refiere a isómeros de constitución idéntica que difieren en la disposición de sus átomos en el espacio. Los enantiómeros y diastereómeros son ejemplos de estereoisómeros. El término "enantiómero" se refiere a uno de un par de especies moleculares que son imágenes especulares una de otra y no son superponibles. El término "diastereómero" se refiere a estereoisómeros que no son imágenes especulares. El término "racemato" o
"mezcla racémica" se refiere a una composición compuesta de cantidades equimolares de dos especies enantioméricas, en donde la composición está desprovista de actividad óptica.
Los símbolos "R" y "S" representan la configuración de los sustituyentes alrededor de un átomo o átomos quirales.
Los descriptores isoméricos "R" y "S" se usan tal como se describe en el presente documento para indicar la configuración o configuraciones de un átomo con respecto a la molécula central y se pretende que se usen como se define en la bibliografía (IUPAC Recommendations 1996, Pure and Applied Chemistry, 68:2193-2222 (1996)).
El término "quiral" se refiere a la característica estructural de una molécula que hace imposible que se superponga sobre su imagen especular. El término "homoquiral" se refiere a un estado de pureza enantiomérica. El término "actividad óptica" se refiere al grado al cual una molécula homoquiral o una mezcla no racémica de moléculas quirales rota un plano de luz polarizada.
Tal como se usa en el presente documento, el término "alquilo" o "alquileno" pretende incluir grupos hidrocarburo alifáticos saturados, tanto de cadena ramificada como lineal, que tienen el número especificado de átomos de carbono.
Mientras que "alquilo" representa un radical alifático, saturado, monovalente (tal como etilo), "alquileno" representa un radical alifático, saturado, bivalente (tal como etileno). Por ejemplo, "alquilo C1 a C10" o "alquilo C1 -10" pretende incluir grupos alquilo C1 , C2 , C3 , C4, C5 , Ce , C7 , Ce, C9 y C10. "Alquileno C1 a C10" o "alquileno C1 -10", pretende inclu alquileno C1 , C2 , C3 , C4, C5, Ce , C7 , Ce, C9 y C10. Además, por ejemplo, "alquilo C1 a Ce" o "alquilo C1-6" representa alquilo que tiene de 1 a 6 átomos de carbono; y "alquileno C1 a C6" o "alquileno C1-6" representa alquileno que tiene de 1 a 6 átomos de carbono; y "alquilo C1 a C4" o "alquilo C1-4" representa alquilo que tiene de 1 a 4 átomos de carbono;
y "alquileno C1 a C4" o "alquileno C1-4" representa alquileno que tiene de 1 a 4 átomos de carbono. El grupo alquilo puede estar sin sustituir o sustituido con al menos un hidrógeno que se reemplaza por otro grupo químico. Los ejemplos de grupos alquilo incluyen, pero sin limitación, metilo (Me), etilo (Et), propilo (por ejemplo, n-propilo e isopropilo), butilo
(por ejemplo, n-butilo, isobutilo, t-butilo) y pentilo (por ejemplo, n-pentilo, isopentilo, neopentilo). Cuando se usa "alquilo
C0" o "alquileno C0", se pretende indicar un enlace directo. Además, el término "alquilo", por sí mismo o como parte de otro grupo, tal como alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxi, alcoxialquilo, haloalcoxialquilo y haloalcoxi, puede ser un alquilo que tiene de 1 a 4 átomos de carbono o de 1 a 6 átomos de carbono o de 1 a 10 átomos de carbono.
"Heteroalquilo" se refiere a un grupo alquilo donde uno o más átomos de carbono se han reemplazado con un heteroátomo, tal como, O, N o S. Por ejemplo, si el átomo de carbono del grupo alquilo que está unido a la molécula precursora se reemplaza con un heteroátomo (por ejemplo, O, N o S) los grupos heteroalquilo resultantes son, respectivamente, un grupo alcoxi (por ejemplo, -OCH3 , etc.), un alquilamino (por ejemplo, -NHCH3 , -N(CH3 )2 , etc.) o un grupo tioalquilo (por ejemplo, -SCH3). Si el átomo de carbono no terminal del grupo alquilo que no está unido a la molécula precursora se reemplaza con un heteroátomo (por ejemplo, O, N o S) y los grupos heteroalquilo resultantes son, respectivamente, un alquil éter (por ejemplo, -CH2CH2-O-CH3 , etc.), un alquilaminoalquilo (por ejemplo, -CH2 NHCH3 , -CH2 N(CH3)2 , etc.) o un tioalquil éter (por ejemplo, -CH2-S-CH3). Si un átomo de carbono del grupo alquilo se reemplaza con un heteroátomo (por ejemplo, O, N o S), los grupos heteroalquilo resultantes son, respectivamente, un grupo hidroxialquilo (por ejemplo, -CH2CH2-OH), un grupo aminoalquilo (por ejemplo, -CH2 NH2 ) o un grupo alquil tiol (por ejemplo, -CH2CH2-SH). Un grupo heteroalquilo puede tener, por ejemplo, de 1 a 20 átomos de carbono, de 1 a 10 átomos de carbono o de 1 a 6 átomos de carbono. Un grupo heteroalquilo C1-C6 significa un grupo heteroalquilo que tiene de 1 a 6 átomos de carbono.
"Alquenilo" o "alquenileno" pretende incluir cadenas hidrocarburo de configuración tanto lineal o ramificada que tienen el número especificado de átomos de carbono y uno o más, preferentemente uno o dos, dobles enlaces carbonocarbono que pueden aparecer en cualquier punto estable a lo largo de la cadena. Por ejemplo, "alquenilo C2 a C6" o "alquenilo C2-6" (o alquenileno), pretende incluir los grupos alquenilo C2 , C3, C4, C5 y C6. Los ejemplos de alquenilo incluyen, pero sin limitación, etenilo, 1-propenilo, 2-propenilo, 2-butenilo, 3-butenilo, 2-pentenilo, 3-pentenilo, 4-pentenilo, 2-hexenilo, 3-hexenilo, 4-hexenilo, 5-hexenilo, 2-metil-2-propenilo y 4-metil-3-pentenilo.
"Alquinilo" o "alquinileno" pretende incluir cadenas hidrocarburo de configuración tanto lineal como ramificada que tienen uno o más, preferentemente de uno a tres, triples enlaces carbono-carbono que pueden aparecer en cualquier punto estable a lo largo de la cadena. Por ejemplo, "alquinilo C2 a C6" o "alquinilo C2-6" (o alquinileno), pretende incluir los grupos alquinilo C2 , C3 , C4, C5 y C6 ; tales como etinilo, propinilo, butinilo, pentinilo y hexinilo.
Tal como se usa en el presente documento, "arilalquilo" (también conocido como aralquilo), "heteroarilalquilo", "carbociclilalquilo" o "heterociclilalquilo" se refiere a un radical alquilo acíclico en el que uno de los átomos de hidrógeno unido a un átomo de carbono, normalmente un átomo de carbono terminal o sp3, se reemplaza con un radical arilo, heteroarilo, carbociclilo o heterociclilo, respectivamente. Los grupos arilalquilo habituales incluyen, pero sin limitación, bencilo, 2-feniletan-1-ilo, naftilmetilo, 2-naftiletan-1-ilo, naftobencilo, 2-naftofeniletan-1-ilo y similares. El grupo arilalquilo, heteroarilalquilo, carbociclilalquilo o heterociclilalquilo puede comprender de 4 a 20 átomos de carbono y de 0 a 5 heteroátomos, por ejemplo, el resto alquilo puede contener de 1 a 6 átomos de carbono.
El término "bencilo", tal como se usa en el presente documento, se refiere a un grupo metilo en el que uno de los átomos de hidrógeno se reemplaza por un grupo fenilo, en donde dicho grupo fenilo puede estar opcionalmente
sustituido con de 1 a 5 grupos, preferentemente de 1 a 3 grupos, OH, OCH3 , Cl, F, Br, I, CN, NO2 , NH2 , N(CH3 )H, N(CH3 )2 , CF3 , OCF3 , C(=O)CH3, SCH3, S(=O)CH3 , S(=O)2CH3 , CH3, CH2CH3 , CO2 H y CO2CH3. "Bencilo" también se puede representar por la fórmula "Bn".
El término "alcoxi" o "alquiloxi" se refiere a un grupo -O-alquilo. "Alcoxi C1 a C6" o "alcoxi C1-6" (o alquiloxi), pretende incluir los grupos alcoxi C1 , C2 , C3, C4, C5 y C6. Los ejemplos de grupos alcoxi incluyen, pero sin limitación, metoxi, etoxi, propoxi (por ejemplo, n-propoxi e isopropoxi) y f-butoxi. De manera análoga, "alquiltio" o "tioalcoxi" representa un grupo alquilo tal como se ha definido anteriormente con el número indicado de átomos de carbono unidos a través de un puente de azufre; por ejemplo, metil-S- y etil-S-.
El término "alcanoílo" o "alquilcarbonilo" como se usa en el presente documento, solo o como parte de otro grupo, se refiere a alquilo unido a un grupo carbonilo. Por ejemplo, alquilcarbonilo puede estar representado por alquil-C(O)-. "Alquilcarbonilo C1 a C6" (o alquilcarbonilo), pretende incluir los grupos alquil-C(O)- C1 , C2 , C3, C4, C5 y C6.
El término "alquilsulfonilo" o "sulfonamida" como se usa en el presente documento, solo o como parte de otro grupo, se refiere a alquilo o amino unido a un grupo sulfonilo. Por ejemplo, el alquilsulfonilo puede estar representado por -S(O)2 R', mientras que la sulfonamida puede estar representada por -S(O)2 NRcRd. R' es alquilo C1 a C6; y Rc y Rd son como se definen a continuación para "amino".
El término "carbamato" como se usa en el presente documento, solo o como parte de otro grupo, se refiere a oxígeno unido a un grupo amido. Por ejemplo, el carbamato puede estar representado por N(RcRd)-C(O)-O-, y Rc y Rd son como se definen a continuación para "amino".
El término "amido" como se usa en el presente documento, solo o como parte de otro grupo, se refiere a amino unido a un grupo carbonilo. Por ejemplo, amido puede estar representado por N(RcRd)-C(O)-, y Rc y Rd son como se definen a continuación para "amino".
El término "amino" se define como -NRc1Rc2, en donde Rc1 y Rc2 son independientemente H o alquilo C1 -6 ; o, como alternativa, Rc1 y Rc2, tomados junto con los átomos a los que están unidos, forman un anillo heterocíclico de 3 a 8 miembros que está opcionalmente sustituido con uno o más grupos seleccionados entre halo, ciano, hidroxilo, amino, oxo, alquilo C1 -6 , alcoxi y aminoalquilo. Cuando Rc1 o Rc2 (o ambos) es alquilo C1 -6 , el grupo amino también se puede denominar alquilamino. Los ejemplos de grupo alquilamino incluyen, sin limitación, metilamino, etilamino, propilamino, isopropilamino y similares. En una realización, amino es -NH2.
El término "aminoalquilo" se refiere a un grupo alquilo en el que uno de los átomos de hidrógeno está reemplazado por un grupo amino. Por ejemplo, aminoalquilo puede estar representado por N(Rc1Rc2)-alquileno-. "Aminoalquilo C1 a C6" o "C1-6" (o aminoalquilo), pretende incluir los grupos aminoalquilo C1 , C2 , C3 , C4, C5 y C6.
El término "halógeno" o "halo" como se usa en el presente documento, solo o como parte de otro grupo, se refiere a cloro, bromo, flúor y yodo, prefiriéndose cloro o flúor.
"Haloalquilo" pretende incluir grupos hidrocarburo alifáticos saturados, de cadena tanto ramificada como lineal, que tienen el número especificado de átomos de carbono, sustituidos con uno o más halógenos. "haloalquilo C1 a C6" o "haloalquilo C1-6" (o haloalquilo), pretende incluir los grupos haloalquilo C1 , C2 , C3, C4, C5 y C6. Los ejemplos de haloalquilo incluyen, pero sin limitación, fluorometilo, difluorometilo, trifluorometilo, triclorometilo, pentafluoroetilo, pentacloroetilo, 2,2,2-trifluoroetilo, heptafluoropropilo y heptacloropropilo. Los ejemplos de haloalquilo también incluyen "fluoroalquilo", lo que pretende incluir grupos hidrocarburo alifáticos saturados, tanto de cadena ramificada como lineal, que tienen el número especificado de átomos de carbono, sustituido con 1 o más átomos de flúor. El término "polihaloalquilo", como se usa en el presente documento, se refiere a un grupo "alquilo" como se ha definido anteriormente que incluye de 2 a 9, preferentemente de 2 a 5, sustituyentes halo, tales como F o Cl, preferentemente F, tal como polifluoroalquilo, por ejemplo, CF3CH2 , CF3 o CF3CF2CH2.
"Haloalcoxi" o "haloalquiloxi" representa un grupo haloalquilo tal como se ha definido anteriormente con el número indicado de átomos de carbono unido a través de un puente de oxígeno. Por ejemplo, "haloalcoxi C1 a C6" o "haloalcoxi C1-6", pretende incluir los grupos haloalcoxi C1 , C2 , C3, C4, C5 y C6. Los ejemplos de haloalcoxi incluyen, pero sin limitación, trifluorometoxi, 2,2,2-trifluoroetoxi y pentafluorotoxi. De manera análoga, "haloalquiltio" o "tiohaloalcoxi" representa un grupo haloalquilo tal como se ha definido anteriormente con el número indicado de átomos de carbono unidas a través de un enlace de azufre; por ejemplo, trifluorometil-S- y pentafluoroetil-S-. El término "polihaloalquiloxi", como se usa en el presente documento, se refiere a un grupo "alcoxi" o "alquiloxi" como se ha definido anteriormente que incluye de 2 a 9, preferentemente de 2 a 5, sustituyentes halo, tales como F o Cl, preferentemente F, tal como polifluoroalcoxi, por ejemplo, CF3CH2O, CF3O o CF3CF2CH2O.
"Hidroxialquilo" pretende incluir grupos hidrocarburo alifáticos saturados, tanto de cadena ramificada como lineal, que tienen el número especificado de átomos de carbono, sustituido con 1 o más hidroxilos (OH). "Hidroxialquilo C1 a C6" (o hidroxialquilo), pretende incluir los grupos hidroxialquilo C1 , C2 , C3, C4, C5 y C6.
El término "cicloalquilo" se refiere a grupos alquilo ciclados, incluyendo sistemas de anillo mono, bi o policíclicos. "Cicloalquilo C3 a C8" o "cicloalquilo C3-8" pretende incluir grupos cicloalquilo C3 , C4, C5 , Ca , C7 y C8 , incluyendo anillos monocíclicos, bicíclicos y policíclicos. Los ejemplos de grupos cicloalquilo incluyen, pero sin limitación, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo y norbornilo. Los grupos cicloalquilo ramificados tales como 1-metilciclopropilo y 2-metilciclopropilo y espiro y grupos cicloalquilo puenteados están incluidos en la definición de "cicloalquilo".
El término "cicloheteroalquilo" se refiere a grupos heteroalquilo ciclados, incluyendo sistemas de anillo mono, bi o policíclicos. "Cicloheteroalquilo C3 a C7" o "cicloheteroalquilo C3-7" pretende incluir grupos cicloheteroalquilo C3 , C4, C5 , Ca y C7. Los ejemplos de grupos cicloheteroalquilo incluyen, pero sin limitación, oxetanilo, tetrahidrofuranilo, tetrahidropiranilo, azetidinilo, pirrolidinilo, piperidinilo, morfolinilo y piperazinilo. Los grupos cicloheteroalquilo ramificados, tales como piperidinilmetilo, piperazinilmetilo, morfolinilmetilo, piridinilmetilo, piridizilmetilo, pirimidilmetilo y pirazinilmetilo, están incluidos en la definición de "cicloheteroalquilo".
Tal como se usa en el presente documento, "carbociclo", "carbociclilo" o "resto carbocíclico" pretende indicar cualquier anillo hidrocarburo monocíclico o bicíclico de 3, 4, 5, 6, 7 u 8 o bicíclico o tricíclico de 7, 8, 9, 10, 11, 12 o 13 miembros estable, cualquiera de los cuales puede estar saturado, parcialmente insaturado, insaturado o aromático. Los ejemplos de dichos carbociclos incluyen, pero sin limitación, ciclopropilo, ciclobutilo, ciclobutenilo, ciclopentilo, ciclopentenilo, ciclohexilo, cicloheptenilo, cicloheptilo, cicloheptenilo, adamantilo, ciclooctilo, ciclooctenilo, ciclooctadienilo, [3.3.0]biciclooctano, [4.3.0]biciclononano, [4.4.0]biciclodecano (decalina), [2.2.2]biciclooctano, fluorenilo, fenilo, naftilo, indanilo, adamantilo, antracenilo y tetrahidronaftilo (tetralina). Como se ha mostrado anteriormente, los anillos puenteados también están incluidos en la definición de carbociclo (por ejemplo, [2.2.2]biciclooctano). Los carbociclos preferidos, a menos que se indique otra cosa, son ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, fenilo e indanilo. Cuando se usa el término "carbociclilo", este pretende incluir "arilo". Un anillo puenteado se produce cuando uno o más átomos de carbono conectan dos átomos de carbono no adyacentes. Los puentes preferidos son uno o dos átomos de carbono. Debe advertirse que un puente siempre convierte un anillo monocíclico en un anillo tricíclico. Cuando un anillo está puenteado, los sustituyentes citados para el anillo también pueden estar presentes en el anillo.
Además, el término "carbociclilo", que incluye "cicloalquilo" y "cicloalquenilo", como se emplea en el presente documento, solo o como parte de otro grupo, incluye grupos hidrocarburo cíclicos saturados o parcialmente insaturados (que contienen 1 o 2 dobles enlaces) que contienen de 1 a 3 anillos, que incluyen monocicloalquilo, bicicloalquilo y tricicloalquilo, que contienen un total de 3 a 20 átomos de carbono que forman los anillos, preferentemente de 3 a 10 carbonos o de 3 a 6 carbonos, formando el anillo y que puede estar condensado con 1 o 2 anillos aromáticos como se describe para arilo, que incluye ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo, ciclooctilo, ciclodecilo y ciclododecilo, ciclohexenilo,
cualquiera de dichos grupos puede estar opcionalmente sustituido con de 1 a 4 sustituyentes tales como halógeno, alquilo, alcoxi, hidroxi, arilo, ariloxi, arilalquilo, cicloalquilo, alquilamido, alcanoilamino, oxo, acilo, arilcarbonilamino, nitro, ciano, tiol y/o alquiltio y/o cualquiera de los sustituyentes de alquilo.
Tal como se usa en el presente documento, el término "carbociclilo bicíclico" o "grupo carbocíclico bicíclico" pretende indicar un sistema de anillo carbocíclico de 9 o 10 miembros estable que contiene dos anillos condensados y consiste en átomos de carbono. De los dos anillos condensados, un anillo es un anillo benzo condensado a un segundo anillo y el segundo anillo es un anillo de carbono de 5 o 6 miembros que está saturado, parcialmente insaturado o insaturado. El grupo carbocíclico bicíclico puede estar unido a su grupo colgante en cualquier átomo de carbono que dé como resultado una estructura estable. El grupo carbocíclico bicíclico descrito en el presente documento puede estar sustituido en cualquier carbono si el compuesto resultante es estable. Son ejemplos de un grupo carbocíclico bicíclico, pero sin limitación, naftilo, 1,2-dihidronaftilo, 1,2,3,4-tetrahidronaftilo e indanilo.
Tal como se usa en el presente documento, el término "arilo", como se emplea en el presente documento, solo o como parte de otro grupo, se refiere a hidrocarburos aromáticos monocíclicos o policíclicos (que incluyen bicíclicos y tricíclicos), incluyendo, por ejemplo, fenilo, naftilo, antracenilo y fenantranilo. Los restos arilo se conocen bien y se describen, por ejemplo, en Lewis, R. J., ed., Hawley's Condensed Chemical Dictionary, 13a edición, John Wiley & Sons, Inc., Nueva York (1997). En una realización, el término "arilo" representa grupos aromáticos monocíclicos y bicíclicos que contienen de 6 a 10 carbonos en la porción anular (tales como fenilo o naftilo, que incluye 1 -naftilo y 2-naftilo). Por ejemplo, "Arilo C6 o C10" o "arilo C6-10" se refiere a fenilo y naftilo. A menos que se especifique otra cosa, "arilo", "arilo C6 o C10", "arilo C6-10" o "resto aromático" puede estar sin sustituir o sustituido con de 1 a 5 grupos, preferentemente de 1 a 3 grupos, seleccionados entre -OH, -OCH3, -Cl, -F, -Br, -I, -CN, -NO2 , -NH2 , -N(CH3)H, -N(CH3)2, -CF3 , -OCF3, -C(O)CH3 , -SCH3 , -S(O)CH3, -S(O)2CH3 , -CH3 , -CH2CH3, -CO2 H y -CO2CH3.
El término "bencilo", tal como se usa en el presente documento, se refiere a un grupo metilo en el que uno de los átomos de hidrógeno se reemplaza por un grupo fenilo, en donde dicho grupo fenilo puede estar opcionalmente sustituido con de 1 a 5 grupos, preferentemente de 1 a 3 grupos, OH, OCH3 , Cl, F, Br, I, CN, NO2 , NH2 , N(CH3 )H, N(CH3)2, CF3, OCF3, C(=O)CH3, SCH3 , S(=O)CH3 , S(=O)2CH3 , CH3, CH2CH3, CO2 H y CO2CH3.
Tal como se usa en el presente documento, el término "heterociclo", "heterociclilo" o "grupo heterocíclico" pretende indicar un anillo heterocíclico monocíclico de 3, 4, 5, 6 o 7 miembros o policíclico de 5, 6, 7, 8, 9, 10, 11, 12, 13 o 14 miembros (que incluye bicíclico y tricíclico) que está saturado o parcialmente insaturado y que contiene átomos de carbono y 1, 2, 3 o 4 heteroátomos seleccionados independientemente entre N, O y S; e incluye cualquier grupo policíclico en el que cualquiera de los anillos heterocíclicos anteriormente definidos está condensado a un anillo carbocíclico o uno arilo (por ejemplo, benceno). Es decir, el término "heterociclo", "heterociclilo" o "grupo heterocíclico" incluye sistemas anulares no aromáticos, tales como heterocicloalquilo y heterocicloalquenilo. Opcionalmente, los heteroátomos de nitrógeno y azufre pueden estar oxidados (es decir, N ^ O y S(O)p, en donde p es 0, 1 o 2). El átomo de nitrógeno puede estar sustituido o sin sustituir (es decir, N o NR, en donde R es H u otro sustituyente, si se define). El anillo heterocíclico puede estar unido a su grupo colgante en cualquier heteroátomo o átomo de carbono que dé como resultado una estructura estable. Los anillos heterocíclicos descritos en el presente documento pueden estar sustituidos en un átomo de carbono o en uno de nitrógeno si el compuesto resultante es estable. Un nitrógeno del heterociclo puede estar opcionalmente cuaternizado. Se prefiere que cuando el número total de átomos de S y O en el heterociclo sea superior a 1, entonces estos heteroátomos no sean adyacentes entre sí. Se prefiere que el número total de átomos de S y O en el heterociclo no sea mayor de 1. Los ejemplos de heterociclilo incluyen, sin limitación, azetidinilo, piperazinilo, piperidinilo, piperidonilo, piperonilo, piranilo, morfolinilo, tetrahidrofuranilo, tetrahidroisoquinolinilo, tetrahidroquinolinilo, morfolinilo, dihidrofuro[2,3-6]tetrahidrofurano.
Tal como se usa en el presente documento, la expresión "heterociclo bicíclico" o "grupo heterocíclico bicíclico" pretende indicar un sistema anular heterocíclico de 9- o 10 miembros estable que contiene dos anillos condensados y que consiste en átomos de carbono y 1, 2, 3 o 4 heteroátomos seleccionados independientemente entre N, O y S. De los dos anillos condensados, un anillo es un anillo aromático monocíclico de 5 o 6 miembros que comprende un anillo heteroarilo de 5 miembros, un anillo heteroarilo de 6 miembros o un anillo benzo, cada uno condensado a un segundo anillo. El segundo anillo es un anillo monocíclico de 5 o 6 miembros que está saturado, parcialmente insaturado o insaturado y comprende un heterociclo de 5 miembros, un heterociclo de 6 miembros o un carbociclo (con la condición de que el primer anillo no sea benzo cuando el segundo anillo es un carbociclo).
El grupo heterocíclico bicíclico puede estar unido a su grupo colgante en cualquier heteroátomo o átomo de carbono que dé como resultado una estructura estable. El grupo heterocíclico bicíclico descrito en el presente documento puede estar sustituido en un átomo de carbono o en uno de nitrógeno si el compuesto resultante es estable. Se prefiere que cuando el número total de átomos de S y O en el heterociclo sea superior a 1, entonces estos heteroátomos no sean adyacentes entre sí. Se prefiere que el número total de átomos de S y O en el heterociclo no sea mayor de 1. Los ejemplos de grupo heterocíclico bicíclico son, pero sin limitación, 1,2,3,4-tetrahidroquinolinilo, 1,2,3,4-tetrahidroisoquinolinilo, 5,6,7,8-tetrahidro-quinolinilo, 2,3-dihidro-benzofuranilo, cromanilo, 1,2,3,4-tetrahidroquinoxalinilo y 1,2,3,4-tetrahidro-quinazolinilo.
Los anillos puenteados también están incluidos en la definición de heterociclo. Un anillo puenteado se da cuando uno o más átomos (es decir, C, O, N o S) unen dos átomos de carbono o nitrógeno no adyacentes. Los ejemplos de anillos puenteados incluyen, pero sin limitación, un átomo de carbono, dos átomos de carbono, un átomo de nitrógeno, dos átomos de nitrógeno y un grupo carbono-nitrógeno. Debe advertirse que un puente siempre convierte un anillo monocíclico en un anillo tricíclico. Cuando un anillo está puenteado, los sustituyentes citados para el anillo también pueden estar presentes en el anillo.
Tal como se usa en el presente documento, el término "heteroarilo" pretende indicar hidrocarburos aromáticos monocíclicos y policíclicos (que incluyen bicíclicos y tricíclicos) estables, que incluyen al menos un miembro del anillo heteroátomo, tal como azufre, oxígeno o nitrógeno. Los grupos heteroarilo incluyen, sin limitación, piridilo, pirimidinilo, pirazinilo, piridazinilo, triazinilo, furilo, quinolilo, isoquinolilo, tienilo, imidazolilo, tiazolilo, indolilo, pirroílo, oxazolilo, benzofurilo, benzotienilo, benzotiazolilo, isoxazolilo, pirazolilo, triazolilo, tetrazolilo, indazolilo, 1,2,4-tiadiazolilo, isotiazolilo, purinilo, carbazolilo, benzoimidazolilo, indolinilo, benzodioxolanilo y benzodioxano. Los grupos heteroarilo están sustituidos o sin sustituir. El átomo de nitrógeno está sustituido o sin sustituir (es decir, N o NR, en donde R es H u otro sustituyente, si se define). Opcionalmente, los heteroátomos de nitrógeno y azufre pueden estar oxidados (es decir, N ^ O y S(O)p, en donde p es 0, 1 o 2).
Los ejemplos de heteroarilo también incluyen, pero sin limitación, acridinilo, azocinilo, benzoimidazolilo, benzofuranilo, benzotiofuranilo, benzotiofenilo, benzoxazolilo, benzoxazolinilo, benzotiazolilo, benzotriazolilo, benzotetrazolilo, benzoisoxazolilo, benzoisotiazolilo, benzoimidazolinilo, carbazolilo, 4aH-carbazolilo, carbolinilo, cromanilo, cromenilo, cinnolinilo, decahidroquinolinilo, 2H,6H-1,5,2-ditiazinilo, furanilo, furazanilo, imidazolidinilo, imidazolinilo, imidazolilo, 1H-indazolilo, imidazolopiridinilo, indolenilo, indolinilo, indolizinilo, indolilo, 3H-indolilo, isatinoílo, isobenzofuranilo, isocromanilo, isoindazolilo, isoindolinilo, isoindolilo, isoquinolinilo, isotiazolilo, isotiazolopiridinilo, isoxazolilo, isoxazolopiridinilo, metilenodioxifenilo, naftiridinilo, octahidroisoquinolinilo, oxadiazolilo, 1,2,3-oxadiazolilo, 1,2,4-oxadiazolilo, 1,2,5-oxadiazolilo, 1,3,4-oxadiazolilo, oxazolidinilo, oxazolilo, oxazolopiridinilo, oxazolidinilperimidinilo,
oxindolilo, pirimidinilo, fenantridinilo, fenantrolinilo, fenazinilo, fenotiazinilo, fenoxatianilo, fenoxazinilo, ftalazinilo, pteridinilo, purinilo, pirazinilo, pirazolidinilo, pirazolinilo, pirazolopiridinilo, pirazolilo, piridazinilo, piridooxazolilo, piridoimidazolilo, piridotiazolilo, piridinilo, pirimidinilo, pirrolidinilo, pirrolinilo, 2-pirrolidonilo, 2H-pirrolilo, pirrolilo, quinazolinilo, quinolinilo, 4H-quinolizinilo, quinoxalinilo, quinuclidinilo, tetrazolilo, tetrahidrofuranilo, tetrahidroisoquinolinilo, tetrahidroquinolinilo, 6H-1,2,5-tiadiazinilo, 1,2,3-tiadiazolilo, 1,2,4-tiadiazolilo, 1,2,5-tiadiazolilo, 1,3,4-tiadiazolilo, tiantrenilo, tiazolilo, tienilo, tiazolopiridinilo, tienotiazolilo, tienooxazolilo, tienoimidazolilo, tiofenilo, triazinilo, 1,2,3-triazolilo, 1,2,4-triazolilo, 1,2,5-triazolilo, 1,3,4-triazolilo y xantenilo.
Los ejemplos de heteroarilo de 5 a 10 miembros incluyen, pero sin limitación, piridinilo, furanilo, tienilo, pirazolilo, imidazolilo, imidazolidinilo, indolilo, tetrazolilo, isoxazolilo, oxazolilo, oxadiazolilo, oxazolidinilo, tiadiazinilo, tiadiazolilo, tiazolilo, triazinilo, triazolilo, benzoimidazolilo, 1H-indazolilo, benzofuranilo, benzotiofuranilo, benzotetrazolilo, benzotriazolilo, benzoisoxazolilo, benzoxazolilo, oxindolilo, benzoxazolinilo, benzotiazolilo, benzoisotiazolilo, isatinoílo, isoquinolinilo, octahidroisoquinolinilo, isoxazolopiridinilo, quinazolinilo, quinolinilo, isotiazolopiridinilo, tiazolopiridinilo, oxazolopiridinilo, imidazolopiridinilo y pirazolopiridinilo. Los ejemplos de heteroarilo de 5 a 6 miembros incluyen, pero sin limitación, piridinilo, furanilo, tienilo, pirrolilo, pirazolilo, pirazinilo, imidazolilo, imidazolidinilo, indolilo, tetrazolilo, isoxazolilo, oxazolilo, oxadiazolilo, oxazolidinilo, tiadiazinilo, tiadiazolilo, tiazolilo, triazinilo y triazolilo. En algunas realizaciones, el heteroarilo se selecciona entre benzotiazolilo, imidazolpiridinilo, pirrolopiridinilo, quinolinilo e indolilo.
A menos que se indique de otro modo, "carbociclilo" o "heterociclilo" incluye de uno a tres anillos más condensados al anillo carbocíclico o el anillo heterocíclico (tal como anillos arilo, cicloalquilo, heteroarilo o cicloheteroalquilo), por ejemplo,
y puede estar opcionalmente sustituido mediante átomos de carbono o nitrógeno (según sea aplicable) con 1, 2 o 3 grupos seleccionados entre hidrógeno, halo, haloalquilo, alquilo, haloalquilo, alcoxi, haloalcoxi, alquenilo, trifluorometilo, trifluorometoxi, alquinilo, cicloalquilalquilo, cicloheteroalquilo, cicloheteroalquilalquilo, arilo, heteroarilo, arilalquilo, ariloxi, ariloxialquilo, arilalcoxi, alcoxicarbonilo, arilcarbonilo, arilalquenilo, aminocarbonilarilo, ariltio, arilsulfinilo, arilazo, heteroarilalquilo, heteroarilalquenilo, heteroarilheteroarilo, heteroariloxi, hidroxi, nitro, ciano, tiol, alquiltio, ariltio, heteroariltio, ariltioalquilo, alcoxiariltio, alquilcarbonilo, arilcarbonilo, alquilaminocarbonilo, arilaminocarbonilo, alcoxicarbonilo, aminocarbonilo, alquilcarboniloxi, arilcarboniloxi, alquilcarbonilamino, arilcarbonilamino, arilsulfinilo, arilsulfinilalquilo, arilsulfonilamino y arilsulfonaminocarbonilo y/o cualquiera de los sustituyentes de alquilo indicados en el presente documento.
Cuando cualquiera de los términos alquilo, alquenilo, alquinilo, cicloalquilo, carbociclilo, heterociclilo, arilo y heteroarilo se usan como parte de otro grupo, el número de átomos de carbono y miembros del anillo son los mismos que los definidos en los términos por sí mismos. Por ejemplo, alcoxi, haloalcoxi, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, haloalcoxi, alcoxialcoxi, haloalquilamino, alcoxialquilamino, haloalcoxialquilamino, alquiltio y similares contienen, cada uno de manera independiente, el número de átomos de carbono que es igual al que se ha definido para el término "alquilo", tal como de 1 a 4 átomos de carbono, de 1 a 6 átomos de carbono, de 1 a 10 átomos de carbono, etc. De manera análoga, cicloalcoxi, heterocicliloxi, cicloalquilamino, heterociclilamino, aralquilamino, arilamino, ariloxi, aralquiloxi, heteroariloxi, heteroarilalquilooxi y similares contienen, cada uno de manera independiente, miembros del anillo que son iguales a los definidos para los términos "cicloalquilo", "heterociclilo", "arilo" y "heteroarilo", tales como de 3 a 6 miembros, de 4 a 7 miembros, de 6 a 10 miembros, de 5 a 10 miembros, 5 o 6 miembros, etc.
De acuerdo con una convención usada en la técnica, un enlace que señala una línea en negrita, tal como
como se usa en las fórmulas estructurales en el presente documento, representa el enlace que es el punto de unión del resto o el sustituyente al núcleo o la estructura principal.
De acuerdo con una convención usada en la técnica, un enlace ondulado o sinuoso en una fórmula estructural, tal como
, se usa para representar un centro estereogénico del átomo de carbono al cual X', Y' y Z' están unidos y se pretende representar a ambos enantiómeros en una única figura. Es decir, una fórmula estructural con dicho enlace ondulado denota cada uno de los enantiómeros por separado, tales como
, así como una mezcla racémica de los mismos. Cuando un enlace ondulado o sinuoso está unido a un resto doble enlace (tal como C=C o C=N), este incluye los isómeros cis o trans (o E y Z-) o una mezcla de los mismos.
En el presente documento se entiende que si un resto carbocíclico o heterocíclico puede estar unido o de otro modo enlazado a un sustrato designado mediante diferentes átomos en el anillo sin denotar un punto de unión específico, entonces se pretenden todos los puntos posibles, ya sea a través de un átomo de carbono o, por ejemplo, un átomo de nitrógeno trivalente. Por ejemplo, el término "piridilo" significa 2, 3 o 4-piridilo, el término "tienilo" significa 2 o 3-tienilo y así sucesivamente.
Cuando se muestra que un enlace a un sustituyente cruza un enlace que conecta dos átomos en un anillo, entonces dicho sustituyente puede estar enlazado a cualquier átomo en el anillo. Cuando se enumera un sustituyente sin indicar el átomo en el que dicho sustituyente está unido al resto del compuesto de una fórmula dada, entonces dicho sustituyente puede estar unido a través de cualquier átomo de dicho sustituyente. Solo se permiten combinaciones de sustituyentes y/o variables si dichas combinaciones dan como resultado compuestos estables.
Un experto en la técnica reconocerá qué sustituyentes y otros restos de los compuestos de la presente invención deberían seleccionarse para proporcionar un compuesto que es suficientemente estable para proporcionar un compuesto farmacéuticamente útil, el cual se puede formular en una composición farmacéuticamente estable. Se contempla que los compuestos de la presente invención que tienen dicha estabilidad están dentro del alcance de la invención.
El término "contraión" se usa para representar una especie cargada negativamente tal como cloruro, bromuro, hidróxido, acetato y sulfato. La expresión "ion metálico" se refiere a iones de metales alcalinos tales como sodio, potasio o litio e iones de metales alcalinotérreos tales como calcio, así como cinc y aluminio.
Como se indica en el presente documento, el término "sustituido" significa que al menos un átomo de hidrógeno (unido al átomo de carbono o al heteroátomo) está sustituido con un grupo distinto de hidrógeno, con la condición de que las valencias normales se mantengan y que la sustitución dé como resultado un compuesto estable. Cuando un sustituyente es oxo (es decir, =O), entonces se reemplazan 2 hidrógenos en el átomo. Los sustituyentes oxo no están presentes en los restos aromáticos. Cuando se dice que un sistema anular (por ejemplo, carbocíclico o heterocíclico) está sustituido por un grupo carbonilo o un doble enlace, se pretende que el grupo carbonilo o el doble enlace sea parte (es decir, esté dentro) del anillo. Los dobles enlaces de anillo, tal como se usan en el presente documento, son dobles enlaces que se forman entre dos átomos adyacentes del anillo (por ejemplo, C=C, C=N o N=N). El término "sustituido" en referencia a alquilo, cicloalquilo, heteroalquilo, cicloheteroalquilo, alquileno, arilo, arilalquilo, heteroarilo, heteroarilalquilo, carbociclilo y heterociclilo, se refiere a alquilo, cicloalquilo, heteroalquilo, cicloheteroalquilo, alquileno, arilo, arilalquilo, heteroarilo, heteroarilalquilo, carbociclilo y heterociclilo, respectivamente, en el que uno o más átomos de hidrógeno, que está unido al carbono o al heteroátomo, está cada uno independientemente sustituido con uno o más sustituyentes distintos de hidrógeno.
En los casos en donde hay átomos de nitrógeno (por ejemplo, aminas) en compuestos de la presente invención, estos pueden convertirse en N-óxidos mediante tratamiento con un agente antioxidante (por ejemplo, mCPBA y/o peróxido
de hidrógeno) para proporcionar otros compuestos.
Cuando cualquier variable aparece más de una vez en cualquier constituyente o fórmula para un compuesto, su definición cada vez que aparece es independiente de su definición en cualquier otro caso. Por lo tanto, por ejemplo, si se muestra que un grupo está sustituido con 0, 1, 2 o 3 grupos R, entonces dicho grupo está sin sustituir cuando está sustituido con 0 grupos R o está sustituido con hasta tres grupos R y cada vez que aparece R se selecciona independientemente a partir de la definición de R.
Asimismo, solo se permiten combinaciones de sustituyentes y/o variables si dichas combinaciones dan como resultado compuestos estables.
Tal como se usa en el presente documento, el término "tautómero" se refiere a cada uno de dos o más isómeros de un compuesto que existen juntos en equilibrio y que son fácilmente intercambiables por la migración de un átomo o grupo dentro de la molécula. Por ejemplo, un experto en la técnica entenderá con facilidad que un 1,2,3-triazol existe en dos formas tautoméricas como se ha definido anteriormente:
1 H - 1,2,3-triazol 2W-1,2.3-triazol
Por lo tanto, esta divulgación pretende cubrir todos los tautómeros posibles, incluso cuando una estructura representa solamente uno de ellos.
En el presente documento, la frase "farmacéuticamente aceptable" se emplea para referirse a aquellos compuestos, materiales, composiciones y/o formas de dosificación que son, dentro del alcance del buen criterio médico, adecuados para su uso en contacto con los tejidos de los seres humanos y animales sin excesiva toxicidad, irritación, respuesta alérgica y/u otro problema o complicación, acorde con una proporción de beneficio/riesgo razonable.
Los compuestos de la presente invención pueden estar presentes en forma de sales farmacéuticamente aceptables, que también se encuentran dentro del alcance de esta invención. Tal como se usa en el presente documento, "sales farmacéuticamente aceptables" se refiere a derivados de los compuestos divulgados en los que el compuesto precursor se modifica fabricando sales ácidas o básicas del mismo. Las sales farmacéuticamente aceptables de la presente invención se pueden sintetizar a partir del compuesto precursor que contiene un resto básico o ácido mediante métodos convencionales. En general, dichas sales se pueden preparar haciendo reaccionar las formas de ácido o de base libre de estos compuestos con una cantidad estequiométrica de la base o el ácido apropiado en agua o en un disolvente orgánico o en una mezcla de los dos; en general, se prefieren medios no acuosos como éter, acetato de etilo, etanol, isopropanol o acetonitrilo. Se encuentran listas de sales adecuadas en Remington's Pharmaceutical Sciences, 18a edición, Mack Publishing Company, Easton, PA (1990).
Si los compuestos de la presente invención tienen, por ejemplo, al menos un centro básico, estos pueden formar sales de adición de ácido. Estas se forman, por ejemplo, con ácidos inorgánicos fuertes, tales como ácidos minerales, por ejemplo, ácido sulfúrico, ácido fosfórico o un ácido hidrácido, con ácidos carboxílicos orgánicos, tales como ácidos alcanocarboxílicos de 1 a 4 átomos de carbono, por ejemplo, ácido acético, los cuales están sin sustituir o sustituidos, por ejemplo, por halógeno como ácido cloroacético, tales como ácidos dicarboxílicos saturados o insaturados, por ejemplo ácido oxálico, malónico, succínico, maleico, fumárico, Itálico o tereftálico, tales como ácidos hidroxicarboxílicos, por ejemplo ácido ascórbico, glicólico, láctico, málico, tartárico o cítrico, tales como aminoácidos, (por ejemplo ácido aspártico o glutámico o lisina o arginina) o ácido benzoico o con ácidos sulfónicos orgánicos, tales como ácidos alquil o arilsulfónicos (C1 -C4) que están sin sustituir o sustituidos, por ejemplo con halógeno, por ejemplo ácido metil o p-toluenosulfónico. También se pueden formar sales de adición de ácido correspondientes que tienen, si se desea, un centro básico adicional presente. Los compuestos de la presente invención que tienen al menos un grupo ácido (por ejemplo COOH) también pueden sales con bases. Las sales con bases adecuadas son, por ejemplo, sales metálicas, tales como sales de metales alcalinos o alcalinotérreos, por ejemplo sales de sodio, potasio o magnesio o sales con amoniaco o una amina orgánica, tal como morfolina, tiomorfolina, piperidina, pirrolidina, una mono, di o trialquilamina inferior, por ejemplo etilo, ferc-butilo, dietilo, diisopropilo, trietilo, tributil o dimetil-propilamina o una mono, di o trihidroxi alquilamina inferior, por ejemplo mono, di o trietanolamina. Además se pueden formar las sales internas correspondientes. Las sales que no son adecuadas para usos farmacéuticos pero que se pueden emplear, por ejemplo, para el aislamiento o la purificación compuestos libres de fórmula (la) o (ib) o sus sales farmacéuticamente aceptables, también están incluidas.
Las sales preferidas de los compuestos de fórmula (la) o (Ib) que contienen un grupo básico incluyen monoclorhidrato, hidrogenosulfato, metanosulfonato, fosfato, nitrato o acetato.
Las sales preferidas de los compuestos de fórmula (la) o (Ib) que contienen un grupo ácido incluyen las sales de sodio, potasio y magnesio y aminas orgánicas farmacéuticamente aceptables.
Además, los compuestos de fórmula (la) o (Ib) pueden tener formas de profármaco. Cualquier convierto que se convierta in vivo para proporcionar el principio bioactivo (es decir, un compuesto de fórmula Ia o Ib) es un profármaco. En la técnica se conocen bien diferentes formas de profármacos. Para ejemplos de dichos derivados de profármacos, véanse:
a) Bundgaard, H., ed., Design of Prodrugs, Elsevier (1985) y Widder, K. et al., eds., Methods in Enzymology, 112:309-396, Academic Press (1985);
b) Bundgaard, H., capítulo 5, "Design and Application of Prodrugs", A Textbook of Drug Design and Development, págs. 113-191, Krosgaard-Larsen, P. et al., eds., Harwood Academic Publishers (1991);
c) Bundgaard, H., Adv. Drug Deliv. Rev., 8:1-38 (1992);
d) Bundgaard, H. et al., J. Pharm. Sci., 77:285 (1988) y
e) Kakeya, N. et al., Chem. Pharm. Bull., 32:692 (1984).
Los compuestos de la presente invención contienen un grupo carboxi que puede formar ésteres fisiológicamente hidrolizables que sirven como profármacos, es decir, "ésteres de profármacos", hidrolizándolos en el cuerpo para producir los compuestos de la presente invención per se. Los ejemplos de los ésteres fisiológicamente hidrolizables de los compuestos de la presente invención incluyen alquilo C1 a C6, alquilbencilo C1 a C6, 4-metoxibencilo, indanilo, ftalilo, metoximetilo, alcanoiloxi C1-6-alquilo C1-6 (por ejemplo, acetoximetilo, pivaloiloximetilo o propioniloximetilo), alcoxicarboniloxi C1 a C6-alquilo C1 a C6 (por ejemplo, metoxicarbonil-oximetilo o etoxicarboniloximetilo, gliciloximetilo, fenilgliciloximetilo, (5-metil-2-oxo-1,3-dioxolen-4-il)-metilo) y otros ésteres fisiológicamente hidrolizables bien conocidos usados, por ejemplo, en las técnicas de la penicilina y la cefalosporina. Dichos ésteres se pueden preparar por técnicas convencionales conocidas en la técnica. Los "ésteres de profármaco" se pueden formar haciendo reaccionar el resto ácido carboxílico de los compuestos de la presente invención con alquilo o alcohol arílico, haluro o sulfonato empleando procedimientos conocidos por los expertos en la técnica. Dichos ésteres se pueden preparar por técnicas convencionales conocidas en la técnica.
La preparación de profármacos se conoce bien en la técnica y se describe en, por ejemplo, King, F. D., ed., Medicinal Chemistry: Principles and Practice, The Royal Society of Chemistry, Cambridge, Reino Unido (1994); Testa, B. et al., Hydrolysis in Drug and Prodrug Metabolism. Chemistry, Biochemistry and Enzymology, VCHA y Wiley-VCH, Zurich, Suiza (2003); Wermuth, C. G., ed., The Practice of Medicinal Chemistry, Academic Press, San Diego, Ca (1999).
La presente divulgación (que no es parte de la invención) pretende incluir todos los isótopos de los átomos que se encuentran en los presentes compuestos. Los isótopos incluyen aquellos átomos que tienen el mismo número atómico pero diferentes números másicos. A modo de ejemplo general y sin limitación, los isótopos de hidrógeno incluyen deuterio y tritio. El deuterio tiene un protón y un neutrón en su núcleo y tiene dos veces la masa del hidrógeno habitual. El deuterio se puede representar mediante símbolos tales como "2H" o "D". El término "deuterado" en el presente documento, en sí mismo o usado para modificar un compuesto o grupo, se refiere al reemplazo de uno o más átomos de hidrógeno, que está unido al carbono o carbonos, con un átomo de deuterio. Los isótopos de carbono incluyen 13C y 14C.
Los compuestos de la divulgación marcados con isótopos (que no son parte de la invención) se pueden prepararse en general mediante técnicas convencionales conocidas por los expertos en la técnica o por procesos análogos a los descritos en el presente documento, usando un reactivo marcado isotópicamente apropiado en lugar del reactivo no marcado empleado de otro modo. Dichos compuestos tienen diversos usos potenciales, por ejemplo, como patrones y reactivos para determinar la capacidad de un compuesto farmacéutico potencial para unirse a las proteínas o receptores diana o para obtener imágenes de compuestos de esta invención unidos a receptores biológicos in vivo o in vitro.
"Compuesto estable" y "estructura estable" pretenden indicar un compuesto que es lo suficientemente robusto para sobrevivir al aislamiento hasta un grado de pureza útil a partir de una mezcla de reacción y su formulación en un agente terapéutico eficaz. Se prefiere que los compuestos de la presente invención no contengan un grupo N-halo, S(O)2H o S(O)H.
El término "solvato" significa una asociación física de un compuesto de esta invención con una o más moléculas de disolvente, ya sea orgánico o inorgánico. Esta asociación física incluye enlaces de hidrógeno. En ciertos casos el solvato podrá aislarse, por ejemplo, cuando una o más moléculas de disolvente se incorporan en la red de cristal del sólido cristalino. Las moléculas de disolvente en el solvato pueden estar presentes en una disposición regular y/o una disposición no ordenada. El solvato puede comprender una cantidad tanto estequiométrica como no estequiométrica de las moléculas de disolvente. "Solvato" abarca solvatos tanto en fase de solución como aislables. Los solvatos a modo de ejemplo incluyen, pero sin limitación, hidratos, etanolatos, metanolatos e isopropanolatos. Los métodos de solvatación se conocen habitualmente en la técnica.
ABREVIATURAS
Las abreviaturas tal como se usan en el presente documento, se definen como sigue: "1 x" para una vez, "2 x" para
dos veces, "3 x" para tres veces, "°C" para grados Celsius, "eq" para equivalente o equivalentes, "g" para gramo o gramos, "mg" para miligramo o miligramos, "L" para litro o litros, " ml" para mililitro o mililitros, "|jl" para microlitro o microlitros, "N" para normal, "M" para molar, "mmol" para milimol o milimoles, "min" para minuto o minutos, "h" para hora u horas, "ta" para temperatura ambiente, "TR" para tiempo de retención, "RBF" para matraz de fondo redondo, "atm" para atmósfera, "kPa, psi" para kilopascal (libras por pulgada cuadrada), "conc." para concentrado, "RCM" para metátesis de cierre de anillo, "sat" o "satd" para saturado, "SFC" para cromatografía de fluidos supercríticos "PM" para peso molecular, "pf' para punto de fusión, "ee" para exceso enantiomérico, "MS" o "Espec. Masas" para espectrometría de masas, "ESI" para espectroscopia de masas con ionización por electropulverización, "HR" para alta resolución, "HRMS" para espectrometría de masas de alta resolución, "LCMS" para cromatografía liquida-espectrometría de masas, "HPLC" para cromatografía líquida de alta presión, "HPLC FI" para HPLC de fase inversa, 'TLC" o "tlc" para cromatografía de capa fina, "RMN" para espectroscopía de resonancia magnética nuclear, "nOe" para espectroscopía nuclear de efecto Overhauser, "1H" para protón, "8" para delta, "s" para singlete, "d" para doblete, "t" para triplete, "c" para cuartete, "m" para multiplete, "a" para ancho, "Hz" para hercio y "a", "p", " y " , "R", "S", "E" y "Z" son denominaciones estereoquímicas familiares para un experto en la técnica.
Me metilo
Et etilo
Pr propilo
i-Pr isopropilo
Bu butilo
/-Bu isobutilo
t-Bu terc-but/lo
Ph fenilo
Bn bencilo
Boc o BOC terc-butiloxicarbonilo
Boc2O dicarbonato de di-terc-butilo
AcOH u HOAc ácido acético
AlCls tricloruro de aluminio
AIBN Azobis-isobutironitrilo
BBr3 tribromuro de boro
BCI3 tricloruro de boro
BEMP 2-terc-butilimino-2-dietilamino-1,3-dimetilperhidro-1,3,2-diazafosforina
reactivo BOP hexafluorofosfato de benzotriazol-1-iloxitris(dimetilamino)fosfonio
reactivo de Burgess 1-metoxi-N-trietilammoniosulfonil-metanimidato
CBz carbobenciloxi
DCM o CH2Cl2 diclorometano
CH3CN o ACN acetonitrilo
CDCl3 deutero-cloroformo
CHCl3 cloroformo
mCPBA o m-CPBA ácido meta-cloroperbenzoico
Cs2CO3 carbonato de cesio
Cu(OAc)2 acetato de cobre (II)
Cy2NMe N-ciclohexil-N-metilciclohexanamina
DBU 1,8-diazabiciclo[5.4.0]undec-7-eno
DCE 1,2 dicloroetano
DEA dietilamina
Dess-Martin 1,1,1-tris(acetiloxi)-1,1-dihidro-1,2-benziodoxol-3-(1H)-ona
DIC o DIPCDI diisopropilcarbodiimida
DIEA, DIPEA o diisopropiletilamina
base de Hunig, DMAP 4-dimetilaminopiridina
DME 1,2-dimetoxietano
DMF dimetilformamida
DMSO dimetilsulfóxido
ADNc ADN complementario
Dppp (R)-(+)-1,2-bis(difenilfosfino)propano
DuPhos (+)-1,2-bis((2S,5S)-2,5-dietilfosfolano)benceno
EDC W-(3-dimetilaminopropil)-A/-etilcarbodiimida
EDCI clorhidrato de A/-(3-dimetillaminopropil)-W-etilcarbodiimida
EDTA ácido etilendiaminatetraacético
(S,S)-EtDuPhosRh(I) trifluorometanosulfonato de (+)-1,2-bis((2S,5S)-2,5-dietilfosfolano)benceno(1,5-ciclooctadien)rodio (I)
Et3N o TEA trietilamina
EtOAc acetato de etilo
Et2O éter dietílico
EtOH etanol
GMF filtro de microfibra de vidrio
Grubbs II (1,3-bis(2,4,6-trimetilfenil)-2-imidazolidiniliden)dicloro(fenilmetileno)(triciclohexilfosfina)rutenio
HCl ácido clorhídrico
HATU hexafluorofosfato de O-(7-azabenzotriazol-1-il)-N,N,N',N'-tetrametiluronio
HEPES ácido 4-(2-hidroxietil)piperaxin-1-etanosulfónico
Hex hexano
HOBt u HOBT 1-hidroxibenzotriazol
H2O2 peróxido de hidrógeno
IBX ácido 2-yodoxibenzoico
H2SO4 ácido sulfúrico
reactivo de Jones CrO3 en H2SO4 acuoso, solución 2 M
K2CO3 carbonato potásico
K2HPO4 fosfato de potasio dibásico (hidrogenofosfato de potasio)
KOAc acetato de potasio
K3PO4 fosfato de potasio tribásico
LAH hidruro de litio y aluminio
LG grupo saliente
LiOH hidróxido de litio
MeOH metanol
MgSO4 sulfato de magnesio
MsOH o MSA ácido metilsulfónico/ácido metanosulfónico
NaCl cloruro sódico
NaH hidruro sódico
NaHCO3 bicarbonato sódico
Na3CO3 carbonato sódico
NaOH hidróxido sódico
Na3SO3 sulfito sódico
Na3SO4 sulfato sódico
NBS N-bromosuccinimida
NCS N-clorosuccinimida
NH3 amoniaco
NH4Cl cloruro de amonio
NH4OH hidróxido de amonio
NH4+HCO2- formiato de amonio
NMM N-metilmorfolina
OTf triflato o trifluorometanosulfonato
Pd2(dba)3 tris(dibencilidenoacetona)dipaladio(0)
Pd(OAc)2 acetato de paladio (II)
Pd/C paladio sobre carbono
Pd(dppf)Cl2 [1,1'-bis(difenilfosfino)-ferroceno]dicloropaladio (II)
Ph3PCl2 dicloruro de trifenilfosfina
PG grupo protector
POCl3 oxicloruro de fósforo
PPTS p-toluenosulfonato de piridinio
i-PrOH o IPA isopropanol
PS poliestireno
TA o ta temperatura ambiente
SEM-Cl cloruro de 2-(trimetisilil)etoximetilo
SiO2 óxido de sílice
SnCl2 cloruro de estaño (II)
TBAF fluoruro de tetra-n-butilamonio
TBAI yoduro de tetra-n-butilamonio
TFA ácido trifluoroacético
THF tetrahidrofurano
THP tetrahidropirano
TMSCHN2 trimetilsilildiazometano
TMSCH2N3 trimetilsililmetil azida
T3P ácido propano fosfónico anhídrido
TRIS tris (hidroximetil) aminometano
pTsOH ácido p-toluenosulfónico
IV. BIOLOGÍA
Los lisofosfolípidos son mediadores lipídicos bioactivos derivados de la membrana. Los lisofosfolípidos incluyen, pero no se limitan a, ácido lisofosfatídico (1-acil-2-hidroxi-sn-glicero-3-fosfato; LPA), esfingosina 1-fosfato (S1P), lisofosfatidilcolina (LPC) y esfingosilfosforilcolina (SPC). Los lisofosfolípidos afectan a funciones celulares
fundamentales que incluyen proliferación celular, diferenciación, supervivencia, migración, adhesión, invasión y morfogénesis celular. Estas funciones influyen en muchos procesos biológicos que incluyen la neurogénesis, la angiogénesis, la curación de heridas, la inmunidad y la carcinogénesis.
El LPA actúa a través de conjuntos de receptores específicos acoplados a proteínas G (GPCR) de forma autocrina y paracrina. El LPA que se une a sus GPCR afines (LPA1 , LPA2 , LPA3, LPA4, LPA5 , LPA6) activa las vías de señalización intracelular para producir diversas respuestas biológicas.
Los lisofosfolípidos, tales como el LPA, son especies de lípidos cuantitativamente menores en comparación con sus homólogos de fosfolípidos principales (por ejemplo, fosfatidilcolina, fosfatidiletanolamina y esfingomielina). El LPA tiene un papel como molécula efectora biológica y tiene una amplia gama de acciones fisiológicas tales como, por ejemplo, pero no limitado a, efectos sobre la presión arterial, activación plaquetaria y contracción del músculo liso, y diversos efectos celulares, que incluyen el crecimiento celular, el redondeo celular, la retracción de neuritas y la formación de fibras de estrés de actina y la migración celular. Los efectos del LPA están predominantemente mediados por el receptor.
La activación de los receptores de LPA (LPAA LPA2 , LPA3, LPA4, LPA5 , LPA6) con LPA media una gama de cascadas de señalización posteriores. Estas incluyen, pero no se limitan a, activación de la proteína quinasa activada por mitógeno (MAPK), inhibición/activación de adenilil ciclasa (AC), activación de fosfolipasa C (PLC)/movilización de Ca2+ , liberación de ácido araquidónico, activación de Akt/PKB y activación de pequeñas GTPasas, Rho, ROCK, Rac y Ras. Otras rutas que se ven afectadas por la activación del receptor de LPA incluyen, pero no se limitan a, adenosín monofosfato cíclico (AMPc), ciclo de división celular 42/proteína de unión a GTP (Cdc42), serina protooncogénica/treonina-proteína quinasa Raf (c-RAF), tirosina protooncogénica-proteína quinasa Src (c-src), quinasa regulada por señal extracelular (ERK), quinasa de adhesión focal (FAK), factor de intercambio de nucleótidos de guanina (GEF), glucógeno sintasa quinasa 3b (GSK3b), quinasa aminoterminal c-jun (JNK), MEK, cadena ligera de miosina II (MLC II), factor nuclear kB (NF-kB), activación del receptor de N-metil-D-aspartato (NMDA), fosfatidilinositol 3-quinasa (PI3K), proteína quinasa A (PKA), proteína quinasa C (PKC), sustrato 1 de toxina botulínica C3 relacionada con ras (RACl). La ruta real y el punto final realizado dependen de un abanico de variables que incluyen el uso del receptor, el tipo celular, el nivel de expresión de un receptor o proteína de señalización y la concentración de LPA. Casi todas las células, tejidos y órganos de mamíferos coexpresan varios subtipos de receptores de LPA, lo que indica que los receptores de LPA señalizan de manera cooperativa. LPA1 , LPA2y LPA3 comparten alta similitud de secuencia de aminoácidos.
El LPA se produce a partir de plaquetas activadas, adipocitos activados, células neuronales y otros tipos de células. El LPA sérico se produce por múltiples rutas enzimáticas que implican monoacilglicerol quinasa, fosfolipasa A i , fosfolipasa secretora A2 y lisofosfolipasa D (lysoPLD), incluyendo autotaxina. Varias enzimas están implicadas en la degradación de LPA: lisofosfolipasa, lípido fosfato fosfatasa y LPA acil transferasa tales como la endofilina. Las concentraciones de LPA en suero humano se estiman en 1-5 pM. El LPA sérico se une a la albúmina, a lipoproteínas de baja densidad u otras proteínas, que posiblemente protegen el LPA de la degradación rápida. Las especies moleculares de LPA con longitudes de cadena de acilo y saturación diferentes se producen de forma natural, incluyendo 1 -palmitoilo (16:0), 1-palmitoleoilo (16:1), 1-estearoilo (18:0), 1 -oleoilo (18:1), 1 -linoleoilo (18:2) y 1-araquidonilo (20:4) LPA. El LPA de alquilo cuantitativamente menor tiene actividades biológicas similares al LPA de acilo, y diferentes especies de LPA activan los subtipos de receptores de LPA con diversas efectividades.
RECEPTORES DE LPA
El LPA1 (anteriormente llamado VZG-1/EDG-2/mrec1.3) se acopla con tres tipos de proteínas G, G i/0, Gq y G12 /13. Mediante la activación de estas proteínas G, el LPA induce varias respuestas celulares a través de LPA1 incluyendo pero no limitado a: proliferación celular, activación del elemento de respuesta sérica (SRE), activación de la proteína quinasa activada por mitógeno (MAPK), inhibición de la adenilil ciclasa (AC), activación de la fosfolipasa C (PLC), movilización de Ca2+ , activación de Akt y activación de Rho.
En ratones adultos se observa una amplia expresión de LPA1 , con clara presencia en testículos, cerebro, corazón, pulmón, intestino delgado, estómago, bazo, timo y músculo esquelético. De manera similar, los tejidos humanos también expresan LPA1 ; está presente en cerebro, corazón, pulmón, placenta, colon, intestino delgado, próstata, testículos, ovario, páncreas, bazo, riñón, músculo esquelético y timo.
El LPA2 (EDG-4) también se combina con tres tipos de proteínas G, G i/0, Gq y G12 /13 , para mediar la señalización celular inducida por LPA. La expresión de LPA2 se observa en los testículos, riñón, pulmón, timo, bazo y estómago de ratones adultos y en los testículos humanos, páncreas, próstata, timo, bazo y leucocitos de sangre periférica. La expresión de LPA2 está regulada positivamente en diversas líneas celulares de cáncer y se han observado variantes transcripcionales de LPA2 humanas con mutaciones en la región 3' no traducida. La eliminación dirigida de LPA2 en ratones no ha mostrado ninguna anomalía fenotípica obvia, pero ha demostrado una pérdida significativa de señalización de LPA normal (por ejemplo, activación de PLC, movilización de Ca2+ y formación de fibras de estrés) en cultivos primarios de fibroblastos embrionarios de ratón (MEF). La creación de ratones doblemente nulos lpa1(-/-) lpa2(-/-) han desvelado que muchas respuestas inducidas por LPA, que incluyen proliferación celular, inhibición de
AC, activación de PLC, movilización de Ca2+ , activación de JNK y Akt y formación de fibras de estrés, están ausentes o gravemente reducidos en MEF doblemente nulos. Todas estas respuestas, a excepción de la inhibición de AC (la inhibición de AC está casi abolida en MEF LPA1 (-/-)), solo están parcialmente afectados en cualquiera de los MEF LPA1 (-/-) o LPA2 (-/-). El LPA2 contribuye a las respuestas de señalización mediadas por LPA normales en al menos algunos tipos de células (Choi et al, Biochemica et Biophysica Acta 2008, 1781, p531-539).
El LPA3 (EDG-7) es distinto del LPA1 y el LPA2 en su capacidad de emparejarse con Gi/0 y Gq pero no G12 /13 y es mucho menos sensible a las especies de LPA con cadenas de acilo saturadas. El LPA3 puede mediar la señalización pleiotrópica inducida por LPA que incluye la activación del PLC, movilización de Ca2+ , inhibición/activación de AC y activación de MAPK. La sobreexpresión de LPA3 en células de neuroblastoma conduce a alargamiento de neuritas, mientras que la de LPA1 o LPA2 da como resultado la retracción de neuritas y el redondeo celular cuando se estimula con LPA. La expresión de LPA3 se observa en testículos de ratones adultos, riñón, pulmón, intestino delgado, corazón, timo y cerebro. En seres humanos, se encuentra en el corazón, páncreas, próstata, testículos, pulmón, ovario y cerebro (corteza frontal, hipocampo y amígdala).
El LPA4 (p2yg/GPR23) es de secuencia divergente en comparación con LPA1 , LPA2 y LPA3 con similitud más cercana con el receptor del factor activador de plaquetas (PAF). El LPA4 media la movilización de Ca2+ inducida por LPA y la acumulación de AMPc y el acoplamiento funcional a la proteína G para la activación de AC, así como el acoplamiento a otras proteínas G. El gen de LPA4 gen se expresa en el ovario, páncreas, timo, riñón y músculo esquelético.
El LPA5 (GPR92) es miembro de la purinoagrupación de GPCR y estructuralmente está más estrechamente relacionado con LPA4. El LPA5 se expresa en el corazón humano, placenta, bazo, cerebro, pulmón e intestino. El LPA5 también muestra una expresión muy alta en el compartimento de linfocitos CD8+ del tracto gastrointestinal.
El LPA6 (p2y5) es miembro de la purinoagrupación de GPCR y estructuralmente está más estrechamente relacionado con LPA4. El LPA6 es un receptor de LPA acoplado a las rutas de señalización de G12/13-Rho y se expresa en las vainas de la raíz interna de los folículos pilosos humanos.
Actividad biológica ilustrativa
Curación de heridas
La curación normal de heridas se produce por una secuencia altamente coordinada de eventos en los cuales los factores solubles celulares y los componentes de la matriz actúan en concierto para reparar la lesión. La respuesta de curación puede describirse teniendo lugar en cuatro fases amplias, superpuestas-hemostasia, inflamación, proliferación y remodelación. Muchos factores de crecimiento y citocinas se liberan en el sitio de una herida para iniciar y perpetuar los procesos de curación de heridas.
Cuando se hieren, los vasos sanguíneos dañados activan las plaquetas. Las plaquetas activadas desempeñan papeles fundamentales en los procesos de reparación posteriores al liberar mediadores bioactivos para inducir la proliferación celular, la migración celular, la coagulación de la sangre y la angiogénesis. El LPA es uno de esos mediadores que se libera de las plaquetas activadas; esto induce la agregación plaquetaria junto con efectos mitogénicos/migratorios en las células circundantes, tales como las células endoteliales, células de músculo liso, fibroblastos y queratinocitos.
La aplicación tópica de LPA a heridas cutáneas en ratones promueve procesos de reparación (cierre de heridas y aumento del grosor neoepitelial) al aumentar la proliferación/migración celular sin afectar la inflamación secundaria.
La activación de fibroblastos dérmicos por factores de crecimiento y citocinas conduce a su posterior migración desde los bordes de la herida hacia la matriz provisional formada por el coágulo de fibrina, con lo cual los fibroblastos proliferan y comienzan a restaurar la dermis secretando y organizando la característica matriz extracelular (MEC) dérmica. El creciente número de fibroblastos dentro de la herida y la precipitación continua de la MEC mejora la rigidez de la matriz mediante la aplicación de pequeñas fuerzas de tracción al tejido de granulación recién formado. El aumento de la tensión mecánica, junto con el factor de crecimiento transformante p (TGFp), induce la expresión de actina de músculo liso a (a-SMA) y la posterior transformación de fibroblastos en miofibroblastos. Los miofibroblastos facilitan la remodelación del tejido de granulación mediante la contracción de miofibroblastos y a través de la producción de componentes de la MEC.
El LPA regula muchas funciones importantes de los fibroblastos en la curación de heridas, incluyendo la proliferación, la migración, la diferenciación y la contracción. La proliferación de fibroblastos se requiere en la curación de heridas para llenar una herida abierta. Por el contrario, la fibrosis se caracteriza por una intensa proliferación y acumulación de miofibroblastos que sintetizan activamente MEC y citocinas proinflamatorias. El LPA puede aumentar o suprimir la proliferación de tipos de células importantes en la curación de heridas, tales como células epiteliales y endoteliales (EC), macrófagos, queratinocitos y fibroblastos. Un papel para el LPA1 en la proliferación inducida por LPA se proporcionó por la observación de que se atenuó la proliferación de fibroblastos estimulada por LPA aislada de ratones nulos para el receptor de LPA1 (Mills et al, Nat Rev. Cancer 2003; 3: 582-591). El LPA induce cambios en el citoesqueleto que son integrales a la adhesión de fibroblastos, la migración, la diferenciación y la contracción.
Fibrosis
La lesión del tejido inicia una serie compleja de respuestas de curación de heridas del hospedador; si tiene éxito, estas respuestas restauran la estructura y función del tejido normal. Si no, estas respuestas pueden conducir a fibrosis tisular y pérdida de la función.
Para la mayoría de los órganos y tejidos, el desarrollo de fibrosis implica una multitud de eventos y factores. Las moléculas implicadas en el desarrollo de la fibrosis incluyen proteínas o péptidos (citocinas profibróticas, quimiocinas, metaloproteinasas etc.) y fosfolípidos. Los fosfolípidos implicados en el desarrollo de la fibrosis incluyen el factor de activación plaquetaria (FAP), fosfatidil colina, fosfato de esfingosina-1 (S1P) y ácido lisofosfatídico (LPA).
Una serie de distrofias musculares se caracteriza por una debilidad progresiva y desgaste de la musculatura y por una fibrosis extensa. Se ha demostrado que el tratamiento con LPA de mioblastos cultivados indujo una expresión significativa del factor de crecimiento del tejido conectivo (CTGF). El CTGF posteriormente induce colágeno, la expresión de fibronectina e integrina e induce la desdiferenciación de estos mioblastos. El tratamiento de diversos tipos de células con LPA induce una inducción reproducible y de alto nivel de CTGF (JP Pradere, et al., LPA1 receptor activation promotes renal interstitial fibrosis, J. Am. Soc. Nephrol. 18 (2007) 3110-3118; N. Wiedmaier, et al., Int J Med Microbiol; 298(3-4):231-43, 2008). El CTGF es una citocina profibrótica, que señaliza después y en paralelo con TGFp.
La expresión de CTGF por células epiteliales gingivales, que están implicadas en el desarrollo de la fibromatosis gingival, se descubrió que estaba exacerbada por el tratamiento con LPA (A. Kantarci, et al., J. Pathol. 210 (2006) 59 66).
El LPA está asociado a la progresión de la fibrosis del hígado. In vitro, el LPA induce la proliferación de células estrelladas y hepatocitos. Estas células activadas son el principal tipo de célula responsable de la acumulación de MEC en el hígado. Adicionalmente, Los niveles plasmáticos de LPA aumentan durante la fibrosis hepática inducida por CCl4 en roedores o en fibrosis hepática inducida por el virus de la hepatitis C en seres humanos (N. Watanabe, et al., Plasma lysophosphatidic acid level and serum autotaxin activity are increased in liver injury in rats in relation to its severity, Life Sci. 81 (2007) 1009-1015; N.Watanabe, et al., J. Clin. Gastroenterol. 41 (2007) 616-623).
Se ha informado un aumento de las concentraciones de fosfolípidos en el líquido de lavado broncoalveolar en conejos y roedores inyectados con bleomicina (K. Kuroda, et al., Phospholipid concentration in lung lavage fluid as biomarker for pulmonary fibrosis, Inhal. Toxicol. 18 (2006) 389-393; K. Yasuda, et al., Lung 172 (1994) 91-102).
El LPA está asociado a enfermedades del corazón y remodelación micocárdica. Los niveles séricos de LPA aumentan después del infarto de miocardio en pacientes y el LPA estimula la proliferación de fibroblastos cardíacos en ratas y la producción de colágeno (Chen et al. FEBSLett. 21 de agosto de 2006;580(19):4737-45).
Fibrosis pulmonar
En el pulmón, las respuestas aberrantes de curación de heridas a las lesiones contribuyen a la patogénesis de las enfermedades pulmonares fibróticas. Las enfermedades pulmonares fibróticas, tales como la fibrosis pulmonar idiopática (FPI), se asocian a alta morbilidad y mortalidad.
El LPA es un mediador importante del reclutamiento de fibroblastos en la fibrosis pulmonar. El LPA y LPA1 desempeñan papeles patogénicos clave en la fibrosis pulmonar. La actividad quimioatrayente de fibroblastos desempeña un papel importante en los pulmones en pacientes con fibrosis pulmonar. Los efectos profibróticos de la estimulación del receptor de LPA1 se explica por la fuga vascular mediada por el receptor de LPAi y el aumento del reclutamiento de fibroblastos, ambos eventos profibróticos. La ruta LPA-LPA1 tiene un papel en la mediación de la migración de fibroblastos y la fuga vascular en la FPI. El resultado final es el proceso de curación aberrante que caracteriza a esta afección fibrótica.
El receptor de LPA1 es el receptor de LPA más altamente expresado en fibroblastos obtenidos de pacientes con IPF. Adicionalmente, el BAL obtenida de pacientes con FPI indujo quimiotaxis de fibroblastos de pulmón fetal humano que fue bloqueada por el antagonista dual del receptor LPA1 -LPA3 Ki16425. En un modelo experimental de ratón con lesión pulmonar inducida por bleomicina, se demostró que los niveles de LPA eran altos en las muestras de lavado broncoalveolar en comparación con los controles no expuestos. Los ratones con inactivación de LPA1 están protegidos de la fibrosis después de la exposición a bleomicina con acumulación reducida de fibroblastos y fuga vascular. En sujetos humanos con FPI, se observaron altos niveles de LPA en muestras de lavado broncoalveolar en comparación con controles sanos. El aumento de la actividad quimiotáctica de fibroblastos en estas muestras fue inhibido por el Ki16425, lo que indica que la migración de fibroblastos está mediada por la vía del receptor o receptores LPA-LPA (Tager et al. Nature Medicine, 2008, 14, 45-54).
La ruta LPA-LPA1 es crucial en el reclutamiento de fibroblastos y la fuga vascular en la fibrosis pulmonar.
La activación del TGF-p latente por la integrina avp6 juega un papel crítico en el desarrollo de la lesión pulmonar y la fibrosis (Munger et al. Cell, vol. 96, 319-328, 1999). LPA induce la activación de TGF-p mediada por avp6 en células epiteliales de pulmón humano (Xu et al. Am. J. Pathology, 2009, 174, 1264-1279). La activación de TGF-p mediada por avp6 inducida por LPA está mediada por el receptor LPA2. La expresión del receptor LPA2 aumenta en las células epiteliales y las células mesenquimales en áreas de fibrosis pulmonar de pacientes con FPI en comparación con el tejido pulmonar humano normal. La ruta LPA-LPA2 contribuye a la activación de la vía TGF-p en la fibrosis pulmonar. En algunas realizaciones, los compuestos que inhiben el LPA2 muestran efectividad en el tratamiento de la fibrosis pulmonar. En algunas realizaciones, los compuestos que inhiben tanto LPA1 como LPA2 muestran una efectividad mejorada en el tratamiento de la fibrosis pulmonar en comparación con los compuestos que inhiben solo LPA1 o LPA2.
Se demostró que el antagonista de LPA1 BMS-986020 reduce significativamente la tasa de disminución de la FVC (capacidad vital forzada) en un ensayo clínico de 26 semanas en pacientes con IPF (Palmer et al., Chest, 2018, 154, 1061-1069).
Fibrosis renal
El LPA y LPA1 están implicados en la etiología de la fibrosis renal. El LPA tiene efectos sobre la proliferación y contracción de las células mesangiales glomerulares y, por lo tanto, se ha implicado en la glomerulonefritis proliferativa (C.N. Inoue, et al., Clin. Sci. (Colch.) 1999, 96, 431-436). En un modelo animal de fibrosis renal [obstrucción ureteral unilateral (UUO)], se descubrió que los receptores de LPA renales se expresan en condiciones basales con un orden de expresión de LPA2>LPA3=l Pa -i>>LPA4. Este modelo imita de manera acelerada el desarrollo de fibrosis renal incluyendo la inflamación renal, la activación de fibroblastos y la acumulación de matriz extracelular en el tubulointersticio. La UUO indujo significativamente la expresión del receptor de LPA1. Esto fue paralelo a la producción renal de LPA (aumento de 3,3 veces) en medios condicionados a partir de explantes renales. Los riñones contralaterales no mostraron cambios significativos en la liberación de LPA y la expresión de los receptores de LPA. Esto muestra que se cumple un requisito previo para una acción de LPA en la fibrosis: producción de un ligando (LPA) e inducción de uno de sus receptores (el receptor de LPA1) (J.P. Pradere et al., Biochimica et Biophysica Acta, 2008, 1781, 582-587).
En ratones donde el receptor de LPA1 se inactivó (LPA1 (-/-), el desarrollo de fibrosis renal se atenuó significativamente. Los ratones con UUO tratados con el antagonista del receptor de LPA Ki 16425 se parecían mucho al perfil de los ratones LPA1 (-/-).
El LPA puede participar en la acumulación intraperitonial de monocitos/macrófagos y el LPA puede inducir la expresión de la citocina profibrótica CTGF en cultivos primarios de fibroblastos humanos (J.S. Koh, et al., J. Clin. Invest., 1998, 102, 716-727).
El tratamiento con LPA de una línea celular renal epitelial de ratón, MCT, indujo un rápido aumento en la expresión de la citocina profibrótica CTGF. CTGF juega un papel crucial en la fibrosis tubulointersticial inducida por u Uo (TIF) y está implicada en la actividad profibrótica de TGFp. Esta inducción se suprimió casi por completo mediante el tratamiento conjunto con el antagonista del receptor de LPA Ki 16425. En un aspecto, la actividad profibrótica de LPA en el riñón resulta de una acción directa de LPA en las células renales que implican la inducción de CTGF.
Fibrosis hepática
El LPA está implicado en la enfermedad hepática y la fibrosis. Los niveles plasmáticos de LPA y autotaxina sérica (enzima responsable de la producción de LPA) están elevados en pacientes con hepatitis y modelos animales de lesión hepática en correlación con el aumento de la fibrosis. El LPA también regula la función de las células hepáticas. Los receptores de LPA1 y LPA2 se expresan por células estrelladas hepáticas de ratón y el LPA estimula la migración de miofibroblastos hepáticos.
Fibrosis ocular
El LPA participa en la curación de heridas en el ojo. Los receptores de LPA1 y LPA3 son detectables en las células epiteliales corneales, queratocitos y células endoteliales de conejos normales y la expresión de LPA1 y LPA3 aumenta en las células epiteliales corneales después de una lesión.
El LPA y sus homólogos están presentes en el humor acuoso y en el líquido de la glándula lagrimal del ojo de conejo y estos niveles aumentan en un modelo de lesión corneal de conejo.
El LPA induce la formación de fibra de estrés de actina en células endoteliales y epiteliales corneales de conejo y promueve la contracción de fibroblastos corneales. El LPA también estimula la proliferación de células epiteliales pigmentadas de la retina humana.
Fibrosis cardíaca
El LPA está implicado en el infarto de miocardio y la fibrosis cardíaca. Los niveles séricos de LPA aumentan en pacientes después de un infarto de miocardio (IM) y el LPA estimula la proliferación y la producción de colágeno (fibrosis) por los fibroblastos cardíacos de rata. Ambos receptores LPA1 y LPA3 se expresan altamente en el tejido cardíaco humano.
Tratamiento de fibrosis
Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en un método para tratar o prevenir la fibrosis en un mamífero. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en un método para tratar la fibrosis de un órgano o tejido en un mamífero. En un aspecto es un compuesto de la invención para uso en un método para prevenir una condición de fibrosis en un mamífero, comprendiendo el método administrar al mamífero con riesgo de desarrollar una o más condiciones de fibrosis una cantidad terapéuticamente eficaz de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo. En un aspecto, el mamífero ha estado expuesto a una o más condiciones ambientales que aumentan el riesgo de fibrosis de un órgano o tejido. En un aspecto, el mamífero ha estado expuesto a una o más condiciones ambientales que aumentan el riesgo de fibrosis pulmonar, hepática o renal. En un aspecto, el mamífero tiene una predisposición genética a desarrollar fibrosis de un órgano o tejido. Un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, puede administrarse a un mamífero para prevenir o minimizar la cicatrización después de una lesión, incluyendo cirugía.
Los términos "fibrosis" o "trastorno fibrosante" como se usan en el presente documento, se refiere a afecciones que están asociadas a la acumulación anormal de células y/o fibronectina y/o colágeno y/o aumento del reclutamiento de fibroblastos e incluyen, pero no se limitan a, fibrosis de órganos o tejidos individuales tales como el corazón, riñón, hígado, articulaciones, pulmón, tejido pleural, tejido peritoneal, piel, córnea, retina, tracto musculoesquelético y digestivo.
Los ejemplos de enfermedades, los trastornos o afecciones que implican fibrosis incluyen, pero no se limitan a: Enfermedades pulmonares asociadas a fibrosis, por ejemplo, fibrosis pulmonar idiopática, fibrosis pulmonar secundaria a enfermedad inflamatoria sistémica tales como artritis reumatoide, esclerodermia, lupus, alveolitis fibrosante criptogénica, fibrosis inducida por radiación, enfermedad pulmonar obstructiva crónica (EPOC), esclerodermia, asma crónico, silicosis, fibrosis pulmonar o pleural inducida por asbesto, lesión pulmonar aguda y dificultad respiratoria aguda (incluyendo neumonía bacteriana inducida, trauma inducido, neumonía vírica inducida, ventilador inducido, sepsis no pulmonar inducida y aspiración inducida); Nefropatías crónicas asociadas a lesiones/fibrosis (fibrosis renal), por ejemplo, glomerulonefritis secundaria a enfermedades inflamatorias sistémicas tales como lupus y esclerodermia, diabetes, nefritis glomerular, esclerosis glomerular segmentaria focal, nefropatía de IgA, hipertensión, aloinjerto y Alport; Fibrosis intestinal, por ejemplo, esclerodermia y fibrosis intestinal inducida por radiación; Fibrosis del hígado, por ejemplo, cirrosis, fibrosis del hígado inducida por alcohol, esteatohepatitis no alcohólica (NASH), lesión del conducto biliar, cirrosis biliar primaria, infección o fibrosis del hígado inducida por virus (por ejemplo, infección crónica por VHC) y hepatitis autoinmune; Fibrosis de cabeza y cuello, por ejemplo, inducida por radiación; Cicatrización corneal, por ejemplo, LASIK (queratomileusis in situ asistida por láser), trasplante de córnea y trabeculectomía; Cicatrices hipertróficas y queloides, por ejemplo, quemaduras inducidas o quirúrgicas; y otras enfermedades fibróticas, por ejemplo, sarcoidosis, esclerodermia, lesión de la médula espinal/fibrosis, mielofibrosis, restenosis vascular, ateroesclerosis, arteriesclerosis, granulomatosis de Wegener, enfermedad mixta del tejido conectivo y enfermedad de Peyronie.
Un mamífero que padece una de las siguientes enfermedades, trastornos o afecciones ilustrativos no limitantes pueden beneficiarse de la terapia con un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo: ateroesclerosis, trombosis, cardiopatía, vasculitis, formación de tejido cicatricial, reestenosis, flebitis, EPOC (enfermedad pulmonar obstructiva crónica), hipertensión pulmonar, fibrosis pulmonar, inflamación pulmonar, adherencias intestinales, fibrosis de vejiga y cistitis, fibrosis de las fosas nasales, sinusitis, inflamación mediada por neutrófilos y fibrosis mediada por fibroblastos.
Un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, puede administrarse a un mamífero con fibrosis de un órgano o tejido o con una predisposición a desarrollar fibrosis de un órgano o tejido con uno o más agentes que se usan para tratar la fibrosis. El uno o más agentes pueden incluir corticosteroides. El uno o más agentes pueden incluir inmunosupresores. El uno o más agentes pueden incluir antagonistas de células B. El uno o más agentes pueden incluir uteroglobina.
Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en un método para tratar un trastorno dermatológico en un mamífero. La frase "trastorno dermatológico", como se usa en el presente documento se refiere a un trastorno de la piel. Dichos trastornos dermatológicos incluyen, pero no se limitan a, trastornos proliferativos o inflamatorios de la piel tales como, dermatitis atópica, trastornos ampulosos, colagenosis, psoriasis, esclerodermia, lesiones psoriásicas, dermatitis, dermatitis de contacto, eccema, urticaria, rosácea, la curación de heridas, formación de cicatrices, cicatrices hipertróficas, queloides, enfermedad de Kawasaki, rosácea, síndrome de Sjogren-Larsso, urticaria. Un aspecto proporciona un compuesto de
Fórmula (la) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en un método para tratar la esclerosis sistémica.
Dolor
Como se libera LPA después de una lesión tisular, el LPA1 juega un papel importante en el inicio del dolor neuropático. LPA1 , a diferencia de LPA2 o LPA3, se expresa tanto en el ganglio de la raíz dorsal (DRG) como en las neuronas de la raíz dorsal. Uso del oligodesoxinucleótido antisentido (AS-ODN) para ratones nulos para LPA1 y LPA1 , se descubrió que la alodinia mecánica inducida por LPA y la hiperalgesia están mediadas de una manera dependiente de LPA1. El LPA1 y la activación de Rho-ROCK posterior juegan un papel en el inicio de la señalización del dolor neuropático. El tratamiento previo con la exoenzima C3 de Clostridium botulinum (BoTXC3, inhibidor de Rho) o Y-27632 (inhibidor de ROCK) abolió por completo la alodinia y la hiperalgesia en ratones con lesiones nerviosas. El LPA también indujo la desmielinización de la raíz dorsal, que se evitó por BoTXC3. La desmielinización de la raíz dorsal por lesión no se observó en ratones nulos a LPA1 o ratones de tipo silvestre inyectados con AS-ODN. La señalización de LPA parece inducir importantes marcadores de dolor neuropático tales como la proteína quinasa Cy (PKCy) y una subunidad a251 del canal de calcio dependiente de voltaje (Caa281) de una manera dependiente de LPA1 y de Rho (M. Inoue, et al., Initiation of neuropathic pain requires lysophosphatidic acid receptor signaling, Nat. Med. 10 (2004) 712-718).
Un aspecto proporciona un compuesto de Fórmula (la) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de dolor en un mamífero. En un aspecto, el dolor es dolor agudo o dolor crónico. En otro aspecto, el dolor es dolor neuropático.
Un aspecto proporciona un compuesto de Fórmula (la) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de fibromialgia. En un aspecto, la fibromialgia proviene de la formación de tejido cicatricial fibroso en músculos contráctiles (voluntarios). La fibrosis se une al tejido e inhibe el flujo sanguíneo, dando como resultado dolor.
Cáncer
La señalización del receptor de lisofosfolípidos juega un papel en la etiología del cáncer. El ácido lisofosfatídico (LPA) y sus receptores acoplados a proteínas G (GPCR) LPA1 , LPA2 y/o LPA3 desempeñan un papel en el desarrollo de varios tipos de cánceres. El inicio, la progresión y la metástasis del cáncer implican varios procesos simultáneos y secuenciales incluyendo la proliferación y el crecimiento y supervivencia celulares y anti-apoptosis, migración de células, la penetración de células extrañas en capas y/u órganos celulares definidos, y promoción de la angiogénesis. El control de cada uno de estos procesos mediante la señalización de LPA en condiciones fisiológicas y fisiopatológicas subraya la potencial utilidad terapéutica de la modulación de las vías de señalización de LPA para el tratamiento del cáncer, especialmente a nivel de los receptores LPA o ATX/lysoPLD. La autotaxina (ATX) es una enzima prometastática aislada inicialmente del medio condicionado de células de melanoma humano que estimula una miríada de actividades biológicas, incluyendo la angiogénesis y la promoción del crecimiento celular, la migración, la supervivencia y la diferenciación a través de la producción de LPA (Mol Cancer Ther 2008;7(10):3352-62).
El LPA señaliza a través de sus propios GPCR conduciendo a la activación de múltiples vías efectoras posteriores. Tales rutas efectoras posteriores juegan un papel en el cáncer. El LPA y sus GPCR están vinculados al cáncer a través de las principales rutas de señalización oncogénicas.
El LPA contribuye a la tumorigénesis al aumentar la motilidad y la invasividad de las células. El LPA ha sido implicado en el inicio o la progresión del cáncer de ovario. El LPA está presente en concentraciones significativas (2-80 pM) en el líquido ascítico de pacientes con cáncer de ovario. Las células de cáncer de ovario producen constitutivamente mayores cantidades de LPA en comparación con las células epiteliales normales de la superficie ovárica, el precursor del cáncer epitelial de ovario. Los niveles elevados de LPA también se detectan en plasma de pacientes con cánceres de ovario en etapa temprana en comparación con los controles. Los receptores de LPA (LPA2 y LPA3 ) también se sobreexpresan en las células de cáncer de ovario en comparación con las células epiteliales de la superficie ovárica normal. El LPA estimula la expresión de Cox-2 a través de la activación transcripcional y la mejora postranscripcional del ARNm de Cox-2 en células de cáncer de ovario. Las prostaglandinas producidas por Cox-2 se han implicado en varios cánceres humanos y la inhibición farmacológica de la actividad de Cox-2 reduce el desarrollo del cáncer de colon y disminuye el tamaño y el número de adenomas en pacientes con poliposis adenomatosa familiar. El LPA también se ha implicado en la iniciación o progresión del cáncer de próstata, cáncer de mama, melanoma, cáncer de cabeza y cuello, cáncer de intestino (cáncer colorrectal), cáncer de tiroides y otros tipos de cáncer (Gardell et al, Trends in Molecular Medicine, vol. 12, n.°2, p 65-75, 2006; Ishii et al, Annu. Rev. Biochem, 73, 321-354, 2004; Mills et al., Nat. Rev. Cancer, 3, 582-591,2003; Murph et al., Biochimica et Biophysica Acta, 1781, 547-557, 2008).
Las respuestas celulares a LPA están mediadas a través de los receptores de ácido lisofosfatídico. Por ejemplo, los receptores de LPA median tanto la migración como la invasión de las líneas celulares de cáncer de páncreas: un antagonista de LPA1 y LPA3 (Ki16425) y ARNip específico de LPA1 bloquearon eficazmente la migración in vitro en respuesta a LPA y líquido peritoneal (ascitis) de pacientes con cáncer de páncreas; además, Ki 16425 bloqueó la actividad de invasión inducida por LPA y ascitis de una línea celular de cáncer pancreático metastásico altamente
peritoneal (Yamada et al, J. Biol. Chem., 279, 6595-6605, 2004).
Las líneas celulares de carcinoma colorrectal muestran una expresión significativa de ARNm de LPA1 y responden al LPA mediante la migración celular y la producción de factores angiogénicos. La sobreexpresión de los receptores de LPA tiene un papel en la patogénesis del cáncer de tiroides. El LPA3 se clonó originalmente de células de cáncer de próstata, concordante con la capacidad de LPA para inducir la proliferación autocrina de células de cáncer de próstata.
El LPA tiene papeles estimulantes en la progresión del cáncer en muchos tipos de cáncer. El LPA se produce a partir de e induce la proliferación de líneas celulares de cáncer de próstata. El LPA induce la proliferación de células DLD1 de carcinoma de colon humano, la migración, la adhesión y la secreción de factores angiogénicos a través de la señalización por LPA1. En otras líneas celulares de carcinoma de colon humano (HT29 y WiDR), el LPA mejora la proliferación celular y la secreción de factores angiogénicos. En otras líneas celulares de cáncer de colon, la activación del receptor de LPA2 y LPA3 da como resultado la proliferación de las células. La manipulación genética o farmacológica del metabolismo de LPA, el bloqueo específico de la señalización del receptor y/o la inhibición de las vías de transducción de señal posteriores, representan enfoques para terapias contra el cáncer.
Se ha informado que el LPA y otros fosfolípidos estimulan la expresión de interleucina-8 (IL-8) en líneas celulares de cáncer de ovario. En algunas realizaciones, las altas concentraciones de IL-8 en el cáncer de ovario se correlacionan con una pobre respuesta inicial a la quimioterapia y con un mal pronóstico, respectivamente. En modelos animales, la expresión de IL-8 y otros factores de crecimiento tales como el factor de crecimiento endotelial vascular (VEGF) se asocia a una mayor tumorigenicidad, formación de ascitis, angiogénesis e invasividad de las células de cáncer de ovario. IL-8 puede ser un modulador importante de la progresión del cáncer, la resistencia a fármacos y el pronóstico en cáncer de ovario. Un compuesto de Fórmula (Ia) o (Ib) puede inhibir o reducir la expresión de IL-8 en líneas celulares de cáncer de ovario.
Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de cáncer. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de enfermedades proliferativas malignas y benignas. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en un método para prevenir o reducir la proliferación de células tumorales, la invasión y la metástasis de carcinomas, el mesotelioma pleural (Yamada, Cancer Sci., 2008, 99(8), 1603 1610) o el mesotelioma peritoneal, dolor por cáncer, metástasis óseas (Boucharaba et al, J. Clin. Invest., 2004, 114(12), 1714-1725; Boucharaba et al, Proc. Natl. acad. Sci., 2006, 103(25) 9643-9648). Un aspecto proporciona un compuesto de la invención para su uso en un método para tratar el cáncer en un mamífero, comprendiendo el método administrar al mamífero un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, y un segundo agente terapéutico, en donde el segundo agente terapéutico es un agente anticáncer.
El término "cáncer", como se usa en el presente documento se refiere a un crecimiento anómalo de las células que tienden a proliferar de una manera incontrolada y, en algunos casos, a metastatizar (propagarse). Los tipos de cáncer incluyen, pero no se limitan a, tumores sólidos (tales como aquellos de la vejiga, intestino, cerebro, mama, endometrio, corazón, riñón, pulmón, tejido linfático (linfoma), ovario, páncreas u otro órgano endocrino (tiroides), próstata, piel (melanoma o cáncer de células basales) o tumores hematológicos (tales como las leucemias) en cualquier etapa de la enfermedad con o sin metástasis.
Algunos ejemplos adicionales no limitantes de cánceres incluyen, leucemia linfoblástica aguda, leucemia mieloide aguda, carcinoma adrenocortical, cáncer de ano, cáncer del apéndice, astrocitomas, tumor rabdoide/teratoide atípico, carcinoma de células basales, cáncer del conducto biliar, cáncer de vejiga, cáncer óseo (por ejemplo, osteosarcoma e histiocitoma fibroso maligno), glioma del tronco encefálico, tumores cerebrales, tumores de cerebro y de médula espinal, cáncer de mama, tumores bronquiales, linfoma de Burkitt, cáncer de cuello uterino, leucemia linfocítica crónica, leucemia mielógena crónica, cáncer de colon, cáncer colorrectal, craneofaringioma, linfoma cutáneo de linfocitos T, tumores embrionarios, cáncer de endometrio, ependimoblastoma, ependimoma, cáncer de esófago, familia de tumores de sarcoma de Ewing, cáncer ocular, retinoblastoma, cáncer de vesícula biliar, cáncer gástrico (estómago), tumor carcinoide gastrointestinal, tumor del estroma gastrointestinal (TEGI), tumor de células del estroma gastrointestinal, tumor de células germinales, glioma, tricoleucemia, cáncer de cabeza y cuello, cáncer hepatocelular (hígado), linfoma de Hodgkin, cáncer hipofaríngeo, melanoma intraocular, tumores de células de los islotes (páncreas endocrino), sarcoma de Kaposi, cáncer de riñón, histiocitosis de células de Langerhans, cáncer de laringe, leucemia, Leucemia linfoblástica aguda, leucemia mieloide aguda, leucemia linfocítica crónica, leucemia mielógena crónica, tricoleucemia, cáncer de hígado, cáncer de pulmón no microcítico, cáncer microcítico de pulmón, linfoma de Burkitt, linfoma cutáneo de linfocitos T, linfoma de Hodgkin, linfoma no hodgkiniano, linfoma, macroglobulinemia de Waldenstrom, meduloblastoma, meduloepitelioma, melanoma, mesotelioma, cáncer de boca, leucemia mielógena crónica, leucemia mieloide, mieloma múltiple, cáncer nasofaríngeo, neuroblastoma, linfoma no hodgkiniano, cáncer de pulmón no microcítico, cáncer oral, cáncer orofaríngeo, osteosarcoma, histiocitoma fibroso maligno de hueso, cáncer de ovario, cáncer epitelial de ovario, tumor de células germinales ováricas, tumor ovárico de bajo potencial maligno, cáncer de páncreas, papilomatosis, cáncer paratiroideo, cáncer de pene, cáncer faríngeo, tumores del parénquima pineal de diferenciación intermedia, pineoblastoma y tumores neuroectodérmicos primitivos supratentoriales, tumor de la pituitaria, neoplasia de células plasmáticas/mieloma múltiple, blastoma pleuropulmonar, linfoma primario del sistema
nervioso central, cáncer de próstata, cáncer de recto, cáncer de células renales (riñón), retinoblastoma, rabdomiosarcoma, cáncer de las glándulas salivales, sarcoma, familia de tumores de sarcoma de Ewing, sarcoma, de Kaposi, síndrome de Sezary, cáncer de piel, cáncer microcítico de pulmón, cáncer del intestino delgado, sarcoma de tejidos blandos, carcinoma de células escamosas, cáncer de estómago (gástrico), tumores neuroectodérmicos primitivos supratentoriales, linfoma de linfocitos T, cáncer de testículo, cáncer de garganta, timoma y carcinoma tímico, cáncer de tiroides, cáncer de uretra, cáncer de útero, sarcoma uterino, cáncer de vagina, cáncer de vulva, macroglobulinemia de Waldenstrom, tumor de Wilms.
El aumento de las concentraciones de LPA y vesículas en la ascitis de pacientes con cáncer de ovario y derrames de cáncer de mama indican que podría ser un marcador de diagnóstico precoz, un indicador pronóstico o un indicador de respuesta a la terapia (Mills et al, Nat. Rev. Cancer., 3, 582-591, 2003; Sutphen et al., Cancer Epidemiol. Biomarkers Prev. 13, 1185-1191, 2004). Las concentraciones de LPA son consistentemente más altas en muestras de ascitis que en muestras de plasma coincidentes.
Trastornos respiratorios y alérgicos
El LPA puede ser un contribuyente a la patogénesis de las enfermedades respiratorias. La enfermedad respiratoria puede ser asma. Los efectos proinflamatorios del LPA incluyen la desgranulación de mastocitos, la contracción de las células del músculo liso y la liberación de citocinas de las células dendríticas. Las células del músculo liso de las vías respiratorias, las células epiteliales y los fibroblastos de pulmón muestran respuestas a LPA. El LPA induce la secreción de IL-8 de las células epiteliales bronquiales humanas. La IL-8 se encuentra en concentraciones aumentadas en fluidos BAL de pacientes con asma, enfermedad pulmonar obstructiva crónica, sarcoidosis pulmonar y síndrome de dificultad respiratoria aguda y se ha demostrado que la IL-8 exacerba la inflamación de las vías aéreas y la remodelación de las vías aéreas de los asmáticos. Se ha demostrado que todos los receptores LPA1 , LPA2 y LPA3 contribuyen a la producción de IL-8 inducida por LPA. Los estudios que clonaron múltiples GPCR activados por LPA permitieron demostrar la presencia de ARNm para el LPA1 , LPA2 y LPA3 en el pulmón (J.J.A. Contos, et al., Mol. Pharmacol. 58, 1188-1196, 2000).
La liberación de LPA de las plaquetas activadas en un sitio de lesión y su capacidad para promover la proliferación y contracción de fibroblastos son características del LPA como mediador de la reparación de heridas. En el contexto de la enfermedad de las vías respiratorias, el asma es una enfermedad inflamatoria en donde los procesos inapropiados de "reparación" de la vía aérea conducen a una "remodelación" estructural de la vía aérea. En el asma, las células de las vías respiratorias están sujetas a lesiones continuas debido a diversos ataques, incluyendo alérgenos, contaminantes, otros agentes ambientales inhalados, bacterias y virus, que conducen a la inflamación crónica que caracteriza al asma.
En el individuo asmático, la liberación de mediadores de reparación normales, incluyendo LPA, puede ser exagerada o las acciones de los mediadores de reparación pueden prolongarse de manera inapropiada y conducen a una remodelación inadecuada de las vías respiratorias. Las principales características estructurales de la vía aérea remodelada observada en el asma incluyen una lámina reticular engrosada (la estructura similar a una membrana basal justo debajo de las células epiteliales de la vía aérea), mayor número y activación de miofibroblastos, engrosamiento de la capa muscular lisa, aumento del número de glándulas mucosas y secreciones mucosas y alteraciones en el tejido conectivo y el lecho capilar a lo largo de la pared de las vías respiratorias. El LPA puede contribuir a estos cambios estructurales en la vía aérea. El LPA puede estar implicado en la hiperreactividad aguda de las vías respiratorias en el asma. La luz de la vía aérea asmática remodelada es más estrecha debido al engrosamiento de la pared de la vía aérea, disminuyendo de esta manera el flujo de aire. El LPA puede contribuir a la remodelación estructural a largo plazo y la hiperreactividad aguda de la vía aérea asmática. El LPA puede contribuir a la hiperreactividad que es una característica principal de las exacerbaciones agudas del asma.
Además de las respuestas celulares mediadas por LPA, varios de los componentes de la vía de señalización de LPA que conducen a estas respuestas son relevantes para el asma. La regulación positiva del receptor de EGF está inducida por LPA y también se observa en las vías respiratorias asmáticas (M. Amishima, et al., Am. J. Respir. Crit. Care Med. 157, 1907-1912, 1998). La inflamación crónica contribuye al asma y se sabe que varios de los factores de transcripción activados por LPA están implicados en la inflamación (Ediger et al., Eur Respir J 21:759-769, 2003).
La proliferación y contracción de fibroblastos y la secreción de matriz extracelular estimulada por LPA puede contribuir a las características fibroproliferativas de otras enfermedades de las vías respiratorias, tales como la fibrosis peribronquiolar presente en la bronquitis crónica, enfisema y enfermedad pulmonar intersticial. El enfisema también se asocia a una fibrosis leve de la pared alveolar, una característica que se cree que representa un intento de reparar el daño alveolar. El LPA puede desempeñar un papel en las enfermedades pulmonares intersticiales fibróticas y la bronquiolitis obliterante, donde se incrementan tanto el colágeno como los miofibroblastos. El LPA puede estar implicado en varios de los diversos síndromes que constituyen la enfermedad pulmonar obstructiva crónica.
La administración de LPA in vivo induce hiperreactividad de las vías respiratorias, respuestas de picazón-rasguño, infiltración y activación de eosinófilos y neutrófilos, remodelación vascular y respuestas flexoras nociceptivas. El LPA también induce la liberación de histamina de mastocitos de ratón y rata. En una reacción alérgica aguda, la histamina
induce varias respuestas, como la contracción del músculo liso, exudación de plasma y producción de moco. La exudación de plasma es importante en la vía aérea, porque la fuga y el posterior edema de la pared de la vía aérea contribuyen al desarrollo de la hiperreactividad de la vía aérea. La exudación de plasma progresa a tumefacción conjuntival en el trastorno alérgico ocular y obstrucción nasal en la rinitis alérgica (Hashimoto et al., J Pharmacol Sci 100, 82 - 87, 2006). La exudación plasmática inducida por LPA puede estar mediada por la liberación de histamina de los mastocitos a través de uno o más receptores de LPA. El receptor o receptores de LPA pueden incluir LPA1 y/o LPA3. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de diversos trastornos alérgicos en un mamífero. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de enfermedades, trastornos o afecciones respiratorios en un mamífero. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento de asma en un mamífero. Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento del asma crónica en un mamífero.
La frase "enfermedad respiratoria", como se usa en el presente documento, se refiere a enfermedades que afectan los órganos implicados en la respiración, tales como la nariz, garganta, laringe, trompas de Eustaquio, tráquea, bronquios, pulmones, músculos relacionados (por ejemplo, diafragma e intercostales) y nervios. Las enfermedades respiratorias incluyen, pero no se limitan a, asma, síndrome de dificultad respiratoria en el adulto y asma alérgico (extrínseco), asma no alérgico (intrínseco), asma grave agudo, asma crónico, asma clínico, asma nocturno, asma inducido por alérgenos, asma sensible a aspirina, asma inducido por ejercicio, hiperventilación isocápnica, asma de aparición en la niñez, asma de aparición en el adulto, asma variante por tos, asma laboral, asma resistente a esteroides, asma estacional, rinitis alérgica estacional, rinitis alérgica perenne, enfermedad pulmonar obstructiva crónica, incluyendo bronquitis crónica o enfisema, hipertensión pulmonar, fibrosis pulmonar intersticial y/o inflamación de las vías respiratorias y fibrosis quística, e hipoxia.
El término "asma", como se usa en el presente documento, se refiere a cualquier trastorno de los pulmones caracterizado por variaciones en el flujo de gas pulmonar asociado a la constricción de la vía aérea por cualquier causa (intrínseca, extrínseca, o ambas; alérgica o no alérgica). El término asma puede usarse con uno o más adjetivos para indicar la causa.
Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento o prevención de la enfermedad pulmonar obstructiva crónica en un mamífero que comprende administrar al mamífero al menos una vez una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo. Además, la enfermedad pulmonar obstructiva crónica incluye, pero no se limita a, bronquitis crónica o enfisema, hipertensión pulmonar, fibrosis pulmonar intersticial y/o inflamación de las vías respiratorias y fibrosis quística.
Sistema nervioso
El sistema nervioso es un lugar importante para la expresión de LPA1 ; allí está regulado espacial y temporalmente a lo largo del desarrollo del cerebro. Los oligodendrocitos, las células mielinizantes en el sistema nervioso central (SNC), expresan LPA1 en mamíferos. Además, las células de Schwann, las células mielinizantes del sistema nervioso periférico, también expresa LPA1 , que participa en la regulación de la supervivencia y la morfología de las células de Schwann. Estas observaciones identifican funciones importantes para la señalización de LPA mediada por receptor en la neurogénesis, la supervivencia celular y la mielinización.
La exposición de las líneas celulares del sistema nervioso periférico a LPA produce una retracción rápida de sus procesos que resulta en el redondeo celular, que estaba, en parte, mediado por la polimerización del citoesqueleto de actina. En un aspecto, el LPA provoca degeneración neuronal en condiciones patológicas cuando la barrera hematoencefálica está dañada y los componentes del suero se escapan al cerebro (Moolenaar, Curr. Opin. Cell Biol.
7:203-10, 1995). Las líneas celulares de neuroblastos del SNC inmortalizadas de la corteza cerebral también muestran respuestas de retracción a la exposición a LPA a través de la activación de Rho y las interacciones de actomiosina. En un aspecto, el LPA se asocia a daño neuronal postisquémico (J. Neurochem. 61, 340, 1993; J. Neurochem., 70:66, 1998).
En un aspecto, se proporciona un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, para su uso en el tratamiento o prevención de un trastorno del sistema nervioso en un mamífero. La frase "trastorno del sistema nervioso", como se usa en el presente documento, se refiere a afecciones que alteran la estructura o función del cerebro, la médula espinal o el sistema nervioso periférico, incluyendo pero no limitado a enfermedad de Alzheimer, edema cerebral, isquemia cerebral, ictus, esclerosis múltiple, neuropatías, enfermedad de Parkinson, aquellas encontradas después de traumatismo directo o quirúrgico (incluyendo disfunción cognitiva post quirúrgica y lesión de la médula espinal o del tronco cerebral), así como los aspectos neurológicos de trastornos tales como enfermedad degenerativa de los discos y ciática.
En un aspecto, se proporciona un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, para su uso en el tratamiento o prevención de un trastorno del SNC en un mamífero. Los trastornos del
SNC incluyen, pero no se limitan a, esclerosis múltiple, enfermedad de Parkinson, enfermedad de Alzheimer, ictus, isquemia cerebral, isquemia retiniana, disfunción cognitiva postquirúrgica, migraña, neuropatía periférica/dolor neuropático, lesión de la médula espinal, edema cerebral y traumatismo craneal.
Trastornos cardiovasculares
Los fenotipos cardiovasculares observados después de la eliminación dirigida de los receptores de lisofosfolípidos revelan funciones importantes para la señalización de lisofosfolípidos en el desarrollo y maduración de los vasos sanguíneos, la formación de placas ateroscleróticas y el mantenimiento de la frecuencia cardíaca (Ishii, I. et al. Annu. Rev. Biochem. 73, 321-354, 2004). La angiogénesis, la formación de nuevas redes capilares a partir de vasculatura preexistente, normalmente se invoca en la curación de heridas, crecimiento de tejido y angiogénesis miocárdica después de lesión isquémica. Los factores de crecimiento peptídico (por ejemplo, factor de crecimiento endotelial vascular (VEGF)) y los lisofosfolípidos controlan la proliferación coordinada, la migración, la adhesión, la diferenciación y el ensamblaje de células endoteliales vasculares (VEC) y células vasculares musculares lisas (VSMC) circundantes. La desregulación de los procesos que median la angiogénesis puede conducir a la aterosclerosis, hipertensión, crecimiento tumoral, artritis reumatoide y retinopatía diabética (Osborne, N. and Stainier, D.Y. Annu. Rev. Physiol. 65, 23-43, 2003).
Las vías de señalización posteriores evocadas por los receptores de lisofosfolípidos incluyen la formación de lamelipodios dependiente de Rac (por ejemplo, l Pa -i) y la formación de fibras de estrés dependiente de Rho (por ejemplo LPA1), que es importante en la migración y adhesión celular. La disfunción del endotelio vascular puede cambiar el equilibrio de la vasodilatación a la vasoconstricción y provocar hipertensión y remodelación vascular, que son factores de riesgo para la aterosclerosis (Maguire, J.J. et al., Trends Pharmacol. Sci. 26, 448-454, 2005).
El LPA contribuye tanto a la fase temprana (disfunción de barrera y adhesión de monocitos del endotelio) como a la fase tardía (activación de plaquetas y formación de trombos intraarteriales) de aterosclerosis, además de su progresión general. En la fase temprana, el l Pa de numerosas fuentes se acumula en las lesiones y activa sus GPCR afines (LPA1 y LPA3) expresado en plaquetas (Siess, W. Biochim. Biophys. Acta 1582, 204-215, 2002; Rother, E. et al. Circulation 108, 741-747, 2003). Esto desencadena el cambio de forma de plaquetas y la agregación, que conduce a la formación de trombos intraarteriales y, potencialmente, infarto de miocardio y apoplejía. En apoyo de su actividad aterogénica, el LPA también puede ser un mitógeno y un motógeno para VSMC y un activador de células endoteliales y macrófagos. En un aspecto, los mamíferos con enfermedad cardiovascular se benefician de los antagonistas de los receptores de LPA que previenen la formación de trombos y placas de neoíntima.
Un aspecto proporciona un compuesto de Fórmula (Ia) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para uso en un método para tratar o prevenir enfermedad cardiovascular en mamíferos.
La frase "enfermedad cardiovascular", como se usa en el presente documento se refiere a enfermedades que afectan al corazón o los vasos sanguíneos o ambos, incluyendo pero no limitado a: arritmia (auricular o ventricular o ambas); ateroesclerosis y sus secuelas; angina; alteraciones del ritmo cardíaco; isquemia miocárdica; infarto de miocardio; aneurisma cardiaco o vascular; vasculitis, ictus; arteriopatía obstructiva periférica de una extremidad, un órgano o un tejido; lesión por reperfusión después de isquemia del cerebro, corazón u otro órgano o tejido; choque endotóxico, quirúrgico o traumático; hipertensión, cardiopatía valvular, insuficiencia cardíaca, presión sanguínea anómala; choque; vasoconstricción (incluyendo la asociada a migrañas); anomalía vascular, inflamación, insuficiencia limitada a un solo órgano o tejido.
En un aspecto, se proporciona en el presente documento un compuesto o una composición farmacéutica de la invención para su uso en métodos para prevenir o tratar vasoconstricción, aterosclerosis y sus secuelas isquemia miocárdica, infarto de miocardio, aneurisma de la aorta, vasculitis y accidente cerebrovascular que comprende administrar al menos una vez al mamífero una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, o una composición farmacéutica o un medicamento que incluye un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
En un aspecto, se proporciona en el presente documento un compuesto de la invención para su uso en métodos para reducir la lesión por reperfusión cardíaca después de isquemia miocárdica y/o choque endotóxico que comprende administrar al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
En un aspecto, se proporciona en el presente documento un compuesto de la invención para su uso en métodos para reducir la constricción de los vasos sanguíneos en un mamífero que comprende administrar al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
En un aspecto, se proporciona en el presente documento un compuesto de la invención para su uso en métodos para disminuir o prevenir un aumento en la presión sanguínea de un mamífero que comprende administrar al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
Inflamación
Se ha demostrado que el LPA regula las respuestas inmunológicas al modular las actividades/funciones de las células inmunes como los linfocitos T-/B y los macrófagos. En las células T activadas, el LPA activa la producción de IL-2/proliferación celular a través de LpA i (Gardell et al, TRENDS in Molecular Medicine Vol.12 N.° 2 febrero de 2006). La expresión de genes de respuesta inflamatoria inducida por LPA está mediada por LPA1 y LPA3 (Biochem Biophys Res Commun. 363(4): 1001-8, 2007). Además, el LPA modula la quimiotaxis de las células inflamatorias (Biochem Biophys Res Commun., 1993, 15;193(2), 497). La proliferación y la actividad secretora de citoquinas en respuesta a LPA de las células inmunes (J. Imuunol. 1999, 162, 2049), actividad de agregación plaquetaria en respuesta a LPA, aceleración de la actividad migratoria en monocitos, activación de NF-kB en fibroblastos, mejora de la unión de fibronectina a la superficie celular, y similares son conocidos. De esta manera, el LPA está asociado a diversas enfermedades inflamatorias/inmunológicas.
Un aspecto proporciona un compuesto de Fórmula (la) o (IIa), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en un método para tratar o prevenir la inflamación en un mamífero. Un aspecto proporciona un compuesto de Fórmula (la) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo para su uso en el tratamiento o prevención de trastornos inflamatorios/inmunitarios en un mamífero.
Los ejemplos de trastornos inflamatorios/inmunológicos incluyen psoriasis, artritis reumatoide, vasculitis, enfermedad inflamatoria intestinal, dermatitis, artrosis, asma, enfermedad muscular inflamatoria, rinitis alérgica, vaginitis, cistitis intersticial, esclerodermia, eccema, rechazo del injerto del trasplante alogénico o xenogénico (órgano, médula ósea, células madre y otras células y tejidos), enfermedad del injerto contra hospedador, lupus eritematoso, enfermedad inflamatoria, diabetes de tipo I, fibrosis pulmonar, dermatomiositis, síndrome de Sjogren, tiroiditis (por ejemplo, de Hashimoto y tiroiditis autoinmune), miastenia grave, anemia hemolítica autoinmunitaria, esclerosis múltiple, fibrosis quística, hepatitis recurrente crónica, cirrosis biliar primaria, conjuntivitis alérgica y dermatitis atópica.
Otras enfermedades, trastornos o afecciones
Un aspecto proporciona un compuesto de la invención para su uso en métodos para el tratamiento, la prevención, la reversión, la detención o la ralentización de la progresión de enfermedades o afecciones dependientes de LPA o mediadas por LPA una vez que sea clínicamente evidente, o tratar los síntomas asociados o relacionados con enfermedades o afecciones dependientes de LPA o mediadas por LPA, administrando al mamífero un compuesto de Fórmula (la) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo. En ciertas realizaciones, el sujeto ya tiene una enfermedad o afección dependiente de LPA o mediada por LPA en el momento de la administración, o está en riesgo de desarrollar una enfermedad o afección dependiente de LPA o mediada por LPA.
La actividad de LPA1 en un mamífero puede modularse directa o indirectamente mediante la administración de (al menos una vez) una cantidad terapéuticamente eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables de los mismos. Tal modulación incluye, pero no se limita a, reducir y/o inhibir la actividad de LPA1. La actividad de LPA en un mamífero puede modularse modulada directa o indirectamente, incluyendo reducir y/o inhibir, por la administración de (al menos una vez) una cantidad terapéuticamente eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo. Tal modulación incluye, pero no se limita a, reduciendo y/o inhibiendo la cantidad y/o actividad de un receptor de LPA. En un aspecto, el receptor de LPA es LPA1.
El LPA puede tener una acción de contracción en las células del músculo liso de la vejiga aisladas de la vejiga y puede promover el crecimiento de las células epiteliales derivadas de la próstata J. Urology, 1999, 162, 1779-1784; J. Urology, 2000, 163, 1027-1032). El LPA puede contraer el tracto urinario y la próstata in vitro y aumenta la presión intrauretral in vivo (documento WO 02/062389).
Determinados aspectos proporcionan compuestos de la invención para su uso en métodos para prevenir o tratar el reclutamiento de eosinófilos y/o basófilos y/o células dendríticas y/o neutrófilos y/o monocitos y/o células T que comprenden administrar al menos una vez al mamífero un agente eficaz cantidad de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
Determinados aspectos proporcionan compuestos de la invención para su uso en métodos para el tratamiento de cistitis, incluyendo, por ejemplo, cistitis intersticial, que comprende administrar al menos una vez al mamífero una cantidad terapéuticamente eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
Un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo puede usarse para diagnosticar o determinar si un paciente padece o no una enfermedad o afección dependiente de LPA o mediada por LPA mediante la administración al someter a una cantidad terapéuticamente eficaz de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo y determinar si el paciente responde o no al tratamiento.
En un aspecto proporcionado en el presente documento, están los compuestos de Fórmula (Ia) o (Ib), sales
farmacéuticamente aceptables y solvatos farmacéuticamente aceptables de los mismos, que son antagonistas de LPA1 , para su uso en un método para tratar pacientes que padecen una o más afecciones o enfermedades dependientes de LPA o mediadas por LPA, incluyendo, pero no limitado a, fibrosis de pulmón, fibrosis del riñón, fibrosis del hígado, formación de cicatrices, asma, rinitis, enfermedad pulmonar obstructiva crónica, hipertensión pulmonar, fibrosis pulmonar intersticial, artritis, alergia, psoriasis, enfermedad inflamatoria intestinal, síndrome de dificultad respiratoria del adulto, infarto de miocardio, aneurisma, ictus, cáncer, dolor, trastornos proliferativos y afecciones inflamatorias. En algunas realizaciones, las afecciones o enfermedades dependientes de LPA incluyen aquellas en donde está presente y/u observado un exceso absoluto o relativo de LPA.
En cualquiera de los aspectos mencionados anteriormente, las enfermedades o afecciones dependientes de LPA o mediadas por LPA incluyen, pero no se limitan a, fibrosis orgánica, asma, trastornos alérgicos, enfermedad pulmonar obstructiva crónica, hipertensión pulmonar, fibrosis pulmonar o pleural, fibrosis peritoneal, artritis, alergia, cáncer, enfermedad cardiovascular, síndrome de dificultad respiratoria máxima, infarto de miocardio, aneurisma, accidente cerebrovascular y cáncer.
Un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, puede usarse para mejorar la disminución de la sensibilidad corneal causada por operaciones corneales como la queratomileusis in situ asistida por láser (LASIK) o la operación de cataratas, disminución de la sensibilidad corneal causada por la degeneración corneal, y síntomas de ojo seco causados por ello.
En un aspecto, se presenta en el presente documento un compuesto de Fórmula (I), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento o prevención de inflamación ocular y conjuntivitis alérgica, queratoconjuntivitis vernal y conjuntivitis papilar en un mamífero que comprende administrar al menos una vez al mamífero una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
En un aspecto, se presenta en el presente documento un compuesto de Fórmula (I), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento o prevención de la enfermedad de Sjogren o enfermedad inflamatoria con ojos secos en un mamífero que comprende administrar al menos una vez al mamífero una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
El LPA y los receptores de LPA (por ejemplo, LPAi ) pueden estar implicados en la patogénesis de la osteoartritis (Kotani et al, Hum. Mol. Genet., 2008, 17, 1790-1797). En un aspecto, se presenta en el presente documento un compuesto de Fórmula (I), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento o la prevención de la osteoartritis en un mamífero que comprende administrar al menos una vez al mamífero una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
Los receptores de LPA (por ejemplo, LPA1 , LPA3 ) pueden contribuir a la patogénesis de la artritis reumatoide (Zhao et al, Mol. Pharmacol., 2008, 73(2), 587-600). En un aspecto, se presenta en el presente documento un compuesto de Fórmula (I), o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento o la prevención de la artritis reumatoide en un mamífero que comprende administrar al menos una vez al mamífero una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
Los receptores de LPA (por ejemplo, LPA1 ) pueden contribuir a la adipogénesis. (Simon et al, J.Biol. Chem., 2005, vol.
280, n.° 15, p.14656). Un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, pueden usarse en la promoción de la formación de tejido adiposo en un mamífero que comprende administrar al menos una vez al mamífero una cantidad eficaz de al menos un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
a. Ensayos in vitro
La eficacia de los compuestos de la presente invención como inhibidores de LPA1 puede determinarse en un ensayo de antagonista funcional de LPA1 como sigue:
Las células de ovario de hámster chino que sobreexpresan LPA1 humano se sembraron durante la noche (15.000 células/pocillo) en microplacas de 384 pocillos recubiertas con poli-D-lisina (Greiner bio-one, Cat n.° 781946) en medio DMEM/F12 (Gibco, Cat n.° 11039). Después del cultivo durante la noche, las células se cargaron con colorante indicador de calcio (AAT Bioquest Inc, Cat n.° 34601) durante 30 minutos a 37 °C. Las células se equilibraron a temperatura ambiente durante 30 minutos antes del ensayo. Los compuestos de prueba solubilizados en DMSO se transfirieron a placas de superficie de no unión de 384 pocillos (Corning, Cat n.° 3575) usando el dispensador acústico Labcyte Echo y se diluyeron con tampón de ensayo [1X HBSS con calcio/magnesio (Gibco Cat n.° 14025-092), HEPES 20 mM (Gibco Cat n.° 15630-080) y BSA libre de ácidos grasos al 0,1 % (Sigma Cat n.° A9205)] a una concentración final de DMSO al 0,5 %. Los compuestos diluidos se añadieron a las células mediante FDSS6000 (Hamamatsu) a concentraciones finales que varían de 0,08 nM a 5 pM. y después se incubaron durante 20 minutos a temperatura ambiente, momento en el cual se añadió LPA (Avanti Polar Lipids Cat n.° 857130C) a concentraciones finales de
10 nM para estimular las células. El valor CI50 del compuesto se definió como la concentración del compuesto de prueba que inhibía el 50 % del flujo de calcio inducido por LPA solo. Los valores CI50 se determinaron ajustando los datos a una ecuación logística de 4 parámetros (GraphPad Prism, San Diego CA).
b. Ensayos in vivo
Provocación de LPA con evaluación de histamina en plasma.
El compuesto se dosifica por vía oral p.o. 2 horas a ratones hembra CD-1 antes de la provocación con LPA. Los ratones se dosifican después a través de la vena de la cola (IV) con 0,15 ml de LPA en 0,1 % de BSA/PBS (2 pg/pl). Exactamente 2 minutos después dela provocación de LPA, los ratones se sacrifican por decapitación y se recoge la sangre del tronco. Estas muestras se centrifugan colectivamente y las muestras individuales de 75 pl se congelan a -20 °C hasta el momento del ensayo de histamina.
El análisis de histamina en plasma se realizó mediante métodos convencionales de EIA (inmunoensayo enzimático). Las muestras de plasma se descongelaron y se diluyeron 1:30 en BSA al 0,1 % en PBS. Se siguió el protocolo de EIA para el análisis de histamina según lo indicado por el fabricante (Histamine EIA, Oxford Biomedical Research, EA#31).
El LPA usado en el ensayo se formula de la siguiente manera: LPA (1-oleoil-2-hidroxi-snglicero-3-fosfato (sal sódica), 857130P, Avanti Polar Lipids) se prepara en BSA/PBS al 0,1 % para una concentración total de 2 pg/pl. Se pesan 13 mg de LPA y se añaden 6,5 ml de b Sa al 0,1 %, se agita en vórtex y se somete a ultrasonidos durante ~1 hora hasta que se logre una solución transparente.
V. COMPOSICIONES FARMACÉUTICAS, FORMULACIONES Y COMBINACIONES
En algunas realizaciones, se proporciona una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo. En algunas realizaciones, la composición farmacéutica también contiene al menos un ingrediente inactivo farmacéuticamente aceptable.
En algunas realizaciones, se proporciona una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo y al menos un ingrediente inactivo farmacéuticamente aceptable. En un aspecto, la composición farmacéutica se formula para inyección intravenosa, inyección subcutánea, administración oral, inhalación, administración nasal, administración tópica, administración oftálmica o administración ótica. En algunas realizaciones, la composición farmacéutica es un comprimido, una píldora, una cápsula, un líquido, un inhalante, una solución de pulverización nasal, un supositorio, una suspensión, un gel, un coloide, una dispersión, una suspensión, una solución, una emulsión, una pomada, una loción, una gota para los ojos o una gota para los oídos.
En algunas realizaciones, la composición farmacéutica comprende además uno o más agentes terapéuticamente activos adicionales seleccionados de: corticosteroides (por ejemplo, dexametasona o fluticasona), inmunosupresores (por ejemplo, tacrolimus y pimecrolimus), analgésicos, agente antineoplásico, antiinflamatorios, antagonistas de los receptores de quimiocinas, broncodilatadores, antagonistas de los receptores de leucotrienos (por ejemplo, montelukast o zafirlukast), inhibidores de la formación de leucotrienos, inhibidores de la monoacilglicerol quinasa, inhibidores de la fosfolipasa A 1 , inhibidores de la fosfolipasa A2 e inhibidores de la lisofosfolipasa D (lysoPLD), inhibidores de la autotaxina, descongestionantes, antihistamínicos (por ejemplo, loratidina), mucolíticos, anticolinérgicos, antitusivos, expectorantes, antiinfecciosos (por ejemplo, ácido fusídico, particularmente para el tratamiento de la dermatitis atópica), antifúngicos (por ejemplo, clotriazol, particularmente para dermatitis atópica), terapias con anticuerpos anti-IgE (por ejemplo, omalizumab), agonistas adrenérgicos p-2 (por ejemplo, albuterol o salmeterol), otros antagonistas de PGD2 que actúan en otros receptores como los antagonistas de DP, inhibidores de PDE4 (por ejemplo, cilomilast), medicamentos que modulan la producción de citocinas, por ejemplo, inhibidores de TACE, fármacos que modulan la actividad de las citocinas Th2 IL-4 e IL-5 (por ejemplo, bloqueando anticuerpos monoclonales y receptores solubles), Agonistas de PPARy (por ejemplo, rosiglitazona y pioglitazona), inhibidores de la 5-lipoxigenasa (por ejemplo, zileuton).
En algunas realizaciones, la composición farmacéutica comprende además uno o más agentes antifibróticos adicionales seleccionados de pirfenidona, nintedanib, talidomida, carlumab, FG-3019, fresolimumab, interferón alfa, superóxido dismutasa lecitinizada, simtuzumab, tanzisertib, tralokinumab, hu3G9, AM-152, IFN-gamma-1b, IW-001, p Rm -151, PXS-25, pentoxifilina/N-acetil-cisteína, pentoxifilina/vitamina E, sulfato de salbutamol, [Sar9,Met(O2)11]-Sustancia P, pentoxifilina, bitartrato de mercaptamina, ácido obeticólico, aramcol, GFT-505, éster etílico del ácido eicosapentaenoico, metformina, metreleptina, muromonab-CD3, oltipraz, IMM-124-E, MK-4074, PX-102, RO-5093151. En algunas realizaciones, se proporciona un compuesto de la invención para su uso en un método que comprende administrar un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, a un ser humano con una enfermedad o afección dependiente de LPA o mediada por LPA. En algunas realizaciones, al ser humano ya se le está administrando uno o más agentes terapéuticamente activos adicionales distintos de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo. En algunas
realizaciones, el método comprende además administrar uno o más agentes terapéuticamente activos adicionales distintos de un compuesto de Fórmula (la) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo.
En algunas realizaciones, el uno o más agentes terapéuticamente activos adicionales distintos de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, se seleccionan de: corticosteroides (por ejemplo, dexametasona o fluticasona), inmunosupresores (por ejemplo, tacrolimus y pimecrolimus), analgésicos, agente antineoplásico, antiinflamatorios, antagonistas de los receptores de quimiocinas, broncodilatadores, antagonistas de los receptores de leucotrienos (por ejemplo, montelukast o zafirlukast), inhibidores de la formación de leucotrienos, inhibidores de la monoacilglicerol quinasa, inhibidores de la fosfolipasa A1, inhibidores de la fosfolipasa A2 e inhibidores de la lisofosfolipasa D (lysoPLD), inhibidores de la autotaxina, descongestionantes, antihistamínicos (por ejemplo, loratidina), mucolíticos, anticolinérgicos, antitusivos, expectorantes, antiinfecciosos (por ejemplo, ácido fusídico, particularmente para el tratamiento de la dermatitis atópica), antifúngicos (por ejemplo, clotriazol, particularmente para dermatitis atópica), terapias con anticuerpos anti-IgE (por ejemplo, omalizumab), agonistas adrenérgicos p-2 (por ejemplo, albuterol o salmeterol), otros antagonistas de PGD2 que actúan en otros receptores como los antagonistas de DP, inhibidores de PDE4 (por ejemplo, cilomilast), medicamentos que modulan la producción de citocinas, por ejemplo inhibidores de TACE, fármacos que modulan la actividad de las citocinas Th2 IL-4 e IL-5 (por ejemplo, bloqueando anticuerpos monoclonales y receptores solubles), agonistas de PPARy (por ejemplo, rosiglitazona y pioglitazona), inhibidores de la 5-lipoxigenasa (por ejemplo, zileuton).
En algunas realizaciones, el uno o más agentes terapéuticamente activos adicionales distintos de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, son otros agentes antifibróticos seleccionados de pirfenidona, nintedanib, talidomida, carlumab, FG-3019, fresolimumab, interferón alfa, superóxido dismutasa lecitinizada, simtuzumab, tanzisertib, tralokinumab, hu3G9, AM-152, IFN-gamma-lb, IW-001, PRM-151, PXS-25, pentoxifilina/N-acetil-cisteína, pentoxifilina/vitamina E, sulfato de salbutamol, [Sar9,Met(O2)11]-Sustancia P, pentoxifilina, bitartrato de mercaptamina, ácido obeticólico, aramcol, GFT-505, eicosapentil etil éster, metformina, metreleptina, muromonab-CD3, oltipraz, IMM-124-E, MK-4074, PX-102, RO-5093151.
En algunas realizaciones, el uno o más agentes terapéuticamente activos adicionales distintos de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, se seleccionan de inhibidores de ACE, ramiprilo, Todos los antagonistas, irbesartán, antiarrítmicos, dronedarona, activadores de PPARa, activadores de PPARy, pioglitazona, rosiglitazona, prostanoides, antagonistas del receptor de endotelina, inhibidores de la elastasa, antagonistas de calcio, betabloqueantes, diuréticos, antagonistas del receptor de aldosterona, eplerenona, inhibidores de la renina, inhibidores de rho quinasa, activadores de guanilato ciclasa soluble (sGC), sensibilizadores de sGC, inhibidores de PDE, inhibidores de PDE5, donadores de NO, fármacos de digitalis, inhibidores de ACE/NEP, estatinas, inhibidores de la recaptación de ácidos biliares, antagonistas de PDGF, antagonistas de vasopresina, acuaréticos, inhibidores de NHE1, antagonistas del Factor Xa, antagonistas del Factor XIIIa, anticoagulantes, antitrombóticos, inhibidores plaquetarios, profibrolíticos, inhibidores de la fibrinólisis activables por trombina (TAFI), inhibidores de PAI-1, cumarinas, heparinas, antagonistas de tromboxano, antagonistas de serotonina, inhibidores de COX, aspirina, anticuerpos terapéuticos, antagonistas de GPIIb/IIIa, antagonistas de ER, SERM, inhibidores de tirosina quinasa, inhibidores de la quinasa RAF, inhibidores de p38 MAPK, pirfenidona, inhibidores multi-quinasa, nintedanib, sorafenib.
En algunas realizaciones, el uno o más agentes terapéuticamente activos adicionales distintos de un compuesto de Fórmula (Ia) o (Ib) o una sal o solvato farmacéuticamente aceptables del mismo, se seleccionan de Gremlin-1 mAb, PA1-1 mAb, Promedior (PRM-151; Pentraxina-2 humana recombinante); FGF21, antagonistas de TGFp, panantagonistas de avp6 y avp; inhibidores de FAK, inhibidores de TG2, inhibidores de LOXL2, inhibidores de NOX4, inhibidores de MGAT2, agonistas de GPR120.
Las formulaciones farmacéuticas descritas en el presente documento se pueden administrar a un sujeto en diversas formas mediante múltiples vías de administración, incluyendo, pero sin limitación, las vías de administración oral, parenteral (por ejemplo, intravenosa, subcutánea, intramuscular), intranasal, bucal, tópica o transdérmica. Las formulaciones farmacéuticas descritas en el presente documento incluyen, pero sin limitación, dispersiones líquidas acuosas, dispersiones autoemulsionantes, soluciones sólidas, dispersiones liposómicas, aerosoles, formas de dosificación sólidas, polvos, formulaciones de liberación inmediata, formulaciones de liberación controlada, formulaciones de fusión rápida, comprimidos, cápsulas, píldoras, formulaciones de liberación retardada, formulaciones de liberación extendida, formulaciones de liberación secuencial, formulaciones de multipartículas y formulaciones mixtas de liberación inmediata y controlada.
El compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se puede administrar por vía oral.
El compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se puede administrar por vía tópica. En dichos casos, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se puede formular en forma de diferentes composiciones administrables por vía tópica, tales como soluciones, suspensiones, lociones, geles, pastas, champús, exfoliantes, solución para frotar, frotis, barras medicinales, vendas medicadas, bálsamos, cremas o pomadas. Dichos compuestos farmacéuticos pueden contener
solubilizantes, estabilizantes, agentes potenciadores de la tonicidad, tampones y conservantes. El compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se puede administrar por vía tópica en la piel.
El compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se puede administrar por inhalación. El compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se puede administrar por inhalación que se dirige directamente al sistema pulmonar.
En otro aspecto, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se formula para administración intranasal. Dichas formulaciones incluyen pulverizaciones nasales, nieblas nasales y similares.
En otro aspecto, el compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se formula en forma de gotas oculares.
En otro aspecto, se proporciona un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, para su uso para tratar una enfermedad, trastorno o afección en la que la actividad de al menos un receptor de LPA contribuye a la patología y/o los síntomas de la enfermedad o afección. En una realización de este aspecto, el LPA se selecciona entre LPA1 , LPA2 , LPA3 , LPA4, LPA5 y LPA6. En un aspecto, el receptor de LPA es LPA1. En un aspecto, la enfermedad o afección es cualquiera de las enfermedades o afecciones especificadas en el presente documento.
En cualquiera de los aspectos mencionados anteriormente hay realizaciones adicionales en las que: (a) la cantidad eficaz del compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, se administra al mamífero por vía sistémica; y/o (b) la cantidad eficaz del compuesto se administra al mamífero por vía oral; y/o (c) la cantidad eficaz del compuesto se administra al mamífero por vía intravenosa; y/o (d) la cantidad eficaz del compuesto se administra por inhalación; y/o (e) la cantidad eficaz del compuesto se administra por administración nasal; o y/o (f) la cantidad eficaz del compuesto se administra al mamífero por inyección; y/o (g) la cantidad eficaz del compuesto se administra al mamífero por vía tópica; y/o (h) la cantidad eficaz del compuesto se administra por administración oftálmica; y/o (i) la cantidad eficaz del compuesto se administra al mamífero por vía rectal; y/o (j) la cantidad eficaz se administra al mamífero por vía no sistémica o vía local.
En cualquiera de los aspectos mencionados anteriormente hay realizaciones adicionales que comprenden administraciones individuales de la cantidad eficaz del compuesto, incluyendo realizaciones adicionales en las que (i) el compuesto se administra una vez; (ii) el compuesto se administra al mamífero múltiples veces durante un día; (iii) ininterrumpidamente o (iv) de manera continua.
En cualquiera de los aspectos mencionados anteriormente hay realizaciones adicionales que comprenden administraciones múltiples de la cantidad eficaz del compuesto, incluyendo realizaciones adicionales en las que (i) el compuesto se administra de manera continua o intermitente: como en una dosis única; (ii) el tiempo entre múltiples administraciones es cada 6 horas; (iii) el compuesto se administra al mamífero cada 8 horas; (iv) el compuesto se administra al mamífero cada 12 horas; (v) el compuesto se administra al mamífero cada 24 horas. En realizaciones adicionales o alternativas, el método comprende un período de reposo farmacológico, en donde la administración del compuesto se suspende de manera temporal o la dosis del compuesto que se administra se reduce de manera temporal; al final del descanso farmacológico, la dosificación del compuesto se reanuda. En una realización, la duración del descanso farmacológico varía de 2 días a 1 año.
Un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo se puede usar en un método para inhibir la actividad fisiológica del LPA en un mamífero, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo al mamífero que lo necesita.
En un aspecto, se proporciona un medicamento para tratar una enfermedad o afección dependiente de LPA o mediada por LPA en un mamífero, que comprende una cantidad terapéuticamente eficaz de un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo.
Un compuesto de fórmula (Ia) o (Ib), o una sal farmacéuticamente aceptable o solvato del mismo, se puede usar en la fabricación de un medicamento para el tratamiento de una enfermedad o afección dependiente de LPA o mediada por LPA.
Un compuesto de fórmula (Ia) o (Ib), o una sal farmacéuticamente aceptable o solvato del mismo, se puede usar en el tratamiento o prevención de una enfermedad o afección dependiente de LPA o mediada por LPA.
Un aspecto proporciona un compuesto de la invención para su uso en un método para tratar o prevenir una enfermedad o afección dependiente de LPA o mediada por LPA-en un mamífero, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del
mismo.
En un aspecto, las enfermedades o afecciones dependientes de LPA o mediadas por LPA incluyen, pero sin limitación, fibrosis de órganos o tejidos, formación de cicatrices, enfermedades hepáticas, afecciones dermatológicas, cáncer, enfermedad cardiovascular, enfermedades o afecciones respiratorias, enfermedad inflamatoria, enfermedad del tracto gastrointestinal, enfermedad renal, enfermedad asociada al tracto urinario, enfermedad inflamatoria del tracto urinario inferior, disuria, micción frecuente, enfermedad pancreática, obstrucción arterial, infarto cerebral, hemorragia cerebral, dolor, neuropatía periférica y fibromialgia.
En un aspecto, la enfermedad o afección dependiente de LPA o mediada por LPA es una enfermedad o afección respiratoria. En algunas realizaciones, la enfermedad o afección respiratoria es asma, enfermedad pulmonar obstructiva crónica (EPOC), fibrosis pulmonar, hipertensión arterial pulmonar o síndrome de dificultad respiratoria aguda.
En algunas realizaciones, la enfermedad o afección dependiente de LPA o mediada por LPA se selecciona de fibrosis pulmonar idiopática; otras enfermedades pulmonares parenquimatosas difusas de diferentes etiologías, incluyendo fibrosis iatrogénica inducida por fármacos, fibrosis laboral y/o ambiental inducida, enfermedades granulomatosas (sarcoidosis, neumonía por hipersensibilidad), enfermedad vascular por colágeno, proteinosis alveolar, granulomatosis de células de Langerhans, linfangioleiomiomatosis, enfermedades hereditarias (síndrome de Hermansky-Pudlak, esclerosis tuberosa, neurofibromatosis, trastornos del almacenamiento metabólico, enfermedad pulmonar intersticial familiar); fibrosis inducida por radiación; enfermedad pulmonar obstructiva crónica (COPD); esclerodermia; fibrosis pulmonar inducida por bleomicina; asma crónica; silicosis; fibrosis pulmonar inducida por el asbesto; síndrome de dificultad respiratoria aguda (ARDS); fibrosis renal; fibrosis del tubulointersticio; nefritis glomerular; esclerosis glomerular segmentaria focal; nefropatía de IgA; hipertensión; Alport; fibrosis intestinal; fibrosis hepática; cirrosis; fibrosis hepática inducida por alcohol; fibrosis hepática tóxica/inducida por fármacos; hemocromatosis; esteatohepatitis no alcohólica (NASH); lesión del conducto biliar; cirrosis biliar primaria; infección inducida por fibrosis hepática; fibrosis hepática inducida por virus; y hepatitis autoinmune; cicatrices corneales; cicatrices hipertróficas; enfermedad de Duputren, queloides, fibrosis cutánea; esclerodermia cutánea; lesión de la médula espinal/fibrosis; mielofibrosis; restenosis vascular; aterosclerosis; arteriosclerosis; granulomatosis de Wegener; enfermedad de Peyronie, leucemia linfocítica crónica, metástasis tumoral, rechazo de trasplante de órgano, endometriosis, síndrome de dificultad respiratoria neonatal y dolor neuropático.
En un aspecto, la enfermedad o afección dependiente de LPA o mediada por LPA se describe en el presente documento.
En un aspecto, se proporciona un compuesto de la invención para su uso en un método para el tratamiento o prevención de fibrosis orgánica en un mamífero, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo a un mamífero que lo necesita.
En un aspecto, la fibrosis orgánica comprende fibrosis pulmonar, fibrosis renal o fibrosis hepática.
En un aspecto, se proporciona un compuesto de la invención para su uso en un método para mejorar la función pulmonar en un mamífero, que comprende administrar una cantidad terapéuticamente eficaz de un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo al mamífero que lo necesita. En un aspecto, el mamífero ha sido diagnosticado con fibrosis pulmonar.
Un aspecto proporciona un compuesto de la invención para su uso en un método para tratar la fibrosis pulmonar idiopática (neumonía intersticial usual) en un mamífero.
Un aspecto proporciona un compuesto de la invención para su uso en un método para tratar enfermedades pulmonares intersticiales parenquimatosas: inducida por fármaco iatrogénico, laboral/ambiental (pulmón de granjero), enfermedades granulomatosas (sarcoidosis, neumonía por hipersensibilidad), enfermedad vascular del colágeno (esclerodermia y otras), proteinosis alveolar, granulomatosis de células de Langerhans, linfangioleiomiomatosis, Síndrome de Hermansky-Pudlak, esclerosis tuberosa, neurofibromatosis, trastornos del almacenamiento metabólico, enfermedad pulmonar intersticial familiar.
En algunas realizaciones, se proporciona un compuesto de la invención para su uso en un método para tratar la fibrosis posterior a trasplante asociada al rechazo crónico, en un mamífero: bronquiolitis obliterante por trasplante pulmonar.
En algunas realizaciones, se proporciona un compuesto de la invención para su uso en un método para tratar fibrosis cutánea en un mamífero: esclerodermia cutánea, enfermedad de Dupuytren, queloides.
Un aspecto proporciona compuestos de la invención para su uso en un método para tratar fibrosis hepática, con o sin cirrosis, en un mamífero: tóxica/inducida por fármacos (hemocromatosis), hepatopatía alcohólica, hepatitis vírica (virus de la hepatitis B, virus de la hepatitis C, VHC), enfermedad hepática no alcohólica (NAFLD, NASH), enfermedad
metabólica y autoinmune.
Un aspecto proporciona compuestos de la invención para su uso en un método para tratar fibrosis renal en un mamífero: fibrosis del tubulointersticio, esclerosis glomerular.
En cualquiera de los aspectos mencionados anteriormente que implican el tratamiento de enfermedades o afecciones dependientes de LPA existen más realizaciones que comprenden administrar al menos otro agente más, además de la administración de un compuesto que tiene la estructura de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo. En diversas realizaciones, cada agente se administra en cualquier orden, incluyendo de manera simultánea.
En cualquiera de las realizaciones divulgadas en el presente documento, el mamífero es un ser humano.
Los compuestos proporcionados en el presente documento se pueden administrar a un ser humano.
Los compuestos proporcionados en el presente documento se pueden administrar por vía oral.
Los compuestos proporcionados en el presente documento se pueden usar como antagonistas de al menos un receptor de LPA. Los compuestos proporcionados en el presente documento se pueden usar para inhibir la actividad de al menos un receptor de LPA o para el tratamiento de una enfermedad o afección que se beneficiaría de la inhibición de la actividad de al menos un receptor de LPA. En un aspecto, el receptor de LPA es LPA1.
Los compuestos proporcionados en el presente documento se pueden usar para la formulación de un medicamento para la inhibición de la actividad de LPA1.
Se proporcionan artículos de fabricación, que incluyen el material de envasado, un compuesto de fórmula (Ia) o (Ib) o una sal farmacéuticamente aceptable o solvato del mismo, dentro del material de envasado y una etiqueta que indica que el compuesto o composición o la sal farmacéuticamente aceptable, los tautómeros, el N-óxido farmacéuticamente aceptable, metabolito farmacéuticamente aceptable, profármaco farmacéuticamente aceptable o solvato farmacéuticamente aceptable del mismo, se puede usar para inhibir la actividad de al menos un receptor de LPA o para el tratamiento, prevención o mejora de uno o más síntomas de una enfermedad o afección que se beneficiaría de la inhibición de la actividad de al menos un receptor de LPA.
VI. SÍNTESIS GENERAL INCLUYENDO ESQUEMAS
Los compuestos de la presente invención se pueden preparar en varias rutas conocidas por un experto en la técnica de la síntesis orgánica. Los compuestos de la presente invención se pueden sintetizar usando los métodos descritos a continuación, junto con los métodos de síntesis conocidos en la técnica de la química orgánica sintética o por variaciones en los mismos como apreciarán los expertos en la técnica. Los métodos preferidos incluyen, pero sin limitación, los descritos a continuación. Las reacciones se llevan a cabo en un disolvente o una mezcla de disolventes apropiada a los reactivos y materiales empleados y adecuada para que las transformaciones se realicen. Los expertos en la técnica de la síntesis orgánica entenderán que la funcionalidad presente en la molécula debe ser consistente con las transformaciones propuestas. En ocasiones esto requerirá una valoración para modificar el orden de las etapas sintéticas o para seleccionar un esquema de proceso particular frente a otro para obtener un compuesto deseado de la invención.
También se reconocerá que otra consideración principal en la planificación de cualquier ruta de síntesis en este campo es la elección juiciosa del grupo protector usado para la protección de los grupos funcionales reactivos presentes en los compuestos descritos en esta invención. Un informe con autoridad que describe las muchas alternativas al médico capacitado es Greene et al., (Protective Groups in Organic Synthesis, cuarta edición, Wiley-Interscience (2006)).
Los compuestos de fórmula (Ia) o (Ib) se pueden preparar mediante los procesos a modo de ejemplo descritos en los esquemas y los ejemplos funcionales siguientes, así como procedimientos relevantes publicados en la bibliografía que son usados por un experto en la técnica. Los reactivos y procedimientos a modo de ejemplo para estas reacciones aparecen en el presente documento a partir de ahora y en los ejemplos de trabajo. La protección y desprotección en los procesos siguientes se puede llevar a cabo mediante procedimientos normalmente conocidos en la técnica (véase, por ejemplo, Wuts, P. G. M., Greene's Protective Groups in Organic Synthesis, 5a edición, Wiley (2014)). Los métodos generales de síntesis orgánica y transformaciones de grupos funcionales se encuentran en: Trost, B. M. et al., Eds., Comprehensive Organic Synthesis: Selectivity, Strategy & Efficiency in Modern Organic Chemistry, Pergamon Press, Nueva York, NY (1991); Smith, M. B. et al., March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure. 7a edición, Wiley, Nueva York, NY (2013); Katritzky, A. R. et al., Eds., Comprehensive Organic Functional Group Transformations II, 2a edición, Elsevier Science Inc., Tarrytown, NY (2004); Larock, R. C., Comprehensive Organic Transformations, 2a edición, Wiley-VCH, Nueva York, NY (1999) y las referencias en los mismos.
El esquema 1 describe la síntesis de los ácidos isoxazol O-carbamoil aril(heteroaril)oxiciclohexílicos 12 y 14. Un ácido 4-halo (preferentemente bromo) fenil o azina (por ejemplo, piridina) benzoico 1 se convierte en el cloruro de ácido
correspondiente (por ejemplo, con SOCh o cloruro de oxalilo/DMF catalítico). Este cloruro de ácido intermedio se hace reaccionar con un p-enamino-éster 2 apropiado, seguido de condensación con hidroxilamina para proporcionar el éster de 4-carboxilato de 5-halo(hetero)aril-isoxazol 3 correspondiente. La desprotección del éster 3, seguido de reducción del ácido resultante (por ejemplo, directamente con diborano o mediante un procedimiento de 2 etapas haciendo reaccionar el ácido con un cloroformiato de alquilo, seguido de reducción con, por ejemplo, NaBH4 a baja temperatura) y la protección del alcohol resultante proporciona el alcohol 5-halo(hetero)aril-isoxazol protegido 4. La reacción de los haloaril o haloheteroaril-isoxazoles 4 con pinacol diboronato en presencia de un catalizador de paladio apropiado (por ejemplo, Ishiyama, T. et al, J. Org. Chem. 1995, 60, 7508-7510) proporciona el pinacol boronato 5 correspondiente, que se oxida después con peróxido de hidrógeno para dar el fenol o el hidroxiheteroareno 6 correspondiente (Fukumoto, S. et al, documento WO 2012137982). La reacción del fenol/hidroxiheteroareno 6 con un éster 3-hidroxi ciclohexílico 7 en condiciones de reacción de Mitsunobu (Kumara Swamy, K. C., Chem. Rev., 2009, 109, 2551-2651) proporciona el isoxazol cicloalquil éter éster 8 correspondiente. La desprotección del hidroximetilisoxazol 8 proporciona el éster ciclohexílico alcohol isoxazol 9. Un ácido carboxílico 10 apropiado se somete a condiciones de reordenamiento de Curtius (por ejemplo, Ph2PON3) para dar el isocianato intermedio, que se hace reaccionar in situ con el alcohol isoxazol 9 para dar el NH-carbamato isoxazol del éster ciclohexílico 11. La desprotección de éster ciclohexílico 11 proporciona los ácidos isoxazol NH-carbamato hexílicos 12. Además, el éster ciclohexílico NH-carbamato isoxazol, después de tratarlo con una base apropiada (por ejemplo, NaH), seguido de reacción con un haluro de alquilo (R4X), proporciona el éster ciclohexílico isoxazol carbamato N,N-disustituido 13. La desprotección del éster ciclohexílico 13 proporciona los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 14.
sq u e m a
Una ruta alternativa para la síntesis, a partir del alcohol isoxazol 9 a los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 14 se muestra en el esquema 2. El alcohol isoxazol 9 se hace reaccionar con un grupo activador en presencia de base (por ejemplo, 4-nitrofenil cloroformiato) para dar el 4-nitrofenil carbonato de isoxazol 15, el cual se somete a reacción con una amina 16 apropiada (R3R4NH) para dar el isoxazol O-carbamato 13. La desprotección de éster ciclohexílico 13 proporciona después los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 14. Si una amina primaria R3NH2 se hace reaccionar con el 4-nitrofenil carbonato de isoxazol 15, después (tras la desprotección del ácido), se obtienen los ácidos isoxazol NH-carbamato ciclohexílicos 12.
E sq u e m a 2
El esquema 3 describe una ruta de síntesis alternativa para los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 14. La protección del alcohol isoxazol 6 seguido de desprotección del hidroxi aril/heteroarilo isoxazol proporciona el alcohol hidroxi-aril/heteroarilo isoxazol protegido 17. El alcohol isoxazol 17 se hace reaccionar con 4-nitrofenil cloroformiato para dar el 4-nitrofenil carbonato de isoxazol 18, el cual se somete a reacción con una amina 16 apropiada (R3R4NH) para dar el isoxazol O-carbamato 19. La desprotección del hidroxi aril/heteroaril isoxazol carbamato 19 proporciona el hidroxi-aril/heteroaril isoxazol carbamato 20. La reacción del hidroxiaril- o hidroxiheteroaril-isoxazol carbamato 20 con un éster 3-hidroxi ciclohexílico 7 en condiciones de reacción de Mitsunobu proporciona el isoxazol cicloalquil éter éster 13 correspondiente. La desprotección del éster ciclohexílico 13 proporciona los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 14.
E sq u e m a 3
Otra ruta alternativa a los ácidos isoxazol carbamato ciclohexílicos 14 se muestra en el esquema 4. Un 5-halo-4-carboalcoxi-isoxazol 21 se somete a una reacción de acoplamiento de Suzuki-Miyaura con un ácido 4-hidroxi-aril- o -heteroarilborónico 22 apropiado para dar el éster aril- o hetero-aril isoxazol 23 correspondiente. La protección del hidroxiaril/heteroarilo 23 seguido de la reducción del ácido carboxílico (ya sea directamente usando diborano o a través de un protocolo en 2 etapas mediante reacción del ácido con un cloroformiato de alquilo seguido de reducción de NaBH4 a baja temperatura) proporciona el alcohol isoxazol 6. Después el alcohol isoxazol 6 se convierte en los ácidos isoxazol carbamato ciclohexílicos 12 y 14 mediante uno de los procedimientos descritos en los esquemas 1-3.
Desproteccion 1) Acido ArOH/ reducido (p.ej. HetArOH ROCOCI/NaBH4)
El esquema 5 muestra otra ruta a los ácidos isoxazol carbamato ciclohexílicos 14. El 4-halo-aril/heteroaril isoxazol 26 (obtenido mediante la desprotección del alcohol isoxazol 4) se somete a una reacción con 4-nitrofenil cloroformiato en presencia de base para dar el 4-nitrofenil carbonato 27, el cual se hace reaccionar con la amina 6 en presencia de base para proporcionar el carbamato de isoxazol 28. Este carbamato de 4-halo-aril/heteroarilo isoxazol se convierte en el aril-4-boronato correspondiente mediante una reacción mediada por paladio con pinacol-diboronato, seguido de oxidación mediada por peróxido de hidrógeno del aril boronato para dar el hidroxi-aril/heteroaril isoxazol 29 correspondiente como se describe en el esquema 1. El hidroxi-areno/heteroareno 29 se somete a una reacción de Mitsunobu con un éster 3-hidroxi-ciclohexílico 7 para proporcionar el éster isoxazol carbamato oxiciclohexílico 13, el cual se desprotege después para dar los ácidos isoxazol carbamato ciclohexílicos 14 (como se describe en el esquema 1).
E sq u e m a 5
El esquema 6 describe la síntesis de los carbamatos de (3-aril-4H-1A3-isoxazol-4-il)metilo isoméricos 40 y 41. Un aril/heteroaril aldehído 30 4-halo sustituido de forma apropiada (por ejemplo, bromo) se hace reaccionar con hidroxilamina para dar la oxima 31, que se clora (por ejemplo, con N-clorosuccinimida) para proporcionar el cloruro de imidoílo 32. La reacción del cloruro de imidoílo 32 con el éster de acetoacetato 33 en presencia de base proporciona el isoxazol éster 34. Después de la secuencia de reacción general descrita en el esquema 1, la desprotección del isoxazol éster 34, seguido de reducción del ácido de isoxazol (ya sea directamente con diborano o por un procedimiento de 2 etapas mediante reducción de NaBH4 del anhídrido carboxílico correspondiente) proporciona el alcohol isoxazol 35, el cual se hace reaccionar con un isocianato (generado in situ mediante reacción de reordenamiento de Curtius (por ejemplo, con (PhO)2PON3) de un ácido carboxílico 10 apropiado) para dar el carbamato de isoxazol 36. El carbamato de bromoaril isoxazol 36 se convierte en el hidroxi-aril isoxazol 37 correspondiente mediante reacción mediada por Pd con B2(pin)2 seguido de oxidación con H2O2. La reacción del fenol/hidroxiheteroareno 37 con un éster 3-hidroxi ciclohexílico 7 en condiciones de reacción de Mitsunobu proporciona el isoxazol ciclohexil éter éster 38 correspondiente, el cual después se transforma en los ácidos isoxazol NH-carbamato ciclohexílicos 39 o los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 40 de acuerdo con las secuencias sintéticas descritas en el esquema 1.
E sq u e m a 6
El esquema 7 muestra una síntesis alternativa de los ácidos de isoxazol carbamato 40. El 4-halo-aril/heteroaril isoxazol 35 se hace reaccionar con 4-nitrofenil cloroformiato en presencia de base para dar el 4-nitro-fenil carbonato 41. El 4 nitrofenil carbonato 41 se hace reaccionar con la amina 6 en presencia de base para proporcionar el carbamato de haloaril/heteroaril isoxazol 36, el cual se convierte después en los ácidos isoxazol carbamato ciclohexílicos 40 (usando la misma secuencia sintética que se describe en el esquema 5).
E sq u e m a 7
El esquema 8 describe la síntesis de los ácidos isoxazol carbamato ciclohexilacéticos 44 y 45. La reacción del carbamato de hidroxi-aril/heteroaril isoxazol 6 con un éster del ácido 2-(3-hidroxicidohexil)acético 42 protegido de manera adecuada en condiciones de Mitsunobu proporciona el aril/hetero-aril ciclohexano éter éster del ácido acético 43. La desprotección del alcohol isoxazol ciclohexano éster acético 43 proporciona el alcohol isoxazol ciclohexano éster acético 44, el cual se usa después en la síntesis de los ácidos isoxazol carbamato ciclohexilacéticos 44 y 45 (usando la misma secuencia sintética que se describe en el esquema 2 para la conversión de 9 ^ 14).
Esquema 8
El esquema 9 describe la síntesis de los ácidos isoxazol 4-il alquil carbamato ciclohexílicos 50 y 51. La oxidación del alcohol isoxazol (por ejemplo, con peryodinano de Dess-Martin) proporciona el isoxazol aldehido 47, el cual se hace reaccionar con un reactivo de Grignard R7-MgBr para dar el alcohol de isoxazol secundario 48. La protección del alcohol de isoxazol 48 seguido de desprotección del hidroxi-areno/heteroareno 48 proporciona el hidroxiareno/heteroareno 49, el cual se usa después en la síntesis de los ácidos isoxazol 4-il alquil carbamato ciclohexílicos sustituidos 50 y 51 (usando la misma secuencia sintética que se describe en el esquema 3 para la
conversión de 6 ^ 14).
Esquema 9
El esquema 10 describe la síntesis de los ácidos pirazin isoxazol carbamato ciclohexílicos 57 y 58. La reacción del acetoacetato 33 con metilamina proporciona el carbamato vinílogo 52. Un ácido 5-halopirazin 2-carboxílico 53 apropiado (preferentemente 5-bromo) se hace reaccionar con cloruro de oxalilo para proporcionar el cloruro de pirazin ácido 54. El cloruro de pirazin ácido 54 se hace reaccionar con el carbamato vinílogo 52 en presencia de base para dar el aducto de pirazina acilado 55, el cual se condensa con hidroxilamina para formar el isoxazol éster de pirazina 56. El isoxazol éster de halo pirazina se usa en la síntesis de los ácidos pirazin isoxazol carbamato ciclohexílicos 57 y 58 en analogía a las secuencias sintéticas descritas anteriormente en los esquemas 1 y 3.
E sq u e m a 10
El esquema 11 describe la síntesis de los a-fluoroácidos isoxazol carbamato ciclohexílicos 66 y 67. La reacción de Diels-Alder del 1,3-butadieno y 2-fluoroacrilato de etilo en condiciones térmicas (por ejemplo, procedimiento de Kotikyan e t a l., B u lle tin o f the A c a d e m y o f S c ie nce s o f the USSR , D iv is ió n o f C h e m ica l S c ie nce (E ng l.), 1971,20, 292) proporciona el a-fluoro ciclohexil éster 59. La hidrólisis del a-fluoro-éster 59 en condiciones básicas proporciona el afluoro-ácido 60. La yodolactonización (por ejemplo, Nols0e, J. M. J. e t a l., E u r . J. O rg. C h e m ., 2014, 3051-3065) del alqueno de 60 da la yodolactona 61. La desyodación en condiciones radicales (por ejemplo AIBN/ (TMS)3SiH, ref. Chatgilialoglu, C. e t a l., M o le c u le s , 2012, 17, 527-555) proporciona la lactona 62. La apertura de la lactona 62 mediante una condición ácida (por ejemplo, AcCl en iPrOH) da el a-fluoro-éster de ciclohexilo 63. La reacción del hidroxi ciclohexil a-fluoro-éster 63 con el hidroxiaril/heteroaril isoxazol 6 en condiciones de reacción de Mitsunobu proporciona el isoxazol ciclohexil éter a-fluoro éster 64 correspondiente, que después se usa para los ácidos isoxazol NH-carbamato ciclohexílicos 65 o los ácidos isoxazol carbamato N,N-disustituido ciclohexílicos 66 de acuerdo con las secuencias sintéticas descritas en los esquemas 1 y 2.
E sq u e m a 11
Reacción de Desproteccion
calor
El esquema 12 describe la síntesis del isoxazol carbamato ciclohexil tetrazol 69. El ácido isoxazol carbamato ciclohexílico 14 se convierte se convierte en el cloruro de ácido correspondiente (con, por ejemplo, cloruro de oxalilo); la reacción posterior con amoniaco da la amida primaria 67. La deshidratación de la amida primaria 67 con, por ejemplo, reactivo de Burgess (Talibi, P. et al., eEROS Encyclopedia of Reagents for Organic Synthesis, publicado online el 15 de septiembre de 2008, DOI: 10.1002/047084289X.rm095m.pub2) proporciona el nitrilo 68. La cicloadición de azida sódica con nitrilo 68 (por ejemplo, H. Yoneyama, et al, Synthesis, 2013, 45, 1051-1059) proporciona el isoxazol carbamato ciclohexil tetrazol 69.
Esquema 12
VII. Ejemplos
Los ejemplos siguientes se ofrecen a modo de ilustración, como un alcance parcial y realizaciones particulares de la invención y no pretenden limitar el ámbito de la invención. Las abreviaturas y símbolos químicos tienen sus significados usuales y habituales a menos que se indique de otro modo. A menos que se indique de otro modo, los compuestos descritos en el presente documento se han preparado, aislado y caracterizado usando los esquemas y otros métodos divulgados en el presente documento o se pueden preparar usando los mismos.
Según sea adecuado, las reacciones se llevaron a cabo en atmósfera de nitrógeno seco (o argón). Para reacciones anhidras, se emplearon disolventes de DRISOLV® de EM. Para otras reacciones, se utilizaron disolventes de calidad de reactivo o calidad de HPLC. A menos que se indique otra cosa, todos los reactivos obtenidos en el mercado se usaron tal cual se recibieron.
Se llevaron a cabo reacciones con microondas usando un instrumento Biotage Initiator de 400 W en recipientes de reacción con microondas con irradiación de microondas (2,5 GHz).
Se emplearon métodos de HPLC/MS y HPLC preparatoria/analítica en la caracterización o purificación de los ejemplos Habitualmente los espectros de RMN (resonancia magnética nuclear) se obtuvieron con instrumentos Bruker o JEOL 400 MHz y 500 MHz en los disolventes indicados. Todos los desplazamientos químicos se indican en ppm a partir de tetrametilsilano con la resonancia del disolvente como patrón interno. Los datos espectrales de RMN 1H normalmente se indican como sigue: desplazamiento químico, multiplicidad (s = singlete, s a = singlete ancho, d = doblete, dd = doblete de dobletes, t = triplete, c = cuartete, sep = septuplete, m = multiplete, ap = aparente), constantes de acoplamiento (Hz) e integración.
En los ejemplos en los que los espectros de RMN 1H se recogieron en d6-DMSO, a menudo se utiliza una secuencia de supresión de agua. Esta secuencia suprime de manera eficaz la señal de agua y cualquier pico protónico en la misma región, normalmente entre 3,30-3,65 ppm, que afectaría la integración protónica global.
El término HPLC se refiere a un instrumento de cromatografía líquida de alta resolución Shimadzu con uno de los métodos siguientes:
HPLC-1: columna Sunfire C18 (4,6 x 150 mm) 3,5 pm, gradiente del 10 al 100 % de B:A durante 12 min, después parada de 3 min al 100% de B.
Fase móvil A: TFA al 0,05 % en agua:CH3CN (95:5)
Fase móvil B: TFA al 0,05 % en CH3CN:agua (95:5)
Tampón de TFA pH = 2,5; Caudal: 1 ml/min; Longitud de onda: 254 nm, 220 nm.
HPLC-2: XBridge Phenyl (4,6 x 150 mm) 3,5 pm, gradiente del 10 al 100 % de B:A durante 12 min, después parada de 3 min al 100% de B.
Fase móvil A: TFA al 0,05 % en agua:CH3CN (95:5)
Fase móvil B: TFA al 0,05 % en CH3CN:agua (95:5)
Tampón de TFA pH = 2,5; Caudal: 1 ml/min; Longitud de onda: 254 nm, 220 nm.
HPLC-3: Chiralpak AD-H, 4,6 x 250 mm, 5 pm.
Fase móvil: EtOH al 30 %-heptano (1:1)/CO2 al 70 %
Caudal = 40 ml/min, 10 MPa (100 Bar), 35 °C; Longitud de onda: 220 nm
HPLC-4: Waters Acquity UPLC BEH C18, 2,1 * 50 mm, partículas de 1,7 pm;
Fase móvil A: 5:95 de CH3CN:agua con NH4OAc 10 mM;
Fase móvil B: 95:5 de CH3CN:agua con NH4OAc 10 mM;
Temperatura: 50 °C; Gradiente: 0-100 % de B durante 3 min, después una parada de 0,75 min al 100 % de B; Caudal: 1,11 ml/min;
Detección: UV a 220 nm.
HPLC-5: Waters Acquity UPLC BEH C18, 2,1 * 50 mm, partículas de 1,7 pm;
Fase móvil A: 5:95 CH3CN:agua con TFA al 0,1 %;
Fase móvil B: 95:5 CH3CN:agua con TFA al 0,1 %;
Temperatura: 50 °C; Gradiente: 0-100 % de B durante 3 min, después una parada de 0,75 min al 100 % de B; Caudal: 1,11 ml/min;
Detección: UV a 220 nm.
Intermedio 1
l-fluoro-3-hidroxicidohexanocarboxilato de (±)-cis-isopropilo
Intermedio 1A 1-fluorociclohex-3-enecarboxilato de (rac)-etilo
Una mezcla de buta-1,3-dieno al 20 % en tolueno (13,81 ml, 41,1 mmol) y 2-fluoroacrilato de etilo (3,07 ml, 27,4 mmol) en un tubo cerrado herméticamente se calentó a 120 °C durante 7 días. La reacción se añadió sobre una columna de gel de sílice de 80 g y se eluyó con EtOAc/hexano (del 0 % al 10 % durante 20 min) para obtener el intermedio 1A (3,8 g, 22,07 mmol, 80 % de rendimiento) en forma de un aceite transparente. RMN de 1H (500 MHz, CDCh) 85,79 (ddd, J = 9,9, 4,7, 2,2 Hz, 1H), 5,64 - 5,58 (m, 1H), 4,26 (c, J = 7,2 Hz, 2H), 2,73 - 2,57 (m, 1H), 2,45 - 2,23 (m, 2H), 2,20 -1,91 (m, 3H), 1,32 (t, J = 7,2 Hz, 3H); RMN de 19F (471MHz, CDCh) 8-162,69 (s, 1F).
Intermedio 1B Ácido (rac)-1-fluorociclohex-3-enecarboxílico
Una mezcla del intermedio 1A (3,8 g, 22,07 mmol) y LiOH ac. 2,0 M (55,2 ml, 110 mmol) en THF (50 ml) se agitó a ta durante 18 h. La reacción se acidificó a pH = 2 con HCl (9,19 ml, 110 mmol) y después se extrajo con EtOAc (x3). Los extractos combinados se lavaron con agua y se concentraron para obtener el intermedio 1B (3,0 g, 20,81 mmol, 94 % de rendimiento) en forma de un aceite de color amarillento claro. RMN de 1H (500 MHz, CDCla) 85,81 (ddd, J = 9,8, 4,6, 2,1 Hz, 1H), 5,66 -5,58 (m, 1H), 2,76 -2,59 (m, 1H), 2,49 -2,37 (m, 1H), 2,35 -2,23 (m, 1H), 2,22 - 1,92 (m, 3H); RMN de 19F (471MHz, CDCh) 8 -163,02 (s, 1F).
Intermedio 1C (Rac)-1-fluoro-4-yodo-6-oxabiciclo[3.2.1]octan-7-ona
Al intermedio 1B (3 g, 20,81 mmol) en agua (20 ml) se le añadió bicarbonato sódico (5,25 g, 62,4 mmol) en porciones y se agitó hasta homogeneizarlo. Se añadió la solución de yodo (5,81 g, 22,89 mmol) y KI (20,73 g, 125 mmol) se disolvió en 20 ml de agua) y la reacción se agitó durante una noche en la oscuridad. A la reacción se le añadió agua y se extrajo con DCM (3x), se lavó con tiosulfato sódico al 10 % (20 ml x 2) y agua, se secó sobre MgSO4 y se concentró. El aceite en bruto se añadió sobre una columna de gel de sílice de 80 g y se eluyó con EtOAc/hexano (del 0 % al 50 % durante 20 min) para obtener el intermedio 1C (3,53 g, 13,07 mmol, 62,8 % de rendimiento) en forma de un sólido de color blanco. RMN de 1H (500 MHz, CDCh) 84,89 (dt, J = 6,5, 3,5 Hz, 1H), 4,44 (c, J = 4,6 Hz, 1H), 3,08 (dd, J=11,6, 1,9 Hz, 1H), 2,75 (tddd, J=11,3, 6,5, 3,3, 1,1 Hz, 1H), 2,50 -2,38 (m, 1H), 2,34 -2,17 (m, 2H), 2,11 -1,99 (m, 1H); RMN de 13C (126 MHz, CDCl3) 8172,2, 172,0, 93,6, 91,9, 78,4, 78,3, 39,2, 39,0, 29,7, 29,6, 28,4, 28,2, 20,2; RMN de 19F (471 MHz, CDCh) 8 -167,97 (s, 1F)
Intermedio 1D (Rac)-1-fluoro-6-oxabiciclo[3.2.1]octan-7-ona
Al intermedio 1C (350 mg, 1,296 mmol) y AIBN (21,28 mg, 0,130 mmol) en benceno (5 ml) se le añadió tris(trimetilsilil)silano (0,600 ml, 1,944 mmol) en porciones durante 10 min a 60 °C. La reacción se agitó después a 70 °C durante 2 h y después se concentró. El residuo se disolvió en EtOAc, se lavó con NH4Cl sat., se secó con MgSO4 y se concentró. El aceite en bruto se añadió sobre una columna de gel de sílice de 12 g y se eluyó con EtOAc/hexano (del 0 % al 30 % durante 10 min) para obtener el intermedio 1D (124 mg, 0,860 mmol, 66,4 % de rendimiento) en forma de un sólido de color blanco. RMN de 19F (471 MHz, CDCh) 8 -167,01 (s, 1F); RMN de 1H (500 MHz, CDCl3) 84,98 4,81 (m, 1H), 2,75 (dtdd, J = 15,9, 6,8, 3,3, 1,7 Hz, 1H), 2,24 - 1,89 (m, 5H), 1,82 - 1,65 (m, 1H), 1,60 - 1,46 (m, 1H); RMN de 13C (126M Hz, CDCla) 8173,2, 173,0, 93,9, 92,3, 75,6, 75,5, 42,0, 41,9, 31,3, 31,1, 26,7, 17,7, 17,6
Intermedio 1
Se añadió cloruro de acetilo (0,061 ml, 0,860 mmol) en porciones a isopropanol (3 ml) a 0 °C y después se agitó a ta durante 30 min. Se añadió al intermedio 1D (124 mg, 0,860 mmol) y se agitó durante una noche. La reacción se concentró. El aceite en bruto se añadió sobre una columna de gel de sílice de 4 g y se eluyó con EtOAc/hexano (del 0 % al 50 % durante 10 min) para obtener el intermedio 1 (140 mg, 0,685 mmol, 80 % de rendimiento) en forma de un aceite transparente. RMN de 1H (500 MHz, CDCl3) 85,08 (spt, J = 6,3 Hz, 1H), 3,91 (tt, J = 10,9, 4,4 Hz, 1H), 2,68 (s a, 1H), 2,28 (dddt, J = 13,5, 9,0, 4,6, 2,1 Hz, 1H), 2,06 - 1,98 (m, 1H), 1,96 - 1,87 (m, 1H), 1,82 - 1,62 (m, 4H), 1,37 -1,22 (m, 7H); RMN de 19F (471 MHz, CDCI3) 8 -162,93 (s, 1F); RMN de 13C (126 MHz, CDCI3) 8170,9, 170,7, 95,7, 94,2, 69,3, 66,1, 40,7, 40,5, 33,9, 31,6, 31,4, 21,5, 19,1.
Intermedio 22-(3-hidroxiciclohexil)acetato de (±)-trans-etilo e intermedio 32-(3-hidroxiciclohexil)acetato de (±)-cis-etilo
Se añadió SOCh (3,58 ml, 49,0 mmol) gota a gota a EtOH (50 ml). La solución se agitó a TA durante 30 min, tras lo cual se añadió ácido 2-(3-hidroxiciclohexil)acético (mezcla de isómeros cis y trans preparado de acuerdo con el procedimiento descrito en Tetrahedron, 1982, 38, 3641-3647; 3,10 g, 19,6 mmol). La reacción se agitó a 50 °C durante una noche, después se enfrió a TA y se concentró al vacío. Se añadió NaHCO3 ac. sat.; la mezcla se extrajo con EtOAc (2x). Los extractos orgánicos combinados se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 20-75 % de EtOAc en hexanos) para dar los compuestos del título cis y trans individuales en forma de aceites.
Intermedio 2. 2-(3-hidroxiciclohexil)acetato de (±)-trans-etilo (1,42 g, 39 %). RMN de 1H (500 MHz, CDCh) 84,13 (c, J = 7,2 Hz, 2H), 4,07 (m, 1H), 2,29-2,21 (m, 1H), 2,20 (m, 2H), 1,80-1,64 (m, 4H), 1,55-1,47 (m, 2H), 1,37 (d, J = 3,6 Hz, 1H), 1,33 (s, 1H), 1,26 (t, J = 7,0 Hz, 3H), 1,10-1,00 (m, 1H).
Intermedio 3. 2-(3-hidroxiciclohexil)acetato de (±)-cis-etilo (235 mg, 6 %). RMN de 1H (500 MHz, CDCh) 84,13 (c, J = 7,2 Hz, 2H), 3,64-3,57 (m, 1H), 2,23 (dd, J=7,0, 4,3 Hz, 2H), 2,04-1,95 (m, 2H), 1,90-1,75 (m, 2H), 1,71-1,66 (m, 1H), 1,43 (d, J = 4,4 Hz, 1H), 1,36-1,29 (m, 1H), 1,26 (t, J = 7,2 Hz, 3H), 1,19-1,09 (m, 1H), 1,01-0,82 (m, 2H).
Ejemplo 1. Ácido (1S,3S)-3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)ciclohexan-1-carboxílico
1A. (5-(4-bromofenil)-3-metilisoxazol-4-il)metanol
A una solución de ácido 5-(4-bromofenil)-3-metilisoxazol-4-carboxílico (sintetizado de acuerdo con el procedimiento descrito en el documento US2011/82164 A1, 2,0 g, 7,09 mmol) en THF (50 ml) se le añadió BH3 THF (28,4 ml de una solución 1 M en THF, 28,4 mmol) en porciones a 0 °C y la solución se dejó calentar a TA y se agitó durante una noche a TA. La mezcla de reacción se inactivó cuidadosamente con H2O, se acidificó con HCl ac. 1 N (50 ml), se agitó durante 1 h a TA, después se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2 ; gradiente continuo del 35-75 % de EtOAc en hexanos) para dar el compuesto del título (1,65 g, 87 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 268. RMN de 1H (CDCh 400 MHz) 87,73-7,64 (m, 4H), 4,66 (d, J = 5,1 Hz, 2H), 2,42 (s, 3H).
1B. 5-(4-bromofenil)-3-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol
A una solución de (5-(4-bromofenil)-3-metilisoxazol-4-il)metanol (626 mg, 2,33 mmol) en CH2Ch (10 ml) se le añadió 3,4-dihidro-2H-pirano (0,64 ml, 7,0 mmol) y PPTS (29 mg, 0,12 mmol). Después de agitar durante una noche a TA, la mezcla se inactivó con NaHCO3 ac. sat. y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO2; gradiente continuo del 35-100 % de EtOAc/Hexanos) para dar el compuesto del título (811 mg, 99 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 358. RMN de 1H (500 MHz, CDCh) 87,82-7,55 (m, 4H), 4,69 (m, 1H), 4,65 (m, 1H), 4,46 (m, 1H), 3,87 (m, 1H), 3,54 (m, 1H), 2,37 (s, 3H), 1,86-1,55 (m, 6H).
1C. 4-(3-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol-5-il)fenol
A una solución de KOH (2,70 g, 48,1 mmol) en H2O (50 ml) se le añadieron sucesivamente el intermedio 1B (5,65 g, 16,0 mmol) y dioxano (50 ml) y la solución se desgasificó con N2. Se añadieron f-BuXphos (0,545 g, 1,28 mmol) y Pd2(dba)3 (0,294 g, 0,321 mmol) y la suspensión se desgasificó con N2, después se agitó a 90 °C durante una noche. La mezcla de reacción se enfrió a TA, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 25-75 % de EtOAc/Hexanos) para dar el compuesto del título (3,63 g, 78 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 290. RMN de 1H (500 MHz, CDCh) 87,72 (d, J = 8,8 Hz, 2H), 6,94 (d, J = 8,8 Hz, 2H), 4,70 (m, 1H), 4,66 (d, J = 12,4 Hz, 1H), 4,48 (d, J = 12,4 Hz, 1H), 3,89 (m, 1H), 3,53 (m, 1H), 2,36 (s, 3H), 1,88-1,70 (m, 2H), 1,65-1,57 (m, 4H).
1D. 5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol
A una solución a TA de 1C (2,0 g, 6,91 mmol) en DMF (50 ml) se le añadió TBSCI (2,08 g, 13,8 mmol) e imidazol (1,88 g, 27,7 mmol). La reacción se agitó a TA durante 6 h, tras lo cual se añadió H2O (4 ml). La mezcla se concentró parcialmente al vacío, se diluyó con H2O, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, LiCl ac. al 10 %, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO2; gradiente continuo del 0-30 % de EtOAc/Hexanos) para dar el compuesto del título (2,55 g, 91 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 404. RMN de 1H (500 MHz, CDCh) 8 7,75-7,67 (m, 2H), 6,93 (d, J = 8,8 Hz, 2H), 4,71-4,68 (m, 1H), 4,66 (d, J = 12,4 Hz, 1H), 4,48 (d, J = 12,4 Hz, 1H), 3,88 (m, 1H), 3,53 (m, 1H), 2,36 (s, 3H), 1,87-1,78 (m, 1H), 1,76-1,69 (m, 1H), 1,65-1,54 (m, 4H), 1,00 (s, 9H), 0,23 (s, 6H).
1E. (5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metilisoxazol-4-il)metanol
A una solución a TA de 1D (2,45 g, 6,07 mmol) en MeOH (75 ml) se le añadió PPTS (0,30 g, 1,21 mmol). Se calentó la reacción a 50 °C durante 2 h, después se enfrió a TA y se concentró al vacío. La mezcla se diluyó con H2O y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO2; gradiente continuo del 25-50 % de EtOAc en hexanos) para dar el compuesto del título (1,18 g, 61 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 320. RMN de 1H (500 MHz, CDCh) 87,68 (d, J = 8,8 Hz, 2H), 6,94 (d, J = 8,8 Hz, 2H), 4,63 (s, 2H), 2,37 (s, 3H), 1,00 (s, 9H), 0,24 (s, 6H).
1F. (5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metilisoxazol-4-il)metil(4-nitrofenil)carbonato
A una solución a TA de 1E (1,8 g, 5,63 mmol) en CH2Ch (50 ml) se le añadieron sucesivamente piridina (2,28 ml, 28,2 mmol) y cloroformiato de 4-nitrofenilo (1,82 g, 9,01 mmol) en porciones. La mezcla de reacción se agitó a TA durante 1 h, después se concentró al vacío y el residuo se cromatografió (SO 2; gradiente continuo del 0-40 % de EtOAc/Hexanos) para dar el compuesto del título ligeramente impuro (2,95 g, 108 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 485. RMN de 1H (500MHz, CDCla) 88,28 (d, J = 9,1 Hz, 2H), 7,68 (d, J = 8,8 Hz, 2H), 7,40 (d, J = 9,4 Hz, 2H), 6,98 (d, J = 8,8 Hz, 2H), 5,27 (s, 2H), 2,43 (s, 3H), 1,00 (s, 9H), 0,25 (s, 6H).
1G. Ciclopentil(metil)carbamato de (5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metilisoxazol-4-il)metilo
A una solución a TA de 1F (1,5 g, 3,10 mmol) en THF (24 ml) se le añadió iPr2NEt (1,62 ml, 9,29 mmol) y N-metilciclopentanamina (0,61 g, 6,19 mmol). La mezcla de reacción se agitó durante una noche a TA, después se diluyó con H2O y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con NaHCO3 ac. sat, H2O, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 10-40 % de EtOAc/Hexanos) para dar el compuesto del título (1,08 g, 78 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 445. RMN de 1H (500 MHz, CDCla) 87,67 (d, J = 8,5 Hz, 2H), 6,94 (d, J = 8,8 Hz, 2H), 5,08 (s, 2H), 4,70-4,29 (m, 1H), 2,76 (s a, 3H), 2,38 (s, 3H), 1,82-1,49 (m, 8H), 1,00 (s, 9H), 0,24 (s, 6H).
1H. Ciclopentil(metil)carbamato de (5-(4-hidroxifenil)-3-metilisoxazol-4-il)metilo
A una solución de 1G (1,08 g, 2,429 mmol) en THF (24 ml) se le añadió Bu4NF (3,04 ml de una solución 1 M en THF, 3,04 mmol). La mezcla de reacción se agitó a TA durante 1,5 h, después se concentró al vacío, se diluyó con H2O, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2 ; gradiente continuo del 25-60 % de EtOAc/Hexanos) para dar el compuesto del título (619 mg, 77 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 331. RMN de 1H (500 MHz, CDCla ) 87,63 (d, J = 8,5 Hz, 2H), 6,97 (d, J = 8,8 Hz, 2H), 5,12 (s, 2H), 4,79-4,19 (m, 1H), 2,78 (s a, 3H), 2,39 (s, 3H), 2,00-1,33 (m, 8H).
1I. 3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metil-isoxazol-5-il)fenoxi)ciclohexan-1-carboxilato de (1S,3S)-isopropilo
A una solución de 3-hidroxiciclohexanocarboxilato de (1S,3R)-isopropilo (sintetizado de acuerdo con el procedimiento descrito en el documentoUS2007/0197788A1, 77 mg, 0,41 mmol), 1H (80 mg, 0,24 mmol) y Ph3P (95 mg, 0,36 mmol) en THF (3 ml) se le añadió DEAD (0,165 ml, 0,36 mmol). La mezcla de reacción se agitó durante una noche a TA, después se concentró al vacío. El residuo se cromatografió (SO2; gradiente continuo del 15-70 % de EtOAc en Hexanos), después se purificó por HPLC preparativa de fase inversa (Phenomenex Lumina Axia; columna de 30 x 100 mm; 70-100 % de MeOH/H2O con TFA al 0,1 %; gradiente de 7 min) para dar el compuesto del título (43 mg, 36 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 499.
Ejemplo 1
A una solución de 1I (43 mg, 0,086 mmol) en MeOH (1 ml) y THF (1 ml) se le añadió LiOH ac. 2 M (1 ml, 2,0 mmol) y
la reacción se calentó a 50 °C durante 1 h, después se enfrió a TA. La mezcla se diluyó con H2O, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El producto en bruto se purificó por HPLC preparativa de fase inversa: Phenomenex Lumina Axia; columna de 30 x 100 mm; 70-100 % de MeOH/H2O con TFA al 0,1 %; gradiente de 10 min para dar el compuesto del título (32 mg, 80 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 457. RMN de 1H (500 MHz, CDCla ) 87,71 (d, J = 8,8 Hz, 2H), 7,01 (d, J = 9,1 Hz, 2H), 5,09 (s, 2H), 4,70 (m, 1H), 2,89 (m, 1H), 2,82-2,72 (m, 3H), 2,39 (s, 3H), 2,17-2,10 (m, 1H), 2,01-1,89 (m, 3H), 1,85-1,72 (m, 3H), 1,71-1,59 (m, 6H), 1,58-1,43 (m, 4H). CI50 de hLPA1 = 14 nM.
Ejemplo 2
Ácido (1S,3S)-3-(4-(4-(((butil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)ciclohexan-1-carboxílico
2A. 3-(4-(3-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol-5-il)fenoxi)ciclohexan-1-carboxilato de (1S,3S)-isopropilo
A una solución a TA de 1C (500 mg, 1,73 mmol), 3-hidroxiciclohexanocarboxilato de (1S,3R)-isopropilo (547 mg, 2,94 mmol), Et3 N (0,41 ml, 2,94 mmol) y Ph3 P (770 mg, 2,94 mmol) en THF (10 ml) se le añadió DEAD (1,34 ml, 2,94 mmol) en porciones durante 15 min. La mezcla de reacción se agitó a TA durante 2 días, después se concentró al vacío, se diluyó con H2O, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2 ; gradiente continuo del 15-70 % de EtOAc/Hexanos) para dar el compuesto del título (458 mg, 58 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 458. RMN de 1H (500 MHz, CDCla) 87,75 (d, J = 8,8 Hz, 2H), 7,03 (d, J = 8,8 Hz, 2H), 5,02 (m, 1H), 4,70 (m, 1H), 4,66 (d, J = 12,4 Hz, 1H), 4,48 (d, J = 12,4 Hz, 1H), 3,88 (m, 1H), 3,54 (m, 1H), 2,80 (m, 1H), 2,35 (s, 3H), 2,08-1,97 (m, 2H), 1,93-1,80 (m, 3H), 1,78-1,52 (m, 10H), 1,24 (m, 6H).
2B. 3-(4-(4-(hidroximetil)-3-metilisoxazol-5-il)fenoxi)ciclohexan-1-carboxilato de (1S,3S)-isopropilo
A una solución a TA de 2A (458 mg, 1,00 mmol) en MeOH (10 ml) se le añadió PPTS (25 mg, 0,10 mmol). La reacción se agitó a TA durante una noche, después se calentó a 50 °C durante 2 h y se enfrió a TA. La mezcla se basificó a pH ~7 con NaHCO3 ac. sat. y se concentró al vacío. La mezcla se diluyó con H2O y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 15-70% de EtOAc/Hexanos) para dar el compuesto del título (263 mg, 70 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 374. RMN de 1H (500 MHz, CDCh) 8 7,71 (d, J = 8,8 Hz, 2H), 7,09 (d, J = 8,8 Hz, 2H), 5,42 (s, 2H), 5,05 (m, 1H), 4,74 (m, 1H), 2,83 (m, 1H), 2,45 (s, 3H), 2,04 (m, 2H), 1,92 (m, 2H), 1,82-1,58 (m, 5H), 1,27 (dd, J = 6,3, 1,4 Hz, 6H).
2C. 3-(4-(3-metil-4-((((4-nitrofenoxi)carbonil)oxi)metil)isoxazol-5-il)fenoxi)ciclohexan-1-carboxilato de (1S,3S)-isopropilo
A una solución a TA de 2B (263 mg, 0,704 mmol) en CH2Ch (7 ml) se le añadieron sucesivamente piridina (0,28 ml, 3,52 mmol) y cloroformiato de 4-nitrofenilo (284 mg, 1,41 mmol) en porciones. La mezcla de reacción se agitó a TA durante 1 h, después se concentró al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 0-50 % de EtOAc/Hexanos) para dar el compuesto del título (348 g, 92 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 539. RMN de 1H (500 MHz, CDCl3) 88,32 (d, J = 9,1 Hz, 2H), 7,75 (d, J = 9,1 Hz, 2H), 7,42 (d, J = 9,1 Hz, 2H), 7,09 (d, J = 9,1 Hz, 2H), 5,30 (s, 2H), 5,06 (m, 1H), 4,74 (m, 1H), 2,84 (m, 1H), 2,49-2,39 (m, 3H), 2,03 (m, 2H), 1,92 (m, 2H), 1,84-1,74 (m, 2H), 1,69-1,56 (m, 2H), 1,28 (dd, J = 6,3, 1,1 Hz, 6H).
2D. 3-(4-(4-(((butil(metil)carbamoil)oxi)metil)-3-metil-isoxazol-5-il)fenoxi)ciclohexan-1-carboxilato de (1S,3S)-isopropilo
A una solución a TA de 2C (54 mg, 0,100 mmol) en THF (2 ml) se le añadió iPr2NEt (0,10 ml, 0,60 mmol) y N-metilbutan-1-amina (26 mg, 0,30 mmol). La reacción se agitó a TA durante una noche, después se diluyó con NaHCO3 ac. sat. y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 15-70 % de EtOAc en hexanos) para dar el compuesto del título ligeramente impuro (54 mg, 111 % de rendimiento) en forma de un sólido de color blanco que se usó tal cual. LC-MS, [M+H]+ = 487.
Ejemplo 2
A una solución a TA de 2D (54 mg, 0,11 mmol) en MeOH (1,25 ml) y THF (1,25 ml) se le añadió LiOH ac. 2 M (1,25 ml, 2,50 mmol) y la reacción se calentó a 50 °C durante 1 h, después se enfrió a TA. La mezcla se diluyó con H2O, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se purificó por HPLC preparativa de fase inversa: Phenomenex Lumina Axia; columna de 30 x 100 mm; 60-100 % de MeOH/H2O con TFA al 0,1 %; gradiente de 8 min para dar el compuesto del título (31 mg, 62 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 445. RMN de 1H (500 MHz, CDCh) 87,71 (d, J = 8,8 Hz, 2H), 7,01 (d, J = 8,8 Hz, 2H), 5,08 (s, 2H), 4,72 (m, 1H),
3,29 (m, 1H), 3,19 (m, 1H), 2,93-2,83 (m, 4H), 2,38 (s, 3H), 2,15 (m, 1H), 2,02-1,90 (m, 3H), 1,83-1,73 (m, 1H), 1,70 1,58 (m, 3H), 1,55-1,39 (m, 2H), 1,37-1,17 (m, 2H), 0,97-0,81 (m, 3H). CI50 de hLPA1 = 28 nM.
Ejemplo 3
Ácido (±)-trans-3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)-1-fluorociclohexanocarboxílico
3A. 3-(4-(4-(((cidopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)-1-fluorocidohexanocarboxilato de (±)-trans-isopropilo
A una solución del intermedio 1 (50,7 mg, 0,248 mmol) y 1H (82 mg, 0,248 mmol) en THF (2 ml) se le añadió Ph3P (98 mg, 0,372 mmol) y TEA (0,052 ml, 0,372 mmol). Mientras se agitaba, se añadió DIAD (0,072 ml, 0,372 mmol) a la mezcla de reacción y la mezcla de reacción se agitó a ta durante 18 h. La mezcla de reacción se filtró. El filtrado se concentró. El aceite en bruto se purificó por HPLC prep. (columna Phenomenex Axia 5 u C1830 x 100 mm; detección a 220 nm; caudal = 40 ml/min; gradiente continuo de B al 40 % a B al 100 % durante 10 min 4 min de parada al 100 % de B, donde A = 90:10:0,1 de H2O:MeOH:TFA y B = 90:10:0,1 de MeOH:H2O:TFA) para obtener 3A (17 mg, 0,033 mmol, 13,26 % de rendimiento) en forma de un aceite transparente. RMN de 19F (471MHz, CDCl3) 8 -151,98 (s, 1F); RMN de 1H (500 MHz, CDCh) 87,71 (d, J = 8,8 Hz, 2H), 7,03 (d, J = 8,8 Hz, 2H), 5,16-5,06 (m, 3H), 4,72 (tt, J = 7,7, 3,7 Hz, 1H), 4,53 (s a, 1H), 2,77 (s a, 3H), 2,59-2,46 (m, 1H), 2,39 (s, 3H), 2,22-2,07 (m, 1H), 2,07-1,41 (m, 14H), 1,32 (dd, J = 6,3, 3,0 Hz, 6H).
Ejemplo 3
Una mezcla de 3A (17 mg, 0,033 mmol) y LiOH ac. 2,0 M (0,165 ml, 0,329 mmol) en THF (0,5 ml)/MeOH (0,1 ml) se agitó a ta durante 2 h y después se purificó por HPLC prep. (columna Phenomenex Axia 5 u C18 30 x 100 mm; detección a 220 nm; caudal = 40 ml/min; gradiente continuo de B al 30 % a B al 100 % durante 10 min 2 min de parada al 100 % de B, donde A = 90:10:0,1 de H2O:MeOH:TFA y B = 90:10:0,1 de MeOH:H2O:TFA) para obtener el ejemplo 3 racémico (15 mg, 0,031 mmol, 94 % de rendimiento) en forma de un sólido de color blanco. [M H]+ = 475,4; RMN de 1H (500 MHz, CDCla ) 87,71 (d, J = 8,8 Hz, 2H), 7,02 (d, J = 9,1 Hz, 2H), 5,09 (s, 2H), 4,77 (tt, J = 7,2, 3,7 Hz, 1H), 4,69-4,19 (m, 1H), 2,76 (s a, 3H), 2,56-2,44 (m, 1H), 2,39 (s, 3H), 2,22-1,43 (m, 15H); RMN de 19F (471 MHz, CDCh ) 8 -149,50 (s, 1F).CIa0 de hLPA1 = 18 nM.
Ejemplo 4 enantiómero I y ejemplo 5 enantiómero II
El ejemplo 3 (9 mg, 0,019 mmol) se separó por separación quiral mediante SFC prep. (Instrumento: Berger Prep SFC; Columna: Chiralpak IC, 21 x 250 mm, 5 micrómetros; Fase móvil: MeOH al 30%/C02 al 70 %; condiciones de caudal: 45 ml/min, 10 MPa (100 Bar), 40 °C; Longitud de onda del detector: 272 nm; Detalles de inyección: 0,5 ml de solución de 2,5 mg/ml en MeOH) para obtener el primer enantiómero I Ejemplo 4 (2 mg, 4,21 jmol, 22,22 % de rendimiento, CI 50 de hLPA1 15 nM) y el segundo enantiómero II Ejemplo 5 (3 mg, 6,32 |jmol, 33,3 de rendimiento, CI50 de hLPA1 = 133 nM) en forma de un aceite.
Ejemplo 6
6A. 3-((ferc-butildimetilsilil)oxi)-1-fluorociclohexanocarboxilato de (rac)-trans-etilo
A una solución de diisopropilamina (0,373 ml, 2,62 mmol) en THF (5 ml) se le añadió n-BuLi 2,5 M en hexano (1,047 ml, 2,62 mmol) gota a gota a -78 °C. Se agitó durante 10 min., después se cambió el baño refrigerante de hielo seco por un baño de agua con hielo. Se agitó durante 40 min. Se baño refrigerante se cambió de nuevo a un baño de hielo seco-acetona, se añadió una solución de 3-((tercbutildimetilsilil)oxi)ciclohexanocarboxilato de etilo (0,5 g, 1,745 mmol) en THF (5 ml) gota a gota durante 40 min a -78 °C. Se agitó durante 10 min. después se cambió el baño refrigerante de hielo seco por un baño de agua con hielo. Se agitó durante 1 h. El baño de refrigeración se volvió a cambiar a hielo seco-acetona y se añadió n-fluorobencenosulfonimida (0,715 g, 2,269 mmol) en THF (5 ml) gota a gota. Se agitó durante 10 min., después se eliminó el baño frío y se dejó calentar a temperatura ambiente. Se agitó durante 1 h. La mezcla de reacción se inactivó con una solución sat. de NH4CI y se extrajo con éter (x2). Las capas orgánicas combinadas se secaron (Na2SO4), se filtraron y se concentraron. El aceite en bruto se añadió sobre una columna de gel de sílice de 12 g y se eluyó con EtOAc/hexano (del 0 % al 20 % durante 15 min) para obtener 6A (0,44 g, 1,445 mmol, 83 % de rendimiento) en forma de un aceite de color amarillento claro. RMN de 1H (500 MHz, CDCh) 64,25 (cd, J = 7,2, 5,0 Hz, 2H), 4,00-3,84 (m, 1H), 2,40-2,28 (m, 1H), 2,26-2,05 (m, 1H), 1,98-1,60 (m, 5H), 1,42-1,24 (m, 5H), 0,94-0,84 (m, 9H), 0,07 (d, J = 2,8 Hz, 6H).
6B . 1 -flu o ro -3 -h id ro x ic ic lo h e xa n o ca rb o x ila to de (ra c )-tra n s -e tilo
Una mezcla de 6A (0,44 g, 1,445 mmol) y TBAF 1,0 M en THF (1,806 ml, 1,806 mmol) en THF (2 ml) se agitó a ta durante 2 h y después se concentró. El residuo se disolvió en MTBE y después se lavó con salmuera. La solución acuosa se extrajo con MTBE (x3). Los extractos orgánicos combinados se secaron sobre MgSO4 y se concentraron. El aceite en bruto se añadió sobre una columna de gel de sílice de 12 g y eluyendo con EtOAc/hexano (del 0 % al 30 % durante 12 min) para obtener 6B (0,232 g, 1,220 mmol, 84 % de rendimiento) en forma de un aceite transparente. RMN de 1H (500MHz, CDCh) 84,24 (c, J = 7,2 Hz, 2H), 4,07-3,84 (m, 1H), 3,12-2,72 (m, 1H), 2,35-2,19 (m, 1H), 2,07 1,47 (m, 7H), 1,36-1,25 (m, 3H); RMN de 19F (471MHz, CDCla) 8-152,13 (s, 1F).
6C. 3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)-1-fluorociclohexanocarboxilato de (rac)-cis-etilo
A una solución de 6B (82 mg, 0,248 mmol) en tolueno (2 ml) se le añadió tri-n-butilfosfina (0,092 ml, 0,372 mmol). Mientras se agitaba, se añadió 1,1'-(azodicarbonil)dipiperidina (94 mg, 0,372 mmol) a la mezcla de reacción y la mezcla de reacción se calentó a 50 °C durante 2 h. La LCMS mostró la masa de producto deseada. La mezcla de reacción se filtró. El filtrado se concentró. El aceite en bruto se añadió sobre una columna de gel de sílice de 4 g y se eluyó con EtOAc/hexano (del 0 % al 30 % durante 10 min) para obtener 6C (40 mg, 0,080 mmol, 32,1 % de rendimiento) en forma de un aceite transparente. [M H]+ = 503,3.
Ejemplo 6
Una mezcla de 6C (40 mg, 0,080 mmol) y LiOH ac. 2,0 M (0,398 ml, 0,796 mmol) en THF (1 ml)/MeOH (0,1 ml) se agitó a ta durante 18 h. La reacción en bruto se purificó por HPLC prep (Columna: XBridge C18, 19 * 200 mm, partículas de 5 pm; Fase móvil A: 5:95 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Fase móvil B: 95:5 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Gradiente: 40-80 % de B durante 25 minutos, después una parada de 5 minutos al 100 % de B; Caudal: 20 ml/min.) para el ejemplo 6 (6,9 mg, 0,013 mmol, 16,44 % de rendimiento) en forma de un aceite. [M Na]+ = 497,1. CI50 de hLPA1 = 103 nM.
Ejemplo 7. Ácido (±)-cis-3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)-1-metilciclohexanocarboxílico
7A. 3 -(( te rc -b u tild im e tils ilil)o x i)c ic lo h e x a n o c a rb o x ila to de e tilo
A una solución de 3-hidroxiddohexanocarboxilato de etilo (1,36 g, 7,90 mmol) y TBSCI (1,309 g, 8,69 mmol) en DMF (5 ml) se le añadió 1H-imidazol (0,645 g, 9,48 mmol) en DMF (5 ml) gota a gota durante 2 h. La reacción se agitó a TA durante una noche, después se diluyó con Et2O. La mezcla se lavó con salmuera; la fase orgánica se lavó con agua, se secó (Na2SO4) y se concentró al vacío. El producto oleoso en bruto se cromatografió (40 g SO 2; gradiente continuo del 0 % al 20 % EtOAc/hexano durante 15 min) para dar el compuesto del título (2,20 g, 7,68 mmol, 97 % de rendimiento) en forma de un aceite transparente.
7B. 3-((ferc-butildimetilsilil)oxi)-1-metilciclohexanocarboxilato de (±)-trans-etilo
A una solución a -78 °C de iPr2 NH (1,64 ml, 11,5 mmol) en THF (12 ml) se le añadió gota a gota BuLi 2,5 M en hexano (4,61 ml, 11,5 mmol). La mezcla se agitó a -78 °C durante 10 min, después se dejó calentar a 0 °C y se agitó durante 40 min a 0 °C. La solución se enfrió a -78 °C y se añadió una solución de 7A (2,20 g, 7,68 mmol) en THF (12 ml) gota a gota durante 40 min a -78 °C. La solución de reacción se agitó a -78 °C durante 10 min, después se dejó calentar a 0 °C y se agitó durante 1 h a 0 °C. La solución se enfrió a -78 °C y se añadió CH3 I (0,720 ml, 11,5 mmol) gota a gota. La reacción se agitó durante 10 min a -78 °C, después se dejó calentar lentamente a TA y se agitó a TA durante 1 h, después se inactivó con NH4CI ac. sat. y se extrajo con Et2O (2x). Los extractos orgánicos combinados se secaron (Na2SO4) y se concentraron al vacío. El aceite en bruto se cromatografió (40 g de SO 2 ; gradiente continuo del 0 % al 20 % de EtOAc en hexano durante 15 min) para dar el compuesto del título (2,2 g, 7,32 mmol, 95 % de rendimiento) en forma de un aceite transparente. RMN de 1H (500MHz, CDCh) 84,14 (c, J = 7,0 Hz, 2H), 3,64 (tt, J = 10,6, 4,3 Hz, 1H), 2,31 (ddt, J = 12,7, 4,2, 2,1 Hz, 1H), 2,12-2,05 (m, 1H), 1,85-1,77 (m, 1H), 1,69-1,59 (m, 1H), 1,33-1,23 (m, 5H), 1,23-1,09 (m, 5H), 0,90 (s, 9H), 0,08 (d, J = 3,6 Hz, 6H).
7C. 3-hidroxi-1-metilciclohexanocarboxilato de (±)-trans-etilo
Una mezcla de 7B (2,20 g, 7,32 mmol) y 1,0 M TBAF en THF (9,15 ml, 9,15 mmol) en THF (10 ml) se agitó a TA durante 18 h, después se concentró al vacío. El residuo se disolvió en MTBE y después se lavó con salmuera. La solución acuosa se extrajo con MTBE (x3). Los extractos orgánicos combinados se secaron (MgSO4) y se concentraron al vacío. El aceite en bruto se cromatografió (40 g de SO 2; gradiente continuo del 0 % al 50 % EtOAc/hexano durante 15 min) para dar el compuesto del título (1,20 g, 6,44 mmol, 88 % de rendimiento) en forma de un aceite transparente. RMN de 1H (500 MHz, CDCla) 84,20-4,08 (m, 2H), 3,67 (tt, J = 11,0, 4,3 Hz, 1H), 2,42 (ddt, J = 12,5, 4,2, 2,2 Hz, 1H), 2,17-2,09 (m, 1H), 1,99-1,89 (m, 1H), 1,68 (dquint., J = 14,0, 3,6 Hz, 1H), 1,45 (s a, 1H), 1,37-1,23 (m, 4H), 1,20 (s, 3H), 1,15-1,10 (m, 1H), 1,10-0,98 (m, 2H); RMN 13C (126 MHz, CDCla) 8176,8, 68,2, 60,4, 44,8, 44,3, 35,1, 34,8, 28,3, 21,7, 14,2.
7D. 3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metil-isoxazol-5-il)fenoxi)-1-metilciclohexanocarboxilato de (±)-cis-etilo
A una solución a TA de 7C (56 mg, 0,303 mmol) y 1H (50 mg, 0,151 mmol) en tolueno (2 ml) se le añadió sucesivamente BU3P (0,056 ml, 0,227 mmol) y 1,1'-(azodicarbonil)dipiperidina (57,3 mg, 0,227 mmol). La mezcla de reacción se calentó a 50 °C durante 18 h, después se enfrió a TA y se concentró al vacío. El aceite en bruto se cromatografió (4 g de SO 2 ; gradiente continuo del 0 % al 30 % de EtOAc/hexano durante 10 min) para dar 7D (22 mg, 0,044 mmol, 29,2 % de rendimiento) en forma de un aceite transparente. [M H]+ = 499,2
Ejemplo 7
Una mezcla de 7D (22 mg, 0,044 mmol) y LiOH ac. 2,0 M (0,22 ml, 0,44 mmol) en THF (1 ml)/MeOH (0,1 ml) se agitó a TA durante 3 días, después se concentró al vacío. El residuo se purificó por HPLC preparativa (COLUMNA Phenomenex Axia 5 u C1830 x 100 mm; detección a 220 nm; caudal = 40 ml/min; gradiente continuo de B al 50 % a B al 100 % durante 10 min 2 min de parada al 100 % de B, donde A = 90:10:0,1 de H2O:MeOH:TFA y B = 90:10:0,1 de MeOH:H2O:TFA) para dar el compuesto del título (15 mg, 0,031 mmol, 70,8 % de rendimiento) en forma de un aceite transparente. [M H]+ = 471,3; RMN 1H (500 MHz, CDCla ) 69,49 (s a, 1H), 7,67 (d, J = 8,8 Hz, 2H), 6,93 (d, J = 8,8 Hz, 2H), 5,13-5,05 (m, 2H), 4,70-4,22 (m, 2H), 2,76 (s a, 3H), 2,39 (s, 3H), 2,36-2,26 (m, 1H), 2,10-1,92 (m, 2H), 1,86-1,38 (m, 13H), 1,30 (s, 3H). CI50 de hLPA1 = 2181 nM.
Ejemplo 8. Ácido (±)-trans-3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)-1-metilciclohexanocarboxílico
8A. 4-nitrobenzoato de (±)-cis-3-(etoxicarbonil)-3-metilciclohexilo
A una mezcla de 3-hidroxi-1-metilciclohexanocarboxilato de (±)-trans-etilo (750 mg, 4,03 mmol), ácido 4-nitrobenzoico (673 mg, 4,03 mmol) y Ph3 P (1584 mg, 6,04 mmol) en THF (5 ml) se le añadió DEAD (1,100 ml, 6,04 mmol) lentamente en porciones durante 30 min. La reacción se agitó durante una noche a TA, después se concentró al vacío. El aceite residual en bruto se cromatografió (24 g S O 2 ; gradiente continuo del 0 % al 40 % de EtOAc/hexano durante 10 min) para dar un aceite de color amarillento claro que se purificó de nuevo por HPLC preparativa (columna Phenomenex Axia 5 u C18 30 x 100 mm; detección a 220 nm; caudal = 40 ml/min; gradiente continuo de B al 30 % a B al 100 % durante 10 min 5 min de parada al 100 % de B, donde A = 90:10:0,1 de H2O:MeOH:TFA y B = 90:10:0,1 de MeOH:H2O:TFA) para dar el compuesto del título (144 mg, 0,429 mmol, 10,7 % de rendimiento) en forma de un aceite transparente que lentamente formó un sólido después de un periodo de reposo.
8B. (±)-1-metil-6-oxabiciclo[3.2.1]octan-7-ona
Una mezcla de 8A (144 mg, 0,43 mmol) y K2CO3 (59 mg, 0,43 mmol) en EtOH (1 ml) se agitó a TA durante 2 h, después se filtró. El filtrado se concentró al vacío. El aceite residual en bruto se cromatografió (4 g SO 2; gradiente continuo del 0 % al 30 % de EtOAc/hexano durante 10 min) para dar el compuesto del título (28 mg, 0,20 mmol, 46,5 % de rendimiento) en forma de un sólido de color blanco (RMN de 1H (500 MHz, CDCh) 84,80-4,72 (m, 1H), 2,29 2,20 (m, 1H), 2,03 - 1,95 (m, 1H), 1,85-1,67 (m, 4H), 1,56-1,45 (m, 2H), 1,20 (s, 3H)).
8C. 3-hidroxi-1-metilciclohexanocarboxilato de (±)-cis-etilo
Se disolvió sodio (14 mg, 0,60 mmol) en EtOH anhidro (1 ml) a TA. Se añadió 8B (28 mg, 0,20 mmol). La mezcla de reacción se agitó a TA durante 1 h, después se diluyó con NH4Cl ac. sat. (3 ml) y se extrajo con CH2Ch (3 x 1 ml). Los extractos orgánicos combinados se secaron (MgSO4) y se concentraron al vacío. El aceite residual en bruto se cromatografió (4 g SO 2; gradiente continuo del 0 % al 50 % de EtOAc en hexano durante 10 min) para dar el compuesto del título (14 mg, 0,075 mmol, 37,6 % de rendimiento) en forma de un aceite transparente. RMN de 1H (500 MHz, CDCla) 84,19-4,10 (m, 2H), 3,93 (tt, J = 6 ,8 , 3,5 Hz, 1H), 1,99 (dd, J=13,6, 6,7 Hz, 1H), 1,94 - 1,85 (m, 1H), 1,77-1,61 (m, 3H), 1,53-1,42 (m, 2H), 1,41-1,32 (m, 1H), 1,26 (t, J = 7,2 Hz, 3H), 1,18 (s, 3H)
8D 3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)-1-metilciclohexanocarboxilato de (±)-trans-etilo
A una solución a TA de 8C (13 mg, 0,07 mmol) y 1H (23 mg, 0,07 mmol) en tolueno (2 ml) se le añadió sucesivamente Bu3P (0,026 ml, 0,104 mmol) y 1'-(azodicarbonil)dipiperidina (26 mg, 0,10 mmol). La mezcla de reacción se calentó a 50 °C durante 2 h, después se enfrió a TA y se concentró al vacío. El aceite residual en bruto se cromatografió (4 g SO 2 ; gradiente continuo del 0 % al 30 % de EtOAc/hexano durante 10 min) para dar el compuesto del título (10 mg, 0,020 mmol, 28,8 % de rendimiento) en forma de un aceite transparente. [M H]+ = 499,3.
Ejemplo 8
Una mezcla de 8D (10 mg, 0,020 mmol) y LiOH ac. 2,0 M (0,20 ml, 0,40 mmol) en MeOH (0,2 ml)/THF (1 ml) se agitó a TA durante 24 h, después se concentró al vacío. El producto en bruto se purificó por HPLC preparativa (columna Phenomenex Axia 5 u C1830 x 100 mm; detección a 220 nm; caudal = 40 ml/min; gradiente continuo de B al 40 % a B al 100 % durante 10 min 2 min de parada al 100 % de B, donde A = 90:10:0,1 de H2O:MeOH:TFA y B = 90:10:0,1 de MeOH:H2O:TFA) para dar el compuesto del título (3 mg, 6,31 pmol, 31,5 % de rendimiento) en forma de un aceite transparente. [M H]+ = 471,3; RMN de 1H (500 MHz, CDCla ) 87,70 (d, J = 8,8 Hz, 2H), 7,07 (d, J = 9,1 Hz, 2H), 5,09 (s, 2H), 4,65-4,23 (m, 2H), 2,77 (s a, 3H), 2,65 (dt, J = 13,0, 1,9 Hz, 1H), 2,39 (s, 3H), 2,23 (d, J = 13,5 Hz, 1H), 2,14 (d, J = 9,1 Hz, 1H), 1,91-1,38 (m, 11H), 1,33 (s, 3H), 1,29-1,18 (m, 2H). CI50 de hLPA1 = 89 nM.
Ejemplo 9. Ácido (±)-trans-3-((5-(4-((((1-ciclopropiletil)(metil)carbamoil)oxi)metil)-3-metil-isoxazol-5-il)pirazin-2-il)oxi)ciclohexanocarboxílico
9A. (Z)-3-(metilamino)but-2-enoato de ferc-butilo
Una mezcla de 3-oxobutanoato de ferc-butilo (14,5 ml, 87 mmol) y metilamina (solución al 33 % en EtOH; 23,9 ml, 192 mmol) se agitó a TA durante 16 h, después se concentró al vacío para dar el compuesto del título (15 g, 88 mmol, 100 % de rendimiento) en forma de un aceite de color amarillo. RMN de 1H (500 MHz, CDCl3) 88,46 (s a, 1H), 4,42 (s, 1H), 2,90 (d, J = 5,2 Hz, 3H), 1,90 (s, 3H), 1,48 (s, 9H).
9B. Cloruro de 5-cloropirazin-2-carbonilo
A una mezcla a 0 °C de ácido 5-cloropirazin-2-carboxílico (1,0 g, 6,31 mmol) en DCM (6,3 ml) se le añadió cloruro de oxalilo (6,3 ml, 12,6 mmol) y varias gotas de DMF. La mezcla se agitó a TA durante una noche, después se concentró al vacío para proporcionar el compuesto del título, que se usó en la etapa siguiente sin más purificación.
9C. (E)-2-(5-cloropirazin-2-carbonil)-3-(metilimino)butanoato de ferc-butilo
Una solución de 9B (1,0 g, 5,65 mmol) en DCM se añadió gota a gota a una solución a 0 °C de 9A (0,97 g, 5,65 mmol) y piridina (1,83 ml, 22,6 mmol) en THF (28 ml) durante 10 min. La reacción se agitó a TA durante 24 h, después se concentró al vacío y se repartió entre EtOAc y agua. La capa orgánica se separó; la fase acuosa se extrajo con EtOAc (3x). Los extractos orgánicos combinados se secaron (MgSO4) y se concentraron al vacío para dar el compuesto del título en bruto en forma de un aceite de color amarillo, que se usó en la reacción siguiente sin más purificación.
9D . 5 -(5 -c lo ro p ira z in -2 - il) -3 -m e tilis o x a z o l-4 -c a rb o x ila to de fe rc -bu tilo
Una mezcla de 9C en bruto (1,90 g, 6,1 mmol) y NH2OH.HCI (0,64 g, 9,14 mmol) en EtOH (58 ml)/agua (2,9 ml) se agitó a 60 °C durante 3 días, después se concentró al vacío. La mezcla se repartió entre EtOAc y agua; la capa orgánica se lavó con agua y salmuera, se secó (MgSO4) y se concentró al vacío. El material en bruto se cromatografió (40 g S O 2; gradiente continuo del 0-50 % de EtOAc en hexanos durante 15 min) para proporcionar el compuesto del título (1,30 g, 4,40 mmol, 72,1 % de rendimiento) en forma de un sólido de color blanquecino. RMN de 1H (500 MHz, CDCla) 89,01 (d, J = 1,4 Hz, 1H), 8,76 (d, J = 1,4 Hz, 1H), 2,55 (s, 3H), 1,55 (s, 9H).
9E. 5-(5-((3-(etoxicarbonil)ciclohexil)oxi)pirazin-2-il)-3-metilisoxazol-4-carboxilato de (±)-trans-terc-butilo
Una mezcla de 9D (166 mg, 0,56 mmol), 3-hidroxiciclohexanocarboxilato de trans-etilo racémico (193 mg, 1,12 mmol) y Cs2COa (366 mg, 1,12 mmol) en MeCN (2,5 ml) se agitó a 80 °C durante 18 h, después se enfrió a TA. La mezcla de reacción se repartió entre EtOAc y agua. La capa orgánica se lavó con agua, se secó (MgSO4) y se concentró al vacío. El producto en bruto se cromatografió (12 g SO 2 ; gradiente continuo del 0 % al 30 % de EtOAc en hexano durante 10 min) para dar el compuesto del título (150 mg, 0,348 mmol, 61,9 % de rendimiento) en forma de un aceite transparente. [M H]+ = 432,3; RMN de 1H (500 MHz, CDCla ) 88,74 (d, J = 1,4 Hz, 1H), 8,31 (d, J = 1,4 Hz, 1H), 5,53 5,46 (m, 1H), 4,14 (c, J = 7,0 Hz, 2H), 2,79 (tt, J = 10,9, 3,9 Hz, 1H), 2,50 (s, 3H), 2,21 (dt, J = 14,0, 4,1 Hz, 1H), 2,04 1,93 (m, 2H), 1,78-1,43 (m, 14H), 1,26 (t, J = 7,2 Hz, 3H).
9F. Ácido (±)-trans-5-(5-((-3-(etoxicarbonil)ciclohexil)oxi)pirazin-2-il)-3-metilisoxazol-4-carboxílico
Una mezcla de 9E (150 mg, 0,348 mmol) y TFA (0,268 ml, 3,48 mmol) en DCM (3 ml) se agitó a TA durante 4 h y después se concentró al vacío para dar el compuesto del título (130 mg, 0,346 mmol, 100 % de rendimiento) en forma de un sólido de color amarillento claro. [M H]+= 376,1; RMN de 1H (500 MHz, CDCh) 89,01 (d, J = 1,4 Hz, 1H), 8,21 (d, J = 1,1 Hz, 1H), 5,67-5,49 (m, 1H), 4,28-4,05 (m, 2H), 2,80 (tt, J = 10,4, 3,9 Hz, 1H), 2,62 (s, 3H), 2,27-2,10 (m, 1H), 2,04-1,88 (m, 3H), 1,84-1,36 (m, 4H), 1,32-1,19 (m, 3H).
9G. 3-((5-(4-(clorocarbonil)-3-metilisoxazol-5-il)pirazin-2-il)oxi)ciclohexanocarboxilato de (±)-trans-etilo
Una mezcla de 9F (130 mg, 0,346 mmol) y 1-cloro-N,N,2-trimetilprop-1-en-1-amina (0,055 ml, 0,416 mmol) en DCM (2 ml) se agitó a TA durante 1 h, después se concentró al vacío para dar el compuesto del título (136 mg, 0,345 mmol, 100 % de rendimiento) en forma de un aceite de color amarillo, que se usó en la reacción siguiente sin más purificación.
9H. 3-((5-(4-(hidroximetil)-3-metilisoxazol-5-il)pirazin-2-il)oxi)ciclohexanocarboxilato de (±)-trans-etilo
Una solución de 9G (136 mg, 0,345 mmol) en THF (2 ml) se añadió gota a gota a una suspensión de NaBH4 (20 mg, 0,529 mmol) en EtOH (2 ml) a -78 °C. La reacción se agitó a -78 °C durante 1 h (la LCMS mostró que la reacción se había completado en ese momento). El pH de la mezcla de reacción se ajustó con HCl ac. 1 N reacción a ~4, la mezcla se extrajo con EtOAc (2X). Los extractos orgánicos combinados se lavaron con agua, se secaron (MgSO4) y se concentraron al vacío. El producto en bruto se cromatografió (12 g SO 2; gradiente continuo del 0 % al 50% de EtOAc/hexano durante 10 min) para dar el compuesto del título (72 mg, 0,20 mmol, 58 % de rendimiento) en forma de un aceite transparente. [M H]+ = 362,2; RMN de 1H (500 MHz, CDCh) 88,75 (d, J = 1,4 Hz, 1H), 8,21 (d, J = 1,4 Hz, 1H), 5,59-5,44 (m, 1H), 4,66-4,51 (m, 2H), 4,21-4,07 (m, 2H), 2,87-2,69 (m, 1H), 2,36 (s, 3H), 2,24-2,12 (m, 1H), 2,03 1,38 (m, 7H), 1,26 (t, J = 7,2 Hz, 3H).
9I. 3-((5-(3-metil-4-((((4-nitrofenoxi)carbonil)oxi)metil)isoxazol-5-il)pirazin-2-il)oxi)ciclohexanocarboxilato de (±)-transetilo
Una solución de cloroformiato de 4-nitrofenilo (34 mg, 0,17 mmol) en CH2Ch (3 ml) se añadió gota a gota a una solución de 9H (50 mg, 0,14 mmol) y piridina (0,056 ml, 0,69 mmol) en CH2Cl2 (1 ml) durante 1 h a 0 °C. La reacción se dejó calentar a TA y se agitó a TA durante 2 h, después se concentró al vacío. El producto en bruto se cromatografió (4 g SO 2; gradiente continuo del 0 % al 30 % de EtOAc/hexano durante 10 min) para dar el compuesto del título (70 mg, 0,133 mmol, 96 % de rendimiento) en forma de un aceite transparente. Rm N de 1H (500 MHz, CDCla) 88,70-8,66 (m, 1H), 8,30-8,23 (m, 3H), 7,42-7,35 (m, 2H), 5,72-5,63 (m, 2H), 5,55-5,42 (m, 1H), 4,20-4,10 (m, 2H), 2,80 (tt, J = 10,8, 3,7 Hz, 1H), 2,45 (s, 3H), 2,21 (dt, J = 14,0, 4,1 Hz, 1H), 2,03-1,81 (m, 3H), 1,78-1,39 (m, 4H), 1,32-1,15 (m, 3H).
Ejemplo 9
Una mezcla de 9I (30 mg, 0,057 mmol), 1-cidopropil-N-metiletanamina (11,30 mg, 0,114 mmol) y DIPEA (0,030 ml, 0,171 mmol) en THF (1 ml) se agitó a TA durante 2 h (la LC-MS mostró formación de producto en este momento). Se añadió LiOH ac. 2,0 M (0,23 ml, 0,46 mmol) y la reacción se agitó a TA durante 3 h, después se concentró al vacío. El producto en bruto se purificó por HPLC preparativa (columna Phenomenex Axia 5 u C18 30 x 100 mm; detección a 220 nm; caudal = 40 ml/min; gradiente continuo de B al 30 % a B al 100 % durante 10 min 3 min de parada al 100 % de B, donde A = 90:10:0,1 de H2O:MeOH:TFA y B = 90:10:0,1 de MeOH:H2O:TFA) para dar el compuesto del título (24 mg, 0,051 mmol, 90 % de rendimiento) en forma de un aceite transparente. [M H]+ = 459,1; RMN 1H (500 MHz, CDCla ) 88,64 (s a, 1H), 8,33-8,12 (m, 1H), 5,58-5,00 (m, 3H), 3,64-3,13 (m, 1H), 3,00-2,70 (m, 4H), 2,39 (s a, 3H), 2,31-1,53 (m, 8H), 1,16 (s a, 3H), 0,92-0,75 (m, 1H), 0,64-0,02 (m, 4H). CI50 de hLPA1 = 85 nM.
Ejemplo 10. Ácido (1S,3S)-3-((6-(4-((((2-ciclopropiletil)(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)-2-metilpiridin-3-il)oxi)ciclohexanocarboxílico
10A. 5-(5-bromo-6-metilpiridin-2-il)-3-metilisoxazol-4-carboxilato de ferc-butilo
A una solución a TA de ácido 5-bromo-6-metilpicolínico (3,0 g, 13,9 mmol) en CH2Ch (25 ml) y DMF (1 ml) en atmósfera de N2 se le añadió SOCh (3,0 ml, 41,7 mmol) y la mezcla de reacción se agitó a 55 °C durante 15 h, después se enfrió a TA y se concentró al vacío. El producto de cloruro de ácido en bruto se disolvió en THF (10 ml) y se añadió a una solución de 3-(metilamino)but-2-enoato de ferc-butilo (4,67 g, 27,3 mmol) y piridina (2,2 ml, 27,3 mmol) en THF (10 ml). La mezcla de reacción se agitó a TA durante 24 h, después se concentró al vacío. El producto en bruto se disolvió en EtOH (40 ml) y agua (2 ml), tras lo cual se añadió NH2OH.HCl (1,98 g, 41,7 mmol). La mezcla de reacción se agitó a 60 °C durante 15 h, después se enfrió a TA y se concentró al vacío. Se añadió agua (50 ml) y la mezcla se extrajo con EtOAc (2 x 50 ml). Los extractos orgánicos combinados se lavaron con salmuera (50 ml), se secaron (Na2SO4) y se concentraron al vacío. El producto en bruto se cromatografió (24 g SO 2; EtOAc al 10 % en hexanos) para proporcionar el compuesto del título (2,55 g, 52 %, en 3 etapas) en forma de un líquido de color naranja. Tiempo de retención de la LC-MS = 1,42 min; m/z = 355,0 [M+H]+ (Método M). RMN de 1H (300 MHz, CDCla) 88,16 (d, J = 8,10 Hz, 1H), 7,67 (d, J = 8,10 Hz, 1H), 2,73 (s, 3H), 2,48 (s, 3H), 1,49 (s, 9H).
10B. Ácido 5-(5-bromo-6-metilpiridin-2-il)-3-metilisoxazol-4-carboxílico
A una solución en agitación de 10A (2,50 g, 7,08 mmol) en CH2CI2 (4 ml) se le añadió TFA (3,82 ml, 49,5 mmol) y la mezcla de reacción se agitó a TA durante 15 h, después se concentró al vacío para proporcionar el compuesto del título (1,75 g, 83 %) en forma de un sólido de color amarillo, que se usó en la reacción siguiente sin más purificación. Tiempo de retención de la LC-MS = 0,67 min; m/z = 297,3 [M+H]+ (Método I). RMN de 1H (400 MHz, CDCh) 88,21 (d, J = 8,80 Hz, 1H), 7,92 (d, J = 8,80 Hz, 1H), 2,79 (s, 3H), 2,63 (s, 3H).
10C. (5-(5-bromo-6-metilpiridin-2-il)-3-metilisoxazol-4-il)metanol
A una solución a 0 °C de 10B (1,50 g, 5,05 mmol) en THF (80 ml) se le añadió cloroformiato de etilo (1,64 g, 12 mmol), TEA (1,41 ml, 10,1 mmol). La reacción se agitó a TA durante 16 h, después se filtró a través de Celite y el filtrado se concentró al vacío. El residuo se disolvió en EtOH (15 ml) y a esto se le añadió solución a 0 °C de NaBH4 (0,573 g, 15,2 mmol). La mezcla de reacción se agitó a TA durante 1 h, después se inactivó con HCl ac. 1,5 N a 0 °C (50 ml) y se extrajo con CH2Ch (2 x 50 ml). Los extractos orgánicos combinados se lavaron con salmuera (50 ml), se secaron (Na2SO4), se filtraron y se concentraron al vacío. El producto en bruto se cromatografió (12 g SO 2; EtOAc al 20 % en n-hexanos) para proporcionar el compuesto del título (1,22 g, 85 %) en forma de un sólido de color blanco. Tiempo de retención de la LC-MS = 1,25 min; m/z = 283,2 [M+H]+ (Método H). RMN de 1H (300 MHz, CDCla) 88,00 (d, J = 8,40 Hz, 1H), 7,70 (d, J = 8,40 Hz, 1H), 4,62 (s, 2H), 2,75 (s, 3H), 2,36 (s, 3H).
10D. 5-(5-bromo-6-metilpiridin-2-il)-3-metil-4-(((tetrahidro-2H-piran-2il)oxi)metil)isoxazol
A una solución a TA de 10C (1,20 g, 4,24 mmol) en dioxano (15 ml) se le añadió 3,4-dihidro-2H-pirano (0,46 g, 5,51 mmol) y PPTS (0,533 g, 2,12 mmol). La mezcla de reacción se agitó a TA durante 15 h, después se diluyó con agua (20 ml) y se extrajo con EtOAc (2 x 30 ml). Los extractos orgánicos combinados se lavaron con salmuera (30 ml), se secaron (Na2SO4) y se concentraron al vacío. El producto en bruto se cromatografió (24 g SO 2; EtOAc al 20 % en nhexanos) para proporcionar el compuesto del título (1,30 g, 84 %) en forma de un líquido incoloro. Tiempo de retención de la LC-MS = 3,32 min; m/z = 367,2 [M+H]+ (Método E). RMN de 1H (400 MHz, CDCh) 87,91 (d, J = 8,40 Hz, 1H), 7,59 (d, J = 8,40 Hz, 1H), 5,02 (ABc, J = 11,60 Hz, 2H), 4,75 (t, J = 3,60 Hz, 1H), 4,00-4,10 (m, 1H), 3,80-3,95 (m, 1H), 2,70 (s, 3H), 2,41 (s, 3H), 1,40-1,90 (m, 6H).
10E. 3-metil-5-(6-metil-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)piridin-2-il)-4(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol
A una solución desgasificada de 10D (1,30 g, 3,54 mmol), bis(pinacolato)diboro (1,80 g, 7,1 mmol) y KOAc (0,695 g, 7,08 mmol) en dioxano (40 ml) se le añadió aducto de 1,1'-bis(difenilfosfino)ferroceno-Pd(N)Cl2-CH2Cl2 (0,578 g, 0,708 mmol) y la mezcla de reacción se calentó a 90 °C durante 8 h, después se enfrió a TA. La mezcla se filtró a través de Celite, que se lavó con EtOAc (50 ml). Los filtrados combinados se concentraron al vacío para dar el producto compuesto del título (1,25 g, 85 %) en forma de un aceite incoloro. Este producto en bruto se usó en la etapa siguiente sin más purificación. Tiempo de retención de la LC-MS = 3,93 min; m/z = 415,2 [M+H]+ (Método E).
10F. 2-metil-6-(3-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol-5-il)piridin-3-ol
A una mezcla de 10E (1,25 g, 3,02 mmol) en THF (15 ml) y agua (2 ml) se le añadió NaBO3.H2O (1,21 g, 12,1 mmol) y la mezcla de reacción se agitó a 55 °C durante 90 min, después se enfrió a TA. La mezcla se diluyó con EtOAc (80 ml), se lavó con agua (2 x 50 ml), se secó (Na2SO4) y se concentró al vacío. El producto en bruto se cromatografió (24 g SiO2, 25 % de EtOAc en hexanos) para proporcionar el compuesto del título (0,78 g, 85 %) en forma de un aceite incoloro. Tiempo de retención de la LC-MS = 1,14 min; m/z = 303,4 [M-H] (Método I). RMN de 1H (300 MHz, DMSO-da) 8 10,44 (s, 1H), 7,59 (d, J = 8,40 Hz, 1H), 7,25 (d, J = 8,40 Hz, 1H), 5,03 (ABc, J = 12,40 Hz, 2H), 4,70 (s a, 1H), 3,75 - 3,90 (m, 1H), 3,40-3,50 (m, 1H), 2,39 (s, 3H), 2,29 (s, 3H), 1,35-1,80 (m, 6H).
10G. 3-((2-metil-6-(3-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol-5-il)piridin-3-il)oxi)ciclohexanocarboxilato de (1S,3S)-etilo
A una solución de 10F (0,78 g, 2,56 mmol) en tolueno (8 ml) se le añadió azodicarboxilato de di-ferc-butilo (1,475 g, 6,41 mmol) y Ph3 P (1,681 g, 6,41 mmol). La solución se agitó a TA durante 5 min, tras lo cual se añadió 3-hidroxiciclohexanocarboxilato de (1S,3R)-etilo (0,75 g, 4,36 mmol). La mezcla de reacción se agitó a 75 °C durante 20 h, después se enfrió a TA y se concentró al vacío. El producto en bruto se cromatografió (24 g SiO2 , eluyendo con EtOAc al 15 % en hexanos) para proporcionar el compuesto del título (0,68 g, 58 %) en forma de un aceite incoloro. Tiempo de retención de la LC-MS = 1,72 min; m/z = 459,2 [M+H]+ (Método I). RMN de 1H (400 MHz, CDCh) 87,67 (d, J = 8,80 Hz, 1H), 7,18 (d, J = 8,80 Hz, 1H), 4,99 (s, 2H), 4,65-4,75 (m, 2H), 4,11 (c, J = 7,20 Hz, 2H), 3,88-3,98 (m, 1H), 3,45-3,58 (m, 1H), 2,75-2,85 (m, 1H), 2,51 (s, 3H), 2,38 (s, 3H), 2,00-2,15 (m, 1H) 1,80-2,00 (m, 3H), 1,40-1,75 (m, 10H), 1,23 (t, J = 7,20 Hz, 3H).
10H. 3-((6-(4-(hidroximetil)-3-metilisoxazol-5-il)-2-metilpiridin-3-il)oxi)ciclohexanocarboxilato de (1S,3S)-etilo
A una solución de 10G (680 mg, 1,48 mmol) en MeOH (5 ml) se le añadió p-TsOH.H2O (141 mg, 0,741 mmol) y la mezcla de reacción se agitó a TA durante 3 h, después se concentró al vacío. El producto en bruto se cromatografió (12 g SiO2, EtOAc al 30 % en hexanos) para proporcionar el compuesto del título (340 mg, 61 %) en forma de un aceite incoloro. Tiempo de retención de la lC-MS = 1,38 min; m/z = 375,5 [M+H]+ (Método I). RMN de 1H (400 MHz, CDCh) 8 7,78 (d, J = 8,40 Hz, 1H), 7,29 (d, J = 8,40 Hz, 1H), 6,57 (t, J = 6,80 Hz, 1H), 4,74 (s a, 1H), 4,60 (d, J = 6,40 Hz, 2H), 4,15 (c, J = 7,2 Hz, 2H), 2,75-2,85 (m, 1H), 2,54 (s, 3H), 2,32 (s, 3H), 1,85 -2,10 (m, 4H), 1,60-1,75 (m, 4H), 1,27 (t, J = 7,2 Hz, 3H).
10I. 3-((6-(4-((((2-ciclopropiletil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)-2-metilpiridin-3-il)oxi)ciclohexanocarboxilato de (1S,3S)-etilo
A una solución a TA de 10G (50 mg, 0,134 mmol), ácido 3-ciclopropilpropanoico (0,03 ml, 0,27 mmol) y Et3 N (0,056 ml, 0,69 mmol) en tolueno (2 ml) se le añadió (PhO)2 PON3 (0,06 ml, 0,27 mmol) y la mezcla de reacción se agitó a 110 °C durante 16 h, después se enfrió a TA y se concentró al vacío. El producto en bruto se cromatografió (4 g SO 2 ; EtOAc al 40 % en hexanos) para proporcionar el compuesto del título (40 mg, 62 %) en forma de un aceite de color amarillo claro. Tiempo de retención de la LC-MS = 3,83 min; m/z = 486,2 [M+H]+ (Método E). RMN 1H (300 MHz, CD3OD) 87,71 (d, J = 8,70 Hz, 1H), 7,46 (d, J = 8,70 Hz, 1H), 5,46 (s a, 2H), 4,80-4,85 (s., 1H), 4,15 (c, J = 7,2 Hz, 2H), 3,21 (t, J = 16,2 Hz, 1H), 2,80-2,90 (m, 1H), 2,52 (s, 3H), 2,37 (s, 3H), 2,10-2,20 (m, 1H), 1,90 - 2,00 (m, 3H), 1,60-1,80 (m, 4H), 1,30-1,60 (m, 3H), 1,29 (t, J = 7,2 Hz, 3H), 0,60-0,80 (m, 1H), 0,35-0,50 (m, 2H), 0,03-0,15 (m, 2H).
10J. 3-((6-(4-((((2-ciclopropiletil)(metil)carbamoil)oxi)metil)-3-metil-isoxazol-5-il)-2-metilpiridin-3-il)oxi)ciclohexanocarboxilato de (1S,3S)-etilo
A una solución de 10I (40 mg, 0,082 mmol) en DMF (2 ml) en atmósfera de N2 se le añadió NaH (5 mg, 0,124 mmol) a 0 °C seguido de yoduro de metilo (10 pl, 0,165 mmol). La mezcla de reacción se agitó a TA durante 6 h, después se inactivó con agua (10 ml) y se extrajo con EtOAc (2 x 20 ml). Los extractos orgánicos combinados se lavaron con salmuera (10 ml), se secaron (Na2SO4) y se concentraron al vacío para formar el compuesto del título (40 mg, 92 %)
en forma de un aceite de color amarillo claro. Tiempo de retención de la LC-MS = 3,85 min; m/z = 500,4 [M+H]+ (Método E). RMN 1H (300 MHz, CD3OD) 87,72 (d, J = 8,70 Hz, 1H), 7,45 (d, J = 8,70 Hz, 1H), 5,44 (s a, 2H), 4,80-4,85 (s a, 1H), 4,14 (c, J = 7,2 Hz, 2H), 3,20-3,30 (m, 1H), 2,73-2,92 (m, 4H), 2,49 (s, 3H), 2,37 (s, 3H), 2,10-2,20 (m, 1H), 1,80 2,00 (m, 3H), 1,50 - 1,80 (m, 3H), 1,20-1,47 (m, 6H), 0,85-0,94 (m, 2H), 0,20-0,48 (m, 2H), 0,05 (s a, 1H), -0,20 (s a,1H).
Ejemplo 10
A una solución de 10J (40 mg, 0,08 mmol) en THF (2 ml) y MeOH (2 ml) se le añadió una solución de LÍOH.H2O (10 mg, 0,240 mmol) en agua (1 ml). La mezcla de reacción se agitó a TA durante 3 h, después se acidificó con HCl ac.
1,5 N (10 ml) y se extrajo con CH2Ch (2 x 20 ml). Los extractos orgánicos combinados se lavaron con salmuera (15 ml), se secaron (Na2SO4) y se concentraron al vacío. El producto en bruto se purificó por HPLC preparativa para proporcionar el compuesto del título (16 mg, 42 %) en forma de un aceite incoloro (columna X-Bridge Phenyl (250 x 19 mm) 5 micrómetros; caudal 17 ml/min; Fase móvil A: NH4OAc 10 mM en agua (pH: 4,5); Fase móvil B: MeCN; tiempo (min)/% de B: 0/20, 8/70, 14/70, 15/100; tiempo de retención: 11,93 min). Tiempo de retención de la LC-MS = 2,17 min; m/z = 472,2 [M+H]+ (Método E). RMN 1H (400 MHz, CD3OD) 87,74 (d, J = 8,80 Hz, 1H), 7,47 (d, J = 8,80 Hz, 1H), 5,46 (s a, 2H), 4,80-4,85 (s a, 1H), 3,20-3,30 (m, 1H), 2,73-2,92 (m, 4H), 2,52 (s, 3H), 2,39 (s, 3H), 2,10-2,20 (m, 1H), 1,86-2,01 (m, 3H), 1,60-1,84 (m, 4H), 1,20-1,48 (m, 3H), 0,56-0,94 (m, 1H), 0,20-0,48 (m, 2H), 0,06 (s a, 1H), -0,18 (s a, 1H). CI50 de hLPA1 = 11 nM.
Los ejemplos de la tabla 1 a continuación se prepararon por los métodos generales/secuencia sintética descritos para la preparación de los ejemplos 1 a 10.
Tabla 1
Ejemplo 47. Ácido (±)-(trans)-2-(3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)cidohexil)acético
El ejemplo 47 se sintetizó usando la misma ruta de síntesis descrita para la preparación del ejemplo 1 a partir del ejemplo 1H y 3-hidroxiciclohexanocarboxilato de (1S,1R)-isopropilo, excepto porque se usó el intermedio 3 en lugar del carboxilato de ciclohexano. LCMS, [M+H]+ = 471. RMN de 1H (500 MHz, DMSO-da ) 87,73 (d, J = 8,9 Hz, 2H), 7,14 (d, J = 8,5 Hz, 2H), 5,06 (s, 2H), 4,79 (s a, 1H), 2,69 (s, 3H), 2,32 (s, 3H), 2,19-2,09 (m, 3H), 1,98-1,82 (m, 2H), 1,75 1,34 (m, 13H), 1,09 (m, 1H). CI50 de hLPA1 = 570 nM
Los siguientes compuestos se prepararon usando la secuencia sintética general como se usa en la preparación del ejemplo 47. Para el ejemplo 49, el carbamato se instaló de acuerdo con el procedimiento descrito para el ejemplo 1 (conversión Ejemplo 1F ^ 1G).
Ejemplo 50. Ácido (1S,3S)-3-(4-(4-(1-((isopentil(metil)carbamoil)oxi)etil)-3-metilisoxazol-5-il)fenoxi)ciclohexan-1-carboxílico (par de diastereómeros)
50A. 5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metilisoxazol-4-carbaldehído
A una solución a TA del ejemplo 1E (500 mg, 1,56 mmol) en DCM (15 ml) se le añadió peryodinano de Dess-Martin (830 mg, 1,96 mmol). La mezcla de reacción se agitó durante una noche a TA, después se inactivó con H2O y se extrajo con DCM (2x). Los extractos orgánicos combinados se lavaron con H2O y salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 0-30 % de EtOAc en hexanos) para dar el compuesto del título (455 mg, 92 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 318. RMN de 1H (400 MHz, CDCh) 810,08 (s, 1H), 7,76 (d, J = 8,8 Hz, 2H), 6,99 (d, J = 8,8 Hz, 2H), 2,54 (s, 3H), 1,01 (s, 9H), 0,26 (s, 6H).
50B. 1-(5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metilisoxazol-4-il)etan-1-ol
A una solución a 0 °C del ejemplo 50A (455 mg, 1,43 mmol) en THF (15 ml) se le añadió MeMgBr 3 M en THF (1,19 ml, 3,58 mmol) gota a gota. La reacción se agitó a 0 °C durante 1 h, después se calentó a TA y se inactivó cuidadosamente con HCI ac. 1 N. La mezcla se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO2; gradiente continuo del 0-30 % de EtOAc en hexanos) para dar el compuesto del título (477 mg, 99 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 334. RMN de 1H (400 MHz, CDCla) 87,52 (d, J = 8,6 Hz, 2H), 6,93 (d, J = 8,6 Hz, 2H), 5,11 (m, 1H), 2,45 (s, 3H), 1,58 (d, J = 6,6 Hz, 3H), 1,00 (s, 9H), 0,24 (s, 6H).
50C. 5-(4-((terc-butildimetilsilil)oxi)fenil)-3-metil-4-(1-((tetrahidro-2H-piran-2-il)oxi)etil)isoxazol
A una solución a TA del ejemplo 50B (477 mg, 1,43 mmol) en DCM (10 ml) se le añadió dihidropirano (361 mg, 4,29 mmol) y PPTS (36 mg, 0,14 mmol). La reacción se agitó durante una noche a TA, después se inactivó con NaHCO3 ac. sat. y se extrajo con DCM (2x). Los extractos orgánicos combinados se lavaron con H2O y salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SiO2; gradiente continuo del 10-40 % de EtOAc en hexanos) para dar el compuesto del título en forma de una mezcla de diastereómeros (540 mg, 90 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 418.
50D. 4-(3-metil-4-(1-((tetrahidro-2H-piran-2-il)oxi)etil)isoxazol-5-il)fenol
A una solución a TA del ejemplo 50C (540 mg, 1,29 mmol) en THF (10 ml) se le añadió Bu4NF 1 M en THF (1,68 ml, 1,68 mmol). La reacción se agitó a TA durante 3 h, después se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SiO2 ; gradiente continuo del 25-50 % de EtOAc en hexanos) para dar el compuesto del título en forma de una mezcla de diastereómeros (352 mg, 90 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 304.
Ejemplo 50
El ejemplo 50 se preparó a partir del ejemplo 50D de acuerdo con la ruta de síntesis descrita para la preparación del ejemplo 2 excepto porque se usó el ejemplo 50D en lugar del ejemplo 1C como el material de partida para la secuencia. LCMS, [M+H]+ = 273. RMN de 1H (500 MHz, DMSO-d6) 87,65 (d, J = 7,9 Hz, 2H), 7,13 (d, J = 7,9 Hz, 2H), 5,83 (m, 1H), 4,74 (s a, 1H), 3,32-3,10 (m, 2H), 2,84 - 2,72 (m, 3H), 2,64 (m, 1H), 2,36 (s, 3H), 1,97-1,46 (m, 12H), 1,42-1,24 (m, 2H), 0,83 (m, 6H). CI50 de hLPA1 = 175 nM.
Los siguientes compuestos se prepararon siguiendo la secuencia sintética general del ejemplo 50.
Ejemplo 53. Ácido (1S,3S)-3-(4-(4-(((cidopentil(metil)carbamoil)oxi)metil)-5-metilisoxazol-3-il)fenoxi)cidohexan-1-carboxílico
53A. (4-nitrofenil)carbonato de (3-(4-bromofenil)-5-metilisoxazol-4-il)metilo
A una solución de (3-(4-bromofenil)-5-metilisoxazol-4-il)metanol (sintetizado de acuerdo con el procedimiento descrito en Bioorg. Med. Chem. 2017, 25, 3223-3234; 2,0 g, 7,46 mmol) en CH2Ch (40 ml) se le añadió piridina (3,02 ml, 37,3 mmol), seguido de cloroformiato de 4-nitrofenilo (3,01 g, 14,92 mmol) en porciones. La mezcla de reacción se agitó durante una noche a TA, después se concentró al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 0 50 % de EtOAc en hexanos) para dar el compuesto del título ligeramente impuro (3,16 g, 98 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 433.
53B. Ciclopentil(metil)carbamato de (3-(4-bromofenil)-5-metilisoxazol-4-il)metilo
A una solución a TA de 53A (3,16 g, 7,29 mmol) en THF (40 ml) se le añadió iPr2NEt (3,82 ml, 21,9 mmol) y N-metilciclopentanamina (1,08 g, 10,9 mmol). La reacción se agitó durante 1 h a TA, después se diluyó con H2O y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con NaHCO3 ac. sat. y H2O, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2; gradiente continuo del 10-50 % de EtOAc en hexanos); el material purificado se trituró con hexanos para dar el compuesto del título (1,96 g, 68 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 393. RMN de 1H (500 MHz, CDCh) 87,65 (m, 2H), 7,62 (m, 2H), 5,01 (s, 2H), 4,62-4,30 (m, 1H), 2,72 (s a, 3H), 2,55 (s, 3H), 1,87-1,61 (m, 4H), 1,57-1,41 (m, 4H).
53C. Ciclopentil(metil)carbamato de (5-metil-3-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil)isoxazol-4-il)metilo
Una mezcla de 53B (1,96 g, 4,98 mmol), bis(pinacolato)diboro (1,90 g, 7,48 mmol) y KOAc (1,96 g, 19,9 mmol) en THF (40 ml) se desgasificó con N2. Se añadió Pd(dppf)Ch (0,36 g, 0,498 mmol). La mezcla de reacción se desgasificó con N2 y se agitó a 60 °C durante una noche, después se enfrió a TA, se concentró parcialmente al vacío y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O y salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO2; gradiente continuo del 15-50 % de EtOAc en hexanos) para dar el compuesto del título (1,84 g, 84 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 441. RMN de 1H (500 MHz, CDCla) 87,91 (d, J = 8,3 Hz, 2H), 7,77 (d a, J = 7,4 Hz, 2H), 5,01 (s, 2H), 4,60-4,19 (m, 1H), 2,72 (s a, 3H), 2,56 (s, 3H), 1,82-1,61 (m, 4H), 1,53-1,42 (m, 4H), 1,37 (s, 12H).
53D. Ácido (4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-5-metilisoxazol-3-il)fenil)borónico
A una solución de 53C (1,84 g, 4,18 mmol) en THF (20 ml) y H2O (5 ml) se le añadió NaIO4 (2,68 g, 12,5 mmol). La mezcla de reacción se agitó a TA durante 1 h, tras lo cual se añadió HCl ac. 1 M (3,76 ml, 3,76 mmol) y la reacción se agitó a TA durante una noche. La reacción se diluyó con H2O y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El sólido resultante se trituró con EtOAc al 25 % en hexanos para dar el compuesto del título (1,22 g, 82 % de rendimiento) en forma de un sólido de color blanco ligeramente impuro. LC-MS, [M+H]+ = 359.
53E. Ciclopentil(metil)carbamato de (3-(4-hidroxifenil)-5-metilisoxazol-4-il)metilo
A una solución de 53D (1,0 g, 2,79 mmol) en MeOH (25 ml) y H2O (4 ml) se le añadió H2O2 ac. al 35 % (1,92 ml, 22,3 mmol). La reacción se agitó durante una noche a TA, después se concentró parcialmente al vacío, se acidificó con HCl ac. 1 N y se extrajo con EtOAc (2x). Los extractos orgánicos combinados se lavaron con H2O, salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se cromatografió (SO 2 ; gradiente continuo del 25-75 % de EtOAc en hexanos) para dar el compuesto del título (880 mg, 95 % de rendimiento) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 331. RMN de 1H (400 MHz, CDCla ) 87,60 (d, J = 8,8 Hz, 2H), 6,89 (d, J = 8,8 Hz, 2H), 5,02 (s, 2H), 4,65-4,20 (m, 1H), 2,74 (s a, 3H), 2,52 (s, 3H), 1,84-1,62 (m, 4H), 1,58-1,41 (m, 4H).
Ejemplo 53
El compuesto del título se preparó de acuerdo con la secuencia sintética descrita para la síntesis del ejemplo 1 a partir del ejemplo 1H excepto porque se usó el ejemplo 53E en lugar del ejemplo 1H. lCm S, [M+H]+ = 457. Rm N de 1H (500 MHz, DMSO-d6) 87,63 (d, J = 8,2 Hz, 2H), 7,09 (d, J = 8,5 Hz, 2H), 5,01 (s, 2H), 4,73 (s a, 1H), 3,18 (m, 1H), 2,68 2,58 (m, 3H), 2,48 (s, 3H), 2,00 - 1,72 (m, 4H), 1,68-1,28 (m, 13H). CI50 de hLPA1 = 6 nM.
Ejemplo 54. Ácido (1S,3S)-3-((5-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-5-metilisoxazol-3-il)piridin-2-il)oxi)ciclohexan-1-carboxílico
54A. 5-(5-metil-4-(((tetrahidro-2H-piran-2-il)oxi)metil)isoxazol-3-il)piridin-2-ol
El compuesto del título se preparó de acuerdo con la ruta de síntesis general descrita para la síntesis del ejemplo 53A (Bioorg. Med. Chem. 2017, 25, 3223-3234) usando 6-bromonicotinaldehído en lugar de 4-bromobenzaldehído y procediendo después de acuerdo con los procedimientos descritos para la síntesis del ejemplo 1A ^ 1C. LCMS, [M+H]+ = 291. RMN de 1H (500 MHz, CDCla ) 88,04-7,99 (m, 2H), 6,68 (m, 1H), 4,67-4,63 (m, 1H), 4,59-4,42 (m, 2H), 3,90 (m, 1H), 3,57 (m, 1H), 2,50 (s, 3H), 1,90-1,80 (m, 1H), 1,79-1,70 (m, 1H), 1,63-1,58 (m, 4H).
Ejemplo 54
El compuesto del título se preparó a partir de 54A de acuerdo con la secuencia sintética descrita para la preparación del ejemplo 2 (a partir de Ejemplo 2 A ^ Ejemplo 2). LCMS, [M+H]+ = 458. RMN de 1H (500 MHz, DMSO-d6) 88,47 (s, 1H), 8,02 (d, J = 8,5 Hz, 1H), 6,96 (d, J = 8,6 Hz, 1H), 5,37 (s a, 1H), 5,05 (s, 2H), 3,17 (m, 1H), 2,67-2,57 (m, 3H), 2,50 (s, 3H), 2,05 (m, 1H), 1,87-1,74 (m, 3H), 1,70-1,26 (m, 13H). CI50 de hLPA1 = 197 nM.
Los siguientes compuestos se sintetizaron de acuerdo con la secuencia sintética general descrita para la preparación de los ejemplos indicados.
Ejemplo 73. Ciclopentil(metil)carbamato de (±)-trans-(5-(4-((3-carbamoilciclohexil)oxi)fenil)-3-metilisoxazol-4-il)metilo
73A. 3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi)ciclohexan-1-carboxilato de etilo
A una mezcla a 0 °C del intermedio 1H (100 mg, 0,303 mmol), 3-hidroxicidohexanocarboxNato de etilo (mezcla de isómeros cis/trans; 94 mg, 0,545 mmol), Et3N (76 pl, 0,545 mmol) y Ph3P (143 mg, 0,545 mmol) en THF (2 ml) se le añadió DIAD (0,106 ml, 0,545 mmol) gota a gota durante 1 min. La reacción se agitó a TA durante 16 h; se añadió HCl ac. 1 N (1 ml) y la mezcla se extrajo con EtOAc (3 x 5 ml). Los extractos orgánicos combinados se lavaron con salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se sometió a cromatografía (12 g SO 2; gradiente continuo del 0 al 100 % de EtOAc en hexanos durante 20 min) para proporcionar el compuesto del título (130 mg, 0,268 mmol, 89 % de rendimiento, mezcla diastereomérica) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 485,1.
73B. Ácido 3-(4-(4-(((ciclopentil(metil)carbamoil)oxi)metil)-3-metilisoxazol-5-il)fenoxi) ciclohexan-1-carboxílico
A una mezcla de 73A (130 mg, 0,268 mmol) en THF (2 ml) y MeOH (1 ml) se le añadió LOH.H2O (225 mg, 5,37 mmol) en H2O (2 ml). La mezcla se agitó a TA durante 5 h, después se concentró al vacío; el pH se ajustó a ~3 con HCl ac.
1 N. La mezcla se extrajo con EtOAc (5 x 5 ml). Los extractos orgánicos combinados se secaron (MgSO4) y se concentraron al vacío para dar el compuesto del título (120 mg, 98 % de rendimiento, mezcla diastereomérica). LC-MS, [M+H]+ = 457,3.
Ejemplo 73
A una solución de 73B (86 mg, 0,19 mmol) y DMF (0,5 pl) en DCM (2 ml) se le añadió lentamente (COCl)2 (32 pl, 0,38 mmol). La mezcla de reacción se agitó a TA durante 30 min, después se concentró al vacío. A una solución del cloruro de ácido en bruto en DCM (1,0 ml) se le añadió NH30,5 N en dioxano (5,65 ml, 2,83 mmol). La mezcla de reacción se agitó a TA durante 30 min, después se concentró al vacío. El producto en bruto se cromatografió (12 g SO 2; gradiente continuo del 100 %-0 % de hexano en EtOAc durante 15 min, después parada durante 10 min al 100 % de EtOAc) para dar la ciclohexil amida en bruto (73 mg, 0,152 mmol, 81 % de rendimiento, mezcla diastereomérica) en forma de un sólido de color blanco. Una muestra de la ciclohexil amida en bruto (mezcla diastereomérica) se purificó por LC/MS preparativa (Columna: XBridge C18, 19 * 200 mm, partículas de 5 pm; Fase móvil A: 5:95 de MeCN:H2O con NH4OAc ac. 10 mM; Fase móvil B: 95:5 de MeCN:H2O con NH4OAc ac. 10 mM; Gradiente: 50-100 % de B durante 25 min, después una parada de 5 min al 100 % de B; Caudal: 20 ml/min). Las fracciones que contenían el producto deseado se combinaron y se secaron por evaporación por centrifugación. La segunda fracción en eluir se purificó otra vez por LC/MS preparativa (Columna: XBridge C18, 19 * 200 mm, partículas de 5 pm; Fase móvil A: 5:95 de MeCN:H2O con NH4OAc ac. 10 mM; Fase móvil B: 95:5 de MeCN:H2O con NH4OAc ac. 10 mM; Gradiente: 30-68 % de B durante 25 min, después una parada de 5 min al 100 % de B; Caudal: 20 ml/min) para dar el compuesto del título (diastereómeros racémico individual). LC-MS, [M+H]+= 456,3. RMN de 1H (500 MHz, DMSO-cfe) 87,74 (d, J = 8,5 Hz, 2H), 7,29 (s, 1H), 7,15 (d, J = 8,8 Hz, 2H), 6,73 (s, 1H), 5,07 (s, 2H), 4,84 (s, 1H), 2,69 (s, 3H), 2,61-2,54 (m, 1H), 2,32 (s, 3H), 1,91-1,37 (m, 16H). (protón de ciclopentilmetino no observado debido a la supresión del agua). CI50 de hLPA1 = 1208 nM.
Ejemplo 74. Ciclopentil(metil)carbamato de (5-(4-((3-cianociclohexil)oxi)fenil)-3-metilisoxazol-4-il)metilo
Una mezcla del ejemplo 73C (70 mg, 0,15 mmol) y reactivo de Burgess (110 mg, 0,46 mmol) en DCM y THF (1 ml cada uno) se agitó a Ta durante 48 h, después se concentró al vacío. El producto en bruto se cromatografió (4 g SO 2 ; gradiente continuo del 0 %-100 % de EtOAc en hexano durante 11 min) para dar el compuesto del título (55 mg, 82 % de rendimiento, 80 % de pureza por LC-MS, mezcla diastereomérica) en forma de un sólido de color blanco. LC-MS, [M+H]+ = 438,1; CI50 de hLPA1 = 3252 nM
Ejemplo 75. Ciclopentil(metil)carbamato de (5-(4-((3-(1H-tetrazol-5-il)ciclohexil)oxi)fenil)-3-metilisoxazol-4-il)metilo
Una mezcla del ejemplo 74 (45 mg, 0,10 mmol), NaN3 (107 mg, 1,65 mmol), Et3 N (0,23 ml, 1,65 mmol) y HOAc (94 pl, 1,65 mmol) en tolueno (1 ml) en un vial cerrado herméticamente se agitó a 100 °C durante 18 h, después se enfrió a TA y se concentró al vacío. La mezcla se recogió en EtOAc (5 ml) y NaHCO3 ac. sat. (3 ml) y se extrajo con EtOAc (5 x 5 ml). Los extractos orgánicos combinados se secaron (MgSO4) y se concentraron al vacío. El producto en bruto se purificó por LC/MS preparativa (Columna: XBridge C18, 19 * 200 mm, partículas de 5 pm; Fase móvil A: 5:95 de MeCN:H2O con TFA al 0,1 %; Fase móvil B: 95:5 de MeCN:H2O con TFA al 0,1 %; Gradiente: 40-65 % de B durante 25 min, después una parada de 3 minutos al 65 % de B; Caudal: 20 ml/min) para dar el compuesto del título (14,9 mg, 100 % de pureza por LC/MS; mezcla diastereomérica de ciclohexilo cis/trans). LC-MS, [M+Na]+ = 503,1. r Mn de 1H (500 MHz, DMSO-cfe) 87,78-7,70 (m, 2H), 7,24-7,15 (m, 2H), 5,06 (s, 2H), 4,91 (s, 0.4H), 4,63 (t, J = 11,3 Hz, 0.6H), 3,38 (s, 0.6H), 3,27 (t, J = 12,4 Hz, 0,4H), 2,68 (s, 3H), 2,32 (s, 3H), 2,27-1,33 (m, 16H). (protón de ciclopentilmetino no observado debido a la supresión del agua). CI50 de hLPA1 = 851 nM.
Ejemplos 76-78. Ciclopentil(metil)carbamato de (5-(4-((3-(1H-tetrazol-5-il)ciclohexil)oxi)fenil)-3-metilisoxazol-4-il)metilo (diastereómeros quirales)
El ejemplo 75 (mezcla de diastereómeros racémicos) se separó en los diastereómeros individuales por SFC quiral
preparativa (Berger Multigram II SFC Prep; Chiralpak ID, 21 x 250 mm, columna de 5 |jm; detección a 220 nm; caudal = 45 ml/min, 15 MPa (150 Bar), 40 °C; Fase móvil: EtOH al 25 %/CO2 al 75 %; Inyección: 0,5 ml de 58 mg/ml en MeOH) para proporcionar el ejemplo 76 como el primer diastereómero quiral en eluir en la SFC quiral, el ejemplo 77 como el segundo diastereómero quiral en eluir en la SFC quiral y el ejemplo 78 como el tercer diastereómero en eluir en la SFC quiral. El cuarto diastereómero no se aisló.
Ejemplo 76: LCMS, [M H]+ = 481,2. RMN de 1H (500 MHz, DMSO-d6) 67,73 (d, J = 8,4 Hz, 2H), 7,20 (d, J = 8,4 Hz, 2H), 5,06 (s, 2H), 4,89 (s, 1H), 3,62-3,50 (m, 1H), 3,21-3,13 (m, 1H), 2,67 (s, 3H), 2,31 (s, 3H), 2,14-1,31 (m, 16H). CI50 de hLPA1 = 2311 nM.
Ejemplo 77: LCMS, [M H]+ = 481,0. RMN de 1H (500 MHz, DMSO-d6) 67,74 (d, J = 8,3 Hz, 2H), 7,20 (d, J = 8,4 Hz, 3H), 5,06 (s, 2H), 4,90 (s, 1H), 3,62-3,50 (m, 1H), 3,21-3,13 (m, 1H), 2,67 (s, 3H), 2,31 (s, 3H), 2,24-1,34 (m, 16H). CI50 de hLPA1 = 379 nM.
Ejemplo 78: LCMS, [M H]+ = 481,2. RMN de 1H (500 MHz, DMSO-d6) 67,73 (d, J = 8,5 Hz, 2H), 7,17 (d, J = 8,5 Hz, 2H), 5,05 (s, 2H), 4,62 (t, J = 11,3 Hz, 1H), 3,58-3,43 (m, 1H), 3,24 (t, J = 12,4 Hz, 1H), 2,67 (s, 3H), 2,31 (s, 3H), 2,21 1,33 (m, 16H). CI50 de hLPA1 = 565 nM.
Otras características de la invención serán evidentes en el trascurso de las descripciones anteriores de las realizaciones a modo de ejemplo que se dan para ilustrar la invención y no se pretende que limiten la misma. La presente invención se puede realizar de otras formas específicas. Esta invención abarca todas las combinaciones de los aspectos preferidos de la invención indicados en el presente documento. Se entiende que cualquiera y todas las realizaciones de la presente invención se pueden tomar en conjunto con cualquier otra realización o realizaciones para describir realizaciones adicionales. También ha de entenderse que cada elemento individual de las realizaciones es su propia realización independiente. Además, cualquier elemento de una realización tiene por objeto combinarse con cualquiera y todos los otros elementos de cualquier realización para describir una realización adicional.
Claims (15)
1. Un compuesto de acuerdo con las fórmulas (la) o (Ib):
o un estereoisómero, un tautómero o una sal farmacéuticamente aceptable o un solvato del mismo, en donde
X1, X2, X3 y X4 son cada uno independientemente CR6 o N; con la condición de que no más de dos de X1, X2, X3 o X4son N;
L es alquileno C1-4 sustituido con de 0 a 4 R7;
R1 es (-CH2 )aR9;
a es un número entero de 0 o 1;
cada R2 es independientemente halo, ciano, hidroxilo, amino, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxi, alcoxialquilo, haloalcoxialquilo o haloalcoxi;
n es un número entero de 0, 1 o 2;
R3 es hidrógeno, alquilo C1 -6 , alquilo C1-6 deuterado, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi y el alquilo, por sí mismo o como parte de otro resto, está opcionalmente sustituido con deuterio de manera parcial o completa;
R4 es alquilo C1 -10 , alquilo C1 -10 deuterado, haloalquilo C1 -10 , alquenilo C1 -10 , cicloalquilo C3-8, arilo de 6 a 10 miembros, heterociclilo de 3 a 8 miembros, -(alquilen C1 -6 )-(cicloalquilo C3-8), -(alquilen C1 -6 )-(arilo de 6 a 10 miembros), -(alquilen C ^H heterociclilo de 3 a 8 miembros) o -(alquilen C ^H heteroarilo de 5 a 6 miembros); en donde cada uno de los alquilo, alquileno, alquenilo, cicloalquilo, arilo, heterociclilo y heteroarilo, por sí mismos o como parte de otro resto, están independientemente sustituidos con de 0 a 3 R8; o, como alternativa, R3 y R4, tomados junto con los átomos de N a los que están unidos, forman un resto anillo heterocíclico de 4 a 9 miembros que está sustituido con de 0 a 3 R8;
R5 y R6 son cada uno independientemente hidrógeno, halo, ciano, hidroxilo, amino, alquilo C1-6 , alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi;
R7 es halo, oxo, ciano, hidroxilo, amino, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi;
cada uno de R8 es independientemente deuterio, halo, hidroxilo, amino, ciano, alquilo C1 -6 , alquilo C1-6 deuterado, alquenilo C2-6, alquinilo C2-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi, fenilo o heteroarilo de 5 a 6 miembros; o, como alternativa, dos R8, tomados junto con los átomos a los que están unidos, forman un anillo carbocíclico de 3 a 6 miembros o un anillo heterocíclico de 3 a 6 miembros cada uno de los cuales está independientemente sustituido con de 0 a 3 R12;
R9 se selecciona de entre -CN, -C(O)OR10, -C(O)NR11 a R11 b ,
Re es alquilo C1 -6 , cicloalquilo C3-6, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo o haloalcoxialquilo; R10 es hidrógeno o alquilo C1 -10 ; y
R11 a y R11b son cada uno independientemente hidrógeno, alquilo C1 -6 , cicloalquilo C3-6, heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi; y R12 es halo, ciano, hidroxilo, amino, alquilo C1-6 , alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi, fenilo o heteroarilo de 5 a 6 miembros;
en donde,
un grupo alquilo, cuando está presente como parte de otro grupo seleccionado de entre alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxi, alcoxialquilo, haloalcoxialquilo o haloalcoxi, es un grupo alquilo que tiene de 1 a 10 átomos de carbono.
2. El compuesto de acuerdo con la reivindicación 1, en donde n es 0 o 1;
y/o en donde a es 0;
y/o en donde R1 es CO2 H o tetrazolilo;
y/o en donde R45 es alquilo C1 -4.
3. El compuesto de acuerdo con una cualquiera de la reivindicación 1 o 2, en donde:
R4 es alquilo C1 -10 , haloalquilo C1 -10 , cicloalquilo C3-6, -(alquilen C^Hcicloalquilo C3-6) o bencilo; en donde los alquilo, alquileno, cicloalquilo y bencilo están cada uno independientemente sustituidos con de 0 a 3 R8; y cada R8 es independientemente halo, hidroxilo, amino, ciano, alquilo C1-6 , alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi, haloalcoxi o fenilo; o, como alternativa, dos R8, tomados junto con los átomos a los que están unidos, forman un anillo carbocíclico de 3 a 6 miembros.
4. El compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 3, que se representa por las fórmulas (IIa) o (Ilb):
cada R7a es independientemente hidrógeno, halo, oxo, ciano, hidroxilo, amino, alquilo C1-6, cicloalquilo C3-6,
heterociclilo C4-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi;
f es un número entero de 1, 2 o 3;
n es 0 o 1;
R3 es hidrógeno, alquilo C1-4 o alquilo C1-4 deuterado;
R5 es alquilo C1-4; y
R1, R2, n, R4, R5, X1, X2, X3 y X4 son tal como se ha definido en una cualquiera de las reivindicaciones 1 a 3.
5. El compuesto de acuerdo con la reivindicación 4, en donde X1 es CR6, donde R6 es hidrógeno o alquilo C1-4;
y/o en donde X3 es N;
y/o en donde X1, X2, X3 y X4 son CR6, donde cada R6 es independientemente hidrógeno o alquilo C1-4.
6. El compuesto de acuerdo con una cualquiera de las reivindicaciones 4 o 5, en donde: el resto
se selecciona entre
cada R6a es independientemente halo, ciano, hidroxilo, amino, alquilo C1-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi;
y
d es un número entero de 0, 1 o 2;
preferentemente en donde:
el resto
se selecciona entre
y
cada R6 es independientemente hidrógeno, halo, ciano, hidroxilo, amino, alquilo Ci-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi.
7. El compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 6 , en donde f es 1.
8. El compuesto de acuerdo con una cualquiera de las reivindicaciones 1 o 7, que se representa por la fórmula (IlIa) o la fórmula (lllb):
R2a es hidrógeno o halo;
R3 es hidrógeno, CH3 o CD3; y
R1, R4, X1, X2, X3 y X4 son tal como se ha definido en una cualquiera de las reivindicaciones 1 a 7; preferentemente en donde el resto
se selecciona entre
10. El compuesto de acuerdo con una cualquiera de las reivindicaciones 8 o 9, en donde:
R4 es alquilo C3 -10 , haloalquilo C3 -10 , cicloalquilo C3-6, -(alquilen C1 -4 )-(alcoxi C1 -3 ), -(alquilen 6), -(alquilen C ^H cicloalquilo C3-6) o, -(alquilen C1 -4 )-fenilo; en donde los alquilo, alquileno, cicloalquilo y fenilo están cada uno independientemente sustituidos con de 0 a 3 R8 ; y
cada R8 es independientemente deuterio, halo, alquilo C1 -6 , cicloalquilo C3-6, alquilamino, haloalquilo, hidroxialquilo, aminoalquilo, alcoxialquilo, haloalcoxialquilo, alcoxi o haloalcoxi.
11. El compuesto de acuerdo con una cualquiera de las reivindicaciones 8 a 10, en donde:
R4 es alquilo C3 -10 , haloalquilo C3 -10 , ciclobutilo, ciclopentilo, -(CH2 )1 -2 -(alquilamino C2-6), -C(HR8a)1 -2-ciclopropilo, -C(HR8a)-ciclobutilo, -C(HR8a)-pentilo o -C(HR8)-fenilo; en donde los ciclopropilo, ciclobutilo, ciclopentilo y fenilo están cada uno independientemente sustituidos con de 0 a 3 R8 ;
cada R8a es independientemente hidrógeno, metilo, ciclopropilo; y
cada R8 es independientemente halo, alquilo C1-4 o haloalquilo C1 -4.
13. Una composición farmacéutica que comprende uno o más compuestos de acuerdo con una cualquiera de las reivindicaciones 1 a 12 o un estereoisómero, un tautómero o una sal farmacéuticamente aceptable o un solvato del mismo; y un vehículo o un diluyente farmacéuticamente aceptables.
14. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 12 o un estereoisómero, un tautómero o una sal farmacéuticamente aceptable o un solvato del mismo, para su uso en terapia.
15. Un compuesto o un estereoisómero, un tautómero o una sal farmacéuticamente aceptable o un solvato del mismo de acuerdo con una cualquiera de las reivindicaciones 1 a 12 o una composición farmacéutica de acuerdo con la reivindicación 13,
(A) para su uso en el tratamiento de una enfermedad, un trastorno o una afección asociados a desregulación del receptor del ácido lisofosfatídico 1 (LPA1), en donde la enfermedad, el trastorno o la afección se seleccionan entre: (I) fibrosis patológica, preferentemente fibrosis pulmonar, hepática, renal, cardíaca, dérmica, ocular o pancreática; rechazo de trasplante; cáncer, preferentemente en donde el cáncer es de vejiga, sangre, hueso, cerebro, mama, sistema nervioso central, cuello del útero, colon, endometrio, esófago, vesícula biliar, genitales,
tracto genitourinario, cabeza, riñón, laringe, hígado, pulmón, tejido muscular, cuello, mucosa oral o nasal, ovario, páncreas, próstata, piel, bazo, intestino delgado, intestino grueso, estómago, testículo o tiroides; osteoporosis; o trastornos inflamatorios; o
(II) fibrosis pulmonar idiopática (IPF), esteatohepatitis no alcohólica (NASH), esteatosis hepática no alcohólica (NAFLD), enfermedad renal crónica, enfermedad renal diabética y esclerosis sistémica; o
(B) para su uso en el tratamiento de fibrosis en un mamífero que lo necesita, preferentemente en donde la fibrosis es fibrosis pulmonar idiopática (IPF), esteatohepatitis no alcohólica (NASH), enfermedad renal crónica, enfermedad renal diabética y esclerosis sistémica; o
(C) para su uso en el tratamiento de fibrosis pulmonar (fibrosis pulmonar idiopática), asma, enfermedad pulmonar obstructiva crónica (EPOC), fibrosis renal, lesión renal aguda, enfermedad renal crónica, fibrosis hepática (esteatohepatitis no alcohólica), fibrosis de la piel, fibrosis del intestino, cáncer de mama, cáncer de páncreas, cáncer de ovario, cáncer de próstata, glioblastoma, cáncer de huesos, cáncer de colon, cáncer de intestino, cáncer de cabeza y cuello, melanoma, mieloma múltiple, leucemia linfocítica crónica, dolor por cáncer, metástasis tumoral, rechazo de trasplante de órgano, esclerodermia, fibrosis ocular, degeneración macular relacionada con la edad (AMD), retinopatía diabética, enfermedad vascular por colágeno, aterosclerosis, fenómeno de Raynaud o dolor neuropático en un mamífero que lo necesita.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762607527P | 2017-12-19 | 2017-12-19 | |
| PCT/US2018/066109 WO2019126084A1 (en) | 2017-12-19 | 2018-12-18 | Isoxazole o-linked carbamoyl cyclohexyl acids as lpa antagonists |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2925626T3 true ES2925626T3 (es) | 2022-10-19 |
Family
ID=65003574
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18830675T Active ES2925626T3 (es) | 2017-12-19 | 2018-12-18 | Acidos isoxazol-O-carbamoilciclohexílicos como antagonistas de LPA |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11180488B2 (es) |
| EP (1) | EP3728240B1 (es) |
| JP (1) | JP7369125B2 (es) |
| KR (1) | KR102697358B1 (es) |
| CN (1) | CN112041316A (es) |
| ES (1) | ES2925626T3 (es) |
| WO (1) | WO2019126084A1 (es) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR108838A1 (es) | 2016-06-21 | 2018-10-03 | Bristol Myers Squibb Co | Ácidos de carbamoiloximetil triazol ciclohexilo como antagonistas de lpa |
| CN112041304A (zh) * | 2017-12-19 | 2020-12-04 | 百时美施贵宝公司 | 作为lpa拮抗剂的异噁唑n-连接的氨基甲酰基环己基酸 |
| BR112020011953A2 (pt) * | 2017-12-19 | 2020-11-17 | Bristol-Myers Squibb Company | ácidos carbamoil ciclo-hexílicos n-ligados a pirazol como antagonistas de lpa |
| CN111434655A (zh) * | 2019-01-15 | 2020-07-21 | 武汉朗来科技发展有限公司 | 溶血磷脂酸受体拮抗剂及其制备方法 |
| CN114728168B (zh) | 2019-11-15 | 2024-04-09 | 吉利德科学公司 | 三唑氨基甲酸酯吡啶基磺酰胺作为lpa受体拮抗剂及其用途 |
| TWI838626B (zh) | 2020-06-03 | 2024-04-11 | 美商基利科學股份有限公司 | Lpa受體拮抗劑及其用途 |
| EP4161936A1 (en) | 2020-06-03 | 2023-04-12 | Gilead Sciences, Inc. | Lpa receptor antagonists and uses thereof |
| WO2022100623A1 (zh) * | 2020-11-10 | 2022-05-19 | 武汉人福创新药物研发中心有限公司 | 氮取代杂环噻吩类化合物及其用途 |
| WO2022100624A1 (zh) * | 2020-11-10 | 2022-05-19 | 武汉人福创新药物研发中心有限公司 | 氧取代氨基碳酸酯噻吩类化合物及其用途 |
| WO2022100625A1 (zh) * | 2020-11-10 | 2022-05-19 | 武汉人福创新药物研发中心有限公司 | 氮取代氨基碳酸酯噻吩类化合物及其用途 |
| KR20240044386A (ko) * | 2021-04-30 | 2024-04-04 | 비바 스타 바이오사이언시즈 (쑤저우) 컴퍼니 리미티드 | Lpa 길항제로서의 신규 트리아졸-피리딘 치환된 피롤리디닐 및 테트라히드로-2h-피라닐 아세트산 화합물 |
| EP4337641A1 (en) | 2021-05-11 | 2024-03-20 | Gilead Sciences, Inc. | Lpa receptor antagonists and uses thereof |
| AU2022405082A1 (en) | 2021-12-08 | 2024-07-11 | Gilead Sciences, Inc. | Lpa receptor antagonists and uses thereof |
| AR128613A1 (es) | 2022-02-25 | 2024-05-29 | Lhotse Bio Inc | Compuestos y composiciones para el tratamiento de afecciones asociadas con la actividad del receptor de lpa |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001060819A1 (fr) | 2000-02-18 | 2001-08-23 | Kirin Beer Kabushiki Kaisha | Nouveaux composes d'isoxazole et de thiazole et leur utilisation en tant que medicaments |
| JP4396808B2 (ja) | 2001-02-08 | 2010-01-13 | 小野薬品工業株式会社 | Lpa受容体調節剤からなる泌尿器疾患治療剤 |
| JP4692281B2 (ja) * | 2003-08-05 | 2011-06-01 | 味の素株式会社 | 新規アゾール化合物 |
| DE102004038403B4 (de) | 2004-08-07 | 2006-08-31 | Sanofi-Aventis Deutschland Gmbh | Verfahren zur Herstellung der enantiomeren Formen von cis-konfigurierten 3-Hydroxycyclohexancarbonsäure-Derivaten |
| WO2011017350A2 (en) * | 2009-08-04 | 2011-02-10 | Amira Pharmaceuticals, Inc. | Compounds as lysophosphatidic acid receptor antagonists |
| GB2474748B (en) | 2009-10-01 | 2011-10-12 | Amira Pharmaceuticals Inc | Polycyclic compounds as lysophosphatidic acid receptor antagonists |
| GB2474120B (en) | 2009-10-01 | 2011-12-21 | Amira Pharmaceuticals Inc | Compounds as Lysophosphatidic acid receptor antagonists |
| US9272990B2 (en) | 2010-12-07 | 2016-03-01 | Amira Pharmaceuticals, Inc. | Lysophosphatidic acid receptor antagonists and their use in the treatment fibrosis |
| WO2012100436A1 (en) | 2011-01-30 | 2012-08-02 | Curegenix Inc. | Compound as antagonist of lysophosphatidic acid receptor, composition, and use thereof |
| WO2012137982A2 (en) | 2011-04-05 | 2012-10-11 | Takeda Pharmaceutical Company Limited | Sulfonamide derivative and use thereof |
| WO2012138648A1 (en) | 2011-04-06 | 2012-10-11 | Irm Llc | Compositions and methods for modulating lpa receptors |
| WO2013025733A1 (en) * | 2011-08-15 | 2013-02-21 | Intermune, Inc. | Lysophosphatidic acid receptor antagonists |
| WO2013070879A1 (en) | 2011-11-10 | 2013-05-16 | Bristol-Myers Squibb Company | Methods for treating spinal cord injury with lpa receptor antagonists |
| WO2013085824A1 (en) | 2011-12-04 | 2013-06-13 | Angion Biomedica Corp. | Small molecule anti-fibrotic compounds and uses thereof |
| CA2869564A1 (en) | 2012-06-20 | 2013-12-27 | F. Hoffmann-La Roche Ag | N-aryltriazole compounds as lpar antagonists |
| KR20150021057A (ko) | 2012-06-20 | 2015-02-27 | 에프. 호프만-라 로슈 아게 | Lpar 길항제로서의 n-알킬트라이아졸 화합물 |
| DK2988743T3 (da) * | 2013-03-15 | 2021-03-01 | Epigen Biosciences Inc | Heterocykliske forbindelser, der kan anvendes til behandling af sygdom |
| AR108838A1 (es) | 2016-06-21 | 2018-10-03 | Bristol Myers Squibb Co | Ácidos de carbamoiloximetil triazol ciclohexilo como antagonistas de lpa |
| RS62710B1 (sr) | 2017-12-19 | 2022-01-31 | Bristol Myers Squibb Co | Triazol n-vezane karbamoil cikloheksil kiseline kao lpa antagonisti |
-
2018
- 2018-12-18 EP EP18830675.7A patent/EP3728240B1/en active Active
- 2018-12-18 ES ES18830675T patent/ES2925626T3/es active Active
- 2018-12-18 KR KR1020207020878A patent/KR102697358B1/ko active IP Right Grant
- 2018-12-18 JP JP2020533721A patent/JP7369125B2/ja active Active
- 2018-12-18 WO PCT/US2018/066109 patent/WO2019126084A1/en unknown
- 2018-12-18 US US16/954,546 patent/US11180488B2/en active Active
- 2018-12-18 CN CN201880088772.1A patent/CN112041316A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP3728240A1 (en) | 2020-10-28 |
| KR20200101957A (ko) | 2020-08-28 |
| WO2019126084A1 (en) | 2019-06-27 |
| CN112041316A (zh) | 2020-12-04 |
| JP7369125B2 (ja) | 2023-10-25 |
| EP3728240B1 (en) | 2022-06-29 |
| JP2021507899A (ja) | 2021-02-25 |
| US20200317655A1 (en) | 2020-10-08 |
| KR102697358B1 (ko) | 2024-08-20 |
| US11180488B2 (en) | 2021-11-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2925626T3 (es) | Acidos isoxazol-O-carbamoilciclohexílicos como antagonistas de LPA | |
| ES2898364T3 (es) | Acidos carbamoilciclohexílicos ligados a N triazol como antagonistas de LPA | |
| ES2942767T3 (es) | Isoxazol azoles del ácido ciclohexílico como antagonistas del LPA | |
| US11319309B2 (en) | Cyclohexyl acid isoxazole azines as LPA antagonists | |
| ES2895385T3 (es) | Acidos de carbamoiloximetil triazol ciclohexilo como antagonistas de LPA | |
| US11447475B2 (en) | Isoxazole N-linked carbamoyl cyclohexyl acids as LPA antagonists | |
| ES2946657T3 (es) | Acidos ciclopentílicos como antagonistas de LPA | |
| US11261174B2 (en) | Pyrazole O-linked carbamoyl cyclohexyl acids as LPA antagonists | |
| US11384067B2 (en) | Pyrazole n-linked carbamoyl cyclohexyl acids as LPA antagonists | |
| ES2924704T3 (es) | Pirazol azoles del ácido ciclohexílico como antagonistas de LPA | |
| ES2948793T3 (es) | Acidos cicloheptílicos como antagonistas de LPA | |
| ES2944304T3 (es) | Pirazol azinas de ácido ciclohexílico como antagonistas de LPA | |
| ES2941774T3 (es) | Acidos oxabiciclo como antagonistas de LPA | |
| EP3986551A1 (en) | Triazole carboxylic acids as lpa antagonists | |
| US20220235027A1 (en) | Cyclobutyl carboxylic acids as lpa antagonists | |
| WO2020257138A1 (en) | Isoxazole carboxylic acids as lpa antagonists |