ES2870521T3 - Derivados de inositol para su uso en la cristalización patológica - Google Patents
Derivados de inositol para su uso en la cristalización patológica Download PDFInfo
- Publication number
- ES2870521T3 ES2870521T3 ES16819297T ES16819297T ES2870521T3 ES 2870521 T3 ES2870521 T3 ES 2870521T3 ES 16819297 T ES16819297 T ES 16819297T ES 16819297 T ES16819297 T ES 16819297T ES 2870521 T3 ES2870521 T3 ES 2870521T3
- Authority
- ES
- Spain
- Prior art keywords
- mol
- compound
- certain embodiments
- iii
- peg
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000001575 pathological effect Effects 0.000 title description 15
- 238000002425 crystallisation Methods 0.000 title description 14
- 230000008025 crystallization Effects 0.000 title description 14
- 150000004001 inositols Chemical class 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 106
- 229920001223 polyethylene glycol Polymers 0.000 claims abstract description 56
- 239000002202 Polyethylene glycol Substances 0.000 claims abstract description 34
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 72
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 41
- 238000011282 treatment Methods 0.000 description 33
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 27
- XCKKIKBIPZJUET-VYKNHSEDSA-N morphine hydrochloride Chemical compound Cl.O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O XCKKIKBIPZJUET-VYKNHSEDSA-N 0.000 description 24
- 230000015572 biosynthetic process Effects 0.000 description 17
- 238000003786 synthesis reaction Methods 0.000 description 17
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 17
- 208000004434 Calcinosis Diseases 0.000 description 16
- 229960000367 inositol Drugs 0.000 description 16
- 239000013259 porous coordination polymer Substances 0.000 description 15
- 230000002308 calcification Effects 0.000 description 14
- 229920000223 polyglycerol Polymers 0.000 description 13
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 12
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 12
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 11
- 239000011575 calcium Substances 0.000 description 11
- 229910052791 calcium Inorganic materials 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 11
- 208000020832 chronic kidney disease Diseases 0.000 description 11
- KJUGUADJHNHALS-UHFFFAOYSA-N 1H-tetrazole Chemical compound C=1N=NNN=1 KJUGUADJHNHALS-UHFFFAOYSA-N 0.000 description 10
- IMQLKJBTEOYOSI-UHFFFAOYSA-N Phytic acid Natural products OP(O)(=O)OC1C(OP(O)(O)=O)C(OP(O)(O)=O)C(OP(O)(O)=O)C(OP(O)(O)=O)C1OP(O)(O)=O IMQLKJBTEOYOSI-UHFFFAOYSA-N 0.000 description 10
- 210000002966 serum Anatomy 0.000 description 10
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- IYYIVELXUANFED-UHFFFAOYSA-N bromo(trimethyl)silane Chemical compound C[Si](C)(C)Br IYYIVELXUANFED-UHFFFAOYSA-N 0.000 description 9
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 8
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 8
- 239000011541 reaction mixture Substances 0.000 description 8
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 8
- 229910019142 PO4 Inorganic materials 0.000 description 7
- 208000005475 Vascular calcification Diseases 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 150000008300 phosphoramidites Chemical class 0.000 description 7
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 6
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 6
- 239000002245 particle Substances 0.000 description 6
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 6
- 239000010452 phosphate Substances 0.000 description 6
- 235000021317 phosphate Nutrition 0.000 description 6
- 230000007704 transition Effects 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 238000005160 1H NMR spectroscopy Methods 0.000 description 5
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 5
- 208000002849 chondrocalcinosis Diseases 0.000 description 5
- 210000003734 kidney Anatomy 0.000 description 5
- 235000002949 phytic acid Nutrition 0.000 description 5
- 230000002265 prevention Effects 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 206010008690 Chondrocalcinosis pyrophosphate Diseases 0.000 description 4
- 208000032064 Chronic Limb-Threatening Ischemia Diseases 0.000 description 4
- IMQLKJBTEOYOSI-GPIVLXJGSA-N Inositol-hexakisphosphate Chemical compound OP(O)(=O)O[C@H]1[C@H](OP(O)(O)=O)[C@@H](OP(O)(O)=O)[C@H](OP(O)(O)=O)[C@H](OP(O)(O)=O)[C@@H]1OP(O)(O)=O IMQLKJBTEOYOSI-GPIVLXJGSA-N 0.000 description 4
- 206010034576 Peripheral ischaemia Diseases 0.000 description 4
- 210000001367 artery Anatomy 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- LULAYUGMBFYYEX-UHFFFAOYSA-N metachloroperbenzoic acid Natural products OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 description 4
- 230000026731 phosphorylation Effects 0.000 description 4
- 238000006366 phosphorylation reaction Methods 0.000 description 4
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 4
- 230000019635 sulfation Effects 0.000 description 4
- 238000005670 sulfation reaction Methods 0.000 description 4
- 239000011593 sulfur Substances 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- FGTJJHCZWOVVNH-UHFFFAOYSA-N tert-butyl-[tert-butyl(dimethyl)silyl]oxy-dimethylsilane Chemical group CC(C)(C)[Si](C)(C)O[Si](C)(C)C(C)(C)C FGTJJHCZWOVVNH-UHFFFAOYSA-N 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 238000004679 31P NMR spectroscopy Methods 0.000 description 3
- 206010051714 Calciphylaxis Diseases 0.000 description 3
- 208000005764 Peripheral Arterial Disease Diseases 0.000 description 3
- 208000030831 Peripheral arterial occlusive disease Diseases 0.000 description 3
- INAPMGSXUVUWAF-GCVPSNMTSA-N [(2r,3s,5r,6r)-2,3,4,5,6-pentahydroxycyclohexyl] dihydrogen phosphate Chemical class OC1[C@H](O)[C@@H](O)C(OP(O)(O)=O)[C@H](O)[C@@H]1O INAPMGSXUVUWAF-GCVPSNMTSA-N 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 230000002526 effect on cardiovascular system Effects 0.000 description 3
- -1 inositol phosphates Chemical class 0.000 description 3
- OKKJLVBELUTLKV-VMNATFBRSA-N methanol-d1 Chemical compound [2H]OC OKKJLVBELUTLKV-VMNATFBRSA-N 0.000 description 3
- 125000006239 protecting group Chemical group 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- RMVRSNDYEFQCLF-UHFFFAOYSA-N thiophenol Chemical compound SC1=CC=CC=C1 RMVRSNDYEFQCLF-UHFFFAOYSA-N 0.000 description 3
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 3
- 230000002792 vascular Effects 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 201000001320 Atherosclerosis Diseases 0.000 description 2
- 208000000913 Kidney Calculi Diseases 0.000 description 2
- ZMANZCXQSJIPKH-UHFFFAOYSA-N N,N-Diethylethanamine Substances CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 2
- 206010029148 Nephrolithiasis Diseases 0.000 description 2
- 208000001132 Osteoporosis Diseases 0.000 description 2
- 208000004777 Primary Hyperoxaluria Diseases 0.000 description 2
- 206010040943 Skin Ulcer Diseases 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 206010002906 aortic stenosis Diseases 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 229940043256 calcium pyrophosphate Drugs 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 208000029078 coronary artery disease Diseases 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 238000000502 dialysis Methods 0.000 description 2
- 239000000385 dialysis solution Substances 0.000 description 2
- 235000019821 dicalcium diphosphate Nutrition 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 238000001631 haemodialysis Methods 0.000 description 2
- 230000000322 hemodialysis Effects 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 210000002414 leg Anatomy 0.000 description 2
- RLSSMJSEOOYNOY-UHFFFAOYSA-N m-cresol Chemical compound CC1=CC=CC(O)=C1 RLSSMJSEOOYNOY-UHFFFAOYSA-N 0.000 description 2
- 230000010198 maturation time Effects 0.000 description 2
- 238000000034 method Methods 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 201000000173 nephrocalcinosis Diseases 0.000 description 2
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 231100000019 skin ulcer Toxicity 0.000 description 2
- 210000004872 soft tissue Anatomy 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- BCNZYOJHNLTNEZ-UHFFFAOYSA-N tert-butyldimethylsilyl chloride Chemical compound CC(C)(C)[Si](C)(C)Cl BCNZYOJHNLTNEZ-UHFFFAOYSA-N 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 2
- 238000006863 thiophosphorylation reaction Methods 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- CJYDNDLQIIGSTH-UHFFFAOYSA-N 1-(3,5,7-trinitro-1,3,5,7-tetrazocan-1-yl)ethanone Chemical compound CC(=O)N1CN([N+]([O-])=O)CN([N+]([O-])=O)CN([N+]([O-])=O)C1 CJYDNDLQIIGSTH-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- WFIYPADYPQQLNN-UHFFFAOYSA-N 2-[2-(4-bromopyrazol-1-yl)ethyl]isoindole-1,3-dione Chemical compound C1=C(Br)C=NN1CCN1C(=O)C2=CC=CC=C2C1=O WFIYPADYPQQLNN-UHFFFAOYSA-N 0.000 description 1
- 200000000007 Arterial disease Diseases 0.000 description 1
- 208000006029 Cardiomegaly Diseases 0.000 description 1
- 206010011703 Cyanosis Diseases 0.000 description 1
- 206010017711 Gangrene Diseases 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- 208000007177 Left Ventricular Hypertrophy Diseases 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 208000031481 Pathologic Constriction Diseases 0.000 description 1
- 208000004210 Pressure Ulcer Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010038478 Renal lithiasis Diseases 0.000 description 1
- 206010038687 Respiratory distress Diseases 0.000 description 1
- 206010040893 Skin necrosis Diseases 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 206010060872 Transplant failure Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 102000012005 alpha-2-HS-Glycoprotein Human genes 0.000 description 1
- 108010075843 alpha-2-HS-Glycoprotein Proteins 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 208000028922 artery disease Diseases 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 239000013060 biological fluid Substances 0.000 description 1
- 230000033558 biomineral tissue development Effects 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- JUNWLZAGQLJVLR-UHFFFAOYSA-J calcium diphosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])(=O)OP([O-])([O-])=O JUNWLZAGQLJVLR-UHFFFAOYSA-J 0.000 description 1
- 208000022458 calcium metabolism disease Diseases 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 208000022831 chronic renal failure syndrome Diseases 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 230000008753 endothelial function Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 210000003414 extremity Anatomy 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000003818 flash chromatography Methods 0.000 description 1
- 125000003827 glycol group Chemical group 0.000 description 1
- 230000003779 hair growth Effects 0.000 description 1
- 238000002615 hemofiltration Methods 0.000 description 1
- 230000023597 hemostasis Effects 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 210000000629 knee joint Anatomy 0.000 description 1
- 208000030175 lameness Diseases 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- XELZGAJCZANUQH-UHFFFAOYSA-N methyl 1-acetylthieno[3,2-c]pyrazole-5-carboxylate Chemical compound CC(=O)N1N=CC2=C1C=C(C(=O)OC)S2 XELZGAJCZANUQH-UHFFFAOYSA-N 0.000 description 1
- 230000004089 microcirculation Effects 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004001 molecular interaction Effects 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 210000004165 myocardium Anatomy 0.000 description 1
- YYHPEVZFVMVUNJ-UHFFFAOYSA-N n,n-diethylethanamine;sulfur trioxide Chemical compound O=S(=O)=O.CCN(CC)CC YYHPEVZFVMVUNJ-UHFFFAOYSA-N 0.000 description 1
- AFDQGRURHDVABZ-UHFFFAOYSA-N n,n-dimethylformamide;sulfur trioxide Chemical compound O=S(=O)=O.CN(C)C=O AFDQGRURHDVABZ-UHFFFAOYSA-N 0.000 description 1
- 230000036562 nail growth Effects 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 150000002905 orthoesters Chemical class 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 208000030613 peripheral artery disease Diseases 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000002250 progressing effect Effects 0.000 description 1
- 230000006916 protein interaction Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000284 resting effect Effects 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 238000001542 size-exclusion chromatography Methods 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 208000037804 stenosis Diseases 0.000 description 1
- 230000036262 stenosis Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/117—Esters of phosphoric acids with cycloaliphatic alcohols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/661—Phosphorus acids or esters thereof not having P—C bonds, e.g. fosfosal, dichlorvos, malathion or mevinphos
- A61K31/6615—Compounds having two or more esterified phosphorus acid groups, e.g. inositol triphosphate, phytic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/04—Drugs for disorders of the urinary system for urolithiasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/06—Antigout agents, e.g. antihyperuricemic or uricosuric agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/12—Drugs for disorders of the metabolism for electrolyte homeostasis
- A61P3/14—Drugs for disorders of the metabolism for electrolyte homeostasis for calcium homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/14—Vasoprotectives; Antihaemorrhoidals; Drugs for varicose therapy; Capillary stabilisers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/16—Esters of thiophosphoric acids or thiophosphorous acids
- C07F9/165—Esters of thiophosphoric acids
- C07F9/177—Esters of thiophosphoric acids with cycloaliphatic alcohols
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/335—Polymers modified by chemical after-treatment with organic compounds containing phosphorus
- C08G65/3353—Polymers modified by chemical after-treatment with organic compounds containing phosphorus containing oxygen in addition to phosphorus
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/335—Polymers modified by chemical after-treatment with organic compounds containing phosphorus
- C08G65/3358—Polymers modified by chemical after-treatment with organic compounds containing phosphorus having sulfur in addition to phosphorus
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Physical Education & Sports Medicine (AREA)
- Rheumatology (AREA)
- Epidemiology (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Dermatology (AREA)
- Pain & Pain Management (AREA)
- Polymers & Plastics (AREA)
- Endocrinology (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Polyethers (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Un compuesto descrito mediante una fórmula general (II) **(Ver fórmula)** en la que -dos o tres X son R1 y el resto de X son OPO32- y -cada R1 es un polietilenglicol.
Description
DESCRIPCIÓN
Derivados de inositol para su uso en la cristalización patológica
La presente invención se refiere al uso de compuestos farmacéuticos para tratar o prevenir dolencias relacionadas con la cristalización patológica del calcio.
Antecedentes de la invención
Los pacientes con enfermedad renal crónica (ERC) padecen una deposición mineral acelerada en los tejidos blandos, especialmente en el sistema vascular, debido a una pérdida en la hemostasia de los factores que regulan los procesos de biomineralización del cuerpo. Dichos depósitos conducen a la rigidización de las paredes arteriales, que finalmente produce un aumento de la presión arterial, hipertrofia ventricular izquierda, caudal sanguíneo coronario reducido, una alteración en el funcionamiento endotelial y daños en la microcirculación de riñones y cerebro. Como resultado, la mortalidad por todas causas de los pacientes de ERC aumenta exponencialmente a medida que la función renal disminuye. Las concentraciones fisiológicas de calcio y fosfato en la sangre están cerca de la sobresaturación. Los componentes de la sangre tales como fetuína A interactúan con el calcio y el fosfato para formar nanopartículas solubles denominadas partículas de calciproteína (PCP) que evitan la precipitación y dan como resultado la calcificación en condiciones normales. Las denominadas PCP primarias son amorfas, y tienen de forma típica un diámetro hidrodinámico de menos de 100 nm, y maduran con el tiempo para reorganizarse en las PCP secundarias cristalinas que tienen un diámetro hidrodinámico de más de 100 nm. Posteriormente, las PCP secundarias prosiguen con la calcificación e inician respuestas patológicas.
Un agente farmacéutico capaz de reducir la propensión a la progresión de las PCP primarias para dar PCP secundarias y, por tanto, finalmente capaz de reducir la cristalización patológica, tendría de esta forma un valor terapéutico significativo. Hasta la fecha, no existe ninguna terapia autorizada o clínicamente validada para la reducción o la prevención de las calcificaciones vasculares.
Los derivados de inositol fosfatos tales como fitato (IP6) se divulgaron en las menciones siguientes como agentes adecuados en el tratamiento de patologías asociadas a trastorno del calcio:
GRASES F ET AL: "PHYTATE (IP6) IS A POWERFUL AGENT FOR PREVENTING CALCIFICATIONS IN BIOLOGICAL FLUIDS: USEFULNESS IN RENAL LITHIASIS TREATMENT", ANTICANCER RESEARCH -INTERNATIONAL JOURNAL OF CANCER RESEARCH Y TREATMENT, INTERNATIONAL INSTITUTE OF ANTICANCER RESEARCH, vol. 19, n.° 5A, 1 enero de 1999, páginas 3717-3722
Documento EP 2324835 A2
Documento EP 2022501 A1
Documento WO 2010/018278 A2
FELIX GRASES ET AL: "Phytate (Myo-inositol hexakisphosphate) inhibits cardiovascular calcifications in rats", FRONTIERS IN BIOSCIENCE, vol. 11, n.° 1, 1 enero de 2006, páginas 136-142
Por lo tanto, el problema subyacente a la presente invención es proporcionar una intervención farmacológica eficaz para reducir la cristalización patológica. Este problema se resuelve mediante la materia sujeto de las reivindicaciones independientes.
Descripción
La presente invención se refiere al uso de derivados de inositol fosfatos de fórmula (II) como se definen en las reivindicaciones pendientes 1 a 3.
La presente descripción se refiere al uso de inositol fosfatos, sulfatos, y/o tiofosfatos de inositol con o sin la adición covalente de poli(etilenglicol) (PEG) o poliglicerol, para prevenir o reducir la cristalización patológica en tejidos blandos.
De acuerdo con un primer aspecto de la presente descripción, un compuesto descrito mediante una fórmula general (I)
se proporciona para su uso en terapia o prevención de dolencias relacionadas con la cristalización patológica del calcio, en la que
- Z es (CHX)pCHX(CHX)q;
- cada uno de p y q, independientemente entre sí, tienen un valor de 0 a 2, con la condición de que (p+q) tiene un valor de 0, 1 o 2;
- uno o dos o tres X pueden ser R1 y el resto de X independientemente entre sí se seleccionan entre OPO32', OPSO22', y OSO3 ', con la condición de que no todo X es OPO32' y no todo X es OSO3 '; y
- R1 comprende una función de solubilidad R2 seleccionada del grupo que incluye
• un polietilenglicol o
• un poliglicerol.
Las dolencias relacionadas con la cristalización patológica del calcio para las que los compuestos de la presente invención son especialmente útiles incluyen la calcificación vascular, arteriopatía coronaria, rigidización vascular, calcificación valvular, nefrocalcinosis, calcinosis cutis, piedras en el riñón, condrocalcinosis, osteoporosis, infarto de miocardio, mortalidad cardiovascular (especialmente en pacientes con enfermedad renal crónica), progresión de la enfermedad renal crónica y del fracaso de los injertos de trasplante renal. Se ha demostrado que la cristalización patológica está asociada a la mortalidad por todas las causas de pacientes con enfermedad renal crónica, por tanto, los compuestos de la presente invención están indicados para los pacientes con enfermedad renal crónica, de una forma general.
Otras dolencias que se beneficiarán de un tratamiento con los compuestos de la invención son la arteriopatía periférica, isquemia crítica de la extremidad, calcifilaxia, calcificación arterial general infantil, estenosis aórtica, ateroesclerosis, pseudogota, hiperoxaluria primaria y pseudoxantoma elástico.
En el contexto de la presente memoria descriptiva, "arteriopatía periférica" se refiere a un estrechamiento de las arterias periféricas en dirección a las piernas (lo más habitualmente), estómago, brazos y cabeza. Los síntomas incluyen cojera intermitente (dolor en la pierna al caminar que desaparece al descansar), úlceras cutáneas, piel azulada, piel fría, o poco crecimiento de uñas y cabello.
En el contexto de la presente memoria descriptiva, "isquemia crítica de la extremidad" se refiere a una obstrucción grave de las arterias que reduce notablemente el flujo sanguíneo hacia las extremidades, y progresa hasta el punto de dolor grave e incluso úlceras cutáneas, escaras, o gangrena. La isquemia crítica de la extremidad es un estado muy grave de la arteriopatía periférica.
En el contexto de la presente memoria descriptiva, "calcifilaxis" o "arteriopatía urémica calcificada" se refiere a un síndrome de calcificación vascular, trombosis y necrosis cutánea.
En el contexto de la presente memoria descriptiva, "pseudogota", también conocida como "enfermedad por depósito de cristales de pirofosfato de calcio dihidrato (PCPD)” o “artropatía por pirofosfato" se refiere a un trastorno reumatológico que se considera producido por la acumulación de cristales de pirofosfato de calcio en tejidos conectivos, especialmente articulaciones, tales como la articulación de la rodilla.
En el contexto de la presente memoria descriptiva, la expresión “calcificación arterial general infantil” (GACI) se refiere a un trastorno que afecta al sistema circulatorio que resulta evidente antes del nacimiento o en los primeros meses de vida, y que se caracteriza por una calcificación anómala de las arterias y el engrosamiento de las paredes arteriales. Estos cambios producen estenosis y rigidez de las arterias, dando como resultado insuficiencia cardiaca en algunos individuos afectados, con signos y síntomas que incluye dificultad respiratoria, edema, cianosis, hipertensión y cardiomegalia.
Existe cierto grado de flexibilidad en la composición óptima para el ligando aniónico, así como para la función de solubilidad polimérica. Sin pretender imponer ninguna teoría, los inventores teorizan que esto se debe al hecho de
que las interacciones que proporcionan beneficio terapéutico pueden consistir principalmente en interacciones electrostáticas entre aniones y cationes pequeños, junto con impedimento estérico, y ambos fenómenos son, en términos de requisitos de encaje de la interacción molecular, menos selectivos que, por ejemplo, una interacción proteína-ligando.
En determinadas realizaciones, R1 es R2 y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, R1 es o comprende un polietilenglicol o un poliglicerol, y R1 tiene una masa molar entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2000 g/mol, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, R1 es o comprende un polietilenglicol o un poliglicerol, y R1 tiene una masa molar entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol a 2000 g/mol, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante una fórmula general (II)
(II),
en la que
- uno o dos o tres X son R1 y el resto de X independientemente de cualquier otro X puede ser OPO32', OPSO22", y OSO3 " y
- R1 es un polietilenglicol o un poliglicerol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
Se entiende que las líneas rectas de la fórmula II indican que la estereoquímica de los átomos de carbono individuales del anillo no está definida. Se entiende que la fórmula abarca cualquier diastereómero.
En determinadas realizaciones, R1 es un polietilenglicol.
En determinadas realizaciones, R1 es un polietilenglicol descrito mediante la fórmula R3-(O-CH2-CH2 )n- o R3-(O-CH2-CH2 )n-O- y R3 es hidrógeno, metilo o etilo, y n tiene un valor de 2 a 200.
En determinadas realizaciones, n tiene un valor de 3 a 200.
En determinadas realizaciones, n tiene un valor de 3 a 20. En determinadas realizaciones, n tiene un valor de 10 a 30. En determinadas realizaciones, n tiene un valor de 9 a 45.
En determinadas realizaciones, n tiene un valor de 7 a 11.
En determinadas realizaciones, n tiene un valor de 2. En determinadas realizaciones, n tiene un valor de 7. En determinadas realizaciones, n tiene un valor de 9. En determinadas realizaciones, n tiene un valor de 11. En determinadas realizaciones, n tiene un valor de 45.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), un X es R1 y el resto de X independientemente de cualquier otro X puede ser OPO32', OPSO22', y OSO3 '; y R1 es un polietilenglicol o un poliglicerol que tiene una masa molar entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2000 g/mol, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), un X es R1 y el resto de X independientemente de cualquier otro X puede ser OPO32-, OPSO22-, y OSO3-; y R1 es un polietilenglicol o un poliglicerol que tiene una masa molar entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol a 2000 g/mol, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- un X es R1 y el resto de X son OPO32-; y
- R1 es un polietilenglicol y tiene una masa molar comprendida entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- un X es R1 y el resto de X son OPO32-; y
- R1 es un polietilenglicol y tiene una masa molar comprendida entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II) y
- dos X son R1 y el resto de X independientemente de cualquier otro X puede ser OPO32", OPSO22", y OSO3"; y - cada R1 se selecciona, independientemente entre sí, de un polietilenglicol y un poliglicerol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), dos X son R1 y el resto de X independientemente de cualquier otro X puede ser OPO32', OPSO22', y OSO3 '; y cada R1 independientemente entre sí es un polietilenglicol o un poliglicerol que tiene una masa molar entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2000 g/mol, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), dos X son R1 y el resto de X independientemente de cualquier otro X puede ser OPO32', OPSO22', y OSO3 '; y cada R1 independientemente entre sí es un polietilenglicol o un poliglicerol que tiene una masa molar entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol a 2000 g/mol, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- dos X son R1 y el resto de X son OPO32'; y
- R1 es un polietilenglicol y tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- dos X son R1 y el resto de X son OPSO22'; y
- R1 es un polietilenglicol y tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- dos X son R1 y el resto de X son OSO3- y
- R1 es un polietilenglicol y tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2 0 0 0 g/mol o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2 0 0 0 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II) y
- tres X son R1 y el resto de X independientemente de cualquier otro X puede ser OPO32', OPSO22', y OSO3 '; y - cada R1 se selecciona, independientemente entre sí, de un polietilenglicol y un poliglicerol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), tres X son R1 y el resto de X independientemente de cualquier otro X puede ser OPO32', OPSO22', y OSO3 '; y cada R1 independientemente entre sí es un polietilenglicol o un poliglicerol que tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2000 g/mol, o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol a 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- tres X son R1 y el resto de X son OPO32- y
- R1 es un polietilenglicol y tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- tres X son R1 y el resto de X son OPSO22'; y
- R1 es un polietilenglicol y tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula general (II), en la que
- tres X son R1 y el resto de X son OSO3 '; y
- R1 es un polietilenglicol y tiene una masa molar
- entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol o
- entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol o de aprox. 2000 g/mol;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se caracteriza mediante una fórmula general (III a), (III b), (III c) o
(III d):
en las que cada X (independientemente) y R1 tienen el significado detallado anteriormente y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se caracteriza mediante una fórmula general (III e), (III f), (III g), (III h), (III i) o (III j):
en las que R1 tiene el significado detallado anteriormente y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, más de un R1 está presente y cada R1 es el mismo que cualquier otro R1.
En determinadas realizaciones, el compuesto se caracteriza mediante una fórmula general (IV a), (IV b), (IV c), (IV d), (V a) o (V b)
en las que cada X (independientemente) y R1 tienen el significado detallado anteriormente y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas. En determinadas realizaciones, uno o dos o tres X son R1 y el resto de X son
- todos OPO32- o
- todos OPSO22" o
- todos OSO3 '.
En determinadas realizaciones,
- uno o dos o tres X son R1 y el resto de X son OPO32'; y
- R1 es un polietilenglicol y tiene una masa molar comprendida entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol.
En determinadas realizaciones,
- uno o dos o tres X son R1 y el resto de X son OPSO22'; y
- R1 es un polietilenglicol y tiene una masa molar comprendida entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol.
En determinadas realizaciones, tres X son R1.
En determinadas realizaciones, un X es R1 y de los restantes X
- tres X son OSO3 ' y dos X son OPSO22', o tres X son OSO3 ' y dos X son OPO32', y
- R1 es un polietilenglicol y tiene una masa molar comprendida entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol o de aprox. 2000 g/mol.
En determinadas realizaciones, R1 es o comprende un polietilenglicol caracterizado por una fórmula R3-(O-CH2-CH2 )n- o R3-(O-CH2-CH2 )n-O- y R3 es hidrógeno, metilo o etilo.
En determinadas realizaciones, el compuesto se describe mediante una fórmula general (III k), (III I), (III m) o (III n)
en la que n tiene un valor de 2 a 200. En determinadas realizaciones, n es 2 o n es de 7 a 50. En determinadas realizaciones, n es 2, 7 a 12 o de 40 a 50. En determinadas realizaciones, n es 2, 7, 9, 11 o 45. El compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante una fórmula general (NI k), (III I), (III m) o (III n), en la que n tiene un valor de 3 a 200, especialmente de 7 a 50, más especialmente de 7 a 12 o de 40 a 50, incluso más especialmente 9 o 45, y el compuesto se utilizar para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
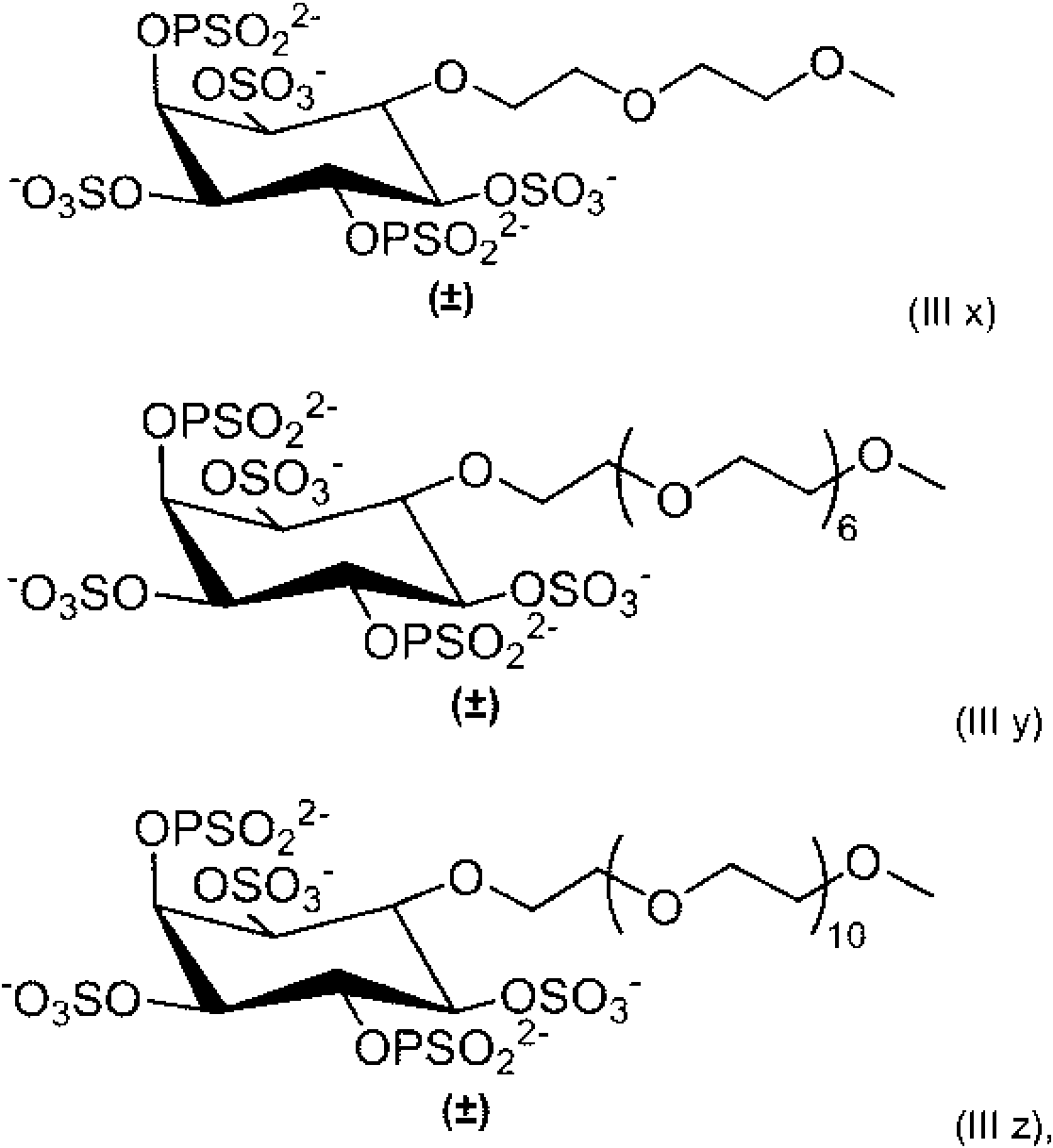
En determinadas realizaciones, el compuesto se describe mediante una cualquiera de las fórmulas (III o), (III p), (III q), (III r), (III s), (III t), (III u), (III v), (III w), (III x), (III y) o (III z)
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
Con respecto a los sustituyentes (OPO32-, OPSO22-, OSO3-) y la longitud de los restos de PEG,
- la fórmula (III m) con n = 2 corresponde a la fórmula (III o) / compuesto INS-2001;
- la fórmula (III m) con n = 7 corresponde a la fórmula (III p) / compuesto INS-2031;
- la fórmula (III m) con n = 11 corresponde a la fórmula (III q) / compuesto INS-2041;
- la fórmula (III n) con n = 2 corresponde a la fórmula (III u) / compuesto INS-4001;
- la fórmula (III n) con n = 7 corresponde a la fórmula (III v) / compuesto INS-4031; y
- la fórmula (III n) con n = 11 corresponde a la fórmula (III w) / compuesto INS-4041.
En determinadas realizaciones, el compuesto se describe mediante una fórmula general (IV e) o (V c)
en la que n tiene un valor de 2 a 200, especialmente 2 o de 7 a 50, más especialmente 2, de 7 a 12 o de 40 a 50, incluso más especialmente 2, 7, 9, 11 o 45, y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
Una realización de la presente descripción que muestra una actividad especialmente alta es el uso de 2-PEG-IP5
(m/'o-pentaquis-fosfato de inositol-(2)-PEG, especificado mediante la fórmula (IV e) con restos de PEG que tienen una masa molar de aproximadamente 400 g/mol (n=9) o aproximadamente 2000 g/mol (n=45) para las indicaciones anteriormente relacionadas. Esta conclusión se extrae de los resultados de un ensayo /n v/tro que mide la propensión a la calcificación del suero humano, que se ha validado clínicamente como un predictor de la mortalidad por todas las causas en pacientes de CKD y pacientes de trasplante renal (Fig. 1). Los inventores muestran que, sorprendentemente, IP5-PEG es un inhibidor mucho más potente que IP6 para reducir la propensión a la calcificación del suero humano. Este resultado es inesperado, porque se supone que la eliminación de un grupo fosfato reduce la afinidad de la molécula por el calcio, pero evidentemente esto queda más que compensado por la adición del resto de PEG. Sin pretender imponer ninguna teoría, los inventores teorizan que esto se debe al hecho de que el resto de PEG aumenta la solubilidad de los complejos de PCP y proporciona impedimento estérico que evita la transformación del fosfato de calcio de amorfo a cristalino, y/o el crecimiento del cristal. Además, la adición de PEG (u otro polímero) a la molécula ofrece la posibilidad de personalizar su tiempo de circulación y, por tanto, ofrece calendarios de dosificación más flexibles que IP6. Este aspecto no se había tenido en cuenta anteriormente para los análogos de IP6, y supone una ventaja competitiva respecto de IP6 para la presente indicación. En determinadas realizaciones, el compuesto se describe mediante una cualquiera de las fórmulas (IV f), (IV g), (IV h), (IV i), (IV j), (IV k), (V d), (V e), (V f), (V g), (V h) o (V i)
- la fórmula (IV e) con n = 2 corresponde a la fórmula (IV f) / compuesto INS-3001;
- la fórmula (IV e) con n = 7 corresponde a la fórmula (IV g) / compuesto INS-3031;
- la fórmula (IV e) con n = 11 corresponde a la fórmula (IV h) / compuesto INS-3041;
- la fórmula (V c) con n = 2 corresponde a la fórmula (V d) / compuesto INS-5001;
- la fórmula (V c) con n = 7 corresponde a la fórmula (V e) / compuesto INS-5031; y
- la fórmula (V c) con n = 11 corresponde a la fórmula (V f) / compuesto INS-5041.
En determinadas realizaciones, cuando una cadena de polietilenglicol se muestra como fórmula de la presente memoria descriptiva, el resto de PEG es un polietilenglicol monodisperso. En determinadas fórmulas, un resto de PEG monodisperso se asigna mediante la abreviatura mdPEG.
En determinadas realizaciones, el compuesto se describe mediante una fórmula general (III o), (III p), (III q), (III u), (III v) o (III w)
En determinadas realizaciones,
a) (p+q) es 0, dos de cinco X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-, o
b) (p+q) es 0, tres de cinco X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-, o
c) (p+q) es 1, dos de seis X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-, o
d) (p+q) es 1, tres de seis X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-, o
e) (p+q) es 1, cuatro de seis X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-, o
f) (p+q) es 2, tres de siete X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-, o
g) (p+q) es 2, cuatro de siete X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3- o
h) (p+q) es 2, cinco de siete X se seleccionan independientemente de OPO32- y OPSO22- y el resto de X son OSO3-;
y el compuesto se utiliza para el tratamiento de cualquiera de las indicaciones anteriormente relacionadas.
En determinadas realizaciones, el compuesto se describe mediante la fórmula
La Fig. 1 demuestra que este compuesto (4,6-di-(0-tiofosfato)-inositoM,2,3,5-tetra-0-sulfato, IT2S4) es más activo que IP6 para inhibir la transición de PCP primarias a secundarias y por tanto puede reducir la propensión a la calcificación del suero humano.
En determinadas realizaciones, el compuesto se describe mediante la fórmula
La Fig. 1 demuestra que este compuesto (4,6-di-(0-fosfato)-inositol-1,2,3,5-tetra-0-sulfato, IP2S4) es más activo que IP6 para inhibir la transición de PCP primarias a secundarias y por tanto puede reducir la propensión a la calcificación del suero humano.
De acuerdo con un segundo aspecto de la presente descripción, se proporciona una forma farmacéutica que comprende el compuesto que se ha especificado en cualquiera de las fórmulas anteriores para su uso en terapia o prevención de dolencias relacionadas con la cristalización patológica del calcio.
La forma farmacéutica puede formularse para administración parenteral, tal como administración intravenosa, intraperitoneal, intramuscular, intraarterial o subcutánea. Opcionalmente, puede estar presente un transportador y/o excipiente farmacéuticamente aceptable.
De acuerdo con un tercer aspecto de la presente descripción, una solución de diálisis para su uso en hemodiálisis, hemofiltración o diálisis peritoneal que comprende el compuesto que se ha especificado en los anteriores aspectos de la presente descripción se proporciona para su uso en terapia o prevención de dolencias relacionadas con la cristalización patológica del calcio.
De acuerdo con otro aspecto de la presente descripción, se proporciona un método para el tratamiento o prevención de cualquiera de las dolencias relacionadas con la cristalización patológica del calcio anteriormente relacionada, que comprende la administración del compuesto como se ha especificado mediante cualquiera de las fórmulas anteriores a un sujeto que lo necesita. El compuesto se puede administrar por vía intravenosa, intraperitoneal, intramuscular, intraarterial o subcutánea. Como alternativa, el compuesto se puede administrar como componente de una solución de diálisis para hemodiálisis o diálisis peritoneal.
Reivindicaciones del compuesto
De acuerdo con otro aspecto adicional de la presente descripción, se proporciona un compuesto de acuerdo con la
fórmula general (II), en la que
- dos o tres X son R1 y el resto de X independientemente de otros X se seleccionan de OPO32', OPSO22" y OSO3 '; y
- R1 es un polietilenglicol o un poliglicerol.
En determinadas realizaciones de este aspecto de la presente descripción, dos o tres X son R1 y el resto de X son - todos OPO32- o
- todos OPSO22- o
- todos OSO3-.
En determinadas realizaciones de este aspecto de la presente descripción, R1 es un polietilenglicol y tiene una masa molar comprendida entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2000 g/mol.
Otro aspecto de la presente descripción se refiere a un compuesto descrito mediante una cualquiera de las fórmulas (IV a), (IV b), (IV c), (IV d), (V a) o (V b), en la que cada X (independientemente) y R1 tienen el significado anteriormente detallado. En determinadas realizaciones de este aspecto de la presente descripción, n (como parte de la definición de R1) tiene un valor de 2 a 200. En determinadas realizaciones de este aspecto de la invención, n es 2 o n es de 7 a 50. En determinadas realizaciones de este aspecto de la presente invención, n es 2, 7 a 12 o de 40 a 50. En determinadas realizaciones de este aspecto de la presente descripción, n es 2, 7, 9, 11 o 45.
En determinadas realizaciones, el compuesto de la presente descripción se describe mediante una cualquiera de las fórmulas (IV e) o (V c), y n tiene un valor de 2 a 200. En determinadas realizaciones de este aspecto de la presente descripción, n es 2 o n es de 7 a 50. En determinadas realizaciones de este aspecto de la presente descripción n es 2, de 7 a 12 o de 40 a 50. En determinadas realizaciones de este aspecto de la invención, n es 2, 7, 9, 11 o 45. En determinadas realizaciones de este aspecto de la presente invención, todo X excepto dos o tres X que son R1 son fosfato.
En determinadas realizaciones de este aspecto de la presente invención, R1 es un polietilenglicol.
En determinadas realizaciones de este aspecto de la presente invención, R1 tiene una masa molar entre 100 g/mol y 3000 g/mol, especialmente entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2000 g/mol. En determinadas realizaciones de este aspecto de la presente invención tiene una masa molar entre 200 g/mol y 3000 g/mol, especialmente entre 300 g/mol y 2500 g/mol, más especialmente de aprox. 400 g/mol a 2000 g/mol. Otro aspecto de la presente invención se refiere a un compuesto descrito mediante una cualquiera de las fórmulas (IV f), (IV g), (IV h), (IV i), (IV j), (IV k), (V d), (V e), (V f), (V g), (V h) o (V i).
Cualquiera de los novedosos compuestos o grupos de compuestos descritas en el presente documento se proporciona per se. Se puede usar ventajosamente como medicamento para el tratamiento de la cristalización patológica y los usos médicos específicos proporcionados en el presente documento.
El compuesto, forma farmacéutica, o composición de acuerdo con una cualquiera de las reivindicaciones anteriores para su uso en una dolencias relacionadas con la cristalización patológica del calcio, en la que dicha dolencia se selecciona entre calcificación vascular, arteriopatía coronaria, rigidización vascular, calcificación valvular, nefrocalcinosis, calcinosis cutis, piedras en el riñón, condrocalcinosis, osteoporosis, infarto de miocardio, mortalidad cardiovascular, progresión de la enfermedad renal crónica, fracaso de injertos de trasplante renal, y arteriopatía periférica, isquemia crítica de la extremidad, calcifilaxia, calcificación arterial general infantil y estenosis aórtica, ateroesclerosis, pseudogota, hiperoxaluria primaria y pseudoxantoma elástico.
Los compuestos divulgados en el presente documento pueden estar presentes en cualquier forma habitualmente utilizada en la tecnología farmacéutica. Las realizaciones particulares incluyen, aunque no de forma limitativa, la sal sódica, sal de magnesio, sal de potasio, sal de amonio, ácido libre, o una mezcla de las formas anteriores. El experto en la materia conoce otras sales farmacéuticamente aceptables y se pueden obtener, entre otros, de Haynes et al., J. Pharmaceutical Sci. 94, 20052111-2120, DOI 10.1002/jps.20441
Términos y definiciones
En el contexto de la presente memoria descriptiva, un polietilenglicol monodisperso es un (mdPEG) PEG que tiene una longitud de cadena y un peso molecular que son únicos y definidos. El mdPEG se suele generar mediante separación de la mezcla de polimerización por cromatografía.
En todas aquellas alternativas para la separación de características separables identificadas en el presente documento como "realizaciones", debe entenderse que dichas alternativas se pueden combinar libremente para formar realizaciones discretas de la invención divulgada en el presente documento.
La invención se ilustra además mediante los siguientes ejemplos y figuras, de las que se pueden extraer otras realizaciones y ventajas adicionales. Se entiende que estos ejemplos ilustran la invención, pero no limitan su alcance.
Breve descripción de las figuras
La Fig. 1 muestra el tiempo de maduración de la partícula de calciproteína (PCP) en suero humano según el ensayo descrito en Pasch et al. JASN 2012. El eje y indica el tiempo de transición semimáximo (T50) en minutos de las PCP primarias a las PCP secundarias. IP6: hexaquisfosfato de m/o-inositol (Biosynth); IS6: hexaquisfosfato de m/o-inositol (Sigma); IP2S4: 4,6-di-(O-fosfato)-m/o-inositol 1,2,3,5-tetra-O-sulfato; IT2S4: 4,6-di-(O-tiofosfato)-m/o-inositol 1,2,3,5-tetra-O-sulfato; IP5-PEG: pentaquisfosfato de 2-PEG(2000)-m/o-inositol. La Fig. 2 muestra los resultados de la determinación del tiempo de maduración de la partícula de calciproteína (PCP) en suero humano según un ensayo similar al de la Fig. 1 (con los compuestos experimentales añadidos a la mezcla de reacción 5 final).
Ejemplos
Tabla 1. Compuestos: los compuestos de las fórmulas IVf, IVg, IVh, Vd, Ve y Vf son parte de la presente invención.
Ensayo de calcificación
Los inventores realizaron un ensayo in vitro que mide la propensión a la calcificación del suero humano, y se ha validado clínicamente como un predictor de la mortalidad por todas las causas de pacientes de CKD y receptores de un trasplante renal (como se describe en Pasch, Journal of the American Society of Nephrology 23, 1744-1752, 2012). El experimento se llevó a cabo mezclando una solución de calcio, suero humano combinado, el compuesto experimental a la concentración final indicada y una solución de fosfato, y se midió el tiempo de transición desde partículas PCP primarias a secundarias a 37 °C usando un nefelómetro durante hasta 600 minutos.
Los datos de la Fig. 1 muestran que los compuestos IP2S4 e IT2S4 son más activos que IP6. Además, el compuesto 2-PEG-IP5 es bastante más activo que cualquier otro compuesto en este ensayo. Este resultado sugiere un papel fundamental del resto polimérico para prevenir la transición desde partículas PCP primarias a secundarias y para reducir la propensión de la calcificación del suero humano.
Los datos de la Fig. 2 muestran que los compuestos INS-2031 (III p), INS-3001 (IV f) e INS-3031 (IV g) son más activo que IP6. Los compuestos que tienen dos restos PEG (INS-3001, INS-3031) son más activos que los compuestos que tienen un solo resto PEG (INS-2031). Este resultado sugiere un papel fundamental del resto polimérico para prevenir la transición desde partículas PCP primarias a secundarias y para reducir la propensión de la calcificación del suero humano.
Síntesis de IT2S4 (VI a)
La síntesis siguió la secuencia representada gráficamente en el esquema siguiente:
PTSA: ácido p-toluenosulfónico; DMF: dimetilformamida; TBDMSCI: cloruro de terc-butildimetilsililo; TBSO: grupo protector de éter de terc-butildimetilsililo; DCM: diclorometano; S8: azufre elemental; pir.: piridina; TMSBr: bromuro de trimetilsililo; TFA: ácido trifluoroacético
Fosforilación
El ortoformiato de 2-tercbutildimetilsililoinositol se evaporó simultáneamente 3x con tolueno y se disolvió en diclorometano (DCM). 1H-tetrazol (4 eq.) seguido por fosforamidita (8 eq.) se añadieron a la reacción y se agitaron durante la noche. Piridina, seguido por escamas de azufre trituradas (20 eq.) se añadieron a la reacción y se agitó durante la noche. La mezcla de reacción en bruto resultante se diluyó con DCM y se lavó con NaHCO3 saturado, se secó con Na2 SO4, se filtró y se concentró. El producto se purificó mediante cromatografía ultrarrápida con DCM en tolueno.
RMN 1H (400 MHz; CDCI3): 87,35-7,29 (m, 4H), 7,15 (dd, J = 6,6, 2,1 Hz, 2H), 7,07-7,04 (m, 2H), 5,54 (d, J = 1,1 Hz, 1H), 5,45-5,41 (m, 2H), 5,30-4,97 (m, 8H), 4,51-4,49 (m, 1H), 4,33-4,32 (m, 2H), 4,27 (d, J= 1,3 Hz, 1H), 0,93 (s, 9H), 0,13 (s, 6H);
RMN 31P (162 MHz; CDCI3): 870,1;
Desprotección
Las siguientes condiciones de desprotección son análogas a la síntesis publicada en el Journal of the American Chemical Society (JACS 2005, 127, 5288).
El material de partida (50 mg) se trató con tiofenol (300 pl), m-cresol (300 pl), ácido trifluoroacético (1,8 ml). A continuación se añadió lentamente bromuro de trimetilsililo (TMSBr) (360 pl). La mezcla se agitó a temperatura ambiente durante 2 h. Y a continuación se evaporó dos veces en tolueno. El residuo en bruto se diluyó con DCM y aproximadamente 5 ml de agua y se neutralizó con NaOH 1 N. La capa acuosa (ligeramente turbia) se vertió directamente en un cartucho de SolEx C18 (Thermofisher, 1 g, 6 ml) y se eluyó con agua. En algunos casos, se
encontraron algunas impurezas aromáticas en el producto final, pero que precipitarían con el tiempo en agua y se podrían eliminar por filtración.
RMN 1H (500 MHz; D2O): 84,36 (q, J = 9,6 Hz, 2H), 4,02 (t, J = 2,7 Hz, 1H), 3,64 (dd, J = 9,7, 2,8 Hz, 2H), 3,50 (t, J= 9,3 Hz, 1H).
RMN 31P (203 MHz; D2 O): 845,7
Sulfatación
La reacción de sulfatación del tiofosfato se debe realizar cuidadosamente porque el tiofosfato se convierte en su caso en el fosfato en las condiciones de reacción. Por tanto, los inventores vigilaron la sulfatación cuidadosamente y ver si la reacción se había completado después de 30 min. y no se pudo observar descomposición durante ese tiempo. Por lo tanto, el complejo de trióxido de azufre-dimetilformamida (SO3-DMF) (12 eq.) se añadió a una suspensión de fosfato de inositol en DMF y la mezcla de reacción se agitó durante 35 min. La reacción se inactivó mediante la adición de NaOH 1 N, hasta aprox. pH 8 seguido por aprox. 3 ml de metanol (MeOH) para precipitar las sales. El sólido se purificó mediante una columna Sephadex lH-20, eluyendo con agua.
RMN 1H (500 MHz; D2O): 85,06 (s, 1H), 5,04-4,98 (m, 4H), 4,79-4,76 (m, 1H).
RMN 31P (203 MHz; D2 O): 844,5
Síntesis de IP2S4 (VI c)
La síntesis siguió la secuencia representada gráficamente en el esquema siguiente:
CN 0,45 M
PTSA: ácido p-toluenosulfónico; DMF: dimetilformamida; TBDMSCI: cloruro de terc-butildimetilsililo; TBDMSO: grupo protector de éter de terc-butildimetilsililo; DCM: diclorometano; ACN: acetonitrilo; mCPBA: ácido meta-cloroperbenzoico; TMSBr: bromuro de trimetilsililo; SO3-Et3 N: trióxido de azufre-trietilamina; TfOH: ácido trifluorometanosulfónico
Hidrólisis
4,6-Di-O-fosfato-mio-inositol (2)
2-0-Terc-butildimetilsilil-1,3,5-ortoformiato-4,6-(O-dixililenofosfo)-mio-inositol (1,00 g, 1,5 mmol, 1 eq.) en metanol/diclorometano (MeOH/DCM) 30 % (30 ml, 0,05 M) se trató con bromuro de trimetilsililo (TMSBr) (11 ml, 83,8 mmol, 56 eq.) y se agitó durante 5 h. La mezcla de reacción se desgasificó con N2 y e1HBr se neutralizó con una solución de NaOH 1 M. Después de 1-2 h, se concentró a sequedad. El producto bruto se lavó dos veces con acetona y dos veces con acetonitrilo (ACN) para dar 2 en forma de un sólido de color blanco (539 mg, rendimiento cuantitativo).
RMN 1H (400 MHz, MeOD): 8 (ppm) = 4,40 (q, 3JHH = 9,1 Hz, 2JHP = 9,1 Hz, 2 H, H-C4/6), 4,01 (t, J = 2,6 Hz, 1 H, H-C2), 3,63 (dd, J = 9,68, 2,76 Hz, 2 H, H-C1/3), 3,61 (t, J = 9,27 Hz, 1 H, H-C5);
RMN 31P (160 MHz, 1H desacoplado, MeOD): 8 (ppm) = 1,15 (P-C4/6); RMN 13C (150 MHz, MeOD): 8 (ppm) = 81,28 (d, 2JCP = 6,1 Hz, 2 C, C4/6), 74,12 (t, 3JCP = 3,8 Hz, 1 C, C5), 73,75 (s, 1 C, C2), 72,13 (d, 3JCP = 3,2 Hz, 2 C, C1/3); [m/z (ESI) (M+H)+ C6H15012P2 necesario 341,0033, encontrado 341,0037].
Sulfatación
1,2,3,5-Tetra-0-sulfonil-4,6-(di-O-fosfato)-m/o-inositol (1)
4,6-di-O-fosfato-m/o-inositol (30 mg, 90 pmol, 1 eq.) se evaporó simultáneamente con tolueno (3x) y se secó con alto vacío durante 1 h. Se añadió dimetilformamida seca (DMF) (1 ml, 0,09 M) y la mezcla de reacción se trató con SO3-Et3 N (197 mg, 109 pmol, 12 eq.) y TfOH (190 pl, 215 pmol, 24 eq.). Se calentó a 45 °C y se agitó durante la noche. La mezcla de reacción se neutralizó mediante la adición de Et3 N (0,15 ml, 12 eq.). Inmediatamente después de la neutralización, la mezcla se diluyó en agua nanopura (2 ml) y se cargó en una columna Sephadex G10. Se recogieron 14 fracciones de 3-4 ml y se introdujeron en el criodesecador durante la noche. Las fracciones 3-7 se combinaron para dar 1 en forma de un sólido de color blanco (46,31 pmol, 51 %).
RMN 1H (400 MHz, D2O): 8 (ppm) = 5,40 (a, 1 H, H-C2), 4,64-4,44 (m, 5 H, H-C1/3, H-C5, H-C4/6), 3,70 (s, 8 H, dioxano como patrón interno), 3,15 (q, J =7,3 Hz, 6 H, CH2-Et3N), 1,23 (t, J = 7,3 Hz, 9 H, CH3-Et3N).
Síntesis de PEG-IP5 (III o, Ill p, Ill q)
La síntesis siguió la secuencia representada gráficamente en el esquema siguiente:
DCM: diclorometano; DMF: dimetilformamida; SBTO: grupo protector de éter de terc-butildimetilsililo; TFA: ácido trifluoroacético; mCPBA: ácido meta-cloroperoxibenzoico
El ortoformiato de inositol se hizo reaccionar con 1 eq. de PEG tosilato para dar el ortoformiato de inositol 4-PEG o 6-PEG monoPEGilado. El grupo de protección del ortoformiato se eliminó usando ácido trifluoroacético y diclorometano. El compuesto se hizo reaccionar con fosforamidita, 1H-tetrazol, diclorometano y ácido meta-cloroperbenzoico. El compuesto resultante se hizo reaccionar con H2 , MeOH y PdO para dar 4-PEG-IP5 o 6-PEG-IP5, respectivamente.
Síntesis de 4.6-PEG-IP4 (IV f, IV g, IV h)
La síntesis siguió la secuencia representada gráficamente en el esquema siguiente:
DCM: diclorometano; DMF: dimetilformamida; SBTO: grupo protector de éter de terc-butildimetilsililo; TFA: ácido trifluoroacético; mCPBA: ácido meta-cloroperoxibenzoico
El ortoformiato de inositol se hizo reaccionar con PEG tosilato para dar el ortoformiato de inositol 4,6-PEG diPEGilado. El grupo de protección del ortoformiato se eliminó usando ácido trifluoroacético y diclorometano. El compuesto se hizo reaccionar con fosforamidita, 1H-tetrazol, diclorometano y ácido meta-cloroperbenzoico. El compuesto resultante se hizo reaccionar con H2 , MeOH y PdO para dar 4,6-PEG-IP4
Síntesis de 4-PEG-IP2S3 (III u, Ill v, Ill w)
La síntesis siguió la secuencia representada gráficamente en el esquema siguiente:
El ortoformiato de m/o-inositol conocido se puede monoalquilar con un tosilato de PEG comercial en presencia de una base fuerte tal como hidruro de sodio en DMF. A continuación, la mezcla de reacción se inactivó con agua y se extrajo con diclorometano. La capa orgánica se secó y se concentró a presión reducida. El producto se puede purificar mediante cromatografía en gel de sílice. La fosforilación de los grupos hidroxilo libres se realiza en condiciones normalizadas usando un reactivo de fosforamidita seguido por oxidación con ácido metacloroperbenzoico. El producto se puede purificar mediante cromatografía en fase normal o en fase invertida. Los grupos ortoéster y fosfato se desprotegen a continuación en paralelo usando un exceso de bromotrimetilsilano en una mezcla de metanol y diclorometano. El producto se puede purificar mediante precipitación o cromatografía de fase invertida. La sulfatación del grupo hidroxilo libre se lleva a cabo suspendiendo el producto en DMF seco y haciéndolo reaccionar con un exceso de complejo de trióxido de azufre-DMF. A continuación, la reacción se inactivó y se neutralizó. El producto final se puede precipitar de la mezcla de reacción mediante la adición de metanol, y purificarse mediante cromatografía de exclusión molecular o cromatografía de fase invertida.
Síntesis de PEG-IT5, 4.6-PEG-IT4 y PEG-IT2S3
La síntesis de PEG-IT5 (III r, III s, III t), 4,6-PEG-IT4 (IV i, IV j, IV k) y PEG-IT2S3 (III x, III y, III z) siguió las secuencias especificados para PEGIP5, 4,6-PEG-IP4 y PEG-IP2S3, salvo que la fosforilación se llevó a cabo mediante la adición de 1H tetrazol (4 eq.) seguido por fosforamidita (8 eq.) a la reacción y agitación durante la noche. Después, piridina, seguido por copos de azufre triturado (20 eq.) se añadieron a la reacción y se agitó durante toda la noche para completar la tiofosforilación.
Síntesis de 2,4,6-PEG-IP3 (V d, V e, V f)
La síntesis siguió la secuencia representada gráficamente en el esquema siguiente:
El ortoformiato de inositol se hizo reaccionar con PEG tosilato para dar el ortoformiato de inositol 2,4,6-PEG tripegilado. El grupo de protección del ortoformiato se eliminó usando ácido trifluoroacético y diclorometano. El compuesto se hizo reaccionar con fosforamidita, 1H-tetrazol, diclorometano y ácido meta-cloroperbenzoico. El compuesto resultante se hizo reaccionar con H2 , MeOH y PdO to 2,4,6-PEG-IP4.
Síntesis de 2,4,6-PEG-IT3 (V g, V h, V i)
La síntesis de 2,4,6-PEG-IT3 siguió lo descrito para 2,4,6-PEG-IP3 salvo que la fosforilación se llevó a cabo mediante adición de 1H tetrazol (4 eq.) seguido de fosforamidita (8 eq.) a la reacción, y se agitó durante la noche. Después, piridina, seguido por copos de azufre triturado (20 eq.) se añadieron a la reacción y se agitó durante toda la noche para completar la tiofosforilación.
Claims (3)
2. El compuesto de acuerdo con la reivindicación 1 en donde R1 es un polietilenglicol y tiene una masa molar de entre 100 g/mol y 3000 g/mol, especialmente de entre 100 g/mol y 2500 g/mol, más especialmente de aprox. 100 g/mol a 2 0 0 0 g/mol.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15199682 | 2015-12-11 | ||
| EP16164299 | 2016-04-07 | ||
| EP16173422 | 2016-06-07 | ||
| PCT/EP2016/080657 WO2017098047A1 (en) | 2015-12-11 | 2016-12-12 | Inositol derivatives for use in pathological crystallization |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2870521T3 true ES2870521T3 (es) | 2021-10-27 |
Family
ID=57629577
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16819297T Active ES2870521T3 (es) | 2015-12-11 | 2016-12-12 | Derivados de inositol para su uso en la cristalización patológica |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US10624909B2 (es) |
| EP (2) | EP3848053A1 (es) |
| JP (2) | JP6958866B2 (es) |
| KR (1) | KR102646016B1 (es) |
| CN (2) | CN113788855B (es) |
| AU (2) | AU2016368547B2 (es) |
| BR (1) | BR112018011732A2 (es) |
| CA (1) | CA3005933A1 (es) |
| DK (1) | DK3386548T3 (es) |
| EA (1) | EA037572B1 (es) |
| ES (1) | ES2870521T3 (es) |
| HR (1) | HRP20211116T1 (es) |
| HU (1) | HUE055165T2 (es) |
| IL (1) | IL259607B (es) |
| LT (1) | LT3386548T (es) |
| MX (1) | MX2018007130A (es) |
| PL (1) | PL3386548T3 (es) |
| SI (1) | SI3386548T1 (es) |
| WO (1) | WO2017098047A1 (es) |
| ZA (1) | ZA201803354B (es) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3848053A1 (en) * | 2015-12-11 | 2021-07-14 | Universität Bern | Inositol derivatives for use in pathological crystallization |
| WO2020058321A1 (en) * | 2018-09-18 | 2020-03-26 | Inositec Ag | Calcium oxalate crystallization inhibitors for renal disorders |
| KR102651652B1 (ko) * | 2018-10-11 | 2024-03-26 | 사니핏 테라퓨틱스 에스.에이. | 이소성 석회화의 치료를 위한 이노시톨 포스페이트 |
| KR20210148078A (ko) * | 2019-01-30 | 2021-12-07 | 사니핏 테라퓨틱스 에스.에이. | 조직 관류 증가에 사용하기 위한 이노시톨 포스페이트 화합물 |
| EP3818983A1 (en) | 2019-11-11 | 2021-05-12 | Sanifit Therapeutics S.A. | Inositol phosphate compounds for use in treating, inhibiting the progression, or preventing cardiovascular calcification |
| RU2731816C1 (ru) * | 2020-03-16 | 2020-09-08 | Федеральное государственное бюджетное научное учреждение "Иркутский научный центр хирургии и травматологии" | Способ диагностики кальциноза коронарных артерий у пациента с вторичным гиперпаратиреозом, получающего заместительную почечную терапию гемодиализом |
| US20230167140A1 (en) | 2020-04-30 | 2023-06-01 | Shanghai Senhui Medicine Co., Ltd. | Inositol derivative and use thereof |
| CA3199478A1 (en) | 2020-11-20 | 2022-05-27 | Vifor (International) Ag | Inositol hexakisphosphate analogues for treatment of calcification associated kidney diseases |
| EP4015494A1 (en) | 2020-12-15 | 2022-06-22 | Sanifit Therapeutics S.A. | Processes for the preparation of soluble salts of inositol phosphates |
| US20240100074A1 (en) | 2021-01-26 | 2024-03-28 | Vifor (International) Ag | Clinical Dosing Schedule of Inositol Phosphate Oligo(Ethylene Glycol) Compounds |
| EP4036097A1 (en) | 2021-01-29 | 2022-08-03 | Sanifit Therapeutics S.A. | Ip4-4,6 substituted derivative compounds |
| WO2024023360A1 (en) | 2022-07-29 | 2024-02-01 | Sanifit Therapeutics, S.A. | Ip5 substituted compounds |
| WO2024023359A1 (en) * | 2022-07-29 | 2024-02-01 | Sanifit Therapeutics, S.A. | Ip4-4,6 substituted derivative compounds for use in the treatment, inhibition of progression, and prevention of ectopic calcification |
| WO2024047037A1 (en) | 2022-08-30 | 2024-03-07 | ETH Zürich | Compositions for parenteral sustained release delivery of hydrophilic drugs |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SE8605063D0 (sv) * | 1986-11-26 | 1986-11-26 | Matti Siren | Derivatives of cyclohexane |
| EP2010477A4 (en) * | 2006-04-27 | 2012-05-30 | Intezyne Technologies Inc | POLY (ETHYLENE GLYCOL) CONTAINING CHEMICALLY DISPARATE ENDOGROUP |
| ES2288126B2 (es) * | 2006-06-01 | 2009-07-06 | Universitat De Les Illes Balears | Utilizacion de fitato como agente inhibidor de la disolucion de cristales de sales calcicas para la prevencion o tratamiento de la osteoporosis. |
| ES2332636B1 (es) * | 2008-08-06 | 2011-02-10 | Universitat De Les Illes Balears | Composicion de liquido de dialisis. |
| US8052931B2 (en) * | 2010-01-04 | 2011-11-08 | International Business Machines Corporation | Ultra low-power CMOS based bio-sensor circuit |
| CN105949234B (zh) * | 2011-09-29 | 2018-07-10 | 苏黎世联邦理工学院 | 用于治疗艰难梭菌感染的药物化合物 |
| US9364490B2 (en) * | 2013-03-15 | 2016-06-14 | Laboratoris Sanifit, S.L. | Use of derivatives containing C—O—P bonds in patients with kidney failure |
| EP3848053A1 (en) | 2015-12-11 | 2021-07-14 | Universität Bern | Inositol derivatives for use in pathological crystallization |
-
2016
- 2016-12-12 EP EP21158307.5A patent/EP3848053A1/en active Pending
- 2016-12-12 DK DK16819297.9T patent/DK3386548T3/da active
- 2016-12-12 SI SI201631268T patent/SI3386548T1/sl unknown
- 2016-12-12 PL PL16819297T patent/PL3386548T3/pl unknown
- 2016-12-12 KR KR1020187015987A patent/KR102646016B1/ko active IP Right Grant
- 2016-12-12 EA EA201891364A patent/EA037572B1/ru unknown
- 2016-12-12 LT LTEP16819297.9T patent/LT3386548T/lt unknown
- 2016-12-12 MX MX2018007130A patent/MX2018007130A/es unknown
- 2016-12-12 ES ES16819297T patent/ES2870521T3/es active Active
- 2016-12-12 CN CN202111074549.1A patent/CN113788855B/zh active Active
- 2016-12-12 CN CN201680071651.7A patent/CN108367080B/zh active Active
- 2016-12-12 HU HUE16819297A patent/HUE055165T2/hu unknown
- 2016-12-12 AU AU2016368547A patent/AU2016368547B2/en active Active
- 2016-12-12 EP EP16819297.9A patent/EP3386548B1/en active Active
- 2016-12-12 BR BR112018011732A patent/BR112018011732A2/pt not_active Application Discontinuation
- 2016-12-12 CA CA3005933A patent/CA3005933A1/en active Pending
- 2016-12-12 JP JP2018528966A patent/JP6958866B2/ja active Active
- 2016-12-12 US US16/060,980 patent/US10624909B2/en active Active
- 2016-12-12 WO PCT/EP2016/080657 patent/WO2017098047A1/en active Application Filing
-
2018
- 2018-05-21 ZA ZA2018/03354A patent/ZA201803354B/en unknown
- 2018-05-25 IL IL259607A patent/IL259607B/en unknown
-
2021
- 2021-07-12 HR HRP20211116TT patent/HRP20211116T1/hr unknown
- 2021-09-29 JP JP2021159270A patent/JP7300685B2/ja active Active
-
2022
- 2022-01-28 AU AU2022200542A patent/AU2022200542B2/en active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2870521T3 (es) | Derivados de inositol para su uso en la cristalización patológica | |
| US10046055B2 (en) | Bone targeted therapeutics and methods of making and using the same | |
| ES2595227T3 (es) | Composición de líquido de diálisis que comprende sustancias inhibidoras de la cristalización | |
| AU2016366503B2 (en) | 4,6-di-(O-thiophosphate)-inositol-1,2,3,5-tetra-O-sulfate for C. difficile infection | |
| US11028112B2 (en) | Inositol derivatives for use in pathological crystallization | |
| US4623742A (en) | Oxazaphosphorin-4-thio-alkanesulphonic acids, and neutral salts thereof | |
| EA016052B1 (ru) | N-α-(БЕНЗИЛОКСИКАРБОНИЛ)-L-γ-ГЛУТАМИЛ-3-[[2-[[БИС[БИС(2-ХЛОРЭТИЛ)АМИНО]ФОСФОНИЛ]ОКСИ]ЭТИЛ]СУЛЬФОНИЛ]-L-АЛАНИЛ-2(R)-ФЕНИЛГЛИЦИН ИЛИ ЕГО СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭТО СОЕДИНЕНИЕ, ПРИМЕНЕНИЕ ЭТОГО СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА И СПОСОБ ЛЕЧЕНИЯ РАКА С ПОМОЩЬЮ ЭТОГО СОЕДИНЕНИЯ | |
| WO2018100560A1 (en) | Coordination compounds and formulations, preparation methods and use thereof as antiphlogistic agents | |
| ES2337154T3 (es) | Bis-(n,n'-bis(2-haloetil)amino)fosforamidatos como agentes antitumorales. | |
| JP7164206B2 (ja) | ヌクレオシド代謝拮抗物質のイバンドロネート結合体 | |
| CA2550104A1 (en) | Use of a compound having two gold (i) atoms each covalently bonded to a carbon atom in a covalent link connecting the two gold (i) atoms for the treatment of cancer | |
| IL113246A (en) | Bisphosphonates and pharmaceutical compositions containing them | |
| CN101553282A (zh) | 2-{[2-(取代的氨基)乙基]磺酰基}乙基n,n,n’,n’-四(2-氯乙基)二氨基磷酸酯 | |
| JPH0373525B2 (es) |