ES2768978T3 - Derivado de pirazolilpirazol sustituido y uso del mismo como herbicida - Google Patents
Derivado de pirazolilpirazol sustituido y uso del mismo como herbicida Download PDFInfo
- Publication number
- ES2768978T3 ES2768978T3 ES16740286T ES16740286T ES2768978T3 ES 2768978 T3 ES2768978 T3 ES 2768978T3 ES 16740286 T ES16740286 T ES 16740286T ES 16740286 T ES16740286 T ES 16740286T ES 2768978 T3 ES2768978 T3 ES 2768978T3
- Authority
- ES
- Spain
- Prior art keywords
- weeds
- compound
- group
- formula
- atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000002363 herbicidal effect Effects 0.000 title claims description 34
- 239000004009 herbicide Substances 0.000 title claims description 23
- LVJQRFPFXVQMJC-UHFFFAOYSA-N 1-(1h-pyrazol-5-yl)pyrazole Chemical class C1=CC=NN1C1=CC=NN1 LVJQRFPFXVQMJC-UHFFFAOYSA-N 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 50
- 125000005843 halogen group Chemical group 0.000 claims abstract description 13
- 125000004093 cyano group Chemical group *C#N 0.000 claims abstract description 8
- 229910052801 chlorine Inorganic materials 0.000 claims abstract description 6
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims abstract description 6
- 125000001309 chloro group Chemical group Cl* 0.000 claims abstract description 5
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 5
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims abstract description 4
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims abstract description 3
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 claims abstract description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 3
- 238000000034 method Methods 0.000 claims description 8
- 239000000203 mixture Substances 0.000 claims description 8
- 238000009472 formulation Methods 0.000 claims description 3
- 241000196324 Embryophyta Species 0.000 description 67
- -1 phosphonomethyl Chemical group 0.000 description 50
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- 239000002689 soil Substances 0.000 description 13
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 12
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 11
- 240000007594 Oryza sativa Species 0.000 description 10
- 235000007164 Oryza sativa Nutrition 0.000 description 9
- 235000009566 rice Nutrition 0.000 description 9
- 235000014113 dietary fatty acids Nutrition 0.000 description 8
- 239000000194 fatty acid Substances 0.000 description 8
- 229930195729 fatty acid Natural products 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 230000000694 effects Effects 0.000 description 7
- 240000003176 Digitaria ciliaris Species 0.000 description 6
- 235000017898 Digitaria ciliaris Nutrition 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- 229910019142 PO4 Inorganic materials 0.000 description 6
- 239000011521 glass Substances 0.000 description 6
- 235000021317 phosphate Nutrition 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000003981 vehicle Substances 0.000 description 6
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- 238000011156 evaluation Methods 0.000 description 5
- 239000008187 granular material Substances 0.000 description 5
- 235000013311 vegetables Nutrition 0.000 description 5
- 108010000700 Acetolactate synthase Proteins 0.000 description 4
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 4
- 239000004492 dustable powder Substances 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 239000004094 surface-active agent Substances 0.000 description 4
- 239000004563 wettable powder Substances 0.000 description 4
- KFSUCTRGHQKXSV-UHFFFAOYSA-N 5-(1h-pyrazol-5-yl)-1h-pyrazole Chemical class N1N=CC=C1C1=CC=NN1 KFSUCTRGHQKXSV-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 244000237956 Amaranthus retroflexus Species 0.000 description 3
- 240000006122 Chenopodium album Species 0.000 description 3
- 235000009344 Chenopodium album Nutrition 0.000 description 3
- 240000004725 Echinochloa crus-galli var. crus-galli Species 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerol Natural products OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- 231100000674 Phytotoxicity Toxicity 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 240000006394 Sorghum bicolor Species 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 239000000440 bentonite Substances 0.000 description 3
- 235000012216 bentonite Nutrition 0.000 description 3
- 229910000278 bentonite Inorganic materials 0.000 description 3
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 239000012141 concentrate Substances 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 238000000227 grinding Methods 0.000 description 3
- 230000009036 growth inhibition Effects 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 238000010899 nucleation Methods 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 150000003217 pyrazoles Chemical class 0.000 description 3
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 239000002562 thickening agent Substances 0.000 description 3
- QNLZIZAQLLYXTC-UHFFFAOYSA-N 1,2-dimethylnaphthalene Chemical compound C1=CC=CC2=C(C)C(C)=CC=C21 QNLZIZAQLLYXTC-UHFFFAOYSA-N 0.000 description 2
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 2
- 229940100484 5-chloro-2-methyl-4-isothiazolin-3-one Drugs 0.000 description 2
- 241000219318 Amaranthus Species 0.000 description 2
- 235000013479 Amaranthus retroflexus Nutrition 0.000 description 2
- 241000208838 Asteraceae Species 0.000 description 2
- JDWQITFHZOBBFE-UHFFFAOYSA-N Benzofenap Chemical compound C=1C=C(Cl)C(C)=C(Cl)C=1C(=O)C=1C(C)=NN(C)C=1OCC(=O)C1=CC=C(C)C=C1 JDWQITFHZOBBFE-UHFFFAOYSA-N 0.000 description 2
- 241000168734 Bolboschoenus planiculmis Species 0.000 description 2
- 235000004977 Brassica sinapistrum Nutrition 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 241000315690 Echinochloa caudata Species 0.000 description 2
- 244000145224 Echinochloa crus galli var. formosensis Species 0.000 description 2
- 244000239348 Echinochloa crus galli var. praticola Species 0.000 description 2
- 244000058871 Echinochloa crus-galli Species 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 241001675558 Galium spurium Species 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 244000143149 Leptochloa chinensis Species 0.000 description 2
- 229920001732 Lignosulfonate Polymers 0.000 description 2
- 240000007038 Lindernia dubia Species 0.000 description 2
- 240000000178 Monochoria vaginalis Species 0.000 description 2
- 241001396199 Murdannia keisak Species 0.000 description 2
- 235000011999 Panicum crusgalli Nutrition 0.000 description 2
- 240000006928 Persicaria lapathifolia Species 0.000 description 2
- 235000006386 Polygonum aviculare Nutrition 0.000 description 2
- 244000292697 Polygonum aviculare Species 0.000 description 2
- 240000009132 Sagittaria sagittifolia Species 0.000 description 2
- 235000015909 Sagittaria sinensis Nutrition 0.000 description 2
- 240000004519 Sagittaria trifolia Species 0.000 description 2
- 241000202758 Scirpus Species 0.000 description 2
- 244000085269 Scirpus juncoides Species 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 235000007230 Sorghum bicolor Nutrition 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- 150000008051 alkyl sulfates Chemical class 0.000 description 2
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 2
- 238000007112 amidation reaction Methods 0.000 description 2
- 239000007798 antifreeze agent Substances 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- 239000004927 clay Substances 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 235000013399 edible fruits Nutrition 0.000 description 2
- 239000004495 emulsifiable concentrate Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 230000035784 germination Effects 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 238000003306 harvesting Methods 0.000 description 2
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- HJOVHMDZYOCNQW-UHFFFAOYSA-N isophorone Chemical compound CC1=CC(=O)CC(C)(C)C1 HJOVHMDZYOCNQW-UHFFFAOYSA-N 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 229920005646 polycarboxylate Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- ASRAWSBMDXVNLX-UHFFFAOYSA-N pyrazolynate Chemical compound C=1C=C(Cl)C=C(Cl)C=1C(=O)C=1C(C)=NN(C)C=1OS(=O)(=O)C1=CC=C(C)C=C1 ASRAWSBMDXVNLX-UHFFFAOYSA-N 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 239000004562 water dispersible granule Substances 0.000 description 2
- JWZZKOKVBUJMES-UHFFFAOYSA-N (+-)-Isoprenaline Chemical compound CC(C)NCC(O)C1=CC=C(O)C(O)=C1 JWZZKOKVBUJMES-UHFFFAOYSA-N 0.000 description 1
- GNPWYHFXSMINJQ-UHFFFAOYSA-N 1,2-dimethyl-3-(1-phenylethyl)benzene Chemical compound C=1C=CC(C)=C(C)C=1C(C)C1=CC=CC=C1 GNPWYHFXSMINJQ-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- NUGZBVBZIDWZAD-UHFFFAOYSA-N 1h-pyrazole-4-carbonitrile Chemical compound N#CC=1C=NNC=1 NUGZBVBZIDWZAD-UHFFFAOYSA-N 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- KUMKNGTWQNSAQW-UHFFFAOYSA-N 2-(2-fluorophenyl)acetyl chloride Chemical compound FC1=CC=CC=C1CC(Cl)=O KUMKNGTWQNSAQW-UHFFFAOYSA-N 0.000 description 1
- MQEQXPDLVJSQFJ-UHFFFAOYSA-N 2-(oxan-2-ylidene)acetonitrile Chemical compound N#CC=C1CCCCO1 MQEQXPDLVJSQFJ-UHFFFAOYSA-N 0.000 description 1
- HXDLWJWIAHWIKI-UHFFFAOYSA-N 2-hydroxyethyl acetate Chemical compound CC(=O)OCCO HXDLWJWIAHWIKI-UHFFFAOYSA-N 0.000 description 1
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 description 1
- GUUULVAMQJLDSY-UHFFFAOYSA-N 4,5-dihydro-1,2-thiazole Chemical class C1CC=NS1 GUUULVAMQJLDSY-UHFFFAOYSA-N 0.000 description 1
- IJALWSVNUBBQRA-UHFFFAOYSA-N 4-Isopropyl-3-methylphenol Chemical compound CC(C)C1=CC=C(O)C=C1C IJALWSVNUBBQRA-UHFFFAOYSA-N 0.000 description 1
- SVNNWKWHLOJLOK-UHFFFAOYSA-N 5-chloropentanoyl chloride Chemical compound ClCCCCC(Cl)=O SVNNWKWHLOJLOK-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 240000006995 Abutilon theophrasti Species 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- 235000004051 Aeschynomene indica Nutrition 0.000 description 1
- 244000144706 Aeschynomene indica Species 0.000 description 1
- 241000509537 Alisma canaliculatum Species 0.000 description 1
- 241000743985 Alopecurus Species 0.000 description 1
- 241001621841 Alopecurus myosuroides Species 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 241000219317 Amaranthaceae Species 0.000 description 1
- 241000482638 Amaranthus tuberculatus Species 0.000 description 1
- DHMQDGOQFOQNFH-UHFFFAOYSA-M Aminoacetate Chemical compound NCC([O-])=O DHMQDGOQFOQNFH-UHFFFAOYSA-M 0.000 description 1
- 241000341973 Ammannia Species 0.000 description 1
- 235000009066 Atriplex patula Nutrition 0.000 description 1
- 244000022181 Atriplex patula Species 0.000 description 1
- 241000209764 Avena fatua Species 0.000 description 1
- 235000007320 Avena fatua Nutrition 0.000 description 1
- 244000075850 Avena orientalis Species 0.000 description 1
- 235000007319 Avena orientalis Nutrition 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 235000016068 Berberis vulgaris Nutrition 0.000 description 1
- 241000335053 Beta vulgaris Species 0.000 description 1
- 235000000621 Bidens tripartita Nutrition 0.000 description 1
- 240000004082 Bidens tripartita Species 0.000 description 1
- 235000008427 Brassica arvensis Nutrition 0.000 description 1
- 235000014698 Brassica juncea var multisecta Nutrition 0.000 description 1
- 244000024671 Brassica kaber Species 0.000 description 1
- 235000006008 Brassica napus var napus Nutrition 0.000 description 1
- 235000006618 Brassica rapa subsp oleifera Nutrition 0.000 description 1
- 244000188595 Brassica sinapistrum Species 0.000 description 1
- 241000219193 Brassicaceae Species 0.000 description 1
- LVDKZNITIUWNER-UHFFFAOYSA-N Bronopol Chemical compound OCC(Br)(CO)[N+]([O-])=O LVDKZNITIUWNER-UHFFFAOYSA-N 0.000 description 1
- 229910014455 Ca-Cb Inorganic materials 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- 235000011305 Capsella bursa pastoris Nutrition 0.000 description 1
- 240000008867 Capsella bursa-pastoris Species 0.000 description 1
- 241000219321 Caryophyllaceae Species 0.000 description 1
- 235000000509 Chenopodium ambrosioides Nutrition 0.000 description 1
- 244000098897 Chenopodium botrys Species 0.000 description 1
- 235000005490 Chenopodium botrys Nutrition 0.000 description 1
- 235000009731 Chenopodium ficifolium Nutrition 0.000 description 1
- 244000035395 Chenopodium ficifolium Species 0.000 description 1
- WJLVQTJZDCGNJN-UHFFFAOYSA-N Chlorhexidine hydrochloride Chemical compound Cl.Cl.C=1C=C(Cl)C=CC=1NC(N)=NC(N)=NCCCCCCN=C(N)N=C(N)NC1=CC=C(Cl)C=C1 WJLVQTJZDCGNJN-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 244000192528 Chrysanthemum parthenium Species 0.000 description 1
- 244000037364 Cinnamomum aromaticum Species 0.000 description 1
- 235000014489 Cinnamomum aromaticum Nutrition 0.000 description 1
- 241000132536 Cirsium Species 0.000 description 1
- 101800004637 Communis Proteins 0.000 description 1
- 241000207894 Convolvulus arvensis Species 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 244000052363 Cynodon dactylon Species 0.000 description 1
- 235000016854 Cyperus rotundus Nutrition 0.000 description 1
- 244000075634 Cyperus rotundus Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 240000008853 Datura stramonium Species 0.000 description 1
- 239000004287 Dehydroacetic acid Substances 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 244000152970 Digitaria sanguinalis Species 0.000 description 1
- 235000010823 Digitaria sanguinalis Nutrition 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- 241000192043 Echinochloa Species 0.000 description 1
- 241000192040 Echinochloa phyllopogon Species 0.000 description 1
- 241000759118 Eleocharis kuroguwai Species 0.000 description 1
- 235000014716 Eleusine indica Nutrition 0.000 description 1
- 244000025670 Eleusine indica Species 0.000 description 1
- 241000508725 Elymus repens Species 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 241001599881 Euphorbia maculata Species 0.000 description 1
- 241001082360 Euphorbia supina Species 0.000 description 1
- 241000221017 Euphorbiaceae Species 0.000 description 1
- 241001289540 Fallopia convolvulus Species 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 241001508646 Galeopsis tetrahit Species 0.000 description 1
- 241000748465 Galinsoga Species 0.000 description 1
- 235000018914 Galinsoga parviflora Nutrition 0.000 description 1
- 244000214240 Galinsoga parviflora Species 0.000 description 1
- 241001077837 Galinsoga quadriradiata Species 0.000 description 1
- 235000014820 Galium aparine Nutrition 0.000 description 1
- 240000005702 Galium aparine Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 241000219146 Gossypium Species 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 241000208818 Helianthus Species 0.000 description 1
- 235000003222 Helianthus annuus Nutrition 0.000 description 1
- 240000005979 Hordeum vulgare Species 0.000 description 1
- 235000007340 Hordeum vulgare Nutrition 0.000 description 1
- 241000638402 Incana Species 0.000 description 1
- 241000207890 Ipomoea purpurea Species 0.000 description 1
- 239000005909 Kieselgur Substances 0.000 description 1
- 241000110847 Kochia Species 0.000 description 1
- 241000207923 Lamiaceae Species 0.000 description 1
- 235000009198 Lamium amplexicaule Nutrition 0.000 description 1
- 244000303225 Lamium amplexicaule Species 0.000 description 1
- 235000009193 Lamium purpureum Nutrition 0.000 description 1
- 240000006503 Lamium purpureum Species 0.000 description 1
- 241001136896 Leersia japonica Species 0.000 description 1
- 241001494499 Leersia oryzoides Species 0.000 description 1
- 240000004428 Lindernia procumbens Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 235000017945 Matricaria Nutrition 0.000 description 1
- 235000007232 Matricaria chamomilla Nutrition 0.000 description 1
- 241000169076 Monochoria korsakowii Species 0.000 description 1
- 241001442135 Myosotis arvensis Species 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- IGFHQQFPSIBGKE-UHFFFAOYSA-N Nonylphenol Natural products CCCCCCCCCC1=CC=C(O)C=C1 IGFHQQFPSIBGKE-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 241000173219 Paspalum distichum Species 0.000 description 1
- 241000881225 Persicaria Species 0.000 description 1
- 244000037751 Persicaria maculosa Species 0.000 description 1
- 241000013557 Plantaginaceae Species 0.000 description 1
- 244000292693 Poa annua Species 0.000 description 1
- 241000209049 Poa pratensis Species 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 235000004442 Polygonum persicaria Nutrition 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 235000001855 Portulaca oleracea Nutrition 0.000 description 1
- 244000234609 Portulaca oleracea Species 0.000 description 1
- 241000219304 Portulacaceae Species 0.000 description 1
- 241000877993 Potamogeton distinctus Species 0.000 description 1
- IHHMUBRVTJMLQO-UHFFFAOYSA-N Pyraclonil Chemical compound C#CCN(C)C1=C(C#N)C=NN1C1=NN(CCCC2)C2=C1Cl IHHMUBRVTJMLQO-UHFFFAOYSA-N 0.000 description 1
- 241000490453 Rorippa Species 0.000 description 1
- 244000155504 Rotala indica Species 0.000 description 1
- 241001153838 Rubia argyi Species 0.000 description 1
- 241001529553 Scoparia <angiosperm> Species 0.000 description 1
- 240000003705 Senecio vulgaris Species 0.000 description 1
- 241000533293 Sesbania emerus Species 0.000 description 1
- 244000010062 Setaria pumila Species 0.000 description 1
- 235000004250 Setaria pumila Nutrition 0.000 description 1
- 240000003461 Setaria viridis Species 0.000 description 1
- 235000002248 Setaria viridis Nutrition 0.000 description 1
- 240000006410 Sida spinosa Species 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- 239000004288 Sodium dehydroacetate Substances 0.000 description 1
- ABBQHOQBGMUPJH-UHFFFAOYSA-M Sodium salicylate Chemical compound [Na+].OC1=CC=CC=C1C([O-])=O ABBQHOQBGMUPJH-UHFFFAOYSA-M 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 241000207763 Solanum Species 0.000 description 1
- 235000002594 Solanum nigrum Nutrition 0.000 description 1
- 244000061457 Solanum nigrum Species 0.000 description 1
- 241000488874 Sonchus Species 0.000 description 1
- 244000113428 Sonchus oleraceus Species 0.000 description 1
- 235000006745 Sonchus oleraceus Nutrition 0.000 description 1
- 235000011684 Sorghum saccharatum Nutrition 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 240000006694 Stellaria media Species 0.000 description 1
- 235000008214 Thlaspi arvense Nutrition 0.000 description 1
- 240000008488 Thlaspi arvense Species 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 244000098338 Triticum aestivum Species 0.000 description 1
- 241000990144 Veronica persica Species 0.000 description 1
- 241000394440 Viola arvensis Species 0.000 description 1
- 241001302463 Viola mandshurica Species 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 229910021536 Zeolite Inorganic materials 0.000 description 1
- HJPOKQICBCJGHE-UHFFFAOYSA-J [C+4].[Cl-].[Cl-].[Cl-].[Cl-] Chemical compound [C+4].[Cl-].[Cl-].[Cl-].[Cl-] HJPOKQICBCJGHE-UHFFFAOYSA-J 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical class [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 239000003905 agrochemical Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 150000001346 alkyl aryl ethers Chemical class 0.000 description 1
- 150000008055 alkyl aryl sulfonates Chemical class 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- 229940045714 alkyl sulfonate alkylating agent Drugs 0.000 description 1
- 150000008052 alkyl sulfonates Chemical class 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 125000005228 aryl sulfonate group Chemical group 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000005998 bromoethyl group Chemical group 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 235000010216 calcium carbonate Nutrition 0.000 description 1
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 1
- 239000000920 calcium hydroxide Substances 0.000 description 1
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 1
- 235000011116 calcium hydroxide Nutrition 0.000 description 1
- RYAGRZNBULDMBW-UHFFFAOYSA-L calcium;3-(2-hydroxy-3-methoxyphenyl)-2-[2-methoxy-4-(3-sulfonatopropyl)phenoxy]propane-1-sulfonate Chemical compound [Ca+2].COC1=CC=CC(CC(CS([O-])(=O)=O)OC=2C(=CC(CCCS([O-])(=O)=O)=CC=2)OC)=C1O RYAGRZNBULDMBW-UHFFFAOYSA-L 0.000 description 1
- 239000004490 capsule suspension Substances 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 239000004359 castor oil Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 235000013339 cereals Nutrition 0.000 description 1
- 229960003333 chlorhexidine gluconate Drugs 0.000 description 1
- YZIYKJHYYHPJIB-UUPCJSQJSA-N chlorhexidine gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O.OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O.C1=CC(Cl)=CC=C1NC(=N)NC(=N)NCCCCCCNC(=N)NC(=N)NC1=CC=C(Cl)C=C1 YZIYKJHYYHPJIB-UUPCJSQJSA-N 0.000 description 1
- 229960004504 chlorhexidine hydrochloride Drugs 0.000 description 1
- 150000008280 chlorinated hydrocarbons Chemical class 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229920005556 chlorobutyl Polymers 0.000 description 1
- 125000002603 chloroethyl group Chemical group [H]C([*])([H])C([H])([H])Cl 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- DHNRXBZYEKSXIM-UHFFFAOYSA-N chloromethylisothiazolinone Chemical compound CN1SC(Cl)=CC1=O DHNRXBZYEKSXIM-UHFFFAOYSA-N 0.000 description 1
- 229910052570 clay Inorganic materials 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 238000012364 cultivation method Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 235000019258 dehydroacetic acid Nutrition 0.000 description 1
- JEQRBTDTEKWZBW-UHFFFAOYSA-N dehydroacetic acid Chemical compound CC(=O)C1=C(O)OC(C)=CC1=O JEQRBTDTEKWZBW-UHFFFAOYSA-N 0.000 description 1
- 229940061632 dehydroacetic acid Drugs 0.000 description 1
- PGRHXDWITVMQBC-UHFFFAOYSA-N dehydroacetic acid Natural products CC(=O)C1C(=O)OC(C)=CC1=O PGRHXDWITVMQBC-UHFFFAOYSA-N 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- GUJOJGAPFQRJSV-UHFFFAOYSA-N dialuminum;dioxosilane;oxygen(2-);hydrate Chemical compound O.[O-2].[O-2].[O-2].[Al+3].[Al+3].O=[Si]=O.O=[Si]=O.O=[Si]=O.O=[Si]=O GUJOJGAPFQRJSV-UHFFFAOYSA-N 0.000 description 1
- JBSLOWBPDRZSMB-FPLPWBNLSA-N dibutyl (z)-but-2-enedioate Chemical compound CCCCOC(=O)\C=C/C(=O)OCCCC JBSLOWBPDRZSMB-FPLPWBNLSA-N 0.000 description 1
- 125000006003 dichloroethyl group Chemical group 0.000 description 1
- 125000004772 dichloromethyl group Chemical group [H]C(Cl)(Cl)* 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Natural products C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 1
- YDEXUEFDPVHGHE-GGMCWBHBSA-L disodium;(2r)-3-(2-hydroxy-3-methoxyphenyl)-2-[2-methoxy-4-(3-sulfonatopropyl)phenoxy]propane-1-sulfonate Chemical compound [Na+].[Na+].COC1=CC=CC(C[C@H](CS([O-])(=O)=O)OC=2C(=CC(CCCS([O-])(=O)=O)=CC=2)OC)=C1O YDEXUEFDPVHGHE-GGMCWBHBSA-L 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- BJXYHBKEQFQVES-NWDGAFQWSA-N enpatoran Chemical compound N[C@H]1CN(C[C@H](C1)C(F)(F)F)C1=C2C=CC=NC2=C(C=C1)C#N BJXYHBKEQFQVES-NWDGAFQWSA-N 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 239000003337 fertilizer Substances 0.000 description 1
- 239000004503 fine granule Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 239000003673 groundwater Substances 0.000 description 1
- 235000010417 guar gum Nutrition 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- 229960002154 guar gum Drugs 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- ZSIAUFGUXNUGDI-UHFFFAOYSA-N hexan-1-ol Chemical compound CCCCCCO ZSIAUFGUXNUGDI-UHFFFAOYSA-N 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-O isopropylaminium Chemical compound CC(C)[NH3+] JJWLVOIRVHMVIS-UHFFFAOYSA-O 0.000 description 1
- NFIDBGJMFKNGGQ-UHFFFAOYSA-N isopropylmethylphenol Natural products CC(C)CC1=CC=CC=C1O NFIDBGJMFKNGGQ-UHFFFAOYSA-N 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 239000003350 kerosene Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 238000004898 kneading Methods 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- BEGLCMHJXHIJLR-UHFFFAOYSA-N methylisothiazolinone Chemical compound CN1SC=CC1=O BEGLCMHJXHIJLR-UHFFFAOYSA-N 0.000 description 1
- 239000004531 microgranule Substances 0.000 description 1
- ZLBGSRMUSVULIE-GSMJGMFJSA-N milbemycin A3 Chemical compound O1[C@H](C)[C@@H](C)CC[C@@]11O[C@H](C\C=C(C)\C[C@@H](C)\C=C\C=C/2[C@]3([C@H](C(=O)O4)C=C(C)[C@@H](O)[C@H]3OC\2)O)C[C@H]4C1 ZLBGSRMUSVULIE-GSMJGMFJSA-N 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 239000010446 mirabilite Substances 0.000 description 1
- 229910052901 montmorillonite Inorganic materials 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- PSZYNBSKGUBXEH-UHFFFAOYSA-N naphthalene-1-sulfonic acid Chemical compound C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-N 0.000 description 1
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical compound CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 239000004535 oil miscible liquid Substances 0.000 description 1
- 239000002420 orchard Substances 0.000 description 1
- 125000005702 oxyalkylene group Chemical group 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- 229960005323 phenoxyethanol Drugs 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 229920001495 poly(sodium acrylate) polymer Polymers 0.000 description 1
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 239000011970 polystyrene sulfonate Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- FKERUJTUOYLBKB-UHFFFAOYSA-N pyrazoxyfen Chemical compound C=1C=C(Cl)C=C(Cl)C=1C(=O)C=1C(C)=NN(C)C=1OCC(=O)C1=CC=CC=C1 FKERUJTUOYLBKB-UHFFFAOYSA-N 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000004576 sand Substances 0.000 description 1
- 125000005920 sec-butoxy group Chemical group 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 235000017550 sodium carbonate Nutrition 0.000 description 1
- 235000019259 sodium dehydroacetate Nutrition 0.000 description 1
- 229940079839 sodium dehydroacetate Drugs 0.000 description 1
- NNMHYFLPFNGQFZ-UHFFFAOYSA-M sodium polyacrylate Chemical compound [Na+].[O-]C(=O)C=C NNMHYFLPFNGQFZ-UHFFFAOYSA-M 0.000 description 1
- 229960004025 sodium salicylate Drugs 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- DSOWAKKSGYUMTF-GZOLSCHFSA-M sodium;(1e)-1-(6-methyl-2,4-dioxopyran-3-ylidene)ethanolate Chemical compound [Na+].C\C([O-])=C1/C(=O)OC(C)=CC1=O DSOWAKKSGYUMTF-GZOLSCHFSA-M 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 238000009331 sowing Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000002344 surface layer Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000004548 suspo-emulsion Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 239000010455 vermiculite Substances 0.000 description 1
- 229910052902 vermiculite Inorganic materials 0.000 description 1
- 235000019354 vermiculite Nutrition 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000004552 water soluble powder Substances 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
- 229940043810 zinc pyrithione Drugs 0.000 description 1
- PICXIOQBANWBIZ-UHFFFAOYSA-N zinc;1-oxidopyridine-2-thione Chemical compound [Zn+2].[O-]N1C=CC=CC1=S.[O-]N1C=CC=CC1=S PICXIOQBANWBIZ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N29/00—Biocides, pest repellants or attractants, or plant growth regulators containing halogenated hydrocarbons
- A01N29/04—Halogen directly attached to a carbocyclic ring system
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N33/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic nitrogen compounds
- A01N33/16—Biocides, pest repellants or attractants, or plant growth regulators containing organic nitrogen compounds containing nitrogen-to-oxygen bonds
- A01N33/18—Nitro compounds
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/56—1,2-Diazoles; Hydrogenated 1,2-diazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/90—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having two or more relevant hetero rings, condensed among themselves or with a common carbocyclic ring system
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/10—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof
- A01N47/18—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof containing a —O—CO—N< group, or a thio analogue thereof, directly attached to a heterocyclic or cycloaliphatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Dentistry (AREA)
- Pest Control & Pesticides (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Agronomy & Crop Science (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plant Pathology (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
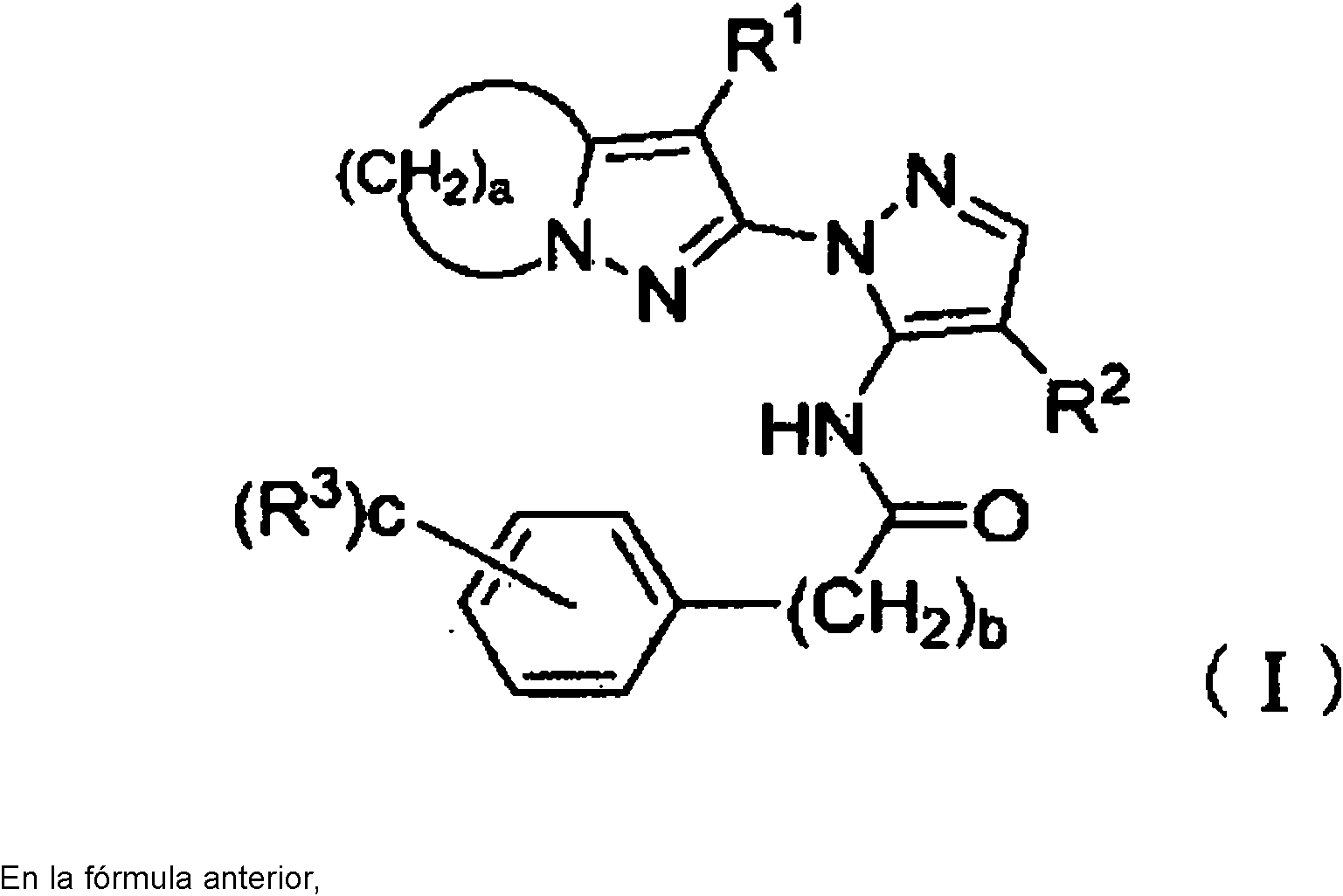
Un compuesto representado por la fórmula (I) siguiente:**Fórmula** en donde, R1 representa un átomo de cloro o átomo de bromo, R2 representa un grupo ciano o grupo nitro, R3 representa un átomo de hidrógeno, átomo de halógeno, grupo hidroxilo, grupo ciano, grupo nitro, grupo alquilo C1-C4 (que puede estar sustituido con uno o más átomos de halógeno dependiendo del caso), o grupo alcoxi C1- C4 (que puede estar sustituido con uno o más átomos de halógeno dependiendo del caso), a representa 3 a 5, b representa 1 a 3, y c representa 1 a 5, y cada R3 puede ser mutuamente igual o diferente cuando c es 2 o más.
Description
DESCRIPCIÓN
Derivado de pirazolilpirazol sustituido y uso del mismo como herbicida
Campo técnico
La presente invención se refiere a un derivado de pirazolilpirazol sustituido y al uso de dicho compuesto como herbicida.
Técnica anterior
Numerosos herbicidas han comenzado a utilizarse recientemente en el cultivo de las cosechas agrícolas, y han contribuido la reducción de la mano de obra para los agricultores y a una productividad mejorada de las cosechas agrícolas. Numerosos herbicidas se utilizan también prácticamente en el cultivo del arroz de campo y arroz en cáscara.
Sin embargo, existe una considerable diversidad en las especies de malezas, los periodos de germinación y crecimiento de cada especie de maleza no son uniformes, y el crecimiento de malezas de plantas perennes se extiende a lo largo de un periodo de tiempo prolongado. Por consiguiente, es extremadamente difícil controlar todas las malezas con una sola pulverización de herbicida.
Se ha demostrado que los herbicidas de un solo uso de precoz a medio plazo son eficaces para el arroz en cáscara por tratamiento durante la etapa de la segunda a la tercera hoja de las malezas de arrozal (término genérico para Echinochloa oryzicola, Echinochloa crus-galli var. crus-galli, Echinochloa crus-galli var. formosensis, Echinochloa crusgalli var. praticola y Echinochloa crus-galli var. caudata), y las malezas principales pueden ser controladas por un solo tratamiento (véase el Documento 1 No de Patente). En cambio, es extremadamente difícil controlar las malezas de arrozal que se han desarrollado hasta la etapa de 3,5 hojas o más con herbicidas de un solo uso en precoz a medio plazo en el uso práctico actual, y el control de las malezas de arrozal en la etapa de la tercera hoja y el control de las malezas de arrozal en la etapa de 3,5 hojas son completamente diferentes en la técnica.
Además, el mantenimiento de los efectos herbicidas (o actividades residuales) durante un periodo de tiempo largo es importante en términos de reducir la pulverización de productos químicos para la agricultura, ahorro de mano de obra y reducción de costes y está considerado como un área esencial de la eficiencia para los herbicidas de un solo uso en plazo corto a medio.
Adicionalmente, en los últimos años han comenzado a utilizarse en gran escala inhibidores de la acetolactato-sintasa (ALS), y las malezas que exhiben resistencia a los inhibidores de ALS se han convertido en un problema. Existen pocos herbicidas que demuestren eficacia adecuada contra los biotipos resistentes los inhibidores de ALS de las plantas de hoja perenne de Sagittaria trifolia y Sagittaria pygmeae. Adicionalmente, ejemplos de malezas perennes que han causado problemas en los últimos años incluyen Eleocharis kuroguwai, Scirpus planiculmis y Scirpus nipponicus, mientras que ejemplos de malezas de hojas anuales incluyen Aeschynomene indica, Leptochloa chinensis y Murdannia keisak, y existen pocos herbicidas que demuestren eficacia contra estas malezas difíciles de controlar.
Por otra parte, numerosos derivados de pirazol se utilizan prácticamente como herbicidas, y aunque se utilizan ampliamente derivados de pirazol tales como p-toluenosulfonato de 4-(2,4-diclorobenzoil)-1,3-dimetil-5-pirazolilo (nombre común: "Pirazolato"), 2-[4-(2,4-diclorobenzoil)-1,3-dimetilpirazol-5-iloxi]acetofenona (nombre común: "Pirazoxifeno") o 2-[4-(2,4-dicloro-m-toluoil)-1,3-dimetilpirazol-5-iloxi]-4'-metilacetofenona (nombre común: Benzofenap"), su intervalo de aplicación registrado para malezas de arrozal en Japón cuando se utilizan solos es hasta la etapa de 1,5 hojas, y aunque estos derivados de pirazol son eficaces contra una extensa gama de malezas, la eficacia de los mismos no es siempre adecuada contra las malezas de arrozal en las etapas foliares mayores.
Adicionalmente, aunque el Compuesto 73 del Ejemplo 4 descrito en el documento WO 94/08999 en la forma de 1-(3-cloro-4,5,6,7-tetrahidropirazolo[1,5-a]piridin-2-il)-5-[metil(prop-2-inil)amino]pirazol-4-carbonitrilo (nombre común: "Piraclonil") es eficaz contra una extensa gama de malezas, su eficacia contra las malezas de arrozal de etapas foliares mayores es inadecuada, y el intervalo de aplicación registrado en Japón, contra las malezas de arrozal cuando este herbicida se utiliza solo es hasta la etapa de 1,5 hojas.
Además, aunque WO 94/08999 describe también compuestos que demuestran efectos herbicidas por tratamiento de las malezas que crecen en tierra de labranza antes y después del crecimiento, puesto que no existe descripción alguna con relación a la etapa foliar, no puede decirse que estos compuestos tengan efectos adecuados contra malezas que se encuentran en etapas foliares mayores. Adicionalmente, aunque el N-(fosfonometil) glicinato de isopropil-amonio (nombre común: "Sal Glifosato de Isopropilamina"), por ejemplo, se utiliza ampliamente como herbicida que demuestra una gama amplia de efectos contra las malezas de tierra de labranza, en los últimos años se han presentado problemas con relación a su eficacia contra malezas resistentes.
Por otra parte, ha surgido recientemente una preocupación creciente en cuanto a la contaminación del agua freática y los ríos por los pesticidas. Como consecuencia, hay necesidad de desarrollo de herbicidas que minimicen los efectos sobre el medio ambiente, por ejemplo, por disminución del riesgo de escorrentía de ingredientes activos en localizaciones distintas de las localizaciones de su aplicación propuesta.
Lista de citas
Documento de la bibliografía de patentes
Documento de Patente 1: WO 94/08999
Documento de la bibliografía no de patentes
Documento No de Patente 1: "Suiden Zasso no Seitai to Sono Bojo - Suitosaku no Zasso to Josozai Kaisetsu (Ecology of Paddy Weeds and their Control - Explanation of Weeds of Rice Paddy Crops and Herbicide)", p. 159.
Compendio de la invención
Problema técnico
Un objeto de la presente invención es proporcionar un compuesto que tiene características excelentes como ingrediente de herbicidas, tal como tener un espectro herbicida amplio que incluye malezas que son resistentes a los herbicidas existentes, ser capaz de controlar las peores malezas de etapas foliares mayores que presentan problemas prácticos, y no causar fitotoxicidad a cosechas tales como el arroz en cáscara.
Solución al Problema
Como resultado de la realización de extensos estudios para conseguir elobjeto mencionado anteriormente, los autores de la presente invención encontraron que un derivado de pirazolilpirazol que tiene una estructura química específica exhibe especialmente un espectro herbicida amplio durante un periodo de tiempo largo, demuestra eficacia herbicida excelente contra las malezas peores de etapas foliares mayores, y presenta una seguridad adecuada con respecto a las cosechas cultivadas, conduciendo con ello a la culminación de la presente invención sobre la base de estos hallazgos. Así pues, la presente invención proporciona un derivado de pirazolilpirazol en la forma de un compuesto representado por la fórmula (I) siguiente:
[Fórmula química 1]
R1 representa un átomo de cloro o átomo de bromo,
R2 representa un grupo ciano o grupo nitro,
R3 representa un átomo de hidrógeno, átomo de halógeno, grupo hidroxilo, grupo ciano, grupo nitro, grupo alquilo C1-C4 (que puede estar sustituido con uno o más átomos de halógeno dependiendo del caso), o grupo alcoxi C1-C4 (que puede estar sustituido con uno o más átomos de halógeno dependiendo del caso),
a representa 3 a 5,
b representa 1 a 3, y
c representa 1 a 5, y cada R3 puede ser mutuamente igual o diferente cuando c es 2 o más.
Preferiblemente,
en la fórmula (I),
R1 representa un átomo de cloro,
R2 representa un grupo ciano,
a representa 4,
b representa 1, y
c representa 1.
En la presente descripción:
la marca "Ca-Cb" que va seguida por un sustituyente significa que el sustituyente tiene a a b átomos de carbono. En "átomos de halógeno" se incluyen átomos de flúor, cloro, bromo y yodo.
"Alquilo" como referente a un grupo per se o un resto de un grupo puede ser lineal o ramificado, y aunque no existen limitaciones en cuanto a ello, ejemplos del mismo incluyen metilo, etilo, n-o isopropilo, n-, iso, sec-o terc-butilo, y cada uno se selecciona dentro de un intervalo del número especificado de átomos de carbono del mismo.
Los "grupos alquilo" pueden ser grupos en los cuales al menos un átomo de hidrógeno contenido en estos grupos está sustituido con un átomo de halógeno, incluyendo los ejemplos en el caso en un grupo alquilo, pero sin limitación, grupos clorometilo, diclorometilo, trifluorometilo, cloroetilo, dicloroetilo, trifluoroetilo, tetrafluoroproplo, bromoetilo, bromopropilo y clorobutilo, y se seleccionan dentro de un intervalo de su número especificado de átomos de carbono respectivo.
Los "grupos alcoxi" hacen referencia a grupos alqui-O- en los cuales el resto alquilo es como se ha definido anteriormente, incluyendo ejemplos de los mismos grupos metoxi, etoxi, n-propoxi, isopropoxy, n-butoxi, iso-butoxi, sec-butoxi y terc-butoxi, y seleccionándose dentro de un intervalo de su número especificado de átomos de carbono respectivo.
En el caso en que el grupo o resto mencionado anteriormente está sustituido con una pluralidad de átomos de halógeno, dicho grupo puede estar sustituido con más de un átomo de halógenoque son iguales o diferentes.
En todas las fórmulas enumeradas a continuación, los sustituyentes y símbolostienen los mismos significados que se definen para la fórmula (I) a no ser que se definan específicamente de otro modo. El compuesto de la fórmula (I) proporcionada por la presente invención, en la cual R3 es un átomo de hidrógeno, puede sintetizarse fácilmente por una reacción de amidación a partir de un compuesto representado por la fórmula (Il).
[Fórmula química 2]
El compuesto de fórmula (II) puede sintetizarse a partir de tetrahidro-2H-piran-2-ilideno-acetonitrilo o cloruro de 5-clorovalerilo conforme a los métodos descritos en WO 93/10100 y WO 94/08999.
La reacción de amidación del compuesto de fórmula (II) per se puede llevarse a cabo con referencia a condiciones de reacción conocidas (véase, por ejemplo, WO 94/08999 y Tetrahedron Lett., 32, 4019 (1991)).
El compuesto de fórmula (I) proporcionado por la presente invención tiene eficacia herbicida excelente y es útil como herbicida como se deduce claramente por los resultados de los ensayos de actividad herbicida descritos en los Ejemplos de Ensayo 1 a 4 que se describirán más adelante.
El compuesto de fórmula (I) de la presente invención tiene actividad contra numerosos tipos de malezas de cosechas y malezas no de cosechas. Ejemplos de plantas cultivadas incluyen plantas gramíneas tales como arroz, trigo, cebada, maíz, avena o sorgo, cosechas de hoja ancha tales como soja, algodón, remolacha, girasol o colza, árboles frutales, hortalizas tales como hortalizas de fruto, hortalizas de raíz u hortalizas hojosas, y céspedes, y el compuesto de fórmula (I) puede utilizarse para el cultivo de los mismos.
El compuesto de la presente invención tiene eficacia herbicida contra las diversas malezas enumeradas más adelante que causan problemas en los campos de arroz en cualquiera de los métodos de tratamiento de tratamiento de suelos en estado irrigado o no irrigado, tratamiento de incorporación en suelo y tratamiento foliar. Aunque lo siguiente enumera ejemplos de las mismas, estas malezas no se limitan a los ejemplos siguientes.
Ejemplos de malezas de arrozal que pueden ser controladas por el compuesto de fórmula (I) de la presente invención incluyen malezas Alismatáceas tales como Alisma canaliculatum, Sagittaria trifolia or Sagittaria pigmaea, malezas Ciperáceas tales como Ciperus difformis, Ciperus serotinus, Scirpus juncoides, Eleocharis kuroguwai, Scirpus planiculmis o Scirpus nipponicus, malezas Escrofulariáceas tales como Lindernia procumbens, Lindernia dubia subsp. dubia o Lindernia dubia, malezas Pontederiáceas tales como Monochoria vaginalis o Monochoria korsakowii, malezas Potamogetonáceas tales como Potamogeton distinctus, malezas Litráceas tales como Rotala indica o Ammannia m ultiflora, malezas Asteráceas tales como Bidens tripartita o Bidens frondosa, malezas Leguminosas tales como Aeschinomene indica, malezas Commelináceas tales como Murdannia keisak, y malezas Gramíneas tales como Echinochloa orizicola, Echinochloa crus-galli var. crus-galli, Echinochloa crus-galli var. formosensis, Echinochloa crusgalli var. praticola, Echinochloa crus-galli var. caudata, Leptochloa chinensis, Leersia japonica, Paspalum distichum o Leersia oryzoides.
Adicionalmente, el compuesto de la presente invención tiene eficacia herbicida contra las diversas malezas enumeradas a continuación que causan problemas en terrenos de campo y terrenos no de cosecha en cualquiera de los métodos de tratamiento de tratamiento de suelos, tratamiento de incorporación al suelo y tratamiento foliar. Aunque lo siguiente enumera ejemplos de las mismas, estas malezas no se limitan a los ejemplos que siguen.
Ejemplos de las mismas incluyen malezas de hoja ancha, con inclusión de malezas Solanáceas tales como Solanum nigrum o Datura stramonium, malezas Malváceas tales como Abutilon avicennae, Sida spinosa o Convolvulus arvensis, malezas Convolvuláceas tales como Ipomoea purpurea, malezas Amarantáceas tales como Amaranthus lividus, Amaranthus retroflexus, Amaranthus palmen o Amaranthus tuberculatus, malezas Asteráceas tales como Xantium strumarium, Ambrosia artemisiilifolia, Galinsoga ciliata, Cirsium arvense, Senecio vulgaris, Stenactis annuus, Galinsoga parviflora, Sonchus arvensis, Sonchus oleraceus o Matricaria indora, malezas Brassicáceas tales como Rorippa indica, Sinapis arvensis, Capsella bursa-pastoris o Thlaspi arvense, malezas Poligonáceas tales como Persicaria longiseta, Fallopia convolvulus, Polygonum aviculare var. condensatum, Polygonum aviculare var. monospeliense, Polygonum persicaria, Persicaria lapathifolia var. incana o Persicaria lapathifolia var. lapathifolia, malezas Portulacáceas tales como Portulaca oleracea, malezas Quenopodiáceas tales como Chenopodium album, Chenopodium ficifolium, Kochia scoparia o Atriplex patula, malezas Cariofiláceas tales como Stellaria media, malezas Escrofulariáceas tales como Veronica persica, malezas Commelináceas tales como Commeiina communis, malezas Lamiáceas tales como Lamium amplexicaule, Lamium purpureum o Galeopsis tetrahit, malezas Euforbiáceas tales como Euphorbia supina o Euphorbia maculata, malezas Rubiáceas tales como Galium spurium, Galium spurium var. Echinospermon, Rubia argyi o Galium aparine, malezas Violáceas tales como Viola mandshurica o Viola arvensis, malezas Boragináceas tales como Myosotis arvensis, y malezas Leguminosas tales como Sesbania exaltata o Cassia obfusitoiia, y malezas Gramíneas tales como Sorghum bicolor, Panicum dichotomiflorum, Sorghum halepense, Echinochloa crus-galli var. crus-galli, Digitaria ciliaris, Avena fatua, Eleusine indica, Setaria viridis, Alopecurus aequaiis, Poa annua, Agropyron repens, Cynodon dactylon, Digitaria sanguinalis, Setaria pumila o Alopecurus myosuroides, y malezas Ciperáceas tales como Cyperus rotundus.
Además, el compuesto de la presente invención es capaz también de controlar una extensa gama de malezas que crecen en franjas segadas, tierra de barbecho, huertos, praderas, parcelas de césped de prado, tapas de líneas de ferrocarril, terreno vacante y suelo forestal, o en caminos agrícolas, calzadas otros terrenos no de cosechas.
Además, el compuesto de fórmula (I) de la presente invención no demuestra fitotoxicidad que llegue a ser un problema para el arroz en cáscara en el caso de cualquier método de cultivo tal como cultivo directo por siembra o cultivo de trasplante de arroz en cáscara.
El compuesto de fórmula (I) de la presente invención puede aplicarse antes o después de la germinación de la planta y puede mezclarse en suelo antes de la siembra.
Aunque la dosis del compuesto de fórmula (I) de la presente invención puede variar a lo largo de un amplio intervalo
correspondiente al tipo de compuesto, tipo de planta objetivo, ventana de aplicación, localización de la aplicación, propiedades de los efectos deseados y análogos, y como referencia general de los mismos, la dosis puede estar comprendida dentro del intervalo de aproximadamente 0,01 g a 100 g, y con preferencia aproximadamente 0,1 a 10 g, como cantidad de compuesto activo por área.
Aunque el compuesto de fórmula (I) de la presente invención puede utilizarse solo, normalmente se incorpora un adyuvante de fórmulación y análogos en el compuesto de fórmula (I) conforme a métodos ordinarios, y aunque no existen limitaciones en cuanto a él, el mismo se fórmula y utiliza preferiblemente en cualquier forma de fármaco arbitraria tal como un polvo espolvoreable, concentrado emulsionable, líquido miscible con aceite, agente solubilizante, suspo-emulsión, gránulo fino, pulverización de aerosol, polvo con menos deriva, fino de micro-gránulos, granos finos F, gránulos, polvo humectable, gránulos dispersables en agua, concentrado fluidificable, tipos de lanzamiento “throwin” (Jumbo), tabletas, pasta, emulsión en aceite, polvo soluble en agua, gránulos solubles en agua, suspensión de concentración soluble o suspensión de cápsulas.
No existe limitación alguna en cuanto a los adyuvantes de fórmulación susceptibles de ser utilizados para fórmulación, y ejemplos incluyen vehículos sólidos, vehículos líquidos, ligantes, espesantes, surfactantes, agentes anti-congelantes y conservantes.
Ejemplo de vehículos sólidos incluyen, pero no se limitan a, talco, bentonita, montmorillonita, arcilla, caolín, carbonato de calcio, carbonato de sodio, bicarbonato de sodio, mirabilita, zeolita, almidón, arcilla ácida, tierra de diatomeas, caoíta, vermiculita, cal apagada, polvo vegetal, alúmina, carbón activado, azúcares, vidrio hueco, arena de sílice, sulfato de amonio y urea.
Ejemplos de vehículos líquidos incluyen, pero no se limitan a, hidrocarburos (tales como queroseno o aceite mineral), hidrocarburos aromáticos (tales como tolueno, xileno, dimetil-naftaleno o fenil-xilil-etano), hidrocarburos clorados (tales como cloroformo o tetracloruro de carbono), éteres (tales como dioxano o tetrahidrofurano), cetonas (tales como acetona, ciclohexanona o isoforona), ésteres (tales como acetato de etilo, acetato de etilenglicol, o maleato de dibutilo), alcoholes (tales como metanol, n-hexanol o etilenglicol), disolventes polares (tales como N,N-dimetilformamida, dimetilsulfóxido o N-metilpirrolidona) y agua.
Ejemplos de ligantes y espesantes incluyen, pero no se limitan a, dextrina, sales de sodio de carboxi-metil-celulosa, compuestos polímeros basados en ácidos policarboxílicos, polivinilpirrolidona, poli (alcohol vinílico), lignin-sulfonato de sodio, lignin-sulfonato de calcio, poliacrilato de sodio, goma arábiga, alginato de sodio, manitol, sorbitol, materia mineral basada en bentonita, poli(ácido acrílico) y derivados de los mismos, caoíta y derivados de azúcares naturales (tales como goma de xantano o goma guar).
Ejemplos de surfactantes incluyen, pero no se limitan a, surfactantes aniónicos tales como sales de ácidos grasos, benzoatos, alquilsulfosuccinatos, dialquilsulfosuccinatos, policarboxilatos, sales éster de sulfatos de alquilo, sulfatos de alquilo, sulfatos de alquilarilo, sulfatos de alquil-diglicoléter, sales éster de sulfatos de alcohol, alquil-sulfonatos, alquilarilsulfonatos, aril-sulfonatos, lignin-sulfonatos, alquil-difeniléter-disulfonatos, sulfonatos de poliestireno, sales éster de alquil-fosfatos, fosfatos de alquilarilo, fosfatos de estiril-arilo, sales éster de polietileno-alquiléter-sulfatos, sulfatos de polioxietileno-alquilaril-éter, sales éster de polioxietileno-alquilaril-éter-sulfato, fosfatos de polioxietilenoalquiléter, sales éster de polioxietileno-alquilaril-fosfato o sales de condensados naftalen-sulfonato-formalina, y surfactantes no iónicos tales como ésteres de ácidos grasos de sorbitán, ésteres de ácidos grasos de glicerina, poliglicéridos de ácidos grasos, poliglicol-éteres de ácidos grasos con alcohol, acetilen-glicol, acetileno-alcohol, polímeros de bloques de oxialquileno, polioxietileno-alquiléteres, polioxietileno-alquilaril-éteres, polioxietilenglicolalquiléteres, polioxietileno-ésteres de ácidos grasos, ésteres de ácidos grasos de polioxietilen-sorbitán, ésteres de ácidos grasos de polioxietileno-glicerina, polioxietileno-aceite de ricino hidrogenado o ésteres polioxipropileno-ácidos grasos.
Ejemplos de agentes anticongelantes incluyen, pero no se limitan a, etilenglicol, dietilenglicol, propilenglicol y glicerina.
Ejemplos de conservantes incluyen, pero no se limitan a, ácido benzoico, benzoato de sodio, paraoxibenzoato de metilo, paraoxibenzoato de butilo, isopropil-metil-fenol, cloruro de benzalconio, hidrocloruro de clorhexidina, peróxido de hidrógeno acuoso, gluconato de clorhexidina, ácido salicílico, salicilato de sodio, cinc-piritiona, ácido sórbico, sorbato de potasio, ácido deshidroacético, deshidroacetato de sodio, fenoxietanol, derivados de isotiazolina tales como 5-cloro-2-metil-4-isotiazolin-3-ona o 2-metil-4-isotiazolin-3-ona, 2-bromo-2-nitropropano-1,3-diol y derivados de ácido salicílico.
Los vehículos sólidos, vehículos líquidos, ligantes, espesantes, surfactantes, agentes anticongelantes y conservantes mencionados anteriormente pueden utilizarse cada uno aisladamente o en una combinación adecuada de los mismos correspondiente para la finalidad de uso, etc.
Aunque la ratio incorporada del compuesto de fórmula (I) de la presente invención con respecto a la composición herbicida total de la presente invención puede aumentarse o disminuirse en caso necesario y no existe limitación particular alguna en cuanto a ello, la misma es normalmente alrededor de 0,01% en peso a 90% en peso, y por ejemplo, en el caso de encontrarse en la forma de un polvo espolvoreable o gránulos, aquélla es con preferencia aproximadamente 0,1% en peso a 50% en peso y con más preferencia aproximadamente 0,5% en peso a 10% en
peso, mientras que en el caso de encontrarse en forma de un concentrado emulsionable, polvo humectable o gránulos dispersables en agua, aquélla es con preferencia aproximadamente 0,1% en peso a 90% en peso y con más preferencia aproximadamente 0,5% en peso a 50% en peso.
Estas preparaciones pueden proporcionarse para uso en diversos tipos de aplicaciones por dilución a una concentración adecuada en caso necesario, seguido por pulverización o aplicación directa al follaje de las plantas, al suelo o a la superficie de un arrozal, etc.
Lo que sigue proporciona una explicación de la presente invención mediante ejemplos de la misma.
EJEMPLOS
Ejemplo 1: Método para la síntesis de metil-N-(1-(3-cloro-4,5,6,7-tetrahidropirazol[1,5-a]piridin-2-il)-4-cianopirazo-5-il)-2-(2-fluorofenil)-acetamida (Compuesto 1)
Se añadió acetonitrilo (5 ml) 5-amino-1-(3-cloro-4,5,6,7-tetrahidropirazol[1,5-a]piridin-2-il)pirazol-4-carbonitrilo (1,3 g) seguido por vertido lento gota a gota en cloruro de (2-fluorofenil)acetilo (1,0 g) y calentamiento a reflujo durante 8 horas. Después de la terminación de la reacción, se añadió agua a la solución de reacción seguido por extracción con acetato de etilo. Después de lavado con una solución acuosa de bicarbonato de sodio y secado con sulfato de sodio, se separó el disolvente por destilación a presión reducida. El producto bruto resultante se lavó con éter isopropílico para obtener el compuesto deseado (1,9 g).
El material de partida en forma del compuesto de fórmula (II) se sintetizó de acuerdo con WO 93/10.100 y WO 94/08999.
Los ejemplos enumerados en las tablas siguientes pueden sintetizarse del mismo modo que en los métodos mencionados anteriormente u obtenerse de igual manera que los métodos mencionados anteriormente.
[Tabla 1]
[Tabla 2]
Ejemplos de Preparación
1. Polvo Espolvoreable
Compuesto de fórmula (I) 10 partes en peso
Talco 90 partes en peso
Se obtiene un polvo espolvoreable por mezcla de los componentes anteriores y trituración fina con un molino de martillos.
2. Polvo Humectable
Compuesto de fórmula(I) 10 partes en peso
Polioxietileno alquilaril-éter sulfato 22,5 partes en peso
Carbono blanco 67,5 partes en peso
Se obtiene un polvo humectable por mezcla de los componentes anteriores y trituración fina de la mezcla con un molino de martillos.
3. Concentrado fluidificare
Compuesto de fórmula (I) 10 partes en peso
Polioxietileno alquil éter fosfato 10 partes en peso
Bentonita 5 partes en peso
Etilenglicol 5 partes en peso
Agua 70 partes en peso
Se obtiene un agente fluidificare por mezcla de los componentes anteriores y trituración utilizando un pulverizador húmedo.
4. Concentrado emulsiona
r
e
Compuesto de fórmula (I) 15 partes en peso
Nonilfenol etoxilado 10 partes en peso
Ciclohexanona 75 partes en peso
Se obtiene un concentrado emulsiona
r
e por mezcla de los componentes anteriores.
5. Gránulos
Compuesto de fórmula (I) 5 partes en peso
Lignin-sulfonato de calcio 3 partes en peso
Policarboxilato 3 partes en peso
Carbonato de calcio 89 partes en peso
Se mezclan los componentes anteriores seguido por adición de agua, amasado, extrusión y granulación. A continuación, se obtienen gránulos por secado seguido de clasificación por tamaños.
<Ejemplos de Ensayos Biológicos>
1. Ensayo de Actividad Herbicida en Arrozal
Se rellenó suelo de arrozal en un tiesto de 1/10000 áreas seguido por la adición de cantidades adecuadas de agua y fertilizante químico, amasado, siembra con Echinochloa crus-galli, Monochoria vaginalis y Scirpus juncoides y mantenimiento en estado irrigado con una profundidad de agua de 3 cm.
Polvos humectables del Compuesto Diana (I) indicado en la Tabla 1 preparados conforme a los ejemplos de preparación se diluyeron con una cantidad adecuada de agua, las plantas de arroz en la etapa de 2,0 hojas se trasplantaron durante la etapa de 3,5 hojas de Echinochloa crus-galli, y se trataron por vertido gota a gota del compuesto químico en la cantidad prescrita por 10 áreas utilizando una pipeta.
Después de tratamiento durante 30 días en un invernadero de vidrío a una temperatura atmosférica media de 30°C, se investigó la eficacia herbicida de los compuestos.
La evaluación de la eficacia herbicida se llevó a cabo por comparación del grado de inhibición del crecimiento (%) con un grupo sin tratar, mientras que la evaluación de la fitotoxicidad se llevó a cabo por comparación del grado de inhibición del crecimiento (%) con el estado de un grupo de erradicación completa, y se evaluaron en 11 niveles indicados a continuación.
0 (exponente): 0% hasta menos de 10% (grado de inhibición del crecimiento)
1: 10% hasta menos de 20%
2: 20% hasta menos de 30%
3: 30% hasta menos de 40%
4: 40% hasta menos de 50%
5 50% hasta menos de 60%
6: 60% hasta menos de 70%
7: 70% hasta menos de 80%
8: 80% hasta menos de 90%:
9: 90% hasta menos de 100%
10: 100%
Los resultados se muestran en la Tabla 2.
Agente de control 2.19 (descrito en WO 94/0899)
[Fórmula química 3]
[Tabla 4]
Tabla 2
2. Ensayo de Tratamiento de Tierra vegetal
Se rellenó suelo del campo en un tiesto de 1/6000 áreas seguido por siembra con Digitaria ciliaris, Chenopodium album y Amaranthus retroflexus y recubrimiento con suelo.
Polvos humectables de los compuestos de fórmula (I) enumerados en la Tabla 1 preparados conforme a los ejemplos de preparación se diluyeron con agua hasta la cantidad prescrita de compuesto químico y se pulverizaron uniformemente sobre cada capa de superficie de tierra vegetal utilizando 100 l de agua pulverizada por 10 áreas antes del crecimiento de las malezas subsiguiente a la siembra.
Después de tratamiento durante 30 días en un invernadero de vidrío a una temperatura atmosférica media de 3CPC, se investigó la eficacia herbicida de los compuestos.
La evaluación de la eficacia herbicida se llevó a cabo del mismo modo que en el Ejemplo de Ensayo 1 mencionado anteriormente.
Los resultados se presentan en la Tabla 3.
[Tabla 5]
Tabla 3
3. Ensayo de Tratamiento Foliar de las Malezas
Se rellenó tierra vegetal en un tiesto de 1/6000 áreas seguido por siembra con Digitaria ciliaris, Chenopodium album y Amaranthus retroflexus, recubrimiento con suelo, y cultivo en un invernadero de vidrio a una temperatura atmosférica media de 25°C.
Polvos humectables del Compuesto Diana (I) enumerados en la Tabla 1, preparados de acuerdo con los ejemplos de preparación se diluyeron con agua hasta la cantidad prescrita del compuesto químico y se pulverizaron uniformemente sobre las malezas utilizando 150 l de agua de pulverización por 10 áreas cuando Digitaria ciliaris había crecido hasta la etapa de 1,0 a 2,0 hojas.
Después de tratamiento durante 3 semanas en un invernadero de vidrio a una temperatura atmosférica media de 25°C, se investigó la eficacia herbicida de los compuestos.
La evaluación de la eficacia herbicida se llevó a cabo de la misma manera que en el Ejemplo de Ensayo 1 mencionado anteriormente.
Los resultados se muestran en la Tabla 4.
[Tabla 6]
Tabla 4
4. Ensayo de Tratamiento Foliar de las Malezas
Se rellenó tierra de campo en un tiesto de 1/4500 áreas seguido por siembra con Digitaria ciliaris y Galinsoga parviflora, recubrimiento con tierra vegetal y cultivo en un invernadero de vidrio a una temperatura atmosférica media de 25°C. Polvos humectables de Compuesto Diana (I) representados en la Tabla 1 preparados de acuerdo con los ejemplos de preparación se diluyeron con agua hasta la cantidad prescrita del compuesto químico y se pulverizaron uniformemente sobre las malezas utilizando 100 l de agua pulverizada por 10 áreas cuando Digitaria ciliaris había crecido hasta la etapa de 4,0 a 5,0 hojas (altura de la planta: 10 cm a 15 cm).
Después de tratamiento durante 20 días en un invernadero de vidrio a una temperatura atmosférica media de 25°C, se investigó la eficacia herbicida de los compuestos.
La evaluación de la eficacia herbicida se llevó a cabo de la misma manera que en el Ejemplo de Ensayo 1 mencionado anteriormente.
Los resultados se muestran en la Tabla 5.
[Tabla 6]
Tabla 5
Aplicabilidad industrial
Conforme a la presente invención, el compuesto para la fórmula (I) de la presente invención es útil como herbicida contra plantas dañinas dado que tiene una eficacia herbicida excelente contra plantas indeseables.
Claims (7)
1. Un compuesto representado por la fórmula (I) siguiente:
en donde,
R1 representa un átomo de cloro o átomo de bromo,
R2 representa un grupo ciano o grupo nitro,
R3 representa un átomo de hidrógeno, átomo de halógeno, grupo hidroxilo, grupo ciano, grupo nitro, grupo alquilo C1-C4 (que puede estar sustituido con uno o más átomos de halógeno dependiendo del caso), o grupo alcoxi C1-C4 (que puede estar sustituido con uno o más átomos de halógeno dependiendo del caso),
a representa 3 a 5,
b representa 1 a 3, y
c representa 1 a 5, y cada R3 puede ser mutuamente igual o diferente cuando c es 2 o más.
2. El compuesto conforme a la reivindicación 1, en donde
R1 representa un átomo de cloro,
R2 representa un grupo ciano,
a representa 4,
b representa 1, y
c representa 1.
3. Una composición herbicida que contiene una cantidad eficaz como herbicida de al menos un tipo del compuesto conforme a la reivindicación 1 o la reivindicación 2.
4. La composición herbicida conforme a la reivindicación 3, que contiene adicionalmente un adyuvante de fórmulación.
5. Un método para controlar plantas indeseables, que comprende el paso de aplicar una cantidad eficaz de al menos un tipo del compuesto conforme a la reivindicación 1 o la reivindicación 4, a una planta indeseable o a la localización de la vegetación indeseable.
6. Un uso del compuesto conforme a la reivindicación 1 o la reivindicación 2, o la composición herbicida conforme a la reivindicación 3 o la reivindicación 4, para controlar plantas indeseables.
7. El uso conforme a la reivindicación 6, en donde el compuesto conforme a la reivindicación 1 o la reivindicación 2 se utiliza para controlar plantas indeseables entre cosechas agrícolas útiles.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015011041 | 2015-01-23 | ||
| PCT/JP2016/051832 WO2016117679A1 (ja) | 2015-01-23 | 2016-01-22 | 置換ピラゾリルピラゾール誘導体とその除草剤としての使用 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2768978T3 true ES2768978T3 (es) | 2020-06-24 |
Family
ID=56417209
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16740286T Active ES2768978T3 (es) | 2015-01-23 | 2016-01-22 | Derivado de pirazolilpirazol sustituido y uso del mismo como herbicida |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US10165776B2 (es) |
| EP (1) | EP3248976B1 (es) |
| JP (1) | JP6640118B2 (es) |
| KR (1) | KR20170103790A (es) |
| CN (1) | CN107108622B (es) |
| AR (1) | AR103472A1 (es) |
| AU (1) | AU2016210168B2 (es) |
| BR (1) | BR112017011588B1 (es) |
| CA (1) | CA2971573A1 (es) |
| DK (1) | DK3248976T3 (es) |
| ES (1) | ES2768978T3 (es) |
| HU (1) | HUE048323T2 (es) |
| LT (1) | LT3248976T (es) |
| PL (1) | PL3248976T3 (es) |
| RS (1) | RS59839B1 (es) |
| RU (1) | RU2693461C2 (es) |
| TW (1) | TWI695835B (es) |
| UA (1) | UA119586C2 (es) |
| WO (1) | WO2016117679A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6783575B2 (ja) * | 2016-07-27 | 2020-11-11 | 協友アグリ株式会社 | 除草剤組成物 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5262382A (en) | 1991-10-03 | 1993-11-16 | Fmc Corporation | Herbicidal 1-pyridylpyrazole compounds |
| US5167691A (en) * | 1991-10-03 | 1992-12-01 | Fmc Corporation | Herbicidal 5-amino-1-phenyl pyrazole compounds |
| DK0663913T3 (da) * | 1992-10-12 | 1999-05-03 | Hoechst Schering Agrevo Gmbh | Nye substituerede pyrazolderivater, fremgangsmåder til deres fremstilling samt deres anvendelse som herbicider |
| DE19623892A1 (de) * | 1996-06-06 | 1997-12-11 | Hoechst Schering Agrevo Gmbh | Substituierte Pyrazolyl-pyrazolderivate |
| DE19630555A1 (de) * | 1996-07-18 | 1998-01-22 | Hoechst Schering Agrevo Gmbh | Substituierte Pyrazolyl-pyrazolderivate |
| AR097245A1 (es) | 2013-08-09 | 2016-03-02 | Kyoyu Agri Co Ltd | Derivado de pirazolilpirazol sustituido y su empleo como herbicida |
-
2016
- 2016-01-21 TW TW105101805A patent/TWI695835B/zh active
- 2016-01-21 AR ARP160100156A patent/AR103472A1/es active IP Right Grant
- 2016-01-22 AU AU2016210168A patent/AU2016210168B2/en active Active
- 2016-01-22 CA CA2971573A patent/CA2971573A1/en not_active Abandoned
- 2016-01-22 WO PCT/JP2016/051832 patent/WO2016117679A1/ja active Application Filing
- 2016-01-22 CN CN201680006853.3A patent/CN107108622B/zh active Active
- 2016-01-22 RU RU2017128813A patent/RU2693461C2/ru active
- 2016-01-22 DK DK16740286.6T patent/DK3248976T3/da active
- 2016-01-22 HU HUE16740286A patent/HUE048323T2/hu unknown
- 2016-01-22 US US15/541,117 patent/US10165776B2/en active Active
- 2016-01-22 LT LTEP16740286.6T patent/LT3248976T/lt unknown
- 2016-01-22 KR KR1020177018053A patent/KR20170103790A/ko not_active Application Discontinuation
- 2016-01-22 BR BR112017011588-3A patent/BR112017011588B1/pt active IP Right Grant
- 2016-01-22 ES ES16740286T patent/ES2768978T3/es active Active
- 2016-01-22 JP JP2016570719A patent/JP6640118B2/ja active Active
- 2016-01-22 UA UAA201708034A patent/UA119586C2/uk unknown
- 2016-01-22 RS RS20200060A patent/RS59839B1/sr unknown
- 2016-01-22 PL PL16740286T patent/PL3248976T3/pl unknown
- 2016-01-22 EP EP16740286.6A patent/EP3248976B1/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| RS59839B1 (sr) | 2020-02-28 |
| BR112017011588A2 (pt) | 2018-03-06 |
| HUE048323T2 (hu) | 2020-07-28 |
| CA2971573A1 (en) | 2016-07-28 |
| TWI695835B (zh) | 2020-06-11 |
| AU2016210168A1 (en) | 2017-06-29 |
| AU2016210168B2 (en) | 2019-10-31 |
| AR103472A1 (es) | 2017-05-10 |
| CN107108622B (zh) | 2019-12-27 |
| PL3248976T3 (pl) | 2020-05-18 |
| WO2016117679A1 (ja) | 2016-07-28 |
| US20170367335A1 (en) | 2017-12-28 |
| UA119586C2 (uk) | 2019-07-10 |
| RU2017128813A (ru) | 2019-02-25 |
| JPWO2016117679A1 (ja) | 2017-11-09 |
| TW201630911A (zh) | 2016-09-01 |
| EP3248976B1 (en) | 2019-11-06 |
| EP3248976A4 (en) | 2018-07-18 |
| KR20170103790A (ko) | 2017-09-13 |
| US10165776B2 (en) | 2019-01-01 |
| LT3248976T (lt) | 2020-02-10 |
| CN107108622A (zh) | 2017-08-29 |
| BR112017011588B1 (pt) | 2022-01-18 |
| DK3248976T3 (da) | 2020-02-10 |
| RU2693461C2 (ru) | 2019-07-03 |
| RU2017128813A3 (es) | 2019-02-28 |
| JP6640118B2 (ja) | 2020-02-05 |
| EP3248976A1 (en) | 2017-11-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2692793C2 (ru) | Производное замещенного пиразолилпиразола и его применение в качестве гербицида | |
| RU2692790C2 (ru) | Производное замещенного пиразолилпиразола и его применение в качестве гербицида | |
| RU2692792C2 (ru) | Производное замещенного пиразолилпиразола и его применение в качестве гербицида | |
| AU2016210159B2 (en) | Substituted pyrazolyl-pyrazole derivative and use of same as herbicide | |
| ES2768978T3 (es) | Derivado de pirazolilpirazol sustituido y uso del mismo como herbicida | |
| RU2702162C2 (ru) | Производное замещенного пиразолилпиразола и его применение в качестве гербицида | |
| RU2692791C2 (ru) | Производное замещенного пиразолилпиразола и его применение в качестве гербицида | |
| CA2918154A1 (en) | Substituted pyrazolylpyrazole derivative and use of same as herbicide |