-
Gebiet der
Erfindung
-
Die
vorliegende Erfindung bezieht sich auf einen Transkriptionsmediator
des nuclearen Rezeptors (NR). Spezifischer werden Nucleinsäuremoleküle bereitgestellt,
die den transkriptionalen intermediären Faktor-2 (TIF2) codieren.
Rekombinante Verfahren zur Herstellung von TIF2-Polypeptiden werden
auch bereitgestellt, ebenso werden Durchmusterungsverfahren zum
Identifizieren von Agonisten und Antagonisten der Aktivierungsfunktion
AF-2 des nuclearen Rezeptors sowie TIF2-Antikörper bereitgestellt. Auch werden
Durchmusterungsverfahren zum Identifizieren von Agonisten und Antagonisten
der Aktivität
der TIF2-AD1-Aktivierungsdomäne,
sowie Durchmusterungsverfahren zum Identifizieren von Agonisten
und Antagonisten der Aktivität
der TIF2-AD2-Aktivierungsdomänen
bereitgestellt.
-
Hintergrund
der Erfindung
-
Aktivatoren,
die den Transkriptionsstart durch RNA-Polymerase B (II) verbessern,
sind mindestens aus zwei funktionellen Domänen zusammengesetzt: eine DNA-bindende
Domäne
und eine Aktivierungsdomäne
(M. Ptashne, Nature 335: 683-689 (1988); P.J. Mitchell et al., Science
245: 371-378 (1989)). Diese zwei Domänen sind allgemein trennbare
funktionelle Einheiten und jede kann sogar mit der komplementären Region
eines nicht verwandten Aktivators ausgetauscht werden und dabei
funktionelle chimäre
Aktivatoren erzeugen (S. Green et al., Nature 325: 75-78 (1987)).
-
Eine
Anzahl von Struktur-Funktions-Analysen von eukaryontischen transkriptionalen
wurde unter anfänglicher
Fokussierung auf die Hefeproteine GAL4 und GCN4 und auf Mitglieder
der nuclearer Rezeptor-Familie durchgeführt. Die GAL4- und GCN4-Proteine
aktivieren die Transkription durch Binden an eine spezifische Stromaufwärts-Aktivierungssequenz,
die viele der Merkmale von höheren
eukaryontischen Verstärkerelementen
hat (K. Struhl, Cell 49:295-297 (1987)). Der Herpes-simplex-Aktivator
VP16 repräsentiert
einen anderen Aktivatortyp, der die Transkription eher durch Binden
an den DNA-gebundenen Oktamer-Transkriptionsfaktor
als durch Binden an die DNA direkt aktiviert (T. Gerster et al.,
Proc. Natl. Acad. Sci. USA 85:6347-6351 (1988)).
-
Die
Familie der nuclearen Rezeptoren, welche die Rezeptoren für Steroidhormone,
Thyroidhormone, Vitamin D und dem Vitamin A-Derivat Retinolsäure beinhaltet,
sind auch transkriptionale Verstärkerfaktoren, die
DNA in der Anwesenheit ihres verwandten Liganden direkt binden durch
Erkennung der spezifischen Verstärkerelemente,
d.h. Hormon- oder Liganden-responsive Elemente (R.M. Evans, Cell
240:889-895 (1988)). Diese verwandten Liganden neigen dazu, kleine,
hydrophobe Moleküle
zu sein, die Steroidhormone wie Östrogen
und Progesteron, Thyroidhormon, Vitamin D und verschiedene Retinoide
beinhalten (S. Halachmi et al., Science 264:1455-1458 (1994); Gronemeyer,
H. und Laudet, V., Protein Profile 2:1173-1308 (1995)).
-
Trotz
ihrer kleinen Größe und offensichtlich
einfachen Struktur sind jedoch die mit NRs assoziierten verwandten
Liganden bekannt, einen weiten Bereich von physiologischen Reaktionen
auszulösen.
Nebennierenhormone zum Beispiel, wie Cortisol und Aldosteron, beeinflussen
weitgehend die Körperhomeostase
unter Kontrolle des Glycogen- und Mineralstoffwechsels, haben ausgedehnte
Wirkungen auf das Immun- und das Nervensystem und beeinflussen das
Wachstum und die Differenzierung von gezüchteten Zellen. Die Geschlechtshormone
(Progesteron, Östrogen
und Testosteron) treiben die Entwicklung und die Ermittlung des embryonalen
reproduktiven Systems an, machen das Gehirn bei der Geburt männlich/weiblich,
kontrollieren Fortpflanzung und zugehöriges Verhalten bei Erwachsenen
und sind verantwortlich für
die Entwicklung von sekundären
Geschlechtsmerkmalen. Vitamin D ist notwendig für angemessene Knochenentwicklung
und spielt eine entscheidende Rolle beim Calciumstoffwechsel und
bei der Knochendifferenzierung. Bezeichnenderweise wurde eine abweichende Produktion
dieser Hormone mit einem breiten Spektrum klinischer Erkrankung
assoziiert, einschließlich
Krebs und ähnliche
pathologische Bedingungen.
-
Alle
NRs stellen eine. modulare Struktur dar, mit fünf bis sechs verschiedenen
Regionen, die als A-F bezeichnet werden. Die N-terminale A/B-Region
enthält
die Aktivierungsfunktion AF-1, die die Transkription wesentlich
aktivieren kann. Region C umfasst die DNA-bindende Domäne (DBD),
die verwandte cis-acting-Elemente erkennt. Region E enthält die Liganden-bindende
Domäne
(LBD), eine Dimerisierungsoberfläche
und die Liganden-abhängige
transkriptionale Aktivierungsfunktion AF-2 (besprochen in Mangelsdorft,
D.J. et al., Cell 83:835-839 (1995a); Mangelsdorft & Evans, Cell 83:841-850
(1995b); Beato, M. et al., Cell 83:851-857 (1995); Gronemeyer & Laudet, „Transcriptional
Factors 3: Nuclear Receptors",
in Protein Profile, Bd. 2, Academic Press (1995); Kastner, P. et
al., EMBO J. 11:629-642 (1992); Chambon, P., FASEB J 10:940-954
(1996)).
-
Mehrere
Klassen von Domänen
bei Aktivatoren sind in der Lage, die Transkriptionsaktivierung
zu vermitteln. Die Hefeaktivatoren GAL4 und GCN4 und der Herpes
simplex VP16 enthalten alle Aktivierungsdomänen, die aus Strecken saurer
Aminosäuren
zusammengesetzt sind, die durch Bildung amphipathischer α-Helices wirken können (I.A.
Hope et al., Cell 46:885-894 (1986); J. Ma et al., Cell 48:847-853
(1987); E. Giniger et al., Nature 330:670-672 (1987); S.J. Triezenberg
et al., Genes Dev. 2:718-729 (1988)). Die Aktivierungsfunktionen
von menschlichen Sp1- und CTF/NF1-Proteinen enthalten jeweils Glutamin-
und Prolin-reiche Bereiche (A.J. Courey et al., Cell 55:887-898
(1988); N. Mermod et al., Cell 58:741-753 (1989)). Studien mit Steroidhormonrezeptoren
zeigten, dass sowohl die N-terminale A/B-Domäne als auch die C-terminale
Hormon-bindende Domäne
(HBD) Transkriptionsaktivierungsfunktionen (AFs) enthalten (M.T.
Bocquel et al., Nucl. Acids. Res., 17:2581-2595 (1989); L. Tora
et al., Cell 59:477-487 (1989)). Die AFs des menschlichen Östrogen-Rezeptors (hER)
enthalten keine Strecken von sauren Aminosäuren (S. Halachmi et al., Science
264:1455-1458 (1994)). Umgekehrt enthält jedoch der menschliche Glucocorticoid-Rezeptor
(hGR) zwei Aktivierungsfunktionen, τ-1 (in der A/B-Domäne gelegen)
und τ-2
(in der N-terminalen Region der HBD gelegen), von denen beide sauer
sind (S.M. Hollenberg et al., Cell 55:899-906 (1988)).
-
Aus
den Ergebnissen der Studien der Transkriptionsinterferenz/"Squelching" zwischen nuclearen
Rezeptoren und der homo- und heterosynergistische Stimulation des
Transkriptionsstarts aus minimalen Promotoren durch die in hER (AF-1
und AF-2) anwesenden
Aktivierungsfunktionen und dem sauren Aktivator VP16 wurde vorgeschlagen,
dass AFs die Transkription durch Interaktion mit verschiedenen Komponenten
des basischen Startkomplexes aktivieren können (Bocquel et al., Nucl.
Acids. Res. 17:2581-2595 (1989); Meyer et al., Cell 57:433-442 (1989);
L. Tora et al., Cell 59:477-487 (1989). Studien der Transkriptionsinterferenz/"Squelching"-Eigenschaften von AADs, hER-AF-1 und
hER-AF-2 zeigten jedoch, dass sowohl hER-AF-1 als auch -AF-2 saure
Aktivatoren wie VP16 unterdrücken
können,
aber dass die Umkehrung nicht wahr war, d.h. AADs unterdrücken nicht
hER-AF-1 oder – AF-2.
Außerdem
unterdrücken
sich hER-AF-1 und -AF-2, die deutlich durch ihre synergistischen
Eigenschaften unterschieden werden, dennoch gegenseitig (D. Tasset
et al., Cell 62:1177-1187 (1990)).
-
Diese
Ergebnisse deuten darauf hin, dass eine Abfolge von transkriptionalen
intermediären
Faktoren (TIFs) existiert, eingeschoben zwischen Verstärkerfaktoren
und den basischen Transkriptionsfaktoren. Zum Beispiel wurde vorgeschlagen,
dass AF-1 und AF-2 mit der Folge der TIFs an funktionell equivalenten
Punkten Kontakt aufnehmen, während
geglaubt wird, dass AADs an einem früheren Punkt in der Serie interagieren
(D. Tasset et al., Cell 62:1177-1187 (1990)).
-
Mehrere
vermeintliche Coaktivator-TIFs für
NR-AF-2s wurden charakterisiert (s. Chambon, P., FASEB J 10:940-954
(1996); Glass, C.K. et al., Current Opin. Cell Biol. 9:222-232 (1997);
Horwitz, K.B. et al., Mol. Endocrinol.10:1167-1177 (1996) für neue Reviews).
Insbesondere zeigte LeDouarin, B. et al., EMBO J. 15:6701-6715 (1996),
dass ein 10-Aminosäuren-Fragment
von TIF1α notwendig
und ausreichend ist, um die Interaktion mit RXR auf eine Liganden-
und AF-2-Integrität-abhängige Weise
zu vermitteln. Besonders identifizierten sie innerhalb dieses TIF1α-Fragments
ein LxxLLL (SEQ ID NO:13)-Motiv, bezeichnet als NR-Box, dessen Integrität für die Interaktion
mit nuclearen Rezeptoren benötigt
wird, und betonten, dass dieses Motiv in mehreren anderen vermeintlichen
Coaktivatoren konserviert ist (LeDouarin, B. et al., EMBO J. 15:6701-6715 (1996))
Während
TIF1α und
mehrere andere vermeintliche Coaktivatoren nicht oder nur sehr schlecht
die Transaktivierung durch NRs in vorübergehend transfizierten Säugetierzellen
stimulieren, wurde eindeutig gezeigt, dass die TIF2/SRC-1-Familie
(Oñate,
S.A. et al, Science 270:1354-1357 (1995); Voegel, J.J. et al., EMBO
J. 15:3667-3675 (1996), die CBP/p300-Familie (Kamel, Y. et al.,
Cell 85:403-414 (1996); Chakravarti, D. et al., Nature 5:99-103
(1996); Hanstein, B., et al., Proc. Natl. Acad. Sci. USA 93:11540-11545
(1996), Smith; C.L. et al., Proc. Natl. Acad. Sci. USA 93:8884-8888
(1996); für
neue Reviews s. Eckner, R., Biol. Chem. 337:685-688 (1996); Janknecht & Hunter, Current
Biol. 6:951-954 (1996b); Shikama, N. et al., Trends in Cell Biol.
7:230-236 (1997)) und der Androgenrezeptor-Coaktivator ARA70 (Yeh & Chang, Proc.
Natl. Acad. Sci. USA 93:5517-5521 (1996)) die AF-2-Aktivität erhöhen.
-
Außer dem
Binden an NRs kann CBP/p300 auch direkt mit SRC-1 interagieren (Kamel,
Y. et al., Cell 85:403-414 (1996); Yao, T.P. et al., Proc. Natl.
Acad. Sci. USA 93:10626-10631 (1996)), und es wurde gezeigt, dass
beide Faktoren Histon-Acetyltransferase-Aktivität ausüben (Bannister & Kouzarides, Nature
384:641-643 (1996); Ogryzko, V.V. et al., Cell 87:953-959 (1996)).
Außerdem
kann CBP/p300 p/CAF rekrutieren, das selbst eine nucleare Histon-Acetyltransferase
ist (Yang, X.J. et al., Nature 382:319-324 (1996)). Abgesehen von
der Interaktion mit Coaktivatoren auf eine Liganden-abhängige Weise,
wurde jedoch auch gezeigt, dass NRs oft auf eine Liganden-unabhängige Art
und Weise direkt oder indirekt mit Komponenten der Transkriptionsmaschinerie
interagieren wie mit TFIIB, TBP, TAFs oder TFIIH (Baniahmad et al.,
(1993)); Jacq, X. et al., Cell 79:107-117 (1994); Schulman, IG.
et al., Mol. Cell. Biol. 16:3807-3813 (1996); May, M. et al., EMBO
J. 15:3093-3104 (1996); Mengus, G. et al., Genes & Dev. 11:1381-1395
(1997)).
-
Hong,
H. et al., Proc. Natl. Acad. Sci. USA 93:4948-4952 (1996) beschrieb
ursprünglich
eine partielle cDNA des Maushomologs von TIF2, GRIP1 genannt, und
berichtete kürzlich über die
Isolierung Volllängen-GRIP1-cDNA
(Hong, H. et al., Mol. Cell. Biol. 17:2735-2744 (1997)). Unter Verwendung
der Hefe Saccharomyces cerevisiae als ein Modellsystem zeigten sie,
dass Transkriptionsaktivierung durch TR, RAR und RXR auch durch
GRIP1-Coexpression stimuliert werden konnte, was darauf hinweist,
dass TIF2/GRIP1 ein allgemeiner Coaktivator für NRs sein könnte (Hong,
H. et al., Mol Cell. Biol. 17:2735-2744 (1997)).
-
Das
Gesamtbild, das sich aus mehreren neuen Studien über die Mechanismen, durch
die nucleare Rezeptoren die Transkription des Zielgens modulieren,
ergibt, bezieht drei aufeinanderfolgende Schritte ein, (i) die Liganden-induzierte Transkonformation
der NR-LBD, die zu (ii) der Dissoziation von Corepressoren und der
Bildung von TIFs/Coaktivator-Komplexen führt, die selbst (iii) durch
Interaktion mit zusätzlichen
stromabwärts-Faktoren
(z.B. CBP, p300) den Acetylierungszustand von Core-Histonen und
demnach die Chromatin-Kondensation/Dekondensation modulieren. Die
Histonacetylierung für
sich allein ist jedoch unzureichend zur Transkriptionsaktivierung
(Wong et al., (1997)) und ein simultanes oder nachfolgendes viertes
Ereignis umfasst die direkte und/oder die indirekte Rekrutierung
von Elementen der Transkriptionsmaschinerie (z.B. TFIB, TBP, TAFs,
TFIIH; Jacq, X. et al., Cell 79:107-117 (1994); Schulman, IG. et
al., Mol. Cell. Biol. 16:3807-3813 (1996); May, M. et al., EMBO
J. 15:3093-3104 (1996); Mengus, G. et al, Genes & Dev. 11:1381-1395 (1997)). Beachten
Sie, dass solche Interaktionen nicht Liganden-abhängig zu
sein brauchen, wenn die primäre
Funktion der ligandierten LBD (AF-2) ist, die DNA-Zugänglichkeit
durch Chromatin-Umbau zu regulieren. Allerdings geschehen mehrere
der berichteten Interaktionen zwischen NRs und allgemeinen Transkriptionsfaktoren
auf eine Liganden-unabhängige
Weise. Demgemäß gibt es
einen Bedarf auf dem Fachgebiet zur Isolierung und Charakterisierung
von transkriptionalen intermediären
Faktoren.
-
Zusammenfassung
der Erfindung
-
Durch
Durchmusterung von 340,000 Klonen einer menschlichen PlazentacDNA-Expressions-Bank mit
einer Estradiol-gebundenen Östrogenrezeptorsonde
identifizierten die anwesenden Erfinder einen cDNA-Klon, der das
Gen enthält,
das den transkriptionalen intermediären Faktor 2 (TIF2) codiert.
Durch die Erfindung wurde gezeigt, dass TIF2 alle die für einen
TIF/Mediator von AF-2 erwarteten Eigenschaften aufweist: er interagiert
direkt mit den LBDs von mehreren NRs auf eine Agonisten- und AF-2-Integrität-abhängige Weise in
vitro und in vivo, beherbergt eine unabhängige AF, erleichtert das NR-Autosquelching
und erhöht
die Aktivität von
NR-AF-2s, wenn er in Säugetierzellen überexprimiert
wird.
-
Demnach
stellt in einem Aspekt die vorliegende Erfindung Nucleinsäuremoleküle bereit,
die ein Polynucleotid umfassen, das TIF2 codiert, dessen Aminosäuresequenz
in 1 gezeigt ist (SEQ ID NO:2), oder ein
Fragment davon mit einer Aktivität,
wie hierin nachstehend beschrieben. In einem anderen Aspekt stellt
die Erfindung Nucleinsäuremoleküle bereit,
die TIF2 mit einer Aminosäuresequenz
codieren, wie sie durch die cDNA codiert wird, die als ATCC-Hinterlegungsnummer
97612 hinterlegt ist.
-
Auch
wird ein Nucleinsäuremolekül beschrieben,
das unter stringenten Bedingungen mit den voranstehend beschriebenen
Nucleinsäuremolekülen hybridisiert.
Außerdem
werden Varianten der Nucleinsäuremoleküle der vorliegenden
Erfindung beschrieben, die Fragmente, Analoga oder Derivate des
TIF2-Proteins codieren, z.B. Polypeptide mit mindestens einer biologischen
Aktivität,
die im Wesentlichen zu mindestens an biologischer Aktivität des TIF2-Proteins
gleich ist.
-
Die
vorliegende Erfindung ist ferner auf Nucleinsäuremoleküle ausgerichtet, die ein cytoplasmatisches TIF2-Polypetid
codieren. Verfahren zur Herstellung von Nucleinsäuremolekülen, die ein cytoplasmatisches TIF2-Polypeptid
codieren, beinhalten Mutieren oder Deletieren der NLSs-codierenden
N-terminalen Region der in 1 gezeigten
Nucleotidsequenz (SEQ ID NO:1). Vorzugsweise werden Nucleinsäuremoleküle, die ein
cytoplasmatisches TIF2-Polypeptid codieren, Fragmente mit einer
Deletion in allen oder einem Teil der N-terminalen NLSs codierenden
Region sein. Durch die Erfindung entfalten die hierin beschriebenen
cytoplasmatischen TIF2-Polypeptide mindestens eine biologische Aktivität, die im
Wesentlichen zu mindestens einer biologischen Aktivität von TIF2
gleich ist, wie hierin beschrieben.
-
Weitere
Ausführungsformen
der Erfindung beinhalten Nucleinsäuremoleküle, die ein Polynucleotid mit einer
mindestens zu 90% identischen und mehr bevorzugt mit einer mindestens
zu 95%, 96%, 97%, 98% oder 99% identischen Nucleotidsequenz zu den
voranstehend beschriebenen Nucleinsäuremolekülen umfasst.
-
Die
vorliegende Erfindung bezieht sich auch auf Vektoren, welche die
voranstehend beschriebenen Nucleinsäuremoleküle enthalten, auf Wirtszellen
die mit den Vektoren transformiert sind und auf die Herstellung
von TIF2-Polypeptiden durch rekombinante Verfahren.
-
Die
vorliegende Erfindung stellt ferner TIF2-Polypeptide mit der in 1 gezeigten Aminosäuresequenz (SEQ ID NO:2) bereit.
In einem weiteren Aspekt werden TIF-Polypeptide bereitgestellt mit
einer Aminosäuresequenz,
wie diejenige die durch die cDNA codiert wird, die als ATCC-Hinterlegungsnummer
97612 hinterlegt ist.
-
Durchmusterungsverfahren
zum Identifizieren von Agonisten und Antagonisten der Funktion des
nuclearen Rezeptors AF-2, zum Identifizieren von Agonisten und Antagonisten
der TIF2-AD1-Aktivität
und zum Identifizieren von Agonisten und Antagonisten der TIF2-AD2-Aktivität werden
auch bereitgestellt. TIF2-Antikörper
werden auch bereitgestellt.
-
Kurze Beschreibung
der Figuren
-
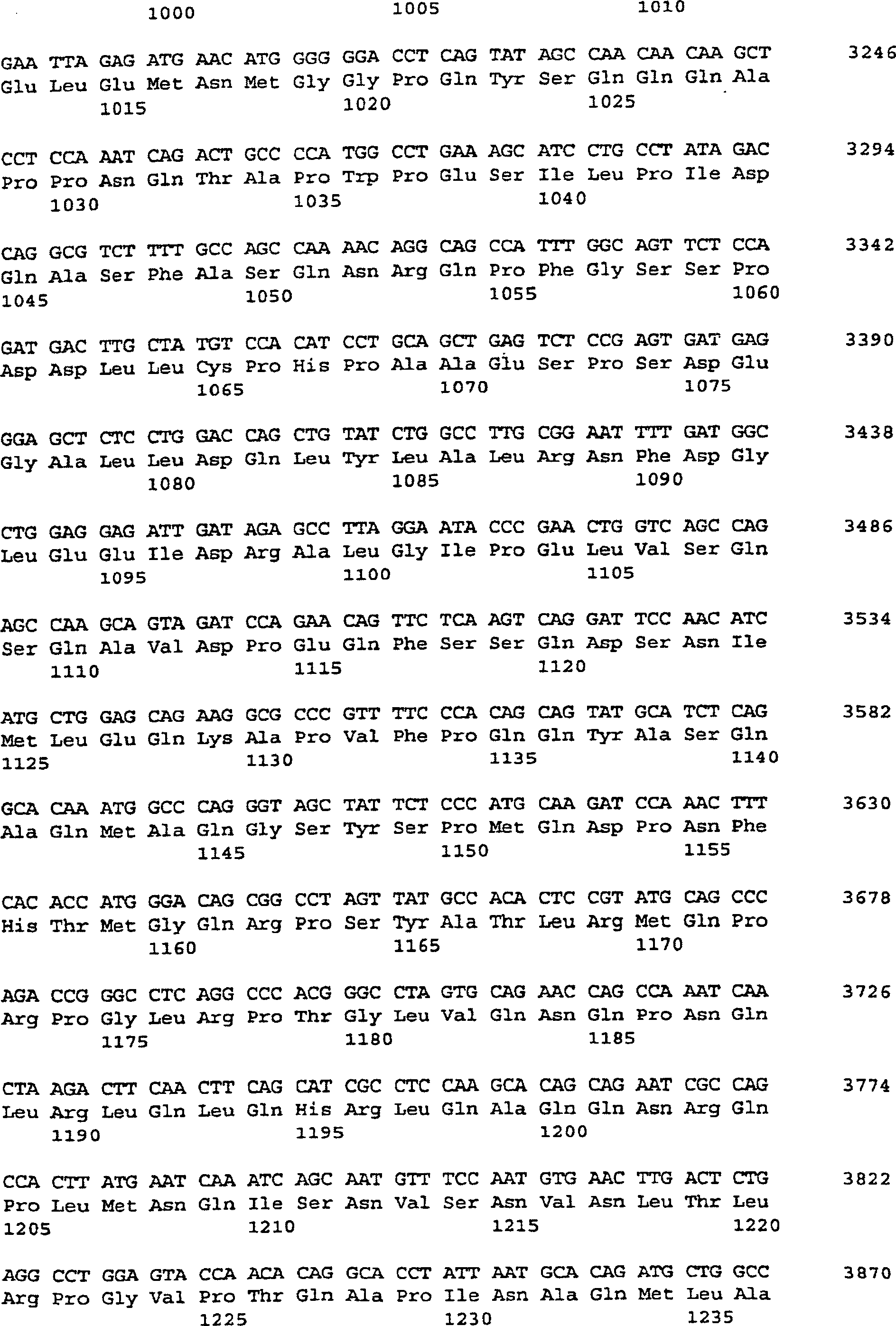
1(a-b). Die Nucleotid-(SEQ ID NO:1) und
die Aminosäuresequenzen
(SEQ ID NO:2) des TIF2-Proteins (transcriptional intermediary factor).
Dieses Protein hat ein abgeleitetes Molekulargewicht von etwa 160
kDa. Die Aminosäuresequenz
des funktionellen Coaktivator-TIF2.1-Proteinfragments ist von dem Aminosäurerest
624 bis zu Rest 1287 gezeigt.
-
2(a-c). TIF2 ist der 160-kDa-nuclearer-Rezeptor-interagierender
Faktor.
- (a) Die GST-Pulldown-Experimente identifizieren
ein 160-kDa-Protein, das mit dem ligandierten Östrogenrezeptor (ER)- und Retinolsäure-Rezeptor
(RAR)-α-Liganden-bindenden
Domänen
(LBDs) (ER(DEF) beziehungsweise RARα(DEF)) interagiert. Beachten
Sie, dass weniger Material in Spur 5 als in Spuren 1-4 ausgeführt wurde.
- (b) Die Immunodepletion gefolgt vom Far-Western-Nachweis zeigt
die Identität
von TIF2 mit dem biochemisch identifizierten 160-kDa-Protein. Offenes
Dreieck, TIF2; Pfeilspitze, TIF1; Kreis, Antikörper-Kreuzreaktion mit GST-ER(DEF).
Die pα-TIF2-immunonachgewiesene
Spezies, die kleiner ist als TIF2 (Spuren 2 und 6) ist höchstwahrscheinlich
ein Abbauprodukt von TIF2, da es durch Immunodepletion mit mα-TIF2 entfernt
wurde (Spuren 4 und 8).
- (c) Das Northern-Blotting offenbart ein ≈9-kb-TIF2-Transkript in verschiedenen
menschlichen Geweben.
-
Verfahren.
-
- (a) Gesamtzellextrakte von in vivo-35S-Met-markierten MCF7 (Cavailles, V. et
al., Proc. Natl. Acad. Sci. USA 91:10009-100013 (1994)), die vorher zweimal
mit GST-geladener Glutathion-Sepharose aufgearbeitet wurden, wurden
(Le Douarin, B. et al., EMBO J. 14:2020-2033 (1995)) mit GST, GST-hER
(DEF) oder GST-hRARα(DEF),
in Anwesenheit oder Abwesenheit von 10–6M
E2 oder T-RA inkubiert. Gebundene Proteine wurden mit SDS-Probenpuffer
zurückgewonnen
und durch Fluorographie (Amplify, Amersham) der SDS-Polyacrylamidgelen
erkennbar gemacht.
- (b) Gesamtzellextrakte von HeLa (2 ml in 500 mM NaCl, 250 mM
TrisHCl pH 7.5, 20% Glycerin, 5 mM DTT) wurden vorher mit Protein-G-Sepharose
(400 μl)
aufgearbeitet und mit Protein-G-Sepharose (3 × 400 μl), beladen mit mα-TIF2 (erzeugt
gegen ein synthetisches Peptid, das die an Ovalbumin gekoppelten
Aminosäuren
E624-Q653 umfasst) oder nicht-spezifischem IgG-Serum der Maus, behandelt.
Nach weiterem Aufarbeiten mit Protein-G-Sepharose (400 μl), wurde
der Überstand
inkubiert (Le Douarin, B. et al., EMBO J. 14:2020-2033 (1995)) mit
GST-hER(DEF) in
Anwesenheit oder Abwesenheit von E2(10–6M).
Zurückgehaltene
Proteine wurden mit SDS-Probenpuffer zurückgewonnen, durch SDS-PAGE
getrennt und auf Nitrocellulose-Membranen elektrogeblottet. Das
Far-Western-Blotting war, wie beschrieben (Cavailles, V. et al., Proc.
Natl. Acad. Sci. USA 91:10009-100013 (1994)). Zum Immunoblotting
wurde polyklonales Kaninchen-Antiserum (pα-TIF2), erzeugt gegen gereinigten
(Chen, Z-P. et al., J. Biol. Chem. 269:25770-25776 (1994)) rekombinanten
E.coli-exprimierten, His-markierten TIF2.1 verwendet. pα-TIF2 und polyklonales Kaninchen-pα-TIF1 wurden
1:2000 für
das ECL-bezogene Western-Blotting (Amersham) verdünnt. Alle
in dieser Studie verwendeten Konstrukte wurden durch DNA-Sequenzierung
verifiziert.
- (c) Der menschliche Northern-Blot (Clonetech, Nr. 7760-1; Abfüllcharge
5×332)
wurde mit 32P-markiertem TIF2.1 erkennbar
gemacht. Um das angemessene Beladen zu bestätigen, wurde die Membran mit 32P-markierter β-Actin-cDNA (Clonetech) rehybridisiert.
-
3(a-b). Aminosäuresequenz von TIF2: Die Homologie
mit SRC-1 zeigt die Existenz einer neuen Familie von NR-Mediatoren
an.
- (a) Die Angleichung und die Aminosäuresequenzen
von TIF-2 (SEQ ID NO:2) und von dem Steroidrezeptor-Coaktivator
SRC-1 (SEQ ID NO:3) (Onate, S.A. et al., Science 270:1354-1357 (1995)).
Zwei geladene Cluster, die reich an sauren und basischen Aminosäureresten
sind, drei Serin/Threonin (S/T)-reiche Regionen und eine Glutamin-reiche
Region sind hervorgehoben. Der N-terminale geladene Cluster enthält die vermeintlichen
zweiteiligen nuclearen Lokalisierungssignale (NLSs) (überstrichen).
Die Regionen, die TIF2.1 (Aminosäuren
624 bis 1287; funktionelles Coaktivator-Fragment) und dnSRC-1 (Aminosäuren 865 bis
1061; dominantnegatives Fragment) codieren, sind angezeigt. Ein
Stern identifiziert das TIF2-Stopp-Codon. Beachten Sie, dass TIF2.1 und
dnSRC-1 nicht überlappen,
was anzeigt, dass dnSRC-1 möglicherweise
eine NR-interagierende Region enthalten kann, die von der von TIF2.1
verschieden ist.
- (b) Schematischer Vergleich von TIF2 und SRC-1. Prozent-Identitäten (Ähnlichkeiten
in Klammern) von homologen Regionen sind angezeigt. Der N-terminale geladene
Cluster, der das vermeintliche NLS beherbergt, und die C-terminale S/T-reiche
Region von TIF2 sind nicht oder nur schwach in SRC-1 konserviert.
-
Verfahren.
-
340,000
Klone der λExlox
Expressions-cDNA-Bank der menschlichen Plazenta wurde mit einer 32P-markierten GST-hER(DEF)-Sonde in Anwesenheit
von 10–6M
E2 unter Verwendung der Far-Western-Methode (Cavailles, V. et al.,
Proc. Natl. Acad. Sci. USA 91:10009-100013 (1994)) durchmustert.
Das 1992-bp-Insert, das dem Ausgangsklon (TIF2.1) entspricht, wurde
verwendet, um dieselbe Genbank wieder zu durchmustern. Fünf stark überlappende
cDNA-Inserts bedeckten eine Region von 6 kb, die ein 1,464-Aminosäuren-ORF enthält. Alle
Inserts wurden an beiden Strängen
sequenziert. Die vorübergehende
Expression der assemblierten cDNA-Inserts, die das vorhergesagte
ORF umfassen, ergab ein 160-kDa-Protein.
-
4(a-n). In vivo- und in vitro-Interaktionen
von TIF2 mit nuclearen Rezeptoren.
- (a) Das überexprimierte
TIF2-Protein ist hauptsächlich
in diskreten nuclearen Körpern
lokalisiert und von den Nucleoli ausgeschlossen. Eine überlagernde
Abbildung der Hoechst-DNA-Färbung
und der TIF2-Immunofärbung
wird gezeigt.
- (b-i) Cytoplasmatisches TIF2.1 interagiert auf eine Agonisten-abhängige Weise
mit nuclearen Rezeptoren in Säugetierzellen.
Die helle Färbung
zeigt die TIF2.1-NO-Kolokalisierung
an.
- (k-n) TIF2.1 interagiert direkt in vitro auf eine Agonisten-abhängige Weise
mit nuclearen Rezeptoren, und Punktmutationen innerhalb der AF-2-Aktivierungsdomäne (AD)-Core
heben diese Interaktion auf. WT, Wildtyp. Ligandenkonzentrationen
für n:
9C-RA, T-RA und T3, 10–6 M; E2, 5 × 10–8M;
OHT, 5 × 10–6M.
Das kleinere immunodetektiert Polypeptid ist ein Abbauprodukt von
TIF2.1. Beachten Sie, dass das anti-TIF2-Serum schwach mit GST-hER(DEF)
kreuzreagiert.
-
Verfahren.
-
- (a-i) Cos-1-Zellen wurden vorübergehend
mit TIF2.1 (10 μg)
transfiziert entweder (a) alleine oder (b-i) zusätzlich mit den angezeigten
NR-Expressionsvektoren
(10 μg,
ausgenommen RARa, 1 μg)
in Abwesenheit oder Anwesenheit des verwandten Liganden (10–6M,
ausgenommen R5020, 10–8 M). In d-f wurde HE0 (Webster,
N.J. et al., Cell 54:199-207 (1988)) verwendet. Die Immunocytofluoreszenz-Assays
waren, wie beschrieben (Kastner, P. et al., EMBO J. 11: 629-642
(1992)). Bilder wurden durch konfokale Lasermikroskopie aufgenommen.
- (k-n) GST-Interaktionsassays mit E.coli-exprimiertem rekombinanten
TIF2.1 (2b) wurden durchgeführt, wie
beschrieben (Le Douarin, B. et al., EMBO J. 14:2020-2033 (1995)).
Gebundene Proteine wurden durch Western-Blotting mit pα-TIF2-Antiserum (Verdünnung 1:30,000)
offenbart, die gleich große
Ladung von Aftinitätsmatrizen
wurde durch SDS-PAGE und Coomassie-Färbung verifiziert. ,Input'-Spuren enthalten
ein Drittel des TIF2.1-Inputs.
-
5(a-e). TIF2 enthält eine unabhängige AF, „Antisquelches" und stimuliert die
NO-AF2-Aktivität
auf eine Agonisten-, Promotor- und Zell-abhängige Weise.
- (a)
Ansteigende Mengen des GAL-TIF2.1-Fusionsproteins (Spuren 2-4) aktiviert
die Transkription eines verwandten Reporters in transfizierten Zellen.
Das Vielfache der Induktion ist unter den CAT-Assays gegeben.
- (b) TIF2.1 kehrt teilweise die transkriptionale Autointerferenz
von ER um. Die normalisierte CAT-Expression (Mittelwert ± s.e.
von 4 unabhängigen
Experimenten) ist gezeigt. Offene Kreise, +E2, +TIF2; Quadrate, +E2,-TIF2;
Kreuze, +OHT, +TIF2.
- (c) TIF2 erhöht
die Transaktivierung, die durch einige NR-AF-2s vermittelt wird,
aber nicht die, die durch andere Transkriptionsfaktoren vermittelt
wird. Die mittleren TIF2-Stimulationen von 3 unabhängigen Experimenten
sind gegeben (Variation <_ 13%).
Liganden: Spuren 3-4, E2; Spuren 7-8, DHT (Dihydrotestosteron);
Spuren 11-12, R5020;
Spuren 15-16, T-RA.
- (d) TIF2 erhöht
die PR-vermittelte Transkriptionsaktivierung von sowohl einem minimalen
(GRE-TATA)- als auch einem komplexen (MMTV)-Promotor;
diese Stimulation ist in Cos-1-Zellen signifikant größer als
in HeLa-Zellen.
- (e) TIF2 erhöht
außerordentlich
die Agonisten-induzierte Aktivierung durch ER in Cos-1- und schwächer in HeLa-Zellen.
Beachten Sie, dass die schwache, anscheinend Liganden-unabhängige TIF2-Induktion
von ER (vgl. Spuren 1 mit 2 und 7 mit 8) an rückständigem Estradiol an dem Kulturmedium
liegt. In d und e sind TIF2-Induktionen
von ≥ 3 Experimenten
gezeigt (Variation ≤ 10%).
-
Verfahren.
-
Mit
der Ausnahme von GAL-TIF2.1, TIF2.1 und TIF2 wurde die Konstruktion
von Reporterplasmiden und Expressionsvektoren beschrieben (Meyer,
M-E. et al., Cell 57:433-442 (1989); Bocquel, M-T. et al., Nucl. Acids
Res. 17:2581-2595
(1989); Tasset, D. et al., Cell 62: 1177-1187 (1990); Gronemeyer,
H. und Laudet, V., Protein Profile 2: 1173-1308 (1995); Webster,
N.J. et al., Cell 54: 199-207 (1988); Strähle, U. et al., EMBO J. 7:3389-3395
(1988); Seipel, K. et al., EMBO J. 11:4961-4968 (1992); Nagpal,
S. et al., EMBO J. 12:2349-2360 (1993); Chen, J-Y. et al., EMBO
J. 14:1187-1197 (1995)). CAT-Assays wurden durchgeführt, wie
beschrieben (Bocquel, M-T. et al., Nucl. Acids Res. 17:2581-2595
(1989)).
- (a) HeLa-Zellen wurden jeweils mit
1 μg (17m)5-βG-CAT
und 10 μg
GAL(1-147) oder 1,3 und 10 μg GAL(1-147)-TIF2.1
cotransfiziert.
- (b) HeLa-Zellen wurden mit 5 μg
Vit-tk-CAT und der angezeigten Menge von HEG0 mit oder ohne 5 μg TIF2.1
in der Anwesenheit von 10–6 M E2 oder OHT cotransfiziert.
Die CAT-Aktivität
wird relativ zu derjenigen gegeben, die durch 100 ng HEG0 in Anwesenheit
von E2 induziert wird.
- (c) HeLa-Zellen wurden mit 1 μg
17m-tk-CAT und 1 μg
der angezeigten GAL-Fusionsvektoren
mit oder ohne die Zugabe von 3 μg
TIF2-Expressionsvektor in Anwesenheit oder Abwesenheit von 10–6M
Ligand cotransfiziert.
- (d) HeLa- (Spuren 1-12) oder Cos-1- (Spuren 13-18) Zellen wurden
mit 5 μg
GRE-TATA-CAT (Spuren 1-6) oder 1 μg
MMTV-CAT (Spuren 7-18) zusammen mit 1 μg hPR mit oder ohne 3 μg TIF 2 in
Anwesenheit oder Abwesenheit von 10–6 M
des angezeigten Liganden transfiziert.
- (e) Cos-1-Zellen wurden mit 1 μg Vit-tk-CAT und 1 μg HEG0 mit
oder ohne 3 μg
TIF2 in Anwesenheit oder Abwesenheit von 10–6 M
der angezeigten Liganden cotransfiziert.
-
6(a-b). Schematische Darstellung der Reportergene
(A) und Rezeptorexpressionsvektoren (B) (s. den Abschnitt Materials
and Methods von Nagpal et al., EMBO J. 12(6):2349-2360 (1993) für eine detaillierte Beschreibung
der Konstruktion). Die Sequenzen von mCRBPII (SEQ ID NO:11) und
mCRBPII(17m-ERE)/CAT (SEQ ID NO:11) sind angezeigt. Minus- und Plus-Zahlen sind hinsichtlich
der RNA-Startstelle (+1). In (B) werden die verschiedenen Regionen
(A-F) der Wildtyp-RARs und -RXRs, sowie ihre Kürzungsmutanten, Substitutionsmutanten
und chimäre
Rezeptor-Konstrukte schematisch dargestellt (nicht maßstabsgetreu)
(s. Zelent et al., Nature 339:714-717 (1989); Leid et al., Trends
Biochem. Sci. 17:427-433 (1992); Leid et al., Cell68:377-395 (1992);
Nagpal et al., Cell 70:1007-1019 (1992); und Allenby et al., Proc.
Natl. Acad. Sci. USA 90:30-34
(1993)). Die Zahlen zeigen die Aminosäurepositionen in dem Wildtyp-Rezeptor
an. Die Positionen der Aminosäuresubstitutionen
sind mit einem Pfeil angezeigt.
-
7(a-e). Kartierung von TIF2-Domänen.
- (a) Schematische Darstellung von in TIF2 identifizierten
funktionellen Domänen.
Die verschiedenen TIF2-Konstrukte sind angegeben; exprimierte Reste
sind in Klammern angegeben. Die fett gedruckten Linien zeigen exprimierte
Sequenzen an. Die Konstrukte, die für die NR-Interaktion, Transaktivierung
oder CBP-Binden positiv oder negativ ausgewertet werden, werden
rechts jeweils durch „+" und „-"-Zeichen identifiziert;
nd, nicht bestimmt.
- (b) Kartierung der nuclearen Rezeptor-Interaktionsdomäne von TIF2.
Glutathion-S-transferase (GST)-Pulldown-Experimente wurden mit 35S-markierten in-vitro-translatierten TIF2-Polypeptiden
und bakteriell hergestellter GST, GST-hERa(DEF) und GST-hRARa(DEF) in der
Anwesenheit oder Abwesenheit von 10–6 M des
verwandten Liganden (E2, Estradiol für ER; RA all-trans-Retinolsäure für RAR) durchgeführt.
- (c) Die Analyse der Transkriptionsaktivität der GAL-TIF2-Fusionsproteine.
Cos-1- und HeLa-Zellen
wurden mit 3 μg
von Plasmiden, die verschiedene Regionen von TIF2 exprimieren, der
mit der DNA-bindenden Domäne
des Hefe-Transkriptionsfaktors
GAL4 fusioniert ist, zusammen mit 1 μg des (17m)5-G-CAT- Reporterplasmids transfiziert. CAT-Assays
wurden durchgeführt,
wie beschrieben (Bocquel, M.T. et al., Nucl. Acids. Res. 17:2581-2595
(1989)). Quantitative Daten über
die CAT-Reporterexpression wurden entweder durch die Phosphoimager-Analyse (BAS2000,
Fuji) von 14C-markierten CAT-Reaktionsprodukten,
die durch Dünnschichtchromatographie
getrennt wurden, oder durch Verwendung des CAT-ELISA-Kits (Boehringer Mannheim) erhalten.
Bei allen Fällen
wurden die CAT-Aktivitäten auf
die β-Galactosidase-Konzentrationen normalisiert,
die aus der Cotransfektion von 1 μg
von pCMVβGal
(Geschenk von T. Lerouge) als interne Kontrolle resultierten. Das
Vielfache der Induktion über
dem GAL4-DBD-Wert ist angezeigt. Der Mittelwert und die Standardabweichung
von mindestens drei Experimenten werden gezeigt. Ein representativer
Western-Blot, der die Expressionsniveaus der GAL4-TIF2-Fusionsproteine,
die aus 10 μg
der entsprechenden Expressionsvektoren exprimiert wurden, veranschaulicht,
ist links gezeigt. Der Blot wurde mit den monoklonalen Antikörpern 2GV3
und 3GV2 der Maus offenbart, die spezifisch für GAL4-DBD und 2GV4B7, spezifisch
für die
VP16-Aktivierungsdomäne, sind.
- (d) Kartierung der CBP-Interaktionsdomäne von TIF2. GST-Pulldown-Experimente wurden
mit 35S-markierten in-vitro-translatierten
TIF2-Polypeptiden und bakteriell hergestellten GST und GST-CBP (das
die CBP-Reste 1872 bis 2165 exprimiert) durchgeführt.
- (e) Zwei-Hybrid-Analyse der CBP-TIF2-Interaktion in Säugetierzellen
in vivo. HeLa-Zellen wurden mit 0.2 μg der GAL4- oder GAL4-CBP- (das
die CBP-Reste 1872 bis 2165 exprimiert) Expressionsvektoren zusammen
mit 0.2 μg
der VP16- oder VP16-TIF2-Expressionsvektoren in der Anwesenheit
von 1 μg
des (17m)5-TATA-CAT-Reporterplasmids transfiziert.
Das Vielfache der Induktion, relativ zur GAL-CBP-Aktivität, ist angezeigt.
Der Mittelwert von drei Experimenten ist gezeigt; bei jedem Fall
variierten die Werte um weniger als ±20%.
-
8(a-e). Kartierung der TIF2-nuclearer-Rezeptor-Interaktionsdomäne (NID).
- (a) Angleichung der TIF2-NID (SEQ ID NO:2)
mit den entsprechenden Regionen von SRC-1 (SEQ ID NO:3) und P/CIP
(SEQ ID NO:5) und Beschreibung der NID-Mutationen. Die drei konservierten
Regionen sind mit den entsprechenden Aminosäurenummern von hTIF2 oder hSRC-1
(F-SRC-1) von ganzer Länge
dargestellt; die Leucine, die zu den drei NR-Box-Motiven (I, II,
III) gehören,
sind umrahmt. Die verschiedenen Deletions- und Leucin-zu-Alanin-Punktmutationskonstrukte
sind angegeben.
- (b) Angleichung der TIF2 (SEQ ID NO:2)-NR-Boxen mit den in mehreren
Cofaktoren identifizierten NR-Boxen: TIF1α (SEQ ID NO:6), RIP140 (SEQ
ID NO:7) und TRIP3 (SEQ ID NO:8). Die konservierten Leucine sind
umrahmt.
- (c-d) Interaktion von TIF2-NID-Mutanten mit NRs in vitro. Die
GST-Aftinitätschromatographie-Experimente wurden
mit 35S-markierten in vitro-translatierten GAL4-DBD-Verbindungen
der TIF2-Deletionsmutanten (c) oder TIF2.1-Punktmutanten (d) und bakteriell exprimierten
GST und GST-Verbindungen der ER(DEF) und RAR(DEF) in der Abwesenheit
oder Anwesenheit von jeweils 10–6 M
Estradiol oder all-trans-Retinolsäure durchgeführt. Zur
Quantifizierung der Punktmutanten-Interaktionen s. nachstehend.
- (e) Wirkung der TIF2-NID-Punktmutation auf die Stimulation der
NR-AF-2-Aktivität. Cos-1-Zellen
wurden mit 1 μg
des (17m)5-TATA-CAT_Reporters, 0.2 μg von GAL-hERα(EF) oder
GAL-mRXRα(DE)
und 2.5 μg des
TIF2.1-Wildtyps oder mutierten Fragmenten cotransfiziert, wie angezeigt.
Die Aktivierung des Reportergens relativ zur TIF2.1-Wildtyp-Aktivität und in
Anwesenheit von jeweils 10–6 M Estradiol (E2) oder all-trans-Retinolsäure (RA)
ist für
jede Mutante angezeigt (schwarze Balken); zum Vergleich ist das
in vitro-Binden der jeweiligen Mutanten relativ zum TIF2.1-Wildtyp-Binden
in Anwesenheit des Liganden durch weiße Balken angezeigt. Jeder
Balken repräsentiert
den jeweils aus mindestens drei (Interaktion) oder mindestens vier
(Transaktivierung) Experimenten erhaltenen Mittelwert; die Standardabweichungen
sind angezeigt. Beachten Sie, dass die absoluten Werte für die TIF2.1-Wildtyp-Aktivität um ±16% variierten,
wenn mit GAL-hERa(EF) cotransfiziert, und um ±34%, wenn mit GAL-mRXRa(DE)
cotransfiziert. Bei den in-vitro-Interaktionsassays
variierte die Affinität
des TIF2.1-Wildtyp-Standards um weniger als ±25%. Die Expressionsniveaus
der TIF2-Mutanten in den Zellen wurden
durch Western-Blot
(nicht gezeigt) mit dem monoklonalen Antikörper 3Ti3F1 der Maus verifiziert,
der gegen ein Epitop außerhalb
des mutierten Bereichs gerichtet ist.
-
9(a-c). Kartierung der TIF2-Aktivierungsfunktion-1
(AF-1) und Interaktion der AF-1-Domäne mit CBP.
- (a)
Angleichung der TIF2-AF-1 mit der entsprechenden Region von SRC-1
(SEQ ID NO:3) und P/CIP (SEQ ID NO:9). Beschreibung der TIF2-AF-1-Deletionsmutanten
und ihrer Eigenschaften. Die Regionen von TIF2 und hSRC-1, die vorhergesagt
wurden, zu α-Helices
zu falten, sind umrahmt (PHD-Programm). Die GAL-TIF2-Konstrukte,
die positiv oder negativ für
die Transaktivierung eines GAL4-Reporters
bewerten, werden rechts jeweils durch „+"- und „-"-Zeichen identifiziert; nd, nicht bestimmt.
- (b) Transkriptionsaktivierung von TIF2-AF-1-Mutanten. Cos-1-
und HeLa-Zellen wurden mit 3 μg
von Plasmiden, die verschiedene Mutanten der TIF2-AF-1 exprimieren,
die mit der DNA-bindenden Domäne
des Hefe-Transkriptionsfaktors GAL4 fusioniert ist, zusammen mit
1 μg des
(17m)5-G-CAT-Reporterplasmids cotransfiziert.
Das Vielfache der Induktion oberhalb der Aktivierung die mit GAL4-DBD alleine gesehen
wird sind angezeigt. Die Werte repräsentieren den Mittelwert von
mindestens drei Experimenten. Beachten Sie, dass alle GAL4-TIF2-Fusionsproteine zu ähnlichen
Niveaus exprimiert wurden, wie durch Western-Blot mit gegen GAL4-DBD
gerichteten Antikörpern
offenbart wurde (Daten nicht gezeigt).
- (c) Interaktion von TIF2-AF-1-Mutanten mit CBP in vitro. GST-Pulldown-Experimente wurden
mit 35S-markierten in-vitro-translatierten
GAL-TIF2-Fusionsproteinen
und bakteriell hergestellter GST und GST-CBP durchgeführt. Beachten
Sie, dass die GAL4-DBD für
sich allein nicht mit der GST-CBP-Affinitätsmatrix interagiert.
-
10(a-c). Identifizierung von TIF2-AF-1-Mutanten,
die sowohl in der Transkriptionsaktivierung als auch in der Interaktion
mit CBP beeinträchtigt
sind.
- (a) Die Transkriptionsaktivierung durch
TIF2.13 und TIF2.13-Mutanten. Cos-1-und HeLa-Zellen wurden mit 3 μg von Plasmiden,
die die TIF2.13-Region und die angezeigten TIF2.13-Mutanten exprimieren,
die mit der DNA-bindenden Domäne
des Hefe-Transkriptionsfaktors GAL4 fusioniert sind, zusammen mit
1 μg des (17m)-G-CAT-Reporterplasmids
cotransfiziert. Das Vielfache der Induktion über dem 1-fachen Wert von GAL4-DBD
ist angezeigt. Der aus mindestens vier Experimenten erhaltene Mittelwert
und die Standardabweichung sind gezeigt. Die Expressionsniveaus
der GAL4-TIF2.13-Fusionsproteine wurden durch Western-Blotting bestätigt (Daten
nicht gezeigt).
- (b) Die durch Zwei-Hybrid-Analyse offenbarte Interaktion von
TIF2.13-Wildtyp und TIF2.13-Mutanten mit CBP in Säugetierzellen.
HeLa-Zellen wurden mit 0.2 μg
von GAL4 oder GAL-CBP-Expressionsvektoren zusammen mit 0.2 μg von VP16
oder VP16-TIF2.13-Expressionsvektoren in der Anwesenheit von 1 μg von (17m)5-TATA-CAT-Reporterplasmid transfiziert.
Die Daten sind als Vielfaches der Induktion der mit GAL-CBP alleine
gesehenen Aktivität
dargestellt. Der aus zehn Experimenten erhaltende Mittelwert und
die Standardabweichung sind gezeigt. Die Expressionsniveaus wurden
durch Western-Blotting mit gegen GAL4-DBD und VP16-AAD gerichteten
Antikörpern
bestätigt
(Daten nicht gezeigt).
- (c) Interaktion von TIF2.13-Wildtyp und TIF2.13-Mutanten mit
CBP in vitro. GST-Pulldown-Experimente wurden mit 35S-markierten
in-vitro-translatierten VP16-TIF2.13-Polypepetiden
und bakteriell hergestellter GST und GST-CBP durchgeführt. Beachten
Sie, dass die VP16-Aktivierungsdomäne alleine nicht mit GST-CBP
interagiert.
-
11. Das TIF2.1-Coaktivator-Fragment stimuliert
effizient die Ligandenabhängige
AF-2 von ER, RAR und RXR in Hefe. Keine stimulatorische Wirkung
von TIF2.1 auf die isolierte AF-1 von ER (HE15) ist beobachtbar.
Plasmide, die verschiedene Regionen von hERa (weiß), hRARa
(grau) und mRXRa (schwarz) exprimieren, die mit der ER-DBD (hERα(C)) fusioniert
sind, wurden in den Hefe-Reporterstamm
PL3(α) zusammen
mit TIF2.1 eingebracht, wie angezeigt. Weiße Boxen repräsentieren
die Sequenzen von Transformanten, die in der Anwesenheit oder Abwesenheit
von 10–6 M
des verwandten Liganden (Östradiol
für ER,
all-trans-Retinolsäure für RAR, 9-cis-Retinolsäure für RXR) gezüchtet wurden.
Die zu jedem zellfreien Extrakt ermittelten OMP-Decase-Aktivitäten sind
in nmol/min/mg Protein ausgedrückt;
der Mittelwert und die Standardabweichung von mindestens vier Experimenten
sind gezeigt.
-
12(a-d). Die isolierte nuclearer Rezeptor-Interaktionsdomäne (NID)
von TIF2 wirkt dominant-negativ auf die Transkriptionsaktivierung
durch die ER, RXR- und
RAR-LBDs. Der Mittelwert der Induktion, der aus der Quantifizierung
von mindestens drei Experimenten (relativ zu der jeweiligen Rezeptor-LBD-Aktivität in Abwesenheit
von rekombinantem TIF2) erhalten wurde, ist unter jeder Tafel angezeigt.
Die Expressionsniveaus von TIF2, TIF2.1 und TIF2.5 wurden routinemäßig durch
Western-Blot mit dem monoklonalen Antikörper 3Ti3C11 der Maus, der
gegen eine Region von TIF2.5 gerichtet ist, verifiziert (nicht gezeigt).
- (a) Die Überexpression
des TIF2.5-Fragments, das die isolierte NID enthält, kehrt die stimulatorische
Wirkung des starken Coaktivator-Fragments TIF2.1 um. Cos-1-Zellen
wurden mit 1 μg
des (17m)5-TATA-CAT-Reporters und 0.2 μg GAL-ERα(EF)-Expressionsvektor
in der Anwesenheit oder Abwesenheit von 10–6 M Östradiol
cotransfiziert. Wo angezeigt, wurden 0.1 μg von TIF2.1 und 2.5 μg von TIF2.5-Expressionsvektoren
zusätzlich
cotransfiziert.
- (b-d) Volllängen-TIF2
und das Coaktivator-Fragment TIF2.1 erhöhen die Aktivität der ER,
RXR- und RAR-LBDs, während
die nuclearer Rezeptor-Interaktionsdomäne TIF2.5
die Aktivität
der ER, RXR- und RAR-LBDs blockiert. Cos-1- und HeLa-Zellen wurden mit 1 μg des (17m)5-TATA-CAT-Reporters und 0.2 μg des Expressionsvektors,
der die jeweilige GAL-DBD-Verbindung von hERα(EF), mRXRα(DE) oder mRARα(DEF) codiert,
cotransfiziert. In der Anwesenheit oder Abwesenheit von 10–6 M
Ligand (E2, Östradiol; 9C-RA,
9-cis-Retinolsäure;
T-RA, alltrans-Retinolsäure),
zusammen mit 0.25 μg
oder 2.5 μg
von TIF2, TIF2.1 und TIF2.5-Expressionsvektoren.
-
Detaillierte
Beschreibung der bevorzugten Ausführungsformen
-
Die
vorliegende Erfindung stellt Nucleinsäuremoleküle bereit, die ein Polynucleotid
umfassen, das den transkriptionalen intermediären Faktor-2 (TIF2) codiert,
dessen Aminosäuresequenz
in 1 (SEQ ID NO:2) gezeigt wird. Das
TIF2-Protein der vorliegenden Erfindung teilt die Sequenzhomologie
mit dem menschlichen Steroidrezeptor-Coaktivator SRC-1 (SEQ ID NO:3)
(3). Die in 1 gezeigte
Nucleotidsequenz (SEQ ID NO:1) wurde durch Sequenzierung eines cDNA-Klons
erhalten, der am 14. Juni 1996 bei der ATCC hinterlegt und dem die
Zugangsnummer 97612 gegeben wurde.
-
Nucleinsäuremoleküle
-
In
einer Ausführungsform
der vorliegenden Erfindung werden Nucleinsäuremoleküle bereitgestellt, die das
TIF2-Protein codieren. Die Sequenzähnlichkeiten zwischen TIF2
und SRC-1 (Onate et al., Science 270:1354 (1995)) zeigen die Existenz
einer neuen Genfamilie von NR-Transkriptionsmediatoren
an. Unter Verwendung der hierin bereitgestellten Information wie
der Nucleotidsequenz in 1 (SEQ ID
NO:1) oder dem voranstehend beschriebenen hinterlegten Klon kann
ein Nucleinsäuremolekül der vorliegenden
Erfindung, das ein TIF2-Polypeptid codiert, unter Verwendung von
Standardklonierung und Durchmusterungsprozeduren erhalten werden.
Veranschaulichend für
die Erfindung wurde das in 1 beschriebene
Nucleinsäuremolekül (SEQ ID
NO:1) in einer cDNA-Expressionsbank von menschlichem Plazenta-Gewebe
entdeckt. Die TIF2-cDNA der vorliegenden Erfindung codiert ein Protein
von etwa 159 kDa (1,464 Aminosäuren),
das N-terminale nucleare
Lokalisierungssignale (NLSs), eine Gln- und drei Ser/Thr-reiche
Regionen und zwei geladene Cluster beinhaltet (3).
TIF2 wird weitgehend exprimiert, da das entsprechende Transkript
in mehreren menschlichen Geweben gefunden wurde, einschließlich in
Pankreas, Niere, Muskel, Leber, Lunge, Plazenta, Gehirn und Herz
(2c).
-
Nucleinsäuren der
vorliegenden Erfindung können
in der Form von RNA, wie mRNA, oder in der Form von DNA sein, einschließlich zum
Beispiel cDNA und genomische DNA, die durch Klonierung erhalten
oder synthetisch hergestellt wird. Die DNA kann doppelsträngig oder
einzelsträngig
sein. Einzelsträngige
DNA oder RNA kann der codierende Strang sein, auch als der Sense-Strang
bekannt, oder sie kann der nicht codierende Strang sein, auch als
Antisense-Strang bezeichnet.
-
Durch
(ein) „isolierte(s)" Nucleinsäuremolekül(e) ist
ein Nucleinsäuremolekül beabsichtigt,
DNA oder RNA, das aus seiner natürlichen
Umgebung entfernt wurde. Zum Beispiel werden in einem Vektor enthaltene rekombinante
DNA-Moleküle
für Zwecke
der vorliegenden Erfindung als isoliert angesehen. Zusätzliche veranschaulichende
Beispiele von isolierten DNA-Molekülen umfassen rekombinante DNA-Moleküle, die
in heterologen Wirtszellen beibehalten werden, und aufgereinigte
(teilweise oder wesentlich) DNA-Moleküle in Lösung. Isolierte RNA-Moleküle umfassen
in vitro-RNA-Transkripte der DNA-Moleküle der vorliegenden Erfindung
sowie teilweise oder wesentlich aufgereinigte mRNA-Moleküle. Isolierte
Nucleinsäuremoleküle gemäß der vorliegenden
Erfindung umfassen weiterhin solche Moleküle die synthetisch hergestellt
wurden.
-
Nucleinsäuremoleküe der vorliegenden
Erfindung schließen
DNA-Moleküle
ein, die ein offenes Leseraster (ORF) mit einem Startcodon an Position
163-165 der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1) umfassen; und DNA-Moleküle, die eine Sequenz umfassen,
die sich deutlich von der voranstehend beschriebenen unterscheidet,
aber die auf Grund der Entartung des genetischen Codes das TIF2-Protein noch codiert.
Natürlich
ist der genetische Code auf dem Fachgebiet gut bekannt. Demnach
würde es
für einen
Fachmann Routine sein, die voranstehend beschriebenen degenerierten
Varianten herzustellen.
-
In
einem anderen Aspekt stellt die Erfindung Nucleinsäuremoleküle bereit,
die das TIF2-Polypeptid mit einer Aminosäuresequenz codieren, wie durch
den cDNA-Klon codiert,
der als ATCC-Hinterlegungsnummer 97612 am 14. Juni 1996 hinterlegt
wurde (American Type Culture Collection, (ATCC) Rockville, MD).
Die Erfindung stellt weiter ein Nucleinsäuremolekül bereit mit der in 1 gezeigten Nucleotidsequenz (SEQ ID NO:1)
oder der Nucleotidsequenz der TIF2-cDNA, die in dem voranstehend
beschriebenen Klon enthalten ist, oder ein Nucleinsäuremolekül mit einer
Sequenz, die komplementär
zu einer der voranstehenden Sequenzen ist. Solche Nucleinsäuremoleküle, vorzugsweise
DNA-Moleküle,
sind brauchbar als Sonden zur Genkartierung durch in situ-Hybridisierung
mit Chromosomen und zum Nachweis der Expression des TIF2-Gens in
menschlichem Gewebe, zum Beispiel durch Northern-Blot-Analyse.
-
In
einem anderen Aspekt wird ein Nucleinsäuremolekül beschrieben, das unter stringenten
Bedingungen mit den voranstehend beschriebenen Nucleinsäuremolekülen hybridisiert.
Wie hierin verwendet, sind unter „stringenten Bedingungen", als ein nicht begrenzendes
Beispiel, eine Inkubation über
Nacht bei 42°C
in einer Lösung,
die 50% Formamid, 5×SSC
(150 mM NaCl, 15mM Trinatriumcitrat), 50 mM Natriumphosphat (pH-Wert
7.6), 5× Denhardt-Lösung, 10% Dextransulfat
und 20 μg/ml
denaturierte, gescherte Lachssperma-DNA umfasst, gefolgt durch Waschen
der Filter in 0.1×SSC
bei etwa 65°C
zu verstehen. Vorzugsweise wird solch „ein isoliertes Nucleinsäuremolekül, das unter
stringenten Bedingungen hybridisiert" mindestens 15 bp, vorzugsweise mindestens
20 bp, bevorzugter mindestens 30 bp und am meisten bevorzugt mindestens
50 bp lang sein.
-
Wie
hierin verwendet, versteht man unter „Fragmente" eines DNA-Moleküls mit der Nucleotidsequenz der
hinterlegten cDNA oder der Nucleotidsequenz, wie in 1 (SEQ
ID NO:1) gezeigt, DNA-Fragmente einer Länge von mindestens 15 bp, bevorzugter
von mindestens 20 bp und am meisten bevorzugt von mindestens 30
bp, die brauchbar sind als diagnostische Sonden und Primer, wie
voranstehend und ausführlicher
nachstehend besprochen. Größere DNA-Fragmente,
bis zu zum Beispiel 500 bp Länge
sind auch als Sonden gemäß der vorliegenden
Erfindung brauchbar. Unter einem Fragment von mindestens 20 bp Länge sind
zum Beispiel, Fragmente zu verstehen, welche 20 oder mehr aufeinanderfolgende
Basen aus der Nucleotidsequenz der hinterlegten cDNA oder der Nucleotidsequenz,
wie in 1 (SEQ ID NO:1) gezeigt, umfassen.
Wie angezeigt, sind solche Fragmente entweder als Sonde gemäß konventioneller
DNA-Hybridisierungsmethoden oder als Primer zur Amplifizierung einer
Zielsequenz durch die Polymerasekettenreaktion (PCR) diagnostisch
brauchbar.
-
Da
das Gen hinterlegt wurde und die in 1 (SEQ
ID NO:1) gezeigte Nucleotidsequenz bereitgestellt wurde, würde das
Herstellen solcher DNA-Fragmente
für den
Fachmann auf dem relevanten Fachgebiet Routine sein. Die Restriktionsendonuclease-Spaltung
oder das Scheren durch Ultraschallbehandlung können zum Beispiel leicht verwendet
werden, um Fragmente von verschiedenen Größen herzustellen. Anderenfalls
können
die DNA-Fragmente der vorliegenden Erfindung synthetisch hergestellt
werden gemäß der bekannten
und für
Fachmänner
erhältlichen
Verfahren und Methoden. Zehn exprimierte Sequenzmarker („tags") mit Homologie zu
einem Teil der TIF-2-Nucleotidsequenz wurden von den Erfindern in
GenBank identifiziert: GenBank Zugangsnummern T77249, R77864, T77464,
R77770, R08880, T85560, R25318, T85561, R08986 und R26517.
-
Darüber hinaus
werden Varianten der Nucleinsäuremoleküle der vorliegenden
Erfindung beschrieben, die für
Fragmente, Analoga oder Derivate des TIF2-Proteins codieren, z.B.
Polypeptide, die eine zu dem beschriebenen TIF2-Protein im wesentlichen ähnliche
biologische Aktivität
haben. Varianten können
natürlich vorkommen,
wie Isoformen und allelische Varianten. Nicht natürlich vorkommende
Varianten können
unter Verwendung einer beliebigen der Mutagenese-Methoden hergestellt
werden, die den Fachmännern
bekannt und erhältlich
sind.
-
Solche
Varianten beinhalten jene, die durch Nucleotidsubstitutionen, -deletionen
oder -additionen hergestellt werden. Die Substitutitionen, Deletionen
oder Additionen können
ein oder mehr Nucleotide einbeziehen. Die Varianten können in
den codierenden oder nicht-codierenden Regionen oder in beiden geändert werden. Änderungen
in den codierenden Regionen können
konservative oder nicht konservative Aminosäuresubstitutionen, -deletionen
oder -additionen herstellen. Besonders bevorzugt unter diesen sind
stille Substitutionen, Additionen und Deletionen, die nicht die
Eigenschaften und Aktivitäten
des TIF2-Proteins oder des Fragments davon ändern. Auch besonders in diesem
Zusammenhang bevorzugt sind konservative Substitutionen.
-
Die
vorliegende Erfindung ist weiter auf Nucleinsäuremoleküle gerichtet, die ein cytoplasmatisches TIF2-Polypetid
codieren. Volllängen-TIF2
ist ein nucleares Protein auf Grund der Anwesenheit von N-terminalen
nuclearen Lokalisierungssignalen (NLSs) (3).
Unter einem „cytoplasmatisches
TIF2-Polypetid" ist
ein TIF2-Polypetid
zu verstehen, das hauptsächlich
in dem Cytoplasma gefunden wird, nachdem es rekombinant in Säugetierzellen
exprimiert wird. Verfahren zur Herstellung von Nucleinsäuremolekülen, die
ein cytoplasmatisches TIF2-Polypetid codieren, beinhalten Mutieren
oder Deletieren der NLSs-codierenden N-terminalen Region der in 1 gezeigten Nucleotidsequenz (SEQ ID NO:1).
Beispiele von NLS-Sequenzen umfassen Aminosäuren 13-20 und 31-39 und Nucleotide
199-222 und 253-279 von 1 (S. auch 3). Passende Mutationen an der NLSs-codierenden N-terminalen
Region beinhalten Substitutionen, Deletionen und Insertionen, die
zu einem Nucleinsäuremolekül führen, das
ein TIF2-Polypetid codiert, dem die nucleare Lokalisierungsfunktion
fehlt. Verfahren zur Herstellung solcher Mutationen werden für den Fachmann
leicht ersichtlich werden und sind beschrieben, zum Beispiel, in
Molecular Cloning, A Laboratory Manual, 2. Ausgabe, herausgegeben
von Sambrook, J., Fritsch, E.F. und Maniatis, T., (1989), Cold Spring
Harbor Laboratory Press.
-
Vorzugsweise
werden die Nucleinsäuremoleküle, die
ein cytoplasmatisches TIF2-Polypetid codieren, Fragmente mit einer
Deletion in allen oder einem Teil der N-terminalen NLSs codierenden Region sein.
Verfahren zur Herstellung solcher Fragmente werden nachstehend beschrieben.
Gemäß der vorliegenden
Erfindung beinhalten solche Nucleinsäurefragmente weiter N-terminate
Deletionen, die sich außerhalb
der NLSs codierenden Region erstrecken, und können auch C-terminale Deletionen
beinhalten. Zum Beispiel haben die anwesenden Erfinder ein Nucleinsäuremolekül hergestellt,
das das cytoplasmatische TIF2.1-Polypetid (Aminosäuren 624
bis 1287 in 1 und 3 (SEQ
ID NO:2)) codiert, das wie das nucleare Volllängen-TIF2 auf eine Agonisten-abhängige Weise
mit den nuclearen Rezeptoren interagiert und die durch den nuclearen
Rezeptorvermittelte Transkriptionsaktivierung erhöht. Die
gegenwärtigen
Erfinder stellten auch ein Nucleinsäuremolekül her, das das cytoplasmatische
TIF2.5-Polypeptid (Aminosäuren
624-869 in den 1 und 3 (SEQ
ID NO:2)) codiert, das mit der NID-Domäne von nuclearen Rezeptoren
interagiert, aber nicht die Transkription erhöht. Auch wurden Nucleinsäuremoleküle hergestellt,
die die cytoplasmatischen TIF2.8- und TIF 2.12-Polypeptide (jeweils
die Aminosäuren
1010-1179 und Aminosäuren
940-1131 in den 1 und 3 (SEQ
ID NO:2)) codieren, die die Transkription erhöhen, aber nicht an nucleare
Rezeptoren binden. Demnach werden durch die Erfindung Nucleinsäuremoleküle bereitgestellt,
die die cytoplasmatischen TIF2-Polypeptide codieren, die auf eine Agonisten-abhängige Weise
mit nuclearen Rezeptoren interagieren und die durch nucleare Rezeptoren
vermittelte Transkriptionsaktivierung erhöhen. Auch werden cytoplasmatische
TIF2-Polypeptide bereitgestellt, die an nucleare Rezeptoren binden,
aber nicht die Transkription erhöhen,
während
cytoplasmatische TIF2-Polypeptide bereitgestellt werden, die die
Transkription erhöhen,
aber nicht an nucleare Rezeptoren binden. Wie der Fachmann erkennen
wird, kann die Länge
solcher Nucleinsäuremoleküle variieren.
-
Weitere
Ausführungsformen
der Erfindung beinhalten isolierte Nucleinsäuremoleküle, die ein Polynucleotid mit
einer Nucleotidsequenz umfassen, die mindestens zu 90% identisch
und bevorzugter zu mindestens 95%, 96%, 97%, 98% oder 99% identisch
ist zu: (a) der Nucleotidsequenz der als ATCC 97612 hinterlegten
cDNA; (b) der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1); (c) der Nucleotidsequenz der als ATCC 97612 hinterlegten
cDNA, die das TIF2-Protein von ganzer Länge codiert; (d) der in 1 gezeigten Nucleotidsequenz (SEQ ID NO:1),
die das Volllängen-TIF2-Protein
codiert; (e) der Nucleotidsequenz der als ATCC 97612 hinterlegten
cDNA, die das funktionelle Coaktivator-TIF2.1-Protein codiert; (f)
der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1), die das funktionelle Coaktivator TIF2.1-Protein codiert;
(g) der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1), die das TIF2.0-Polypeptid codiert; (h) der in 1 gezeigten Nucleotidsequenz (SEQ ID NO:1),
die das TIF2.2-Polypeptid codiert; (i) die in 1 gezeigte
Nucleotidsequenz (SEQ ID NO:1), die das TIF2.3-Polypeptid codiert;
(j) der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1), die das TIF2.4-Polypeptid
codiert; (k) der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1), die das TIF2.5-Polypeptid codiert; (l) der in 1 gezeigten Nucleotidsequenz (SEQ ID NO:1),
die das TIF2.6-Polypeptid codiert; (m) der in 1 gezeigten
Nucleotidsequenz (SEQ ID NO:1), die das TIF2.7-Polypeptid codiert; (n)
der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1), die das TIF2.8-Polypeptid codiert; (o) der in 1 gezeigten Nucleotidsequenz (SEQ ID NO:1),
die das TIF2.9-Polypeptid codiert; (p) der in 1 gezeigten
Nucleotidsequenz (SEQ ID NO:1), die das TIF2.10-Polypeptid codiert;
(q) der in 1 gezeigten Nucleotidsequenz
(SEQ ID NO:1), die das TIF2.12-Polypeptid codiert und (r) einer
Nucleotidsequenz, die komplementär
zu einer beliebigen der Nucleotidsequenzen in (a-q) ist.
-
Ob
zwei beliebige Nucleinsäuremoleküle Nucleotidsequenzen
haben, die mindestens zu 90%, 95%, 96%, 97%, 98% oder 99% „identisch" sind, kann konventionell
unter Verwendung bekannter Computeralgorithmen wie des „fastA"-Programms ermittelt werden zum Beispiel
unter Verwendung der Standardparameter (Pearson und Lipman, Proc.
Natl. Acad. Sci. USA 85:2444 (1988)). Die vorliegende Anmeldung
ist auf solche Nucleinsäuremoleküle gerichtet
mit einer Nucleotidsequenz, die mindestens zu 90%, 95%, 96%, 97%,
98%, 99% identisch zu der Nucleotidsequenz der voranstehend vorgetragenen
Nucleinsäuremoleküle ist,
unabhängig
davon ob sie ein Polypeptid mit TIF2-Aktivität codieren. Dies deshalb, weil
sogar wenn ein bestimmtes Nucleinsäuremolekül nicht ein Polypeptid mit
TIF2-Aktivität codiert,
ein Fachmann noch wissen würde,
wie das Nucleinsäuremolekül als Sonde
verwendet wird. Verwendungen von Nucleinsäuremolekülen der vorliegenden Erfindung,
die nicht ein Polypeptid mit TIF2-Aktivität codieren, beinhalten unter
anderem (1) Isolieren des TIF2-Gens oder allelische Varianten davon
in einer cDNA-Bank;
(2) in situ-Hybridisierung (FISH) zur Chromosomenspreitung in der
Metaphase, um den genauen Ort des TIF2-Gens auf dem Chromosom zu
liefern, wie beschrieben in Verma et al., Human Chromosomes: a Manual
of Basic Techniques, Pergamon Press, New York (1988); und Northern-Blot-Analyse
zum Nachweis der TIF2-mRNA-Expression in spezifischen Geweben, wie
dem Plazenta-Gewebe.
-
Jedoch
werden Nucleinsäueremoleküle bevorzugt
mit einer Nucleotidsequenz, die mindestens zu 90% und bevorzugter
zu mindestens 95%, 96%, 97%, 98% oder 99% identisch mit der Nucleotidsequenz
der voranstehend beschriebenen Nucleinsäuremolekülen ist, die tatsächlich ein
Polypeptid mit mindestens einer TIF2-Protein-Aktivität codieren. Wie hierin verwendet,
sind unter „ein
Polypeptid mit einer TIF2-Protein-Aktivität", Polypeptide zu verstehen, die eine ähnliche,
aber nicht notwendigerweise identische Aktivität aufweisen, wie mindestens
eine biologische Aktivität
des TIF2-Proteins, wie in einem besonderen biologischen Assay gemessen
wird. Zum Beispiel interagiert das TIF2-Protein der vorliegenden
Erfindung direkt auf eine Agonisten-abhängige Weise mit den Liganden
bindenden Domänen
von mehreren nuclearen Rezeptoren. Außerdem erhöht das TIF2-Protein der vorliegenden
Erfindung die Transkription über
CBP-abhängige
und CBP-unabhängige Routen,
wenn es rekombinant in Säugetierzellen
exprimiert wird.
-
Demnach
beinhaltet „ein
Polypeptid mit einer TIF2-Protein-Aktivität" Polypetide mit einer oder mehr der
folgenden Aktivitäten:
Interaktion mit der LBD von einem oder mehr NRs auf eine Agonisten-abhängige Weise;
Verstärkung
von CBP-abhängiger Transkriptionsaktivierung
oder Verstärkung
von CBP-unabhängiger Transkriptionsaktivierung.
-
Durchmusterungsassays
zur Ermittlung, ob ein Kandidaten-Polypeptid TIF2-Protein-Aktivität hat, werden
ausführlich
in den Beispielen 1, 3, 4 und 6, nachstehend, beschrieben. Zum Beispiel
entdeckten die Erfinder beim Durchführen solcher Assays, dass das
funktionelle Coaktivator-Fragment TIF2.1 (Aminosäuren 624 bis 1287 in den 1 und 3 (SEQ
ID NO:2)) „ein
Polypeptid mit einer TIF2-Protein-Aktivität" ist. Die gegenwärtigen Erfinder entdeckten
auch, dass das Fragment TIF2.5 (Aminosäuren 624-869) an die LBD von
NRs ohne Aktivierung der Transkription bindet und „ein Polypeptid
mit einer TIF2-Protein-Aktivität" ist. Auch entdeckt
wurde das Fragment TIF2.2 (Aminosäuren 1288-1464, wie in 1 (SEQ ID NO:2) gezeigt), das die CBP-unabhängige Transkription
erhöht.
Demnach ist TIF2.2 „ein
Polypeptid mit einer TIF2-Protein-Aktivität". Ein anderes Fragment wurden von den
Erfindern entdeckt, TIF 2.8 (Aminosäuren 1010-1179, wie in 1 (SEQ ID NO:2) gezeigt) ist „ein Polypeptid
mit einer TIF2-Protein-Aktivität", da es die CBP-abhängige Transkription
aktiviert.
-
Auf
Grund der Degeneriertheit des genetischen Codes wird ein normaler
Fachmann sofort erkennen, dass eine große Anzahl von Nucleinsäuremolekülen mit
einer Nucleotidsequenz, die mindestens zu 90%, vorzugsweise mindestens
zu 95%, 96%, 97%, 98%, 99% identisch mit der Nucleotidsequenz der
voranstehend beschriebenen Nucleinsäuremoleküle ist, „ein Polypeptid mit einer
TIF2-Protein-Aktivität" codieren wird. Tatsächlich wird
dies dem Fachmann sogar ohne Durchführung des voranstehend beschriebenen
Durchmusterungsassays deutlich werden, da die degenerierten Varianten
alle das gleiche Polypeptid codieren. Es wird von den Fachmännern weiter
erkannt werden, dass für
solche Nucleinsäuremoleküle, die
nicht degenerierte Varianten sind, eine angemessene Anzahl auch
ein Polypeptid mit einer TIF2-Protein-Aktivität codieren wird. Dies deshalb,
weil der Fachmann jede mögliche
Aminosäuresubstitution
kennt, welche die Proteinfunktion entweder weniger wahrscheinlich
oder nicht wahrscheinlich signifikant beeinflusst (z.B. Austauschen
von einer aliphatischen Aminosäure
mit einer zweiten aliphatischen Aminosäure).
-
Die
Anleitung hinsichtlich der Herstellung von phänotypisch „stillen" Aminosäuresubstitutionen wird zum
Beispiel bereitgestellt in J.U. Bowie et al., „Deciphering the Message in
Protein Sequences: Tolerance to Amino Acid Substitutions," Science 247:1306-1310
(1990), worin die Autoren anzeigen, dass es zwei hauptsächliche
Herangehensweisen zum Studieren der Toleranz einer Aminosäuresequenz
gegenüber
deren Austausch gibt. Das erste Verfahren beruht auf dem Evolutionsprozess,
bei dem Mutationen durch die natürliche Selektion
entweder angenommen oder abgelehnt werden. Die zweite Herangehensweise
verwendet die Gentechnik, um einen Aminosäureaustausch an spezifischen
Positionen eines klonierten Gens einzubringen, und Selektionen oder
Durchmusterungen, um Sequenzen zu identifizieren, die die Funktionalität beibehalten.
Wie die Autoren feststellten, offenbarten diese Studien, dass Proteine überraschenderweise
tolerant gegenüber Aminosäuresubstitutionen
sind. Die Autoren zeigen weiter an, welcher Aminosäureaustausch
wahrscheinlich tolerant an einer bestimmten Position des Proteins
ist. Zum Beispiel benötigen
die meisten verdeckten Aminosäurereste
unpolare Seitenketten, während
einige Merkmale der Oberflächenseitenketten
allgemein konserviert sind. Andere solche phänotypisch stillen Substitutionen
sind beschrieben in Bowie et al., oben, und in den darin zitierten
Literaturhinweisen.
-
Vektoren und
Wirtszellen
-
Die
vorliegende Erfindung bezieht sich auch auf Vektoren, die die DNA-Moleküle der vorliegenden
Erfindung beinhalten, Wirtszellen, die mit den rekombinanten Vektoren
genetisch manipuliert werden, und die Herstellung von TIF2-Polypeptiden
oder Fragmenten davon, wie TIF2.1, durch rekombinante Methoden.
-
Rekombinante
Konstrukte können
in Wirtszellen unter Verwendung gut bekannter Methoden eingebracht
werden wie Infektion, Transduktion, Transfektion, Transvection,
Elektroporation und Transformation. Der Vektor kann zum Beispiel
ein Phage, ein Plasmid, ein viraler oder ein retroviraler Vektor
sein. Retrovirale Vektoren können
replikationsbefähigt
oder replikationsgestört
sein. In dem letzteren Fall wird die virale Fortpflanzung allgemein
nur in ergänzenden
Wirtszellen vorkommen.
-
Die
Polynucleotide können
mit einem Vektor verbunden werden, der einen selektierbaren Marker
zur Fortpflanzung in einem Wirt enthält. Allgemein wird ein Plasmidvektor
in ein Präzipitat
eingebracht, wie Calciumphosphatpräzipitat, oder in einen Komplex
mit einem geladenen Lipid. Wenn der Vektor ein Virus ist, kann er
in vitro unter Verwendung einer geeigneten Verpackungszelllinie
verpackt werden und dann in Wirtszellen transduziert werden.
-
Bevorzugt
werden Vektoren, die cis-agierende Kontrollregionen zu dem Polynucleotid
von Interesse umfassen. Geeignete trans-agierende Faktoren können vom
Wirt, vom ergänzenden
Vektor oder vom Vektor selbst beim Einbringen in den Wirt geliefert
werden.
-
In
bestimmten bevorzugten Ausführungsformen
in dieser Hinsicht gewährleisten
die Vektoren die spezifische Expression, die induzierbar und/oder
Zelltyp-spezifisch sein kann. Besonders bevorzugt unter solchen Vektoren
sind jene, die durch umgebende Faktoren, die leicht zu manipulieren
sind, wie Temperatur und Nährstoffzusätze, induzierbar
sind.
-
In
der vorliegenden Erfindung brauchbare Expressionsvektoren beinhalten
chromosomal-, episomal- und Virus-abgeleitete Vektoren, z.B. Vektoren,
die aus bakteriellen Plasmiden, Bakteriophagen, Hefeepisomen, chromosomalen
Elementen der Hefe, Viren, wie Baculoviren, Papovaviren, Vacciniaviren,
Adenoviren, Fowlpoxviren, Pseudoarabiesviren und Retroviren, abgeleitet
werden, und Vektoren, die aus Kombinationen davon abgeleitet werden,
wie Cosmide und Phagemide.
-
Das
DNA-Insert sollte funktionell mit einem geeigneten Promotor verbunden
sein, wie mit dem Phage-lambda-PL-Promotor, den lac-, trp- und tac-Promotoren
von E. coli, den frühen
und späten
Promotoren von SV40 und den Promotoren der retroviralen LTRs, um
einige zu nennen. Andere passende Promotoren werden dem Fachmann
bekannt sein. Die Expressionskonstrukte werden weiter Stellen zum
Transkriptionsstart, -stopp und in der transkribierten Region eine
Ribosom bindende Stelle zur Translation enthalten. Der codierende
Anteil der reifen Transkripte, die durch die Konstrukte exprimiert
werden, werden vorzugsweise ein Translation startendes AUG am Anfang
und ein Stoppcodon (UAA, UGA oder UAG), das geeigneterweise am Ende
des zu translatierenden Polypeptids positioniert ist, beinhalten.
-
Wie
angezeigt, werden die Expressionsvektoren vorzugsweise mindestens
einen selektierbaren Marker beinhalten. Solche Marker beinhalten
Dihydrofolat-Reduktase
oder Neomycin-Resistenz für
die eurkayontische Zellkultur und Tetracyclin- oder Ampicillin-Resistenzgene
zum Züchten
in E. coli und anderen Bakterien. Repräsentative Beispiele von geeigneten
Wirten beinhalten, aber sind nicht begrenzt auf, Bakterienzellen,
wie E. coli-, Streptomyces- und Salmonella typhimurium-Zellen; Pilzzellen
wie Hefezellen; Insektenzellen wie Drosophila S2- und Spodoptera
Sf9-Zellen; Tierzellen wie CHO, Cos und Bowes Melanomzellen; und
Pflanzenzellen. Geeignete Kulturmedien und Bedingungen für die voranstehend
beschriebenen Wirtszellen sind auf dem Fachgebiet bekannt.
-
Veranschaulichende
Beispiele von für
die Verwendung in Bakterien bevorzugte Vktoren beinhalten, aber
sind nicht begrenzt auf, pA2, pQE70, pQE60 und pQE-9, erhältlich von
Qiagen; pBS-Vektoren, Phagescript-Vektoren, Bluescript-Vektoren, PNH8A,
pNH16a, pNH18A, pNH46A,, erhältlich
von Stratagene; und ptrc99a, pKK223-3, pKK233-3, pDR540, pRIT5,
erhältlich
von Pharmacia. Bevorzugte eukaryontische Vektoren beinhalten, aber
sind nicht begrenzt auf, pWLNEO, pSV2CAT, pOG44, pXT1 und pSG, erhältlich von
Stratagene; und pSVK3, pBPV, pMSG und pSVL, erhältlich von Pharmacia. Andere
geeignete Vektoren werden dem Fachmann leicht ersichtlich werden.
-
Unter
den bekannten bakteriellen Promotoren, die passend für die Verwendung
in der vorliegenden Erfindung sind, befinden sich die lacI- und
IacZ-Promotoren von E. coli, die T3- und T7-Promotoren, der gpt-Promotor,
die lambda-PR- und PL-Promotoren
und der trp-Promotor. Passende eukaryontische Promotoren beinhalten
den unmittelbar frühen
Promotor von CMV, den HSV-Thymidinkinase-Promotor, die frühen und späten SV40-Promotoren,
die Promotoren der retroviralen LTRs, wie jene des Rous-Sarcomavirus
(„RSV") und Metallothionein-Promotoren,
wie den Metallothionein-I-Promotor der Maus.
-
Das
Einbringen des Konstrukts in die Wirtszelle kann durch Calciumphosphat-Transfektion, DEAE-Dextran-vermittelte
Transfektion, kationisches Lipid-vermittelte Transfektion, Elektroporation,
Transduktion, Infektion oder anderen Verfahren bewirkt werden. Solche
Verfahren sind in vielen Standard-Laborhandbüchern beschrieben, wie in Davis
et al., Basic Methdods in Molecular Biology (1986).
-
Die
Transkription der DNA, die die Polypeptide der vorliegenden Erfindung
durch höhere
Eukaryonten codiert, kann durch Einfügen einer Verstärkersequenz
in den Vektor gesteigert werden. Verstärker sind cis-agierende Elemente
der DNA, allgemein etwa 10 bis 300 bp an Größe, die wirken, um die Transkriptionsaktivität eines
Promotors in einem gegebenen Wirtszelltyp zu steigern. Veranschaulichende
Beispiele von Verstärkern
beinhalten, aber sind nicht begrenzt auf, den SV40-Verstärker, der
an der späten
Seite des Replikationsursprungs bei bp 100 bis 270 gelegen ist,
der frühe
Promotor-Verstärker
des Cytomegalievirus, der Polyoma-Verstärker an der späten Seite
des Replikationsursprungs und die Adenovirus-Verstärker.
-
Zur
Sekretion des translatierten Proteins in das Lumen des endoplasmatischen
Retikulums, in den Periplasmaraum oder in die extrazelluläre Umgebung
können geeignete
Sekretionssignale in das exprimierte Polypeptid eingebaut werden.
Die Signale können
zum Polypeptid endogen sein oder sie können heterologe Signale sein.
-
Das
Polypeptid kann in einer modifizierten Form exprimiert werden, wie
ein Fusionsprotein, und kann nicht nur Sekretionssignale, sondern
auch zusätzliche
heterologe funktionelle Regionen beinhalten. Demnach kann zum Beispiel
eine Region von zusätzlichen
Aminosäuren,
besonders von geladenen Aminosäuren,
zu dem N-Terminus des Polypeptids angefügt werden, um die Stabilität und Persistenz
in der Wirtszelle während der
Aufreinigung oder während
der nachfolgenden Bearbeitung und Lagerung zu verbessern. Auch können Peptidteile
an das Polypeptid angefügt
werden, um die Aufreinigung zu erleichtern.
-
Das
TIF2-Protein oder die Fraktion davon kann aus rekombinanten Zellkulturen
durch gut bekannte Verfahren wieder hergestellt und aufgereinigt
werden, einschließlich
der Präzipitation
mit Ammoniumsulfat oder Ethanol, der sauren Extraktion, der Anionen-
oder Kationenaustausch-Chromatographie, der Phosphocellulose-Chromatographie,
der hydrophoben Interaktionschromatographie, der Affinitätschromatographie,
der Hydroxylapatit-Chromatographie und der Lectin-Chromatographie.
Am meisten bevorzugt wird die Hochleistungsflüssigkeitschromatographie („HPLC") zur Aufreinigung
verwendet.
-
Die
Polypeptide der vorliegenden Erfindung beinhalten, aber sind nicht
begrenzt auf natürlich
aufgereinigte Produkte, Produkte von chemischen synthetischen Prozeduren
und Produkte, die durch rekombinante Methoden aus einem prokaryontischen
oder eukaryontischen Wirt hergestellt werden, einschließlich zum
Beispiel Bakterien-, Hefe-, höhere
Pflanzen- Insekten- und Säugetierzellen.
Abhängig
von dem in einer rekombinanten Herstellungsprozedur verwendeten
Wirt können
die Polypeptide der vorliegenden Erfindung posttranslational modifiziert
(z.B. glycosyliert, phosphoryliert, farnesyliert usw.) werden. Zusätzlich können die
Polypeptide der Erfindung auch einen anfänglichen modifizierten Methioninrest
beinhalten, bei einigen Fällen
als ein Ergebnis von Wirt-vermittelten Prozessen.
-
TIF2-Polypeptide und -Fragmente
-
Die
Erfindung stellt weiter ein TIF2-Polypeptid mit der Aminosäuresequenz
bereit, die durch die hinterlegte cDNA codiert wird, oder der Aminosäuresequenz,
wie in 1 (SEQ ID NO:2) gezeigt, oder
ein Fragment davon. Bevorzugte Polypeptid-Fragmente werden eine TIF2-Protein-Aktivität haben.
Um für
ein TIF2-Polypeptidfragment
auf eine Agonisten-abhängige
Weise mit den nuclearen Rezeptoren zu interagieren und die durch den
nuclearen Rezeptor vermittelte Transkriptionsaktivierung zu erhöhen, sollten
solche TIF2-Polypeptidfragmente mindestens die Aminosäurereste
624 bis 1131 beinhalten, wie in 1 (SEQ
ID NO:2) gezeigt, oder Aminosäuresubstitutionen,
-additionen oder -deletionen davon, die nicht signifikant nachteilig
für die
Fähigkeit der
Polypeptide sind, auf eine Agonisten-abhängige Weise mit den nuclearen
Rezeptoren zu interagieren und die durch den nuclearen Rezeptor
vermittelte Transkriptionsaktivierung zu erhöhen. Um für ein TIF2-Polypeptidfragment
mit der LBD eines NR ohne Aktivierung der Transkription zu interagieren,
sollten die TIF2-Polypeptidfragmente mindestens die Aminosäuren 624-869
beinhalten, wie in 1 (SEQ ID NO:2)
gezeigt, oder Aminosäuresubstitutionen,
-additionen oder -deletionen davon, die nicht signifikant nachteilig
für die
Fähigkeit
der Polypeptide sind, mit der LBD eines NRs zu interagieren. Um
für ein
TIF2-Polypeptidfragment die CBP-abhängige Transkription zu aktivieren,
sollte das TIF2-Polypeptid mindestens die Aminosäurereste 1010-1131 beinhalten,
wie in 1 (SEQ ID NO:2) gezeigt, oder
Aminosäuresubstitutionen,
-additionen oder -deletionen davon, die nicht signifikant nachteilig
für die
Fähigkeit
der Polypeptide sind, die CBP-abhängige Transkription zu aktivieren.
Um für
ein TIF2-Polypetid
die CBP-unabhängige
Transkription zu aktivieren, sollte das TIF2-Polypeptid mindestens die Aminosäurereste
1288-1464 beinhalten, wie in 1 (SEQ
ID NO:2) gezeigt, oder Aminosäuresubstitutionen,
-additionen oder -deletionen davon, die nicht signifikant nachteilig
für die
Fähigkeit
der Polypeptide sind, die CBP-unabhängige Transkription
zu aktivieren.
-
Beispielhafte
TIF2-Polypeptidfragmente gemäß der vorliegenden
Erfindung beinhalten cytoplasmatische TIF2-Polypeptide mit mindestens
einer Mutation oder Deletion in einer N-terminalen NLS-Region, die
die nucleare Lokalisierungsfunktion beeinträchtigt. Verfahren zur Herstellung
von cytoplasmatischen TIF2-Polypeptiden sind voranstehend beschrieben.
-
Wie
hierin verwendet, ist unter einem „isoliertes" Polypeptid oder
Protein ein Polypeptid oder Protein zu verstehen, das aus seiner
natürlichen
Umgebung entfernt wurde, wie rekombinant hergestellte Polypeptide und
Proteine, die in Wirtszellen exprimiert werden, und natürliche oder
rekombinante Polypeptide, die durch eine beliebige passende Methode
wesentlich aufgereinigt wurden (z.B. das Einzelschritt-Aufreinigungsverfahren,
das in Smith und Johnson, Gene 67:31-40 (1988) bekannt gegeben wird,
das hierin durch Literaturhinweis berücksichtigt wird). Isolierte
Polypeptide oder Proteine gemäß der vorliegenden
Erfindung beinhalten weiter solche synthetisch hergestellten Verbindungen.
-
Die
gegenwärtigen
Erfinder entdeckten, dass das Volllängen-TIF2-Protein ein Protein
von etwa 1464 Aminosäureresten
ist mit einem abgeleiteten Molekulargewicht von etwa 160 kDa. Es
wird von den Fachmännern
erkannt werden, dass manches der Aminosäuresequenz des TIF2-Protein
ohne signifikante Wirkung auf die Struktur oder die Funktion des
Proteins variiert werden kann. Wenn solche Unterschiede in der Sequenz betrachtet
werden, sollte daran gedacht werden, dass es entscheidende Bereiche
an dem Protein geben wird, die die Aktivität bestimmen, wie die voranstehend
beschriebene Region, die von den Erfindern als entscheidend für die Fähigkeit
des Proteins, die nuclearer Rezeptor-vermittelte Transkriptionsaktivierung
zu erhöhen, bestimmt
wurde. Im Allgemeinen ist es oft möglich, Reste zu ersetzen, die
die Tertiärstruktur
bilden, vorausgesetzt dass die Reste venrwendet werden, die eine ähnliche
Funktion durchführen.
Bei anderen Umständen kann
der Typ des Rests vollständig
unwichtig sein, wenn die Änderung
in einer nicht-entscheidenden Region des Proteins vorkommt.
-
Demnach
beinhaltet die vorliegende Offenbarung weiter Variationen des TIF2-Polypeptids, die
wesentliche TIF2-Polypeptid-Aktivität zeigen oder die Regionen
des TIF2-Proteins umfassen, wie die nachstehend besprochenen Proteinfragmente.
Solche Mutanten beinhalten Deletionen, Insertionen, Inversionen,
Wiederholungen und Typsubstitutionen (zum Beispiel Austausch eines
hydrophilen Rests mit einem anderen, aber in der Regel nicht stark
hydrophilen für
einen stark hydrophoben). Kleine Änderungen oder solche „neutralen" Aminosäuresubstitutionen
werden allgemein kaum Wirkung auf die Aktivität haben.
-
Typisch
als konservative Substitutionen betrachtet werden Austausche, eine
für eine
andere, unter den aliphatischen Aminosäuren Ala, Val, Leu und Ile;
Austausch der Hydroxylreste Ser und Thr; Austausch der sauren Reste
Asp und Glu, Substitution zwischen den Amidresten Asn und Gln, Austausch
der basischen Reste Lys und Arg und Austausche unter den aromatischen
Resten Phe und Tyr.
-
Wie
voranstehend ausführlich
darauf hingewiesen wurde, kann eine weitere Anleitung hinsichtlich
darauf, welche Aminosäureänderungen
wahrscheinlich phänotypisch
still sind, (d.h. bei welchen es nicht wahrscheinlich ist, dass
sie eine signifikant schädliche
Wirkung auf eine Funktion haben) gefunden werden in Bowie et al., „Deciphering
the Message in Protein Sequences: Tolerance to Amino Acid Substitutions," Science 247:1306-1310
(1990)).
-
Die
Polypeptide der vorliegenden Erfindung beinhalten Polypeptide mit
einer Aminosäuresequenz,
wie durch die hinterlegte cDNA codiert, einer Aminosäuresequenz,
wie in SEQ ID NO:2 gezeigt, sowie einer Aminosäuresequenz, die mindestens
zu 90% identisch und bevorzugter zu mindestens 95%, 96%, 97%, 98%
oder 99% identisch ist zu der von der hinterlegten cDNA codierten
Aminosäuresequenz,
zu der Aminosäuresequenz,
wie in SEQ ID NO:2 gezeigt oder zu der Aminosäuresequenz eines voranstehend
beschriebenen Polypeptidfragments. Ob zwei Polypeptide eine Aminosäuresequenz
haben, die mindestens 90% oder 95% identisch ist, kann unter Verwendung
eines Computeralgorithmus ermittelt werden, wie voranstehend beschrieben.
-
Wie
nachstehend ausführlich
beschrieben, sind die Nucleinsäuremoleküle und Polypeptide
der vorliegenden Erfindung brauchbar bei Durchmusterungsassays zum
Identifizieren von Agonisten und Antagonisten einer NR-AF2-vermittelten
Transaktivierung. Zum Beispiel zeigen in Halachmi, S., et al., Science
264: 1455 (1994) die Autoren, dass Tamoxifen, das wachstumshemmende
Wirkungen bei Brustkrebs hat, die Bildung eines Komplexes, der den Östrogenrezeptor
und ERAP160 beinhaltet, unterbricht. Demgemäß sind die Nucleinsäuremoleküle und Polypeptide
der vorliegenden Erfindung brauchbar in Assays zum Identifizieren
von Arzneistoffen, die in der Lage sind, nuclearer Rezeptor-vermittelte
Signalwege zu verstärken
oder zu hemmen.
-
Die
Nucleinsäuremoleküle und Polypeptide
der vorliegenden Erfindung sind brauchbar bei Durchmusterungsassays
zum Identifizieren von Agonisten und Antagonisten der TIF2-AD1-Aktivität, und in
Durchmusterungsassays zum Identifizieren von Agonisten und Antagonisten
der TIF2-AD2-Aktivität,
wie nachstehend ausführlich
beschrieben.
-
Durchmusterungsverfahren
-
Nucleare
Rezeptoren (NRs) sind Mitglieder einer Superfamilie von Liganden
induzierbaren transkriptionalen regulatorischen Faktoren, die Steroidhormon,
Thyroidhormon, Vitamin D3 und Retinoidrezeptoren beinhalten (Leid,
M., et al., Trends Biochem. Sci. 17:427-433 (1992); Leid, M. et
al., Cell 68:377-395 (1992); und Linney, E. Curr. Top. Dev. Biol.,
27:309-350 (1992)). NRs weisen eine modulare Struktur auf, die die
Existenz von mehreren unabhängigen
funktionellen Domänen
widerspiegelt. Auf Grundlage der Ähnlichkeit der Aminosäuresequenz
zwischen dem Östrogenrezeptor
des Huhns, dem menschlichen Östrogen-
und Glucocorticoidrezeptor und dem v-erb-A-Onkogen definierten Krust,
A. et al., EMBO J: 5:891-897 (1986), sechs Regionen, A, B, C, D,
E und F (s. 6), die verschiedene Ausmaße evolutionärer Konservierung
unter verschiedenen Mitgliedern der nuclearer Rezeptor-Superfamilie
darstellen. Die hoch konservierte Region C enthält zwei Zinkfinger und entspricht
dem Kernstück
der DNA-bindenden Domäne
(DBD), die für
die spezifische Erkennung der verwandten Response-Elemente verantwortlich
ist. Region E ist funktionell komplex, da sie zusätzlich zur Liganden-bindenden
Domäne
(LBD) eine Liganden-abhängige
Aktivierungsfunktion (AF-2) und eine Dimerisierungsgrenzfläche enthält. Eine
unabhängige
transkriptionale Aktivierungsfunktion (AF-1) ist in den nicht-konservierten
N-terminalen A/B-Regionen
der Steroidrezeptoren vorhanden. Interessanterweise weisen sowohl
AF-1 als auch AF-2 der Steroidrezeptoren unterschiedliche Transkriptionsaktivierungseigenschaften auf,
die sowohl für
den Zelltyp als auch für
den Promotorzusammenhang spezifisch erscheinen (Gronemeyer, H. Annu.
Rev. Genet. 25:89-123 (1991)).
-
Die
all-trans (T-RA)- und 9-cis (9C-RA)-Retinolsäure-Signale werden von zwei
Familien von nuclearen Rezeptoren transduziert, RAR α, β und γ (und ihre
Isoformen) werden von sowohl T-RA als auch 9C-RA aktiviert, während RXR α, β und γ ausschließlich von
9C-RA aktiviert werden (Allenby, G. et al., Proc. Natl. Acad.
-
Sci.
USA 90:30-34 (1993)). Die drei RAR-Typen unterscheiden sich in ihren
B-Regionen, und
ihre hauptsächlichen
Isoformen (α1
und α2, β1-4 und γ1 und γ2) haben
unterschiedliche N-terminale A-Regionen (Leid, M. et al., Trends
Biochem. Sci. 17:427-433 (1992)). Gleichermaßen unterscheiden sich die
RXR-Typen in ihren A/B-Regionen (Mangelsdorf, D.J. et al., Genes
Dev. 6:329-344 (1992)).
-
Es
wurde auch gezeigt, dass die E-Region der RARs und RXRs eine Dimerisierungsgrenzfläche enthalten
(Yu, V.C. et al., Curr. Opin. Biotechnol. 3:597-602 (1992)). Am interessantesten war;
dass gezeigt wurde, dass RAR/RXR-Heterodimere
viel effizienter als Homodimere von beiden Rezeptoren in vitro mit
einer Anzahl von RA Response-Elementen (RAREs) binden (Yu, V.C.
et al., Cell 67: 1251-1266 (1991); Berrodin, T.J. et al., Mol. Endocrinol
6:1468-1478 (1992); Bugge, T.H. et al., EMBO J. 11:1409-1418 (1992);
Hall, R. K. et al., Mol. Cell. Biol. 12: 5527-5535 (1992); Hallenbeck, P. L. et al.,
Proc. Natl. Acad. Sci. USA 89:5572-5576 (1992); Husmann, M. et al.,
Biochem. Biophys. Res. Commun. 187:1558-1564 (1992); Kliewer, S.A.
et al., Nature 355:446-449 (1992b); Leid, M. et al., Cell 68:377-395 (1992); Marks,
M. S. et al., EMBO J. 11:1419-1435 (1992); Zhang, X. K, et al.,
Nature 355:441-446 (1992)). RAR- und RXR-Heterodimere werden auch
vorzugsweise in vitro in Lösung
gebildet (Yu, V.C. et al., Cell 67:1251-1266 (1991); Leid, M. et
al., Cell 68:377-395 (1992); Marks, M. S. et al., EMBO J. 11:1419-1435
(1992)), obwohl die Zugabe von 9C-RA die Bildung von RXR-Homodimeren
in vitro zu erhöhen
scheint (Lehman, J.M. et al., Science 258:1944-1946 (1992); Zhang, X.K.
et al., Nature 358: 587-591 (1992b)). Dass RAR-RXR-Heterodimere,
eher als die entsprechenden Homodimere, vorzugsweise an die RAREs
in gezüchteten
Zellen in vivo binden, wurde durch Experimente stark gestützt, die
in Durand, B. et al., Cell 71:73-85 (1992) beschrieben sind.
-
Da
bekannt ist, dass Retinolsäure
die proliferativen und difterentiativen Funktionen von mehreren
Säugetier-Zelltypen
reguliert (Gudas, L.J. et al., (1994) In Sporn, M.B., Roberts, A.B.
und Goodman, D.S. (Hrsg.), The Retinoids, 2. Auflage, Raven Press,
New York, S. 443-520), werden Retinoide bei einer Vielfalt von chemopreventiven
und chemotherapeutischen Einstellungen verwendet. Die Prävention
von oralem, Haut- und Kopf- und Halskrebs bei Patienten, die für diese
Tumoren gefährdet
sind, wurde berichtet (Hong, W.K. et al., N. Engl. J. Med. 315:1501-1505
(1986); Hong, W. K. et al., N. Engl. J. Med. 323:795-801 (1990); Kraemer,
K. H. et al., N. Engl. J. Med. 318:1633-1637 (1988); Bollag, W.
et al., Ann. Oncol. 3:513-526 (1992); Chiesa, F. et al., Eur. J.
Cancer B. Oral Oncol. 28:97-102 (1992); Costa, A. et al., Cancer
Res. 54: Suppl. 7, 2032-2037 (1994)), und Retinoide werden bei der
Therapie von akuter promyelocytischer Leukämie verwendet (Huang, M.E.
et al., Blood 72: 567-572 (1988); Castaigne, S. et al., Blood 76:1704-1709
(1990); Chomienne, C. et al., Blood 76:1710-1717 (1990); Chomienne,
C. et al., J. Clin. Invest. 88:2150-2154 (1991); Chen Z. et al.,
Leukemia 5:288-292 (1991); Lo Coco, F. et al., Blood 77:165701659
(1991); Warrell, R.P., Jr. et al., N. Engl. J. Med. 324: 1385-1393
(1991), Plattenepithelkarzinom der Zervix und der Haut (Verma, A.
K., Cancer Res. 47:5097-5101 (1987); Lippman S. M. et al., J. Natl
Cancer Inst. 84:235-241 (1992); Lippman S. M. et al., J. Natl Cancer
Inst. 84:241-245 (1992)) und Kaposi-Sarkom (Bonhomme, L. et al.,
Ann. Oncol. 2:234-235 (1991)).
-
Zum
Beispiel wird in Chen, J-Y et al., EMBO J. 14(6):1187-1197 (1995)
eine Anzahl von dissoziierenden synthetischen Retinoiden charakterisiert,
die die in der LBD von RARβ (βAF-2) anwesende
AF-2 Aktivierungsfunktion selektiv induzierten. Die Autoren berichten
auch, dass diese synthetischen Retinoide, wie RA, das Wachstum unabhängig von
der Verankerung von Onkogen-transformierten 3T3-Zellen hemmen kann. Weiter wird der
Promotor des menschlichen Interleukin-6 (IL-6)-Gens, dessen Produkt bei der Regulation
der Hämatopoese,
den Immunreaktionen und der Entzündung
einbezogen wird (Kishimoto, T. et al., Science 258:593-597 (1992)),
durch die RA induziert, aber nicht durch die ,dissoziierenden` Retinoide, die seine Aktivität unterdrückten.
-
Neben
den Retinoid-Rezeptoren wurden auch Verbindungen mit agonistischen
und antagonistischen Eigenschaften auf Funktionen der Steroidrezeptoren
gemeldet. Zum Beispiel wurde in Meyer, M-E. et al., EMBO J. 9(12):3923-3932
(1990) eine vorübergehende
Expression/ein Gel-Retardations-System verwendet, um die Wirkungen
von RU486 und R5020 auf die Glucocorticoid- und Progesteron-Rezeptor-Funktion
zu studieren. Weiter wurde in Halachimi, S. et al., Science 264:1455-1458
(1994) gezeigt, dass Tamoxifen das Estradiol-induzierte ERAP160-Binden an den Östrogenrezeptor
kompetitiv hemmt, was einen Mechanismus für seine wachstumshemmende Wirkungen
bei Brustkrebs vorschlägt.
Demgemäß gibt es
wegen ihrer klinischen Wichtigkeit ein großes Interesse in der Entwicklung
von Durchmusterungsverfahren, die in der Lage sind, den Agonisten
und Antagonisten der Transaktivierung des nuclearen Rezeptors zu
identifizieren.
-
Wie
angezeigt, klonierten die gegenwärtigen
Erfinder ein Gen, das TIF2 codiert, und zeigten, dass TIF2 und ein
cytoplasmatisches Fragment davon auf eine Agonisten-abhängige Weise
an alle analysierten nuclearen Rezeptoren binden – RAR, RXR,
ER, TR, VDR, GR und AR. Weiter zeigten die gegenwärtigen Erfinder,
dass TIF2-Polypeptide Transkiptionsmediatoren des nuclearen Rezeptors
AF-2 sind. Demnach stellt die vorliegende Erfindung weiter ein Durchmusterungsverfahren
zum Identifizieren eines nuclearen Rezeptor (NR)-Antagonisten bereit,
der umfasst: (a) das Bereitstellen einer Wirtszelle, die rekombinante
Gene enthält, die
ein Polypeptid, das eine NR-Liganden-bindende Domäne (LBD)
umfasst, und ein Polypeptid, das transkriptionalen intermediären Faktor-2
(TIF-2) oder ein TIF-2-Fragment umfasst, exprimieren, wobei, in
Anwesenheit eines Agonisten, der TIF-2 und das TIF-2-Fragment die NR-LBD
binden; (b) das Verabreichen eines Kandidaten-Antagonisten an die
Zelle; und (c) das Ermitteln, ob der Kandidaten-Antagonist entweder:
(1) das TIF-2- oder TIF-2-Fragment-Binden an die AF-2 der NR-LBD,
verglichen mit dem Binden in Abwesenheit des Kandidaten-Antagonisten;
oder (2) die TIF-2- oder TIF-2-Fragment-stimulierte
NR-LBD-AF-2-vermittelte Transaktivierung, verglichen mit der Transaktivierung
in Abwesenheit des Kandidaten-Antagonisten reduziert.
-
In
einem weiteren Aspekt wird ein Durchmusterungsverfahren zum Identifizieren
eines nuclearen Rezeptor (NR)-Agonisten bereitgestellt, der umfasst:
(a) das Bereitstellen einer Wirtszelle, die rekombinante Gene enthält, die
ein Polypeptid, das eine NR-Liganden-bindende Domäne (LBD)
umfasst, und ein Polypeptid, das transkriptionalen intermediären Faktor-2
(TIF-2) oder ein TIF-2-Fragment
umfasst, exprimieren, wobei, in Anwesenheit eines Agonisten, der
TIF-2 und das TIF-2-Fragment die NR-LBD binden; (b) das Verabreichen eines
Kandidaten-Agonisten an die Zelle; und (c) das Ermitteln, ob der
Kandidaten-Agonist entweder: (1) das TIF-2- oder TIF-2-Fragment-Binden
an die AF-2 der NR-LBD, verglichen mit dem Binden in Abwesenheit
des Kandidaten-Agonisten; oder (2) die TIF-2- oder TIF-2-Fragment-stimulierte
NR-LBD-AF-2-vermittelte Transaktivierung, verglichen mit der Transaktivierung
in Abwesenheit des Kandidaten-Agonisten erhöht.
-
Unter „einer
Wirtszelle, die rekombinanten Gene umfasst" sind Wirtszellen zu verstehen, in die
ein oder mehr der hierin beschriebenen rekombinanten Konstrukte
eingebracht wurden, oder an ein Abkömmling solcher Wirtszellen.
-
Der
Kandidaten-Antagonist und -Agonist gemäß der vorliegenden Erfindung
beinhalten ,dissoziierende' Liganden
für die
nuclearen Rezeptoren wie jene, die beschrieben sind in Chen et al.,
EMBO J. 14:1187-1197 (1995) und Ostrowski et al., Proc. Natl. Acad.
Sci. USA 92:1812-1816 (1995). Progesteron- und Glucocorticoid-Rezeptor-Agonisten
und Antagonisten sind beschrieben in Meyer et al., EMBO J. 9 (12): 3923-3932
(1990). Ein Östrogenrezeptor-Antagonist
ist beschrieben in Halachmi et al., Science 264:1455-1458 (1994).
Demnach sind auf dem Fachgebiet Verfahren zur Entwicklung von Kandidaten
für Agonisten
und -Antagonisten der nuclearen Rezeptoren zum Durchmustern gemäß der vorliegenden
Erfindung bekannt. Zum Beispiel wurde die Kristallstruktur der Liganden
bindenden Domänen
von bestimmten nuclearen Rezeptoren beschrieben. Insbesondere ist
die Kristallstruktur der RXR-LBD beschrieben in Bourguet et al., Nature
375:377-382 (1995); die Kristallstruktur der RAR-LBD ist beschrieben
in Renaud et al., Nature 378: 681-689 (1995); und die Kristallstruktur
eines Thyroidhormonrezeptors ist beschrieben in Wagner et al., Nature 378:690-697
(1995). Unter Verwendung der Information aus der Kristallstruktur
eines nuclearen Rezeptors sind Computerprogramme zur Konstruktion
der Struktur des Kandidaten-Agonisten und – Antagonisten, die wahrscheinlich
an die Liganden bindende Domäne
binden würden,
erhältlich.
Passende Computerprogrammpakete für diesen Zweck beinhalten WHAT
IF (Vriend G., J. Mol. Graphics 8:52-56 (1990)) und GRID (Goodford,
J. Med. Chem. 28:849-857 (1985)).
-
Rekombinante
Gene, die ein Polypeptid codieren, das TIF2 oder ein TIF2-Fragment umfasst,
die in der Lage sind, nucleare Rezeptoren auf eine Agonistenabhängige Weise
zu binden, sind voranstehend beschrieben. Rekombinante Gene, die
ein Polypeptid codieren, das eine NR-LBD umfasst, wurden sehr ausführlich auf
dem Fachgebiet beschrieben. Verfahren zur Ermittlung, ob ein Kandidaten-Agonist
oder -Antagonist das Binden von TIF-2- oder TIF-2-Fragment an einen
NR erhöht
oder beeinträchtigt,
sind auf dem Fachgebiet bekannt. Zum Beispiel kann die Wirkung eines
Kandidaten-Agonisten oder -Antagonisten auf das Binden von TIF2- oder TIF2-Fragment
an eine NR-LBD unter Verwendung des Glutathion-S- Transferase (GST)-Interaktionsassays
durch Markieren der NR-LBDs mit GST untersucht werden, wie ausführlich in
dem experimentellen Abschnitt nachstehend und in Le Douarin et al.,
EMBO J 14: 2020-2033 (1995) beschrieben.
-
Wo
die Wirkung eines Kanidaten-Agonisten oder -Antagonisten auf die
NR-AF-2-Transaktivierung
untersucht werden muss, werden die rekombinanten Gene vorzugsweise
ein chimäres
Polypeptid codieren, das eine NR-LBD umfasst, die mit einer DNA
bindenden Domäne
von einem Transaktivator-Protein fusioniert ist. In einer weiteren
bevorzugten Ausführungsform
wird die Wirtszelle, die die rekombinanten Gene exprimiert, auch
ein Reportergen exprimieren. Zum Beispiel wurden in Chen et al.,
EMBO J. 14(6):1187-1197 (1995) drei ,Reporter'-Zelllinien etabliert, bei denen RARα-, RARβ- oder RARγ-Agonisten
die Luciferase-Aktivität
induzieren, die in den intakten Zellen unter Verwendung einer Einzelphoton-zählende Kamera
gemessen werden kann. Diese Zelllinien exprimieren beständig chimäre Proteine,
die die DNA-bindende Domäne
des Hefe-Transaktivators GAL4, der mit den EF-Regionen (die die
LBD und die AF-2-Aktivierungsfunktion enthalten) von RARa (GAL-RARa),
RARß (GAL-RARß) oder
RARγ (GAL-RARγ) fusioniert
ist, und ein Luciferase-Reportergen, das von einem Pentamer der
GAL4-Erkennungssequenz
(,17m') vor dem β-Globin-Promotor (17mx5-G-Luc)
angesteuert wird, enthalten. Das Reportersystem ist unempfindlich
gegenüber
endogenen Rezeptoren, die die GAL4-Bindungsstelle nicht erkennen
können.
Weitere Beispiele von Reportergenen und Reporter-Expressionsvektoren
für die
Anwendung gemäß der vorliegenden
Erfindung, um den Kandidaten-Agonisten und -Antagonisten von Retinoid-Rezeptoren
zu durchmustern, werden in 6 bereitgestellt.
-
Die
ER-Expressionsvektoren HEO, HE19 und HE15, die GR-Expressionvektoren
HG1 und HG3 und die PR-Expression cPR1 und cPR3 sind beschrieben
in Kumar et al., Cell 51: 941-951 (1987) und Gronemeyer et al.,
EMBO J. 6:3985-3994 (1987). Der GR-Expressionsvektor HG8 und der
PR-Expressionsvektor
cPR5A sind beschrieben in Bocquel et al., Nucl. Acids Res. 17:2581-2595
(1989). Reportergene für
die voranstehend beschriebenen ER-, GR- und PR-Expressionsvektoren beinhalten
MMTV-CAT (in dem Fall von PR und GR; Cato et al., EMBO J. 5:2237-2240
(1986)) und vit-tk-CAT (in dem Fall von ER; Klein-Hitpass et al.,
Cell 41: 1055-1061 (1986)).
-
Der
TR-Expressionsvektor LexA-TR ist beschrieben in Lee et al., Nature
374:91-94 (1995), worin auch die Verwendung des Hefe-Zweihybridsystems
beschrieben ist, um Verbindungen zu identifizieren, die die TR-Transaktivierung
beeinflussen.
-
Noch
weitere Literaturhinweise, die die Reporterplasmide offenbaren,
die ein Reportergen und einen Expressionsvektor, der eine NR-LBD
codiert, enthalten, beinhalten Meyer et al., Cell 57:433-442 (1989);
Meyer et al., EMBO J. 9(12):3923-3932
(1990); Tasset et al., Cell 62:1177-1187 (1990); Gronemeyer, H.
und Laudet, V., Protein Profile 2:1173-1308 (1995); Webster et al.,
Cell 54:199-207 (1988); Strähle
et al., EMBO J. 7:3389-3395 (1988); Seipel et al., EMBO J. 11:4961-4968
(1992); und Nagpal et al., EMBO J. 12:2349-2360 (1993). In einer
besonders bevorzugten Ausführungsform
wird die Wirkung eines Kandidaten-Agonisten oder – Antagonisten
auf die NR-AF-2-vermittelte Transaktivierung untersucht gemäß des Verfahrens,
das in der Legende zu 5 voranstehend
beschrieben ist.
-
Die
gegenwärtigen
Erfinder identifizierten eine Aktivierungsdomäne von TIF2, AD1 (Aminosäuren 1010-1131,
wie in 1 (SEQ ID NO:2) gezeigt), die
die CBP-abhängige Transkriptionsaktivierungsfunktion von
TIF2 vermittelt. Weiter zeigten die gegenwärtigen Erfinder, dass Polypeptide,
die diese Aktivierungsdomäne
enthalten, in der Lage sind, die Transkription über einen CBP-abhängigen Signalweg
zu aktivieren, wenn sie mit einer DNA-bindenden Domäne eines
Transkriptionsaktivators fusioniert sind. Demgemäß stellt die vorliegende Erfindung
weiter ein Durchmusterungsverfahren bereit, um einen Agonisten der
Aktivität
der TIF2-AD1-Aktivierungsdomäne
zu identifizieren, das umfasst: (a) das Bereitstellen einer Wirtszelle,
die ein rekombinantes Gen oder Gene enthält, die ein Polypeptid, das
eine Transkriptionsaktivator-DNA-bindende Domäne (DBD) und eine TIF-2-AD1-Aktivierungsdomäne 1 umfassen,
exprimieren; (b) das Verabreichen eines Kandidaten-Agonisten an
die Zelle; und (c) das Ermitteln, ob der Kandidaten-Agonist die
Aktivität
der TIF2-AD1-Aktivierungsdomäne
erhöht.
-
Die
Erfindung liefert weiter ein Durchmusterungsverfahren zum Identifizieren
eines Antagonisten der Aktivität
der TIF2-AD1-Aktivierungsdomäne,
das umfasst: (a) das Bereitstellen einer Wirtszelle, die ein rekombinantes
Gen oder Gene enthält,
die ein Polypeptid, das eine Transkriptionsaktivator-DNA-bindende
Domäne (DBD)
und eine TIF-2-AD1-Aktivierungsdomäne 1 umfasst, exprimieren;
(b) das Verabreichen eines Kandidaten-Antagonisten an die Zelle;
und (c) das Ermitteln, ob der Kandidaten-Antagonist die Aktivität der TIF2-AD1-Aktivierungsdomäne hemmt.
-
Unter „Transkriptionsaktivator" sind Moleküle zu verstehen,
die den Transkriptionsstart durch RNA-Polymerase B (II) erhöhen. Transkriptionsaktivatoren
beinhalten Hefe-Transkriptionsaktivatoren, wie GAL4 und GCN4; den
Herpes simplex-Aktivator, VP16; und Mitglieder der nuclearer Rezeptor-Familie,
die RAR, RXR, ER, TR, VDR, GR und AR beinhaltet.
-
Rekombinante
Gene, die ein Polypeptid codieren, das eine TIF2-AD1-Aktivierungsdomäne umfasst, werden
nachstehend beschrieben. Rekombinante Gene, die ein Polypeptid codieren,
das eine Transkriptionsaktivator-DBD umfasst, sind auf dem Fachgebiet
gut bekannt. Verfahren zum Ermitteln, ob ein Kandidaten-Agonist oder -Antagonist
die Transkription erhöht
oder beeinträchtigt,
sind auf dem Fachgebiet gut bekannt. Zum Beispiel kann die Wirkung
eines Kandidaten-Agonisten oder -Antagonisten auf die Aktivität der TIF2-AD1-Aktivierungsdomäne unter
Verwendung der CAT-Assays ermittelt werden, wie nachstehend und
in Gronemeyer et al. (1987) und Bocquel et al., Nucl. Acids Res.
(1989) beschrieben.
-
Wo
die Wirkung eines Kandidaten-Agonisten oder -Antagonisten der Aktivität der TIF2-AD1-Aktivierungsdomäne ermittelt
werden muss, werden vorzugsweise rekombinante Gene ein chimäres Polypeptid
codieren, das eine Transkriptionsaktivator-DBD umfasst, die mit
einem TIF2-Polypeptid fusioniert ist, das die AD1-Aktivierungsdomäne umfasst.
In einer weiteren Ausführungsform
wird die Wirtszelle, die die rekombinanten Gene exprimiert, auch
ein Reportergen exprimieren. Beispiele von Reportergenen sind voranstehend
beschrieben. In einer besonders bevorzugten Ausführungsform wird die Wirkung
eines Kandidaten-Agonisten oder
-Antagonisten der Funktion der TIF2-AD1-Aktivierungsdomäne ermittelt
werden, wie in der Legende zu 7(c) beschrieben.
-
Die
gegenwärtigen
Erfinder identifizierten auch eine zweite Aktivierungsdomäne von TIF2,
AD2 (Aminosäuren
1288-1464, wie in 1 (SEQ ID NO:2)
gezeigt), die die CBP-unabhängige
Transkriptionsaktivierung vermittelt. Weiter zeigten die gegenwärtigen Erfinder,
dass die Polypeptide, die diese Aktivierungsdomäne enthalten, in der Lage sind,
die Transkription über
einen CBP-unabhängigen
Weg zu aktivieren, wenn sie mit einer DNA-bindenden Domäne des Transkriptionsaktivators
fusioniert sind. Demgemäß stellt
die vorliegende Erfindung ein Durchmusterungsverfahren bereit, um
einen Agonisten der Aktivität
der TIF2-AD2-Aktivierungsdomäne zu identifizieren,
das umfasst: (a) das Bereitstellen einer Wirtszelle, die ein rekombinantes
Gen oder Gene enthält,
die ein Polypeptid exprimieren, das eine Transkriptionsaktivator-DNA-bindende
Domäne (DBD)
und eine TIF-2-AD2-Aktivierungsdomäne umfasst; (b) das Verabreichen
eines Kandidaten-Agonisten an die Zelle; und (c) das Ermitteln,
ob der Kandidaten-Agonist die Aktivität der TIF2-AD2-Aktivierungsdomäne erhöht.
-
Die
Erfindung stellt weiterhin ein Durchmusterungsverfahren zum Identifizieren
eines Antagonisten der Aktivität
der TIF2-AD2-Aktivierungsdomäne
zur Verfügung,
das umfasst: (a) das Bereitstellen einer Wirtszelle, die das rekombinante
Gen oder Gene enthält,
die ein Polypeptid exprimieren, das eine Transkriptionsaktivator-DNA-bindende Domäne (DBD)
und eine TIF-2-AD2-Aktivierungsdomäne umfasst; (b) das Verabreichen
eines Kandidaten-Antagonisten an die Zelle; und (c) das Ermitteln,
ob der Kandidaten-Antagonist die Aktivität der TIF2-AD2-Aktivierungsdomäne hemmt.
-
Rekombinante
Gene, die ein Polypeptid codieren, das eine TIF2-AD2-Aktivierungsdomäne umfassen, werden
nachstehend beschrieben. Rekombinante Gene, die ein Polypeptid codieren,
das eine Transkriptionsaktivator-DBD umfasst, sind auf dem Fachgebiet
gut bekannt. Verfahren zur Ermittlung, ob ein Kandidaten-Agonist oder -Antagonist
die Transkription erhöht
oder beeinträchtigt,
sind auf dem Fachgebiet bekannt.
-
Wo
die Wirkung eines Kandidaten-Agonisten oder -Antagonisten der Aktivität der TIF2-AD2-Aktivierungsdomäne ermittelt
werden muss, werden vorzugsweise rekombinante Gene ein chimäres Polypeptid
codieren, das eine Transkriptionsaktivator-DBD umfasst, die mit
einem TIF2-Polypeptid fusioniert ist, das die AD2-Aktivierungsdomäne umfasst.
Die Transkriptionsaktivatoren sind voranstehend beschrieben. In
einer weiteren Ausführungsform
wird die Wirtszelle, die die rekombinanten Gene exprimiert, auch
ein Reportergen exprimieren. Beispiele von Reportergenen sind voranstehend
beschrieben. In einer besonders bevorzugten Ausführungsform wird die Wirkung
eines Kandidaten-Agonisten oder -Antagonisten der Aktivität der TIF2-AD2-Aktivierungsdomäne ermittelt
werden, wie in der Legende zu 7(c) beschrieben.
-
TIF-2-Antikörper und
Verfahren
-
TIF2-Antikörper werden
auch durch die vorliegende Erfindung bereitgestellt, da sie spezifisch
für ein TIF2-Protein,
ein TIF2-Polypeptid, ein TIF2-Proteinfragment oder ein TIF2-Polypeptidfragment
sind. Unter dem Begriff „Antikörper" sind zu verstehen,
dass sie polyklonale Antikörper,
monoklonale Antikörper
(mAbs), chimäre
Antikörper,
anti-idiotypische (anti-Id) Antikörper bis Antikörper, die
in löslicher
oder gebundener Form markiert werden können, sowie die Fragmente davon
beinhalten, die durch eine bekannte Methode bereitgestellt werden,
wie, aber nicht begrenzt auf enzymatische Spaltung, Peptidsynthese
oder rekombinante Methoden. Polyklonale Antikörper sind heterogene Populationen
von Antikörpermolekülen, die
aus den Seren von den mit Antigen immunisierten Tieren abgeleitet
werden. Ein monoklonaler Antikörper
enthält
eine wesentlich homogene Population von Antikörpern, die spezifisch für Antigene
sind, deren Population im wesentlichen gleiche Epitop-Bindungsstellen
enthalten. MAbs können
durch Verfahren, die dem Fachmann bekannt sind, erhalten werden.
S. zum Beispiel Kohler und Milstein, Nature 256:495-497 (1975);
U.S.-Patent No. 4,376,110; Ausubel et al. Hrsg., CURRENT PROTOCOLS
IN MOLECULAR BIOLOGY, Greene Publishing Assoc. und Wiley Interscience,
N.Y., (1987-1996); und Harlow und Lane ANTIBODIES: A LABORATORY
MANUAL Cold Spring Harbor Laboratory (1988); Colligan et al., Hrsg.,
Current Protocols in Immunology, Greene Publishing Assoc. und Wiley
Interscience, N.Y., (1992-1996), die Inhalte, von denen die Literaturhinweise
vollkommen durch Literaturhinweis berücksichtigt sind.
-
Solche
Antikörper
können
von einer beliebigen Immunglobulin-Klasse sein, einschließlich IgG,
IgM, IgE, IgA, GILD und einer beliebigen Unterklasse davon. Ein
Hybridom, das einen mAb der vorliegenden Erfindung produziert, kann
in vitro, in situ oder in vivo kultiviert werden. Die Erzeugung
von hohen Titern der mAbs in vivo oder in situ macht dies zum derzeit
bevorzugten Verfahren der Herstellung.
-
Chimäre Antikörper sind
Moleküle,
von denen verschiedene Anteile aus verschiedenen Tierarten abgeleitet
werden, wie jene mit einer variablen Region, die aus einem Maus-mAb
und einer menschlichen konstanten Immunoglobulin- Region abgeleitet
werden, die hauptsächlich
verwendet werden, um die Immunogenität bei der Anwendung zu reduzieren
und die Ausbeuten bei der Herstellung zu steigern. Zum Beispiel,
wo Maus-mAbs höhere
Ausbeuten von Hybridomen haben, aber höhere Immunogenität bei Menschen,
so dass chimäre
mAbs des Menschen/der Maus verwendet werden. Chimäre Antikörper und
Verfahren zu ihrer Herstellung sind auf dem Fachgebiet bekannt (Cabilly
et al., Proc. Natl. Acad. Sci. USA 81:3273-3277 (1984); Europäische Patentanmeldung
125023 (publiziert am 14. November 1984); Neuberger et al., Nature
314:268-270 (1985); Taniguchi et al., Europäische Patentanmeldung 171496
(1985); Morrison et al., Europäische
Patentanmeldung 173494 (1986); Neuberger et al., PCT Application
WO 86/01533, (1986); Kudo et al., Europäische Patentanmeldung 184187
(1986); Morrison et al., Europäische
Patentanmeldung 173494 (1986); Robinson et al., PCT Publication
PCT/US86/02269 (1987); Liu et al., Proc. Natl. Acad. Sci. USA 84:3439-3443
(1987); Sun et al., Proc. Natl. Acad. Sci. USA 84:214-218 (1987);
Better et al., Science 240: 1041-1043 (1988); und Harlow und Lane,
ANTIBODIES: A LABORATORY MANUAL Cold Spring Harbor Laboratory (1988)).
Diese Literaturhinweise sind durch Bezugnahme vollkommen hierin
berücksichtigt.
-
Ein
anti-idiotypischer (anti-ID) Antikörper ist ein Antikörper, der
einzelne Determinanten erkennt, die allgemein mit der Antigen-bindenden
Stelle des Antikörpers
verbunden sind. Ein Id-Antikörper
kann durch Immunisieren eines Tiers derselben Art und desselben
genetischen Typs (z.B. Mausstamm) als Quelle des mAb mit dem mAb
präpariert
werden, an dem ein Anti-Id präpariert
wird. Das immunisierte Tier wird die idiotypischen Determinanten
des immunisierenden Antikörpers
erkennen und auf sie durch Herstellung eines Antikörpers gegen
diese idiotypischen Determinanten (den Anti-Id-Antikörper) reagieren.
Siehe zum Beispiel U.S. patent No. 4,699,880, das hierin vollkommen
durch Bezugnahme aufgenommen ist.
-
Der
Anti-Id-Antikörper
kann auch als ein „Immunogen" verwendet werden,
um eine Immunantwort in noch einem anderen Tier, das einen so genannten
Anti-anti-ID-Antikörper herstellt,
zu induzieren. Der Anti-anti-ID muss epitopisch identisch zu dem
ursprünglichen
mAb sein, der den Anti-Id induzierte. Demnach ist es unter Verwendung
von Antikörpern
gegen die idiotypischen Determinanten eines mAb möglich, andere
Klone zu identifizieren, die Antikörper von identischer Spezifität exprimieren.
Die Anti-Id-mAbs haben demnach ihre eigenen idiotypischen Epitope oder „Idiotope", die strukturell ähnlich zu
dem Epitop sind, das evaluiert wird, wie das G RB-Protein-α.
-
Unter
dem Begriff „Antikörper" ist auch verstehen,
dass er beide intakten Immunglobulinmoleküle sowie Fragmente davon beinhaltet,
wie zum Beispiel Fab und F(ab')2, die in der Lage sind, Antigen zu binden. Den
Fab und F(ab')2-Fragmenten
fehlt das Fc-Fragment des intakten Antikörpers, sie kommen schneller
aus dem Kreislauf frei und können
weniger unspezifische Gewebebindung haben als ein intakter Antikörper (Wahl et
al., J. Nucl. Med. 24:316-325 (1983)). Es wird geschätzt werden,
dass Fab und F(ab')2 und andere Fragmente der in der vorliegenden
Erfindung brauchbaren Antikörper
für den
Nachweis und die Quantifizierung eines TIF2 gemäß der hierin offenbarten Verfahren
für intakte
Antikörpermoleküle verwendet
werden können.
Solche Fragmente werden normalerweise durch proteolytische Spaltung
unter Verwendung von Enzymen wie Papain (um Fab-Fragmente herzustellen)
oder Pepsin (um F(ab')2-Fragmente herzustellen) hergestellt.
-
Ein
Antikörper
gilt als „in
der Lage zum Binden" eines
Moleküls,
wenn er in der Lage ist, spezifisch mit dem Molekül zu reagieren,
um dadurch das Molekül
an den Antikörper
zu binden. Der Begriff „Epitop" bezieht sich auf
den Anteil eines beliebigen Moleküls, der in der Lage ist, von
einem Antikörper,
der auch von dem Antikörper
erkannt werden kann, gebunden zu werden. Epitope oder „antigene
Determinanten" bestehen
gewöhnlich
aus chemisch aktiven Oberflächengruppierungen
von Molekülen
wie Aminosäuren-
oder Zucker-Seitenketten und haben spezifische dreidimensionale
strukturelle Merkmale sowie spezifische Ladungsmerkmale.
-
Ein „Antigen" ist ein Molekül oder ein
Anteil eines Moleküls,
das in der Lage ist, von einem Antikörper gebunden zu werden, das
zusätzlich
in der Lage ist, ein Tier zu induzieren, den Antikörper herzustellen,
der in der Lage ist, an ein Epitop dieses Antigens zu binden. Ein
Antigen kann ein oder mehr als ein Epitop haben. Die spezifische
Reaktion auf die voranstehend Bezug genommen wird ist so zu verstehen,
dass das Antigen auf eine hoch selektive Weise mit seinem entsprechenden
Antikörper
reagieren wird und nicht mit der Vielzahl anderer Antikörper, die
durch andere Antigene hervorgerufen werden können.
-
Die
in der vorliegenden Erfindung brauchbaren Antikörper oder Fragmente der Antikörper können verwendet
werden, um quantitativ oder qualitativ ein TIF2-Protein, -Polypeptid
oder -Fragment in einer Probe nachzuweisen oder die Anwesenheit
von Zellen nachzuweisen, die einen TIF2 der vorliegenden Erfindung
exprimieren. Dies kann durch Immunfluoreszenz-Methoden erreicht
werden, die einen fluoreszenzmarkierten Antikörper (s. nachstehend) anwenden,
der mit lichtmikroskopischem, durchflusscytometrischem oder fluorometrischem
Nachweis gekoppelt ist.
-
Die
in der vorliegenden Erfindung brauchbaren Antikörper (oder Fragmente davon)
können
histologisch verwendet werden, wie in Immunfluoreszenz- oder Immun-Elektronenmikroskopie,
zum in situ-Nachweis eines TIF2-Proteins, -Polypeptids oder -Fragment
der vorliegenden Erfindung. Der in situ-Nachweis kann durch Entfernen
einer histologischen Probe von einem Patienten und dem Bereitstellen
eines markierten Antikörpers
der vorliegenden Erfindung zu solch einer Probe durchgeführt werden.
Der Antikörper
(oder das Fragment) wird vorzugsweise durch Anwenden oder durch Überlagern
des markierten Antikörpers
(oder Fragments) mit einer biologischen Probe bereitgestellt. Durch
die Anwendung einer solchen Prozedur ist es möglich, nicht nur die Anwesenheit
eines TIF2-Proteins, -Polypeptids oder -Fragments, sondern auch
seine Verteilung in dem untersuchten Gewebe zu ermitteln. Unter
Verwendung der vorliegenden Erfindung wird der durchschnittliche
Fachmann leicht erkennen, dass eine beliebige der weiten Vielfalt
von histologischen Verfahren (wie Färbeprozeduren) modifiziert
werden kann, um einen solchen in situ-Nachweis zu erzielen.
-
Solche
Assays für
ein TIF2-Protein, -Polypeptid oder -Fragment der vorliegenden Erfindung
umfasst normalerweise das Inkubieren einer biologischen Probe, wie
einer biologische Körperflüssigkeit,
eines Gewebeextrakts, frisch geernteter Zellen wie Lymphozyten oder
Leukozyten, oder Zellen, die in Gewebekultur inkubiert wurden, in
Anwesenheit eines nachweisbar markierten Antikörpers, der in der Lage ist,
ein TIF2-Protein, -Polypeptid oder -Fragment zu identifizieren und
den Antikörper
durch eine beliebige einer Anzahl von auf dem Fachgebiet gut bekannten
Methoden nachzuweisen.
-
Die
biologische Probe kann mit einer Festphasen-Unterstützung oder
einem Festphasen-Träger
wie Nitrocellulose, oder einer/einem anderen festen Unterstützung oder
Träger,
die/der in der Lage ist, Zellen, Zellpartikel oder lösliche Proteine
zu immobilisieren, behandelt werden. Die Unterstützung oder der Träger kann dann
mit passenden Puffern gewaschen werden, gefolgt durch die Behandlung
mit einem nachweisbar markierten TIF2-spezifischen Antikörper. Die
Festphasen-Unterstützung oder
der Festphasen-Träger
kann dann mit dem Puffer ein zweites Mal gewaschen werden, um ungebundenen
Antikörper
zu entfernen. Die Menge des gebundenen Markers auf der festen Unterstützung oder
dem festen Träger
kann dann durch konventionelle Mittel nachgewiesen werden.
-
Mit „Festphasen-Unterstützung", „Festphasen-Träger", „feste
Unterstützung", „fester
Träger", „Unterstützung" oder „Träger" ist eine beliebige
Unterstützung
oder ein beliebiger Träger
beabsichtigt, der/die in der Lage ist, ein Antigen oder Antikörper zu
binden. Gut bekannte Unterstützungen
oder Träger
beinhalten Glas, Polystyrol, Polypropylen, Polyethylen, Dextran,
Nylonamylasen, natürliche
und modifizierte Zellulosen, Polyacrylamide, Gabbros und Magnetit.
Die Beschaffenheit des Trägers
kann entweder zu einem gewissen Ausmaß löslich oder für die Zwecke
der vorliegenden Erfindung unlöslich
sein. Das Unterstützungsmaterial
kann praktisch eine beliebige mögliche
strukturelle Anordnung haben, solange das gekoppelte Molekül in der
Lage ist, an ein Antigen oder einem Antikörper zu binden. Demnach kann
die Anordnung der Unterstützung
oder des Trägers
spherisch, wie in einem Kügelchen,
oder zylindrisch, wie in der inneren Oberfläche eines Teströhrchen oder
der äußeren Oberfläche eines
Stabs, sein. Anderenfalls kann die Oberfläche flach sein wie bei einem Blatt,
Teststreifen usw. Bevorzugte Unterstützungen oder Träger beinhalten
Polystyrol-Kügelchen.
Der Fachmann wird viele andere passende Träger zum Binden von Antikörper oder
Antigen kennen oder werden das Gleiche durch Verwendung von Routine-Experimentieren
herausfinden können.
-
Die
Bindungsaktivität
einer gegebenen Menge von Anti-TIF2-Antikörpern kann gemäß gut bekannten Verfahren
ermittelt werden. Der Fachmann wird die wirksamen und optimalen
Assay-Bedingungen für
jede Bestimmung durch Anwenden von Routine-Experimentieren ermitteln
können.
Andere solche Schritte wie Waschen, Rühren, Schütteln, Filtern und desgleichen
können
den Assays angefügt
werden, wie es für
die besondere Situation gebräuchlich
oder notwendig ist.
-
Einer
der Wege, bei denen ein TIF2-spezifischer Antikörper nachweisbar markiert werden
kann, ist durch Verbinden desselben mit einem Enzym und die Verwendung
in einem Enzymimmunoassay (EIA). Wenn es später einem geeigneten Substrat
ausgesetzt wird, wird dieses Enzym wiederum mit dem Substrat derart reagieren,
dass es einen chemischen Rest erzeugt, der zum Beispiel durch spektrophotometrische,
fluorometrische oder durch visuelle Mittel nachgewiesen werden kann.
Enzyme, die verwendet werden können,
um den Antikörper
nachweisbar zu markieren, beinhalten, aber sind nicht begrenzt auf,
Malatdehydrogenase, Staphylococcen-Nuclease, delta-5-Steroid-Isomerase,
Hefe-Alkoholdehydrogenase,
alpha-Glycerophosphatdehydrogenase, Triosephosphat-Isomerase, Meerrettich-Peroxidase,
Alkalische Phosphatase, Asparaginase, Glucoseoxidase, beta-Galactosidase,
Ribonuclease, Unease, Katalase, Glucose-6-Phosphat-Dehydrogenase, Glucoamylase
und Acetylcholinesterase. Der Nachweis kann durch colorimetrische
Verfahren erreicht werden, die ein chromogenes Substrat für das Enzym
verwenden. Der Nachweis kann auch durch visuellen Vergleich des
Ausmaßes
der enzymatischen Reaktion eines Substrats im Vergleich mit ähnlich präparierten
Standards erreicht werden.
-
Der
Nachweis kann durch Verwendung eines beliebigen von einer Vielfalt
von anderen Immunoassays erreicht werden. Zum Beispiel ist es durch
Radioaktivitätsmarkierung
der Antikörper
oder Antikörperfragmente möglich, die
R-PTPase durch die
Verwendung eines Radioimmunoassays (RIA) nachzuweisen. Eine gute
Beschreibung des RIA kann gefunden werden in Laboratory Techniques
and Bio chemistry in Molecular Biology, von Work, T.S. et al., North
Holland Publishing Company, NY (1978) mit einem besonderen Literaturhinweise zu
dem Kapitel, mit dem Titel "An
Introduction to Radioimmune Assay and Related Techniques" von Chard, T., hierin
berücksichtigt
durch Literaturhinweis. Das radioaktive Isotop kann durch solche
Mittel wie die Verwendung eines γ-Zählers oder
eines Szintillationszählers
oder durch Autoradiographie nachgewiesen werden.
-
Es
ist auch möglich,
einen Anti-TIF2-Antikörper
mit einer fluoreszierenden Verbindung zu markieren. Wenn der fluoreszenzmarkierte
Antikörper
Licht von geeigneter Wellenlänge
ausgesetzt wird, kann seine Anwesenheit auf Grund der Fluoreszenz
nachgewiesen werden. Unter den meisten allgemein verwendeten Verbindungen
für die
Fluoreszenzmarkierung sind Fluorescein Isothiocyanat, Rhodamin,
Phycoerythrin, Phycocyanin, Allophycocyanin, o-Phthaldehyd und Fluorescamin.
-
Der
Antikörper
kann auch nachweisbar unter Verwendung von Fluoreszenzemittierenden
Metallen wie 152EU oder andere der Lanthanidenreihe
nachgewiesen werden. Diese Metalle können an den Antikörper unter Verwendung
von solchen Metallchelat-bildenden Gruppen wie Diethylentriaminpentaessigsäure (EDTA)
angehängt
werden.
-
Der
Antikörper
kann auch nachweisbar durch Kopplung mit einer chemilumineszierenden
Verbindung markiert werden. Die Anwesenheit eines chemilumineszent-markierten
Antikörpers
wird dann durch Nachweis der Anwesenheit von Lumineszenz ermittelt,
die während
des Verlaufs einer chemischen Reaktion entsteht. Beispiele von besonders
brauchbaren chemilumineszentmarkierenden Verbindungen sind Luminol,
Isoluminol, theromatischer Acridiniumester, Imidazol, Acridiniumsalz
und Oxalatester.
-
Ebenso
kann eine biolumineszente Verbindung verwendet werden, um den Antikörper der
vorliegenden Erfindung zu markieren. Biolumineszenz ist eine Art
der Chemilumineszenz, die in biologischen Systemen gefunden wird,
bei denen ein katalytisches Protein die Effizienz der chemilumineszenten
Reaktion steigert. Die Anwesenheit eines biolumineszenten Proteins
wird durch Nachweis der Anwesenheit von Lumineszenz ermittelt. Wichtige
biolumineszente Verbindungen für
Markierungszwecke sind Luciferin, Luciferase und Aequorin.
-
Ein
Antikörpermolekül der vorliegenden
Erfindung kann für
den Gebrauch in einem immunometrischen Assay angepasst werden, auch
bekannt als „Two-Site" oder „Sandwich"-Assay. In einem
typischen immunometrischen Assay wird eine Anzahl von unmarkierten
Antikörper
(oder Antikörperfragment)
an eine feste Unterstützung
oder einen festen Träger
gebunden und eine Anzahl von nachweisbar markierten löslichen
Antikörper
wird zugegeben, um den Nachweis und/oder die Quantifizierung des
ternären
Komplexes, der zwischen Festphasen-Antikörper, Antigen und markiertem
Antikörper
gebildet wird, zu erlauben.
-
Typische
und bevorzugte immunometrische Assays beinhalten „Forward" Assays, bei denen
der an die feste Phase gebundene Antikörper zuerst mit der zu testenden
Probe in Kontakt gebracht wird, um das Antigen aus der Probe durch
Bildung eines binären
Festphasen-Antikörper-Antigen-Komplex
zu extrahieren. Nach einer passenden Inkubationsdauer wird die feste
Unterstützung
oder der feste Träger
gewaschen, um den Rest der flüssigen
Probe zu entfernen, einschließlich
nicht umgesetztes Antigen, wenn überhaupt,
und dann mit der Lösung
in Kontakt gebracht, die eine unbekannte Menge des markierten Antikörpers (der
als ein „Reportermolekül" fungiert) enthält. Nach
einer zweiten Inkubationsdauer, um dem markierten Antikörper zu ermöglichen,
einen Komplex mit dem an die feste Unterstützung oder an den festen Träger durch
den unmarkierten Antikörper
gebundenen Antigen zu bilden, wird die feste Unterstützung oder
der feste Träger
ein zweites Mal gewaschen, um den nicht reagierten markierten Antikörper zu
entfernen.
-
In
einem anderen Typ von „Sandwich-"Assay, der auch mit
den Antigenen der vorliegenden Erfindung verwendet werden kann,
werden die so genannten „simultanen" und „reversen" Assays verwendet.
Ein „simultaner" und ein „reverser" Assay werden verwendet.
Ein simultaner Assay umfasst einen einzelnen Inkubationsschritt,
indem der an die feste Unterstützung
oder den festen Träger
gebundene Antikörper
und der markierte Antikörper
beide zu derselben Zeit zu der zu testenden Probe zugegeben werden.
Nachdem die Inkubation abgeschlossen ist, wird die feste Unterstützung oder
der feste Träger
gewaschen, um den Rest der flüssigen Probe
und nicht komplexierten markierten Antikörper zu entfernen. Die Anwesenheit
des markierten Antikörpers,
verbunden mit der festen Unterstützung
oder dem festen Träger,
wird dann ermittelt, wie in einem konventionellen „Forward" Sandwich-Assay.
-
Bei
dem „reversen" Assay wird die schrittweise
Zugabe erst einer Lösung
von markiertem Antikörper zu
der flüssigen
Probe, gefolgt durch die Zugabe von nicht markiertem Antikörper, der
an eine feste Unterstützung
oder einen festen Träger
gebunden ist, nach einer passenden Inkubationsdauer angewendet.
Nach einer zweiten Inkubation wird die feste Phase auf konventionelle
Art und Weise gewaschen, um sie von dem Rest der zu testenden Probe
und der Lösung
von nicht umgesetzten markierten Antikörpern zu befreien. Die Bestimmung
des markierten Antikörpers
verbunden mit einer festen Unterstützung oder einen festen Träger wird dann
ermittelt wie in den „simultanen" und „Forward" Assays.
-
Nach
allgemeiner Beschreibung der Erfindung wird dieselbe durch Verweis
zu den folgenden Beispielen, die durch Veranschaulichung bereitgestellt
werden und nicht als Begrenzung beabsichtigt sind, leichter verstanden
werden.
-
Beispiel 1: TIF2-Klonierung
und -Expression
-
In Übereinstimmung
mit früheren
Berichten (Halachmi, S. et al., Science 264:1455-1458 (1994); Cavailles,
V. et al., Proc. Natl. Acad. Sci. USA 91:10009-10013 (1994); Kurokawa, R. et al, Nature
377:451-454 (1995)), beobachteten wir in vitro ein Agonisten-abhängiges Binden
von einem 160-kDa-Protein von 35S-markierten Gesamtzellextrakten
(HeLa, Cos-1, P19.6, MCF-7) mit den Glutathion-S-Transferase (GST)-markierten LBDs von
Retinolsäure
(RAR)- und Östrogen
(ER)-Rezeptoren
(2a). Ein cDNA-Klon, der durch Durchmustern von
340,000 Klone der menschlichen Plazenta-cDNA-Expressionsbibliothek
mit einer Estradiol (E2)-gebundenen 32P-markierten ER(DEF)-Sonde identifiziert
wurde, codierte ein Proteinfragment (TIF2.1), das auf Far-Western-Blots
mit drei unterschiedlichen 32P-markierten NR-LBDs
(ER, RAR, RXR) auf eine Agonisten-abhängige Weise interagierte (nicht
gezeigt), und könnte
daher dem voranstehenden 160-kDa-Protein entsprechen. Die TIF2 codierende
Sequenz (3a), vorausgegangen durch
in-Raster-Stopp-Codons
5' des Initiators
AUG, wurden beim Wieder-Durchmustern mit einer TIF2.1-cDNA-Sonde
erhalten. Menschliche TIF2-cDNA codiert ein 159,160 Da-Protein (1,464 Aminosäuren), das
N-terminale vermeintliche nucleare Lokalisierungssignale (NLSs),
eine Gln- und drei Ser/Thr-reiche Regionen und zwei geladenen Cluster
beinhaltet (3). Einige Regionen von
TIF2 zeigen signifikante Sequenzähnlichkeiten
mit dem neulich beschriebenen (Onate, S.A. et al., Science 270:1354-1357
(1995)) Steroidrezeptor-Coaktivator SRC-1 (3).
TIF2 scheint weit exprimiert zu werden, da das entsprechende Transkript
in mehreren menschlichen Geweben gefunden wurde, obgleich zu einem
viel niedrigeren Niveau in der Niere (2c und
nicht gezeigt).
-
Immunodepletion-Studien
unterstützen
stark, dass TIF2 eine 160-kDa-Proteinspezies
ist, die auf eine Agonisten-abhängige
Weise mit den NR-LBDs interagiert (s. voranstehend und Halachmi,
S. et al., Science 264:1455-1458 (1994); Cavailles, V. et al., Proc.
Natl. Acad. Sci. USA 91:10009-10013 (1994); und Kurokawa, R. et
al., Nature 377:451-454 (1995)). Das Western-Blotting mit einem
Kaninchen-Antiserum (pα-TIF2),
das gegen bakteriell exprimiertem TIF2.1 ansprach, offenbarte überwiegend
ein 160-kDa-HeLa-Zellprotein, das mit dem Agonist gebundenen GST-ER(DEF)
interagierte (2b, Spuren 1 und 2; s. auch
die Legende zu 2b). Die Immunodepletion mit
einem monoklonalen TIF2-Antikörper
der Maus (mα-TIF2)
vor der Affinitätsaufreinigung
führte
zu einer spezifischen Abnahme von TIF2-, aber nicht von TIF1-Mengen
(Le Douarin, B. et al., EMBO J. 14:2020-2033 (1995)), die an E2-gebundenem
GST-ER(DEF) zurückgehalten
wurden (2b, vgl. Spuren 2 mit 4 und
6 mit 8). Wichtigerweise offenbarte die nachfolgende Far-Western-Analyse
mit einer E2-gebundenen 32P-GST-ER(DEF)-Sonde die 160-kDa-Spezies
nur in der Kontrolle, aber nicht in den TIF2-immunodepletierten Extrakten (2b,
vgl. Spuren 10 und 12).
-
Vorübergehend
exprimiertes TIF2 von ganzer Länge
war nuclear und hauptsächlich
mit diskreten Körpern
verbunden (4a). Da das überexprimierte
TIF2.1-Fragment im Wesentlichen cytoplasmatisch war (was die voranstehende
Zuordnung eines N-terminalen TIF2-NLS stützt), konnte die Interaktion
von TIF2.1 mit NRs in Säugetierzellen
unter Verwendung von nuclearen Co-Translokalisierungsassays untersucht
werden. Bei Abwesenheit des Liganden blieb TIF2.1 cytoplasmatisch
und die NRs waren nuclear (für
RARa, ER und PR, s. 4b, 4d, 4g). Die
Agonisten-Aussetzung führte
jedoch bei allen drei Fällen
zu nuclearer Colokalisierung von TIF2.1 und NR, was die NR-TIF2-Interaktion
in vivo anzeigte (4c, 4e, 4h). Agonisten-abhängige Interaktion von TIF2.1
mit NRs wurde für
alle anderen analysierten Rezeptoren (RXR, TR, VDR, GR und AR; nicht
gezeigt) beobachtet. Interessanterweise wurde keine Interaktion
zwischen ER und TIF2.1 in Anwesenheit des ER-AF-2-Antagonisten Hydroxytamoxifen
(OHT) (4f) nachgewiesen, und der PR-AF-2-Antagonist
RU 486 kehrte die R5020-induzierte PR-TIF2.1-Interaktion um (4i).
-
In Übereinstimmung
mit den Far-Western-Blot-Experimenten interagierten NRs und TIF2
direkt, wie das aufgereinigte gebundene TIF2.1-Protein in vitro
in der Anwesenheit eines Agonisten mit GST-ER(DEF), GST-RARa(DEF),
GST-RXRa(DE) und GST-TR(DE) (4k, 4l, 4m, Spuren 3 und 4; 4n, Spuren 5 und 6). Wie erwartet, geschah das
TIF2-Binden an GST-RXRα(DE)
mit 9cis-RA (9C-RA), aber nicht mit all-trans-RA (T-RA) (4n, Spuren 1 und 2), und OHT verhinderte das E2-abhängige Binden
von TIF2 an GST-ER(DEF) (4n,
Spuren 7-9). Die Integrität
des konservierten Kernstücks
der ER, RARα und
RXRα-AF-2
aktivierenden Domänen
(AF-2 AD), von denen gezeigt wurde, dass sie entscheidend für die AF-2- Aktivität sind (Le
Douarin, B. et al., EMBO J. 14:2020-2033 (1995); Danielian, P.S.
et al., EMBO J. 11:1025-1033 (1992); Durand, B. et al., EMBO J.
13:5370-5382 (1994); und Gronemeyer, H. und Laudet, V., Protein
Profile 2:1173-1308 (1995) und darin), wurde für die TIF2-Interaktion in vitro
benötigt.
Die meisten AF-2-AD-Kernstückmutanten,
die die AF-2-Aktivität
verloren (ER, 4k, Spuren 5-8; RARa, 4l; Spuren 5-10; RXRa, 4m,
Spuren 5-8), assoziierten nicht nachweisbar oder nur schwach mit
TIF2, während
die GST-LBD-Verbindung der RXRα-Mutante
E461Q, deren AF-2 nur teilweise geschwächt ist (Le Douarin, B. et
al., EMBO J. 14:2020-2033 (1995)), noch eine signifikante RA-abhängige Interaktion
mit TIF2.1 in vitro aufwies (4m, Spuren
9 und 10). Keine signifikante Interaktion von TIF2.1 wurde mit entweder
GST-VP16 (saure Aktivierungsdomäne),
GST-TBP, GST-TFIIB oder einer Reihe von GST-TAFs (hTAFII18,
hTAFII20, hTAFII28
und hTAFII55; s. Jacq, X. et al., Cell 79:107-117
(1994); Mengus, G. et al., EMBO J. 14:1520-1531 (1995)) beobachtet
(nicht gezeigt).
-
Bezeichnenderweise
könnte
ein TIF, der in der Lage ist, die Transkriptionsaktivität eines
verwandten AF zur Transkriptionsmaschinerie zu vermitteln, selbst
ein Aktivator sein, wenn er mit einer heterologen DNA-bindenden
Domäne
fusioniert ist. Interessanterweise transaktivierte in vorübergehend
transfizierten HeLa-Zellen TIF2.1, der mit der GAL4-DNA-bindenden
Domäne
fusioniert ist, stark einen GAL4-Reporter (5a).
Demnach kann TIF2 einem der hypothetischen begrenzenden Faktoren)
entsprechen, die früher
vorgeschlagen wurden, bei der/dem NR transkriptionalen Interferenz/Squelching
einbezogen zu sein (Meyer, M.-E. et al., Cell57:433-442 (1989);
Bocquel, M.-T. et al., Nucl. Acids. Res. 17:2581-2595 (1989); Tasset,
D. et al., Cell 62:1177-1187 (1990)). Unter Unterstützung dieser
Möglichkeit
zeigten „Anti-Squelching"-Experimente, dass
die Expression von TIF2.1 in ER-transfizierten Zellen die transkriptionale
Autointerferenz zumindest teilweise umkehren konnten (Bocgel, M.-T.
et al., Nucl. Acids. Res. 17:2581-2595 (1989)), die durch Exprimieren erhöhter Mengen
von ER erzeugt wurde (5b; beachten Sie die markierte
Verschiebung der glockenförmigen
Aktivierungskurve zu höheren
ER-Konzentrationen in der Anwesenheit von TIF2.1). Bei hohen ER-Expressionsniveaus
nahm die TIF2.1-stimulierte Transaktivierung ab, möglicherweise
auf Grund von Squelching oder anderer vermeintlicher Mediatoren
(Jacq, X. et al., Cell 79:107-117 (1994); Lee, J.W. et al., Nature 374:91-94
(1995); Le Douarin, B. et al., EMBO J. 14:2020-2033 (1995); vom
Baur, E. et al., EMBO J. 15:110-124 (1996); Lee, J.W. et al., Endocrinology
9:243-254 (1995); Cavailles, V. et al., EMBO J. 14:3741-3751 (1995);
Onate, S.A. et al., Science 270:1354-1357 (1995)) und/oder Transkriptionsfaktoren.
-
Wie
erwartet, führte
die Coexpression von TIF2.1 mit Antagonist-gebundenem NR nicht zu
einer beliebigen Stimulation der Transaktivierung, die durch AF-1
in der Anwesenheit von reinen AF-2-Antagonisten bewirkt wird (Berry,
M. et al., EMBO J. 9:2811-2818 (1990); Meyer, M.E. et al., EMBO
J. 9:3923-3932 (1990)), die weiter stützen, dass TIF2 AF-2-spezifisch
ist (5b und 5e für ER, OHT; 5d für
PR, RU486). Die TIF2-Expression steigerte auch die AF-2/Agonisten-vermittelte
Transaktivierung durch die Androgen (AR)- und Progesteron (PR)-Rezeptoren,
aber nicht die Transaktivierung durch GAL-VP16 und GAL-AP2 (5c). Unter ähnlichen
Bedingungen waren die Transaktivierungen durch GAL-RAR, GAL-RXR,
GAL-VDR, GAL-TR und GAL-GR durch TIF2 unbeeinflusst (5c, und nicht gezeigt), was vorschlägt, dass
für diese
NRs entweder TIF2 nicht entscheidend bei der Vermittlung ihrer AF-2-Aktivitäten einbezogen
wird oder endogene TIF2-Mengen ausreichend sind, um die Transaktivierung
optimal zu unterstützen,
weil TIF2 zum Beispiel eine höhere Affinität zu diesen
Rezeptoren hat. Die TIF2-Stimulation wird zu einigem Ausmaß durch
die Promotorumgebung des reagierenden Gens beeinflusst, wie die
TIF2-Wirkung auf die PR/5020-induzierte Transaktivierung für einen
Komplex (MMTV) größer war
als für
einen minimalen (GRE-TATA) Promotor, obwohl der letztere auch reproduzierbar
stimuliert wurde (5d). Wie von den unterschiedlichen
Niveaus der TIF2-Transkripte in verschiedenen Geweben erwartet (2c),
war die Wirkung von TIF2 Zelltyp-abhängig, da TIF2 eine viel stärkere Wirkung
auf die PR- und ER-induzierte Transaktivierungen in Cos-1 als in
HeLa-Zellen hatte
(5d, 5e).
-
Das
Squelching (Meyer, M.-E. et al., Cell 57: 433-442 (1989); Bocquel,
M.-T. et al., Nucl. Acids Res. 17:2581-2595 (1989); Tasset, D. et
al., Cell 62: 1177-1187 (1990)) und strukturelle Studien (Bourguet,
M. et al., Nature, 375:377-382 (1995); Benaud, J.-P. et al., Nature
378: 681-689 (1995); Wagner, R.L. et al., Nature 378:690-697 (1995);
Wurtz, J.-M. et al., Nature Struct. Biol. 3:87-94 (1996)) stützten ein
Modell, bei dem das Binden des Liganden an die LBD der NRs zu Konformationsänderungen
führt,
die die Oberfläche(n)
erzeugten, die für
die Interaktion mit den transkriptionalen intermediären Faktoren
(TIFs/Mediatoren), die die AF-2-Aktivität zur Transkriptionsmaschinerie übertragen,
benötigt
werden. Begreifenderweise sollten solche Mediatoren die folgenden
Eigenschaften aufweisen: (i) sie sollten an Agonist-, aber nicht
an Antagonist-gebundene NR-LBDs binden, (ii) ihr Binden sollte durch
Mutationen, die die AF-2-Aktivität
aufheben, vermieden werden, (iii) sie sollten gemeinsam (eine) Transaktivierungsfunktion(en)
aufweisen, (iv) ihre Expression sollte das AF-2-Autosquelching erleichtern,
und (v) ihre Überexpression
sollte die Aktivität
von AF-2 stimulieren, wann immer sie in begrenzenden Mengen anwesend
sind. Die vorliegende Studie ist der erste Bericht eines echten Mediators
von NR AF-2, der alle diese Eigenschaften aufweist.
-
Beispiel 2: Herstellung
von TIF2-Antikörpern
-
Die
folgenden TIF2-Antikörper
wurden unter Verwendung bekannter Methoden hergestellt, wenn nicht andererseits
nachstehend spezifiziert. S. z.B. Ausubel et al., Hrsg. CURRENT
PROTOCOLS IN MOLECULAR BIOLOGY, Greene Publishing Assoc. und Wiley
Interscience, N.Y., (1987-1996); Harlow und Lane ANTIBODIES: A LABORATORY
MANUAL Cold Spring Harbor Laboratory (1988); und Colligan et al.,
Hrsg., Current Protocols in Immunology, Greene Publishing Assoc.
und Wiley Interscience, N.Y., (1992-1996), die Inhalte, von denen
die Literaturhinweise hierin vollkommen durch Literaturhinweis berücksichtigt
sind.
-
Polyklonale Antikörper.
-
Die
TIF2.1 codierende Sequenz (Aminosäuren 624-1287) wurde in pET15b kloniert und das
resultierende Plasmid in den E. coli-Stamm BL21 (DE3) transformiert.
Nach Überexpression
des (His)6-TIF2.1-Proteins wurden die Bakterien
lysiert und das Protein aus dem Rohextrakt über Affinitätschromatographie auf einer chelatbildenden
HiTrap-Säule
(Pharmacia) aufgereinigt, wie beschrieben (s. Bourguet et al., Prot.
Expr. Purif. 6:604-608 (1995) für
technische Details). Aliquots des gereinigten Proteins (50μg) in Emulsion
(Freundsches Adjuvans) wurden (nur einmal) in ein Neuseeland-Kaninchen
unter Verwendung eines Multisite-intradermalen Injektionsprotokolls
injiziert. Antiseren, die von fortlaufenden Bleeds erhalten wurden,
offenbarten eine einzelne Bande von etwa 160 kDa auf den Western-Blots
der Extrakte aus Cos-1 Zellen, die mit einem TIF2-Expressionsvektor
von ganzer Länge
transformiert wurden.
-
Monoklonale Antikörper.
-
Ein
20mer-Aminosäurepeptid
von TIF2 (mit einem angefügten
C-terminalen Cystein) wurde auf der Grundlage seiner möglichen
immunogenen Merkmale in Begriffen von hydrophiler Eigenschaft, Flexibilität, Oberflächenwahrscheinlichkeit
und des ,antigenen Indexes' gemäß den Software-Programmen Plot und
Peptidestructure aus dem GCG-Paket ausgewählt.
-
Das
ausgewählte
Peptid entspricht dem N-terminalen Fragment, das von einer anfänglich isolierten TIF2-Teil-cDNA
codiert wurde (die die Aminosäuren
624 bis 1287 codiert) und entspricht den Aminosäuren 624 bis 643 des gesamten
Proteins (SEQ ID NO:2):
-
Das
Peptid wurde an Ovalbumin über
das zusätzliche
Cystein unter Verwendung des MBS heterobifunktionalen Crosslinkers
gekoppelt. Die Injektionen wurden in BALB/c-Mäusen intraperitoneal und intravenös durchgeführt.
-
Milzzellen
von den immunisierten Mäusen
wurden mit Sp2/0 Ag14-Myelom fusioniert. Wachsende Hybridome wurde
zuerst durch ELISA unter Verwendung des rekombinanten TIF2.1-Proteins
und des freien Peptids durchmustert. Positive Kulturen wurden dann
durch Immunozytofluoreszenz auf Cos-Zellen, die mit TIF2.1 (in dem
pSG5-Vektor) transfiziert waren, sowie durch Western-Blot unter
Verwendung der transfizierten Cos-Zellextrakte und nuclearen HeLa-Extrakte
getestet. Die positiven Kulturen wurden auch auf ihre Fähigkeit getestet,
das TIF2.1-Protein
aus den Cos-transfizierten Zellen zu immunopräzipitieren.
-
Kulturen
wurden zweimal auf weichem Agar kloniert. 5 Hybridome wurden etabliert,
4, die IgG
1, κ und 1 der IgG
2a, κ-Antikörper absonderten,
wie in der Tabelle gezeigt:
-
Beispiel 3: Identifizierung
von TIF2-NID
-
Die
ganze rekombinante DNA-Arbeit wurde gemäß Standardprozeduren durchgeführt (Ausubel,
F.M. et al., Current Protocols in Molecular Biology, John Wiley & Sons, New York
(1993)). Die GST-Verbindungen der nuclearen Rezeptoren wurden aus
den folgenden früher
beschriebenen Plasmiden exprimiert: GST (pGEX2T; Pharmacia), GST-ER
(pGEX2T-hERα(DEF),
auch pGEX2THE14G genannt, Aminosäuren 282-295),
GST-RXR (pGEX2T-mRXRa(DE), Aminosäuren 205-467) und GST-RAR (pGEX2T-hRARα(DEF), Aminosäuren 153-462)
(alle LeDourain, B. et al., EMBO J. 14:2020-2033 (1995a)).
-
Um
die TIF2-NR-Interaktionsdomäne
(NID) weiter zu beschreiben, studierten wir die Interaktion zwischen
einer Reihe von TIF2-Deletionsmutanten und den ER- oder RARa-LBDs unter
Verwendung von GST-Fusionsprotein-basierten in vitro-Assays. In beiden
Fällen
wurde eine NID auf die zentrale Region von TIF2 abgebildet (Aminosäuren 624-869
in der Mutante TIF2.5; s. 7a und 7b). Keine zusätzliche NID konnte in den N-
oder C-Termini von TIF2 identifiziert werden (7a und 7b; Mutanten
TIF2.0, TIF2.2 und TIF2.7). Beachten Sie, dass dagegen SRC-1, ein
Paralog von TIF2, offenbar zwei unterschiedliche nichtaufeinanderfolgende
NIDS beherbergt, die in den zentralen und C-terminalen Regionen
gelegen sind (Oñate,
S.A. et al., Science 270:1354-1357 (1995); Yao, T.P. et al., Proc.
Natl. Acad. Sci. USA 93: 10626-10631 (1996); Zhu, Y. et al., Gene
Expression 6: 185-195 (1996)).
-
Um
die TIF2-NID weiter einzugrenzen, wurde TIF2.5 C-terminal zu Pro
775 gekürzt,
was TIF2.34 ergab, der auch mit den ER und RARa-LBDs auf eine Liganden-abhängige Weise
interagierte (8a und 8c). Auf
weitere Kürzung
zu Ser697 interagierte die resultierende Mutante noch sowohl mit
den ER- als auch mit RARa-LBDs, aber überraschenderweise wurde eine
Liganden-abhängige
Interaktion auch mit TIF2.36 (8a und 8c) gefunden, das demnach anzeigt, dass
die TIF2-NID aus mindestens zwei unabhängigen NO-interagierenden Molekülen zusammengesetzt
ist.
-
Eine
Angleichung der TIF2-NID-Aminosäuresequenz,
die im TIF2.34 vorhanden ist, mit der entsprechenden Region von
SRC-1 (Oñate,
S.A. et al., Science 270:1354-1357 (1995)) offenbarte drei hoch
konservierte Regionen (8a).
Interessanterweise enthalten alle drei das Motiv LxxLL (SEQ ID NO:12)(8b), das ursprünglich in der so genannten „nuclearer
Rezeptor-Box" (NR-Box)
von TIF1α identifiziert
wurde, wie das LxxLLL (SEQ ID NO:13)-Motiv, das auch in RIP140 anwesend
war (Cavailles, V. et al., EMBO J. 14:3741-3751 (1995)) und TRIP3
(Lee, J.W. et al. (1995)) (s. LeDouarin, B. et al., EMBO J. 15:6701-6715 (1996)
und 8b). Wichtigerweise waren die
10-Aminosäuren-Sequenzen,
die die TIF1α-
oder RP140-NR-Boxen umfassten, ausreichend für die funktionelle Interaktion
mit RXR auf eine Liganden- und AF-2-AD-Integrität-abhängige Weise, und die Mutation
der Leucine an Position 4 und 5 (LL → AA) des LxxLLL (SEQ ID NO:13)-Motivs
von TIF1α hob
die TIF1α-RXR-Interaktion
auf (LeDouarin, B. et al., EMBO J. 15: 6701-6715 (1996)). Die Funktionalität der RIP140-NR-Box
wurde neulich bestätigt
(Heery, D.M. et al., Nature 387:733-736 (1997)).
-
Um
die funktionelle Bedeutung dieser drei Motive in der TIF2-NID zu
erforschen, wurde die voranstehende LL → AA-Mutation in TIF2.1 eingebracht,
entweder in jedes Motiv alleine oder in allen möglichen Kombinationen der drei
Motive (TIF2.1m1 zu m123 in 8a;
die Zahlen, die „m" folgen, verweisen
auf die mutierten Motive). Die Mutation aller drei NR-Boxen wurden
benötigt,
um sowohl das Binden an ER, RARα und
RXRα (8d, Quantifizierung in 8e,
weiße
Balken), als auch die TIF2-abhängige
Stimulation der Liganden-induzierte Transaktivierung durch ER und
RXRα-AF-2s
(8e, schwarze Balken und Daten nicht
gezeigt; in dem Fall von RARα-AF-2
war die Stimulation schwach und wurde nicht quantifiziert) aufzuheben.
Die TIF2.1-Konstrukte, bei denen zwei NR-Box-Motive mutiert waren,
wiesen noch das ER-Binden und die Stimulation der AF-2-Aktivität auf, insbesondere,
wenn das NR-Box-Motiv II intakt war, was vorschlägt, dass die drei NR-Box-enthaltenden
Module mindestens teilweise funktionell überflüssig sind (8d und 8e; TIF2.1m12, m13 und m23). Diese Überflüssigkeit
war deutlich, wenn nur ein NR-Box-Motiv mutiert war; im Gegensatz
zu TIF1α,
der nur eine NR-Box
enthält
(LeDouarin, B. et al., EMBO J. 15:6701-6715 (1996)), hob die Mutation einer
einzelnen TIF2-Box das ER-Binden und die Stimulation der ER-AF-2-Aktivität nicht
auf. Alle drei Mutanten (TIF2.1m1 bis m3) banden an ER und stimulierten
die Estradiol-abhängige
Transaktivierung durch den ER mit ähnlicher Effizienz wie TIF2.1
selbst (8d und 8e).
In dem Fall von RARα und
RXRα hatten
die Mutationen allgemein eine schädlichere Wirkung auf das Rezeptor-LBD-Binden
und die Stimulation der AF-2-Aktivität als in dem Fall von ER (8d und 8e).
Dies kann möglicherweise
eine schwächere
Interaktion zwischen TIF2 und entweder RARα oder RXRα als mit ER widerspiegeln. Jedoch
waren trotz des allgemeinen Aufweisens von geringer Aktivität die Muster
des NR-Bindens und der Stimulation von AF-2-Aktivität der NR-Box-Mutanten ähnlich für ER und
RARα und
RXRα, wie
die Mutation von Motiv II immer schädlicher in Doppelmutanten war
als die Mutation der Motive I und III (s. 8e).
Wichtigerweise gab es sowohl für
ER als auch RXRα eine gute
Korrelation zwischen der Wirkung einer beliebigen der verschiedenen
Mutationen an das TIF2.1-Rezeptor-Binden in vitro und der TIF2.1-vermittelten
Stimulation der AF2-Aktivität
(8e), was einen Mechanismus stützt, wodurch
die Stimulation der AF-2-Aktivität
durch TIF2 die TIF2-NO-Interaktion durch das/die NR-holo-LBD-TIF2-NR-Box-Zwischenstück(e) einbezieht.
-
Unsere
vorliegende Struktur-Funktion-Analyse offenbart, dass TIF2 eine
einzelne nuclearer Rezeptor-Interaktionsdomäne (NID) enthält. Beachten
Sie im Gegensatz zu dem anderen TIF2-Familienmitglied SRC-1, von
dem berichtet wurde, nur zwei NIDs zu enthalten (Oñate, S.A.
et al., Science 270:1354-1357 (1995); Yao, T.P. et al., Proc. Natl.
Acad. Sci. USA 93: 10626-10631 (1996); Zhu, Y. et al., Gene Expression
6: 185-195 (1996)). Beachten Sie jedoch, dass eine der zwei SRC-1-NID
am wahrscheinlichsten homolog zu der hier charakterisierten TIF2-NID
ist (s. 8a). Die TIF2-NID ist aus drei
Modulen zusammengesetzt, und jedes kann unabhängig auf eine Liganden-abhängige Weise
an die in dieser Studie gestesteten NRs binden. Interessanterweise
enthalten diese Module das NR-Box-Motiv LxxLL (SEQ ID NO:12), das
ursprünglich
(als das Motiv LxxLLL (SEQ ID NO:13), 8b)
innerhalb eines 10-Aminosäure-NR-bindenden
Modul von TIF1α aufgenommen
wurde, das gefunden wurde, konserviert in der NID von RIP140 und
auch in TRIP3 anwesend zu sein (LeDouarin, B. et al., EMBO J. 15:6701-6715
(1996) und Literaturhinweise darin). Darüber hinaus wurde gezeigt, dass
die TIF1α-
und RIP140-Module
funktionell mit den NRs interagieren (LeDouarin, B. et al., EMBO J.
15:6701-6715 (1996)).
Die Auswirkung der NR-Box-Motive beim NO-Coaktivator-Binden und
ihre Anwesenheit in einen Anzahl von verschiedenen Coaktivatoren
wurde in neuen Berichten aufgezeigt (Heery, D.M. et al., Nature
387:733-736 (1997); Torchia, J. et al., Nature 387:677-684 (1987);
LeDouarin, B. et al., EMBO J. 15:6701-6715 (1996)). Beachten Sie,
dass alle drei hier beschriebenen TIF2-NR-Box-Motive in dem neulich entdeckten
TIF2-Paralog p/CIP konserviert sind (Torchia, J. et al., Nature
387:677-684 (1987)).
Im Gegensatz zu TIF1α,
für den
die Mutation von Leucinen zu Alanin an den Positionen 4 und 5 seines
einzelnen NR-Box-Motivs (LL → AA)
das NR-Binden aufhebt, wird die Mutation von allen drei Motiven
in der TIF2-NID benötigt,
um das NR-Binden aufzuheben, was anzeigt, dass jedes dieser Motive
zu einer TIF2-Oberfläche, die
mit einer verwandten Oberfläche
der NR-holo-LBDs interagiert, beitragen kann. Dass die NR-Boxen
von TIF2 funktionelle Überflüssigkeit
aufweisen, wird durch die Beobachtung gestützt, dass die LL → AA-Mutation
in einem beliebigen der drei TIF2-NID-Motive offenbar nicht (in
dem Fall des ER) oder nur schwach (in dem Fall von RARα, RXRα) die Effizienz
der NR-Interaktion reduziert. Darüber hinaus war in der TIF2.1-Umgebung
ein beliebiges einzelnes intaktes NR-Box-Motiv für sich allein (d.h., wenn die
zwei anderen Motive mutiert waren) ausreichend für die Interaktion mit der holo-ER-LBD,
obwohl nur Motiv II für
sich allein eine fast Wildtyp-NR-Bindungseffizienz
bewirken konnte. Dagegen waren für
die RARα-
und RXRα-Interaktion die Mutanten
mit einzelnen intakten NR-Boxen 5mal (Box II) bis 20mal (Box I oder
III) weniger effizient als der Wildtyp-TIF2, der die drei NR-Boxen
enthält.
Kristallographie-Studien werden notwendig sein, um zwischen den
zwei möglichen
Modellen zu unterscheiden, bei denen die drei NR-Box-Motive (i)
zu der Bildung einer dreiteiligen NID-Oberfläche beitragen, die spezifisch
eine verwandte holo-NO-LBD-Oberfläche erkennt,
oder (ii) zu unabhängigen
Oberlächen
gehört,
von denen jede, wenn auch mit unterschiedlichen Effizienzen, mit
derselben holo-NO- Oberfläche interagieren
kann. Beachten Sie, dass jedoch das zweite Modell TIF2 erlauben
könnte,
kooperativ mit beiden Partnern der NR-Homo- oder Heterodimere zu
interagieren, die demnach die Transaktivierung durch NRs erbringen,
die empfindlich zu kleinen Variationen in den TIF2-Niveaus sind.
Beachten Sie auch, dass für
sowohl BR als auch RXRα die
Wirkungen der NR-Box-Mutationen auf das NR-Binden und die Stimulation
der AF-2-Aktivität
korreliert wurden, was weiter die Feststellung stützt, dass
die Transkriptionswirkung von TIF2 die Bildung eines NR-Box-NO-LBD-Interaktionszwischenstücks einbezieht.
-
Das
Motiv LxxLL (SEQ ID NO:12) wurde in einer Anzahl von anderen NR-Coaktivatoren gefunden
(s. voranstehend), was demnach einige Ähnlichkeit in der Art und Weise
der NO-Coaktivator-Interaktionen vorschlägt. Dies schließt jedoch
nicht die NO-spezifische Modulation dieser Interaktionen aus, da
die NR-Box umgebenden Sequenzen hoch variabel sind. In dieser Hinsicht
beachten Sie auch, dass vorhergesagt wird, dass die TIF2-NR-Boxen
II und III α-Helices
bilden, während
vorhergesagt wird, dass die NR-Box I in eine β-Faltblatt-Struktur faltet (Strukturvorhersaagen
gemäß SOPMA;
Geourjdon und Deleage, 1994).
-
Beispiel 4: Identifizierung
der AD1- und AD2-Aktivierungsdomänen
von TIF2
-
Vorübergehende
Transfektionsassays mit einem GAL4-Reporterplasmid und Chimäre, die
verschiedene TIF2-Fragmente enthielten, die mit der GAL4-DNA-bindenden Domäne (DBD)
verbunden sind, zeigten die Anwesenheit von zwei unabhängigen Transkriptionsaktivierungsdomänen in den
C-terminalen 460 Aminosäuren
vor TIF2, AD1 und AD2 genannt (beschrieben durch die Mutanten TIF2.8,
TIF2.12 und TIF2.2 in 7a und 7c).
Vorübergehende
Transfektionen von HeLa- und Cos-1-Zellen wurden durchgeführt, wie
beschrieben (Gronemeyer et al., (1987); Bocquel, M.T. et al., Nucl.
Acids. Res. 17:2581-2595 (1989)).
-
Die
N-terminale AD1 (Aminosäuren
1010-1131), die in TIF2.1 vorhanden ist, zeigte eine stärkere Aktivität als die
C-terminale AD2 (Aminosäuren
1288-1464) (vgl. TIF2.8 und TIF2.12 mit TIF2.2 in 7a und 7c). Beachten
Sie, dass jedoch die schwächere
Aktivität
von AD2 (relativ zu AD1) auf Grund eines geringeren Expressionsniveaus
des GAL-TIF2.2-Fusionsproteins sein könnte (vgl. mit GAL- TIF2.8 und GAL-TIF2.12
in 7c). Beide TIF2-Aktivierungsfunktionen
waren in Cos-1- und HeLa-Zellen aktiv (7c).
Besonders die minimalen AD1 (TIF2.8)- und AD2 (TIF2.2)-Konstrukte
wiesen einige zellspezifische Aktivitäten auf, weil GALTIF2.8 aktiver
in HeLa- als in Cos-Zellen war, während das Gegenteil für GAL-TIF2.2 (7c) beobachtet wurde. Interessanterweise
konnte die Glutamin-reiche Region von TIF2 weder die Transkription
für sich
alleine aktivieren, wenn sie mit der GAL4-DBD (7a und 7c; Mutante
TIF2.6) fusioniert war, noch wurde sie für die Transkriptionsaktivierung
durch AD1 oder AD2 benötigt.
Keine Aktivierungsfunktion konnte in dem N-terminalen Teil von TIF2
nachgewiesen werden (s. 7a und 7c; Mutante TIF2.0).
-
Wir
schließen
aus diesen Daten, dass die nuclearer Rezeptor-interagierende Domäne (NID)
und die zwei Transkriptionsaktivierungsfunktionen von TIF2 den unterschiedlichen
modularen Domänen
entsprechen, da TIF2.5 an die NRs binden kann, aber nicht die Transkription
aktivieren kann, während
TIF2.2 und TIF2.8 nicht an die NRs binden können, aber die Transkription
aktivieren können
(7a).
-
Beispiel 5: Charakterisierung
der TIF2-AD1- und -AD2-Aktivierungsdomänen
-
Neulich
wurde gezeigt, dass CBP und p300, die ursprünglich als Coaktivatoren des
Transkriptionsfaktors CREB identifiziert wurden, als allgemeine
Integratoren von mehreren Signalwegen wirken, einschließlich der
Aktivierung über
die Agonistgebundenen RARa und TR (für Reviews und Literaturhinweise
s. Eckner, R. Biol. Chem. 377:685-688 (1996); Janknecht & Hunter, (1996);
Glass, C.K. et al., Current Opin. Cell Biol. 9:222-232 (1997); Shikama,
N. et al., Trends in Cell Biol. 7:230-236 (1997)). Darüber hinaus
wurde berichtet, dass SRC-1, das zu derselben Genfamilie wie TIF2
gehört,
mit CBP und p300 interagiert (Kamel, Y. et al., Cell 85:403-414
(1996); Yao, T.P. et al., Proc. Natl. Acad. Sci. USA 93:10626-10631
(1996); Hanstein, B. et al., Proc. Natl. Acad. Sci. USA 93: 11540-11545
(1996)). Unter Verwendung der GST-Fusionsprotein-basierten Interaktion
und Tierzell-basierten Zwei-Hybrid-Assays analysierten wird daher,
ob TIF2 auch mit CBP interagieren könnte. In dem Zwei-Hybrid-System
bewertete nur das zentrale TIF2.1-Fragment, aber nicht das N-terminale
TIF2.0- oder das C-terminale TIF2.2-Fragment (7a) positiv für
die Interaktion mit GAL-CBP (das die Aminosäuren 18722-2165 von CBP enthält, das
die SRC-1 interagierende Domäne
von CBP umfasst; 7e). Ein GST-CBP-Fusionsprotein
wurde in E. coli exprimiert und für Pulldown-Assays mit in vitro
translatierten TIF2-Polypeptiden (7d)
verwendet. TIF2 interagierte mit CBP und interessanterweise überlappte die
CBP-interagierende Domäne
(CID) offensichtlich die AD1-Aktivierungsdomäne von TIF2 (vgl. 7a, 7c und 7d; Mutanten TIF2.8 und TIF2.12). Die Interaktion
von TIF2 mit CBP war direkt, da ein aufgereinigtes E.coli-exprimiertes
TIF2.1-Protein auch mit GST-CBP interagierte (Daten nicht gezeigt).
Nur diese Region von TIF2 interagierte signifikant mit dem GST-CBP-Fusionsprotein, was
demnach vorschlägt,
dass die TIF2-AD1-Aktivität
aus der Rekrutierung von CBP entstehen kann. Abführer N-terminale Regionen ( 7a und 7d; Mutanten
TIF2.10 und TIF2.4) oder die C-terminale AD2-Aktivierungsdomäne (7a und 7d; Mutante TIF2.2) zeigten kein Binden
an GST-CBP. Beachten Sie, dass TIF2.2 auch nicht mit CBP ganzer
Länge interagierte
(Daten nicht gezeigt), was vorschlägt, dass die Aktivität von TIF2-AD
durch (einen) Faktoren) vermittelt wird, der/die von CBP unterschiedlich
ist/sind.
-
Um
zu erforschen, ob die CID von TIF2 von der AD1-Aktivierungsdomäne getrennt
werden könnte, wurde
die Fähigkeit
einer Reihe von GAL-TIF2-Kürzungsmutanten,
einen GAL4-Reporter zu aktivieren, mit ihrer Fähigkeit verglichen, mit dem
GST-CBP-Protein in vitro zu interagieren (9).
TIF2.13 (der Pro1011 bis Ser1122 umfasst)
wies eine starke Transkriptionsaktivität auf, vergleichbar mit der
eines größeren TIF2-Fragments
(vgl. 7 und 9).
Das Entfernen von 26 C-terminalen (TIF2.15) oder 20 N-terminalen
(TIF2.18) Aminosäureresten
reduzierte die Transkriptionsaktivität nur schwach (9a und 9b). Beachten
Sie, dass TIF2.13 auch mit CBP in vivo interagierte, wie durch Verwendung
eines Zwei-Hybrid-Assays bei transfizierten Säugetierzellen gezeigt (10b).
-
Während die
interne Deletion der Reste Aspios1061 bis
Ala1070 (TIF2.19) nur eine geringe Wirkung
auf die Fähigkeit
von TIF2.13 hatte, zu transaktivieren, reduzierte die Deletion des
Abschnitts von Glu1071 bis Leu1080 (Mutante
TIF2.20) signifikant die Transkriptionsaktivität von TIF2-AD1. In besonderem
Maße gehören diese
Reste zu einer Sequenz, die vorhergesagt wurde, in eine amphipathische α-helicale
Struktur zu falten, die zwischen TIF2 und SRC-1 hoch konserviert
ist (9a). Die Einbeziehung dieser
Region in die Transaktivierung wurde durch Analyse der Mutanten
TIF2.21 bis TIF2.32 bestätigt
(9a und 9b). Alle
Konstrukte, die die TIF2-Wildtyp-Sequenz von Asp1075 bis
Leu1087 enthielten, stimulierten die Transkription,
während
selbst eine Deletion von nur einigen dieser Reste die Transkriptionsaktivierung
signifikant reduzierte. Jedoch für
sich allein transaktivierte dieses α-helicale Peptid sehr schlecht
und musste in zusätzliche
Stromaufwärts- und/oder Stromabwärts-TIF2-Sequenzen
eingebaut werden, um signifikante Transkriptionsaktivität zu erzeugen (9a und 9b; vgl. Mutanten
TIF2.13, TIF2.21 und TIF2.32). Wichtigerweise deckte sich in allen
Fällen
die ADD-Aktivität
mit der CBP-Interaktion, da transkriptional inaktive Konstrukte
nicht mit CBP interagierten (TIF2.24, TIF2.27 und TIF2.29 in 9a-9c), während transkriptional
aktive Mutanten auch CBP banden. Außerdem korrelierte die Stärke der
in vitro-Interaktion mit GST-CBP offensichtlich mit der Transaktivierungseffizienz
(9a-9c; z.B., vgl.
TIF2.21 und TIF2.31).
-
Um
zu erforschen, ob die Integrität
der vermeintlichen amphipathischen α-helicalen Region sowohl für die AD1-Transkriptionsaktivität als auch
für die
Interaktion mit CBP benötigt
wird, brachten wir Punktmutationen in TIF2.13 ein; die drei konservierten
hydrophoben Leu- oder die hydrophilen Asp-Glu-Reste wurden mit Alaninen
getauscht [9a; TIF2.13(LLL) und TIF2.13(DQ)].
Interessanterweise hob die Mutation der drei Leucinreste fast vollständig die
AD1-Aktivität
auf, während
die Mutation der Asp-Glu-Sequenz eine sehr geringe Wirkung, wenn überhaupt,
hatte (10a). Wieder waren AD1-Aktivität und Interaktion
mit CBP in vitro (10c), sowie in vivo
(10b), strengstens korreliert, da
GAL-TIF2.13(DQ), der so effizient wie der Wildtyp GAL-TIF2.13 transaktivierte,
stark mit CBP interagierte, während
der transkriptional inaktive GAL-TIF2.13(LLL) sehr schwach mit CBP
interagierte. Zusammen zeigen diese Ergebnisse an, dass (i) CBP
die AD1-Aktivität von
TIF2 vermittelt, (ii) ein vermeintliches amphipathisches α-Helix-Motiv,
das innerhalb der AD1-Domäne
gelegen ist, entscheidend in, aber nicht ausreichend für effizientes/effiziente
CBP-Binden/Transaktivierung einbezogen wird und (üi) die Amphiphilizität des Motivs
für die
AD1-Aktivität
und das CBP-Binden nicht benötigt wird.
-
Die
zwei TIF2-Aktivierungsfunktionen AD1 und AD2 operieren offensichtlich
durch verschiedene Transkriptionsaktivierungskaskaden. Während die
TIF2-AD1-Aktivierungsdomäne durch
Mutationsanalyse von der TIF2-Domäne, die in vitro und in vivo
mit einer Region der CBP-Oberfläche
interagiert, die auch das SRC-1-Binden vermittelt (Kamel, Y. et
al., Cell 85:403-414 (1996)), nicht getrennt werden konnte, interagierte weder
diese Region noch CBP von ganzer Länge mit TIF2-AD2. Dass die
zwei TIF2-Aktivierungsfunktionen durch unterschiedliche Wege operieren
können,
wird auch durch die unterschiedliche Zellspezifität der minimalen
Fragmente, die AD1-Aktivität
(z.B. TIF2.8, TIF2.7, TIF2.9, TIF2.12) und AD2-Aktivität (TIF2.2)
aufweisen, vorgeschlagen. Während
TIF2.2 in Cos-1-Zellen aktiver ist als in HeLa-Zellen, sind alle
der minimalen Fragmente, die AD1 enthalten, aktiver in HeLa-Zellen. Analog führte das
Entfernen in TIF2.3 von Sequenzen, die N-terminal von TIF2.8 sind,
zu einer jeweils 10-fachen und 2-fachen erhöhten Transaktivierung in HeLa- und
Cos-1-Zellen, und das Entfernen in TIF2.1 von Sequenzen, die C-terminal
von TIF2.3 sind, ergaben jeweils eine 9-fache und 3-fache höhere Transaktivierung
in HeLa- und Cos-1-Zellen. Dies schlägt vor, dass die deletierten
Sequenzen entweder eine intra- oder intermolekulare Hemmung auf
die TIF2-AD1-Aktivität/CBP-Interaktion
ausüben
könnten.
Zusätzlich
kann die Coaktivator-Aktivität
von TIF2 zellspezifisch durch die unterschiedliche Effizienz seiner
zwei ADs und Faktoren, die mit den Sequenzen N- und C-terminal der AD1-Aktivierungsfunktion
interagieren, moduliert werden.
-
Es
ist wert, zu beachten, dass das Kernstück von AD1 (TIF2.32) für sich allein
ein sehr schwacher Transaktivator und CBP-Binder ist, und zusätzliche
umgebende Sequenzen benötigt,
um eine vollständig
aktive (d.h. effiziente CBP-bindende) Oberfläche zu erzeugen. Jedoch offenbart
die Mutationsanalyse des AD1-Kernstücks in dem Zusammenhang eines
starken Aktivatorfragments (TIF2.13) die entscheidende Wichtigkeit
für die
Transaktiverung das das CBP-Binden in vivo und in vitro von drei
Leucinresten (10). Diese Leucine gehören zu einem
konservierten LLxxLxxxL (SEQ ID NO:14)-Motiv bei allen drei Mitgliedern
der TIF2-Coaktivatorfamilie (9a;
Torchia, J. et al., Nature 387:677-684 (1987)), das von dem LxxLL
(SEQ ID NO:12) NR-Box-Motiv verschieden ist. In besonderem Maße, obwohl
diese Leucine in einer vorhergesagten amphipathischen α-Helix eingebettet
sind, wird die Amphiphilizität
für die
Funktion nicht benötigt,
da eine Mutation der hydrophilen Reste (vgl. TIF2.13 mit TIF2.13(DQ))
nicht die Transaktivierung/das CBP-Binden beeinflusst.
-
TIF2
kann offensichtlich mindestens zwei Mediatorfunktionen erfüllen, (i)
als ein „Brücke schlagender Faktor" zwischen der AF-2-Funktion
von nuclearen Rezeptoren und CBP über seine AD1-Aktivierungsdomäne und (ii)
als ein Transkriptionsmediator durch (eine) bisher unbekannte CBP-Bindungs-unabhängige Route(n) über seine
AD2-Funktion. Zur Zeit haben wir keinen Beweis, dass TIF2 eine intrinsische
enzymatische Aktivität besitzen
könnte;
keines der bakteriell exprimierten aufgereinigten TIF2-Fragmente,
insbesondere TIF2.1, das gezeigt wurde, bei NR- und CBP-Interaktionen in vitro vollständig befähigt zu
sein, wies eine beliebige Histonacetylase-Aktivität unter
Bedingungen auf, wo bakteriell exprimiertes aufgereinigtes Hefe-GXNS
hoch aktiv war (unsere nicht publizierten Ergebnisse).
-
Beispiel 6: TIF2-Verstärkung der
NR-AF2-Aktivifät
-
Die
Beobachtung, dass Transkriptionsaktivatoren vom Tier, wie der menschliche
ER (Metzger, D. et al., Nature 334:31-36 (1988)) auch in der Hefe
Saccharomyces cerevisiae aktiv sind, zeigte, dass die grundlegenden
Prinzipien der Transkriptionsverstärkung von der Hefe zum Menschen
konserviert wurden. Wir erforschten daher, ob TIF2 die Transkriptionsaktivierung
durch verschiedene NR-Konstrukte,
die in S. cerevisiae exprimiert werden, erhöhen könnte. Sowohl NRs als auch TIF2.1
wurden aus Multikopie-Plasmiden in dem Hefestamm PL3(α) exprimiert,
der ein URA3-Reportergen unter der Kontrolle von drei Östrogen-Response-Elementen enthält (ERE)3-URA3; Pierrat, B. et al., Gene 119:237-245
(1992)).
-
In
der Hefe wurden die hERα-Konstrukte
aus den folgenden YEp90-basierenden
Plasmiden exprimiert: HEGO (hERα,
YEp90-HEG19, Aminosäuren
1-595) HE15 (Yep90-HE15;
Aminosäuren
1-282) und HEG19 (Yep90-HEG19, Aminosäuren 179-595) (alle Pierrat,
B. et al., Gene 119:237-245 (1992)), HE179-338 (YEp90-HE179-338;
Pierrat, B. et al., Gene 143:193-200 (1994)). Aus dem Hefe-Multikopie-Plasmid
pBL1 (LeDouarin, B. et al., Nucleic Acids Res. 23:876-878 (1995b)),
das für
ER(F)-Epitop-markierte ER(C)-Verbindungen codiert, wurden die folgenden
Plasmide exprimiert: ER(C)-RAR(DEF) (pBL1-hRARa(DEF), Aminosäuren 154-462)
und ER(C)-RXR(DE) (pBL1-mRXRα(DE),
Aminosäuren
205-467) (beide vom Baur, E. et al., EMBO J. 15:110-124 (1996)).
TIF2 wurde in Hefe aus dem Multikopie-Plasmid pAS3 (Geschenk von
B.LeDouann) exprimiert, das ein Derivat von YEp90 ist, das den LEU2-Marker
enthält.
Hefe-PL3(α)-Transformanten
(Pierrat, B. et al., Gene 119:237-245 (1992)) wurden exponentiell
in der Anwesenheit oder Abwesenheit des Liganden für etwa fünf Generationen
in selektivem Medium gezüchtet,
das Uracil enthielt. Hefeextrakte wurden präpariert und nach OMP-Decase-Aktivität untersucht,
wie früher
beschrieben (Pierrat, B. et al., Gene 119:237-245 (1992)).
-
Wie
aus früheren
Studien erwartet (Metzger, Nucl. Acids. Res. (1992); Pierrat, B.
et al., Gene 119:237-245 (1992); Pierrat, B. et al., Gene 143:193-200
(1994)), induzierte der ER (HEGO) von ganzer Länge die Aktivität der Orotidin-5'-Monophosphat-Decarboxylase (OMP-Decase)
auf eine Liganden-abhängige
Weise (11, Spuren 1 und 3). Interessanterweise
wurde die Transkriptionsaktivität
von ER durch Coexpression des TIF2.1-Fragments weiter erhöht (11, vgl. Spuren 3 und 4). In der Abwesenheit von
Hormon hatte TIF2.1 keine signifikante Wirkung auf die ER-induzierte
Transkriptionsaktivierung (11,
vgl. Spuren 1 und 2). Im Wesentlichen wurden die gleichen Ergebnisse
für HEG19
beobachtet, das frei von der N-terminalen Region A/B ist, was anzeigt,
dass TIF2 seine Wirkung auf die Liganden-abhängige ER-AF-2 ausübt (11, Spuren 5-8). Dagegen wurden weder die AF-1-Aktivität von HE15,
(das die ER-Regionen A, B und C umfasst; Kumar & Chambon, Cell 55: 145-156 (1988)),
noch die AF-2a-Aktivität
des HE179-338-Konstrukts
(Pierrat, B. et al., Gene 143:193-200 (1994)) durch coexprimierendes
TIF2.1 stimuliert (11 Spuren 9-12). Dies ist in Übereinstimmung
mit den in Säugetierzellen
erhaltenen Ergebnissen und mit der Beobachtung, dass eine intakte
LBD für
TIF2.1 benötigt
wird, um mit dem ER zu interagieren (Voegel, J.J. et al., EMBO J.
15:3667-3675 (1996)).
-
TIF2.1
stimulierte auch die AF-2-Aktivität der ligandierten RXRα(DEF)-Region
in der Hefe (11, vgl. Spuren 19 und 20).
Diese Verstärkung
war Ligandenabhängig;
keine Aktivierung über
die RXRα(DEF)-Region wurde
beobachtet, wenn die ER(C)-RXRα(DEF)-Chimäre mit TIF2.1
in der Abwesenheit des Liganden coexprimiert wurde (11, vgl. Spuren 18 und 20). Wieder liefen diese
Beobachtungen parallel zu jenen, die bei HeLa- und Cos-1-Zellen
gemacht wurden (s. 12c).
-
Überraschenderweise
erhöhte
TIF2.1 sogar in Abwesenheit des Liganden und im Gegensatz mit den mit
ER und RXRα gemachten
Beobachtungen sehr effizient die Transaktivierung durch die RARα-LBD (11, Spuren 13 und 14). Die Zugabe von Retinolsäure steigerte
weiter diese Transkriptionsaktivierung (11,
Spuren 14 und 16). Beachten Sie, dass, wie früher berichtet (Heery, D.M.
et al., Nature 387:733-736 (1997)), sowohl RARα als auch RXRα-AF-2 für sich alleine
die Transkription von dem URA3-Reporter schlecht aktivierten.
-
Die
Verstärkung
der AF-2-Aktivität,
die besonders stark in Hefezellen war, wurde auch neulich für GRIP1,
dem Maushomolog von TIF2 beobachtet (Hong, H. et al., Mol. Cell
Biol. 17:2735-2744 (1997)). Diese Beobachtungen schlagen vor, dass
Hefezellen Coaktivatoren enthalten, die nur schlecht die Wirkung
der Säugetier-NR-Coaktivatoren imitieren.
Da Hefezellen offensichtlich kein CBP-Homolog enthalten, wird es
interessant werden, zu erforschen, welcher Hefefaktor die Aktivität von TIF2
vermittelt. Beachten Sie in dieser Hinsicht, dass GAL-TIF2.1 ein
starker Transkativator in der Hefe ist (unsere nicht publizierten
Ergebnisse).
-
Interessanterweise
führte
die Expression von TIF2 in Hefe zu einer merklichen Stimulation
der Transaktivierung durch den nicht ligandierten ER(C)-RARα(DEF), die
nicht mit nicht ligandierten LBDs von ER oder RXRα beobachtet
wurde. Strukturuntersuchungen offenbarten, dass das Binden des Liganden
zu einer Konformationsänderung
der LBD führt,
die die Oberfläche(n)
für das
Coaktivator-Binden
erzeugt (Renaud, J.P. et al., Nature 378:681-689 (1995)). Daher
schlägt
unser vorliegendes Ergebnis vor, dass ein hohes Niveau von Coaktivatoren
in der Abwesenheit von Ligand die LBD einiger Rezeptoren in eine
holo-LBD-ähnliche
Konformation treibt, die demnach zur Liganden-unabhängigen Transkriptionsaktivität führt. Bei
Analogie könnte
einer spekulieren, dass hohe Niveaus von Coexpressoren die NR-LBDs
in die apo-LBD-Konformation „einschließen" könnte. Es
würde daher
interessant sein, zu erforschen, ob Niveaus von Coregulatoren zu
einer aufbauenden Aktivität
(sogar in Anwesenheit von Antagonisten) oder umgekehrt zum Mangel
der Induzierbarkeit von nuclearen Rezeptoren in einigen pathologischen
Zuständen
führen.
-
Beispiel 7: TIF2-NID-Hemmung
der NR-AF-2-Aktivität
-
Die Überexpression
des TIF2.1-Fragments, das sowohl die NID als auch die AD1-Aktivierungsfunktion enthält, stimuliert
vorübergehend
die ER-AF-2-Aktivität
der ER-LBD in Cos-1-Zellen (12a, Spuren
2 und 3; Voegel, J.J. et al., EMBO J. 15:3667-3675 (1996)). Dass
diese Stimulation auf eine direkte Interaktion zwischen der ER-LBD
und der NID von TIF2 beruhte, wurde stark durch die Beobachtung
vorgeschlagen, dass die Überexpression
der TIF2.5-Mutante, die die isolierte NID enthält, der aber AD1 fehlt (s. 7a), die stimulatorische Wirkung von TIF2.1 verhinderte
(12a, vgl. Spuren 3 und 4). Beachten
Sie, dass in der Abwesenheit von TIF2.1 die TIF2.5-Überexpression
auch die Transaktivierung durch die ER-AF-2 verringerte, die vermutlich
durch Cos-1-endogene Coaktivatoren vermittelt wurde (12a, vgl. Spur 4 mit Spur 2), was demnach
vorschlägt,
dass diese Cos-1-Mediatoren
entweder endogenen TIF2s entsprechen oder mit der ER-holo-LBD durch
Oberflächen
interagieren, die identisch mit oder in direkter Nachbarschaft von
der TIF2-NID-Interaktionsoberfläche
sind.
-
Wir
berichteten früher über eine
Agonisten-abhängige
Interaktion von TIF2 mit RAR- und RXR-LBDs, die abhängig von
der Integrität
des NR-AF-2-AD-Kernstücks
war, aber versagten, eine stimulatorische Wirkung von TIF2 auf die
Transkriptionsaktivierung eines (17m)5-Globin-Promotor-CAT-Reporter
durch die Fusionsproteine GAL-RAR-LBD oder GAL-RXR-LBD zu beobachten
(Voegel, J.J. et al., EMBO J. 15:3667-3675 (1996)). Da der Misserfolg
wahrscheinlich auf der Anwesenheit von ausreichenden Mengen von
endogenen Mediatoren zur Ausführung
maximaler Transaktivierung aus diesem Reportergen beruhte, modifizierten
wir die Transfektionsbedingungen und verwendeten ein Reporterkonstrukt,
das einen minimalen Promotor trug. Eine deutliche TIF2 und TIF2.1
stimulatorische Aktivität
für RXRα-AF2 wurde
bei HeLa- und Cos-1-Zellen während
der Verwendung des (17m)5-TATA-CAT-Reporters
beobachtet (12c, vgl. Spuren 3-6 und
11-14). Diese stimulatorische Wirkung war weniger merklich mit RARα-AF-2 und
konnte reproduzierbar nur mit dem TIF2.1-Fragment in Cos-1-Zellen
beobachtet werden (12d, vgl. Spur
10 mit Spuren 13 und 14; beachten Sie, dass TIF2.1 bei > 10-fach höheren Niveaus
als TIF2 exprimiert wird; Daten nicht gezeigt). Die Reporterplasmide (17m)5-TATA-CAT (May, M. et al., EMBO J. 15:3093-3104 (1996)) und
17M5-G/CAT ((17m)5-β-Globin-CAT; Durand, B. et al.,
EMBO J. 13:5370-5382 (1994)) enthalten jeweils fünf Kopien des GAL4-Response-Elements jeweils
vor einem einfachen TATA-Motiv oder einem β-Globin-Promotor stromaufwärts von
dem CAT-Reportergen.
-
Angenommen,
dass TIF2 oder Coaktivatoren, die die TIF2 interagierende Oberfläche auf
NR-LBDs erkennen, allgemein die AF-2-Funktion von NRs vermitteln,
sollte die TIF2.5 enthaltenden NID ihre vorherrschende negative
Aktivität
nicht nur auf ER, sondern auch auf andere NRs, unabhängig von
dem zellulären Zusammenhang,
ausüben.
Wir analysierten daher die Wirkung von TIF2.5 auf die AF-2-Aktivität von ER,
RXRα und
RARα in
HeLa- und in Cos-1-Zellen ( 12b-12d). Bei allen Fällen führt die TIF2.5-Expression zu
einer Dosis-abhängigen
Hemmung der NR-AF-2-Aktivität,
was anzeigt, dass die endogen vorhandenen Mediatoren von der isolierten überexprimierten
TIF2-NID verdrängt
wurden, und was stark vorschlägt,
dass TIF2 oder transkriptionale intermediäre Faktoren, die die gleiche
oder überlappende
Oberflächen
erkennen, die NR-AF-2-Aktivität
in diesen transfizierten Zellen vermitteln (12b-12d, vgl. Spur 2 mit Spuren 7 und 8; Spur
10 mit Spuren 15 und 16).
-
Es
ist wichtig zu betonen, dass unsere vorliegenden Daten zeigen, dass
TIF2 mit NRs durch eine Oberfläche
(NID) interagiert, die entscheidend für die NR-AF-2-Aktivität ist, da
die Expression von TIF2.5, der die NID umfasst, die Ligandeninduzierte
Aktivität
von allen getesteten NR-AF-2s blockierte. Diese Beobachtung, die
deutlich festlegt, dass, mindestens in transfizierten Zellen, TIF2
oder andere Coaktivatoren, die mit einer überlappenden, wenn nicht identischen,
holo-LBD-Oberfläche interagieren,
entscheidend sind, um die NR-AF-2-Aktivierungsfunktion zu vermitteln.
Dies ist im Einklang mit der Anwesenheit von drei NR-Box-Motiven
in der TIF2-NID und von mindestens einem konservierten LxxLL (SEQ
ID NO:12) NR-Box-Motiv
in allen bis heute beschriebenen Coaktivatoren.
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-