CN1521268A - 检测儿童失神癫痫主效基因cacna1h突变基因的方法及cacna1h突变基因 - Google Patents
检测儿童失神癫痫主效基因cacna1h突变基因的方法及cacna1h突变基因 Download PDFInfo
- Publication number
- CN1521268A CN1521268A CNA031020372A CN03102037A CN1521268A CN 1521268 A CN1521268 A CN 1521268A CN A031020372 A CNA031020372 A CN A031020372A CN 03102037 A CN03102037 A CN 03102037A CN 1521268 A CN1521268 A CN 1521268A
- Authority
- CN
- China
- Prior art keywords
- cacna1h
- gene
- mutational site
- mutator gene
- absence epilepsy
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Abstract
本发明涉及一种检测儿童失神癫痫主效基因之一CACNAlH突变基因的方法,所述方法为直接测序法或限制内切酶法。本发明同时涉及CACNAlH突变基因。本发明进一步涉及检测上述突变基因的试剂盒及应用。另外,本发明还涉及上述检测方法和突变基因的应用。本发明将CACNAlH基因与儿童失神癫痫的药物治疗联系起来,为此病的药物治疗提供了新的靶点,同时也为儿童失神癫痫和其他类型的特发性全身性癫痫以及与CACNAlH基因相关的其他系统疾病的新药研发奠定了基础。
Description
发明领域
本发明涉及一种检测儿童失神癫痫突变基因的方法及其突变基因。更具体地说,本发明涉及一种检测儿童失神癫痫主效基因之一CACNA1H突变基因的方法及CACNA1H突变基因。本发明进一步涉及检测上述突变基因的试剂盒,以及该试剂盒的应用。另外,本发明还涉及上述检测方法和突变基因在儿童失神癫痫的检测和/或治疗方法中的应用。
背景技术
儿童失神癫痫(childhood absence epilepsy,CAE)是特发性全身性癫痫的一种,约占小儿癫痫的5%-15%,女孩受累多于男孩,发病年龄3-12岁多见,发病高峰年龄为6-7岁。临床表现为突然发生的意识丧失,但不跌倒,两眼凝视前方,停止正在进行的动作,持续数秒至1-2分钟后意识恢复,继续原来的活动,发作后无嗜睡或精神恍惚,发作频繁,每天数次甚至百余次。发作时脑电图表现为双侧对称弥漫性、同步高波幅3Hz棘慢波,持续10秒左右。棘慢波开始时较快,为3.5-4Hz,中间为3Hz,结束时可以慢到2.5-2Hz。发作间期背景波正常,过度换气可诱发。失神发作频繁会影响学习,失神发作如未能及时控制或停药过早,40%可合并全身强直-阵挛发作,严重影响患者的学习和生活,给家庭和社会带来严重的经济负担。儿童失神癫痫(CAE)是特发性全身性癫痫的常见类型,有显著的遗传倾向,目前认为该病是一种复杂遗传病,发病机制十分复杂,其致病基因未明。
T-型钙通道的核苷酸序列同其它类型的钙通道不同,但其结构同其它类型的钙通道一样,也是由四个重复的结构域(I-IV)组成,每个域由6个跨膜区(S1-6)组成,表现为短暂、易于失活、易于被低电压激活的功能特性,在丘脑皮层节律性振荡的产生起了一个关键的作用。
至今为止,已有三种编码T-型钙通道的基因家族已被克隆,它们是CACNA1G,CACNA1H,CACNA1I。CACNA1H定位在染色体16p13.3,编码alpha1h亚单位,由35个外显子组成,CACNA1H基因在心脏,脑,肾脏广泛表达。尽管CACNA1H基因(genbank登记号AF051946)作为编码T-型钙通道的基因家族成员之一已经克隆,但是其功能和疾病的联系尚未见报道,至今还没有利用CACNA1H基因来研究儿童失神癫痫的报道。
发明内容
发明人从众多候选基因中选取T-型钙通道基因CACNA1H作为研究对象,通过大量的实验,大样本的统计分析,在118名中国北方汉族CAE患儿中对CACNA1H基因的35个外显子进行了直接测序,在14名CAE患儿中找到了12个不同的错义突变位点,进一步得到了突变的CACNA1H基因,其中两个突变位点均在两个不同的CAE患儿中出现,而230名正常对照均未发现上述突变,说明这些突变不是良性多态。其中,两个突变发生在跨膜区,六个突变位点高度保守。从而本发明找到了儿童失神癫痫的主效基因之一。
本发明提供了一种检测儿童失神癫痫的主效基因之一CACNA1H突变基因的方法,该方法为直接测序法或限制酶内切法。
本发明还提供了儿童失神癫痫的主效基因之一CACNA1H突变基因。
本发明进一步提供了一种检测儿童失神癫痫的主效基因之一CACNA1H突变基因的试剂盒以及上述试剂盒在儿童失神癫痫检测和/或治疗方法中的应用。
本发明还提供了上述检测方法和突变基因在儿童失神癫痫检测和/或治疗方法中的应用。
根据本发明的一个方面,本发明提供了一种检测儿童失神癫痫的主效基因之一CACNA1H基因突变的方法,该方法为直接测序法或限制酶内切法。
优选直接测序法,具体的说,包括如下步骤:
A:对CACNA1H基因的35个外显子设计PCR引物,进行PCR扩增;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank中的序列比较,确定CACNA1H基因的突变位点。
如实施例3所述,可以于基因水平直接确定基因的突变,还可进一步按正常读码框架进行翻译后于蛋白质水平确定,包括如下步骤:
C:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
另一方面,本发明提供了另一种检测儿童失神癫痫的主效基因之一CACNA1H的突变位点的方法,包括如下步骤:
A:提取DNA,在突变位点附近设计PCR引物,进行PCR反应;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank中的序列比较确定突变位点。
如实施例3所述,可以于基因水平直接测定基因的突变,还可进一步按正常读码框架进行翻译后于蛋白质水平测定,包括如下步骤:
C:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
优选突变位点定位于结构域I跨膜区2和3(IS2-IS3)、结构域II跨膜区2(IIS2)、结构域I和II的连接部(linker I-II)、结构域I跨膜区S5同核心区连接处(IS5-SS1)或结构域III跨膜区S5同核心区连接处(IIIS5-SS1)。更优选其核苷酸突变位点至少位于C562A(氨基酸突变F161L)、G923A(氨基酸突变E282K)、T1445A(氨基酸突变C456S)、G1574A(氨基酸突变G499S)、C2022T(氨基酸突变P648L)、G2310A(氨基酸突变R744Q)、C2322T(氨基酸突变A748V)、G2397A(氨基酸突变G773D)、G2429A(氨基酸突变G784S)、G2570A(氨基酸突变V831M)、G2621A(氨基酸突变G848S)、G4466A(氨基酸突变D1463N)。最优选突变位点位于结构域I跨膜区2和3(IS2-IS3)的突变C562A(氨基酸突变F161L)、结构域I跨膜区S5同核心区连接处(IS5-SS1)的突变G923A(氨基酸突变E282K)、结构域II跨膜区2(IIS2)的突变G2570A(氨基酸突变V831M)和G2621A(氨基酸突变G848S)、结构域I和II的连接部(linker I-II)的突变T1445A(氨基酸突变C456S)以及结构域III跨膜区S5同核心区连接处(IIIS5-SS1)的突变G4466A(氨基酸突变D1463N)。
根据本发明的另一个方面,通过本发明的直接测序方法,在CAE患儿中找到了12个不同的错义突变位点(如表3所示),并进一步得到了突变的CACNA1H基因,其中突变位点R744Q和G773D均在两个不同的CAE患儿中出现,而230名正常对照均未发现上述突变,说明这些突变不是良性多态。两个突变发生在跨膜区,六个突变位点高度保守。从而本发明找到了儿童失神癫痫的主效基因之一CACNA1H突变基因,其含有T-型钙通道基因CACNA1H序列,并且至少一个突变位点定位于结构域I跨膜区2和3(IS2-IS3)、结构域I跨膜区S5同核心区连接处(IS5-SS1)、结构域II跨膜区2(IIS2)、结构域I和II的连接部(linker I-II)、结构域III跨膜区S5同核心区连接处(IIIS5-SS1)。优选其至少一个突变位点位于CACNA1H序列的C562A(氨基酸突变F161L)、G923A(氨基酸突变E282K)、T1445A(氨基酸突变C456S)、G1574A(氨基酸突变G499S)、C2022T(氨基酸突变P648L)、G2310A(氨基酸突变R744Q)、C2322T(氨基酸突变A748V)、G2397A(氨基酸突变G773D)、G2429A(氨基酸突变G784S)、G2570A(氨基酸突变V831M)、G2621A(氨基酸突变G848S)、G4466A(氨基酸突变D1463N)其中之一。更优选至少一个突变位点位于结构域I跨膜区2和3(IS2-IS3)的突变C562A(氨基酸突变F161L)、结构域I跨膜区S5同核心区连接处(IS5-SS1)的突变G923A(氨基酸突变E282K)、结构域II跨膜区2(IIS2)的突变G2570A(氨基酸突变V831M)和G2621A(氨基酸突变G848S)、结构域I和II的连接部(linker I-II)的突变T1445A(氨基酸突变C456S)以及结构域III跨膜区S5同核心区连接处(IIIS5-SS1)的突变G4466A(氨基酸突变D1463N)。
本发明还提供了一种检测儿童失神癫痫的主效基因之一CACNA1H突变基因的试剂盒,其内装有一个或多个容器,容器内装有用以检测CACNA1H突变基因的一种或多种组分。按照检测方法及检测位点的不同,试剂盒可含有不同组分。与之同时提供的可以是经政府药物管理机构审核的、有关药品或生物制品制造、使用及销售的信息。例如,采用PCR扩增后(参见实施例1),直接检测样品中CACNA1H突变位点的试剂盒,可含有如表1所示的扩增用引物,dNTP,用于PCR反应的DNA聚合酶及其缓冲液等的一种或多种。本领域技术人员已知,以上的组分仅是示意性的,例如,所述的引物可以依据已知的核苷酸序列设计,通常为15-30个碱基,GC含量为45%-50%左右,在适当的温度下与模板特异性结合,其可以利用专门的计算机程序设计,例如(OLIGO 4.06引物分析软件,Primer 3 software);所述的用于PCR反应的DNA聚合酶可以是TaqDNA聚合酶,例如,Hotstar Taq酶,Klenow片段,Tth DNA聚合酶,VENT DNA聚合酶等能够用于PCR扩增的酶。
并说明使用方法如下:
1)PCR扩增
用软件Primer 3对CACNA1H基因35个外显子设计PCR引物,共35对引物(表1)。反应条件为94℃变性30秒,63℃退火60秒,72℃延伸110秒,前15个循环退火温度每次递减0.5℃,后25个循环退火温度固定为56℃30秒,72℃延伸40秒。最后72℃延伸10分钟。
2)PCR产物的纯化
将含有PCR产物的MultiScreen-PCR板抽真空,加入去离子水,静置,随后将MultiScreen-PCR板置于混合器上震荡,纯化后的PCR产物重新溶解后至另一洁净96孔板中。
3)测序反应及验证
以PCR引物作为测序引物进行测序反应,在Perkin Elmer 9700热循环仪上进行测序反应。反应结束后,延伸产物上样于ABI PRISM 3700 DNA分析仪。将所得到的序列图谱进行分析,凡有杂合双峰处,说明该位点为杂合状态,需进一步验证,首先用另一侧PCR引物作为测序引物进行测序反应,如结果证实该位点为突变位点,再将该患儿父母的DNA进行该基因位点的测序反应,结果发现所有的突变均在患儿父母双亲之一出现,均为杂合突变。然后在230名正常对照进行该基因所有的突变位点的测序反应,结果没有发现任何突变位点。该试剂盒可简便快捷地检测儿童失神癫痫主效基因CACNA1H突变基因,从而应用于儿童失神癫痫检测和/或治疗方法中。
另外,也可直接针对某个或某些突变位点设计引物,例如可含有如表1所示的引物的一种或多种,dNTP,用于PCR反应的DNA聚合酶及其缓冲液等的一种或多种。进行PCR扩增、纯化和测序,从而制备包含扩增该突变位点的引物的试剂盒。
本发明的试剂盒还可以利用限制内切酶的方法制备,例如本发明的试剂盒可包括:
1)扩增突变位点的引物;
2)PCR扩增酶及相应缓冲液;
3)酶切不同突变位点相应的限制内切酶;
4)不同的突变位点酶切图谱。
本领域普通技术人员已知,对于不同的突变位点,上述引物和限制内切酶可以有利于检测为标准,有针对性设计;方法包括先PCR扩增来自病人的血DNA样本,然后酶切PCR产物,并同试剂盒酶切图谱比较等步骤。
本发明还提供了CACNA1H突变基因检测方法在儿童失神癫痫检测和/或治疗方法中的应用以及突变的CACNA1H基因在儿童失神癫痫检测和/或治疗方法中的应用。例如,由于本发明证实CACNA1H基因是失神癫痫的主效基因,尤其突变集中在linker I-II之间,从而将CACNA1H基因与儿童失神癫痫的药物治疗联系起来,为此病的药物治疗提供了新的靶点。今后可以研究相应的药物如寻找某些作用于这些位点的因子来治疗癫痫,同时为儿童失神癫痫的新药研发提供了理论根据。
最后,本发明也为其他类型的特发性癫痫的发病机制及易感基因的研究开辟了新的思路。例如,CACNA1H基因其他位点突变可能引起特发性癫痫其他类型的临床发作。实际上,在这个丘脑皮层环路上丰富表达的基因突变都有可能引起特发性癫痫的临床发作。
附图简述
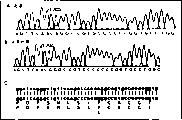
图1显示儿童失神癫痫患者CACNA1H基因与正常对照的C562A(氨基酸突变F161L)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:F161L突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图2显示儿童失神癫痫患者CACNA1H基因与正常对照的G923A(氨基酸突变E282K)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:E282K突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图3显示儿童失神癫痫患者CACNA1H基因与正常对照的T1445A(氨基酸突变C456S)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:C456S突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图4显示儿童失神癫痫患者CACNA1H基因与正常对照的G1574A(氨基酸突变G499S)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:G499S突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图5显示儿童失神癫痫患者CACNA1H基因与正常对照的C2022T(氨基酸突变P648L)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:P648L突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图6显示儿童失神癫痫患者CACNA1H基因与正常对照的G2310A(氨基酸突变R744Q)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:R744Q突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图7显示儿童失神癫痫患者CACNA1H基因与正常对照的C2322T(氨基酸突变A748V)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:A748V突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图8显示儿童失神癫痫患者CACNA1H基因与正常对照的G2397A(氨基酸突变G773D)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:G773D突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图9显示儿童失神癫痫患者CACNA1H基因与正常对照的G2429A(氨基酸突变G784S)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:G784S突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图10显示儿童失神癫痫患者CACNA1H基因与正常对照的G2570A(氨基酸突变V831M)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:V831M突变位点附近的部分核苷酸序列和相应氨基酸序列。
图11显示儿童失神癫痫患者CACNA1H基因与正常对照的G2621A(氨基酸突变G848S)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:G848S突变位点附近的部分核苷酸序列和相应氨基酸序列。
图12显示儿童失神癫痫患者CACNA1H基因与正常对照的G4466A(氨基酸突变D1463N)突变位点附近的部分测序图谱。其中,A:患者的突变位点附近的部分测序图谱,B:正常对照的部分测序图谱,C:D1463N突变位点附近的部分核苷酸序列和相应氨基酸序列。其中nt表示突变核苷酸在AF051946的位置。
图13显示CACNA1H基因结构域示意图,图中显示突变位点。
图14显示突变位点的保守性研究结果,图中a1A_homo_s、a1B_homo_s、a1C_homo_s、a1D_homo_s、a1E_homo_s、a1F_homo_s、a1G_homo_s、a1H_homo_s、a1I_homo_s、a1S_homo_s代表人类的a1A、a1B、a1C、a1D、a1E、a1F、a1G、a1H、a1I、a1S基因;a1H_Mus_mu、a1G_Mus_mu代表小鼠的a1H、a1G基因;a1G_Rattus、a1I_Rattus代表大鼠的a1G、a1I基因。
实施例
实施例1
1.CACNA1H基因各外显子的PCR扩增
1.对象:118例北方汉族CAE患儿,分别来自北京大学第一医院、北京儿童医院以及首都儿科研究所小儿神经专业门诊及病房。患儿年龄2.9-14岁,平均年龄8.5岁,平均发病年龄7.2岁。230例正常人作为对照,也来自北方汉族同一地区,年龄17-23岁,平均年龄19.5岁。CAE诊断依据1989年国际抗癫痫协会提出的癫痫及癫痫综合征分类诊断标准。CAE患儿入选病例组的临床标准包括:(1)3-12岁起病,以失神发作为首发类型,病程中可有少量全身强直-阵挛发作和/或肌阵挛发作;(2)发作期脑电图(EEG)为双侧对称同步3Hz节律性棘慢波爆发,也可为多棘慢波,一般开始部分可稍快于3Hz(3.5-4Hz),结束前可稍慢于3Hz(2.5Hz左右),中间主体部分为3Hz。背景活动正常。未经治疗的患者在过度换气时容易诱发出放电及临床发作;(3)神经系统检查正常;(4)神经影像学(CT或MRI)检查正常。
2.DNA提取:采用Miller改良盐析法提取外周血白细胞基因组DNA。
1)取柠檬酸钠或EDTANa2抗凝全血5-15ml(尽量不用肝素抗凝),置于50ml有盖离心管中。
2)加入3-5倍体积冷蒸馏水,反复颠倒混匀,冰中放置5分钟,4℃2000rpm离心20分钟。
3)缓慢倾倒上清,沉淀加入预冷0.1%Triton-X100(体积同上),轻柔混匀沉淀,如上离心,弃上清。
4)沉淀中加入4ml裂解液(50mM Tris-Cl-10mM EDTA,PH8.0),彻底打碎沉淀,然后加入10%SDS至终浓度为0.5%,混匀。
5)加入蛋白酶K(10mg/ml)至终浓度为200ug/ml,混匀,55℃3小时或37℃过夜消化(以过夜为佳)。
6)加入6M NaCl 1.2ml。剧烈震荡20秒。
7)2200rpm离心10分钟,将上清移至另一有盖离心管中。
8)加入2倍体积无水乙醇,反复颠倒混匀至出现絮状DNA沉淀,挑出DNA至一Eppendorf管中。
9)75%乙醇洗涤DNA 2遍。
10)以0.5ml TE(10mM Tirs-Cl-EDTA,pH8.0)或蒸馏水溶解DNA,电泳检测DNA片段大小,或测260nm/280nm OD比值。
3.PCR扩增:用软件Primer 3对CACNA1H基因35个外显子设计PCR引物,共32对引物(表1)。PCR总体积15μl,含有50ng基因组DNA,10mMTris-HCl(pH8.4),50mM KCl,3.0mM MgCl2,200μM of dNTPs(AmershamPharmcia公司产品),0.6U HotStartaqTM DNA Polymerase,引物各0.3μM在Perkin Elmer 9700热循环仪产品上(美国应用生物系统公司)进行PCR反应。反应条件为94℃变性30秒,63℃退火60秒,72℃延伸110秒,前15个循环退火温度每次递减0.5℃,后25个循环退火温度固定为56℃ 30秒,72℃延伸40秒。最后72℃延伸10分钟。
表1 PCR引物
| 外显子 | 正向引物 | 反向引物 |
| 外显子1 | 5-gttggggagcacgaaaag | 5-gtctcacctcgctctgct |
| 外显子2 | 5-gggcgcgtttgtctctaata | 5-cccgccactctcagaaatta |
| 外显子3 | 5-acctggtggctgctttca | 5-cgccttgaaccataaacctc |
| 外显子4 | 5-gctgagctgagctgttcca | 5-tctttacaggtgggacacagg |
| 外显子5 | 5-ttcctggccagtacaaggtc | 5-ggagtgcctggtaaccttca |
| 外显子6 | 5-cgtggacacccactgtga | 5-ggtggggcatatgtgcag |
| 外显子7 | 5-gactctgaccgtccctga | 5-acgacccctcctcctcct |
| 外显子8 | 5-acttcgacaacatcggctac | 5-cctggaccctgtctaggtg |
| 外显子9 | 5-cagctactgtatgccgtctg | 5-aggcatagctggtctgtttc |
| 外显子10 | 5-tcctgtgtgtgagggttcc | 5-ctaccatcaggtcaggcatc |
| 外显子11 | 5-agatcagtgccggtgagg | 5-ctctgcaggtgggatttctg |
| 外显子12 | 5-agctgttcatgcaccttgat | 5-cccaatcagtgcttctcaaa |
| 外显子13 | 5-tgagttgtagggcaggaagt | 5-cgttgtacaggaccacgtt |
| 外显子14 | 5-atccatagctgcctctgc | 5-caggtaggtgaggaatctgc |
| 外显子15 | 5-aggcagattcctcacctacc | 5-agggaacacatcttcagctct |
| 外显子16 | 5-ctaggttgggggattcct | 5-tcactcatcttcagggaagg |
| 外显子17 | 5-aatagtgatgccaccaggtc | 5-agagagacgaaggcgagtc |
| 外显子18 | 5-atggagaaggctgagaaggt | 5-ggaaatatccaccatgtgct |
| 外显子19 | 5-atccactctgccatccac | 5-gatgtaattggagacgctga |
| 外显子20 | 5-tcctcgtcttcatcttcctc | 5-caggttccagctgctctg |
| 外显子21 | 5-cggagatgatggtgaaggta | 5-gtcaggggactgtgcttc |
| 外显子22 | 5-cttgggacctttgctgag | 5-cttccctttgaagagctgac |
| 外显子23-24 | 5-atcttgggtgtgcaggtgt | 5-atccaggggttgtggttc |
| 外显子25 | 5-tgggtcacctcagggtct | 5-tcctcgtggagtgaggact |
| 外显子26 | 5-cgagtcctcactccacgag | 5-gagatgcaggcagactgtga |
| 外显子27 | 5-gcccccaacttctaccctac | 5-gggaggggagtttcaatca |
| 外显子28 | 5-ggagcacttcctgtatgctg | 5-cgttgcttctgcagacct |
| 外显子29-30 | 5-ttcaaggacaggtgtgtgtg | 5-agcagggacacagcttca |
| 外显子31-32 | 5-ggagcacctggaagaaggt | 5-tagctcaggcagtgcttgtc |
| 外显子33 | 5-agcggtttttcaggctct | 5-acacccagcctcctcaat |
| 外显子34 | 5-attgaggaggctgggtgt | 5-cagcaggcagaaaccttc |
| 外显子35 | 5-gtttggcctctccagtacc | 5-ctctcccttgagaagctgag |
实施例2
PCR产物的纯化
PCR产物1μl经1%琼脂糖电泳检测并粗略定量后采用96孔(millipore公司)纯化板进行纯化。纯化步骤如下:
(1)在第一次PCR(15μl)中加入80μl去离子水,振荡混匀后移入Multiscreen-PCR板孔中;
(2)将Multiscreen-PCR板置于真空抽滤支架上抽真空。压力:0.085Mpa,时间:5-10分钟。待每个孔都抽干后再多抽30秒;
(3)将Multiscreen-PCR板从真空支架上取下,每孔加入15-30μl去离子水,室温放置30分钟;
(4)将Multiscreen-PCR板置于混合器上振荡5分钟,使纯化后的产物重新溶解。用移液器转移至一新的96孔板中;
(5)纯化后产物取2μl电泳定量。
实施例3
测序反应及验证
1)测序反应:取以上纯化产物2μl为模板,用美国应用生物系统公司(PE公司)生产的Big-Dye末端标记试剂盒,以PCR反应一侧引物(稀释为2μM)为测序引物在PE公司生产的3700自动测序仪进行测序反应。反应体系10μl,各组分如表2所示:
表2 反应体系
| 名称 | 原液浓度 | 加样量(μl) | 体系终浓度 |
| 缓冲液 | 5× | 2 | 1× |
| 引物 | 2μM | 2 | 4pmol |
| Big-Dye mix | 1.2 | ||
| 模板 | 2 | 3-10ng |
ddH2O补齐至10μl,在Perkin Elmer 9700热循环仪(美国应用生物系统公司产品)上进行测序反应。
2)测序反应产物纯化及序列测定:测序反应产物经乙醇沉淀,ABI377或3700自动测序仪(美国应用生物系统公司产品)行核苷酸序列测定。
3)进一步按正常读码框架进行翻译后于蛋白质水平确定,包括如下步骤:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
结果分析
将所得到的序列图谱进行分析,凡有杂合双峰处,如图1-图12所示,说明该位点为杂合状态,需进一步验证,首先用另一侧PCR引物作为测序引物进行测序反应,如结果证实该位点为突变位点,再将该患儿父母的DNA进行该基因位点的测序反应,结果发现所有的突变均在患儿父母双亲之一出现,均为杂合突变。然后在230名正常对照进行该基因所有的突变位点的测序反应,结果没有发现任何突变位点。
本发明通过大量的实验,大样本的统计分析,在118名中国北方汉族CAE患儿中对该基因的外显子进行了直接测序,在14名CAE患儿中找到了12个不同的错义突变位点,其所在的外显子、核苷酸替换、氨基酸替换、结构定位如表3所示,结构域示意图如图13所示:
表3
| 患者号 | 外显子 | 核苷酸替换 | 氨基酸替换 | 结构定位 |
| 1234567891011121314 | 4799910101010101011123 | C562AG923AT1445AG1574AC2022TG2310AG2310AC2322TG2397AG2397AG2429AG2570AG2621AG4466A | F161LE282KC456SG499SP648LR744QR744QA748VG773DG773DG784SV831MG848SD1463N | IS2-IS3IS5-SS1连接部I-II连接部I-II连接部I-II连接部I-II连接部I-II连接部I-II连接部I-II连接部I-II连接部I-IIIIS2IIS2(IIIS5-SS1) |
注:突变核苷酸和相应的氨基酸改变位置根据genbank的数据,登记号是AF051946.1.
实施例4
突变位点的保守性研究
将人类3个T型钙通道基因(CACNA1G、CACNA1H和CACNA1I)编码氨基酸与小鼠和大鼠各2个T型钙通道基因编码氨基酸进行比较,通过研究发现,如图14所示,位于结构域I跨膜区2和3(IS2-IS3)的突变F161L,结构域I跨膜区S5同核心区连接处E282K(IS5-SS1)、结构域III跨膜区S5同核心区连接处D1463N(IIIS5-SS1),结构域II跨膜区2(IIS2)的突变V831M和G848S以及结构域I和II的连接部(linker I-II)的突变C456S都位于7个T型钙通道基因产物的高度保守的氨基酸位点。而且,结构域II跨膜区2(IIS2)的突变位点G848S在人类其他7个高电压激活(highvoltage-activated,HVA)的钙通道基因产物中也是高度保守的。
实施例5
检测儿童失神癫痫的主效基因之一CACNA1H突变基因的试剂盒及其应用
1.试剂盒含有:
扩增用引物:
| 外显子 | 正向引物 | 反向引物 |
| 外显子1 | 5-gttggggagcacgaaaag | 5-gtctcacctcgctctgct |
| 外显子2 | 5-gggcgcgtttgtctctaata | 5-cccgccactctcagaaatta |
| 外显子3 | 5-acctggtggctgctttca | 5-cgccttgaaccataaacctc |
| 外显子4 | 5-gctgagctgagctgttcca | 5-tctttacaggtgggacacagg |
| 外显子5 | 5-ttcctggccagtacaaggtc | 5-ggagtgcctggtaaccttca |
| 外显子6 | 5-cgtggacacccactgtga | 5-ggtggggcatatgtgcag |
| 外显子7 | 5-gactctgaccgtccctga | 5-acgacccctcctcctcct |
| 外显子8 | 5-acttcgacaacatcggctac | 5-cctggaccctgtctaggtg |
| 外显子9 | 5-cagctactgtatgccgtctg | 5-aggcatagctggtctgtttc |
| 外显子10 | 5-tcctgtgtgtgagggttcc | 5-ctaccatcaggtcaggcatc |
| 外显子11 | 5-agatcagtgccggtgagg | 5-ctctgcaggtgggatttctg |
| 外显子12 | 5-agctgttcatgcaccttgat | 5-cccaatcagtgcttctcaaa |
| 外显子13 | 5-tgagttgtagggcaggaagt | 5-cgttgtacaggaccacgtt |
| 外显子14 | 5-atccatagctgcctctgc | 5-caggtaggtgaggaatctgc |
| 外显子15 | 5-aggcagattcctcacctacc | 5-agggaacacatcttcagctct |
| 外显子16 | 5-ctaggttgggggattcct | 5-tcactcatcttcagggaagg |
| 外显子17 | 5-aatagtgatgccaccaggtc | 5-agagagacgaaggcgagtc |
| 外显子18 | 5-atggagaaggctgagaaggt | 5-ggaaatatccaccatgtgct |
| 外显子19 | 5-atccactctgccatccac | 5-gatgtaattggagacgctga |
| 外显子20 | 5-tcctcgtcttcatcttcctc | 5-caggttccagctgctctg |
| 外显子21 | 5-cggagatgatggtgaaggta | 5-gtcaggggactgtgcttc |
| 外显子22 | 5-cttgggacctttgctgag | 5-cttccctttgaagagctgac |
| 外显子23-24 | 5-atcttgggtgtgcaggtgt | 5-atccaggggttgtggttc |
| 外显子25 | 5-tgggtcacctcagggtct | 5-tcctcgtggagtgaggact |
| 外显子26 | 5-cgagtcctcactccacgag | 5-gagatgcaggcagactgtga |
| 外显子27 | 5-gcccccaacttctaccctac | 5-gggaggggagtttcaatca |
| 外显子28 | 5-ggagcacttcctgtatgctg | 5-cgttgcttctgcagacct |
| 外显子29-30 | 5-ttcaaggacaggtgtgtgtg | 5-agcagggacacagcttca |
| 外显子31-32 | 5-ggagcacctggaagaaggt | 5-tagctcaggcagtgcttgtc |
| 外显子33 | 5-agcggtttttcaggctct | 5-acacccagcctcctcaat |
| 外显子34 | 5-attgaggaggctgggtgt | 5-cagcaggcagaaaccttc |
| 外显子35 | 5-gtttggcctctccagtacc | 5-ctctcccttgagaagctgag |
Hotstar Tag酶5U/μl;
10×缓冲液(含15mM Mgcl2);
dNTP 2mM;
Big-Dye mix
2.使用方法:
主要包括如下步骤:
A:提取DNA,利用上述引物,进行PCR反应;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank(登记号AF051946.1)中的序列比较确定突变位点。
进一步包括C:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
具体方法参见实施例1、2和3。
实施例6
检测儿童失神癫痫的主效基因之一CACNA1H的突变位点F161L的试剂盒及其应用
1.试剂盒含有扩增外显子4的引物:
正向引物:5-gctgagctgagctgttcca
反向引物:5-tctttacaggtgggacacagg
Hotstar Tag酶 5U/μl
10×缓冲液(含15mM Mgcl2),
dNTP 2mM,
Big-Dye mix
2.使用方法:
主要包括如下步骤:
A:提取DNA,利用上述PCR引物,进行PCR反应;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank中的序列比较确定突变位点。
进一步包括C:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
实施例7
检测儿童失神癫痫的主效基因之一CACNA1H的突变位点E282K的试剂盒及其应用
1.试剂盒含有扩增突变位点
正向引物:5-GGGAAGTTCTACTACTGCGAGGGCCCCTATAGACACCAGG
反向引物:5-CTGTGCGCACCTGCTGGTCGACACCCACGGCATCCAGCCCG
Hotstar Tag酶 5U/μl
10×缓冲液(含15mM Mgcl2),
dNTP 2mM,
限制内切酶EcoRV
酶切图谱
2.使用方法
A:提取DNA,利用上述PCR引物,进行PCR反应;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank中的序列比较确定突变位点。
C:EcoRV酶切PCR产物;
D:同试剂盒的酶切图谱比较。
本领域普通技术人员已知,上述试剂盒的有些组分,例如引物,限制内切酶等可依据检测的突变位点不同,作相应的改变,先利用上述方法PCR扩增来自病人的血DNA样本,然后酶切PCR产物,并同试剂盒酶切图谱比较。
应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,但改动或修改的等价形式同样落在本申请权利书所限定的范围内。
Claims (16)
1、一种检测儿童失神癫痫主效基因之一CACNA1H突变基因的方法,其中该方法为直接测序法或限制内切酶法。
2、如权利要求1所述CACNA1H突变基因的检测方法,其中所述CACNA1H突变基因的至少一个突变位点定位于结构域I跨膜区2和3、结构域I跨膜区S5同核心区连接处、结构域II跨膜区2、结构域I和II的连接部或结构域III跨膜区S5同核心区连接处。
3、如权利要求2所述CACNA1H突变基因的检测方法,其中所述CACNA1H突变基因的至少一个突变位点位于C562A、G923A、T1445A、G1574A、C2022T、G2310A、C2322T、G2397A、G2429A、G2570A、G2621A、G4466A。
4、如权利要求3所述的CACNA1H突变基因的检测方法,其中所述CACNA1H突变基因的至少一个突变位点位于C562A、G923A、G2570A、G2621A、T1445A、G4466A。
5、如权利要求1-4任一权利要求所述的CACNA1H突变基因的检测方法,其特征在于包括如下步骤:
A:对CACNA1H基因的35个外显子设计PCR引物,进行PCR扩增;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank中的序列比较,确定CACNA1H基因的突变位点。
6、如权利要求5所述CACNA1H突变基因的检测方法,其特征在于进一步包括如下步骤:
C:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
7、如权利要求1-4任一权利要求所述的CACNA1H突变基因的检测方法,其特征在于,包括如下步骤:
A:提取DNA,在突变位点附近设计PCR引物,进行PCR反应;
B:PCR反应产物经纯化后直接测序,将所得到的序列与Genbank中的序列比较确定突变位点。
8、如权利要求7所述CACNA1H突变基因的检测方法,其特征在于进一步包括如下步骤:
C:按正常读码框架进行翻译以确定CACNA1H基因的突变位点。
9、一种儿童失神癫痫主效基因之一CACNA1H突变基因,其含有T-型钙通道基因CACNA1H序列,并且至少一个突变位点定位于结构域I跨膜区2和3、结构域I跨膜区S5同核心区连接处、结构域II跨膜区2、结构域I和II的连接部、结构域III跨膜区S5同核心区连接处。
10、如权利要求9所述CACNA1H突变基因,其中所述CACNA1H序列的至少一个突变位点位于C562A、G923A、T1445A、G1574A、C2022T、G2310A、C2322T、G2397A、G2429A、G2570A、G2621A、G4466A。
11、如权利要求10所述的CACNA1H突变基因,其中所述CACNA1H序列的至少一个突变位点位于C562A、G923A、G2570A、G2621A、T1445A、G4466A。
12、一种检测儿童失神癫痫主效基因之一CACNA1H突变基因的试剂盒,其包括:扩增用引物,dNTP,用于PCR反应的DNA聚合酶及其缓冲液的一种或多种。
13、一种检测儿童失神癫痫主效基因之一CACNA1H突变基因的试剂盒,其包括:
1)扩增突变位点的引物;
2)PCR扩增酶及相应缓冲液;
3)酶切不同突变位点相应的限制内切酶;
4)不同的突变位点酶切图谱。
14、如权利要求12或13所述的试剂盒在儿童失神癫痫检测和/或治疗方法中的应用。
15、权利要求1-8任一项所述的CACNA1H突变基因检测方法在儿童失神癫痫检测和/或治疗方法中的应用。
16、权利要求9-11任一项所述的突变基因在儿童失神癫痫检测和/或治疗方法中的应用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN 03102037 CN1279183C (zh) | 2003-01-27 | 2003-01-27 | 检测儿童失神癫痫主效基因cacna1h突变基因的方法及cacna1h突变基因 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN 03102037 CN1279183C (zh) | 2003-01-27 | 2003-01-27 | 检测儿童失神癫痫主效基因cacna1h突变基因的方法及cacna1h突变基因 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1521268A true CN1521268A (zh) | 2004-08-18 |
| CN1279183C CN1279183C (zh) | 2006-10-11 |
Family
ID=34281563
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN 03102037 Expired - Fee Related CN1279183C (zh) | 2003-01-27 | 2003-01-27 | 检测儿童失神癫痫主效基因cacna1h突变基因的方法及cacna1h突变基因 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN1279183C (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018058489A1 (zh) * | 2016-09-30 | 2018-04-05 | 武汉华大吉诺因生物科技有限公司 | Cacna1h衍生的肿瘤抗原多肽及其应用 |
-
2003
- 2003-01-27 CN CN 03102037 patent/CN1279183C/zh not_active Expired - Fee Related
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018058489A1 (zh) * | 2016-09-30 | 2018-04-05 | 武汉华大吉诺因生物科技有限公司 | Cacna1h衍生的肿瘤抗原多肽及其应用 |
| US11548925B2 (en) | 2016-09-30 | 2023-01-10 | Genoimmune Therapeutics Co., Ltd. | CACNA1H-derived tumor antigen polypeptide and use thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1279183C (zh) | 2006-10-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101729340B1 (ko) | 질환 위험 인자의 식별 방법 | |
| CA2362533A1 (en) | Gene sequence variations with utility in determining the treatment of disease | |
| US20040248092A1 (en) | Methods of screening for parkinsons's disease | |
| CN1873027A (zh) | 一种用于体外诊断非综合征性常染色体隐性遗传耳聋基因gjb2突变的引物及其应用 | |
| CN108715893B (zh) | 一组与放疗引起的放射性脑损伤相关的snp标志物及其应用 | |
| CN101029336A (zh) | 预测5-羟色胺再摄取抑制剂类药物作用效果的试剂盒 | |
| CN1279183C (zh) | 检测儿童失神癫痫主效基因cacna1h突变基因的方法及cacna1h突变基因 | |
| CN101037708A (zh) | 多态性位点基因型预测同型半胱氨酸水平的用途、方法和试剂盒 | |
| DK2247752T3 (en) | FORECAST AND DIAGNOSIS OF CANINE degeneration of myelopathy | |
| CN1257205A (zh) | 一种检测或预测老年痴呆病的方法和试剂盒 | |
| CN1763196A (zh) | 基因突变类型及基因测序方法 | |
| CN104372010A (zh) | 热性惊厥新的突变致病基因及其编码蛋白和应用 | |
| EP1206578A2 (en) | Bdnf polymorphism and association with bipolar disorder | |
| CN1730655A (zh) | 与人类遗传性耳聋相关的gjb6突变基因及其在诊断遗传性耳聋中的应用 | |
| JP2012205590A (ja) | 遺伝子発現を用いた疲労の判定方法 | |
| WO2011068610A1 (en) | Methods for detecting risk of myelodysplastic syndrome by genotypic analysis | |
| WO2012096680A1 (en) | Disease risk factors and methods of use | |
| US20220235418A1 (en) | Use of Biomarkers for Degenerative Disc Disease | |
| CN1786188A (zh) | 检测载脂蛋白e基因型的方法和试剂盒 | |
| CN100338230C (zh) | 一种检测pon2基因第九外显子多态性的方法及试剂 | |
| CN101029337A (zh) | 多态性位点基因型预测5-羟色胺再摄取抑制剂类药物作用效果的用途和方法 | |
| CN1710106A (zh) | 一种预测2型糖尿病易感性的方法及试剂 | |
| CN1766127A (zh) | 一种鉴定pgc-1基因启动子-1998位snp分子标记的引物、方法及试剂盒 | |
| CN104293813B (zh) | 皮肤剥脱综合征新的致病基因及其编码蛋白质和应用 | |
| CN101029338A (zh) | 通过醛糖还原酶基因型确定白内障的风险率 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20061011 Termination date: 20170127 |