CN116368226A - 用于加帽rna的组合物和方法 - Google Patents
用于加帽rna的组合物和方法 Download PDFInfo
- Publication number
- CN116368226A CN116368226A CN202180074617.6A CN202180074617A CN116368226A CN 116368226 A CN116368226 A CN 116368226A CN 202180074617 A CN202180074617 A CN 202180074617A CN 116368226 A CN116368226 A CN 116368226A
- Authority
- CN
- China
- Prior art keywords
- och
- motif
- mrna sequence
- terminal region
- independently
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
- C07H21/02—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids with ribosyl as saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/12—Transferases (2.) transferring phosphorus containing groups, e.g. kinases (2.7)
- C12N9/1241—Nucleotidyltransferases (2.7.7)
- C12N9/1247—DNA-directed RNA polymerase (2.7.7.6)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/26—Preparation of nitrogen-containing carbohydrates
- C12P19/28—N-glycosides
- C12P19/30—Nucleotides
- C12P19/34—Polynucleotides, e.g. nucleic acids, oligoribonucleotides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y207/00—Transferases transferring phosphorus-containing groups (2.7)
- C12Y207/07—Nucleotidyltransferases (2.7.7)
- C12Y207/07006—DNA-directed RNA polymerase (2.7.7.6)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/20—Type of nucleic acid involving clustered regularly interspaced short palindromic repeats [CRISPRs]
Abstract
本文提供了用于制备5’端区域修饰的mRNA的组合物和方法。具体地,本公开涉及新的mRNA 5’端区域基序及其序列起始子,以及能够测量这些基序和序列起始子的功能方面的测定。本文还提供了治疗与冠状动脉疾病相关的病状的组合物和方法。
Description
交叉引用
本申请要求2020年9月4日提交的美国临时申请第63/074,993号的权益,该申请通过引用以其整体并入本文。
技术领域
本公开涉及RNA,并且具体为mRNA分子的5’端区域,包括例如新的mRNA 5’端区域基序(或mRNA帽)及其起始子。
背景技术
mRNA的5’端区域可以是真核mRNA分子的重要结构和/或功能特征,因为它能够为mRNA提供稳定性(例如,通过提供针对5’核酸外切酶的保护)并参与RNA剪接、mRNA转运和支持蛋白质翻译的其他活动。常规mRNA帽的结构元件通常包括在5’端连接到三磷酸(ppp)桥的反向7-甲基鸟苷(m7G),该磷酸桥又连接到mRNA转录物的第一核苷酸(N1)。本文所述的5’端区域mRNA基序及其序列起始子在若干方面不同于常规的mRNA帽,包括例如,它们包括化学修饰的反向7-甲基鸟苷(m7G)核苷结构和/或经修饰的三磷酸(ppp)键。常规的帽通常是制造mRNA分子中最昂贵的部件之一。因此,在保持或提高加帽效率和/或mRNA产量的同时,常规帽的替代方案对本领域来说是各自独立的重要方面。
发明内容
本文描述了新的mRNA 5’端区域基序及其起始子。
在一个方面,本文描述了一种体外转录的(IVT)mRNA序列起始子,其包含式(I)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在另一方面,本文所述的式(I)的化合物满足以下限制性条件(i)至(iii)中的一个或多个:(i)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(ii)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;和(iii)A、A1和A2中的至少一个为-S-。
在另一方面,IVT mRNA序列起始子满足X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或A、A1和A2中的至少一个为-S-。
在一个方面,本文描述了一种体外转录的(IVT)mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在一个方面,本文描述了一种体外转录的(IVT)mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在另一方面,Z3为氢、氟、-OH、-OCH3、-或-OCH2CH3。在另一方面,其中Z3为-OCH3。在另一方面,Z4和Zn独立地为-OH或-OCH3。在另一方面,Z3、Z4和Zn各自独立地为-OH或-OCH3。在另一方面,Y2、Y4和Yn独立地为=O或=S。在另一方面,X2和X3独立地为-O-或-S-。
在一个方面,本文描述了一种具有5’端区域基序(I’)的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在另一方面,式(I)满足以下限制性条件(i)至(iii)中的一个或多个:(i)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(ii)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;和(iii)A、A1和A2中的至少一个为-S-。在另一方面,X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或者A、A1和A2中的至少一个为-S-。
在一个方面,本文描述了一种具有5’端区域基序(II’)的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在一个方面,本文描述了一种具有5’端区域基序(II”)的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在一个方面,本文描述了一种具有5’端区域基序的mRNA序列,其中5’端区域基序是来自表1的化合物或其盐或溶剂化物。
在另一方面,本文描述了一种具有5’端区域基序的mRNA序列,其中5’端区域基序是来自表2的化合物或其盐或溶剂化物。
在另一方面,本文描述了一种具有5’端区域基序的mRNA序列,其中5’端区域基序是来自表3的化合物或其盐或溶剂化物。
在具有5’端区域基序的mRNA序列的另一方面,Z3为氢、氟、-OH、-OCH3、-或-OCH2CH3。
在具有5’端区域的mRNA序列的另一方面,Z3为-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Z4和Zn各自独立地为-OH或-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Z3、Z4和Zn各自独立地为-OH或-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Z1为氟、-OH或-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Z1为氟。
在具有5’端区域基序的mRNA序列的另一方面,Z1为-OH。
在具有5’端区域基序的mRNA序列的另一方面,Z1为-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Z2为氟、-OH或-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Z2为氟。
在具有5’端区域基序的mRNA序列的另一方面,Z2为-OH。
在具有5’端区域基序的mRNA序列的另一方面,Z2为-OCH3。
在具有5’端区域基序的mRNA序列的另一方面,Q1和Q4为-CH2O-。
在具有5’端区域基序的mRNA序列的另一方面,Q2和Q3各自为-O-。
在具有5’端区域基序的mRNA序列的另一方面,Y1和Y3各自为=O。
在具有5’端区域基序的mRNA序列的另一方面,Y2、Y4和Yn各自独立地为=O或=S。
在具有5’端区域基序的mRNA序列的另一方面,Y1、Y2、Y3、Y4和Yn中的一个或多个为=S。
在具有5’端区域基序的mRNA序列的另一方面,Y2为=S。
在具有5’端区域基序的mRNA序列的另一方面,Y4为=S。
在具有5’端区域基序的mRNA序列的另一方面,Y1、Y2、Y3、Y4和Yn各自为=O。
在具有5’端区域基序的mRNA序列的另一方面,X1、X4和Xn各自为-O-。
在具有5’端区域基序的mRNA序列的另一方面,X2和X3各自独立地为-O-或-S-。
在具有5’端区域基序的mRNA序列的另一方面,X3为-O-。
在具有5’端区域基序的mRNA序列的另一方面,X1、X2、X3、X4和Xn中的一个或多个为-S-。
在具有5’端区域基序的mRNA序列的另一方面,X2为-S-。
在具有5’端区域基序的mRNA序列的另一方面,X4为-S-。
在具有5’端区域基序的mRNA序列的另一方面,X1、X2、X3、X4和Xn各自为-O-。
在具有5’端区域基序的mRNA序列的另一方面,A、A1和A2各自为-O-。
在具有5’端区域基序的mRNA序列的另一方面,A、A1和A2中的一个或多个为-S-。
在具有5’端区域基序的mRNA序列的另一方面,A为-S-,并且A1和A2为-O-。
在具有5’端区域基序的mRNA序列的另一方面,A2为-S-,并且A和A1为-O-。
在具有5’端区域基序的mRNA序列的另一方面,A、A1和A2为-O-。
在具有5’端区域基序的mRNA序列的另一方面,p为0。
在具有5’端区域基序的mRNA序列的另一方面,p为1。
在具有5’端区域基序的mRNA序列的另一方面,p为2。
在具有5’端区域基序的mRNA序列的另一方面,其中B2、B3和Bn各自独立地为腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、胸腺嘧啶、次黄嘌呤或嘌呤。
在具有5’端区域基序的mRNA序列的另一方面,B2为腺嘌呤,并且B3为鸟嘌呤。
在具有5’端区域基序的mRNA序列的另一方面,B2为鸟嘌呤,并且B3为腺嘌呤。
在具有5’端区域基序的mRNA序列的另一方面,蛋白质表达增加。
在另一方面,本文描述了一种复合物,其包含具有5’端区域基序的mRNA序列和DNA模板,其中具有5’端区域基序的mRNA序列包括本文所述的化合物,其中DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸、在核苷酸位置+2处的第二核苷酸和在核苷酸位置+3处的第三核苷酸;并且其中具有5’端区域基序的mRNA序列至少在核苷酸位置+1、+2和+3处与DNA模板杂交。
在另一方面,本文描述了一种复合物,其包含具有5’端区域基序的mRNA序列和DNA模板,其中具有5’端区域基序的mRNA序列包括本文所述的化合物,其中DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸和在核苷酸位置+2处的第二核苷酸;并且其中具有5’端区域基序的mRNA序列至少在核苷酸位置+1和+2处与DNA模板杂交。
在另一方面,本文描述了一种RNA分子,其包含具有5’端区域基序的mRNA序列。在另一方面,RNA包括向导RNA或核酸酶mRNA。在另一方面,RNA包括mRNA。
在另一方面,本文描述了一种表达mRNA的方法,所述方法包括将本文所述的mRNA引入到细胞裂解物中以表达mRNA。在另一方面,所述方法还包括测量mRNA的表达水平。在另一方面,如本文方法中所述,mRNA的表达水平与不含具有5’端区域基序的mRNA序列的相应mRNA相比高至少2倍、3倍、4倍、6倍、8倍或20倍。在另一方面,本文所述的方法涉及HeLa细胞。
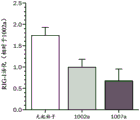
在另一方面,本文描述了一种检测由mRNA产生的细胞免疫刺激的方法,所述方法包括(a)使包含根据本文所述的化合物的加帽mRNA的制剂与细胞报告细胞系接触,和(b)测量所述细胞报告细胞系中的RIG-I活化。在另一方面,报告细胞系是HEK-Lucia RIG-I模型。在另一方面,与未加帽的mRNA相比,本文所述的细胞免疫刺激减少至少20%、50%、70%、100%和150%。
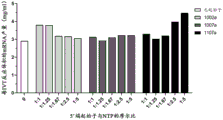
在另一方面,本文描述了一种使用IVT反应产生本文所述的具有5’端区域基序的mRNA序列的方法,所述方法包括(a)将DNA模板、聚合酶、包含硫代磷酸酯基团(PS)的mRNA序列基序和核苷三磷酸(NTP)以所述mRNA序列基序与所述NTP的特定摩尔比混合,以产生混合物,(b)在特定温度和持续时间下温育所述混合物,以及(c)从所述混合物中收获并纯化所述具有5’端区域基序的mRNA序列。在另一方面,摩尔比为1:5,并且所述方法能够以至少80%的加帽效率产生至少80%的产率。在另一方面,摩尔比为1:2.5,并且所述方法能够以至少85%的加帽效率产生至少80%的产率。在另一方面,摩尔比为1:1.67,并且所述方法能够以至少90%的加帽效率产生至少80%的产率。在另一方面,摩尔比为1:1.25,并且所述方法能够以至少90%的加帽效率产生至少80%的产率。在另一方面,摩尔比为1.0:1.0,并且所述方法能够以至少80%的加帽效率产生至少80%的产率。在另一方面,摩尔比为1:5,并且所述方法能够以至少80%的加帽效率产生每毫升(mL)IVT反应至少3mg mRNA的产量。在另一方面,摩尔比为1:2.5,并且所述方法能够以至少85%的加帽效率产生每毫升(mL)IVT反应至少3mg mRNA的产量。在另一方面,摩尔比为1:1.67,并且所述方法能够以至少90%的加帽效率产生每毫升(mL)IVT反应至少3mg mRNA的产量。在另一方面,摩尔比为1:1.25,并且所述方法能够以至少90%的加帽效率产生每毫升(mL)IVT反应至少3mg mRNA的产量。在另一方面,摩尔比为1.0:1.0,并且所述方法能够以至少80%的加帽效率产生每毫升(mL)IVT反应至少3mg mRNA的产量。在另一方面,NTP为GTP、ATP、CTP、UTP、经修饰的NTP或其组合。在另一方面,经修饰的NTP是N1-甲基假尿苷。
在另一方面,本文描述了一种细胞,其含有RNA分子,所述RNA分子包含本文所述的具有5’端区域基序的mRNA序列。
在另一方面,本文描述了一种细胞,其含有从RNA分子翻译的多肽,所述RNA分子包含本文所述的具有5’端区域基序的mRNA序列。
在另一方面,本文描述了一种药物组合物,其包含RNA分子和一种或多种药学上可接受的赋形剂,所述RNA分子包含本文所述的具有5’端区域基序的mRNA序列。在另一方面,药物包括脂质纳米颗粒。在另一方面,药物组合物被包封在脂质纳米颗粒中。在另一方面,药物组合物还包含一种或多种单一向导RNA,所述单一向导RNA被设计成靶向一种或多种感兴趣基因的一个或多个特定位置,以在施用于哺乳动物后引发药理学效应。
在另一方面,本文描述了一种用于合成RNA分子的方法,所述方法包括:将本文所述的具有5’端区域基序的mRNA序列引入到包含RNA聚合酶的混合物中,以及将混合物温育足以允许RNA分子转录的时间。在另一方面,混合物还包含DNA模板和核苷三磷酸。
在另一方面,本文描述了一种基因编辑的方法,所述方法包括将RNA分子或药物组合物引入到细胞中,其中RNA分子包括向导RNA或核酸酶mRNA,其中RNA分子在细胞中被翻译。
在另一方面,本文描述了一种用于在有需要的对象中降低冠状动脉疾病的风险的方法,所述方法包括向所述对象施用有效量的本文所述的药物组合物。
援引并入
本说明书中提及的所有出版物、专利和专利申请均通过引用的方式并入本文,如同每个单独的出版物、专利或专利申请都被明确且单独地指示通过引用并入。
附图说明
本发明的新颖特征在所附权利要求中具体阐述,并体现在本文所述的mRNA 5’端区域结构中。通过参考对其中利用了本发明的原理的5’端区域结构或化合物(在本文中有时被称为基序)的说明性实施方案进行阐述的详细描述和附图,将获得对本发明的特征和优点的更好理解,在附图中:
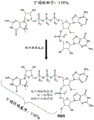
图1A示出了硫代磷酸酯修饰的5’端起始子和相应的体外转录的mRNA,其具有在说明书中被鉴定为1007a的5’端区域基序。
图1B示出了硫代磷酸酯修饰的5’端起始子和相应的体外转录的mRNA,其具有在说明书中被鉴定为1107a的5’端区域基序。
图2示出了使用不同5’端起始子制备的mRNA的生产产率的比较。
图3示出了使用不同5’端起始子制备的mRNA之间的mRNA全长纯度的比较。
图4示出了使用不同5’端起始子制备的mRNA之间的mRNA加帽效率的比较。
图5示出了包括不同5’端区域基序的mRNA在HeLa细胞裂解物中的蛋白质表达。
图6示出了包括不同5’端区域基序的mRNA在原代人类肝细胞中的蛋白质表达。
图7示出了在小鼠体内使用由包括不同5’端区域基序的mRNA编码的蛋白质进行ABE碱基编辑的比较。
图8示出了包括不同5’端区域基序的mRNA在HEK293细胞中的免疫刺激。
具体实施方式
阐述了本描述的某些具体细节,以便提供对各种实施方案的透彻理解。然而,本领域技术人员将理解,本公开可以在没有这些细节的情况下实践。在其他情况下,没有详细地示出或描述熟知的结构和/或方法,以避免不必要地模糊对实施方案的描述。除非上下文另有要求,否则在整个说明书和所附的权利要求书中,词语“包括(comprise)”及其变体,如“包括(comprises)”和“包括(comprising)”应被解释为开放的、包括的意义,即“包括,但不限于”。此外,本文提供的标题仅是为了方便,并且不解释所要求保护的公开的范围或含义。本文使用的章节标题仅用于组织目的,并且不应被解释为限制所描述的主题。
编码用于治疗性应用的生理学上重要的蛋白质的信使RNA(mRNA)已经显示出优于用于递送遗传材料的基于DNA的质粒和病毒载体的显著优点。此类重要的优点包括:(i)当与可能由病毒或质粒整合导致的潜在基因组损伤相比时,潜在地提高的安全性水平,(ii)在mRNA递送时更迅速的蛋白质表达(不同于在质粒的情况下通常发生的延迟响应),(iii)对蛋白质的表达的稳健的剂量依赖性控制,以及(iv)与质粒和病毒载体的制造相比,能够促进mRNA的大规模合成的简化。
信使RNA可以编码几乎任何已知的蛋白质,并且可以通过本领域技术人员已知的多种方法递送至特定的细胞、组织和器官。一旦递送,此类mRNA能够在靶向的细胞或组织内引导核糖体蛋白质表达,导致从单个mRNA分子产生编码的蛋白质的潜在数百个拷贝。
存在于活性mRNA分子中的若干种结构元件用于有效地翻译编码的蛋白质。这些元件中的一种是mRNA的5’端区域。在天然存在的mRNA中,5’端区域包括帽结构,这是真核mRNA分子(和一些病毒)的重要特征。已知此类帽结构参与蛋白质翻译、5’核酸外切酶保护、剪接和mRNA转运。天然存在的5’帽的一致结构元件是通过三磷酸(ppp)桥连接在mRNA的5’端的反向7-甲基鸟苷(m7G),并且该磷酸桥被连接到mRNA转录物的第一核苷酸(N1)。这种通常由m7G(ppp)N1代表的5’帽部分被称为帽-0。已知N1核糖环(即帽-1)上2’-羟基的甲基化能够提供自身RNA的标识符,其从而用于保护mRNA免受先天免疫系统的影响,这进而能够改善蛋白质表达。这种m7G(ppp)N1m帽-1结构是用于mRNA的体外转录(IVT)的已知常规帽部分。
此处,我们提出了新的mRNA 5’端区域基序和起始子。这些新的设计包括m7G部分的嘌呤碱基的修饰;三磷酸桥中的硫代磷酸酯(PS)取代和磷酸二酯键的化学修饰,用非常规碱基取代5’端区域核苷酸,延伸5’端区域核苷酸寡聚体,以及核糖环的化学修饰。具体地说,这些mRNA 5’端区域结构充当mRNA的末端5’端区域,并为mRNA提供稳定性。基序的化学结构能够促进和/或调节mRNA活性以及翻译起始和延伸的速率;通过建立屏障来保护mRNA,该屏障防止或干扰mRNA被5’核酸外切酶活性脱帽化;影响加帽效率并减少免疫刺激副产物的形成,这可以提高mRNA的安全性;并且通过在IVT反应期间调节对DNA模板的结合亲和力来促进mRNA的可制造性。
定义
除非另有定义,否则本文使用的所有技术和科学术语具有与本公开所属领域的普通技术人员通常理解的相同的含义。尽管在本公开的实践或测试中可以使用类似于或等同于本文所述的方法和材料的方法和材料,但是合适的方法和材料在下文中描述。本文引用的所有参考文献都通过引用以其整体并入,如同完全阐述一样。Singleton等人,Dictionary of Microbiology and Molecular Biology,第3版,约翰·威利父子出版公司(J.Wiley&Sons)(纽约,纽约州2001);March,Advanced Organic Chemistry Reactions,Mechanisms and Structure,第5版,约翰·威利父子出版公司(纽约,纽约州2001);以及Sambrook和Russel,Molecular Cloning:A Laboratory Manual,第3版,冷泉港实验室出版社(Cold Spring Harbor Laboratory Press)(冷泉港,纽约州2001),为本领域技术人员提供了本申请中使用的许多术语的一般指南。
如在本说明书和所附权利要求书中使用的,单数形式“一种(a)”、“一个(an)”和“所述(the)”包括复数指示物,除非上下文另外清楚地指出。还应该注意,术语“或”通常以其包括“和/或”的含义使用,除非上下文另外清楚地指出。
当表示取代基的数目时,术语“一个或多个”是指从一个取代基到最高可能数目的取代基的范围,例如一个氢的取代直到所有氢被取代基取代。
术语“任选的”或“任选地”表示随后描述的事件或情况可以但不必须发生,并且该描述包括其中事件或情况发生的情况和事件或情况不发生的情况。
如本文所用的术语“核酸”通常是指一个或多个核碱基、核苷或核苷酸,并且该术语包括多核碱基(polynucleobases)、多核苷和多核苷酸。核酸可以包括多核苷酸、单核苷酸和寡核苷酸。核酸可以包括DNA、RNA或其混合物,并且可以是单链、双链或部分单链或双链,并且可以形成二级结构。在一些实施方案中,核酸具有多个双链区段和单链区段。例如,核酸可以包括多核苷酸,例如mRNA,其中具有多个双链区段。
术语“mRNA序列起始子”、“IVT mRNA序列起始子”和“起始子”在本文中可互换使用,通常指单链的核糖寡核苷酸或脱氧核糖寡核苷酸或嵌合核糖/脱氧核糖寡核苷酸,其可以是天然存在的或合成的,并且通常包含约2至约10个核苷酸、约3至约8个核苷酸或约3至约5个核苷酸的序列。mRNA序列起始子可以含有一个或多个修饰基团。mRNA序列起始子可以是引物,例如寡核苷酸引物。mRNA序列起始子,例如寡核苷酸引物,可以包括RNA、DNA和/或其他经修饰的核苷。熟练的技术人员能够设计和制备适于DNA模板序列的转录的mRNA序列起始子。
mRNA序列起始子可以是加帽引物或加帽寡核苷酸类似物。例如,加帽mRNA序列起始子可以含有起始加帽寡核苷酸类似物或起始加帽寡核苷酸,其在5’端上具有帽0、帽1、帽2或TMG帽结构。在一些情况下,加帽起始子,例如加帽引物或加帽寡核苷酸类似物具有未修饰的或开放的3’-OH基团,并且它可以通过在3’端上并入NTP而被RNA聚合酶延伸。在一些情况下,如本文所述的起始子可以在转录系统中的启动子的控制下引发体外转录,所述转录系统包含必要的组分:DNA模板(例如DNA质粒)、RNA聚合酶、核苷5’-三磷酸和适当的缓冲液。起始子可以是携带末端3’-OH基团的寡核苷酸,该基团是RNA聚合酶的有效底物。在某些实施方案中,起始子是RNA聚合酶的底物,并且可以通过在3’端上并入NTP而被延长。在一些实施方案中,起始子在起始位点处与DNA模板互补。
术语“未取代的”或“未修饰的”在如本文所用的mRNA序列起始子和核苷三磷酸(NTP)的上下文中通常指起始加帽起始子和未被修饰的NTP。
如本文所用的术语“经修饰的起始加帽起始子”通常指起始加帽mRNA序列起始子,其在序列起始子内含有一个或多个额外的修饰基团或部分。
如本文所用的术语“修饰基团或部分”通常指可以附接到或取代至mRNA序列起始子的任何化学部分,例如一定位置处的起始引物,包括但不限于糖、核苷碱基、三磷酸桥和/或核苷酸间磷酸(例如,美国专利申请第20070281308号)。加帽起始子的修饰基团可以是与转录过程相容的任何性质的基团。
如本文所用的术语“核苷酸间键”通常指连接起始子(例如寡核苷酸引物或核酸)的两个核苷的一个或多个键,并且可以是天然磷酸二酯键或化学修饰的核酸主链键。
如本文所用的术语“多核苷酸”通常指包含两个或更多个连接的核酸亚基(例如核苷酸)的分子,并且可以与“寡核苷酸”互换使用。例如,多核苷酸可以包括一个或多个选自携带核碱基-腺嘌呤(A)、胞嘧啶(C)、鸟嘌呤(G)、胸腺嘧啶(T)和尿嘧啶(U)或其变体和组合的相应核苷的核苷酸。核苷酸通常包含核苷和至少1、2、3、4、5、6、7、8、9、10或更多个磷酸(PO3)基团。核苷酸可以包含核碱基、五碳糖(核糖或脱氧核糖)和一个或多个磷酸基团。核糖核苷酸包括其中糖是核糖的核苷酸。脱氧核糖核苷酸包括其中糖是脱氧核糖的核苷酸。核苷酸可以是核苷单磷酸、核苷二磷酸、核苷三磷酸或核苷多磷酸。例如,核苷酸可以是脱氧核糖核苷多磷酸,如脱氧核糖核苷三磷酸(dNTP),示例性的dNTP包括脱氧腺苷三磷酸(dATP)、脱氧胞苷三磷酸(dCTP)、脱氧鸟苷三磷酸(dGTP)、尿苷三磷酸(dUTP)和脱氧胸苷三磷酸(dTTP)。dNTP还可以包括可检测的标签,如发光标签或标志物(例如荧光团)。例如,核苷酸可以是嘌呤(例如,A或G,或其变体)或嘧啶(例如,C、T或U,或其变体)。在一些实例中,多核苷酸是脱氧核糖核酸(DNA)、核糖核酸(RNA)或其衍生物或变体。示例性的多核苷酸包括但不限于短干扰RNA(siRNA)、微小RNA(miRNA)、质粒DNA(pDNA)、短发夹RNA(shRNA)、小核RNA(snRNA)、信使RNA(mRNA)、前体mRNA(pre-mRNA)、反义RNA(asRNA)和异核RNA(hnRNA),并且涵盖核苷酸序列及其任何结构实施方案,如单链、双链、三链、螺旋、发夹、茎环、隆起等。在一些情况下,多核苷酸是圆形的。多核苷酸可以具有各种长度。例如,多核苷酸可以具有至少约7个碱基、8个碱基、9个碱基、10个碱基、20个碱基、30个碱基、40个碱基、50个碱基、100个碱基、200个碱基、300个碱基、400个碱基、500个碱基、1千碱基(kb)、2kb、3kb、4kb、5kb、10kb、50kb或更多的长度。多核苷酸可以从细胞或组织中分离。例如,多核苷酸序列可以包括分离的和纯化的DNA/RNA分子、合成的DNA/RNA分子和/或合成的DNA/RNA类似物。
多核苷酸可以包括一种或多种核苷酸变体,包括非标准核苷酸、非天然核苷酸、核苷酸类似物和/或经修饰的核苷酸,包括酰基和碳环核苷酸。经修饰的核苷酸的实例包括但不限于:二氨基嘌呤、5-氟尿嘧啶、5-溴尿嘧啶、5-氯尿嘧啶、5-碘尿嘧啶、次黄嘌呤、黄嘌呤、4-乙酰胞嘧啶、5-(羧基羟甲基)尿嘧啶、5-羧甲基氨基甲基-2-硫尿苷、5-羧甲基氨基甲基尿嘧啶、二氢尿嘧啶、β-D-半乳糖基辫苷(beta-D-galactosylqueosine)、肌苷、N6-异戊烯腺嘌呤、1-甲基鸟嘌呤、1-甲基肌苷、2,2-二甲基鸟嘌呤、2-甲基腺嘌呤、2-甲基鸟嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶、N6-腺嘌呤、7-甲基鸟嘌呤、5-甲基氨基甲基尿嘧啶、5-甲氧基氨基甲基-2-硫尿嘧啶、β-D-甘露糖基辫苷(beta-D-mannosylqueosine)、5’-甲氧基羧甲基尿嘧啶、5-甲氧基尿嘧啶、2-甲硫基-N6-异戊烯腺嘌呤、尿嘧啶-5-氧乙酸(v)、怀丁氧苷(wybutoxosine)、假尿嘧啶、辫苷、2-硫胞嘧啶、5-甲基-2-硫尿嘧啶、2-硫尿嘧啶、4-硫尿嘧啶、5-甲基尿嘧啶、尿嘧啶-5-氧乙酸甲酯、5-甲基-2-硫尿嘧啶、3-(3-氨基-3-N-2-羧丙基)尿嘧啶、(acp3)w、2,6-二氨基嘌呤等。在一些情况下,核苷酸可以包括其磷酸部分中的修饰,包括对三磷酸部分的修饰。此类修饰的非限制性实例包括更长长度的磷酸链(例如,具有4、5、6、7、8、9、10或更多个磷酸部分的磷酸链)和用硫醇部分的修饰(例如,α-硫代三磷酸和β-硫代三磷酸)。核酸分子也可以在碱基部分(例如,在通常可用于与互补性核苷酸形成氢键的一个或多个原子处和/或在通常不能与互补性核苷酸形成氢键的一个或多个原子处)、糖部分或磷酸主链处被修饰。核酸分子也可以含有胺修饰的基团,如氨基烯丙基1-dUTP(aa-dUTP)和氨基己基丙烯酰胺-dCTP(aha-dCTP),以允许胺反应性部分的共价附接,如N-羟基琥珀酰亚胺酯(NHS)。本公开的寡核苷酸中标准DNA碱基对或RNA碱基对的替代物可以提供更高的位/立方mm的密度、更高的安全性(抵抗天然毒素的意外或有意合成)、更容易区分光编程的聚合酶或更低的二级结构。在Betz K,Malyshev DA,Lavergne T,Welte W,Diederichs K,Dwyer TJ,Ordoukhanian P,Romesberg FE,Marx A.Nat.Chem.Biol.2012,8(7):612-4(其出于所有目的通过引用并入本文)中描述了与用于从头合成和/或扩增合成的天然和突变聚合酶相容的此类替代性碱基对。
如本文所用,术语“多肽”、“蛋白质”和“肽”可互换使用,并且是指经由肽键连接的氨基酸残基的聚合物,并且其可以由两条或更多条多肽链组成。术语“多肽”、“蛋白质”和“肽”是指通过酰胺键结合在一起的至少两种氨基酸单体的聚合物。氨基酸可以是L-光学异构体或D-光学异构体。更具体地,术语“多肽”、“蛋白质”和“肽”是指由两个或更多个氨基酸以特定顺序组成的分子;例如,如由编码蛋白质的基因或RNA中核苷酸的碱基序列确定的顺序。蛋白质是身体的细胞、组织和器官的结构、功能和调节所必需的,并且每种蛋白质都有其独特的功能。实例是激素、酶、抗体及其任何片段。在一些情况下,蛋白质可以是蛋白质的一部分,例如,蛋白质的结构域、子结构域或基序。在一些情况下,蛋白质可以是蛋白质的变体(或突变),其中一个或多个氨基酸残基被插入、缺失和/或取代到该蛋白质的天然存在的(或至少已知的)氨基酸序列中。蛋白质或其变体可以是天然存在的或重组的。
如本文所用,“杂交”是指在转录反应期间,在适当严格的条件下,根据Watson-Crick碱基配对规则,起始加帽mRNA序列起始子退火至DNA模板的过程。核酸杂交技术在本领域中是熟知的。参见,例如,Sambrook等人,1989,Molecular Cloning:A LaboratoryManual,第二版,冷泉港出版社(Cold Spring Harbor Press),普莱恩维尤,纽约州。本领域技术人员理解如何确定杂交/洗涤条件的适当严格性,使得具有至少期望水平的互补性的序列将稳定地杂交,而那些具有较低互补性的序列则不会稳定地杂交。关于杂交条件和参数的实例,参见例如Sambrook等人,1989,Molecular Cloning:A Laboratory Manual,第二版,冷泉港出版社,普莱恩维尤,纽约州;Ausubel,F.M.等人,1994,Current Protocols inMolecular Biology,约翰·威利父子出版公司,斯考克斯市,新泽西州,所有这些文献通过引用以其整体并入本文。在某些实施方案中,杂交可以发生在长度为20-100个核苷酸的核酸分子之间。在一些实施方案中,杂交可以发生在至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100个连续核苷酸之间。在一些实施方案中,杂交核酸分子可以含有高达1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20个被容许的错配。
如本文所用,在例如起始加帽寡核苷酸引物和DNA模板的复合物的上下文中,“互补(complement)”、“互补的(complementary)”或“互补性(complementarity)”是指标准Watson/Crick碱基配对规则。例如,序列“5’-A-G-T-C-3’”与序列“3’-T-C-A-G-5’”是互补的。在本文所述的核酸中可以包括某些非天然或合成的核苷酸;这些包括但不限于碱基和糖修饰的核苷、核苷酸和核酸,如肌苷、7-脱氮鸟苷、2’-O-甲基鸟苷、2’-氟-2’-脱氧胞苷、假尿苷、锁定核酸(LNA)和肽核酸(PNA)。互补性不需要是完美的;双链体可以含有错配的碱基对、变性的或不匹配的核苷酸。本领域技术人员可以考虑许多变量根据经验确定双链体稳定性,所述变量包括例如寡核苷酸的长度、寡核苷酸的碱基组成和序列、错配碱基对的发生率、离子强度、杂交缓冲液的组分和反应条件。
互补性可以是“完全的”或“全部的”,其中两条核酸链的所有核苷酸碱基根据公认的碱基配对规则是匹配的;互补性可以是“部分的”,其中只有加帽mRNA序列起始子和DNA靶标的一些核苷酸碱基根据公认的碱基配对规则是匹配的;或者互补性可以是“不存在的”,其中两条核酸链的任何核苷酸碱基根据公认的碱基配对规则都不匹配。加帽mRNA序列起始子(例如加帽引物)和DNA模板之间的互补性程度可能对起始加帽寡核苷酸和DNA模板之间的杂交强度以及相应的反应效率具有显著影响。术语互补性也可以用于指单独的核苷酸。例如,与加帽mRNA序列起始子的其余部分和DNA链之间的互补性相反或比较,寡核苷酸中的特定核苷酸可以注意到其与另一条链中的核苷酸的互补性或缺乏互补性。
如本文所用,术语“完全”、“全部”或“完美地”互补意指加帽mRNA序列起始子和DNA靶标的每个核苷酸碱基根据公认的碱基配对规则精确匹配。
如本文所用,术语“基本上互补”是指在严格杂交条件下杂交的两个序列。本领域技术人员将理解,基本上互补的序列不需要沿其整个长度杂交。具体地,基本上互补的序列可以包括不与靶序列杂交的连续碱基序列,并且可以位于在严格杂交条件下与靶序列杂交的连续碱基序列的3’或5’处。
如本文所用,术语“核苷”包括所有天然存在的核苷,包括在自然界中发现的所有形式的核苷碱基和呋喃糖苷。在天然存在的核苷中最常发现的碱基环是嘌呤环和嘧啶环。天然存在的嘌呤环包括,例如,腺嘌呤、鸟嘌呤和N6-甲基腺嘌呤。天然存在的嘧啶环包括,例如,胞嘧啶、胸腺嘧啶、5-甲基胞嘧啶、假尿嘧啶。例如,天然存在的核苷包括但不限于腺苷、鸟苷、胞苷、胸苷、尿苷、肌苷、7-甲基鸟苷或假尿苷的核糖、2’-O-甲基或2’-脱氧核糖衍生物。
如本文所用,术语“核苷类似物”、“经修饰的核苷”或“核苷衍生物”包括如本文所述的合成核苷。核苷衍生物还包括具有经修饰的碱基或/和糖部分的核苷,有或没有保护基团,并且包括例如2’-脱氧-2’-氟尿苷、5-氟尿苷等。本文提供的化合物和方法包括此类碱基环及其合成类似物,以及非天然杂环取代的碱基糖和无环取代的碱基糖。可以用于本公开的其他核苷衍生物包括,例如,LNA核苷、卤素取代的嘌呤(例如,6-氟嘌呤)、卤素取代的嘧啶、N6-乙基腺嘌呤、N4-(烷基)-胞嘧啶、5-乙基胞嘧啶等(美国专利第6,762,298号)。
如本文所用,术语“通用碱基”、“简并碱基”、“通用碱基类似物”和“简并碱基类似物”包括,例如,具有人工碱基的核苷类似物,其在某些实施方案中可被RNA聚合酶识别为天然NTP(例如,ATP、UTP、CTP和GTP)或其他特异性NTP中的一种的替代物。通用碱基或简并碱基公开于Loakes,D.,Nucleic Acids Res.,29:2437-2447(2001);Crey-Desbiolles,C.等人,Nucleic Acids Res.,33:1532-1543(2005);Kincaid,K.,等人,Nucleic Acids Res.,33:2620-2628(2005);Preparata,F P,Oliver,J S,J.Comput.Biol.753-765(2004);和Hill,F.等人,Proc Natl Acad.Sci.USA,95:4258-4263(1998))中。
如本文所用,术语“经修饰的NTP”是指具有结合在任何位置的化学部分基团的核苷5’-三磷酸,包括糖、碱基、三磷酸链或这三个位置的任何组合。此类NTP的实例可以在例如“Nucleoside Triphosphates and Their Analogs:Chemistry,Biotechnology andBiological Applications,”Vaghefi,M.编著,泰勒-弗朗西斯出版集团(Taylor andFrancis),博卡拉顿(2005)中找到。
如本文所用,术语“特异性”当用于指5’加帽mRNA序列起始子序列及其与DNA模板杂交的能力时,是一种当加帽mRNA序列起始子和DNA链比对时,与DNA模板的一部分具有至少50%序列同一性的序列。可能优选的较高水平的序列同一性包括至少75%、至少80%、至少85%、至少90%、至少95%、至少99%和最优选100%的序列同一性。
除了“未修饰的”或“天然的”核碱基如嘌呤核碱基腺嘌呤(A)和鸟嘌呤(G)以及嘧啶核碱基胸腺嘧啶(T)、胞嘧啶(C)和尿嘧啶(U),本领域技术人员已知的许多经修饰的核碱基或核碱基模拟物也适用于本文所述的化合物。未修饰的或天然的核碱基可以被修饰或取代以提供具有改进的性质的寡核苷酸。例如,核酸酶抗性寡核苷酸可以用这些碱基或用合成的和天然的核碱基(例如,肌苷、黄嘌呤、次黄嘌呤、nubularine、异鸟嘌呤核苷(isoguanisine)或杀结核菌素)和本文所述的任何一种寡聚体修饰来制备。可替代地,可以使用任何上述碱基和“通用碱基”的取代或修饰的类似物。当天然碱基被非天然碱基和/或通用碱基取代时,核苷酸被认为包括本文的经修饰的核碱基和/或核碱基修饰。经修饰的核碱基和/或核碱基修饰还包括天然碱基、非天然碱基和通用碱基,其包括缀合的部分,例如本文所述的配体。用于与核碱基缀合的优选的缀合物部分包含阳离子氨基,其可以经由合适的烷基、烯基或具有酰胺键的接头与核碱基缀合。
如本文所用,“未修饰的”或“天然的”核碱基包括嘌呤碱基腺嘌呤(A)和鸟嘌呤(G),以及嘧啶碱基胸腺嘧啶(T)、胞嘧啶(C)和尿嘧啶(U)。示例性的经修饰的核碱基包括但不限于其他合成的和天然核碱基,如肌苷、黄嘌呤、次黄嘌呤、nubularine、异鸟嘌呤核苷、杀结核菌素、2-(卤代)腺嘌呤、2-(烷基)腺嘌呤、2-(丙基)腺嘌呤、2-(氨基)腺嘌呤、2-(氨基烷基)腺嘌呤、2-(氨基丙基)腺嘌呤、2-(甲硫基)-N6-(异戊烯基)腺嘌呤、6-(烷基)腺嘌呤、6-(甲基)腺嘌呤、7-(脱氮)腺嘌呤、8-(烯基)腺嘌呤、8-(烷基)腺嘌呤、8-(炔基)腺嘌呤、8-(氨基)腺嘌呤、8-(卤代)腺嘌呤、8-(羟基)腺嘌呤、8-(硫代烷基)腺嘌呤、8-(硫醇)腺嘌呤、N6-(异戊基)腺嘌呤、N6-(甲基)腺嘌呤、N6,N6-(二甲基)腺嘌呤、2-(烷基)鸟嘌呤、2-(丙基)鸟嘌呤、6-(烷基)鸟嘌呤、6-(甲基)鸟嘌呤、7-(烷基)鸟嘌呤、7-(甲基)鸟嘌呤、7-(脱氮)鸟嘌呤、8-(烷基)鸟嘌呤、8-(烯基)鸟嘌呤、8-(炔基)鸟嘌呤、8-(氨基)鸟嘌呤、8-(卤代)鸟嘌呤、8-(羟基)鸟嘌呤、8-(硫代烷基)鸟嘌呤、8-(硫醇)鸟嘌呤、N-(甲基)鸟嘌呤、2-(硫代)胞嘧啶、3-(脱氮)-5-(氮杂)胞嘧啶、3-(烷基)胞嘧啶、3-(甲基)胞嘧啶、5-(烷基)胞嘧啶、5-(炔基)胞嘧啶、5-(卤代)胞嘧啶、5-(甲基)胞嘧啶、5-(丙炔基)胞嘧啶、5-(丙炔基)胞嘧啶、5-(三氟甲基)胞嘧啶、6-(偶氮)胞嘧啶、N4-(乙酰基)胞嘧啶、3-(3-氨基-3-羧丙基)尿嘧啶、2-(硫代)尿嘧啶、5-(甲基)-2-(硫代)尿嘧啶、5-(甲氨基甲基)-2-(硫代)尿嘧啶、4-(硫代)尿嘧啶、5-(甲基)-4-(硫代)尿嘧啶、5-(甲氨基甲基)-4-(硫代)尿嘧啶、5-(甲基)-2,4-(二硫代)尿嘧啶、5-(甲氨基甲基)-2,4-(二硫代)尿嘧啶、5-(2-氨基丙基)尿嘧啶、5-(烷基)尿嘧啶、5-(炔基)尿嘧啶、5-(烯丙基氨基)尿嘧啶、5-(氨基烯丙基)尿嘧啶、5-(氨基烷基)尿嘧啶、5-(胍基烷基)尿嘧啶、5-(l,3-二唑-l-烷基)尿嘧啶、5-(氰基烷基)尿嘧啶、5-(二烷基氨基烷基)尿嘧啶、5-(二甲氨基烷基)尿嘧啶、5-(卤代)尿嘧啶、5-(甲氧基)尿嘧啶、尿嘧啶-5-氧乙酸、5-(甲氧羰基甲基)-2-(硫代)尿嘧啶、5-(甲氧羰基-甲基)尿嘧啶、5-(丙炔基)尿嘧啶、5-(丙炔基)尿嘧啶、5-(三氟甲基)尿嘧啶、6-(偶氮)尿嘧啶、二氢尿嘧啶、N-(甲基)尿嘧啶、5-尿嘧啶(即,假尿嘧啶)、2-(硫代)假尿嘧啶、4-(硫代)假尿嘧啶、2,4-(二硫代)假尿嘧啶、5-(烷基)假尿嘧啶、5-(甲基)假尿嘧啶、5-(烷基)-2-(硫代)假尿嘧啶、5-(甲基)-2-(硫代)假尿嘧啶、5-(烷基)-4-(硫代)假尿嘧啶、5-(甲基)-4-(硫代)假尿嘧啶、5-(烷基)-2,4-(二硫代)假尿嘧啶、5-(甲基)-2,4-(二硫代)假尿嘧啶、1-甲基假尿嘧啶(N1-甲基假尿嘧啶)、1-取代的假尿嘧啶、1-取代的2(硫代)-假尿嘧啶、1-取代的4-(硫代)假尿嘧啶、1-取代的2,4-(二硫代)假尿嘧啶、1-(氨基羰基亚乙基)-假尿嘧啶、1-(氨基羰基亚乙基)-2(硫代)-假尿嘧啶、1-(氨基羰基亚乙基)-4-(硫代)假尿嘧啶、l-(氨基羰基亚乙基)-2,4-(二硫代)假尿嘧啶、1-(氨基烷基氨基羰基亚乙基)-假尿嘧啶、1-(氨基烷基氨基-羰基亚乙基)-2(硫代)-假尿嘧啶、l-(氨基烷基氨基羰基亚乙基)-4-(硫代)假尿嘧啶、l-(氨基烷基氨基羰基亚乙基)-2,4-(二硫代)假尿嘧啶、l,3-(二氮杂)-2-(氧代)-吩噁嗪-1-基、l-(氮杂)-2-(硫代)-3-(氮杂)-吩噁嗪-l-基、l,3-(二氮杂)-2-(氧代)-吩噻嗪-l-基、l-(氮杂)-2-(硫代)-3-(氮杂)-吩噻嗪-l-基、7-取代的l,3-(二氮杂)-2-(氧代)-吩噁嗪-l-基、7-取代的-1-(氮杂)-2-(硫代)-3-(氮杂)-吩噁嗪-l-基、7-取代的l,3-(二氮杂)-2-(氧代)-吩噻嗪-l-基、7-取代的l-(氮杂)-2-(硫代)-3-(氮杂)-吩噻嗪-l-基、7-(氨基烷基羟基)-l,3-(二氮杂)-2-(氧代)-吩噁嗪-1-基、7-(氨基烷基羟基)-1-(氮杂)-2-(硫代)-3-(氮杂)-吩噁嗪-1-基、7-(氨基烷基羟基)-1,3-(二氮杂)-2-(氧代)-吩噻嗪-1-基、7-(氨基烷基羟基)-1-(氮杂)-2-(硫代)-3-(氮杂)-吩噻嗪-1-基、7-(胍烷基羟基)-1,3-(二氮杂)-2-(氧代)-吩噁嗪-1-基、7-(胍烷基羟基)-l-(氮杂)-2-(硫代)-3-(氮杂)-吩噁嗪-l-基、7-(胍烷基-羟基)-1,3-(二氮杂)-2-(氧代)-吩噻嗪-1-基、7-(胍烷基羟基)-1-(氮杂)-2-(硫代)-3-(氮杂)-吩噻嗪-l-基、l,3,5-(三氮杂)-2,6-(二氧杂环己烷)-萘、肌苷、黄嘌呤、次黄嘌呤、nubularine、杀结核菌素、异鸟嘌呤核苷、肌苷基(inosinyl)、2-氮杂-肌苷基、7-脱氮-肌苷基、硝基咪唑基、硝基吡唑基、硝基苯并咪唑基、硝基吲唑基、氨基吲哚基、吡咯并嘧啶基、3-(甲基)异喹诺酮基、5-(甲基)异喹诺酮基、3-(甲基)-7-(丙炔基)异喹诺酮基、7-(氮杂)吲哚基、6-(甲基)-7-(氮杂)吲哚基、咪唑并吡啶基、9-(甲基)-咪唑并吡啶基、吡咯并吡嗪基、异喹诺酮基、7-(丙炔基)异喹诺酮基、丙炔基-7-(氮杂)吲哚基、2,4,5-(三甲基)苯基、4-(甲基)吲哚基、4,6-(二甲基)吲哚基、苯基、萘基、蒽基、菲基、芘基、均二苯乙烯基、并四苯基、并五苯基、二氟甲苯基、4-(氟代)-6-(甲基)苯并咪唑、4-(甲基)苯并咪唑、6-(偶氮)胸腺嘧啶、2-吡啶酮、5-硝基吲哚、3-硝基吡咯、6-(氮杂)嘧啶、2-(氨基)嘌呤、2,6-(二氨基)嘌呤、5-取代的嘧啶、N2-取代的嘌呤、N6-取代的嘌呤、06-取代的嘌呤、取代的1,2,4-三唑、吡咯并嘧啶-2-酮-3-基、6-苯基-吡咯并嘧啶-2-酮-3-基、对位取代的-6-苯基-吡咯并嘧啶-2-酮-3-基、邻位取代的-6-苯基-吡咯并嘧啶-2-酮-3-基、双邻位取代的6-苯基-吡咯并嘧啶-2-酮-3-基、对-(氨基烷基羟基)-6-苯基-吡咯并嘧啶-2-酮-3-基、邻-(氨基烷基羟基)-6-苯基-吡咯并嘧啶-2-酮-3-基、双邻-(氨基烷基羟基)-6-苯基-吡咯并嘧啶-2-酮-3-基、吡啶并嘧啶-3-基、2-氧代-7-氨基-吡啶并嘧啶-3-基、2-氧代-吡啶并嘧啶-3-基,或者其任何O-烷基化或其N-烷基化衍生物。可替代地,可以使用上述碱基和“通用碱基”中的任何一种的取代的或修饰的类似物。通用核碱基是可以与所有四种天然存在的核碱基进行碱基配对而基本上不影响解链行为、通过胞内酶的识别或寡核苷酸双链体的活性的任何核碱基。一些示例性的通用核碱基包括但不限于2,4-二氟甲苯、硝基吡咯基、硝基吲哚基、8-氮杂-7-脱氮腺嘌呤、4-氟代-6-甲基苯并咪唑、4-甲基苯并咪唑、3-甲基异喹诺酮基、5-甲基异喹诺酮基、3-甲基-7-丙炔基异喹诺酮基、7-氮杂吲哚基、6-甲基-7-氮杂吲哚基、咪唑并吡啶基、9-甲基-咪唑并吡啶基、吡咯并吡嗪基、异喹诺酮基、7-丙炔基异喹诺酮基、丙炔基-7-氮杂吲哚基、2,4,5-三甲基苯基、4-甲基吲哚基、4,6-二甲基吲哚基、苯基、萘基、蒽基、菲基、芘基、均二苯乙烯基、并四苯基、并五苯基及其结构衍生物(参见例如,Loakes,2001,Nucleic Acids Research,29,2437-2447,其通过引用以其整体并入本文)。另外的核碱基包括在美国专利第3,687,808号中公开的那些;2009年3月26日提交的国际申请第PCT US09/038425号中公开的那些;Concise Encyclopedia Of PolymerScience And Engineering,第858-859页,Kroschwitz,J.I,编著,约翰·威利父子出版公司,1990中公开的那些;English等人,Angewandte Chemie,国际版,1991,30,613中公开的那些;Modified Nucleosides in Biochemistry,Biotechnology and Medicine,Herdewijin,P.编著,Wiley-VCH,2008中公开的那些;以及由Sanghvi,Y.S.,第15章,dsRNAResearch and Applications,第289-302页,Crooke,S.T.和Lebleu,B.,编著.,CRC出版社(CRC Press),1993公开的那些。上述文献中的所有内容均通过引用并入本文。
如本文所用,术语“生物样品”意指可以从中制备或可以从中提取并检查多核苷酸、多肽、生物标志物和/或代谢物的任何生物材料。非限制性实例涵盖全血、血浆、唾液、颊拭子、粪便样本、尿液样本、细胞群(cell mass)或任何其他体液或组织。
如本文所用的术语“施用(administer)”、“施用(administering)”、“施用(administration)”等是指可以用于将化合物或组合物递送至期望的生物作用位点的方法。这些方法包括但不限于口服途径(p.o.)、十二指肠内途径(i.d.)、肠胃外注射(包括静脉内(i.v.)、皮下(s.c.)、腹膜内(i.p.)、肌内(i.m.)、血管内或输注(inf.))、局部(top.)和直肠(p.r.)施用。本领域技术人员熟知可以用于本文所述的化合物和方法的施用技术。在一些实施方案中,本文所述的化合物和组合物被口服施用。
如本文所用,术语“共同施用”等意指涵盖向单一患者施用选定的治疗性药剂,并且旨在包括其中通过相同或不同施用途径或在相同或不同时间施用药剂的治疗方案。
如本文所用的术语“有效量”或“治疗有效量”是指被施用的药剂或化合物的足够量,其将在一定程度上缓解所治疗的疾病或病状的一种或多种症状;例如疾病的一种或多种体征、症状或病因的减少和/或减轻,或者生物系统的任何其他期望的改变。例如,用于治疗用途的“有效量”可以是提供一种或多种疾病症状的临床显著减少的药剂的量。适当的“有效”量可以在个体情况下使用如剂量递增研究的技术来确定。
如本文所用的术语“增强(enhance)”或“增强(enhancing)”意指增加或延长期望效果的量、效力或持续时间。
如本文所用,“碳水化合物”是指这样的化合物,其本身是由一个或多个具有至少6个碳原子的单糖单元组成的碳水化合物(其可以是直链、支链或环状的),其中氧、氮或硫原子与每个碳原子键合;或是具有作为其一部分的碳水化合物部分的化合物,该碳水化合物部分由一个或多个单糖单元组成,每个单糖单元具有至少六个碳原子(其可以是直链、支链或环状的),其中氧、氮或硫原子与每个碳原子键合。代表性的碳水化合物包括糖(含有约4-9个单糖单元的单糖、二糖、三糖和寡糖)和多糖,如淀粉、糖原、纤维素和多糖胶。具体的单糖包括C5及以上(优选地C5-C8)糖;二糖和三糖包括具有两个或三个单糖单元(优选地C5-C8)的糖。
术语“单糖”包括阿洛糖、阿卓糖、阿拉伯糖、克拉定糖、赤藓糖、赤藓酮糖、果糖、D-岩藻糖醇、L-岩藻糖醇、岩藻糖胺、岩藻糖、墨角藻糖、半乳糖胺、D-半乳糖醇、N-乙酰基-半乳糖胺、半乳糖、葡糖胺、N-乙酰基-葡糖胺、葡糖胺醇、葡萄糖、葡萄糖-6-磷酸古洛糖甘油醛、L-甘油-D-甘露庚糖(L-glycero-D-mannos-heprose)、甘油、甘油酮、古洛糖艾杜糖、来苏糖、甘露糖胺、甘露糖、甘露糖-6-磷酸、阿洛酮糖、奎诺糖、奎诺糖胺、鼠李糖醇、鼠李糖胺、鼠李糖、核糖、核酮糖、景天庚酮糖、山梨糖、塔格糖、塔罗糖、酒石酸、throse、木糖和木酮糖的基团。单糖可以是D-或L-构型。单糖还可以是脱氧糖(醇羟基被氢置换)、氨基糖(醇羟基被氨基置换)、硫糖(醇羟基被硫醇置换,或C=O被C=S置换,或环状形式的环氧被硫置换)、硒基糖、碲基糖、氮杂糖(环碳被氮置换)、亚氨基糖(环氧被氮置换)、phosphano糖(环氧被磷置换)、磷杂糖(phospha sugar)(环碳被磷置换)、C取代的单糖(非末端碳原子上的氢被碳置换)、不饱和单糖、糖醇(羰基被CHOH基团置换)、醛糖酸(醛基被羧基置换)、酮醛糖酸、糖醛酸、醛糖二酸等。氨基糖包括氨基单糖,优选半乳糖胺、谷氨酰胺(glusamine)、甘露糖胺、岩藻糖胺、quinavosamine、神经氨酸、胞壁酸、乳糖二胺(lactosediamine)、acosamine、bacillosamine、六碳氨糖(daunosamine)、红霉脱氧糖胺、福洛氨糖(forosamine)、加拉糖胺、kanosamine、kanosamine、碳霉糖、myosamine、persosamine、pneumosamine、绛红糖胺环(purpurosamine)、rhodosmine。应理解,单糖等还可以被取代。
术语“二糖”、“三糖”和“多糖”包括阿比可糖、阿卡波糖、amicetose、支链淀粉、直链淀粉、芹菜糖、阿卡诺糖(arcanose)、蛔糖、抗坏血酸、波依文糖(boivinose)、纤维二糖、纤维三糖、纤维素、马铃薯三糖、查耳糖、壳多糖、可立糖、环糊精、磁麻糖、糊精、2-脱氧核糖、2-脱氧葡萄糖、狄吉糖、毛地黄糖、毛地黄毒糖、evalose、依维米特糖(evemitrose)、低聚果糖、galto-低聚糖、龙胆三糖、龙胆二糖(genitiobiose)、葡聚糖、gluicogen、glylcogen、金缕梅糖、肝素、菊粉、异左旋葡萄糖酮(isolevoglucosenone)、异麦芽糖、异麦芽三糖、异葡糖基麦芽糖、曲二糖、乳糖、氨基乳糖苷、乳糖二胺、昆布二糖、左旋葡聚糖、左旋葡萄糖酮、β-麦芽糖、麦芽三糖、甘露聚糖-寡糖、甘露三糖(amnninotriose)、松三糖、蜜二糖、胞壁酸、碳霉糖、阿洛糖、神经氨酸、migerose、nojirimycon、诺维糖、齐墩果糖、潘糖、泊雷糖、车前糖、樱草糖、棉子糖、rhodone、芸香糖、齐墩果糖、潘糖、泊雷糖、车前糖、樱草糖、棉子糖、玫红糖(rhodinose)、芸香糖、长匐茎糖、景天庚酮糖、景天庚酮糖酐、茄三糖、槐糖、水苏糖、链霉糖、蔗糖、α,α-海藻糖、海藻糖胺(trahalosamine)、松二糖、泰威糖、木二糖、伞形糖等的基团。此外,应当理解,“二糖”、“三糖”和“多糖”等还可以被取代。二糖还包括氨基糖及其衍生物,特别是在C-4’位衍生的碳霉糖或在C-6’位衍生的4-脱氧-3-氨基-葡萄糖。
术语“对象”或“患者”涵盖哺乳动物。哺乳动物的实例包括但不限于哺乳动物纲的任何成员:人类、非人灵长类动物(如黑猩猩)以及其他猿和猴物种;农场动物,如牛、马、绵羊、山羊、猪;家畜,如兔、狗和猫;实验室动物,包括啮齿动物,如大鼠、小鼠和豚鼠等。在一个方面,哺乳动物是人类。如本文所用的术语“动物”包括人类和非人动物。在一个实施方案中,“非人动物”是哺乳动物,例如啮齿动物,如大鼠或小鼠。在一个实施方案中,非人动物是小鼠。
如本文所用的术语“治疗(treat)”、“治疗(treating)”或“治疗(treatment)”包括减轻、减少或改善疾病或病状的至少一种症状,预防另外的症状,抑制疾病或病状,例如,阻止疾病或病状的发展、缓解疾病或病状、引起疾病或病状的消退、缓解由疾病或病状引起的病状或预防性地和/或治疗性地停止疾病或病状的症状。术语“治疗”还涵盖如下所述的“预防(prevent)”、“预防(preventing)”和“预防(prevention)”的概念。应当理解,尽管不排除,但治疗病症或病状不要求完全消除与其相关的病症、病状或症状。
术语疾病状态的“预防(preventing)”或“预防(prevention)”表示使疾病状态的临床症状不在可暴露于或易患疾病状态但尚未经历或显示疾病状态的症状的对象中发展。
术语“药物组合物”和“药物制剂”(或“制剂”)可互换使用,并且表示包含治疗有效量的活性药物成分以及一种或多种药学上可接受的赋形剂的混合物或溶液,以施用至对象,例如有需要的人。
如本文所用的术语“药物组合”是指由混合或组合多于一种药学上的活性成分产生的产物,并且包括活性成分的固定和非固定组合。术语“固定组合”意指活性成分(例如,本文所述的化合物和共同药剂)均以单一实体或剂量的形式同时施用至患者。术语“非固定组合”意指活性成分(例如,本文所述的化合物和共用药剂)作为单独实体同时、并行或依次施用至患者,没有特定的间隔时间限制,其中这种施用在患者体内提供两种化合物的有效水平。后者也适用于混合物疗法,例如,三种或更多种活性成分的施用。
术语“药学上可接受的”表示可用于制备药物组合物的材料的属性,其通常是安全、无毒的,并且在生物学上或其他方面都不是不希望的,并且对于兽用以及人类药物用途是可接受的。“药学上可接受的”可以指不消除化合物的生物活性或特性并且相对无毒的材料,如载剂或稀释剂,例如,该材料可以施用至个体,而不会引起不希望的生物效应或以有害的方式与含有它的组合物的组分中的任一种相互作用。
术语“药学上可接受的赋形剂”、“药学上可接受的载剂”、“药学上可接受的媒介物”和“治疗惰性赋形剂”可以互换使用,并且表示在药物组合物中不具有治疗活性并且对施用的对象无毒的任何药学上可接受的成分,如用于配制药物产品的崩解剂、粘合剂、填充剂、溶剂、缓冲液、张度剂、稳定剂、抗氧化剂、表面活性剂、载剂、稀释剂、赋形剂、防腐剂或润滑剂。
术语“碱基编辑”和“碱基校正”可互换使用,以指示在靶基因内的靶序列处导致碱基修饰的碱基改变或突变。在某些实施方案中,碱基编辑发生在靶序列的单个碱基处。在优选的实施方案中,碱基编辑不涉及靶序列的双链断裂。
如本文所用,术语“siRNA”是指介导RNA转录物的靶向切割的药剂。这些药剂与被称为RNAi诱导的沉默复合体(RISC)的胞质多蛋白复合体相关。有效诱导RNA干扰的药剂在本文中也被称为siRNA、RNAi药剂或iRNA药剂。如本文所用,术语siRNA包括微小RNA和前体微小RNA(pre-microRNA)。如本文所用,术语“siRNA活性”和“RNAi活性”是指通过siRNA的基因沉默。
术语“2’-O-甲氧基乙基”(也被称为2’-MOE、2’-O(CH2)2—OCH3和2’-O-(2-甲氧基乙基))是指呋喃糖基环(furosyl ring)的2’位的O-甲氧基-乙基修饰。2’-O-甲氧基乙基修饰的糖是经修饰的糖。
术语“2’-O-甲氧基乙基核苷酸”意指包含2’-O-甲氧基乙基修饰的糖部分的核苷酸。
术语“5-甲基胞嘧啶”意指用附接至5’位置的甲基修饰的胞嘧啶。5-甲基胞嘧啶是经修饰的核碱基。
术语“氧代”是指=O取代基。
术语“烷基”是指具有一个至二十个碳原子的直链或支链烃链基团,并且其通过单键附接至分子的其余部分。包含高达10个碳原子的烷基被称为C1-C10烷基,同样地,例如,包含高达6个碳原子的烷基是C1-C6烷基。相似地表示包含其他数量碳原子的烷基(和本文定义的其他部分)。烷基包括但不限于C1-C10烷基、C1-C9烷基、C1-C8烷基、C1-C7烷基、C1-C6烷基、C1-C5烷基、C1-C4烷基、C1-C3烷基、C1-C2烷基、C2-C8烷基、C3-C8烷基和C4-C8烷基。代表性的烷基包括但不限于甲基、乙基、正丙基、1-甲基乙基(异丙基)、正丁基、异丁基、仲丁基、正戊基、1,1-二甲基乙基(叔丁基)、3-甲基己基、2-甲基己基、1-乙基丙基等。在一些实施方案中,烷基是甲基或乙基。在一些实施方案中,烷基是-CH(CH3)2或-C(CH3)3。除非在本说明书中另有具体陈述,否则烷基可以如下所述任选地被取代。“亚烷基”或“亚烷基链”是指将分子的其余部分连接至基团的直链或支链二价烃链。在一些实施方案中,亚烷基是-CH2-、-CH2CH2-或-CH2CH2CH2-。在一些实施方案中,亚烷基是-CH2-。在一些实施方案中,亚烷基是-CH2CH2-。在一些实施方案中,亚烷基是-CH2CH2CH2-。
术语“烷氧基”是指式-OR的基团,其中R为如定义的烷基。除非在本说明书中另有具体陈述,否则烷氧基可以如下所述任选地被取代。代表性的烷氧基包括但不限于甲氧基、乙氧基、丙氧基、丁氧基、戊氧基。在一些实施方案中,烷氧基是甲氧基。在一些实施方案中,烷氧基是乙氧基。
术语“烷基氨基”是指式-NHR或-NRR的基团,其中每个R独立地为如上定义的烷基。除非在本说明书中另有具体陈述,否则烷基氨基可以如下所述任选地被取代。
术语“烯基”是指其中存在至少一个碳-碳双键的一类烷基。在一个实施方案中,烯基具有式-C(R)=CR2,其中R是指烯基的剩余部分,其可以相同或不同。在一些实施方案中,R为H或烷基。在一些实施方案中,烯基选自次乙基(即,乙烯基)、丙烯基(即,烯丙基)、丁烯基、戊烯基、戊二烯基等。烯基的非限制性实例包括-CH=CH2、-C(CH3)=CH2、-CH=CHCH3、-C(CH3)=CHCH3和-CH2CH=CH2。根据结构,烯基可以是单价或二价的(即,亚烯基)。
术语“炔基”是指其中存在至少一个碳-碳三键的一类烷基。因此,“亚炔基”可以指二价炔基。在一个实施方案中,烯基具有式-C≡C-R,其中R指炔基的剩余部分。在一些实施方案中,R为H或烷基。在一些实施方案中,炔基选自乙炔基、丙炔基、丁炔基、戊炔基、己炔基等。炔基的非限制性实例包括-C≡CH、-C≡CCH3-C≡CCH2CH3、-CH2C≡CH。
术语“芳基”是指其中形成环的原子中的每一个是碳原子的芳族环。芳基可以任选地被取代。芳基的实例包括但不限于苯基和萘基。在一些实施方案中,芳基是苯基。根据结构,芳基可以是单价或二价的(即,“亚芳基”)。除非在本说明书中另有具体陈述,否则术语“芳基”或前缀“芳(ar-)”(例如在“芳烷基”中)意指包含任选取代的芳基。在一些实施方案中,芳基被部分还原,以形成本文定义的环烷基。在一些实施方案中,芳基被完全还原,以形成本文定义的环烷基。在一些实施方案中,芳基是C6-C14芳基。在一些实施方案中,芳基是C6-C10芳基。
术语“环烷基”是指单环或多环非芳族基团,其中形成环的原子中的每一个(即骨架原子)是碳原子。在一些实施方案中,环烷基是饱和的或部分不饱和的。在一些实施方案中,环烷基是螺环或桥连化合物。在一些实施方案中,环烷基与芳族环稠合(在这种情况下,环烷基通过非芳族环碳原子键合)。环烷基包含具有3至10个环原子的基团。代表性的环烷基包括但不限于具有三至十个碳原子、三至八个碳原子、三至六个碳原子或三至五个碳原子的环烷基。单环环烷基包括例如环丙基、环丁基、环戊基、环己基、环庚基以及环辛基。在一些实施方案中,单环环烷基是环丙基、环丁基、环戊基或环己基。在一些实施方案中,单环环烷基是环戊烯基或环己烯基。在一些实施方案中,单环环烷基是环戊烯基。多环基团包括例如金刚烷基、1,2-二氢萘基、1,4-二氢萘基、四氢化萘基(tetrainyl)、十氢化萘基(decalinyl)、3,4-二氢萘基-1(2H)-酮、螺[2.2]戊基、降冰片基以及二环[1.1.1]戊基。除非在本说明书中另有具体陈述,否则环烷基可以任选地被取代。根据结构,环烷基可以是单价或二价的(即,亚环烷基)。
术语“卤代烷基”表示其中烷基的氢原子中的至少一个已被相同或不同的卤素原子、特别是氟原子置换的烷基。卤代烷基的实例包括单氟-、二氟-或三氟-甲基、-乙基或-丙基,例如3,3,3-三氟丙基、2-氟乙基、2,2,2-三氟乙基、氟甲基或三氟甲基。术语“全卤代烷基”表示其中烷基的所有氢原子已被相同或不同的卤素原子置换的烷基。
术语“杂亚烷基”是指其中烷基的一个或多个碳原子被O、N或S原子置换的如上所述的烷基。“杂亚烷基”或“杂亚烷基链”是指将分子的其余部分连接至基团的直链或支链二价杂烷基链。除非在本说明书中另有具体陈述,否则杂烷基或杂亚烷基可以如下所述任选地被取代。代表性的杂亚烷基包括但不限于-OCH2CH2O-、-OCH2CH2OCH2CH2O-或-OCH2CH2OCH2CH2OCH2CH2O-。
术语“杂环烷基”是指包含至少一个选自氮、氧和硫的杂原子的环烷基。除非在本说明书中另有具体陈述,否则杂环烷基可以是单环或双环状环系统,其可以包括稠合的(当与芳基或杂芳基环稠合时,杂环烷基通过非芳族环原子键合)或桥连环系统。杂环基中的氮、碳或硫原子可以任选被氧化。氮原子可以任选地被季铵化。杂环烷基是部分或完全饱和的。杂环烷基的实例包括但不限于二氧戊环基(dioxolanyl)、噻吩基[1,3]二噻烷基、四氢喹啉基、四氢异喹啉基、十氢喹啉基、十氢异喹啉基、咪唑啉基、咪唑烷基、异噻唑烷基、异噁唑烷基、吗啉基、八氢吲哚基、八氢异吲哚基、2-氧代哌嗪基、2-氧代哌啶基、2-氧代吡咯烷基、噁唑烷基、哌啶基、哌嗪基、4-哌啶酮基、吡咯烷基、吡唑烷基、奎宁环基、噻唑烷基、四氢呋喃基、三噻烷基(trithianyl)、四氢吡喃基、硫代吗啉基、硫吗啉基(thiamorpholinyl)、1-氧代-硫代吗啉基、1,1-二氧代-硫代吗啉基。术语杂环烷基还包括碳水化合物的所有环形式,包括但不限于单糖、二糖和寡糖。除非另有说明,否则杂环烷基的环具有2至12个碳。在一些实施方案中,杂环烷基的环具有2至10个碳。在一些实施方案中,杂环烷基的环具有2至10个碳以及1或2个N原子。在一些实施方案中,杂环烷基的环具有2至10个碳以及3或4个N原子。在一些实施方案中,杂环烷基的环具有2至12个碳、0-2个N原子、0-2个O原子、0-2个P原子以及0-1个S原子。在一些实施方案中,杂环烷基的环具有2至12个碳、1-3个N原子、0-1个O原子以及0-1个S原子。应理解,当提及杂环烷基中的碳原子数量时,杂环烷基中的碳原子数量与构成杂环烷基(即杂环烷基环的骨架原子)的原子(包括杂原子)总数不同。除非在本说明书中另有具体陈述,否则杂环烷基可以任选地被取代。如本文所用,术语“杂环亚烷基”可以指二价杂环烷基。
术语“杂芳基”是指包含一个或多个选自氮、氧和硫的环杂原子的芳基。杂芳基是单环或双环的。单环杂芳基的说明性实例包括吡啶基、咪唑基、嘧啶基、吡唑基、三唑基、吡嗪基、四唑基、呋喃基、噻吩基、异噁唑基、噻唑基、噁唑基、异噻唑基、吡咯基、哒嗪基、三嗪基、噁二唑基、噻二唑基、呋吖基、吲嗪、吲哚、苯并呋喃、苯并噻吩、吲唑、苯并咪唑、嘌呤、喹嗪、喹啉、异喹啉、噌啉、酞嗪、喹唑啉、喹喔啉、1,8-萘啶以及蝶啶。单环杂芳基的说明性实例包括吡啶基、咪唑基、嘧啶基、吡唑基、三唑基、吡嗪基、四唑基、呋喃基、噻吩基、异噁唑基、噻唑基、噁唑基、异噻唑基、吡咯基、哒嗪基、三嗪基、噁二唑基、噻二唑基以及呋吖基。双环杂芳基的说明性实例包括吲嗪、吲哚、苯并呋喃、苯并噻吩、吲唑、苯并咪唑、嘌呤、喹嗪、喹啉、异喹啉、噌啉、酞嗪、喹唑啉、喹喔啉、1,8-萘啶以及蝶啶。在一些实施方案中,杂芳基是吡啶基、吡嗪基、嘧啶基、噻唑基、噻吩基、噻二唑基或呋喃基。在一些实施方案中,杂芳基的环含有0-6个N原子。在一些实施方案中,杂芳基的环含有1-4个N原子。在一些实施方案中,杂芳基的环含有4-6个N原子。在一些实施方案中,杂芳基的环含有0-4个N原子、0-1个O原子、0-1个P原子以及0-1个S原子。在一些实施方案中,杂芳基的环含有1-4个N原子、0-1个O原子以及0-1个S原子。在一些实施方案中,杂芳基是C1-C9杂芳基。在一些实施方案中,单环杂芳基是C1-C5杂芳基。在一些实施方案中,单环杂芳基是5元或6元杂芳基。在一些实施方案中,双环杂芳基是C6-C9杂芳基。在一些实施方案中,杂芳基被部分还原,以形成本文定义的杂环烷基。在一些实施方案中,杂芳基被完全还原,以形成本文定义的杂环烷基。根据结构,杂芳基可以是单价或二价的(即,“杂亚芳基”基团)。
除非另有说明,否则术语“取代的”、“取代基”等可以指用特定取代基的基团单独地和独立地置换给定结构中的一个或多个氢基团,该特定取代基包括但不限于:D、卤素、-CN、-NH2、-NH(烷基)、-N(烷基)2、-OH、-CO2H、-CO2烷基、-C(=O)NH2、-C(=O)NH(烷基)、-C(=O)N(烷基)2、S(=O)2NH2、-S(=O)2NH(烷基)、-S(=O)2N(烷基)2、烷基、环烷基、氟烷基、杂烷基、烷氧基、氟代烷氧基、杂环烷基、芳基、杂芳基、芳氧基、烷硫基、芳硫基、烷基亚砜、芳基亚砜、烷基砜以及芳基砜。在一些其他实施方案中,任选的取代基独立地选自D、卤素、-CN、-NH2、-NH(CH3)、-N(CH3)2、-OH、-CO2H、-CO2(C1-C4烷基)、-C(=O)NH2、-C(=O)NH(C1-C4烷基)、-C(=O)N(C1-C4烷基)2、-S(=O)2NH2、-S(=O)2NH(C1-C4烷基)、-S(=O)2N(C1-C4烷基)2、C1-C4烷基、C3-C6环烷基、C1-C4氟烷基、C1-C4杂烷基、C1-C4烷氧基、C1-C4氟烷氧基、-SC1-C4烷基、-S(=O)C1-C4烷基和-S(=O)2(C1-C4烷基)。在一些实施方案中,任选的取代基独立地选自D、卤素、-CN、-NH2、-OH、-NH(CH3)、-N(CH3)2、-NH(环丙基)、-CH3、-CH2CH3、-CF3、-OCH3和-OCF3。在一些实施方案中,被取代的基团被前述基团中的一种或两种取代。在一些实施方案中,脂肪族碳原子(无环或环状)上的任选的取代基包括氧代(=O)。
术语“未取代的”是指特定基团不带有取代基。术语“任选取代的”是指特定基团是未取代的或被一个或多个取代基取代,取代基独立地选自可能的取代基。当指示取代基的数量时,术语“一个或多个”是指从一个取代基至可能的最高取代数量,即一个氢被取代基置换直至所有氢被取代基置换。
“约”是指在值的±10%内。例如,如果陈述“标志物可以增加约50%”,则暗示着标志物可以增加45%-55%。
“活性药物剂”是指在施用至个体时提供治疗益处的药物组合物中的物质。
“剂量单位”是指其中提供药物制剂的形式,例如丸剂、片剂或本领域已知的其他剂量单位。在某些实施方案中,剂量单位是含有冻干的反义寡核苷酸的小瓶。在某些实施方案中,剂量单位是含有重构的反义寡核苷酸的小瓶。
“剂量”是指在单次施用中或在特定时间段内提供的药物制剂的特定量。在某些实施方案中,剂量可以以一次、两次或更多次大丸剂、片剂或注射剂施用。例如,在需要皮下施用的某些实施方案中,所需剂量需要单次注射不容易容纳的体积,因此,可以使用两次或更多次注射来实现所需剂量。在某些实施方案中,通过在延长的时间段内或连续输注来施用药物制剂。剂量可以陈述为每小时、每天、每周或每月药物制剂的量。剂量也可以表述为每单位质量对象组织的药物产品或药物物质的质量(例如mg/kg或g/kg)。
“经修饰的核苷间键”是指天然存在的核苷间键的取代或任何改变。例如,硫代磷酸酯键是经修饰的核苷间键。
“经修饰的核碱基”是指除腺嘌呤、胞嘧啶、鸟嘌呤、胸腺嘧啶或尿嘧啶以外的任何核碱基。例如,5-甲基胞嘧啶是经修饰的核碱基。“未修饰的核碱基”是指嘌呤碱基腺嘌呤(A)和鸟嘌呤(G),以及嘧啶碱基胸腺嘧啶(T)、胞嘧啶(C)和尿嘧啶(U)。
“经修饰的核苷”是指具有至少一个经修饰的糖部分和/或经修饰的核碱基的核苷。
“经修饰的核苷酸”是指具有至少一个经修饰的糖部分、经修饰的核苷间键和/或经修饰的核碱基的核苷酸。
“经修饰的寡核苷酸”是指包含至少一个经修饰的核苷酸的寡核苷酸。
“经修饰的糖”是指天然糖的取代或改变。例如,2’-O-甲氧基乙基修饰的糖是经修饰的糖。
“基序”是指反义化合物中化学上不同区域的模式。
“他汀”是指抑制HMG-CoA还原酶活性的药剂。
“心血管疾病或病症的症状”是指由心血管疾病或病症引起并伴随心血管疾病或病症的现象,并用作心血管疾病或病症的指示。例如,心绞痛;胸痛;呼吸短促;心悸;虚弱;头晕;恶心;出汗;心动过速;心动过缓;心律失常;心房颤动;下肢肿胀;发绀;疲劳;昏厥;面部麻痹;四肢麻痹;跛行或肌肉痉挛;腹胀;或发热是心血管疾病或病症的症状。
“靶核酸”和“靶序列”是指能够被基因组编辑组合物靶向的核酸。例如,ANGPTL3基因内或邻近ANGPTL3基因的靶DNA序列可被与Cas9核酸酶相关的引导核苷酸靶向。
用于检测和/或测量生物材料中多肽的方法是本领域熟知的,并且包括但不限于蛋白质印迹、流式细胞术、ELISA、RIA以及各种蛋白质组学技术。测量或检测多肽的示例性方法是免疫测定,如ELISA。这种类型的蛋白质定量可以基于能够捕获特定抗原的抗体以及能够检测被捕获的抗原的第二抗体。在Harlow,E.和Lane,D.Antibodies:A LaboratoryManual,(1988),冷泉港实验室出版社中描述了用于检测和/或测量多肽的示例性测定。
用于检测和/或测量生物材料中RNA的方法是本领域熟知的,并且包括但不限于Northern印迹、RNA保护测定、RT-PCR。合适的方法描述于Michael R.Green,JosephSambrook的Molecular Cloning:ALaboratory Manual(第四版),Peter MacCallum 2012,第2,028页,ISBN 978–1–936113–42–2。
核糖核蛋白(RNP)是指含有RNA的核蛋白。RNP可以是核糖核酸和RNA结合蛋白的复合体。这种组合也可以称为蛋白质-RNA复合体。这些复合体可以发挥许多生物学功能,包括但不限于DNA复制、DNA修饰、基因表达、代谢和RNA的修饰,以及pre-mRNA剪接。
如本文所用,术语“生物标志物”或“标志物”可互换使用,是指任何生物化学标志物、血清学标志物、遗传标志物,或可以用于将来自患者的样品分类为与病理状况(如心血管疾病或病症)相关的其他临床或回波描记特征。
如本文所用,术语“抗体”包括但不限于免疫球蛋白分子群体或免疫球蛋白分子的片段,该免疫球蛋白分子可以是多克隆或单克隆的,并且具有任何类别和同种型。免疫球蛋白有五大类:IgA、IgD、IgE、IgG和IgM,并且这些中的若干种还可以分为亚类(同种型),例如,IgG1、IgG2、IgG3、IgG4、IgA1(人)、IgA2(人)、IgAa(犬)、IgAb(犬)、IgAC(犬)和IgAd(犬)。这种片段通常包含特异性结合抗原的抗体分子的一部分。例如,本领域称为Fab、Fab’或F(ab’)2的免疫球蛋白分子的片段包括在术语抗体的含义内。
如本文所用,术语“标记物”是指可检测的化合物、组合物或固体支持物,其可以(例如,经由共价或非共价手段、单独或包封)直接或间接缀合至单克隆抗体或蛋白质。标记物可以是本身可检测的(例如,放射性同位素标记物、化学发光染料、电化学标记物、金属螯合物、乳胶颗粒或荧光标记物),或者在酶标记物的情况下,可以催化可检测的底物化合物或组合物的化学改变(例如,酶,如辣根过氧化物酶、碱性磷酸酶等)。本公开中使用的标记物可以是但不限于碱性磷酸酶;葡萄糖-6-磷酸脱氢酶(“G6PDH”);辣根过氧化物酶(HRP);化学发光剂(如异鲁米诺)、荧光剂(如荧光素和罗丹明化合物);核酶;以及染料。标记物也可以是本身可检测的特异性结合分子(例如,生物素、亲和素、链霉亲和素、洋地黄毒甙元、麦芽糖、寡组氨酸(例如,六组氨酸)、2,4-二硝基苯、苯基砷酸盐、ssDNA、dsDNA等)。标记物的使用产生信号,该信号可以通过如电磁辐射的检测或直接可视化的手段来检测,并且其可以任选地被测量。
“基本结合(Substantial binding)”或“基本上结合(substantially binding)”是指在特定测定条件下测定混合物中分子之间的特异性结合或识别的量。在其最广泛的方面,基本结合涉及第一分子不能结合或识别第二分子与第一分子结合或识别第三分子的能力之间的差异,使得该差异足以允许进行有意义的测定,以区分一组特定测定条件下的特异性结合,包括分子的相对浓度以及温育的时间和温度。在另一方面,在交叉反应性意义上,一种分子基本上不能结合或识别另一种分子,其中在包括分子的相对浓度和温育的一组特定测定条件下,第一分子对第二分子显示的反应性小于对第三分子显示的反应性的25%,例如小于10%,例如,小于5%。可以使用许多广泛已知的方法来测试特异性结合,例如,免疫组织化学测定、酶联免疫吸附测定(ELISA)、放射免疫测定(RIA)或蛋白质印迹测定。
如本文所用,术语“基本上相同的氨基酸序列”包括与天然存在的氨基酸序列相似但不相同的氨基酸序列。例如,具有与鞭毛蛋白基本上相同的氨基酸序列的氨基酸序列(例如,多肽)相对于天然存在的鞭毛蛋白的氨基酸序列可以具有一个或多个修饰,如氨基酸添加、缺失或取代,条件是经修饰的多肽基本上保留鞭毛蛋白的至少一种生物活性,如免疫反应性。两条序列之间的“相似性百分比”是含有两条序列共有的匹配残基或保守残基的位置数目除以比较位置数目乘以100的函数。在这方面,序列中的保守残基是与相应的参考残基在物理上或功能上相似的残基,例如,其具有相似的大小、形状、电荷、化学特性,包括具有形成共价键或氢键的能力等。
术语“靶向部分”是指对选定的靶标(例如,细胞、细胞类型、组织、器官、身体区域或隔室(例如,细胞、组织或器官隔室))提供增强的亲和力的任何分子。一些示例性靶向部分包括但不限于抗体、抗原、碳水化合物碱基部分、叶酸、受体配体、碳水化合物、适体、整联蛋白受体配体、趋化因子受体配体、转铁蛋白、生物素、血清素受体配体、PSMA、内皮素、GCPII、生长抑素、LDL和HDL配体。
术语“异源性”是指在自然界中通常彼此未发现相同关系的任何两条或更多条核酸或多肽序列。例如,异源性核酸通常是重组产生的,具有两条或更多条序列,例如,来自不相关基因的序列,其经排列以产生新的功能性核酸,例如,来自一个来源的启动子和来自另一个来源的编码区。相似地,异源性多肽通常是指在自然界中彼此未发现相同关系的两条或更多条子序列(例如,融合蛋白)。
如本文所用,术语“片段”包括全长蛋白质的氨基酸的肽、多肽或蛋白质区段,条件是该片段保留与疾病患者血清中的至少一种抗体的反应性。
“表位”是多肽上的抗原决定簇,其由多肽特异性抗体(例如,IBD相关抗体)上的互补位识别结合。
术语“临床因素”包括与疾病相关的患者的症状。心血管疾病的临床因素的实例包括但不限于心绞痛;胸痛;呼吸短促;心悸;虚弱;头晕;恶心;出汗;心动过速;心动过缓;心律失常;心房颤动;下肢肿胀;发绀;疲劳;昏厥;面部麻痹;四肢麻痹;跛行或肌肉痉挛;腹胀;或发热。在一些实施方案中,心血管疾病的诊断基于使用统计学算法分析患者中一种或多种标志物的存在或水平以及确定患者是否具有一种或多种临床因素的组合。
术语“预后”包括对病理状况(例如心血管疾病)的可能过程和结果的预测,或从疾病中恢复的可能性。在一些实施方案中,统计学算法的使用提供了患者心血管疾病的预后。例如,预后可以是手术、一种或多种临床因素的发展、肠癌的发展或从疾病中恢复。
本文提及的术语“CRISPR-Cas系统”包括由编码所述蛋白质的mRNA和单一向导RNA翻译的CRISPR相关蛋白质。在一些实施方案中,CRISPR相关蛋白质可以具有固有的核酸内切活性。在一些实施方案中,CRISPR-Cas系统促进向导RNA介导的基因改变。蛋白质或由蛋白质编码的mRNA产生的蛋白质可以促进感兴趣的基因的靶向的区段内的碱基或核碱基和/或基因编辑。
本文提供了用于靶向递送治疗性药剂(如核酸药剂)的方法和组合物。如本文所用的治疗性药剂可以与靶向部分连接或相关,以帮助靶向递送。例如,治疗性药剂和靶向部分可以形成缀合物。治疗性药剂可以包含与核酸(如向导RNA)复合的核酸引导的可编程核酸酶系统。在一些实施方案中,向导RNA可以被化学修饰。在一些实施方案中,经修饰的向导RNA可以用于制备治疗与基因相关的任何疾病、病症或病状的药物,其中基因可通过DNA的插入或缺失而改变、操纵、编辑和修饰。根据本公开的另外的方面,经修饰的向导RNA可以用于通过缺失、取代、修复或插入一个或多个核苷酸或DNA的区段来改变基因。这可以在微生物或动物、特别是哺乳动物、更特别是人类中进行。可以使用本公开的向导RNA和本领域已知的CRISPR/Cas系统在体外对人类细胞或组织进行遗传改变或修正,然后将其插回到有需要的患者中。在本公开的另一方面,提供了一种药物组合物,其包含根据本公开的经修饰的向导RNA和CRISPR-Cas系统以及药学上可接受的载剂或赋形剂。药物组合物可以包含具有本公开的经修饰的向导RNA的载体或细胞。
化合物
在一个方面,本文描述了一种式(I)的IVT mRNA序列起始子或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6,
条件是(i)Z1、Z2和Z3为氢;(ii)Q1和Q4为-CH2O-;(iii)Q2和Q3为氧;(iv)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(v)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或者(vi)A、A1和A2中的至少一个为-S-。
在一些实施方案中,IVT mRNA序列起始子具有式(I-a)的结构:
在一些实施方案中,IVT mRNA序列起始子具有式(I-b)的结构:
在一些实施方案中,IVT mRNA序列起始子具有式(I-c)的结构:
在一些实施方案中,IVT mRNA序列起始子具有式(I-d)的结构:
在一些实施方案中,IVT mRNA序列起始子具有式(I-e)的结构:
在一些实施方案中,IVT mRNA序列起始子具有式(I-f)的结构:
在一些实施方案中,IVT mRNA序列起始子具有式(I-g)的结构
在一些实施方案中,IVT mRNA序列起始子具有式(I-h)的结构
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Z1为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z1为氢。在一些实施方案中,Z1为F。在一些实施方案中,Z1为-OH。在一些实施方案中,Z1为-SH。在一些实施方案中,Z1为-CH3。在一些实施方案中,Z1为-CH2CH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中,Z1为-OCH2CH3。在一些实施方案中,Z1为-SCH3。在一些实施方案中,Z1为-NH2。在一些实施方案中,Z1为NHCH3。在一些实施方案中,Z1为NHC(=O)CH3。
在式(I)、(I-a)、(I-b)、(I-a)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Z2为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z2为氢。在一些实施方案中,Z2为F。在一些实施方案中,Z2为-OH。在一些实施方案中,Z2为-SH。在一些实施方案中,Z2为-CH3。在一些实施方案中,Z2为-CH2CH3。在一些实施方案中,Z2为-OCH3。在一些实施方案中,Z2为-OCH2CH3。在一些实施方案中,Z2为-SCH3。在一些实施方案中,Z2为-NH2。在一些实施方案中,Z2为NHCH3。在一些实施方案中,Z2为NHC(=O)CH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Z3为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z3为氢。在一些实施方案中,Z3为氟。在一些实施方案中,Z3为-OH。在一些实施方案中,Z3为-SH。在一些实施方案中,Z3为-CH3。在一些实施方案中,Z3为-CH2CH3。在一些实施方案中,Z3为-OCH2OCH3。在一些实施方案中,Z3为-OCH2CH2CH3。在一些实施方案中,Z3为-OCH(CH3)2。在一些实施方案中,Z3为-SCH3。在一些实施方案中,Z3为-OCH2CH2OCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Z4为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z4为氢。在一些实施方案中,Z4为氟。在一些实施方案中,Z4为-OH。在一些实施方案中,Z4为-SH。在一些实施方案中,Z4为-CH3。在一些实施方案中,Z4为-CH2CH3。在一些实施方案中,Z4为-OCH2OCH3。在一些实施方案中,Z4为-OCH2CH2CH3。在一些实施方案中,Z4为-OCH(CH3)2。在一些实施方案中,Z4为-SCH3。在一些实施方案中,Z4为-OCH2CH2OCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Zn为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Zn为氢。在一些实施方案中,Zn为氟。在一些实施方案中,Zn为-OH。在一些实施方案中,Zn为-SH。在一些实施方案中,Zn为-CH3。在一些实施方案中,Zn为-CH2CH3。在一些实施方案中,Zn为-OCH2OCH3。在一些实施方案中,Zn为-OCH2CH2CH3。在一些实施方案中,Zn为-OCH(CH3)2。在一些实施方案中,Zn为-SCH3。在一些实施方案中,Zn为-OCH2CH2OCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,B2独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B2为鸟嘌呤。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B2为胞嘧啶。在一些实施方案中,B2为尿嘧啶,在一些实施方案中,B2为胸腺嘧啶,在一些实施方案中,B2为次黄嘌呤。在一些实施方案中,B2为嘌呤。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,B3独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B3为鸟嘌呤。在一些实施方案中,B3为腺嘌呤。在一些实施方案中,B3为胞嘧啶。在一些实施方案中,B3为尿嘧啶,在一些实施方案中,B3为胸腺嘧啶,在一些实施方案中,B3为次黄嘌呤。在一些实施方案中,B3为嘌呤。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Bn独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,Bn为鸟嘌呤。在一些实施方案中,Bn为腺嘌呤。在一些实施方案中,Bn为胞嘧啶。在一些实施方案中,Bn为尿嘧啶,在一些实施方案中,Bn为胸腺嘧啶,在一些实施方案中,Bn为次黄嘌呤。在一些实施方案中,Bn为嘌呤。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,B2、B3和Bn中的至少一个为腺嘌呤。在一些实施方案中,B2、B3和Bn中的至少一个为鸟嘌呤。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B3为腺嘌呤。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Q1为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH2-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q1为-CH2S-。在一些实施方案中,Q1为-CH2CH2-。在一些实施方案中,Q1为-CH2CF2-。在一些实施方案中,Q1为-CH2NH2-。在一些实施方案中,Q1为-CH2NH(CH3)-。在一些实施方案中,Q1为-CH2N(C(=O)CH3)-。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Q4为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q4为-CH2-。在一些实施方案中,Q4为-CH=CH-。在一些实施方案中,Q4为-CH2O-。在一些实施方案中,Q4为-CH2S-。在一些实施方案中,Q4为-CH2CH2-。在一些实施方案中,Q4为-CH2CF2-。在一些实施方案中,Q4为-CH2NH2-。在一些实施方案中,Q4为-CH2NH(CH3)-。在一些实施方案中,Q4为-CH2N(C(=O)CH3)-。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Q2为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,Q2为-O-。在一些实施方案中,Q2为-S-。在一些实施方案中,Q2为-CH2-。在一些实施方案中,Q2为-CF2-。在一些实施方案中,Q2为-NH-。在一些实施方案中,Q2为-N(CH3)-。在一些实施方案中,Q2为-N(C(=O)CH3)。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Q3为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,Q3为-O-。在一些实施方案中,Q3为-S-。在一些实施方案中,Q3为-CH2-。在一些实施方案中,Q3为-CF2-。在一些实施方案中,Q3为-NH-。在一些实施方案中,Q3为-N(CH3)-。在一些实施方案中,Q3为-N(C(=O)CH3)。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,X1为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X1为-OH。在一些实施方案中,X1为-SH。在一些实施方案中,X1为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X1为-NH2。在一些实施方案中,X1为-NHCH3。在一些实施方案中,X1为-NH(C(=O)CH3)。在一些实施方案中,X1为-CH3。在一些实施方案中,X1为-CH2CH3。在一些实施方案中,X1为-CH2CH2CH3。在一些实施方案中,X1为-CH(CH3)2。在一些实施方案中,X1为-OCH3。在一些实施方案中,X1为-OCH2CH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,X2为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X2为-OH。在一些实施方案中,X2为-SH。在一些实施方案中,X2为-O-。在一些实施方案中,X2为-S-。在一些实施方案中,X2为-NH2。在一些实施方案中,X2为-NHCH3。在一些实施方案中,X2为-NH(C(=O)CH3)。在一些实施方案中,X2为-CH3。在一些实施方案中,X2为-CH2CH3。在一些实施方案中,X2为-CH2CH2CH3。在一些实施方案中,X2为-CH(CH3)2。在一些实施方案中,X2为-OCH3。在一些实施方案中,X2为-OCH2CH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,X3为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X3为-OH。在一些实施方案中,X3为-SH。在一些实施方案中,X3为-O-。在一些实施方案中,X3为-S-。在一些实施方案中,X3为-NH2。在一些实施方案中,X3为-NHCH3。在一些实施方案中,X3为-NH(C(=O)CH3)。在一些实施方案中,X3为-CH3。在一些实施方案中,X3为-CH2CH3。在一些实施方案中,X3为-CH2CH2CH3。在一些实施方案中,X3为-CH(CH3)2。在一些实施方案中,X3为-OCH3。在一些实施方案中,X3为-OCH2CH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,X4为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X4为-OH。在一些实施方案中,X4为-SH。在一些实施方案中,X4为-O-。在一些实施方案中,X4为-S-。在一些实施方案中,X4为-NH2。在一些实施方案中,X4为-NHCH3。在一些实施方案中,X4为-NH(C(=O)CH3)。在一些实施方案中,X4为-CH3。在一些实施方案中,X4为-CH2CH3。在一些实施方案中,X4为-CH2CH2CH3。在一些实施方案中,X4为-CH(CH3)2。在一些实施方案中,X4为-OCH3。在一些实施方案中,X4为-OCH2CH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Xn为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,Xn为-OH。在一些实施方案中,Xn为-SH。在一些实施方案中,Xn为-O-。在一些实施方案中,Xn为-S-。在一些实施方案中,Xn为-NH2。在一些实施方案中,Xn为-NHCH3。在一些实施方案中,Xn为-NH(C(=O)CH3)。在一些实施方案中,Xn为-CH3。在一些实施方案中,Xn为-CH2CH3。在一些实施方案中,Xn为-CH2CH2CH3。在一些实施方案中,Xn为-CH(CH3)2。在一些实施方案中,Xn为-OCH3。在一些实施方案中,Xn为-OCH2CH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Y1为=O、=S、=NH或=NCH3。在一些实施方案中,Y1为=O。在一些实施方案中,Y1为=S。在一些实施方案中,Y1为=NH。在一些实施方案中,Y1为=NHCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Y2为=O、=S、=NH或=NCH3。在一些实施方案中,Y2为=O。在一些实施方案中,Y2为=S。在一些实施方案中,Y2为=NH。在一些实施方案中,Y2为=NHCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Y3为=O、=S、=NH或=NCH3。在一些实施方案中,Y3为=O。在一些实施方案中,Y3为=S。在一些实施方案中,Y3为=NH。在一些实施方案中,Y3为=NHCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Y4为=O、=S、=NH或=NCH3。在一些实施方案中,Y4为=O。在一些实施方案中,Y4为=S。在一些实施方案中,Y4为=NH。在一些实施方案中,Y4为=NHCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,Yn为=O、=S、=NH或=NCH3。在一些实施方案中,Yn为=O。在一些实施方案中,Yn为=S。在一些实施方案中,Yn为=NH。在一些实施方案中,Yn为=NHCH3。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,A为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A为-O-。在一些实施方案中,A为-S-。在一些实施方案中,A为-CH2-。在一些实施方案中,A为-NH-。在一些实施方案中,A为-N(CH3)-。在一些实施方案中,A为-N(C(=O)CH3)-。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,A1为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A1为-O-。在一些实施方案中,A1为-S-。在一些实施方案中,A1为-CH2-。在一些实施方案中,A1为-NH-。在一些实施方案中,A1为-N(CH3)-。在一些实施方案中,A1为-N(C(=O)CH3)-。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,A2为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A2为-CH2-。在一些实施方案中,A2为-NH-。在一些实施方案中,A2为-N(CH3)-。在一些实施方案中,A2为-N(C(=O)CH3)-。
在式(I)、(I-a)、(I-b)、(I-c)、(I-d)、(I-e)、(I-f)、(I-g)或(I-h)的化合物的一些实施方案中,p为0、1、2、3、4、5或6。在一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。在一些实施方案中,p为3。在一些实施方案中,p为4。在一些实施方案中,p为5。在一些实施方案中,p为6。
在式(I)的化合物的一些实施方案中,X1、X2、X3、X4和Xn中的至少一个为-SH。
在式(I)的化合物的一些实施方案中,X1、X2、X3、X4和Xn中的至少一个为-S-。
在式(I)的化合物的一些实施方案中,Y1、Y2、Y3、Y4和Yn中的至少一个为=S。
在式(I)的化合物的一些实施方案中,A、A1和A2中的至少一个为-S-。
在式(I)的化合物的一些实施方案中,Z1、Z2、Z3、Z4和Zn中的至少一个为-OCH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z3和Z1为-OCH3。在式(I)的化合物的一些实施方案中,Z1、Z2、Z3、Z4和Zn中的至少一个为-OH。在一些实施方案中,Z1、Z2和Z4为-OH。在一些实施方案中,Z2和Z4为-OH。
在式(I)的化合物的一些实施方案中,Q1、Q2、Q3和Q4中的至少一个为-OCH3。在式(I)的化合物的一些实施方案中,Q1、Q2、Q3和Q4中的至少一个为-O-。在一些实施方案中,Q1和Q4为-OCH3。在一些实施方案中,Q2和Q3为-O-。
在式(I)的化合物的一些实施方案中,Y1、Y2、Y3、Y4和Yn中的至少一个为=O。在一些实施方案中,Y1、Y2、Y3和Y4为=O。在一些实施方案中,Y1、Y2、Y3、Y4和Yn为=S。在一些实施方案中,Y2为=S。在一些实施方案中,Y4为=S。
在式(I)的化合物的一些实施方案中,X1、X2、X3、X4和Xn中的至少一个为-O-。在一些实施方案中,X1、X2、X3和X4为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X2为-S-。在一些实施方案中,X3为-S-。在一些实施方案中,X4为-S-。
在式(I)的化合物的一些实施方案中,在式(I)的化合物的一些实施方案中,A、A1和A2中的至少一个为-O-。在一些实施方案中,A、A1和A2为-O-。
在一个方面,本文描述了一种具有基序(I’)的5’端区域基序的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6,
条件是(i)Z1、Z2和Z3为氢;(ii)Q1和Q4为-CH2O-;(iii)Q2和Q3为氧;(iv)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(v)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或者(vi)A、A1和A2中的至少一个为-S-。
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-a)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-b)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-c)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-d)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-e)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-f)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-g)的结构:
在一些实施方案中,具有5’端区域基序的mRNA序列具有基序(I’-h)的结构:
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Z1为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z1为氢。在一些实施方案中,Z1为F。在一些实施方案中,Z1为-OH。在一些实施方案中,Z1为-SH。在一些实施方案中,Z1为-CH3。在一些实施方案中,Z1为-CH2CH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中,Z1为-OCH2CH3。在一些实施方案中,Z1为-SCH3。在一些实施方案中,Z1为-NH2。在一些实施方案中,Z1为NHCH3。在一些实施方案中,Z1为NHC(=O)CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-a)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Z2为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z2为氢。在一些实施方案中,Z2为F。在一些实施方案中,Z2为-OH。在一些实施方案中,Z2为-SH。在一些实施方案中,Z2为-CH3。在一些实施方案中,Z2为-CH2CH3。在一些实施方案中,Z2为-OCH3。在一些实施方案中,Z2为-OCH2CH3。在一些实施方案中,Z2为-SCH3。在一些实施方案中,Z2为-NH2。在一些实施方案中,Z2为NHCH3。在一些实施方案中,Z2为NHC(=O)CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Z3为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z3为氢。在一些实施方案中,Z3为氟。在一些实施方案中,Z3为-OH。在一些实施方案中,Z3为-SH。在一些实施方案中,Z3为-CH3。在一些实施方案中,Z3为-CH2CH3。在一些实施方案中,Z3为-OCH2OCH3。在一些实施方案中,Z3为-OCH2CH2CH3。在一些实施方案中,Z3为-OCH(CH3)2。在一些实施方案中,Z3为-SCH3。在一些实施方案中,Z3为-OCH2CH2OCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Z4为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z4为氢。在一些实施方案中,Z4为氟。在一些实施方案中,Z4为-OH。在一些实施方案中,Z4为-SH。在一些实施方案中,Z4为-CH3。在一些实施方案中,Z4为-CH2CH3。在一些实施方案中,Z4为-OCH2OCH3。在一些实施方案中,Z4为-OCH2CH2CH3。在一些实施方案中,Z4为-OCH(CH3)2。在一些实施方案中,Z4为-SCH3。在一些实施方案中,Z4为-OCH2CH2OCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Zn为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Zn为氢。在一些实施方案中,Zn为氟。在一些实施方案中,Zn为-OH。在一些实施方案中,Zn为-SH。在一些实施方案中,Zn为-CH3。在一些实施方案中,Zn为-CH2CH3。在一些实施方案中,Zn为-OCH2OCH3。在一些实施方案中,Zn为-OCH2CH2CH3。在一些实施方案中,Zn为-OCH(CH3)2。在一些实施方案中,Zn为-SCH3。在一些实施方案中,Zn为-OCH2CH2OCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,B2独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B2为鸟嘌呤。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B2为胞嘧啶。在一些实施方案中,B2为尿嘧啶,在一些实施方案中,B2为胸腺嘧啶,在一些实施方案中,B2为次黄嘌呤。在一些实施方案中,B2为嘌呤。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,B3独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B3为鸟嘌呤。在一些实施方案中,B3为腺嘌呤。在一些实施方案中,B3为胞嘧啶。在一些实施方案中,B3为尿嘧啶,在一些实施方案中,B3为胸腺嘧啶,在一些实施方案中,B3为次黄嘌呤。在一些实施方案中,B3为嘌呤。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Bn独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,Bn为鸟嘌呤。在一些实施方案中,Bn为腺嘌呤。在一些实施方案中,Bn为胞嘧啶。在一些实施方案中,Bn为尿嘧啶,在一些实施方案中,Bn为胸腺嘧啶,在一些实施方案中,Bn为次黄嘌呤。在一些实施方案中,Bn为嘌呤。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,B2、B3和Bn中的至少一个为腺嘌呤。在一些实施方案中,B2、B3和Bn中的至少一个为鸟嘌呤。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B3为腺嘌呤。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Q1为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH2-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q1为-CH2S-。在一些实施方案中,Q1为-CH2CH2-。在一些实施方案中,Q1为-CH2CF2-。在一些实施方案中,Q1为-CH2NH2-。在一些实施方案中,Q1为-CH2NH(CH3)-。在一些实施方案中,Q1为-CH2N(C(=O)CH3)-。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Q4为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q4为-CH2-。在一些实施方案中,Q4为-CH=CH-。在一些实施方案中,Q4为-CH2O-。在一些实施方案中,Q4为-CH2S-。在一些实施方案中,Q4为-CH2CH2-。在一些实施方案中,Q4为-CH2CF2-。在一些实施方案中,Q4为-CH2NH2-。在一些实施方案中,Q4为-CH2NH(CH3)-。在一些实施方案中,Q4为-CH2N(C(=O)CH3)-。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Q2为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,Q2为-O-。在一些实施方案中,Q2为-S-。在一些实施方案中,Q2为-CH2-。在一些实施方案中,Q2为-CF2-。在一些实施方案中,Q2为-NH-。在一些实施方案中,Q2为-N(CH3)-。在一些实施方案中,Q2为-N(C(=O)CH3)。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Q3为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,Q3为-O-。在一些实施方案中,Q3为-S-。在一些实施方案中,Q3为-CH2-。在一些实施方案中,Q3为-CF2-。在一些实施方案中,Q3为-NH-。在一些实施方案中,Q3为-N(CH3)-。在一些实施方案中,Q3为-N(C(=O)CH3)。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,X1为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X1为-OH。在一些实施方案中,X1为-SH。在一些实施方案中,X1为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X1为-NH2。在一些实施方案中,X1为-NHCH3。在一些实施方案中,X1为-NH(C(=O)CH3)。在一些实施方案中,X1为-CH3。在一些实施方案中,X1为-CH2CH3。在一些实施方案中,X1为-CH2CH2CH3。在一些实施方案中,X1为-CH(CH3)2。在一些实施方案中,X1为-OCH3。在一些实施方案中,X1为-OCH2CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,X2为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X2为-OH。在一些实施方案中,X2为-SH。在一些实施方案中,X2为-O-。在一些实施方案中,X2为-S-。在一些实施方案中,X2为-NH2。在一些实施方案中,X2为-NHCH3。在一些实施方案中,X2为-NH(C(=O)CH3)。在一些实施方案中,X2为-CH3。在一些实施方案中,X2为-CH2CH3。在一些实施方案中,X2为-CH2CH2CH3。在一些实施方案中,X2为-CH(CH3)2。在一些实施方案中,X2为-OCH3。在一些实施方案中,X2为-OCH2CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,X3为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X3为-OH。在一些实施方案中,X3为-SH。在一些实施方案中,X3为-O-。在一些实施方案中,X3为-S-。在一些实施方案中,X3为-NH2。在一些实施方案中,X3为-NHCH3。在一些实施方案中,X3为-NH(C(=O)CH3)。在一些实施方案中,X3为-CH3。在一些实施方案中,X3为-CH2CH3。在一些实施方案中,X3为-CH2CH2CH3。在一些实施方案中,X3为-CH(CH3)2。在一些实施方案中,X3为-OCH3。在一些实施方案中,X3为-OCH2CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,X4为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X4为-OH。在一些实施方案中,X4为-SH。在一些实施方案中,X4为-O-。在一些实施方案中,X4为-S-。在一些实施方案中,X4为-NH2。在一些实施方案中,X4为-NHCH3。在一些实施方案中,X4为-NH(C(=O)CH3)。在一些实施方案中,X4为-CH3。在一些实施方案中,X4为-CH2CH3。在一些实施方案中,X4为-CH2CH2CH3。在一些实施方案中,X4为-CH(CH3)2。在一些实施方案中,X4为-OCH3。在一些实施方案中,X4为-OCH2CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Xn为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,Xn为-OH。在一些实施方案中,Xn为-SH。在一些实施方案中,Xn为-O-。在一些实施方案中,Xn为-S-。在一些实施方案中,Xn为-NH2。在一些实施方案中,Xn为-NHCH3。在一些实施方案中,Xn为-NH(C(=O)CH3)。在一些实施方案中,Xn为-CH3。在一些实施方案中,Xn为-CH2CH3。在一些实施方案中,Xn为-CH2CH2CH3。在一些实施方案中,Xn为-CH(CH3)2。在一些实施方案中,Xn为-OCH3。在一些实施方案中,Xn为-OCH2CH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Y1为=O、=S、=NH或=NCH3。在一些实施方案中,Y1为=O。在一些实施方案中,Y1为=S。在一些实施方案中,Y1为=NH。在一些实施方案中,Y1为=NHCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Y2为=O、=S、=NH或=NCH3。在一些实施方案中,Y2为=O。在一些实施方案中,Y2为=S。在一些实施方案中,Y2为=NH。在一些实施方案中,Y2为=NHCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Y3为=O、=S、=NH或=NCH3。在一些实施方案中,Y3为=O。在一些实施方案中,Y3为=S。在一些实施方案中,Y3为=NH。在一些实施方案中,Y3为=NHCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Y4为=O、=S、=NH或=NCH3。在一些实施方案中,Y4为=O。在一些实施方案中,Y4为=S。在一些实施方案中,Y4为=NH。在一些实施方案中,Y4为=NHCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,Yn为=O、=S、=NH或=NCH3。在一些实施方案中,Yn为=O。在一些实施方案中,Yn为=S。在一些实施方案中,Yn为=NH。在一些实施方案中,Yn为=NHCH3。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,A为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A为-O-。在一些实施方案中,A为-S-。在一些实施方案中,A为-CH2-。在一些实施方案中,A为-NH-。在一些实施方案中,A为-N(CH3)-。在一些实施方案中,A为-N(C(=O)CH3)-。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,A1为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A1为-O-。在一些实施方案中,A1为-S-。在一些实施方案中,A1为-CH2-。在一些实施方案中,A1为-NH-。在一些实施方案中,A1为-N(CH3)-。在一些实施方案中,A1为-N(C(=O)CH3)-。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,A2为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A2为-CH2-。在一些实施方案中,A2为-NH-。在一些实施方案中,A2为-N(CH3)-。在一些实施方案中,A2为-N(C(=O)CH3)-。
在基序(I’)、(I’-a)、(I’-b)、(I’-c)、(I’-d)、(I’-e)、(I’-f)、(I’-g)或(I’-h)的化合物的一些实施方案中,p为0、1、2、3、4、5或6。在一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。在一些实施方案中,p为3。在一些实施方案中,p为4。在一些实施方案中,p为5。在一些实施方案中,p为6。
在基序(I’)的化合物的一些实施方案中,X1、X2、X3、X4和Xn中的至少一个为-SH。
在基序(I’)的化合物的一些实施方案中,X1、X2、X3、X4和Xn中的至少一个为-S-。
在基序(I’)的化合物的一些实施方案中,Y1、Y2、Y3、Y4和Yn中的至少一个为=S。
在基序(I’)的化合物的一些实施方案中,A、A1和A2中的至少一个为-S-。
在基序(I’)的化合物的一些实施方案中,Z1、Z2、Z3、Z4和Zn中的至少一个为-OCH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z3和Z1为-OCH3。在基序(I’)的化合物的一些实施方案中,Z1、Z2、Z3、Z4和Zn中的至少一个为-OH。在一些实施方案中,Z1、Z2和Z4为-OH。在一些实施方案中,Z2和Z4为-OH。
在基序(I’)的化合物的一些实施方案中,Q1、Q2、Q3和Q4中的至少一个为-OCH3。在式(I)的化合物的一些实施方案中,Q1、Q2、Q3和Q4中的至少一个为-O-。在一些实施方案中,Q1和Q4为-OCH3。在一些实施方案中,Q2和Q3为-O-。
在基序(I’)的化合物的一些实施方案中,Y1、Y2、Y3、Y4和Yn中的至少一个为=O。在一些实施方案中,Y1、Y2、Y3和Y4为=O。在一些实施方案中,Y1、Y2、Y3、Y4和Yn为=S。在一些实施方案中,Y2为=S。在一些实施方案中,Y4为=S。
在基序(I’)的化合物的一些实施方案中,X1、X2、X3、X4和Xn中的至少一个为-O-。在一些实施方案中,X1、X2、X3和X4为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X2为-S-。在一些实施方案中,X3为-S-。在一些实施方案中,X4为-S-。
在基序(I’)的化合物的一些实施方案中,在基序(I’)的化合物的一些实施方案中,A、A1和A2中的至少一个为-O-。在一些实施方案中,A、A1和A2为-O-。
在一个方面,本文描述了一种mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,B2独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B2为鸟嘌呤。在一些实施方案中,B2为胞嘧啶。在一些实施方案中,B2为尿嘧啶,在一些实施方案中,B2为胸腺嘧啶,在一些实施方案中,B2为次黄嘌呤。在一些实施方案中,B2为嘌呤。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,B3独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B3为腺嘌呤。在一些实施方案中,B3为鸟嘌呤。在一些实施方案中,B3为胞嘧啶。在一些实施方案中,B3为尿嘧啶,在一些实施方案中,B3为胸腺嘧啶,在一些实施方案中,B3为次黄嘌呤。在一些实施方案中,B3为嘌呤。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Bn独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,Bn为腺嘌呤。在一些实施方案中,Bn为鸟嘌呤。在一些实施方案中,Bn为胞嘧啶。在一些实施方案中,Bn为尿嘧啶,在一些实施方案中,Bn为胸腺嘧啶,在一些实施方案中,Bn为次黄嘌呤。在一些实施方案中,Bn为嘌呤。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z1为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z1为氢。在一些实施方案中,Z1为氟。在一些实施方案中,Z1为-OH。在一些实施方案中,Z1为-SH。在一些实施方案中,Z1为-CH3。在一些实施方案中,Z1为-CH2CH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中,Z1为-NH(CH3),在一些实施方案中,Z1为-NH2-。在一些实施方案中,Z1为-NH(C(=O)CH3)。在一些实施方案中,Z1为-SCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z’为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z’为氢。在一些实施方案中,Z’为氟。在一些实施方案中,Z’为-OH。在一些实施方案中,Z’为-SH。在一些实施方案中,Z’为-CH3。在一些实施方案中,Z’为-CH2CH3。在一些实施方案中,Z’为-OCH3。在一些实施方案中,Z’为-NH(CH3),在一些实施方案中,Z’为-NH2-。在一些实施方案中,Z’为-NH(C(=O)CH3)。在一些实施方案中,Z’为-SCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z2为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z2为氟。在一些实施方案中,Z2为-OH。在一些实施方案中,Z2为-SH。在一些实施方案中,Z2为-CH3。在一些实施方案中,Z2为-CH2CH3。在一些实施方案中,Z2为-OCH3。在一些实施方案中,Z2为-SCH3。在一些实施方案中,Z2为-OCH2CH3。在一些实施方案中,Z2为-NH2。在一些实施方案中,Z2为NHCH3。在一些实施方案中,Z2为NHC(=O)CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z”为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z”为氟。在一些实施方案中,Z”为-OH。在一些实施方案中,Z”为-SH。在一些实施方案中,Z”为-CH3。在一些实施方案中,Z”为-CH2CH3。在一些实施方案中,Z”为-OCH3。在一些实施方案中,Z”为-SCH3。在一些实施方案中,Z”为-OCH2CH3。在一些实施方案中,Z”为-NH2。在一些实施方案中,Z”为NHCH3。在一些实施方案中,Z”为NHC(=O)CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3。在一些实施方案中,Z”’为氢。在一些实施方案中,Z”’为氟。在一些实施方案中,Z”’为-CH3。在一些实施方案中,Z”’为-CH2CH3。在一些实施方案中,Z”’为-OCH3。在一些实施方案中,Z”’为-OCH2CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z3为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z3为氢。在一些实施方案中,Z3为氟。在一些实施方案中,Z3为-OH。在一些实施方案中,Z3为-CH3。在一些实施方案中,Z3为-CH2CH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z3为-NH2。在一些实施方案中,Z3为-NHCH3。在一些实施方案中,Z3为-NH(C(=O)CH3)。在一些实施方案中,Z3为-OCH2CH3。在一些实施方案中,Z3为-OCH2OCH3。在一些实施方案中,Z3为-OCH2CH2CH3。在一些实施方案中,Z3为-OCH(CH3)2。在一些实施方案中,Z3为-SCH3。在一些实施方案中,Z3为-OCH2CH2OCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Z4为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z4为氢。在一些实施方案中,Z4为氟。在一些实施方案中,Z4为-OH。在一些实施方案中,Z4为-CH3。在一些实施方案中,Z4为-CH2CH3。在一些实施方案中,Z4为-OCH3。在一些实施方案中,Z4为-NH2。在一些实施方案中,Z4为-NHCH3。在一些实施方案中,Z4为-NH(C(=O)CH3)。在一些实施方案中,Z4为-OCH2CH3。在一些实施方案中,Z4为-OCH2OCH3。在一些实施方案中,Z4为-OCH2CH2CH3。在一些实施方案中,Z4为-OCH(CH3)2。在一些实施方案中,Z4为-SCH3。在一些实施方案中,Z4为-OCH2CH2OCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Zn为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Zn为氢。在一些实施方案中,Zn为氟。在一些实施方案中,Zn为-OH。在一些实施方案中,Zn为-CH3。在一些实施方案中,Zn为-CH2CH3。在一些实施方案中,Zn为-OCH3。在一些实施方案中,Zn为-NH2。在一些实施方案中,Zn为-NHCH3。在一些实施方案中,Zn为-NH(C(=O)CH3)。在一些实施方案中,Zn为-OCH2CH3。在一些实施方案中,Zn为-OCH2OCH3。在一些实施方案中,Zn为-OCH2CH2CH3。在一些实施方案中,Zn为-OCH(CH3)2。在一些实施方案中,Zn为-SCH3。在一些实施方案中,Zn为-OCH2CH2OCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Q1为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q1为-CH2-。在一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q1为-CH2S-。在一些实施方案中,Q1为-CH2CH2-。在一些实施方案中,Q1为-CH2CF2-。在一些实施方案中,Q1为-CH2NH2-。在一些实施方案中,Q1为-CH2NH(CH3)-。在一些实施方案中,Q1为-CH2N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Q4为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q4为-CH2-。在一些实施方案中,Q4为-CH2O-。在一些实施方案中,Q4为-CH2S-。在一些实施方案中,Q4为-CH2CH2-。在一些实施方案中,Q4为-CH2CF2-。在一些实施方案中,Q4为-CH2NH2-。在一些实施方案中,Q4为-CH2NH(CH3)-。在一些实施方案中,Q4为-CH2N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Q2为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q2为-O-。在一些实施方案中Q2为-S-。在一些实施方案中Q2为-CH2-。在一些实施方案中Q2为-CF2-。在一些实施方案中Q2为-NH-。在一些实施方案中Q2为-N(CH3)-。在一些实施方案中Q2为-N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Q3为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q3为-O-。在一些实施方案中Q3为-S-。在一些实施方案中Q3为-CH2-。在一些实施方案中Q3为-CF2-。在一些实施方案中Q3为-NH-。在一些实施方案中Q3为-N(CH3)-。在一些实施方案中Q3为-N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,X1为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X1为-OH。在一些实施方案中,X1为-SH。在一些实施方案中,X1为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X1为-NH2。在一些实施方案中,X1为-NHCH3。在一些实施方案中,X1为-NH(C(=O)CH3)。在一些实施方案中,X1为-CH3。在一些实施方案中,X1为-CH2CH3。在一些实施方案中,X1为-CH2CH2CH3。在一些实施方案中,X1为-CH(CH3)2。在一些实施方案中,X1为-OCH3。在一些实施方案中,X1为-OCH2CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,X2为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X2为-OH。在一些实施方案中,X2为-SH。在一些实施方案中,X2为-O-。在一些实施方案中,X2为-S-。在一些实施方案中,X2为-NH2。在一些实施方案中,X2为-NHCH3。在一些实施方案中,X2为-NH(C(=O)CH3)。在一些实施方案中,X2为-CH3。在一些实施方案中,X2为-CH2CH3。在一些实施方案中,X2为-CH2CH2CH3。在一些实施方案中,X2为-CH(CH3)2。在一些实施方案中,X2为-OCH3。在一些实施方案中,X2为-OCH2CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,X3为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X3为-OH。在一些实施方案中,X3为-SH。在一些实施方案中,X3为-O-。在一些实施方案中,X3为-S-。在一些实施方案中,X3为-NH2。在一些实施方案中,X3为-NHCH3。在一些实施方案中,X3为-NH(C(=O)CH3)。在一些实施方案中,X3为-CH3。在一些实施方案中,X3为-CH2CH3。在一些实施方案中,X3为-CH2CH2CH3。在一些实施方案中,X3为-CH(CH3)2。在一些实施方案中,X3为-OCH3。在一些实施方案中,X3为-OCH2CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,X4为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X4为-OH。在一些实施方案中,X4为-SH。在一些实施方案中,X4为-O-。在一些实施方案中,X4为-S-。在一些实施方案中,X4为-NH2。在一些实施方案中,X4为-NHCH3。在一些实施方案中,X4为-NH(C(=O)CH3)。在一些实施方案中,X4为-CH3。在一些实施方案中,X4为-CH2CH3。在一些实施方案中,X4为-CH2CH2CH3。在一些实施方案中,X4为-CH(CH3)2。在一些实施方案中,X4为-OCH3。在一些实施方案中,X4为-OCH2CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Xn为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,Xn为-OH。在一些实施方案中,Xn为-SH。在一些实施方案中,Xn为-O-。在一些实施方案中,Xn为-S-。在一些实施方案中,Xn为-NH2。在一些实施方案中,Xn为-NHCH3。在一些实施方案中,Xn为-NH(C(=O)CH3)。在一些实施方案中,Xn为-CH3。在一些实施方案中,Xn为-CH2CH3。在一些实施方案中,Xn为-CH2CH2CH3。在一些实施方案中,Xn为-CH(CH3)2。在一些实施方案中,Xn为-OCH3。在一些实施方案中,Xn为-OCH2CH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Y1为=O、=S、=NH或=NCH3。在一些实施方案中,Y1为=O。在一些实施方案中,Y1为=S。在一些实施方案中,Y1为=NH。在一些实施方案中,Y1为=NCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Y2为=O、=S、=NH或=NCH3。在一些实施方案中,Y2为=O。在一些实施方案中,Y2为=S。在一些实施方案中,Y2为=NH。在一些实施方案中,Y2为=NCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Y3为=O、=S、=NH或=NCH3。在一些实施方案中,Y3为=O。在一些实施方案中,Y3为=S。在一些实施方案中,Y3为=NH。在一些实施方案中,Y3为=NCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Y4为=O、=S、=NH或=NCH3。在一些实施方案中,Y4为=O。在一些实施方案中,Y4为=S。在一些实施方案中,Y4为=NH。在一些实施方案中,Y4为=NCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,Yn为=O、=S、=NH或=NCH3。在一些实施方案中,Yn为=O。在一些实施方案中,Yn为=S。在一些实施方案中,Yn为=NH。在一些实施方案中,Yn为=NCH3。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,A为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A为-O-。在一些实施方案中,A为-S-。在一些实施方案中,A为-CH2-。在一些实施方案中,A为-NH-。在一些实施方案中,A为-N(CH3)-。在一些实施方案中,A为-N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,A1为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A1为-O-。在一些实施方案中,A1为-S-。在一些实施方案中,A1为-CH2-。在一些实施方案中,A1为-NH-。在一些实施方案中,A1为-N(CH3)-。在一些实施方案中,A1为-N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,A2为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A2为-CH2-。在一些实施方案中,A2为-NH-。在一些实施方案中,A2为-N(CH3)-。在一些实施方案中,A2为-N(C(=O)CH3)-。
在式(II)、(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、(II-h)、(II-i)、(II-j)、(II-k)、(II-l)、(II-m)、(II-n)、(II-o)、(II-p)、(II-q)、(II-r)、(II-s)、(II-t)或(II-u)的化合物的一些实施方案中,p为0、1、2、3、4、5或6。在一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。在一些实施方案中,p为3。在一些实施方案中,p为4。在一些实施方案中,p为5。在一些实施方案中,p为6。
在一些实施方案中,Z1、Z2、Z3和Z4各自独立地为-OH或-OCH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中Z2为-OH。在一些实施方案中,Z1、Z2和Z4为-OH,并且Z3为-OCH3。在一些实施方案中,Z1和Z3为-OCH3,并且Z2和Z4为-OH。在一些实施方案中,Z’、Z”和Z”’为氢。
在一些实施方案中,Q1和Q4为-OCH2-。在一些实施方案中Q2和Q3为-O-。
在一些实施方案中,X1、X2、X3和X4为-O-。在一些实施方案中,X1、X2、X3和X4为-S-。在一些实施方案中,X1、X3、X4为-O-,并且X2为-S-。
在一些实施方案中,Y1、Y2、Y3和Y4为=O。在一些实施方案中,Y1、Y2、Y3和Y4为=S。在一些实施方案中,Y1、Y3和Y4为=O,并且Y2为=S。在一些实施方案中,Y1、Y2、Y3为=O,并且Y4为=S。
在一些实施方案中,A、A1和A2为-O-。
在一些实施方案中,p为0。
在一个方面,本文描述了一种具有5’端区域基序(基序(II’))的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,B2独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B2为鸟嘌呤。在一些实施方案中,B2为胞嘧啶。在一些实施方案中,B2为尿嘧啶,在一些实施方案中,B2为胸腺嘧啶,在一些实施方案中,B2为次黄嘌呤。在一些实施方案中,B2为嘌呤。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,B3独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B3为腺嘌呤。在一些实施方案中,B3为鸟嘌呤。在一些实施方案中,B3为胞嘧啶。在一些实施方案中,B3为尿嘧啶,在一些实施方案中,B3为胸腺嘧啶,在一些实施方案中,B3为次黄嘌呤。在一些实施方案中,B3为嘌呤。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Bn独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,Bn为腺嘌呤。在一些实施方案中,Bn为鸟嘌呤。在一些实施方案中,Bn为胞嘧啶。在一些实施方案中,Bn为尿嘧啶,在一些实施方案中,Bn为胸腺嘧啶,在一些实施方案中,Bn为次黄嘌呤。在一些实施方案中,Bn为嘌呤。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z1为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z1为氢。在一些实施方案中,Z1为氟。在一些实施方案中,Z1为-OH。在一些实施方案中,Z1为-SH。在一些实施方案中,Z1为-CH3。在一些实施方案中,Z1为-CH2CH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中,Z1为-NH(CH3),在一些实施方案中,Z1为-NH2-。在一些实施方案中,Z1为-NH(C(=O)CH3)。在一些实施方案中,Z1为-SCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z’为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z’为氢。在一些实施方案中,Z’为氟。在一些实施方案中,Z’为-OH。在一些实施方案中,Z’为-SH。在一些实施方案中,Z’为-CH3。在一些实施方案中,Z’为-CH2CH3。在一些实施方案中,Z’为-OCH3。在一些实施方案中,Z’为-NH(CH3),在一些实施方案中,Z’为-NH2-。在一些实施方案中,Z’为-NH(C(=O)CH3)。在一些实施方案中,Z’为-SCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z2为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z2为氟。在一些实施方案中,Z2为-OH。在一些实施方案中,Z2为-SH。在一些实施方案中,Z2为-CH3。在一些实施方案中,Z2为-CH2CH3。在一些实施方案中,Z2为-OCH3。在一些实施方案中,Z2为-SCH3。在一些实施方案中,Z2为-OCH2CH3。在一些实施方案中,Z2为-NH2。在一些实施方案中,Z2为NHCH3。在一些实施方案中,Z2为NHC(=O)CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z”为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z”为氟。在一些实施方案中,Z”为-OH。在一些实施方案中,Z”为-SH。在一些实施方案中,Z”为-CH3。在一些实施方案中,Z”为-CH2CH3。在一些实施方案中,Z”为-OCH3。在一些实施方案中,Z”为-SCH3。在一些实施方案中,Z”为-OCH2CH3。在一些实施方案中,Z”为-NH2。在一些实施方案中,Z”为NHCH3。在一些实施方案中,Z”为NHC(=O)CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3。在一些实施方案中,Z”’为氢。在一些实施方案中,Z”’为氟。在一些实施方案中,Z”’为-CH3。在一些实施方案中,Z”’为-CH2CH3。在一些实施方案中,Z”’为-OCH3。在一些实施方案中,Z”’为-OCH2CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z3为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z3为氢。在一些实施方案中,Z3为氟。在一些实施方案中,Z3为-OH。在一些实施方案中,Z3为-CH3。在一些实施方案中,Z3为-CH2CH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z3为-NH2。在一些实施方案中,Z3为-NHCH3。在一些实施方案中,Z3为-NH(C(=O)CH3)。在一些实施方案中,Z3为-OCH2CH3。在一些实施方案中,Z3为-OCH2OCH3。在一些实施方案中,Z3为-OCH2CH2CH3。在一些实施方案中,Z3为-OCH(CH3)2。在一些实施方案中,Z3为-SCH3。在一些实施方案中,Z3为-OCH2CH2OCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Z4为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z4为氢。在一些实施方案中,Z4为氟。在一些实施方案中,Z4为-OH。在一些实施方案中,Z4为-CH3。在一些实施方案中,Z4为-CH2CH3。在一些实施方案中,Z4为-OCH3。在一些实施方案中,Z4为-NH2。在一些实施方案中,Z4为-NHCH3。在一些实施方案中,Z4为-NH(C(=O)CH3)。在一些实施方案中,Z4为-OCH2CH3。在一些实施方案中,Z4为-OCH2OCH3。在一些实施方案中,Z4为-OCH2CH2CH3。在一些实施方案中,Z4为-OCH(CH3)2。在一些实施方案中,Z4为-SCH3。在一些实施方案中,Z4为-OCH2CH2OCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Zn为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Zn为氢。在一些实施方案中,Zn为氟。在一些实施方案中,Zn为-OH。在一些实施方案中,Zn为-CH3。在一些实施方案中,Zn为-CH2CH3。在一些实施方案中,Zn为-OCH3。在一些实施方案中,Zn为-NH2。在一些实施方案中,Zn为-NHCH3。在一些实施方案中,Zn为-NH(C(=O)CH3)。在一些实施方案中,Zn为-OCH2CH3。在一些实施方案中,Zn为-OCH2OCH3。在一些实施方案中,Zn为-OCH2CH2CH3。在一些实施方案中,Zn为-OCH(CH3)2。在一些实施方案中,Zn为-SCH3。在一些实施方案中,Zn为-OCH2CH2OCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Q1为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q1为-CH2-。在一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q1为-CH2S-。在一些实施方案中,Q1为-CH2CH2-。在一些实施方案中,Q1为-CH2CF2-。在一些实施方案中,Q1为-CH2NH2-。在一些实施方案中,Q1为-CH2NH(CH3)-。在一些实施方案中,Q1为-CH2N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Q4为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q4为-CH2-。在一些实施方案中,Q4为-CH2O-。在一些实施方案中,Q4为-CH2S-。在一些实施方案中,Q4为-CH2CH2-。在一些实施方案中,Q4为-CH2CF2-。在一些实施方案中,Q4为-CH2NH2-。在一些实施方案中,Q4为-CH2NH(CH3)-。在一些实施方案中,Q4为-CH2N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Q2为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q2为-O-。在一些实施方案中Q2为-S-。在一些实施方案中Q2为-CH2-。在一些实施方案中Q2为-CF2-。在一些实施方案中Q2为-NH-。在一些实施方案中Q2为-N(CH3)-。在一些实施方案中Q2为-N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Q3为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q3为-O-。在一些实施方案中Q3为-S-。在一些实施方案中Q3为-CH2-。在一些实施方案中Q3为-CF2-。在一些实施方案中Q3为-NH-。在一些实施方案中Q3为-N(CH3)-。在一些实施方案中Q3为-N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,X1为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X1为-OH。在一些实施方案中,X1为-SH。在一些实施方案中,X1为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X1为-NH2。在一些实施方案中,X1为-NHCH3。在一些实施方案中,X1为-NH(C(=O)CH3)。在一些实施方案中,X1为-CH3。在一些实施方案中,X1为-CH2CH3。在一些实施方案中,X1为-CH2CH2CH3。在一些实施方案中,X1为-CH(CH3)2。在一些实施方案中,X1为-OCH3。在一些实施方案中,X1为-OCH2CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,X2为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X2为-OH。在一些实施方案中,X2为-SH。在一些实施方案中,X2为-O-。在一些实施方案中,X2为-S-。在一些实施方案中,X2为-NH2。在一些实施方案中,X2为-NHCH3。在一些实施方案中,X2为-NH(C(=O)CH3)。在一些实施方案中,X2为-CH3。在一些实施方案中,X2为-CH2CH3。在一些实施方案中,X2为-CH2CH2CH3。在一些实施方案中,X2为-CH(CH3)2。在一些实施方案中,X2为-OCH3。在一些实施方案中,X2为-OCH2CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,X3为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X3为-OH。在一些实施方案中,X3为-SH。在一些实施方案中,X3为-O-。在一些实施方案中,X3为-S-。在一些实施方案中,X3为-NH2。在一些实施方案中,X3为-NHCH3。在一些实施方案中,X3为-NH(C(=O)CH3)。在一些实施方案中,X3为-CH3。在一些实施方案中,X3为-CH2CH3。在一些实施方案中,X3为-CH2CH2CH3。在一些实施方案中,X3为-CH(CH3)2。在一些实施方案中,X3为-OCH3。在一些实施方案中,X3为-OCH2CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,X4为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X4为-OH。在一些实施方案中,X4为-SH。在一些实施方案中,X4为-O-。在一些实施方案中,X4为-S-。在一些实施方案中,X4为-NH2。在一些实施方案中,X4为-NHCH3。在一些实施方案中,X4为-NH(C(=O)CH3)。在一些实施方案中,X4为-CH3。在一些实施方案中,X4为-CH2CH3。在一些实施方案中,X4为-CH2CH2CH3。在一些实施方案中,X4为-CH(CH3)2。在一些实施方案中,X4为-OCH3。在一些实施方案中,X4为-OCH2CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Xn为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,Xn为-OH。在一些实施方案中,Xn为-SH。在一些实施方案中,Xn为-O-。在一些实施方案中,Xn为-S-。在一些实施方案中,Xn为-NH2。在一些实施方案中,Xn为-NHCH3。在一些实施方案中,Xn为-NH(C(=O)CH3)。在一些实施方案中,Xn为-CH3。在一些实施方案中,Xn为-CH2CH3。在一些实施方案中,Xn为-CH2CH2CH3。在一些实施方案中,Xn为-CH(CH3)2。在一些实施方案中,Xn为-OCH3。在一些实施方案中,Xn为-OCH2CH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Y1为=O、=S、=NH或=NCH3。在一些实施方案中,Y1为=O。在一些实施方案中,Y1为=S。在一些实施方案中,Y1为=NH。在一些实施方案中,Y1为=NCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Y2为=O、=S、=NH或=NCH3。在一些实施方案中,Y2为=O。在一些实施方案中,Y2为=S。在一些实施方案中,Y2为=NH。在一些实施方案中,Y2为=NCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Y3为=O、=S、=NH或=NCH3。在一些实施方案中,Y3为=O。在一些实施方案中,Y3为=S。在一些实施方案中,Y3为=NH。在一些实施方案中,Y3为=NCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Y4为=O、=S、=NH或=NCH3。在一些实施方案中,Y4为=O。在一些实施方案中,Y4为=S。在一些实施方案中,Y4为=NH。在一些实施方案中,Y4为=NCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,Yn为=O、=S、=NH或=NCH3。在一些实施方案中,Yn为=O。在一些实施方案中,Yn为=S。在一些实施方案中,Yn为=NH。在一些实施方案中,Yn为=NCH3。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,A为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A为-O-。在一些实施方案中,A为-S-。在一些实施方案中,A为-CH2-。在一些实施方案中,A为-NH-。在一些实施方案中,A为-N(CH3)-。在一些实施方案中,A为-N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,A1为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A1为-O-。在一些实施方案中,A1为-S-。在一些实施方案中,A1为-CH2-。在一些实施方案中,A1为-NH-。在一些实施方案中,A1为-N(CH3)-。在一些实施方案中,A1为-N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,A2为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A2为-CH2-。在一些实施方案中,A2为-NH-。在一些实施方案中,A2为-N(CH3)-。在一些实施方案中,A2为-N(C(=O)CH3)-。
在基序(II’)、(II’-a)、(II’-b)、(II’-c)、(II’-d)、(II’-e)、(II’-f)、(II’-g)、(II’-h)、(II’-i)、(II’-j)、(II’-k)、(II’-l)、(II’-m)、(II’-n)、(II’-o)、(II’-p)、(II’-q)、(II’-r)、(II’-s)、(II’-t)或(II’-u)的化合物的一些实施方案中,p为0、1、2、3、4、5或6。在一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。在一些实施方案中,p为3。在一些实施方案中,p为4。在一些实施方案中,p为5。在一些实施方案中,p为6。
在一些实施方案中,Z1、Z2、Z3和Z4各自独立地为-OH或-OCH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中Z2为-OH。在一些实施方案中,Z1、Z2和Z4为-OH,并且Z3为-OCH3。在一些实施方案中,Z1和Z3为-OCH3,并且Z2和Z4为-OH。在一些实施方案中,Z’、Z”和Z”’为氢。
在一些实施方案中,Q1和Q4为-OCH2-。在一些实施方案中Q2和Q3为-O-。
在一些实施方案中,X1、X2、X3和X4为-O-。在一些实施方案中,X1、X2、X3和X4为-S-。在一些实施方案中,X1、X3、X4为-O-,并且X2为-S-。
在一些实施方案中,Y1、Y2、Y3和Y4为=O。在一些实施方案中,Y1、Y2、Y3和Y4为=S。在一些实施方案中,Y1、Y3和Y4为=O,并且Y2为=S。在一些实施方案中,Y1、Y2、Y3为=O,并且Y4为=S。
在一些实施方案中,A、A1和A2为-O-。
在一些实施方案中,p为0。
在一个方面,本文描述了一种mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,B1为 在一些实施方案中,B1为/>在一些实施方案中,B1为
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,B2独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B2为鸟嘌呤。在一些实施方案中,B2为胞嘧啶。在一些实施方案中,B2为尿嘧啶,在一些实施方案中,B2为胸腺嘧啶,在一些实施方案中,B2为次黄嘌呤。在一些实施方案中,B2为嘌呤。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,B3独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B3为腺嘌呤。在一些实施方案中,B3为鸟嘌呤。在一些实施方案中,B3为胞嘧啶。在一些实施方案中,B3为尿嘧啶,在一些实施方案中,B3为胸腺嘧啶,在一些实施方案中,B3为次黄嘌呤。在一些实施方案中,B3为嘌呤。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Bn独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,Bn为腺嘌呤。在一些实施方案中,Bn为鸟嘌呤。在一些实施方案中,Bn为胞嘧啶。在一些实施方案中,Bn为尿嘧啶,在一些实施方案中,Bn为胸腺嘧啶,在一些实施方案中,Bn为次黄嘌呤。在一些实施方案中,Bn为嘌呤。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z’为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z’为氢。在一些实施方案中,Z’为氟。在一些实施方案中,Z’为-OH。在一些实施方案中,Z’为-SH。在一些实施方案中,Z’为-CH3。在一些实施方案中,Z’为-CH2CH3。在一些实施方案中,Z’为-OCH3。在一些实施方案中,Z’为-NH(CH3),在一些实施方案中,Z’为-NH2-。在一些实施方案中,Z’为-NH(C(=O)CH3)。在一些实施方案中,Z’为-SCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z”为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z”为氢。在一些实施方案中,Z”为氟。在一些实施方案中,Z”为-OH。在一些实施方案中,Z”为-SH。在一些实施方案中,Z”为-CH3。在一些实施方案中,Z”为-CH2CH3。在一些实施方案中,Z”为-OCH3。在一些实施方案中,Z”为-NH(CH3),在一些实施方案中,Z”为-NH2-。在一些实施方案中,Z”为-NH(C(=O)CH3)。在一些实施方案中,Z”为-SCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3。在一些实施方案中,Z”’为氢。在一些实施方案中,Z”’为氟。在一些实施方案中,Z”’为-CH3。在一些实施方案中,Z”’为-CH2CH3。在一些实施方案中,Z”’为-OCH3。在一些实施方案中,Z”’为-OCH2CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z1为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z1为氢。在一些实施方案中,Z1为氟。在一些实施方案中,Z1为-OH。在一些实施方案中,Z1为-SH。在一些实施方案中,Z1为-CH3。在一些实施方案中,Z1为-CH2CH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中,Z1为-SCH3。在一些实施方案中,Z1为-OCH2CH3。在一些实施方案中,Z1为-NH2。在一些实施方案中,Z1为NHCH3。在一些实施方案中,Z1为NHC(=O)CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z2为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z2为氢。在一些实施方案中,Z2为氟。在一些实施方案中,Z2为-OH。在一些实施方案中,Z2为-SH。在一些实施方案中,Z2为-CH3。在一些实施方案中,Z2为-CH2CH3。在一些实施方案中,Z2为-OCH3。在一些实施方案中,Z2为-SCH3。在一些实施方案中,Z2为-OCH2CH3。在一些实施方案中,Z2为-NH2。在一些实施方案中,Z2为NHCH3。在一些实施方案中,Z2为NHC(=O)CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z3为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z3为氢。在一些实施方案中,Z3为氟。在一些实施方案中,Z3为-OH。在一些实施方案中,Z3为-CH3。在一些实施方案中,Z3为-CH2CH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z3为-NH2。在一些实施方案中,Z3为-NHCH3。在一些实施方案中,Z3为-NH(C(=O)CH3)。在一些实施方案中,Z3为-OCH2CH3。在一些实施方案中,Z3为-OCH2OCH3。在一些实施方案中,Z3为-OCH2CH2CH3。在一些实施方案中,Z3为-OCH(CH3)2。在一些实施方案中,Z3为-SCH3。在一些实施方案中,Z3为-OCH2CH2OCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Z4为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z4为氢。在一些实施方案中,Z4为氟。在一些实施方案中,Z4为-OH。在一些实施方案中,Z4为-CH3。在一些实施方案中,Z4为-CH2CH3。在一些实施方案中,Z4为-OCH3。在一些实施方案中,Z4为-NH2。在一些实施方案中,Z4为-NHCH3。在一些实施方案中,Z4为-NH(C(=O)CH3)。在一些实施方案中,Z4为-OCH2CH3。在一些实施方案中,Z4为-OCH2OCH3。在一些实施方案中,Z4为-OCH2CH2CH3。在一些实施方案中,Z4为-OCH(CH3)2。在一些实施方案中,Z4为-SCH3。在一些实施方案中,Z4为-OCH2CH2OCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Zn为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Zn为氢。在一些实施方案中,Zn为氟。在一些实施方案中,Zn为-OH。在一些实施方案中,Zn为-CH3。在一些实施方案中,Zn为-CH2CH3。在一些实施方案中,Zn为-OCH3。在一些实施方案中,Zn为-NH2。在一些实施方案中,Zn为-NHCH3。在一些实施方案中,Zn为-NH(C(=O)CH3)。在一些实施方案中,Zn为-OCH2CH3。在一些实施方案中,Zn为-OCH2OCH3。在一些实施方案中,Zn为-OCH2CH2CH3。在一些实施方案中,Zn为-OCH(CH3)2。在一些实施方案中,Zn为-SCH3。在一些实施方案中,Zn为-OCH2CH2OCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Q1为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q1为-CH2-。在一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q1为-CH2S-。在一些实施方案中,Q1为-CH2CH2-。在一些实施方案中,Q1为-CH2CF2-。在一些实施方案中,Q1为-CH2NH2-。在一些实施方案中,Q1为-CH2NH(CH3)-。在一些实施方案中,Q1为-CH2N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Q4为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q4为-CH2-。在一些实施方案中,Q4为-CH2O-。在一些实施方案中,Q4为-CH2S-。在一些实施方案中,Q4为-CH2CH2-。在一些实施方案中,Q4为-CH2CF2-。在一些实施方案中,Q4为-CH2NH2-。在一些实施方案中,Q4为-CH2NH(CH3)-。在一些实施方案中,Q4为-CH2N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Q2为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q2为-O-。在一些实施方案中Q2为-S-。在一些实施方案中Q2为-CH2-。在一些实施方案中Q2为-CF2-。在一些实施方案中Q2为-NH-。在一些实施方案中Q2为-N(CH3)-。在一些实施方案中Q2为-N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Q3为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q3为-O-。在一些实施方案中Q3为-S-。在一些实施方案中Q3为-CH2-。在一些实施方案中Q3为-CF2-。在一些实施方案中Q3为-NH-。在一些实施方案中Q3为-N(CH3)-。在一些实施方案中Q3为-N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,X1为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X1为-OH。在一些实施方案中,X1为-SH。在一些实施方案中,X1为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X1为-NH2。在一些实施方案中,X1为-NHCH3。在一些实施方案中,X1为-NH(C(=O)CH3)。在一些实施方案中,X1为-CH3。在一些实施方案中,X1为-CH2CH3。在一些实施方案中,X1为-CH2CH2CH3。在一些实施方案中,X1为-CH(CH3)2。在一些实施方案中,X1为-OCH3。在一些实施方案中,X1为-OCH2CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,X2为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X2为-OH。在一些实施方案中,X2为-SH。在一些实施方案中,X2为-O-。在一些实施方案中,X2为-S-。在一些实施方案中,X2为-NH2。在一些实施方案中,X2为-NHCH3。在一些实施方案中,X2为-NH(C(=O)CH3)。在一些实施方案中,X2为-CH3。在一些实施方案中,X2为-CH2CH3。在一些实施方案中,X2为-CH2CH2CH3。在一些实施方案中,X2为-CH(CH3)2。在一些实施方案中,X2为-OCH3。在一些实施方案中,X2为-OCH2CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,X3为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X3为-OH。在一些实施方案中,X3为-SH。在一些实施方案中,X3为-O-。在一些实施方案中,X3为-S-。在一些实施方案中,X3为-NH2。在一些实施方案中,X3为-NHCH3。在一些实施方案中,X3为-NH(C(=O)CH3)。在一些实施方案中,X3为-CH3。在一些实施方案中,X3为-CH2CH3。在一些实施方案中,X3为-CH2CH2CH3。在一些实施方案中,X3为-CH(CH3)2。在一些实施方案中,X3为-OCH3。在一些实施方案中,X3为-OCH2CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,X4为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X4为-OH。在一些实施方案中,X4为-SH。在一些实施方案中,X4为-O-。在一些实施方案中,X4为-S-。在一些实施方案中,X4为-NH2。在一些实施方案中,X4为-NHCH3。在一些实施方案中,X4为-NH(C(=O)CH3)。在一些实施方案中,X4为-CH3。在一些实施方案中,X4为-CH2CH3。在一些实施方案中,X4为-CH2CH2CH3。在一些实施方案中,X4为-CH(CH3)2。在一些实施方案中,X4为-OCH3。在一些实施方案中,X4为-OCH2CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Xn为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,Xn为-OH。在一些实施方案中,Xn为-SH。在一些实施方案中,Xn为-O-。在一些实施方案中,Xn为-S-。在一些实施方案中,Xn为-NH2。在一些实施方案中,Xn为-NHCH3。在一些实施方案中,Xn为-NH(C(=O)CH3)。在一些实施方案中,Xn为-CH3。在一些实施方案中,Xn为-CH2CH3。在一些实施方案中,Xn为-CH2CH2CH3。在一些实施方案中,Xn为-CH(CH3)2。在一些实施方案中,Xn为-OCH3。在一些实施方案中,Xn为-OCH2CH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Y1为=O、=S、=NH或=NCH3。在一些实施方案中,Y1为=O。在一些实施方案中,Y1为=S。在一些实施方案中,Y1为=NH。在一些实施方案中,Y1为=NCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Y2为=O、=S、=NH或=NCH3。在一些实施方案中,Y2为=O。在一些实施方案中,Y2为=S。在一些实施方案中,Y2为=NH。在一些实施方案中,Y2为=NCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Y3为=O、=S、=NH或=NCH3。在一些实施方案中,Y3为=O。在一些实施方案中,Y3为=S。在一些实施方案中,Y3为=NH。在一些实施方案中,Y3为=NCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Y4为=O、=S、=NH或=NCH3。在一些实施方案中,Y4为=O。在一些实施方案中,Y4为=S。在一些实施方案中,Y4为=NH。在一些实施方案中,Y4为=NCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,Yn为=O、=S、=NH或=NCH3。在一些实施方案中,Yn为=O。在一些实施方案中,Yn为=S。在一些实施方案中,Yn为=NH。在一些实施方案中,Yn为=NCH3。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,A为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A为-O-。在一些实施方案中,A为-S-。在一些实施方案中,A为-CH2-。在一些实施方案中,A为-NH-。在一些实施方案中,A为-N(CH3)-。在一些实施方案中,A为-N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,A1为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A1为-O-。在一些实施方案中,A1为-S-。在一些实施方案中,A1为-CH2-。在一些实施方案中,A1为-NH-。在一些实施方案中,A1为-N(CH3)-。在一些实施方案中,A1为-N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,A2为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A2为-CH2-。在一些实施方案中,A2为-NH-。在一些实施方案中,A2为-N(CH3)-。在一些实施方案中,A2为-N(C(=O)CH3)-。
在式(II)、(II-a’)、(II-b’)、(II-c’)、(II-d’)、(II-e’)、(II-f’)、(II-g’)、(II-h’)、(II-i’)、(II-j’)、(II-k’)、(II-l’)、(II-m’)、(II-n’)、(II-o’)、(II-p’)、(II-q’)、(II-r’)、(II-s’)、(II-t’)或(II-u’)的化合物的一些实施方案中,p为0、1、2、3、4、5或6。在一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。在一些实施方案中,p为3。在一些实施方案中,p为4。在一些实施方案中,p为5。在一些实施方案中,p为6。
在一些实施方案中,Z1、Z2、Z3和Z4各自独立地为-OH或-OCH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中Z2为-OH。在一些实施方案中,Z1、Z2和Z4为-OH,并且Z3为-OCH3。在一些实施方案中,Z1和Z3为-OCH3,并且Z2和Z4为-OH。在一些实施方案中,Z’、Z”和Z”’为氢。
在一些实施方案中,Q1和Q4为-OCH2-。在一些实施方案中Q2和Q3为-O-。
在一些实施方案中,X1、X2、X3和X4为-O-。在一些实施方案中,X1、X2、X3和X4为-S-。在一些实施方案中,X1、X3、X4为-O-,并且X2为-S-。
在一些实施方案中,Y1、Y2、Y3和Y4为=O。在一些实施方案中,Y1、Y2、Y3和Y4为=S。在一些实施方案中,Y1、Y3和Y4为=O,并且Y2为=S。在一些实施方案中,Y1、Y2、Y3为=O,并且Y4为=S。
在一些实施方案中,A、A1和A2为-O-。
在一些实施方案中,p为0。
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-a)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-a’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-b)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-b’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-c)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-c’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-d)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-d’)
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-e)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-e’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-f)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-g)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-g’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-h)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-h’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-i)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-I’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-j)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-j’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-k)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-k’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-l)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-l’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-m)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-m’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-n)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-n’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-o)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-o’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-p)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-p’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-q)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-q’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-r)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-r’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-s)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-s’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-t)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-t’)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-u)的结构:
在一些实施方案中,所述IVT mRNA序列起始子具有式(II-u’)的结构:
在式(II)或式(II-a)至(II-u’)的一些实施方案中,每个B独立地为天然的核碱基。在式(II)或式(II-a)至(II-u’)的一些实施方案中,每个B独立地为经修饰的核碱基。在式(II)或式(II-a)至(II-u’)的一些实施方案中,每个B独立地为非天然的核碱基。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Z1为氟。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Z1为-OH。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Z1为-OCH3。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Z2为氟。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Z2为-OH。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Z2为-OCH3。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q1为-CH2O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q1为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q4为-CH2O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q4为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q2为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q3为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y1为=O。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y3为=O。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y2为=O。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y4为=O。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Yn为=O。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y1、Y2、Y3、Y4和Yn中的一个或多个为=S。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y2为=S。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y4为=S。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Yn为=S。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Y1、Y2、Y3、Y4和Yn各自为=O。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X1、X4和Xn各自为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X2为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X3为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X1、X2、X3、X4和Xn中的一个或多个为-S-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X2为-S-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X4为-S-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X3为-S-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,X1、X2、X3、X4和Xn各自为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,A、A1和A2各自为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,A、A1和A2中的一个或多个为-S-。在一些实施方案中,A为-S-。在一些实施方案中,A1为-O-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A为-O-。在一些实施方案中,A1为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,B2为腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、胸腺嘧啶、次黄嘌呤或嘌呤。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,B3为腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、胸腺嘧啶、次黄嘌呤或嘌呤。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Bn为腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、胸腺嘧啶、次黄嘌呤或嘌呤。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q4为-CH2O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q2为-O-。在一些实施方案中,Q3为-O-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,每个Xn独立地为-OH、-SH、O-或S-。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,每个Yn独立地为=O或=S。
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q1为-CH2O-;Q4为-CH2O-;Q2为-O-;Q3为-O-;每个Xn独立地为-OH、-SH、O-或S-;每个Yn独立地为=O或=S;B1为
在式(II)或式(II-a)至(II-u’)的一些实施方案中,Q1为-CH2O-;Q4为-CH2O-;Q2为-O-;Q3为-O-,每个Xn独立地为-OH、-SH、O-或S-;每个Yn独立地为=O或=S;B1为/>
在式(II)或式(II-a)至(II-u’)的一些实施方案中,B2为腺嘌呤。在式(II)或式(II-a)至(II-u’)的一些实施方案中,B3为鸟嘌呤。
在一个方面,本文描述了一种具有5’端区域基序(基序(II”))的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,B1为在一些实施方案中,B1为/>在一些实施方案中,B1为/>
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,B2独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B2为腺嘌呤。在一些实施方案中,B2为鸟嘌呤。在一些实施方案中,B2为胞嘧啶。在一些实施方案中,B2为尿嘧啶,在一些实施方案中,B2为胸腺嘧啶,在一些实施方案中,B2为次黄嘌呤。在一些实施方案中,B2为嘌呤。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,B3独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,B3为腺嘌呤。在一些实施方案中,B3为鸟嘌呤。在一些实施方案中,B3为胞嘧啶。在一些实施方案中,B3为尿嘧啶,在一些实施方案中,B3为胸腺嘧啶,在一些实施方案中,B3为次黄嘌呤。在一些实施方案中,B3为嘌呤。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Bn独立地为天然的、经修饰的或非天然的核碱基。在一些实施方案中,Bn为腺嘌呤。在一些实施方案中,Bn为鸟嘌呤。在一些实施方案中,Bn为胞嘧啶。在一些实施方案中,Bn为尿嘧啶,在一些实施方案中,Bn为胸腺嘧啶,在一些实施方案中,Bn为次黄嘌呤。在一些实施方案中,Bn为嘌呤。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z’为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z’为氢。在一些实施方案中,Z’为氟。在一些实施方案中,Z’为-OH。在一些实施方案中,Z’为-SH。在一些实施方案中,Z’为-CH3。在一些实施方案中,Z’为-CH2CH3。在一些实施方案中,Z’为-OCH3。在一些实施方案中,Z’为-NH(CH3),在一些实施方案中,Z’为-NH2-。在一些实施方案中,Z’为-NH(C(=O)CH3)。在一些实施方案中,Z’为-SCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z”为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3。在一些实施方案中,Z”为氢。在一些实施方案中,Z”为氟。在一些实施方案中,Z”为-OH。在一些实施方案中,Z”为-SH。在一些实施方案中,Z”为-CH3。在一些实施方案中,Z”为-CH2CH3。在一些实施方案中,Z”为-OCH3。在一些实施方案中,Z”为-NH(CH3),在一些实施方案中,Z”为-NH2-。在一些实施方案中,Z”为-NH(C(=O)CH3)。在一些实施方案中,Z”为-SCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3。在一些实施方案中,Z”’为氢。在一些实施方案中,Z”’为氟。在一些实施方案中,Z”’为-CH3。在一些实施方案中,Z”’为-CH2CH3。在一些实施方案中,Z”’为-OCH3。在一些实施方案中,Z”’为-OCH2CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z1为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z1为氢。在一些实施方案中,Z1为氟。在一些实施方案中,Z1为-OH。在一些实施方案中,Z1为-SH。在一些实施方案中,Z1为-CH3。在一些实施方案中,Z1为-CH2CH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中,Z1为-SCH3。在一些实施方案中,Z1为-OCH2CH3。在一些实施方案中,Z1为-NH2。在一些实施方案中,Z1为NHCH3。在一些实施方案中,Z1为NHC(=O)CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z2为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3。在一些实施方案中,Z2为氢。在一些实施方案中,Z2为氟。在一些实施方案中,Z2为-OH。在一些实施方案中,Z2为-SH。在一些实施方案中,Z2为-CH3。在一些实施方案中,Z2为-CH2CH3。在一些实施方案中,Z2为-OCH3。在一些实施方案中,Z2为-SCH3。在一些实施方案中,Z2为-OCH2CH3。在一些实施方案中,Z2为-NH2。在一些实施方案中,Z2为NHCH3。在一些实施方案中,Z2为NHC(=O)CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z3为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z3为氢。在一些实施方案中,Z3为氟。在一些实施方案中,Z3为-OH。在一些实施方案中,Z3为-CH3。在一些实施方案中,Z3为-CH2CH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z3为-NH2。在一些实施方案中,Z3为-NHCH3。在一些实施方案中,Z3为-NH(C(=O)CH3)。在一些实施方案中,Z3为-OCH2CH3。在一些实施方案中,Z3为-OCH2OCH3。在一些实施方案中,Z3为-OCH2CH2CH3。在一些实施方案中,Z3为-OCH(CH3)2。在一些实施方案中,Z3为-SCH3。在一些实施方案中,Z3为-OCH2CH2OCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Z4为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Z4为氢。在一些实施方案中,Z4为氟。在一些实施方案中,Z4为-OH。在一些实施方案中,Z4为-CH3。在一些实施方案中,Z4为-CH2CH3。在一些实施方案中,Z4为-OCH3。在一些实施方案中,Z4为-NH2。在一些实施方案中,Z4为-NHCH3。在一些实施方案中,Z4为-NH(C(=O)CH3)。在一些实施方案中,Z4为-OCH2CH3。在一些实施方案中,Z4为-OCH2OCH3。在一些实施方案中,Z4为-OCH2CH2CH3。在一些实施方案中,Z4为-OCH(CH3)2。在一些实施方案中,Z4为-SCH3。在一些实施方案中,Z4为-OCH2CH2OCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Zn为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3。在一些实施方案中,Zn为氢。在一些实施方案中,Zn为氟。在一些实施方案中,Zn为-OH。在一些实施方案中,Zn为-CH3。在一些实施方案中,Zn为-CH2CH3。在一些实施方案中,Zn为-OCH3。在一些实施方案中,Zn为-NH2。在一些实施方案中,Zn为-NHCH3。在一些实施方案中,Zn为-NH(C(=O)CH3)。在一些实施方案中,Zn为-OCH2CH3。在一些实施方案中,Zn为-OCH2OCH3。在一些实施方案中,Zn为-OCH2CH2CH3。在一些实施方案中,Zn为-OCH(CH3)2。在一些实施方案中,Zn为-SCH3。在一些实施方案中,Zn为-OCH2CH2OCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Q1为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q1为-CH2-。在一些实施方案中,Q1为-CH2O-。在一些实施方案中,Q1为-CH2S-。在一些实施方案中,Q1为-CH2CH2-。在一些实施方案中,Q1为-CH2CF2-。在一些实施方案中,Q1为-CH2NH2-。在一些实施方案中,Q1为-CH2NH(CH3)-。在一些实施方案中,Q1为-CH2N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Q4为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-。在一些实施方案中,Q1为-CH=CH-。在一些实施方案中,Q4为-CH2-。在一些实施方案中,Q4为-CH2O-。在一些实施方案中,Q4为-CH2S-。在一些实施方案中,Q4为-CH2CH2-。在一些实施方案中,Q4为-CH2CF2-。在一些实施方案中,Q4为-CH2NH2-。在一些实施方案中,Q4为-CH2NH(CH3)-。在一些实施方案中,Q4为-CH2N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Q2为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q2为-O-。在一些实施方案中Q2为-S-。在一些实施方案中Q2为-CH2-。在一些实施方案中Q2为-CF2-。在一些实施方案中Q2为-NH-。在一些实施方案中Q2为-N(CH3)-。在一些实施方案中Q2为-N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Q3为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中Q3为-O-。在一些实施方案中Q3为-S-。在一些实施方案中Q3为-CH2-。在一些实施方案中Q3为-CF2-。在一些实施方案中Q3为-NH-。在一些实施方案中Q3为-N(CH3)-。在一些实施方案中Q3为-N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,X1为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X1为-OH。在一些实施方案中,X1为-SH。在一些实施方案中,X1为-O-。在一些实施方案中,X1为-S-。在一些实施方案中,X1为-NH2。在一些实施方案中,X1为-NHCH3。在一些实施方案中,X1为-NH(C(=O)CH3)。在一些实施方案中,X1为-CH3。在一些实施方案中,X1为-CH2CH3。在一些实施方案中,X1为-CH2CH2CH3。在一些实施方案中,X1为-CH(CH3)2。在一些实施方案中,X1为-OCH3。在一些实施方案中,X1为-OCH2CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,X2为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X2为-OH。在一些实施方案中,X2为-SH。在一些实施方案中,X2为-O-。在一些实施方案中,X2为-S-。在一些实施方案中,X2为-NH2。在一些实施方案中,X2为-NHCH3。在一些实施方案中,X2为-NH(C(=O)CH3)。在一些实施方案中,X2为-CH3。在一些实施方案中,X2为-CH2CH3。在一些实施方案中,X2为-CH2CH2CH3。在一些实施方案中,X2为-CH(CH3)2。在一些实施方案中,X2为-OCH3。在一些实施方案中,X2为-OCH2CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,X3为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X3为-OH。在一些实施方案中,X3为-SH。在一些实施方案中,X3为-O-。在一些实施方案中,X3为-S-。在一些实施方案中,X3为-NH2。在一些实施方案中,X3为-NHCH3。在一些实施方案中,X3为-NH(C(=O)CH3)。在一些实施方案中,X3为-CH3。在一些实施方案中,X3为-CH2CH3。在一些实施方案中,X3为-CH2CH2CH3。在一些实施方案中,X3为-CH(CH3)2。在一些实施方案中,X3为-OCH3。在一些实施方案中,X3为-OCH2CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,X4为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,X4为-OH。在一些实施方案中,X4为-SH。在一些实施方案中,X4为-O-。在一些实施方案中,X4为-S-。在一些实施方案中,X4为-NH2。在一些实施方案中,X4为-NHCH3。在一些实施方案中,X4为-NH(C(=O)CH3)。在一些实施方案中,X4为-CH3。在一些实施方案中,X4为-CH2CH3。在一些实施方案中,X4为-CH2CH2CH3。
在一些实施方案中,X4为-CH(CH3)2。在一些实施方案中,X4为-OCH3。
在一些实施方案中,X4为-OCH2CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Xn为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3。在一些实施方案中,Xn为-OH。在一些实施方案中,Xn为-SH。在一些实施方案中,Xn为-O-。在一些实施方案中,Xn为-S-。在一些实施方案中,Xn为-NH2。在一些实施方案中,Xn为-NHCH3。在一些实施方案中,Xn为-NH(C(=O)CH3)。在一些实施方案中,Xn为-CH3。在一些实施方案中,Xn为-CH2CH3。在一些实施方案中,Xn为-CH2CH2CH3。
在一些实施方案中,Xn为-CH(CH3)2。在一些实施方案中,Xn为-OCH3。
在一些实施方案中,Xn为-OCH2CH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Y1为=O、=S、=NH或=NCH3。在一些实施方案中,Y1为=O。在一些实施方案中,Y1为=S。在一些实施方案中,Y1为=NH。在一些实施方案中,Y1为=NCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Y2为=O、=S、=NH或=NCH3。在一些实施方案中,Y2为=O。在一些实施方案中,Y2为=S。在一些实施方案中,Y2为=NH。在一些实施方案中,Y2为=NCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Y3为=O、=S、=NH或=NCH3。在一些实施方案中,Y3为=O。在一些实施方案中,Y3为=S。在一些实施方案中,Y3为=NH。在一些实施方案中,Y3为=NCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Y4为=O、=S、=NH或=NCH3。在一些实施方案中,Y4为=O。在一些实施方案中,Y4为=S。在一些实施方案中,Y4为=NH。在一些实施方案中,Y4为=NCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,Yn为=O、=S、=NH或=NCH3。在一些实施方案中,Yn为=O。在一些实施方案中,Yn为=S。在一些实施方案中,Yn为=NH。在一些实施方案中,Yn为=NCH3。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,A为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A为-O-。在一些实施方案中,A为-S-。在一些实施方案中,A为-CH2-。在一些实施方案中,A为-NH-。在一些实施方案中,A为-N(CH3)-。在一些实施方案中,A为-N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,A1为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A1为-O-。在一些实施方案中,A1为-S-。在一些实施方案中,A1为-CH2-。在一些实施方案中,A1为-NH-。在一些实施方案中,A1为-N(CH3)-。在一些实施方案中,A1为-N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,A2为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-。在一些实施方案中,A2为-O-。在一些实施方案中,A2为-S-。在一些实施方案中,A2为-CH2-。在一些实施方案中,A2为-NH-。在一些实施方案中,A2为-N(CH3)-。在一些实施方案中,A2为-N(C(=O)CH3)-。
在基序(II”)、(II”-a’)、(II”-b’)、(II”-c’)、(II”-d’)、(II”-e’)、(II”-f’)、(II”-g’)、(II”-h’)、(II”-i’)、(II”-j’)、(II”-k’)、(II”-l’)、(II”-m’)、(II”-n’)、(II”-o’)、(II”-p’)、(II”-q’)、(II”-r’)、(II”-s’)、(II”-t’)或(II”-u’)的化合物的一些实施方案中,p为0、1、2、3、4、5或6。在一些实施方案中,p为0。在一些实施方案中,p为1。在一些实施方案中,p为2。在一些实施方案中,p为3。在一些实施方案中,p为4。在一些实施方案中,p为5。在一些实施方案中,p为6。
在一些实施方案中,Z1、Z2、Z3和Z4各自独立地为-OH或-OCH3。在一些实施方案中,Z3为-OCH3。在一些实施方案中,Z1为-OCH3。在一些实施方案中Z2为-OH。在一些实施方案中,Z1、Z2和Z4为-OH,并且Z3为-OCH3。在一些实施方案中,Z1和Z3为-OCH3,并且Z2和Z4为-OH。在一些实施方案中,Z’、Z”和Z”’为氢。
在一些实施方案中,Q1和Q4为-OCH2-。在一些实施方案中Q2和Q3为-O-。
在一些实施方案中,X1、X2、X3和X4为-O-。在一些实施方案中,X1、X2、X3和X4为-S-。在一些实施方案中,X1、X3、X4为-O-,并且X2为-S-。
在一些实施方案中,Y1、Y2、Y3和Y4为=O。在一些实施方案中,Y1、Y2、Y3和Y4为=S。在一些实施方案中,Y1、Y3和Y4为=O,并且Y2为=S。在一些实施方案中,Y1、Y2、Y3为=O,并且Y4为=S。
在一些实施方案中,A、A1和A2为-O-。
在一些实施方案中,p为0。
在某些实施方案中,序列起始子化合物如表1中所述。
表1
在一些实施方案中,本文公开了一种包含一种或多种mRNA的药学上可接受的盐或药学上可接受的溶剂化物或药物组合物,所述mRNA由选自表1的一种或多种序列起始子化合物产生/制造,其中所述mRNA编码一种或多种药学活性蛋白质。
在某些实施方案中,序列起始子化合物如表2中所述。
表2
在一些实施方案中,本文公开了一种包含一种或多种mRNA的药学上可接受的盐或药学上可接受的溶剂化物或药物组合物,所述mRNA由选自表2的一种或多种序列起始子化合物产生/制造,其中所述mRNA编码一种或多种药学活性蛋白质。
在某些实施方案中,序列起始子化合物如表3中所述。
表3
在一些实施方案中,本文公开了一种包含一种或多种mRNA的药学上可接受的盐或药学上可接受的溶剂化物或药物组合物,所述mRNA由选自表3的一种或多种序列起始子化合物产生/制造。
在另一方面,本文描述了一种包含IVT mRNA序列起始子和DNA模板的复合物,其中所述IVT mRNA序列起始子包括本文所述的化合物,其中(a)所述DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸、在核苷酸位置+2处的第二核苷酸和在核苷酸位置+3处的第三核苷酸;并且(b)其中IVTmRNA序列起始子至少在核苷酸位置+1、+2和+3处与DNA模板杂交。
在另一方面,本文描述了一种包含IVT mRNA序列起始子和DNA模板的复合物,其中所述IVT mRNA序列起始子包括本文所述的化合物,其中(a)所述DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸和在核苷酸位置+2处的第二核苷酸;并且(b)其中IVT mRNA序列起始子至少在核苷酸位置+1和+2处与DNA模板杂交。
药物组合物
在一些实施方案中,本文所述的化合物被配制成药物组合物。使用一种或多种药学上可接受的非活性成分以常规方式配制药物组合物,所述非活性成分有助于将活性化合物加工成药学上可以使用的制剂。合适的制剂取决于所选择的施用途径。本文所述药物组合物的概述可以在例如Remington:The Science and Practice of Pharmacy,第十九版(伊斯顿,宾夕法尼亚州:马克出版公司(Mack Publishing Company),1995);Hoover,JohnE.,Remington’s Pharmaceutical Sciences,马克出版公司,伊斯顿,宾夕法尼亚州1975;Liberman,H.A.和Lachman,L.编著,Pharmaceutical Dosage Forms,Marcel Decker,纽约,纽约州,1980;和Pharmaceutical Dosage Forms and Drug Delivery Systems,第七版(利平科特·威廉姆斯和威尔金斯出版社(Lippincott Williams&Wilkins)1999)中找到,此类公开通过引用并入本文。
药物组合物可以是本文所述的序列起始子化合物与一种或多种其他化学组分(即,药学上可接受的成分)的混合物,所述化学组分为如载剂、赋形剂、粘合剂、填充剂、悬浮剂、调味剂、甜味剂、崩解剂、分散剂、表面活性剂、润滑剂、着色剂、稀释剂、增溶剂、润湿剂、增塑剂、稳定剂、渗透增强剂、润湿剂、消泡剂、抗氧化剂、防腐剂或其一种或多种组合。该药物组合物有助于将该化合物施用于生物体。
本文所述的组合物可以以多种方式施用于对象,包括肠胃外、静脉内、皮内、肌内、结肠、直肠或腹膜内施用。在一些实施方案中,本文所述的序列起始子化合物或其药学上可接受的盐通过对象的腹膜内注射、肌内注射、皮下注射或静脉内注射施用。在一些实施方案中,药物组合物可以肠胃外、静脉内、肌内或口服施用。包含本文所述的序列起始子化合物的口服药剂可以是任何用于口服施用的合适的形式,如液体、片剂、胶囊等。口服制剂还可以被包衣或处理以防止或减少在胃中的溶解。本公开的组合物可以使用本领域已知的任何合适的方法施用于对象。用于本公开的合适的制剂和递送方法通常是本领域众所周知的。例如,本文所述的序列起始子化合物可以与药学上可接受的稀释剂、载剂或赋形剂一起配制成药物组合物。所述组合物可以含有接近生理条件所需的药学上可接受的辅助物质,包括pH调节剂和缓冲剂、张力调节剂、湿润剂等,如例如乙酸钠、乳酸钠、氯化钠、氯化钾、氯化钙、失水山梨醇单月桂酸酯、三乙醇胺油酸酯等。
本文所述的药物制剂可以通过多种施用途径以多种方式施用于对象,包括但不限于口服、肠胃外(例如,静脉内、皮下、肌内、髓内注射、鞘内、直接心室内、腹膜内、淋巴管内、鼻内注射)、鼻内、颊、局部或经皮施用途径。本文所述的药物制剂包括但不限于水性液体分散体、自乳化分散体、固体溶液、脂质体分散体、气雾剂、固体剂型、粉末、速释制剂、控释制剂、速熔(fast melt)制剂、片剂、胶囊、丸剂、延迟释放制剂、延长释放制剂、脉冲释放制剂、多颗粒制剂以及混合的速释制剂和控释制剂。
在一些实施方案中,药物制剂是片剂的形式。在其他实施方案中,含有本文所述的序列起始子化合物的药物制剂为胶囊形式。在一个方面,用于口服施用的液体制剂剂型是水性悬浮液或溶液的形式,所述水性悬浮液或溶液选自但不限于水性口服分散体、乳液、溶液、酏剂、凝胶和糖浆。
对于通过吸入施用,本文所述的序列起始子化合物可以被配制成用作气雾剂、雾剂或粉剂。对于颊施用或舌下施用,组合物可以采用以常规方式配制的片剂、锭剂或凝胶的形式。在一些实施方案中,本文所述的序列起始子化合物可以制备成经皮剂型。在一些实施方案中,可以将本文所述的序列起始子化合物配制成适于肌内、皮下或静脉注射的药物组合物。在一些实施方案中,本文所述的序列起始子化合物可以局部施用,并且可以配制成多种可局部施用的组合物,如溶液、悬浮液、洗液、凝胶、糊剂、含药棒、香膏、乳膏或软膏。在一些实施方案中,本文所述的序列起始子化合物可以配制在直肠组合物如灌肠剂、直肠凝胶、直肠泡沫、直肠气雾剂、栓剂、胶冻栓剂或保留灌肠剂中。
在一个方面,本文描述了一种包含RNA分子和一种或多种药学上可接受的赋形剂的药物组合物,所述RNA分子包括本文公开的IVT mRNA序列起始子。在一些实施方案中,所述药物组合物包括脂质纳米颗粒。在一些实施方案中,RNA被包封在脂质纳米颗粒中。
转录
在真核生物中,信使RNA(mRNA)的转录由RNA聚合酶II完成。这是一种具有复杂调节的复杂的多亚基酶。为了在体外进行大规模转录,研究通常使用来自T7、T3、SP6、K1-5、K1E、K1F或K11噬菌体的单亚基噬菌体聚合酶。该聚合酶家族具有简单的、最小的约17个核苷酸的启动子序列,其不需要辅助蛋白,并且对起始核苷酸序列具有最小的限制。虽然本申请集中于T7 RNA聚合酶(T7 RNAP),但是本领域技术人员将理解本公开可以用其他RNA聚合酶来实施。
T7 RNAP以至少两种蛋白质状态存在。第一种被称为“无效复合物(abortivecomplex)”并且与转录起始有关。第二种是非常渐进的构象,被称为“延伸复合物”。体外转录可以分为六个步骤:1)RNA聚合酶与启动子序列的结合,2)转录的起始,3)被称为无效转录的非进行性延伸,在此期间聚合酶经常释放DNA模板和短无效转录物,4)开放复合物转化为封闭的复合物,5)进行性延伸和6)转录终止。在转录期间产生的大量RNA由长度为约2-8个核苷酸的短的无效片段组成(Biochemistry19:3245-3253(1980);Nucleic AcidsRes.9:31-45(1981);Nucleic Acids Res.15:8783-8798(1987);Biochemistry 27:3966-3974(1988))。在合成约10-14个碱基之后,RNA聚合酶从无效循环中逃脱,同时失去与启动子DNA的序列特异性接触,并形成进行性延伸复合物,其中RNA链以非序列依赖性的方式延伸(J.Mol.Biol.183:165-177(1985);Proc.Natl.Acad.Sci.U.S.A.83:3614-3618(1986);Mol.Cell Biol.7:3371-3379(1987))。
最具活性的III类T7启动子的共有序列涵盖转录起始位点上游的17bp序列和下游的6bp序列(Cell 16:815-25.(1979))。第一转录核苷酸的位置通常被称为RNA的+1转录物核苷酸,第二转录核苷酸被称为+2转录物核苷酸,依此类推(表2)。在转录期间,两条链解链以形成转录泡,并且双链体的底部链(表4中3’至5’所示)是用于转录的模板。对于转录物核苷酸+3及以上,模板链主要通过Watson-Crick碱基配对相互作用来限定转录核苷酸的特性。此处,编码第一RNA转录物核苷酸的核苷酸被定义为模板的+1核苷酸。在表4所示的实例中,+1转录物核苷酸是G,并且+1模板核苷酸是C。同样地,+4转录物核苷酸是A,并且+4模板核苷酸是T。
表4
与DNA聚合酶不同,T7 RNAP在没有引物的情况下启动RNA合成。启动的第一步被称为从头RNA合成,其中RNA聚合酶识别DNA模板上的特定序列,选择与位置+1和+2处的模板残基互补的第一对核苷酸三磷酸,并催化磷酸二酯键的形成以形成二核苷酸。起始核苷酸对聚合酶的亲和力低于在延伸期间使用的那些核苷酸。对于第一次引发NTP,Kd值为2mM,并且对于第二次引发NTP,Kd值为80μM,而对于在延伸期间的NTP,Kd为约5μM(J.Mol.Biol.(2007)370,256-268)。已经发现从头合成是转录期间的限速步骤。T7 RNAP表现出对GTP作为起始核苷酸的强烈偏见(J.Biol.Chem.248:2235-2244(1973))。在基因组中的17个T7启动子中,15个由GTP起始(并且13个由ppGpG起始),而在转录延伸期间没有明显的NTP偏好性(J.Mol.Biol.370:256-268(2007))。T7RNA聚合酶在位置+1处编码A的启动子上启动不良;而是,转录主要由位置+2处编码的G启动(J.Biol.Chem.278:2819-2823(2003))。
在从头RNA合成期间,起始核苷酸的结合主要是通过由碱基堆积、聚合酶残基之间的特异性相互作用、起始核苷酸的鸟嘌呤部分和碱基互补性相互作用产生的自由能实现的(J.Mol.Biol.370:256-268(2007))。
已知T7 RNAP也可以由短寡核苷酸引物起始。例如,已知T7基因组中的13个启动子由pppGpG起始(J.Mol.Biol.370:256-268(2007))。几组研究表明,T7 RNAP可以从二核苷酸引物起始(Biochemistry24:5716-5723(1985))。Axelrod等人表明,未加帽的GpA二核苷酸可以分别从+1和+2模板核苷酸(分别为2’-脱氧胞苷和2’-脱氧胸苷)(“CT”模板)起始。其反应条件为200微摩尔(μM)二聚体和100μM的ATP、CTP、GTP和UTP。它们的反应混合物还含有100μM的3’dATP、3’dCTP、3’dUTP或50μM的3’dGTP。他们仅观察到GpA起始的RNA,并且未观察到GpA起始的RNA和来自GTP起始的5’-三磷酸RNA的混合物。这可能是由于所采用的反应条件。100μM的GTP远远低于第一起始鸟苷的T7聚合酶的2mM Kd(J.Mol.Biol.(2007)370,256-268)。由于GTP与起始寡核苷酸竞争起始,使用低GTP浓度有利于GpA起始,但导致低转录产率(估计最大计算产率为<150ug/mL反应)。当使用ApG、CpG、UpG或GpG在“CT”模板上启动转录时,他们观察到形成了含有额外的未模板化的5’核苷酸(分别为A、C、U或G)的RNA转录物。
本文提供的用于制备5’-加帽RNA的方法和组合物包括但不限于mRNA、小核RNA(snRNA)、小核仁RNA(snoRNA)、小cajal体特异性RNA(scaRNA)。这些方法涉及使用mRNA序列起始子,例如含有帽的寡核苷酸引物,以及核苷5’-三磷酸(NTP)和RNA聚合酶,用于DNA模板化的和启动子控制的RNA合成。在某些方面,所述方法使用起始加帽寡核苷酸引物,所述引物在RNA合成,特别是加帽mRNA的合成中提供效用。示例性的起始寡核苷酸引物具有类似于天然RNA分子的帽0、帽1、帽2或TMG-帽的结构,其在RNA的倒数第二个帽1位置处和在RNA的倒数第二个帽2 5’位置附近包含2’-O-甲基化核苷单元。天然的帽0结构不具有2’-O-甲基化核苷单元。
用于制备RNA的方法和组合物包括但不限于mRNA、snRNA、snoRNA、scaRNA、转移RNA(tRNA)、核糖体RNA(rRNA)和转移信使RNA(tmRNA),其在分子的5’端处或其附近携带修饰。这些方法涉及使用起始子,例如有或没有帽的起始寡核苷酸引物、核苷5’-三磷酸(NTP)和RNA聚合酶,用于DNA模板化的和启动子控制的RNA合成。在某些方面,所述方法使用携带结构修饰的经修饰的起始寡核苷酸引物,所述结构修饰在RNA合成中提供效用;特别是在5’-修饰的RNA合成中提供效用。
示例性的起始加帽寡核苷酸引物具有开放的3’-OH基团,其允许通过向引物的3’端添加核苷酸单元来起始RNA聚合酶介导的在DNA模板上的RNA合成。起始加帽寡核苷酸引物在转录起始位点处与模板DNA序列基本上互补(即起始位点位于启动子序列的3’端附近,并且可以与启动子序列重叠)。在某些实施方案中,起始加帽寡核苷酸引物主要从引物的3’端开始在一个方向(“正向”)上引导RNA的合成。在某些方面和实施方案中,起始加帽寡核苷酸引物优于任何核苷5’-三磷酸以用于起始RNA合成,从而最大化以起始加帽寡核苷酸引物开始的RNA的产生,并最小化以5’-三磷酸核苷(通常为GTP)开始的RNA的产生。
通过体外转录制造mRNA利用高度活性的噬菌体RNA聚合酶(T3、T7、SP6以及其他)。RNA聚合酶在特定启动子的控制下工作,该启动子被整合到模板核苷酸序列前面的DNA质粒构建体中。转录过程通常从嘌呤核苷5’-三磷酸(通常为GTP)开始,并且继续直到RNA聚合酶遇到终止序列或完成DNA模板。
如上所述,含有帽0的mCAP二核苷酸类似物7mG(5’)ppp(5’)N已经用于启动体外转录(例如RNA 1:957-967(1995))。使用这些二核苷酸类似物产生的加帽RNA分子含有帽0。然而,仅约50%的合成的加帽RNA分子具有帽0的正确“正向”取向。为了将具有帽0的RNA转化为具有帽1的RNA,必须使用(核苷-2’-O)甲基转移酶进行额外的酶促反应。然而,这种转化可能不是定量的;不易控制且难以将剩余的帽0RNA与帽1RNA分离。此外,来自NTP(特别是GTP)的对起始转录的竞争还减少了产生的活性加帽RNA分子的数量。
此外,经修饰的二核苷酸类似物如7mG3’Ome(5’)ppp(5’)N和其他相关的ARCA类似物,其携带经修饰的7mG残基,在核糖上具有封闭的3’和/或2’位置,已被用于启动体外转录(例如,RNA 7:1486-1495(2001))。这些ARCA帽类似物仅在“正向”方向引导RNA合成,因此产生在5’端上具有(天然)帽0的RNA分子(对7mG残基具有2’和/或3’修饰)。与使用标准二核苷酸类似物7mG(5’)ppp(5’)N制备的RNA相比,此类RNA在翻译系统中更为活跃。为了将具有ARCA帽0的RNA转化为具有ARCA帽1的RNA,必须使用(核苷-2’-O)甲基转移酶进行额外的酶促反应,类似于前面讨论的二核苷酸类似物所需的酶促反应。该方法与针对mCAP二核苷酸类似物阐述的方法具有相同的缺点;将具有帽0的RNA转化为具有ARCA帽1的RNA可能不是定量的;该反应不易控制,难以将剩余的帽0RNA与帽1RNA分离,并且来自NTP(特别是GTP)的对转录起始的竞争还减少了产生的活性加帽RNA分子的数量。
带有3’端鸟苷残基的短寡核苷酸引物(2至6聚体)已经用于体外转录的启动(Pitulle,C.等人,Gene,112:101-105(1992))。这些寡核苷酸引物含有经修饰的和未修饰的核糖核苷残基(例如,经修饰的核糖核苷残基包括2’-O-甲基化核苷残基和2’-脱氧核糖核苷残基)。与GTP相比,较短的寡核苷酸引物(二聚体至四聚体)在启动转录方面基本上胜过GTP,而较长的引物(五聚体至六聚体)在启动转录方面效率低得多。这可能是因为这些较长的引物(如它们所设计的)在起始位点与DNA模板具有较低百分比的互补性。相反,二聚体AG(如所设计的)在起始位点与DNA模板互补。使用本节讨论的寡核苷酸引物产生的RNA分子具有内部2’-O-甲基化核苷,但不含5’-帽0、帽1、帽2或TMG-帽。为了将不含帽结构的RNA转化为具有帽1、帽2或TMG-帽结构的RNA,必须使用加帽酶进行额外的酶促反应。然而,这种转化具有与上述相同的缺点。
其他含有帽结构和内部2’-O-甲基化核苷残基的短RNA寡核苷酸已经化学制备(Ohkubo等人,Org.Letters 15:4386-4389(2013))。使用T4 DNA连接酶和互补DNA碎片寡核苷酸,将这些短的加帽寡核苷酸与长RNA的“去头的”(无5’-帽结构)片段连接。使用这种化学-酶促方法合成的最终RNA具有内部2’-O-甲基化核苷残基和5’-TMG-帽结构两者。然而,使用这种连接方法仅制备了短的加帽RNA(<200聚体)。此外,产率较低(15-30%)。控制和优化T4 DNA连接反应并不容易,而且需要使用聚丙烯酰胺凝胶电泳和从剩余的未加帽RNA中分离加帽RNA的费力的分离过程。通过PAGE方法从剩余的未加帽mRNA中分离长的(500-10000个碱基)加帽mRNA是不可行的。
最后,5’-修饰的核苷或5’-修饰的单核苷酸或5’-修饰的二核苷酸,通常是鸟苷的衍生物,已经被用于启动RNA的体外转录(Gene,112:101-105(1992)和Bioconjug.Chem.,10371-378(1999))。这些起始子核苷和核苷酸可能带有标记物或亲和基团(例如,生物素),并且当并入RNA的5’端时,将允许合成RNA的容易的检测、分离和纯化。这种5’-标记的或带标签的RNA可能是一些应用所必需的。然而,该策略未用于制备具有帽0、帽1、帽2或TMG-帽结构的mRNA。
在本公开的某些方面,提供了如本文所述的加帽mRNA序列起始子的组合物。在相关方面,是其中使用本文所述的加帽mRNA序列起始子合成RNA的方法。
mRNA序列起始子
本文提供了可以用于RNA合成的mRNA序列起始子。mRNA序列起始子可能具有杂交序列,该杂交序列可能与起始位点处DNA模板上的序列互补。在一些实施方案中,用于本文提供的方法和组合物中的起始子的杂交序列的长度取决于若干因素,包括模板核苷酸序列的同一性和该起始子与DNA模板杂交或在体外转录期间使用的温度。本领域普通技术人员或通过常规实验可以容易地确定用于转录的加帽起始子的特定核苷酸序列的期望的长度的确定。例如,核酸或寡核苷酸的长度可以基于期望的杂交特异性或选择性来确定。
mRNA序列起始子可以是加帽寡核苷酸引物。在一些实施方案中,起始加帽寡核苷酸引物(包括反向5’-5’帽核苷酸)的核苷酸长度在3至约9之间,在一些实施方案中起始加帽寡核苷酸引物(包含帽)的核苷酸长度在3至约7之间,在一些实施方案中起始加帽寡核苷酸引物(包含帽)的核苷酸长度在3至约5之间,并且在一些实施方案中起始加帽寡核苷酸引物(包含帽)的核苷酸长度为约3。起始子(例如起始加帽寡核苷酸引物)中杂交序列的长度可以等于或短于起始加帽寡核苷酸引物的总长度。
杂交序列的存在迫使起始子,例如起始加帽寡核苷酸引物,仅在期望的方向(即“正向”方向)上主要与起始位点处的DNA模板的互补序列比对。在一些实施方案中,在正向方向上,RNA转录物开始于反向的鸟苷残基。通过杂交复合物的热力学来维持DNA模板上引物对齐的正向方向相对于不正确的“反向”方向的优势。后者可以通过起始加帽寡核苷酸引物的杂交序列长度和与DNA模板杂交所涉及的碱基的同一性来确定。在期望的正向方向上的杂交也可能取决于在体外转录期间杂交或使用DNA模板和起始加帽寡核苷酸引物的温度和反应条件。
与用标准GTP、ATP、CTP或UTP起始的效力相比,示例性的起始子,例如本公开的起始加帽寡核苷酸引物,增强了转录起始的效力。在一些实施方案中,当RNA的合成主要从起始加帽寡核苷酸引物开始而不是从转录混合物中的任何NTP开始时,转录的起始被认为是增强的。转录起始的提高的效率导致RNA转录物的更高的产率。与使用常规方法而不启动加帽引物的RNA合成相比,转录起始的增强的效率可以增加到约10%、约20%、约40%、约60%、约80%、约90%、约100%、约150%、约200%或约500%。在某些实施方案中,加帽mRNA序列起始子,例如起始加帽寡核苷酸引物,在转录的起始方面胜过任何NTP(包括GTP)。本领域普通技术人员能够容易地确定底物活性水平和起始加帽寡核苷酸引物的效力。确定底物效力的方法的一个实例在实施例13中举例说明。在某些实施方案中,起始发生于加帽寡核苷酸引物,而不是NTP,这导致转录mRNA的更高水平的加帽。
在一些方面,提供了其中利用具有取代或修饰的起始加帽寡核苷酸引物合成RNA的方法。在一些方面,起始加帽寡核苷酸引物的取代和修饰基本上不损害RNA的合成。可以进行常规测试合成,以确定使用经修饰的起始加帽寡核苷酸引物是否可以获得期望的合成结果。本领域技术人员可以进行这种常规实验,以确定是否可以获得期望的结果。起始加帽寡核苷酸引物的取代或修饰包括例如一个或多个经修饰的核苷碱基、一种或多种经修饰的糖、一个或多个经修饰的核苷酸间键和/或一个或多个经修饰的三磷酸桥。
起始子(例如经修饰的起始加帽寡核苷酸引物),其可以包含本文提供的方法和组合物的一个或多个修饰基团,可以通过将NTP并入到开放的3’-OH基团上而被DNA模板上的RNA聚合酶延长。起始加帽寡核苷酸引物可以包含天然RNA和DNA核苷、经修饰的核苷或核苷类似物。起始加帽寡核苷酸引物可以含有天然的核苷酸间磷酸二酯键或其修饰,或其组合。
在一个实施方案中,修饰基团可以是热不稳定基团,其随着酶反应介质温度的升高以增加的速率从经修饰的起始加帽寡核苷酸引物解离。寡核苷酸和NTP的热不稳定基团的实例描述于Nucleic Acids Res.,36:e131(2008),Collect.Symp.Ser.,10:259-263(2008)和Analytical Chemistry,81:4955-4962(2009)。
在一些方面,提供了合成RNA的方法,其中向转录反应中加入至少一种或多种NTP可以具有如本文公开的修饰。在一些方面,所述至少一种NTP的修饰基本上不损害RNA聚合酶介导的RNA合成。NTP的修饰可以包括,例如,一个或多个经修饰的核苷碱基、一种或多种经修饰的糖、一个或多个经修饰的5’-三磷酸。经修饰的NTP可以并入到起始加帽寡核苷酸引物的3’端,并且它不阻断转录并支持引物的进一步延伸。
在另一实施方案中,起始加帽寡核苷酸引物的修饰基团可以是可检测的标记物或可检测的标志物。因此,在转录后,可以通过大小、质量、颜色和/或亲和捕获来鉴定含有可检测的标记物或标志物的靶RNA。在一些实施方案中,可检测的标记物或标志物是荧光染料;并且亲和捕获标记物为生物素。在某些实施方案中,转录反应的一种或多种组分(起始加帽寡核苷酸引物和/或NTP)可以用可检测的标记物或标志物标记。因此,在转录后,可以通过例如大小、质量、亲和捕获或颜色来鉴定RNA分子。在一些实施方案中,可检测的标记物是荧光染料;并且亲和捕获标记物为生物素。
标准化学和酶促合成方法可以用于合成本公开的mRNA序列起始子,并在本文的实施例部分中公开。
试剂盒
还考虑了包含用于进行转录的mRNA序列起始子的试剂盒。例如,试剂盒可以含有用于合成常见RNA(例如,FLuc mRNA)的所有转录试剂。更具体地,试剂盒可以含有:mRNA序列起始子;标记用于转录的容器;进行RNA合成的说明书;和一种或多种试剂,所述试剂选自一种或多种经修饰的或未修饰的起始加帽寡核苷酸引物、一种或多种未修饰的NTP、一种或多种经修饰的NTP(例如,5’-三磷酸假尿苷)、RNA聚合酶、其他酶、反应缓冲液、镁和DNA模板。
本公开的mRNA序列起始子与涉及使用各种起始核苷、核苷酸和寡核苷酸或使用含有帽0结构的多磷酸二核苷酸衍生物如mCAP和ARCA的现有方法和组合物相比具有显著优势。mRNA序列起始子,例如起始加帽寡核苷酸引物可以与现有的转录系统和试剂兼容,并且不需要额外的酶或试剂。此外,使用起始加帽寡核苷酸引物使得若干个非酶促和酶促步骤(如加帽和2’-O-甲基化)变得不必要,从而降低了过程的复杂性和RNA合成的成本。
虽然本文所述的示例性方法涉及T7 RNA聚合酶介导的转录反应,但本领域已知的用于转录反应的许多其他RNA聚合酶可以用于本公开的组合物和方法。其他酶(包括可以使用的天然或突变的变体)包括例如SP6和T3 RNA聚合酶和来自其他来源的RNA聚合酶,包括热稳定的RNA聚合酶。
一些核酸复制和扩增方法可以包括转录作为过程的一部分。这些方法为:转录介导的扩增(TMA)和基于核酸序列的扩增(NASBA)、DNA和RNA测序以及本领域已知的其他核酸延伸反应。本领域技术人员将理解,其他方法可以用于替代转录方法或与转录方法一起使用,包括未来开发的转录反应的变体。
治疗用途
在一个方面,本文描述了一种用于在有需要的对象中降低冠状动脉疾病的风险的方法,所述方法包括向所述对象施用有效量的本文所述的药物组合物。
在一个方面,本文描述了含有加帽mRNA序列起始子的mRNA的生产,例如用作药物组合物中的治疗性药剂的起始加帽寡核苷酸引物,将含有加帽起始子的RNA引入到细胞中以治疗细胞的医学病状,或将含有加帽起始子的RNA引入到细胞中,所述细胞利用那些RNA来产生可能对宿主细胞具有治疗作用的蛋白质。
一种利用含有加帽起始子的RNA来治疗病症的方法,包括向患有或怀疑患有其症状/症候学的严重程度可以降低或消除的病症的对象施用本文所述的含有加帽起始子的RNA或包含此类RNA的组合物的步骤。
当以4mg/ml或更低的浓度配制在药学上可接受的载剂和/或药学上可接受的盐中时,本文所述的含有加帽起始子的RNA比使用单独的药学上可接受的载剂的未治疗的个体有效地产生至少20%、30%、40%、50%、60%、70%、80%、90%或更大的症状和/或症候学的减少。
可以将药物组合物配制成用于通过注射或本领域技术人员已知的其他合适途径施用以用于治疗特定病状。用于肠胃外施用的可注射组合物通常含有在合适的溶液和/或药物载剂如无菌生理盐水中的活性化合物。该组合物还可以配制成在脂质或磷脂中的悬浮液、在脂质体悬浮液中或在水性乳液中。
用于制备各种组合物和/或制剂的方法是本领域技术人员已知的,参见Remington's Pharmaceutical Sciences(第19版,威廉姆斯和威尔金斯出版社(Williams&Wilkins),1995)。待施用的组合物将含有一定量的药学上安全和有效量的所选化合物,以用于增加靶细胞或组织中期望的蛋白质的表达。
在一些实施方案中,药物组合物含有至少0.1%(w/v)的如上所述的化合物,在一些实施方案中,药物组合物含有大于0.1%的化合物,在一些实施方案中,药物组合物含有高达约10%的化合物,在一些实施方案中,药物组合物含有高达约5%的化合物,并且在一些实施方案中,药物组合物含有高达约1%(w/v)的化合物。合适浓度的选择取决于多种因素,如期望的剂量、频率和递送活性药剂的方法。
对于如哺乳动物或人类的对象的治疗,基于如对象的体重和总体健康状况、所治疗的病状、症状的严重程度等因素来确定剂量。确定剂量和浓度以产生期望的益处,同时避免任何不期望的副作用。对于人类患者,本主题化合物的典型剂量在约0.0005至500mg/天的范围内,并且在一些实施方案中在约1-100mg/天的范围内。例如,较高的剂量方案包括例如50-100、75-100或50-75mg/天,并且较低的剂量方案包括例如1-50、25-50或1-25mg/天。
RNA修饰
本文提供了用起始子修饰的RNA分子,例如本文所述的适合于靶向的离体和体内递送系统的起始加帽寡核苷酸引物。经修饰的RNA分子可以包含两个或更多个连接的核糖核酸亚基。非限制性的示例性经修饰的RNA包括CRISPR向导RNA、短干扰RNA(siRNA)、微小RNA(miRNA)、短发夹RNA(shRNA)、小核RNA(snRNA)、信使RNA(mRNA)、前体mRNA(pre-mRNA)、反义RNA(asRNA)和异核RNA(hnRNA)。如本文所述的经修饰的RNA涵盖RNA序列及其任何结构实施方案,例如单链、双链、三链、环状、螺旋、发夹、茎环、隆起等。经修饰的RNA可以包括至少约3、4、5、6、7、8、9、10、20、30、40、50、100、200、300、400或500个碱基的长度。经修饰的RNA可以包括至少约1千碱基(kb)、2kb、3kb、4kb、5kb、10kb、20kb、50kb或更多的长度。在一些实施方案中,经修饰的RNA是CRISPR向导RNA(gRNA)。gRNA可以是单向导RNA或双向导RNA。在一些实施方案中,经修饰的RNA是mRNA。在一些实施方案中,mRNA可以从细胞或组织中分离出来。在一些实施方案中,mRNA可以从DNA转录而来。在一些实施方案中,mRNA可以化学合成。
在某些实施方案中,本文提供的经修饰的RNA分子抵抗RNA酶或其他核酸外切酶的降解。在某些实施方案中,本文提供的经修饰的RNA分子被稳定化以防止被核酸内切酶降解。在一些实施方案中,与未修饰的RNA相比,本文提供的经修饰的RNA分子适用于体内递送,并且诱导较少的细胞免疫受体活化(例如TLR,RIG-I)。RNA修饰如Diebold(2008)AdvDrug Deliv Rev.4月29日;60(7):813-23和Sorrentino(1998)Cell Mol Life Sci.Aug;54(8):785-94中所述,两者的全部内容通过引用并入本文。
如本文所述的核苷酸可以是合成的或化学修饰的。例如,本文提供的向导RNA可以是合成的或化学修饰的向导RNA。被修饰的向导RNA中的核苷酸可以是对应于向导RNA与Cas9的结合区中的一个或多个核苷酸和/或向导RNA与靶DNA的结合区中的核苷酸。向导RNA的剩余的未修饰的核苷酸可能是需要被鉴定以使Cas9与碱基上的2’-OH位置最小结合的核苷酸。在一些实施方案中,核苷酸可以在核苷酸的糖部分的2’位置被修饰。在一些实施方案中,糖部分的2’-OH基团由选自H、OR、R、卤素、SH、SR、H2、NHR、N(R)2或CN的基团取代,其中R是C1-C6烷基、烯基或炔基,并且卤素是F、CI、Br或I。其他修饰可以包括,反式(脱氧)无碱基、氨基、氟、氯、溴、CN、CF、甲氧基、咪唑、羧酸盐、硫醇盐、C1至C10低级烷基、取代的低级烷基、烷芳基或芳烷基、杂环烷基;杂环烷芳基;氨基烷基氨基;聚烷基氨基或取代的甲硅烷基。用于制备具有特定序列和修饰的RNA的方法是本领域技术人员已知的,例如,在Dellinger等人(2011),J.Am.Chem.Soc,133,11540;US 8,202,983;Kumar等人,(2007),J.Am.Chem.Soc,129,6859-64;WO2013176844,其全部内容通过引用并入本文。
在一些实施方案中,如本文提供的多核苷酸或寡核苷酸可以是合成的。例如,mRNA可以是化学合成的mRNA。合成RNA的生产产率基于序列和修饰。已经显示2’-O-甲基修饰增加了RNA合成期间的偶联功效或效率,因此增加了化学合成的RNA的产率。此外,核苷酸可以被硫代磷酸酯修饰。硫代磷酸酯(硫代磷酸酯)(PS)键用一个硫原子取代寡核苷酸的磷酸主链中的非桥氧。因此,本公开的示例性核苷酸包括但不限于核糖核酸(RNA)、脱氧核糖核酸(DNA)、苏糖核酸(TNA)、乙二醇核酸(GNA)、肽核酸(PNA)、锁定核酸(LNA,包括具有β-D-核糖构型的LNA、具有a-L-核糖构型的a-LNA(LNA的非对映异构体)、具有2’-氨基官能化的2’-氨基-LNA和具有2’-氨基官能化的2’-氨基-a-LNA)或其杂交体。
用于靶向递送的缀合物
本文提供了适合于试剂的靶向递送的缀合物,所述试剂为如mRNA、向导RNA、miRNA、siRNA、DNA、肽或其他小分子或大分子。缀合物可以含有用于离体或体内靶向递送的一个或多个适体、配体或部分。在一些实施方案中,缀合物包括靶向部分(或配体)、接头和与靶向部分连接的活性药剂(或有效载荷)。活性药剂可以是治疗性药剂、预防剂或诊断/预后剂。活性药剂可以具有操纵对象中的生理功能(例如基因表达)的能力。活性药剂可以是向导RNA、mRNA、miRNA、siRNA、DNA或肽。活性药剂可以经由接头、经由非共价键、经由核碱基配对或其任意组合与靶向部分连接。在一些实施方案中,缀合物可以是单一活性药剂和单一靶向部分之间的缀合物,具有下式:X-Y-Z,其中X是靶向部分;Y是接头;并且Z是向导RNA。在某些实施方案中,一个靶向配体可以与两种或更多种活性药剂缀合,其中缀合物具有式:X-(Y-Z)n。例如,缀合物可以包括向导RNA和mRNA。在某些实施方案中,一种活性药剂可以与两种或更多种靶向配体连接,其中缀合物具有式:(X-Y)n-Z。在其他实施方案中,一个或多个靶向部分可以连接到一个或多个活性有效载荷,其中缀合物的式可以是(X-Y-Z)n。在各种组合中,缀合物的式可以是,例如,X-Y-Z-Y-X、(X-Y-Z)n-Y-Z或X-Y-(X-Y-Z)n,其中X是靶向部分;Y是接头;Z是活性药剂,例如向导RNA。缀合物中每个部分的数量可以根据药剂的类型、缀合物的大小、递送靶标、用于包装缀合物的颗粒、其他活性药剂(例如免疫佐剂)和施用途径而变化。X、Y和Z每次出现时可以相同或不同,例如缀合物可以含有多于一种类型的靶向部分、多于一种类型的接头和/或多于一种类型的活性药剂,n是等于或大于1的整数。在一些实施方案中,n是在1和50之间,或在2和20之间,或在5和40之间的整数。在一些实施方案中,n可以是2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、41、43、44、45、46、47、48、49或50的整数。
在一些实施方案中,可以使用病毒制剂、聚合物制剂和脂质体制剂、细胞穿透肽、适体、配体或缀合物和抗体方法将活性药剂(例如,向导RNA)递送至细胞和组织。部分或配体可以将向导RNA引导至特定器官、组织或细胞,例如肝细胞,并且可以被称为靶向部分。在一些实施方案中,靶向部分修饰附着的分子(例如,mRNA或向导RNA)的一种或多种性质,包括但不限于药效学、药代动力学、结合、吸收、细胞分布、细胞摄取、电荷和清除。
可以附接至本文所述的活性药剂的示例性部分包括但不限于嵌入剂、报告分子、聚胺、聚酰胺、聚乙二醇、硫醚、聚醚、胆固醇、硫代胆固醇、胆酸部分、叶酸、脂质、磷脂、生物素、吩嗪、菲啶、蒽醌、金刚烷、吖啶、荧光素、罗丹明、香豆素、染料、脂质部分如胆固醇部分(Letsinger等人,Proc.Natl.Acad.Sci.USA,1989,86,6553);胆酸(Manoharan等人,Bioorg.Med.Chem.Lett.,1994,4,1053);硫醚,例如己基-S-三苯甲基硫醇(Manoharan等人,Ann.NY.Acad.Sci.,1992,660,306;Manoharan等人,Bioorg.Med.Chem.Let.,1993,3,2765);硫代胆固醇(Oberhauser等人,Nucl.Acids Res.,1992,20,533);脂肪族链,例如十二烷二醇或十一烷基残基(Saison-Behmoaras等人,EMBO J.,1991,10,111;Kabanov等人,FEBS Lett.,1990,259,327;Svinarchuk等人,Biochimie,1993,75,49);磷脂,例如二-十六烷基-外消旋-甘油或三乙基铵-1,2-二-0-十六烷基-外消旋-甘油-3-H-膦酸酯(Manoharan等人,Tetrahedron Lett.,1995,36,3651;Shea等人,Nucl.Acids Res.,1990,18,3777);多胺或聚乙二醇链(Manoharan等人,Nucleosides&Nucleotides,1995,14,969);金刚烷乙酸(Manoharan等人,Tetrahedron Lett.,1995,36,3651);棕榈酰部分(Mishra等人,Biochim.Biophys.Acta,1995,1264,229);或十八胺或己胺基-羰基-氧基胆甾醇部分(Crooke等人,J.Pharmacol.Exp.Ther.,1996,277,923),所有参考文献以其整体并入本文。靶向部分可以包含天然存在的分子,或重组分子或合成分子,包括但不限于聚赖氨酸(PLL)、聚L-天冬氨酸、聚L-谷氨酸、苯乙烯-马来酸酐共聚物、聚(L-丙交酯-共-乙交酯)共聚物、二乙烯基醚-马来酸酐共聚物、N-(2-羟丙基)甲基丙烯酰胺共聚物(HMPA)、聚乙二醇(PEG,例如PEG-2K、PEG-5K、PEG-10K、PEG-12K、PEG-15K、PEG-20K、PEG-40K)、MPEG、[MPEG]2、聚乙烯醇(PVA)、聚氨酯、聚(2-乙基丙烯酸)、N-异丙基丙烯酰胺聚合物、聚膦嗪、聚乙烯亚胺、阳离子基团、精胺、亚精胺、聚胺、假肽-聚胺、模拟肽聚胺、树状聚胺、精氨酸、脒、鱼精蛋白、阳离子脂质、阳离子卟啉、聚胺的季盐、促甲状腺素、促黑素、凝集素、糖蛋白、表面活性蛋白A、粘蛋白、糖基化的聚氨基酸、转铁蛋白、二磷酸酯、聚谷氨酸盐、聚天冬氨酸盐、适体、脱唾液酸胎球蛋白、透明质酸、前胶原、免疫球蛋白(例如,抗体)、胰岛素、转铁蛋白、白蛋白、糖-白蛋白缀合物、插入剂(例如,吖啶)、交联剂(例如,补骨脂素、丝裂霉素C)、卟啉(例如,TPPC4、德克萨卟啉(texaphyrin)、噻啉(Sapphyrin))、多环芳烃(例如,吩嗪、二氢吩嗪)、人工核酸内切酶(例如,EDTA)、亲脂性分子(例如,类固醇、胆汁酸、胆固醇、胆酸、金刚烷乙酸、1-芘丁酸、二氢睾酮、1,3-双-0(十六烷基)甘油、香叶基氧己基基团、十六烷基甘油、冰片、薄荷醇、1,3-丙二醇、十七烷基基团、棕榈酸、肉豆蔻酸、03-(油酰基)石胆酸、03-(油酰基)胆烯酸、二甲氧基三苯甲基或吩噁嗪)、肽(例如,α螺旋肽、两亲性肽、RGD肽、细胞渗透肽、内体裂解性/融合肽)、烷化剂、磷酸酯、氨基、巯基、聚氨基、烷基、取代的烷基、放射性标记的标志物、酶、半抗原(例如,生物素)、转运/吸收促进剂(例如,萘普生、阿司匹林、维生素E、叶酸)、合成核糖核酸酶(例如,咪唑、双咪唑、组胺、咪唑簇、吖啶-咪唑缀合物、四氮杂大环的Eu3+复合体)、二硝基苯基、HRP、AP、抗体、激素和激素受体、凝集素、碳水化合物、多价碳水化合物、维生素(例如,维生素A、维生素E、维生素K、维生素B,例如,叶酸、B12、核黄素、生物素和吡哆醛)、维生素辅因子、脂多糖、p38 MAP激酶的活化剂、NF-κB的活化剂、分类单元(taxon)、长春新碱、长春花碱、细胞松弛素、诺考达唑、杰斯内酯(japlakinolide)、拉春库林A、鬼笔环肽、swinholide A、印丹诺辛(indanocine)、肌基质蛋白(myoservin)、肿瘤坏死因子α(TNFα)、白介素-1β、γ干扰素、天然或重组低密度脂蛋白(LDL)、天然或重组高密度脂蛋白(HDL),以及细胞渗透剂(例如,螺旋细胞渗透剂)、肽和模拟肽配体,包括具有天然存在或经修饰的肽(例如,D或L肽)的那些;α、β或γ肽;N-甲基肽;氮杂肽;具有一个或多个被一个或多个脲、硫脲、氨基甲酸酯或磺酰脲键置换的酰胺键(即,肽键)的肽;或环状肽;两亲性肽,包括但不限于天蚕抗菌肽、lycotoxin、paradaxin、buforin、CPF、铃蟾抗菌肽样肽(BLP)、凯萨林菌素(cathelicidin)、ceratotoxin、柄海鞘肽、八目鳗肠抗微生物肽(HFIAP)、magainine、brevinins-2、蛙皮抗菌肽(dermaseptin)、蜂毒肽、pleurocidin、H2A肽、爪蟾肽、esculentinis-1以及caerin。模拟肽(在本文中也被称为模拟寡肽)是能够折叠成与天然肽相似的限定三维结构的分子。肽或模拟肽配体或部分可以为约5-50个氨基酸长,例如,约5、10、15、20、25、30、35、40、45或50个氨基酸长。在一些实施方案中,靶向部分可以是其他肽,如生长激素抑制素、奥曲肽、LHRH(促黄体激素释放激素)、表皮生长因子受体(EGFR)结合肽、aptide或双足肽(bipodal peptide)、含RGD的肽、蛋白质支架(如纤连蛋白结构域)、单结构域抗体、稳定的scFv或其他归巢肽。作为非限制性实例,基于蛋白质或肽的靶向部分可以是蛋白质,如血小板反应蛋白、肿瘤坏死因子(TNF)、膜联蛋白V、干扰素、血管抑素、内皮抑素、细胞因子、转铁蛋白、GM-CSF(粒细胞-巨噬细胞集落刺激因子)或生长因子,如血管内皮生长因子(VEGF)、肝细胞生长因子(HGF)、血小板衍生生长因子(PDGF)、碱性成纤维细胞生长因子(bFGF)和表皮生长因子(EGF)。在一些实施方案中,靶向部分可以是抗体、抗体片段、RGD肽、叶酸或前列腺特异性膜抗原(PSMA)。在一些实施方案中,蛋白质支架可以是抗体衍生的蛋白质支架。非限制性实例包括单结构域抗体(dAb)、纳米抗体、单链可变片段(scFv)、抗原结合片段(Fab)、Avi抗体(Avibody)、微抗体(minibody)、CH2D结构域、Fcab以及双特异性T细胞接合器(BiTE)分子。在一些实施方案中,scFv是稳定的scFv,其中scFv具有超稳定的性质。在一些实施方案中,纳米抗体可以衍生自骆驼科抗体的单可变结构域(VHH)。
在一些实施方案中,靶向部分识别或结合仅存在于或主要存在于特定细胞的表面上的靶细胞、标志物或分子。例如,靶向部分可以结合肿瘤抗原,并且将活化剂(例如向导RNA-Cas复合体)引导至恶性细胞。在一些实施方案中,靶向部分识别细胞内蛋白质。在一些实施方案中,靶向部分将缀合物引导至特定组织、细胞或细胞中的特定位置(例如,三价N-乙酰半乳糖胺靶向哺乳动物中的肝细胞的表面上的去唾液酸糖蛋白受体(ASGPR);Nair等人,J.Am.Chem.Soc.2014,136,16958,还参见US17/192,709)。靶向部分可以在培养物中或在整个生物体中或在两者中引导缀合物。在每种情况下,靶向部分可以结合至存在于靶向的细胞的表面上或靶向的细胞内的受体,其中靶向部分以有效的特异性、亲和力和亲合力结合至受体。在其他实施方案中,靶向部分将缀合物靶向至特定组织,如肝脏、肾、肺或胰腺。在其他情况下,靶向部分可以将缀合物引导至网状内皮或淋巴系统的细胞,或引导至专门的吞噬细胞,如巨噬细胞或嗜酸性粒细胞。在一些实施方案中,靶向部分可以识别RTK受体、EGF受体、丝氨酸或苏氨酸激酶、G蛋白偶联受体、甲基CpG结合蛋白、细胞表面糖蛋白、癌症干细胞抗原或标志物、碳酸酐酶、溶细胞性T淋巴细胞抗原、DNA甲基转移酶、胞外酶、糖基磷脂酰肌醇锚定的共受体、磷脂酰肌醇聚糖相关整合膜蛋白聚糖、热休克蛋白、缺氧诱导蛋白、多药物抗性转运体、肿瘤相关巨噬细胞标志物、肿瘤相关糖抗原、TNF受体家族成员、跨膜蛋白、肿瘤坏死因子受体超家族成员、肿瘤分化抗原、锌依赖性金属外肽酶、锌转运体、钠依赖性跨膜转运蛋白、凝集素SIGLEC家族成员或基质金属蛋白酶。
靶向部分可以与核酸(例如向导RNA或mRNA)的核碱基、糖部分或核苷间键缀合。与嘌呤核碱基或其衍生物的缀合可以发生在任何位置,包括环内原子和环外原子。在一些实施方案中,嘌呤核碱基的2位置、6位置、7位置或8位置附接至一个部分。与嘧啶核碱基或其衍生物的缀合也可以发生在任何位置。在一些实施方案中,嘧啶核碱基的2位置、5位置和6位置可以被一个部分取代。当一个部分与核碱基缀合时,优选的位置是不干扰杂交的位置,即不干扰碱基配对所需的氢键相互作用。
与核苷的糖部分的缀合可以发生在任何碳原子上。可以附接到缀合物部分的糖部分的示例性碳原子包括2’、3’和5’碳原子。γ位置也可以附接到缀合物部分,如在无碱基残基中。核苷间键也可以带有缀合物部分。对于含磷的键(例如,磷酸二酯、硫代磷酸酯、二硫代磷酸酯、磷酰胺酯等),缀合部分可以直接附接到磷原子或附接到与磷原子结合的O、N或S原子上。对于含有胺的或含有酰胺的核苷间键(例如,PNA),缀合物部分可以附接到胺或酰胺的氮原子或相邻的碳原子上。
存在许多用于制备寡核苷酸的缀合物的方法。通常,通过使寡核苷酸上的反应性基团(例如,OH、SH、胺、羧基、醛等)与缀合物部分上的反应性基团接触,将寡核苷酸的附接到缀合物部分上。在一些实施方案中,一个反应基团是亲电的,并且另一个是亲核的。例如,亲电基团可以是含羰基的官能团,并且亲核基团可以是胺或硫醇。在有或没有连接基团的情况下核酸和相关寡聚化合物的缀合方法在文献中很好地描述,如例如Manoharan inAntisense Research and Applications,Crooke和LeBleu编著,CRC出版社,波卡拉顿,佛罗里达州,1993,第17章,该文献通过引用以其整体并入本文。
可以经由RNA-RNA或RNA-DNA碱基配对和杂交将靶向部分附接至本文所述的活性药剂或治疗性核酸,如向导RNA。不旨在受任何理论的束缚,靶向部分可以包括能够识别或结合活性药剂的偶联序列,例如向导RNA或mRNA。在一些实施方案中,靶向部分包括能够与向导RNA的5’部分、3’部分或中间部分杂交的偶联序列。与偶联序列杂交的向导RNA可以包括延伸部分。例如,偶联序列可能能够与向导RNA的延伸序列杂交,从而将向导RNA引导至期望的体内、离体、细胞间或细胞内的位置,而向导RNA的功能性如与CRISPR酶的相互作用或与靶序列的结合不受影响。在一些实施方案中,向导RNA包括延伸部分,该延伸部分包含多核苷酸尾。在一些实施方案中,引导核酸包括能够分别与聚(U)尾、聚(A)尾或偶联序列的聚(A)尾杂交的聚(A)尾、聚(U)尾或聚(T)尾。在一些实施方案中,引导核酸可以是包括(A)n或(U)n的序列的向导RNA。在一些实施方案中,引导核酸可以包括DNA并且可以包括(A)n或(T)n的序列。在一些实施方案中,偶联序列可以包括(A)n、(U)n或(T)n的序列。如立即使用的,n可以为在1和200之间的任何整数。
偶联序列可以与核酸活性剂或其部分共享序列同一性或互补性。在一些实施方案中,偶联序列可以与本文所述的向导RNA或此类向导RNA的一部分共享至少10%、至少15%、至少20%、至少25%、至少30%、至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少98%、至少99%或100%的同一性。在一些实施方案中,偶联序列可以与本文所述的向导RNA的互补序列或此类向导RNA的一部分的互补序列共享至少10%、至少15%、至少20%、至少25%、至少30%、至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少98%、至少99%或100%的同一性。在一些实施方案中,偶联序列可以包括与向导RNA或其互补序列的至少2、至少3、至少4、至少5、至少6、至少7、至少8、至少9、至少10、至少11、至少12、至少13、至少14、至少15、至少16、至少17、至少18、至少19、至少20、至少21、至少22、至少23、至少24、至少25、至少26、至少27、至少28、至少29、至少30、至少31、至少32、至少33、至少34、至少35、至少36、至少37、至少38、至少39、至少40、至少41、至少42、至少43、至少44、至少45、至少46、至少47、至少48、至少49、至少50、至少51、至少52、至少53、至少54、至少55、至少56、至少57、至少58、至少59、至少60、至少61、至少62、至少63、至少64、至少65、至少66、至少67、至少68、至少69、至少70、至少71、至少72、至少73、至少74、至少75、至少76、至少77、至少78、至少79、至少80、至少81、至少82、至少83、至少84、至少85、至少86、至少87、至少88、至少89、至少90、至少91、至少92、至少93、至少94、至少95、至少96、至少97、至少98、至少99或至少100个连续核碱基的同一性或互补性。
在一些实施方案中,靶向部分可以包括经化学修饰的偶联序列或与该偶联序列相关联。在一些实施方案中,偶联序列包括与治疗性核酸,例如向导RNA或其部分杂交的延伸部分。在一些实施方案中,偶联序列的延伸部分可以被化学修饰。在一些实施方案中,治疗性核酸(例如向导RNA)可以包括延伸部分。在一些实施方案中,向导RNA的延伸部分可以被化学修饰。
靶向部分可以经由载剂附接至本文所述的核酸。载剂可以包含(i)至少一个“主链附接点”,优选地两个“主链附接点”,以及(ii)至少一个“系链附接点”。如本文所用的“主链附接点”是指官能团(例如羟基),或者通常可用于且适合于将载剂单体并入到寡核苷酸的主链(例如,磷酸酯或经修饰的磷酸酯,例如,含硫的主链)中的键。“系链附接点”(TAP)是指连接选定的部分的载剂单体的原子,例如,碳原子或杂原子(不同于提供主链附接点的原子)。选定的部分可以是例如碳水化合物,例如单糖、二糖、三糖、四糖、寡糖和多糖。任选地,选定的部分通过居间系链连接至载剂单体。因此,载剂通常将包含官能团(例如,氨基)或通常提供键,其适合于将另一化学实体(例如,配体)并入到或系链至组成原子。教导核酸的缀合物的制备的代表性美国专利包括但不限于美国专利号4,828,979;4,948,882;5,218,105;5,525,465;5,541,313;5,545,730;5,552,538;5,578,717;5,580,731;5,580,731;5,591,584;5,109,124;5,118,802;5,138,045;5,414,077;5,486,603;5,512,439;5,578,718;5,608,046;4,587,044;4,605,735;4,667,025;4,762,779;4,789,737;4,824,941;4,835,263;4,876,335;4,904、582;4,958,013;5,082,830;5,112,963;5,214,136;5,082、830;5,112,963;5,149,782;5,214,136;5,245,022;5,254,469;5,258,506;5,262,536;5,272,250;5,292,873;5,317,098;5,371,241、5,391,723;5,416,203、5,451,463;5,510,475;5,512,667;5,514,785;5,565,552;5,567,810;5,574,142;5,585,481;5,587,371;5,595,726;5,597,696;5,599,923;5,599,928;5,672,662;5,688,941;5,714,166;6,153,737;6,172,208;6,300,319;6,335,434;6,335,437;6,395,437;6,444,806;6,486,308;6,525,031;6,528,631;6,559,279;其内容通过引用以其整体并入本文。
靶向部分可以经由接头附接至活性药剂,例如向导RNA。接头可以结合至一种或多种活性药剂和靶向部分配体,以形成缀合物,其中缀合物在递送至靶细胞后释放至少一种活性药剂,例如向导RNA或向导RNA-Cas复合体。接头可以通过官能团附接至靶向部分和活性药剂,该官能团独立地选自酯键、二硫化物、酰胺、酰腙、醚、氨基甲酸酯、碳酸酯和脲。可替代地,接头可以通过如由硫醇和马来酰亚胺之间、叠氮化物和炔烃之间的缀合提供的不可切割基团附接至靶向部分或活性药剂。在一些实施方案中,靶向部分包括一个或多个接头。在一些实施方案中,如本文所述的一个或多个接头将靶向部分的一部分连接至靶向部分的不同部分。
接头可以各自独立地包括一个或多个官能团,所述官能团选自乙二醇、丙二醇、酰胺、酯、醚、烷基、环烷基、杂环基、芳基和杂芳基,其中烷基、烯基、环烷基、杂环基、芳基和杂芳基中的每一个任选地由一个或多个基团取代,该基团各自独立地选自卤素、氰基、硝基、羟基、羧基、氨基甲酰基、醚、烷氧基、芳氧基、氨基、酰胺、氨基甲酸酯、烷基、烯基、炔基、芳基、芳烷基、环烷基、杂芳基、杂环基,其中羧基、氨基甲酰基、醚、烷氧基、芳氧基、氨基、酰胺、氨基甲酸酯、烷基、烯基、炔基、芳基、芳烷基、环烷基、杂芳基或杂环基中的每一个任选地由一个或多个基团取代,该基团各自独立地选自卤素、氰基、硝基、羟基、羧基、氨基甲酰基、醚、烷氧基、芳氧基、氨基、酰胺、氨基甲酸酯、烷基、烯基、炔基、芳基、芳基烷基、环烷基、杂芳基、杂环基。在一些实施方案中,接头独立地包括磷酸酯、硫代磷酸酯、酰胺、醚、肟、肼或氨基甲酸酯。
在一些实施方案中,接头可以独立地包括C1-C10直链烷基、C1-C10直链O-烷基、C1-C10直链取代的烷基、C1-C10直链取代的O-烷基、C4-C13支链烷基、C4-C13支链O-烷基、C2-C12直链烯基、C2-C12直链O-烯基、芳烷基、C3-C12直链取代的烯基、C3-C12直链取代的O-烯基、聚乙二醇、聚乳酸、聚乙醇酸、聚(丙交酯-共-乙交酯)、聚己内酯、聚氰基丙烯酸酯、酮、芳基、杂环、琥珀酸酯、氨基酸、芳族基团、醚、冠醚、脲、硫脲、酰胺、嘌呤、嘧啶、双吡啶、用作交联剂的吲哚衍生物、螯合剂、醛、酮、双胺、双醇、杂环结构、吖丙啶、二硫化物、硫醚、腙及其组合。例如,接头可以是C3直链烷基或酮。接头的烷基链可以由一个或多个取代基或杂原子取代。在一些实施方案中,接头的烷基链可以任选地由一个或多个原子或基团中断,该原子或基团选自-O-、-C(=O)-、-NR、-O-C(=O)-NR-、-S-、-S-S-。
在一些实施方案中,接头可以是可切割的并且被切割以释放活性药剂。可切割官能团可以在体内水解或可以设计成(例如通过组织蛋白酶B)酶促水解。如本文所用,“可切割”接头是指可以物理或化学切割的任何接头。物理切割的实例可以是通过光、放射性发射或热来切割,而化学切割的实例包括通过氧化还原反应、水解、pH依赖性切割来切割。
接头可以包括直接键或原子(如氧或硫)、单元(如NR1、C(O)、C(O)NH、SO、SO2、SO2NH)或原子链,如但不限于取代或未取代的烷基、取代或未取代的烯基、取代或未取代的炔基、芳烷基、芳烯基、芳炔基、杂芳烷基、杂芳烯基、杂芳炔基、杂环烷基、杂环烯基、杂环炔基、芳基、杂芳基、杂环基、环烷基、环烯基、烷基芳烷基、烷基芳烯基、烷基芳炔基、烯基芳烷基、烯基芳烯基、烯基芳炔基、炔基芳烷基、炔基芳烯基、炔基芳炔基、烷基杂芳烷基、烷基杂芳烯基、烷基杂芳炔基、烯基杂芳烷基、烯基杂芳烯基、烯基杂芳炔基、炔基杂芳烷基、炔基杂芳烯基、炔基杂芳炔基、烷基杂环烷基、烷基杂环烯基、烷基杂环炔基、烯基杂环烷基、烯基杂环烯基、烯基杂环炔基、炔基杂环烷基、炔基杂环烯基、炔基杂环炔基、烷基芳基、烯基芳基、炔基芳基、烷基杂芳基、烯基杂芳基、炔基杂芳基,其中一个或多个亚甲基可以被O、S、S(O)、SO2、N(R’)、C(O)、取代或未取代的芳基、取代或未取代的杂芳基、取代或未取代的杂环中断或封端;其中R’为氢、酰基、脂肪族或取代的脂肪族。在一个实施方案中,接头为1-24个原子,优选地4-24个原子,优选地6-18个原子,更优选地8-18个原子,并且最优选地8-16个原子。
在一个实施方案中,接头包括至少一个可切割连接基团。在某些实施方案中,接头是支链接头。支链接头的分支点可以是至少三价,但可以是四价、五价或六价的原子,或呈现此类多价的基团。在某些实施方案中,分支点是—N、—N(O)—C、—O—C、—S—C、—SS—C、—C(O)N(O)—C、—OC(O)N(O)—C、—N(O)C(O)—C或—N(O)C(O)O—C;其中Q在每次出现时独立地为H或任选取代的烷基。在其他实施方案中,分支点是甘油或甘油衍生物。
在一个实施方案中,接头可以被酶切割。作为非限制性实例,接头可以是多肽部分,例如Govindan的WO2010093395中的AA,其内容通过引用以其整体并入本文;其可被细胞内肽酶切割。Govindan教导了接头中的AA可以是二肽、三肽或四肽,如Ala-Leu、Leu-Ala-Leu和Ala-Leu-Ala-Leu。在另一实例中,可切割接头可以是分支肽。分支肽接头可以包括两个或更多个提供酶切割位点的氨基酸部分。Dubowchik的WO 1998019705(其内容通过引用以其整体并入本文)中公开的任何分支肽接头可以用作本公开的缀合物中的接头。作为另一实例,接头可以包括Govindan等人的US 8877901中公开的溶酶体可切割多肽,其内容通过引用以其整体并入本文。作为另一实例,接头可以包括可被肿瘤相关蛋白酶选择性酶切割的蛋白肽序列,如Firestone等人的US 6214345中公开的任何Y和Z结构,其内容通过引用以其整体并入本文。
在一些实施方案中,接头可以包含可切割连接基团。可切割连接基团是在细胞外足够稳定、但在进入靶细胞后被切割以释放接头结合的两个部分的连接基团。在优选的实施方案中,可切割连接基团在靶细胞中或在第一参考条件(其可以例如经选定以模拟或代表细胞内条件)下的切割比在对象的血液中或在第二参考条件(其可以例如经选定以模拟或代表在血液或血清中发现的条件)下的切割快至少10倍或更多,优选地快至少100倍。可切割连接基团可以对切割剂敏感,例如,pH、氧化还原电位或降解分子的存在。通常,切割剂在细胞内比在血清或血液中更普遍或以更高水平或活性发现。此类降解剂的实例包括:针对特定底物选定的或不具有底物特异性的氧化还原剂,包括例如存在于细胞中的氧化或还原酶或还原剂(如硫醇),其可以通过还原降解氧化还原可切割连接基团;酯酶;可以产生酸性环境的内体或药剂,例如,导致pH为五或更低的那些;可以通过用作通用酸、肽酶(其可以是底物特异性的)和磷酸酶来水解或降解酸可切割连接基团的酶。
可切割连接基团(如二硫键)可以对pH敏感。人血清的pH为7.4,而细胞内平均pH稍低,范围为约7.1-7.3。内体具有更酸性的pH,范围为5.5-6.0,并且溶酶体具有甚至更酸性的pH,约5.0。一些接头将具有可切割连接基团,其在优选的pH下被切割,从而将阳离子脂质从细胞内的配体释放,或释放至细胞的期望的隔室中。
接头可以包含可被特定酶切割的可切割连接基团。并入到接头中的可切割连接基团的类型可以取决于待靶向的细胞。例如,肝脏靶向配体可以通过包含酯基团的接头与阳离子脂质连接。肝脏细胞富含酯酶,因此接头在肝脏细胞中比在不富含酯酶的细胞类型中将更有效地被切割。其他富含酯酶的细胞类型包括肺、肾皮质和睾丸的细胞。
一类可切割连接基团是氧化还原可切割连接基团,其在还原或氧化后被切割。可还原切割连接基团的实例是二硫化物连接基团(—S—S—)。为了确定候选可切割连接基团是否是合适的“可还原切割连接基团”或例如是否适合于与特定的RNA部分和特定的靶向剂一起使用,可以考虑本文所述的方法。例如,可以使用本领域已知的试剂通过与二硫苏糖醇(DTT)或其他还原剂一起温育来评估候选物,该试剂模拟将在细胞(例如,靶细胞)中观察到的切割速率。也可以在经选定以模拟血液或血清条件的条件下评估候选物。在优选的实施方案中,候选化合物在血液中至多切割10%。在优选的实施方案中,与血液(或在经选定以模拟细胞外条件的体外条件下)相比,有用的候选化合物在细胞中(或在经选定以模拟细胞内条件的体外条件下)的降解快至少2、4、10或100倍。在经选定以模拟细胞内介质的条件下,并且与经选定以模拟细胞外介质的条件相比,可以使用标准酶动力学测定来确定候选化合物的切割速率。
在一些实施方案中,接头可以包含基于磷酸酯的可切割连接基团。基于磷酸酯的可切割连接基团被降解或水解磷酸酯基团的试剂切割。切割细胞中磷酸酯基团的试剂的实例是酶,如细胞中的磷酸酶。基于磷酸酯的连接基团(即,含磷键或含磷接头)的实例是—P(O)(ORk)-O—、—O—P(S)(ORk)—O—、—O—P(S)(SRk)—O—、—S—P(O)(ORk)—O—、—O—P(O)(ORk)-S—、—S—P(O)(ORk)-S—、—O—P(S)(ORk)-S—、—S—P(S)(ORk)—O—、—O—P(O)(Rk)—O—、—O—P(S)(Rk)—O—、—S—P(O)(Rk)—O—、—S—P(S)(Rk)—O—、—S—P(O)(Rk)-S—、—O—P(S)(Rk)-S—。在一些实施方案中,基于磷酸酯的连接基团是—O—P(O)(OH)—O—、—O—P(S)(OH)—O—、—O—P(S)(SH)—O—、—S—P(O)(OH)—O—、—O—P(O)(OH)—S—、—S—P(O)(OH)—S—、—O—P(S)(OH)—S—、—S—P(S)(OH)—O—、—O—P(O)(H)—O—、—O—P(S)(H)—O—、—S—P(O)(H)—O—、—S—P(S)(H)—O—、—S—P(O)(H)—S—、—O—P(S)(H)—S—S—。在一些实施方案中,基于磷酸酯的接头是—O—P(O)(OH)—O—。
在一些实施方案中,接头可以包含酸可切割连接基团。酸可切割连接基团是在酸性条件下被切割的连接基团。在优选的实施方案中,酸可切割连接基团在pH为约6.5或更低(例如,约6.0、5.5、5.0或更低)的酸性环境中被切割,或通过可以用作通用酸的药剂(如酶)被切割。在细胞中,特定的低pH细胞器(如内体和溶酶体)可以提供酸可切割连接基团的切割环境。酸可切割连接基团的实例包括但不限于腙、酯和氨基酸的酯。酸可切割基团可以具有通式—C═NN—、C(O)O或—OC(O)。优选的实施方案是当附接至酯的氧的碳(烷氧基基团)是芳基基团、取代的烷基基团或叔烷基(如二甲基戊基或叔丁基)时。这些候选物可以使用与上述那些类似的方法来评估。
在一些实施方案中,接头可以包含基于酯的连接基团。基于酯的可切割连接基团在细胞中被酶(如酯酶和酰胺酶)切割。基于酯的可切割连接基团的实例包括但不限于亚烷基、亚烯基和亚炔基的酯。酯可切割连接基团具有通式—C(O)O—或—OC(O)—。这些候选物可以使用与上述那些类似的方法来评估。
在一些实施方案中,接头可以包含基于肽的连接基团。基于肽的可切割连接基团在细胞中被酶(如肽酶和蛋白酶)切割。基于肽的可切割连接基团是在氨基酸之间形成以产生寡肽(例如,二肽、三肽等)和多肽的肽键。基于肽的可切割基团不包括酰胺基团(—C(O)NH—)。酰胺基团可以在任何亚烷基、亚烯基或亚炔基之间形成。肽键是在氨基酸之间形成以产生肽和蛋白质的特殊类型的酰胺键。基于肽的可切割基团通常限于在产生肽和蛋白质的氨基酸之间形成的肽键(即,酰胺键),并且不包含整个酰胺官能团。基于肽的可切割连接基团具有通式—NHCHRAC(O)NHCHRBC(O)—,其中RA和RB是两个相邻氨基酸的R基团。
当靶向富含肽酶的细胞类型(如肝脏细胞和滑膜细胞)时,可以使用含有肽键的接头。
通常,候选可切割连接基团的适合性可以通过测试降解剂(或条件)切割候选连接基团的能力来评估。还需要测试候选可切割连接基团在血液中或当与其他非靶组织接触时抵抗切割的能力。因此,可以确定第一条件和第二条件之间对切割的相对敏感性,其中第一条件被选定以指示靶细胞中的切割,并且第二条件被选定以指示其他组织或生物流体(例如,血液或血清)中的切割。可以在无细胞系统中、在细胞中、在细胞培养物中、在器官或组织培养物中或在整个动物中进行评估。优选的实施方案,与血液或血清(或在经选定以模拟细胞外条件的体外条件下)相比,有用的候选化合物在细胞中(或在经选定以模拟细胞内条件的体外条件下)的切割快至少2、4、10或100倍。
在一些实施方案中,MA004 mRNA包括Seq.ID.0001的mRNA序列(表5)。在一些实施方案中,MA004 mRNA的序列和另一序列之间的相似性程度可以是至少50%相同、55%相同、60%相同、65%相同、70%相同、75%相同、80%相同、85%相同、90%相同、95%相同、97%相同、98%相同、99%相同或100%相同。如表5中所用,大写的核苷酸A、G和C分别表示核糖核苷酸腺嘌呤、鸟嘌呤和胞嘧啶。如表5中所用,小写u’表示N1-甲基假尿苷。
可以使用计算机程序或直接序列比较来计算序列同一性百分比。确定两个序列之间同一性的优选的计算机程序方法包括但不限于GCG程序包、FASTA、BLASTP和TBLASTN(参见,例如,D.W.Mount,2001,Bioinformatics:Sequence and Genome Analysis,冷泉港实验室出版社,冷泉港,纽约州)。BLASTP和TBLASTN程序可从NCBI和其他来源公开获得。SmithWaterman算法也可以用于确定同一性百分比。用于氨基酸序列比较的示例性参数包括以下:1)来自Needleman和Wunsch(J.Mol.Biol.,48:443-453(1970))的算法;2)来自Hentikoff和Hentikoff(Proc.Nat.Acad.Sci.USA.,89:10915-10919(1992))的BLOSSUM62比较矩阵;3)间隙罚分=12;以及4)间隙长度罚分=4。对这些参数有用的程序可以作为“gap”程序(遗传学计算机课题组(Genetics Computer Group),麦迪逊,威斯康星州)公开获得。上述参数是多肽比较的默认参数(没有末端间隙的罚分)。可替代地,多肽序列同一性可以使用以下等式计算:同一性%—(相同残基的数量)/(氨基酸残基中的比对长度)*100。对于此计算,比对长度包含内部间隙,但不包含末端间隙。
表5
靶序列
本公开提供了活性药剂或治疗性药剂(如基因组编辑组合物)以及用于其靶向递送的方法和组合物。本文所述的治疗性药剂可以包括基因组编辑组合物,其被引导至并修饰、改变或切割靶核酸分子上的靶序列。例如,活性药剂可以包括能够实现对靶序列的修饰的核酸或核酸-蛋白质复合体。
靶序列可以是DNA序列或RNA序列。在一些实施方案中,活性药剂或治疗性药剂可以包括RNA干扰因子。在一些实施方案中,活性药剂可以包括siRNA、shRNA、反义寡核苷酸、微小RNA、抗微小RNA或antimir、supermir、antagomir、核酶、三链体形成寡核苷酸、诱饵寡核苷酸、剪接转换寡核苷酸、免疫刺激性寡核苷酸、RNA活化剂或Ul衔接子。活性药剂可以识别靶序列并介导靶序列的切割和/或降解。在一些实施方案中,活性或治疗性药剂可以包括向导RNA。向导RNA可以与核酸引导的可编程核酸酶(如CRISPR酶,如Cas9)或其还包括功能性结构域的融合蛋白复合。靶序列可以由核酸引导的可编程核酸酶结构域识别。靶序列可以被核酸引导的可编程核酸酶结构域切割和/或被功能性结构域(如脱氨酶结构域、甲基化酶结构域、甲基转移酶结构域、激活结构域、阻遏物结构域、核酸酶结构域、转座酶结构域或重组酶结构域)修饰。在一些实施方案中,通过向导RNA可以将Cas9蛋白引导至靶核酸分子的靶序列,其中向导RNA与靶序列杂交,并且Cas蛋白切割靶序列。在一些实施方案中,靶序列可以与向导RNA的靶向序列互补。在一些实施方案中,向导RNA的靶向序列与其相应靶序列之间的互补性程度可以为约50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、98%、99%或100%。在一些实施方案中,靶序列和向导RNA的靶向序列可以是100%互补的。在其他实施方案中,靶序列和向导RNA的靶向序列可以含有至少一个错配。例如,靶序列和向导RNA的靶向序列可以含有1、2、3、4、5、6、7、8、9或10个错配。在一些实施方案中,靶序列和向导RNA的靶向序列可以含有1-6个错配。在一些实施方案中,靶序列和向导RNA的靶向序列可以含有5或6个错配。
靶序列的长度可以取决于所用的核酸酶系统。例如,CRISPR/Cas系统的靶序列的长度可以包括5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50或多于50个核苷酸。在一些实施方案中,靶序列的长度可以包括18-24个核苷酸。在一些实施方案中,靶序列的长度可以包括19-21个核苷酸。在一些实施方案中,靶序列的长度可以包括20个核苷酸。当使用切口酶时,靶序列可以包括由DNA分子相反链上的一对切口酶识别的一对靶序列。
在一些实施方案中,活性药剂或治疗性药剂可以包括大范围核酸酶系统。大范围核酸酶的靶序列的长度可以包括12-40个或更多个核苷酸。当使用ZFN时,靶序列可以包括由DNA分子相反链上的一对ZFN识别的两个半靶序列,其间具有互连序列。在一些实施方案中,ZFN的每个半靶序列的长度可以独立地包括9、12、15、18或更多个核苷酸。在一些实施方案中,ZFN的互连序列的长度可以包括4-20个核苷酸。在一些实施方案中,ZFN的互连序列的长度可以包括5-7个核苷酸。
当使用TALEN时,靶序列可以类似地包括由DNA分子相反链上的一对TALEN识别的两个半靶序列,其间具有互连序列。在一些实施方案中,TALEN的每个半靶序列的长度可以独立地包括10-20个或更多个核苷酸。在一些实施方案中,TALEN的互连序列的长度可以包括4-20个核苷酸。在一些实施方案中,TALEN的互连序列的长度可以包括12-19个核苷酸。
在一些实施方案中,靶序列可以邻近前间隔区相邻基序(PAM),即由CRISPR/Cas复合体识别的短序列。前间隔区相邻基序或PAM对于CRISPR/Cas复合体的靶结合是必需的。通常,PAM是紧接Cas核酸酶的DNA靶序列的2-6个碱基对DNA序列。PAM可以是5’PAM或3’PAM。PAM的确切序列取决于Cas蛋白的类型。例如,通常的SpCas9结合需要3’-NGG-5’PAM(也被称为标准PAM),其中N为A、G、C或T中的任一个。具有某些氨基酸取代(例如D1135E、R1335Q、G1218R和/或T1337R)的SpCas9可以识别NGA PAM或NGCG PAM。SaCas9结合需要3’-NNGRRT-5’PAM。具有某些氨基取代(例如K781E、K697N、H1014R)的SaCas9可以识别NNNRRT PAM。
在一些实施方案中,PAM可以邻近或在靶序列的3’端的1、2、3或4个核苷酸内。PAM的长度和序列可以取决于所用的Cas9蛋白。例如,PAM可以选自特定Cas9蛋白或Cas9直向同源物的共有序列或特定PAM序列,包括Ran等人,Nature,520:186-191(2015)的图1中公开的那些,其通过引用并入本文。在一些实施方案中,PAM的长度可以包括2、3、4、5、6、7、8、9或10个核苷酸。非限制性示例性PAM序列包括NGG、NGGNG、NG、NAAAAN、NNAAAAW、NNNNACA、GNNNCNNA和NNNNGATT(其中N被定义为任何核苷酸,并且W被定义为A或T)。在一些实施方案中,PAM序列可以是NGG。在一些实施方案中,PAM序列可以是NGGNG。在一些实施方案中,PAM序列可以是NNAAAAW。如Hu等人,Evolved Cas9 variants with broad PAM compatibilityand high DNA specificity,Nature 2018 556(7699):57-63中所述的额外的进化型Cas变体和PAM序列以其整体并入本文。
靶核酸分子可以是细胞内源性或外源性的任何DNA或RNA分子。如本文所用,术语“内源性序列”是指细胞天然的序列。术语“外源性序列”是指细胞非天然的序列,或其在细胞基因组中的天然位置在不同位置的序列。在一些实施方案中,靶核酸分子可以是来自细胞或细胞中的质粒、基因组DNA或染色体。在一些实施方案中,靶核酸分子的靶序列可以是来自细胞或细胞中的基因组序列。在一些实施方案中,细胞可以是原核细胞。在其他实施方案中,细胞可以是真核细胞。在一些实施方案中,真核细胞可以是哺乳动物细胞。在一些实施方案中,真核细胞可以是啮齿动物细胞。在一些实施方案中,真核细胞可以是人类细胞。在一些实施方案中,真核细胞可以是肝脏细胞。在一些实施方案中,真核细胞可以是肝细胞。在一些实施方案中,真核细胞可以是实质细胞、肝窦内皮细胞、吞噬枯式(phagocyticKupffer)细胞或星状细胞。在另外的实施方案中,靶序列可以是病毒序列。在其他实施方案中,靶序列可以是合成序列。在一些实施方案中,靶序列可以在真核染色体(如人染色体)上。
在一些实施方案中,靶序列可以位于基因的编码序列、基因的内含子序列、基因的转录控制序列、基因的翻译控制序列或基因之间的非编码序列中。在一些实施方案中,基因可以是蛋白质编码基因。在其他实施方案中,基因可以是非编码RNA基因。在一些实施方案中,靶序列可以包括疾病相关基因的全部或一部分。在一些实施方案中,靶序列可以包括与冠状动脉疾病相关联的基因的全部或一部分。在一些实施方案中,靶序列可以包括编码载脂蛋白的基因的至少一部分。在一些实施方案中,靶序列可以包括编码前蛋白转化酶枯草杆菌蛋白酶/Kexin 9型(PCSK9)、血管生成素样蛋白3(ANGPTL3)、载脂蛋白C3(APOC3)、载脂蛋白A(LPA)、LDL受体(LDL-R)、肌球蛋白调节轻链相互作用蛋白或LDL受体的可诱导降解物(IDOL)、甲状腺素运载蛋白(TTR)、抗凝血酶、AT3、载脂蛋白B(ApoB)或Hup的基因的至少一部分。本公开还考虑使用修饰来操纵靶基因的表达和活性,例如使用去稳定突变来抵消功能获得性PCSK9变体的作用。
示例性靶基因的核酸序列和人类起源的家族的其他成员的核酸序列以及许多动物的核酸序列是可公开获得的,例如,可从NCBI网站或ENSEMBL网站获得。实例包括但不限于以下序列:染色体1上的野生型PCSK9基因(NG_009061.1)、智人前蛋白转化酶枯草杆菌蛋白酶/kexin9型(PCSK9)、RefSeqGene(LRG_275);人APOC3保藏号NP_000031.1,基因库登录号:NG_008949.1;小鼠、大鼠和猴APOC3核酸序列Ensembl登录号分别为ENSMUSG00000032081、ENSRNOG00000047503和ENSMFAG00000001837;例如在NG_028169.1中提供了人ANGPTL3;小鼠、大鼠和猴ANGPTL3核酸序列Ensembl登录号分别为ENSMUSG00000028553、ENSRNOG00000008638和ENSMFAG00000007083;这些序列中的每一个都以其整体并入本文。
在一些实施方案中,使靶序列与本文所述的基因组编辑组合物接触导致在靶序列内或邻近靶序列的碱基编辑事件。例如,由于与如本公开中公开的包括融合蛋白的基因组编辑组合物接触,靶序列内或邻近靶序列的靶碱基(例如C碱基)可以转化为T碱基,该融合蛋白包括核酸引导的核酸酶结构域和脱氨酶结构域。在一些实施方案中,靶碱基位于PAM上游(5’端)。在一些实施方案中,靶碱基位于PAM上游(5’端)的1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个碱基对的位置。在一些实施方案中,靶碱基位于PAM上游(5’端)的13至17个碱基对内的位置。在一些实施方案中,靶碱基位于PAM上游(5’端)的13至17个碱基对以外的位置。在一些实施方案中,靶碱基对位于PAM上游(5’端)的10-15个碱基对的位置。在一些实施方案中,靶碱基位于PAM上游的11-12个碱基对的位置。在一些实施方案中,靶碱基是PAM上游(5’端)的11个碱基对。在一些实施方案中,靶碱基位于靶序列(例如ANGPTL3编码多核苷酸(例如,ANGPTL3基因座))的编码区(例如,外显子)中。例如,ANGPTL3基因座编码区中碱基的转化可以导致ANGPTL3蛋白序列中的氨基酸改变,即,突变。在一些实施方案中,突变是功能缺失突变。在一些实施方案中,突变可以将成熟前终止密码子(pre-mature stop codon)引入至靶序列的编码区,例如ANGPTL3基因的编码区。在一些实施方案中,功能缺失突变是天然存在的功能缺失突变。在一些实施方案中,突变位于PCSK9基因的编码区中,例如G106R、L253F、A443T、R93C、G24D、S47F、R46H、S153N或H193Y突变。在一些实施方案中,功能缺失突变将成熟前终止密码子引入到ANGPTL3基因的编码区中。在一些实施方案中,可以将功能缺失突变引入到APOC3基因的编码区,例如R19X突变。在一些实施方案中,可以将功能缺失突变引入到低密度脂蛋白受体(LDL-R)蛋白中。在一些实施方案中,可以将功能缺失突变引入到LDL受体(IDOL)蛋白的可诱导降解剂中。
在一些实施方案中,靶序列位于靶序列的非编码区中,例如,位于靶基因的内含子或剪接位点中。在一些实施方案中,靶序列位于剪接位点中,并且此类靶碱基的编辑导致靶基因mRNA的选择性剪接。在一些实施方案中,选择性剪接导致功能缺失突变体。在一些实施方案中,选择性剪接导致在靶mRNA中引入成熟前终止密码子或移码,从而导致截短的、不稳定的或折叠缺陷型多肽。在一些实施方案中,可以将终止密码子引入到正常终止密码子(被称为“成熟前终止密码子”)上游的载脂蛋白编码基因的编码序列中。在一些实施方案中,可以将终止密码子引入到靶基因的编码区中。成熟前终止密码子导致翻译提前终止,进而导致截短的和无功能性蛋白质,并且经由无义介导的mRNA衰变途径诱导mRNA快速降解。参见例如,Baker等人,Current Opinion in Cell Biology16(3):293-299,2004;Chang等人,Annual Review of Biochemistry 76:51-74,2007;以及Behm-Ansmant等人,Genes&Development 20(4):391-398,2006,其中的每一个通过引用并入本文。本文所述的基因组编辑组合物可以用于将多个编辑事件引入至靶序列。例如,基因组编辑组合物可以包括核酸引导可编程核酸酶,其在靶基因中诱导双链断裂、缺失、插入、移码、回复或其他改变。例如,基因组编辑组合物可以包括核酸引导的可编程核酸酶-脱氨酶融合蛋白,其可以转化若干个氨基酸,以产生终止密码子(例如,TAA、TAG或TGA)。
在一些实施方案中,提供了将突变同时引入到LDL介导的胆固醇清除途径中的多于一种蛋白质因子中。例如,在一些实施方案中,可以将突变同时引入到ANGPTL3、PCSK9、LDLR、APOB、APOE、IDOL和其他LDL介导的途径相关基因中的一种或多种,优选地至少两种。在一些实施方案中,可以将功能缺失突变同时引入到ANGPTL3、PCSK9、APOB和另一LDL介导的途径相关基因中的一种或多种,优选地至少两种。在一些实施方案中,可以将突变同时引入到ANGPTL3、PCSK9、LDLR和IDOL中。为了将功能缺失突变同时引入到多于一种蛋白质中,使用多个引导核苷酸序列。
在一些实施方案中,靶序列可以位于基因组中控制染色质组织方面的非基因功能性位点,如支架位点或基因座控制区。在一些实施方案中,靶序列可以是遗传安全港(genetic safe harbor)位点,即,促进安全遗传修饰的基因座。
模板
在一些实施方案中,在修复切割的靶核酸分子期间,可以提供至少一种模板作为底物。在一些实施方案中,模板可以用于同源重组,如例如高保真同源重组。在一些实施方案中,同源重组可以导致模板序列整合至靶核酸分子中。在一些实施方案中,可以提供单个模板或相同模板的多个拷贝。在其他实施方案中,可以提供两个或更多个模板,使得同源重组可以发生在两个或更多个靶位点处。例如,可以提供不同的模板来修复细胞中的单个基因或细胞中的两个不同基因。在一些实施方案中,可以以独立的拷贝数提供不同的模板。
在一些实施方案中,模板可以用于同源定向修复,需要DNA链侵入核酸中的切割位点。在一些实施方案中,同源定向修复可以导致模板序列拷贝至靶核酸分子中。在一些实施方案中,可以提供单个模板或相同模板的多个拷贝。在其他实施方案中,具有不同序列的两个或更多个模板可以通过同源定向修复在两个或多个位点插入。例如,可以提供不同的模板来修复细胞中的单个基因或细胞中的两个不同基因。在一些实施方案中,可以以独立的拷贝数提供不同的模板。
在一些实施方案中,模板可以作为通过非同源性末端连接介导的插入并入到切割的核酸中。在一些实施方案中,模板序列与切割位点附近的核酸序列没有相似性。在一些实施方案中,模板序列(例如,模板中的编码序列)与切割位点附近的核酸序列没有相似性。模板序列可以侧接靶序列,靶序列可以与切割位点附近的靶序列具有相似或相同序列。在一些实施方案中,可以提供单个模板或相同模板的多个拷贝。在其他实施方案中,具有不同序列的两个或多个模板可以通过非同源性末端连接在两个或更多个位点插入。例如,可以提供不同的模板来向细胞中插入单个模板或向细胞中插入两个不同模板。在一些实施方案中,可以以独立的拷贝数提供不同的模板。
在一些实施方案中,模板序列可以对应于靶细胞的内源性序列。在一些实施方案中,内源性序列可以是细胞的基因组序列。在一些实施方案中,内源性序列可以是染色体或染色体外序列。在一些实施方案中,内源性序列可以是细胞的质粒序列。在一些实施方案中,模板序列可以与切割位点处或附近的细胞中的内源性序列的一部分基本上相同,但包括至少一个核苷酸改变。在一些实施方案中,用模板修复切割的靶核酸分子可以导致突变,包括靶核酸分子的一个或多个核苷酸的插入、缺失或取代。在一些实施方案中,突变可以导致由包含靶序列的基因表达的蛋白质中的一个或多个氨基酸改变。在一些实施方案中,突变可以导致由靶基因表达的RNA中的一个或多个核苷酸改变。在一些实施方案中,突变可以改变靶基因的表达水平。在一些实施方案中,突变可以导致靶基因的表达增加或减少。在一些实施方案中,突变可以导致基因敲低。在一些实施方案中,突变可以导致基因敲除。在一些实施方案中,用模板修复切割的靶核酸分子可以导致靶基因的外显子序列、内含子序列、转录控制序列、翻译控制序列或非编码序列的置换。
在其他实施方案中,模板序列可以包括外源性序列。在一些实施方案中,外源性序列可以包括可操作连接至外源性启动子序列的蛋白质或RNA编码序列,使得在外源性序列整合到靶核酸分子中后,细胞能够表达由整合的序列编码的蛋白质或RNA。在其他实施方案中,在外源性序列整合到靶核酸分子中后,整合的序列的表达可以由内源性启动子序列调控。在一些实施方案中,外源性序列可以是染色体或染色体外序列。在一些实施方案中,外源性序列可以提供编码蛋白质或蛋白质的一部分的cDNA序列。在其他实施方案中,外源性序列可以包括外显子序列、内含子序列、转录控制序列、翻译控制序列或非编码序列。在一些实施方案中,外源性序列的整合可以导致基因敲入。
模板可以具有任何合适的长度。在一些实施方案中,模板的长度可以包括10、15、20、25、50、75、100、150、200、500、1000、1500、2000、2500、3000、3500、4000、4500、5000、5500、6000或更多个核苷酸。在一些实施方案中,模板可以包括与包括靶序列的靶核酸分子的一部分互补的核苷酸序列(即,“同源臂”)。在一些实施方案中,同源臂的长度可以包括10、15、20、25、50、75、100、150、200、500、1000、1500、2000、2500、3000或更多个核苷酸。在一些实施方案中,模板可以包括与位于靶核酸分子上的切割位点上游或下游的序列互补的同源臂。在一些实施方案中,模板可以包括第一核苷酸序列和第二同源臂,其分别与位于切割位点上游和下游的序列互补。当模板含有两个同源臂时,每个臂可以具有相同长度或不同长度,并且同源臂之间的序列可以与同源臂之间的靶序列基本上相似或相同,或完全不相关。在一些实施方案中,模板上的第一核苷酸序列与切割位点上游的序列之间以及模板上的第二核苷酸序列与切割位点下游的序列之间的互补性程度可以允许模板与靶核酸分子之间的同源重组,如例如高保真同源重组。在一些实施方案中,互补性程度可以为约50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、98%、99%或100%。在一些实施方案中,互补性程度可以为约95%、97%、98%、99%或100%。在一些实施方案中,互补性程度可以为约98%、99%或100%。在一些实施方案中,互补性程度可以为100%。在一些实施方案中,例如本文所述的那些,其中模板作为通过非同源性末端连接介导的插入被并入到切割的核酸中,该模板不具有同源臂。在一些实施方案中,例如,如本文所述,不具有同源臂的模板包括在模板序列的一端或两端侧翼的靶序列。在一些实施方案中,不具有同源臂的模板包括在模板序列的两端侧翼的靶序列。在一些实施方案中,在模板序列的末端侧翼的靶序列是约10-50个核苷酸。在一些实施方案中,在模板序列的末端侧翼的靶序列是约10-20个核苷酸、约15-20个核苷酸、约20-25个核苷酸或约20-30个核苷酸。在一些实施方案中,在模板序列的末端侧翼的靶序列是约17-23个核苷酸。在一些实施方案中,在模板序列的末端侧翼的靶序列是约20个核苷酸。
在一些实施方案中,如果在模板和基因组序列之间发生同源重组,则由模板表达核酸分子。在一些实施方案中,例如,模板不具有用于表达核酸分子的启动子,和/或ATG转录起始位点从编码序列中除去。
递送
本文提供了用于用核酸酶系统编辑细胞中的核酸分子及其靶向递送的方法和组合物。在一些实施方案中,核酸包含编码基因的核酸序列。在一些实施方案中,核酸包含编码与疾病或病症相关的基因的核酸序列。
包含本文所述的核酸(例如经修饰的向导RNA)的活性药剂可以与一个或多个靶向部分缀合,以用于靶向递送至期望的体内位置。可以经由本领域已知的任何方法将向导RNA缀合物或向导RNA-蛋白质复合体缀合物引入到细胞中,如例如病毒或噬菌体感染、转染、缀合、原生质体融合、脂质转染、脂质颗粒或囊泡转导、电穿孔、磷酸钙沉淀、聚乙烯亚胺(PEI)介导的转染、DEAE-葡聚糖介导的转染、脂质体介导的转染(例如通过阳离子脂质体介导的转染)、粒子枪技术、磷酸钙沉淀、剪切驱动的细胞渗透、与细胞穿透肽融合随后细胞接触、显微注射和纳米颗粒介导的递送。在一些实施方案中,可以经由病毒感染将核酸酶系统引入到细胞中。在一些实施方案中,可以经由噬菌体感染将核酸酶系统引入到细胞中。脂质体可以包括由l,2-二油基氧基-N,N-二甲基氨基丙烷(DODMA)脂质体、来自Marina BioteCH(博塞尔,华盛顿州)的DiLa2脂质体、l,2-二亚油基氧基-3-二甲基氨基丙烷(DLin-DMA)、2,2-二亚油基-4-(2-二甲氨基乙基)-[l,3]-二氧戊环(DLin-KC2-DMA)和可以递送小分子药物,如但不限于(来自杨森生物技术公司(Janssen Biotech,Inc.)(霍舍姆,宾夕法尼亚州))的脂质体形成的那些。
在一些实施方案中,本文提供的方法和组合物可以包括将本文所述的载体系统引入到细胞中。在一些实施方案中,载体系统整体或部分编码核酸酶系统。在一些实施方案中,载体系统包括一个、两个、三个或更多个载体。在一些实施方案中,将载体系统引入到细胞中可以产生具有编辑的核酸分子的稳定细胞系,同时载体丢失,例如,靶向自毁。在一些实施方案中,细胞是真核细胞。真核细胞的非限制性实例包括酵母细胞、植物细胞、昆虫细胞、来自无脊椎动物的细胞、来自脊椎动物的细胞、哺乳动物细胞、啮齿动物细胞、小鼠细胞、大鼠细胞以及人类细胞。在一些实施方案中,真核细胞可以是哺乳动物细胞。在一些实施方案中,真核细胞可以是啮齿动物细胞。在一些实施方案中,真核细胞可以是人类细胞。类似地,靶序列可以来自任何此类细胞或在任何此类细胞中。
在一些实施方案中,本文提供的多核苷酸或寡核苷酸(例如向导RNA或mRNA)可以配制在脂质囊泡中,其可以在官能化脂质双层或脂质-聚阳离子复合体之间形成交联。脂质体制剂可以受到但不限于阳离子脂质组分的选择、阳离子脂质饱和的程度、PEG化的性质、所有组分的比率和生物物理参数(如大小)或聚阳离子组合物的影响。在一个实施方案中,本文所述的药物组合物可以包括但不限于脂质体,如由稳定的质粒-脂质颗粒(SPLP)或稳定的核酸脂质颗粒(SNALP)的合成形成的那些,稳定的质粒-脂质颗粒(SPLP)或稳定的核酸脂质颗粒(SNALP)先前已被描述并显示出适合于体外和体内寡核苷酸递送。脂质纳米颗粒可以被工程改造以改变颗粒的表面特性,使得脂质纳米颗粒可以穿透粘膜屏障。粘液位于粘膜组织上,如但不限于口腔(例如,颊和食管膜以及扁桃体组织)、眼、胃肠(例如,胃、小肠、大肠、结肠、直肠)、呼吸道(例如,鼻、咽、气管和支气管膜)、生殖器(例如,阴道、宫颈和尿道膜)。制剂可以使用大于10-200nm的纳米颗粒,其对于较高的药物包封效率和提供多种药物持续递送的能力是优选的,该药物被认为过大而不能通过粘膜屏障快速扩散。纳米颗粒的动态转运可以使用荧光漂白恢复(FRAP)和高分辨率多颗粒跟踪(MPT)来测量。可以制备用于控释和/或靶向递送的制剂。被工程改造以穿透粘液的脂质纳米颗粒可以包含表面改变剂,如但不限于mRNA、阴离子蛋白质(例如,牛血清白蛋白)、表面活性剂(例如,阳离子表面活性剂,如例如二甲基二-十八烷基溴化铵)、糖或糖衍生物(例如,环糊精)、核酸、聚合物(例如,肝素、聚乙二醇和泊洛沙姆)、粘液溶解剂(例如,N-乙酰半胱氨酸、艾蒿、菠萝蛋白酶、木瓜蛋白酶、大青属(clerodendrum)、乙酰半胱氨酸、溴己新、羧甲司坦、依普拉酮、美司钠、氨溴索、索布瑞醇、多米奥醇、来托司坦、司替罗宁、硫普罗宁、凝溶胶蛋白、胸腺素β4、阿法链道酶、奈替克新、厄多司坦)和包括rhDNase在内的各种DNA酶。表面改变剂可以包埋或拌入在颗粒的表面中或者(例如,通过涂覆、吸附、共价键或其他过程)设置或分散在脂质纳米颗粒的表面上。
在另外的实施方案中,本公开的向导RNA和CRISPR系统可以配制为脂质复合物,如但不限于ATUPLEXTM系统、DACC系统、DBTC系统和其他siRNA-脂质复合物技术。脂质体、脂质复合物或脂质纳米颗粒可以用于改善经修饰的向导RNA的功效,如通过增加细胞转染、增加编码蛋白的翻译或提高稳定性。细胞穿透肽可以与本公开的药物制剂一起使用,如附接至促进递送至细胞内空间的聚阳离子的细胞穿透肽序列,例如,HIV衍生的TAT肽、穿透蛋白、转运蛋白或hCT衍生的细胞穿透肽。在另一实施方案中,可以使用靶向特定细胞类型的脂质纳米颗粒。可替代地,可以将脂质纳米颗粒包封到本领域已知的任何聚合物或水凝胶中,当注射到对象中时,其可以形成凝胶。作为另一非限制性实例,可以将脂质纳米颗粒包封到可生物降解的聚合物基质中。在仍另一实施方案中,药物组合物可以是缓释制剂。在另一实施方案中,缓释制剂可以用于皮下递送。缓释制剂可以包括但不限于PLGA微球、乙烯乙酸乙烯酯(EVAc)、泊洛沙姆、(纳米疗法公司(Nanotherapeutics,Inc.),阿拉楚阿(Alachua),佛罗里达州)、/>(奥洛兹美医疗(Halozyme Therapeutics),圣地亚哥,加利福尼亚州)、外科密封剂(如纤维蛋白原聚合物(爱惜康公司(Ethicon Inc.),科尼利亚,佐治亚州))、/>(百特国际有限公司(Baxter International,Inc),迪尔菲尔德,伊利诺伊州)、基于PEG的密封剂以及/>(百特国际有限公司,迪尔菲尔德,伊利诺伊州)。
在一些实施方案中,如本文所述的核酸(如向导RNA)可以与CRISPR酶复合。在一些实施方案中,可以经由包括一个或多个载体的载体系统递送复合体的部分或全部。在一些实施方案中,载体可以是DNA载体。在其他实施方案中,载体可以是RNA载体。在一些实施方案中,RNA载体可以是mRNA,例如编码核酸酶(如Cas9)的mRNA。在一些实施方案中,载体可以是环状的。在其他实施方案中,载体可以是线性的。非限制性的示例性载体包括质粒、噬菌粒、粘粒、人工染色体、微染色体、转座子、病毒载体以及表达载体。在一些实施方案中,核酸酶由RNA载体(例如,作为mRNA)提供,并且模板由病毒载体提供。在一些实施方案中,载体可以是病毒载体。在一些实施方案中,病毒载体可以从其野生型对应物进行遗传修饰。例如,病毒载体可以包括一个或多个核苷酸的插入、缺失或取代,以促进克隆或使得载体的一种或多种特性改变。此类特性可以包括包装能力、转导效率、免疫原性、基因组整合、复制、转录以及翻译。在一些实施方案中,可以缺失病毒基因组的一部分,使得病毒能够包装具有更大大小的外源性序列。在一些实施方案中,病毒载体可以具有增强的转导效率。在一些实施方案中,可以降低宿主中病毒诱导的免疫应答。在一些实施方案中,促进病毒序列整合至宿主基因组的病毒基因(如,例如整合酶)可以突变,使得病毒变成非整合。在一些实施方案中,病毒载体可以是复制缺陷型的。在一些实施方案中,病毒载体可以包括外源性转录或翻译控制序列,以驱动载体上的编码序列表达。在一些实施方案中,病毒可以是辅助依赖性的。例如,病毒可能需要一种或多种辅助病毒来提供将载体扩增和包装成病毒颗粒所需的病毒组分(如,例如病毒蛋白)。在这种情况下,可以将一种或多种辅助组分(包括一种或多种编码病毒组分的载体)与本文所述的载体系统一起引入到宿主细胞中。在其他实施方案中,病毒可以是无辅助的。例如,病毒可以能够扩增和包装载体,而不需要任何辅助病毒。在一些实施方案中,本文所述的载体系统还可以编码病毒扩增和包装所需的病毒组分。
非限制性的示例性病毒载体包括腺相关病毒(AAV)载体、慢病毒载体、腺病毒载体、单纯疱疹病毒(HSV-1)载体、噬菌体T4、杆状病毒载体以及逆转录病毒载体。在一些实施方案中,病毒载体可以是AAV载体。在其他实施方案中,病毒载体可以是慢病毒载体。在一些实施方案中,慢病毒可以是非整合的。在一些实施方案中,病毒载体可以是腺病毒载体。在一些实施方案中,腺病毒可以是高克隆能力或“裸(gutless)”腺病毒,其中除5’和3’端反向重复(ITR)和包装信号(Ψ)之外的所有编码病毒区域从病毒中缺失,以提高其包装能力。在其他实施方案中,病毒载体可以是HSV-1载体。在一些实施方案中,基于HSV-1的载体是辅助依赖性的,而在其他实施方案中,它是非辅助依赖性的。例如,仅保留包装序列的扩增子载体需要具有用于包装的结构组分的辅助病毒,而除去非必需病毒功能的30kb缺失的HSV-1载体不需要辅助病毒。在另外的实施方案中,病毒载体可以是噬菌体T4。在一些实施方案中,当病毒头部清空时,噬菌体T4可以能够包装任何线性或环状DNA或RNA分子。在另外的实施方案中,病毒载体可以是杆状病毒载体。在仍另外的实施方案中,病毒载体可以是逆转录病毒载体。在使用具有较小克隆能力的AAV或慢病毒载体的实施方案中,可能需要使用多于一种载体来递送如本文公开的载体系统的所有组分。例如,一种AAV载体可以含有编码Cas9蛋白的序列,同时第二种AAV载体可以含有一个或多个引导序列以及一个或多个拷贝的模板。
在某些实施方案中,病毒载体可以被修饰,以靶向特定的组织或细胞类型。例如,可以改变病毒表面蛋白,以减少或消除结合至其天然细胞表面受体的病毒蛋白。在一些实施方案中,载体可以被修饰以用于肝脏特异性递送。表面蛋白也可以被工程改造,以与对期望的细胞类型具有特异性的受体相互作用。病毒载体可以具有改变的宿主向性,包括有限的或重定向的向性。在一些实施方案中,病毒载体可以被工程改造,以表达或展示第一结合部分。第一结合部分可以与病毒表面蛋白或糖蛋白融合、与病毒缀合、与病毒体化学交联、与病毒包膜结合,或通过任何其他合适的方法与病毒载体连接。第一结合部分能够结合至第二结合部分,其可以用于将病毒引导至期望的细胞类型。在一些实施方案中,第一结合部分是抗生物素蛋白、链霉亲和素、中性抗生物素蛋白、captavidin或另一生物素结合部分,并且第二结合部分是生物素或其类似物。然后可以将生物素化的靶向剂结合至病毒载体上的抗生物素蛋白,并用于将病毒引导至所需的细胞类型。例如,T4载体可以被工程改造,以在其表面蛋白中的一种或多种上展示生物素结合部分。然后可以通过结合引导至所选细胞的生物素化抗体或配体来改变此类T4载体的细胞特异性。在可替代的实施方案中,第一结合部分和第二结合部分是半抗原和抗-半抗原结合蛋白;地高辛配基和抗地高辛配基结合蛋白;荧光素和抗荧光素结合蛋白;或为结合配偶体的任何其他合适的第一结合部分和第二结合部分。
在一些实施方案中,载体可以能够驱动细胞中一种或多种编码序列的表达。在一些实施方案中,细胞可以是原核细胞,如,例如细菌细胞。在一些实施方案中,细胞可以是真核细胞,如,例如酵母、植物、昆虫或哺乳动物细胞。在一些实施方案中,真核细胞可以是哺乳动物细胞。在一些实施方案中,真核细胞可以是啮齿动物细胞。在一些实施方案中,真核细胞可以是人类细胞。在不同类型的细胞中驱动表达的合适的启动子是本领域已知的。在一些实施方案中,启动子可以是野生型的。在其他实施方案中,启动子可以被修饰以用于更有效或高效地表达。在其他实施方案中,启动子可以是截短的但保留其功能。例如,启动子可以具有适合于将载体正确包装到病毒中的正常大小或减小的大小。
在一些实施方案中,载体可以包括编码本文所述的核酸酶的核苷酸序列。在一些实施方案中,载体系统可以包括一个拷贝的编码核酸酶的核苷酸序列。在其他实施方案中,载体系统可以包括多于一个拷贝的编码核酸酶的核苷酸序列。在一些实施方案中,编码核酸酶的核苷酸序列可以可操作地连接到至少一个转录或翻译控制序列。在一些实施方案中,编码核酸酶的核苷酸序列可以可操作地连接到至少一个启动子。在一些实施方案中,编码核酸酶的核苷酸序列可以可操作地连接到至少一个转录或翻译控制序列。
在一些实施方案中,启动子可以是组成型、诱导型或组织特异性的。在一些实施方案中,启动子可以是组成型启动子。非限制性的示例性组成型启动子包括巨细胞病毒立即早期启动子(CMV)、猿猴病毒(SV40)启动子、腺病毒主要晚期(MLP)启动子、劳斯肉瘤病毒(RSV)启动子、小鼠乳腺肿瘤病毒(MMTV)启动子、磷酸甘油酸激酶(PGK)启动子、延长因子-α(EF1α)启动子、泛素启动子、肌动蛋白启动子、微管蛋白启动子、免疫球蛋白启动子、其功能性片段或前述中任一种的组合。在一些实施方案中,启动子可以是CMV启动子。在一些实施方案中,启动子可以是截短的CMV启动子。在其他实施方案中,启动子可以是EF1α启动子。在一些实施方案中,启动子可以是诱导型启动子。非限制性的示例性诱导型启动子包括可由热休克、光、化学品、肽、金属、类固醇、抗生素或醇诱导的那些。在一些实施方案中,诱导型启动子可以是具有低基础(非诱导)表达水平的启动子,如,例如启动子(Clontech)。在一些实施方案中,启动子可以是组织特异性启动子。在一些实施方案中,组织特异性启动子仅或主要在肝脏组织中表达。非限制性的示例性组织特异性启动子包括B29启动子、CD14启动子、CD43启动子、CD45启动子、CD68启动子、结蛋白启动子、弹性蛋白酶-1启动子、内皮糖蛋白启动子、纤连蛋白启动子、Flt-1启动子、GFAP启动子、GPIIb启动子、ICAM-2启动子、INF-β启动子、Mb启动子、Nphsl启动子、OG-2启动子、SP-B启动子、SYN1启动子以及WASP启动子。
在一些实施方案中,载体可以编码Cas蛋白或Cas蛋白的一部分,如Cas9蛋白或Cpf1蛋白。载体系统还可以包括有包括编码本文所述的向导RNA的核苷酸序列的载体。在一些实施方案中,载体系统可以包括一个拷贝的向导RNA。在其他实施方案中,载体系统可以包括多于一个拷贝的向导RNA。在具有多于一种向导RNA的实施方案中,向导RNA可以不相同,使得它们靶向不同的靶序列或具有其他不同的特性,如Cas9RNP复合体内的活性或稳定性。在一些实施方案中,编码向导RNA的核苷酸序列可以可操作地连接到至少一个转录或翻译控制序列。在一些实施方案中,编码向导RNA的核苷酸序列可以可操作地连接到至少一个启动子。在一些实施方案中,启动子可以由RNA聚合酶III(Pol III)识别。Pol III启动子的非限制性实例包括U6、H1以及tRNA启动子。在一些实施方案中,编码向导RNA的核苷酸序列可以可操作地连接至小鼠或人U6启动子。在其他实施方案中,编码向导RNA的核苷酸序列可以可操作地连接至小鼠或人H1启动子。在一些实施方案中,编码向导RNA的核苷酸序列可以可操作地连接至小鼠或人tRNA启动子。在具有多于一种向导RNA的实施方案中,用于驱动表达的启动子可以相同或不同。在一些实施方案中,编码向导RNA的crRNA的核苷酸和编码向导RNA的tracr RNA的核苷酸可以在相同的载体上提供。在一些实施方案中,编码crRNA的核苷酸和编码tracr RNA的核苷酸可以由相同的启动子驱动。在一些实施方案中,crRNA和tracr RNA可以转录为单一转录物。例如,可以从单一转录物加工crRNA和tracr RNA,以形成双分子向导RNA。可替代地,crRNA和tracr RNA可以转录为单分子向导RNA。在其他实施方案中,crRNA和tracr RNA可以由它们相同载体上的相应启动子驱动。在其他实施方案中,crRNA和tracr RNA可以由不同的载体编码。
在一些实施方案中,载体系统还可以包括有包括本文所述的模板的载体。在一些实施方案中,载体系统可以包括一个拷贝的模板。在其他实施方案中,载体系统可以包括多于一个拷贝的模板。在一些实施方案中,载体系统可以包括2、3、4、5、6、7、8、9、10或更多个拷贝的模板。在一些实施方案中,载体系统可以包括4、5、6、7、8或更多个拷贝的模板。在一些实施方案中,载体系统可以包括5、6、7或更多个拷贝的模板。在一些实施方案中,载体系统可以包括6个拷贝的模板。模板的多个拷贝可以位于相同或不同的载体上。模板的多个拷贝也可以彼此相邻,或者被其他核苷酸序列或载体元件分离。在其他实施方案中,可以提供两个或更多个模板,使得同源重组可以发生在两个或更多个靶位点处。例如,可以提供不同的模板来修复细胞中的单个基因或细胞中的两个不同基因。在一些实施方案中,可以以独立的拷贝数提供不同的模板。
载体系统可以包括1-3个载体。在一些实施方案中,载体系统可以包括一个单一载体。在其他实施方案中,载体系统可以包括两个载体。在另外的实施方案中,载体系统可以包括三个载体。
在一些实施方案中,编码核酸酶的核苷酸序列和模板可以位于相同或单独的载体上。在一些实施方案中,编码核酸酶的核苷酸序列和模板可以位于相同的载体上。在一些实施方案中,编码核酸酶的核苷酸序列和模板可以位于单独的载体上。序列可以在载体上以相同或不同的方向和任意顺序取向。
在一些实施方案中,编码Cas9蛋白的核苷酸序列和模板可以位于相同或单独的载体上。在一些实施方案中,序列中的全部可以位于相同的载体上。在一些实施方案中,两个或更多个序列可以位于相同的载体上。序列可以在载体上以相同或不同的方向和任意顺序取向。在一些实施方案中,编码Cas9蛋白的核苷酸序列和编码向导RNA的核苷酸序列可以位于相同的载体上。在一些实施方案中,编码Cas9蛋白的核苷酸序列和模板可以位于相同的载体上。在特定实施方案中,载体系统可以包括有包括编码Cas9蛋白的核苷酸序列的第一载体以及包括编码模板或模板的多个拷贝的核苷酸序列的第二载体。
在一些实施方案中,模板可以通过由载体系统编码的核酸酶系统从其所位于的载体释放。在一些实施方案中,模板可以通过由mRNA提供的Cas9蛋白从载体释放。模板可以包括至少一个由向导RNA识别的靶序列。在一些实施方案中,模板可以在模板的5’和3’端处侧接靶序列。在表达Cas9蛋白和递送向导RNA后,向导RNA可以与模板两端的靶序列杂交,并且Cas9蛋白可以切割该靶序列,使得模板从载体释放。在另外的实施方案中,通过在模板的5’和3’端由核酸酶识别靶序列,由载体系统编码的核酸酶可以从载体释放模板。在模板的任一端的靶序列可以被取向为使得PAM序列更接近模板。在此类取向上,从载体释放之后,较少的非模板核酸保留在模板的末端。在一些实施方案中,模板侧翼的靶序列可以相同。在一些实施方案中,模板侧翼的靶序列可以与例如通过HR、HDR或非同源性末端连接并入模板的切割位点处发现的靶序列相同。在其他实施方案中,模板侧翼的靶序列可以不同。例如,模板5’端的靶序列可以由一种向导RNA或核酸酶识别,而模板3’端的靶序列可以由另一种向导RNA或核酸酶识别。
在一些实施方案中,编码核酸酶系统的载体可以在载体内包括至少一个靶序列,以产生自毁(或“自切割”或“自失活”)载体系统,从而控制待表达的核酸酶系统的量。在一些实施方案中,自毁载体系统导致核酸酶活性的量降低。在另外的实施方案中,自毁载体系统导致载体核酸的量减少。在其中系统包括Cas9的实施方案中,其还包括识别靶序列的向导RNA。以这种方式,可以暂时控制核酸酶系统的停留时间和/或活性水平,以避免与核酸酶系统过表达相关的副作用。此类副作用可以包括例如核酸酶的脱靶标效应。在一些实施方案中,一个或多个靶序列可以位于载体上的任何位置处,使得在核酸酶表达后,核酸酶识别并切割含有核酸酶编码序列的载体中的靶序列。自毁载体的一个或多个靶序列可以相同。任选地,自毁载体可以包括多个靶序列。在一些实施方案中,靶序列处的切割可以减少核酸酶系统的至少一种组分(如,例如Cas9)的表达。在一些实施方案中,切割可以减少核酸酶转录物的表达。例如,靶序列可以位于编码核酸酶的核苷酸序列内,使得切割导致编码区的破坏。在其他实施方案中,靶序列可以位于编码核酸酶的载体上的非编码区内。在一些实施方案中,靶序列可以位于驱动核酸酶表达的启动子内,使得切割导致启动子序列的破坏。例如,载体可以含有靶向Cas9序列的靶序列(及其相应的向导RNA)。在某些实施方案中,靶序列可以位于启动子和编码核酸酶的核苷酸序列之间,使得切割导致编码序列与其启动子分离。在某些实施方案中,包括在核酸酶编码序列以外的靶序列和在核酸酶编码序列内的靶序列。
在一些实施方案中,编码Cas9蛋白的载体可以包括至少一个由向导RNA识别的靶序列。在一些实施方案中,靶序列可以位于载体上的任何位置处,使得在表达Cas9蛋白和向导RNA后,向导RNA与编码Cas9蛋白的载体中的靶序列杂交,并且Cas9蛋白切割该靶序列。在一些实施方案中,靶序列处的切割可以减少Cas9蛋白转录物的表达。例如,靶序列可以位于编码Cas9蛋白的核苷酸序列内,使得切割导致编码区的破坏。在其他实施方案中,靶序列可以位于编码Cas9蛋白的载体上的非编码区内。在一些实施方案中,靶序列可以位于驱动Cas9蛋白表达的启动子内,使得切割导致启动子序列的破坏。在一些实施方案中,靶序列可以位于编码Cas9蛋白的核苷酸序列内,使得切割导致编码序列的破坏。在其他实施方案中,靶序列可以位于启动子和编码Cas9蛋白的核苷酸序列之间,使得切割导致编码序列与其启动子分离。
用于释放模板、用于载体自毁以及用于细胞中核酸酶系统靶向的靶序列可以相同或不同。例如,在模板的3’端处的靶序列可以存在于驱动核酸酶(例如,Cas9蛋白)表达的启动子内,使得模板的释放同时导致核酸酶(例如,Cas9蛋白)表达的破坏。在一些实施方案中,模板侧翼的靶序列、用于破坏核酸酶(例如,Cas9蛋白)表达的靶序列以及细胞中靶核酸分子中的靶序列可以是由单个向导RNA或核酸酶识别的相同序列。因此,在一些实施方案中,载体系统可以仅包括一种类型的靶序列,并且核酸酶系统可以仅包括一种向导RNA。在其他实施方案中,这些靶序列可以包括由不同向导RNA识别的不同序列。
在一些实施方案中,载体系统可以包括诱导型启动子,以仅在其被递送至靶细胞之后开始表达。非限制性的示例性诱导型启动子包括可由热休克、光、化学品、肽、金属、类固醇、抗生素或醇诱导的那些。在一些实施方案中,诱导型启动子可以是具有低基础(非诱导)表达水平的启动子,如例如启动子(Clontech)。
在另外的实施方案中,载体系统可以包括组织特异性启动子,以仅在其被递送到特定组织中后启动表达。非限制性的示例性组织特异性启动子包括白蛋白启动子、α-1抗胰蛋白酶启动子、血红素结合蛋白启动子、B29启动子、CD14启动子、CD43启动子、CD45启动子、CD68启动子、结蛋白启动子、弹性蛋白酶-1启动子、内皮糖蛋白启动子、纤连蛋白启动子、Flt-1启动子、GFAP启动子、GPIIb启动子、ICAM-2启动子、INF-β启动子、Mb启动子、Nphsl启动子、OG-2启动子、SP-B启动子、SYN1启动子以及WASP启动子。在特定实施方案中,组织特异性启动子是白蛋白启动子、α-1抗胰蛋白酶启动子、乙型肝炎病毒核心启动子或血红素结合蛋白基因启动子。在Kramer等人,Molecular Therapy 7(3):375-385(2003)(其通过引用以其整体并入本文)中描述了检查肝脏特异性启动子的方法。
在本公开的一些实施方案中,核酸酶系统的活性可以暂时通过调节核酸酶系统的表达组分的停留时间、量和/或活性来调控。例如,如本文所述,核酸酶可以与能够改变核酸酶的细胞内半衰期的蛋白质结构域融合。在涉及两个或更多个载体(例如,本文所述的组分编码在两个或更多个单独的载体上的载体系统)的某些实施方案中,核酸酶系统的活性可以暂时通过控制递送载体的时间来调控。例如,在一些实施方案中,编码核酸酶系统的载体可以在编码模板的载体之前递送核酸酶。在其他实施方案中,编码模板的载体可以在编码核酸酶系统的载体之前递送模板。在一些实施方案中,编码核酸酶系统和模板的载体同时递送。在某些实施方案中,同时递送的载体暂时递送例如核酸酶、模板和/或向导RNA组分。在另外的实施方案中,从载体上的编码序列转录的RNA(如,例如核酸酶转录物)还可以包括至少一个元件,该元件能够改变RNA的细胞内半衰期和/或调节翻译控制。在一些实施方案中,RNA的半衰期可以增加。在一些实施方案中,RNA的半衰期可以降低。在一些实施方案中,元件可以能够提高RNA的稳定性。在一些实施方案中,元件可以能够降低RNA的稳定性。在一些实施方案中,元件可以在RNA的3’UTR内。在一些实施方案中,元件可以包括多腺苷酸化信号(PA)。在一些实施方案中,元件可以包括帽,例如,上游mRNA末端。在一些实施方案中,可以将PA添加到RNA的3’UTR。在一些实施方案中,RNA可以不包括PA,使得它在转录之后在细胞中经历更快降解。在一些实施方案中,元件可以包括至少一个富含AU的元件(ARE)。ARE可以通过ARE结合蛋白(ARE-BP)以依赖于组织类型、细胞类型、时间、细胞定位和环境的方式结合。在一些实施方案中,去稳定元件可以促进RNA衰变、影响RNA稳定性或激活翻译。在一些实施方案中,ARE的长度可以包括50至150个核苷酸。在一些实施方案中,ARE可以包括至少一个拷贝的序列AUUUA。在一些实施方案中,可以将至少一个ARE添加到RNA的3’UTR。在一些实施方案中,元件可以是土拨鼠肝炎病毒(WHP)转录后调控元件(WPRE),其产生三级结构以增强来自转录物的表达。在另外的实施方案中,如例如Zufferey等人,J Virol,73(4):2886-92(1999)和Flajolet等人,J Virol,72(7):6175-80(1998)中所述的,元件是经修饰的和/或截短的WPRE序列,其能够增强来自转录物的表达。在一些实施方案中,可以将WPRE或等效物添加到RNA的3’UTR。在一些实施方案中,元件可以选自富集于快速或缓慢衰变转录物的其他RNA序列基序。
本公开的实施方案还涵盖用本文所述的载体系统治疗患者。在一些实施方案中,该方法可以包括向患者施用本文所述的载体系统。该方法可以作为单一疗法使用,或者与本领域可用的其他疗法组合使用。在一些实施方案中,患者可以在疾病相关基因中具有突变(如,例如插入、缺失、取代、染色体易位)。在一些实施方案中,施用载体系统可以导致突变,包括患者中的疾病相关基因的一个或多个核苷酸的插入、缺失或取代。某些实施方案可以包括修复患者疾病相关基因中的突变的方法。在一些实施方案中,突变可以导致由疾病相关基因表达的蛋白质中的一个或多个氨基酸改变。在一些实施方案中,突变可以导致由疾病相关基因表达的RNA中的一个或多个核苷酸改变。在一些实施方案中,突变可以改变疾病相关基因的表达水平。在一些实施方案中,突变可以导致基因表达的增加或减少。在一些实施方案中,突变可以导致患者的基因敲低。在一些实施方案中,施用载体系统可以导致患者疾病相关基因中突变的纠正。在一些实施方案中,施用载体系统可以导致患者的基因敲除。在一些实施方案中,施用载体系统可以导致疾病相关基因的外显子序列、内含子序列、转录控制序列、翻译控制序列或非编码序列的置换。
在一些实施方案中,施用载体系统可以导致模板的外源性序列整合到患者的基因组DNA中。在一些实施方案中,外源性序列可以包括可操作地连接至外源性启动子序列的蛋白质或RNA编码序列,使得在外源性序列整合到患者基因组DNA中后,患者能够表达由整合的序列编码的蛋白质或RNA。外源性序列可以提供补充的或置换的蛋白质编码或非编码序列。例如,施用载体系统可以导致患者中疾病相关基因的突变部分的置换。在一些实施方案中,突变部分可以包括疾病相关基因的外显子。在其他实施方案中,外源性序列的整合可以导致整合序列由存在于患者的基因组DNA上的内源性启动子序列表达。例如,施用载体系统可以导致提供疾病相关基因的功能基因产物,以纠正患者的突变。在一些实施方案中,施用载体系统可以导致编码蛋白质或蛋白质的一部分的cDNA序列的整合。在其他实施方案中,施用载体系统可以导致外显子序列、内含子序列、转录控制序列、翻译控制序列或非编码序列整合至患者的基因组DNA中。在一些实施方案中,施用载体系统可以导致患者的基因敲入。
施用
本文提供了用于编辑细胞中的靶核酸的方法和组合物。本文还提供了用于改变对象的细胞中靶基因的功能和活性的药物组合物和方法。本文所述的基因组编辑组合物可以以治疗有效量施用至有需要的对象,以治疗与高循环胆固醇水平和/或冠状动脉疾病(例如高胆固醇血症)、升高的总胆固醇水平、升高的低密度脂蛋白(LDL)水平、升高的LDL-胆固醇水平、降低的高密度脂蛋白水平、肝脏脂肪变性、冠心病、局部缺血、中风、周围血管疾病、血栓形成、2型糖尿病、升高的高血压、动脉粥样硬化、肥胖症、阿尔茨海默病、神经变性及其组合相关联的病状,其可以以多种方式施用至对象,包括肠胃外、静脉内、皮内、肌内、结肠、直肠或腹膜内。在一些实施方案中,药物组合物可以与药学上可接受的盐通过对象的腹膜内注射、肌内注射、皮下注射或静脉内注射共同施用。在一些实施方案中,药物组合物可以直接注射至特定组织,如肝脏组织。在一些实施方案中,药物组合物可以经肠胃外、静脉内、肌内或口服施用。口服制剂还可以被包衣或处理,以防止或减少在胃中溶解。可以使用本领域已知的任何合适的方法向对象施用本公开的组合物。用于本公开的合适的制剂和递送方法通常是本领域熟知的。例如,本公开的组合物可以与药学上可接受的稀释剂、载剂或赋形剂一起配制为药物组合物。组合物可以含有如接近生理条件所需的药学上可接受的辅助物质,包括pH调节和缓冲剂、张力调节剂、润湿剂等,如例如,乙酸钠、乳酸钠、氯化钠、氯化钾、氯化钙、脱水山梨醇单月桂酸酯、三乙醇胺油酸酯等。
本文所述的药物制剂可以通过多种施用途径以多种方式施用至对象,包括但不限于口服、肠胃外(例如,静脉内、皮下、肌内、髓内注射、鞘内、直接心室内、腹膜内、淋巴管内、鼻内注射)、鼻内、颊、局部或经皮施用途径。本文所述的药物制剂包括但不限于水性液体分散体、自乳化分散体、固体溶液、脂质体分散体、气溶胶、固体剂型、粉末、速释制剂、控释制剂、速熔制剂、片剂、胶囊、丸剂、延迟释放制剂、缓释制剂、脉冲释放制剂、多颗粒制剂以及混合的速释制剂和控释制剂。
在一些实施方案中,药物制剂为片剂形式。在其他实施方案中,含有本文所述的组合物或抑制剂的药物制剂为胶囊形式。在一个方面,用于口服施用的液体制剂剂型为水性悬浮液或溶液形式,其选自包括但不限于水性口服分散体、乳液、溶液、酏剂、凝胶和糖浆。
对于通过吸入的施用,本文所述的组合物或抑制剂可以被配制成用作气溶胶、雾剂或粉末。对于颊或舌下施用,组合物可以采用以常规方式配制的片剂、锭剂或凝胶的形式。在一些实施方案中,本文所述的组合物或抑制剂可以被制备为经皮剂型。在一些实施方案中,本文所述的组合物或抑制剂可以被配制为适合于肌内、皮下或静脉内注射的药物组合物。在一些实施方案中,本文所述的组合物或抑制剂可以局部施用,并且可以被配制为多种可局部施用的组合物,如溶液、悬浮液、洗剂、凝胶、糊剂、含药棒、香膏、乳膏或软膏。在一些实施方案中,本文所述的组合物或抑制剂可以被配制为直肠组合物,如灌肠剂、直肠凝胶、直肠泡沫、直肠气溶胶、栓剂、胶冻栓剂或保留灌肠剂。
剂量
如本领域技术人员认识到的,用于施用的适当的剂量或有效量根据所治疗的特定病状、病状的严重程度、个体对象参数(包括年龄、身体状况、体型、性别和体重)、治疗的持续时间、并行疗法的性质(如果有的话)、施用的具体途径以及健康护理人员的知识和专业内的类似因素而变化。剂量确定中涉及的因素是本领域普通技术人员已知的,除常规测试以外无需额外的实验。通常优选的是,使用单独的组分或其组合的最大剂量,即,根据合理的医学判断的最高安全剂量。经验上的考虑(如半衰期)通常将有助于剂量的确定。例如,与人免疫系统相容的治疗性药剂(如包括来自人源化抗体或完全人抗体的区域的多肽)可以用于延长多肽的半衰期,并且防止多肽受到宿主的免疫系统的攻击。
施用的频率可以在疗法过程中确定和调节,并且通常但不一定基于疾病的治疗和/或抑制和/或改善和/或延迟。可替代地,多肽或多核苷酸的持续连续释放制剂可能是合适的。用于实现持续释放的各种制剂和装置是本领域已知的。在一些实施方案中,剂量是每天、每两天、每三天、每四天、每五天或每六天。在一些实施方案中,给药频率为每周、每2周、每4周、每5周、每6周、每7周、每8周、每9周或每10周一次;或每月、每2个月或每3个月或更长时间一次。这种疗法的进展容易通过常规技术和测定来监测。
给药方案可以随时间改变。在一些实施方案中,对于正常体重的成年对象,可以施用在约0.01至1000mg/kg的范围内的剂量。在一些实施方案中,剂量为1至200mg。在一些实施方案中,剂量的范围可以为约0.01至0.05mg/kg、约0.01至0.1mg/kg、约0.01至1mg/kg、约0.01至10mg/kg、约0.01至100mg/kg、0.01至500mg/kg、约0.1至1mg/kg、约0.1至5mg/kg、约0.1至10mg/kg、约0.1至100mg/kg、约0.1至500mg/kg、约0.1至1000mg/kg、约1至5mg/kg、约1至10mg/kg、约1至100mg/kg、约1至500mg/kg、约1至1000mg/kg、约10至100mg/kg、约10至500mg/kg、约10至1000mg/kg或约100至1000mg/kg。特定的给药方案(即,剂量、时间和重复)将取决于特定对象和该对象的病史,以及多肽或多核苷酸的性质,如多肽或多核苷酸的半衰期,以及本领域熟知的其他考虑。
如对于本领域技术人员显而易见的是,如本文所述的治疗性药剂的适当剂量将取决于所用的具体药剂(或其组合物)、制剂和施用途径、疾病的类型和严重程度、多肽或多核苷酸是否出于预防性或治疗性目的施用、先前的疗法、对象的临床病史和对拮抗剂的应答,以及主治医生的判断。通常,临床医生将施用多肽,直到达到实现期望的结果的剂量。
一种或多种治疗性组合物(例如多肽、多核苷酸或RNP)的施用可以是连续的或间歇的,这取决于例如接受者的生理状况、施用的目的是治疗性的还是预防性的以及技术从业者已知的其他因素。多肽的施用可以在预选的时间段内基本上是连续的,或者可以是以一系列间隔的剂量,例如,在疾病发展之前、期间或之后。
生物样品
样品(例如,生物样品)可以取自对象。生物样品可以包括多个生物样品。多个生物样品可以含有两个或更多个生物样品;例如,约2-1000、2-500、2-250、2-100、2-75、2-50、2-25、2-10、10-1000、10-500、10-250、10-100、10-75、10-50、10-25、25-1000、25-500、25-250、25-100、25-75、25-50、50-1000、50-500、50-250、50-100、50-75、60-70、100-1000、100-500、100-250、250-1000、250-500、500-1000、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、30、35、40、45、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、90、95、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、275、300、325、350、375、400、425、450、475、500、550、600、650、700、750、800、850、900、950、1000或更多个生物样品。生物样品可以从多个对象中获得,得到多个样品的多个集合。生物样品可以从约2至约1000个对象或更多对象中获得;例如,约2-1000、2-500、2-250、2-100、2-50、2-25、2-20、2-10、10-1000、10-500、10-250、10-100、10-50、10-25、10-20、15-20、25-1000、25-500、25-250、25-100、25-50、50-1000、50-500、50-250、50-100、100-1000、100-500、100-250、250-1000、250-500、500-1000,或至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、30、35、40、45、50、55、60、65、68、70、75、80、85、90、95、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、275、300、325、350、375、400、425、450、475、500、550、600、650、700、750、800、850、900、950或1000或更多个对象。
生物样品可以从人类对象中获得。生物样品可以从不同年龄的人类对象中获得。人类对象可以是产前的(例如,胎儿)、儿童(例如,新生儿、婴儿、学步儿童、青春期前儿童)、青少年、青春期青少年或成人(例如,早期成人、中年成人、老年人)。人类对象可以为约0个月至约120岁或更大年龄。人类对象可以为约0至约12个月;例如,约1、2、3、4、5、6、7、8、9、10、11或12个月。人类对象可以为约0至12岁;例如,约0至30天;约1个月至12个月;约1岁至3岁;约4岁至5岁;约4岁至12岁;约1、2、3、4、5、6、7、8、9、10、11或12岁。人类对象可以为约13岁至19岁;例如,约13、14、15、16、17、18或19岁。人类对象可以为约20岁至约39岁;例如,约20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38或39岁。人类对象可以为约40岁至约59岁;例如,约40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58或59岁。人类对象可以大于59岁;例如,约60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119或120岁。人类对象可以包括活的对象或死的对象。人类对象可以包括男性对象和/或女性对象。
生物样品可以从允许确定基因表达水平的任何合适来源中获得,例如从细胞、组织、体液或分泌物,或从其衍生的基因表达产物(例如,核酸,如DNA或RNA;多肽,如蛋白质或蛋白质片段)中获得。生物样品的性质可以取决于对象的性质。如果生物样品来自单细胞生物体或具有未分化组织的多细胞生物体的对象,则生物样品可以包括细胞,如细胞培养物的样品、生物体的切除物或整个生物体。如果生物样品来自多细胞生物体,则生物样品可以是组织样品、流体样品或分泌物。
生物样品可以从不同的组织中获得。术语组织意指包括具有共同发育起源并具有相似或相同功能的细胞的集合。术语组织还意指涵盖器官,其可以是可以具有不同起源的细胞的功能性分组和组织。生物样品可以从任何组织中获得。
生物样品可以从一个或多个人或非人动物的不同组织样品中获得。合适的组织可以包括结缔组织、肌肉组织、神经组织、上皮组织或其一部分或组合。合适的组织还可以包括肺、心脏、血管(例如,动脉、静脉、毛细血管)、唾液腺、食管、胃、肝脏、胆囊、胰腺、结肠、直肠、肛门、下丘脑、垂体、松果腺、甲状腺、甲状旁腺、肾上腺、肾、输尿管、膀胱、尿道、淋巴结、扁桃体、腺样体、胸腺、脾、皮肤、肌肉、脑、脊髓、神经、卵巢、输卵管、子宫、阴道组织、乳腺、睾丸、输精管、精囊、前列腺、阴茎组织、咽、喉、气管、支气管、隔膜、骨髓、毛囊或其组合的全部或一部分。来自人或非人动物的生物样品还可以包括体液、分泌物或排泄物;例如,生物样品可以是水状液、玻璃状液、胆汁、血液、血清、母乳、脑脊液、内淋巴、外淋巴、女性精液、羊水、胃液、月经、粘液、腹膜液、胸膜液、唾液、皮脂、精液、汗液、泪液、阴道分泌物、呕吐物、尿液、粪便或其组合的样品。生物样品可以来自健康组织、患病组织、疑似患病的组织或其组合。
在一些实施方案中,生物样品是流体样品,例如血液、血清、痰、尿液、精液或其他生物流体的样品。在某些实施方案中,样品是血液样品。在一些实施方案中,生物样品是组织样品,如用于确定组织中疾病存在与否而采取的组织样品。在某些实施方案中,样品是甲状腺组织的样品。
生物样品可以从处于疾病进展的不同阶段或不同病状的对象中获得。疾病进展的不同阶段或不同病状可以包括健康、在原发性症状的发作时、在继发性症状的发作时、在三级症状的发作时、在原发性症状过程期间、在继发性症状过程期间、在三级症状过程期间、在原发性症状结束时、在继发性症状结束时、在三级症状结束时、在原发性症状结束之后、在继发性症状结束之后、在三级症状结束之后或其组合。疾病进展的不同阶段可以是在被诊断或疑似患有疾病之后的一段时间;例如,在被诊断或疑似患有疾病之后的至少约或至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23或24小时;1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27或28天;1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20周;1、2、3、4、5、6、7、8、9、10、11或12个月;1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50年。疾病进展的不同阶段或不同病状可以包括在行动或状态之前、期间或之后;例如,用药物治疗、用手术治疗、用程序治疗、执行标准护理程序、休息、睡眠、进食、禁食、行走、跑步、执行认知任务、性活动、思考、跳跃、排尿、放松、固定不动、情感创伤、休克等。
本公开的方法提供了对来自对象或一组对象的生物样品的分析。对象可以是例如任何动物(例如,哺乳动物),包括但不限于人类、非人灵长类动物、啮齿动物、狗、猫、猪、鱼等。如本文所述,本发明的方法和组合物可以应用于来自人的生物样品。
生物样品可以通过本领域已知的方法获得,如本文提供的活检方法、拭取、刮取、静脉切开术或任何其他合适的方法。可以使用本公开的试剂盒的组分获得、储存或运输生物样品。在一些情况下,可以获得多个生物样品,如多个甲状腺样品,以用于根据本公开的方法分析、表征或诊断。在一些情况下,可以获得多个生物样品,如来自一种组织类型(例如,甲状腺)的一个或多个样品以及来自另一种组织类型(例如,颊)的一个或多个样品,以用于通过本公开的方法诊断或表征。在一些情况下,可以在相同或不同时间获得多个样品,如来自一种组织类型(例如,甲状腺)的一个或多个样品以及来自另一种组织(例如,颊)的一个或多个样品。在一些情况下,在不同时间获得的样品通过不同的方法储存和/或分析。例如,可以获得样品并通过细胞学分析(例如,使用常规染色)进行分析。在一些情况下,可以基于细胞学分析的结果从对象中获得另外的样品。疾病或病状(例如冠状动脉疾病)的诊断可以包括由医生、护士或其他医学专家检查对象。检查可以是常规检查的一部分,或者检查可以是由于具体异议,包括但不限于以下中的一种:疼痛、疾病、疾病的预期、可疑肿块或团块的存在、疾病或病状。对象可能知道或可能不知道疾病或病状。医学专家可以获得生物样品,以用于测试。在一些情况下,医学专家可以将对象转至测试中心或实验室,以用于提交生物样品。本文提供的获得方法包括活检方法,包括细针抽吸、芯针活检、真空辅助活检、切开活检、切除活检、钻取活检、刮取活检或皮肤活检。在一些情况下,本文提供的方法和组合物应用于仅来自通过FNA获得的生物样品的数据。在一些情况下,本文提供的方法和组合物应用于仅来自通过FNA或手术活检获得的生物样品的数据。在一些情况下,本文提供的方法和组合物应用于仅来自通过手术活检获得的生物样品的数据。生物样品可以通过非侵入性方法获得,此类方法包括但不限于:皮肤或子宫颈的刮取、脸颊的拭取、唾液收集、尿液收集、粪便收集、月经、泪液或精液的收集。生物样品可以通过侵入性程序获得,此类程序包括但不限于:活检、肺泡或肺灌洗、针抽吸或静脉切开术。活检的方法还可以包括切开活检、切除活检、钻取活检、刮取活检或皮肤活检。针抽吸的方法还可以包括细针抽吸、芯针活检、真空辅助活检或粗芯活检。可以通过本文的方法获得多个生物样品,以确保足够量的生物材料。用于获得生物样品的通用方法也是本领域已知的,并且还在例如Ramzy,IbrahimClinical Cytopathology and Aspiration Biopsy 2001(其通过引用以其整体并入本文)中描述。生物样品可以是甲状腺结节或疑似甲状腺肿瘤的细针抽吸物。细针抽吸取样程序可以通过使用超声、X射线或其他成像装置来引导。
在一些情况下,可以将对象转至专家,如肿瘤学家、外科医生或内分泌学家,以进一步进行诊断。专家同样可以获得生物样品,以用于测试,或者将个体转至测试中心或实验室,以用于提交生物样品。在任何情况下,生物样品可以由医生、护士或其他医学专家(如医学技术人员、内分泌学家、细胞学家、抽血者、放射科医生或肺脏学家)获得。医学专家可以指示对样品执行的适当测试或测定,或者本公开的分子分析业务可以咨询最适当地指示哪些测定或测试。分子分析业务可以为个人或其医疗或保险提供者开具账单以用于咨询工作、用于样品获取和/或储存、用于材料或用于提供的所有产品和服务。
医疗专家无需参与初始诊断或样品获取。个体可以可替代地通过使用非处方试剂盒获得样品。试剂盒可以含有如本文所述的用于获得所述样品的手段、用于储存样品以供检查的手段以及试剂盒的正确使用说明书。在一些情况下,分子分析服务包括在购买试剂盒的价格中。在其他情况下,分子分析服务被单独开具账单。
适用于分子分析业务的生物样品可以是含有待测试的个体的组织、细胞、核酸、基因、基因片段、表达产物、基因表达产物和/或基因表达产物片段的任何材料。提供了用于确定样品适合性和/或充分性的方法。生物样品可以包括但不限于组织、细胞和/或来自个体细胞或衍生自个体细胞的生物材料。样品可以是细胞或组织的异质或同质群体。可以使用本领域已知的可以提供适合于本文所述的分析方法的样品的任何方法获得生物样品。
通过使用试剂盒可以帮助获得生物样品。可以提供含有用于获得、储存和/或运输生物样品的材料的试剂盒。试剂盒可以含有例如用于收集生物样品的材料和/或仪器(例如,无菌拭子、无菌棉、消毒剂、针、注射器、手术刀、麻醉拭子、刀、刮刀、液氮等)。试剂盒可以含有例如用于储存和/或保存生物样品的材料和/或仪器(例如,容器;用于温度控制的材料,如冰、冰袋、冷袋、干冰、液氮;化学防腐剂或缓冲液,如甲醛、福尔马林、多聚甲醛、戊二醛、醇(如乙醇或甲醇)、丙酮、乙酸、HOPE固定剂(Hepes-谷氨酸缓冲液介导的有机溶剂保护效应)、肝素、盐水、磷酸盐缓冲盐水、TAPS、N,N-二羟乙基甘氨酸(bicine)、Tris、三(羟甲基)甲基甘氨酸(tricine)、TAPSO、HEPES、TES、MOPS、PIPES、cadodylate、SSC、MES、磷酸盐缓冲液;蛋白酶抑制剂,如抑肽酶、苯丁抑制素、钙蛋白酶抑制素I和II、胰凝乳蛋白酶抑制素、E-64、亮抑酶肽、α-2-巨球蛋白、pefabloc SC、胃酶抑素、苯甲磺酰氟、胰蛋白酶抑制剂;DNA酶抑制剂,如2-巯基乙醇、2-硝基-5-三氰基苯甲酸、钙、EGTA、EDTA、十二烷基硫酸钠、碘乙酸酯等;RNA酶抑制剂,如核糖核酸酶抑制剂蛋白;双蒸水;经DEPC(二乙基丙碳酸酯)处理的水等)。试剂盒可以含有使用说明书。试剂盒可以作为合适的容器提供或可以含有合适的容器,以用于运输。运输容器可以是保温容器。运输容器可以自寻址到代收者(例如,实验室、医学中心、遗传测试公司等)。试剂盒可以提供给对象以供家庭使用或由医学专家使用。可替代地,试剂盒可以直接提供给医学专家。
一个或多个生物样品可以从给定的对象中获得。在一些情况下,约1至约50个的生物样品从给定的对象中获得;例如,约1-50、1-40、1-30、1-25、1-20、1-15、1-10、1-7、1-5、5-50、5-40、5-30、5-25、5-15、5-10、10-50、10-40、10-25、10-20、25-50、25-40,或至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个生物样品可以从给定的对象中获得。来自给定的对象的多个生物样品可以从相同来源(例如,相同组织)中获得,例如,多个血液样品或多个组织样品,或者从多个来源(例如,多个组织)中获得。来自给定的对象的多个生物样品可以同时或在不同时间获得。来自给定的对象的多个生物样品可以在相同条件或不同条件下获得。来自给定的对象的多个生物样品可以在对象的相同疾病进展或不同疾病进展时获得。如果从来自特定对象的相同来源(例如,相同组织)收集多个生物样品,则可以将样品组合成单个样品。以此方式组合样品可以确保获得足够的材料用于测试和/或分析。
本文还描述了一种包括本文所述的IVT mRNA序列起始子的RNA分子。在一些实施方案中,RNA包括向导RNA或核酸酶mRNA。
本文还描述了一种含有RNA分子的细胞,所述RNA分子包括本文所述的IVT mRNA序列起始子。
本文还描述了一种含有从包括本文所述的IVT mRNA序列起始子的RNA分子翻译的多肽的细胞。
本文还描述了一种用于合成RNA分子的方法,所述方法包括:a.将本文所述的IVTmRNA序列起始子引入到包含RNA聚合酶的混合物中,和
b.将混合物温育足以允许RNA分子转录的时间。
本文还描述了一种基因编辑的方法,所述方法包括将本文所述的RNA分子或本文所述的药物组合物引入到细胞中,其中RNA分子包括向导RNA或核酸酶mRNA,其中RNA分子在细胞中翻译。
实施例
提供以下实施例以更好地说明本公开,并且这些实施例不应被解释为限制本公开的范围。就提及的具体材料而言,其仅出于说明的目的,并且不旨在限制本公开。本领域技术人员可以在不行使发明能力和不脱离本公开范围的情况下开发等效手段或反应物。
帽结构的合成
实施例1.三核苷酸帽1007a、1032a、1037a、1107a、1112a、1137a、1141a、3102a、3107a、3207a、3212a、1007c、1112c、3102c、3107c、3207c和3212c的制备
通过按照标准固相寡核苷酸合成和去保护方案(Methods in MolecularBiology,1993,20,81-114;ACS Chem.Biol.2015,10,1181-1187,通过引用以其整体并入本文)由固体支持物1和亚磷酰胺3制备二核苷酸5’-磷酸7。亚磷酰胺2购自商业来源和/或为定制合成。支持物结合完全保护的二核苷酸3的去三苯甲基化在支持物上提供了5’-去保护的二核苷酸中间体。根据报告的程序(EP 816368A1,https://www.glenresearch.com/solid-chemical-phosphorylation-reagent-ii.html,The Glen Report,2011,23,10-11),将由此获得的中间体培养成5’-磷酸化药剂4。在偶联和氧化后,用碱处理5’-磷酸化的二核苷酸,然后进行HPLC纯化,以获得完全去保护的二核苷酸5’-磷酸5(https://www.glenresearch.com/solid-chemical-phosphorylation-reagent-ii.html)。
化合物12根据报告的程序(Nucleic Acids Research,2016,44,9578;RNA,2001,7,1486;WO 2017/053297 Al)由鸟苷或2’和/或3’糖修饰的鸟苷制备。如文献(NucleicAcids Research,2016,44,9578,WO 2017/053297Al)中所述,将化合物12与二核苷酸5’-单磷酸5偶联,以提供期望的化合物1007a、1032a、1037a、1107a、1112a、1137a、1141a、3102a、3107a、3207a、3212a、1007c、1112c、3102c、3107c、3207c和3212c。
如本文实施例1中一般所述,合成了化合物1007a和1107a(图1)。产生最终量约1克的化合物1007a;该材料通过质谱和HPLC表征为具有1161道尔顿的实际质量和98.4%的纯度。此外,产生最终量约250毫克的化合物1107a;该材料通过质谱和HPLC表征为具有1161道尔顿的实际质量和97.5%的纯度。如实施例5中所述,这些化合物被用作mRNA起始子。
实施例2.三核苷酸帽1002e和1007e的制备
化合物13由肌苷或2’和/或3’糖修饰的肌苷制备(Nucleic Acids Research,2016,44,9578;RNA,2001,7,1486;WO 2017/053297 Al)。然后将化合物13与二核苷酸5’-单磷酸5偶联,以得到化合物1002e和1007e,如以上实施例1中所述。
实施例3.三核苷酸帽1002i和1007i的制备
化合物14由水粉蕈素或2’和/或3’糖修饰的水粉蕈素制备。然后将化合物13与二核苷酸5’-单磷酸5偶联,以得到化合物1002i和1007i,如以上实施例1中所述。
实施例4.四核苷酸帽5203、5204、5207、5208、5209、5210和5211的制备
通过遵循实施例1中所述的用于合成二核苷酸5’-单磷酸的类似程序,由固体支持物1制备三核苷酸5’-单磷酸7。在与5’-磷酸化药剂4反应之前,在标准固相寡核苷酸条件下,额外的亚磷酰胺与完全保护的固体支持物结合的二核苷酸的5’端偶联。然后将如此获得的化合物7与化合物12反应,以得到化合物5203、5204、5207、5208、5209、5210和5211。
实施例5.四核苷酸帽5201和5205的制备
如实施例1-4中所述,由化合物7和化合物13制备期望的化合物5201和5205。
实施例6.四核苷酸帽5202和5206的制备
如实施例1-4中所述,由化合物7和化合物14制备期望的化合物5202和5206。
实施例7. 5’加帽mRNA的一锅法制备
A.mRNA生产
5’端起始子1007a(图1A)用于制备编码ABE和荧光素酶蛋白的加帽mRNA。在该实施例中并且对于本文所述的所有其他实施例,ABE mRNA序列是MA004(SEQ.0001),并且荧光素酶mRNA序列是在NCBI参考序列XM_031473197.1中描述的萤火虫(Photinus pyralis)(萤火虫(Firefly))荧光素酶序列。这些mRNA可以通过本领域熟知的不同方法产生。本文使用的此类方法中的一种是使用T7聚合酶的体外转录(IVT);或在其他实施方案中,额外的RNA聚合酶变体。这种产生mRNA的IVT反应使用线性化的DNA模板,该模板包括T7聚合酶启动子和相关的调控序列、mRNA编码序列(CDS)、3’和5’非翻译区(UTR)、聚A尾以及促进和调节mRNA稳定性和体内性能的附加序列元件。在IVT之前,DNA模板是质粒的形式;在其他实施方案中,DNA模板是PCR产物、合成DNA产物或任何其他双链DNA构建体的形式。用限制性消化酶对DNA模板进行线性化,以便促进失控转录。典型的IVT反应包含T7聚合酶、DNA模板、RNA酶抑制剂、帽类似物、无机焦磷酸酶和天然存在的核糖核苷三磷酸(NTP),如GTP、ATP、CTP和N1-甲基假尿苷三磷酸;在一些实施方案中,NTP包括UTP或经修饰的NTP,如假尿苷、5’甲基胞苷、5-甲氧基尿苷、N6-甲基腺苷和N4-乙酰胞苷。将1007a 5’端起始子与ATP、GTP、CTP和N1-甲基假尿苷三磷酸以1:1的起始子与NTP摩尔比和实施例5(B)中所述的额外比率一起加入到IVT反应中。聚A尾编码在转录期间添加到mRNA中的DNA模板中;在一些情况下,使用RNA连接酶在IVT反应后将聚A尾添加到mRNA上。最后,向混合物中加入T7 RNA聚合酶,并且IVT反应在37℃下运行约1-4小时。在IVT之后,向转录混合物中加入DNA酶以除去DNA模板;在一些情况下,残余的DNA用色谱法去除。纯化该mRNA以除去残余的反应产物和杂质,并储存在1mM柠檬酸盐缓冲液中。通过本领域已知的UV光谱法和毛细管凝胶电泳方法进行生产产率和mRNA全长纯度的表征。编码ABE的具有5’端区域基序的mRNA(1007a)的最终生产产率为每1ml IVT反应约3.3mg(图2),并且mRNA具有约88%的全长纯度(图3)。作为比较,编码ABE的具有5’端基序的mRNA(1002a,一种本领域已知的可商购的加帽化合物)的生产产率为每1mlIVT反应约3.8mg(图2),并且mRNA具有约86%的全长纯度(图3)。类似的IVT和纯化过程用于产生编码SpCas9、Cas12b、CBE和其他ABE的mRNA;在所有情况下,DNA模板、反应条件和纯化参数都是针对感兴趣的特定基因而优化的。
类似地,编码ABE的具有5’端区域的mRNA(1107a)(图1B)如上一段所述产生并表征。具有5’端区域的mRNA(1107a)的最终生产产率为每1ml IVT反应约3.3mg(图2),并且具有约86%的全长纯度(图3)。
类似地,示例性的三核苷酸5’端起始子1007e、1007i、1002e、1002i、1032a、1037a、1112a、1137a、1141a、3102a、3107a、3207a、3212a、1007c、1107c、1112c、3102c、3107c、3207c、3212c、5212、5213和5214(在表1中描述)用于如上所述产生5’加帽mRNA,所述三核苷酸5’端起始子包含对三磷酸桥、磷酸二酯键、核糖环官能团和四核苷酸碱基的额外修饰以及其他修饰。
类似地,示例性的四核苷酸5’端起始子5201、5202、5203、5204、5205、5206、5207、5208、5209、5210和5211(如表1所述)用于如上所述产生5’加帽mRNA。
类似地,在其他实施方案中,表1中所示的三核苷酸和四核苷酸5’端起始子可以用于如在上一段中所述产生5’加帽mRNA,并且如该实施例和产生的数据所示,基于该实施例的结果,这些将显示出相似的性质。
B.mRNA 5’端起始子与NTP的摩尔比的调节
在IVT反应中产生的加帽mRNA的量与反应混合物中帽与NTP的比率成正比(Stepinski,J.等人,RNA.2006,7,1486-1495)。IVT反应中5’端起始子与NTP的比率影响变得被加帽的mRNA的量,这主要是因为帽可以与NTP竞争mRNA的5’端处的插入。二核苷酸帽结构的典型的起始子与NTP的比率是4:1,并且三核苷酸帽结构的典型的起始子与NTP的摩尔比是1:1;其中NTP代表GTP、ATP、CTP、UTP或经修饰的NTP如N1-甲基假尿苷。在二核苷酸帽的4:1的比率和三核苷酸帽的1:1的比率下,所得的mRNA将具有至少80%在5’端加帽并且高达20%未加帽的转录物的混合物,这也被描述为80%的加帽效率。加帽效率是加帽mRNA的测量的量除以加帽mRNA加上未加帽的mRNA的总量。因此,三核苷酸帽可以被认为是比二核苷酸帽更有效的加帽化合物,因为产生含有相似量的加帽5’端的最终mRNA产物需要更少的输入帽。在一些情况下,与二核苷酸帽相比,三核苷酸帽在较低的起始子与NTP比率下产生高(>90%)加帽效率的能力可以归因于三核苷酸帽对DNA模板的亲和力增加。在一些情况下,最佳的帽与NTP的比率可以随着帽结构的组成而变化,其中帽结构的修饰可以影响加帽效率。例如,与常规的磷酸二酯主链相比,具有硫代磷酸酯主链修饰的帽结构在1:1的起始子与NTP比率下可能表现出降低的加帽效率,因为硫代磷酸酯基团可以削弱互补核酸的杂交强度。出乎意料的是,用含有硫代磷酸酯的化合物1007a加帽的mRNA在从1:1到1:2.5的范围内的起始子与NTP的比率下具有大于90%的加帽效率(图4);这与使用相似的生产条件,用常规的含有磷酸二酯的5’端起始子1002a加帽的mRNA的加帽效率相似。类似地,基于前面实施例中观察到的结果,三核苷酸起始子1007e、1007i、1037a、1112a、1141a、3107a、3212a、1007c、1112c、3107c、3212c、5214和表1中描述的在前两个起始核苷酸之间具有硫代磷酸酯键的其他三核苷酸帽结构预期也具有与化合物1002a相比类似的加帽效率。
预计帽结构中三磷酸桥的硫代磷酸酯修饰不会降低加帽效率,并且含有三磷酸桥修饰的二核苷酸帽的mRNA的产生在本领域中是熟知的。有趣的是,用帽化合物1107a产生了mRNA(图2),其证明含有三磷酸桥的硫代磷酸酯修饰的三核苷酸帽可以在1:1至1:1.67的范围内的起始子与NTP的比率下以>90%的加帽效率并入到mRNA中(图4)。类似地,基于在前面实施例中看到的观察结果,表1中描述的具有三磷酸桥硫代磷酸酯修饰的三核苷酸帽结构预期具有与5’端起始子1107a相比相似的加帽效率。
此外,表1中描述的四核苷酸帽化合物5201、5202、5203、5204、5205、5206、5207、5208、5209、5210、5211和其他帽结构也可以在1:1及更低的起始子与NTP比率时产生>90%加帽效率的mRNA,这是由于与三核苷酸和二核苷酸帽相比,四核苷酸帽的杂交强度增加。
此外,如用化合物1007a和1107a制备的mRNA所看到的,1:1至1:5范围内的起始子与NTP的比率不会减少产生的全长mRNA的量(图3),因此本文所述的化学修饰的帽化合物能够在一系列反应条件下充当mRNA起始子。如该实施例和产生的数据所示,基于该实施例的结果,预期表1中描述的其余化合物将表现出相似的性质。
C.mRNA加帽效率的确定
加帽mRNA相对于存在的mRNA的总量的量,即加帽效率,可以通过本领域熟知的多种方法测量。此类方法中的一种是将mRNA消化成小片段,然后进行色谱分离和检测。在一些情况下,用序列特异性RNA或DNA核酸酶或切割酶进行消化。加帽RNA的色谱分离和测量通常通过HPLC、FPLC、薄层色谱法、凝胶电泳或毛细管凝胶电泳技术进行。加帽RNA和未加帽的mRNA的同一性通过质谱法来验证。
实施例8.加帽mRNA稳定性的测量
从mRNA上去除帽,即脱帽,是细胞内mRNA降解的常见起始步骤。报告的用于测量脱帽和mRNA降解的方法用于评估加帽mRNA的稳定性(Grudzien,E.等人,J.Biol.Chem.2006,281,1857-1867)。防止脱帽酶的相互作用的帽结构可以提高mRNA的稳定性和在细胞中的半衰期。例如,具有5’端区域基序的mRNA,1032a、1037a、1107a、5207a、1112a、1137a、1141a、5208、3207a、3212a、1107c、1112c、3207c和3212c,在三磷酸键中含有硫代磷酸酯修饰,其可以抑制dcp2脱帽酶的活性。类似地,基于前面实施例的结果,如表1中所述的在三磷酸键中含有硫代磷酸酯修饰的其他化合物也可以抑制dcp2脱帽酶的活性。mRNA的稳定性也可以通过抑制核酸外切酶活性的帽修饰来提高。例如,在帽结构中前两个或三个起始核苷酸之间引入硫代磷酸修饰,如存在于具有5’端区域基序的mRNA中,1007a、1007e、1007i、1037a、1112a、1141a、3107a、3212a、1007c、1112c、3107c、3212c、5203、5204、5205、5206、5209、5210、5211、5214,可以降低细胞中mRNA降解的速率。类似地,如表1中所述的在帽结构中前两个或三个起始核苷酸之间具有硫代磷酸酯修饰的其他化合物也可以降低细胞中mRNA降解的速率,如通过前面的实施例所看到的。
实施例9.HeLa细胞和裂解物中加帽荧光素酶mRNA的翻译
在RPMI中,在37℃下在5% CO2气氛下,用10% FBS培养HeLa细胞。按照制造商推荐的接种条件,将细胞铺板到适当大小的孔板中。在过夜温育后,检查细胞的单层形成,然后使用转染剂如MessengerMAX转染。溶液A:将期望量的荧光素酶mRNA在OptiMEM中稀释,并与溶液B:OptiMEM中的MessengerMAX混合。在将溶液A和B混合后,将混合物在室温下温育20分钟,然后滴加到每个细胞孔中。然后将细胞在37℃下温育12-72小时,以允许mRNA表达成蛋白质。收获细胞,并按照Promega荧光素酶测定系统方案制备以用于测量荧光素酶蛋白水平。在一些情况下,将mRNA直接施用于含有用于蛋白质表达的细胞组分的HeLa裂解物,这种方法不需要使用转染剂。例如,将编码具有5’端区域基序的mRNA(1007a)的荧光素酶加入到商业上可获得的HeLa裂解物体外翻译试剂盒中,以产生荧光素酶蛋白。使用发光检测板读取器测量荧光素酶蛋白活性(如通过在存在荧光素底物的情况下产生发光所测量的)。每次测定测量的相对光单位与从mRNA翻译的荧光素酶蛋白的量成比例。使用商业上可获得的5’端起始子1002a制备的mRNA作为参照来比较本实施例的结果。在该实施例中,具有起始子1007a的mRNA产生比具有起始子1002a的mRNA高约2x的荧光素酶活性(图5)。如该实施例和产生的数据所示,基于该实施例的结果,预期表1中所述的其余化合物将表现出相似的性质。
实施例10.用于基因组编辑的原代肝细胞中加帽mRNA的翻译
根据制造商的方案培养原代人肝细胞(hPH)、原代食蟹猴肝细胞(cPH)或原代小鼠肝细胞(mPH)。简而言之,将细胞解冻并重新悬浮于肝细胞解冻培养基中,随后在4℃下以100g离心10min。弃去上清液,并将沉淀的细胞重新悬浮于肝细胞铺板培养基中。每个小瓶含有约500万个细胞,其用于铺板一个24孔板。在37℃下在5% CO2气氛下在组织培养箱中,允许铺板的细胞沉降并粘附4-6小时。在温育后,检查细胞单层的形成。然后用新鲜的肝细胞维持培养基替换温育培养基,因此细胞准备好使用转染剂如MessengerMAX进行转染。溶液A:期望的量的单一向导RNA(sgRNA)与1:1wt率的mRNA在OptiMEM中混合。溶液B:OptiMEM中的MessengerMAX。在将溶液A和B混合后,将混合物在室温下温育20分钟,然后将温育的溶液滴加到每个细胞孔中。然后允许细胞在37℃下保持3天。收获细胞,并使用ThermoKingfisher仪器制备以用于基因组DNA提取。通过PCR处理提取的基因组DNA,然后使扩增的PCR产物经受NGS(MiSeq)以分析基因组编辑。在一些情况下,如上所述用编码ABE的mRNA转染hPH,并且翻译的ABE蛋白的水平用于评估mRNA的功能。例如,具有5’端区域基序的mRNA(1007a和1107a)如上所述被转染到hPH细胞中,细胞被裂解,并且通过ELISA确定ABE蛋白水平。使用用商业上可获得的起始子1002a制备的ABE mRNA作为参照,比较本实施例的结果。在该实施例中,与具有5’端区域基序的mRNA 1002a相比,具有5’端区域基序的mRNA 1007a和1107a产生相似的ABE蛋白水平(图6)。如该实施例和产生的数据所示,基于该实施例的结果,预期表1中所述的其余化合物将表现出相似的性质。
实施例11.用于基因组编辑的小鼠体内加帽mRNA的翻译
A.用于体外转染和体内评价的LNP制剂
脂质纳米颗粒(LNP)是根据制造商的方案,使用Precision NanosystemsNanoAssemblr系统,通过微流体混合产生的,对单独的有效载荷进行了一些优化。使用0.2微米过滤器过滤所得的LNP,并在4℃下储存或在80℃下冷冻。
B.小鼠体内评估
在这些研究中使用的LNP如以上实施例6(A)中所述制备,包括1:1重量比的靶向小鼠ANGPTL3(mANGPTL3)和/或小鼠PCSK9(mPCSK9)基因的化学合成的sgRNA和SpCas9或ABE8.8 mRNA,经由侧尾静脉或眶后窦以5-10ml/kg的总体积静脉内施用于C57BL/6小鼠(n=5)。给药后4或5天进行尸检,收集肝脏和血液用于编辑效率的NGS测量,以及血清PCSK9、甘油三酯和胆固醇分析。
C.基因组DNA分离
根据制造商的方案,使用基于珠的提取试剂盒,MagMAX-96DNA多样品试剂盒,在KingFisher Flex自动提取仪器上,从约20微升全小鼠肝裂解物中分离基因组DNA。根据制造商的方案,使用FastPrep-24系统裂解小鼠全肝。将肝脏装入含有0.5mL的PBS的2mL裂解基质管中。提取的基因组DNA在4℃下储存直到进一步使用,或在-80℃下储存以用于长期储存。
D.下一代测序(NGS)和编辑效率的分析
对感兴趣的区域进行下一代测序或深度测序,以确定基因编辑的程度。根据制造商的方案,使用Nextera XT DNA文库制备试剂盒(Illumina)制备样品。简而言之,进行两轮PCR,首先扩增感兴趣的区域,然后将深度测序和样品鉴定所需的DNA序列添加到初始产物中。根据制造商的方案,在Illumina MiSeq仪器上对最终扩增子进行测序。
用CRISPResso2管道分析成对末端读数(Clement,K.等人,Nat.Biotech.2019,37,224-226)。简而言之,过滤掉低质量的读数,从读数中修剪出衔接子序列,并且合并成对的末端读数并与扩增子序列比对。编辑百分比被计算为支持插入或缺失的读取的数量相对于比对的读取的总数。对于ABE,编辑百分比被计算为支持插入或缺失的读取的数量相对于比对的读取的总数。
在一些情况下,用靶向mPCSK9的sgRNA和编码ABE的具有5’端区域基序的mRNA1007a配制LNP,体内施用于小鼠,并如实施例11中所述评估编辑效率。使用由商业上可获得的5’端起始子1002a制备的ABE编码mRNA作为参照,比较了该实施例的结果。在该实施例中,与具有5’端区域基序的mRNA 1002a相比,具有5’端区域基序的mRNA 1007a产生了相似的肝细胞编辑水平(图7)。如该实施例和产生的数据所示,基于该实施例的结果,预期表1中的其余化合物将表现出相似的性质。
实施例12.小鼠体内或体外HEK293细胞模型中加帽mRNA的免疫刺激的确定
如实施例11(A,B)中所述,制备LNP并体内施用于小鼠。在适当的时间点(通常在给药后1-48小时和终点之间的间隔)收集血液,并按照本领域熟知的技术加工成血清或血浆。血清或血浆细胞因子和趋化因子水平使用V-PLEX细胞因子和趋化因子检测试剂盒测量。将细胞因子和趋化因子水平与用单独的缓冲液处理的动物以及处理动物的给药前取样进行比较。在一些情况下,在体外转染报告细胞系如HEK-Lucia RIG-I细胞报告模型后,评估加帽mRNA的免疫刺激,所述报告细胞系在存在IFN刺激的应答元件如未加帽的mRNA的情况下产生荧光素酶信号。如实施例7所述培养和转染该细胞模型,并且使用荧光素酶活性试剂盒和板读数器测量荧光素酶活性。本领域已知未加帽的mRNA产生RIG-I依赖性IFN免疫应答,并且加帽mRNA减少这种免疫刺激。在该实施例中,与使用HEK-Lucia RIG-I细胞报告模型的未加帽的mRNA相比,具有5’端区域基序的mRNA 1007a显示降低的RIG-I活性(图8)。此外,具有5’端区域基序的mRNA 1007a似乎并没有由于帽结构的化学修饰而增加RIG-I的活化。使用商业上可获得的5’端起始子1002a制备的mRNA作为参照,比较该实施例的结果。如该实施例和产生的数据所示,基于该实施例的结果,预期表1中的其余化合物将表现出相似的性质。
其他实施方案
从前述描述中,将显而易见的是,可以对本文所述的公开内容进行改变和修改,以将其用于各种用途和条件。此类实施方案也在所附权利要求的范围内。
在本文变量的任何定义中对要素列表的叙述包括将该变量定义为所列要素的任何单个要素或组合(或子组合)。本文实施方案的叙述包括作为任何单个实施方案的实施方案,或者与任何其他实施方案或其部分相结合的实施方案。
本说明书中提及的所有专利和出版物均通过引用并入本文,如同每个独立的专利和出版物都明确且单独地指出通过引用并入。
虽然已经提供了具体实施例和许多实施方案来说明前述的方面和方面的组合,但应当理解和明白,示例性或公开的实施方案的任何方面或其组合可以从其中排除,以构成另一实施方案而没有限制,并且预期任何此类实施方案可以构成单独和独立的权利要求。类似地,应当理解和明白,一个或多个实施方案的任何方面或方面的组合也可以包括在一个或多个实施方案的任何方面或方面的组合中,或者与一个或多个实施例的任何方面或方面的组合结合,并且本文预期其所有此类组合落入本公开的范围内,并且可以作为单独和独立的权利要求存在而无限制。因此,应当理解,存在于一项权利要求中的任何特征可以包括在另一项权利要求中;存在于一项权利要求中的任何特征可以从该权利要求中去除,以构成没有该特征的权利要求;并且存在于一项权利要求中的任何特征可以与另一项权利要求中的任何特征组合,其中的每一个特征都在本文中被预期。以下列举的条款是前述实施方案和实施例的方面和方面的组合的进一步说明性实例:
1.一种体外转录的(IVT)mRNA序列起始子,其包含式(I)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6,
条件是式(I)的化合物满足以下限制性条件(i)至(iii)中的一个或多个:(i)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(ii)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;和(iii)A、A1和A2中的至少一个为-S-。
2.根据条款1所述的IVT mRNA序列起始子,其中X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或者A、A1和A2中的至少一个为-S-。
3.一种体外转录的(IVT)mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
4.一种体外转录的(IVT)mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
5.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-a)的结构:
6.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-b)的结构:
7.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-c)的结构:
8.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-d)的结构:
9.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-e)的结构:
10.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-f)的结构:
11.根据条款1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-g)的结构:
12.根据权利要求1所述的IVT mRNA序列起始子,其中所述起始子具有式(I-h)的结构:
13.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-a)的结构:
14.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-b)的结构:
15.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-c)的结构:
16.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-d)的结构:
17.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-e)的结构:
18.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-f)的结构:
19.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-g)的结构:
20.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-h)的结构:
21.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-i)的结构
22.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-j)的结构:
23.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-k)的结构:
24.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-l)的结构:
25.根据条款17或18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-m)的结构:
26.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-n)的结构:
27.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-o)的结构:
28.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-p)的结构:
29.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-q)的结构:
30.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-r)的结构:
31.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-s)的结构:
32.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-t)的结构:
33.根据条款18所述的IVT mRNA序列起始子,其中所述起始子具有式(II-u)的结构:
34.根据条款1-18中任一项所述的IVT mRNA序列起始子,其中Z3为氢、氟、-OH、-OCH3、-或-OCH2CH3。
35.根据条款48所述的IVT mRNA序列起始子,其中Z3为-OCH3。
36.根据条款48所述的IVT mRNA序列起始子,其中Z4和Zn各自独立地为-OH或-OCH3。
37.根据条款1-18中任一项所述的IVT mRNA序列起始子,其中Z3、Z4和Zn各自独立地为-OH或-OCH3。
41.根据条款1-30中任一项所述的IVT mRNA序列起始子,其中Z1为氟、-OH或-OCH3。
42.根据条款55所述的IVT mRNA序列起始子,其中Z1为氟。
43.根据条款55所述的IVT mRNA序列起始子,其中Z1为-OH。
44.根据条款55所述的IVT mRNA序列起始子,其中Z1为-OCH3。
45.根据条款1-30中任一项所述的IVT mRNA序列起始子,其中Z2为氟、-OH或-OCH3。
46.根据条款59所述的IVT mRNA序列起始子,其中Z2为氟。
47.根据条款59所述的IVT mRNA序列起始子,其中Z2为-OH。
48.根据条款59所述的IVT mRNA序列起始子,其中Z2为-OCH3。
49.根据条款1-62中任一项所述的IVT mRNA序列起始子,其中Q1和Q4为-CH2O-。
50.根据条款1-63中任一项所述的IVT mRNA序列起始子,其中Q2和Q3各自为-O-。
51.根据条款1-64中任一项所述的IVT mRNA序列起始子,其中Y1和Y3各自为=O。
52.根据条款1-64中任一项所述的IVT mRNA序列起始子,其中Y2、Y4和Yn各自独立地为=O或=S。
53.根据条款1-64中任一项所述的IVT mRNA序列起始子,其中Y1、Y2、Y3、Y4和Yn中的一个或多个为=S。
54.根据条款67所述的IVT mRNA序列起始子,其中Y2为=S。
55.根据条款67所述的IVT mRNA序列起始子,其中Y4为=S。
56.根据条款1-64中任一项所述的IVT mRNA序列起始子,其中Y1、Y2、Y3、Y4和Yn各自为=O。
57.根据条款1-70中任一项所述的IVT mRNA序列起始子,其中X1、X4和Xn各自为-O-。
58.根据条款1-70中任一项所述的IVT mRNA序列起始子,其中X2和X3各自独立地为-O-或-S-。
59.根据条款72所述的IVT mRNA序列起始子,其中X3为-O-。
60.根据条款1-70中任一项所述的IVT mRNA序列起始子,其中X1、X2、X3、X4和Xn中的一个或多个为-S-。
61.根据条款74所述的IVT mRNA序列起始子,其中X2为-S-。
62.根据条款74所述的IVT mRNA序列起始子,其中X4为-S-。
63.根据条款1-70中任一项所述的IVT mRNA序列起始子,其中X1、X2、X3、X4和Xn各自为-O-。
64.根据条款1-77中任一项所述的IVT mRNA序列起始子,其中A、A1和A2各自为-O-。
65.根据条款1-77中任一项所述的IVT mRNA序列起始子,其中A、A1和A2中的一个或多个为-S-。
66.根据条款1-77或79中任一项所述的IVT mRNA序列起始子,其中A为-S-,并且A1和A2为-O-。
67.根据条款1-77或79中任一项所述的IVT mRNA序列起始子,其中A2为-S-,并且A和A1为-O-。
68.根据条款1-77中任一项所述的IVT mRNA序列起始子,其中A、A1和A2为-O-。
69.根据条款1、17或48-81中任一项所述的IVT mRNA序列起始子,其中p为0。
70.根据条款1、17或48-81中任一项所述的IVT mRNA序列起始子,其中p为1。
71.根据条款1、17或48-81中任一项所述的IVT mRNA序列起始子,其中p为2。
72.根据条款1-85中任一项所述的IVT mRNA序列起始子,其中B2、B3和Bn各自独立地为腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、胸腺嘧啶、次黄嘌呤或嘌呤。
73.根据条款86所述的IVT mRNA序列起始子,其中B2为腺嘌呤,并且B3为鸟嘌呤。
74.根据条款86所述的IVT mRNA序列起始子,其中B2为鸟嘌呤,并且B3为腺嘌呤。
75.根据条款1-88中任一项所述的IVT mRNA序列起始子,其中蛋白质表达增加。
79.根据条款86-92所述的IVT mRNA序列起始子,其中B2为腺嘌呤。
80.根据条款86-92所述的IVT mRNA序列起始子,其中B3为鸟嘌呤。
81.一种复合物,其包含IVT mRNA序列起始子和DNA模板,其中所述IVT mRNA序列起始子包括根据条款1-94中任一项所述的化合物,其中
所述DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸、在核苷酸位置+2处的第二核苷酸和在核苷酸位置+3处的第三核苷酸;并且
其中所述IVT mRNA序列起始子至少在核苷酸位置+1、+2和+3处与所述DNA模板杂交。
82.一种复合物,其包含IVT mRNA序列起始子和DNA模板,其中所述IVT mRNA序列起始子包括根据条款1-94中任一项所述的化合物,其中
所述DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸和在核苷酸位置+2处的第二核苷酸;并且
其中所述IVT mRNA序列起始子至少在核苷酸位置+1和+2处与所述DNA模板杂交。
83.一种RNA分子,其包含根据条款1-94中任一项所述的IVT mRNA序列起始子。
84.根据条款97所述的RNA,其中所述RNA包括向导RNA或核酸酶mRNA。
85.根据条款97所述的RNA,其中所述RNA包括mRNA。
86.一种表达mRNA的方法,所述方法包括(a)使根据条款99所述的mRNA与细胞或其细胞裂解物接触,和(b)表达所述mRNA。
87.根据条款100所述的方法,其还包括测量所述mRNA的表达水平。
88.根据条款100所述的方法,其中所述mRNA的表达水平与不含所述IVT mRNA序列起始子的相应mRNA相比高至少6倍、8倍或20倍。
89.根据条款100所述的方法,其中所述细胞是HeLa细胞。
90.一种减少加帽mRNA的细胞免疫刺激的方法,所述方法包括(a)使根据条款1-94中任一项所述的加帽mRNA与细胞报告细胞系接触,和(b)测量所述细胞报告细胞系中的RIG-I活化。
91.根据条款104所述的方法,其中所述细胞报告细胞系是HEK-Lucia RIG-I模型。
92.根据条款104或105中任一项所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少20%。
93.根据条款106所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少50%。
94.根据条款107所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少70%。
95.根据条款108所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少100%。
96.根据条款109所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少150%。
97.一种细胞,其含有RNA分子,所述RNA分子包含根据条款1-94中任一项所述的IVT mRNA序列起始子。
98.一种细胞,其含有从RNA分子翻译的多肽,所述RNA分子包含根据条款1-94中任一项所述的IVT mRNA序列起始子。
99.一种药物组合物,其包含RNA分子和一种或多种药学上可接受的赋形剂,所述RNA分子包含根据条款1-94中任一项所述的IVT mRNA序列起始子。
100.根据条款126所述的药物组合物,其包括脂质纳米颗粒。
101.根据条款126所述的药物组合物,其中所述RNA被包封在脂质纳米颗粒中。
102.一种用于合成RNA分子的方法,所述方法包括:
a.将根据条款1-94中任一项所述的IVT mRNA序列起始子引入到包含RNA聚合酶的混合物中,和
b.将所述混合物温育足以允许所述RNA分子转录的时间。
103.根据条款81所述的方法,其中所述混合物还包含DNA模板和核苷三磷酸。
104.一种基因编辑的方法,所述方法包括将根据条款97或98所述的RNA分子或根据条款126-129中任一项所述的药物组合物引入到细胞中,其中所述RNA分子包括向导RNA或核酸酶mRNA,其中所述RNA分子在所述细胞中被翻译。
105.一种用于在有需要的对象中降低冠状动脉疾病的风险的方法,所述方法包括向所述对象施用有效量的根据条款126-129中任一项所述的药物组合物。
Claims (133)
1.一种体外转录的(IVT)mRNA序列起始子,其包含式(I)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6,
条件是式(I)的化合物满足以下限制性条件(i)至(iii)中的一个或多个:(i)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(ii)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;和(iii)A、A1和A2中的至少一个为-S-。
2.根据权利要求1所述的IVT mRNA序列起始子,其中X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或者A、A1和A2中的至少一个为-S-。
3.一种体外转录的(IVT)mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
4.一种体外转录的(IVT)mRNA序列起始子,其包含式(II)的化合物或其盐或溶剂化物:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
9.根据权利要求1-4中任一项所述的IVT mRNA序列起始子,其中Z3为氢、氟、-OH、-OCH3、-或-OCH2CH3。
10.根据权利要求9所述的IVT mRNA序列起始子,其中Z3为-OCH3。
11.根据权利要求9所述的IVT mRNA序列起始子,其中Z4和Zn各自独立地为-OH或-OCH3。
12.根据权利要求1-11中任一项所述的IVT mRNA序列起始子,其中Z3、Z4和Zn各自独立地为-OH或-OCH3。
13.根据权利要求1-12中任一项所述的IVT mRNA序列起始子,其中Y2、Y4和Yn各自独立地为=O或=S。
14.根据权利要求1-13中任一项所述的IVT mRNA序列起始子,其中X2和X3各自独立地为-O-或-S-。
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-OCH2CH3、-SCH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH2-、-CH=CH-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6,
条件是式(I)的化合物满足以下限制性条件(i)至(iii)中的一个或多个:(i)X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;(ii)Y1、Y2、Y3、Y4和Yn中的至少一个为=S;和(iii)A、A1和A2中的至少一个为-S-。
16.根据权利要求15所述的具有5’端区域基序的mRNA序列,其中X1、X2、X3、X4和Xn中的至少一个为-SH或-S-;Y1、Y2、Y3、Y4和Yn中的至少一个为=S;或者A、A1和A2中的至少一个为-S-。
17.一种具有5’端区域基序(II’)的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z1和Z’各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z2和Z”各自独立地为氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
18.一种具有5’端区域基序(II”)的mRNA序列:
其中
B2、B3和Bn各自独立地为天然的、经修饰的或非天然的核碱基;
Z’和Z”各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-NH(CH3)、-NH2、-NH(C(=O)CH3)或-SCH3;
Z”’为氢、氟、-CH3、-CH2CH3、-OCH3或-OCH2CH3;
Z1和Z2各自独立地为氢、氟、-OH、-SH、-CH3、-CH2CH3、-OCH3、-SCH3、-OCH2CH3、-NH2、NHCH3或NHC(=O)CH3;
Z3、Z4和Zn各自独立地为氢、氟、-OH、-CH3、-CH2CH3、-OCH3、-NH2、-NHCH3、-NH(C(=O)CH3)、-OCH2CH3、-OCH2OCH3、-OCH2CH2CH3、-OCH(CH3)2、-SCH3或-OCH2CH2OCH3;
Q1和Q4各自独立地为-CH=CH-、-CH2-、-CH2O-、-CH2S-、-CH2CH2-、-CH2CF2-、-CH2NH2-、-CH2NH(CH3)-或-CH2N(C(=O)CH3)-;
Q2和Q3各自独立地为-O-、-S-、-CH2-、-CF2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;
X1、X2、X3、X4和Xn各自独立地为-OH、-SH、-O-、-S-、-NH2、-NHCH3、-NH(C(=O)CH3)、-CH3、-CH2CH3、-CH2CH2CH3、-CH(CH3)2、-OCH3或-OCH2CH3;
Y1、Y2、Y3、Y4和Yn各自独立地为=O、=S、=NH或=NCH3;
A、A1和A2各自独立地为-O-、-S-、-CH2-、-NH-、-N(CH3)-或-N(C(=O)CH3)-;并且
p=0、1、2、3、4、5或6。
48.根据权利要求15-18中任一项所述的具有5’端区域基序的mRNA序列,其中Z3为氢、氟、-OH、-OCH3、-或-OCH2CH3。
49.根据权利要求48所述的具有5’端区域基序的mRNA序列,其中Z3为-OCH3。
50.根据权利要求48所述的具有5’端区域基序的mRNA序列,其中Z4和Zn各自独立地为-OH或-OCH3。
51.根据权利要求15-18中任一项所述的具有5’端区域基序的mRNA序列,其中Z3、Z4和Zn各自独立地为-OH或-OCH3。
55.根据权利要求15-30中任一项所述的具有5’端区域基序的mRNA序列,其中Z1为氟、-OH或-OCH3。
56.根据权利要求55所述的具有5’端区域基序的mRNA序列,其中Z1为氟。
57.根据权利要求55所述的具有5’端区域基序的mRNA序列,其中Z1为-OH。
58.根据权利要求55所述的具有5’端区域基序的mRNA序列,其中Z1为-OCH3。
59.根据权利要求15-30中任一项所述的具有5’端区域基序的mRNA序列,其中Z2为氟、-OH或-OCH3。
60.根据权利要求59所述的具有5’端区域基序的mRNA序列,其中Z2为氟。
61.根据权利要求59所述的具有5’端区域基序的mRNA序列,其中Z2为-OH。
62.根据权利要求59所述的具有5’端区域基序的mRNA序列,其中Z2为-OCH3。
63.根据权利要求15-62中任一项所述的具有5’端区域基序的mRNA序列,其中Q1和Q4为-CH2O-。
64.根据权利要求15-63中任一项所述的具有5’端区域基序的mRNA序列,其中Q2和Q3各自为-O-。
65.根据权利要求15-64中任一项所述的具有5’端区域基序的mRNA序列,其中Y1和Y3各自为=O。
66.根据权利要求15-64中任一项所述的具有5’端区域基序的mRNA序列,其中Y2、Y4和Yn各自独立地为=O或=S。
67.根据权利要求15-64中任一项所述的具有5’端区域基序的mRNA序列,其中Y1、Y2、Y3、Y4和Yn中的一个或多个为=S。
68.根据权利要求67所述的具有5’端区域基序的mRNA序列,其中Y2为=S。
69.根据权利要求67所述的具有5’端区域基序的mRNA序列,其中Y4为=S。
70.根据权利要求15-64中任一项所述的具有5’端区域基序的mRNA序列,其中Y1、Y2、Y3、Y4和Yn各自为=O。
71.根据权利要求15-70中任一项所述的具有5’端区域基序的mRNA序列,其中X1、X4和Xn各自为-O-。
72.根据权利要求15-70中任一项所述的具有5’端区域基序的mRNA序列,其中X2和X3各自独立地为-O-或-S-。
73.根据权利要求72所述的具有5’端区域基序的mRNA序列,其中X3为-O-。
74.根据权利要求15-70中任一项所述的具有5’端区域基序的mRNA序列,其中X1、X2、X3、X4和Xn中的一个或多个为-S-。
75.根据权利要求74所述的具有5’端区域基序的mRNA序列,其中X2为-S-。
76.根据权利要求74所述的具有5’端区域基序的mRNA序列,其中X4为-S-。
77.根据权利要求15-70中任一项所述的具有5’端区域基序的mRNA序列,其中X1、X2、X3、X4和Xn各自为-O-。
78.根据权利要求15-77中任一项所述的具有5’端区域基序的mRNA序列,其中A、A1和A2各自为-O-。
79.根据权利要求15-77中任一项所述的具有5’端区域基序的mRNA序列,其中A、A1和A2中的一个或多个为-S-。
80.根据权利要求15-77或79中任一项所述的具有5’端区域基序的mRNA序列,其中A为-S-,并且A1和A2为-O-。
81.根据权利要求15-77或79中任一项所述的具有5’端区域基序的mRNA序列,其中A2为-S-,并且A和A1为-O-。
82.根据权利要求15-77中任一项所述的具有5’端区域基序的mRNA序列,其中A、A1和A2为-O-。
83.根据权利要求15、17或48-81中任一项所述的具有5’端区域基序的mRNA序列,其中p为0。
84.根据权利要求15、17或48-81中任一项所述的具有5’端区域基序的mRNA序列,其中p为1。
85.根据权利要求15、17或48-81中任一项所述的具有5’端区域基序的mRNA序列,其中p为2。
86.根据权利要求15-85中任一项所述的具有5’端区域基序的mRNA序列,其中B2、B3和Bn各自独立地为腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、胸腺嘧啶、次黄嘌呤或嘌呤。
87.根据权利要求86所述的具有5’端区域基序的mRNA序列,其中B2为腺嘌呤,并且B3为鸟嘌呤。
88.根据权利要求86所述的具有5’端区域基序的mRNA序列,其中B2为鸟嘌呤,并且B3为腺嘌呤。
89.根据权利要求15-88中任一项所述的具有5’端区域基序的mRNA序列,其中蛋白质表达增加。
93.根据权利要求86-92所述的具有5’端区域基序的mRNA序列,其中B2为腺嘌呤。
94.根据权利要求86-92所述的具有5’端区域基序的mRNA序列,其中B3为鸟嘌呤。
95.一种复合物,其包含具有5’端区域基序的mRNA序列和DNA模板,其中所述具有5’端区域基序的mRNA序列包括根据权利要求15-94中任一项所述的化合物,其中
所述DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸、在核苷酸位置+2处的第二核苷酸和在核苷酸位置+3处的第三核苷酸;并且
其中所述具有5’端区域基序的mRNA序列至少在核苷酸位置+1、+2和+3处与所述DNA模板杂交。
96.一种复合物,其包含具有5’端区域基序的mRNA序列和DNA模板,其中所述具有5’端区域基序的mRNA序列包括根据权利要求15-94中任一项所述的化合物,其中
所述DNA模板包括启动子区域,所述启动子区域包括转录起始位点,所述转录起始位点具有在核苷酸位置+1处的第一核苷酸和在核苷酸位置+2处的第二核苷酸;并且
其中所述具有5’端区域基序的mRNA序列至少在核苷酸位置+1和+2处与所述DNA模板杂交。
97.一种RNA分子,其包含根据权利要求15-94中任一项所述的具有5’端区域基序的mRNA序列。
98.根据权利要求97所述的RNA,其中所述RNA包括向导RNA或核酸酶mRNA。
99.根据权利要求97所述的RNA,其中所述RNA包括mRNA。
100.一种表达mRNA的方法,所述方法包括将根据权利要求99所述的mRNA引入到细胞裂解物中以表达所述mRNA。
101.根据权利要求100所述的方法,其还包括测量所述mRNA的表达水平。
102.根据权利要求100所述的方法,其中所述mRNA的表达水平与不含所述具有5’端区域基序的mRNA序列的相应mRNA相比高至少2倍、3倍、4倍、6倍、8倍或20倍。
103.根据权利要求100所述的方法,其中所述细胞是HeLa细胞。
104.一种检测由mRNA产生的细胞免疫刺激的方法,所述方法包括(a)使包含根据权利要求15-94中任一项所述的加帽mRNA的制剂与细胞报告细胞系接触,以及(b)测量所述细胞报告细胞系中的RIG-I活化。
105.根据权利要求104所述的方法,其中所述细胞报告细胞系是HEK-Lucia RIG-I模型。
106.根据权利要求104或105中任一项所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少20%。
107.根据权利要求106所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少50%。
108.根据权利要求107所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少70%。
109.根据权利要求108所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少100%。
110.根据权利要求109所述的方法,其中与未加帽的mRNA相比,细胞免疫刺激减少至少150%。
111.一种使用IVT反应产生根据权利要求15-99中任一项所述的具有5’端区域基序的mRNA序列的方法,所述方法包括(a)将DNA模板、聚合酶、包含硫代磷酸酯基团的mRNA序列起始子和核苷三磷酸(NTP)以所述mRNA序列起始子与所述NTP的特定摩尔比混合,以产生混合物,(b)在特定温度和持续时间下温育所述混合物,以及(c)从所述混合物中收获并纯化所述具有5’端区域基序的mRNA序列。
112.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:5,并且其中所述方法能够以至少80%的加帽效率产生至少80%的产率。
113.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为1:2.5,并且其中所述方法能够以至少85%的加帽效率产生至少80%的产率。
114.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:1.67,并且其中所述方法能够以至少90%的加帽效率产生至少80%的产率。
115.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:1.25,并且其中所述方法能够以至少90%的加帽效率产生至少80%的产率。
116.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:1,并且其中所述方法能够以至少90%的加帽效率产生至少80%的产率。
117.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:5,并且其中所述方法能够以至少80%的加帽效率产生每毫升(mL)IVT反应至少3mg mRNA的产量。
118.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:2.5,并且其中所述方法能够以至少85%的加帽效率产生每mL IVT反应至少3mg mRNA的产量。
119.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:1.67,并且其中所述方法能够以至少90%的加帽效率产生每mL IVT反应至少3mg mRNA的产量。
120.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:1.25,并且其中所述方法能够以至少90%的加帽效率产生每mL IVT反应至少3mg mRNA的产量。
121.根据权利要求111所述的方法,其中所述mRNA序列起始子与NTP的所述摩尔比为约1:1,并且其中所述方法能够以至少90%的加帽效率产生每mL IVT反应至少3mg mRNA的产量。
122.根据权利要求111所述的方法,其中所述NTP为GTP、ATP、CTP、UTP或经修饰的NTP或其组合。
123.根据权利要求122所述的方法,其中所述经修饰的NTP是N1-甲基假尿苷的5’-三磷酸。
124.一种细胞,其含有RNA分子,所述RNA分子包含根据权利要求15-94中任一项所述的具有5’端区域基序的mRNA序列。
125.一种细胞,其含有从RNA分子翻译的多肽或蛋白质,所述RNA分子包含根据权利要求15-94中任一项所述的具有5’端区域基序的mRNA序列。
126.一种药物组合物,其包含RNA分子和一种或多种药学上可接受的赋形剂,所述RNA分子包含根据权利要求15-94中任一项所述的具有5’端区域基序的mRNA序列。
127.根据权利要求126所述的药物组合物,其还包含一种或多种单一向导RNA,所述单一向导RNA被设计成靶向一种或多种感兴趣基因的一个或多个特定位置,以在施用于哺乳动物后引发药理学效应。
128.根据权利要求126所述的药物组合物,其包括脂质纳米颗粒。
129.根据权利要求126所述的药物组合物,其中所述RNA被包封在脂质纳米颗粒中。
130.一种用于合成RNA分子的方法,所述方法包括:
a.将根据权利要求15-94中任一项所述的具有5’端区域基序的mRNA序列引入到包含RNA聚合酶的混合物中,和
b.将所述混合物温育足以允许所述RNA分子转录的时间。
131.根据权利要求81所述的方法,其中所述混合物还包含DNA模板和核苷三磷酸。
132.一种基因编辑的方法,所述方法包括将根据权利要求97或98所述的RNA分子或根据权利要求126-129中任一项所述的药物组合物引入到细胞中,其中所述RNA分子包括向导RNA或核酸酶mRNA,其中所述RNA分子在所述细胞中被翻译。
133.一种用于在有需要的对象中降低冠状动脉疾病的风险的方法,所述方法包括向所述对象施用有效量的根据权利要求126-129中任一项所述的药物组合物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063074993P | 2020-09-04 | 2020-09-04 | |
| US63/074,993 | 2020-09-04 | ||
| PCT/US2021/049158 WO2022051677A1 (en) | 2020-09-04 | 2021-09-03 | Compositions and methods for capping rnas |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116368226A true CN116368226A (zh) | 2023-06-30 |
Family
ID=80492066
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180074617.6A Pending CN116368226A (zh) | 2020-09-04 | 2021-09-03 | 用于加帽rna的组合物和方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20230331763A1 (zh) |
| EP (1) | EP4208549A1 (zh) |
| JP (1) | JP2023540562A (zh) |
| CN (1) | CN116368226A (zh) |
| WO (1) | WO2022051677A1 (zh) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023167880A2 (en) * | 2022-03-01 | 2023-09-07 | Verve Therapeutics, Inc. | Compositions and methods for capping rnas |
| CN117645642A (zh) * | 2022-09-05 | 2024-03-05 | 广州市恒诺康医药科技有限公司 | 用于rna加帽的化合物及其应用 |
| CN116375781B (zh) * | 2023-03-24 | 2023-12-29 | 江苏申基生物科技有限公司 | 一种tna修饰的帽类似物及其制备方法和应用 |
| CN116987137B (zh) * | 2023-09-26 | 2024-01-02 | 江苏申基生物科技有限公司 | 一种加帽化合物及其在mRNA加帽中的应用 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2734052A1 (en) * | 2003-05-30 | 2005-01-13 | Pharmasset, Inc. | Modified fluorinated nucleoside analogues |
| EP3682905B1 (en) * | 2011-10-03 | 2021-12-01 | ModernaTX, Inc. | Modified nucleosides, nucleotides, and nucleic acids, and uses thereof |
| SI4140491T1 (sl) * | 2015-09-21 | 2024-01-31 | Trilink Biotechnologies, Llc | Postopek sinteze 5'-omejenih RNK |
| WO2017066781A1 (en) * | 2015-10-16 | 2017-04-20 | Modernatx, Inc. | Mrna cap analogs with modified phosphate linkage |
| US11866754B2 (en) * | 2015-10-16 | 2024-01-09 | Modernatx, Inc. | Trinucleotide mRNA cap analogs |
-
2021
- 2021-09-03 CN CN202180074617.6A patent/CN116368226A/zh active Pending
- 2021-09-03 WO PCT/US2021/049158 patent/WO2022051677A1/en unknown
- 2021-09-03 JP JP2023515146A patent/JP2023540562A/ja active Pending
- 2021-09-03 EP EP21865230.3A patent/EP4208549A1/en active Pending
-
2023
- 2023-03-01 US US18/176,609 patent/US20230331763A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023540562A (ja) | 2023-09-25 |
| EP4208549A1 (en) | 2023-07-12 |
| US20230331763A1 (en) | 2023-10-19 |
| WO2022051677A1 (en) | 2022-03-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN116368226A (zh) | 用于加帽rna的组合物和方法 | |
| US11414453B2 (en) | Compositions and methods for synthesizing 5′-capped RNAs | |
| CN109414448B (zh) | 用于减少PAPD5或PAPD7 mRNA治疗乙型肝炎感染的核酸分子 | |
| EP3350333B1 (en) | Polynucleotides containing a stabilizing tail region | |
| CN106434665B (zh) | 用于抑制乙型肝炎病毒的基因表达的组合物和方法 | |
| KR102014061B1 (ko) | 변형된 뉴클레오사이드, 뉴클레오타이드, 및 핵산, 및 이들의 용도 | |
| US8883752B2 (en) | 5′ and 2′ BIS-substituted nucleosides and oligomeric compounds prepared therefrom | |
| CN115484932A (zh) | 用于靶向rna递送的组合物和方法 | |
| JP2008501693A (ja) | 遺伝子調節で使用するための個別に調節された鎖を有する二本鎖組成物 | |
| US10947543B2 (en) | Interferon production using short RNA duplexes | |
| CN1780922A (zh) | 治疗严重急性呼吸道综合症(sars)的组合物和方法 | |
| CN110724687A (zh) | 用于调节补体因子b表达的组合物和方法 | |
| CN105452465B (zh) | 鞘脂-聚烷基胺-寡核苷酸化合物 | |
| EP4234567A1 (en) | Oligonucleotide for 5'-capped rna synthesis | |
| CA3128615A1 (en) | Topical delivery of polyribonucleic acids | |
| JP2021511042A (ja) | Aldh2発現を阻害するための組成物及び方法 | |
| CN111372594A (zh) | ENaC表达的调节剂 | |
| WO2023167880A2 (en) | Compositions and methods for capping rnas | |
| KR20230173116A (ko) | 보체 성분 3 발현을 저해하기 위한 조성물 및 방법 | |
| JPWO2016031247A1 (ja) | 非酵素的核酸鎖結合方法 | |
| KR20230083197A (ko) | 5'-캡핑된 rna 합성용 올리고뉴클레오티드 | |
| CN117425735A (zh) | 富集环状多核糖核苷酸的方法 | |
| TW202003844A (zh) | 核酸分子之製造方法 | |
| JP2011504357A (ja) | 修飾ヌクレオチドを含む転写物を生成させるための材料および方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |